Изобретение относится к области биотехнологии и микробиологической промышленности и касается применения штамма мицелиального гриба Aspergillus awamori ВКПМ F-148.
В настоящее время в мировой практике для повышения уровня биосинтеза целевых ферментов грибными продуцентами широко применяют технологии рекомбинантных ДНК. При создании продуцентов гемицеллюлаз мицелиальные грибы не только служат источником генов ферментов с технологически важными свойствами, но и часто используются в качестве реципиентов. В последние годы создан целый ряд рекомбинантных штаммов на основе аспергиллов, эффективно экспрессирующих гомологичные и гетерологичные гены, в частности гены гемицеллюлаз. Имеется ряд примеров успешного клонирования генов ксиланазы аспергиллов в клетках аспергиллов того же или другого вида: экспрессия гена ксиланазы A. niger, в результате которой были получены стабильные трансформанты с продукцией ксиланазы 625 ед./мл [1]; экспрессия гена маннаназы man1 Aspergillus aculeatus в клетках A. niger, где был достигнут выход фермента 1000 ед./мл [2], использование системы клонирования A. niger для наработки ксиланазы A. tubigensis [ЕР 0463706], экспрессия гена маннаназы A. aculeatus в A. oryzae [US 5795764]. На основе рекомбинантных штаммов A. niger - CBS 109.713 и DSM 18404 - создан двухкомпонентный ферментный препарат Natugrain TS с активностью ксиланазы и β-глюканазы 5600 ед./г и 2500 ед./г соответственно [3].
Известны также штаммы-продуценты гемицеллюлаз, полученные путем гетерологичной экспрессии генов из различных других грибов в системе клонирования Aspergillus. Множественная интеграция гена xemA термостабильной ксиланазы Talaromyces emersonii в клетках Aspergillus niger привела к получению рекомбинантного фермента, на основе которого создан препарат Natugrain Wheat TS [4]. Препарат Ronozyme WX, созданный в компании DSM, содержит термостабильную ксиланазу мицелиального гриба Т. lanuginosus DSM 4109, клонированную в генно-модифицированном штамме A. oryzae [5]. Введение гена ксиланазы Penicillum canescens в клетки продуцента глюкоамилазы A. awamori позволило получить штамм с высокими уровнями продукции обоих ферментов, при этом уровень активности ксиланазы составляет 150-200% относительно исходного штамма [6].
Возможность использования конкретного штамма в качестве реципиента определяют как его способностью экспрессировать чужеродную ДНК (трансформируемость), так и наличием у него низкого уровня продукции секреторных протеаз, что обеспечивает стабильность синтезируемого рекомбинантного фермента. К дополнительным преимуществам видов рода Aspergillus в качестве реципиентов относят такие технологически значимые признаки, как способность расти на простых по составу питательных средах в достаточно широких диапазонах температур и рН, способность эффективно секретировать ферменты в среду.
Технической задачей заявляемого изобретения является расширение арсенала мицелиальных грибов, пригодных для конструирования на их основе штаммов-продуцентов, способных экспрессировать целевой белок.
Задача решена путем применения штамма Aspergillus awamori ВКПМ F-148 в качестве реципиента для конструирования на его основе штаммов, способных экспрессировать целевые ферменты.
Штамм отобран в ходе скрининга коллекции аспергиллов ВКПМ для выявления наиболее активных продуцентов гемицеллюлаз. Ранее он был депонирован в ВКПМ как продуцент α-галактозидазы [7], регистрационный номер ВКПМ F-148.
Культурально-морфологические признаки штамма A. awamori ВКПМ F-148
Макроскопические характеристики: после 7 суток роста колонии на агаре Чапека имеют диаметр 35-40 мм, темно-серые с тонким ободком белого мицелия (1-2 мм), радиально-складчатые, реверс по центру светло-желтый, сильноскладчатый.
На агаре Чапека с дрожжевым экстрактом (CYA) при 25°С диаметр колонии 60 мм; колонии темно-серые с широким ободком белого мицелия, хлопьевидно опушенные, слегка радиально-бороздчатые, реверс по центру светло-коричневый, сильноскладчатый (складки в виде лучей).
Диаметр колонии на агаре Чапека с дрожжевым экстрактом при 37°С равен 50-60 мм; колонии темно-серые с коричневым оттенком, складчатые (в центре неупорядоченно, на периферии радиально) с белым ободком; реверс коричневый по центру, мелкоскладчатый, радиально-волнистый.
Колонии на агаре Чапека с дрожжевым экстрактом и 20% сахарозы (CY20S) при 25°С имеют диаметр 45-50 мм, темно-серые с широким белым ободком вегетативного мицелия, реверс по центру желтовато-светлокоричневый, сильноскладчатый (лучами и произвольно).
Колонии на Мальт-агаре (МЕА) 60 мм в диаметре, серые с ободком белого мицелия, плоские, рыхлые, реверс чуть темнее среды, складчатый (складки в виде тонких лучей).
Микроскопические характеристики: конидиальные головки шаровидные, затем рыхлорадиальные, распадающиеся на отдельные колонки, конидиеносцы слабо окрашенные в верней части, гладкостенные, длиной 600-1000 мкм и толщиной 6-12 мкм, везикулы шаровидные 20-45 мкм в диаметре, покрытые метулами по большей части поверхности. Штамм бисериатный, метулы 15-20×4-7 мкм, фиалиды 5-8×2-4 мкм. Конидии шаровидные, 3-6 мкм, гладкие, серые.
Физиолого-биохимические свойства штамма: хорошо утилизирует глюкозу, сахарозу, арабинозу, рамнозу, слабо - лактозу, галактозу, сорбозу и креатин.
Штамм ассимилирует аммонийные соли неорганических кислот. Потребляет пептон, казеин, аминокислоты.
Для таксономической характеристики штамма F-148, наряду с морфологическими и биохимическими тестами, проведена молекулярно-генетическая идентификация по следующим маркерам: нуклеотидная последовательность домена D1/D2 28S субъединицы рибосомальной РНК, нуклеотидная последовательность внутренних транскрибируемых спейсеров ITS1 и ITS4 гена 5.8S рРНК. Результаты идентификации подтверждают принадлежность штамма ВКПМ F-148 к виду Aspergillus awamori.
При исследовании спектра секретируемых ферментов штамма A. awamori ВКПМ F-148 и их активностей продуцент выращивали на ферментационной среде следующего состава (масс. %): отруби пшеничные - 2,0; свекловичный жом - 1,0; дрожжевой экстракт - 0,5; NaNO3 - 0,6; КН2РO4 - 0,15; КСl - 0,05; MgSO4 × 7Н2O - 0,05; смесь микроэлементов - 0,2 мл; рН 6,0. Состав смеси микроэлементов (масс. %): ЭДТА - 1,0; ZnSO4 × 7Н2O - 0,44; MnCl2 × 4Н2O - 0,1; СоСl2 × 6Н2O - 0,032; CuSO4 × 5Н2O - 0,0315; (NH4)6Mo7O24 × 4Н2O - 0,022; СаСl2 × 2Н2O - 0,147; FeSO4 × 7Н2O - 0,1, вода дистиллированная - остальное, рН 6,2. Измерение активности проводили колориметрическим методом с 3,5-динитросалициловой кислотой (ДНС) [8]. Получены следующие результаты: ксиланаза - 76,3 ед./мл, маннаназа - 16,5 ед./мл, β-глюканаза - 3,8 ед./мл, пектиназа - 1,8 ед./мл. Температурные оптимумы ферментов в основном составляют 50°С, а рН-оптимумы находятся в интервале рН 4,0-6,0. Показатели термостабильности ферментов не выходят за пределы 60°С, а рН-стабильность наиболее выражена в диапазоне рН 4,0-7,0, при этом ферменты обнаруживают высокую устойчивость к протеолизу панкреатическими ферментами.
Изобретение проиллюстрировано следующими фигурами:
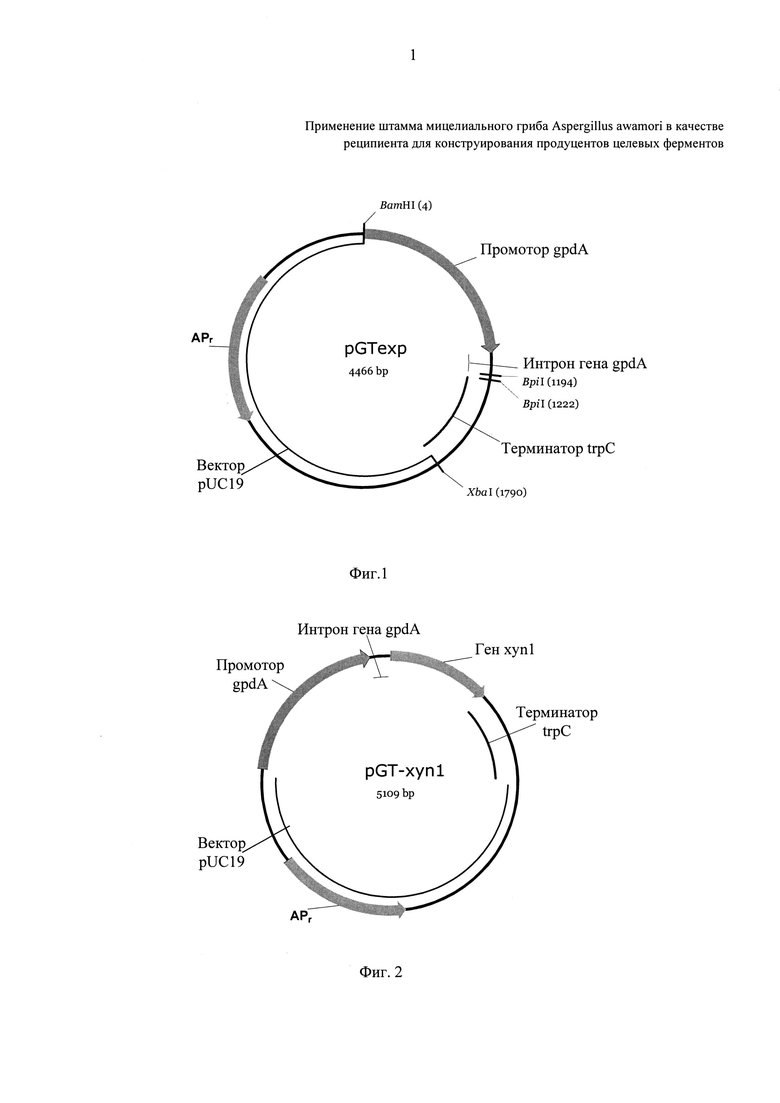
Фиг. 1. Генетическая карта плазмиды pGTexp.
Фиг. 2. Генетическая карта плазмиды pGT-xyn1.
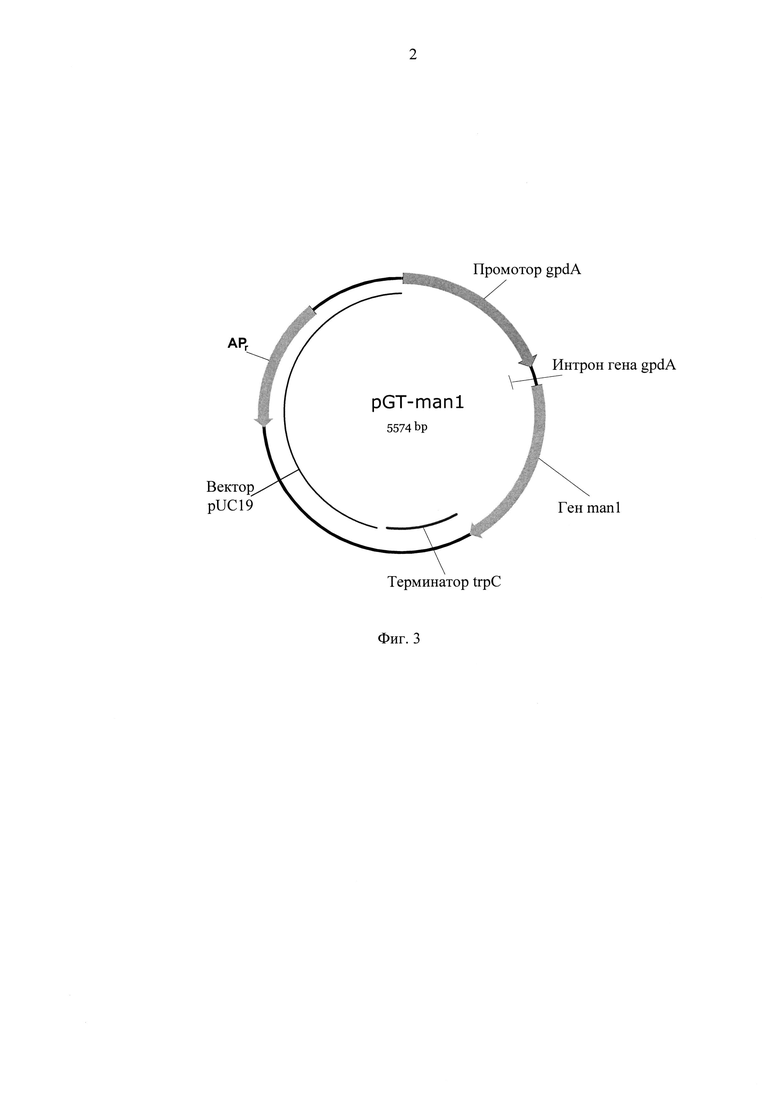
Фиг. 3. Генетическая карта плазмиды pGT-man1.
Пример 1. Получение продуцента ксиланазы с использованием в качестве реципиента штамма Aspergillus awamori ВКПМ F-148
Конструирование плазмид для экспрессии гена ксиланазы
Конструируют базовый экспрессионный вектор pGTexp, на основе которого получают плазмиду pGT-xyn1, предназначенную для множественной интеграции в геном Aspergillus awamori ВКПМ F-148.
Базовая плазмида pGTexp представляет собой стандартный вектор pUC19, между сайтами BamHI и XbaI которого находятся промотор gpdA, кодон ATG, интрон гена gpdA, а также терминатор trpC. Промотор gpdA, интрон гена gpdA, а также терминатор trpC получают с помощью ПЦР, в качестве матрицы используют плазмиду рМЕ2891 (FGSC 645 = ВКПМ В-10715) [9], а также пар праймеров: gpdA -F 5'-ggggatcctaatacagcccctacaacgacc-3' - gpdA -R 5'-cttcccgtacgcgaagacagcatggtgatgtctgctcaagcg-3' и trpC-F 5'-cttcgcgtacgggaagactggcgcctgatttaatagctccatgtcaacaagaataaaacg-3', - trpC-R 5'-cgactctagaaagaaggattacctctaaacaagtgtacc-3' соответственно. После наработки полученные фрагменты сшивают друг с другом методом ПЦР при использовании пары праймеров gpdA-F 5'-ggggatcctaatacagcccctacaacgacc-3' - trpC-R 5'-cgactctagaaagaaggattacctctaaacaagtgtacc-3' и затем клонируют между сайтами BamHI и XbaI вектора pUC 19.
Ген xyn1 синтезируют методом ПЦР, в качестве матрицы используют геномную ДНК Trichoderma reesei Rut С-30 (ВКПМ F-1093). Кодирующие области гена xyn1, включая сигнальную последовательность, амплифицируют с помощью двух пар праймеров:
Xyn1-1-F 5'-gtgaagacttcatggtctccttcacctccctcc-3' - Xyn1-1-R 5'-gttgatgaccttgttcttggtgccgggctgcc-3' и Xyn1-2-F 5'-ccaagaacaaggtcatcaacttctcgggcagc-3' - Xyn1-2-R 5'-tgaagactggcgccttagctgacggtgatggaagcagagcc-3'. После наработки полученные фрагменты сшивают друг с другом методом ПЦР при использовании пары праймеров Xyn1-1-F 5'-gtgaagacttcatggtctccttcacctccctcc-3' - Xyn1-2-R 5'-tgaagactggcgccttagctgacggtgatggaagcagagcc-3' с образованием ПЦР-фрагмента - гена xyn1, не содержащего интроны. Полученный фрагмент обрабатывают эндонуклеазой рестрикции BpiI и клонируют в вектор pGTexp, обработанный сходным образом, в результате чего получают плазмиду pGT-xyn1.
Трансформация и культивирование
Штамм A. awamori ВКПМ F-148 трансформируют методом котрансформации плазмидой pGT-xyn1 в смеси со вспомогательной плазмидой p3SR2 (FGSC 66), полученной из коллекции Fungal Genetics Stock Center (США) и депонированной в ВКПМ (В-10724). Трансформацию проводят с использованием протопластов согласно стандартным методикам [10; 11]. Трансформационная смесь содержит около 107 протопластов в 100 мкл суспензии и 1-2 мкг плазмидной ДНК. Аликвоты трансформационной смеси переносят на поверхность чашки Петри с селективно-регенерационной средой, содержащей (масс. %) сорбит - 18,2, дрожжевой экстракт - 0,5, казаминовые кислоты - 0,2, хлорид цезия - 0,25, селективный агент - ацетамид - 0,059, смесь микроэлементов - 0,2 мл, вода дистиллированная - остальное [12]. Чашки инкубируют при 28°С в течение 5 дней, после чего выросшие трансформанты очищают двумя пассажами на чашках Петри с аналогичной средой.
Выход трансформантов в описанных условиях составляет 100-150 клонов/мкг ДНК.
Оценка уровня активности ксиланазы у полученных трансформантов
Исходный штамм и трансформанты выращивают в течение 5 дней при 28°С в колбах Эрленмейера объемом 750 мл, содержащих 100 мл модельной среды 2хММ с 10% глюкозы [12].
Биомассу отделяют фильтрованием через фильтровальную бумагу Ватман №1, а затем надосадочную жидкость осветляют центрифугированием 15 мин при 5000 об/мин. Активность ксиланазы в полученном центрифугате оценивают по способности гидролизовать субстрат, в качестве которого используют 2,0% раствор ксилана из древесины бука (Sigma) в 0,05 М натрий-ацетатном буфере, рН 4,5.
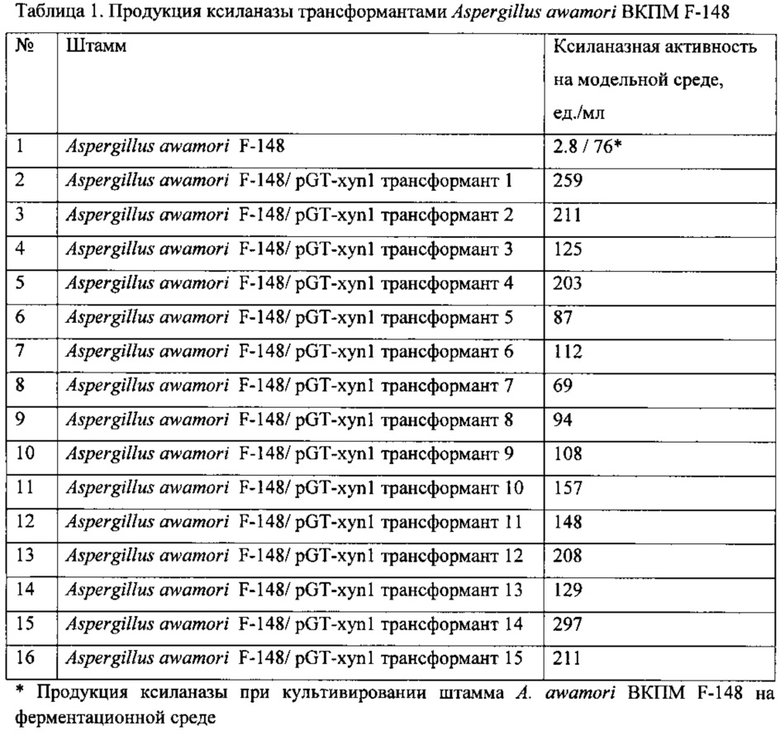
Из приведенных в табл. 1 данных видно, что активность ксиланазы у трансформантов намного превышает активность родительского штамма, максимальная ксиланазная активность составила 297 ед./мл.
Пример 2. Получение продуцента маннаназы с использованием в качестве реципиента штамма Aspergillus awamori ВКПМ F-148
Конструирование плазмиды для экспрессии гена маннаназы
На основе базового экспрессионного вектора pGTexp конструируют плазмиду pGT-man1, предназначенную для множественной интеграции в геном Aspergillus awamori F-148. Для экспрессии гена, кодирующего маннаназу гриба Aspergillus aculeatus, ген man1 синтезируют методом ПЦР, в качестве матрицы используют геномную ДНК Aspergillus aculeatus ВКПМ F-1086. Кодирующие области гена man1, включая сигнальную последовательность, амплифицируют с помощью трех пар праймеров:
Man1-1-F 5'-gtgaagacttcatgaagctttctcacatgctcc-3' - Man1-1-R 5'-gaagccctcatcgccaatcgtgaccaggtgc-3',
Man1-2-F 5'-gattggcgatgagggcttcggtctcgacgtcgactcc-3' - Man1-2-R 5'-ggtgccccagctatcggggtacagatgc-3' и
Man1-3-F 5'-cgatagctggggcacctcctacgactgg-3' - Man1-3-R 5'-tgaagactggcgccttacttcgactgcgcattgatgg-3'. После наработки полученные фрагменты сшивают друг с другом методом ПЦР при использовании пары праймеров Man1-1-F 5'-gtgaagacttcatgaagctttctcacatgctcc-3'- Man1-3-R 5'-tgaagactggcgccttacttcgactgcgcattgatgg-3' с образованием ПЦР-фрагмента - гена man1, не содержащего интроны. Полученный фрагмент обрабатывают эндонуклеазой рестрикции BpiI и клонируют в вектор pGTexp, обработанный сходным образом, в результате чего получают плазмиду pGT-man1.
Трансформация и культивирование
Штамм A. awamori ВКПМ F-148 трансформируют плазмидой pGT-man1, в смеси с вспомогательной плазмидой p3SR2. Трансформацию и культивирование трансформантов проводят, как описано в Примере 1.
Оценка уровня активности маннаназы
Активность маннаназы определяют по методике, аналогичной определению активности ксиланазы, в качестве субстрата используют 1,0% раствор галактоманнана (камеди плодов рожкового дерева, Sigma) в 0,05 М натрий-цитратном буфере рН 4,8.
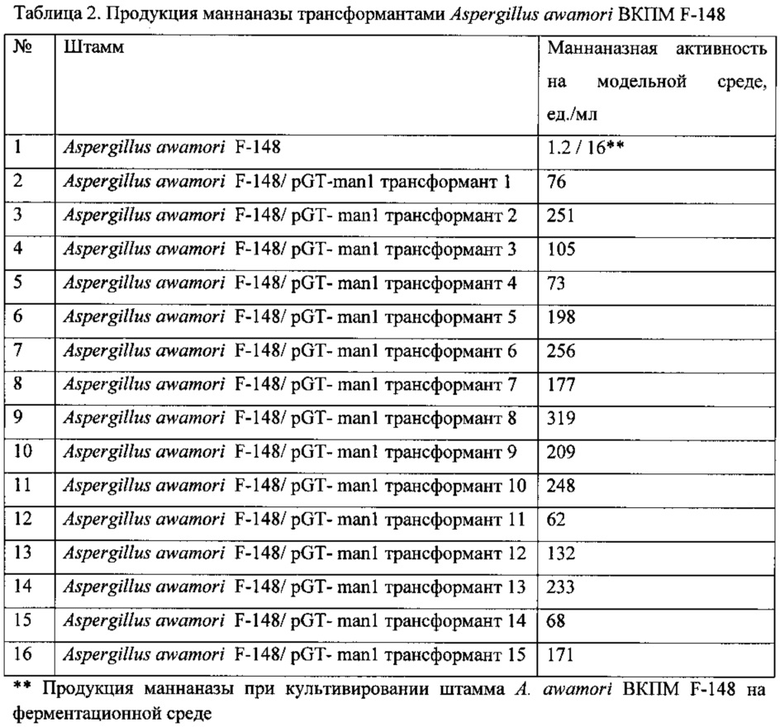
Из приведенных в таблице 2 данных видно, что активность маннаназы из культуральной жидкости штаммов, трансформированных плазмидой pGT-man1, намного превышает активность родительского штамма, при этом наибольшая маннаназная активность составила 319 ед./мл.
Таким образом, подтверждено эффективное применение штамма мицелиального гриба Aspergillus awamori ВКПМ F-148 в качестве штамма-реципиента для конструирования продуцентов, способных синтезировать целевой белок, в частности ксиланазу и маннаназу.
Дополнительным преимуществом штамма Aspergillus awamori ВКПМ F-148 в качестве перспективного реципиента для клонирования генов грибов, в частности генов гемицеллюлаз, является низкий уровень секретируемых протеаз на всех средах, что уменьшает опасность протеолиза рекомбинантных полипептидов и тем самым повышает их стабильность.
Очень важным является также то, что штаммы вида Aspergillus awamori непатогенны и имеют длительную историю безопасного применения, а многие препараты на их основе получили за рубежом статус GRAS (Generally recognized as safe), т.е. признаны безопасными для использования в различных отраслях промышленности, в частности в пищевой и кормопроизводстве. Это дает возможность использовать штамм A. awamori F-148 для конструирования штаммов-продуцентов ферментов для использования в промышленности.
Литература
1. Levasseur A., Asther М., Record Е. // Canadian Journal of Microbiology. - 2005. - V. 51. - P. 177-183.
2. van Zyl P.J, Moodley V., Rose S.H., Roth R.L., van Zyl W.H. // Journal of Industrial Microbiology and Biotechnology. - 2009. - V. 36. P. 611-617.
3. EFSA Journal. - 2013. - V. 11. - P. 3385-2294.
4. WO 02/24926.
5. WO 2003062409.
6. RU 2457246.
7. A.C. СССР 958503.
8. Miller C.L. Analytical Chemistry. - 1959. - V. 31. - P. 436-428.
9. Krappmann S., Bayram O., Braus G.H. // Eukaryotic Cell. - 2005. - V. 4. - P. 1298-1307.
10. He Z. - M., Price M.S., O'Brian G.R., Georgianna D.R., Payne G.A. // BMC Microbiology. - 2007. - V. 7: 104. - 11 P.
11. De Bekker C., Wiebenga A., Aguilar G., Wosten H.A.B. - Journal of Microbiological methods. - 2009. - V. 76. - №3. - P. 305-306.
12. Rose S.H., van Zyl W.H. // Applied Microbiology and Biotechnology. - 2002. - V. 58. - P. 461-468.
Изобретение относится к области биохимии, генной инженерии и биотехнологии, в частности к применению штамма мицелиального гриба Aspergillus awamori ВКПМ F-148 в качестве реципиента для конструирования продуцентов целевых ферментов. Настоящее изобретение позволяет конструировать продуцентов рекомбинантных целевых ферментов, в том числе продуцентов ксиланаз и маннаназ. 3 ил., 2 табл., 2 пр.
Применение штамма мицелиального гриба Aspergillus awamori ВКПМ F-148 в качестве реципиента для конструирования продуцентов целевых ферментов.
| РОЖКОВА И ДР, Создание системы экспрессии гетерологичных генов на основе штамма гриба Aspergillus awamori, ПРИКЛАДНАЯ БИОХИМИЯ И МИКРОБИОЛОГИЯ, 2011 | |||
| Штамм плесневого гриба aSpeRGILLUS аWамоRI-10-3-продуцент @ -галактозидазы | 1980 |
|
SU958503A1 |
| WO 2014088934 A1, 12.06.14. | |||
Авторы
Даты
2017-06-01—Публикация
2015-11-06—Подача