Изобретение относится к области медицины, в частности к медицинской диагностике, конкретно к способу определения видовой принадлежности возбудителя бруцеллеза при исследовании чистых культур микроорганизмов, а также материала от людей, животных и из объектов окружающей среды, и может быть использовано в научно-исследовательских учреждениях, лабораториях регионального и федерального уровней.
В основе лабораторной диагностики бруцеллеза лежат культуральные методы исследования. Так, для дифференциации видов бруцелл необходимо определение следующих параметров: отношение к избыточному содержанию углекислоты в атмосфере воздуха; продукция сероводорода; способность редуцировать основные красители (фуксин и тионин); агглютинация моноспецифическими сыворотками anti-abortus и anti-melitensis; лизис бруцеллезным диагностическим бактериофагом Тб. Выполнение таких исследований трудоемко и продолжительно.
В настоящее время одним из наиболее перспективных методов диагностики вирусных и бактериальных инфекций, в частности индикации и идентификации возбудителя бруцеллеза, является метод ПЦР, который характеризуется высокой чувствительностью и специфичностью.
Известен способ определения видовой принадлежности возбудителя бруцеллеза, включающий в себя амплификацию локуса отр2, дальнейшую рестрикцию продуктов амплификации различными ферментами с последующим анализом рестрикционных профилей, специфичных для разных видов и биоваров бруцелл [1].
Однако учет результатов данного способа происходит методом электрофореза, что требует дополнительного оборудования, повышает риск контаминации и не дает возможности проведения количественной оценки содержания ДНК в пробе. Кроме того, для проведения видовой идентификации необходимым является проведение рестрикции продуктов амплификации, что связано с увеличением количества используемых реактивов и требует дополнительных временных затрат.
Одним из первых способов определения видовой принадлежности бруцелл, применяющихся по сегодняшний день? является AMOS-ПЦР и его модификации. Данный метод основан на выявление мобильного генетического элемента IS711 и позволяет дифференцировать виды В. abortus (биовары 1, 2, 4), В. melitensis, В. ovis и В. suis (биовар 1) [2]. Позднее данный метод был усовершенствован путем добавления праймеров для идентификации ряда вакцинных штаммов В. abortus, а также штаммов В. abortus 5, 6, 9 биоваров и некоторых 3 биовара. Однако с помощью данного методического приема не представляется возможным дифференциация видов В. canis, В. neotomae и всех биоваров В. suis. Кроме того, данный метод характеризуется электрофоретическим учетом результатов [3, 4, 5].
Известен способ видовой идентификации бруцелл, основанный на амплификации фрагментов wboA, bp26, отр31, eryC, rpsL и CRP, который позволяет идентифицировать виды В. abortus, В. melitensis, В. ovis, В. suis, В. neotomae, В. canis, культуры, изолированные от морских видов, и три вакцинных штамма. Однако вышеуказанный способ не позволяет в полной мере дифференцировать виды В. suis и В. canis, вследствие образования близких амплификационных профилей у этих видов. Помимо этого, детекция результатов производится с помощью электрофореза, что увеличивает временные затраты, риск контаминации и, как следствие, появления ложноположительных результатов [6, 7].
Известны способы и наборы реагентов для одновременного обнаружения видов В. abortus, В. melitensis и В. abortus, В. melitensis, В. suis, В. canis. Данные методики так же, как и предыдущие, не позволяют определять все основные виды бруцелл и учет результатов проводится методом электрофореза [8, 9].
На сегодняшний день имеется ряд зарубежных публикаций, посвященных определению видовой принадлежности бруцелл с помощью ПЦР с учетом результатов в режиме реального времени. Однако, в большинстве случаев, авторам удалось определить лишь 3 основных вида возбудителя бруцеллеза: В. abortus, В. melitensis, В. suis [10, 11].
Одним из методов, позволяющих дифференцировать виды В. abortus, В. melitensis, В. suis, В. canis, В. ovis, В. neotomae и штаммы, относящиеся к морским видам бруцелл, является ПЦР-РВ с анализом кривых плавления высокого разрешения, предложенная Winchell с соавторами. Однако данная методика требует определенной приборной базы и характеризуется увеличением временных затрат за счет анализа кривых плавления отдельно с каждым набором праймеров. Также вышеуказанный способ, как и многие другие подходы, не позволил дифференцировать В. suis 4 биовар от штаммов, принадлежащих виду В. canis [12].
Наиболее близким по технической сущности является способ определения шести видов бруцелл методом ПЦР с учетом результатов в режиме реального времени. Праймеры и олигонуклеотидные зонды для определения видов В. abortus, В. melitensis, В. suis, В. canis, В. ovis, В. neotomae были подобраны к участкам генов BruAb2_0168, BMEII0466, BR0952, BMEII0635-0636, BOV_A0504, BMEII0986-0988 соответственно.
Также авторами была использована последовательность IS711 для определения рода Brucella spp. [13]. Недостатком рассматриваемого способа является постановка ПЦР не в мультиплексном формате, а отдельно с каждой парой праймеров и зондов, т.е. невозможность одновременной идентификации всех указанных видов и, как следствие, значительное увеличение времени проведения реакции. Кроме того, постановка семи различных ПЦР требует затрат большего количества реактивов. Также авторами представлены данные по результатам исследования чистых культур микроорганизмов и нет информации о возможности применения вышеуказанного способа с целью исследования клинических и биологических образцов, а также проб из объектов окружающей среды.
Техническим результатом предлагаемого изобретения является повышение эффективности и сокращение времени идентификации 6 основных видов бруцелл: В. abortus, В. melitensis, В. suis, В. canis, В. ovis, В. neotomae за счет одновременного выявления генетических локусов, специфичных для отдельных видов патогена, и фрагмента гомологичного у всех Brucella spp. Дополнительный технический результат заключается в повышении диагностических возможностей за счет определения видовой принадлежности возбудителя бруцеллеза как при исследовании чистых культур, так и материала от людей и животных, проб из объектов окружающей среды.
Технический результат достигается способом определения видовой принадлежности возбудителя бруцеллеза, включающим выделение ДНК исследуемой пробы, проведение ПЦР с гибридизационно-флуоресцентным учетом результатов в режиме реального времени, согласно изобретению, ПЦР с гибридизационно-флуоресцентным учетом результатов в режиме реального времени проводят в один этап в двух реакционных смесях, одна из которых содержит специально подобранное сочетание праймеров SEQ ID N 1, 3, 5 и зондов SEQ ID N 2, 4, 6 к генам bcspSl, BRA0541, BRA0420, другая смесь праймеров SEQ ID N 7, 9, 11 и зондов SEQ ID N 8, 10, 12 к генам BMEI1426, BMEII0711, BMEI0994. Видовую принадлежность возбудителя бруцеллеза определяют в соответствии с таблицей: по отсутствию сигнала флуоресценции с видоспецифичной ДНК-мишенью и его наличию с остальными используемыми ДНК-мишенями определяют принадлежность к видам В. abortus, В. melitensis, В. ovis, В. canis, В. neotomae, а по наличию сигнала флуоресценции со всеми ДНК-мишенями определяют принадлежность к виду В. suis.
Генетический локус bcsp31 был выбран для определения рода Brucella spp. из литературных источников [10]. Другие ДНК-мишени: BRA0541, BRA0420, BMEI1426, BMEII0711, BMEI0994, которые позволяют проводить видовую идентификацию возбудителя бруцеллеза, подобраны авторами по результатам анализа in silico в базе данных GenBank NCBI. Для проведения способа были сконструированы специфические для вышеуказанных генов праймеры и олигонуклеотидные зонды. Подбор праймеров и зондов проводили с помощью программного обеспечения на сайте www.genscript.com и программы GeneRanner 3.1. Указанные последовательности праймеров и зондов представлены на фигуре.
Способ осуществляют следующим образом.
Подготовку проб проводят согласно МУ 1.3.2569-09 «Организация работы лабораторий, использующих методы амплификации нуклеиновых кислот при работе с материалом, содержащим микроорганизмы I-IV групп патогенности». Материалом для исследования могут служить: чистые культуры микроорганизмов, клинические и биологические образцы, а также пробы из объектов окружающей среды. Для обеззараживания проб к ним добавляют мертиолят натрия до конечной концентрации 1:10000 (0,01%), прогревают при 56°C в течение 30 мин, с последующим смешиванием 100 мкл полученной суспензии с лизирующим буфером на основе 6 моль гуанидинизотиоцианата в объеме, указанном в инструкции к набору для выделения ДНК, и инкубированием 15 минут при температуре (65±1)°C. Выделение ДНК осуществляют с помощью наборов «ДНК-сорб В», «Рибо-преп», «Рибо-Сорб» в соответствии с инструкциями к препаратам.
После выделения ДНК приступают к сборке реакционных смесей. Для этого отбирают необходимое количество микропробирок, соответствующее числу исследуемых проб, а также по одной пробирке для положительного и отрицательного контролей. Затем готовят две реакционные смеси. Для упрощения и стандартизации подготовки реакционных смесей праймеры, зонды, дНТФ, MgCl2 и 2,5хБ объединены в три ПЦР-смеси, одна из которых - ПЦР-смесь 1 содержит праймеры SEQ ID N 1, 3, 5 и зонды SEQ ID N 2, 4, 6 на основе bcsp31, BRA0420, BRA0541 в концентрации 8 и 4 пмоль соответственно, смесь дНТФ (дАТФ, дТТФ, дГТФ, дСТФ), каждый в концентрации 1 ммоль, азид натрия - 0,02%; ПЦР-смесь 2 содержит праймеры SEQ ID N 7, 9, 11 и зонды SEQ ID N 8, 10, 12 на основе BMEI1426, BMEII0711, BMEI0994 в концентрации 8 и 4 пМоль соответственно, смесь дНТФ (дАТФ, дТТФ, дГТФ, дСТФ), каждый в концентрации 1 ммоль, азид натрия - 0,02%; ПЦР-смесь 3 содержит 6,25 ммоль MgCl2, 2,5хБ, азид натрия - 0,01%. Для приготовления реакционной смеси №1 смешивают 5 мкл ПЦР-смеси 1, 10 мкл ПЦР-смеси 3 и 0,4 мкл фермента Taq-полимеразы. Для приготовления реакционной смеси для №2 смешивают 5 мкл ПЦР-смеси 2, 10 мкл ПЦР-смеси 3 и 0,4 мкл фермента Taq-полимеразы. В подготовленные пробирки с реакционными смесями вносят по 10 мкл пробы. В пробирки, обозначенные как отрицательные контроли, вносят 10 мкл деионизованной воды, а в пробирки с положительными контролями соответственно по 10 мкл ДНК контрольного штамма. В качестве контрольного штамма используют В. suis 1330 в концентрации 1×105 м.к./мл. Конечный объем реакционной смеси составляет 25 мкл. Микропробирки переносят в амплификатор и проводят амплификацию на приборе типа RotorGene («Qiagen», Германия) при следующих температурных режимах: прогревание 95°С - 5 мин; 10 циклов: 95°C - 30 с, 60°C - 30 с, 72°C - 30 с; 35 циклов: 95°C -15 с, 57°C - 20 с, 72°C - 20 с.
Учет результатов проводят на основании отсутствия сигнала флуоресценции с видоспецифичной ДНК-мишенью и его наличию с остальными используемыми ДНК-мишеням в соответствии с таблицей. С помощью праймеров и зондов, содержащихся в первой реакционной смеси, определяется принадлежность к роду Brucella и видам В. abortus, В. melitensis. Праймеры, входящие в состав второй реакционной смеси, позволяют разделять виды В. ovis, В. canis и В. neotomae. Принадлежность к виду В. suis подтверждается при наличии амплификации со всеми праймерами и зондами, находящимися в двух реакционных смесях.
Чувствительность реакции амплификации каждого из указанных генов составляет не менее 5×103 м.к./мл, а специфичность 100%.
Заявляемый способ позволяет определять видовую принадлежность бруцелл как при исследовании чистых культур микроорганизмов, так и материала от людей, животных и из объектов окружающей среды.
Пример 1. Определение видовой принадлежности возбудителя бруцеллеза при исследовании биоматериала от животных.
Для определения эффективности заявляемого способа исследована 101 проба биологического материала от мелкого и крупного рогатого скота: суспензии печени, селезенки, легких, лимфатических узлов, маток с плодами, околоплодная жидкость. Подготовку проб проводили согласно МУ 1.3.2569-09 «Организация работы лабораторий, использующих методы амплификации нуклеиновых кислот при работе с материалом, содержащим микроорганизмы I-IV групп патогенности». Выделение ДНК осуществляли с помощью набора «ДНК-Сорб В» (ИЛС, Москва). Постановку ПЦР с гибридизационно-флуоресцентным учетом результатов осуществляли на приборе типа RotorGene («Qiagen», Германия).
При постановке ПЦР в 38 образцах (14 суспензий лимфатических узлов, 6 суспензий маток, 6 проб околоплодной жидкости, 8 суспензий печени, 4 суспензии селезенки) была получена амплификации локуса bcsp31, что свидетельствует о наличии в пробе ДНК Brucella spp. В этих же пробах было выявлено накопление флуоресцентного сигнала по каналу JOY(BRA0541) и отсутствие амплификации по каналу ROX(BRA0420) с первой реакционной смесью. При анализе образцов с реакционной смесью - 2 положительный сигнал регистрировался по всем 3 каналам. Таким образом, по наличию амплификации с праймерами и зондами к ДНК-мишеням bcsp31, BRA0541, BMEI1426, BMEII0711, BMEI0994 и отсутствию амплификации с праймерами и зондом к локусу BRA0420 исследуемые пробы были отнесены к виду В. abortus. Одновременно все пробы биоматериала были исследованы с помощью наборов реагентов «ГенБру» (ФКУЗ РосНИПЧИ «Микроб»), «АмплиСенс Brucella spp.-FL» (ООО ИнтерЛабСервис), которые подтвердили результаты, полученные с использованием разработанного способа, определив наличие ДНК бруцелл в 38 пробах. При исследовании этих образцов бактериологическим методом культуру возбудителя бруцеллеза удалось выделить в 14 случаях. Далее при постановке дифференциальных биохимических тестов была определена принадлежность выделенных культур к виду В. abortus.
Пример 2. Определение видовой принадлежности возбудителя бруцеллеза при исследовании чистых культур микроорганизмов.
Для определения эффективности заявляемого способа исследованы чистые культуры 45 штаммов бруцелл, относящихся к основным 6 видам, в количестве: В. abortus - 12, В. melitensis - 15, В. suis - 10, В. ovis - 3, В. canis - 2, В. neotomae - 3. При постановке ПЦР в реакционной смеси №1 амплификация фрагмента bcsp31 была получена у всех исследуемых видов бруцелл, что подтверждает их принадлежность к роду Brucella spp. У штаммов, относящихся к виду В. melitensis, наблюдалась амплификация фрагментов BRA0420, BMEI1426, BMEII0711, BMEI0994 и отсутствие амплификация фрагмента BRA0541, так как данный локус делетирован у вида В. melitensis. При исследовании штаммов В. abortus была получена амплификация всех видоспецифичных участков: BRA0541, BMEI1426, BMEII0711, BMEI0994, за исключением BRA0420, что является характерным для представителей данного вида. У штаммов, относящихся к виду В. canis, не наблюдалось амплификации с фрагментом BMEI1426, у В. ovis с фрагментом BMEI0994, а у В. neotomae с фрагментом BMEII0711, что также является характерным для данных видов, так как они не содержат вышеуказанные фрагменты. При исследовании штаммов, принадлежащих к виду В. suis, флуоресцентный сигнал регистрировался со всеми видоспецифичными участками: BRA0541, BRA0420, BMEI1426, BMEII0711, BMEI0994. В результате, с помощью предложенного способа была подтверждена видовая принадлежность 45 штаммов бруцелл.
Таким образом, предлагаемый способ позволяет быстро и достоверно проводить детекцию и идентификацию на уровне вида возбудителя бруцеллеза при исследовании чистых культур и различных видов биологического материала.
1. Патент US 5348857 A. Probes and method for identifying species and biovars of Brucella / Ficht T.A., Adams L.G. Опубл. 20 сентября 1994.
2. Bricker, В.J., Hailing S.M. Differentiation of Brucella abortus bv. 1, 2, and 4, Brucella melitensis, Brucella ovis, and Brucella suis bv. 1 by PCR J. Clin. Microbiol. 1994; 32: 2660-2666.
3. Bricker, B.J., Hailing S.M. Enhancement of the Brucella AMOS PCR assay for differentiation of Brucella abortus vaccine strains S19 and RB51. J. Clin. Microbiol. 1995; 33:1640-1642.
4. Bricker J., Ewalt D.R., Olsen S.C., Jensen A.E. Evaluation of the Brucella abortus species- specific polymerase chain reaction assay, an improved version of the Brucella AMOS polymerase chain reaction assay for cattle. J. Vet. Diagn. Investig. 2003; 15: 374-378.
5. Ica Т., Aydin F., Gumussoy K.S., Percin D., Sumerkan A.B., Ocak F., Abay S., Dogan H.O., Findik A., Ciftci A. Conventional and molecular biotyping of Brucella strains isolated from cattle, sheep and human Ankara Univ. Vet. Fak. Derg. 2012; 59: 259-264.
6. Патент ES WO 2006097347 A3. Methods for detecting, identifying and differentiating species and vaccine strains of the brucella genus / I. Lopez-Goni, D. Garcia-Yoldi. Опубл. 4 января 2007.
7. Lopez-Goni I., Garcia-Yoldi D., Martin С.М., Miguel M.J., Munoz P.M., Blasco J.M., Jacques I., Grayon M., Cloeckeart A., Ferreira A.C., Carloso R., Correa de Sa, M.I., Walravens K., Albert D., Garin-Bastuji B. Evaluation of a multiplex PCR assay (Bruce-ladder) for molecular typing of all Brucella species including the vaccine strains. J. Clin. Microbiol. 2008; 46: 3484- 3487.
8. Патент DE 10261468 A1. Test kit for detecting Brucella species, potential biological warfare agents, in the environment, comprises primers for specific amplification, optionally also hybridization probe / G. Grote, S. Dipl.-Biol. Dr. Kohne. Опубл. 15 июля 2004.
9. Патент CN 103409520 A. PCR kit for simultaneously detecting Brucella abortus, Brucella melitensis, Brucella suis and Brucella canis as well as preparation method and using method thereof / W. Xinglong, C. Si, W. Xiuran, Q. Jing, L. Xulong, W. Xiaoxu. Опубл. 26 ноября 2014.
10. Probert W.S., Schrader K.N., Khuong N.Y., Bystrom S.L., Graves M.H. Real-Time Multiplex PCR Assay for Detection of Brucella spp., B. abortus, and B. melitensis. Journal Of Clinical Microbiology. 2004; 42(3): 1290-1293.
11. Redkar R., Rose S., Bricker В., DelVecchio V. Real-time detection of Brucella abortus, Brucella melitensis, and Brucella suis. Mol. Cell. Probes. 2001; 15: 43-52.
12. Winchell J.M., Wolff В.J., Tiller R., Bowen M.D., Hoffmaster A.R. Rapid identification and discrimination of Brucella isolates by use of real-time PCR and high-resolution melt analysis. J Clin Microbiol. 2010; 48(3): 697-702.
13. Hinic V., Brodard I., Thomann A., 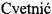 Z., Makaya P.V., Frey J., Abril C. Novel identification and differentiation of Brucella melitensis, B. abortus, B. suis, B. ovis, B. canis, and B. neotomae suitable for both conventional and real-time PCR systems. J. Microbiol. Methods. 2008; 75(2): 375-8.
Z., Makaya P.V., Frey J., Abril C. Novel identification and differentiation of Brucella melitensis, B. abortus, B. suis, B. ovis, B. canis, and B. neotomae suitable for both conventional and real-time PCR systems. J. Microbiol. Methods. 2008; 75(2): 375-8.
| название | год | авторы | номер документа |
|---|---|---|---|
| НАБОР РЕАГЕНТОВ ДЛЯ ВЫЯВЛЕНИЯ И ИДЕНТИФИКАЦИИ ДНК ВОЗБУДИТЕЛЕЙ БРУЦЕЛЛЕЗА МЕТОДОМ ПОЛИМЕРАЗНОЙ ЦЕПНОЙ РЕАКЦИИ В РЕАЛЬНОМ ВРЕМЕНИ "ОМ-СКРИН-БРУЦЕЛЛЕЗ-РВ" | 2018 |
|
RU2715333C1 |
| Набор олигонуклеотидных праймеров и флуоресцентно-меченых зондов и способ выявления ДНК возбудителя бруцеллеза | 2022 |
|
RU2795987C1 |
| НАБОР ШТАММОВ БАКТЕРИЙ ДЛЯ ОБУЧЕНИЯ ВОПРОСАМ МИКРОБИОЛОГИИ И МЕТОДАМ ЛАБОРАТОРНОЙ ДИАГНОСТИКИ ТУЛЯРЕМИИ | 2022 |
|
RU2822665C2 |
| ШТАММ F26 ПОСТОЯННОЙ ГИБРИДОМНОЙ ЛИНИИ КЛЕТОК МЫШИ MUS. MUSCULUS - ПРОДУЦЕНТ МОНОКЛОНАЛЬНЫХ АНТИТЕЛ К ОЛИГОПОЛИСАХАРИДНОМУ (ОПС) АНТИГЕНУ B. ABORTUS | 2014 |
|
RU2560260C1 |
| СПОСОБ ГЕНЕТИЧЕСКОГО INDEL-ТИПИРОВАНИЯ ШТАММОВ BRUCELLA MELITENSIS | 2019 |
|
RU2732425C1 |
| Набор реагентов и способ детекции возбудителя малярии Plasmodium falciparum | 2024 |
|
RU2839159C1 |
| СПОСОБ ПОДВИДОВОЙ ДИФФЕРЕНЦИАЦИИ ШТАММОВ ВОЗБУДИТЕЛЯ ЧУМЫ МЕТОДОМ ПОЛИМЕРАЗНОЙ ЦЕПНОЙ РЕАКЦИИ С ГИБРИДИЗАЦИОННО-ФЛУОРЕСЦЕНТНЫМ УЧЕТОМ РЕЗУЛЬТАТОВ В РЕЖИМЕ РЕАЛЬНОГО ВРЕМЕНИ | 2016 |
|
RU2621869C1 |
| Набор олигонуклеотидных праймеров Ft 101 и способ определения бактерий Francisella tularensis (варианты) | 2019 |
|
RU2703803C1 |
| Набор олигонуклеотидных праймеров Ft 182 и способ определения бактерий Francisella tularensis (Варианты) | 2019 |
|
RU2706564C1 |
| Способ идентификации токсигенных генетических вариантов возбудителя холеры Эль Тор с набором мутаций в генах вирулентости и генах острова пандемичности VSPII методом мультиплексной полимеразной цепной реакции | 2022 |
|
RU2815711C2 |


Изобретение относится к биохимии. Описан способ определения видовой принадлежности возбудителя бруцеллеза. Видовую принадлежность возбудителя бруцеллеза определяют методом полимеразной цепной реакции с гибридизационно-флуоресцентным учетом результатов в режиме реального времени, которую ставят в один этап в двух реакционных смесях. Одна смесь содержит сочетание праймеров SEQ ID N 1, 3, 5 и зондов SEQ ID N 2, 4, 6 к генам bcsp31, BRA0541, BRA0420, другая смесь содержит праймеры SEQ ID N 7, 9, 11 и зонды SEQ ID N 8, 10, 12 к генам BMEI1426, BMEII0711, BMEI0994. По отсутствию сигнала флуоресценции с видоспецифичной ДНК-мишенью и его наличию с остальными используемыми ДНК-мишенями определяют принадлежность к видам В. abortus, В. melitensis, B. ovis, B. canis, В. neotomae, а по наличию сигнала флуоресценции со всеми ДНК-мишенями определяют принадлежность к виду B. suis. Изобретение позволяет повысить эффективность и сократить время идентификации 6 основных видов бруцелл. 1 ил., 1 табл., 2 пр.
Способ определения видовой принадлежности возбудителя бруцеллеза методом ПЦР с гибридизационно-флуоресцентным учетом результатов в режиме реального времени, включающий выделение ДНК исследуемой пробы, проведение ПЦР с гибридизационно-флуоресцентным учетом результатов в режиме реального времени, отличающийся тем, что ПЦР с гибридизационно-флуоресцентным учетом результатов в режиме реального времени проводят в один этап в двух реакционных смесях, одна из которых содержит специально подобранное сочетание праймеров SEQ ID N 1, 3, 5 и зондов SEQ ID N 2, 4, 6 к генам bcsp31, BRA0541, BRA0420, другая смесь праймеров SEQ ID N 7, 9, 11 и зондов SEQ ID N 8, 10, 12 к генам BMEI1426, BMEII0711, BMEI0994, видовую принадлежность возбудителя бруцеллеза определяют в соответствии с таблицей: по отсутствию сигнала флуоресценции с видоспецифичной ДНК-мишенью и его наличию с остальными используемыми ДНК-мишенями определяют принадлежность к видам B. abortus, B. melitensis, B. ovis, B. canis, B. neotomae, а по наличию сигнала флуоресценции со всеми ДНК-мишенями определяют принадлежность к виду B. suis.
| WO 2006097347 A2, 21.09.2006 | |||
| Электрический куб для нагревания непрерывно протекающей жидкости | 1929 |
|
SU23496A1 |
Авторы
Даты
2017-06-07—Публикация
2016-09-19—Подача