Изобретение относится к технологии переработки газообразного углеводородного сырья и касается, в частности, способа газофазной гидрогенизационной конверсии диоксида углерода в жидкие углеводороды (у/в) или синтетическое моторное топливо.
В изобретении предложены нанокатализаторы, содержащие наночастицы металлического кобальта размером 5-10 нм, нанесенные на новый класс металлорганических каркасных носителей, типа MIL-53(Al), полученных в ходе СВЧ активированного синтеза. Изобретение обеспечивает частичную утилизацию парникового газа - диоксида углерода и упрощение технологии процесса получения жидких углеводородов.
Один из подходов к проблеме утилизации СО2 - это превращение диоксида углерода в оксид углерода и метан (синтетический природный газ) - ключевые промежуточные продукты гидрогенизации СО2, которые с помощью известных технологий могут быть трансформированы в жидкие углеводороды.
Каталитическая конверсия по реакции СО2+Н2=СО+Н2О (RWGS), которая является обратной к реакции водяного сдвига, более актуальна в связи с большей реакционной способностью оксида углерода при умеренных температурах, по сравнению с метаном. Известно, что ряд металлов способны превращать углекислый газ в СО [Wang W., Wang S., Ma X., Gong J. // Recent advances in catalytic hydrogenation of carbon dioxide // Chem. Soc. Rev. (2011) 40: 3703-3727].
Нанесенные металлические катализаторы на основе благородных металлов (Pt, Ru, Rh) имеют высокую способность к диссоциации Н2, и таким образом они являются эффективными катализаторами гидрирования CO2. В работе [K.K. Bando, K. Soga, K. Kunimori and Н. Arakawa // Effect of Li additive on CO2 hydrogenation reactivity of zeolite supported Rh catalysts // Appl. Catal., A, 1998, 175, 67-81] в реакции гидрогенизации CO2 изучены родиевые катализаторы на основе цеолитов Y, промотированные литием. Установлено, что когда атомное отношение Li/Rh выше 10, основным продуктом является СО (селективность выше 87%), и образование метана значительно подавляется. Наличие атомов Li на поверхности создает новые активные центры, которые повышают адсорбцию СО2 и стабилизацию адсорбированного СО.
В [R.W. Dorner, D.R. Hardy, F.W. Williams, В.H. Davis and H.D. Willauer // Influence of Gas Feed Composition and Pressure on the Catalytic Conversion of CO2 to Hydrocarbons Using a Traditional Cobalt-Based Fischer-Tropsch Catalyst // Energy Fuels, 2009, 23, 4190-4195] при исследовании Pt-Co/Al2O3 катализаторов для конверсии CO2 в у/в было показано, что при давлении 20 атм и 220°С образуются углеводороды, в том числе и жидкие. Существенным недостатком Pt, Ru, Rh содержащих катализаторов является их высокая стоимость. Недостатком предлагаемого способа является низкая селективность по у/в С5+. Так, например, в смеси с соотношением Н2:CO2=1:1 селективность по метану составляет 93%, а при увеличении этого соотношения до 2:1 и 3:1 она растет до значения 100%.
Получение углеводородов в ходе прямого (одностадийного) гидрирования CO2 является, по существу, модификацией синтеза Фишера-Тропша (Ф-Т), где вместо СО используется СО2. Исследования в этой области разделены на две категории: получение углеводородов через метанол и напрямую из CO2 [J.F. Lee, W.S. Chern, М.D. Lee and Т.Y. Dong // Green Carbon Dioxide: Advances in CO2 Utilization // J. Chem. Eng., 2009, 70, 511-515]. Во втором случае гидрирование CO2 протекает через две стадии: RWGS реакцию и последующий синтез Ф-Т.
В [R.W. Dorner, D.R. Hardy, F.W. Williams, В.H. Davis and H.D. Willauer, Energy Fuels, 2009, 23, 4190-4195] отмечается, что в традиционных кобальтовых катализаторах синтеза Ф-Т в газовой смеси CO2 и H2, кобальт выступает в первую очередь в качестве катализатора метанизации, а не как катализатор синтеза Ф-Т. Так, в работе [А.N. Akin, М. Ataman, А.Е. Aksoylu and Z.I.  // CO2 fixation by hydrogenation over Co-precipitated CO/Al2O3 // React. Kinet. Catal. Lett., 2002, 76, 265-270] показано, что продукты гидрогенизации CO2 на Со/Al2О3 катализаторах содержат 70% метана. Смешанные Fe/Co катализаторы также демонстрируют низкую селективность в отношении жидких углеводородов [F. Tihay, А.С. Roger. G. Pourroy and A. Kiennemann // Role of the Alloy and Spinel in the Catalytic Behavior of Fe-Co/Cobalt Magnetite Composites under CO and CO2 Hydrogenation // Energy Fuels, 2002, 16, 1271-1276].
// CO2 fixation by hydrogenation over Co-precipitated CO/Al2O3 // React. Kinet. Catal. Lett., 2002, 76, 265-270] показано, что продукты гидрогенизации CO2 на Со/Al2О3 катализаторах содержат 70% метана. Смешанные Fe/Co катализаторы также демонстрируют низкую селективность в отношении жидких углеводородов [F. Tihay, А.С. Roger. G. Pourroy and A. Kiennemann // Role of the Alloy and Spinel in the Catalytic Behavior of Fe-Co/Cobalt Magnetite Composites under CO and CO2 Hydrogenation // Energy Fuels, 2002, 16, 1271-1276].
В патенте РФ №2430780 (10.10.2011) предложен способ приготовления нанокатализатора для синтеза Ф-Т на основе комплекса кобальта CoClo2⋅6Н2О, диспергированного в растворе полимерного стабилизатора – поли-N-винил-2-пирролидона (ПВП). Недостатком предлагаемой каталитической системы с использованием комплекса кобальта в ПВП является его низкая каталитическая активность в ходе конверсии синтез-газа (СГ). Так, в примере №9 при температуре 170°С и давлении 30 атм активность, выражаемая в частоте оборотов (мольСО/мольМе⋅ч), составляет всего 0,02.
В настоящее время большой ряд пористых металлорганических структур, типа MIL, изучается в катализе и других областях применения [V.P. Ananikov, Е.А. Khokhlova, M.P. Egorov, A.M. Shakharov, S.G. Zlotin, A.V. Kucherov. L.M. Kustov, M.L. Gening, N.E. Nifantiev // Organic and hybrid molecular systems // Mendeleev Commun., 2015, 25, 75-82]. Для гетерогенного катализа они имеют ряд неоспоримых преимуществ, по сравнению с традиционными микропористыми и мезопористыми неорганическими носителями, поскольку имеют правильную кристаллическую структуру, высокую удельную поверхность и перестраиваемые размеры пор, т.к могут быть синтезированы с использованием различных по размеру молекулы органических линкеров [F.A.A. Paz, J. Klinowski, S.M.F. Vilela, J.P.C.  , J.A.S. Cavaleiro, J. Rocha // Ligand design for functional metal-organic frameworks // Chem. Soc. Rev. 2012, 41, 1088-1110]. Однако известны лишь единичные примеры использования таких носителей для катализаторов в процессах получения жидких у/в из оксидов углерода.
, J.A.S. Cavaleiro, J. Rocha // Ligand design for functional metal-organic frameworks // Chem. Soc. Rev. 2012, 41, 1088-1110]. Однако известны лишь единичные примеры использования таких носителей для катализаторов в процессах получения жидких у/в из оксидов углерода.
Наиболее близким к настоящему изобретению является способ гидрогенизационной конверсии CO2, описанный в работе [R.Е. Owen, J.P. O'Byrne, D. Mattia, P. Plucinski, S.I. Pascu and M.D. Jones // Cobalt catalysts for the conversion of CO2 to light hydrocarbons at atmospheric pressure // Chem. Commun., 2013, 49, 11683]. В качестве носителей для кобальтовых катализаторов исследовались силикагели с различными текстурными характеристиками, а наночастицы кобальта наносили методом пропитки по влагоемкости из водных растворов нитрата кобальта. Авторами было установлено, что с увеличением размера пор силикагеля с 60 до 500 выход углеводородов С5+ существенно снижается при резком росте селективности по метану, которая приближается к 100%. Было показано, что при атмосферном давлении на катализаторе 20%Co/SiO2 в смеси Н2/CO2=3 конверсия CO2 составила 67,4%, при этом преимущественно (с селективностью 99,7%) образуется метан, а не жидкие продукты. Максимальный выход жидких углеводородов С5+ для модифицированного калием образца 20%Co/SiO2 составил около 2,6%, при селективности по С5+ углеводородам 9,5%, при этом селективность по метану достигала значения 54,7%.
выход углеводородов С5+ существенно снижается при резком росте селективности по метану, которая приближается к 100%. Было показано, что при атмосферном давлении на катализаторе 20%Co/SiO2 в смеси Н2/CO2=3 конверсия CO2 составила 67,4%, при этом преимущественно (с селективностью 99,7%) образуется метан, а не жидкие продукты. Максимальный выход жидких углеводородов С5+ для модифицированного калием образца 20%Co/SiO2 составил около 2,6%, при селективности по С5+ углеводородам 9,5%, при этом селективность по метану достигала значения 54,7%.
Существенными недостатками способа являются сравнительно высокая температура процесса (более 370°С), а также интенсивная метанизация, препятствующая образованию оксида углерода, который на второй стадии может быть вовлечен в последовательную реакцию Ф-Т с образованием С5+ у/в. Это и приводит к низкому выходу жидких у/в.
Техническим результатом изобретения является разработка эффективного нанокатализатора для одностадийного синтеза жидких углеводородов из диоксида углерода, позволяющего существенно увеличить выход и селективность по жидким С5+ у/в. Предлагаемый катализатор и способ конверсии диоксида углерода в жидкие у/в обеспечивает частичную утилизацию парникового газа - диоксида углерода, а также упрощение технологии процесса получения жидких углеводородов из CO2.
Для достижения технического результата предложен способ получения катализатора для гидрогенизационной конверсии диоксида углерода в жидкие углеводороды, в котором носитель для катализатора выполнен в виде пористой металлорганической каркасной структуры MIL-53(Al), которую получают в ходе сверхвысокочастотного СВЧ - активированного синтеза при атмосферном давлении и температуре 125-130°С путем реакции взаимодействия AlCl3×6H2O и 1,4-бензолдикарбоновой кислоты в смешанном растворителе - смеси воды и диметилформамида, а наночастицы металлического кобальта размером 5-10 нм наносят на носитель методом пропитки по влагоемкости из водных растворов соли Со(СН3СОО)2⋅4Н2O. Содержание наночастиц кобальта в катализаторе составляет 5-15% масс.
Способ гидрогенизационной конверсии диоксида углерода в жидкие углеводороды включает подачу сырьевой газовой смеси СО2 и водорода в проточный реактор с нагретым до температуры 260-340°С стационарным слоем катализатора, при этом в реактор подают газовую смесь с соотношением Н2/СО2=(3-4)/5 с объемной скоростью 500-1000 ч-1 при давлении 30 атм.
Изобретение поясняется чертежами, где на Фиг. 1 представлена микрофотография сканирующей электронной микроскопии (СЭМ) носителя MIL-53(Al), а на Фиг. 2 микрофотография сканирующей просвечивающей электронной микроскоскопии с полевой эмиссией (STEM-FE) предлагаемого в изобретении катализатора 5% Co/MIL-53(Al).
Из Фиг. 1 видно, что катализатор для конверсии диоксида углерода в жидкие углеводороды включает носитель в виде микропористого материала с гомогенным распределением нанокристаллов по размерам (длина около 500 нм). Кроме того, носитель характеризуется высокой удельной поверхностью ~ 1000 м2/г (БЭТ) и имеет поры с диаметром около 6,7  . Из Фиг. 2 видно, что наночастицы металлического кобальта с узким распределением по размеру (5-10 нм) располагаются как в порах, так и на поверхности носителя.
. Из Фиг. 2 видно, что наночастицы металлического кобальта с узким распределением по размеру (5-10 нм) располагаются как в порах, так и на поверхности носителя.
Образец MIL-53(Al) был выбран в качестве носителя для катализаторов из-за своей исключительной химической и термической стабильности. Его кристаллическая структура остается неизменной при температуре выше 520°С. Предлагаемый в изобретении катализатор обладает свойствами бифункционального катализатора, обладающего одновременно активностью в гидрогенизационной конверсии СО2 в синтез-газ (смесь СО и Н2), а также в процессе получения жидких углеводородов в смесях СО и Н2 по реакции Ф-Т. Такие свойства катализатора обеспечиваются, по-видимому, высокой дисперсностью металлических частиц кобальта, а также за счет регулирования распределения активного металла внутри и вне пор пористого каркасного металлорганического носителя.
Изобретение иллюстрируется следующими примерами.
Образец носителя для катализаторов MIL-53(Al) синтезировали при 125°С в течение 30 мин в ходе СВЧ активированной реакции взаимодействия AlCl3×6H2O и 1,4-бензолдикарбоновой кислоты в смешанном растворителе (Н2О и ДМФА) с использованием бытовой СВЧ печи "Vigor" с мощностью 200 ватт по методике, представленной в [Заявка на патент РФ №2015112652 от 08.04.2015].
Пример №1. Катализаторы Co/MIL-53(Al) были приготовлены методом пропитки полученного MIL-53(Al) по влагоемкости с использованием водного раствора Со(СН3СОО)2⋅4Н2O необходимой концентрации. Содержание кобальта составило 5, 10 и 15% масс. Перед проведением опытов образцы активировали в проточном реакторе в токе водорода при температуре 450°С и объемной скорости 1000 ч-1 в течение 2 часов.
Примеры №2-5. Испытания катализаторов проводили в проточной установке с трубчатым металлическим реактором (D=7 мм) с неподвижным слоем катализатора при давлении 1 и 30 атм. Смесь СО2 и водорода подавали в реактор с объемной скоростью 500-1000 ч-1 при загрузке катализатора 0,6 г (фракция 0,05-0,1 мм, объем слоя катализатора 1 см3). Температуру реакции задавали контроллером Термодат-17, связанным с термопарой Т1, размещенной в слое катализатора.
Газ на выходе из реактора анализировали на хроматографе модели 3700 на двух набивных колонках (2 м) - сита 5 (Н2, СН4 и СО) и HayeSep-Q (Н2, СО, СН4, CO2 С2) с использованием детектора катарометр, а в качестве устройства для ввода газовых проб использовали две обогреваемые петли постоянного объема. Объемное содержание этих газов определяли по соотношению площадей пиков компонентов в хроматограмме к площадям пиков чистых индивидуальных газов, при этом остальное (до 100%) приходится на неанализируемые углеводороды С3-C8.
(Н2, СН4 и СО) и HayeSep-Q (Н2, СО, СН4, CO2 С2) с использованием детектора катарометр, а в качестве устройства для ввода газовых проб использовали две обогреваемые петли постоянного объема. Объемное содержание этих газов определяли по соотношению площадей пиков компонентов в хроматограмме к площадям пиков чистых индивидуальных газов, при этом остальное (до 100%) приходится на неанализируемые углеводороды С3-C8.
Углеводородный газ реакции C1-C8, включающий унос жидких углеводородов С5-C8, анализировали in-situ на том же хроматографе на колонке SE-30 с использованием пламенно-ионизационного детектора. Хроматографические анализы проводили в изотермическом режиме при 65°С. Газ носитель - азот.
Результаты испытаний Co/MIL-53(Al) образцов в процессе одностадийного получения углеводородов в ходе гидрогенизационной конверсии углекислого газа представлены в таблице.
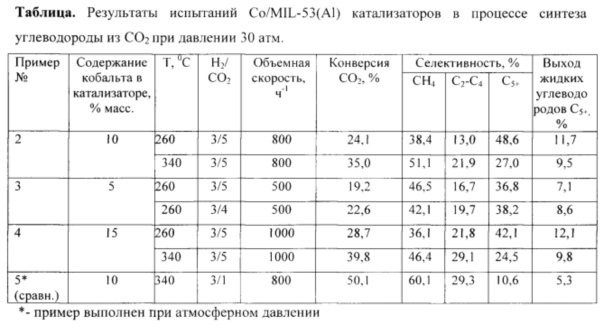
Сравнение результатов по настоящему изобретению (примеры №2-4 выполнены при давлении 30 атм) с результатами по изобретению-прототипу показывает, что при повышенном давлении с использованием предлагаемых в настоящем изобретении катализаторов при более низких температурах процесса достигается существенно более высокий выход жидких С5+углеводородов (до 12,1% против 2,6%, максимально полученного в изобретении прототипе). Кроме того, в сравнительном примере №5, проведенном в условиях, аналогичных изобретению-прототипу (при атмосферном давлении, в смеси с соотношением Н2/СО2=3), выход жидких углеводородов (5,3%) на предлагаемом в настоящем изобретении катализаторе также в 2 раза выше, чем в изобретении-прототипе (2,6%), при том что температура процесса конверсии диоксида углерода ниже (340°С, вместо 370°С в изобретении-прототипе), а содержание кобальта в предлагаемом катализаторе в 2 раза ниже.
Из сопоставления примеров №3 и 4 видно, что некоторый рост конверсии СО2 и выхода жидких у/в достигаются при изменении соотношения Н2/СО2 с 3/5 до 3/4, т.е. незначительном увеличении концентрации водорода в сырьевой смеси.
В составе жидких продуктов, полученных в настоящем изобретении в примерах №2-4, представляющих фракцию C5-C8 углеводородов, наблюдается образование как парафиновых, так и олефиновых углеводородов. Соотношение н-парафины/изопарафины составляет около 2-2,5, что не совсем типично для реакции ФТ с использованием традиционных кобальтовых катализаторов, когда преимущественно (до 80-85%) образуются н-алканы. Однако известно [О.Л. Елисеев // Технологии «газ в жидкость» // Ж. Рос. хим. об-ва им. Д.И. Менделеева, 2008, т. LII, №6], что с разбавлением СГ (в нашем случае в качестве разбавителя служит непрореагировавший CO2) существенно увеличивается количество изомеров. Содержание олефинов в составе образующихся по примерам №2-4 углеводородов C2-C8 находится в пределах 20-30%.
Следует отметить, что согласно термодинамическим расчетам равновесных концентраций реагентов и продуктов в реакции гидрирования CO2 в области исследованных температур при давлении 30 атм конверсия CO2 в СО не может превышать значений 18-20%. В примерах №2-4 по изобретению нами получены существенно более высокие значения конверсии CO2 по сравнению с термодинамическими расчетами (см. табл.). По нашему мнению, использование бифункционального Co/MIL-53(Al) катализатора, обладающего гидрирующей активностью и одновременно активностью в синтезе ФТ, приводит к смещению равновесия в реакции гидрирования CO2 в сторону образования СО, поскольку СО одновременно быстро вступает в реакцию синтеза ФТ, что и приводит к увеличению общей конверсии CO2 в двухстадийном процессе синтеза жидких углеводородов из CO2 с промежуточным образованием СО.
| название | год | авторы | номер документа |
|---|---|---|---|
| Двухстадийный способ получения пропионового альдегида | 2016 |
|
RU2619951C1 |
| Двухстадийный способ получения пропионовой кислоты | 2016 |
|
RU2616623C1 |
| Способ получения синтез-газа из CO | 2017 |
|
RU2668863C1 |
| Катализатор для получения синтез-газа и способ получения синтез-газа с его использованием | 2022 |
|
RU2784334C1 |
| ПОЛУЧЕНИЕ АЛКИЛИРОВАННЫХ АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ ИЗ МЕТАНА | 2005 |
|
RU2417974C2 |
| Катализатор для селективного гидрирования диоксида углерода с получением метанола | 2023 |
|
RU2804195C1 |
| КАТАЛИЗАТОР, СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ И СПОСОБ ГИДРИРОВАНИЯ ДИОКСИДА УГЛЕРОДА В МОНООКСИД УГЛЕРОДА | 2009 |
|
RU2395340C1 |
| Способ получения синтез-газа из CO | 2016 |
|
RU2632701C1 |
| Способ получения синтез-газа из CO | 2017 |
|
RU2660139C1 |
| МНОГОСТАДИЙНЫЙ СПОСОБ ФИШЕРА-ТРОПША | 2006 |
|
RU2409608C2 |

Изобретение относится к технологии переработки газообразного углеводородного сырья, а именно к способу получения катализатора для гидрогенизационной конверсии диоксида углерода в жидкие углеводороды, который включает нанесение наночастиц металлического кобальта на поверхность пористого носителя, при этом носитель выполнен в виде металлорганической каркасной структуры MIL-53(Al), которую получают в ходе сверхвысокочастотного СВЧ-активированного синтеза при атмосферном давлении и температуре 125-130°C путем реакции взаимодействия AlCl3×6H2O и 1,4-бензолдикарбоновой кислоты в смешанном растворителе - смеси воды и диметилформамида, а наночастицы металлического кобальта размером 5-10 нм наносят на носитель методом пропитки по влагоемкости из водных растворов соли Со(СН3СОО)2⋅4H2O, при этом содержание наночастиц в катализаторе составляет 5-15% масс. Изобретение также относится к способу гидрогенизационной конверсии диоксида углерода в жидкие углеводороды. Технический результат заключается в частичной утилизации парникового газа - диоксида углерода и упрощении технологии процесса получения жидких углеводородов. 2 н.п. ф-лы, 1 табл., 2 ил., 5 пр.
1. Способ получения катализатора для гидрогенизационной конверсии диоксида углерода в жидкие углеводороды, включающий нанесение наночастиц металлического кобальта на поверхность пористого носителя, отличающийся тем, что носитель выполнен в виде металлорганической каркасной структуры MIL-53(Al), которую получают в ходе сверхвысокочастотного СВЧ-активированного синтеза при атмосферном давлении и температуре 125-130°C путем реакции взаимодействия AlCl3×6H2O и 1,4-бензолдикарбоновой кислоты в смешанном растворителе - смеси воды и диметилформамида, а наночастицы металлического кобальта размером 5-10 нм наносят на носитель методом пропитки по влагоемкости из водных растворов соли Со(СН3СОО)2⋅4H2O, при этом содержание наночастиц в катализаторе составляет 5-15% масс.
2. Способ гидрогенизационной конверсии диоксида углерода в жидкие углеводороды, включающий подачу сырьевой газовой смеси СО2 и водорода в проточный реактор с нагретым стационарным слоем катализатора, отличающийся тем, что в проточный реактор подают сырьевую газовую смесь с соотношением Н2/СО2=(3-4)/5 в присутствии стационарного слоя катализатора, полученного по п. 1, нагретого до температуры 260-340°C с объемной скоростью 500-1000 ч-1 при давлении 30 атм.
| RHODRI E.OWEN et al., Cobalt catalysts for the conversion of CO 2 to light hydrocarbons at atmospheric pressure, Chem | |||
| Commun., 2013, 49, 11683-11685 | |||
| КАТАЛИЗАТОР ДЛЯ ПРОИЗВОДСТВА УГЛЕВОДОРОДА ИЗ СИНТЕЗ-ГАЗА, СПОСОБ ПОЛУЧЕНИЯ КАТАЛИЗАТОРА, СПОСОБ РЕГЕНЕРАЦИИ КАТАЛИЗАТОРА И СПОСОБ ПОЛУЧЕНИЯ УГЛЕВОДОРОДА ИЗ СИНТЕЗ-ГАЗА | 2007 |
|
RU2436627C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРИСТЫХ КООРДИНАЦИОННЫХ ПОЛИМЕРОВ MIL-53 | 2015 |
|
RU2578600C1 |
| Фармацевтическая композиция нейропротекторного действия для перорального применения на основе гексаметиленамид бис-(N-моносукцинил-L-глутамил-L-лизина) (варианты), выполненная в виде таблетки, диспергируемой в полости рта | 2018 |
|
RU2740754C1 |
| СПОСОБ ПОЛУЧЕНИЯ КАТАЛИЗАТОРА И СПОСОБ ПОЛУЧЕНИЯ УГЛЕВОДОРОДОВ С ЕГО ИСПОЛЬЗОВАНИЕМ | 2001 |
|
RU2286211C2 |
Авторы
Даты
2017-06-14—Публикация
2016-06-30—Подача