Изобретение относится к медицине, в частности к ревматологии и кардиологии.
Ревматоидный артрит является самым распространенным системным аутоиммунным ревматическим заболеванием, в основе развития которого лежит хроническое персистирующее воспаление синовиальной оболочки суставов с широким спектром внесуставных (системных) проявлений. Данные мета-анализов и ряда публикаций свидетельствуют, что ревматоидный артрит ассоциируется с увеличением на 50-60% риска сердечно-сосудистой летальности (Cardiovascular risk factor management in patients with RA compared to matched non-RA patients / Evo Alemao [et al.] // Rheumatology (Oxford). - 2016. - May, 55(5). - P. 809-816). При этом сердечно-сосудистая патология рассматривается как одно из внесуставных проявлений заболевания, а активность аутоиммунного воспаления обсуждается в качестве нового фактора риска атеросклеротического поражения сосудов. Поэтому важными характеристиками препаратов патогенетической терапии наряду с высокой противовоспалительной и болезнь-модифицирующей активностью является наличие свойств влиять на развитие и прогрессирование субклинического атеросклероза, диагностическими маркерами которого являются снижение эластичности и повышение резистентности артериальной стенки.
В соответствии с концепцией «treat tо target» основной целью фармакотерапии ревматоидного артрита является достижение ремиссии (или низкой активности) (EULAR recommendations for the management of rheumatoid arthritis with synthetic and biological disease-modifying antirheumatic drugs: 2013 update / Josef S. Smolen [et al.] // Ann. Rheum. Dis. - 2014. - 73. - P. 492-509), снижение риска коморбидных заболеваний, ухудшающих качество жизни пациентов и прогноз (Проект рекомендаций по лечению ревматоидного артрита Общероссийской общественной организации «Ассоциация ревматологов России». - 2014 (часть 1) / Е.Л. Насонов [и др.] // Научно-практическая ревматология. - 2014. - №52(5). - С. 477-494). В связи с чем особое значение имеет изучение кардиоваскулярных эффектов новой группы базисных противовоспалительных препаратов (БПВП), классифицируемых как генно-инженерные биологические препараты (ГИБП), в частности ингибиторов ФНО-α, поскольку до настоящего времени их влияние на прогрессирование атеросклероза при РА остается дискутабельным. Решение этой проблемы направлено на развитие персонизированного подхода к назначению ГИБП, позволяющего оптимизировать терапию, что сопряжено с уменьшением риска кардиоваскулярных осложнений, улучшением прогноза у больных ревматоидным артритом, позитивным влиянием на фармакоэкономическую составляющую применяемой терапии.
В качестве прототипа предлагаемого способа коррекции кардиоваскулярного риска и структурно-функциональных нарушений артериального русла при ревматоидном артрите можно рассматривать использование ингибиторов ФНО-α, в частности этанерцепта и инфликсимаба (Tumour necrosis factor antagonists and the risk of cardiovascular disease in patients with rheumatoid arthritis: a systematic literature review / Sarah L. Westlake [et al.] // Rheumatology. - 2011. - Vol. 50(5). - P. 518-531), которые являются одними из препаратов «первой линии» при недостаточном ответе на метотрексат и/или другие синтетические БПВП. В ряде работ установлено уменьшение толщины КИМ сонных артерий и снижение такого предиктора ССО, как скорость распространения пульсовой волны на фоне терапии ингибиторами ФНО-α при PA (Infliximab improves vascular stiffness in patients with rheumatoid arthritis / M. Wong [et al.] // Ann. Rheum. Dis. - 2009. - Vol. 68, N 8. - P. 1277-1284; Maki-Petaja, K.M. Anti-inflammatory drugs and statins for arterial stiffness reduction / K.M. Maki-Petaja, I.B. Wilkinson // Curr. Pharm. Des. - 2009. -Vol. 15, N 3. - P. 290-303; Rheumatoid arthritis is associated with increased aortic pulse-wave velocity, which is reduced by anti-tumor necrosis factor-alpha therapy / K.M. Maki-Petaja [et al.] // Circulation. - 2006. - Vol. 114. - P. 1185-1192; TNF-alpha antagonists reduce arterial stiffness in patients with rheumatoid arthritis and related arthropaties: a controlled study / K. Angel [et al.] // Ann. Rheum. Dis. - 2008. - Vol. 67 (Suppl. 21). - P. 160; Мещерина, H.C. Подходы к коррекции активности иммунного воспаления и ремоделирования кардиоваскулярного русла у больных ревматоидным артритом генно-инженерными биологическими препаратами: автореф. дис. … д-ра мед. наук: 14.03.09 / Н.С. Мещерина. - Курск, 2014. - 46 с.).
Однако указанный прототип имеет ряд недостатков, в частности, существует мнение о проатерогенном влиянии инфликсимаба на липидный спектр крови (Impact of TNF inhibition on insulin resistance and lipids levels in patients with rheumatoid arthritis / L.S. Tam [et al.] // Clin. Rheumatol. - 2007. - Vol. 26, N 9. - P. 1495-1498; Insulin resistance in rheumatoid arthritis: the impact of the anti-TNF-alpha therapy / M.A. Gonzalez-Gay [et al.] // Ann. NY. Acad. Sci. - 2010. - Vol. 1193. - P. 153-159; Modulation of lipoprotein plasma concentrations during long-term anti-TNF therapy in patients with active rheumatoid arthritis / C. Popa [et al.] // Ann. Rheum. Dis. - 2007. - Vol. 66, N 11. - P 1503-1507; Randomized, double blind, placebo-controlled, pilot trial of infliximab, a chimeric monoclonal antibody to tumor necrosis factor-alpha, in patients with moderate-to-severe heart failure: results of the anti-TNF Therapy Against Congestive Heart Failure [AT TACH] trial / E.S. Chung [et al.] // Circulation. - 2003. - Vol. 107. - P. 3133-3140), отсутствии действия на толщину КИМ и артериальную ригидность у больных РА с ССЗ (Генно-инженерные биологические препараты в лечении ревматоидного артрита / под ред. Е.Л. Насонова. - М.: ИМА-ПРЕСС, 2013. - 552 с.; Новикова, Д.С. Безболевая ишемия миокарда, нарушения вегетативной регуляции сердечной деятельности и эластических свойств артерий у женщин с ревматоидным артритом: автореф. дис. … д-ра мед. наук: 14.01.22, 14.01.05 / Д.С. Новикова. - М., 2013. - 58 с.; Gonzalez-Gay, М.А. Insulin resistance in rheumatoid arthritis: the impact of the anti-TNF-alpha therapy / M.A. Gonzalez-Gay, C. Gonzalez-Juanatey, T.R. Vazguez-Rodriguez // Ann. N.Y. Acad. Sci. - 2010. - Vol. 1193, N 1. - P. 153-159; The association between functional and morphological assessments of endothelial function in patients with rheumatoid arthritis: a cross-sectional study [Electronic resource] / A. Sandoo [et al.] // Arthritis Res. Ther. - 2013. - Vol. 15. - P. R107). Напротив, согласно данным других исследований инфликсимаб не вызывает проатерогенных изменений липидного спектра крови у больных РА (Линева, О.Г. Кардиоваскулярные эффекты генно-инженерных биологических препаратов (ингибиторов ФНОα и анти-В-клеточной терапии) у больных РА: автореф. дис. … канд. мед. наук: 14.01.22 / О.Г. Линева. - М., 2012. - 22 с.).
Среди группы ингибиторов ФНО-α голимумаб, относительно недавно (в 2012 году) зарегистрированный в Российской Федерации, занимает особое положение в связи с высокой клинической эффективностью, хорошей переносимостью и безопасностью, доказанными в рандомизированных плацебоконтролируемых исследованиях (Чичасова Н.В. Ингибитор фактора некроза опухоли-α голимумаб в лечении ревматоидного артрита / Н.В. Чичасова // Современная ревматология. - 2014. - №4. - С. 76-85).
Кроме того, установлено, что преимуществом голимумаба, несмотря на принципиальное сходство с другими генно-инженерными биологическими препаратами из категории моноклональных антител, является значительно меньшая частота обнаружения антител к препарату, высокая стойкость сывороточной концентрации и стабильность достигнутого уровня клинического ответа (Каратеев Д.Е. Голимумаб в лечении воспалительных заболеваний: роль иммуногенности / Д.Е. Каратеев // Современная ревматология. - 2015. - №9(4). - С. 20-24).
Установлено, что аффинность голимумаба к растворимому ФНО, определенная in vitro, превышает таковую инфликсимаба в 2,4 раза (Shealy D, Cai A, Lacy A, et al. Characterisation of golimumab (CNTO 148), a novel monoclonal antibody specific for human TNFα. Ann Rheum Dis. - 2007. - Vol. 66. - P. 151), что определяет высокую его активность связывать и нейтрализовать и растворимые, и мембранно-связанные формы ФНО (Voulgari PV. Emerging drugs for rheumatoid arthritis. Expert Opin Emerg Drags. - 2008. - Vol. 13. - P. 175-96. DOI: http://dx.doi.org/10.1517/14728214.13.l.175) Поэтому голимумаб рассматривается в качестве альтернативы первого ингибитора ФНО-α.
Однако следует отметить, что данные, касающиеся влияния голимумаба на снижение кардиоваскулярного риска, крайне немногочисленны и противоречивы.
Так, эффекты голимумаба на липидный спектр и маркеры воспаления (С-реактивный белок, фибриноген, интерлейкин-6, интерлейкин-8, молекулы адгезии и васкулоэндотелиальный фактор роста) были изучены в ходе рандомизированных двойных слепых плацебоконтролируемых исследованиях GO-BEFORE и CO-FORWARD. Полученные результаты свидетельствуют, что у больных РА, получавших комбинацию голимумаб и метотрексат, несмотря на некоторое увеличение уровня общего холестерина и липопротеидов низкой плотности (ЛПНП), индекс атерогенности, как правило, оставался стабильным, наблюдались благоприятные изменения в субфракции ЛПНП и положительная динамика в изменении концентрации воспалительных маркеров. При этом авторы полагают, что контроль активности воспаления при РА может положительно сказываться на маркерах сердечно-сосудистых заболеваний, однако для оценки влияния голимумаба на кардиоваскулярный риск необходимы долгосрочные исследования с большей численностью обследованных (Effects of golimumab, an anti-tumour necrosis factor-α human monoclonal antibody, on lipids and markers of inflammation / B.W. Kirkham [et al.] // Ann. Rheum. Dis. - 2014. - Vol. 73. - P. 161-169. doi:10.1136/annrheumdis-2012-202089).
Кроме того, в исследованиях GO-BEFORE, CO-FORWARD, а также GO-AFTER после 52 недель комбинированной терапии голимумабом и метотрексатом были получены чрезвычайно вариабельные и разнонаправленные изменения толщины КИМ, отмечалась некоторая тенденция к ее увеличению (Golimumab and cardiovascular disease: carotid artery ultrasound evaluation and cardiovascular adverse events / J. Bathon [et al.] // Ann. Rheum. Dis. - 2010. - Vol. 69 (Suppl 3). - P. 464). В то же время в другой работе продемонстрированы неубедительные доказательства влияния длительной терапии голимумабом на толщину КИМ общей сонной артерии, также не было обнаружено увеличение или снижение значимых кардиоваскулярных событий (Effect of Golimumab on Carotid Atherosclerotic Disease Measures and Cardiovascular Events in Inflammatory Arthritides / M.C. Wasko [et al.] // Journal of Clinical Rheumatology. - January 2014 - Vol. 20, Issue 1. - P. 1-10. doi:10.1097/RHU.0000000000000053).
Таким образом, до настоящего времени отсутствуют достоверные подтверждения влияния голимумаба на ранние проявления и выраженность атеросклеротического поражения сосудов при ревматоидном артрите, что не позволяет вынести окончательное суждение о действии препарата на структурно-функциональное состояние артериального русла.
Техническим результатом изобретения является разработка способа коррекции артериальной ригидности у больных ревматоидным артритом.
Технический результат достигается тем, что для уменьшения артериальной ригидности в качестве базисной противовоспалительной терапии больным ревматоидным артритом назначают голимумаб в дозе 50 мг подкожно 1 раз в 4 недели в один и тот же день, который наряду с иммуномодулирующим (иммуносупрессивным) и противовоспалительным эффектами, обладает вазопротективным действием, как на крупные сосуды эластического типа (уменьшение толщины КИМ и индекса жесткости ОСА, снижение индексов аугментации и жесткости), так и на мелкие артерии мышечного типа (снижение индекса отражения).
Способ осуществляется следующим образом: после установления диагноза больному ревматоидным артритом с активным течением заболевания и неэффективностью предшествующей терапии метотрексатом и/или другими синтетическими БПВП, для уменьшения артериальной ригидности в качестве базисной противовоспалительной терапии назначают голимумаб в дозе 50 мг подкожно 1 раз в 4 недели в один и тот же день.
Клиническая апробация предлагаемого метода проведена у 38 больных ревматоидным артритом молодого и среднего возраста без кардиоваскулярной патологии. Среди обследованных больных было 28 женщин и 10 мужчин, средний возраст которых составил 36,1 [26,3; 47,8] года, средняя длительность болезни - 18,2 [9,6; 35,6] мес. У 3 пациентов наблюдалась умеренная активность заболевания по DAS28, высокая активность имела место у 35 больных. У 79% (n=30) больных была II и у 21% (n=8) - III рентгенологическая стадия по Штейнброккеру. До включения в исследование пациенты получали предшествующую терапию БПВП: метотрексат - 63,1% (n=24), сульфасалазин - 5,2% (n=2), лефлуномид - 31,5% (n=12), а также нестероидные противовоспалительные препараты - 42,1% (n=16) и глюкокортикоиды - 26,3% (n=10). Все больные РА, включенные в исследование, были «наивными» по терапии ГИБП. Системные проявления заболевания были определены у 30 (79%) больных, среди которых наиболее часто встречались ревматоидные узелки (n=10) и амиотрофический синдром (n=21), также наблюдались анемия (n=3), нейропатия (n=2) и капиллярит (n=2).
Среди пациентов, включенных в исследование, у 8 (21%) больных имел место отягощенный по сердечно-сосудистым заболеваниям семейный анамнез, при оценке по модифицированной шкале SCORE, адаптированной для больных РА, в соответствии с рекомендациями EULAR и Клиническими рекомендациями по снижению риска сердечно-сосудистых осложнений у пациентов с хроническими воспалительными артритами (http://rheumatolog.ru/system/files/pdf/nacrec/natrec20.pdf) определен умеренный (n=20) или низкий (n=18) суммарный кардиоваскулярный риск. У 26 пациентов имел место РФ/АЦЦП-серонегативный субтип заболевания, 20 больных ревматоидным артритом были серопозитивны по РФ и/или АЦЦП.
Группу контроля составили 26 здоровых лиц в возрасте 38,8 [31,6; 46,7] лет (из них 19 (73%) женщин и 7 (27%) мужчин).
Для оценки структурно-функционального состояния артериального русла выполняли визуализацию сонных артерий с использованием метода дуплексного сканирования в М- и В-режимах после 10 минутного отдыха пациента на ультразвуковом комплексе Acuson X /10, оснащенного линейным датчиком 7,5 МГц. Измерение толщины КИМ ОСА осуществлялось в В-режиме в соответствии со стандартным протоколом (Кардиоваскулярная профилактика: нац. рек. // Кардиоваскулярная терапия и профилактика. - 2011. - №10, прил. 2. - 64 с.). В соответствии с рекомендациям ASE Consensus Statement для оценки толщины КИМ использовались средние значения, полученные в Carotid Atherosclerosis Progression Study, где показатели выше 75-й процентили в соответствующей возрастной группе считались высокими и соответствовали увеличению кардиоваскулярного риска (Use of carotid ultrasound to identify subclinical vascular disease and evaluate cardiovascular disease risk: A consensus statement from the American society of echocardiography carotid intima-media thickness task force endorsed by the society for vascular medicine / J.H. Stein [et al.] // J. Am. Soc. Echocar. - 2008. - Vol. 21, N 2. - P. 93-111). Оценка структурно-функциональных свойств OCA включала определение индекса жесткости (stiffnes index β), характеризующего локальную ригидность сосудистого русла, который вычисляли по формуле: β=log (САД/ДАД)/(ΔД/Д) (усл. ед.), где Д - диаметр общей сонной артерии в диастолу; ΔД - разница диаметров общей сонной артерии в систолу и диастолу; САД - систолическое артериальное давление (АД); ДАД - диастолическое АД (Kawasaki Т, Sasayama S, Yagi S. Noninvasive measurement of the age related changes in stiffness if major branches of the human arteries. Cardiovasc Res 1987; 144: 345-52).
Исследование региональной артериальной ригидности осуществлялось на основе контурного анализа пульсовой волны, регистрируемой методом фотоплетизмографии на аппарате «АнгиоСкан-01» (ООО «АнгиоСкан-Электроникс», Россия) в соответствии с требованиями по подготовке испытуемого и следующим протоколом: тест проводился в затемненной комнате после 15 минутного отдыха, в утренние часы, натощак, в удобном сидячем положении с неподвижными кистями с фотоплетизмографическими датчиками на концевых фалангах указательных пальцев. За 24 часа до исследования исключался прием кофеина, алкоголя и других стимуляторов, физические нагрузки и курение. По результатам контурного анализа пульсовой волны анализировали такие параметры, как индекс жесткости (SI, stiffness index), индекс отражения (RI, reflection index), индекс аугментации (Alp, augmentation index), центральное систолическое давление - прогноз (Spa, SystolicPressureAortic - prognosis).
Анализ результативности вмешательства базировался на промежуточных «суррогатных» критериях. Для оценки клинической эффективности терапии использовали критерии EULAR, основанные на динамике индекса DAS28. Оценку структурно-функциональных параметров артериального русла у больных РА проводили дважды: до лечения и после 52 недель терапии голимумабом.
На фоне применения голимумаба было установлено значимое снижение DAS28, начиная с 8-й недели лечения, к концу наблюдения хороший/умеренный эффект по критериям EULAR был достигнут у 79% больных (n=30), ремиссия наблюдалась у 40% пациентов с РА (n=Т5).
Определение структурно-функциональных показателей ОСА после лечения голимумабом показало, что среди больных ревматоидным артритом имело место уменьшение количества пациентов с толщиной КИМ ОСА, превышавшей значение 75-й процентили, высокий кардиоваскулярный риск сохранялся у 8 (21%) больных vs 30 (79%) пациентов до лечения. Анализ морфофункциональных показателей ОСА у больных ревматоидным артритом показал уменьшение среднегрупповых значений толщины КИМ ОСА в среднем на 31% (р<0,01), индекс жесткости ОСА снизился на 25% (р<0,05).
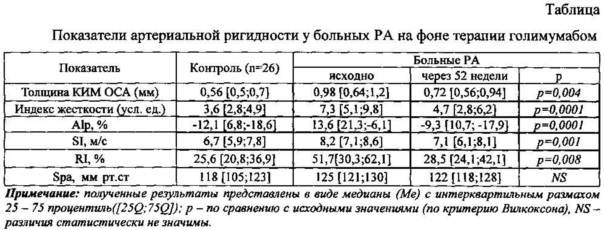
Установлено, что после терапии голимумабом у больных ревматоидным артритом индекс аугментации уменьшился в 2,8 раза (р=0,001) и приобрел отрицательное значение (см. таблицу). Также у обследованных больных на фоне терапии голимумабом было достигнуто уменьшение до контрольных значений индекса жесткости (SI), отражающего среднюю СРПВ по крупным резистивным сосудам, и индекса отражения (RI), который характеризует тонус мелких мышечных артерий и определяет наличие спазма, являющегося важным компонентом патогенеза ССЗ. Кроме того, выявлено, что у больных ревматоидным артритом изменения индекса SI не зависели от уровня АД в проксимальном отделе аорты и брахиоцефальных сосудах, потому как величина Spa у обследованного контингента ни исходно, ни после проведенной терапии не имела статистически значимых межгрупповых отличий.
Клинический пример. Больной Н., 34 года, поступил в ревматологическое отделение с жалобами на припухлость мелких суставов обеих кистей, ограничение движения в них, утреннюю скованность, сохраняющуюся до обеда; немотивированное снижение веса, слабость, повышение температуры тела до 37,8°С.
Из анамнеза: считает себя больным около года, принимает НПВП с непродолжительным эффектом, метотрексат 25 мг в неделю, фолиевую кислоту 5 мг.
Объективно: пониженного питания, кожные покровы бледные, отмечается припухлость лучезапястных, пястно-фаланговых и проксимальных межфаланговых суставов обеих кистей, гипертермия кожи над ними, положительный симптом поперечного сжатия кисти, ограничение движений; на разгибательной поверхности проксимальных межфаланговых суставов 2-го и 3-го пальцев правой кисти ревматоидные узелки; имеет место дефигурация коленных и голеностопных суставов, повышение температуры кожи над ними, ограничение объема движений из-за болей. Дыхание в легких везикулярное, хрипов нет. Тоны сердца ясные, ритм правильный. ЧСС-78 уд. в мин, АД - 130/70 мм рт.ст. Живот мягкий безболезненный. Печень не увеличена, селезенка не пальпируется.
При обследовании:
- общий анализ крови: эр. - 2,8⋅1012 /л, Нв - 110 г/л, ЦП - 0,95; тромб. - 352⋅109 /л, лейк. - 8,4⋅109/л, п - 6%, с - 68%, э - 1%, лимф. - 21%, мон. - 4%, СОЭ - 48 мм/ч.
- ИФА сыворотки крови: АЦЦП - 21 Ед/мл (N≤5 Ед/мл), РФ - 64 МЕ/мл (N≤20 МЕ/мл);
- рентгенография кистей и стоп: околосуставной остеопороз, щели кистевых суставов сужены, множественные эрозии.
Заключение: Ревматоидный артрит, серопозитивный по РФ и АЦЦП, активность III (DAS28 - 7,06), развернутая стадия, эрозивный вариант, III стадия по Штейнброккеру, с системными проявлениями: анемия, ревматоидные узелки, лихорадка, ФК II.
В рамках апробации метода выполнены:
- дуплексное сканирование сонных артерий: ход сонных артерий без значимых деформаций, просвет без патологических включений с обеих сторон, гемодинамика кровотока с обеих сторон не изменена. Средний диаметр левой ОСА - 5,7 мм, правой ОСА - 5,1 мм. Эхогенность КИМ повышена, дифференцировка на слои сохранена, в типичном месте ОСА утолщена - до 1,1 мм слева и 1,2 мм справа;
- контурный анализ пульсовой волны: ЧСС - 75 уд/мин, возраст сосудистой системы - 72 года, тип кривой - А: 100%, AIp - 28,4%, SI - 9,1 м/сек, RI - 62,1%, Spa - 128 мм рт.ст.
В качестве базисной терапии назначен голимумаб в дозе 50 мг подкожно 1 раз в 4 недели в один и тот же день.
На фоне терапии голимумабом через 52 недели имело место статистически значимое снижение СОЭ с 48 мм/ч до 12 мм/ч и СРБ с 15,6 мг % до 1,2 мг %, уровень АЦЦП уменьшился до 7 Ед/мл, IgM РФ в сыворотке крови - 10 МЕ/мл.
Начиная с 6-й недели лечения отмечалась положительная динамика DAS28, к концу наблюдения DAS28 составил 1,8 балла, что свидетельствует о достижении ремиссии РА.
При дуплексном сканировании сонных артерий: ход сонных артерий без значимых деформаций, просвет без патологических включений с обеих сторон, гемодинамика кровотока с обеих сторон не изменена. Средний диаметр левой ОСА - 5,4 мм, правой - 5,2 мм. Эхогенность КИМ повышена, дифференцировка на слои сохранена, в типичном месте ОСА не утолщена - до 0,7 мм слева, до 0,8 мм справа.
При контурном анализе пульсовой волны: ЧСС - 76 уд/мин, возраст сосудистой системы - 45 лет, тип кривой - В: 20%; С: 80%, AIp - -8,9%, SI - 7,2 м/сек, RI - 32,7%, Spa - 124 мм рт.ст.
Таким образом, приведенная клиническая ситуация свидетельствует, что голимумаб, наряду с иммуномодулирующим (иммуносупрессивным) и противовоспалительным эффектами, обладает вазопротективным действием на крупные сосуды эластического типа (уменьшение толщины КИМ и индекса жесткости ОСА, снижение индексов аугментации и жесткости) и на мелкие артерии мышечного типа (снижение индекса отражения). Достигнутое уменьшение признаков субклинического поражения артериального русла под влиянием терапии голимумабом потенциально связано со снижением кардиоваскулярного риска на фоне контроля хронического воспаления при ревматоидном артрите, что открывает перспективы для профилактики сердечно-сосудистых заболеваний, улучшения прогноза и качества жизни данной категории больных.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ коррекции вазомоторной дисфункции эндотелия и артериальной ригидности у больных ревматоидным артритом | 2018 |
|
RU2696285C1 |
| СПОСОБ КОРРЕКЦИИ СТРУКТУРНО-ФУНКЦИОНАЛЬНЫХ НАРУШЕНИЙ АРТЕРИАЛЬНОГО РУСЛА У БОЛЬНЫХ РЕВМАТОИДНЫМ АРТРИТОМ | 2015 |
|
RU2572709C1 |
| СПОСОБ ДИАГНОСТИКИ ГИПЕРТРОФИИ ЛЕВОГО ЖЕЛУДОЧКА У БОЛЬНЫХ РЕВМАТОИДНЫМ АРТРИТОМ | 2009 |
|
RU2429785C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ АКТИВНОСТИ ЗАБОЛЕВАНИЯ У ПАЦИЕНТОВ С РЕВМАТОИДНЫМ АРТРИТОМ | 2022 |
|
RU2790525C1 |
| СПОСОБ ПРОГНОЗА ЭФФЕКТИВНОСТИ ЛЕЧЕНИЯ РЕВМАТОИДНОГО АРТРИТА СИМВАСТАТИНОМ | 2008 |
|
RU2367430C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АКТИВНОСТИ ПСОРИАТИЧЕСКОГО АРТРИТА | 2020 |
|
RU2746884C1 |
| Способ определения высокого риска атеросклероза сонных артерий при ревматоидном артрите | 2020 |
|
RU2740246C1 |
| СПОСОБ ДИАГНОСТИКИ АНЕМИИ ХРОНИЧЕСКОГО ЗАБОЛЕВАНИЯ У БОЛЬНЫХ РЕВМАТОИДНЫМ АРТРИТОМ | 2021 |
|
RU2783248C1 |
| СПОСОБ ОЦЕНКИ ТЯЖЕСТИ ЭНДОТЕЛИАЛЬНОЙ ДИСФУНКЦИИ У ПАЦИЕНТОВ С РЕВМАТОИДНЫМ АРТРИТОМ | 2013 |
|
RU2536294C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПОКАЗАНИЙ К НАЧАЛУ ПРИЕМА ГЕННО-ИНЖЕНЕРНЫХ БИОЛОГИЧЕСКИХ ПРЕПАРАТОВ ПРИ НЕЭФФЕКТИВНОСТИ БАЗИСНЫХ ПРОТИВОВОСПАЛИТЕЛЬНЫХ ПРЕПАРАТОВ ПРИ РАННИХ ФОРМАХ ПСОРИАТИЧЕСКОГО АРТРИТА | 2020 |
|
RU2731807C1 |
Изобретение относится к медицине, в частности к ревматологии и кардиологии, и может быть использовано для коррекции артериальной ригидности у больных ревматоидным артритом. Способ включает введение больному с активным течением заболевания и неэффективностью предшествующей терапии метотрексатом и/или другими синтетическими БПВП в качестве базисной противовоспалительной терапии голимумаба в дозе 50 мг подкожно 1 раз в 4 недели в один и тот же день. Использование изобретения обеспечивает уменьшение артериальной ригидности у данной категории больных за счет вазопротективного действия голимумаба как на крупные сосуды эластического типа (уменьшение толщины КИМ и индекса жесткости ОСА, снижение индексов аугментации и жесткости), так и на мелкие артерии мышечного типа (снижение индекса отражения). 1 табл., 1 пр.
Способ коррекции артериальной ригидности у больных ревматоидным артритом, включающий оценку вазопротективного действия базисных противовоспалительных препаратов, отличающийся тем, что больному с активным течением заболевания и неэффективностью предшествующей терапии метотрексатом и/или другими синтетическими БПВП, в качестве базисной противовоспалительной терапии назначают голимумаб в дозе 50 мг подкожно 1 раз в 4 недели в один и тот же день.
Авторы
Даты
2017-06-21—Публикация
2016-07-11—Подача