Область техники, к которой относится изобретение
Настоящее изобретение относится к лекарственному препарату для лечения и/или профилактики рака, характеризуемому сочетанием антитела или его фрагмента, обладающего иммунологической реактивностью по отношению к белку CAPRIN-1, с противоопухолевым средством, и к применению такого препарата.
Уровень техники
Рак является лидирующей причиной смертности. Проводимая в настоящее время терапия рака заключается в сочетании основного хирургического вмешательства с лучевой терапией и химиотерапией. Кроме того, современное лечение включает в себя проведение сходного терапевтического лечения всех пациентов, имеющих рак одного и того же типа и на одной и той же стадии. По меньшей мере, в случае 40% пациентов первичная терапия оказывается неудачной, и поэтому их подвергают воздействию дополнительной серии лечения. Если лечение пациентов снова оказывается неудачным, появляются метастазы рака, в конце концов приводя к повышенной вероятности смертельного исхода. Таким образом, современная лучевая терапия и химиотерапия не могут быть совместимы с различными типами рака или отдельными пациентами с раком, и хирургическое лечение само по себе в настоящее время также недостаточно для полного излечения рака почти во всех случаях.
Различные основанные на антителах лекарственные средства, мишенью которых являются антигенные белки на злокачественных клетках, для лечения рака появились во всем мире в качестве способа преодоления указанных выше проблем в лечении рака. Конкретными примерами являются следующие средства. Было показано, что герцептин (зарегистрированная торговая марка), содержащий в качестве активного ингредиента моноклональное антитело, специфично связывающееся с Her2, продажи которого были одобрены в 1998 году в качестве терапевтического средства для пациентов с метастатическим раком молочной железы, оказывает такое клиническое действие, что герцептин может снижать количество смертельных исходов у пациентов с рецидивирующим и метастатическим раком молочной железы среди пациентов с метастатическим раком молочной железы, экспрессирующими Her2. Также было продемонстрировано, что герцептин не вызывает каких-либо других тяжелых побочных эффектов, кроме токсичности для сердца, по сравнению с обычными химиотерапевтическими средствами. В качестве другого заслеживающего внимания признака были показаны терапевтические эффекты комбинированного применения герцептина с химиотерапевтическими средствами против рака молочной железы (патентная литература 1-3). Однако большинство антигенных белков на злокачественных клетках, являющихся мишенью основанных на антителах лекарственных средств, таких как Her2, также экспрессируются в нормальных клетках, так что при введении антител цитотоксически повреждаются не только злокачественные клетки, но также и нормальные клетки, экспрессирующие антигены. В результате побочные эффекты могут вызывать беспокойство.
Цитоплазматический и ассоциированный с пролиферацией белок 1 (CAPRIN-1) экспрессируется, когда нормальные клетки в фазе покоя активируются или подвергаются клеточному делению, и он является внутриклеточным белком, который, как известно, образует внутриклеточные стрессовые гранулы с РНК в клетках для участия в транспорте мРНК и регуляции трансляции. При этом существует много других названий указанного CAPRIN-1, таких как GPI-заякоренный мембранный белок 1 или поверхностный маркерный белок 1 мембранного компонента (M11S1), поскольку такие белки были известны как якобы белки клеточной мембраны. Такие названия происходят на основании сообщения о том, что последовательность гена CAPRIN-1 соответствует мембранному белку, имеющему GPI-связывающую область и экспрессируемому в злокачественных клетках прямой и ободочной кишки (непатентная литература 1). Однако последовательность гена CAPRIN-1, представленная в указанном сообщении, оказалась неправильной, как было выявлено позднее. Недавно появилось следующее сообщение; а именно, делеция одного нуклеотида в последовательности гена CAPRIN-1, зарегистрированной в GenBank или тому подобной, вызывает сдвиг рамки, так что происходит утрата 80 аминокислот из C-конца, приводя к образованию артефакта (74 аминокислоты), который соответствует GPI-связывающей части, указанной в предыдущем сообщении, и кроме того, также присутствует другая ошибка с 5’-стороны генной последовательности, так что происходит утрата 53 аминокислот из N-конца (непатентная литература 2). Также недавно появилось сообщение о том, что белок, кодируемый последовательностью гена CAPRIN-1, зарегистрированной в GenBank или тому подобной, не является белком клеточной мембраны (непатентная литература 2).
Кроме того, на основе сообщения в непатентной литературе 1 о том, что CAPRIN-1 является белком клеточной мембраны, в патентной литературе 4 и 5 описано, что CAPRIN-1 (в качестве белка клеточной мембраны) под названием M11S1 может быть использован в качестве мишени для основанного на антителах лекарственного средства при терапии рака, хотя в рабочих примерах не описано лечение с применением антитела против данного белка. Однако, как сообщается в непатентной литературе 2, обычно полагали со времени подачи патентного документа 4 до настоящего времени, что CAPRIN-1 не экспрессируется на поверхности клетки. Содержание патентных документов 4 и 5, основанных только на неверной информации о том, что CAPRIN-1 является белком клеточной мембраны, не следует понимать как обычный уровень техники, известный специалистам в данной области.
Литература известного уровня техники
Патентная литература
Патентная литература 1: Публикация патента Японии (Kokai) No. 2006-316040A.
Патентная литература 2: патент США № 7485302.
Патентная литература 3: патент США № 7449184.
Патентная литература 4: публикация патента США № 2008/0075722.
Патентная литература 5: международная публикация WO2005/100998.
Непатентная литература
Непатентная литература 1: J. Biol. Chem., 270: 20717-20723, 1995.
Непатентная литература 2: J. Immunol., 172: 2389-2400, 2004.
Сущность изобретения
Задача, решаемая изобретением
Целью настоящего изобретения является идентификация белка ракового антигена, специфично экспрессируемого на поверхности злокачественной клетки, для сочетания антитела, мишенью которого является белок ракового антигена, с противоопухолевым средством, и таким образом обеспечение применения в качестве лекарственного препарата для лечения и/или профилактики рака.
Проблема, решаемая изобретением
Целями настоящего изобретения являются: идентификация белка ракового антигена, специфично экспрессируемого на поверхности злокачественной клетки, и применение антитела, мишенью которого является белок ракового антигена, в качестве средства для лечения и/или профилактики рака.
Способы решения проблемы
В результате интенсивных исследований авторы настоящего изобретения в настоящее время получили кДНК, кодирующую белок, который связывается с антителом, присутствующем в сыворотке собак с раком молочной железы, способом SEREX, используя как библиотеки кДНК, полученные из тканей семенников собак, так и сыворотки собак с раком молочной железы. Кроме того, авторы настоящего изобретения получили в настоящее время белки CAPRIN-1, имеющие аминокислотные последовательности, пронумерованные четными числами среди последовательностей SEQ ID NO: 2-30, и антитела против таких белков CAPRIN-1, на основе полученного гена собак и соответствующих гомологичных генов человека, коровы, лошади, мыши и кур. Таким образом, авторы настоящего изобретения обнаружили в настоящее время, что белки CAPRIN-1 специфично экспрессируются в клетках рака, таких как рак молочной железы, опухоль головного мозга, лейкоз, лимфома, рак легкого, рак шейки матки, рак мочевого пузыря, рак пищевода, рак прямой и ободочной кишки, рак желудка и рак почек, и что часть белка CAPRIN-1 специфично экспрессируется на поверхности каждой злокачественной клетки. Таким образом, авторы изобретения в настоящее время обнаружили, что антитело или антитела против части CAPRIN-1, экспрессируемой на поверхности каждой злокачественной клетки можно сочетать с конкретным противоопухолевым средством, получая при этом значимые терапевтические эффекты при лечении рака. На основе указанных открытий было осуществлено настоящее изобретение, которое описано ниже.
Термин «рак», в используемом в настоящем описании смысле, применяют взаимозаменяемо с терминами «опухоль» или «карцинома».
Настоящее изобретение имеет следующие отличительные признаки.
(1) Лекарственный препарат для лечения и/или профилактики рака, включающий в себя сочетание антитела или его фрагмента, обладающего иммунологической реактивностью по отношению к белку CAPRIN-1, и одного или двух или больше типов противоопухолевых средств, при этом антитело или фрагмент и противоопухолевое средство или противоопухолевые средства объединяют вместо или используют по отдельности.
(2) Лекарственный препарат по п. (1) указанному выше, в котором антитело или его фрагмент, обладающий иммунологической реактивностью по отношению к указанному выше белку CAPRIN-1, представляет собой антитело или его фрагмент, который специфично связывается с внеклеточной областью белка CAPRIN-1, существующей на поверхности злокачественной клетки.
(3) Лекарственный препарат по п. (1) или (2), указанному выше, в котором антитело или его фрагмент, обладающий иммунологической реактивностью по отношению к указанному выше белку CAPRIN-1, представляет собой антитело или его фрагмент, который специфично связывается с полипептидом, имеющим аминокислотную последовательность, представленную в виде SEQ ID NO: 37, во внеклеточной области белка CAPRIN-1, существующей на поверхности злокачественной клетки, или аминокислотную последовательность, имеющую 80% или более высокую идентичность последовательности с аминокислотной последовательностью, представленной в виде SEQ ID NO: 37.
(4) Лекарственный препарат по любому из пп. (1)-(3), указанному выше, в котором указанный выше белок CAPRIN-1 является белком человека.
(5) Лекарственный препарат по любому из пп. (1)-(4), указанному выше, в котором указанным выше противоопухолевым средством являются любые противоопухолевые средства, которые описаны в настоящей публикации.
(6) Лекарственный препарат по п. (5), указанному выше, в котором противоопухолевое средство выбрано из группы, состоящей из циклофосфамида, паклитаксела, доцетаксела, винорелбина и их фармацевтически приемлемых солей и производных.
(7) Лекарственный препарат по любому из п.п. (1)-(6), указанному выше, в котором злокачественной опухолью является рак молочной железы, опухоль головного мозга, лейкоз, лимфома, рак легкого, мастоцитома, рак почек, рак шейки матки, рак мочевого пузыря, рак пищевода, рак желудка или рак прямой и ободочной кишки.
(8) Лекарственный препарат по любому из пп. (1)-(7), указанному выше, в котором антитело является моноклональным антителом, поликлональным антителом или рекомбинантным антителом.
(9) Лекарственный препарат по любому из пп. (1)-(8), указанному выше, в котором антитело является антителом человека, гуманизированным антителом, химерным антителом, одноцепочечным антителом или биспецифичным антителом.
(10) Способ лечения и/или профилактики рака, включающий в себя введение лекарственного препарата по любому из пп. (1)-(9), указанному выше, субъекту, у которого предполагается наличие рака.
(11) Способ по п. (10), указанному выше, включающий в себя введение субъекту антитела или его фрагмента и противоопухолевого средства, которые находятся в указанном выше лекарственном препарате, одновременно или раздельно.
Настоящее описание включают все или часть содержания, которое раскрыто в описаниях и/или на чертежах в заявке на выдачу патента Японии № 2010-023455, на основании которой настоящая заявка притязает на приоритет.
Преимущества настоящего изобретения
Согласно настоящему изобретению могут быть получены неожиданные синергетические эффекты в виде уменьшения и регрессии массивного рака без выявления значимых побочных эффектов.
Краткое описание чертежей
Фиг.1 показывает картины экспрессии генов, кодирующих белки CAPRIN-1, в нормальных тканях и в линиях опухолевых клеток. Указатель № 1 обозначает картины экспрессии генов, кодирующих белки CAPRIN-1, и указатель № 2 обозначает картины экспрессии генов GAPDH.
Фиг.2 показывает цитотоксичность, проявляемую моноклональными анти-CAPRIN-1-антителами (№1-№11), которые взаимодействуют с клеточной поверхностью линии злокачественных клеток молочной железы MDA-MB-157, которые экспрессируют CAPRIN-1. Указатель №3 обозначает цитотоксическую активность, проявляемую в случае добавления моноклонального анти-CAPRIN-1-антитела №1. Указатель №4 обозначает цитотоксическую активность, проявляемую в случае добавления моноклонального анти-CAPRIN-1-антитела № 2. Указатель № 5 обозначает цитотоксическую активность, проявляемую в случае добавления моноклонального анти-CAPRIN-1-антитела №5. Указатель №6 обозначает цитотоксическую активность, проявляемую в случае добавления моноклонального анти-CAPRIN-1-антитела №4. Указатель № 7 обозначает цитотоксическую активность, проявляемую в случае добавления моноклонального анти-CAPRIN-1-антитела № 5. Указатель № 8 обозначает цитотоксическую активность, проявляемую в случае добавления моноклонального анти-CAPRIN-1-антитела №6. Указатель № 9 обозначает цитотоксическую активность, проявляемую в случае добавления моноклонального анти-CAPRIN-1-антитела №7. Указатель № 10 обозначает цитотоксическую активность, проявляемую в случае добавления моноклонального анти-CAPRIN-1-антитела №8. Указатель № 11 обозначает цитотоксическую активность, проявляемую в случае добавления моноклонального анти-CAPRIN-1-антитела №9. Указатель № 12 обозначает цитотоксическую активность, проявляемую в случае добавления моноклонального анти-CAPRIN-1-антитела №10. Указатель № 13 обозначает цитотоксическую активность, проявляемую в случае добавления моноклонального анти-CAPRIN-1-антитела №11. Указатель № 14 обозначает цитотоксическую активность, проявляемую в случае добавления моноклонального антитела, которое реактивно по отношению к самому белку CAPRIN-1, но не взаимодействует с поверхностью злокачественной клетки. Указатель № 15 обозначает цитотоксическую активность, проявляемую в случае добавления PBS вместо антител.
Фиг. 3 показывает противоопухолевое действие, получаемое при использовании противоопухолевого средства циклофосфамида в сочетании с моноклональным анти-CAPRIN-1-антителом, взаимодействующим с поверхностью злокачественных клеток, у голых мышей, которым трансплантировали линию злокачественных клеток молочной железы MCF-7, экспрессирующих CAPRIN-1. Указатель №16 обозначает размер опухоли у мыши при добавлении PBS вместо антитела. Указатель № 17 обозначает размер опухоли у мыши при введении циклофосфамида. Указатель № 18 обозначает размер опухоли у мыши при введении моноклонального анти-CAPRIN-1-антитела №2. Указатель № 19 обозначает размер опухоли у мыши при введении циклофосфамида и анти-Her2-антитела. Указатель № 20 обозначает размер опухоли у мыши при введении циклофосфамида и моноклонального анти-CAPRIN-1-антитела №2.
На фиг. 4 показано противоопухолевое действие, полученное при использовании противоопухолевого средства паклитаксела в сочетании с моноклональным анти-CAPRIN-1-антителом, которое взаимодействует с поверхностью злокачественных клеток, у голых мышей, которым трансплантировали линию злокачественных клеток молочной железы MCF-7, экспрессирующих CAPRIN-1. Указатель № 21 обозначает размер опухоли у мыши при введении PBS вместо антитела. Указатель № 22 обозначает размер опухоли у мыши при введении паклитаксела. Указатель № 23 обозначает размер опухоли у мыши при введении моноклонального анти-CAPRIN-1-антитела №2. Указатель № 24 обозначает размер опухоли у мыши при введении паклитаксела и анти-Her2-антитела. Указатель № 25 обозначает размер опухоли у мыши при введении паклитаксела и моноклонального анти-CAPRIN-1-антитела №2.
На фиг. 5 показано противоопухолевое действие, полученное при использовании противоопухолевого средства доцетаксела в сочетании с моноклональным анти-CAPRIN-1-антителом, взаимодействующим с поверхностью злокачественных клеток, у голых мышей, которым трансплантировали линию злокачественных клеток молочной железы MCF-7, экспрессирующих CAPRIN-1. Указатель № 26 обозначает размер опухоли у мыши при введении PBS вместо антитела. Указатель № 27 обозначает размер опухоли у мыши при введении доцетаксела. Указатель № 28 обозначает размер опухоли у мыши при введении моноклонального анти-CAPRIN-1-антитела №2. Указатель № 29 обозначает размер опухоли у мыши при введении доцетаксела и анти-Her2-антитела. Указатель № 30 обозначает размер опухоли у мыши при введении доцетаксела и моноклонального анти-CAPRIN-1-антитела №2.
На фиг. 6 показано противоопухолевое действие, полученное при использовании противоопухолевого средства винорелбина в сочетании с моноклональным анти-CAPRIN-1-антителом, взаимодействующим с поверхностью злокачественных клеток у голой мыши, которой трансплантировали линию злокачественных клеток молочной железы MCF-7, экспрессирующих CAPRIN-1. Указатель № 31 обозначает размер опухоли у мыши при введении PBS вместо антитела. Указатель № 32 обозначает размер опухоли у мыши при введении винорелбина. Указатель № 33 обозначает размер опухоли у мыши при введении моноклонального анти-CAPRIN-1-антитела №2. Указатель № 34 обозначает размер опухоли у мыши при введении винорелбина и анти-Her2-антитела. Указатель № 35 обозначает размер опухоли у мыши при введении винорелбина и моноклонального анти-CAPRIN-1-антитела №2.
На фиг. 7 показано противоопухолевое действие, полученное при использовании противоопухолевого средства циклофосфамида в сочетании с моноклональным анти-CAPRIN-1-антителом, взаимодействующим с поверхностью злокачественных клеток, у голой мыши, которой трансплантировали линию злокачественных клеток молочной железы MCF-7, экспрессирующих CAPRIN-1. Указатель № 36 обозначает размер опухоли у мыши при введении PBS вместо антитела. Указатель № 37 обозначает размер опухоли у мыши при введении циклофосфамида. Указатель № 38 обозначает размер опухоли у мыши при введении моноклонального анти-CAPRIN-1-антитела №9. Указатель № 39 обозначает размер опухоли у мыши при введении циклофосфамида и анти-Her2-антитела. Указатель № 40 обозначает размер опухоли у мыши при введении циклофосфамида и моноклонального анти-CAPRIN-1-антитела №9.
На фиг. 8 показано противоопухолевое действие, полученное при использовании противоопухолевого средства паклитаксела в сочетании с моноклональным анти-CAPRIN-1-антителом, взаимодействующим с поверхностью злокачественных клеток, у голой мыши, которой трансплантировали линию злокачественных клеток молочной железы MCF-7, экспрессирующих CAPRIN-1. Указатель № 41 обозначает размер опухоли у мыши при введении PBS вместо антитела. Указатель № 42 обозначает размер опухоли у мыши при введении паклитаксела. Указатель № 43 обозначает размер опухоли у мыши при введении моноклонального анти-CAPRIN-1-антитела №9. Указатель № 44 обозначает размер опухоли у мыши при введении паклитаксела и анти-Her2-антитела. Указатель № 45 обозначает размер опухоли у мыши при введении паклитаксела и моноклонального анти-CAPRIN-1-антитела №9.
На фиг. 9 показано противоопухолевое действие, полученное при использовании противоопухолевого средства доцетаксела в сочетании с моноклональным анти-CAPRIN-1-антителом, взаимодействующим с поверхностью злокачественных клеток, у голой мыши, которой трансплантировали линию злокачественных клеток молочной железы MCF-7, экспрессирующих CAPRIN-1. Указатель № 46 обозначает размер опухоли у мыши при введении PBS вместо антитела. Указатель № 47 обозначает размер опухоли у мыши при введении доцетаксела. Указатель № 48 обозначает размер опухоли у мыши при введении моноклонального анти-CAPRIN-1-антитела №9. Указатель № 49 обозначает размер опухоли у мыши при введении доцетаксела и анти-Her2-антитела. Указатель № 50 обозначает размер опухоли у мыши при введении доцетаксела и моноклонального анти-CAPRIN-1-антитела №9.
На фиг. 10 показано противоопухолевое действие, полученное при использовании противоопухолевого средства винорелбина в сочетании с моноклональным анти-CAPRIN-1-антителом, взаимодействующим с поверхностью злокачественных клеток, у голой мыши, которой трансплантировали линию злокачественных клеток молочной железы MCF-7, экспрессирующих CAPRIN-1. Указатель № 51 обозначает размер опухоли у мыши при введении PBS вместо антитела. Указатель № 52 обозначает размер опухоли у мыши при введении винорелбина. Указатель № 53 обозначает размер опухоли у мыши при введении моноклонального анти-CAPRIN-1-антитела №9. Указатель № 54 обозначает размер опухоли у мыши при введении винорелбина и анти-Her2-антитела. Указатель № 55 обозначает размер опухоли у мыши при введении винорелбина и моноклонального анти-CAPRIN-1-антитела №9.
Способ осуществления изобретения
Противоопухолевую активность антитела против полипептида, представленного любой из последовательностей SEQ ID NO: 2-30, пронумерованных четными числами, используемого в настоящем изобретении, можно оценить благодаря определению in vivo подавления опухолевого роста у животных с раком или благодаря исследованию того, проявляет ли антитело или не проявляет цитотоксичность посредством иммуноцитов или комплемента по отношению к опухолевым клеткам, экспрессирующим полипептид, in vitro, как описано далее.
В данном контексте нуклеотидные последовательности полинуклеотидов, кодирующих белки, содержащие аминокислотные последовательности, пронумерованные четными числами (т.е. SEQ ID NO: 2, 4, 6, ... , 28, 30) среди последовательностей SEQ ID NO: 2-30, представлены последовательностями, пронумерованными нечетными числами (т.е. SEQ ID NO: 1, 3, 5, ... , 27, 29) среди последовательностей SEQ ID NO: 1-29.
Аминокислотные последовательности, которые представлены в виде SEQ ID NO: 6, 8, 10, 12 и 14 в списке последовательностей, приведенном в настоящем описании, представляют собой аминокислотные последовательности CAPRIN-1, выделенные в виде полипептидов, которые связываются с антителами, специфично присутствующими в сыворотке от собаки с раком, способом SEREX с использованием библиотеки кДНК из ткани семенников собаки и сыворотки собаки с раком молочной железы. Аминокислотные последовательности, представленные в виде SEQ ID NO: 2 и 4, представляют собой аминокислотные последовательности CAPRIN-1, выделенные в виде гомологов человека. Аминокислотная последовательность, представленная в SEQ ID NO: 16, является аминокислотной последовательностью CAPRIN-1, выделенной в качестве гомолога, присутствующего у коров. Аминокислотная последовательность, представленная в SEQ ID NO: 18, является аминокислотной последовательностью CAPRIN-1, выделенной в качестве гомолога, присутствующего у лошади. Аминокислотные последовательности, представленные SEQ ID NO: 20-28, являются аминокислотными последовательностями CAPRIN-1, выделенными в качестве мышиных гомологов. Аминокислотная последовательность, представленная в виде SEQ ID NO: 30, является аминокислотной последовательностью CAPRIN-1, выделенного в качестве куриного гомолога (см. пример 1, описанный далее). Известно, что CAPRIN-1 экспрессируется, когда нормальные клетки в фазе покоя подвергаются активации или стимуляции клеточного деления.
Было известно, что CAPRIN-1 не экспрессируется на поверхности клеток; однако исследование, проведенное авторами настоящего изобретения, в настоящее время показало, что часть белка CAPRIN-1 экспрессируется на поверхности различных злокачественных клеток. В настоящем изобретении предпочтительно применяют антитела, которые связываются с частью белка CAPRIN-1, экспрессируемой на поверхности злокачественных клеток. Примером неполного пептида белка CAPRIN-1, который экспрессируется на поверхности злокачественных клеток, является полипептид, состоящий из последовательности из 7 или более непрерывно следующих друг за другом аминокислотных остатков в области аминокислотных остатков № (аа) 50-98 или 233-305 в аминокислотных последовательностях, представленных в виде пронумерованных четными числами последовательностей SEQ ID NO: 2-30 в списке последовательностей, за исключением последовательностей SEQ ID NO: 6 и 18. Конкретные примеры включают аминокислотную последовательность, представленную в виде SEQ ID NO: 37, и аминокислотную последовательность, имеющую 80% или более высокую, предпочтительно 85% или более высокую, более предпочтительно 90% или более высокую, еще более предпочтительно 95% или более высокую идентичность последовательности с указанной аминокислотной последовательностью. Примеры антитела, используемого в настоящем изобретении, включают все антитела, которые (специфично) связываются с такими пептидами (или (специфично) узнают такие пептиды, или обладают иммунологической реактивностью по отношению к таким пептидам) и проявляют противоопухолевую активность.
Описанное выше анти-CAPRIN-1-антитело, используемое в настоящем изобретении, может быть антителом любого типа, при условии, что оно может проявлять противоопухолевую активность. Примеры таких антител включают моноклональные антитела, поликлональные антитела, рекомбинантные антител, такие как синтетические антитела, полиспецифичные антитела, гуманизированные антитела, химерные антитела и одноцепочечные антитела (scFv), человеческие антитела и их фрагменты, такие как Fab, F(ab’)2 и Fv. Такие антитела и их фрагменты могут быть получены способами, известными специалистам в данной области. В настоящем изобретении требуются антитела, способные специфично связываться с белком CAPRIN-1. Предпочтительно они являются моноклональными антителами. Также можно применять поликлональные антитела, при условии, что могут быть стабильно продуцированы гомогенные антитела. Также в том случае, когда субъектом является человек, требуются человеческие антитела или гуманизированные антитела, чтобы избежать, или чтобы подавить отторжение.
Термин «специфично связывающееся с белком CAPRIN-1» в используемом в настоящем описании смысле означает, что антитело специфично связывается с белком CAPRIN-1, но по существу не связывается с другими белками, отличными от белка CAPRIN-1.
Противоопухолевую активность антитела, которое можно применять в настоящем изобретении, можно оценивать, как описано ниже, путем исследования in vivo подавления роста опухоли у животных с раком или путем исследования того, проявляет ли оно или не проявляет цитотоксическую активность in vitro, которая опосредована иммуноцитами или комплементом, по отношению к опухолевым клеткам, экспрессирующим полипептид.
Кроме того, примерами субъектов для лечения и/или профилактики рака согласно настоящему изобретению являются млекопитающие, такие как человек, комнатные животные, домашние животные и животные для соревнований. Предпочтительным субъектом является человек.
Получение антигенов и антител, лекарственных препаратов и тому подобного, относящихся к настоящему изобретению, описано ниже.
Получение антигенов для получения антител
Белки или их фрагменты, используемые в качестве сенсибилизирующих антигенов для получения анти-CAPRIN-1-антител, применяемых в настоящем изобретении, могут быть получены из любого вида животного без особого ограничения, такого как человек, собаки, крупный рогатый скот, лошади, мыши, крысы и куры. Однако белки или их фрагменты предпочтительно выбраны с учетом совместимости с исходными клетками, используемыми для слияния клеток. В общем, предпочтительными являются полученные от млекопитающих белки и, в частности, предпочтительным является белок, полученный из организма человека. Например, когда CAPRIN-1 является CAPRIN-1 человека, можно использовать белок CAPRIN-1 человека, его неполный пептид или клетки, экспрессирующие CAPRIN-1 человека.
Нуклеотидные последовательности и аминокислотные последовательности CAPRIN-1 человека и его гомологов можно получить, осуществляя доступ в GenBank (NCBI, U.S.A.) и используя такие алгоритмы, как BLAST или FASTA (Karlin and Altschul, Proc. Natl. Acad. Sci. U.S.A., 90: 5873-5877, 1993; Altschul et al., Nucleic Acids Res. 25: 3389-3402, 1997).
В настоящем изобретении на основе нуклеотидной последовательности (SEQ ID NO: 1 или 3) или аминокислотной последовательности (SEQ ID NO: 2 или 4) CAPRIN-1 человека определили, что нуклеиновая кислота-мишень или белок-мишень содержит последовательность, имеющую 70-100%, предпочтительно 80-100%, более предпочтительно 90-100%, еще более предпочтительно 95-100% (например, 97-100%, 98-100%, 99-100% или 99,5-100%) идентичность последовательности с нуклеотидной последовательностью или аминокислотной последовательностью ORF или зрелой части CAPRIN-1 человека. В используемом в настоящем описании смысле термин «идентичность последовательности в %» относится к процентному содержанию (%) идентичных аминокислот (или нуклеотидов) относительно общего количества аминокислот (или нуклеотидов) при выравнивании двух последовательностей для достижения наибольшего сходства с введением или без введения пробелов.
Длина фрагмента белка CAPRIN-1 варьирует от длины аминокислот эпитопа (антигенной детерминанты), который является минимальной единицей, узнаваемой антителом, до длины, составляющей менее полной длины белка. Термин «эпитоп» относится к полипептидному фрагменту, обладающему антигенностью или иммуногенностью у млекопитающих, предпочтительно у человека, и минимальная единица эпитопа состоит примерно из 7-12 (непрерывно следующих друг за другом) аминокислот, например, 8-11 (непрерывно следующих друг за другом) аминокислот. Примеры неполной последовательности белка CAPRIN-1, специфично связывающейся с антителом, включают неполную последовательность, содержащую, по меньшей мере, примерно 7-12 аминокислот из аминокислотной последовательности, представленной в виде SEQ ID NO: 37, или аминокислотной последовательности, имеющей 80% или более высокую, предпочтительно 85% или более высокую, более предпочтительно 90% или более высокую, еще более предпочтительно 95% или более высокую идентичность последовательности с аминокислотной последовательностью SEQ ID NO: 37.
Полипептиды, содержащие указанный выше белок CAPRIN-1 человека или неполные пептиды белка, могут быть синтезированы способом химического синтеза, таким как Fmoc-способ (способ с использованием флуоренилметилоксикарбонила) или tBoc-способ (способ с использованием трет-бутилоксикарбонила) (под редакцией The Japanese Biochemical Society, Seikagaku Jikken Koza (Biochemical Experimental Lecture Series) 1, Protein Chemistry IV, Chemical Modification and Peptide Synthesis, TOKYO KAGAKU DOZIN (Japan), 1981). Альтернативно указанные выше полипептиды также могут быть синтезированы обычными способами с использованием различных коммерчески доступных синтезаторов пептидов. Кроме того, с применением известных способов генетической инженерии (например,

получают полинуклеотид, кодирующий указанный выше полипептид, и затем включают в экспрессирующий вектор, который затем вводят в клетку-хозяина, чтобы получить представляющий интерес полипептид в клетке-хозяине, и затем извлекают его.
Полинуклеотиды, кодирующие указанные выше полипептиды, можно легко получить известными способами генетической инженерии или обычными способами с использованием коммерчески доступного синтезатора нуклеиновых кислот. Например, ДНК, содержащая нуклеотидную последовательность SEQ ID NO: 1, может быть получена в ПЦР с использованием библиотеки хромосомной ДНК человека или кДНК в качестве матрицы и пары праймеров, сконструированных так, чтобы можно было амплифицировать нуклеотидную последовательность, представленную в SEQ ID NO: 1. Условия ПЦР могут быть соответствующим образом определены. Например, условия ПЦР включают в себя проведение 30 следующих циклов реакции: денатурация при 94°C в течение 30 секунд; отжиг при 55°C в течение периода времени от 30 секунд до 1 минуты; и элонгация при 72°C в течение 2 минут, с использованием термостабильной ДНК-полимеразы (например, Taq-полимеразы или Pfu-полимеразы) и буфера для ПЦР, содержащего Mg2+, с последующим проведением реакции при 72°C в течение 7 минут. Однако условия ПЦР не ограничены приведенным выше примером. Способы ПЦР, условия и тому подобное описаны в публикации Ausubel с соавторами (Short Protocols in Molecular Biology, 3rd Edition, A compendium of Methods from Current Protocols in Molecular Biology (1995), John Wiley and Sons (в частности в главе 15)).
Также на основе информации о нуклеотидной последовательности и аминокислотной последовательности, представленной в виде последовательностей SEQ ID NO: 1-30 в списке последовательностей, приведенном в настоящем описании, получают соответствующие зонды или праймеры и затем, используя их, проводят скрининг библиотеки кДНК человека или тому подобной, с тем, так что можно выделить требуемую ДНК. Библиотеку кДНК предпочтительно конструируют из клеток, органов или тканей, которые экспрессируют белки, имеющие последовательности SEQ ID NO: 2-30, пронумерованные четными числами. Примеры таких клеток или тканей включают клетки или ткани, полученные из семенников, и рак или опухоли, такие как лейкоз, рак молочной железы, лимфома, опухоль головного мозга, рак легкого, рак прямой и ободочной кишки и тому подобные. Способы, такие как получение зондов или праймеров, конструирование библиотеки кДНК, скрининг библиотеки кДНК и клонирование генов-мишеней, известны специалисту в данной области и могут быть осуществлены способами, описанными Sambrook с соавторами (Molecular Cloning, 2nd Edition, Current Protocols in Molecular Biology (1989)), Ausbel с соавторами (выше), и тому подобными. Из полученной таким образом ДНК может быть получена ДНК, кодирующая белок CAPRIN-1 человека или его неполный пептид.
Клетками-хозяевами могут быть любые клетки, при условии, что они могут экспрессировать указанный выше полипептид. Примерами прокариотических клеток являются без ограничения клетки Escherichia coli и тому подобные. Примерами эукариотических клеток являются без ограничения клетки млекопитающих, такие как клетки почки обезьяны (COS1) и клетки яичника китайского хомячка (CHO), линия клеток почки плода человека (HEK293), линии клеток кожи плода мыши (NIH3T3), дрожжевые клетки, такие как почкующиеся дрожжи и делящиеся дрожжи, клетки шелкопряда и ооциты Xenopus.
В случае использования прокариотических клеток в качестве клеток-хозяев экспрессирующий вектор, используемый в настоящем изобретении, содержит начало, реплицируемое в прокариотических клетках, промотор, сайт связывания рибосомы, сайт множественного клонирования, терминатор, ген лекарственной резистентности, ген, комплементирующий ауксотрофность, и тому подобное. Примеры экспрессирующего вектора для Escherichia coli включают вектор на основе pUC, pBluescript II, систему экспрессии pET и систему экспрессии pGEX. ДНК, кодирующую указанный выше полипептид, включают в такой экспрессирующий вектор, прокариотические клетки-хозяева трансформируют вектором, полученные таким образом трансформированные клетки культивируют и, таким образом, полипептид, кодируемый ДНК, может быть экспрессирован в прокариотических клетках-хозяевах. В то же время полипептид также может быть экспрессирован в виде белка, слитого с другим белком.
При использовании в качестве клеток-хозяев эукариотических клеток экспрессирующий вектор, используемый в настоящем изобретении, представляет собой экспрессирующий вектор для эукариотических клеток, который содержит промотор, область сплайсинга, сайт добавления поли(A) и тому подобное. Примеры такого экспрессирующего вектора включают pKA1, pCDM8, pSVK3, pMSG, pSVL, pBK-CMV, pBK-RSV, вектор EBV, pRS, pcDNA3 и pYES2. Подобно упоминаемому выше случаю ДНК, кодирующую указанный выше полипептид, включают в такой экспрессирующий вектор, эукариотические клетки-хозяева трансформируют вектором, полученные таким образом трансформированные клетки культивируют и таким образом, полипептид, кодируемый ДНК, может быть экспрессирован в эукариотических клетках-хозяевах. Когда используют векторы pIND/V5-His, pFLAG-CMV-2, pEGFP-N1, pEGFP-C1 или тому подобные в качестве экспрессирующего вектора, указанный выше полипептид может быть экспрессирован в виде слитого белка, к которому может быть добавлена метка из числа различных меток, таких как His-метка (например, (His)6-(His)10), FLAG-метка, myc-метка, HA-метка и GFP.
Для введения экспрессирующего вектора в клетки-хозяева можно применять известный способ, такой как электропорация, способ с использованием фосфата кальция, способ на основе липосом, способ с использованием DEAE-декстрана, микроинъекция, вирусная инфекция, липофекция и связывание с проникающим через клеточную мембрану пептидом.
Представляющий интерес полипептид может быть выделен и очищен из клеток-хозяев с использованием сочетания известных способов разделения. Примеры таких способов включают без ограничения обработку денатурирующим агентом, таким как мочевина или поверхностно-активное вещество, обработку ультразвуком, ферментативное расщепление, высаливание или фракционирование в растворителях и преципитация, диализ, центрифугирование, ультрафильтрация, гель-фильтрация, SDS-ПААГ, изоэлектрическое фокусирование ионообменная хроматография, гидрофобная хроматография, аффинная хроматография и обращено-фазовая хроматография.
Структура антитела
Антитело является гетеромультимерным гликопротеидом, который, в общем, содержит, по меньшей мере, две тяжелых цепи и две легких цепи. Антитела, отличные от IgM, представляют собой гетеротетрамерный гликопротеид с молекулярной массой примерно 150 кД, состоящий из двух идентичных легких (L) цепей и двух идентичных тяжелых (H) цепей. Обычно каждая легкая цепь связана с тяжелой цепью одной дисульфидной ковалентной связью, однако количество дисульфидных связей между тяжелыми цепями различных изотипов иммуноглобулинов варьируют. Каждая тяжелая цепь или каждая легкая цепь также имеет внутрицепочечную дисульфидную связь. Каждая тяжелая цепь имеет вариабельный домен (VH-область) на одном конце, за которой следует несколько константных областей. Каждая легкая цепь имеет вариабельный домен (VL-область) и имеет одну константную область на конце, противоположном другому концу. Константная область легкой цепи совмещена с первой константной областью тяжелой цепи, а вариабельный домен легкой цепи совмещен с вариабельным доменом тяжелой цепи. Специфичная область вариабельного домена антитела имеет специфичную вариабельность, и такую область называют определяющей комплементарность областью (CDR), в силу того, что она придает антителу специфичность связывания. Часть вариабельной области, которая является относительно консервативной, называют каркасной областью (FR). Полные вариабельные домены тяжелой цепи и легкой цепи по отдельности содержат четыре FR, соединенные тремя CDR. Три CDR в тяжелой цепи называют CDRH1, CDRH2 и CDRH3 в порядке, начиная с N- конца. Подобным образом в случае легкой цепи CDRL называют CDRL1, CDRL2 и CDRL3. CDRH3 наиболее важна для специфичности связывания антитела с антигеном. Также CDR каждой цепи удерживаются вместе в состоянии близкого соседства друг с другом благодаря FR-областям, внося вклад в образование антигенсвязывающего участка антитела вместе с CDR из другой цепи. Константная область непосредственно не вносит вклад в связывание антитела с антигеном, но проявляет различные эффекторные функции, такие как участие в зависимой от антител опосредованной клетками цитотоксичности (ADCC), фагоцитоз посредством связывания с рецептором Fcγ, определение показателя времени полужизни/клиренса посредством неонатального Fc-рецептора (FcRn) и зависимая от комплемента цитотоксичность (CDC) посредством компонента C1q каскада комплемента.
Получение антитела
Термин «анти-CAPRIN-1-антитело» в используемом в настоящем описании смысле относится к антителу, обладающему иммунологической реактивностью по отношению к полноразмерному белку CAPRIN-1 белок или его фрагменту.
В используемом в настоящем описании смысле термин «иммунологическая реактивность» относится к свойству антитела связываться in vivo с антигеном CAPRIN-1. Посредством такого связывания in vivo осуществляется функция повреждения опухоли (например, гибель, супрессия или деградация). В частности, антитело, используемое в настоящем изобретении, может представлять собой антитело любого типа, при условии, что оно связывается с белком CAPRIN-1, таким образом, становясь способным повреждать опухоль, такую как лейкоз, лимфома, рак молочной железы, опухоль головного мозга, рак легкого, рак пищевода, рак желудка, рак почек или рак прямой и ободочной кишки.
Примеры антитела включают моноклональное антитело, поликлональные антитело (например, синтетические антитело, полиспецифичное антитело, гуманизированные антитело, химерное антитело или одноцепочечное антитело), человеческое антитело и фрагмент антитела (например, Fab, F(ab’)2 или Fv). Также антитело может представлять собой молекулу иммуноглобулина любого класса, такого как IgG, IgE, IgM, IgA, IgD или IgY, или любого подкласса, такого как IgG1, IgG2, IgG3, IgG4, IgA1 или IgA2. Любое из таких антител и их фрагментов обладает иммунологической реактивностью по отношению к белку CAPRIN-1, существующему на поверхности злокачественных клеток, и предпочтительно к полипептиду его внеклеточной области (предпочтительно, специфично связывается с белком или полипептидом), и проявляет цитотоксическую активность, направленную против рака.
Антитело может быть дополнительно модифицировано в дополнение к гликозилированию, ацетилированию, формилированию, амидированию, фосфорилированию, пегилированию (ПЭГ) или тому подобному.
Различные примеры получения антител описаны ниже.
Когда антитело является моноклональным антителом, мыши вводят, например, линию злокачественных клеток молочной железы SK-BR-3, экспрессирующую CAPRIN-1, для иммунизации, из организма мыши извлекают селезенку, отделяют клетки и затем такие клетки и клетки миеломы мышей сливают. Из полученных таким образом слитых клеток (гибридом) отбирают клон, продуцирующий антитело, обладающее эффектом подавления пролиферации злокачественных клеток. Гибридому, продуцирующую моноклональное антитело, которое оказывает действие, подавляющее пролиферацию злокачественных клеток, выделяют, гибридому культивируют и затем очищают антитело из надосадка культуры общим способом аффинной очистки, таким образом может быть получено антитело.
Гибридому, продуцирующую моноклональное антитело, также можно получить, например, как описано ниже. Сначала животное иммунизируют сенсибилизирующим антигеном согласно известному способу. Обычно способ осуществляют путем инъекции сенсибилизирующего антигена млекопитающему внутрибрюшинно или подкожно. В частности, сенсибилизирующий антиген разбавляют в PBS (фосфатно-солевом буфере), физиологическом растворе или тому подобном до соответствующего количества, затем суспендируют. Полученную суспензию при необходимости затем смешивают с подходящим количеством обычного адъюванта, такого как полный адъювант Фрейнда. После эмульгирования раствор вводят млекопитающему несколько раз каждый 4-21 день. Кроме того, при иммунизации сенсибилизирующим антигеном также можно использовать подходящий носитель.
Млекопитающего иммунизируют, как описано выше. После подтверждения появления требуемого уровня антител в сыворотке иммунизированные клетки собирают из организма млекопитающего и затем подвергают клеточному слиянию. Особенно предпочтительными иммунизированными клетками являются спленоциты.
Клетки миеломы млекопитающих используют в качестве других клеток-партнеров, сливаемых с иммунизированными клетками. В качестве клеток миеломы предпочтительно используют различные известные линии клеток, такие как P3U1 (P3-X63Ag8U1), P3 (P3x63Ag8. 653) (J. Immunol. (1979) 123, 1548-1550), P3x63Ag8U.1 (Current Topics in Microbiology and Immunology (1978) 81, 1-7), NS-1 (Kohler. G. and Milstein, C. Eur. J. Immunol. (1976) 6, 511-519), MPC-11 (Margulies. D. H. et al., Cell (1976) 8, 405-415), SP2/0 (Shulman, M. et al., Nature (1978) 276, 269-270), FO (deSt. Groth, S. F. et al., J. Immunol. Methods (1980) 35, 1-21), S194 (Trowbridge, I. S. J. Exp. Med. (1978) 148, 313-323) и R210 (Galfre, G. et al., Nature (1979) 277, 131-133).
Слияние иммунизированной клетки и клетки миеломы можно осуществить, в основном, согласно известному способу, такому как, например, способ, описанный Kohler и Milstein (Kohler, G. and Milstein, C. Methods Enzymol. (1981) 73, 3-46).
Более конкретно, описанное выше слияние клеток осуществляют, например, в присутствии ускорителя клеточного слияния в обычной питательной культуральной среде. В качестве такого ускорителя слияния используют полиэтиленгликоль (ПЭГ), вирус Сендай (HVJ), или тому подобные. При необходимости может быть добавлено вспомогательное средство, такое как диметилсульфоксид, и использовано, чтобы усилить эффективность слияния.
Отношение иммунизированных клеток к клеткам миеломы, используемое в настоящем изобретении, может быть установлено произвольно. Например, количество иммунизированных клеток, которое предпочтительно используется, составляет один к десяти к количеству клеток миеломы. В качестве культуральной среды, используемой для указанного выше слияния клеток, можно использовать культуральную среду RPMI1640, подходящую для пролиферации указанной выше линии клеток миеломы, культуральную среду MEM и другие культуральные среды, обычно используемые для культивирования такого вида клеток. Кроме того, вместе со средами можно использовать жидкость, дополняющую сыворотку, такую как фетальная сыворотка теленка (FCS).
Слияние клеток можно осуществлять, тщательно смешивая предварительно определяемые количества указанных выше иммунизированных клеток и клеток миеломы в указанной выше культуральной среде и добавляя раствор ПЭГ (например, имеющего среднюю молекулярную массу в диапазоне примерно от 1000 до 6000), предварительно нагретый примерно до 37°C, обычно в концентрации 30-60% (масс./об.) и смешивая с получением при этом культуры, содержащей представляющие интерес гибридомы. Затем подходящую культуральную среду последовательно добавляют к полученной таким образом культуре, которую затем центрифугируют, чтобы удалить надосадок, и такую процедуру повторяют, чтобы удалить агент для слияния клеток или тому подобное, что не желательно для роста гибридом.
Полученные таким образом гибридомы культивируют для селекции в обычной культуральной селекционной среде (например, культуральной среде HAT, содержащей гипоксантин, аминоптерин и тимидин). Культивирование в такой культуральной среде HAT продолжают в течение периода времени (обычно от нескольких суток до нескольких недель), достаточного для того, чтобы другие клетки (неслитые клетки), отличные от целевых гибридом, погибли. Затем осуществляют скрининг и разовое клонирование гибридомы, которая продуцирует представляющее интерес антитело, используя общий способ лимитирующего разведения.
Указанные выше гибридомы получают иммунизацией животного, отличного от человека, антигеном. Кроме указанного способа гибридомы, которые продуцируют антитело человека, обладающее требуемой активностью (например, активностью в подавлении пролиферации клеток), также может быть получено сенсибилизацией лимфоцитов человека in vitro, таких как лимфоциты человека, которые были инфицированы вирусом EB, белком, экспрессирующей белок клеткой или ее лизатом, с последующим слиянием сенсибилизированных таким образом лимфоцитов с клетками миеломы, полученными от человека, обладающими способностью непрерывно делиться, такими как U266 (№ регистрации TIB196).
Полученную таким образом гибридому, которая продуцирует представляющее интерес моноклональное антитело, можно пересевать в обычной культуральной среде и можно хранить в жидком азоте в течение длительного периода времени.
В частности, гибридома может быть получена иммунизацией обычным способом иммунизации с использованием в качестве сенсибилизирующего антигена требуемого антигена или клетки, которая экспрессирует требуемый антиген, слиянием полученной таким образом иммунизированной клетки с известной родительской клеткой обычным способом слияния клеток, и затем скринингом в отношении продуцирующей моноклональное антитело клетки (т.е. гибридомы) обычным способом скрининга.
Другим примером антитела, которое можно использовать в настоящем изобретении, является поликлональные антитело. Поликлональные антитело может быть получено, например, как описано ниже.
Небольшое животное, такое как мышь, продуцирующая антитело человека мышь или кролик, иммунизируют природным белком CAPRIN-1, рекомбинантным белком CAPRIN-1, экспрессируемым в таком микроорганизме, как Escherichia coli, в форме слитого с GST белка или тому подобным белком или его неполным пептидом и затем получают сыворотку. Сыворотку очищают преципитацией сульфатом аммония, хроматографией на колонке с белком A, на колонке с белком G, ионообменной хроматографией на DEAE, на аффинной колонке, с которой был связан белок CAPRIN-1 или синтетический пептид, или тому подобным способом, при этом может быть получено поликлональное антитело. В примерах, описанных далее, получали поликлональное антитело кролика против пептида (представленного последовательностью SEQ ID NO: 37) неполной области (в аминокислотной последовательности белка CAPRIN-1), которая экспрессируется на поверхности злокачественных клеток, и подтверждали противоопухолевые эффекты.
В качестве мыши, продуцирующей антитело человека, известны, например, мышь KM mouse (Kirin Pharma/Medarex) и ксеномышь (Amgen) (например, международные патентные публикации WO 02/43478 и WO 02/092812). Когда такую мышь иммунизируют белком CAPRIN-1 или его фрагментом, полностью человеческие поликлональные антитела могут быть получены из крови. Также собирают спленоциты иммунизированной мыши, и затем моноклональное антитело человеческого типа может быть получено способом слияния с клетками миеломы.
Антиген может быть получен способом с использованием, например, животных клеток (публикация патента Японии (Kohyo) No. 2007-530068) или бакуловируса (например, международная патентная публикация WO 98/46777), например. Когда антиген имеет низкую иммуногенность, антиген может быть связан с макромолекулой, обладающей иммуногенностью, такой как альбумин, и затем может быть осуществлена иммунизация.
Кроме того, ген антитела клонируют из указанной гибридомы и затем включают в подходящий вектор. Затем вектор вводят в хозяина и затем можно применять генетически рекомбинантное антитело, полученное с использованием методики рекомбинации генов (например, см. публикацию Carl, A. K. Borrebaeck, James, W. Larrick, Therapeutic Monoclonal Antibodies, опубликованную в Великобритании MACMILLAN PUBLISHERS LTD, 1990). В частности, кДНК вариабельной области (V-области) антитела синтезируют из мРНК гибридомы, используя обратную транскриптазу. Когда может быть получена ДНК, кодирующая V-область представляющего интерес антитела, такую ДНК лигируют с ДНК, кодирующей константную область (C-область) требуемого антитела и затем полученный слитый продукт включают в экспрессирующий вектор. Альтернативно ДНК, кодирующая V-область антитела, может быть включена в экспрессирующий вектор, содержащий ДНК для C-области антитела. В тоже время ДНК может быть включена в экспрессирующий вектор так, чтобы она экспрессировалась под контролем областей регуляции экспрессии, таких как энхансер и промотор. Затем клетки-хозяева трансформируют экспрессирующим вектором так, чтобы могло экспрессироваться антитело.
Анти-CAPRIN-1-антитело, используемое в настоящем изобретении, предпочтительно является моноклональным антителом. Однако анти-CAPRIN-1-антитело согласно настоящему изобретению также может быть, например, поликлональным антителом или рекомбинантным антителом или генетически модифицированным антителом (например, химерным антителом, гуманизированным антителом, одноцепочечным антителом или биспецифичным антителом).
Примеры моноклонального антитела включают моноклональные антитела человека и моноклональные антитела животного, отличного от человека (например, мышиное моноклональное антитело, моноклональное антитело крысы, моноклональное антитело кролика и моноклональное антитело кур). Моноклональное антитело может быть получено в результате культивирования гибридомы, полученной слиянием спленоцита млекопитающего, отличного от человека (например, мыши или продуцирующей человеческие антитела мыши), иммунизированного белком CAPRIN-1, с клеткой миеломы. В примерах, описанных далее, получали мышиные моноклональные антитела и подтверждали противоопухолевые эффекты.
Такие моноклональные антитела содержат вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO: 43, 73, 83, 93, 103, 113 или SEQ ID NO: 123, и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO: 47, 53, 58, 63, 68, 77, 87, 97, 107, 117 или 127, при этом: VH-область содержит CDR1, представленную аминокислотной последовательностью SEQ ID NO: 40, 70, 80, 90, 100, 110 или 120, CDR2, представленную аминокислотной последовательностью SEQ ID NO: 41, 71, 81, 91, 101, 111 или 121, и CDR3, представленную аминокислотной последовательностью SEQ ID NO: 42, 72, 82, 92, 102, 112 или 122; и VL-область содержит CDR1, представленную аминокислотной последовательностью SEQ ID NO: 44, 50, 55, 60, 65, 74, 84, 94, 104,114 или 124, CDR2, представленную аминокислотной последовательностью SEQ ID NO: 45, 51, 56, 61, 66, 75, 85, 95, 105, 115 или 125, и CDR3, представленную аминокислотной последовательностью SEQ ID NO: 46, 52, 57, 62, 67, 76, 86, 96, 106, 116 или 126.
Химерное антитело получают, комбинируя последовательности от разных животных. Например, химерное антитело содержит вариабельные области тяжелой цепи и легкой цепи мышиного антитела и константные области тяжелой цепь и легкой цепи антитела человека. Такое химерное антитело может быть получено известными способами. Например, химерное антитело может быть получено лигированием ДНК, кодирующей V-область антитела, с ДНК, кодирующей C-область антитела человека, включением полученного в результате слитого продукта в экспрессирующий вектор и затем введением вектора в хозяина и затем вызывая продуцирование антитела у хозяина.
Примеры поликлонального антитела включают антитело, полученное иммунизацией животного, продуцирующего антитела человека (например, мыши), белком CAPRIN-1.
Гуманизированные антитело представляет собой модифицированное антитело, которое также называют реконструированным антителом человека. Гуманизированные антитело может быть сконструировано пересадкой CDR антитела от иммунизированного животного в определяющие комплементарность области антитела человека. Общие методики рекомбинации генов для этого также известны.
В частности, последовательности ДНК, сконструированные так, чтобы они имели каждую из CDR антитела мыши или цыпленка, лигированную с каждой из каркасных областей (FR) антитела человека, синтезируют ПЦР-способом из нескольких олигонуклеотидов, которые получают таким образом, чтобы они, например, имели перекрывающиеся части в своих концевых частях. Гуманизированное антитело может быть получено лигированием полученной таким образом ДНК с ДНК, кодирующей константную область антитела человека, включением полученного в результате слитого продукта в экспрессирующий вектор, введением вектора в хозяина, что таким образом вызывает у хозяина продукцию генного продукта (см. публикацию европейского патента EP239400 и международную патентную публикацию WO 96/02576). В качестве FR антитела человека, которые лигируют посредством CDR, выбирают FR, которые обеспечивают возможность образования антигенсвязывающего участка с хорошими областями, определяющими комплементарность. При необходимости для образования антигенсвязывающего участка, имеющего соответствующие определяющие комплементарность области реконструированного антитела человека, аминокислоты каркасных областей вариабельной области антитела могут быть заменены (Sato, K. et al., Cancer Research, 1993, 53: 851-856). Также аминокислоты FR могут быть заменены аминокислотами каркасных областей их разных антител человека (см. международную патентную публикацию WO 99/51743).
В качестве каркасных областей (FR) антитела человека, которые лигируют посредством CDR, выбирают FR, которые обеспечивают возможность образования антигенсвязывающего участка с хорошими областями, определяющими комплементарность. При необходимости для образования антигенсвязывающего участка, имеющего соответствующие определяющие комплементарность области реконструированного антитела человека, аминокислоты каркасных областей вариабельной области антитела могут быть заменены (Sato, K. et al., Cancer Research, 1993, 53: 851-856).
После получения химерного антитела или гуманизированного антитела аминокислоты в вариабельной области (например, FR) или константной области могут быть заменены другими аминокислотами.
Аминокислотная замена представляет собой замену, например, менее чем 15, менее чем 10, 8 или менее, 7 или менее, 6 или менее, 5 или менее, 4 или менее, 3 или менее или 2 или менее аминокислот и предпочтительно замену 1-5 аминокислот и более предпочтительно 1 или 2 аминокислот. Антитело с заменами должно быть функционально эквивалентным антителу без замен. Замена желательно представляет собой замену консервативной аминокислоты (аминокислот) из аминокислот, обладающих аналогичными свойствами, такими как электрический заряд, боковая цепь, полярность и ароматичность. Аминокислоты, обладающие аналогичными свойствами, могут быть классифицированы, например, как основные аминокислоты (аргинин, лизин и гистидин), кислые аминокислоты (аспарагиновая кислота и глутаминовая кислота), незаряженные полярные аминокислоты (глицин, аспарагин, глутамин, серин, треонин, цистеин и тирозин), неполярные аминокислоты (лейцин, изолейцин, аланин, валин, пролин, фенилаланин, триптофан и метионин), аминокислоты с разветвленной цепью (треонин, валин и изолейцин) и ароматические аминокислоты (фенилаланин, тирозин, триптофан и гистидин).
Антитела могут быть химически модифицированы. Примеры такого модифицированного антитела включают антитела, связанные с различными молекулами, такими как полиэтиленгликоль (ПЭГ) и противоопухолевые соединения (например, противоопухолевые средства в качестве примера последних). Вещества, связываемые в модифицированном продукте антитела согласно настоящему изобретению, не ограничены. Такой модифицированный продукт антитела может быть получен, когда полученное таким образом антитело подвергают химической модификации. Способы такой модификации уже разработаны в данной области.
В используемом в настоящем описании смысле термин «функциональный эквивалент» относится к случаю, когда данное антитело обладает биологической или биохимической активностью, сходной с активностью антитела согласно настоящему изобретению и, в частности, относится к случаю, когда, например, данное антитело обладает функцией повреждения опухоли, по существу не вызывая отторжения при его применении на человеке. Примером такой активности является активность в подавлении клеточной пролиферации или активность связывания.
В качестве способа, хорошо известного специалистам в данной области для получения полипептида, функционально эквивалентного определенному полипептиду, известен способ введения мутации в полипептид. Например, специалисты в данной области могут получить антитело, функционально эквивалентное антителу согласно настоящему изобретению, посредством введения соответствующим образом мутации в антитело с использованием, например, сайт-специфичного мутагенеза

Антитело, которое узнает эпитоп белка CAPRIN-1, узнаваемый описанным выше анти-CAPRIN-1-антителом, т.е. антителом, которое специфично связывается с эпитопом, может быть получено способами, известными специалистам в данной области. Например, такое антитело может быть получено способом, который включает в себя определение эпитопа белка CAPRIN-1, узнаваемого анти-CAPRIN-1-антителом, обычным способом (например, картированием эпитопов) и затем получение антитела с использованием полипептида, имеющего аминокислотную последовательность, входящую в эпитоп, в качестве иммуногена, или способом, который заключается в определении эпитопа такого антитела, получаемого обычным способом, и затем отборе антитела, имеющего эпитоп, идентичный эпитопу анти-CAPRIN-1-антитела. В используемом в настоящем описании смысле термин «эпитоп» относится к полипептидному фрагменту млекопитающего и предпочтительно человека, обладающему антигенностью или иммуногенностью. Единица минимального размера эпитопа состоит примерно из 7-12 аминокислот и предпочтительно из 8-11 аминокислот.
Константа аффинности Ka(kon/koff) антитела, используемого в настоящем изобретении, предпочтительно составляет, по меньшей мере, 107 М-1, по меньшей мере 108 М-1, по меньшей мере 5×108 М-1, по меньшей мере 109 М-1, по меньшей мере 5×109 М-1, по меньшей мере 1010 М-1, по меньшей мере 5×1010 М-1, по меньшей мере 1011 М-1, по меньшей мере 5×1011 М-1, по меньшей мере, 1012 М-1 или по меньшей мере 1013 М-1.
Антитело, используемое в настоящем изобретении, может быть конъюгировано с противоопухолевым средством. Конъюгирование антитела с противоопухолевым средством можно осуществить через спейсер, имеющий группу, взаимодействующую с аминогруппой, карбоксильной группой, гидроксигруппой, тиольной группой или тому подобной (например, сукцинимидилсукцинатную группу, формильную группу, 2-пиридилдитиогруппу, группу малеимидила, алкоксикарбонильную группу и гидроксигруппу).
Примеры противоопухолевого средства, применимого в настоящем изобретении, включают следующие известные противоопухолевые средства, описанные в литературе известного уровня техники и тому подобные, такие как паклитаксел, доксорубицин, даунорубицин, циклофосфамид, метотрексат, 5-фторурацил, тиотепа, бусульфан, импросульфан, пипосульфан, бензодопа, карбоквон, метуредопа, уредопа, алтретамин, триэтиленмеламин, триэтиленфосфорамид, триэтилентиофосфорамид, триметилоломеламин, буллатацин, буллатацинон, камптотецин, бриостатин, каллистатин, криптофицин 1, криптофицин 8, доластатин, дуокармицин, элеутеробин, панкратистатин, саркодиктиин, спонгистатин, хлорамбуцил, хлорнафазин, хлорфосфамид, эстрамустин, ифосфамид, мехлорэтамин, гидрохлорид оксида мехлорэтамина, мелфалан, новембихин, фенестерин, преднимустин, трофосфамид, урамустин, кармустин, хлорозотоцин, фотемустин, ломустин, нимустин, ранимустин, калихеамицин, динемицин, клодронат, эсперамицин, аклациномицин, актиномицин, аутрамицин, азасерин, блеомицин, кактиномицин, карабицин, карминомицин, карцинофилин, хромомицин, дактиномицин, деторбицин, 6-диазо-5-оксо-L-норлейцин, адриамицин, эпирубицин, эзорубицин, идарубицин, марцелломицин, митомицин C, микофеноловая кислота, ногаламицин, оливомицины, пепломицин, потфиромицин, пуромицин, квеламицин, родорубицин, стрептонигрин, стрептозоцин, туберцидин, убенимекс, зиностатин, зорубицин, деноптреин, птероптерин, триметрексат, флударабин, 6-меркаптопурин, тиамиприн, тиогуанин, анцитабин, азацитидин, 6-азауридин(азауридин), кармофур, цитарабин, дидезоксиуридин, доксифлуридин, эноцитабин, флоксуридин, андрогены (например, калустерон, пропионат дромостанолона, эпитиостанол, мепитиостан и тестолактон), аминоглютетимид, митотан, трилостан, фолиновая кислота, ацеглатон, гликозид альдофосфамида, аминолевулиновая кислота, энилурацил, амсакрин, бестрабуцил, бисантрен, эдатраксат, дефофамин, демеколцин, диазихон, элфорнитин, ацетат эллиптиния(эллиптиний), эпотилон, этоглуцид, лентинан, лонидамин, мейтанзин, ансамитоцин, митогуазон, митоксантрон, мопиданмол, нитраэрин, пентостатин, фенамет, пирарубицин, лозоксантрон, подофиллиновая кислота, 2-этилгидразид, прокарбазин, разоксан, ризоксин, шизофиллан, спирогерманий, тенуазоновая кислота, триазиквон, роридин A, ангуидин, уретан, виндезин, дакарбазин, манномустин, митобронитол, митолактол, пипоброман, гацитозин, доцетаксел, хлорамбуцил, гемцитабин, 6-тиогуанин, меркаптопурин, цисплатин, оксалиплатин, карбоплатин, винбластин, этопозид, ифосфамид, митоксантрон, винкристин, винорелбин, новантрон, тенипозид, эдатрексат, дауномицин, аминоптерин, кселода, ибандронат, иринотекан, ингибитор топоизомеразы, дифторметилорнитин (DMFO), ретиноевая кислота, капецитабин и их фармацевтически приемлемые (известные) соли или (известные) производные.
Альтернативно известный радиоактивный изотоп, который описан в литературе известного уровня техники или тому подобный, такой как 211At, 131I, 125I, 90Y, 186Re, 188Re, 153Sm, 212Bi, 32P, 175Lu или 176Lu, может быть связан с антителом, используемым в настоящем изобретении. Требуемый радиоактивный изотоп является эффективным для лечения или диагностики опухоли.
Антитело, согласно настоящему изобретению представляет собой антитело, обладающее иммунологической реактивностью по отношению к CAPRIN-1, антитело, специфично узнающее CAPRIN-1, или антитело, специфично связывающееся с CAPRIN-1, которое проявляет цитотоксическую активность против рака или оказывает подавляющее рост опухоли действие. Антитело должно иметь такую структуру, чтобы почти или полностью избежать отторжения у данного животного, которому вводят антитело. Примеры такого антитела в том случае, когда данным животным является человек, включают человеческое антитело, гуманизированные антитело, химерные антитело (например, химерное антитело человека-мыши), одноцепочечное антитело и биспецифичное антитело. Такими антителами являются: рекомбинантные антитела, в которых вариабельные области тяжелой цепи и легкой цепи получены из антитела человека; рекомбинантные антитела, в которых вариабельные области тяжелой цепи и легкой цепи содержат определяющие комплементарность области (CDR1, CDR2 и CDR3) из антитела животного, отличного от человека, и каркасные области из антитела человека; или рекомбинантные антитела, в которых вариабельные области тяжелой цепи и легкой цепи получены из антитела животного, отличного от человека, и константные области тяжелой цепи и легкой цепи получены из антитела человека. Предпочтительными антителами являются первые два антитела.
Такие рекомбинантные антитела могут быть получены, как указано далее, с использованием клонирования ДНК, кодирующей моноклональное антитело против CAPRIN-1 человека (например, моноклональное антитело человека, моноклональное антитело мыши, моноклональное антитело крысы, моноклональное антитело кролика или моноклональное антитело цыпленка), из продуцирующей антитела клетки, такой как гибридома, получения ДНК, кодирующей вариабельную область легкой цепи и вариабельную область тяжелой цепи антитела способом на основе ОТ-ПЦР, использования ее в качестве матрицы и затем определения последовательности каждой вариабельной области легкой цепи и тяжелой цепи или каждой последовательности CDR1, CDR2 и CDR3 на основе системы нумерации EU по Кабату (Kabat et al., Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institute of Health, Bethesda, Md. (1991)).
Кроме того, ДНК, кодирующая каждую из таких вариабельных областей, или ДНК, кодирующую каждую CDR, получают, используя методику рекомбинации генов (Sambrook et al., Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory Press (1989)) или синтезатор ДНК. В данном случае указанная выше гибридома, продуцирующая моноклональное антитело человека может быть получена иммунизацией животного, продуцирующего антитело человека (например, мыши), CAPRIN-1 человека и затем слиянием спленоцитов, извлеченных из организма иммунизированного животного, с клетками миеломы. Альтернативно ДНК, кодирующую вариабельную область легкой цепи или тяжелой цепи, и константную область из антитела человека получают в случае необходимости с использованием методики рекомбинации генов или синтезатора ДНК.
В случае гуманизированного антитела ДНК получают заменой последовательности, кодирующей CDR, в ДНК, кодирующей вариабельную область легкой цепи или тяжелой цепи, полученную из антитела человека, соответствующей ей последовательностью, кодирующей CDR, из антитела, полученного от животного, отличного от человека (например, мыши, крысы или цыпленка), и затем лигированием полученной таким образом ДНК с ДНК, кодирующей константную область легкой цепи или тяжелой цепи, полученной из антитела человека. Таким образом может быть получена ДНК, кодирующая гуманизированные антитело.
В случае химерного антитела ДНК, кодирующая химерное антитело, может быть получена лигированием ДНК, кодирующей вариабельную область легкой цепи или тяжелой цепи антитела животного, отличного от человека (например, мыши, крысы и цыпленка), с ДНК, кодирующей константную область легкой цепи или тяжелой цепи из антитела человека.
В случае одноцепочечного антитела такое антитело представляет собой антитело, полученное линейным лигированием вариабельной области тяжелой цепи с вариабельной областью легкой цепи через линкер. Таким образом, ДНК, кодирующая одноцепочечное антитело, может быть получена связыванием ДНК, кодирующей вариабельную область тяжелой цепи, ДНК, кодирующей линкер, и ДНК, кодирующей вариабельную область легкой цепи. В данном случае и вариабельная область тяжелой цепи, и вариабельная область легкой цепи являются областями из антитела человека, или только CDR заменяют CDR антитела животного, отличного от человека (например, мыши, крысы и цыпленка), хотя другие области являются областями из антитела человека. Также линкер содержит 12-19 аминокислот, например, (G4S)3 из 15 аминокислот (G.-B. Kim et al., Protein Engineering Design and Selection 2007, 20 (9): 425-432).
В случае биспецифичного антитела (диантитела) такое антитело способно специфично связываться с двумя разными эпитопами. Например, ДНК, кодирующую биспецифичное антитело, можно получить связыванием ДНК, кодирующей вариабельную область тяжелой цепи A, ДНК, кодирующей вариабельную область легкой цепи B, ДНК, кодирующую вариабельную область тяжелой цепи B, и ДНК, кодирующей вариабельную область легкой цепи A в указанном порядке (в данном случае ДНК, кодирующая вариабельную область легкой цепи B, связана с ДНК, кодирующей вариабельную область тяжелой цепи B, через ДНК, кодирующую указанный выше линкер). В данном случае вариабельная область тяжелой цепи и вариабельная область легкой цепи происходят из антитела человека, или только CDR заменены CDR антитела животного, отличного от человека (например, мыши, крысы или цыпленка), хотя другие области происходят из антитела человека.
Полученную как описано выше рекомбинантную ДНК включают в один или множество подходящих векторов, векторы вводят в клетки-хозяева (например, клетки млекопитающего, дрожжевые клетки или клетки насекомого) и затем вызывают (ко)экспрессию так, чтобы можно было получить рекомбинантное антитело

Примеры антитела согласно настоящему изобретению, полученные указанным выше способом, включают следующие антитела (a)-(k):
(a) антитело, содержащее CDR1, CDR2 и CDR3 вариабельной области тяжелой цепи, содержащие последовательности SEQ ID NO: 40, 41 и 42, и CDR1, CDR2 и CDR3 вариабельной области легкой цепи, содержащие последовательности SEQ ID NO: 44, 45 и 46 (предпочтительно, антитело, содержащее вариабельную область тяжелой цепи с последовательностью SEQ ID NO: 43 и вариабельную область легкой цепи с последовательностью SEQ ID NO: 47);
(b) антитело, содержащее CDR1, CDR2 и CDR3 вариабельной области тяжелой цепи, содержащие последовательности SEQ ID NO: 40, 41 и 42, и CDR1, CDR2 и CDR3 вариабельной области легкой цепи, содержащие последовательности SEQ ID NO: 50, 51 и 52 (предпочтительно, антитело, содержащее вариабельную область тяжелой цепи с последовательностью SEQ ID NO: 43 и вариабельную область легкой цепи с последовательностью SEQ ID NO: 53);
(c) антитело, содержащее CDR1, CDR2 и CDR3 вариабельной области тяжелой цепи, содержащие последовательности SEQ ID NO: 40, 41 и 42, и CDR1, CDR2 и CDR3 вариабельной области легкой цепи, содержащие последовательности SEQ ID NO: 55, 56 и 57 (предпочтительно, антитело, содержащее вариабельную область тяжелой цепи с последовательностью SEQ ID NO: 43 и вариабельную область легкой цепи с последовательностью SEQ ID NO: 58);
(d) антитело, содержащее CDR1, CDR2 и CDR3 вариабельной области тяжелой цепи, содержащие последовательности SEQ ID NO: 40, 41 и 42, и CDR1, CDR2 и CDR3 вариабельной области легкой цепи, содержащие последовательности SEQ ID NO: 60, 61 и 62 (предпочтительно, антитело, содержащее вариабельную область тяжелой цепи с последовательностью SEQ ID NO: 43, и вариабельную область легкой цепи с последовательностью SEQ ID NO: 63);
(e) антитело, содержащее CDR1, CDR2 и CDR3 вариабельной области тяжелой цепи, содержащие последовательности SEQ ID NO: 40, 41 и 42 в качестве CDR1, CDR2 и CDR3 вариабельной области тяжелой цепи и CDR1, CDR2 и CDR3 вариабельной области легкой цепи, содержащие последовательности SEQ ID NO: 65, 66 и 67 (предпочтительно, антитело, содержащее вариабельную область тяжелой цепи с последовательностью SEQ ID NO: 43 и вариабельную область легкой цепи с последовательностью SEQ ID NO: 68);
(f) антитело, содержащее CDR1, CDR2 и CDR3 вариабельной области тяжелой цепи, содержащие последовательности SEQ ID NO: 70, 71 и 72, и CDR1, CDR2 и CDR3 вариабельной области легкой цепи, содержащие последовательности SEQ ID NO: 74, 75 и 76 (предпочтительно, антитело, содержащее вариабельную область тяжелой цепи с последовательностью SEQ ID NO: 73 и вариабельную область легкой цепи с последовательностью SEQ ID NO: 77);
(g) антитело, содержащее CDR1, CDR2 и CDR3 вариабельной области тяжелой цепи, содержащие последовательности SEQ ID NO: 80, 81 и 82, и CDR1, CDR2 и CDR3 вариабельной области легкой цепи, содержащие последовательности SEQ ID NO: 84, 85 и 86 (предпочтительно, антитело, содержащее вариабельную область тяжелой цепи с последовательностью SEQ ID NO: 83 и вариабельную область легкой цепи с последовательностью SEQ ID NO: 87);
(h) антитело, содержащее CDR1, CDR2 и CDR3 вариабельной области тяжелой цепи, содержащие последовательности SEQ ID NO: 90, 91 и 92, и CDR1, CDR2 и CDR3 вариабельной области легкой цепи, содержащие последовательности SEQ ID NO: 94, 95 и 96 (например, антитело, содержащее вариабельную область тяжелой цепи с последовательностью SEQ ID NO: 93 и вариабельную область легкой цепи с последовательностью SEQ ID NO: 97);
(i) антитело, содержащее CDR1, CDR2 и CDR3 вариабельной области тяжелой цепи, содержащие последовательности SEQ ID NO: 100, 101 и 102, и CDR1, CDR2 и CDR3 вариабельной области легкой цепи, содержащие последовательности SEQ ID NO: 104, 105 и 106 (например, антитело, содержащее вариабельную область тяжелой цепи с последовательностью SEQ ID NO: 103 и вариабельную область легкой цепи с последовательностью SEQ ID NO: 107);
(j) антитело, содержащее CDR1, CDR2 и CDR3 вариабельной области тяжелой цепи, содержащие последовательности SEQ ID NO: 110, 111 и 112, и CDR1, CDR2 и CDR3 вариабельной области легкой цепи, содержащие последовательности SEQ ID NO: 114, 115 и 116 (например, антитело, содержащее вариабельную область тяжелой цепи с последовательностью SEQ ID NO: 113 и вариабельную область легкой цепи с последовательностью SEQ ID NO: 117); и
(k) антитело, содержащее CDR1, CDR2 и CDR3 вариабельной области тяжелой цепи, содержащие последовательности SEQ ID NO: 120, 121 и 122, и CDR1, CDR2 и CDR3 вариабельной области легкой цепи, содержащие последовательности SEQ ID NO: 124, 125 и 126 (например, антитело, содержащее вариабельную область тяжелой цепи с последовательностью SEQ ID NO: 123 и вариабельную область легкой цепи с последовательностью SEQ ID NO: 127).
В данном случае аминокислотные последовательности, представленные в виде SEQ ID NO: 40, 41 и 42, SEQ ID NO: 70, 71 и 72, SEQ ID NO: 80, 81 и 82, SEQ ID NO: 90, 91 и 92, SEQ ID NO: 100, 101 и 102, SEQ ID NO: 110, 111 и 112 или SEQ ID NO: 120, 121 и 122, представляют собой CDR1, CDR2 и CDR3, соответственно, вариабельной области тяжелой цепи антитела мыши. Аминокислотные последовательности, представленные в виде SEQ ID NO: 44, 45 и 46, SEQ ID NO: 50, 51 и 52, SEQ ID NO: 55, 56 и 57, SEQ ID NO: 60, 61 и 62, SEQ ID NO: 65, 66 и 67, SEQ ID NO: 74, 75 и 76, SEQ ID NO: 84, 85 и 86, SEQ ID NO: 94, 95 и 96, SEQ ID NO: 104, 105 и 106, SEQ ID NO: 114, 115 и 116 или SEQ ID NO: 124, 125 и 126, представляют собой CDR1, CDR2 и CDR3, соответственно, вариабельной области легкой цепи антитела мыши. Также гуманизированное антитело, химерное антитело, одноцепочечное антитело или биспецифичное антитело согласно настоящему изобретению представляет собой, например, следующее антитело (приведенное, в качестве примера как «антитело (a)»):
(i) антитело, в котором вариабельная область тяжелой цепи содержит аминокислотные последовательности SEQ ID NO: 40, 41 и 42 и аминокислотные последовательности каркасных областей из антитела человека, и вариабельная область легкой цепи содержит аминокислотные последовательности SEQ ID NO: 44, 45 и 46 и аминокислотные последовательности каркасных областей из антитела человека (например, антитело, в котором вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 43 и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 47); и
(ii) антитело, в котором вариабельная область тяжелой цепи содержит аминокислотные последовательности SEQ ID NO: 40, 41 и 42 и аминокислотные последовательности каркасных областей из антитела человека, и константная область тяжелой цепи содержит аминокислотную последовательность из антитела человека, и вариабельная область легкой цепи содержит аминокислотные последовательности SEQ ID NO: 44, 45 и 46 и аминокислотные последовательности каркасных областей из антитела человека, и константная область легкой цепи содержит аминокислотную последовательность из антитела человека (например, антитело, в котором вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 43 и константная область тяжелой цепи содержит аминокислотную последовательность из антитела человека, а также вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 47 и константная область легкой цепи содержит аминокислотную последовательность из антитела человека).
В данном контексте последовательности константных областей и вариабельных областей тяжелой цепи и легкой цепи антитела человека могут быть получены, например, из NCBI (например, США: GenBank, UniGene). Например, последовательность с регистрационным номером J00228 может быть отнесена к константной области тяжелой цепи IgG1 человека, последовательность с регистрационным номером J00230 может быть отнесена к константной области тяжелой цепи IgG2 человека, последовательность с регистрационным номером X03604 может быть отнесена к константной области тяжелой цепи IgG3 человека, последовательность с регистрационным номером K01316 может быть отнесена к константной области тяжелой цепи IgG4 человека, последовательности с регистрационными номерами V00557, X64135, X64133 и тому подобные могут быть отнесены к константным областям легкой цепи κ человека и последовательности с номерами регистрации X64132, X64134 и тому подобные могут быть отнесены к константным областям легкой цепи λ человека.
Указанные выше антитела предпочтительно обладают цитотоксической активностью и, следовательно, могут проявлять противоопухолевые эффекты.
Также конкретные последовательности вариабельных областей или CDR тяжелой цепи и легкой цепи в указанных выше антителах приведены просто в целях иллюстрации и, таким образом, четко не ограничены такими конкретными последовательностями. Получают гибридому, способную продуцировать другое антитело человека или антитело животного, отличного от человека (например, мышиное антитело) против CAPRIN-1 человека, собирают моноклональное антитело, которое продуцируется гибридомой, и затем определяют, является ли оно или не является целевым антителом на основе свойства иммунологического связывания с CAPRIN-1 человека и цитотоксической активности в качестве показателей. После идентификации таким образом гибридомы, продуцирующей целевое моноклональное антитело, ДНК, кодирующую вариабельные области тяжелой цепи и легкой цепи целевого антитела получают из гибридомы, как описано выше, осуществляют секвенирование и затем ДНК используют для получения другого антитела.
Кроме того, что касается указанного выше антитела согласно настоящему изобретению, то последовательность указанных выше антител (a) и (b), в частности последовательность каркасной области и/или последовательность константной области каждого из антител может иметь замену, делецию или добавление одной или нескольких (предпочтительно 1 или 2) аминокислот, при условии, что антитело обладает специфичностью для специфичного узнавания CAPRIN-1. В данном случае термин «несколько» относится к 2-5 и предпочтительно к 2 или 3.
Антитела, используемые в настоящем изобретении, также могут быть получены способами рекомбинации генов с использованием ДНК, кодирующей указанное выше антитело согласно настоящему изобретению, или ДНК, кодирующей тяжелую цепь или легкую цепь указанного выше антитела, или ДНК, кодирующей вариабельную область тяжелой цепи или легкой цепи указанного выше антитела. Примеры таких ДНК включают в случае антитела (a) ДНК, кодирующую вариабельную область тяжелой цепи, содержащую нуклеотидные последовательности, кодирующие аминокислотные последовательности SEQ ID NO: 40, 41 и 42, и ДНК, кодирующую вариабельную область легкой цепи, содержащую нуклеотидные последовательности, кодирующие аминокислотные последовательности SEQ ID NO: 44, 45 и 46.
Определяющие комплементарность области (CDR), кодируемые последовательностями ДНК, представляют собой области для определения специфичности антитела. Следовательно, последовательности, кодирующие другие области антитела, отличные от CDR (в частности, константную область и каркасную область), могут быть из других антител. В данном случае примеры таких «других антител» включают антитела из организмов животных, отличных от человека, и предпочтительно антитела человека с точки зрения уменьшения побочных эффектов. Таким образом, в случае указанной выше ДНК области, кодирующие каждую каркасную область и каждую область контакта тяжелых цепей и легких цепей, предпочтительно содержат нуклеотидные последовательности, кодирующие соответствующие аминокислотные последовательности из антитела человека.
Следующие альтернативные примеры ДНК, кодирующей антитело, используемое в настоящем изобретении, включают в случае антитела (a) ДНК, кодирующую вариабельную область тяжелой цепи, содержащую нуклеотидную последовательность, кодирующую аминокислотную последовательность SEQ ID NO: 43, и ДНК, кодирующую вариабельную область легкой цепи, содержащую нуклеотидную последовательность, кодирующую аминокислотную последовательность SEQ ID NO: 47. В данном случае примером нуклеотидной последовательности, кодирующей аминокислотную последовательность SEQ ID NO: 43, является нуклеотидная последовательность SEQ ID NO: 48. Также примером нуклеотидной последовательности, кодирующей аминокислотную последовательность SEQ ID NO: 47, является нуклеотидная последовательность SEQ ID NO: 49. В указанных ДНК области, кодирующие каждую константную область тяжелых цепей и легких цепей, предпочтительно содержат нуклеотидные последовательности, кодирующие соответствующие аминокислотные последовательности из антитела человека.
ДНК согласно настоящему изобретению может быть получена, например, указанными выше способами или описанным далее способом. Сначала получают суммарную РНК из гибридомы, относящейся к антителу согласно настоящему изобретению, используя коммерчески доступный набор для экстракции РНК, и затем синтезируют кДНК с использованием обратной транскриптазы и случайных праймеров и тому подобных. Затем кДНК, кодирующую антитело, амплифицируют способом ПЦР, используя в качестве праймеров олигонуклеотиды с последовательностями, консервативными для каждой вариабельной области известных генов тяжелой цепи и легкой цепи мышиных антител. Последовательность, кодирующую константную область, можно получить в результате амплификации известной последовательности способом ПЦР. Нуклеотидная последовательность ДНК может быть определена обычным способом, таким как встраивание в плазмиду или фаг для секвенирования.
Примерами ДНК, имеющей отношение к указанным выше антителам (a)-(k), являются следующие ДНК.
(i) В качестве ДНК, кодирующей полипептид, который содержит аминокислотную последовательность SEQ ID NO: 43, 73, 83, 93, 103, 113, 123, 133, 143 или 153, ДНК, содержащая нуклеотидную последовательность SEQ ID NO: 48, 78, 88, 98, 108, 118 или 128.
(ii) В качестве ДНК, кодирующей полипептид, который содержит аминокислотную последовательность SEQ ID NO: 47, 53, 58, 63, 68, 77, 87, 97, 107, 117, 127, 137, 147 или 157, ДНК, содержащая нуклеотидную последовательность SEQ ID NO: 49, 54, 59, 64, 69, 79, 89, 99, 109, 119 или 129.
Считается, что анти-CAPRIN-1-антитело, применяемое в настоящем изобретении, оказывает противоопухолевое действие, направленное против CAPRIN-1-экспрессирующих злокачественных клеток, посредством следующего механизма:
зависимая от антител опосредованная эффекторными клетками цитотоксичность (ADCC) по отношению к CAPRIN-1-экспрессирующим клеткам и зависимая от комплемента цитотоксичность (CDC) по отношению к CAPRIN-1-экспрессирующим клеткам.
Таким образом, активность анти-CAPRIN-1-антитела, применяемого в настоящем изобретении, можно оценить, как конкретно описано в примерах ниже, с использованием измерения ex vivo указанной выше ADCC-активности или CDC-активности, направленной против экспрессирующих белок CAPRIN-1 злокачественных клеток.
ADCC-активность может быть измерена с использованием коммерчески доступного набора для измерения цитотоксической активности, такого как набор для определения цитотоксичности (Roche). Согласно данной методике ADCC-активность может быть измерена способами, включающими в себя осуществление взаимодействия злокачественной клетки-мишени с анти-CAPRIN-1-антителом на льду, культивирование клетки с эффекторной клеткой (например, PBMC) в течение 4 часов и затем измерение ферментативной активности лактатдегидрогеназы (LDH) или радиоактивности Cr51, высвобождаемого в среду в надосадок культуры. Также CDC-активность может быть измерена способами, включающими в себя осуществление взаимодействия злокачественной клетки-мишени с анти-CAPRIN-1-антителом на льду, культивирование клетки с использованием раствора, содержащего добавки (например, сыворотку), в течение 4 часов и затем измерение ферментативной активности или радиоактивности подобно указанным выше измерениям в надосадке культуры.
Анти-CAPRIN-1-антитело, применяемое в настоящем изобретении, связывается с белком CAPRIN-1 на злокачественной клетке и оказывает противоопухолевое действие вследствие указанной выше активности и, следовательно, оно применимо для лечения или профилактики рака. В частности, настоящее изобретение относится к фармацевтической композиции для лечения и/или профилактики рака, которая содержит анти-CAPRIN-1-антитело в качестве активного ингредиента. Когда анти-CAPRIN-1-антитело применяют для его введения в организм человека (терапия антителами), предпочтительно оно является антителом человека или гуманизированным антителом, чтобы уменьшить иммуногенность.
Кроме того, чем выше аффинность связывания между анти-CAPRIN-1-антителом и белком CAPRIN-1 на поверхности злокачественных клеток, тем более высокую противоопухолевую активность анти-CAPRIN-1-антитела можно получить. Следовательно, когда может быть получено анти-CAPRIN-1-антитело, обладающее высокой аффинностью связывания с белком CAPRIN-1, можно ожидать более сильные противоопухолевые эффекты, и становится возможным применение такого антитела в виде фармацевтической композиции в целях лечения и/или профилактики рака. Такая высокая аффинность связывания желательно должна быть такой, как указано далее. Как описано выше, константа связывания (константа аффинности) Ka (kon/koff) предпочтительно составляет, по меньшей мере, 107 М-1, по меньшей мере, 108 М-1, по меньшей мере, 5×108 М-1, по меньшей мере, 109 М-1, по меньшей мере, 5×109 М-1, по меньшей мере, 1010 М-1, по меньшей мере, 5×1010 М-1, по меньшей мере, 1011 М-1, по меньшей мере, 5×1011 М-1, по меньшей мере, 1012 М-1 или, по меньшей мере, 1013 М-1.
Связывание с антигенэкспрессирующей клеткой
Способность антитела связываться с белком CAPRIN-1 можно определить в анализе связывания с использованием ELISA, способа Вестерн-блоттинга, иммунофлуоресценции и проточно-цитометрического анализа или тому подобного, как описано в примерах.
Иммуногистохимическое окрашивание
Антитело, которое узнает белок CAPRIN-1, можно тестировать в отношении реактивности к CAPRIN-1 способом иммуногистохимии, известным специалистам в данной области, с использованием фиксированных параформальдегидом или ацетоном замороженных срезов или фиксированных параформальдегидом залитых в парафин срезов ткани, которые готовят из образцов ткани, полученных от пациента во время хирургической операции, или из образцов ткани, полученных от животного, имеющего гетеротрансплантат ткани, инокулированный линией клеток, экспрессирующих CAPRIN-1 естественным образом или после трансфекции.
Антитело, реактивное по отношению к CAPRIN-1, можно красить различными способами иммуногистохимического окрашивания. Например, конъюгированное с пероксидазой хрена антитело козы против Ig мыши или антитело козы против Ig кролика подвергают взаимодействию, в результате может быть визуализировано антитело-мишень.
Противоопухолевое средство
Настоящее изобретение характеризуется сочетанием анти-CAPRIN-1-антитела с противоопухолевым средством, примеры которого приведены выше. Анти-CAPRIN-1-антитело и противоопухолевое средство, каждое из которых обладает противоопухолевой активностью, вводят в сочетании пациенту с раком, так, чтобы можно было получить значимый синергетический противоопухолевый эффект, в частности, эффект, вызывающие почти полную регрессию опухоли в модели на животном, несущем рак, как описано в примерах. Такое специфичный противоопухолевый эффект наблюдают в том случае, когда анти-CAPRIN-1-антитело и противоопухолевое средство применяют в сочетании, даже когда рост опухоли постепенно увеличивается с течением времени. Такой эффект является совершенно необычным.
В настоящем изобретении примеры противоопухолевого средства, используемого в сочетании с анти-CAPRIN-1-антителом, включают все химиотерапевтические средства, которые применяют или будут применять для лечения различных типов рака или опухолей. Примеры такого противоопухолевого средства включают антиметаболическое лекарственное средство, антибиотическое противоопухолевое средство, основанное на растительном алкалоиде противораковое средство, ингибитор топоизомеразы и антивоопухолевое алкилирующее средство. Например, в данном случае включены все противоопухолевые средства (приведенные выше в качестве примеров), известные в литературе и тому подобные. Примеры таких средств включают без ограничения противоопухолевые средства, которые использованы в описанных ниже примерах, такие как средства против рака (например, циклофосфамид, паклитаксел, доцетаксел и винорелбин), значимые противоопухолевые эффекты которых были подтверждены. Таким образом, в настоящем изобретении, одно или два или больше лекарственных средств, выбранных из циклофосфамида, паклитаксела, доцетаксела, винорелбина и их фармакологически приемлемых солей или производных можно использовать в качестве противоопухолевых средств.
Лекарственный препарат для лечения и/или профилактики рака
Мишень фармацевтической композиции для лечения и/или профилактики рака согласно настоящему изобретению особым образом не ограничена, при условии, что она является раком (клеткой), экспрессирующей ген CAPRIN-1.
Термины «опухоль» и «рак» в используемом в настоящем описании смысле относятся к злокачественной неоплазме и использованы взаимозаменяемо.
Лекарственный препарат согласно настоящему изобретению характеризуется содержанием в нем сочетания антитела или его фрагмента, обладающего иммунологической реактивностью по отношению к белку CAPRIN-1, и одного или двух или больше типов противоопухолевых средств, при этом антитело или фрагмент и противоопухолевые средства объединяют вместе, или они находятся по отдельности. В частности, когда такие активные ингредиенты объединяют вместе, указанное выше антитело или его фрагмент и указанное выше противоопухолевое средство (средства) можно смешивать вместе с носителем (или эксципиентом), для приготовления в форме фармацевтической композиции. С другой стороны, когда такие активные ингредиенты сочетают, беря их по отдельности, готовят по отдельности фармацевтическую композицию, содержащую указанное выше антитело или его фрагмент в качестве активного ингредиента, и фармацевтическую композицию, содержащую указанное выше противоопухолевое средство (средства) в качестве активного ингредиента, так что лекарственный препарат может быть получен в форме фармацевтического набора. Такая фармацевтическая композиция и фармацевтический набор более конкретно описаны ниже.
Рак, подвергаемый воздействию согласно настоящему изобретению, представляет собой рак, экспрессирующий гены, кодирующие белки CAPRIN-1, имеющие аминокислотные последовательности, пронумерованные четными числами среди последовательностей SEQ ID NO: 2-30. Примеры такого рака включают предпочтительно рак молочной железы, опухоль головного мозга, лейкоз, рак легкого, лимфому, мастоцитому, рак почек, рак шейки матки, рак мочевого пузыря, рак пищевода, рак желудка и рак прямой и ободочной кишки.
Примеры такого конкретного рака включают без ограничения аденокарциному молочной железы, аденокарциному молочной железы комплексного типа, злокачественную смешанную опухоль молочной железы, внутрипротоковую папиллярную аденокарциному, аденокарциному легкого, плоскоклеточную карциному, мелкоклеточную карциному, крупноклеточную карциному, глиому, которая является опухолью эпителиальной ткани вокруг нейронов, эпендимому, нейроцитому, нейроэктодермальную опухоль плода, шванному, нейрофиброму, менингиому, хронический лимфоцитарный лейкоз, лимфому, лимфому желудочно-кишечного тракта, лимфому пищеварительной системы, мелкоклеточную и среднеклеточную лимфому, рак слепой кишки, рак восходящей ободочной кишки, рак нисходящей ободочной кишки, рак поперечной ободочной кишки, рак сигмовидной ободочной кишки и рак прямой кишки.
Кроме того, предпочтительными субъектами являются млекопитающие, включая приматов, комнатных животных, домашних животных, животных для скачек и тому подобные, и особенно предпочтительными человек, собаки и кошки.
Фармацевтическая композиция
Активные ингредиенты, входящие в состав лекарственного препарата для лечения и/или профилактики рака согласно настоящему изобретению, т.е. указанное выше антитело или его фрагмент и указанное выше противоопухолевое средство, могут быть приготовлены способом, известным специалистам в данной области в форме фармацевтической композиции, полученной их смешиванием или в форме их отдельных фармацевтических композиций.
Например, фармацевтическая композиция может быть использована парентерально в форме инъекционного препарата, такого как асептический раствор, приготовленный с использованием воды или другого фармакологически приемлемого раствора, отличного от воды, или суспензия. Например, она может быть приготовлена смешиванием в стандартной лекарственной форме, требуемой в общепринятой фармацевтической практике, в подходящем сочетании с фармакологически приемлемым носителем или средой, в частности, стерильной водой или физиологическим раствором, растительным маслом, эмульгатором, суспендирующим средством, поверхностно-активным веществом, стабилизатором, корригентом, эксципиентом, носителем, антисептиком, связывающим средством и тому подобным. Также фармацевтическая композиция согласно настоящему изобретению может содержать фармакологически приемлемую соль. В качестве фармакологически приемлемой соли можно использовать, например, соль неорганической кислоты, такой как хлористоводородная кислота или фосфорная кислота, или органической кислоты, такой как уксусная кислота, винная кислота или миндальная кислота. Кроме того, можно использовать соль, образованную со свободной карбоксильной группой. Например, такая соль также может быть получена из неорганического основания, такого как натрий, калий, аммоний, кальций, гидроксид железа (I) или тому подобные, или органического основания, такого как изопропиламин, триметиламин, 2-этиламиноэтанол, гистидин или прокаин.
Асептическая композиция для инъекции может быть назначена согласно общей фармацевтической практике с использованием такого носителя, как дистиллированная вода для инъекций.
Примеры водного раствора для инъекций включают физиологический раствор, изотонический раствор, содержащий декстрозу или другие вспомогательные вещества, такие как D-сорбит, D-манноза, D-маннит и хлорид натрия. Такие примеры можно использовать в сочетании с подходящим солюбилизирующим средством, таким как спирт, в частности, этанол и полиспирт (например, пропиленгликоль и полиэтиленгликоль), и неионогенное поверхностно-активное вещество (например, полисорбат 80 (TM) и HCO-60).
Примеры масла включают кунжутное масло и соевое масло, которые можно использовать в сочетании с солюбилизирующим средством, таким как бензилбензоат или бензиловый спирт. Также с ними можно сочетать буферное средство, такое как фосфатный буфер или натрий-ацетатный буфер, успокаивающее средство, такое как гидрохлорид прокаина, стабилизатор, такой как бензиловый спирт или фенол, и антиоксидант. Подходящую ампулу обычно заполняют приготовленным таким образом инъекционным раствором.
Введение является пероральным или парентеральным введением. Примеры парентерального введения включают инъекцию, введение через нос, легочное введение и трансдермальное введение. Примеры инъекции включают внутривенную инъекцию, внутримышечную инъекцию, внутрибрюшинную инъекцию и подкожную инъекцию, так что возможно системное или местное введение. Также в случае парентерального введения возможно инфузионное введение, которое осуществляют постепенно или медленно и которое занимает много времени. Способы введения могут быть соответствующим образом выбраны в зависимости от возраста, массы тела, пола пациента, симптомов и тому подобного. Фармацевтическую композицию, содержащую антитело, предпочтительно вводят парентерально. С другой стороны, в случае фармацевтической композиции, содержащей противоопухолевое средство, выбирают либо пероральное введение, либо парентеральное введение, в зависимости от типов противоопухолевых средств и показаний.
В случае фармацевтической композиции для лечения и/или профилактики рака согласно настоящему изобретению доза указанного выше антитела может быть выбрана, например, из диапазона от 0,0001 мг до 1000 мг на кг массы тела. Альтернативно, например, доза может быть выбрана из диапазона от 0,001 мг/организм до 100000 мг/организм пациента; однако диапазон доз не всегда ограничен указанными числовыми значениями. Кроме того, доза указанного выше противоопухолевого средства может быть выбрана, например, из диапазона от 1 до 1000 мг/организм пациента и предпочтительно от 10 до 500 мг/организм пациента; однако диапазон доз не всегда ограничен указанными числовыми значениями. Кроме того, доза и способ введения варьируют в зависимости от массы тела, возраста, пола пациента, симптомов и тому подобного, но могут быть соответствующим образом выбраны специалистами в данной области.
Способ введения
Лечение и/или профилактика рака с использованием средства для лечения и/или профилактики рака согласно настоящему изобретению, включает в себя различные формы в дополнение к введению средства в виде указанной выше фармацевтической композиции. Например, активные ингредиенты средства для лечения и/или профилактики рака согласно настоящему изобретению можно вводить одновременно или можно вводить по отдельности в определенном порядке. В конкретном примере активные ингредиенты можно вводить с интервалами вплоть до примерно 3 недель, то есть, в течение примерно 3 недель после введения первого активного ингредиента можно вводить второй активный ингредиент. На данном этапе такое введение можно осуществлять после хирургической операции, или хирургическую операцию также можно проводить между введением первого средства и введением второго средства. Также средство для лечения и/или профилактики рака согласно настоящему изобретению можно вводить согласно множеству циклов введения. Например, когда осуществляют одновременное введение активных ингредиентов средства для лечения и/или профилактики рака согласно настоящему изобретению, фармацевтическую композицию, содержащую оба активных ингредиента, вводят, используя цикл примерно от 2 дней до примерно 3 недель. Затем при необходимости терапевтический цикл также можно повторить в соответствии с решением лечащего врача. Подобным образом, когда планируется препарат для введения активных ингредиентов в определенном порядке, периоды введения отдельных средств корректируют так, чтобы они составляли такой же период. Интервал между циклами может варьировать от 0 до 2 месяцев. Дозу каждого активного ингредиента средства для лечения и/или профилактики рака согласно настоящему изобретению можно устанавливать подобно дозе, используемой для введения каждого активного ингредиента фармацевтической композиции.
Фармацевтический набор
Лекарственный препарат для лечения и/или профилактики рака согласно настоящему изобретению может быть в форме фармацевтического набора. Термин «фармацевтический набор» в используемом в настоящем описании смысле относится в случае способа лечения или профилактики рака к упаковке для использования указанного выше анти-CAPRIN-1-антитела или его фрагмента и указанного выше противоопухолевого средства, которые являются активными ингредиентами, в форме отдельных фармацевтических композиций. Упаковка содержит инструкции по введению каждого активного ингредиента. Каждый активный ингредиент указанной выше фармацевтической композиции для лечения и/или профилактики рака, который находится в фармацевтическом наборе, может быть в форме фармацевтической композиции, которая была приготовлена, как описано выше, так чтобы активные ингредиенты можно было вводить вместе или раздельно. Также фармацевтический набор содержит определенные количества активных ингредиентов, достаточные для однократной дозы или множества доз, так чтобы каждый активный ингредиент можно было вводить согласно указанному выше способу введения.
На основе содержания, конкретно описано выше, настоящее изобретение, кроме того, относится к способу лечения и/или профилактики рака, включающему в себя введение указанного выше лекарственного препарата согласно настоящему изобретению субъекту, у которого предполагается наличие рака (включая субъекта с раком). В одном варианте антитело или его фрагмент и противоопухолевое средство, которые содержатся в указанном выше лекарственном препарате, вводят одновременно или по отдельности указанному выше субъекту.
Настоящее изобретение описано более конкретно на основе примеров, но объем настоящего изобретения не ограничен такими конкретными примерами.
Пример 1. Идентификация нового белка ракового антигена способом SEREX
(1) Получение библиотеки кДНК
Суммарную РНК экстрагировали из ткани семенников здоровой собаки способом с использованием кислоты-гуанидиния-фенола-хлороформа. Поли-A-РНК очищали согласно протоколам, прилагаемым к набору для очистки мРНК Oligotex-dT30 (Takara Shuzo Co., Ltd.), используя набор.
Фаговую библиотеку кДНК семенников собаки синтезировали, используя полученную таким образом мРНК (5 мкг). Для получения фаговой библиотеки кДНК использовали набор для синтеза кДНК ZAP-cDNA, и набор для клонирования ZAP-cDNA gigapack III gold (STRATAGENE) и библиотеку получали согласно протоколам, прилагаемым к набору. Размер полученной таким образом фаговой библиотеки кДНК оставлял 7,73×105 БОЕ/мл.
(2) Скрининг библиотеки кДНК с использованием сыворотки
Иммунологический скрининг осуществляли, используя фаговую библиотеку кДНК семенников собаки, полученную как описано выше. В частности, хозяина Escherichia coli (XL1-Blue MRF’) инфицировали фагом так, что 2210 клонов присутствовали на чашке с агарозой NZY φ90×15 мм. Клетки культивировали при 42°C в течение 3-4 часов, чтобы вызвать образование бляшек. Чашку покрывали нитроцеллюлозной мембраной (Hybond C Extra: GE HealthCare Bio-Sciences), пропитанной IPTG (изопропил-β-D-тиогалактозидом) при 37°C в течение 4 часов. Белки индуцировали, экспрессировали и затем переносили на мембрану. Затем мембрану извлекали, погружали и встряхивали в TBS (10 мМ трис-HCl, 150 мМ NaCl, pH 7,5), содержащем 0,5% сухого обезжиренного молока, при 4°C в течение ночи, чтобы подавить неспецифичную реакцию. Фильтр подвергали взаимодействию с разбавленной в 500 раз сывороткой собак с раком при комнатной температуре в течение 2-3 часов.
В качестве указанной выше сыворотки от собак с раком использовали сыворотку, собранную у собак с раком молочной железы. Сыворотки хранили при -80°C и затем подвергали предварительной обработке непосредственно перед использованием. Предварительную обработку сыворотки осуществляли следующим способом. В частности, хозяина Escherichia coli (XL1-Blure MRF’) инфицировали фагом λ ZAP Express, в который не был встроен чужеродный ген, и затем культивировали на чашке со средой NZY при 37°C в течение ночи. Затем в чашку добавляли 0,2 М буфер NaHCO3 (pH 8,3), содержащий 0,5 М NaCl, и затем чашку оставляли стоять при 4°C в течение 15 часов. Надосадки собирали в виде экстрактов Escherichia coli/фага. Затем собранный экстракт Escherichia coli/фага пропускали через NHS-колонку (GE HealthCare Bio-Sciences), чтобы иммобилизовать полученный из Escherichia coli/фага белок. Сыворотку собак с раком пропускали через колонку, на которой был иммобилизован белок, для взаимодействия, таким образом удаляя из сыворотки антитела к Escherichia coli и антитела, адсорбируемые на фаге. Каждую фракцию сыворотки, которая была пропущена через колонку, разбавляли в 500 раз в TBS, содержащем 0,5% сухого обезжиренного молока, и полученную разбавленную сыворотку использовали в качестве материала для иммунологического скрининга.
Мембрану, на которую с помощью блоттинга переносили обработанную таким образом сыворотку и слитый белок, промывали 4 раза TBS-T (0,05% твин 20/TBS). Мембрану подвергали взаимодействию с антителом козы против IgG собаки (конъюгированное с HRP антитело козы против IgG-h+I собаки: BETHYL Laboratories) в качестве второго антитела, разбавленным в 5000 раз в TBS, содержащем 0,5% сухого обезжиренного молока, при комнатной температуре в течение 1 часа. Регистрацию осуществляли на основе цветной ферментативной реакции, используя раствор для реакции NBT/BCIP (Roche). Колонии, соответствующие участкам позитивной цветной реакции, собирали из чашки с агарозой размером φ90×15 мм и затем разбавляли в 500 мкл буфера SM (100 мМ NaCl, 10 мМ MgClSO4, 50 мМ трис-HCl, 0,01% желатин, pH 7,5). Вторичный скрининг и третичный скрининг повторяли способом, подобным указанному выше, вплоть до унификации позитивных в цветной реакции колоний. Таким образом проведен скрининг 30940 фаговых клонов, которые были подвергнуты взаимодействию с IgG сыворотки, и выделено 5 позитивных клонов.
(3) Поиск гомологии выделенного гена антигена
Процедуру превращения фаговых векторов в плазмидные векторы осуществляли для 5 позитивных клонов, выделенных указанным выше способом, с целью проведения анализа нуклеотидных последовательностей клонов. В частности, 200 мкл раствора, содержащего хозяина Escherichia coli (XL1-Blue MRF’), приготовленного так, чтобы получить оптическую плотность OD600 1,0, 250 мкл раствора, содержащего очищенный фаг, и 1 мкл хелперного фага ExAssist (STRATAGENE) смешивали и давали возможность взаимодействовать при 37°C в течение 15 минут. Затем добавляли 3 мл среды LB, клетки культивировали при 37°C в течение 2,5-3 часов и затем полученный продукт сразу помещали на водяную баню при 70°C и инкубировали в течение 20 минут. Центрифугирование осуществляли при 4°C, 1000×g в течение 15 минут и затем собирали надосадок в качестве раствора, содержащего фагмиду. Затем 200 мкл раствора, приготовленного с внесением хозяина фагмиды Escherichia coli SOLR так, чтобы получить оптическую плотность OD600 1,0, и 10 мкл раствора, содержащего очищенный фаг, смешивали, затем подвергали взаимодействию в течение 15 минут при 37°C. 50 мкл полученного продукта высевали на агаризованную среду LB, содержащую ампициллин (в конечной концентрации 50 мкг/мл) и затем культивировали в течение ночи при 37°C. Собирали отдельную колонию трансформированных SOLR и затем культивировали на среде LB, содержащей ампициллин (в конечной концентрации 50 мкг/мл) при 37°C. После культивирования плазмидную ДНК, несущую представляющую интерес вставку, очищали, используя набор для выделения плазмид QIAGEN Miniprep (QIAGEN).
Очищенную плазмиду подвергали анализу полной последовательности вставки способом опосредованной праймером «прогулки», используя праймер T3 с последовательностью SEQ ID NO: 31 и праймер T7 с последовательностью SEQ ID NO: 32. Последовательности генов SEQ ID NO: 5, 7, 9, 11 и 13 получали анализом последовательностей. Используя нуклеотидные последовательности генов и соответствующие им аминокислотные последовательности (SEQ ID NO: 6, 8, 10, 12 и 14), проводили поиск с использованием программы поиска гомологии BLAST search (http://www.ncbi.nlm.nih.gov/BLAST/), чтобы найти гомологию с известными генами. А результате было обнаружено, что все пять полученных генов представляли собой гены, кодирующие CAPRIN-1. Идентичность последовательностей пяти генов составляла 100% на уровне нуклеотидных последовательностей и 99% на уровне аминокислотных последовательностей в областях, транслируемых в белки. Идентичность последовательностей таких генов и гена, кодирующего гомолог человека, составляла 94% на уровне нуклеотидных последовательностей и 98% на уровне аминокислотных последовательностей в областях, транслируемых в белки. Нуклеотидные последовательности гомологов человека представлены в SEQ ID NO: 1 и 3, и их аминокислотные последовательности представлены в SEQ ID NO: 2 и 4. Также идентичности последовательностей полученных генов собаки и гена, кодирующего гомолог коров, составляли 94% на уровне нуклеотидных последовательностей и 97% на уровне аминокислотных последовательностей в областях, транслируемых в белки. Нуклеотидная последовательность гомолога коров представлена в SEQ ID NO: 15, и его аминокислотная последовательность представлена в SEQ ID NO: 16. Кроме того, идентичность последовательностей генов, кодирующих гомологи человека, и гена, кодирующего гомолог коров, составляла 94% на уровне нуклеотидных последовательностей, и 93%-97% на уровне аминокислотных последовательностей в областях, транслируемых в белки. Также идентичности последовательностей полученных генов собак и гена, кодирующего гомолог лошади, составляли 93% на уровне нуклеотидных последовательностей и 97% на уровне аминокислотных последовательностей в областях, транслируемых в белки. Нуклеотидная последовательность гомолога лошади представлена в SEQ ID NO: 17, и его аминокислотная последовательность представлена в SEQ ID NO: 18. Кроме того, идентичности последовательностей генов, кодирующих гомологи человека, и гена, кодирующего гомолог лошади, составляли 93% на уровне нуклеотидных последовательностей и 96% на уровне аминокислотных последовательностей в областях, транслируемых в белки. Также идентичности последовательностей полученных генов собаки и генов, кодирующих гомологи мыши, составляли 87-89% на уровне нуклеотидных последовательностей и 95-97% на уровне аминокислотных последовательностей в областях, транслируемых в белки. Нуклеотидные последовательности гомологов мыши представлены в SEQ ID NO: 19, 21, 23, 25 и 27, а их аминокислотные последовательности представлены в SEQ ID NO: 20, 22, 24, 26 и 28. Кроме того, идентичности последовательностей генов, кодирующих гомологи человека, и генов, кодирующих гомологи мыши, составляли 89-91% на уровне нуклеотидных последовательностей и составляли 95-96% на уровне аминокислотных последовательностей в областях, транслируемых в белки. Также идентичности последовательностей полученных генов собаки и гена, кодирующего гомолог цыпленка, составляли 82% на уровне нуклеотидных последовательностей и 87% на уровне аминокислотных последовательностей в областях, транслируемых в белки. Нуклеотидная последовательность гомолога цыпленка представлена в SEQ ID NO: 29, а его аминокислотная последовательность представлена в SEQ ID NO: 30. Кроме того, идентичности последовательностей генов, кодирующих гомологи человека, и гена, кодирующего гомолог цыпленка, составляли 81-82% на уровне нуклеотидных последовательностей и 86% на уровне аминокислотных последовательностей в областях, транслируемых в белки.
(4) Анализ экспрессии генов в каждой ткани
Экспрессию генов, полученных указанным выше способом, исследовали в нормальных тканях собаки и человека и различных клеточных линиях способом ОТ-ПЦР. Реакцию обратной транскрипции осуществляли следующим образом. Конкретно, суммарную РНК экстрагировали из 5 мг каждой ткани или 5-10×106 клеток клеточной линии, используя реагент TRIZOL (Invitrogen) согласно прилагаемым протоколам. На суммарной РНК синтезировали кДНК, используя систему для синтеза первой нити Superscript для ОТ-ПЦР (Invitrogen) согласно пролагаемым протоколам. ПЦР осуществляли следующим образом, используя праймеры с последовательностями SEQ ID NO: 33 и 34, специфичные для полученных генов. В частности, реагенты и прилагаемый буфер добавляли к 0,25 мкл образца, полученного в реакции обратной транскрипции до общего объема 25 мкл, так чтобы полученная смесь содержала указанные выше праймеры по 2 мкМ каждого, dNTP по 0,2 мМ каждого и 0,65 единиц полимеразы ExTaq (Takara Shuzo Co., Ltd.). ПЦР осуществляли повторением цикла: при 94°C в течение 30 секунд, при 60°C в течение 30 секунд и при 72°C в течение 30 секунд, 30 раз, используя термоциклер (BIO RAD). Указанные выше специфичные по отношению к генам праймеры способны амплифицировать область в диапазоне от нуклеотида 206 до нуклеотида 632 в нуклеотидной последовательности SEQ ID NO: 5 (ген CAPRIN-1 собаки) и область в диапазоне от нуклеотида 698 до нуклеотида 1124 в нуклеотидной последовательности SEQ ID NO: 1 (ген CAPRIN-1 человека). В качестве контроля для сравнения также одновременно использовали GAPDH-специфичные праймеры с последовательностями SEQ ID NO: 35 и 36. В результате, как показано на фиг. 1, среди исследованных нормальных тканей собаки сильную экспрессию наблюдали в семенниках, кроме того, наблюдали экспрессию в тканях рака молочной железы собаки и аденокарциномы. Кроме того, также проводили исследование экспрессии гомолога человека с полученных генов. В результате, подобно случаю с геном CAPRIN-1 собаки, из всех нормальных тканей экспрессию можно было наблюдать только семенниках. Однако в случае злокачественных клеток экспрессию регистрировали во многих типах линий злокачественных клеток, включая линии злокачественных клеток молочной железы, опухоли головного мозга, лейкоза, линии злокачественных клеток легкого и пищевода. Экспрессию, в частности, наблюдали во многих линиях злокачественных клеток молочной железы. Результаты подтвердили, что экспрессия CAPRIN-1 не наблюдается в нормальных тканях, отличных от ткани семенников, тогда как CAPRIN-1 экспрессировался во многих злокачественных клетках и, в частности, в линиях злокачественных клеток молочной железы.
На фиг. 1, цифровой указатель 1 на каждой вертикальной оси обозначает картины экспрессии генов, идентифицированных выше, а цифровой указатель 2 обозначает картины экспрессии гена GAPDH в качестве контроля.
(5) Иммуногистохимическое окрашивание
(5)-1. Экспрессия CAPRIN-1 в нормальных тканях мыши и собаки
У мышей (Balb/c, самки) и собак (бигль, самки) собирали кровь при анестезии эфиром и анестезии кетамином/изофлураном. После лапаротомии каждый орган (желудок, печень, глазное яблоко, вилочковую железу, мышцу, костный мозг, матку, тонкую кишку, пищевод, сердце, почку, слюнную железу, толстую кишку, молочную железу, головное мозг, легкое, кожу, надпочечник, яичник, поджелудочную железу, селезенку и мочевой пузырь) переносили в чашку диаметром 10 см, содержащую PBS. Каждый орган рассекали в PBS и затем подвергали перфузионной фиксации в течение ночи в 0,1 М фосфатном буфере (pH 7,4), содержащем 4% параформальдегида (PFA). Перфузируемый раствор удаляли, поверхность ткани каждого органа промывали PBS, раствор PBS, содержащий 10% сахарозы, заливали в центрифужную пробирку объемом 50 мл, каждую ткань добавляли в пробирку и затем пробирку встряхивали, используя ротор, при 4°C в течение 2 часов. Раствор заменяли раствором PBS, содержащим 20% сахарозы, и затем оставляли стоять при 4°C вплоть до оседания и погружения ткани. Раствор заменяли раствором PBS, содержащим 30% сахарозы и затем оставляли стоять при 4°C вплоть до оседания и погружения ткани. Ткань извлекали и затем нужные части вырезали хирургическим скальпелем. Затем к ткани добавляли соединение OCT (Tissue Tek), так чтобы оно было тщательно нанесено на поверхность ткани, и затем ткань помещали в Cryomold. Cryomold помещали на сухой лед для быстрого замораживания. Затем делали срезы ткани толщиной от 10 мкм до 20 мкм, используя криостат (LEICA). Срезы сушили на воздухе на предметных стеклах, используя фен для волос, в течение 30 минут, получая срезы ткани на предметных стеклах. Затем каждый образец помещали в сосуд для окрашивания, заполненный PBS-T (раствор соли, содержащий 0,05% твин 20), и затем осуществляли замену PBS-T, повторяемую три раза каждые 5 минут. Избыточную воду вокруг срезов удаляли, используя салфетки Kimwipes, и затем срезы обводили, используя карандаш DAKOPEN (DAKO). В качестве блокирующих растворов реагент, блокирующий Ig мыши MOM (VECTASTAIN), и раствор PBS-T, содержащий 10% FBS, наслаивали на ткань мыши и ткань собаки, соответственно, и затем оставляли стоять во влажной камере при комнатной температуре в течение 1 часа. Затем сверху помещали раствор моноклонального анти-CAPRIN-1-антитела (моноклональное антитело №6; полученного, как описано в примере 3) в концентрации 10 мкг/мл, доведенной с использованием блокирующего раствора, которое взаимодействует с поверхностями злокачественных клеток и имеет вариабельную область тяжелой цепи SEQ ID NO: 73 и вариабельную область легкой цепи SEQ ID NO: 77, и затем оставляли стоять в течение ночи во влажной камере при 4°C. 10-минутную промывку в PBS-T осуществляли 3 раза и затем наносили меченое биотином анти-IgG-антитело MOM (VECTASTAIN), разбавленное в 250 раз блокирующим раствором, и затем оставляли стоять во влажной камере при комнатной температуре на 5 минут. После 10-минутной промывки в PBS-T, проводимой 3 раза, наносили раствор для развития окраски DAB (DAB 10 мг + 30% H2O2, 10 мкл/0,05 М трис-HCl (pH 7,6) 50 мл) и затем образец оставляли стоять во влажной камере при комнатной температуре на 30 минут. После промывки дистиллированной водой наносили реагент гематоксилин (DAKO), образец оставляли стоять при комнатной температуре в течение 1 минуты и затем промывали дистиллированной водой. Предметные стекла погружали в 70%, 80%, 90%, 95% и затем в 100% растворы этанола в указанном порядке на 1 минуту в каждый и затем оставляли стоять в течение ночи в ксилене. Предметные стекла извлекали, герметично заливали в среду для заливки Glycergel (DAKO) и затем анализировали. В результате незначительная экспрессия CAPRIN-1 наблюдалась в клетках каждой ткани слюнной железы, почки, ободочной кишки и желудка, но экспрессия этого белка не наблюдалась на поверхности клеток. Кроме того, в тканях других органов экспрессию не наблюдали. Кроме того, сходные результаты получали в случае использования моноклонального антитела против CAPRIN-1 (моноклонального антитела №9), содержащего вариабельную область тяжелой цепи SEQ ID NO: 103 и вариабельную область легкой цепи SEQ ID NO: 107.
(5)-2 Экспрессия CAPRIN-1 в ткани рака молочной железы собаки
Замороженные срезы на стеклах готовили способом, подобным способу, описанному выше, используя 108 замороженных образцов ткани рака молочной железы собак, у которых диагностировано наличие патологии, рака молочной железы, и осуществляли иммуногистохимическое окрашивание, используя моноклональное антитело №6, полученное, как описано в примере 3. В результате экспрессию CAPRIN-1 наблюдали в 100 из 108 образцов (92,5%) и высокую экспрессию CAPRIN-1 наблюдали на поверхности злокачественных клеток с особенно высокой степенью атипии. Кроме того, сходные результаты получали в случае использования моноклонального антитела №9, полученного, как описано в примере 3.
(5)-3 Экспрессия CAPRIN-1 в тканях рака молочной железы человека
Иммуногистохимическое окрашивание осуществляли, используя 188 образцов ткани рака молочной железы, на залитой в парафин матрице тканей рака молочной железы человека (BIOMAX). После 3-часовой обработки матрицы тканей рака молочной железы человека при 60°C матрицу помещали в сосуд для окрашивания, заполненный ксиленом, с последующими сменами ксилена, повторяемыми три раза каждые 5 минут. Затем подобную процедуру осуществляли с использованием этанола и PBS-T вместо ксилена. Матрицу тканей рака молочной железы человека помещали в сосуд для окрашивания, наполненный 10 мМ цитратным буфером (pH 6,0), содержащим 0,05% твин 20. После 5-минутной обработки при 125°C матрицу оставляли стоять при комнатной температуре на 40 минут или больше. Избыточную воду вокруг срезов удаляли, используя салфетки Kimwipes, и затем срезы обводили, используя карандаш DAKOPEN, и по каплям добавляли соответствующие количества блокатора пероксидазы (DAKO). После отстаивания при комнатной температуре в течение 5 минут матрицу помещали в сосуд для окрашивания, наполненный PBS-T, с последующими сменами PBS-T, повторяемыми три раза каждые 5 минут. В качестве блокирующего раствора раствор PBS-T, содержащий 10% FBS наносили на матрицу и затем матрицу оставляли стоять во влажной камере при комнатной температуре в течение 1 часа. Затем наносили раствор, содержащий моноклональное антитело №6 (полученного, как описано в примере 4), имеющий концентрацию 10 мкг/мл, которую доводили, используя раствор PBS-T, содержащий 5% FBS, которое взаимодействует с поверхностями злокачественных клеток, и матрицу оставляли стоять в течение ночи во влажной камере при 4°C. Затем 3 раза проводили десятиминутные (10 минут) промывки PBS-T, по каплям добавляли меченый пероксидазой конъюгированный полимер (DAKO) в соответствующих количествах и затем матрицу оставляли стоять во влажной камере при комнатной температуре на 30 минут. Затем 3 раза осуществляли десятиминутные (10 минут) промывки в PBS-T, наносили красящий раствор DAB (DAKO) и затем оставляли стоять при комнатной температуре в течение примерно 10 минут. Красящий раствор удаляли, 3 раза промывали в PBS-T по 10 минут и затем промывали дистиллированной водой. Матрицу погружали в 70%, 80%, 90%, 95% и затем 100% растворы этанола в указанном порядке на 1 минуту в каждый и затем оставляли стоять в ксилене в течение ночи. Предметные стекла извлекали, герметично заливали в среду для заливки Glycergel (DAKO) и затем анализировали. В результате наблюдали сильную экспрессию CAPRIN-1 в 138 из 188 образцов тканей рака молочной железы (73%). Кроме того, сходные результаты получали в случае использования моноклонального антитела №2 или №9, полученного, как описано в примере 3.
(5)-4 Экспрессия CAPRIN-1 в злокачественной опухоли головного мозга человека
Иммуногистохимическое окрашивание осуществляли способом, подобным способу, используемому как описано в разделе (5)-3 выше, на 247 образцах ткани злокачественной опухоли головного мозга на залитой в парафин матрице тканей злокачественных опухолей головного мозга человека (BIOMAX), используя антитело №6, полученное, как описано в примере 3. В результате наблюдали высокую экспрессию CAPRIN-1 в 227 из 247 образцов тканей злокачественных опухолей головного мозга (92%). Кроме того, сходные результаты получали в случае использования моноклонального антитела №2 или №9, полученного, как описано в примере 3.
(5)-5 Экспрессия CAPRIN-1 в метастазах рака молочной железы человека в лимфатических узлах
Иммуногистохимическое окрашивание осуществляли способом, подобным способу, описанному в разделе (5)-3 выше, используя 150 образцов ткани метастазов рака молочной железы в лимфатических узлах на залитой в парафин матрице метастазов рака молочной железы человека в лимфатических узлах (BIOMAX), используя моноклональное антитело №6, полученное, как описано в примере 3. В результате наблюдали высокую экспрессию CAPRIN-1 в 136 из 150 образцов тканей метастазов рака молочной железы в лимфатических узлах (90%). В частности, было выявлено, что CAPRIN-1 экспрессируется на высоком уровне также в злокачественных тканях, которые метастазировали из рака молочной железы. Кроме того, сходные результаты получали в случае использования моноклонального антитела №2 или №9, полученного, как описано в примере 3.
(5)-6 Экспрессия CAPRIN-1 в различных тканях рака человека
Иммуногистохимическое окрашивание осуществляли способом, подобным способу, описанному выше, используя образцы на различных залитых в парафин матрицах рака человека (BIOMAX) с использованием моноклонального антитела №6, полученного, как описано в примере 3. В результате наблюдали высокую экспрессию CAPRIN-1 в ткани рака пищевода, рака ободочной кишки, рака прямой кишки, рака легкого, рака почек, рака мочевого пузыря и рака шейки матки. Кроме того, сходные результаты получали в случае использования моноклонального антитела №2 или №9.
Пример 2. Получение нового белка ракового антигена человека
(1) Получение рекомбинантного белка
На основе гена с последовательностью SEQ ID NO: 1, полученного, как описано в примере 1, получали рекомбинантный белок с гомологичного гена человека следующим способом. ПЦР осуществляли в общем объеме 50 мкл, содержащем 1 мкл кДНК (экспрессия которой была подтверждена способом ОТ-ПЦР для кДНК, используемой в данной случае из числа кДНК, полученной из злокачественной ткани молочной железы или злокачественных клеток молочной железы), два праймера (SEQ ID NO: 38 и 39, содержащие последовательности расщепления ферментами рестрикции Sac I и Xho I) по 0,4 мкМ каждого, 0,2 мМ dNTP и 1,25 единиц полимеразы PrimeSTAR HS (Takara Shuzo Co., Ltd.), полученном добавлением реагентов и прилагаемого буфера. ПЦР осуществляли, повторяя следующий цикл: 98°C в течение 10 секунд и 68°C в течение 2,5 минут, 30 раз, используя термоциклер (BIO RAD). Два праймера, указанные выше, способны амплифицировать область, кодирующую полную аминокислотную последовательность SEQ ID NO: 2. После ПЦР амплифицированную таким образом ДНК подвергали электрофорезу в 1% агарозном геле и затем фрагмент ДНК размером примерно 2,1 т.п.н. очищали, используя набор для экстракции из геля QIAquick (QIAGEN).
Очищенный таким образом фрагмент ДНК фрагмент лигировали в клонирующий вектор PCR-Blunt (Invitrogen). После трансформации Escherichia coli указанным вектором собирали плазмиду. Секвенированием было подтверждено, что амплифицированный таким образом фрагмент гена имеет представляющую интерес последовательность. Плазмиду, имеющую последовательность, совпадающую с представляющей интерес последовательностью, обрабатывали ферментами рестрикции Sac I и Xho I и затем очищали, используя набор для экстракции из геля QIAquick. Представляющую интерес последовательность гена встраивали в экспрессирующий вектор Escherichia coli pET30a (Novagen), обработанный ферментами рестрикции Sac I и Xho I. С использованием такого вектора может быть получен слитый с His-меткой рекомбинантный белок. Плазмидой трансформировали Escherichia coli для рекомбинантной экспрессии, BL21(DE3), и затем индуцировали экспрессию, используя 1 мМ IPTG, так что клетки Escherichia coli экспрессировали представляющий интерес белок.
(2) Очистка рекомбинантного белка
Полученные как описано выше рекомбинантные клетки Escherichia coli, экспрессирующие ген с последовательностью SEQ ID NO: 1, культивировали в среде LB, содержащей 30 мкг/мл канамицина, при 37°C вплоть до достижения оптической плотности при 600 нм около 0,7, добавляли изопропил-β-D-1-тиогалактопиранозид в конечной концентрации 1 мМ и затем клетки культивировали при 37°C в течение 4 часов. Затем осуществляли центрифугирование при 4800 об/мин в течение 10 минут и затем клетки собирали. Полученный осадок клеток суспендировали в фосфатно-солевом буфере и центрифугировали при 4800 об/мин в течение 10 минут и затем клетки промывали.
Клетки суспендировали в фосфатно-солевом буфере и затем разрушали обработкой ультразвуком на льду. Полученный лизат обработанных ультразвуком клеток Escherichia coli подвергали центрифугированию при 6000 об./мин в течение 20 минут и затем полученный надосадок считали растворимой фракцией, а преципитат считали нерастворимой фракцией.
Растворимую фракцию наносили на никель-хелатную колонку, подготовленную обычным способом (носитель: хелатирующая сефароза Fast Flow (GE HealthCare); емкость колонки 5 мл; и буфер для уравновешивания: 50 мМ гидрохлоридный буфер (pH 8,0)). Неадсорбированные фракции смывали, используя 50 мМ гидрохлоридный буфер (pH 8,0) в количестве, в 10 раз превышающем емкость колонки, и 20 мМ фосфатный буфер (pH 8,0) содержащий 20 мМ имидазола. Сразу после промывки элюировали 6 слоев, используя 20 мМ фосфатный буфер (pH 8,0), содержащий 100 мМ имидазола. Элюирование представляющего интерес белка подтверждали окрашиванием Кумасси фракции, элюируемой 20 мМ фосфатным буфером (pH 8,0), содержащим 100 мМ имидазола, и затем элюированную фракцию наносили на колонку с сильным анионообменником (носитель: Q-сефароза Fast Flow (GE HealthCare); емкость колонки 5 мл; и 20 мМ фосфатный буфер (pH 8,0) в качестве буфера для уравновешивания). Неадсорбированную фракцию смывали 20 мМ фосфатным буфером (pH 7,0) в количестве, в 10 раз превышающим емкость колонки, и 20 мМ фосфатным буфером (pH 7,0), содержащим 200 мМ хлорида натрия. Сразу после промывки элюировали 5 слоев с использованием 20 мМ фосфатного буфера (pH 7,0), содержащего 400 мМ хлорида натрия, и таким образом получали очищенную фракцию белка, имеющего аминокислотную последовательность, представленную в SEQ ID NO: 2.
200 мкл каждого очищенного образца, полученного описанным выше способом, вносили в 1 мл буфера для реакции (20 мМ трис-HCl, 50 мМ NaCl, 2 мМ CaCl2, pH 7,4) с последующим добавлением 2 мкл энтерокиназы (Novagen). Затем полученную смесь оставлял стоять в течение ночи при комнатной температуре для осуществления реакции, чтобы отщепить His-метку, и затем осуществляли очистку, используя набор для улавливания продукта расщепления энтерокиназой (Novagen) согласно прилагаемым протоколам. Затем 1,2 мл очищенного образца, полученного указанным выше способом, подвергали замене буфера на физиологический фосфатный буфер (Nissui Pharmaceutical Co., Ltd.), используя устройство для ультрафильтрации NANOSEP 10K OMEGA (PALL). Затем осуществляли стерильную фильтрацию, используя HT Tuffryn Acrodisc 0,22 мкм (PALL) и затем полученный материал использовали для дальнейшего эксперимента.
Пример 3
Получение моноклонального антитела цыпленка против CAPRIN-1
100 мкг антигенного белка (CAPRIN-1 человека), показанного в виде SEQ ID NO: 2, полученного согласно примеру 2, смешивали с эквивалентным количеством адъюванта MPL+TDM (Sigma) и затем использовали в качестве раствора антигена для одной мыши. Раствор антигена вводили внутрибрюшинно мышам Balb/c 6-недельного возраста (Japan SLC Inc.) и затем введение осуществляли 3 раза каждую неделю (всего 24 введения), таким образом осуществляя иммунизацию. Каждую селезенку вырезали через 4 дня после конечной иммунизации, и помещали между двумя стерилизованными предметными стеклами и затем раздавливали. Полученный материал промывали PBS(-) (Nissui) и затем центрифугировали при 1500 об/мин в течение 10 минут, чтобы удалить надосадок. Указанную процедуру повторяли 3 раза, получая спленоциты. Полученные таким образом спленоциты и клетки миеломы мышей SP2/0 (приобретенные из ATCC) смешивали в соотношении 10:1. К смеси добавляли раствор ПЭГ, приготовленный смешиванием 200 мкл среды RPMI1640, содержащей 10% FBS, нагретой до 37°C, и 800 мкл ПЭГ1500 (Boehringer), оставляли стоять в течение 5 минут для слияния клеток и затем подвергали центрифугированию при 1700 об/мин в течение 5 минут. После удаления надосадка клетки суспендировали в 150 мл среды RPMI1640, содержащей 15% FBS, с добавлением раствора HAT (Gibco) (2% эквивалент) (селективная среда HAT), и затем суспензию клеток высевали на тридцать 96-луночных планшетов (Nunc) по 100 мкл на лунку. Клетки культивировали в течение 7 суток при 37°C в условиях 5% CO2, получая гибридомы в результате слияния спленоцитов и клеток миеломы цыпленка.
Гибридомы отбирали, используя в качестве маркера аффинность связывания антитела, продуцируемого полученными гибридомами, с белком CAPRIN-1. Раствор белка CAPRIN-1 (1 мкг/мл), полученный, как описано в примере 1, добавляли в 96-луночный планшет по 100 мкл на лунку и затем оставляли стоять при 4°C в течение 18 часов. Каждую лунку промывали 3 раза PBS-T, в лунки добавляли по 400 мкл 0,5% раствора бычьего сывороточного альбумина (БСА) (SIGMA) и затем планшет оставляли стоять при комнатной температуре в течение 3 часов. Раствор удаляли и затем лунки три раза промывали 400 мкл PBS-T на лунку. Надосадок культуры полученных как описано выше гибридом добавляли по 100 мкл на лунку и затем оставляли стоять при комнатной температуре на 2 часа. После промывки каждой лунки три раза PBS-T добавляли HRP-меченое антитело против IgG (H+L) мыши (Invitrogen), разбавленное в 5000 раз в PBS, по 100 мкл на лунку и затем полученную смесь оставляли стоять при комнатной температуре на 1 час. После промывки лунок три раза PBS-T в лунки добавляли по 100 мкл раствора субстрата TMB (Thermo) и затем оставляли стоять на 15-30 минут для цветной реакции. После развития окраски в лунки добавляли по 100 мкл 1N серной кислоты, чтобы остановить реакцию, и затем измеряли оптическую плотность при 450 нм и 595 нм, используя абсорбционный спектрометр. В результате было отобрано несколько гидридом, продуцирующих антитела, с высокими значениями оптической плотности.
Отобранные таким образом гибридомы добавляли в 96-луночный планшет по 0,5 клеток на лунку и затем культивировали. Спустя 1 неделю наблюдали гибридомы, которые образовали отдельные колонии в лунках. Такие клетки в лунках дополнительно культивировали и затем отбирали гибридомы, используя в качестве маркера аффинность связывания антител, продуцируемых клонированными гибридомами, с белком CAPRIN-1. Раствор белка CAPRIN-1 (1 мкг/мл), полученного согласно примеру 1, добавляли в 96-луночный планшет по 100 мкл на лунку и затем оставляли стоять при 4°C на 18 часов. Каждую лунку промывали три раза PBS-T, добавляли по 400 мкл 0,5% раствора БСА и затем планшет оставляли стоять при комнатной температуре на 3 часа. Раствор удаляли и затем лунки три раза промывали, добавляя по 400 мкл PBS-T на лунку. По 100 мкл каждого надосадка культуры полученных как описано выше гибридом добавляли на лунку и затем планшет оставляли стоять при комнатной температуре на 2 часа. После промывки каждой лунки три раза PBS-T в лунки добавляли по 100 мкл HRP-меченого антитела против IgG (H+L) мыши (Invitrogen), разбавленного в 5000 раз в PBS, и затем оставляли стоять при комнатной температуре на 1 час. После промывки лунок три раза PBS-T в лунки добавляли по 100 мкл раствора субстрата TMB (Thermo) и затем оставляли стоять на 15-30 минут для цветной реакции. После развития окраски добавляли по 100 мкл 1N серой кислоты на лунку, чтобы остановить реакцию и затем измеряли оптические плотности при 450 нм и 595 нм, используя абсорбционный спектрометр. В результате получили 150 линий клеток гибридом, продуцирующих моноклональные антитела, реактивные по отношению к белку CAPRIN-1.
Затем из указанных моноклональных антител отбирали антитела, реактивные по отношению к клеточным поверхностям злокачественных клеток молочной железы, экспрессирующих CAPRIN-1. В частности, 106 клеток линии злокачественных клеток молочной железы человека MDA-MB-231V центрифугировали в микроцентрифужной пробирке объемом 1,5 мл и в пробирку добавляли 100 мкл надосадка культуры каждой из указанных выше гибридом и затем пробирку оставляли стоять на льду на 1 час. После промывки в PBS добавляли ФИТЦ-меченое антитело козы против IgG мыши (Invitrogen), разбавленное в 500 раз в PBS, содержащем 0,1% FBS, и затем оставляли стоять на льду на 1 час. После промывки PBS измеряли интенсивность флуоресценции, используя FACS caliber (Becton, Dickinson and Company). Тем временем осуществляли операции, сходные с указанными выше, используя сыворотку (мыши Balb/c 6-недельного возраста, не обработанную антителами), разбавленную в 500 раз средой для культивирования гибридом, таким образом получая контрольный образец. В результате, были отобраны 11а моноклональных антител (№1-№11), которые давали более высокую интенсивность флуоресценции, чем в контроле, а значит, которые взаимодействовали с клеточными поверхностями злокачественных клеток молочной железы.
Пример 4. Характеристика отобранных антител
(1) Клонирование гена вариабельной области моноклонального анти-CAPRIN-1-антитела
мРНК экстрагировали из каждой линии клеток гибридомы, продуцирующей каждое из 11 мышиных моноклональных антител, отобранных, как описано в примере 3. Гены вариабельной области тяжелой цепи (VH) и вариабельной области легкой цепи (VL) всех моноклональных анти-CAPRIN-1-антител получали способом ОТ-ПЦР с использованием праймеров, специфичных для последовательности, полученной из FR1 мыши и последовательности, полученной из FR4 мыши. Для определения последовательности такие гены клонировали в векторе pCR2.1 (Invitrogen). Кроме того, экстрагировали мРНК из двух линий клеток гибридом, полученных от мышей, продуцирующих моноклональные антитела, взаимодействующие с поверхностью злокачественных клеток молочной железы, экспрессирующих CAPRIN-1. Гены вариабельной области тяжелой цепи (VH) и вариабельной области легкой цепи (VL) каждого антитела получали способом ОТ-ПЦР, используя праймеры, специфичные для последовательности, полученной из FR1 мыши, и последовательности, полученной из FR4 мыши. Для определения последовательности такие гены клонировали в векторе pCR2.1 (Invitrogen).
(1)-1 ОТ-ПЦР
После экстракции суммарной РНК из 106 клеток каждой линии клеток гибридом с использованием набора для выделения высокоочищенной РНК (Roche) синтезировали кДНК, используя набор для синтеза 1-й нити кДНК PrimeScriptII (Takara). Указанный способ осуществляли согласно протоколам, прилагаемым к каждому набору.
Ген вариабельной области тяжелой цепи антитела мыши и ген вариабельной области легкой цепи мыши амплифицировали способом ПЦР согласно обычной методике, используя синтезированную таким образом кДНК в качестве матрицы и полимеразу KOD-Plus-DNA (TOYOBO).
Чтобы получить гены VH- и VL-областей антитела мыши, использовали праймер (SEQ ID NO: 130), специфичный к последовательности FR1 тяжелой цепи мыши, праймер (SEQ ID NO: 131), специфичный к последовательности FR4 тяжелой цепи мыши, праймер (SEQ ID NO: 132), специфичный к последовательности FR1 легкой цепи мыши, праймер (SEQ ID NO: 133), специфичный к последовательности FR4 легкой цепи мыши.
Каждый из полученных таким образом продуктов ПЦР подвергали электрофорезу в агарозном геле и полосы ДНК VH-области и VL-области вырезали. Фрагменты ДНК очищали, используя набор для очистки из геля QIAquick (QIAGEN) согласно прилагаемым протоколам. Очищенную кДНК клонировали в векторе pCR2.1, используя набор для клонирования TA (Invitrogen). Лигированным вектором трансформировали компетентные клетки DH5 (TOYOBO) согласно стандартному способу. 10 клонов каждого трансформанта культивировали в течение ночи в среде (100 мкг/мл ампициллина) при 37°C и затем плазмидную ДНК очищали, используя набор Qiaspin Miniprep (QIAGEN).
(1)-2. Определение последовательности
Последовательности генов VH-области и VL-области в каждой плазмиде, полученной как описано выше, анализировали, используя прямой праймер M13 (SEQ ID NO: 134) и обратный праймер M13 (SEQ ID NO: 135) на флуоресцентном секвенаторе (секвенатор ДНК 3130XL; ABI), используя набор для секвенирования Big Dye Terminator Ver3.1 Cycle (ABI) согласно прилагаемым протоколам. В результате определили последовательности каждого гена. Последовательности в 10 клонах были идентичными.
Последовательности генов вариабельных областей тяжелой цепи полученных таким образом моноклональных антител представлены в виде SEQ ID NO: 48, 78, 88, 98, 108, 118 и 128, и аминокислотные последовательности вариабельных областей тяжелой цепи представлены в виде последовательностей SEQ ID NO: 43, 73, 83, 93, 103, 113 и 123. Последовательности генов вариабельных областей легкой цепи тех же моноклональных антител представлены в виде SEQ ID NO: 49, 54, 59, 64, 69, 79, 89, 99, 109, 119 и 129, и аминокислотные последовательности вариабельных областей легкой цепи представлены в виде SEQ ID NO: 47, 53, 58, 63, 68, 77, 87, 97, 107,117 и 127.
В частности, моноклональное антитело №1 содержит вариабельную область тяжелой цепи с последовательностью SEQ ID NO: 43 и вариабельную область легкой цепи с последовательностью SEQ ID NO: 47, №2 содержит вариабельную область тяжелой цепи с последовательностью SEQ ID NO: 43 и вариабельную область легкой цепи с последовательностью SEQ ID NO: 53, №3 содержит вариабельную область тяжелой цепи с последовательностью SEQ ID NO: 43 и вариабельную область легкой цепи с последовательностью SEQ ID NO: 58, №4 содержит вариабельную область тяжелой цепи с последовательностью SEQ ID NO: 43 и вариабельную область легкой цепи с последовательностью SEQ ID NO: 63, №5 содержит вариабельную область тяжелой цепи с последовательностью SEQ ID NO: 43 и вариабельную область легкой цепи с последовательностью SEQ ID NO: 68, №6 содержит вариабельную область тяжелой цепи с последовательностью SEQ ID NO: 73 и вариабельную область легкой цепи с последовательностью SEQ ID NO: 77, №7 содержит вариабельную область тяжелой цепи с последовательностью SEQ ID NO: 83 и вариабельную область легкой цепи с последовательностью SEQ ID NO: 87, №8 содержит вариабельную область тяжелой цепи с последовательностью SEQ ID NO: 93 и вариабельную область легкой цепи с последовательностью SEQ ID NO: 97, №9 содержит вариабельную область тяжелой цепи с последовательностью SEQ ID NO: 103 и вариабельную область легкой цепи с последовательностью SEQ ID NO: 107, №10 содержит вариабельную область тяжелой цепи с последовательностью SEQ ID NO: 113 и вариабельную область легкой цепи с последовательностью SEQ ID NO: 117, и №11 содержит вариабельную область тяжелой цепи с последовательностью SEQ ID NO: 123 и вариабельную область легкой цепи с последовательностью SEQ ID NO: 127.
(2) Экспрессия CAPRIN-1 на поверхности различных злокачественных клеток, исследованная с использованием анти-CAPRIN-1-антител №2 и №9
Затем 7 линий злокачественных клеток молочной железы (MDA-MB-157, T47D, MRK-nu-1, MDA-MB-231V, BT20, SK-BR-3 и MDA-MB-231T), в случае которых наблюдали экспрессию гена CAPRIN-1, и 3 других линии злокачественных клеток молочной железы (MDA-MB-231C, MCF-7 и ZR75-1), 5 линий клеток глиомы (T98G, SNB19, U251, U87MG и U373), 4 линии злокачественных клеток почек (Caki-1, Caki-2, A498 и ACHN), 2 линии злокачественных клеток желудка (MKN28 и MKN45), 5 линий злокачественных клеток прямой и ободочной кишки (HT29, LoVo, Caco2, SW480 и HCT116), 3 линии злокачественных клеток легкого (A549, QG56 и PC8), 4 линии лейкозных клеток (AML5, Namalwa, BDCM, RPI1788), одну (1) линию клеток лимфомы (Ramos), одну линию злокачественных клеток шейки матки (SW756), одну линию злокачественных клеток мочевого пузыря (T24) и одну линию злокачественных клеток пищевода (KYSE180) исследовали в отношении экспрессии белка CAPRIN-1 на поверхности клеток каждой линии клеток, используя надосадки культур гибридом, продуцирующих антитела №2 и №9, полученные как описано в примере 3. 106 клеток каждой линии клеток центрифугировали, используя микроцентрифужную пробирку объемом 1,5 мл. Каждый надосадок (100 мкл) культуры гибридом, продуцирующих антитела №2 и №9, полученные как описано в примере 3, добавляли и затем оставляли стоять на льду в течение 1 часа. После промывки PBS добавляли ФИТЦ-меченое антитело козы против IgG (H+L) человека (SouthernBiotech), разбавленное в 500 раз в PBS, содержащем 0,1% FBS, и ФИТЦ-меченое антитело против IgG (H+L) мыши (Invitrogen) и затем полученную смесь оставляли стоять на льду в течение 1 часа. После промывки PBS измеряли интенсивность флуоресценции, используя FACS Calibur (Becton, Dickinson и Company). Тем временем осуществляли способ, подобный описанному выше, используя среду для культивирования гибридом, и использовали в качестве негативного контроля. В результате, клетки, к которым были добавлены антитела №2 и №9, имели интенсивность флуоресценции выше на 20% или больше, чем в случае контроля. Полученные результаты показали, что белок CAPRIN-1 экспрессировался на поверхности клеточной мембраны указанных выше различных линий злокачественных клеток человека. Усиление указанной выше интенсивности флуоресценции в процентах выражали в виде увеличения в процентах средней интенсивности флуоресценции (уровень MFI) в каждом типе клеток и вычисляли по следующей формуле.
Увеличение средней интенсивности флуоресценции в процентах (усиление интенсивности флуоресценции в процентах) (%) = ((уровень MFI клеток, подвергнутых взаимодействию с антителом против CAPRIN-1 человека) - (уровень MFI в контроле))/(уровень MFI в контроле) ×100.
(3) Противоопухолевое действие анти-CAPRIN-1-антител на злокачественные клетки (ADCC-активность).
Отобранные, как описано выше, моноклональные анти-CAPRIN-1-антитела №1-№11 оценивали в отношении их цитотоксической активности против злокачественных клеток (ADCC-активности). Каждую из гибридом, продуцирующих моноклональные антитела №1-№11, культивировали, используя среду для гибридом SFM (Invitrogen). Полученный при этом надосадок очищали, используя колонку с белок-A-сефарозой FF Hitrap (GE HealthCare) с заменой на PBS(-) и затем фильтровали, используя фильтр 0,22 мкм (Millipore). Полученные фильтраты использовали в качестве антител для анализа. Линию злокачественных клеток молочной железы человека MDA-MB-157 (106 клеток) собирали в центрифужную пробирку объемом 50 мл, в которую добавляли 100 микрокюри хрома (Cr)-51 и инкубировали при 37°C в течение 2 часов. Затем клетки 3 раза промывали средой RPMI1640, содержащей 10% FBS, и затем разносили в каждую лунку 96-луночного планшета с V-образным дном по 103 клеток на лунку. Полученные таким образом клетки использовали в качестве клеток-мишеней. К клеткам добавляли очищенные как описано выше антитела (1 мкг каждого). Отдельно добавляли спленоциты мыши, выделенные из селезенки мышей (2×105 клеток) и затем культивировали в условиях 37°C и 5% CO2 в течение 4 часов. После культивирования измеряли количество хрома (Cr)- 51, высвобождаемого из цитотоксически поврежденных опухолевых клеток в надосадок культуры, при этом вычисляя ADCC-активность для каждого анти-CAPRIN-1-антитела, направленную против злокачественных клеток. В результате все моноклональные антитела №1-№11 проявляли 20% или более высокую ADCC-активность против MDA-MB-157. В частности, например, в случае антитела №1 наблюдали 22,1% цитотоксическую активность, в случае №2 наблюдали 29,1% цитотоксическую активность, в случае №6 наблюдали 30,2% цитотоксическую активность и в случае №9 наблюдали 32,4% цитотоксическую активность (см. фиг. 1). С другой стороны сходные процедуры осуществляли, используя моноклональные антитела (которые получены, как описано в примере 2), реактивные по отношению к самому белку CAPRIN-1, но не взаимодействующие с поверхностью злокачественных клеток, при этом не наблюдали цитотоксической активности (см. фиг. 1). На основании приведенных выше результатов продемонстрировано, что полученные таким образом моноклональные анти-CAPRIN-1-антитела (№1-№11) цитотоксически повреждают CAPRIN-1-экспрессирующие злокачественные клетки посредством ADCC-активности. Подобным образом исследовали анти-CAPRIN-1-антитела в отношении ADCC-активности, направленной против других линий злокачественных клеток человека, включая линии клеток глиомы (T98G и U373), линии злокачественных клеток легкого (A549 и QG56), линии злокачественных клеток почек (Caki-1 и ACHN), линию злокачественных клеток шейки матки (SW756), линию злокачественных клеток мочевого пузыря (T24), линию злокачественных клеток пищевода (KYSE180), линии злокачественных клеток желудка (MKN28 и MKN45), линию злокачественных клеток прямой и ободочной кишки (SW480), линию лейкозных клеток (AML5) и линию клеток лимфомы (Ramos). В результате все моноклональные антитела №1-№11 проявляли более высокую ADCC-активность, чем антитела изотипического контроля. В частности, например, антитело №9 проявляло 12% или более высокую активность (1,3% в случае изотипического контроля) против T98G, №9 проявляло 16% или более высокую активность (3% в случае изотипического контроля) против U373, №9 проявляло 24% или более высокую активность (2,6% в случае изотипического контроля) против A549, №9 проявляло 20% или более высокую активность (0,2% в случае изотипического контроля) против QG56, №9 проявляло 23% или более высокую активность (3,0% в случае изотипического контроля) против Caki-1, №9 проявляло 14% или более высокую активность (1,5% в случае изотипического контроля) против ACHN, №9 проявляло 16% или более высокую активность (2,5% в случае изотипического контроля) против SW756, №9 проявляло 18% или более высокую активность (2,1% в случае изотипического контроля) против T24, №9 проявляло 22% или более высокую активность (3,0% в случае изотипического контроля) против KYSE180, №9 проявляло 15% или более высокую активность (1,7% в случае изотипического контроля) против MNK28, №9 проявляло 10% или более высокую активность (2,3% в случае изотипического контроля) против MNK45, №9 проявляло 17% или более высокую активность (1,3% в случае изотипического контроля) против SW480, №9 проявляло 10% или более высокую активность (3,0% в случае изотипического контроля) против AML5, и №9 проявляло 10% или более высокую активность (4,1% в случае изотипического контроля) против Ramos. Приведенные выше результаты показали, что полученные анти-CAPRIN-1-антитела (№1-№11) цитотоксически повреждали различные злокачественные клетки человека, экспрессирующие CAPRIN-1.
(4) Противоопухолевое действие анти-CAPRIN-1-антител на злокачественные клетки (CDC-активность)
Отобранные, как описано выше анти-CAPRIN-1-антитела №1-№11 оценивали в отношении их цитотоксической активности против злокачественных клеток (CDC-активности). Кровь, собранную у кролика, добавляли в пробирку Эппендорф, оставляли стоять при комнатной температуре на 60 минут и затем центрифугировали при 3000 об./мин в течение 5-минут. Таким образом получали сыворотку для анализа CDC-активности. 105 клеток линии злокачественных клеток молочной железы человека MDA-MB-231V собирали в центрифужной пробирке объемом 50 мл, в которую добавляли 100 микрокюри хрома-51 и инкубировали при 37°C в течение 2 часов. Клетки 3 раза промывали средой RPMI, содержащей 10% FBS, суспендировали в среде RPMI, содержащей полученную, как описано выше сыворотку кролика в концентрации 50% и затем разносили в каждую лунку 96-луночного планшета с V-образным дном по 103 клеток на лунку. К клеткам добавляли каждое из моноклональных антител №1-№13, полученных, как описано в примере 3 (1 мкг каждого), которые затем культивировали в условиях 37°C и 5% CO2 в течение 4 часов. После культивирования измеряли количество хрома-51, высвобождаемого из цитотоксически поврежденных опухолевых клеток в надосадок культуры, и вычисляли CDC-активность каждого моноклонального анти-CAPRIN-1-антитела, направленную против MDA-MB-231V, в надосадке культуры. В результате, все моноклональные антитела №1-№11 проявляли 30% или более высокую CDC-активность. С другой стороны, не наблюдали цитотоксической активности в том случае, когда сходные способ осуществляли с использованием моноклональных антител (которые получены, как описано в примере 2), реактивных по отношению к самому белку CAPRIN-1, но не взаимодействующие с поверхностью злокачественных клеток. Таким образом, было обнаружено, что моноклональные антитела (№1-№11) могут цитотоксически повреждать опухолевые клетки, экспрессирующие CAPRIN-1, также наблюдаемую по результатам анализа CDC-активности.
Пример 5. Идентификация пептида в белке CAPRIN-1, с которым связываются анти-CAPRIN-1-антитела, взаимодействующие с поверхностью злокачественных клеток
Неполную последовательность белка CAPRIN-1, узнаваемого полученными, как описано выше, моноклональными анти-CAPRIN-1-антителами №1-№11, взаимодействующими с поверхностью злокачественных клеток, идентифицировали, используя каждое антитело.
Сначала добавляли DTT (Fluka) к 100 мкл раствора рекомбинантного белка CAPRIN-1, приготовленного растворением белка до концентрации 1 мкг/мкл в PBS так, чтобы конечная концентрация составляла 10 мМ, с последующим 5-минутным взаимодействием при 95°C. Дисульфидные связи в белке CAPRIN-1 восстанавливали, добавляли йодацетамид (Wako Pure Chemical Industries, Ltd.) в конечной концентрации 20 мМ и затем осуществляли реакцию алкилирования тиольной группы при 37°C в защищенных от света условиях в течение 30 минут. Каждое из моноклональных анти-CAPRIN-1-антител №1-№11 добавляли (по 50 мкг каждого) к 40 мкг таким образом восстановленного и алкилированного белка CAPRIN-1. Каждый раствор разбавляли до объема 1 мл, 20 мМ фосфатным буфером (pH 7,0), с последующим взаимодействием при 4°C в течение ночи при встряхивании и перемешивании раствора.
Затем добавляли трипсин (Promega) до конечной концентрации 0,2 мкг. После взаимодействия при 37°C в течение 1 часа, 2 часов, 4 часов или 12 часов каждый полученный в результате продукт предварительно блокировали PBS, содержащим 1% БСА (Sigma), и затем смешивали со стеклянными шариками, несущими белок A (GE), которые предварительно промывали в PBS, и 1 мМ карбонатом кальция в буфере NP-40 (20 мМ фосфатный буфер (pH 7,4), 5 мМ EDTA, 150 мМ NaCl, 1% NP-40), затем проводили реакцию в течение 30 минут для каждого раствора.
Реакционную смесь промывали 25 мМ буфером на основе карбоната аммония (pH 8,0) и затем комплекс антиген-антитело элюировали, используя 100 мкл 0,1% муравьиной кислоты. Элюат подвергали ЖХ-МС-анализу, используя Q-TOF Premier (Waters-MicroMass). ЖХ-МС-анализ проводили согласно протоколам, прилагаемым к устройству.
В результате идентифицировали полипептид SEQ ID NO: 37 как неполную последовательность CAPRIN-1, которую узнает любое из моноклональных анти-CAPRIN-1-антител №1-№11.
Пример 6. Влияние противоопухолевых средств на экспрессию CAPRIN-1 на поверхности злокачественных клеток
(1) Вычисление 50% ингибирующей концентрации противоопухолевых средств против злокачественных клеток
Чтобы оценить влияние противоопухолевых средств на экспрессию CAPRIN-1 на поверхности злокачественной клетки, вычисляли 50% ингибирующую концентрацию каждого противоопухолевого средства, используя злокачественные клетки MCF-7. Используя линию злокачественных клеток молочной железы человека MCF-7, определяли 50% ингибирующие концентрации 4 типов противоопухолевых средств, которые в настоящее время применяют в качестве лекарственных средств в случае рака молочной железы (т.е. циклофосфамид: «эндоксан» (зарегистрированная торговая марка, Shionogi & Co., Ltd.), паклитаксел: «таксол» (зарегистрированная торговая марка, Bristol-Myers), доцетаксел: «таксотер» (зарегистрированная торговая марка, Sanofi-aventis K.K.), винорелбин: «навелбин» (зарегистрированная торговая марка, Kyowa Hakko Kirin Co., Ltd.)). Линию клеток готовили в концентрации 1×105 клеток/мл и затем культивировали на 6-луночной чашке в условиях 37°C и 5% CO2 в течение одних суток. Затем клетки обрабатывали каждым противоопухолевым средством в конечных концентрациях 0,001 мкМ, 0,01 мкМ, 0,1 мкМ, 1,0 мкМ и 10 мкМ с последующим 2-дневным культивированием в условиях 37°C и 5% CO2. После удаления культуральной среды клетки дважды промывали PBS(-), к которому затем добавляли 0,25% трипсин-EDTA, чтобы открепить клетки от чашки. Открепленные таким образом клетки суспендировали в PBS(-) до объема 100 мкл, к которому затем добавляли 10 мкл 0,4% исходного раствора трипанового синего, и в смеси подсчитывали количество живых клеток, используя гемоцитометр. Вычисляли долю живых клеток в случае, когда клетки были обработаны каждым противоопухолевым средством (т.е. химиотерапевтическим средством), при этом количество живых клеток в случае, когда клетки не обрабатывали никаким противоопухолевым средством, принимали за 100%. 50% ингибирующую концентрацию грубо оценивали на основе полученных значений, и каждое из противоопухолевых средств готовили так, чтобы концентрация была примерно равна определенной концентрации, которая вызывает 50% ингибирование, и затем дополнительно осуществляли способ, описанный выше, чтобы вычислить более точную концентрацию, вызывающую 50% ингибирование.
В качестве примера результаты оценки циклофосфамида (противоопухолевого средства) описаны ниже. Линию клеток MCF-7 готовили в концентрации 1×105 клеток/мл и затем культивировали на 6-луночной чашке в условиях 37°C и 5% CO2 в течение одних суток. Затем клетки обрабатывали циклофосфамидом в конечных концентрациях 1×10-1 мкМ, 5×10-2 мкМ, 2×10-2 мкМ и 1×10-2 мкМ с последующим 2-дневным культивированием в условиях 37°C и 5% CO2. После удаления культуральной среды клетки дважды промывали PBS(-), к которому добавляли 0,25% трипсин-EDTA, чтобы открепить клетки от чашки. Открепленные клетки суспендировали в PBS(-) до объема 100 мкл, к которому затем добавляли 10 мкл 0,4% исходного раствора трипанового синего. В смеси подсчитывали количество живых клеток, используя гемоцитометр. В результате определили, что вызывающая 50% ингибирование концентрация составляла 3x10-2 мкМ. Значения IC50 для соответствующих противоопухолевых средств в случае каждого типа злокачественных клеток вычисляли, используя такой же способ. Результаты показаны в таблице 1.
50% ингибирующая концентрация противоопухолевых средств против MCF-7
(2) Влияние противоопухолевых средств на экспрессию CAPRIN-1 при обработке ими злокачественных клеток
Линию злокачественных клеток MCF-7 обрабатывали каждым противоопухолевым средством в 50% ингибирующей концентрации, которую вычисляли, как описано в разделе (1) выше, и исследовали характер экспрессии белка CAPRIN-1 на клеточной поверхности.
Исследовали характер экспрессии белка CAPRIN-1 на поверхности обработанных, как описано выше, злокачественных клеток молочной железы человека MCF-7. Клетки готовили в концентрации 1×105 клеток/мл и затем культивировали на 6-луночной чашке в условиях 37°C и 5% CO2 в течение 1 суток. Затем клетки обрабатывали противоопухолевыми средствами в 50% ингибирующей концентрации, вычисленной, как описано в разделе (1) выше, или PBS(-) в качестве контроля и затем культивировали в условиях 37°C и 5% CO2 в течение 2 суток. После удаления культуральной среды клетки дважды промывали PBS(-) и затем открепляли от чашки, используя скребок для клеток. Затем клетки центрифугировали в центрифужной пробирке объемом 1,5 мл. К отделенным клеткам добавляли один (1) мкг (5 мкл) мышиного моноклонального анти-CAPRIN-1-антитела №9, затем клетки суспендировали в 95 мкл PBS, содержащего 0,1% фетальной сыворотки теленка, и затем оставляли стоять на льду на 1 час. После промывки PBS клетки суспендировали в PBS, содержащем 5 мкл ФИТЦ-меченого антитела козы против IgG кролика (SantaCruz) и 95 мкл 0,1% фетальной сыворотки теленка (FBS,) и затем оставляли стоять на льду на 1 час. После промывки PBS измеряли интенсивность флуоресценции, используя FACS caliber (Becton, Dickinson and Company). Одновременно осуществляли такой же способ, как описано выше, используя контрольное антитело вместо мышиного моноклонального анти-CAPRIN-1-антитела, и использовали в качестве контроля. В результате не наблюдали значимого различия в интенсивности флуоресценции, несмотря на обработку противоопухолевым средством. В частности, интенсивность флуоресценции, полученная в случае добавления анти-CAPRIN-1-антитела к MCF-7, не обработанным никаким противоопухолевым средством, была усилена на 32% по сравнению с интенсивностью флуоресценции в случае добавления контрольного антитела. С другой стороны, когда MCF-7 обрабатывали противоопухолевым средством, используя такой же способ, наблюдали 32% усиление интенсивности флуоресценции, и, следовательно, полученный результат был таким же, как в случае без обработки противоопухолевым средством. На основании полученных результатов выявлено, что обработка злокачественных клеток молочной железы противоопухолевым средством не оказывает влияния на экспрессию CAPRIN-1 на поверхности злокачественных клеток молочной железы. В данном случае процент усиления интенсивности флуоресценции представляли в виде увеличения в процентах средней интенсивности флуоресценции (уровень MFI) в каждой клетке и вычисляли по следующей формуле.
Процент увеличении средней интенсивности флуоресценции (усиление интенсивности флуоресценции в процентах)(%)=((уровень MFI клеток, подвергаемых взаимодействию с антителом против CAPRIN-1 человека)-( уровень MFI в контроле))÷(уровень MFI в контроле) ×100.
Пример 7. Комбинированная терапия in vivo с использованием анти-CAPRIN-1-антитела и противоопухолевого средства
(1) С использованием несущих опухоли мышей, которым трансплантировали линию злокачественных клеток молочной железы человека MCF-7, экспрессирующих CAPRIN-1, исследовали противоопухолевое действие комбинированного применения моноклонального анти-CAPRIN-1-антитела и противоопухолевых средств. Способ исследования противоопухолевого действия с использованием мышей, которым трансплантировали MCF-7, и его результаты описаны ниже. 106 клеток MCF-7 (приобретенных из ATCC) трансплантировали подкожно в область спины каждой из 280 голых мышей (Japan SLC Inc.). Мышей выращивали вплоть до момента, когда каждая опухоль достигала размера примерно 7 мм в диаметре.
Затем, как конкретно описано в следующем экспериментальном разделе 1 и экспериментальном разделе 2, несущих опухоли мышей, которым трансплантировали MCF-7, делили на 5 групп: группу, в которой вводили только анти-CAPRIN-1-антитело, группу, в которой вводили только противоопухолевое средство (4 типов), группу, в которой противоопухолевое средство и анти-Her2-антитело (мышиное моноклональное антитело против ErbB2 человека, изотип: IgG2b (R&D systems, № в каталоге MAB11291)) вводили в сочетании, группу, в которой противоопухолевое средство и моноклональное анти-CAPRIN-1-антитело вводили в сочетании, и группу, в которой вводили контрольный (PBS(-). Кроме того, PBMC мышей вводили во всех группах введения.
Экспериментальный раздел 1
(Группа, в которой вводили только анти-CAPRIN-1-антитело).
Моноклональное анти-CAPRIN-1-антитело №2 вводили внутрибрюшинно каждой из 5 несущих опухоли мышей по 5 мг/кг/инъекцию в 0, 4, 8, 11, 15 и 17 день после начала эксперимента. PBMC, выделенные из селезенки мыши Balb/c, вводили внутривенно каждой мыши по 1×107 клеток/0,2 мл (RPMI1640) в 0, 8 и 15 дни после начала эксперимента.
(Группа, в которой вводили циклофосфамид)
Циклофосфамид вводили внутрибрюшинно каждой из 5 несущих опухоли мышей по 80 мг/кг/инъекцию в 0 и 4 дни после начала эксперимента. PBMC, выделенные из селезенки мыши Balb/c, вводили внутривенно каждой мыши по 1×107 клеток/0,2 мл (RPMI1640) в 0, 8 и 15 дни после начала эксперимента.
(Группа, в которой вводили паклитаксел).
Паклитаксел вводили внутрибрюшинно каждой из 5 несущих опухоли мышей по 15 мг/кг/инъекцию в 0 и 3 дни после начала эксперимента. PBMC, выделенные из селезенки мыши Balb/c, вводили внутривенно каждой мыши по 1×107 клеток/0,2 мл (RPMI1640) в 0, 8 и 15 дни после начала эксперимента.
(Группа, в которой вводили доцетаксел)
Доцетаксел вводили внутрибрюшинно каждой из 5 несущих опухоли мышей по 10 мг/кг/инъекцию в 0 и 3 дни после начала эксперимента. PBMC, выделенные из селезенки мыши Balb/c, вводили внутривенно каждой мыши по 1×107 клеток/0,2 мл (RPMI1640) в 0, 8 и 15 дни после начала эксперимента.
(Группа, в которой вводили винорелбин)
Винорелбин вводили внутрибрюшинно каждой из 5 несущих опухоли мышей по 1 мг/кг/инъекцию в 0 день после начала эксперимента. PBMC, выделенные из селезенки мыши Balb/c, вводили внутривенно каждой мыши по 1×107 клеток/0,2 мл (RPMI1640) в 0, 8 и 15 дни после начала эксперимента.
(Группа, в которой вводили циклофосфамид и анти-Her2-антитело)
Циклофосфамид вводили внутрибрюшинно каждой из 5 несущих опухоли мышей по 80 мг/кг/инъекцию в 0 и 4 дни после начала эксперимента, и одновременно внутрибрюшинно вводили анти-Her2-антитело каждой мыши по 5 мг/кг/инъекцию в 0, 4, 8, 11, 15 и 17 дни после начала эксперимента. PBMC, выделенные из селезенки мыши Balb/c, вводили внутривенно каждой мыши по 1 x 107 клеток/0,2 мл (RPMI1640) в 0, 8 и 15 дни после начала эксперимента.
(Группа, в которой вводили паклитаксел и анти-Her2-антитело)
Паклитаксел вводили внутрибрюшинно каждой из 5 несущих опухоли мышей по 15 мг/кг/инъекцию в 0 и 3 дни после начала эксперимента, и одновременно каждой мыши внутрибрюшинно вводили анти-Her2-антитело по 5 мг/кг/инъекцию в 0, 4, 8, 11, 15 и 17 дни после начала эксперимента. PBMC, выделенные из селезенки мыши Balb/c, вводили внутривенно каждой мыши по 1×107 клеток/0,2 мл (RPMI1640) в 0, 8 и 15 дни после начала эксперимента.
(Группа, в которой вводили доцетаксел и анти-Her2-антитело)
Доцетаксел вводили внутрибрюшинно каждой из 5 несущих опухоли мышей по 10 мг/кг/инъекцию в 0 и 3 дни после начала эксперимента, и одновременно каждой мыши внутрибрюшинно вводили анти-Her2-антитело по 5 мг/кг/инъекцию в 0, 4, 8, 11, 15 и 17 дни после начала эксперимента. PBMC, выделенные из селезенки мыши Balb/c, вводили внутривенно каждой мыши по 1×107 клеток/0,2 мл (RPMI1640) в 0, 8 и 15 дни после начала эксперимента.
(Группа, в которой вводили винорелбин и анти-Her2)
Винорелбин вводили внутрибрюшинно каждой из 5 несущих опухоли мышей по 1 мг/кг/инъекцию в 0 день после начала эксперимента, и одновременно каждой мыши внутрибрюшинно вводили анти-Her2-антитело по 5 мг/кг/инъекцию в 0, 4, 8, 11, 15 и 17 дни после начала эксперимента. PBMC, выделенные из селезенки мыши Balb/c, вводили внутривенно каждой мыши по 1x107 клеток/0,2 мл (RPMI1640) в 0, 8 и 15 дни после начала эксперимента.
(Группа, в которой вводили циклофосфамид и анти-CAPRIN-1-антитело).
Циклофосфамид вводили внутрибрюшинно каждой из 5 несущих опухоли мышей по 80 мг/кг/инъекцию в 0 и 4 дни после начала эксперимента, и одновременно каждой мыши внутрибрюшинно вводили моноклональное анти-CAPRIN-1-антитело №2 по 5 мг/кг/инъекцию в 0, 4, 8, 11, 15 и 17 дни после начала эксперимента. PBMC, выделенные из селезенки мыши Balb/c, вводили внутривенно каждой мыши по 1×107 клеток/0,2 мл (RPMI1640) в 0, 8 и 15 дни после начала эксперимента.
(Группа, в которой вводили паклитаксел и анти-CAPRIN-1-антитело)
Паклитаксел вводили внутрибрюшинно каждой из 5 несущих опухоли мышей по 15 мг/кг/инъекцию в 0 и 3 дни после начала эксперимента, и одновременно каждой мыши внутрибрюшинно вводили моноклональное анти-CAPRIN-1-антитело №2 по 5 мг/кг/инъекцию в 0, 4, 8, 11, 15 и 17 дни после начала эксперимента. PBMC, выделенные из селезенки мыши Balb/c, вводили внутривенно каждой мыши по 1×107 клеток/0,2 мл (RPMI1640) в 0, 8 и 15 дни после начала эксперимента.
(Группа, в которой вводили доцетаксел и анти-CAPRIN-1-антитело)
Доцетаксел вводили внутрибрюшинно каждой из 5 несущих опухоли мышей по 10 мг/кг/инъекцию в 0 и 3 дни после начала эксперимента, и одновременно каждой мыши внутрибрюшинно вводили моноклональное анти-CAPRIN-1-антитело №2 по 5 мг/кг/инъекцию в 0, 4, 8, 11, 15 и 17 дни после начала эксперимента. PBMC, выделенные из селезенки мыши Balb/c, вводили внутривенно каждой мыши по 1×107 клеток/0,2 мл (RPMI1640) в 0, 8 и 15 дни после начала эксперимента.
(Группа, в которой вводили винорелбин и анти-CAPRIN-1-антитело)
Винорелбин вводили внутрибрюшинно каждой из 5 несущих опухоли мышей по 1 мг/кг/инъекцию в 0 день после начала эксперимента, и одновременно каждой мыши внутрибрюшинно вводили моноклональное анти-CAPRIN-1-антитело №2 по 5 мг/кг/инъекцию в 0, 4, 8, 11, 15 и 17 дни после начала эксперимента. PBMC, выделенные из селезенки мыши Balb/c, вводили внутривенно каждой мыши по 1×107 клеток/0,2 мл (RPMI1640) в 0, 8 и 15 дни после начала эксперимента.
Экспериментальный раздел 2
Экспериментальные условия, сходные с условиями, описанными в экспериментальном разделе 1, использовали для группы, в которой вводили только анти-CAPRIN-1-антитело, для группы, в которой вводили циклофосфамид и анти-CAPRIN-1-антитело, для группы, в которой вводили паклитаксел и анти-CAPRIN-1-антитело, для группы, в которой вводили доцетаксел и анти-CAPRIN-1-антитело, и для группы, в которой вводили винорелбин и анти-CAPRIN-1-антитело, за исключением того, что в качестве анти-CAPRIN-1-антитела вводили моноклональное анти-CAPRIN-1-антитело №9.
Экспериментальные условия, сходные с условиями, описанными в экспериментальном разделе 1, использовали для группы, в которой вводили циклофосфамид, для группы, в которой вводили паклитаксел, для группы, в которой вводили доцетаксел, для группы, в которой вводили винорелбин, для группы, в которой вводили циклофосфамид и анти-Her2-антитело, для группы, в которой вводили паклитаксел и анти-Her2-антитело, для группы, в которой вводили доцетаксел и анти-Her2-антитело, и для группы, в которой вводили винорелбин и анти-Her2-антитело.
Размеры опухолей измеряли каждый день и наблюдали противоопухолевое действие для каждой группы введения, описанной в приведенных выше экспериментальных разделах. Группу из 5 несущих опухоли мышей, которым вводили PBS(-)вместо антитела, использовали в качестве контрольной группы. Кроме того, размер опухоли определяли посредством вычислением объема с использованием формулы основная ось×малая ось×малая ось×0,5.
В результате наблюдения противоопухолевого действия, как описано в экспериментальном разделе 1, обнаружено, что опухоли регрессировали примерно до 79% в группах, в которых было введено каждое из противоопухолевых средств, примерно до 56% в группе, в которой было введено только анти-CAPRIN-1-антитело, и примерно до 74% в группах, в которых было введено каждое из противоопухолевых средств и анти-Her2-антитело, при этом объем опухоли в контрольной группе, в которой был введен PBS(-), на 26 день после начала эксперимента принимали за 100%. С другой стороны, обнаружено, что в группах, в которых было введено каждое из противоопухолевых средств и анти-CAPRIN-1-антитело, опухоли регрессировали примерно до нескольких десятков % на 14 день, а также обнаружено, что они почти полностью регрессировали на 22 день и позже (см. фиг. 3-6).
Также согласно экспериментальному разделу 2 обнаружено, что опухоли регрессировали примерно до 68% в группах, в которых было введено каждое из противоопухолевых средств, примерно до 45% в группе, в которой было введено только анти-CAPRIN-1-антитело, и примерно до 55% в группах, в которых было введено каждое из противоопухолевых средств и анти-Her2-антитело, при этом объем опухоли в контрольной группе, в которой был введен PBS(-), на 26 день после начала эксперимента принимали за 100%. С другой стороны, обнаружено, что в группах, в которых было введено каждое из противоопухолевых средств и анти-CAPRIN-1-антитело, опухоли регрессировали до нескольких десятков % на 14 день, и также обнаружено, что они почти полностью регрессировали на 22 день и позже (см. фиг. 7-10).
Промышленная применимость
Антитела согласно настоящему изобретению применимы для лечения и/или профилактики рака.
Все публикации, патенты и заявки на выдачу патентов, цитированные в настоящем описании, включены в настоящую публикацию в виде ссылки в полном объеме.
Свободный текст списка последовательностей
SEQ ID NO: 31: праймер T3
SEQ ID NO: 32: праймер T7
SEQ ID NO: 33 и 34: праймер
SEQ ID NO: 35 и 36: праймер GAPDH
SEQ ID NO: 38 и 39: праймер
SEQ ID NO: 130-135: праймер.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ И/ИЛИ ПРОФИЛАКТИКИ РАКА | 2011 |
|
RU2603742C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ЗЛОКАЧЕСТВЕННОЙ ОПУХОЛИ | 2012 |
|
RU2641260C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ИЛИ ПРОФИЛАКТИКИ РАКА | 2013 |
|
RU2631804C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ И/ИЛИ ПРОФИЛАКТИКИ ЗЛОКАЧЕСТВЕННОЙ ОПУХОЛИ | 2012 |
|
RU2595400C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ И/ИЛИ ПРОФИЛАКТИКИ ЗЛОКАЧЕСТВЕННОЙ ОПУХОЛИ | 2012 |
|
RU2610428C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ И/ИЛИ ПРОФИЛАКТИКИ ЗЛОКАЧЕСТВЕННОЙ ОПУХОЛИ | 2012 |
|
RU2611197C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ | 2009 |
|
RU2498819C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ И/ИЛИ ПРОФИЛАКТИКИ РАКА | 2013 |
|
RU2633505C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ И/ИЛИ ПРОФИЛАКТИКИ РАКА | 2011 |
|
RU2607366C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ЗЛОКАЧЕСТВЕННОЙ ОПУХОЛИ | 2012 |
|
RU2624049C2 |

































































































































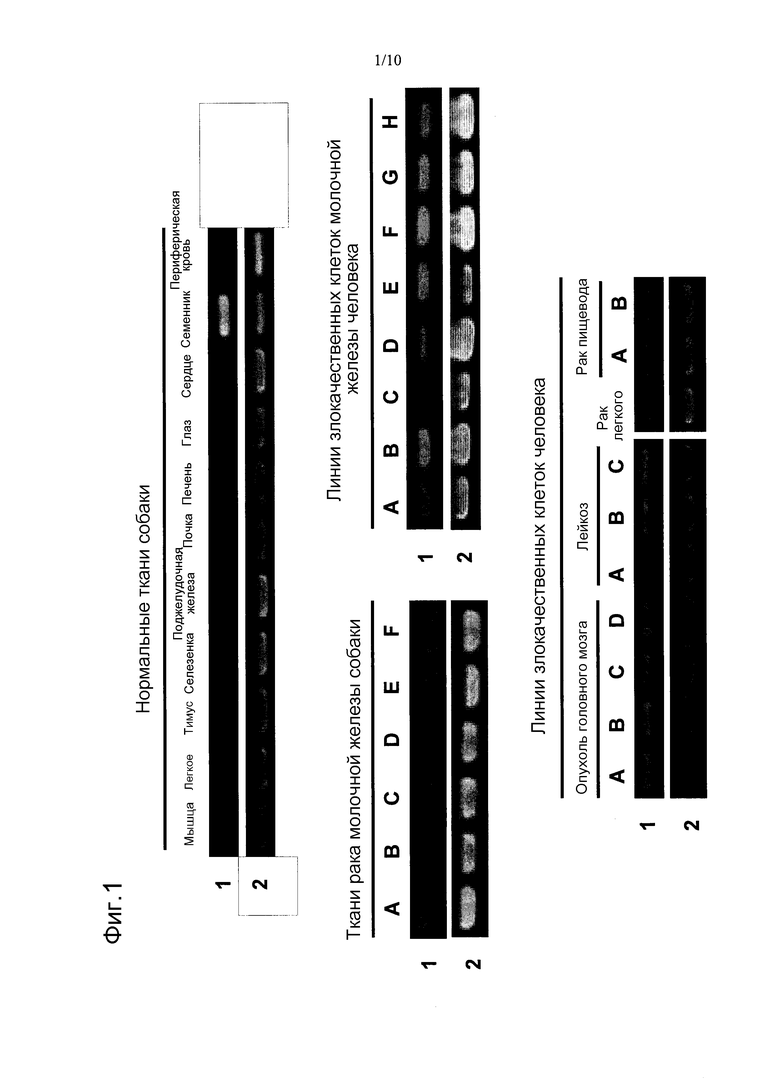
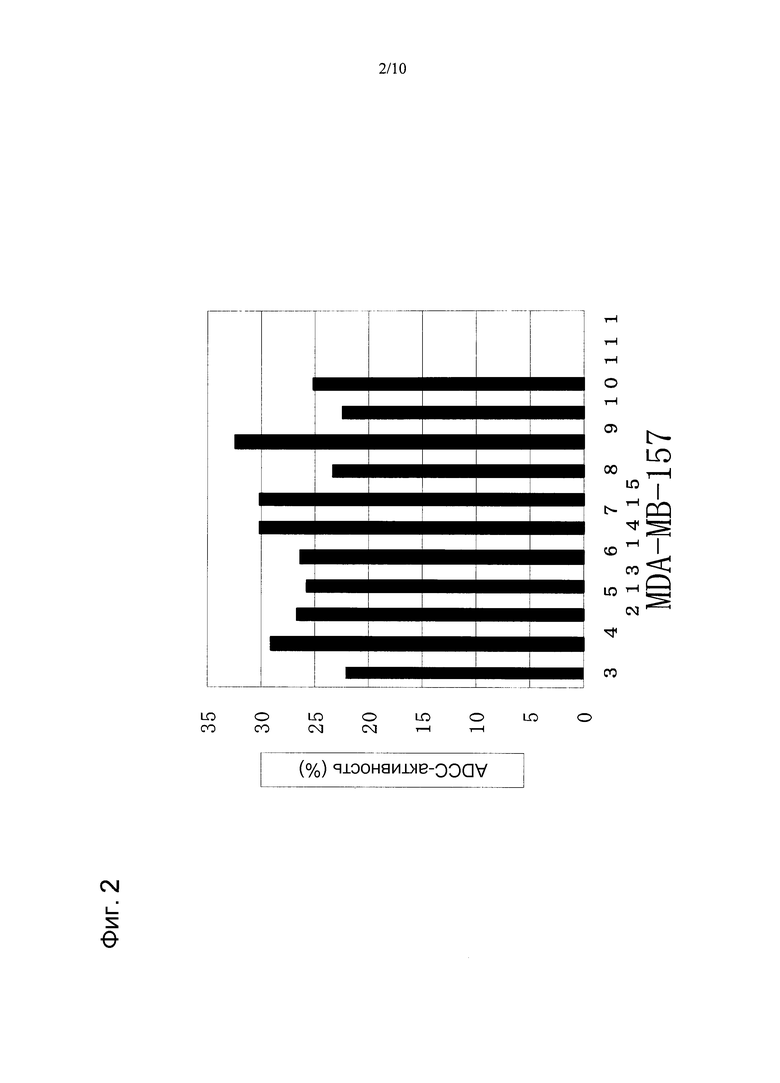
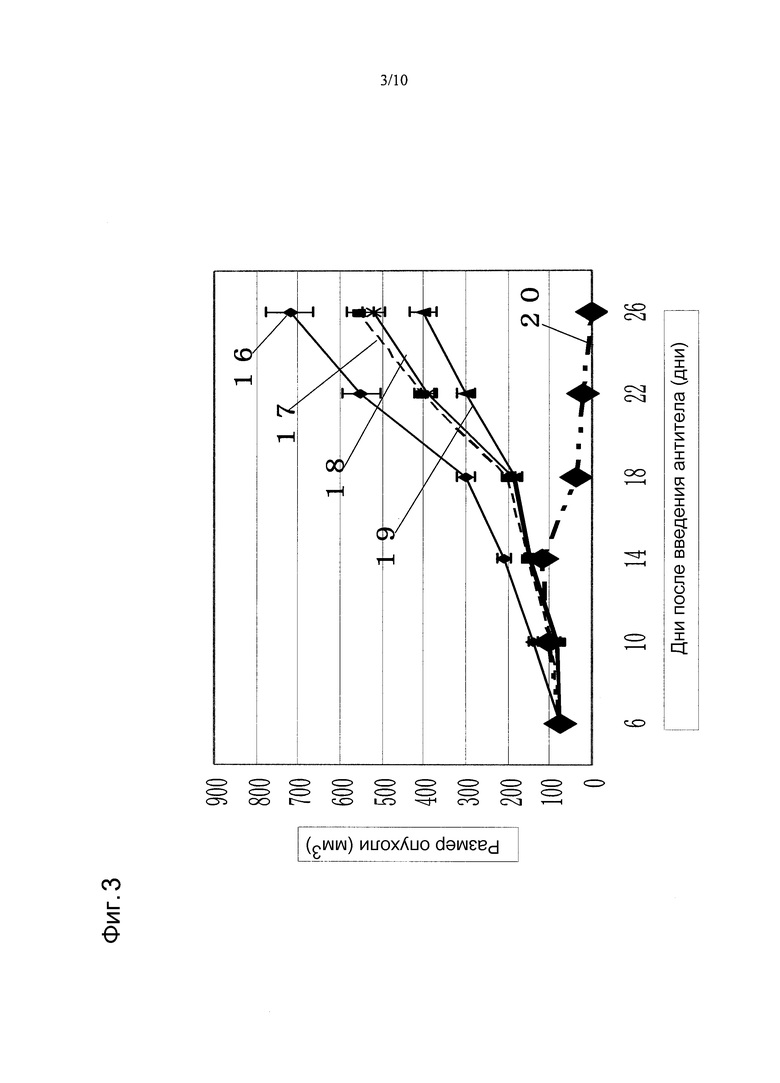
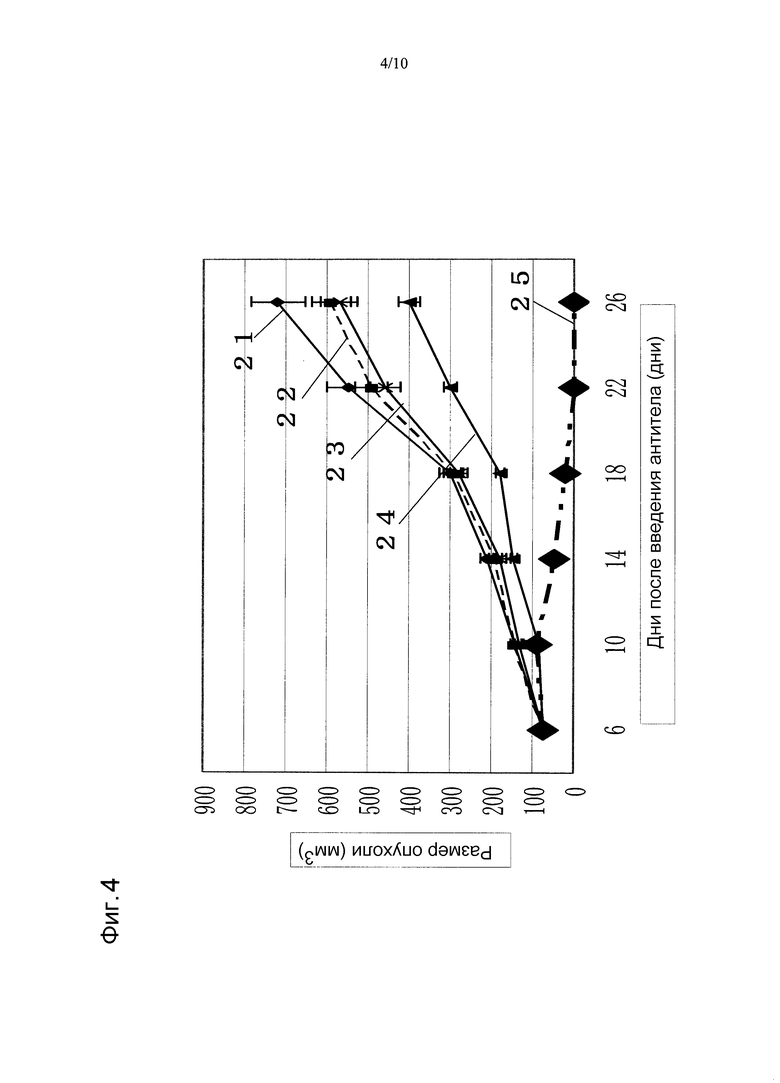
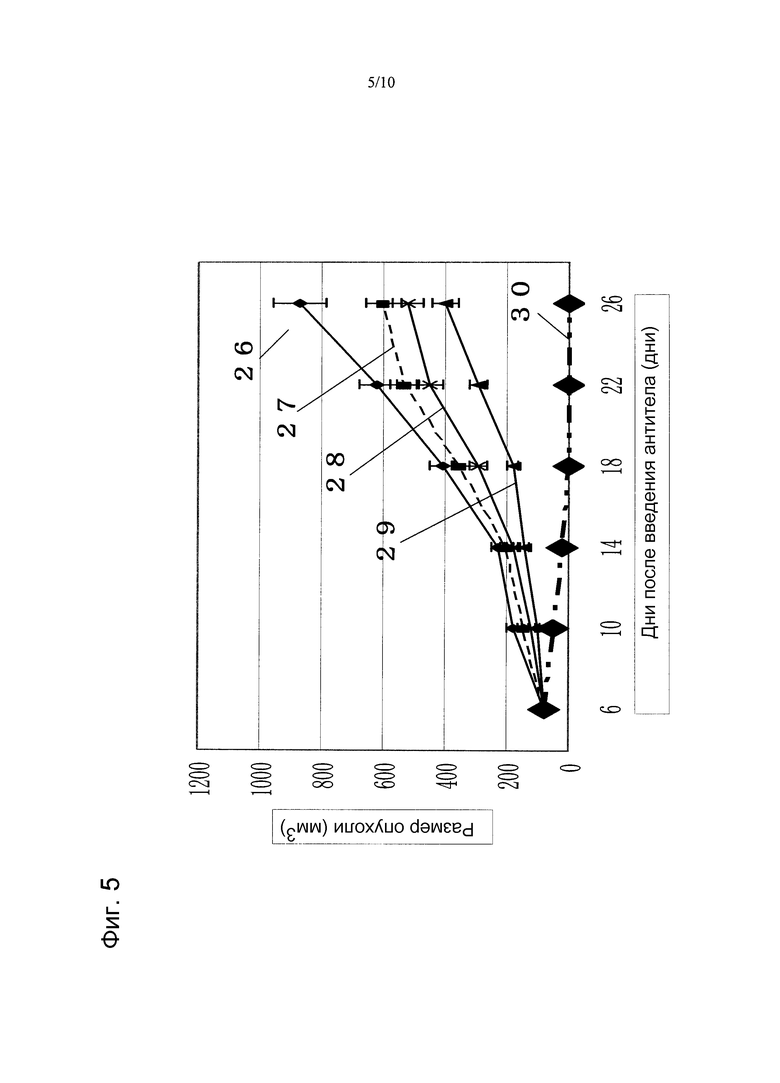
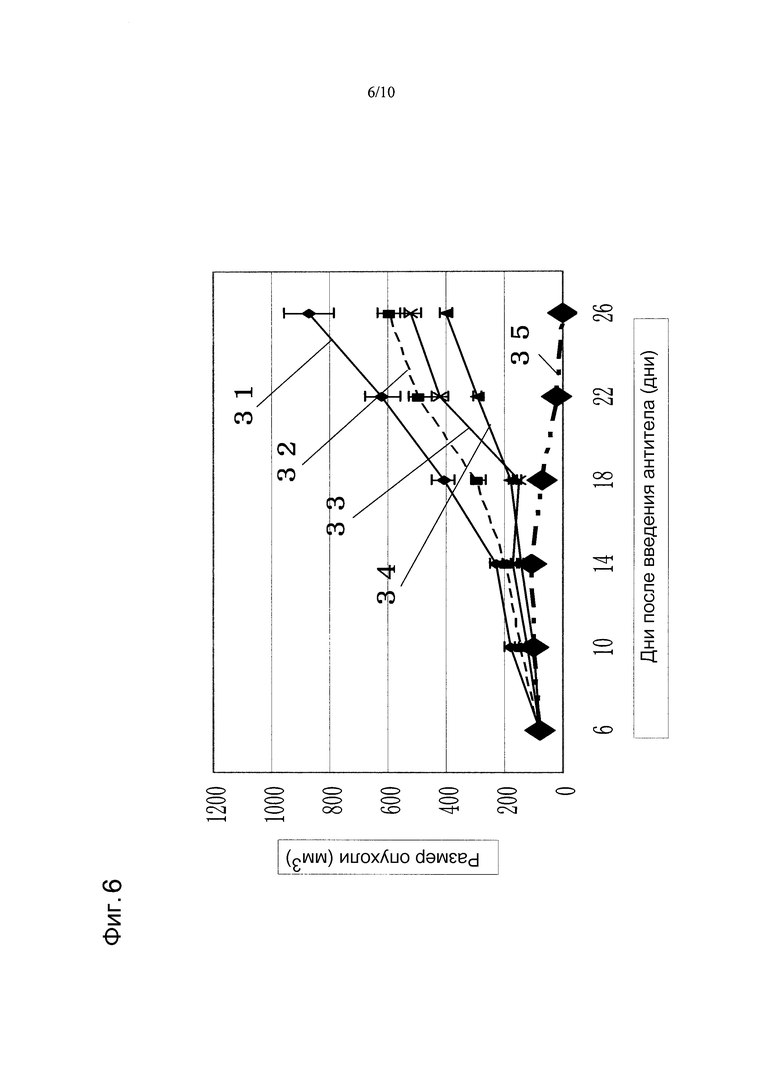
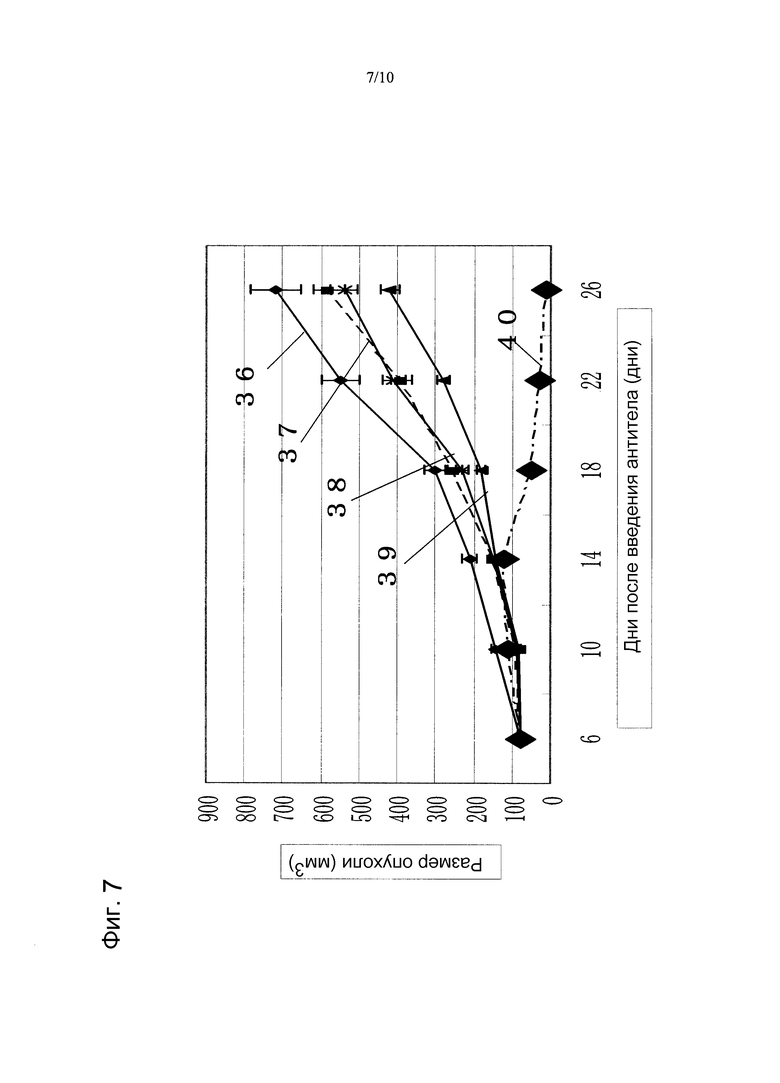
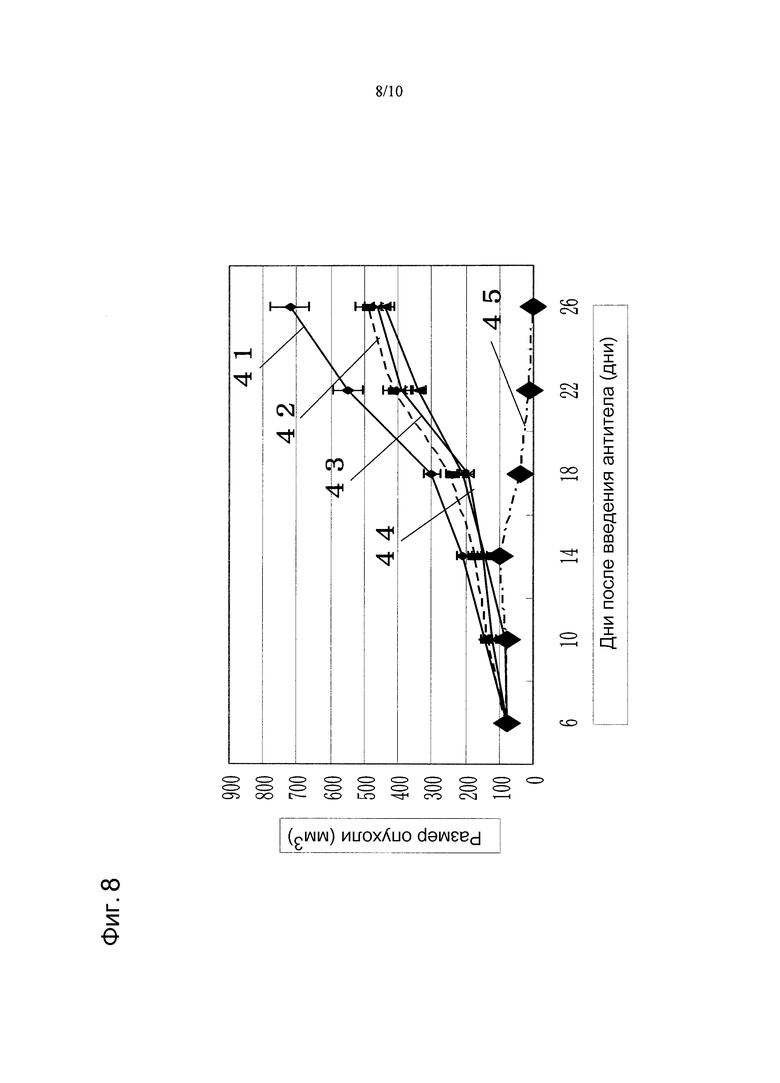
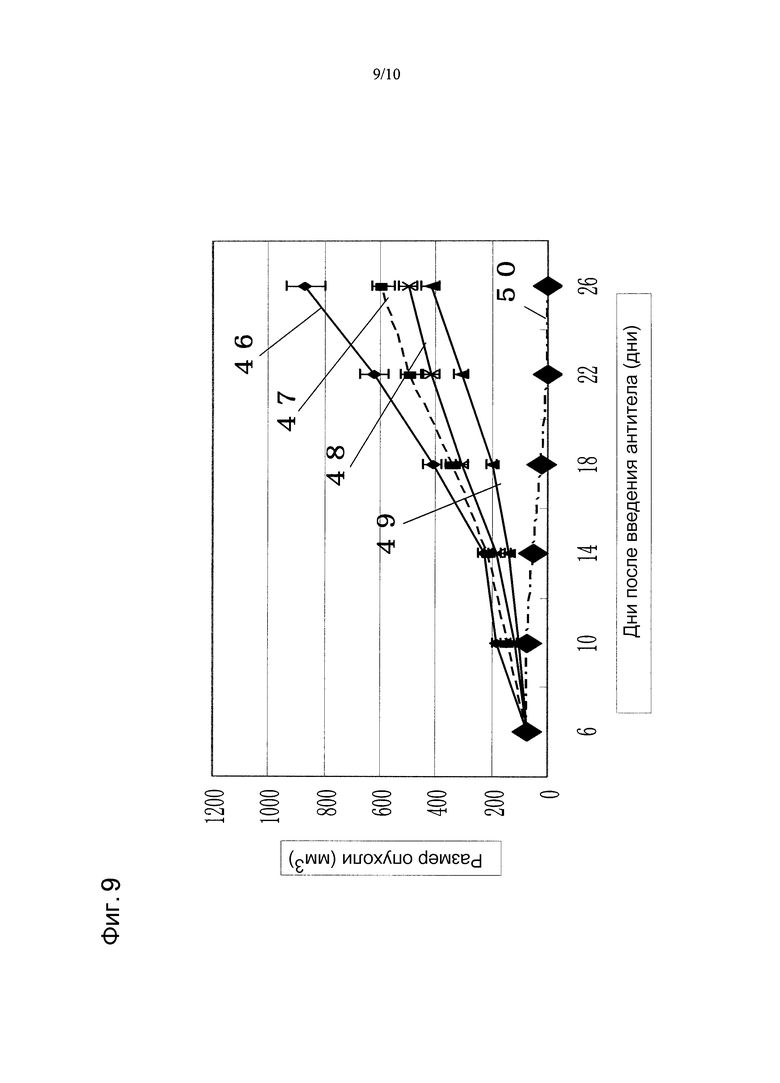
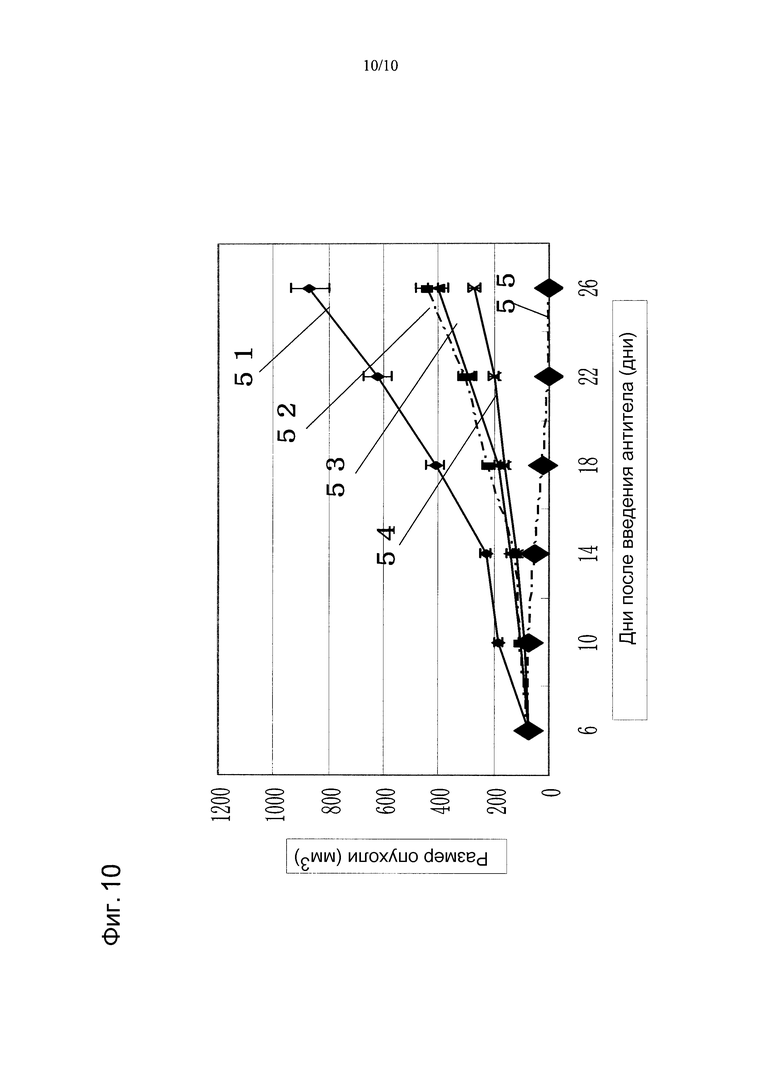
Изобретение относится к области биохимии, в частности к лекарственному препарату для лечения или профилактики рака, экспрессирующего белок CAPRIN-1. Также раскрыт способ лечения или профилактики рака, экспрессирующего белок CAPRIN-1. Изобретение позволяет эффективно лечить опосредуемый CAPRIN-1 рак. 2 н. и 8 з.п. ф-лы, 10 ил., 1 табл., 7 пр.
1. Лекарственный препарат для лечения или профилактики рака, экспрессирующего белок CAPRIN-1 на поверхности клеток рака, включающий в себя сочетание антитела, обладающего иммунологической реактивностью по отношению к белку CAPRIN-1, имеющему аминокислотную последовательность, пронумерованную четными числами среди последовательностей SEQ ID NO: 2-30, и одного или двух или больше типов противоопухолевых средств, при этом антитело и противоопухолевое средство или противоопухолевые средства объединяют вместе или используют последовательно, где рак экспрессирует белок CAPRIN-1 на поверхности клеток рака, и антитело специфически связывается с внеклеточной областью белка CAPRIN-1, существующей на поверхности клетки рака.
2. Лекарственный препарат по п. 1, в котором антитело, обладающее иммунологической реактивностью по отношению к белку CAPRIN-1, представляет собой антитело, которое специфично связывается с полипептидом, имеющим аминокислотную последовательность, представленную в виде SEQ ID NO: 37, во внеклеточной области белка CAPRIN-1, существующей на поверхности клеток рака.
3. Лекарственный препарат по п. 1, в котором белок CAPRIN-1 является белком человека.
4. Лекарственный препарат по п. 1, в котором противоопухолевое средство представляет собой одно или более, выбранное из группы, состоящей из паклитаксела, доксорубицина, даунорубицина, циклофосфамида, метотрексата, 5-фторурацила, тиотепа, бусульфана, импросульфана, пипосульфана, бензодопа, карбоквона, метуредопа, уредопа, алтретамина, триэтиленмеламина, триэтиленфосфорамида, триэтилентиофосфорамида, триметилоломеламина, буллатацина, буллатацинона, камптотецина, бриостатина, каллистатина, криптофицина1, криптофицина8, доластатина, дуокармицина, элеутеробина, панкратистатина, саркодиктиина, спонгистатина, хлорамбуцила, хлорнафазина, хлорфосфамида, эстрамустина, ифосфамида, мехлорэтамина, гидрохлорида оксида мехлорэтамина, мелфалана, новембихина, фенестерина, преднимустина, трофосфамида, урамустина, кармустина, хлорозотоцина, фотемустина, ломустина, нимустина, ранимустина, калихеамицина, динемицина, клодроната, эсперамицина, аклациномицина, актиномицина, аутрамицина, азасерина, блеомицина, кактиномицина, карабицина, карминомицина, карцинофилина, хромомицина, дактиномицина, деторбицина, 6-диазо-5-оксо-L-норлейцина, адриамицина, эпирубицина, эзорубицина, идарубицина, марцелломицина, митомицина С, микофеноловой кислоты, ногаламицина, оливомицинов, пепломицина, потфиромицина, пуромицина, квеламицина, родорубицина, стрептонигрина, стрептозоцина, туберцидина, убенимекса, зиностатина, зорубицина, деноптреина, птероптерина, триметрексата, флударабина, 6-меркаптопурина, тиамиприна, тиогуанина, анцитабина, азацитидина, 6-азауридина(азауридина), кармофура, цитарабина, дидезоксиуридина, доксифлуридина, эноцитабина, флоксуридина, андрогенов (например, калустерона, пропионата дромостанолона, эпитиостанола, мепитиостана и тестолактона), аминоглютетимида, митотана, трилостана, фолиновой кислоты, ацеглатона, гликозида альдофосфамида, аминолевулиновой кислоты, энилурацила, амсакрина, бестрабуцила, бисантрена, эдатраксата, дефофамина, демеколцина, диазихона, элфорнитина, ацетата эллиптиния(эллиптиния), эпотилона, этоглуцида, лентинана, лонидамина, мейтанзина, ансамитоцина, митогуазона, митоксантрона, мопиданмола, нитраэрина, пентостатина, фенамета, пирарубицина, лозоксантрона, подофиллиновой кислоты, 2-этилгидразида, прокарбазина, разоксана, ризоксина, шизофиллана, спирогермания, тенуазоновой кислоты, триазиквона, роридина А, ангуидина, уретана, виндезина, дакарбазина, манномустина, митобронитола, митолактола, пипобромана, гацитозина, доцетаксела, хлорамбуцила, гемцитабина, 6-тиогуанина, меркаптопурина, цисплатина, оксалиплатина, карбоплатина, винбластина, этопозида, ифосфамида, митоксантрона, винкристина, винорелбина, новантрона, тенипозида, эдатрексата, дауномицина, аминоптерина, кселода, ибандроната, иринотекана, ингибитора топоизомеразы, дифторметилорнитина (DMFO), ретиноевой кислоты, капецитабина и их фармацевтически приемлемых солей или производных.
5. Лекарственный препарат по п. 4, в котором противоопухолевое средство выбрано из группы, состоящей из циклофосфамида, паклитаксела, доцетаксела, винорелбина и их фармацевтически приемлемых солей и производных.
6. Лекарственный препарат по п. 1, в котором раком является рак молочной железы, опухоль головного мозга, лейкоз, лимфома, рак легкого, мастоцитома, рак почек, рак шейки матки, рак мочевого пузыря, рак пищевода, рак желудка или рак прямой и ободочной кишки.
7. Лекарственный препарат по п. 1, в котором антитело является моноклональным антителом, поликлональным антителом или рекомбинантным антителом.
8. Лекарственный препарат по п. 1, в котором антитело является антителом человека, гуманизированным антителом, химерным антителом, одноцепочечным антителом.
9. Способ лечения или профилактики рака, экспрессирующего белок CAPRIN-1, включающий в себя введение лекарственного препарата по любому из пп. 1-8 субъекту, у которого предполагается наличие рака.
10. Способ по п. 9, включающий в себя введение субъекту антитела и противоопухолевого средства, которые находятся в указанном выше лекарственном препарате, одновременно или раздельно.
| US 2005129690 A1 от 16 | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| and et al., Distinct Structural Features of Caprin-1 Mediate Its Interaction with G3BP-1 and Its Induction of Phosphorylation of Eukaryotic Translation Initiation Factor 2a, Entry to Cytoplasmic Stress Granules, and Selective Interaction with a Subset of mRNAs v , Molecular and Cellular Biology, 2007, V | |||
| Прибор с двумя призмами | 1917 |
|
SU27A1 |
| and et al., Activation/Division of Lymphocytes Results in Increased Levels of Cytoplasmic Activation/Proliferation-Associated Protein-1: Prototype of a New Family of Proteins, The Journal of Immunology, 2004; V.172, pp.2389-2400;Kaddar T | |||
| and et al, Two new miR-16 targets: caprin-1 and HMGA1, proteins implicated in cell proliferation, Biology of the Cell, 2009, V.101, N.9, pp | |||
| СПОСОБ ПОЛУЧЕНИЯ ТВЕРДЫХ ПРОДУКТОВ УПЛОТНЕНИЯ ФОРМАЛЬДЕГИДА С ФЕНОЛАМИ И ДРУГИМИ ВЕЩЕСТВАМИ | 1925 |
|
SU511A1 |
Авторы
Даты
2017-06-30—Публикация
2011-02-04—Подача