Уровень техники, предшествующий изобретению
[0001] Люди выращивают кукурузу для продуктов питания и энергетических применений. Люди также выращивают многие другие культуры, включая соевые бобы и хлопок. Насекомые поедают и повреждают растения, и таким образом наносят вред этим видам деятельности человека. Ежегодно тратят миллиарды долларов на борьбу с насекомыми-вредителями и дополнительные миллиарды тратят на наносимый ими ущерб. Синтетические органические химические инсектициды являлись первичными средствами, используемыми для борьбы с насекомыми-вредителями, но биологические инсектициды, такие как инсектицидные белки, получаемые из Bacillus thuringiensis (Bt), играли важную роль на некоторых площадях. Возможность получать устойчивые к насекомым-вредителям растения посредством трансформации генами инсектицидного белка Bt полностью изменило современное сельское хозяйство и увеличило важность и ценность инсектицидных белков и их генов.
[0002] К настоящему времени использовали несколько белков Bt для создания устойчивых к насекомым-вредителям трансгенных растений, которые успешно регистрировали и вводили в коммерческое обращение. Такие белки включают Cry1Ab, Cry1Ac, Cry1F и Cry3Bb в кукурузе, Cry1Ac и Cry2Ab в хлопке и Cry3A в картофеле.
[0003] Коммерческие продукты, экспрессирующие эти белки, экспрессируют один белок за исключением случаев, когда желательным является комбинированный инсектицидный спектр 2 белков (например, Cry1Ab и Cry3Bb в кукурузе, комбинированные для обеспечения устойчивости к чешуекрылым вредителям и повреждающим корни личинкам соответственно), или когда независимое действие белков делает их пригодными в качестве средства для замедления развития устойчивости в популяциях чувствительных насекомых (например, Cry1Ac и Cry2Ab в хлопке, комбинированные для обеспечения возможности управления устойчивостью табачной листовертки-почкоеда). SMART STAX представляет собой коммерческий продукт, который включает несколько белков Cry. См. также публикацию патентной заявки США № 2008/0311096, которая частично относится к Cry1Ab для борьбы с устойчивым к Cry1F кукурузным мотыльком (ECB, Ostrinia nubilalis (Hubner)). Публикация патентной заявки США № 2010/0269223 относится к DIG-3.
[0004] Быстрое и широко распространенное введение устойчивых к насекомым-вредителям трансгенных растений вызывало обеспокоенность, что популяции вредителей выработают устойчивость к инсектицидным белкам, продуцируемым растениями. Несколько стратегий были предложены для сохранения полезности признаков устойчивости к насекомым-вредителям на основе Bt, которые включаю применение белков в высокой дозе в комбинации с убежищем, и изменение или совместное использование с различными токсинами (McGaughey et al., (1998), "B.t. Resistance Management", Nature Biolechnol., 16:144-146).
[0005] Выбранные белки для применения в стэке для управления устойчивостью насекомых-вредителей (IRM) должны проявлять свой инсектицидный эффект независимо, таким образом, что устойчивость, развивающаяся к одному белку, не придает устойчивости ко второму белку (т.е. не существует перекрестной устойчивости к белкам). Например, если популяция вредителей, выбранная по устойчивости к "белку A", является чувствительной к "белку B", то можно сделать вывод, что не существует перекрестной устойчивости, и что комбинация белка A и белка B будет эффективной для замедления развития устойчивости к одному белку A.
[0006] При отсутствии устойчивых популяций насекомых можно проводить оценки на основании других характеристик, для которых предполагают, что ни связаны с механизмом действия и потенциалом перекрестной устойчивости. Была предложена пригодность опосредованного рецептором связывания для идентификации инсектицидных белков, которые, вероятно, не обладают перекрестной устойчивостью, (van Mellaert et al., 1999). Ключевой прогнозирующий параметр отсутствия перекрестной устойчивости, характерный для этого подхода, заключается в том, что инсектицидные белки не конкурируют за связывание с рецепторами у чувствительных видов насекомых.
[0007] В случае, когда два Bt-токсина конкурируют за один и тот же рецептор у насекомого, и в дальнейшем у такого насекомого рецептор мутирует таким образом, что один из токсинов больше не связывается с этим рецептором и, таким образом, больше не является инсектицидным для насекомого, это может быть в случае, когда насекомое также является устойчивым ко второму токсину (который конкурентно связывается с тем же рецептором). Таким образом, насекомое является перекрестно устойчивым к обоим Bt-токсинам. Однако если два токсина связываются с двумя различными рецепторами, это может являться показателем, что насекомое не будет являться одновременно устойчивым к этим двум токсинам.
[0008] Дополнительные токсины Cry перечислены на веб-сайте комитета по официальной номенклатуре B.t. (Crickmore et al., lifesci.sussex.ac.uk/home/Neil_Crickmore/Bt/). В настоящее время существует приблизительно 60 основных групп токсинов "Cry" (Cry1-Cry59) с дополнительными токсинами Cyt и токсинами VIP и т.п. Многие из каждой числовой группы содержат подгруппы с заглавными буквами, и подгруппы с заглавными буквами сдержат подподгруппы со сточными буквами. (например, Cry1 содержит A-L, и Cry1A содержит a-i).
КРАТКОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
[0009] Настоящее изобретение частично относится к неожиданному открытию, что DIG-3 и Cry1Ab не конкурируют за связывание с участками в препаратах клеточных мембран кишечника кукурузного мотылька (ECB, Ostrinia nubilalis (Hubner)). Как специалисту в данной области будет понятно в соответствии с настоящим описанием, растения, которые продуцируют оба этих белка (включая инсектицидные части полноразмерных белков), можно использовать для замедления или предотвращения развития устойчивости к любому из этих отдельных инсектицидных белков. Кукуруза является предпочтительным растением для использования по настоящему изобретению. ECB представляет собой предпочтительное насекомое-мишень для рассматриваемой пары токсинов.
[0010] Таким образом, настоящее изобретение частично относится к использованию белка Cry1Ab в комбинации с белком DIG-3. Растения (и площади, засеянные такими растениями), которые продуцируют оба таких белка, входят в объем настоящего изобретения.
[0011] Настоящее изобретение также частично относится к тройным стэкам или "пирамидам" трех (или более) токсинов, где Cry1Ab и DIG-3 являются основной парой. В некоторых предпочтительных вариантах осуществления пирамид комбинация выбранных токсинов обеспечивает три места приложения действия против ECB. Некоторые предпочтительные комбинации пирамид "трех мест приложения действия" включают рассматриваемую основную пару белков плюс Cry1F в качестве третьего белка для направленного воздействия на ECB. (Из US 2008 0311096 известно, что Cry1Ab является эффективным против устойчивой к Cry1Fa ECB). Этот конкретные тройной стэк, например, согласно настоящему изобретению, преимущественно и неожиданно обеспечивает три места приложения действия против ECB. Это может помочь снизить или устранить требования для площади-убежища.
[0012] Хотя настоящее изобретение описано в настоящем описании в виде основной пары токсинов Cry1Ab и DIG-3, которые совместно в качестве пары или в "пирамиде" трех или более токсинов обеспечивают устойчивость к насекомым-вредителям против ECB в кукурузе, следует понимать, что другие комбинации с Cry1Ab и DIG-3 также можно использовать по настоящему изобретению, предпочтительно в кукурузе.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
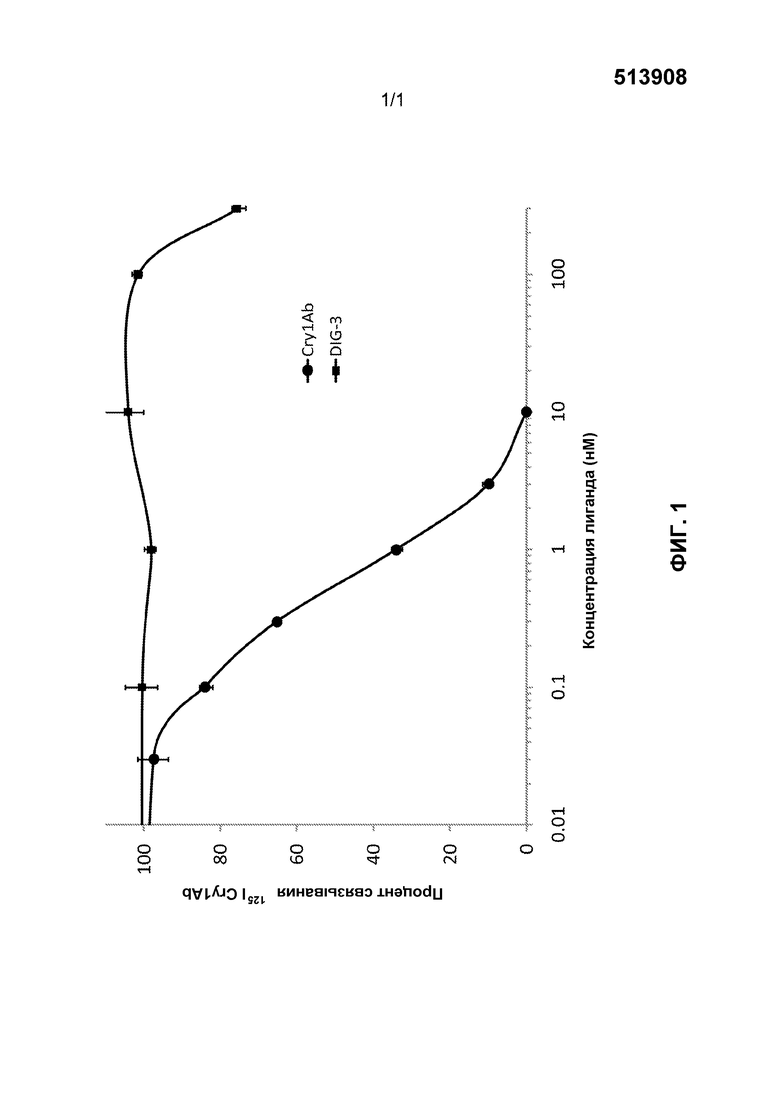
[0013] На фиг.1 представлен процент специфического связывания 125I Cry1Ab (0,5 нМ) в BBMV от Ostrinia nubilalis в сравнении с конкурентным связыванием немеченым гомологичным Cry1Ab (•) и гетерологичным DIG-3 (■). Кривая замещения для гомологичного связывания Cry1Ab приводит к кривой сигмоидальной формы, демонстрирующей 50% замещение радиоактивного лиганда приблизительно при 0,5 нМ Cry1Ab. DIG-3 не замещает любого из связывания 125I Cry1Ab на своем участке связывания при концентрациях 100 нМ или ниже (в 200 раз выше чем концентрация 125I Cry1Ab в анализе). Только при 300 нМ авторы наблюдают приблизительно 25% замещение связывания 125I Cry1Ab на DIG-3. Эти результаты демонстрируют, что DIG-3 не конкурирует эффективно за связывание Cry1Ab с участками рецептора, локализованными в BBMV от Ostrinia nubilalis.
КРАТКОЕ ОПИСАНИЕ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
SEQ ID NO:1 представляет собой полноразмерный иллюстративный белок Cry1Ab. (MR818)
SEQ ID NO:2 представляет собой полноразмерный иллюстративный белок DIG-3.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0014] Настоящее изобретение частично относится к неожиданному открытию, что Cry1Ab и DIG-3 не конкурируют друг с другом за участки связывания в кишечнике кукурузного мотылька (ECB, Ostrinia nubilalis (Hubner)) или травяной совки (FAW, Spodoptera frugiperda). Таким образом, белок Cry1Ab можно использовать в комбинации с белком DIG-3 предпочтительно в трансгенной кукурузе для замедления или предотвращения развития устойчивости у ECB к любому из этих отдельных белков. Рассматриваемая пара белков может являться эффективной для защиты растений (таких как растения кукурузы) от повреждений устойчивой к Cry ECB. Таким образом, одно из применений настоящего изобретения заключается в защите кукурузы и других экономически важных видов растений от повреждений и потерь урожая, вызываемых популяциями ECB, которые могут развивать устойчивость к Cry1Ab или DIG-3.
[0015] Таким образом, настоящее изобретение относится к стэку для управления устойчивостью насекомых-вредителей (IRM), содержащему Cry1Ab и DIG-3, для предотвращения или снижения развития устойчивости ECB к любому или обоим этим белкам.
[0016] Кроме того, хотя настоящее изобретение, описываемое в настоящем описании, относится к стэку IRM, содержащему Cry1Ab и DIG-3 для предотвращения устойчивости ECB к любому одному или обоим этим белкам, в объем изобретения, описываемого в настоящем описании, входит то, что один или оба Cry1Ab и DIG-3 можно адаптировать отдельно или в комбинации для предотвращения устойчивости FAW к любому одному или обоим этим белкам.
[0017] Настоящее изобретение относится к композициям для борьбы с чешуекрылыми вредителями, содержащим клетки, которые продуцируют содержащий коровый токсин Cry1Ab белок и содержащий коровый токсин DIG-3 белок.
[0018] Изобретение дополнительно содержит организм, трансформированный для продуцирования инсектицидного белка Cry1Ab и инсектицидного белка DIG-3, где указанный хозяин представляет собой микроорганизм или растительную клетку. Рассматриваемый полинуклеотид(ы) предпочтительно находится в генетической конструкции под контролем промотора(ов), не относящихся к Bacillus-thuringiensis. Рассматриваемые полинуклеотиды могут содержать частоту использования кодона для усиления экспрессии у растения.
[0019] Дополнительно предполагают, что изобретение относится к способу борьбы с чешуекрылыми вредителями, включающему контактирование указанных вредителей или окружающей среды указанных вредителей с эффективным количеством композиции, которая содержит инсектицидный белок Cry1Ab и дополнительно содержит инсектицидный белок DIG-3.
[0020] Один из вариантов осуществления изобретения содержит растение кукурузу, содержащее экспрессируемый в растениях ген, кодирующий содержащий коровой токсин белок DIG-3 и экспрессируемый в растениях ген, кодирующий содержащий коровой токсин белок Cry1Ab, и семена такого растения.
[0021] Дополнительный вариант осуществления изобретения содержит растение кукурузы, где экспрессируемый в растениях ген, кодирующий инсектицидный белок DIG-3 и экспрессируемый в растениях ген, кодирующий инсектицидный белок Cry1Ab, подвергали интрогрессии в указанное растение кукурузу, и семена такого растения.
[0022] Как описано в примерах, исследования конкурентного связывания с рецептором с использованием белков DIG-3 и радиоактивно меченых белков Cry1Ab демонстрируют, что белок DIG-3 не конкурирует за связывание в тканях ECB, с которыми связывается Cry1Ab. Эти результаты также свидетельствуют о том, что комбинация белков Cry1Ab и DIG-3 может представлять собой эффективное средство для снижения развития устойчивости в популяциях ECB к любому из этих белков. Таким образом, частично на основании данных, описываемых в настоящем описании, для высокой дозы можно использовать совместную продукцию (стэкинг) DIG-3 и Cry1Ab в стэках IRM для борьбы с ECB.
[0023] К этой паре можно добавлять другие белки. Например, настоящее изобретение также частично относится к тройным стэкам или "пирамидам" из трех (или более) токсинов, где Cry1Ab и DIG-3 являются основной парой. В некоторых предпочтительных варианты осуществления пирамиды выбранные токсины содержат три отдельных места приложения действия против ECB. Некоторые предпочтительные комбинации пирамид из "трех мест приложения действия" включают рассматриваемые основные пары белков плюс Cry1Fa в качестве третьего белка для направленного воздействия на ECB. Эти конкретные тройные стэки по настоящему изобретению преимущественно и неожиданно обеспечивают три места приложения действия против ECB. Это может помогать сокращать или устранять необходимость площадей-убежищ. Под "отдельными местами приложения действия" подразумевают, что любой из данных белков не вызывает перекрестную устойчивость друг с другом.
[0024] Таким образом, один из вариантов применения представляет собой использование рассматриваемых основных белков в комбинации с третьим токсином/геном и использование такого тройного стэка для снижения развития устойчивости у ECB к любому из этих токсинов. Таким образом, настоящее изобретение также частично относится к тройным стэкам или "пирамидам" из трех (или более) токсинов. В некоторых предпочтительных вариантах осуществления пирамид выбранные токсины содержат три отдельных места приложения действия против ECB.
[0025] В число вариантов применения настоящего изобретения входит использование двух, трех или более белков из рассматриваемых белков в областях возделывания сельскохозяйственных культур, где ECB может (или уже известно, что) развивать устойчивые популяции.
[0026] Cry1Fa применяют, например, в продуктах Herculex® и SmartStax™. Рассматриваемую пару генов (Cry1Ab и DIG-3) можно объединять, например, в продукте Cry1Fa, таком как Herculex® и/или SmartStax™. Таким образом, рассматриваемая пара белков может являться существенной для снижения давления отбора в отношении этих и других белков. Таким образом, рассматриваемую пару белков можно использовать в трех комбинациях генов кукурузы.
[0027] Как указано выше, также можно добавлять дополнительные токсины/гены по настоящему изобретению. Например, для использования Cry1Ab совместно с Cry1Be для направленного воздействия на ECB см. WO 2011/084631. Для использования Cry1Ab совместно с Cry2Aa для направленного воздействия ECB см. WO 2011/075590. Таким образом, Cry1Be и/или Cry2Aa можно использовать (необязательно совместно с Cry1Fa) во многочисленных стэках белков с рассматриваемой парой белков.
[0028] Растения (и площади, засеянные такими растениями), которые продуцируют любую из рассматриваемых комбинаций белков входят в объем настоящего изобретения. Также можно добавлять дополнительные токсины/гены, но конкретные описанные выше стэки преимущественно и неожиданно обеспечивают многие места приложения действия против ECB. Это может способствовать снижению или устранению необходимости площадей-убежищ. Таким образом, поля, засеянные более десяти акров, таким образом, входят в настоящее изобретение.
[0029] Также можно использовать GENBANK для получения последовательностей для любого из генов и белков, описываемых в настоящем описании. Также можно использовать патенты. Например, в патенте США № 5188960 и патенте США № 5827514 описаны содержащие коровой токсин Cry1Fa белки, пригодные для использования для практического осуществления настоящего изобретения. В патенте США № 6218188 описаны оптимизированные для растений последовательности ДНК, кодирующие содержащие коровый токсин Cry1Fa белки, которые являются пригодными для использования в настоящем изобретении.
[0030] Насекомые, родственные ECB, также могут являться мишенью. Они могут включать стеблевых точильщиков и/или точащих стебель насекомых. Юго-западная кукурузная огневка (Diatraea grandiosella - подпорядок Heterocera) представляет собой один из примеров. Точильщик стеблей сахарного тростника также представляет собой вид Diatraea (Diatraea saccharalis). Комбинации белков, описываемых в настоящем описании, можно использовать для направленного воздействия на личиночных стадиях насекомого-мишени. Взрослые чешуекрылые, например, бабочки и мотыльки, преимущественно питаются цветочным нектаром и представляют собой существенный действующий элемент опыления. Практически все личинки чешуекрылых, т.е. гусеницы, питаются растениями, и многие представляют собой опасных вредителей. Гусеницы питаются наружной или внутренней частью листвы или корнями или стеблями растения, лишая растение питательных веществ и часто разрушая физическую опорную структуру растения. Кроме того, гусеницы питаются фруктами, волокнами и хранящимся зерном и мукой, делая непригодными эти продукты для продажи или значительно снижая их стоимость.
[0031] Некоторые химерные токсины по настоящему изобретению содержат полный N-концевой участок корового токсина Bt-токсина и в некоторой точке после конца участка корового токсина, белок содержит переход к гетерологичной последовательности протоксина. N-концевой, инсектицидно активный участок токсина Bt-токсина обозначают как "коровый" токсин. Переход от сегмента корового токсина к гетерологичному сегменту протоксина может находиться приблизительно в области соединения токсина/протоксина или, альтернативно, участок нативного протоксина (удлиняя область после участка корового токсина) может сохраняться, где переходом к гетерологичному участку протоксина располагается ниже.
[0032] Характерные полноразмерные трехдоменные белки Cry B.t. составляют приблизительно от 130 кДа до 150 кДа. Cry1Ab представляет собой один из примеров. DIG-3 также представляет собой трехдоменный токсин размером приблизительно 142 кДа.
[0033] Например, один из химерных токсинов по настоящему изобретению представляет собой целый участок корового токсина Cry1Ab (приблизительно аминокислоты от 1 до 601) и/или гетерологичный протоксин (приблизительно аминокислоты от 602 до C-конца). В одном из предпочтительных вариантов осуществления участок химерного токсина, содержащего протоксин, получают из белкового токсина Cry1Ab. В предпочтительном варианте осуществления участок химерного токсина содержит протоксин, получаемый из белкового токсина Cry1Ab.
[0034] Специалисту в данной области понятно, что Bt-токсины (даже в определенных классах, таких как Cry1B) могут изменяться до некоторой степени по длине и точной локализации перехода от участка корового токсина к участку протоксина. Длина характерных полноразмерных токсинов Cry составляет приблизительно от 1150 приблизительно до 1200 аминокислот. Переход от участка корового токсина к участку протоксина, как правило, составляет приблизительно от 50% приблизительно до 60% полноразмерного токсина. Химерный токсин по настоящему изобретению содержит полную протяженность этого N-концевого участка корового токсина. Таким образом, химерный токсин содержит по меньшей мере приблизительно 50% полноразмерного белка Cry1. Как правило, он составляет по меньшей мере приблизительно 590 аминокислот (и может содержать 600-650 или таких остатков). Касательно участка протоксина полная протяженность участка протоксина Cry1Ab составляет от конца участка корового токсина до C-конца молекулы.
[0035] Гены и токсины. Гены и токсины, пригодные по настоящему изобретению, включают не только описываемые полноразмерные последовательности, а также фрагменты этих последовательностей, варианты, мутанты и слитые белки, которые сохраняют характерную пестицидную активность токсинов, конкретно иллюстрируемых в настоящем описании. Как используют в настоящем описании, термины "варианты" или "вариации" генов относятся к нуклеотидным последовательностям, которые кодируют аналогичные токсины или которые кодируют эквивалентные токсины, обладающие пестицидной активностью. Как используют в настоящем описании, термин "эквивалентные токсины" относится к токсинам, обладающим аналогичной или по существу аналогичной биологической активностью против вредителей-мишеней как заявленные токсины.
[0036] Как используют в настоящем описании, границы составляют приблизительно 95% (например, Cry1Ab), 78% (Cry1A и Cry1B) и 45% (Cry1) идентичности последовательности согласно "Revision of the Nomenclature for the Bacillus thuringiensis Pesticidal Crystal Proteins", N. Crickmore, D.R. Zeigler, J. Feitelson, E. Schnepf, J. Van Rie, D. Lereclus, J. Baum and D.H. Dean. Microbiology and Molecular Biology Reviews (1998), Vol 62: 807-813. Эти пороги также можно применять только к коровым токсинам.
[0037] Специалисту в данной области должно быть очевидно, что гены, кодирующие активные токсины можно идентифицировать и получать несколькими способами. Конкретные гены или участки генов, иллюстрируемых в настоящем описании, можно получать из изолятов, депонированных в хранилище культур. Эти гены или их участки или варианты также можно синтетически конструировать, например, с использованием синтезатора генов. Вариации гены можно легко конструировать стандартными способами получения точечных мутаций. Кроме того, можно получать фрагменты таких генов с использованием коммерчески доступных экзонуклеаз или эндонуклеаз стандартными способами. Например, ферменты, такие как Bal31, или сайт-специфический мутагенез можно использовать для систематического отсечения нуклеотидов от концов таких генов. Гены, которые кодируют активные фрагменты, можно также получать с использованием ряда ферментов рестрикции. Для непосредственного получения активных фрагментов таких белковых токсинов можно использовать протеазы.
[0038] Фрагменты и эквиваленты, которые сохранят пестицидную активность иллюстрируемых токсинов входят в объем настоящего изобретения. Кроме того, вследствие избыточности генетического кода ряд различных последовательностей ДНК, может кодировать аминокислотные последовательности, описываемые в настоящем описании. Специалист в данной области может получать такие альтернативные последовательности ДНК, кодирующие аналогичные или по существу аналогичные токсины. Такие варианты последовательностей ДНК входят в объем настоящего изобретения. Как используют в настоящем описании, ссылка на "по существу аналогичную" последовательность относится к последовательностям, которые содержат замены аминокислот, делеции, добавления или вставки, которые существенно не влияют на пестицидную активность. Фрагменты генов, кодирующих белки, которые сохраняют пестицидная активность, также включены в это определение.
[0039] Дополнительный способ идентификации генов, кодирующих токсины и участки генов, пригодные по настоящему изобретению, заключается в использовании олигонуклеотидных зондов. Такие зонды представляют собой детектируемые нуклеотидные последовательности. Такие последовательности можно детектировать посредством подходящей метки или их можно получать по совей природе флуоресцентными, как описано в международной заявке № WO93/16094. Как хорошо известно в данной области, если молекула зонда и образец нуклеиновой кислоты гибридизуются посредством образования сильной связи между двумя молекулами, на полном основании можно предполагать, что зонд и образец обладают существенной гомологией. Предпочтительно гибридизацию проводят в жестких условиях хорошо известными в данной области способами, как описано, например, у Keller G.H., M.M. Manak (1987) DNA Probes, Stockton Press, New York, N.Y., pp. 169-170. Некоторые примеры комбинаций концентраций солей и температур являются такими, как указано ниже (в порядке повышения жесткости): 2X SSPE или SSC при комнатной температуре; 1X SSPE или SSC при 42°C; 0,1X SSPE или SSC при 42°C; 0,1X SSPE или SSC при 65°C. Детекция зондов предоставляет средство определения известным способом, произошла ли гибридизация. Такой анализ с использованием зонда обеспечивает быстрый способ идентификации кодирующих токсин генов по настоящему изобретению. Сегменты нуклеотидов, которые используют в качестве зондов по изобретению, можно синтезировать с использованием синтезатора ДНК и стандартными способами. Такие нуклеотидные последовательности также можно использовать в качестве праймеров для ПЦР для амплификации генов по настоящему изобретению.
[0040] Варианты токсинов. Определенные токсины по настоящему изобретению конкретно проиллюстрированы в настоящем описании. Вследствие того, что эти токсины являются только иллюстративными для токсинов по настоящему изобретению, следует понимать, что настоящее изобретение содержит варианты токсинов или эквивалентные токсины (и нуклеотидные последовательности, кодирующие эквивалентные токсины), обладающие аналогичной или сходной пестицидной активностью иллюстрируемого токсина. Эквивалентные токсины обладают аминокислотной гомологией по отношению к иллюстрируемому токсину. Такая аминокислотная гомология, как правило, составляет более 75%, предпочтительно более 90% и наиболее предпочтительно более 95%. Аминокислотная гомология является наиболее высокой в критических областях токсина, которые отвечают за биологическую активность или участвуют в определении трехмерной конфигурации, которая в конечном итоге обуславливает биологическую активность. В отношении этого приемлемыми являются определенные замены аминокислот, и их можно ожидать в случае, если эти замены не находятся в областях критических по отношению к активности или представляют собой консервативные аминокислотные замены, которые не влияют на трехмерную конфигурацию молекулы. Например, аминокислоты можно относить к следующим классам: неполярные, незаряженные полярные, основные и кислые. Консервативные замены, где аминокислоту из одного класса заменяют другой аминокислотой того же типа, входят в объем настоящего изобретения при условии, что замена существенно не изменяет биологической активности соединения. Ниже приведен список примеров аминокислот, принадлежащих к каждому классу.
[0041] В некоторых случаях также можно проводить неконсервативные замены. Критический фактор заключается в том, что эти замены не должны существенно снижать биологическую активность токсина.
[0042] Рекомбинантные хозяева. Гены, кодирующие токсины по настоящему изобретению, можно вводить широкому спектру хозяев, являющихся микроорганизмами или растениями. Экспрессия гена токсина приводит к непосредственной или опосредованной внутриклеточной продукции и содержанию пестицида. Для получения штамма Bt, который экспрессирует оба токсина по настоящему изобретению, можно использовать конъюгационный перенос и рекомбинантный перенос. Другие организмы-хозяева также можно трансформировать одним или обоими генами токсинов, затем использовать для получения синергического действия. С использованием подходящих микробных хозяев, например, Pseudomonas, микроорганизмы можно вносить в местонахождение вредителя, где они будут размножаться, и их будут поглощать. Результатом является борьба с вредителем. Альтернативно, микроорганизм, содержащий ген токсина, можно обрабатывать в условиях, которые пролонгируют активность токсина и стабилизируют клетку. Обрабатываемую клетку, которая сохраняет токсическую активность, затем можно применять в среде вредителя-мишени.
[0043] В случае, когда ген Bt-токсина вводят посредством подходящего вектора в микроорганизм-хозяина, и указанного хозяина вносят в окружающую среду в живом состоянии, важно использовать определенные микроорганизмы-хозяева. Выбирают микроорганизмы-хозяева, для которых известно, что они заселяют "фитосферу" (филлоплану, филлосферу, ризосферу и/или ризоплану) одной или нескольких представляющих интерес культур. Такие микроорганизмы, выбирают таким образом, чтобы они являлись способными успешно конкурировать в конкретной окружающей среде (культуре и других естественных средах насекомых) с микроорганизмами дикого типа, предоставляемыми для стабильного поддержания и экспрессии гена, экспрессирующего полипептидный пестицид, и, желательно, обеспечивают улучшенную защиту пестицида от деградации и инактивации под действием окружающей среды.
[0044] Известно, что большое число микроорганизмов заселяет филлоплану (поверхность листьев растений) и/или ризосферу (почву, окружающую корни растения) широкого спектра важных культур. Такие микроорганизмы включают бактерии, водоросли и грибы. Особый интерес представляют микроорганизмы, такие как бактерии, например, рода Pseudomonas, Erwinia, Serratia, Klebsiella, Xanthomonas, Streptomyces, Rhizobium, Rhodopseudomonas, Methylophilius, Agrobactenum, Acetobacter, Lactobacillus, Arthrobacter, Azotobacter, Leuconostoc и Alcaligenes; грибы, в частности дрожжи, например, рода Saccharoimces, Cryptococcus, Kluyveromyces, Sporobolomyces, Rhodotorula и Aureobasidium. Особый интерес представляют такие виды бактерий фитосферы как Pseudomonas syringae, Pseudomonas fluorescens, Serratia marcescens, Acetobacter xylinum, Agrobactenium tumefaciens, Rhodopseudomonas spheroides, Xanthomonas campestris, Rhizobium melioti, Alcaligenes entrophus и Azotobacter vinlandii, и виды дрожжей фитосферы, такие как Rhodotorula rubra, R. glutinis, R. marina, R. aurantiaca, Cryptococcus albidus, C. diffluens, C. laurentii, Saccharomyces rosei, S. pretoriensis, S. cerevisiae, Sporobolomyces roseus, S. odorus, Kluyveromyces veronae и Aureobasidium pollulans. Особый интерес представляют пигментированные микроорганизмы.
[0045] Широкий спектр способов является доступным для введения кодирующего токсин гена Bt в микроорганизм-хозяина в условиях, которые обеспечивают стабильное поддержание и экспрессию гена. Эти способы хорошо известны специалистам в данной области и описаны, например, в патенте США № 5135867, включенном в настоящее описание посредством ссылки.
[0046] Обработка клеток. Bacillus thuringiensis или рекомбинантные клетки, экспрессирующие Bt-токсины, можно обрабатывать для пролонгирования активности токсина и стабилизации клетки. Пестицидная микрокапсула, которая образуется, содержит Bt-токсин или токсины в клеточной структуре, которую стабилизировали, и которая защищает токсин, когда микрокапсулу применяют в среде вредителя-мишени. Подходящие клетки-хозяева могут включать прокариотов или эукариотов, обычно ограниченные такими клетками, которые не продуцируют вещества, токсичные для высших организмов, таких как млекопитающие. Однако можно использовать организмы, которые продуцируют вещества токсичные для высших организмов, в случае, когда токсические вещества являются нестабильными или уровень применения является существенно низким, чтобы предотвращать любую возможную токсичность для млекопитающего-хозяина. В качестве хозяев особый интерес представляют прокариоты и низшие эукариоты, такие как грибы.
[0047] Как правило, при обработке клетка является интактной и по существу находится в пролиферативной форме, а не в форме споры, хотя в некоторых случаях модно применять споры.
[0048] Обработку микробной клетки, например, микроорганизма, содержащего ген или гены Bt-токсина, можно проводить химическими или физическими способами или комбинацией химических и/или физических способов при условии, что способ не оказывает вредного воздействия на свойства токсина, не снижает способность клетки защищать токсин. Примеры химических реагентов представляют собой галогенирующие средства, в частности галогены с атомным номером 17-80. Более конкретно, можно использовать иод при умеренных условиях и в течение достаточного периода времени для получения желаемых результатов. Другие подходящие способы включают обработку альдегидами, такими как глутаральдегид, противоинфекционными средствами, такими как зефиранхлорид и цетилпиридинийхлорид, спиртами, такими как изопропил и этанол, различными гистологическими фиксаторами, такими как Люголь-иод, фиксатор Бауэна, различные кислоты и фиксатор Хелли (см. Humason, Gretchen L., Animal Tissue Techniques, W.H. Freeman and Company, 1967), или комбинацией физических (тепло) и химических средств, которые сохраняют и пролонгируют активность токсина, продуцируемого в клетке, когда клетку вводят в окружающую среду хозяина. Примеры физических средств представляю собой коротковолновое излучение, такое как гамма-излучение и рентгеновское излучение, замораживание, УФ-излучение, лиофилизацию и т.п. Способы обработки микробных клеток описаны в патентах США №№ 4695455 и 4695462, которые включены в настоящее описание посредством ссылки.
[0049] Как правило, клетки обладают повышенной структурной стабильностью, которая повышает устойчивость к условиям окружающей среды. В случае если пестицид находится в проформе, необходимо выбирать способ обработки клеток таким образом, чтобы он не ингибировал процессинг проформы в зрелую форму пестицида патогеном вредителя-мишени. Например, формальдегид образует поперечные связи белков и может ингибировать процессинг проформы полипептидного пестицида. Способ обработки должен сохранять по меньшей мере существенную часть биодоступности или биологической активности токсина.
[0050] Характеристики, представляющие особый интерес при выборе клетки-хозяина для целей продуцирования, включают простоту введения гена или генов Bt в хозяина, доступность экспрессирующих систем, эффективность экспрессии, стабильность пестицида в хозяине и наличие вспомогательных генетических способностей. Представляющие интерес характеристики для применения в качестве пестицидной микрокапсулы включают защитные свойства для пестицида, такие как толщина клеточных стенок, пигментация и внутриклеточная упаковка или образование телец включения; выживание в водных средах; отсутствие токсичности для млекопитающих; привлекательность для проглатывания вредителями; простота лизиса и фиксации без повреждения токсина и т.п. Другие рассматриваемые факторы включают простоту получения и обращения, экономические аспекты, стабильность при хранении и т.п.
[0051] Выращивание клеток. Клетку-хозяина, содержащую инсектицидный ген или гены Bt, можно выращивать в любой подходящей питательной среде, где ДНК-конструкция обеспечивает селективное преимущество, обеспечивая селективную среду, так что по существу все или все клетки сохраняют ген Bt. Такие клетки можно затем собирать общепринятыми способами. Альтернативно, клетки можно обрабатывать перед сбором.
[0052] Клетки Bt, продуцирующие токсины по изобретению, можно культивировать с использованием стандартной в данной области среды и способов ферментации. После завершения ферментационного цикла можно собирать бактерии, сначала выделяя споры и кристаллы Bt из ферментационного бульона хорошо известными в данной области способами. Выделенные споры и кристаллы Bt можно формулировать в виде смачивающегося порошка, жидкого концентрата, гранул или других составов добавлением поверхностно-активных веществ, дисперсантов, инертных носителей и других компонентов для облегчения обращения и применения для конкретных вредителей-мишеней. Такие составы и способы применения являются хорошо известными в данной области.
[0053] Составы. Формулируемые гранулы-приманки, содержащие аттрактант и споры, кристаллы и токсины изолятов Bt, или рекомбинантные микроорганизмы, содержащие гены, получаемые из изолятов Bt, описываемых в настоящем описании, можно наносить на почву. Формулируемый продукт также можно наносить в виде дражирования семян или обработки корней или обработки всего растения на поздних стадиях цикла урожая. Обработки растений и почвы клетками Bt можно проводить в виде смачивающихся порошков, гранул или порошков путем смешивания с различными инертными веществами, такими как неорганические минералы (филлосиликаты, карбонаты, сульфаты, фосфаты и т.п.) или растительными веществами (порошкообразные стержни кукурузных початков, шелуха риса, скорлупа грецкого ореха и т.п.). Составы могут содержать поверхностно-активные адъюванты, стабилизаторы, другие пестицидные добавки или поверхностно-активные вещества. Жидкие составы могут являться на водной или неводной основе, и их можно применять в виде пен, гелей, суспензий, эмульгируемых концентратов или т.п. Ингредиенты могут содержать реологические средства, поверхностно-активные вещества, эмульгаторы, дисперсанты или полимеры.
[0054] Как будет понятно специалисту в данной области, концентрация пестицидов широко варьирует в зависимости от природы конкретного состава, в частности представляет ли она собой концентрат, или ее следует непосредственно использовать. Пестицид содержится в количестве по меньшей мере 1% по массе и может составлять 100% по массе. Сухие составы содержат приблизительно 1-95% по массе пестицида, тогда как жидкие составы, как правило, составляют приблизительно 1-60% по массе твердых веществ в жидкой фазе. Как правило, составы содержат приблизительно от 102 приблизительно до 104 клеток/мг. Такие составы вводят приблизительно при 50 мг (жидкости или сухого вещества) на 1 кг или более на гектар.
[0055] Составы можно вносить в окружающую среду чешуекрылого вредителя, например, наносить на листву или почву, путем распрыскивания, распыления, орошения или т.п.
[0056] Трансформация растений. Предпочтительный рекомбинантный хозяин для продукции инсектицидных белков по настоящему изобретению представляет собой трансформированное растение. Гены, кодирующие белки Bt-токсина, как описано в настоящем описании, можно вводить в растительные клетки различными способами, которые хорошо известны в данной области. Например, большое число клонирующих векторов, содержащих систему репликации в Escherichia coli и маркер, который обеспечивает отбор трансформированных клеток, являются доступными для получения для встраивания чужеродных генов в высшие растения. Векторы содержат, например, в числе прочего pBR322, серию pUC, серию M13mp, pACYC184. Таким образом, фрагмент ДНК, содержащий последовательность, кодирующую белок Bt-токсина можно встраивать в вектор в подходящем участке рестрикции. Получаемую плазмиду используют для трансформации в E. coli. Клетки E. coli культивируют в подходящей питательной среде, затем собирают и лизируют. Выделяют плазмиду. В качестве способов анализа, как правило, проводят анализ последовательности, рестрикционный анализ, электрофорез и другие биохимические молекулярные биологические способы. После каждой манипуляции используемую последовательность ДНК можно расщеплять и присоединять к следующей последовательности ДНК. Каждую последовательность плазмиды можно клонировать в одни и те же или другие плазмиды. В зависимости от способа введения желаемых генов в растение необходимыми могут являться другие последовательности ДНК. Например, если для трансформации растительной клетки используют Ti- или Ri-плазмиду, то по меньшей мере правую границу, а часто правую и левую границу Т-ДНК Ti- или Ri-плазмиды необходимо присоединять в качестве фланкирующей области генов, которые необходимо встраивать. Использование Т-ДНК для трансформации растительных клеток тщательно исследовано и достаточно описано в EP 120516, Lee and Gelvin (2008), Hoekema (1985), Fraley et al., (1986), и An et al., (1985), и хорошо определено в данной области.
[0057] После того как встраиваемая ДНК интегрировалась в геном растения, она является относительно стабильной. Вектор для трансформации обычно содержит селектируемый маркер, который придает трансформируемым растительным клеткам устойчивость к биоциду или антибиотику, такому как в числе прочего биалафос, канамицин, G418, блеомицин или гигромицин. Таким образом, индивидуально применяемый маркер должен обеспечивать возможность отбора трансформированных клеток, а не клеток, которые не содержат встраиваемой ДНК.
[0058] Для введения ДНК в растительную клетку-хозяина доступно большое число способов. Такие способы включают трансформацию Т-ДНК с использованием в качестве средства для трансформации Agrobacterium tumefaciens или Agrobacterium rhizogenes, слияние, инъекцию, биолистику (бомбардировку микрочастицами) или электропорацию, а также другие возможные способы. Если для трансформации используют агробактерии, подлежащую встраиванию ДНК необходимо клонировать в специальные плазмиды, а именно в промежуточный вектор или в бинарный вектор. Промежуточные векторы можно интегрировать в Ti- или Ri-плазмиду гомологичной рекомбинацией благодаря последовательностям, которые являются гомологичными последовательностям в Т-ДНК. Ti- или Ri-плазмида также содержит vir-область, необходимую для переноса Т-ДНК. Промежуточные векторы не могут реплицироваться в агробактериях. Промежуточный вектор можно переносить в Agrobacterium tumefaciens посредством плазмиды-помощника (конъюгации). Бинарные векторы могут реплицироваться в E. coli и в агробактериях. Они содержат селектируемый маркерный ген и линкер или полилинкер, которые находятся в рамках правой и левой граничной области Т-ДНК. Их можно трансформировать непосредственно в агробактерии (Holsters et al., 1978). Используемая в качестве клетки-хозяина Agrobacterium должна содержать плазмиду, несущую vir-область. Vir-область является необходимой для переноса Т-ДНК в растительную клетку. Может содержаться дополнительная Т-ДНК. Трансформированную таким образом бактерию используют для трансформации растительных клеток. Эксплантаты растений можно преимущественно культивировать с Agrobacterium tumefaciens или Agrobacterium rhizogenes для переноса ДНК в растительную клетку. Затем можно регенерировать целые растения из инфицированного растительного вещества (например, кусочков листа, сегментов стебля, корней, а также протопластов или культивируемых в суспензии клеток) в подходящей среде, которая может содержать антибиотики или биоциды для отбора. Получаемые таким образом растения можно затем тестировать на наличие встраиваемой ДНК. В случае инъекции и электропорация к плазмидам не существует специальных требований. Можно использовать общепринятые плазмиды, такие как, например, производные pUC.
[0059] Трансформированные клетки растут внутри растения обычным образом. Они могут образовывать половые клетки и передавать трансформированный признак(и) растениям потомства. Такие растения можно выращивать обычным образом и скрещивать с растениями, которые содержат аналогичные трансформированные наследственные факторы или другие наследственные факторы. Получаемые гибридные индивидуумы обладают соответствующими фенотипическими свойствами.
[0060] В предпочтительном варианте осуществления настоящего изобретения растения трансформируют генами, где частота использования кодона является оптимизированной для растений. См., например, патент США № 5380831, таким образом, включенный посредством ссылки. Несмотря на то, что некоторые усеченные токсины проиллюстрированы в настоящем описании, в области Bt хорошо известно, что токсины типа 130 кДа (полноразмерные) содержат N-концевую часть, которая представляет собой коровый токсин, и C-концевую часть, которая представляет собой "хвост" протоксина. Таким образом, соответствующие "хвосты" можно использовать совместно с усеченными/коровыми токсинами по настоящему изобретению. См., например, патент США № 6218188 и патент США № 6673990. Кроме того, в данной области известны способы получения синтетических генов Bt для применения в растениях (Stewart and Burgin, 2007). Один из неограничивающих примеров предпочтительных трансформированных растений представляет собой фертильное растение кукурузы, содержащее экспрессируемый в растениях ген, кодирующий белок Cry1Ab, и дополнительно содержащее второй экспрессируемый в растениях ген, кодирующий белок Cry1Be.
[0061] Перенос (или интрогрессию) определяемого Cry1Ab и Cry1Be признака(ов) в инбредных линиях кукурузы можно получать существующей в настоящее время селекционного разведения, например, путем обратного скрещивания. В этом случае желаемого рекуррентного родителя сначала скрещивают с донорным инбредным (нерекуррентным) родителем, который несет подходящий ген(ы) для определяемых Cry1A и Cry1Be признаков. Затем потомство такого скрещивания спаривают обратно с рекуррентным родителем с последующим отбором получаемого поколения для передачи желаемого признака(ов) от нерекуррентного родителя. После трех, предпочтительно четырех, более предпочтительно пяти или более генераций от обратного скрещивания с рекуррентным родителем с отбором по желаемому признаку(ам) потомство является гетерозиготным по локусам, контролирующим признак(и), которые переносятся, но является подобным рекуррентному родителю в отношении большинства или почти всех других генов (см., например, Poehlman & Sleper (1995) Breeding Field Crops, 4th Ed., 172-175; Fehr (1987) Principles of Cultivar Development, Vol. 1: Theory and Technique, 360-376).
[0062] Стратегии управления устойчивостью насекомых-вредителей (IRM). Roush et al., например, указывают две стратегии на основании токсинов, также называемых "пирамидированием" или "стэкингом" для управления инсектицидными трансгенными культурами. (The Royal Society. Phil. Trans. R. Soc. Lond. B. (1998) 353, 1777-1786).
[0063] На своем веб-сайте Управление по охране окружающей среды США (epa.gov/oppbppdl/biopesticides/pips/bt_corn_refuge_2006.htm) опубликовало следующие требования для обеспечения нетрансгенных (т.е. не-B.t.) убежищ (раздел культуры не-Bt crops/кукуруза) для использования с трансгенными культурами, продуцирующими один белок Bt, активный против вредителей-мишеней.
"Конкретно составленные требования для продуктов кукурузы, защищенных Bt (Cry1Ab или Cry1F) от кукурузного мотылька, являются такими, как указано ниже:
Структурированные убежища: 20% нечешуекрылых Bt кукурузы на площадях убежищах в поясе кукурузы;
50% нечешуекрылых Bt убежищ в поясе кукурузы
Блоки
Внутренние (т.е. в поле Bt)
Внешние (т.е. отдельные поля в 1/2 милях (1/4 милях при возможности) поля Bt для максимального увеличения случайного спаривания)
Полосы на полях
Полосы должны составлять по меньшей мере 4 ряда в ширину (предпочтительно 6 рядов) для снижения эффектов движения личинок"
[0064] Кроме того, Национальная ассоциация кукурузоводов на своем веб-сайте: (ncga.com/insect-resistance-management-fact-sheet-bt-com)
[0065] также предоставляет аналогичное руководство касательно требований к убежищам. Например:
"Требования для IRM кукурузного мотылька:
- Высаживать по меньшей мере 20% от ваших площадей кукурузы для убежища для гибридов
- В областях продукции хлопка убежище должно составлять 50%
- Необходимо высаживать в 1/2 милях от убежища для гибридов
- Убежище можно высаживать в виде полос на поле Bt; полосы-убежище должны составлять по меньшей мере 4 ряда в ширину
- Убежище можно обрабатывать общепринятыми пестицидами, только если получают экономические пороги в отношении насекомого-мишени
- Нельзя использовать распрыскиваемые инсектициды на основе Bt для кукурузы на площадях убежищах
- Соответствующее убежище необходимо высаживать на каждой ферме с Bt-кукурузой"
[0066] Как определено Roush et al. (например, на страницах 1780 и 1784 правая колонка), стэкинг или пирамидирование двух различных белков, где каждый является эффективным против вредителей-мишеней и с небольшой перекрестной устойчивостью или ее отсутствием, может обеспечивать использование меньшего убежища. Roush позволяет предположить, что для успешного стэка размер убежища менее 10% убежища может обеспечивать сравнимое управление устойчивостью приблизительно до 50% убежища для одного (не входящего в пирамиду) признака. Для доступных в настоящее время продуктов кукуруз с пирамидированным Bt Агентство США по охране окружающей среды требует посадку значительно менее (как правило 5%) структурированного убежища для не-Bt кукурузы по сравнению с продуктами с одним признаком (как правило, 20%).
[0067] Существуют различные пути получения эффектов IRM убежища, включая различные геометрические схемы посадки на полях (как указано выше) и смеси семян в мешках, как обсуждается подробно у Roush et al. (выше) и в патенте США № 6551962.
[0068] Указанные выше проценты или аналогичные отношения убежищ можно использовать для рассматриваемых двойных или тройных стэков или пирамид. Для тройных стэков с тремя местами приложения действия против одного вредителя-мишени целью будет являться ноль убежищ (или, например, менее 5% убежища). В частности это характерно для промышленной площади, например, более 10 акров.
[0069] Все патенты, патентные заявки, предварительные заявки и публикации, на которые указаны ссылки или цитируемые в настоящем описании, полностью включены посредством ссылки в такой степени, что они не противоречат явным указаниям настоящего описания.
[0070] Если конкретно не указано или подразумевается иное, термины в форме единственного числа означают "по меньшей мере один", как используют в настоящем описании.
[0071] Ниже следуют примеры, которые иллюстрируют способы практического осуществления изобретения. Эти примеры не следует трактовать как ограничивающие. Все проценты являются массовыми и все пропорции смесей растворителей являются объемными, если не указано иное. Все температуры приведены в градусах Цельсия.
ПРИМЕРЫ
Пример 1 - Мечение 125I Labeling белка Cry1Ab
Иодирование корового токсина Cry1Ab. Токсин Cry1Ab (SEQ ID NO:1) активировали трипсином и подвергали иодированию с использованием иодогранул (Pierce). В кратком изложении, две иодогранулы дважды промывали 500 мкл фосфатно-солевого буфера, PBS (20 мМ фосфата натрия, 0,15M NaCl, pH 7,5) и помещали в 1,5 мл центрифужную пробирку за свинцовым экраном. В нее добавляли 100 мкл PBS. В вытяжном шкафу и с применением надлежащих техник обращения с радиоактивными веществами к раствору PBS с иодогранулой добавляли 0,5 мКи Na125I (17,4 Ки/мг, Amersham). Компоненты оставляли взаимодействовать в течение 5 минут при комнатной температуре, затем к раствору добавляли 10 мкг усеченного белка Cry1Ab высокой чистоты и оставляли взаимодействовать в течение еще 5 минут. Реакцию останавливали удалением раствора из иодогранул и наносили реакционную смесь на 0,5 мл центрифужную колонку для обессоливания Zeba (InVitrogen), уравновешенную 20 мМ буфером CAPS, pH 10,5+1 мМ DTT. Каждую иодогранулу дважды промывали 10 мкл PBS, а также наносили раствор для промывания в колонку для обессоливания. Радиоактивный раствор элюировали из колонки для обессоливания центрифугированием при 1000×g в течение 2 минут. Радиоактивную чистоту радиоактивно иодированного Cry1Ab определяли SDS-PAGE, визуализацией фосфора и гаммаметрией. В кратком изложении, 2 мкл радиоактивного белка разделяли SDS-PAGE с использованием 4-20% трис-глициновых полиакриламидных гелей (толщиной 1 мм, InVitrogen). После разделения гели сушили с использованием устройства для сушки гелей BioRad по инструкциям производителя. Сухие гели визуализировали путем обертывания их в пленку Mylar (толщиной 12 мкм) и экспонированием их под экраном с длительным послесвечением фосфора Molecular Dynamics (35×43 см) в течение 1 часа. Планшеты проявляли с использованием фосфор-визуализирующей системы Molecular Dynamics Storm 820 и анализировали изображения с использованием программного обеспечения ImageQuant™. Специфическая активность составляла приблизительно 4 мкКи/мкг белка.
Пример 2 - Протокол получения BBMV
Препарат и фракционирование солюбилизированных BBMV. Личинок Ostrinia nubilalis на последней личиночной стадии лишали корма в течение ночи, а затем утром иссекали после охлаждения на льду в течение 15 минут. Ткань средней кишки удаляли из полости тела, оставляя позади заднюю кишку, прикрепленную к наружному покрову. Среднюю кишку помещали в 9X объем ледяного буфера для гомогенизации (300 мМ маннита, 17 мМ трис-основания, pH 7,5) с добавлением смеси ингибиторов протеаз1 (1конечная концентрация компонентов смеси (в мкМ) является следующей AEBSF (500), ЭДТА (250 мМ), бестатин (32), E-64 (0,35), леупептин (0,25) и апротитин (0,075)) (Sigma P-2714), разбавленной как рекомендовано поставщиком. Ткань гомогенизировали 15 движениями гомогенизатора из стеклоткани. BBMV получали способом осаждения MgCl2 Wolfersberger (1993). В кратком изложении, равный объем 24 мМ раствора MgCl2 в 300 мМ маннита смешивали с гомогенатом средней кишки, перемешивали в течение 5 минут и оставляли отстаиваться на льду в течение 15 минут. Раствор центрифугировали при 2500×g в течение 15 минут при 4°C. Сохраняли супернатант и суспендировали осадок в исходном объеме 0,5-X разбавленного буфера для гомогенизации и снова центрифугировали. Объединяли два супернатанта, центрифугировали при 27000×g в течение 30 минут при 4°C с образованием фракции BBMV. Осадок суспендировали в 10 мл буфера для гомогенизации с добавлением ингибиторов протеаз и снова центрифугировали при 27000×g в течение 30 минут при 4°C для промывания BBMV. Получаемый осадок суспендировали в буфере для хранения BBMV (10 мМ HEPES, 130 мМ KC1, 10% глицерина, pH 7,4) до концентрации приблизительно 3 мг/мл белка. Концентрацию белка определяли способом Брэдфорд (1976) с бычьим сывороточным альбумином (BSA) в качестве стандарта. Определение щелочной фосфатазы проводили до замораживания образцов анализом Sigma по инструкциям производителя. Специфическая активность такого маркерного фермента во фракции BBMV, как правило, повышалась в 7 раз по сравнению с активностью, выявляемой во фракции гомогената средней кишки. BBMV разделяли на аликвоты по 250 мкл образцов, быстро замораживали в жидком N2 и хранили при -80°C.
Пример 3 - Способ измерения связывания белка 125I Cry1Ab с белками BBMV
Связывание белка 125I Cry1Ab с BBMV. Для определения оптимального количества белка BBMV для использования в анализах связывания получали кривую насыщения. Радиоактивно меченый 125I белок Cry1Ab (0,5 нМ) инкубировали в течение 1 часа при 28°C с различными количествами белка BBMV в диапазоне 0-500 мкг/мл в связывающем буфере (8 мМ NaHPO4, 2 мМ KH2PO4, 150 мМ NaCl, 0,1% бычьего сывороточного альбумина, pH 7,4). Общий объем составлял 0,5 мл. Связанный белок 125I Cry1Ab отделяли от несвязанного, отбирая образец 150 мкл реакционной смеси в трех повторениях из 1,5 мл центрифужной пробирки в 500 мкл центрифужную пробирку и центрифугируя образцы при 14000×g в течение 6 минут при комнатной температуре. Супернатант аккуратно удаляли и аккуратно промывали осадок три раза ледяным связывающим буфером. Дно центрифужной пробирки, содержащей осадок, отрезали и помещали в 13×75 мм стеклянную культуральную пробирку. Образцы определяли в течение каждых 5 минут в гамма-счетчике. Подсчеты для образца вычитали из подсчетов фона (реакция без какого-либо белка) и наносили на график в зависимости от концентрации белка BBMV. Оптимальное для использования количество белка определяли как равное 0,15 мг/мл белка BBMV.
Для определения кинетики связывания получали кривую насыщения. В кратком изложении, BBMV (150 мкг/мл) инкубировали в течение 1 часа при 28°C с увеличивающимися концентрациями токсина 125I Cry1Ab в диапазоне от 0,01 до 10 нМ. Общее связывание определяли, отбирая пробу 150 мкл каждой концентрации в тех повторениях, центрифугируя образец и проводя подсчет, как описано выше. Неспецифическое связывание определяли аналогичным образом с добавлением 1000 нМ гомологичного трипсинизированного нерадиоактивного токсина Cry1Ab, добавляемого в реакционную смесь для насыщения всех неспецифических участков связывания рецептора. Специфическое связывание рассчитывали как разницу между общим связыванием и неспецифическим связыванием.
Анализы конкурентного связывания гомологичного (Cry1Ab) и гетерологичного (DIG-3) проводили с использованием 150 мкг/мл белка BBMV и 0,5 нМ радиоактивно меченого 125I белка Cry1Ab. Cry1Ab и DIG-3 (SEQ ID NO:2) активировали трипсином и использовали в качестве конкурирующих белков. Концентрация конкурирующего нерадиоактивно меченого токсина Cry1Ab или DIG-3, добавляемого к реакционной смеси, находилась в диапазоне от 0,03 до 1000 нМ, и их добавляли одновременно с радиоактивным лигандом для обеспечения настоящего конкурентного связывания. Инкубации проводили в течение 1 часа при 28°C и измеряли количество белка 125I Cry1Ab, связанного со своим рецептором токсина, как описано выше, с вычитанием неспецифического связывания. Сто процентов общего связывания определяли при отсутствии какого-либо конкурирующего лиганда. Результаты наносили на график в полулогарифмическом масштабе в виде процента общего специфического связывания в зависимости от концентрации добавляемого конкурирующего лиганда.
Пример 4 - Обобщающие результаты
На фиг.1 представлен процент специфического связывания 125I Cry1Ab (0,5 нМ) в BBMV от Ostrinia nubilalis в сравнении с конкурентным связыванием немеченым гомологичным Cry1Ab (•) и гетерологичным DIG-3 (■). Кривая замещения для гомологичного конкурентного связывания Cry1Ab результаты приводит к кривой сигмоидальной формы, демонстрирующей 50% замещение радиоактивного лиганда при приблизительно 0,5 нМ Cry1Ab. DIG-3 не замещает какого-либо связывания 125I Cry1Ab на своем участке связывания при концентрациях 100 нМ или ниже (200 раз выше чем концентрация 125I Cry1Ab в анализе). Только при 300 нМ авторы наблюдают приблизительно 25% замещение связывания 125I Cry1Ab DIG-3. Эти результаты демонстрируют, что DIG-3 не конкурирует эффективно за связывание Cry1Ab с участками рецептора, локализованными в BBMV от Ostrinia nubilalis.
СПИСОК ЛИТЕРАТУРЫ
Heckel, D.G., Gahan, L.J., Baxter, S.W., Zhao, J.Z., Shelton, A.M., Gould, F., and Tabashnik, B-E. (2007). The diversity of Bt resistance genes in species of Lepidoptera. J Invertebr Pathol 95, 192-197.
Luo, K., Banks, D., and Adang, M.J. (1999). Toxicity, binding, and permeability analyses of four bacillus thuringiensis cryl delta-endotoxins using brush border membrane vesicles of spodoptera exigua and spodoptera frugiperda. Appl. Environ. Microbiol. 65, 457-464.
Palmer, M., Buchkremer, M, Valeva, A, and Bhakdi, S. Cysteine-specific radioiodination of proteins with fluorescein maleimide. Analytical Biochemistry 253, 175-179. 1997. Ref Type: Journal (Full)
Sambrook, J. and Russell, D.W. (2001). Molecular Cloning: A Laboratory Manual. Cold Spring Harbor Laboratory).
Schlenz, M.L., Babcock, J.M., and Storer, N.P. Response of CrylF-resistant and Susceptible European Corn Borer and Fall Armyworm Colonies to Cry 1A. 105 and Cryl2Ab2. DAI 0830, 2008. Indianapolis, Dow AgroSciences. Derbi Report.
Sheets, J.J. and Storer, N.P. Analysis of CrylAc Binding to Proteins in Brush Border Membrane Vesicles of Corn Earworm Larvae (Heleothis zed). Interactions with Cry IF Proteins and Its Implication for Resistance in the Field. DAI-0417, 1-26. 2001. Indianapolis, Dow AgroSciences.
Tabashnik, B.E., Liu, Y.B., Finson, N., Masson, L., and Heckel, D.G. (1997). One gene in diamondback moth confers resistance to four Bacillus thuringiensis toxins. Proc. Natl. Acad. Sci. U.S.A 94, 1640-1644.
Tabashnik, B.E., Malvar, T., Liu, Y.B., Finson, N., Borthakur, D., Shin, B.S., Park, S.FL, Masson, L., de Maagd, R.A., and Bosch, D. (1996). Cross-resistance of the diamondback moth indicates altered interactions with domain II of Bacillus thuringiensis toxins. Appl. Environ. Microbiol. 62, 2839-2844.
Tabashnik, B.E., Roush, R.T., Earle, E.D., and Shelton, A.M. (2000). Resistance to Bt toxins. Science 287, 42.
Wolfersberger, M.G. (1993). Preparation and partial characterization of amino acid transporting brush border membrane vesicles from the larval midgut of the gypsy moth (Lymantria dispar). Arch. Insect Biochem. Physiol 24, 139-147.
Xu, X., Yu, L., and Wu, Y. (2005). Disruption of a cadherin gene associated with resistance to CrylAc {delta}-endotoxin of Bacillus thuringiensis in Helicoverpa armigera. Appl Environ Microbiol 71, 948-954.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМБИНИРОВАННОЕ ИСПОЛЬЗОВАНИЕ БЕЛКОВ CRY1Ca И CRY1Ab ДЛЯ КОНТРОЛЯ УСТОЙЧИВОСТИ НАСЕКОМЫХ | 2010 |
|
RU2596406C2 |
| ПРИМЕНЕНИЕ CRY1AB В КОМБИНАЦИИ С CRY1BE ДЛЯ УПРАВЛЕНИЯ РЕЗИСТЕНТНОСТЬЮ НАСЕКОМЫХ | 2010 |
|
RU2583288C2 |
| КОМБИНИРОВАННОЕ ПРИМЕНЕНИЕ БЕЛКОВ CRY1Ca И CRY1Fa ДЛЯ БОРЬБЫ С РЕЗИСТЕНТНОСТЬЮ У НАСЕКОМЫХ | 2010 |
|
RU2593961C2 |
| ПРИМЕНЕНИЕ Cry1Da В СОЧЕТАНИИ С Cry1Be ДЛЯ УПРАВЛЕНИЯ УСТОЙЧИВЫМИ НАСЕКОМЫМИ | 2010 |
|
RU2590592C2 |
| ПРИМЕНЕНИЕ Cry1Da В СОЧЕТАНИИ С Cry1Ca ДЛЯ УПРАВЛЕНИЯ УСТОЙЧИВЫМИ НАСЕКОМЫМИ | 2010 |
|
RU2569108C2 |
| КОМБИНИРОВАННОЕ ПРИМЕНЕНИЕ БЕЛКОВ Vip3Ab И Cry1Fa ДЛЯ ВЫРАБАТЫВАНИЯ РЕЗИСТЕНТНОСТИ К НАСЕКОМЫМ | 2010 |
|
RU2607666C2 |
| КОМБИНИРОВАННОЕ ПРИМЕНЕНИЕ БЕЛКОВ Cry1Da И Cry1Fa ДЛЯ ВЫРАБАТЫВАНИЯ РЕЗИСТЕНТНОСТИ К НАСЕКОМЫМ | 2010 |
|
RU2603257C2 |
| ПРИМЕНЕНИЕ Vip3Ab В СОЧЕТАНИИ С Cry1Ca ДЛЯ УПРАВЛЕНИЯ УСТОЙЧИВЫМИ НАСЕКОМЫМИ | 2010 |
|
RU2575084C2 |
| КОМБИНИРОВАННОЕ ПРИМЕНЕНИЕ VIP3AB И CRY1AB ДЛЯ РЕГУЛИРОВАНИЯ УСТОЙЧИВЫХ НАСЕКОМЫХ | 2011 |
|
RU2608500C2 |
| КОНТРОЛЬ УСТОЙЧИВОСТИ НАСЕКОМЫХ С ПОМОЩЬЮ КОМБИНАЦИИ БЕЛКОВ Cry1Be И Cry1F | 2010 |
|
RU2575611C2 |











Изобретение относится к области биохимии, в частности к трансгенному растению для замедления или предотвращения развития устойчивости к белкам Cry1Ab и DIG-3 у кукурузного мотылька (ЕСВ), его семени, а также к способу предотвращения развития устойчивости к белку Cry1Ab и DIG-3 у ECB с его использованием. Также раскрыты смесь семян для замедления или предотвращения развития устойчивости к белкам Cry1Ab и DIG-3 у ЕСВ, растительная клетка для замедления или предотвращения развития устойчивости к белкам Cry1Ab и DIG-3 у ЕСВ. Изобретение также относится к способу борьбы с ECB, включающему приведение указанного насекомого или окружающей среды указанного насекомого в контакт с эффективным количеством композиции, которая содержит белок Cry1Ab и белок DIG-3, а также к способу получения композиции, которая содержит белок Cry1Ab и белок DIG-3. Изобретение позволяет эффективно бороться с кукурузным мотыльком. 7 н. и 9 з.п. ф-лы, 1 ил., 1 табл., 4 пр.
1. Трансгенное растение для замедления или предотвращения развития устойчивости к белкам Cry1Ab и DIG-3 у кукурузного мотылька (ЕСВ), содержащее полинуклеотид Cry1Ab, кодирующий инсектицидный белок Cry1Ab с SEQ ID NO: 1, и полинуклеотид DIG-3, кодирующий инсектицидный белок DIG-3 с SEQ ID NO: 2.
2. Трансгенное растение по п. 1 для предотвращения развития устойчивого к Cry кукурузного мотылька (ЕСВ), где указанное растение дополнительно содержит ДНК, кодирующую третий инсектицидный белок, предпочтительно, выбранный из группы, состоящей из Cry1Fa, Cry1Be и Cry2Aa.
3. Трансгенное растение по п. 2, где указанное растение дополнительно содержит ДНК, кодирующую четвертый инсектицидный белок, предпочтительно, выбранный из группы, состоящей из Cry1Be и Cry2Aa, где третий инсектицидный белок представляет собой белок Cry1Fa.
4. Семя трансгенного растения по п. 1, для выращивания растения, которое защищено от повреждений указанными насекомыми, обладающими устойчивостью к белкам Cry1Ab и DIG-3, где указанное семя содержит полинуклеотид Cry1Ab, кодирующий инсектицидный белок Cry1Ab с SEQ ID NO: 1, и полинуклеотид DIG-3, кодирующий инсектицидный белок DIG-3 с SEQ ID NO: 2.
5. Смесь семян для замедления или предотвращения развития устойчивости к белкам Cry1Ab и DIG-3 у ЕСВ, содержащая семена с площадей убежищ от не-Bacillus thuringiensis (не-Bt) растений с площадей убежищ, которые не экспрессируют трансгенные инсектицидные белки, и множество семян по п. 4, где указанные семена с площадей убежищ составляют от 5% до 40% от всех семян в смеси.
6. Смесь семян по п. 5, где указанные семена с площадей убежищ составляют от 5% до 30% от всех семян в смеси.
7. Смесь семян по п. 5, где указанные семена с площадей убежищ составляют от 5% до 20% от всех семян в смеси.
8. Смесь семян по п. 5, где указанные семена с площадей убежищ составляют от 5% до 10% от всех семян в смеси.
9. Смесь семян по п. 5, где указанные семена с площадей убежищ составляют 5% от всех семян в смеси.
10. Способ предотвращения развития устойчивости к белку Cry1Ab и DIG-3 у ЕСВ, где указанный способ включает посев семян для получения множества растений по п. 1, и приведение в контакт указанного ЕСВ с указанным множеством растений.
11. Растение по п. 1, где указанное растение выбрано из группы, состоящей из кукурузы, соевых бобов и хлопка.
12. Растение по п. 11, где указанное растение представляет собой растение кукурузы.
13. Растительная клетка для замедления или предотвращения развития устойчивости к белкам Cry1Ab и DIG-3 у кукурузного мотылька (ЕСВ), содержащая полинуклеотид Cry1Ab, кодирующий инсектицидный белок Cry1Ab с SEQ ID NO: 1, и полинуклеотид DIG-3, кодирующий инсектицидный белок DIG-3 с SEQ ID NO: 2.
14. Способ борьбы с насекомым кукурузным мотыльком, где указанный способ включает приведение указанного насекомого или окружающей среды указанного насекомого в контакт с эффективным количеством композиции, которая содержит инсектицидный белок Cry1Ab с SEQ ID NO: 1 и дополнительно содержит инсектицидный белок DIG-3 с SEQ ID NO: 2.
15. Способ по п. 14, где указанная композиция представляет собой множество растительных клеток.
16. Способ получения композиции, которая содержит инсектицидный белок Cry1Ab с SEQ ID NO: 1 и инсектицидный белок DIG-3 с SEQ ID NO: 2, включающий репродукцию указанных клеток по п. 13.
| US2010269223 A1, 21.10.2010) | |||
| BRAVO A | |||
| et al., How to cope with insect resistance to Bt toxins?, Trends Biotechnol, 2008, Vol.26, N.10, pp.573-579 | |||
| WO2011084631 A1, 14.07.2011 | |||
| ФРАГМЕНТ ГИБРИДНОГО ТОКСИНА Bacillus thuringiensis, ОБЛАДАЮЩИЙ ИНСЕКТИЦИДНОЙ АКТИВНОСТЬЮ, КОДИРУЮЩАЯ ЕГО РЕКОМБИНАНТНАЯ ДНК, СПОСОБ БОРЬБЫ С НАСЕКОМЫМИ | 1994 |
|
RU2210593C2 |
Авторы
Даты
2017-06-30—Публикация
2012-08-03—Подача