Изобретение относится к аналитической химии, а именно к способам определения содержания ионов металлов, и может быть использовано для анализа вод различного происхождения (питьевые воды, геотермальные источники, смывы хвостов обогащения), а также технологических сливов методом инверсионной вольтамперометрии (ИВ).
Известен метод вольтамперометрического определения родия(III) с использованием платинового электрода и фона 0,1 M NaNO3. Катодная вольтамперная кривая электровосстановления родия(III) имеет форму волны с потенциалом полуволны 0,2 В нас. к.э. Определяемая концентрация родия(III) составила 4,5⋅10-3 г/дм3 [Бардин М.Б., Ляликов Ю.С., Темянко B.C. «Полярографическое определение некоторых благородных металлов с применением платиновых электродов» // Сб. «Анализ благородных металлов» - 1959. - М.: АН СССР - С. 80-87]. Недостатками метода являются низкая чувствительность определения родия, использование дорогостоящей платиновой проволоки, определению мешают все платиновые металлы.
Известен метод определения ионов родия(III) методом инверсионной вольтамперометрии с использованием стеклоуглеродного электрода в растворе 1 M HCl с добавлением соли Hg(I). Определяемые содержания родия(III) составили 2⋅10-5 г/дм3. Потенциал электролиза -0,5 В, время электролиза составляет 6 мин [Попов Г.Н., Пнев В.В., Захаров М.С. «Определение родия методом инверсионной вольтамперометрии» // Журнал аналитической химии. - 1972, - Т. 27. - Вып. 12. - С. 2456-2458]. Недостатками метода являются низкая чувствительность метода, использование в анализе токсичных соединений ртути, определению мешают все платиновые металлы, серебро и золото.
Известен метод определения родия(III) в водном растворе методом пленочной полярографии с использованием пропитанных эпоксидной смолой графитовых электродов в растворах 0,1 M HCl с добавлением Hg(NO3)2. Определяемая концентрация родия(III) составила 1,03⋅10-4 г/дм3 [Чемерис М.С, Колпакова Н.А., Стромберг А.Г., Васильев Ю.Б. «Механизм разряда и ионизации ионов родия и иридия на графитовом электроде в присутствиии ионов ртути(II)» // Электрохимия - 1976. - Т. 2. - №5. - С. 717-722]. Недостатками метода являются низкая чувствительность метода, использование солей токсичной ртути, определению мешают все платиновые металлы, серебро и золото.
Известен метод определения родия методом инверсионной вольтамперометрии с использованием импрегнированного полиэтиленом графитового электрода [Шифрис Б.С., Колпакова Н.А. «Совместное определение родия и иридия методом инверсионной вольтамперометрии в медно-никелевых концентратах» // Журнал аналитической химии. - 1982. - Т. 37. - Вып. 12. - С. 2217-2220]. Определение ионов родия(III) проводилось в растворе 0,5 M HCl с добавлением ионов Hg(II). Электроконцентрирование родия проводилось в сплав со ртутью при потенциале электролиза минус 0,6 В нас. к.э. в течение от 1 до 25 мин. Потенциал аналитического сигнала равен плюс 0,3 В. Недостатками метода являются низкая чувствительность метода, использование солей токсичной ртути, определению мешают все платиновые металлы, серебро и золото.
Известен метод определения родия в водных растворах с использованием сажевого электрода. Определение проводили по пику селективного электроокисления индия из интерметаллического соединения RhxIny [Пат. №2540261 от 10.02.2015 г. Российская Федерация. Способ определения родия в водных растворах методом инверсионной вольтамперометрии по пику селективного электроокисления индия из интерметаллического соединения RhxIny / Нестеров А.А., Устинова Э.М., Колпакова Η.Α., Горчаков Э.В., Пакриева Е.Г. // Бюл. №4. - 2015. - 7 с.](прототип).
В литературе отсутствуют сведения об интерметаллических соединениях родия и индия. Электроконцентрирование ионов родия(III) и индия(III) проводили на сажевый электрод при потенциале электроконцентрирования минус 1,2 В из раствора 1 M HCl. Концентрацию ионов родия(III) определяли по высоте анодного пика селективного электроокисления индия из интерметаллического соединения с родием, наблюдаемого в диапазоне потенциалов от -0,2 до 0,1 В относительно насыщенного хлоридсеребряного электрода. Недостатком метода является мешающее влияние платиновых металлов, серебра и золота.
Задача изобретения: разработать методику определения ионов родия(III) в растворах 1 M HCl + 10-3 M Pb(II) методом инверсионной вольтамперометрии с использованием импрегнированного полиэтиленом графитового электрода по пикам селективного электроокисления свинца из интерметаллических соединений с родием. Для этого родий осаждают на поверхность графитового электрода совместно со свинцом, образуя сплав в присутствии ионов платины(IV, II), палладия(II) и золота(III) в соотношениях Rh:Pt=1:1, Rh:Pd=1:10, Rh:Au=1:10. Накопление ионов родия на графитовом электроде в перемешивающемся растворе в присутствии ионов свинца проводят в течение 180-240 секунд при потенциале электролиза минус 1,5 В из фонового электролита 1 M HCl с последующей регистрацией анодных пиков селективного электроокисления свинца из сплава с родием при скорости развертки потенциала 0,05-0,06 В/с. Концентрацию ионов родия определяют по площади под пиками селективного электроокисления свинца в диапазоне потенциалов от -0,5 до -0,2 В отн. нас. х.с.э., используя метод добавок аттестованных смесей.
Новым в способе является:
- для получения полезного сигнала, зависящего от концентрации ионов родия(III) в растворе, используют процесс селективного электроокисления свинца(II) из интерметаллических соединений с родием. Из литературных данных это соединения Rh3Pb2 и Rh5Pb7, образующиеся на электроде на стадии предэлектролиза. В предлагаемом способе впервые установлена способность свинца образовывать на электроде сплавы с родием в фазе интерметаллических соединений и затем селективно окисляться из интерметаллических соединений с родием при потенциалах, отличных от потенциала электроокисления свинца. В прототипе состав ИМС не установлен;
- в качестве индикаторного применяют пропитанный полиэтиленом графитовый электрод, имеющий меньшее сопротивление, чем сажевый электрод (прототип) и потому обладающий большей электроактивной поверхностью;
- определение проводят по пикам селективного электроокисления свинца(II) из интерметаллических соединений с родием(III), которые наблюдают при более отрицательных потенциалах (от -0,5 до -0,2 В нас. х.с.э.), чем селективное электроокисление индия из интерметаллического соединения с родием (+0,1 В), что и позволяет определять ионы родия(III) в присутствии ионов платины(IV, II), палладия(II) и золота(III). Определению ионов родия(III) не мешают ионы платины(IV, II), палладия(II) и золота(III), если они находятся в растворе в соотношениях: Rh:Pt=1:1; Rh:Pd=1:10 и Rh:Au=1:10.
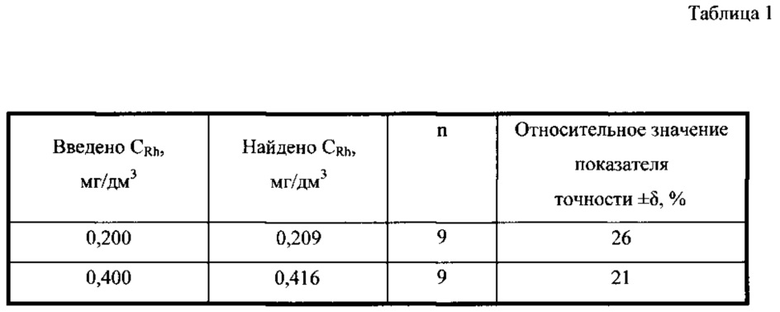
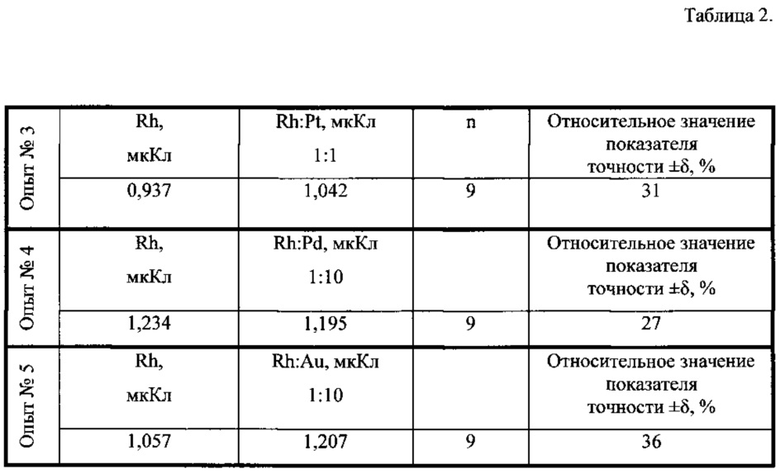
Результаты определения ионов родия(III) в электролите 1М HCl методом инверсионной вольтамперометрии по площади под пиками селективного электроокисления свинца(II) из интерметаллического соединения с родием приведены в таблице 1. Результаты определения родия в фоновом электролите в присутствии платины, палладия и золота приведены в таблице 2. Правильность определения оценивалась методом «введено-найдено».
Таким образом, установленные условия впервые позволили количественно определять содержание ионов родия(III) методом инверсионной вольтамперометрии с использованием пропитанного полиэтиленом графитового электрода в интервале содержаний 0,1-1 мг/дм3 по пикам селективного электроокисления свинца(II) из интерметаллических соединений с родием в присутствии ионов платины(IV, II), палладия(II) и золота(III), если они находятся в растворе в соотношениях: Rh:Pt=1:1; Rh:Pd=1:10 и Rh:Au=1:10.
Пример конкретного выполнения.
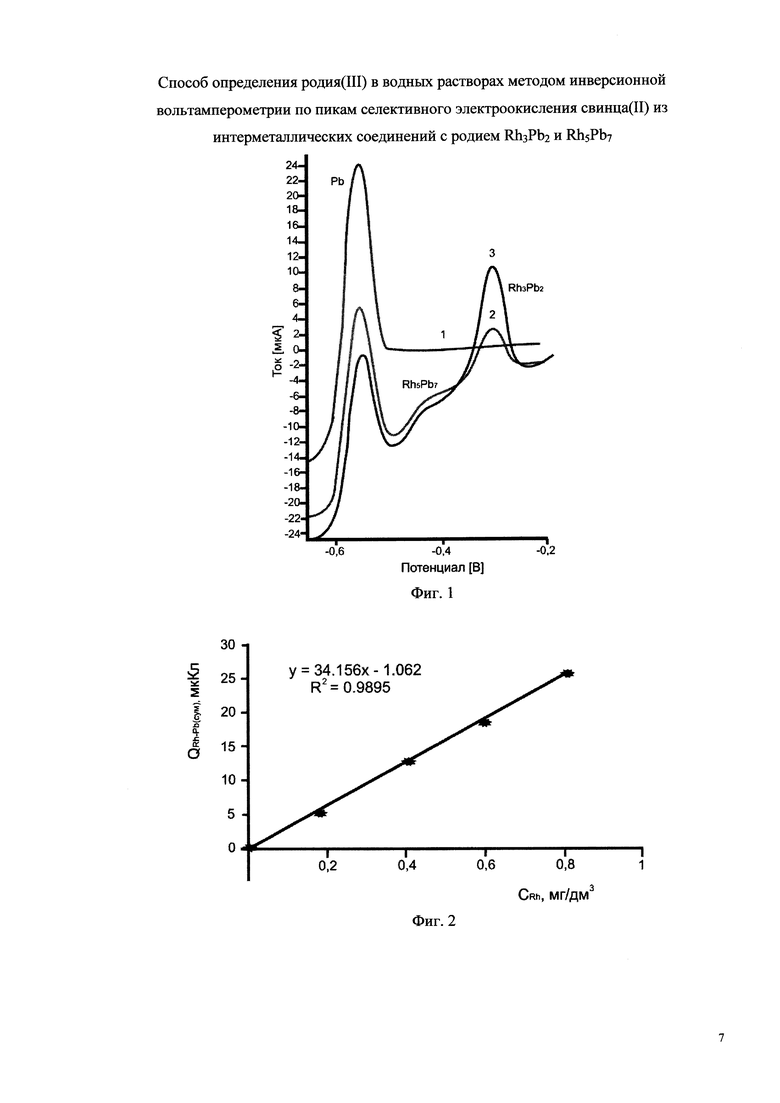
Пример 1. (фиг. 1). Измерения проведены на искусственных смесях. 10 мл фонового электролита (1 M HCl) помещают в кварцевый стаканчик. Затем добавляют аттестованный раствор Pb(II) 0,02 мл из 100 мг/дм3. Не прекращая перемешивания, проводят электролиз раствора, при ЕЭ=-1,5 В и при τэ=180 сек, снимают вольтамперную кривую электроокисления при скорости развертки потенциала 0,06 В/с. Вносят добавку стандартного раствора Rh(III) 0,02 мл из 10 мг/дм3 и регистрируют аналитический сигнал пиков селективного электроокисления свинца из ИМС с родием в диапазоне потенциалов от -0,5 до -0,2 В (нас. х.с.э.). Затем вносят еще одну добавку стандартного образца Rh 0,02 мл из 10 мг/дм3 и регистрируют аналитический сигнал при аналогичных условиях. По величине площади под пиками в указанном диапазоне вычисляют концентрацию родия(III) в растворе.
На фиг. 1 представлены вольтамперные кривые селективного электроокисления свинца из интерметаллических соединений с родием. Кривая 1 - фон 1М HCl + CPb(II) = 2 мг/дм3, кривая 2 - фон 1M HCl + CPb(II) = 2 мг/дм3 + CPh(III) = 0,2 мг/дм3, кривая 3 - фон 1M HCl + CPb(II) = 2 мг/дм3 + CRh(III) = 0,4 мг/дм3.
Пример 2. Измерения проведены на искусственных смесях в присутствии ионов платины(IV, II), палладия(II) и золота(III).
Опыт №1. 10 мл фонового электролита (1М HCl) помещают в кварцевый стаканчик, добавляют аттестованный раствор Pb(II) 0,02 мл из 100 мг/дм3, не прекращая перемешивания, проводят электроосаждение свинца на поверхность импрегнированного полиэтиленом графитового электрода при Еэ=-1,5 В и времени электролиза 180 сек, регистрируют вольтамперную кривую электроокисления свинца при скорости развертки 0,06 В/с в области потенциалов от -0,7 до -0,6 В нас. х.с.э.
Опыт №2. В раствор опыта №1 добавляют стандартный раствор родия(III) 0,02 из 10 мг/дм3, проводят концентрирование бинарного сплава родий-свинец и регистрируют вольтамперную кривую селективного электроокисления свинца из интерметаллических соединений с родием в диапазоне потенциалов от -0,5 до -0,2 В нас. х.с.э.
Опыт №3. К раствору опыта №2 добавляют стандартный раствор платины 0,02 из 10 мг/дм3 (Rh:Pt=1:1). Проводят электроосаждение осадка при ЕЭ=-1,5 В в течение 180 секунд при постоянном перемешивании раствора. Проводят регистрацию вольтамперной кривой при скорости изменения потенциала 0,06 В/с в диапазоне от -0,5 до -0,2 В.
Опыт №4. К раствору опыта №2 добавляют стандартный раствор палладия 0,02 из 100 мг/дм3 (Rh:Pd=1:10). Проводят электроосаждение осадка при ЕЭ=-1,5 В в течение 180 секунд при постоянном перемешивании раствора. Проводят регистрацию вольтамперной кривой при скорости изменения потенциала 0,06 В/с в диапазоне от -0,5 до -0,2 В.
Опыт №5. К раствору опыта №2 добавляют стандартный раствор золота 0,02 из 100 мг/дм3 (Rh:Au=1:10). Проводят электроосаждение осадка при ЕЭ=-1,5 В в течение 180 секунд при постоянном перемешивании раствора. Регистрируют вольтамперную кривую при скорости изменения потенциала 0,06 В/с в диапазоне от -0,5 до -0,2 В.
Таким образом, впервые установлена способность количественного анализа ионов родия(III) в присутствии платины(IV, II), палладия(II) и золота(III) по пикам селективного электроокисления свинца из интерметаллических соединений с родием.
Изобретение может быть использовано в различных отраслях народного хозяйства для определения содержания родия в растворах. Способ определения родия(III) в водных растворах методом инверсионной вольтамперометрии по пикам селективного электроокисления свинца(II) из интерметаллических соединений Rh3Pb2 и Rh5Pb7 заключается в том, что родий осаждают на поверхность графитового электрода совместно со свинцом, образуя сплав в присутствии ионов платины(IV, II), палладия(II) и золота(III) в соотношениях Rh:Pt=1:1, Rh:Pd=1:10, Rh:Au=1:10, накопление ионов родия на графитовом электроде в перемешивающемся растворе в присутствии ионов свинца проводят в течение 180-240 секунд при потенциале электролиза минус 1,5 В из фонового электролита 1 М HCl с последующей регистрацией анодных пиков селективного электроокисления свинца из сплава с родием при скорости развертки потенциала 0,05-0,06 В/с, а концентрацию ионов родия определяют по площади под пиками селективного электроокисления свинца в диапазоне потенциалов от -0,5 до -0,2 В отн. нас. х.с.э., используя метод добавок аттестованных смесей. Техническим результатом изобретения является определение ионов родия в водных растворах методом инверсионной вольтамперометрии в присутствии ионов платины, палладия, золота. 2 табл, 2 ил., 1 пр.
Способ определения родия(III) в водных растворах методом инверсионной вольтамперометрии по пикам селективного электроокисления свинца(II) из интерметаллических соединений Rh3Pb2 и Rh5Pb7, заключающийся в том, что родий осаждают на поверхность графитового электрода совместно со свинцом, образуя сплав в присутствии ионов платины(IV, II), палладия(II) и золота(III) в соотношениях Rh:Pt=1:1, Rh:Pd=1:10, Rh:Au=1:10, накопление ионов родия на графитовом электроде в перемешивающемся растворе в присутствии ионов свинца проводят в течение 180-240 секунд при потенциале электролиза минус 1,5 В из фонового электролита 1 М HCl с последующей регистрацией анодных пиков селективного электроокисления свинца из сплава с родием при скорости развертки потенциала 0,05-0,06 В/с, а концентрацию ионов родия определяют по площади под пиками селективного электроокисления свинца в диапазоне потенциалов от -0,5 до -0,2 В отн. нас. х.с.э., используя метод добавок аттестованных смесей.
| СПОСОБ ОПРЕДЕЛЕНИЯ РОДИЯ В ВОДНЫХ РАСТВОРАХ МЕТОДОМ ИНВЕРСИОННОЙ ВОЛЬТАМПЕРОМЕТРИИ ПО ПИКУ СЕЛЕКТИВНОГО ЭЛЕКТРООКИСЛЕНИЯ ИНДИЯ ИЗ ИНТЕРМЕТАЛЛИЧЕСКОГО СОЕДИНЕНИЯ Rhx Iny | 2013 |
|
RU2540261C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ РОДИЯ В ВОДНЫХ РАСТВОРАХ МЕТОДОМ ИНВЕРСИОННОЙ ВОЛЬТАМПЕРОМЕТРИИ ПО ПИКУ СЕЛЕКТИВНОГО ЭЛЕКТРООКИСЛЕНИЯ МЕДИ ИЗ RhCu | 2012 |
|
RU2498290C1 |
| СПОСОБ ИНВЕРСИОННО-ВОЛЬТАМПЕРОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ РОДИЯ В НИТРИТНОЙ СРЕДЕ | 2009 |
|
RU2406995C1 |
| JP 2003279559 A, 02.10.2003. | |||
Авторы
Даты
2017-07-06—Публикация
2016-03-21—Подача