Уровень техники
Область техники
[0001] Настоящее изобретение относится к комбинации ингибитора киназы CHK1 с ингибитором киназы WEE1, а также способам ее применения.
Описание уровня техники
[0002] Чекпойнт-киназа 1 («CHK1») является серин/треонинкиназой. CHK1 регулирует развитие клеточного цикла и является основным фактором ответа на повреждение ДНК внутри клетки. Известно, что ингибиторы CHK1 сенсибилизируют клетки опухоли к различным генотоксичным агентам, таким как химиотерапия и радиация. (Tse, Archie N., et al., "Targeting Checkpoint Kinase 1 in Cancer Therapeutics." Clin. Cancer Res. 13(7) (2007) 1955-1960). Наблюдалось, что многие опухоли обладают недостатком чекпойнта повреждения ДНК в стадии G1, что приводит к зависимости восстановления повреждения ДНК и выживания от чекпойнтов S и G2. (Janetka, James W., et al., "Inhibitors of checkpoint kinases: From discovery to the clinic." Drug Discovery & Development, том. 10, №4 (2007) 473-486). Чекпойнты S и G2 регулируются действием СНК1. Было показано, что ингибирование CHK1 аннулирует чекпойнты S и G2, ослабляя за счет этого восстановление ДНК и приводя к повышенной гибели опухолевых клеток. Однако нераковые клетки обладают действующим чекпойнтом G1, что дает возможность восстановления ДНК и выживания. Основной мишенью CHK1 является фосфатаза CDC25A, которая является активатором циклин-зависимых киназ («CDK»). При фосфорилировании CDC25A под действием CHK1, разложение CDC25A ускоряется, что, в свою очередь, замедляет репликацию ДНК и предотвращает вход в митоз до восстановления повреждения (Beck, Haldan, et al., "Regulators of cyclin dependent kinases are crucial for maintaining genome integrity in S phase." J. Cell Biol, том 188, №5 (2010) 629-638).
[0003] Известны ингибиторы CHK1, например, в Международной публикации WO 2009/004329, Международной публикации WO 2008/012635, Международной публикации WO 2007/090493, Международной публикации WO 2007/090494, Международной публикации WO 2006/106326, Международной публикации WO 2006/120573, Международной публикации WO 2005/103036, Международной публикации WO 2005/066163 и Международной публикации WO 03/028724.
[0004] Ингибиторы CHK1 включают PF-00477736 (известный также как PF-477736), AZD7762, XL844, IC-83, CHIR-124, PD-321852, LY2603618, LY2606368 и SCH 900776.
[0005] В Международной публикации номер WO 2009/140320 описаны соединения, включая такие как (R)-N-(4-(3-аминопиперидин-1-ил)-5-бром-1H-пирроло[2,3-b]пиридин-3-ил)никотинамид (здесь и далее «Соединение 1») и (R)-N-(4-(3-аминопиперидин-1-ил)-5-бром-1H-пирроло[2,3-b]пиридин-3-ил)изобутирамид (здесь и далее «Соединение 2»), (R)-N-(5-бром-4-(3-(метиламино)пиперидин-1-ил)-1H-пирроло[2,3-b]пиридин-3-ил)никотинамид (здесь и далее «Соединение 3»), (R)-N-(4-(3-аминопиперидин-1-ил)-5-бром-1H-пирроло[2,3-b]пиридин-3-ил)-5-метилникотинамид (здесь и далее «Соединение 4»), (R)-N-(4-(3-аминопиперидин-1-ил)-5-бром-1H-пирроло[2,3-b]пиридин-3-ил)циклопропанкарбоксамид (здесь и далее «Соединение 5»), (R)-N-(4-(3-аминопиперидин-1-ил)-5-бром-1H-пирроло[2,3-b]пиридин-3-ил)-3-метилбутанамид (здесь и далее «Соединение 6») и (R)-N-(4-(3-аминопиперидин-1-ил)-5-бром-1H-пирроло[2,3-b]пиридин-3-ил)-2-циклопропилацетамид (здесь и далее «Соединение 7»). Соединения 1, 2, 3, 4, 5, 6 и 7 (вместе «ингибиторы '926 CHK1») представляют собой ингибиторы CHK1 для перорального применения. [0006] В Международной публикации номер WO 2009/151589 описаны ингибиторы СНК1 (здесь и далее «ингибиторы CHK1 заявки '589»). В Международной публикации номер WO 2009/151598 описаны ингибиторы CHK1 (здесь и далее «ингибиторы CHK1 заявки '598»).
[0007] Wee1-подобная протеинкиназа («WEE1») является тирозинкиназой. WEE1 инактивирована в нормальных клетках за счет фосфорилирования и разложения на фазе М. WEE1 отрицательно регулирует вход в митоз за счет фосфорилирования Cdc2 (Stathis, Anastaslos and Amit Oza, "Targeting Weel-like Protein Kinase To Treat Cancer." Drug News & Perspectives. 23(7) (2010) 425-429). Вход в митоз запускается действием CDC25, которая дефосфорилирует Cdc2. Ингибирование WEE1 может приводить к аннулированию G2/M и неконтролируемому входу в митоз, несмотря на повреждение ДНК. При неактивном чекпойнте G2/M клетки могут становиться более восприимчивыми к ДНК-повреждающим агентам. Также могут выживать и здоровые клетки с нормальным чекпойнтом G1/S.
[0008] Известны ингибиторы WEE1; например, в Международной публикации WO 2010/098367, Международной публикации WO 2010/067886, Международной публикации WO 2008/115742, Международной публикации WO 2008/115738, Международной публикации WO 2007/126122, Международной публикации WO 2007/126128, Международной публикации WO 2004/007499 и публикации заявки на патент США 2005/0037476.
[0009] Ингибиторы WEE1 включают MK-1775, PD-166285 (известный также как PD0166285) и PF-00120130.
[0010] Остается необходимость в способах лечения заболеваний, в частности, гиперпролиферативных заболеваний, таких как рак.
Сущность изобретения
[0011] Было обнаружено, что введение ингибитора CHK1 и ингибитора WEE1 в комбинации может быть полезным при лечении рака. Неожиданно, эта комбинация демонстрирует синергетический потенциал, обеспечивая более сильное действие такой комбинации, чем при введении любого ингибитора по отдельности.
[0012] В одном аспекте настоящего изобретения представлено применение ингибитора CHK1 в комбинации с ингибитором WEE1.
[0013] В другом аспекте настоящего изобретения представлено применение ингибитора CHK1 в комбинации с ингибитором WEE1 для лечения гиперпролиферативного заболевания, такого как рак.
[0014] В другом аспекте настоящего изобретения представлено применение ингибитора CHK1 для производства лекарственного средства для комплексного применения с ингибитором WEE1 при лечении гиперолиферативного заболевания, такого как рак.
[0015] В другом аспекте настоящего изобретения представлена фармацевтическая композиция, включающая ингибитор CHK1 и ингибитор WEE1.
[0016] В другом аспекте настоящего изобретения представлена фармацевтическая композиция для лечения или предупреждения гиперпролиферативного заболевания, такого как рак, включающая ингибитор CHK1 и ингибитор WEE1.
[0017] В другом аспекте настоящего изобретения представлен способ лечения или предупреждения гиперпролиферативного заболевания, такого как рак, который включает введение ингибитора CHK1 в комбинации с ингибитором WEE1.
[0018] В другом аспекте настоящего изобретения представлен способ лечения или предупреждения гиперпролиферативного заболевания, такого как рак, который включает введение ингибитора CHK1 в комбинации с ингибитором WEE1, где ингибитор CHK1 вводится в дозе, находящейся в диапазоне от биологически эффективной дозы до максимально переносимой дозы, и ингибитор WEE1 вводится в дозе, находящейся в диапазоне от биологически эффективной дозы до максимально переносимой дозы.
[0019] В другом аспекте настоящего изобретения представлен способ лечения или предупреждения гиперпролиферативного заболевания, такого как рак, включающий введение млекопитающему, нуждающемуся в таком лечении, эффективного количества ингибитора CHK1 в комбинации с эффективным количеством ингибитора WEE1.
[0020] В другом аспекте настоящего изобретения представлен набор, включающий ингибитор CHK1 и ингибитор WEE1.
[0021] В другом аспекте настоящего изобретения представлен набор, включающий ингибитор CHK1 и ингибитор WEE1 для применения в комбинации для лечения или предупреждения гиперпролиферативного заболевания, такого как рак.
[0022] В другом аспекте настоящего изобретения представлен набор, включающий отдельные контейнеры ингибитора CHK1 и ингибитора WEE1 для применения в комбинации для лечения или предупреждения гиперпролиферативного заболевания, такого как рак.
[0023] В другом аспекте настоящего изобретения представлен набор, включающий в одной упаковке фармацевтические композиции в отдельных контейнерах для применения в комбинации для лечения или предупреждения гиперпролиферативного заболевания, такого как рак, который включает в одном контейнере фармацевтическую композицию, включающую эффективное количество ингибитора CHK1, а во втором контейнере - фармацевтическую композицию, включающую эффективное количество ингибитора WEE1.
[0024]
Краткое описание фигур
[0025] На Фигуре 1 изображена клеточная жизнеспособность клеток HEL92.1.7 после обработки ингибитором CHK1.
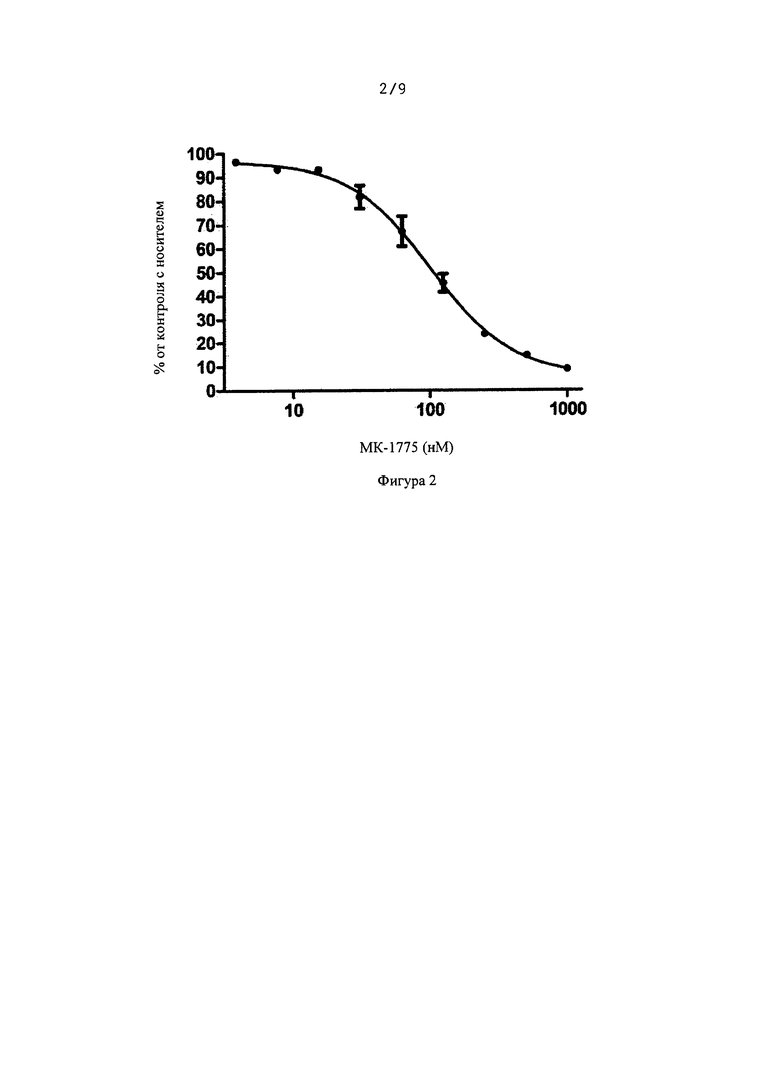
[0026] На Фигуре 2 изображена клеточная жизнеспособность клеток HEL92.1.7 после обработки ингибитором WEE1.
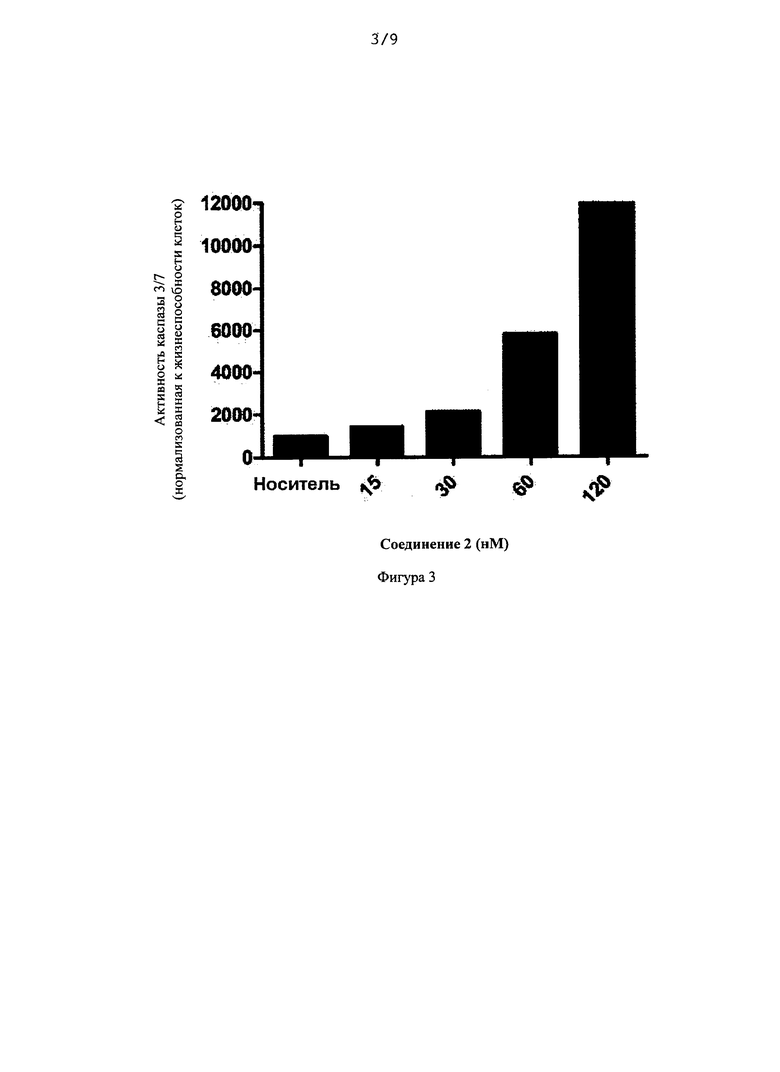
[0027] На Фигуре 3 изображена активность каспазы 3/7 после обработки ингибитором CHK1.
[0028] На Фигуре 4 изображена активность каспазы 3/7 после обработки ингибитором WEE1.
[0029] На Фигуре 5 изображен эксперимент по фосфорилированию Cdk2 по pY15.
[0030] На Фигуре 6 изображен эксперимент по фосфорилированию Cdc2 по pT14/Y15.
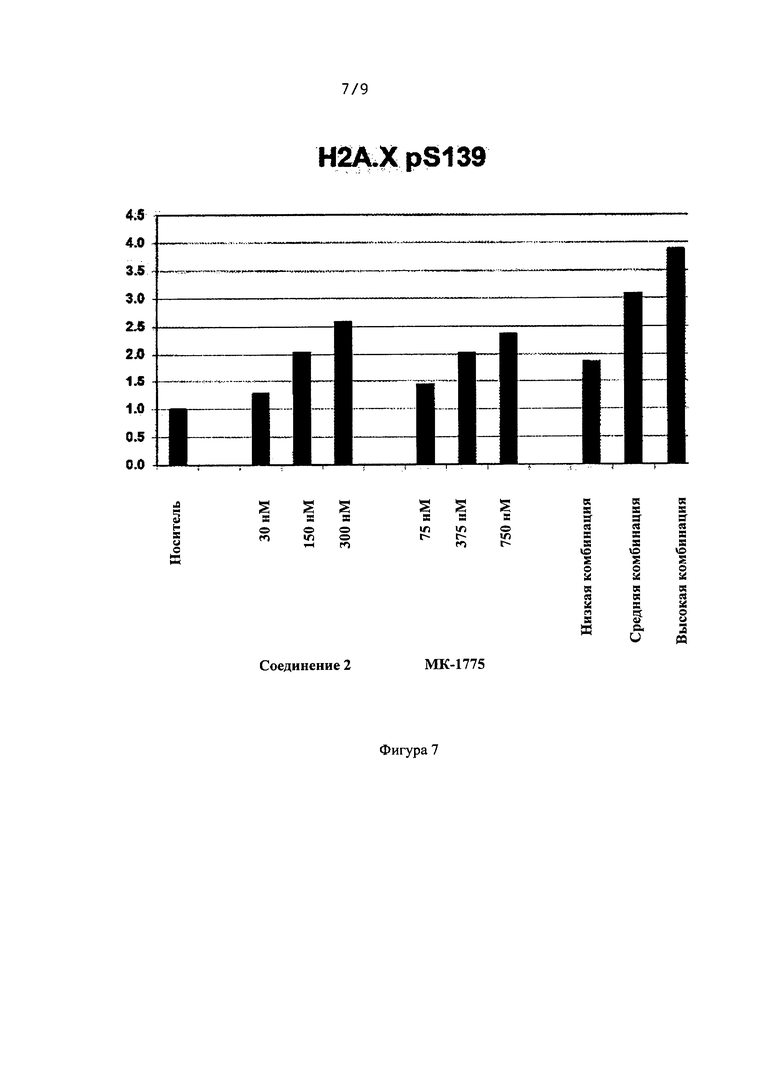
[0031] На Фигуре 7 изображен эксперимент по фосфорилированию Н2А.Х по pS139.
[0032] На Фигуре 8 изображен эксперимент по фосфорилированию СНК1 по pS345.
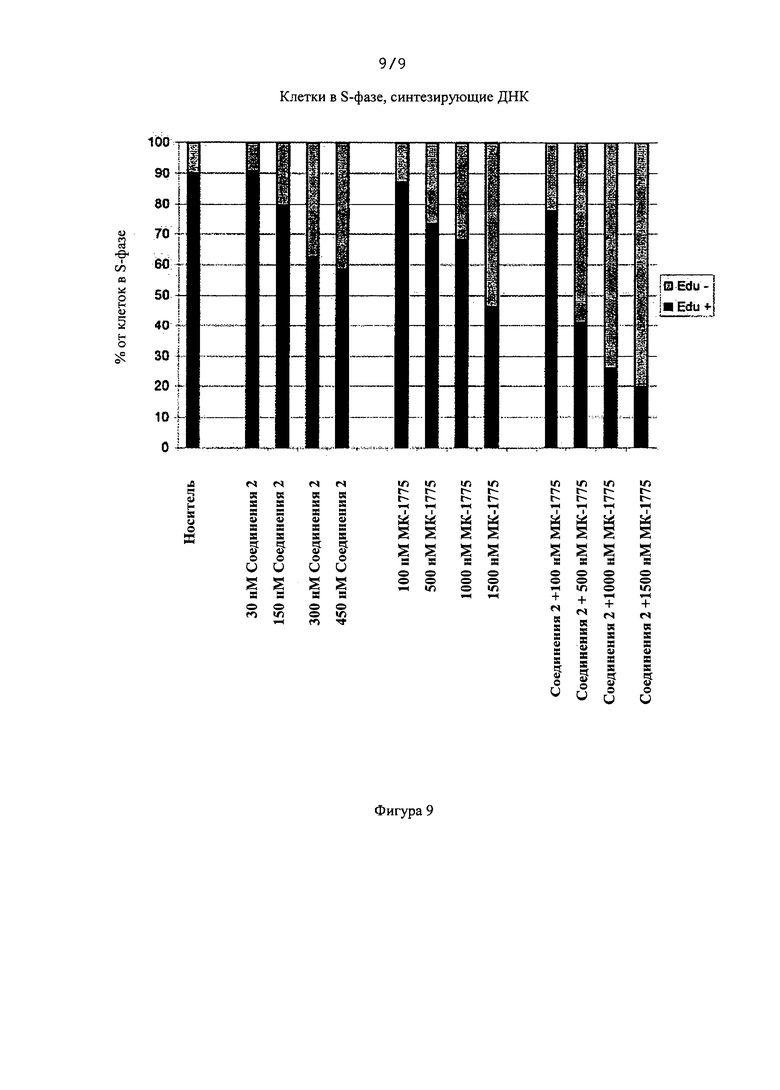
[0033] На Фигуре 9 изображен эксперимент по внедрению нуклеозида в клетки HEL92.1.7.
[0034]
Подробное описание изобретения
[0035] Ниже будут сделаны подробные ссылки на некоторые варианты настоящего изобретения. Несмотря на то, что настоящее изобретение будет описываться по нумерованным вариантам, следует понимать, что они не предназначены для ограничения настоящего изобретения до этих вариантов. Напротив, в настоящем изобретении сделана попытка охватить все варианты, модификации и эквиваленты, которые могут быть включены в рамки настоящего изобретения, как описано в формуле изобретения. Специалистам в данной области понятны многие способы и материалы, похожие или равноценные описанным в настоящем документе, которые могут использоваться при практическом осуществлении настоящего изобретения. Настоящее изобретение никоим образом не ограничивается описанными способами и материалами. В случае если один или несколько из включенных литературных источников и аналогичных материалов отличаются или противоречат настоящей заявке, включая, но не ограничиваясь этим, определенные термины, применение терминов, описанные методики или тому подобные, следует руководствоваться настоящей заявкой.
Определения
[0036] Термины «рак» и «раковый» относятся или описывают физиологическое состояние млекопитающего, обычно характеризующееся нерегулируемым клеточным ростом. Термин «опухоль» включает одну или несколько раковых клеток. Примеры рака включают, но не ограничиваясь этим, карциному, лимфому, бластому, саркому и лейкоз или лимфолейкоз. Более конкретные примеры таких раковых заболеваний включают плоскоклеточный рак (например, плоскоклеточный рак эпителиальных клеток), рак легких, включая мелкоклеточный рак легких, немелкоклеточный рак легких («NSCLC»), аденокарциному легких и плоскоклеточную карциному легких, рак брюшины, гепатоцеллюлярный рак, гастральный рак или рак желудка, включая гастроинтестинальный рак, рак поджелудочной железы, глиобластому, рак шейки матки, рак яичников, рак печени, рак мочевого пузыря, гепатому, рак груди, рак толстой кишки, рак прямой кишки, рак толстой и прямой кишок, эндометриальный рак или рак тела матки, карциному слюнной железы, почечный или ренальный рак, рак простаты, рак вульвы, рак щитовидной железы, рак печени, анальный рак, пенильный рак, рак кожи, включая меланому, а также рак головы и шеи.
[0037] Термин «млекопитающее» относится к теплокровному животному в состоянии заболевания или с риском развития заболевания, описанного в настоящем документе, и включает, но не ограничиваясь этим, морских свинок, собак, кошек, крыс, мышей, хомяков и приматов, включая человека.
[0038] Выражение «фармацевтически приемлемый» показывает, что вещество или композиция совместима химически и/или токсикологически с другими компонентами, входящими в состав композиции, и/или с организмом млекопитающего, подлежащим лечению.
[0039] Выражения «терапевтически эффективное количество» или «эффективное количество» означают такое количество соединения, описанного в настоящем документе, которое при введении млекопитающему, нуждающемуся в таком лечении, является достаточным для (i) лечения или предупреждения конкретного заболевания, состояния или нарушения, (ii) облегчения, улучшения или исключения одного или нескольких симптомов конкретного заболевания, состояния или нарушения, или (iii) предупреждения или отсрочки возникновения одного или нескольких симптомов конкретного заболевания, состояния или нарушения, описанного в настоящем документе. Количество соединения, которое соответствует такому количеству, варьируется в зависимости от факторов, таких как конкретное соединение, состояние заболевания и его степень, свойств (например, веса) млекопитающего, нуждающегося в лечении, но, тем не менее, может быть определено обычным способом специалистом в данной области. Эффективное количество может составлять биологически эффективное количество или превышать его, но быть на уровне максимально переносимой дозы или ниже ее. Эффективное количество может быть максимально переносимой дозой. В случае рака, эффективное количество ингибитора может снижать количество раковых клеток; уменьшать размер опухоли; ингибировать (то есть до некоторой степени замедлять и, предпочтительно, останавливать) инфильтрацию раковых клеток в периферийные органы; ингибировать (то есть до некоторой степени замедлять и, предпочтительно, останавливать) метастаз опухоли; до некоторой степени ингибировать рост опухоли; и/или до некоторой степени облегчать симптомы, связанные с раком. В той степени, в которой ингибитор может предотвращать рост и/или убивать существующие раковые клетки, он может быть цитостатическим и/или цитотоксическим. В случае противораковой терапии эффективность можно измерить, например, оценкой времени прогрессирования заболевания («ТТР») и/или определением частоты ответов («RR»).
[0040] Термины «лечить» или «лечение» относятся к терапевтическим, профилактическим, паллиативным или предупредительным мерам. Для целей настоящего изобретения, преимущественные или желаемые клинические результаты включают, но не ограничиваясь этим, облегчение симптомов, уменьшение распространения заболевания, стабилизацию (то есть отсутствие ухудшения) болезненного состояния, отсрочку или замедление прогрессирования заболевания, улучшение или ослабление болезненного состояния и ремиссию (частичную или полную), явные или не явные. «Лечение» также означает увеличение продолжительности жизни по сравнению с ожидаемой продолжительностью жизни без лечения. Те, кто нуждается в лечении, включают тех, кто уже страдает состоянием или заболеванием, а также тех, кто предрасположен к возникновению такого состояния или заболевания, или тех, у кого это состояние или заболевание необходимо предотвратить.
[0041]
Комбинация chk1 и wee1
[0042] В настоящем изобретении представлено применение ингибитора CHK1 в комбинации с ингибитором WEE1 при лечении гиперпролиферативного заболевания. В некоторых вариантах гиперпролиферативное заболевание является раком.
[0043] Использование контроля клеточного цикла является фундаментальной возможностью, от которой зависит рост клеток опухоли. Одним механизмом, по которому это может осуществляться, является управление чекпойнтами клеточного цикла и восстановлением повреждения ДНК. Существующие данные позволяют предположить, что клетки опухоли могут эволюционировать и становиться невосприимчивыми к химиотерапии за счет гиперактивации восстановления поврежденной ДНК в чекпойнте G2/M, клеточном процессе, зависящем от CHK1. Ингибирование CHK1 исключает этот путь выживания.
[0044] Киназа CHK1 участвует в активации чекпойнта клеточного цикла и восстановлении ДНК в ответ на повреждение ДНК. Соответственно, ингибиторы CHK1 обладают доклинической активностью в комбинации с ДНК-повреждающими агентами. Известно также, что CHK1 является решающей для прогрессирования клеточного цикла в невозмущенных клетках (то есть в отсутствие экзогенного повреждения ДНК), и ингибирование CHK1 действием одного агента является антипролиферативным в культивированных клеточных линиях рака in vitro (представлено в Примере 2 и на Фигурах 1 и 2). Был выполнен скрининг искусственной летальности с миРНК в комбинации с ингибитором CHK1. В ходе этого скрининга, выполненного в клеточных линиях РС3, LNCaP и А549, миРНК к киназе Wee1 демонстрируют способность усиливать антипролиферативное действие ингибитора CHK1 (представлено в Примере 1).
[0045] Следующие исследования были выполнены в клеточной линии HEL92.1.7. Было показано, что эта линия является восприимчивой к ингибированию CHK1 и к ингибированию WEE1 в отношении клеточной пролиферации (представлено в Примере 2 и на Фигурах 1 и 2). При смешивании ингибитора CHK1 и ингибитора WEE1 матричным образом наблюдался синергетический эффект (представлено в Примере 2). Комбинирование этих двух ингибиторов приводит примерно к четырехкратному усилению антипролиферативного действия по сравнению с действием, ожидаемым от простой аддитивности. Более того, оба ингибитора CHK1 и WEE1 вызывают апоптоз при введении в качестве единственных агентов (представлено в Примере 3 и на Фигурах 3 и 4). В корреляции с антипролиферативной синергией, комбинация этих ингибиторов приводит примерно к пятикратному усилению апоптоза по сравнению с апоптозом, ожидаемым от аддитивности (представлено в Примере 3).
[0046] Действие CHK1 приводит к сексвестрации и разрушению фосфатаз CDC25, ускоряя, таким образом, ингибирующее фосфорилирование CDK. Киназа Weel1 напрямую фосфорилирует CDK по тем же остаткам. Cdk2 и Cdc2 представляют собой CDK, которые, предположительно, принципиально контролируют развитие S-фазы и митотический вход, соответственно. Предполагается, что оба ингибитора CHK1 и WEE1 приводят к пониженному ингибирующему фосфорилированию Cdk2 и Cdc2, а их комбинация дополнительно уменьшает фосфорилирование (представлено в Примере 4 и на Фигурах 5 и 6). Так, комбинация ингибитора CHK1 и ингибитора WEE1 приводит к мощному де-ингибированию Cdk2 и Cdc2.
[0047] Было показано, что де-ингибирование CDK приводит к повреждению ДНК на S-фазе, вероятно, в результате де-регуляции первоначального возбуждения репликации ДНК (Beck, supra). В соответствии с этим, оба ингибитора CHK1 и WEE1 приводят к усилению фосфорилирования S139 Н2А.Х (биохимического маркера ДНК-повреждения), а комбинация этих ингибиторов дополнительно усиливает фосфорилирование (представлено в Примере 5 и на Фигуре 7). Повреждение ДНК приводит к активации чекпойнта клеточного цикла. В корреляции с наблюдаемым повреждением ДНК, оба ингибитора CHK1 и WEE1 увеличивают фосфорилирование S345 CHK1 (представлено в Примере 5 и на Фигуре 8). Более того, комбинация низких концентраций ингибитора CHK1 и ингибитора WEE1 приводит к усиленному фосфорилированию S345 CHK1.
[0048] Повреждение ДНК, связанное с де-ингибированием CDK, предположительно, является результатом коллапса репликативной вилки и/или преждевременного входа в митоз. Оба этих события приводят к ингибированию синтеза ДНК в S-фазе. В подтверждение этого, оба ингибитора CHK1 и WEE1 приводят к ингибированию синтеза ДНК в клетках S-фазы, и этот эффект усиливается при комбинировании ингибиторов (представлено на Фигуре 9).
[0049] В одном варианте представлено применение ингибитора СНК1 в комбинации с ингибитором WEE1.
[0050] В другом варианте представлено применение ингибитора CHK1 в комбинации с ингибитором WEE1 для лечения гиперпролиферативного заболевания, такого как рак. В следующем варианте это применение включает применение ДНК-повреждающего агента.
[0051] В другом варианте представлено применение фармацевтической композиции, включающей ингибитор CHK1, в комбинации с фармацевтической композицией, включающей ингибитор WEE1, для лечения гиперпролиферативного заболевания, такого как рак. В другом варианте представлено применение фармацевтической композиции, включающей эффективное количество ингибитора CHK1, в комбинации с фармацевтической композицией, включающей эффективное количество ингибитора WEE1, для лечения гиперпролиферативного заболевания, такого как рак. В следующем варианте это применение включает применение ДНК-повреждающего агента.
[0052] В другом варианте представлено применение ингибитора CHK1 для производства лекарственного средства для комплексного применения с ингибитором WEE1 при лечении гиперолиферативного заболевания, такого как рак.
[0053] В другом варианте представлена фармацевтическая композиция, включающая ингибитор CHK1 и ингибитор WEE1. В другом варианте представлена фармацевтическая композиция, включающая эффективное количество ингибитора CHK1 и эффективное количество ингибитора WEE1. В следующем варианте эта композиция включает также эффективное количество ДНК-повреждающего агента.
[0054] В другом варианте представлена фармацевтическая композиция для лечения или предупреждения гиперпролиферативного заболевания, такого как рак, включающая ингибитор CHK1 и ингибитор WEE1. В другом варианте представлена фармацевтическая композиция для лечения или предупреждения гиперпролиферативного заболевания, такого как рак, включающая эффективное количество ингибитора CHK1 и эффективное количество ингибитора WEE1. В следующем варианте эта композиция включает также эффективное количество ДНК-повреждающего агента.
[0055] В другом аспекте настоящего изобретения представлен способ лечения или предупреждения гиперпролиферативного заболевания, такого как рак, который включает введение ингибитора CHK1 в комбинации с ингибитором WEE1. В другом аспекте настоящего изобретения представлен способ лечения или предупреждения гиперпролиферативного заболевания, такого как рак, который включает введение эффективного количества ингибитора CHK1 в комбинации с эффективным количеством ингибитора WEE1. В следующем варианте этот способ включает также введение эффективного количества ДНК-повреждающего агента.
[0056] В другом варианте представлен способ лечения или предупреждения гиперпролиферативного заболевания, такого как рак, который включает введение ингибитора CHK1 в комбинации с ингибитором WEE1, где ингибитор CHK1 вводится в дозе, находящейся в диапазоне от биологически эффективной дозы до максимально переносимой дозы, а ингибитор WEE1 вводится в дозе, находящейся в диапазоне от биологически эффективной дозы до максимально переносимой дозы. В следующем варианте этот способ включает также введение эффективного количества ДНК-повреждающего агента.
[0057] В другом варианте представлен способ лечения или предупреждения гиперпролиферативного заболевания, такого как рак, включающий введение млекопитающему, нуждающемуся в таком лечении, эффективного количества ингибитора CHK1 в комбинации с эффективным количеством ингибитора WEE1. В следующем варианте этот способ включает также введение эффективного количества ДНК-повреждающего агента.
[0058] В одном варианте представлен набор, включающий ингибитор CHK1 и ингибитор WEE1. В следующем варианте этот набор включает также ДНК-повреждающий агент.
[0059] Набор может включать контейнер, содержащий такую комбинацию. Пригодные контейнеры включают, например, бутылки, пробирки, шприцы, блистерные упаковки и так далее. Контейнер может быть сделан из различных материалов, таких как стекло или пластик. В контейнере может содержаться комбинация, которая является эффективной для лечения определенного состояния, и может иметь стерильное входное отверстие (например, контейнер может представлять собой пакет с раствором для внутривенного введения или пробирку с пробкой, которую можно проткнуть иглой для подкожных инъекций).
[0060] Набор может дополнительно включать этикетку или рекламный вкладыш, наклеенный на контейнер или сопровождающий его. Термин «рекламный вкладыш» используется для обозначения инструкций, обычно входящих в товарные упаковки лекарственных средств, в которых содержится информация о показаниях, применении, дозировке, введении, противопоказаниях и/или мерах предосторожности, касающихся применения таких лекарственных средств. В одном варианте на этикетке или рекламных вкладышах указано, что композиция, включающая ингибитор CHK1 и/или ингибитор WEE1 может использоваться для лечения определенного нарушения. На этикетке или в рекламном вкладыше также может быть указано, что композиция может использоваться для лечения других нарушений.
[0061] В некоторых вариантах наборы пригодны для доставки твердых пероральных форм ингибитора CHK1 и ингибитора WEE1, таких как таблетки или капсулы. Такой набор предпочтительно включает несколько разовых доз. Такие наборы могут включать карточку, в которой дозы указаны в порядке их предназначенного применения. Примером такого набора является «блистерная упаковка». Блистерные упаковки хорошо известны в упаковочной промышленности и широко используются для упаковки фармацевтических разовых лекарственных форм. При необходимости может предоставляться также памятка, например, в виде номеров, букв или других обозначений, или с вложенным календарем, указывающим дни схемы лечения, в которые нужно вводить дозы.
[0062] В соответствии с другим вариантом, набор может включать (a) первый контейнер, в котором содержится ингибитор CHK1; и (b) второй контейнер, в котором содержится ингибитор WEE1. Альтернативно или дополнительно, набор может включать, помимо этого, третий контейнер, содержащий фармацевтически приемлемый буфер, такой как бактериостатическая вода для инъекций (BWFI), фосфатно-солевой буферный раствор, раствор Рингера и раствор декстрозы. Он может дополнительно включать другие материалы, необходимые с коммерческой и потребительской точки зрения, в том числе другие буферы, разбавители, фильтры, иглы и шприцы.
[0063] Набор может дополнительно включать инструкции по введению ингибитора CHK1 и ингибитора WEE1. Например, набор может дополнительно включать инструкции для одновременного, последовательного или раздельного введения ингибитора CHK1 и ингибитора WEE1 пациенту, нуждающемуся в этом.
[0064] В некоторых других вариантах набор может включать контейнер для хранения отдельных композиций, такой как секционная бутылка или секционный пленочный пакет, однако отдельные композиции могут также содержаться в одном, неразделенном контейнере. В некоторых вариантах набор включает инструкции по введению отдельных компонентов. Форма набора имеет особое преимущество в случае, если отдельные компоненты предпочтительно вводятся в различных лекарственных формах (например, перорально и парентерально), вводятся с различными интервалами дозировок или если предписанием врача или ветеринара предусмотрено капельное введение отдельных компонентов композиции.
[0065] В другом аспекте настоящего изобретения представлен набор, включающий отдельные контейнеры ингибитора CHK1 и ингибитора WEE1 для применения в комбинации для лечения или предупреждения гиперпролиферативного заболевания, такого как рак. В следующем варианте этот набор включает также ДНК-повреждающий агент.
[0066] В другом аспекте настоящего изобретения представлен набор, включающий в одной упаковке фармацевтические композиции в отдельных контейнерах для применения в комбинации для лечения или предупреждения гиперпролиферативного заболевания, такого как рак, который включает в одном контейнере фармацевтическую композицию, включающую эффективное количество ингибитора CHK1, а во втором контейнере - фармацевтическую композицию, включающую эффективное количество ингибитора WEE1. В следующем варианте этот набор включает также ДНК-повреждающий агент.
[0067] В другом варианте представлен набор, включающий:
(a) ингибитор СНК1 и
(b) ингибитор WEE1
для применения в комбинации для лечения или предупреждения гиперпролиферативного заболевания, такого как рак.
[0068] В другом варианте представлен набор, включающий:
(a) ингибитор СНК1,
(b) ингибитор WEE1 и
(c) ДНК-повреждающий агент
для применения в комбинации для лечения или предупреждения гиперпролиферативного заболевания, такого как рак.
[0069] В другом варианте представлен набор, включающий:
(a) фармацевтическую композицию, включающую ингибитор СНК1 и
(b) фармацевтическую композицию, включающую ингибитор WEE1
для применения в комбинации для лечения или предупреждения гиперпролиферативного заболевания, такого как рак.
[0070] В другом варианте представлен набор, включающий:
(a) фармацевтическую композицию, включающую ингибитор CHK1,
(b) фармацевтическую композицию, включающую ингибитор WEE1 и
(c) фармацевтическую композицию, включающую ДНК-повреждающий агент для применения в комбинации для лечения или предупреждения гиперпролиферативного заболевания, такого как рак.
[0071] В другом варианте представлен набор, включающий:
(a) фармацевтическую композицию, включающую эффективное количество ингибитора CHK1 и
(b) фармацевтическую композицию, включающую эффективное количество ингибитора WEE1
для применения в комбинации для лечения или предупреждения гиперпролиферативного заболевания, такого как рак.
[0072] В другом варианте представлен набор, включающий:
(a) фармацевтическую композицию, включающую эффективное количество ингибитора CHK1,
(b) фармацевтическую композицию, включающую эффективное количество ингибитора WEE1 и
(c) фармацевтическую композицию, включающую эффективное количество ДНК-повреждающего агента
для применения в комбинации для лечения или предупреждения гиперпролиферативного заболевания, такого как рак.
[0073] В некоторых вариантах настоящего изобретения ингибитор CHK1 выбран из группы, состоящей из ингибиторов '926 CHK1. В некоторых вариантах настоящего изобретения ингибитор CHK1 выбран из группы, состоящей из Соединения 1, Соединения 2, Соединения 3, Соединения 4, Соединения 5, Соединения 6 и Соединения 7. В некоторых вариантах настоящего изобретения ингибитором CHK1 является Соединение 1. В некоторых вариантах настоящего изобретения ингибитором CHK1 является Соединение 2. В некоторых вариантах настоящего изобретения ингибитором CHK1 является Соединение 3. В некоторых вариантах настоящего изобретения ингибитором CHK1 является Соединение 4. В некоторых вариантах настоящего изобретения ингибитором CHK1 является Соединение 5. В некоторых вариантах настоящего изобретения ингибитором CHK1 является Соединение 6. В некоторых вариантах настоящего изобретения ингибитором CHK1 является Соединение 7.
[0074] В некоторых вариантах настоящего изобретения ингибитор CHK1 выбран из группы, состоящей из ингибиторов '926 CHK1, PF-00477736, AZD7762, XL844, IC-83, CHIR-124, PD-321852, LY2603618, LY2606368 и SCH 900776. В некоторых вариантах настоящего изобретения ингибитор CHK1 выбран из группы, состоящей из PF-00477736, AZD7762, XL844, IC-83, CHIR-124, PD-321852, LY2603618, LY2606368 и SCH 900776. В некоторых вариантах настоящего изобретения ингибитор CHK1 выбран из группы, состоящей из ингибиторов '926 CHK1, PF-00477736, AZD7762, XL844, IC-83 и CHIR-124. В некоторых вариантах настоящего изобретения ингибитор CHK1 выбран из группы, состоящей из PF-00477736, AZD7762, XL844, IC-83 и CHIR-124. В некоторых вариантах ингибитор CHK1 исключает ингибиторы '926 CHK1.
[0075] В некоторых вариантах ингибитор CHK1 выбран из ингибиторов CHK1 заявки '589 и ингибиторов CHK1 заявки '598. В некоторых вариантах ингибитор CHK1 представляет собой ингибиторы CHK1 заявки '589. В некоторых вариантах ингибитор CHK1 представляет собой ингибиторы CHK1 заявки '598.
[0076] Пероральный ингибитор CHK1 является ингибитором CHK1, который можно вводить перорально. Если ингибитор CHK1 вводится перорально, он может быть составлен в композицию в форме пилюли, твердой или мягкой капсулы, таблетки, лепешки, водной или масляной суспензии, эмульсии, диспергируемых порошков или гранул, сиропа, эликсира и так далее, с фармацевтически приемлемым носителем или формообразующим средством. Ингибиторы CHK1 '926 являются пероральными ингибиторами CHK1.
[0077] В некоторых вариантах настоящего изобретения ингибитор WEE1 выбран из группы, состоящей из МК-1775, PD-166285 и PF-00120130. В некоторых вариантах настоящего изобретения ингибитор WEE1 выбран из группы, состоящей из МК-1775 и PD-166285. В некоторых вариантах настоящего изобретения ингибитор WEE1 представляет собой МК-1775. В некоторых вариантах настоящего изобретения ингибитор WEE1 представляет собой PD-166285. В некоторых вариантах настоящего изобретения ингибитор WEE1 представляет собой PF-00120130.
[0078] Пероральный ингибитор WEE1 является ингибитором WEE1, который можно вводить перорально. Если ингибитор WEE1 вводится перорально, он может быть составлен в композицию в форме пилюли, твердой или мягкой капсулы, таблетки, лепешки, водной или масляной суспензии, эмульсии, диспергируемых порошков или гранул, сиропа, эликсира и так далее, с фармацевтически приемлемым носителем или формообразующим средством. МК-1775 является пероральным ингибитором WEE1.
[0079] Ингибиторы CHK1 и WEE1 могут вводиться до, одновременно или после введения друг друга. Последовательное введение каждого агента может осуществляться через короткий или более длительный промежуток времени.
[0001] Как правило, ингибиторы CHK1 и WEE1 отдельно составляются в композиции смешиванием при комнатной температуре при соответствующем pH и при заданной степени чистоты с физиологически приемлемыми носителями, то есть с носителями, которые не являются токсичными для реципиентов в дозировках и концентрациях, используемых в галеновых формах введения. pH композиции зависит, в основном, от конкретного применения и концентрации соединения, но может находиться в любом диапазоне от около 3 до около 8. Композиция в ацетатном буфере при pH 5 представляет собой приемлемый вариант. В одном варианте, композиции, включающие соединения настоящего изобретения, являются стерильными. Соединения обычно хранятся в виде твердой композиции, хотя приемлемыми являются лиофилизированные композиции или водные растворы.
[0002] Композиции, включающие ингибиторы CHK1 и WEE1, составляются, дозируются и вводятся таким образом, который согласуется с надлежащей медицинской практикой. В этом контексте следует учитывать такие факторы как конкретное нарушение, подлежащее лечению, конкретное млекопитающее, подлежащее лечению, клиническое состояние индивидуального пациента, причина нарушения, место введения, способ введения, схема введения и другие факторы, известные практикующим врачам.
[0003] Ингибиторы могут вводиться в любой удобной форме введения, например, таблетках, порошках, капсулах, растворах, дисперсиях, суспензиях, сиропах, спреях, суппозиториях, гелях, эмульсиях, пластырях и так далее. Такие композиции могут содержать соединения, обычно применяемые в фармацевтических препаратах, например, разбавители, носители, модификаторы pH, подсластители, наполнители и дополнительные активные агенты. При необходимости парентерального введения соединения должны быть стерильными и в форме раствора или суспензии, пригодной для инъекции или инфузии.
[0004] Как правило, первоначальное фармацевтически эффективное количество ингибитора, вводимого парентерально, на одну дозу находится в диапазоне около 0,01-100 мг/кг/день, например, от около 0,1 до 20 мг/кг веса тела пациента в день, со стандартным первоначальным диапазоном используемого соединения-ингибитора, составляющим от 0,3 до 15 мг/кг/день. Пероральные разовые лекарственные дозы, такие как таблетки и капсулы, могут содержать от около 25 до около 1000 мг ингибитора.
[0005] Ингибиторы CHK1 и WEE1 могут индивидуально вводиться любым подходящим способом, включая пероральное, сублингвальное, буккальное, локальное, трансдермальное, парентеральное, подкожное, внутрибрюшинное, внутрилегочное и интраназальное, и, при необходимости местного лечения, внутриочаговое введение. Парентеральные инфузии включают внутримышечное, внутривенное, внутриартериальное, внутрибрюшинное или подкожное введение. Примером подходящей пероральной лекарственной формы является таблетка, содержащая около 25 мг, 50 мг, 100 мг, 250 мг или 500 мг соединения, смешанного с 90-30 мг безводной лактозы, около 5-40 мг кроскармеллозы натрия, около 5-30 мг поливинилпирролидона («РУР») К30 и около 1-10 мг стеарата магния. Порошковые компоненты сначала смешиваются вместе, а затем смешиваются с раствором PVP. Полученную композицию можно высушить, гранулировать, смешать со стеаратом магния и спрессовать в форму таблетки при помощи стандартного оборудования. Аэрозольная композиция может быть получена растворением ингибитора, например, 5-400 мг, в соответствующем буферном растворе, например, фосфатном буфере, с добавлением, при необходимости, регулятора тоничности, например, соли, такой как хлорид натрия. Раствор обычно фильтруется, например, с использованием 0,2-микронного фильтра, для удаления примесей и загрязнителей.
[0080] Другую композицию можно получить смешиванием ингибитора и носителя или формообразующего средства. Соответствующие носители и формообразующие средства хорошо известны специалистам в данной области и подробно описаны, например, в книгах Ansel, Howard С, et al., Ansel's Pharmaceutical Dosage Forms and Drug Delivery Systems. Philadelphia: Lippincott, Williams & Wilkins, 2004; Gennaro, Alfonso R., et al. Remington: The Science and Practice of Pharmacy. Philadelphia: Lippincott, Williams & Wilkins, 2000; и Rowe, Raymond C. Handbook of Pharmaceutical Excipients. Chicago, Pharmaceutical Press, 2005. Композиции могут также включать один или несколько буферов, стабилизаторов, поверхностно-активных веществ, увлажняющих агентов, смазывающих агентов, эмульгаторов, суспендирующих средств, консервантов, антиоксидантов, матирующих средств, глидантов, технологических добавок, красителей, подсластителей, отдушек, ароматизаторов, разбавителей и других известных добавок для получения простых форм лекарства (то есть ингибитора CHK1 и/или ингибитора CHK1, или их фармацевтической композиции) или добавки в производстве фармацевтического продукта (то есть лекарственного средства).
[0081] Ингибитор CHK1 и ингибитор WEE1 должны дозироваться, по меньшей мере, в таком количестве, чтобы обеспечивать заданный биологический эффект. Так, эффективный режим дозирования является дозой, которая, по меньшей мере, является минимальным количеством для достижения заданного биологического эффекта, или биологически эффективной дозой.
[0082] Однако доза не должна быть настолько высокой, чтобы неприемлемые побочные эффекты превышали преимущество биологического действия. Поэтому эффективный режим дозирования является дозой, не превышающей максимально переносимую дозу («MTD»). Максимально переносимая доза определяется как наивысшая доза, вызывающая приемлемый коэффициент дозолимитирующей токсичности («DLT»). Дозы, вызывающие неприемлемый коэффициент DLT, считаются непереносимыми. Как правило, MTD для определенного режима определяется на 1 фазе клинических испытаний. Они обычно проводятся у пациентов, начиная с безопасной первоначальной дозы, составляющей 1/10 от тяжелой токсической дозы («STD10») грызунов (в пересчете на мг/м2), и продолжая наращиванием в группах по три пациента, с увеличением дозы в соответствии с модифицированной последовательностью Фибоначчи, в которой чем выше этап увеличения, тем ниже относительное наращивание (например, доза увеличивается на 100%, 65%, 50%, 40% и далее 30%-35%). Увеличение дозы продолжается в группах по три пациента до достижения непереносимой дозы. Следующий более низкий уровень дозы, вызывающий приемлемый коэффициент DLT, считается MTD.
[0083] Также MTD варьируется в зависимости от конкретного ингибитора, вида и режима введения. Например, введение только на первый день, по сравнению с введением на первый и второй день, по сравнению с циклами дозирования «день через три» в течение семи, четырнадцати, двадцати одного или двадцати восьми дней, могут иметь различные значения MTD. Также дозирование только ингибитора CHK1 или в комбинации с ДНК-повреждающим агентом, могут иметь различные MTD, как и в случае дозирования ингибитора CHK1 в комбинации с ингибитором WEE1. Также дозирование только ингибитора WEE1 или в комбинации с ДНК-повреждающим агентом, могут иметь различные MTD, как и в случае дозирования ингибитора WEE1 в комбинации с ингибитором CHK1. Однако, как рассмотрено выше, в эффективных режимах введения необходимо дозировать ингибитор достаточно высоко, чтобы он был биологически эффективным. Дозирование только на первый день может обеспечить биологически эффективную дозу, но оно может быть недостаточно продолжительным для предотвращения восстановления ДНК поврежденных клеток. Альтернативно, дозирование «день через три» может обеспечить достаточно продолжительное действие, но может не давать достаточно высокой дозы для достижения биологически эффективной дозы. Это может быть результатом того, что MTD при дозировании в течение трех дней ниже, чем биологически эффективная доза. Следовательно, эффективный режим дозирования имеет MTD, равный или выше, чем биологически эффективная доза. Обычно при лечении рака пациентам вводят определенное соединение при его MTD, чтобы достичь максимальной пользы от лечения.
[0084] В одном варианте настоящего изобретения заданным биологическим эффектом ингибитора CHK1 является 80% или выше ингибирование pCHK1. В другом варианте настоящего изобретения заданным биологическим эффектом ингибитора CHK1 является 80% или выше ингибирование pCHK1 после введения ДНК-повреждающего агента (по сравнению с введением только ДНК-повреждающего агента).
[0085] В другом варианте настоящего изобретения заданным биологическим эффектом ингибитора CHK1 является 90% или выше ингибирование pCHK1. В другом варианте настоящего изобретения заданным биологическим эффектом ингибитора CHK1 является 90% или выше ингибирование pCHK1 после введения ДНК-повреждающего агента (по сравнению с введением только ДНК-повреждающего агента).
[0086] В другом варианте настоящего изобретения заданным биологическим эффектом ингибитора CHK1 является 95% или выше ингибирование pCHK1. В другом варианте настоящего изобретения заданным биологическим эффектом ингибитора CHK1 является 95% или выше ингибирование pCHK1 после введения ДНК-повреждающего агента (по сравнению с введением только ДНК-повреждающего агента).
[0087] В другом варианте настоящего изобретения заданным биологическим эффектом ингибитора CHK1 является 66% или выше ингибирование p-cdc2. В другом варианте настоящего изобретения заданным биологическим эффектом ингибитора CHK1 является 66% или выше ингибирование p-cdc2 после введения ингибитора WEE1 (по сравнению с введением только ингибитора WEE1). В другом варианте настоящего изобретения заданным биологическим эффектом ингибитора СНК1 является 66% или выше ингибирование p-cdc2 после введения ДНК-повреждающего агента (по сравнению с введением только ДНК-повреждающего агента).
[0088] В одном варианте настоящего изобретения заданным биологическим эффектом ингибитора WEE1 является 80% или выше ингибирование p-cdc2. В другом варианте настоящего изобретения заданным биологическим эффектом ингибитора WEE1 является 80% или выше ингибирование p-cdc2 после введения ДНК-повреждающего агента (по сравнению с введением только ДНК-повреждающего агента).
[0089] В другом варианте настоящего изобретения заданным биологическим эффектом ингибитора WEE1 является 90% или выше ингибирование p-cdc2. В другом варианте настоящего изобретения заданным биологическим эффектом ингибитора WEE1 является 90% или выше ингибирование p-cdc2 после введения ДНК-повреждающего агента (по сравнению с введением только ДНК-повреждающего агента).
[0090] В другом варианте настоящего изобретения заданным биологическим эффектом ингибитора WEE1 является 95% или выше ингибирование p-cdc2. В другом варианте настоящего изобретения заданным биологическим эффектом ингибитора WEE1 является 95% или выше ингибирование p-cdc2 после введения ДНК-повреждающего агента (по сравнению с введением только ДНК-повреждающего агента).
[0091] В другом варианте настоящего изобретения заданным биологическим эффектом ингибитора WEE1 является 66%» или выше ингибирование p-cdc2. В другом варианте настоящего изобретения заданным биологическим эффектом ингибитора WEE1 является 66% или выше ингибирование p-cdc2 после введения ингибитора CHK1 (по сравнению с введением только ингибитора CHK1). В другом варианте настоящего изобретения заданным биологическим эффектом ингибитора WEE1 является 66% или выше ингибирование p-cdc2 после введения ДНК-повреждающего агента (по сравнению с введением только ДНК-повреждающего агента).
[0092] В одном варианте ингибитор CHK1 вводится в дозе, равной или находящейся в диапазоне между биологически эффективной дозой и максимально переносимой дозой ингибитора. В одном варианте ингибитор СНК1 вводится в максимально переносимой дозе ингибитора.
[0093] В одном варианте ингибитор WEE1 вводится в дозе, равной или находящейся в диапазоне между биологически эффективной дозой и максимально переносимой дозой ингибитора. В одном варианте ингибитор WEE1 вводится в максимально переносимой дозе ингибитора.
[0094] Опубликованы некоторые данные для MTD МК-1775 в комбинации с гемцитабином, карбоплатином и цисплатином (Leijen, S., et al. "A phase I pharmacological and pharmacodynamic study of MK-1775, a Weel tyrosine kinase inhibitor, in monotherapy and combination with gemcitabine, cisplatin, or carboplatin in patients with advanced solid tumors". J. Clin. Oncol. 28:15s (2010) (доп.; реф. 3067); 2010 ASCO Annual Meeting, and Schellens, J.H., et al. "A phase I and pharmacological study of MK-1775, a Weel tyrosine kinase inhibitor, in both monotherapy and in combination with gemcitabine, cisplatin, or carboplatin in patients with advanced solid tumors". J. Clin. Oncol. 27:15s (2009) (доп.; реф. 3510); 2009 ASCO Annual Meeting). MTD однократной дозы МК-1775 в комбинации с гемцитабином (1000 мг/м2) указана как 200 мг. MTD однократной дозы МК-1775 в комбинации с цисплатином (75 мг/м2) указана как 200 мг. MTD однократной дозы МК-1775 в комбинации с карбоплатином (AUC 5) указана как 325 мг. MTD многократной дозы МК-1775 (дважды в день на 1 день, дважды в день на 2 день и 1 раз на 3 день) в комбинации с гемцитабином (1000 мг/м2) указана как 50 мг дважды в день на 1 день, 25 мг дважды в день на 2 день и 25 мг 1 раз на 3 день. MTD многократной дозы МК-1775 (5 доз дважды в день) в комбинации с цисплатином (75 мг/м2) указана как 125 мг, при продолжающихся испытаниях. MTD многократной дозы МК-1775 (5 доз дважды в день) в комбинации с карбоплатином (AUC 5) указана как 225 мг, при продолжающихся испытаниях.
[0095] В некоторых вариантах настоящего изобретения дозы ингибитора CHK1 и/или WEE1 могут быть разделены на два или более дневных введения (то есть дозирование BID означает дважды в день). Многократные введения могут быть разбиты на весь день. Они могут включать также многократные введения в течение нескольких дней.
[0096] В некоторых вариантах настоящего изобретения представлено применение композиции для лечения рака. В некоторых вариантах настоящего изобретения представлен способ лечения рака. Более конкретно, раковые заболевания, которые можно лечить композициями и способами настоящего изобретения, включают, но не ограничиваясь этим: раковые заболевания мягких тканей: саркому (ангиосаркому, фибросаркому, рабдомиосаркому, липосаркому), миксому, рабдомиому, фиброму, липому и тератому; легких: бронхогенную карциному (плоскоклеточную, недифференцированную мелкоклеточную, недифференцированную крупноклеточную, аденокарциному), альвеолярную (бронхиолярную) карциному, бронхиальную аденому, саркому, лимфому, хондроматозную гамартому, мезотелиому; желудочно-кишечные: пищевода (плоскоклеточную карциному, аденокарциному, лейомиосаркому, лимфому), желудка (карциному, лимфому, лейомиосаркому), поджелудочной железы (дуктальную аденокарциному, инсулиному, глюкагоному, гастриному, карциноидные опухоли, випому), тонкого кишечника (аденокарциному, лимфому, карциноидные опухоли, саркому Капоши, лейомиому, гемангиому, липому, нейрофиброму, фиброму), толстого кишечника (аденокарциному, тубулярную аденому, ворсинчатую аденому, гамартому, лейомиому); мочеполовой системы: почек (аденокарциному, опухоль Вильмса [нефробластому], лимфому, лейкоз), мочевого пузыря и уретры (плоскоклеточную карциному, транзиторно-клеточную карциному, аденокарциному), предстательной железы (аденокарциному, саркому), семенников (семиному, тератому, эмбриональную карциному, тератокарциному, хориокарциному, саркому, интерстициально-клеточную карциному, фиброму, фиброаденому, аденоматоидные опухоли, липому); печени: гепатому (гепатоцеллюлярную карциному), холангиокарциному, гепатобластому, ангиосаркому, гепатоцеллюлярную аденому, гемангиому; костей: остеогеную саркому (остеосаркому), фибросаркому, злокачественную фиброзную гистиоцитому, хондросаркому, саркому Юинга, злокачественную лимфому (ретикуло-клеточную саркому), множественную миелому, злокачественную гигантоклеточную хордому, остеохронфрому (костно-хрящевые экзостозы), доброкачественную хондрому, хондробластому, хондромиксофиброму, остеоидную остеому и гигантоклеточные опухоли; нервной системы: черепа (остеому, гемангиому, гранулему, ксантому, деформирующий остоз), мозговых оболочек (менингиому, менингиосаркому, глиоматоз), головного мозга (астроцитому, медулобластому, глиому, эпендимому, герминому [пинеалому], мультиформную глиобластому, олигодендроглиому, шванному, ретинобластому, врожденные опухоли), нейрофиброму спинного мозга, менингиому, глиому, саркому); гинекологические: матки (эндометриальную карциному), шейки матки (цервикальную карциному, предопухолевую цервикальную дисплазию), яичников (карциному яичников [серозную цистаденокарциному, муцинозную цистаденокарциному, неклассифицированную карциному], гранулоза-текально-клеточные опухоли, опухоли из сертоли-лейдиговских клеток, дисгерминому, злокачественная тератома), вульвы (плоскоклеточную карциному, интраэпителиальную карциному, аденокарциному, фибросаркому, меланому), влагалища (паренхиматозно-клеточную карциному, плоскоклеточную карциному, ботриоидную саркому (эмбриональную рабдомиосаркому), фаллопиевых труб (карциному); гематологические: крови и костного мозга (миелоидный лейкоз [острый и хронический], острый лимфобластный лейкоз, хронический лимфоцитарный лейкоз, миелопролиферативные заболевания, множественную миелому, миелодиспластический синдром), болезнь Ходжкина, неходжкинскую лимфому [злокачественную лимфому]; кожи: злокачественную меланому, базально-клеточную карциному, плоскоклеточную карциному, саркому Капоши, невоидные опухоли, липому, ангиому, дерматофиброму, келоиды, псориаз; и надпочечников: нейробластому. Термин «раковая клетка», представленный в настоящем документе, включает клетки, пораженные любым из указанных выше состояний.
[0097] В некоторых вариантах настоящего изобретения рак выбран из рака толстой и прямой кишок (включая мутации Ras), мелкоклеточного рака легких, немелкоклеточного рака легких, глиомы, рака яичников, метастатического рака молочной железы, рака поджелудочной железы, гепатобилиарного рака (включая гепатоцеллюлярный рак, рак внепеченочных желчных протоков и холангиокарциному), рака желудка, рака семенников, плоскоклеточного рака головы и шеи, лейкоза (включая острый миелоидный лейкоз, острый лимфобластный лейкоз, хронический миелоидный лейкоз и хронический лимфоидный лейкоз), лимфомы (включая лимфому мантийных клеток, лимфому Ходжкина и неходжкинскую лимфому) и рака простаты.
[0098] В некоторых вариантах настоящего изобретения рак является раком с солидной опухолью.
[0099] В некоторых вариантах настоящего изобретения рак выбран из рака поджелудочной железы, рака яичников и рака толстой и прямой кишок.
[00100] В некоторых вариантах настоящего изобретения рак выбран из рака толстой и прямой кишок (включая мутации Ras), мелкоклеточного рака легких, немелкоклеточного рака легких и глиомы.
[00101] В некоторых вариантах настоящего изобретения рак выбран из немелкоклеточного рака легких, рака яичников, метастатического рака молочной железы, рака поджелудочной железы, гепатобилиарного рака (включая гепатоцеллюлярный рак, рак внепеченочных желчных протоков и холангиокарциному) и рака желудка.
[00102] В некоторых вариантах настоящего изобретения рак выбран из рака толстой и прямой кишок (включая мутации Ras), мелкоклеточного рака легких, немелкоклеточного рака легких, рака яичников, гепатобилиарного рака (включая гепатоцеллюлярный рак, рак внепеченочных желчных протоков и холангиокарциному), рака желудка, рака семенников и плоскоклеточной карциномы головы и шеи.
[00103] В некоторых вариантах настоящего изобретения рак выбран из лейкоза (включая острый миелоидный лейкоз, острый лимфобластный лейкоз, хронический миелоидный лейкоз и хронический лимфоидный лейкоз), лимфомы (включая лимфому мантийных клеток, лимфому Ходжкина и неходжкинскую лимфому) и рака простаты.
[00104] В некоторых вариантах комбинация дополнительно включает сочетание с ДНК-повреждающим агентом. ДНК-повреждающие агенты включают Gemzar® (гемцитабин), Camptosar® (иринотекан или СРТ-11), Temodar® (темозоломид), Xeloda® (капецитабин), Hycamtin® (топотекан), цисплатин, Eloxatin® (оксалиплатин), Paraplatin® (карбоплатин), камптотецин, ara-С (цитарабин), 5-FU (фторурацил), Cytoxan® (циклофосфамид), Etopophos® или Vepesid® (этопозид фосфат), Vumon® (тенипозид), Adriamycin PFS® или Adriamycin RDF® (доксорубицин), даунорубицин, Alimta® (пеметрексед), и радиацию. В некоторых вариантах ДНК-повреждающий агент выбран из группы, состоящей из гемцитабина, иринотекана, темозоломида, капецитабина, камптотецина, цисплатина, ara-С и 5-FU. В некоторых вариантах ДНК-повреждающий агент выбран из гемцитабина, иринотекана, темозоломида и капецитабина. В некоторых вариантах ДНК-повреждающий агент выбран из гемцитабина, иринотекана, цисплатина, оксалиплатина, карбоплатина и цитарабина. В некоторых вариантах ДНК-повреждающий агент выбран из гемцитабина и иринотекана. ДНК-повреждающий агент вводится в его одобренной или рекомендованной дозе. В одном варианте ДНК-повреждающий агент вводится в максимально переносимой дозе.
[00105] В некоторых вариантах ДНК-повреждающий агент выбран из группы, состоящей из цисплатина, оксалиплатина и карбоплатина.
[00106] В некоторых вариантах ДНК-повреждающим агентом является гемцитабин.
[00107] В дополнительном варианте ДНК-повреждающим агентом является цитарабин.
ПРИМЕРЫ
[00108] Для иллюстрации настоящего изобретения включены следующие Примеры. Однако следует понимать, что эти Примеры не ограничивают настоящее изобретение и подразумевают лишь способ практического осуществления настоящего изобретения.
Пример 1
миРНК к Wee1 усиливают антипролиферативную активность ингибитора Chk1
[00109] Скрининг искусственной летальности с использованием миРНК к 197 генам (3 миРНК на ген) выполнили в клеточных линиях РС3, LNCaP (2 независимых эксперимента) и А549. Клетки обратно трансфицировали с миРНК в 96-луночных планшетах, обработанных на следующий день Соединением 2 или носителем, а затем анализировали анализом жизнеспособности с реагентом CellTiter Blue через три дня после обработки. Представленные данные являются результатами, полученными с 3 миРНК к киназе WEE1 (обозначены A, B и C). Значения представляют процент от контрольного значения, где контрольным значением является среднее всех значений для каждого отдельного планшета.
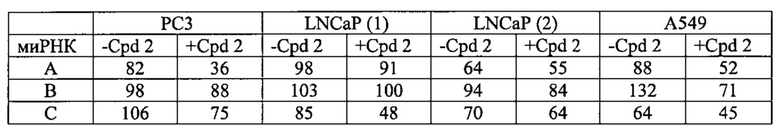
Пример 2
Комбинация ингибирования Chk1 и ингибирования Wee1 для ингибирования клеточной пролиферации
[00110] Клетки HEL92.1.7 поместили в 96-луночные планшеты, а затем обработали Соединением 2 или МК-1775 в качестве одиночных агентов. Через три дня обработки оценили клеточную жизнеспособность по анализу с CellTiter Blue (Promega). Данные представляют среднее значение±стандартная погрешность (n=5 для Соединения 2, n=2 для МК-1775). Значения IC50 составили 30 нМ для Соединения 2 и 103 нМ для МК-1775. Представлены на Фигурах 1 и 2. Клетки HEL92.1.7 поместили в 96-луночные планшеты, а затем обработали комбинациями Соединения 2 и МК-1775 матричным образом при указанных концентрациях. Через три дня обработки оценили клеточную жизнеспособность по анализу с CellTiter Blue. Указанное значение для каждой комбинации представляет коэффициент комбинации (фактическое значение, разделенное на ожидаемое значение при аддитивном действии соединений; ожидаемые значения представляют парциальные действия одиночных агентов, умноженные друг на друга, например, если каждый одиночный агент ингибирует рост на 50%, то ожидаемое значение составляет 0,5×0,5=0,25). Данные представляют среднее значение для двух независимых экспериментов (для каждого отдельного эксперимента усреднили планшеты в трех экземплярах).

Пример 3
Комбинация ингибирования Chk1 и ингибирования Wee1 для инициации апоптоза
[00111] Клетки HEL92.1.7 поместили на 96-луночные планшеты в двух экземплярах, а затем обработали Соединением 2 или МК-1775. Через 2 дня обработки один планшет анализировали анализом Caspase-Glo 3/7 (Promega), а другой - анализом с CellTiter Blue. Значения анализа Caspase-Glo 3/7 разделили на значения анализа с CellTiter Blue, чтобы нормализовать активность каспазы к аппроксимации количества клеток. Диаграммы представляют активацию каспазы 3/7 Соединением 2 и МК-1775 при обработке одиночными агентами (представлено на Фигурах 3 и 4). Соединение 2 и МК-1775 смешали матричным образом. Значения представляют фактические значения, разделенные на значения, ожидаемые при действии соединений аддитивным образом (ожидаемые значения являются парциальными эффектами одиночных агентов, умноженными друг на друга).

Пример 4
Ингибирование Chk1 и ингибирование Wee1 приводит к снижению ингибирующего фосфорилирования циклин-зависимых киназ
[00112] Клетки HEL92.1.7 обрабатывали Соединением 2, МК-1775 или их комбинациями (низкая комбинация = 30 нМ Соединения 2+75 нМ МК-1775, средняя комбинация = 150 нМ Соединения 2+375 нМ МК-1775, высокая комбинация=300 нМ Соединения 2+750 нМ МК-1775) в течение 8 часов. Затем лизаты клеток анализировали вестерн-блоттингом с использованием антител, специфичных к Cdk2, фосфорилированной по тирозину 15 (CDK2 pY15) и Cdc2, фосфорилированной по треонину 14 и тирозину 15 (Cdc2 pT14/Y15). Интенсивности полос нормализовали к контрольному образцу с загрузкой GAPDH. Записаны значения, нормализованные к контролю с носителем. Представлены на Фигурах 5 и 6.
Пример 5
Ингибирование Chk1 и ингибирование Wee1 приводит к увеличению биохимических маркеров повреждения DNA и активации чекпойнта клеточного цикла
[00113] Клетки HEL92.1.7 обрабатывали Соединением 2, МК-1775 или их комбинациями (низкая комбинация = 30 нМ Соединения 2+75 нМ МК-1775, средняя комбинация = 150 нМ Соединения 2+375 нМ МК-1775, высокая комбинация = 300 нМ Соединения 2+750 нМ МК-1775) в течение 8 часов. Затем лизаты клеток анализировали по вестерн-блоттингу, используя антитела, специфичные к Н2А.Х, фосфорилированной по серину 139 (Н2А.Х pS139) и Chk1, фосфорилированной по серину 345 (Chk1 р345). Интенсивности полос нормализовали к контрольному образцу с загрузкой GAPDH. Записаны значения, нормализованные к контролю с носителем. Представлены на Фигурах 7 и 8.
Пример 6
Ингибирование Chk1 и ингибирование Wee1 приводит к коллапсу репликации ДНК
[00114] Клетки HEL92.1.7 обрабатывали Соединением 2, МК-1775 или их комбинациями в течение 16 часов. Затем клетки анализировали при помощи набора для проточного цитометрического анализа Click-iT EdU (Invitrogen) по инструкциям производителя. Клетки с нарушенной репликацией ДНК определили по наличию содержания ДНК в S-фазе, но отрицательному окрашиванию для EdU. Представлено на Фигуре 9.
[00115] Несмотря на то, что настоящее изобретение описано по нумерованным вариантам, следует понимать, что они не предназначены для ограничения настоящего изобретения до этих вариантов. Напротив, в настоящем изобретении сделана попытка охватить все варианты, модификации и эквиваленты, которые могут быть включены в рамки настоящего изобретения, как описано в формуле изобретения. Следовательно, изложенное выше описание считается лишь иллюстративным для принципов настоящего изобретения.
[00116] Слова «включают», «включающий», «включая» и «включает», при использовании в настоящем описании и в следующей формуле изобретения, предназначены для указания наличия указанных свойств, целых чисел, компонентов или этапов, но они не исключают наличие или добавление одного или нескольких других свойств, целых чисел, компонентов, этапов или групп.





Группа изобретений относится к медицине, а именно к онкологии и может быть использована для ингибирования клеточной пролиферации и инициации апоптоза у человека. Для этого применяют ингибитор CHK1, представляющий собой (R)-N-(4-(3-аминопиперидин-1-ил)-5-бром-1Н-пирроло[2,3-b]пиридин-3-ил)изобутирамид, в комбинации с ингибитором WEE1, представляющим собой MK-1775. Группа изобретений обеспечивает режим дозирования, который является минимальным количеством для достижения заданного биологического эффекта без побочных эффектов. 2 н. и 2 з.п. ф-лы, 9 ил., 6 пр.
1. Применение ингибитора CHK1, представляющего собой (R)-N-(4-(3-аминопиперидин-1-ил)-5-бром-1Н-пирроло[2,3-b]пиридин-3-ил)изобутирамид, в комбинации с ингибитором WEE1, представляющим собой MK-1775, для ингибирования клеточной пролиферации.
2. Применение по п. 1 для ингибирования клеточной пролиферации клеток человека.
3. Применение ингибитора CHK1, представляющего собой (R)-N-(4-(3-аминопиперидин-1-ил)-5-бром-1Н-пирроло[2,3-b]пиридин-3-ил)изобутирамид, в комбинации с ингибитором WEE1, представляющим собой MK-1775, для инициации апоптоза.
4. Применение по п. 3 для инициации апоптоза клеток человека.
| WO2010118390 A1, 11.04.2009 | |||
| WO2005027907 A1, 31.03.2005 | |||
| HIRAI H., MK-1775, a small molecule Wee1 inhibitor, enhances anti-tumor efficacy of various DNA-damaging agents, including 5-fluorouracil, Cancer Biology & Therapy, 2010, 9, 7, pp | |||
| СПОСОБ ПОЛУЧЕНИЯ ПРОДУКТОВ КОНДЕНСАЦИИ ФЕНОЛОВ С ФОРМАЛЬДЕГИДОМ | 1925 |
|
SU514A1 |
| HARVEY S.L., Cdk1-Dependent Regulation of the Mitotic Inhibitor Wee1, Cell, 2005, 122, 3, pp | |||
| Ручная тележка для реклам | 1923 |
|
SU407A1 |
| MIZUARAI S., Discovery of gene expression-based pharmacodynamics biomarker for P53 context-specific anti-tumor drug WEE1 inhibitor, Mol | |||
| Cancer, 2009, 8, pp 34-46 найдено 11.11.2015 в Интернете [on-line] на сайте http://citeseerx.ist.psu.edu/viewdoc/download?doi=10.1.1.359.3464&rep=rep1&type=pdf. | |||
Авторы
Даты
2017-08-14—Публикация
2011-11-16—Подача