ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Изобретение относится к кристаллической форме дималеата ингибиторов тирозинкиназы, в частности к кристаллам формы I дималеата (R,Е)-N-(4-(3-хлор-4-(пиридин-2-ил-метокси)фениламино)-3-циано-7-этоксихинолин-6-ил)-3-(1-метилпирролидин-2-ил)акриламида, их получению и применению.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
За последние годы смертность от рака в нашей стране заметно возросла. Рак серьезно угрожает жизни и качеству жизни людей. Таким образом, на сегодняшний день приоритетной задачей и значимым предметом изысканий медико-биологических наук являются новые лекарственные средства для лечения онкологических заболеваний, обладающие высокой эффективностью и низкой токсичностью. Рецепторная тирозинкиназа представляет собой вид трансмембранного белка, вовлеченного в передачу сигнала. Показано, что более 50% продуктов протоонкогенов и онкогенов, аномальная экспрессия которых вызывает образование опухолей, обладают тирозинкиназной активностью. С 2001 ингибитор тирозинкиназы был одобрен для коммерческого использования, он стал представителем нового класса лекарственных средств для лечения онкологических заболеваний (противораковых) с выдающимися свойствами.
Рецептор эпидермального фактора роста (EGFR) является представителем семейства рецепторных тирозинкиназ. Каскад реакций рецептора эпидермального фактора роста играет очень важную роль в образовании и прогрессировании опухолей, указанный рецептор стал основным предметом исследований и одной из разрабатываемых мишеней в области лечения рака. Подобные лекарственные средства, которые сейчас уже присутствуют на рынке, включают эрлотиниб, гефитиниб и лапатиниб (тайкерб, GW572016), а также нератиниб, который сейчас находится в фазе клинических испытаний. В WO 2011029265 раскрыт способ получения соединения (R,E)-N-(4-(3-хлор-4-(пиридин-2-ил-метокси)фениламино)-3-циано-7-этоксихинолин-6-ил)-3-(1-метилпирролидин-2-ил)акриламида (в целях удобства обозначен ниже как SHR1258). Молекула этого лекарственного средства имеет явные преимущества в отношении фармакокинетики и фармакодинамики. Хотя в WO 2011029265 раскрыта химическая структура и способ получения соединения SHR1258, но указания об условиях перевода указанного соединения в соль отсутствуют. В китайской заявке на изобретение 201110062359,8 приведено описание дималеата этого соединения (обозначаемого ниже как дималеат SHR1258), и его структура соответствует следующей:
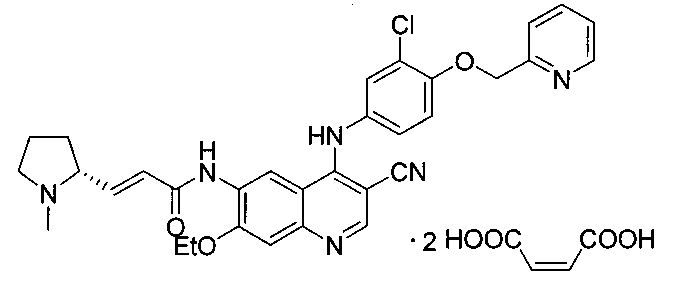
Тем не менее, авторы изобретения не проводили дополнительного исследования указанной полиморфной формы вещества и способа получения дималеата SHR1258. Как известно специалистам в данной области техники, полиморфная структура фармацевтически активного компонента всегда влияет на химическую стабильность лекарственного средства. Различные условия хранения и кристаллизации могут приводить к изменению в полиморфной структуре соединения, которое иногда сопровождается другими формами полиморфной формы вещества. В основном, аморфный лекарственный продукт не имеет регулярной кристаллической структуры, часто имеет другие недостатки, такие как низкая стабильность продукта, меньший размер частиц, затрудненная фильтрация, легкость образования агломератов и низкая текучесть. Таким образом, необходимо улучшать все параметры вышеуказанного продукта. Необходим поиск новой полиморфной формы вещества, которая обладает более высокой полиморфной чистотой и лучшей химической стабильностью.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Согласно настоящему изобретению предложена стабильная кристаллическая форма дималеата SHR1258 и способ ее получения.
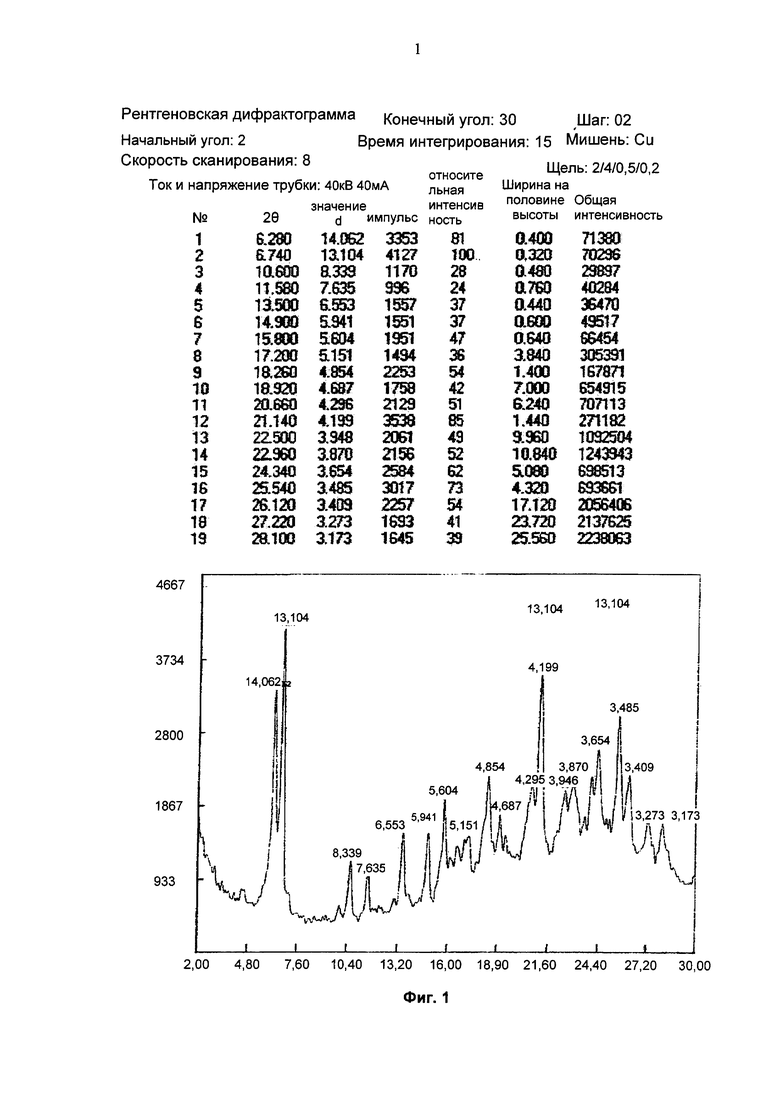
Автор изобретения протестировал серию продуктов кристаллизации дималеата SHR1258, полученных в разных условиях, методом рентгеновской дифрактограммы и в тесте дифференциальной сканирующей калориметрии (ДСК). Результаты подтвердили, что стабильная кристаллическая форма дималеата SHR1258, которая обозначена как кристаллы формы I, может быть получена при нормальных условиях кристаллизации. Изображения ДСК кристаллов формы I дималеата SHR1258 показывают отчетливый объединенный пик поглощения при 130°С. Рентгеновская дифрактограмма представлена на Фиг. 1 при использовании Cu-Kα излучения для получения рентгеновских дифрактограмм, представленных 2θ углами и межплоскостным расстоянием в кристаллах (значение d), на которой характеристическими пиками являются: 6,28 (14,06), 6,74 (13,10), 10,60 (8,34), 11,58 (7,64), 13,50 (6,55), 14,90 (5,94), 15,80 (5,60), 18,26 (4,85), 20,66 (4,30), 21,14 (4,20), 22,96 (3,87), 24,34 (3,65), 25,54 (3,49) и 26,12 (3,41).
Способ получения кристаллов формы I согласно настоящему изобретению не предполагает особых ограничений для существующей формы дималеата SHR1258 в качестве исходного материала, который может быть использован в любой кристаллической или аморфной форме. Способ получения кристаллов формы I дималеата SHR1258 согласно настоящему изобретению включает следующие стадии.
При использовании низкомолекулярных органических растворителей предпочтительно выбирают полярные органические растворители с малым числом углеродных атомов и высокой летучестью, которые могут быть использованы в качестве кристаллизующего растворителя, такие как спирты, кетоны, сложные эфиры или их смесь; для перекристаллизации дималеата SHR1258 более предпочтительны изопропиловый спирт, ацетон, этилацетат, тетрагидрофуран или их смесь. Растворитель для кристаллизации может быть одиночным растворителем или смесью растворителей, включающей вышеупомянутые растворители.
Более конкретно, способ получения кристаллов формы I дималеата SHR1258 включает следующие стадии:
(1) смесь SHR1258 и малеиновой кислоты или дималеата SHR1258 в твердом состоянии растворяют в достаточном количестве органических растворителей и полученный раствор охлаждают для кристаллизации;
(2) кристаллы фильтруют, промывают и высушивают.
Согласно предпочтительному варианту реализации настоящего изобретения органический растворитель стадии 1 выбирают из одного или более растворителя, включающего спирты с не более чем тремя углеродными атомами, ацетон, сложные этиловые эфиры, тетрагидрофуран, предпочтительно этанол, изопропиловый спирт, тетрагидрофуран.
Кроме того, наиболее предпочтительный одиночный растворитель представляет собой изопропиловый спирт.
Согласно еще одному варианту реализации настоящего изобретения предпочтительная смесь растворителей представляет собой смесь этанола и тетрагидрофурана. Соотношение двух указанных растворителей не ограничено, при этом согласно варианту реализации предпочтительно объемное соотношение 1:1.
Способ перекристаллизации не ограничен каким-либо определенным, и перекристаллизация может быть проведена обычными методами данной области техники, например, дималеат SHR1258 нагревают, чтобы растворить в органическом растворителе, а затем раствор оставляют постепенно охлаждаться для начала кристаллизации или раствор перемешивают, чтобы началась кристаллизация; после кристаллизации полученный в результате осадок собирают с помощью фильтрации и затем высушивают. В частности, необходим способ полного превращения для образования стабильной кристаллической формы, а когда процесс кристаллизации протекает слишком быстро, что обычно вызвано пересыщенным состоянием раствора, легко образуются аморфные структуры или кристаллы с более низкой растворимостью. Увеличение объема растворителя или снижение скорости кристаллизации будет способствовать образованию стабильной формы кристаллов высокой чистоты. Кристаллы, полученные с помощью фильтрации, обычно высушивают под вакуумом приблизительно при температуре от 30 до 100°С, предпочтительно при температуре от 40 до 60°С, чтобы удалить используемый для перекристаллизации растворитель.
Полученную кристаллическую форму дималеата SHR1258 определяют с помощью ДСК и рентгеновской дифрактограммы. При этом также определяют и остаточный растворитель.
Кристаллы дималеата SHR1258, полученные согласно настоящему способу, не содержат или содержат очень мало остаточного растворителя, что соответствует требованию государственной фармакопеи для остаточного растворителя в лекарственных средствах. Таким образом, кристаллы согласно настоящему изобретению могут быть надлежащим образом использованы в качестве активного фармацевтического компонента.
Результаты исследования показывают, что стабильность кристаллов формы I дималеата SHR1258, полученных согласно настоящему изобретению, значительно лучше, чем аморфной формы в условиях высокой температуры и высокой влажности. Кроме того, кристаллы формы I обладают хорошей стабильностью в условиях размалывания, давления и нагревания, что соответствует требованиям получения, транспортировки и хранения лекарственных средств. Заявленный способ получения стабилен и воспроизводим, что особенно хорошо подходит для промышленного производства.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
На Фиг. 1 представлена рентгеновская дифрактограмма для кристаллов формы I дималеата SHR1258.
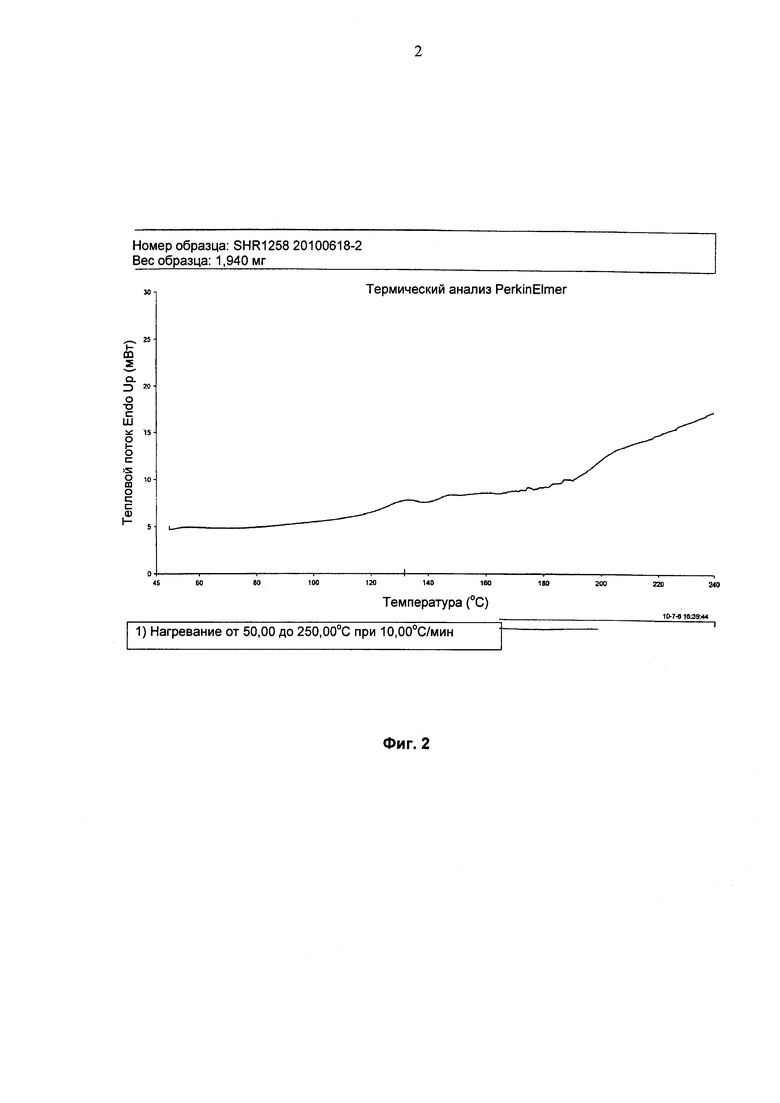
На Фиг. 2 представлено изображение дифференциальной сканирующей калориметрии для кристаллов формы I дималеата SHR1258.
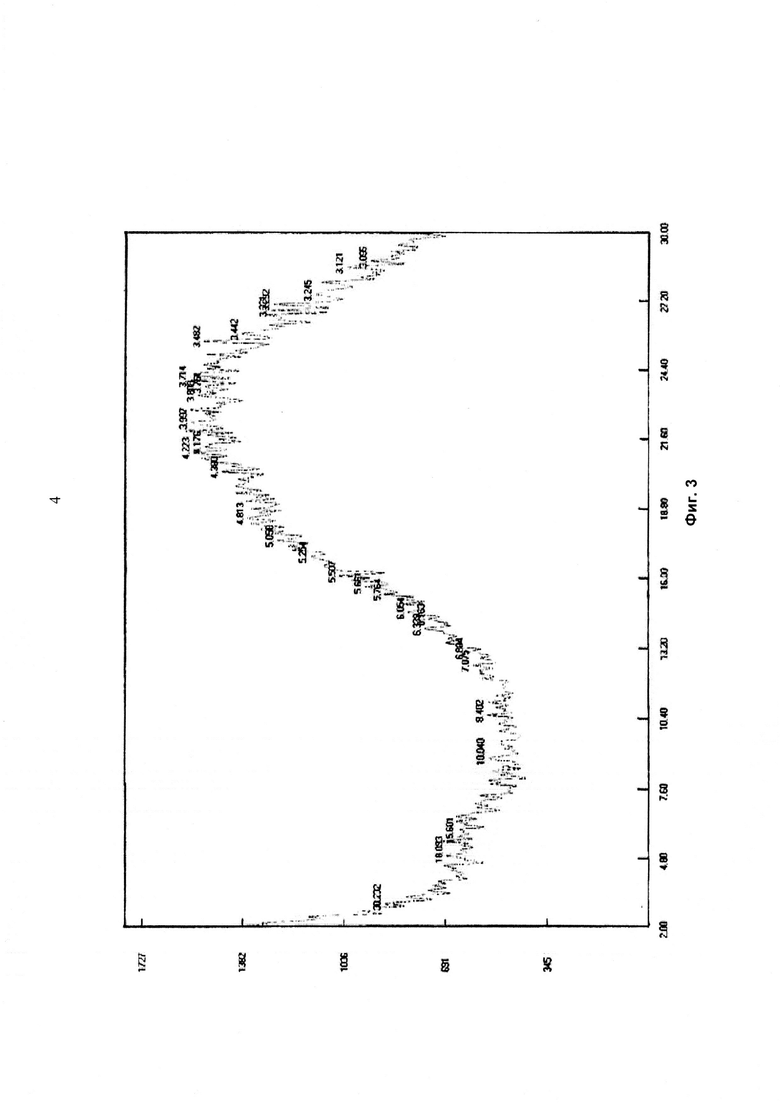
На Фиг. 3 представлена рентгеновская дифрактограмма для аморфной формы дималеата SHR1258.
На Фиг. 4 представлено изображение дифференциальной сканирующей калориметрии для аморфной формы дималеата SHR1258.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение проиллюстрировано следующими подробными примерами, которые никоим образом не следует понимать как ограничивающие объем настоящего изобретения.
Экспериментальные приборы
1. Температурный анализ (ДСК)
Тип прибора: Perkin-Elmer Pyris 1 Series Thermal Analysis System
Газ продувки: азот
Скорость нагревания: 10,0°С/мин
Температурный диапазон: от 50 до 300°С
2. Спектр рентгеновской дифрактограммы
Тип прибора: D/Max-RA Japan rigaku X-ray powder diffraction
Излучение: монохроматическое Cu-Kα излучение (λ=1,5418Å)
Режим сканирования: θ/2θ, угловое сканирование 2-40°
Напряжение: 40 кВ, Ток: 40 мА
Пример 1
1,0 г SHR1258 (полученного в соответствии с патентом WO 2011029265) и 0,4 г малеиновой кислоты растворяли в 25 мл изопропилового спирта при нагревании. Твердое вещество присутствовало в конденсате. После завершения нагревания полученную смесь перемешивали, чтобы выпал осадок. Полученный осадок собирали с помощью фильтрации и затем высушивали при 45°С под вакуумом в течение ночи с получением 0,85 г кристаллов дималеата SHR1258. Выход: 60%. На Фиг. 1 показана рентгеновская дифрактограмма, на которой характеристическими пиками являются: 6,28 (14,06), 6,74 (13,10), 10,60 (8,34), 11,58 (7,64), 13,50 (6,55), 14,90 (5,94), 15,80 (5,60), 18,26 (4,85), 20,66 (4,30), 21,14 (4,20), 22,96 (3,87), 24,34 (3,65), 25,54 (3,49) и 26,12 (3,41). Изображение ДСК показано на Фиг. 2 с острым пиком поглощения плавления при 131,429°С. Кристаллы были определены как кристаллы формы I.
Пример 2
1,0 г SHR1258 и 0,4 г малеиновой кислоты растворяли в 20 мл этанола при нагревании. После завершения нагревания смесь перемешивали в течение ночи (отделившееся твердое вещество было липким). На следующий день к смеси добавляли 30 мл диэтилового эфира и перемешивали. Полученный в результате осадок собирали с помощью фильтрации, промывали диэтиловым эфиром и затем высушивали с получением 1,03 г твердого вещества желтого цвета. Выход: 73,5%. На Фиг. 3 показана рентгеновская дифрактограмма этого твердого вещества, характеристические пики на изображении отсутствуют. Изображение ДСК, показанное на Фиг. 4, не содержит пика поглощения плавления ниже 170°С. Указанные данные свидетельствуют, что продукт находился в аморфной форме.
Пример 3
К 1,0 г дималеата SHR1258 (полученного в соответствии с примером 2) добавляли 5 мл метанола и смесь нагревали до появления конденсата, пока не был получен раствор. Растворитель удаляли испарением под вакуумом и добавляли 20 мл изопропилового спирта. Твердое вещество растворялось полностью при нагревании, но конденсат содержал некоторое количество твердого вещества. После завершения нагревания смесь оставляли для кристаллизации. Осадок собирали с помощью фильтрации и высушивали с получением 0,80 г твердого вещества. Выход: 80,0%. После сравнения рентгеновской дифрактограммы и изображений ДСК кристаллы были определены как кристаллы формы I дималеата SHR1258.
Пример 4
2,0 г SHR1258 и 0,8 г малеиновой кислоты нагревали, чтобы растворить в 26 мл смеси этанола и тетрагидрофурана (в объемном соотношении 1:1). Указанный раствор перемешивали на водяной бане при 45°C с отделением твердого вещества. После завершения нагревания смесь перемешивали для кристаллизации. Осадок собирали с помощью фильтрации и высушивали при 45°С под вакуумом в течение ночи с получением 2,3 г кристаллов. Выход: 82,0%. После сравнения рентгеновской дифрактограммы и изображений ДСК указанные кристаллы были определены как кристаллы формы I дималеата SHR1258.
Пример 5
1,0 г дималеата SHR1258 в твердом состоянии (полученного в соответствии с примером 2) добавляли в 5 мл воды. Смесь нагревали до появления конденсата, пока не был получен раствор. Раствор перемешивали, чтобы вызвать выпадение осадка, и на следующий день появлялось твердое липкое вещество. Осадок собирали с помощью фильтрации и высушивали с получением 0,68 г твердого вещества. Выход: 68,3%. После сравнения рентгеновской дифрактограммы и изображений ДСК указанное вещество было определено как аморфная форма дималеата SHR1258.
Пример 6
Кристаллы формы I дималеата SHR1258, полученные в примере 1, и аморфную форму дималеата SHR1258, полученную в примере 2, подвергали контакту с воздухом, чтобы протестировать стабильность в разнообразных условиях, включая освещение (4500 лк (люкс)), нагревание (60°С), влажность (относительная влажность 90%). Продолжительность указанного исследования составляла пять и десять дней, результаты ВЭЖХ (высокоэффективная жидкостная хроматография) приведены в таблице 1.
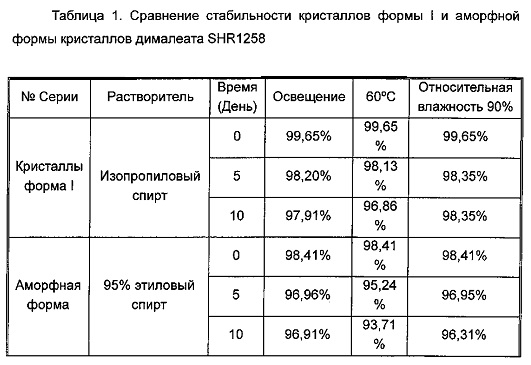
Кристаллы формы I дималеата SHR1258 и аморфную форму дималеата SHR1258 подвергали контакту с воздухом в разнообразных условиях, включая освещение, нагревание и влажность. Результаты показывают, что стабильность кристаллов формы I дималеата SHR1258 и аморфной формы дималеата SHR1258 является сходной на свету, не обладая статистически значимым различием. Кристаллы формы I дималеата SHR1258 более стабильны, чем аморфный дималеат SHR1258, в условиях высокой температуры и влажности.
Пример 7
Кристаллы формы I SHR1258 дималеата, полученные в примере 1, размалывали, нагревали и спрессовывали, затем оценивали с помощью изображений рентгеновской дифрактограммы и изображений ДСК. Результаты показывают, что кристаллы стабильны, данные приведены в таблице 2.
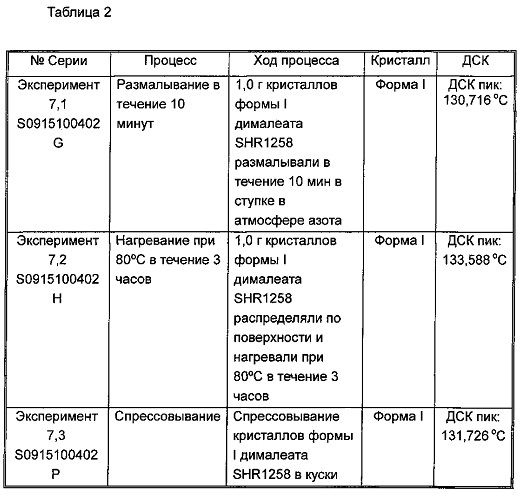


Изобретение относится к области органической химии, а именно к кристаллической форме I дималеата (R,Е)-N-(4-(3-хлор-4-(пиридин-2-ил-метокси)фениламино)-3-циано-7-этоксихинолин-6-ил)-3-(1-метилпирролидин-2-ил)акриламида, способу ее получения, фармацевтической композиции на ее основе и ее применению. Технический результат: полученная кристаллическая форма I дималеата обладает хорошей стабильностью кристаллов и химической стабильностью и может быть применена для получения лекарственных средств для лечения заболеваний, связанных с EGFR (рецептор эпидермального фактора роста) тирозиновой протеинкиназой или HER-2 рецепторной тирозиновой протеинкиназой. 5 н. и 2 з.п. ф-лы, 4 ил., 2 табл., 7 пр.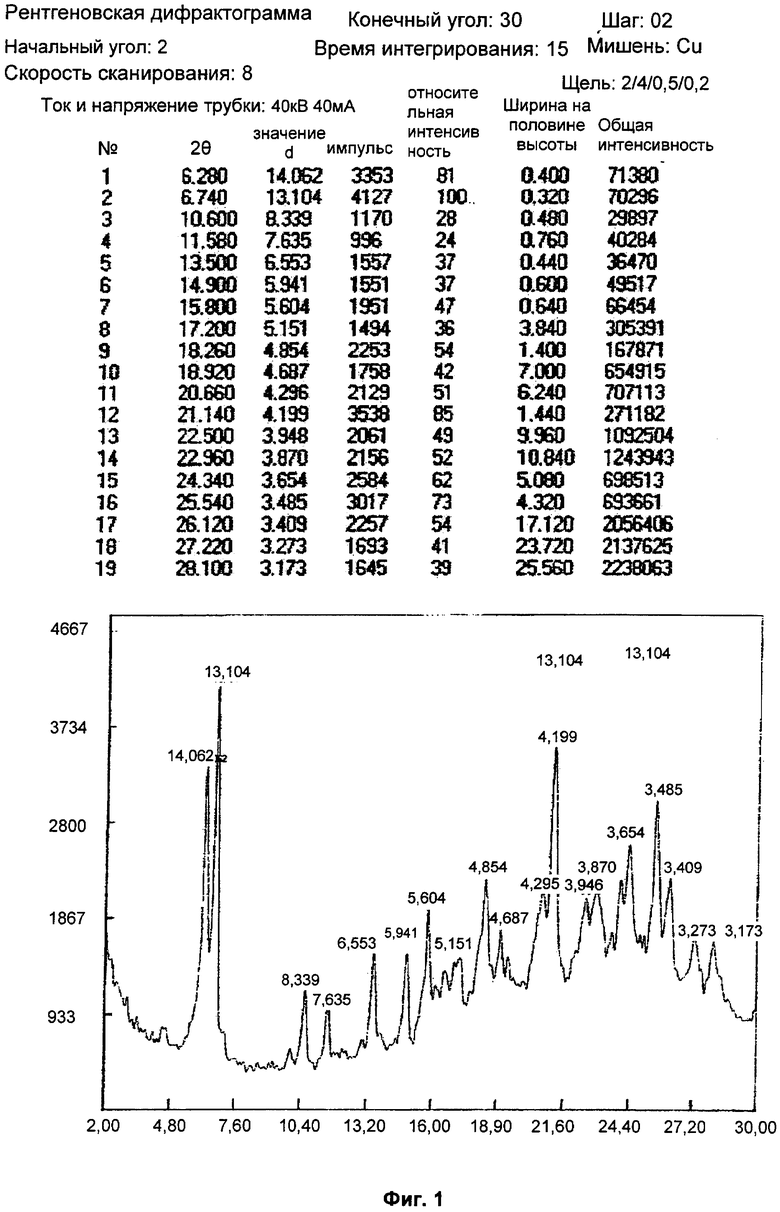
1. Кристаллы формы I дималеата (R,Е)-N-(4-(3-хлор-4-(пиридин-2-ил-метокси)фениламино)-3-циано-7-этоксихинолин-6-ил)-3-(1-метилпирролидин-2-ил)акриламида, отличающиеся тем, что при использовании Cu-Kα излучения для получения рентгеновских дифрактограмм, представленных 2θ углами и межплоскостным расстоянием в кристаллах, кристаллы характеризуются рентгеновской дифрактограммой, как показано на Фиг.1, на которой характеристическими пиками являются: 6,28 (14,06), 6,74 (13,10), 10,60 (8,34), 11,58 (7,64), 13,50 (6,55), 14,90 (5,94), 15,80 (5,60), 18,26 (4,85), 20,66 (4,30), 21,14 (4,20), 22,96 (3,87), 24,34 (3,65), 25,54 (3,49) и 26,12 (3,41).
2. Способ получения кристаллов формы I дималеата (R,Е)-N-(4-(3-хлор-4-(пиридин-2-ил-метокси)фениламино)-3-циано-7-этоксихинолин-6-ил)-3-(1-метилпирролидин-2-ил)акриламида по п.1, включающий следующие стадии:
1) смесь любой кристаллической или аморфной формы (R,E)-N-(4-(3-хлор-4-(пиридин-2-ил-метокси)фениламино)-3-циано-7-этоксихинолин-6-ил)-3-(1-метилпирролидин-2-ил)акриламида и малеиновой кислоты или любой кристаллической формы или аморфной формы дималеата (R,E)-N-(4-(3-хлор-4-(пиридин-2-ил-метокси)фениламино)-3-циано-7-этоксихинолин-6-ил)-3-(1-метилпирролидин-2-ил)акриламида в твердом состоянии нагревают для растворения в достаточном количестве органического растворителя, затем охлаждают для кристаллизации, при этом указанный органический растворитель представляет собой один или более растворителей, выбранных из спирта с не более чем 3 углеродными атомами, ацетона, этилацетата, тетрагидрофурана, предпочтительно этанола, изопропилового спирта, тетрагидрофурана;
2) кристаллы фильтруют, промывают и высушивают.
3. Способ по п.2, отличающийся тем, что органический растворитель на стадии 1) представляет собой изопропиловый спирт.
4. Способ по п.2, отличающийся тем, что органический растворитель на стадии 1) представляет собой смесь этанола и тетрагидрофурана.
5. Фармацевтическая композиция для лечения заболеваний, связанных с протеинкиназой, включающая кристаллы формы I дималеата (R,Е)-N-(4-(3-хлор-4-(пиридин-2-ил-метокси)фениламино)-3-циано-7-этоксихинолин-6-ил)-3-(1-метилпирролидин-2-ил)акриламида по п.1 и фармацевтически приемлемый носитель.
6. Применение кристаллов формы I по п.1 или фармацевтической композиции по п.5 для получения лекарственного средства для лечения заболеваний, связанных с протеинкиназой, при этом указанную протеинкиназу выбирают из EGFR (рецептор эпидермального фактора роста) тирозиновой протеинкиназы или HER-2 рецепторной тирозиновой протеинкиназы.
7. Применение кристаллов формы I по п.1 или фармацевтической композиции по п.5 для получения лекарственного средства для лечения рака, при этом указанная форма рака представляет собой рак легких, рак молочной железы, плоскоклеточную карциному или рак желудка.
| СПОСОБ КОНТРОЛЯ ЦЕЛОСТНОСТИ МНОГОМЕРНЫХ МАССИВОВ ДАННЫХ НА ОСНОВЕ ПРАВИЛ ПОСТРОЕНИЯ ТРЕУГОЛЬНЫХ КОДОВ | 2021 |
|
RU2774099C1 |
| WO 2009052264 A2, 23.04.2009 | |||
| ЗАМЕЩЕННЫЕ 3-ЦИАНОХИНОЛИНЫ | 1998 |
|
RU2202551C2 |
Авторы
Даты
2017-09-21—Публикация
2013-06-04—Подача