Область техники
Настоящее изобретение относится к области фармацевтических композиций и, в частности, относится к фармацевтической композиции, включающей (R,E)-N-(4-(3-хлор-4-(пиридин-2-илметокси)фениламино)-3-циано-7-этоксихинолин-6-ил)-3-(1-метилпирролидин-2-ил)пропенамид или его фармакологически приемлемую соль. Фармацевтическая композиция обладает свойством быстрого растворения.
Предшествующий уровень техники
В патентном документе CN 102471312 B раскрыто низкомолекулярное соединение (R,Е)-N-(4-(3-хлор-4-(пиридин-2-илметокси)фениламино)-3-циано-7-этоксихинолин-6-ил)-3-(1-метилпирролидин-2-ил)пропенамид, имеющее структуру, изображенную формулой I.
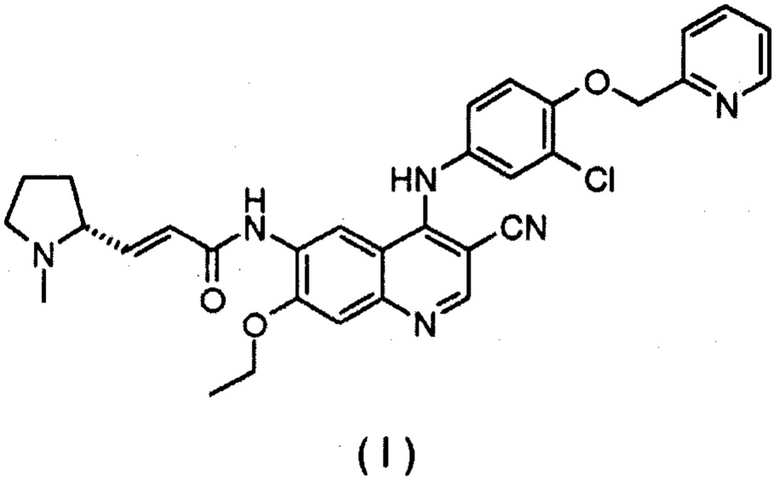
Это соединение известно как низкомолекулярный ингибитор рецепторной тирозинкиназы, ингибирующий рецептор эпидермального фактора роста (EGFR, от англ. epidermal growth factor receptor) и рецептор 2 эпидермального фактора роста человека (ERBB2). Он может ковалентно связываться с АТФ-связывающим сайтом киназного домена EGFR и ERBB2 в клетках, предотвращать образование гомогенных и гетерогенных димеров EGFR и ERBB2 в опухолевых клетках, ингибировать свое собственное фосфорилирование и блокировать активацию нисходящего сигнального пути, тем самым ингибируя рост опухолевых клеток. Это соединение может найти применение в клинической практике для лечения различных опухолей, таких как рак желудочно-кишечного тракта, рак легких и рак молочной железы и т.д.
В патентном документе CN 102933574 В раскрыто соединение формулы I в форме соли малеиновой кислоты, имеющей больше преимуществ в плане растворимости, биологической доступности и фармакокинетических свойств по сравнению с другими солями и непосредственно с соединением формулы I.
В патентном документе CN 103974949 В раскрыта кристаллическая форма I кислой соли малеиновой кислоты соединения формулы I. Такая кристаллическая форма обладает хорошей стабильностью кристаллов и высокой химической стойкостью и может использоваться при получении лекарственного средства для лечения заболеваний, связанных с рецепторной тирозинкиназой EGFR или рецепторной тирозинкиназой HER-2.
Однако при приготовлении из (R,Е)-N-(4-(3-хлор-4-(пиридин-2-илметокси)фениламино)-3-циано-7-этоксихинолин-6-ил)-3-(1-метилпирролидин-2-ил)пропенамида или его фармацевтически приемлемой соли твердой фармацевтической композиции при растворении активного ингредиента в воде будет происходить локальное повышение вязкости. Это не способствует приготовлению фармацевтической композиции и вызывает снижение скорости растворения действующего вещества.
Сущность изобретения
Целью настоящего изобретение является создание быстро растворяющейся фармацевтической композиции. Способ приготовления фармацевтической композиции является простым и удобным для крупномасштабного производства.
Фармацевтическая композиция, предлагаемая настоящим изобретением, включает активный фармацевтический ингредиент и поперечно-сшитый поливинилпирролидон. Активный фармацевтический ингредиент представляет собой (R,Е)-N-(4-(3-хлор-4-(пиридин-2-илметокси)фениламино)-3-циано-7-этоксихинолин-6-ил)-3-(1-метилпирролидин-2-ил)пропенамид или его фармакологически приемлемую соль, например, гидрохлорид, малеат, гидробромид, пара-толуолсульфонат, метансульфонат, сульфат или этансульфонат, предпочтительно, малеат и, еще более предпочтительно, дималеат. Активный ингредиент может присутствовать в количестве от 5 до 70%, предпочтительно, от 10 до 50% и, еще более предпочтительно, от 20 до 40 мас. % от общей массы композиции. Поперечно-сшитый поливинилпирролидон может присутствовать в количестве приблизительно от 2 до 20%, предпочтительно, от 4 до 15% и, еще более предпочтительно, от 6 до 10 мас. % от общей массы композиции.
Фармацевтическая композиция, предлагаемая настоящим изобретением, может также включать наполнитель, например, один или более из микрокристаллической целлюлозы, вторичного кислого фосфата кальция, маннита, прежелатинизированного крахмала и лактозы и т.д. Наполнитель присутствует в количестве приблизительно от 5 до 80 мас. % от общей массы композиции.
Фармацевтическая композиция, предлагаемая настоящим изобретением, может также включать связующее вещество, например, одно или более из гидроксипропилметилцеллюлозы, гидроксипропилцеллюлозы, натриевой соли карбоксиметилцеллюлозы, поливинилпирролидона и метилцеллюлозы и т.д. Связующее вещество присутствует в количестве приблизительно от 0,5 до 15 мас. % от общей массы композиции.
Фармацевтическая композиция, предлагаемая настоящим изобретением, может также включать другой разрыхлитель (разрыхлители), например, один или более из кроскармеллозы натрия, карбоксиметилкрахмала натрия, крахмала и гидроксипропилцеллюлозы с низкой степенью замещения и т.д. Разрыхлитель присутствует в количестве приблизительно от 0 до 20 мас. % от общей массы композиции.
Фармацевтическая композиция, предлагаемая настоящим изобретением, может также включать одно или более смазывающее вещество (вещества), облегчающее заполнение капсул или таблетирование. Смазывающее вещество включает тальк, стеарат магния, стеарат цинка, бегенат глицерина, лаурилсульфат натрия, гидрогенизированное растительное масло, коллоидный диоксид кремния и тому подобное. Смазывающее вещество присутствует в количестве приблизительно от 0,5 до 5 мас. % от общей массы композиции.
Настоящее изобретение также предлагает фармацевтическую композицию, включающую:
1) от 5 до 70 мас. % (R,Е)-N-(4-(3-хлор-4-(пиридин-2-илметокси)фениламино)-3-циано-7-этоксихинолин-6-ил)-3-(1-метилпирролидин-2-ил)пропенамида или его фармакологически приемлемой соли;
2) от 2 до 20 мас. % поперечно-сшитого поливинилпирролидона;
3) от 5 до 80 мас. % наполнителя, где наполнитель является одним или более, выбранным из группы, состоящей из лактозы и микрокристаллической целлюлозы;
4) от 0,5 до 15 мас. % связующего вещества, где связующее вещество является одним или более, выбранным из группы, состоящей из поливинилпирролидона, гидроксипропилметилцеллюлозы и гидроксипропилцеллюлозы; и
5) от 0,5 до 5 мас. % смазывающего вещества, где смазывающее вещество является одним или более, выбранным из группы, состоящей из стеарата магния и талька.
На основании испытания на растворение можно заметить, что благодаря добавлению в фармацевтическую композицию по настоящему изобретению поперечно-сшитого поливинилпирролидона скорость растворения активного ингредиента значительно повышается. Растворение становится быстрым и полным, что является благоприятным для поступления действующего вещества в организм и оперативного воздействия и быстрого проявления его эффективности.
Настоящее изобретение также предлагает фармацевтическую композицию, где во время приготовления фармацевтической композиции в нее может быть добавлен увлажняющий агент. Увлажняющий агент может включать по меньшей мере один органический растворитель, а также может включать воду, где органический растворитель может быть органическим растворителем с низкой токсичностью, предпочтительно, этанолом и ацетоном и тому подобным, более предпочтительно - этанолом. Органический растворитель может присутствовать в количестве от 20 до 100%, предпочтительно, от 50 до 95% и, еще более предпочтительно, от 50 до 80 мас. % от общей массы увлажняющего агента.
Поскольку увлажняющий агент, добавляемый во время приготовления фармацевтической композиции, включает органический растворитель с низкой токсичностью, такой как этанол и тому подобное, получаемые в результате гранулы имеют требуемый гранулометрический состав, а растворение активного ингредиента является быстрым и полным, что облегчает проявление эффективности лекарственного средства.
Фармацевтическая композиция по настоящему изобретению быстро растворяется, имеет выраженный эффект и может применяться для лечения раковых заболеваний, таких как рак желудочно-кишечного тракта, рак легких или рак молочной железы и т.д.
Настоящее изобретение также предлагает способ приготовления фармацевтической композиции, включающий стадию смешивания (R,E)-N-(4-(3-хлор-4-(пиридин-2-илметокси)фениламино)-3-циано-7-этоксихинолин-6-ил)-3-(1-метилпирролидин-2-ил)пропенамида или его фармакологически приемлемой соли и поперечно-сшитого поливинилпирролидона. Фармацевтическая композиция может быть приготовлена в виде гранул с помощью общепринятых способов, таких как влажное гранулирование, и в конечном итоге может быть приготовлена в виде композиции для перорального применения, такой как таблетка или капсула.
Краткое описание графических материалов
На Фиг. 1 показаны профили растворимости таблеток Примера 1 и Сравнительных примеров 1-4 в 0,1 моль/л растворе соляной кислоты.
На Фиг. 2 показаны профили растворимости таблеток Примеров со 2 по 7 в 0,1 моль/л растворе соляной кислоты.
На Фиг. 3 показан гранулометрический состав Примеров 8-12 и Сравнительного примера 5.
Фиг. 4 показаны профили растворимости нескольких образцов таблеток из Сравнительного примера 5 в 0,1 моль/л растворе соляной кислоты.
Фиг. 5 показаны профили растворимости нескольких образцов таблеток Примера 8 в 0,1 моль/л растворе соляной кислоты.
Фиг. 6 показаны профили растворимости нескольких образцов таблеток Примера 9 в 0,1 моль/л растворе соляной кислоты.
Фиг. 7 показаны профили растворимости нескольких образцов таблеток Примера 10 в 0,1 моль/л растворе соляной кислоты.
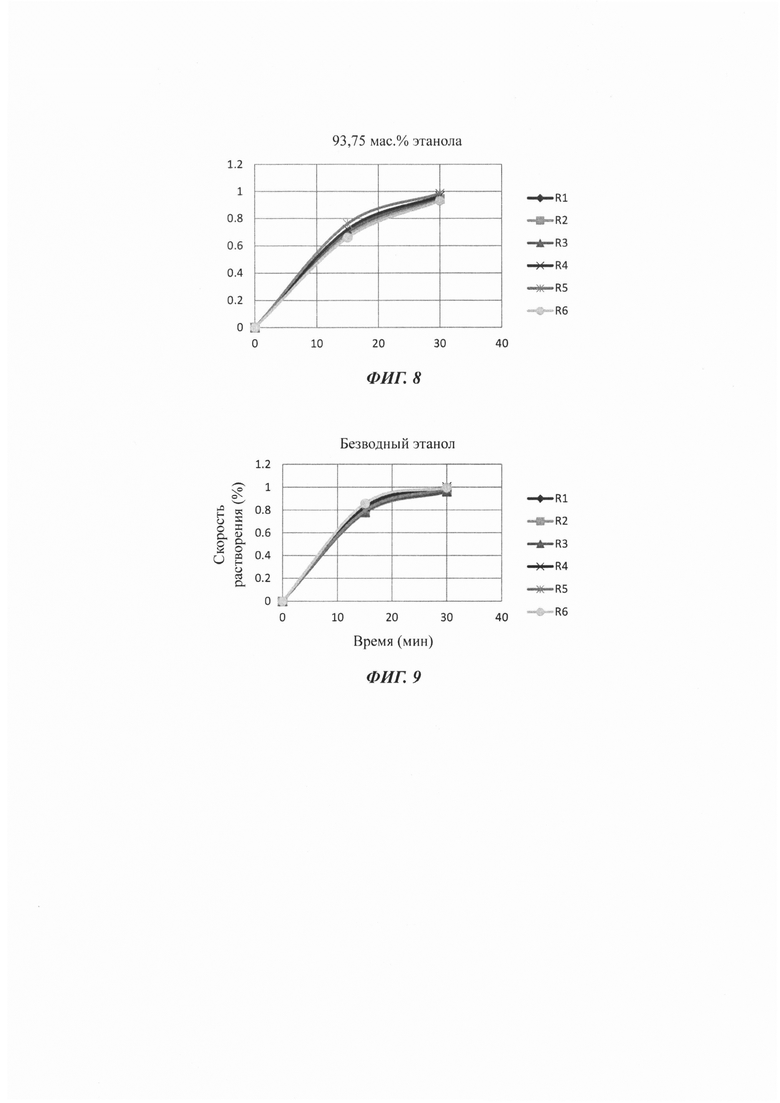
Фиг. 8 показаны профили растворимости нескольких образцов таблеток Примера 11 в 0,1 моль/л растворе соляной кислоты.
Фиг. 9 показаны профили растворимости нескольких образцов таблеток Примера 12 в 0,1 моль/л растворе соляной кислоты.
Подробное описание изобретения
Настоящее изобретение будет дополнительно подробно описано с помощью следующих примеров и экспериментальных примеров. Эти примеры и экспериментальные примеры приведены исключительно для иллюстрации и не предназначены для ограничения объема изобретения.
Описание примеров осуществления изобретения
Пример 1, сравнительные примеры 1-4
Малеат (R,Е)-N-(4-(3-хлор-4-(пиридин-2-илметокси)фениламино)-3-циано-7-этоксихинолин-6-ил)-3-(1-метилпирролидин-2-ил)пропенамида (далее называемый соединением А), лактозу, микрокристаллическую целлюлозу, поливинилпирролидон и поперечно-сшитый поливинилпирролидон смешивали в соотношении, указанном в Таблице 1 для Примера 1. При влажном гранулировании в качестве увлажняющего агента использовали соответствующее количество 93,75 мас. % раствора этанола в воде. Гранулы сушили до тех пор, пока содержание влаги не стало менее 2%, после чего выполняли сухой размол. Добавляли предписанное количество стеарата магния, и смесь перемешивали с помощью вращающегося смесителя. Полученную общую смесь гранул таблетировали, наносили покрытие и получали таблетки. Таблетки из Сравнительных примеров 1-4, содержащие гидроксипропилцеллюлозу с низкой степенью замещения, карбоксиметилкрахмал натрия, кроскармеллозу натрия или крахмал, получали с помощью такого же способа.
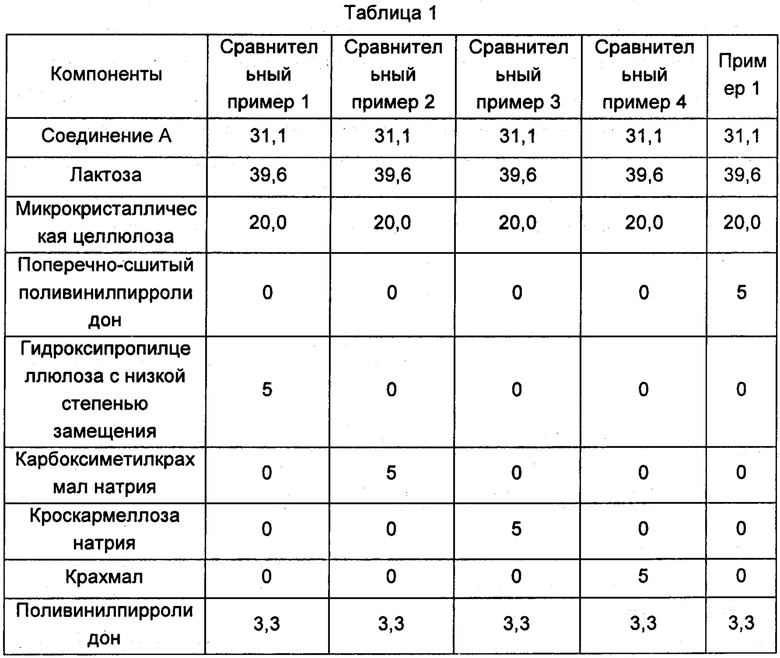

Единица: мас. %
Экспериментальный пример 1: испытание на растворение
Испытания на растворение таблеток Примера 1 и Сравнительных примеров 1-4 выполняли в соответствии со вторым способом (способом с использованием лопастной мешалки) тестирования скорости растворения, описанным в дополнении ко II тому Фармакопеи Китая (редакция 2010 г.), используя в качестве среды для растворения 900 мл 0,1 моль/л раствора соляной кислоты при температуре 37 плюс/минус 0,5°С и скорости вращения лопастей 50 об./мин. Результаты показали, что в случае таблеток Примера 1, содержащих поперечно-сшитый поливинилпирролидон, растворение соединения А является быстрым и полным, тогда как в случае таблеток из Сравнительных примеров 1-4, содержащих гидроксипропилцеллюлозу с низкой степенью замещения, карбоксиметилкрахмал натрия, кроскармеллозу натрия или крахмал, растворение соединения А происходит медленно и неполно.
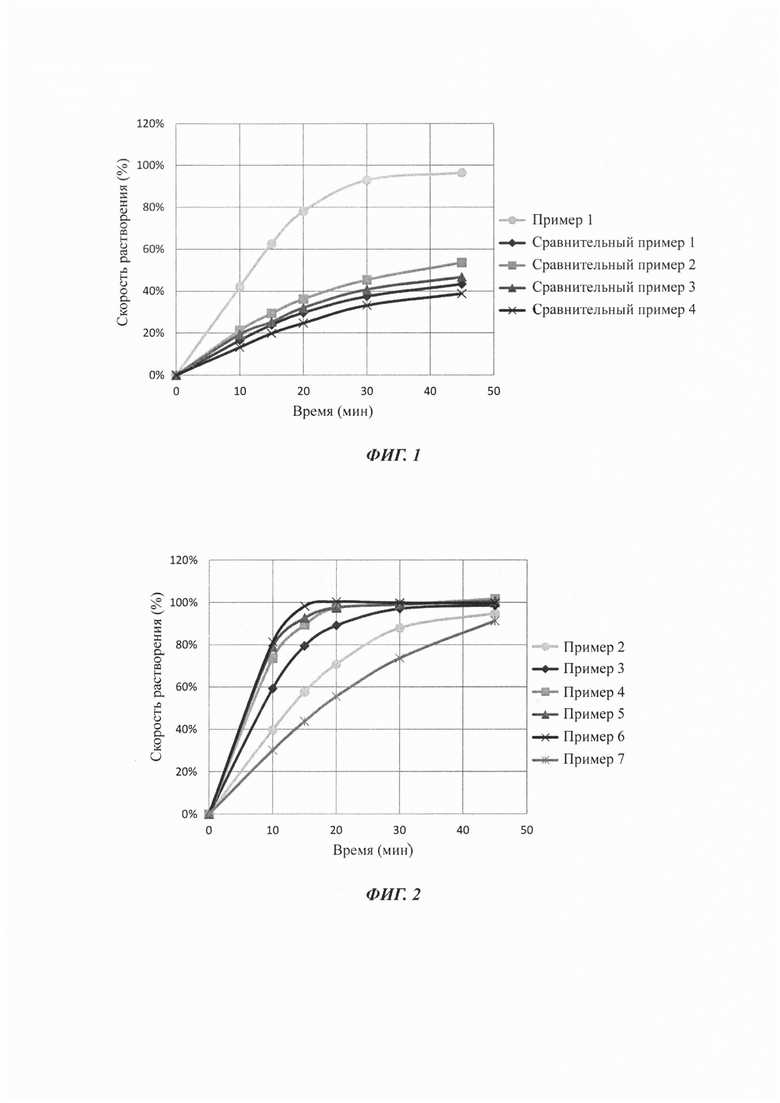
Профили растворимости изображены на Фиг. 1.
Примеры 2-7
Соединение А, лактозу, микрокристаллическую целлюлозу, поливинилпирролидон и поперечно-сшитый поливинилпирролидон смешивали в соотношении, указанном в Таблице 2. При влажном гранулировании в качестве увлажняющего агента использовали соответствующее количество 93,75 мас. % раствора этанола в воде. Гранулы сушили до тех пор, пока содержание влаги не стало менее 2%, после чего выполняли сухой размол. Добавляли предписанное количество стеарата магния, и смесь перемешивали с помощью вращающегося смесителя. Полученную общую смесь гранул таблетировали, наносили покрытие и получали таблетки.
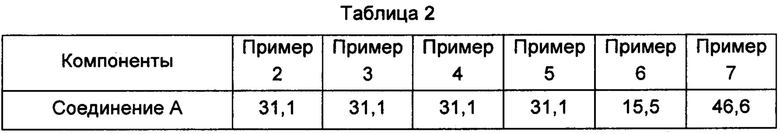
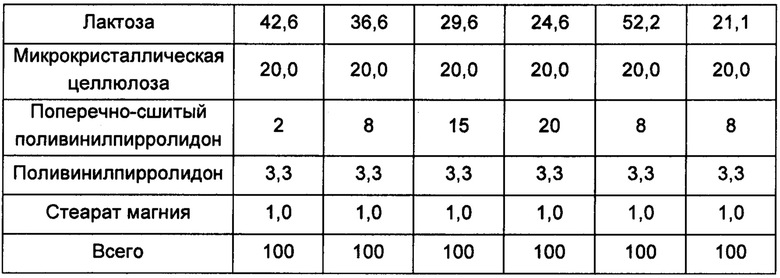
Единица: мас. %
Экспериментальный пример 2: испытание на растворение
Испытания на растворение таблеток Примеров 2-7 выполняли в соответствии со вторым способом (способом с использованием лопастной мешалки) тестирования скорости растворения, описанным в дополнении ко II тому Фармакопеи Китая (редакция 2010 г.), используя в качестве среды для растворения 900 мл 0,1 моль/л раствора соляной кислоты при температуре 37 плюс/минус 0,5°С и скорости вращения лопастей 50 об./мин. Результаты показали, что в случае таблеток Примеров 2-5, содержащих поперечно-сшитый поливинилпирролидон в различных соотношениях, и таблеток Примеров 6-7, содержащих соединение А в различных соотношениях, растворение соединения А является быстрым и полным.
Профили растворимости изображены на Фиг. 2.
Примеры 8-12, Сравнительный пример 5
Соединение А, лактозу, микрокристаллическую целлюлозу, поливинилпирролидон и поперечно-сшитый поливинилпирролидон смешивали в соотношении, указанном в Таблице 3. При влажном гранулировании в качестве увлажняющего агента использовали соответствующее количество очищенной воды, 20 мас. % раствора этанола в воде, 50 мас. % раствора этанола в воде, 80 мас. % раствора этанола в воде, 93,75 мас. % раствора этанола в воде и безводного этанола, соответственно. Гранулы сушили до тех пор, пока содержание влаги не стало менее 2%, после чего выполняли сухой размол. Добавляли предписанное количество стеарата магния, и смесь перемешивали с помощью вращающегося смесителя. 100 г полученной общей смеси гранул отделяли для просеивания, а остальные гранулы таблетировали и наносили покрытие с получением таблеток.
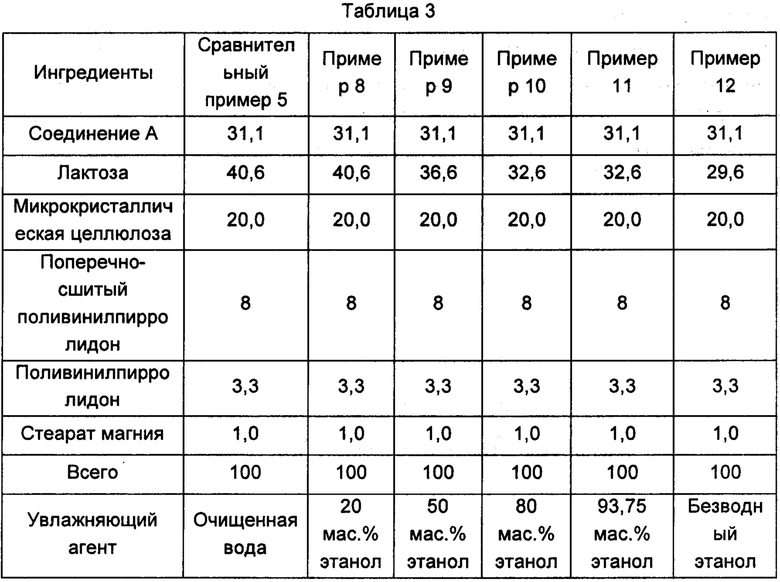
Единица: мас. %
Экспериментальный пример 3: ситовый анализ
100 г отделенных гранул, полученных в Примерах 8-12 и Сравнительном примере 5, встряхивали и просеивали с помощью сит с размером ячеек 50 меш и 100 меш. В Сравнительном примере 5, в котором в качестве увлажняющего агента использовали очищенную воду, в полученной грануле было много крупных частиц и мелкого порошка, и гранулометрический состав был неудовлетворительным. В Примерах 8-12 были использованы увлажняющие агенты, содержащие этанол, в этом случае в полученной грануле было меньше крупных частиц и мелкого порошка, а гранулометрический состав был более однородным.
Результаты просеивания изображены на Фиг. 3.
Экспериментальный пример 4: испытание на растворение
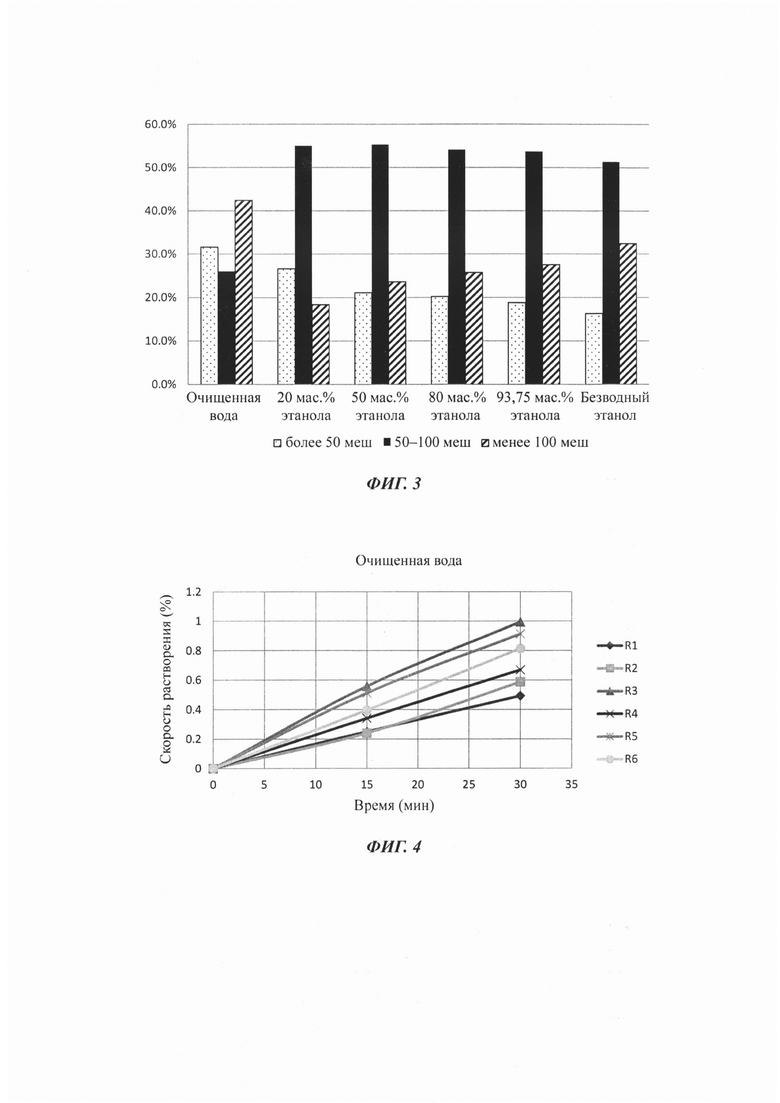
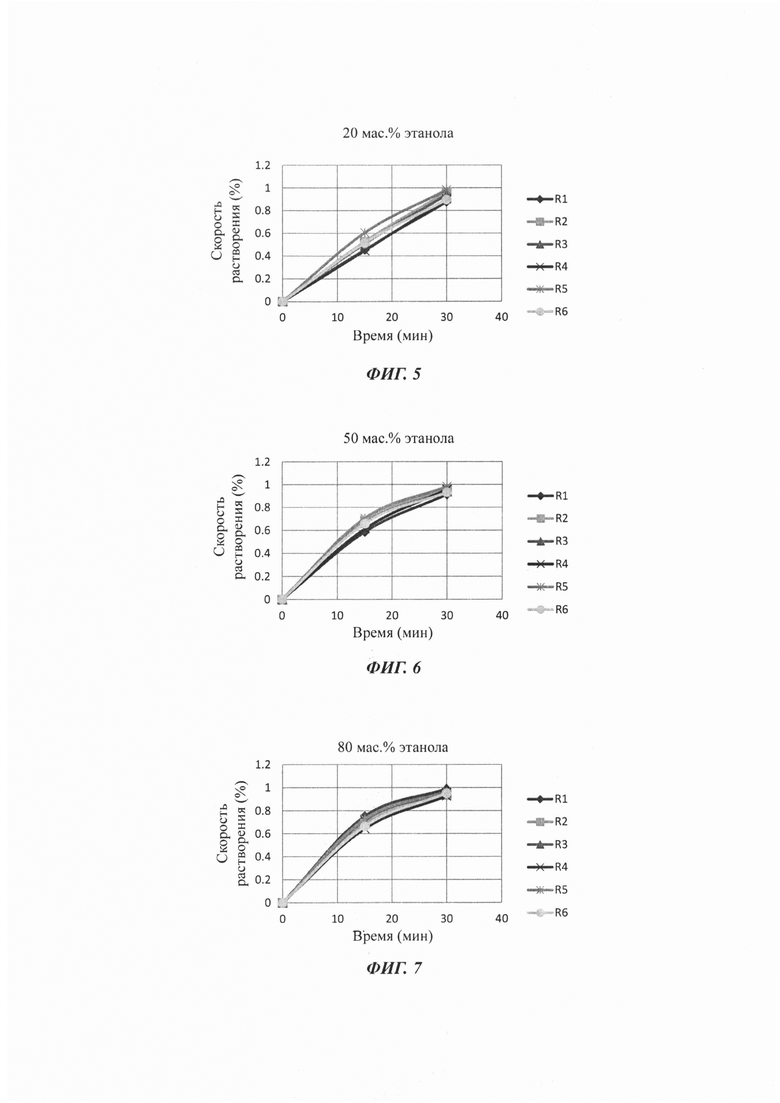
Испытания на растворение таблеток Примеров 8-12 и Сравнительного примера 5 выполняли в соответствии со вторым способом (способом с использованием лопастной мешалки) тестирования скорости растворения, описанным в дополнении ко II тому Фармакопеи Китая (редакция 2010 г.), используя в качестве среды для растворения 900 мл 0,1 моль/л раствора соляной кислоты при температуре 37 плюс/минус 0,5°С и скорости вращения лопастей 50 об./мин. Результаты показали, что когда в качестве увлажняющего агента в Примерах 8-12 использовали 20 мас. % раствор этанола в воде, 50 мас. % раствор этанола в воде, 80 мас. % раствор этанола в воде, 93,75 мас. % раствор этанола в воде и безводный этанол, соответственно, получаемые в результате гранулы имели требуемый гранулометрический состав, при этом растворение соединения А было быстрым и полным; когда в Сравнительном примере 5 в качестве увлажняющего агента использовали очищенную воду, в получаемых в результате таблетках равномерность растворения соединения А была плохой. Когда в качестве увлажняющих агентов в Примерах 8-12 использовали увлажняющие агенты, содержащие этанол, в получаемых в результате таблетках равномерность растворения соединения А была хорошей.
Профили растворимости изображены на Фиг. 4-9, a R1-R6, указанные на рисунках, соответствуют тестируемым образцам таблеток с 1 по 6.
Группа изобретений относится к области фармацевтики, а именно к фармацевтической композиции и ее применению для лечения рака желудочно-кишечного тракта, рака легких и рака молочной железы, а также к способу приготовления фармацевтической композиции. Композиция включает (R,E)-N-(4-(3-хлор-4-(пиридин-2-илметокси)фениламино)-3-циано-7- этоксихинолин-6-ил)-3-(1-метилпирролидин-2-ил)пропенамид или его фармакологически приемлемую соль, поперечно-сшитый поливинилпирролидон, лактозу и микрокристаллическую целлюлозу в качестве наполнителя, поливинилпирролидон в качестве связующего вещества, стеарат магния в качестве смазывающего вещества в определенных количествах. Способ приготовления фармацевтической композиции включает стадию смешивания (R,E)-N-(4-(3-хлор-4-(пиридин-2-илметокси)фениламино)-3-циано-7-этоксихинолин-6-ил)-3-(1-метилпирролидин-2-ил)пропен-амида или его фармакологически приемлемой соли и поперечно-сшитого поливинилпирролидона. Группа изобретений обеспечивает создание быстро растворяющейся фармацевтической композиции для лечения рака. 3 н. и 3 з.п. ф-лы, 9 ил., 3 табл., 17 пр.
1. Фармацевтическая композиция для лечения рака, выбранного из рака желудочно-кишечного тракта, рака легких и рака молочной железы, включающая:
1) от 15,5 до 46,6 мас.% (R,E)-N-(4-(3-хлор-4-(пиридин-2-илметокси)фениламино)-3-циано-7-этоксихинолин-6-ил)-3-(1-метилпирролидин-2-ил)пропенамида или его фармакологически приемлемой соли;
2) от 2 до 20 мас.% поперечно-сшитого поливинилпирролидона;
3) наполнитель, где наполнитель представляет собой 21,1-42,6 мас.% лактозы и 20 мас.% микрокристаллической целлюлозы;
4) 3,3 мас.% связующего вещества, где связующее вещество представляет собой поливинилпирролидон; и
5) 1 мас.% смазывающего вещества, где смазывающее вещество представляет собой стеарат магния.
2. Фармацевтическая композиция по п. 1, отличающаяся тем, что во время приготовления фармацевтической композиции добавляют увлажняющий агент, при этом увлажняющий агент представляет собой водный или безводный раствор этанола.
3. Фармацевтическая композиция по п. 2, где этанол присутствует в количестве от 20 до 100 мас.%, предпочтительно от 50 до 95 мас.% и еще более предпочтительно от 50 до 80 мас.% от общей массы увлажняющего агента.
4. Фармацевтическая композиция по любому из пп. 1-3, являющаяся твердой композицией для перорального применения, предпочтительно таблеткой и капсулой и еще более предпочтительно таблеткой.
5. Применение фармацевтической композиции по любому из пп. 1-4 при приготовлении лекарственного средства для лечения рака, выбранного из рака желудочно-кишечного тракта, рака легких или рака молочной железы.
6. Способ приготовления фармацевтической композиции по п. 1, включающий стадию смешивания (R,E)-N-(4-(3-хлор-4-(пиридин-2-илметокси)фениламино)-3-циано-7-этоксихи-нолин-6-ил)-3-(1-метилпирролидин-2-ил)пропенамида или его фармакологически приемлемой соли и поперечно-сшитого поливинилпирролидона.
| US 2013338172 A1, 19.12.2013 | |||
| УНИФИЦИРОВАННАЯ КОСМИЧЕСКАЯ ПЛАТФОРМА МОДУЛЬНОГО ПРИНЦИПА ПОСТРОЕНИЯ | 2018 |
|
RU2684877C1 |
| WO 2013131424 A1, 12.09.2013 | |||
| ПРОИЗВОДНЫЕ 6-АМИНОХИНАЗОЛИНА ИЛИ 3-ЦИАНОХИНОЛИНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРА РЕЦЕПТОРНЫХ ТИРОЗИНКИНАЗ EGFR ИЛИ HER-2 | 2010 |
|
RU2536102C2 |
Авторы
Даты
2021-02-12—Публикация
2017-01-23—Подача