Область техники
Настоящее изобретение относится к кристаллической форме I (3aR,5s,6aS)-N-(3-метокси-1,2,4-тиадиазол-5-ил)-5-(метил(7H-пирроло[2,3-d]пиримидин-4-ил)амино)гексагидроциклопента[с]пиррол-2(1H)-формамида бисульфата и способу ее получения и ее применению. Соединение формулы (I), полученное согласно способу по настоящему изобретению, может применяться при лечении артрита.
Уровень техники
Артрит является самым распространенным хроническим заболеванием в мире, существует множество причин его возникновения, и также различны поражения суставов, вызванные артритом. На сегодняшний день тофацитиниб (CP-690550) является новым пероральным ингибитором пути JAK (Янус-киназы, от англ. Janus kinase), разработанным Pfizer Inc. (Пфайзер Инк.), и тофацитиниб является первым в своем классе лекарственным средством, разработанным для лечения ревматоидного артрита. После того как тофацитиниб был получен в лабораториях Pfizer, ожидалось, что лекарственно средство станет лидером продаж. Успех лекарственного средства станет большой победой для подвергнутой значительной критике научно-исследовательской деятельности Pfizer. Результаты III фазы клинических испытаний показали, что эффективность тофацитиниба от Pfizer была значительно лучше, чем метотрексата.

Исходя из структуры тофацитиниба, был разработан целый ряд ингибирующих JAK соединений, которые являются активными in vitro и in vivo и высоко абсорбируемыми, см. WO 2013091539. Соединения, раскрытые в WO 2013091539, проверяли и получали в виде солей, в ходе чего получили (3aR,5s,6aS)-N-(3-метокси-1,2,4-тиадиазол-5-ил)-5-(метил(7H-пирроло[2,3-d]пиримидин-4-ил)амино)гексагидроциклопента[с]пиррол-2(1H)-формамида бисульфат формулы (I), способ его получения раскрыт в PCT заявке № PCT/CN2014/076794 (заявка, ранее поданная заявителем). Ожидается, что соединение формулы (I) будет предпочтительным соединением среди ингибиторов JAK, и обладает большим значением для исследования лечения ревматического и ревматоидного артрита.
Кристаллическая структура фармацевтически активного ингредиента часто влияет на химическую стабильность лекарственного средства. Разные условия кристаллизации и условия хранения могут приводить к изменениям в кристаллической структуре соединения и иногда сопутствующему образованию других форм кристаллической формы. В общем, аморфный лекарственный препарат не имеет регулярной кристаллической структуры и часто обладает другими недостатками, такими как низкая стабильность препарата, меньший размер частиц, трудная фильтрация, легкая аггломерация и низкая текучесть. Таким образом, необходимо улучшать различные свойства вышеуказанного препарата. Существует необходимость в поиске новой кристаллической формы, обладающей высокой чистотой и хорошей химической стабильностью.
Краткое описание изобретения
Целью настоящего изобретения является обеспечение стабильной кристаллической формы соединения формулы (I) и способа ее получения.
Изобретатель исследовал целый ряд кристаллических продуктов соединения формулы (I), полученных при различных условиях кристаллизации, с помощью измерений рентгеновской дифракции и дифференциальной сканирующей калориметрии (ДСК). Было обнаружено, что стабильная кристаллическая форма соединения формулы (I), называемая кристаллической формой I, может быть получена в условиях нормальной кристаллизации. График ДСК кристаллической формы I соединения формулы (I) согласно настоящей заявке демонстрирует эндотермический пик плавления приблизительно при 220°C. Порошковая рентгеновская дифрактограмма, полученная с использованием излучения Cu-Kα и характеризующаяся углами 2θ и межплоскостными расстояниями (величина d), показана на фиг. 1 и содержит характеристические пики при 6,38 (13,85), 10,38 (8,51), 10,75 (8,23), 14,49 (6,11), 15,07 (5,88), 15,58 (5,69), 16,23 (5,46), 17,84 (4,97), 18,81 (4,72), 19,97 (4,44), 20,77 (4,27), 22,12 (4,02), 23,19 (3,83), 24,12 (3,69), 25,51 (3,49), 26,62 (3,35), 27,38 (3,26), 28,56 (3,12) и 29,91 (2,99).
В способе получения кристаллической формы I по настоящему изобретению существующая форма соединения формулы (I), используемая в качестве исходного вещества, конкретно не ограничена, и можно использовать любую кристаллическую форму или аморфное твердое вещество. Способ получения кристаллической формы I соединения формулы (I) по настоящему изобретению включает:
применение нескольких низших органических растворителей, предпочтительно спиртов, имеющих 3 или менее атомов углерода, и более предпочтительно метанола, в качестве растворителей для перекристаллизации.
В частности, в настоящем изобретении предложен способ получения кристаллической формы I соединения формулы (I), включающий следующие стадии:
(1) растворение твердого соединения формулы (I) в любой форме в соответствующем количестве органического растворителя при нагревании, затем выпаривание части растворителя;
(2) отфильтровывание полученного кристалла, затем его промывка и сушка.
В предпочтительном варианте осуществления настоящего изобретения органический растворитель на стадии (1) представляет собой спирт, имеющий 3 или менее атомов углерода, более предпочтительно органический растворитель представляет собой метанол.
Способ перекристаллизации отличается от общепринятого способа перекристаллизации. Любую форму соединения формулы (I) растворяют в органическом растворителе при нагревании, и затем часть растворителя выпаривают при атмосферном давлении; по окончании кристаллизации полученный кристалл отфильтровывают и сушат с получением целевого кристалла. Кристалл, полученный в ходе фильтрации, обычно сушат в вакууме при приблизительно 30-100°C, предпочтительно 40-60°C, для удаления растворителя для перекристаллизации.
Кристаллическую форму полученного соединения формулы (I) определяют с помощью графика ДСК и рентгеновской дифрактограммы. При этом также определяют остаточный растворитель в полученном кристалле.
Кристаллическая форма I соединения формулы (I), полученная согласно способу по изобретению, не содержит или содержит только относительно низкое количество остаточного растворителя, что удовлетворяет требованию национальной фармакопеи касательно ограничения содержания остаточного растворителя в лекарственных препаратах. Таким образом, кристалл по настоящему изобретению подходит для использования в качестве фармацевтически активного ингредиента.
В настоящем изобретении дополнительно предложена фармацевтическая композиция, содержащая кристаллическую форму I соединения формулы (I) и по меньшей мере один фармацевтически приемлемый носитель. Фармацевтически приемлемый носитель выбран из по меньшей мере одного из лактозы, маннита, микрокристаллической целлюлозы, кроскармеллозы натрия, карбоксиметилкрахмала натрия, гидроксипропилметилцеллюлозы, повидано и стеарата магния. Содержание кристаллической формы I в фармацевтической композиции по настоящему изобретению составляет 0,5 мг-200 мг.
Настоящее изобретение дополнительно относится к применению кристаллической формы I соединения формулы (I) или фармацевтической композиции по настоящему изобретению для получения лекарственного средства для лечения связанного с JAK заболевания, предпочтительного ревматического и ревматоидного артрита.
Краткое описание графических материалов
На фиг. 1 показана порошковая рентгеновская дифрактограмма кристаллической формы I соединения формулы (I) (обозначенной на фигуре символом SHR0302).
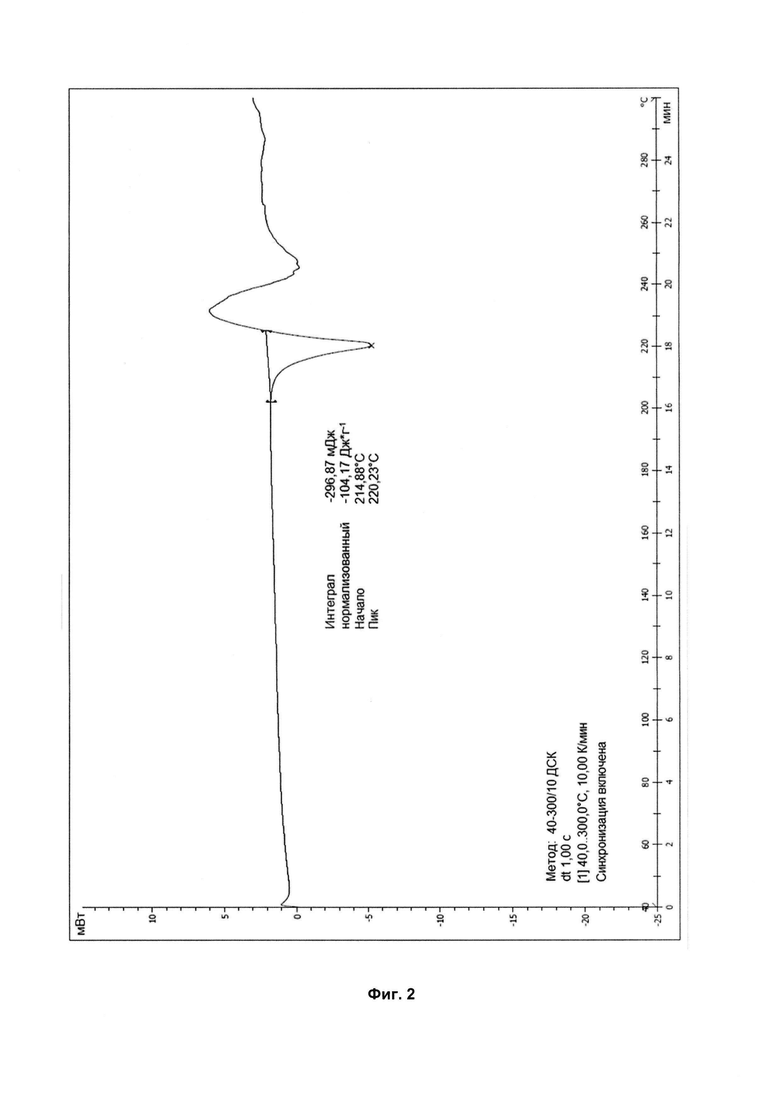
На фиг. 2 показан график ДСК кристаллической формы I соединения формулы (I).
На фиг. 3 показана порошковая рентгеновская дифрактограмма аморфного твердого соединения формулы (I).
На фиг. 4 показан график ДСК аморфного твердого соединения формулы (I).
Подробное описание изобретения
Настоящее изобретение подробно проиллюстрировано следующими примерами, но примеры изобретения предназначены только для описания технического решения согласно изобретению, и не должны рассматриваться в качестве ограничивающих объем настоящего изобретения.
Измерительные приборы, использованные в исследованиях
1. График ДСК
Тип прибора: Система Mettler Toledo DSC 1 Staree
Продувочный газ: Азот
Скорость нагрева: 10,0°C/мин
Температурный диапазон: 40-300°C
2. Рентгеновская дифрактограмма
Тип прибора: порошковый рентгеновский дифрактометр D/Max-RA Japan rigaku
Излучение: монохроматические Cu-Kα лучи 
Режим сканирования: θ/2θ, диапазон углов: 2-40°
Напряжение: 40 кВ, сила тока: 40 мА
Пример 1: Образец соединения формулы (I) получали способом согласно примеру 2 PCT заявки № PCT/CN2014/076794
Получение (3aR,5s,6aS)-N-(3-метокси-1,2,4-тиадиазол-5-ил)-5-(метил(7H-пирроло[2,3-d]пиримидин-4-ил)амино)гексагидроциклопента[с]пиррол-2(1H)-формамида бисульфата формулы (I)
140 г (0,34 моль) (3aR,5s,6aS)-N-(3-метокси-1,2,4-тиадиазол-5-ил)-5-(метил(7H-пирроло[2,3-d]пиримидин-4-ил)амино)гексагидроциклопента[с]пиррол-2(1H)-формамида, 350 г безводного метанола и 2,0 кг дихлорметана добавляли в реакционную колбу объемом 10 л при перемешивании. 34,8 г (0,36 моль) серной кислоты медленно добавляли по каплям при комнатной температуре, затем реакционный раствор становился прозрачным, и его перемешивали в течение 30 минут. Нерастворимые вещества удаляли в ходе фильтрации, фильтрат концентрировали при пониженном давлении досуха с получением 135 г-168 г целевого продукта, выход: 80-90%.
МС (масс-спектрометрия) m/z (ЭСИ (ионизация электрораспылением)): 415,1651 [M+1].
1H ЯМР (ядерный магнитный резонанс) (400 МГц, ДМСО (диметилсульфоксид)-d6): δ 12,75 (s, 1Н), 11,04 (s, 1Н), 8,37 (s, 1Н), 7,41-7,42 (t, 1Н), 6,89 (s, 1Н), 5,15-5,19 (m, 1Н), 3,89 (s, 3Н), 3,68-3,70 (m, 2Н), 3,38-3,40 (m, 2Н), 3,29 (s, 3Н), 2,95 (s, 2Н), 2,09-2,16 (m, 2Н), 1,92-1,97 (m, 2Н).
Пример 2: Измерение кристаллической формы образца из примера 1
Рентгеновская дифрактограмма твердого образца, полученного в примере 1, показана на фиг. 3, при этом на ней отсутствуют характеристические абсорбционные пики кристалла. График ДСК этого твердого образца показан на фиг. 4, при этом на нем отсутствует характеристический абсорбционный пик плавления ниже 300°C. Таким образом, продукт был определен как аморфное твердое вещество.
Пример 3
1,0 г (2,4 ммоль) соединения формулы (I) (полученного способом согласно примеру 1) и 100 мл метанола добавляли в одногорлую колбу объемом 250 мл и кипятили с обратным холодильником до появления прозрачного раствора, затем раствор кипятили с обратным холодильником в течение еще 10 минут. Около 90 мл метанола удаляли выпариванием при атмосферном давлении, и большое количество белого твердого вещества выпадало в осадок. Смесь фильтровали, пока она была горячей, и сушили с получением 784 мг белого твердого вещества с выходом 78,4%. Рентгеновская дифрактограмма этого кристаллического образца показана на фиг. 1 и содержит характеристические пики при 6,38 (13,85), 10,38 (8,51), 10,75 (8,23), 14,49 (6,11), 15,07 (5,88), 15,58 (5,69), 16,23 (5,46), 17,84 (4,97), 18,81 (4,72), 19,97 (4,44), 20,77 (4,27), 22,12 (4,02), 23,19 (3,83), 24,12 (3,69), 25,51 (3,49), 26,62 (3,35), 27,38 (3,26), 28,56 (3,12) и 29,91 (2,99). График ДСК этого кристаллического образца показан на фиг. 2, при этом на нем присутствует эндотермический пик плавления при 220,23°C. Эта кристаллическая форма была определена как кристаллическая форма I.
Пример 4
Аморфный образец, полученный в примере 1, и кристаллическую форму I, полученную в примере 3, распределяли по поверхности на воздухе, чтобы исследовать их стабильность в условиях освещенности (4500 лк), нагревания (40°C, 60°C) и высокой влажности (ОВ (относительная влажность) 75%, ОВ 90%). Исследовали продолжительность измерения 5 дней и 10 дней, и чистота, определенная с помощью ВЭЖХ (высокоэффективная жидкостная хроматография), приведена в таблице 1.


После того распределения кристаллической формы I и аморфного образца соединения формулы (I) по поверхности на воздухе для исследования устойчивости в условиях освещенности, высокой температуры, высокой влажности, результаты исследования устойчивости показали, что высокая влажность не оказывает существенного воздействия на оба образца, но в условиях освещенности и высокой температуры устойчивость кристаллической формы I значительно выше, чем аморфного образца.
| название | год | авторы | номер документа |
|---|---|---|---|
| КРИСТАЛЛИЧЕСКАЯ ФОРМА БИСУЛЬФАТНОГО ИНГИБИТОРА JAK-КИНАЗЫ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2015 |
|
RU2716260C2 |
| БИСУЛЬФАТ ИНГИБИТОРА ЯНУС-КИНАЗЫ (JAK) И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2014 |
|
RU2665680C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ВКЛЮЧАЮЩАЯ ИНГИБИТОР ЯНУС-КИНАЗЫ ИЛИ ЕГО ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМУЮ СОЛЬ | 2017 |
|
RU2744432C2 |
| ПРОИЗВОДНЫЕ ПИРРОЛОПИРИМИДИНА, ПОЛЕЗНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ JAK-КИНАЗЫ | 2012 |
|
RU2618673C2 |
| ИНГИБИТОРЫ MAGL НА ОСНОВЕ ПИРАЗОЛА | 2018 |
|
RU2789157C2 |
| ФЕНИЛАМИНОПИРИМИДИН ИЛИ ПОЛИМОРФНАЯ ФОРМА СОЛИ ФЕНИЛАМИНОПИРИМИДИНА | 2016 |
|
RU2712226C2 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ ДЛЯ ОПОСРЕДОВАНИЯ АКТИВНОСТИ ТИРОЗИНКИНАЗЫ 2 | 2020 |
|
RU2826012C2 |
| ИНГИБИТОРЫ RMT5 | 2019 |
|
RU2814198C2 |
| ПРОИЗВОДНЫЕ ПИРРОЛО[2,3-d]ПИРИМИДИНА | 2009 |
|
RU2493157C2 |
| КЛАСС БИФУНКЦИОНАЛЬНЫХ ХИМЕРНЫХ ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ ДЛЯ НАПРАВЛЕННОГО РАЗРУШЕНИЯ АНДРОГЕННЫХ РЕЦЕПТОРОВ И ИХ ПРИМЕНЕНИЕ | 2020 |
|
RU2825000C2 |



Изобретение относится к кристаллической форме I (3aR,5s,6aS)-N-(3-метокси-1,2,4-тиадиазол-5-ил)-5-(метил(7Н-пирроло[2,3-d]пиримидин-4-ил)амино)гексагидроциклопента[с]пиррол-2(1H)-формамида бисульфата, отличающейся тем, что кристалл имеет порошковую рентгеновскую дифрактограмму, полученную с использованием излучения Cu-Kα и характеризующуюся углами 2θ и межплоскостными расстояниями, как показано на Фиг. 1, содержащую характеристические пики при приблизительно 6,38 (13,85), 10,38 (8,51), 10,75 (8,23), 14,49 (6,11), 15,07 (5,88), 15,58 (5,69), 16,23 (5,46), 17,84 (4,97), 18,81 (4,72), 19,97 (4,44), 20,77 (4,27), 22,12 (4,02), 23,19 (3,83), 24,12 (3,69), 25,51 (3,49), 26,62 (3,35), 27,38 (3,26), 28,56 (3,12) и 29,91 (2,99). Соединение формулы (I) в кристаллической форме предназначено для получения лекарственного средства для лечения связанного с JAK заболевания, такого как ревматический и ревматоидный артрит. 4 н. и 1 з.п. ф-лы, 4 ил., 1 табл., 4 пр.
1. Кристаллическая форма I (3aR,5s,6aS)-N-(3-метокси-1,2,4-тиадиазол-5-ил)-5-(метил(7Н-пирроло[2,3-d]пиримидин-4-ил)амино)гексагидроциклопента[с]пиррол-2(1H)-формамида бисульфата, отличающаяся тем, что кристалл имеет порошковую рентгеновскую дифрактограмму, полученную с использованием излучения Cu-Kα и характеризующуюся углами 2θ и межплоскостными расстояниями, как показано на Фиг. 1, содержащую характеристические пики при приблизительно 6,38 (13,85), 10,38 (8,51), 10,75 (8,23), 14,49 (6,11), 15,07 (5,88), 15,58 (5,69), 16,23 (5,46), 17,84 (4,97), 18,81 (4,72), 19,97 (4,44), 20,77 (4,27), 22,12 (4,02), 23,19 (3,83), 24,12 (3,69), 25,51 (3,49), 26,62 (3,35), 27,38 (3,26), 28,56 (3,12) и 29,91 (2,99).
2. Фармацевтическая композиция для лечения связанного с JAK заболевания, содержащая кристаллическую форму I (3aR,5s,6aS)-N-(3-метокси-1,2,4-тиадиазол-5-ил)-5-(метил(7Н-пирроло[2,3-d]пиримидин-4-ил)амино)гексагидроциклопента[с]пиррол-2(1Н)-формамида бисульфата по п. 1 и фармацевтически приемлемый носитель, отличающаяся тем, что содержание кристаллической формы I (3aR,5s,6aS)-N-(3-метокси-1,2,4-тиадиазол-5-ил)-5-(метил(7Н-пирроло[2,3-d]пиримидин-4-ил)амино)гексагидроциклопента[с]пиррол-2(1Н)-формамида бисульфата составляет 0,5 мг-200 мг.
3. Фармацевтическая композиция по п. 2, отличающаяся тем, что фармацевтически приемлемый носитель выбран из по меньшей мере одного из лактозы, маннита, микрокристаллической целлюлозы, кроскармеллозы натрия, карбоксиметилкрахмала натрия, гидроксипропилметилцеллюлозы, повидона и стеарата магния.
4. Применение кристаллической формы I по п. 1 или фармацевтической композиции по п. 2 для получения лекарственного средства для лечения, связанного с JAK заболевания.
5. Применение кристаллической формы I по п. 1 или фармацевтической композиции по п. 2 для получения лекарственного средства для лечения ревматического и ревматоидного артрита.
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| ПРОИЗВОДНЫЕ ПИРРОЛОПИРИМИДИНА, ПОЛЕЗНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ JAK-КИНАЗЫ | 2012 |
|
RU2618673C2 |
| Sherry L.Morissette et al | |||
| "High-throughput crystallization: polymorphs, salts, co-crystals and solvates of pharmaceutical solids", ADVANCED DRUG DELIVERY REVIEWS, 2004, v.56, pp.275-300 | |||
| STEPHEN M.BERGE et al | |||
| Pharmaceuticals Salts, JOURNAL of PHARMACEUTICAL SCIENCES, 1977, v.66(1), p.1-19 | |||
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| Устройство для ограждения зоны работ на станционных путях | 1987 |
|
SU1439010A1 |
| Муфта | 1990 |
|
SU1798559A1 |
Авторы
Даты
2019-10-31—Публикация
2015-09-09—Подача