Настоящее изобретение относится к полипептидам, которые ковалентно связаны с молекулярными каркасами таким образом, что две или более пептидных петель стянуты сайтами присоединения к каркасу. В частности, изобретение относится к пептидам, которые являются специфическими для плазматической человеческой протеазы калликреина.
Циклические пептиды способны связываться с высокой аффинностью и целевой специфичностью с белками-мишенями и, следовательно, они являются привлекательной группой молекул для разработки терапевтических агентов. Фактически, несколько циклических пептидов уже успешно применяются в клинике, как например, антибактериальный пептид ванкомицин, иммуносупрессор циклоспорин или противоопухолевый препарат окреотид (Driggers et al., Nat. Rev. Drug Discov., 2008, 7(7), 608-624). Хорошие связывающие свойства являются результатом относительно большой поверхности взаимодействия, образованной между пептидом и мишенью, а также пониженной конформационной гибкости циклических структур. Как правило, макроциклы связываются с поверхностями площадью несколько сотен ангстрем, как например, циклический пептид CXCR4 антагонист CVX15 (400 Å2; Wu B. et al., Science, 330 (6007), 1066-1071), циклический пептид с мотивом Arg-Gly-Asp, который связывается с интегрином αVb3 (355 Å2) (Xiong J.P. et al., Science, 2002, 296(5565), 151-155) или циклический пептид ингибитор upain-1, связывающийся с активатором плазминогена урокиназного типа (603 Å2; Zhao G. et al., J. Struct. Biol., 2007, 160(1), 1-10).
За счет их циклической конфигурации пептидные макроциклы являются менее гибкими по сравнению с линейными пептидами, что приводит к меньшей потере энтропии при связывании с мишенями и к более высокой аффинности связывания. Также пониженная гибкость приводит к фиксирующим мишень-специфическим конформациям, что повышает специфичность связывания по сравнению с линейными пептидами. В качестве примера данного эффекта может служить эффективный и селективный ингибитор матричной металлопротеиназы 8 (ММР-8), который теряет свою селективность к другим ММР, когда его кольцо раскрыто (Cherney R.J. et al., J. Med. Chem., 1998, 41(11), 1749-1751). Благоприятные связывающие свойства, достигаемые посредством макроциклизации, являются еще более выраженными у полициклических пептидов, содержащих более чем один пептидный цикл, как например, ванкомицин, низин или актиномицин.
Различные исследовательские группы ранее провели присоединение полипептидов, содержащих цистеиновые остатки, к синтетической молекулярной структуре (Kemp D.S. and McNamara P.E., J. Org. Chem., 1985; Timmerman P. et al., ChemBioChem, 2005). Meloen с сотрудниками использовал трис(бромметил)бензол и близкие молекулы для быстрой и количественной циклизации многочисленных пептидных петель на синтетических каркасах для структурной имитации белковых поверхностей (Timmerman P. et al., ChemBioChem, 2005). Способы получения кандидатов лекарственных препаратов, где указанные препараты получают связыванием полипептидов, содержащих цистеин, с молекулярным каркасом, например, трис(бромметил)бензолом, раскрыты в WO 2004/077062 и WO 2006/078161.
В WO 2004/077062 раскрывается способ селекции кандидатов лекарственных препаратов. В частности, в данном документе раскрываются различные молекулы-каркасы, содержащие первую и вторую реакционноспособные группы, и контактирование указанного каркаса с дополнительной молекулой с образованием по меньшей мере двух связей между каркасом и дополнительной молекулой в реакции сочетания.
В WO 2006/078161 раскрываются связывающие соединения, имунногенные соединения и пептидомиметики. В данном документе описывается химический синтез различных групп пептидов, взятых из существующих белков. Затем данные пептиды объединяют с постоянным синтетическим пептидом, содержащим некоторые аминокислотные модификации, введенные для получения комбинаторных библиотек. Посредством введения данного разнообразия через химическое связывание с отдельными пептидами, характеризующимися различными аминокислотными модификациями, обеспечивается повышенная возможность найти требуемую активность связывания. На фигуре 1 в данном документе показана схема синтеза различных конструкций пептидных петель. Конструкции, раскрытые в данном документе, основаны на пептидах, содержащих функциональную группу -SH, как правило, содержащих цистеиновые остатки, и гетероароматических группах на каркасе, обычно содержащем бензол, замещенный галогенами, такой как бис- или трис-бромфенилбензол. Такие группы взаимодействуют с образованием тиоэфирной связи между пептидом и каркасом.
Недавно заявители разработали комбинаторный подход, основанный на фаговом дисплее, для получения и скрининга крупных библиотек бициклических пептидов к интересующим мишеням (Heinis et al., Nat. Chem. Biol., 2009, 5(7), 502-507; также см. международную заявку на патент WO 2009/098450). В кратком изложении, комбинаторные библиотеки линейных пептидов, содержащих три цистеиновых остатка и две области из шести произвольных аминокислот (Cys-(Xaa)6-Cys-(Xaa)6-Cys), экспонировали на фаге и циклизовали ковалентным связыванием боковых цепей цистеина с небольшой молекулой (трис(бромметил)бензолом). Бициклические пептиды, выделенные в аффинной селекции к человеческим протеазам, катепсину G и плазматическому калликреину (РК), имели константы ингибирования на уровне наномоль. Наилучший ингибитор, РК15, ингибирует РК человека (hPK) с Ki, равной 3 нМ. На основании аналогий аминокислотных последовательностей нескольких выделенных бициклических пептидов было предположено, что обе пептидные петли вносят свой вклад в связывание. РК15 не ингибировал крысиный РК (81% идентичность последовательностей), гомологичную человеческую сериновую протеазу фактор XIa (hfXIa; 69% идентичность последовательностей) или тромбин (36% идентичность последовательностей) в самой высокой тестированной концентрации (10 мкМ) (Heinis et al., Nat. Chem. Biol., 2009, 5(7), 502-507). На основании этого установленного факта можно предположить, что бициклический ингибитор является высокоспецифическим и что другие человеческие трипсин-подобные сериновые протеазы не будут ингибироваться. Синтетический, небольшой пептидный ингибитор, такой как РК15, обладающий вышеописанной активностью и селективностью к мишени, имеет возможность применения в качестве лекарственного препарата для контроля активности РК при врожденной ангиоэдеме, угрожающем жизни заболевании, которое характеризуется эпизодами отечности, или для предупреждения контактной активации при операциях в условиях искусственного кровообращения.
Пептид РК15 был выделен из библиотеки, основанной на пептиде РК2, H-ACSDRFRNCPLWSGTCG-NH2, в котором вторая петля из 6 аминокислот была рандомизирована. Последовательность РК15 представляла последовательность H-ACSDRFRNCPADEALCG-NH2, и константа связывания IC50 с человеческим калликреином составляла 1,7 нМ.
Сущность изобретения
Заявители проанализировали специфичность структурированных полипептидов, отобранных по отношению к человеческому калликреину из набора библиотек, с различной длиной петли. В результате заявителям удалось выделить структурированные пептиды, способные связываться с калликреином, с повышенной специфичностью связывания.
В первом аспекте изобретение относится к пептидному лиганду, специфическому для человеческого калликреина, содержащему полипептид, включающий по меньшей мере три реакционноспособные группы, разделенные по меньшей мере двумя последовательностями петель, и молекулярный каркас, который образует ковалентные связи с реакционноспособными группами полипептида таким образом, что по меньшей мере две полипептидные петли образуются на молекулярном каркасе, где петли пептидного лиганда содержат три, четыре или пять, но менее шести, аминокислот.
С удивлением было обнаружено, что пептиды, содержащие менее 6 аминокислот в каждой петле, могут обладать значительно более высокой аффинностью связывания для калликреина. Например, пептиды 5×5, описанные в данном документе, достигают значений констант связывания, равных 0,08 нМ или ниже.
В одном варианте осуществления петли пептидного лиганда содержат три аминокислоты, и полипептид имеет консенсусную последовательность GrFxxGrRVxGr, где Gr представляет собой реакционноспособную группу.
Например, полипептид может представлять собой один из полипептидов, приведенных в таблице 3.
В одном варианте осуществления петли пептидного лиганда содержат пять аминокислот, и первая петля содержит консенсусную последовательность GrGGxxNGr, где Gr представляет собой реакционноспособную группу.
Например, две смежные петли полипептида могут содержать консенсусную последовательность GrGGxxNGrRxxxxGr.
Например, полипептид может представлять собой один из полипептидов, приведенных в таблице 4.
В одном варианте осуществления петли пептидного лиганда содержат пять аминокислот, и первая петля содержит мотив GrxW/FPxK/RGr, где Gr является реакционноспособной группой. В настоящем контексте обращение к «первой» петле не обязательно означает конкретное положение петли в последовательности. Однако в некоторых вариантах осуществления первая петля может быть проксимальной петлей в направлении от аминоконца к карбоксиконцу пептидной последовательности. Например, полипептид дополнительно содержит вторую дистальную петлю, которая содержит мотив GrT/LHQ/TxLGr. Примеры последовательностей первой петли включают GrxWPARGr, GrxWPSRGr, GrxFPFRGr и GrxFPYRGr. В данных примерах х может быть любой аминокислотой, например, S или R.
В одном варианте осуществления петли пептидного лиганда содержат пять аминокислот, и первая петля содержит мотив GrxHxDLGr, где Gr является реакционноспособной группой.
В одном варианте осуществления петли пептидного лиганда содержат пять аминокислот, и первая петля содержит мотив GrTHxxLGr, где Gr является реакционноспособной группой.
В одном варианте осуществления полипептид содержит две смежные петли, которые содержат мотив GrxW/FPxK/RGrT/LHQ/TDLGr.
Заявители показали, что природа некоторых положений может оказывать влияние на другие положения в последовательности. В частности, результаты опытов, проведенных с пептидами 06-34 и 06-34-03, показывают, что положения 1 и 6 оказывают влияние на положение 4. Предпочтительно положение 4 представляет собой А, если положения 1 и 6 являются соответственно S и T.
В примерах, приведенных в данном документе, нумерация относится к положениям в петлях и пропускает реакционноспособные группы. Так, в GrxW/FPxK/RGrT/LHQ/TDLGr, х находится в положении 1 и T/L в положении 6.
Например, полипептид может представлять собой один из полипептидов, приведенных в таблице 4, таблице 5 или таблице 6.
Например, полипептидный лиганд может содержать один из полипептидов, приведенных в таблицах 4-6.
В вышеупомянутых вариантах осуществления реакционноспособная группа предпочтительно представляет собой реакционноспособную аминокислоту. Предпочтительно реакционноспособная аминокислота представляет собой цистеин.
Варианты полипептидов по данному аспекту изобретения можно получить, как описано выше, идентификацией таких остатков, которые доступны для мутации, и получением библиотек, которые включают мутации в данных положениях. Например, полипептид 06-56 в таблице 4 может быть мутирован без потери активности в положениях Q4 и Т10 (см. примеры ниже). Полипептидные лиганды, содержащие мутации в данных положениях, могут быть выбраны как имеющие повышенную активность связывания по сравнению с пептидом 06-56.
В дополнительном аспекте изобретение относится к полипептидному лиганду по предшествующему аспекту изобретения, который содержит один или более заместителей на основе неприродных аминокислот и устойчив к деградации под действием протеаз.
Заявители установили, что некоторые неприродные аминокислоты обеспечивают связывание с плазматическим калликреином с Ki на уровне наномоль, что существенно удлиняет время нахождения в плазме крови.
В одном варианте осуществления неприродная аминокислота выбрана из N-метиларгинина, гомоаргинина и гидроксипролина. Предпочтительно, N-метильные и гомопроизводные аргинина используются для замещения аргинина, и пролин 3 может быть предпочтительно замещен гидроксипролином, азетидинкарбоновой кислотой или альфа-замещенной аминокислотой, такой как аминоизомасляная кислота. В еще одном варианте осуществления аргинин может быть замещен гуанидилфенилаланином.
В еще одном варианте осуществления полипептид содержит первую петлю, которая включает мотив GrxWPARGr, где Р замещен азетидинкарбоновой кислотой; и/или R замещен N-метиларгинином; и/или R замещен гомоаргинином; и/или R замещен гуанидилфенилаланином.
В одном варианте осуществления полипептид содержит первую петлю, которая включает мотив GrxFPYRGr, где R замещен N-метиларгинином; и/или R замещен гомоаргинином; и где пролин замещен азетидинкарбоновой кислотой; и/или R замещен гуанидилфенилаланином.
Согласно второму аспекту изобретение относится к способу получения мутантного полипептидного лиганда с получением повышенного уровня активности связывания с мишенью по сравнению с таковой исходного полипептидного лиганда, где исходный полипептидный лиганд содержит полипептид, содержащий по меньшей мере три реакционноспособные группы, разделенные по меньшей мере двумя последовательностями петель, и молекулярный каркас, который образует ковалентные связи с реакционноспособными группами полипептида так, что по меньшей мере две полипептидные петли образуются на молекулярном каркасе, включающему следующие стадии: (а) для каждого из двух или более аминокислотных положений в каждой из петлевых последовательностей, получение n различных библиотек мутантов, где каждая библиотека состоит из исходных полипептидов, в которых одно из указанных аминокислотных положений в петлевой последовательности мутировано замещением одной из n различных аминокислот, отличных от исходных; (b) скрининг каждой библиотеки на связывание с исходной мишенью и оценка каждой мутации; (с) идентификация аминокислотных положений, в которых допускаются мутации; (d) получение одного или более мутантных полипептидов, содержащих одну или более мутаций, расположенных в аминокислотных положениях, идентифицированных на стадии (с).
В одном варианте осуществления стадия (d) включает получение библиотеки, содержащей полипептиды, которые включают мутации в двух или более аминокислотных положениях, идентифицированных на стадии (с), и скрининг библиотеки на полипептиды с повышенным уровнем активности связывания с мишенью.
Значение n может быть выбрано согласно числу различных мутантов, предназначенных для получения в каждой библиотеке. Например, если требуется мутанты, содержащие все возможные природные аминокислоты, то n может быть равно 20. Если включаются неприродные аминокислоты, такие как N-метилированные аминокислоты, то n может быть выше 20, например, равняться 22 или 23. Например, n может быть равно 2 или более; 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20.
В третьем аспекте изобретение относится к библиотеке полипептидных лигандов, где полипептидные лиганды содержат полипептид, включающий по меньшей мере три реакционноспособные группы, разделенные по меньшей мере двумя последовательностями петель, и молекулярный каркас, который образует ковалентные связи с реакционноспособными группами полипептида таким образом, что по меньшей мере две полипептидных петли образуются на молекулярном каркасе, где указанная библиотека состоит из m различных мутантов полипептидного лиганда, в которых определенное аминокислотное положение в петлевых последовательностях мутировано замещением одной из m различных аминокислот, где m равно по меньшей мере 2.
В четвертом аспекте изобретение относится к набору библиотек полипептидных лигандов, где полипептидные лиганды содержат полипептид, включающий по меньшей мере три реакционноспособные группы, разделенные по меньшей мере двумя последовательностями петель, и молекулярный каркас, который образует ковалентные связи с реакционноспособными группами полипептида таким образом, что по меньшей мере две полипептидных петли образуются на молекулярном каркасе, где указанный набор включает две или более библиотеки полипептидных лигандов, где каждая из указанных библиотек полипептидных лигандов состоит из m различных мутантов полипептидного лиганда, в которых определенное аминокислотное положение в петлевых последовательностях мутировано замещением одной из m различных аминокислот.
Предпочтительно, m находится в пределах от 2 до 20; в вариантах осуществления m равно по меньшей мере 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20, или более, как было указано в отношении n.
В дополнительном аспекте изобретение относится к пептидному лиганду, содержащему полипептид, включающий по меньшей мере три реакционноспособные группы, разделенные по меньшей мере двумя последовательностями петель, и молекулярный каркас, который образует ковалентные связи с реакционноспособными группами полипептида таким образом, что по меньшей мере две полипептидных петли образуются на молекулярном каркасе, где пептид модифицирован включением по меньшей мере одной неприродной аминокислоты.
Предпочтительно, пептидный лиганд по настоящему изобретению является устойчивым к протеазам. Замена(ы) на неприродные аминокислоты повышает уровень устойчивости полипептида к протеазам.
В одном варианте осуществления неприродная аминокислота выбрана из N-метиларгинина, гомоаргинина и азетидинкарбоновой кислоты и гуанидилфенилаланина. Предпочтительно, N-метильные и гомопроизводные аргинина используются для замещения аргинина, и азетидинкарбоновая кислота замещает пролин. В еще одном варианте осуществления аргинин может быть замещен гуанидилфенилаланином.
Краткое описание фигур
Фигура 1. Селекция фаговых библиотек бициклических пептидов. (а) Фаговые библиотеки бициклических пептидов. Произвольные аминокислоты указаны как «Х», аланин как «А» и константные три цистеиновых остатка как «С». (b) Формат структур химически синтезированных бициклических пептидов, содержащих петли из 3, 5 или 6 аминокислот. Структуры получены связыванием линейных пептидов через три цистеиновые боковые цепи с трис(бромметил)бензолом (TBMB). Аминокислоты, которые различаются в бициклических пептидах, указаны «Хаа». (с-е) Последовательности бициклических пептидов, выделенные из библиотеки 5×5 (с), библиотеки 3×3 А (d) и библиотеки 3×3 В (е). Гомологии аминокислот выделены штриховкой.
Фигура 2. Сравнение поверхностных аминокислот hPK и гомологичных сериновых протеаз. (а) Структура hPK (вход PDB 2ANW) с поверхностным представлением. Атомы аминокислот, экспонированные к поверхности и ближе, чем 4, 8 и 12 Å, к бензамидину (серым цветом), связанные с «карманом» S1, окрашены более темным цветом. (b) Структура hPK. Выделены боковые цепи аминокислот, которые отличаются от hfXIa. (с) Структура hPK. Выделены боковые цепи аминокислот, которые отличаются от rPK.
Фигура 3. Схематичное представление способа, использованного для определения предпочтительных остатков для мутации в полипептидных лигандах.
Фигура 4. Анализ аминокислотных замен в пептиде 06-34 (таблица 4) на связывание пептида с плазматическим калликреином при 2 нМ. Для каждого положения показан эффект различных мутаций в этом положении в сравнении с исходной последовательностью.
Фигура 5. Анализ аминокислотных замен в пептиде 06-56 (таблица 4) на связывание пептида с плазматическим калликреином при 2 нМ. Для каждого положения показан эффект различных мутаций в этом положении в сравнении с исходной последовательностью.
Фигура 6. Анализ аминокислотных замен в пептиде 06-56 (таблица 4) на связывание пептида с плазматическим калликреином при 10 нМ. Для каждого положения показан эффект различных мутаций в этом положении в сравнении с исходной последовательностью.
Фигура 7. Результаты масс-спектрометрии, показывающие масс-спектры Ас-06-34-18(TMB)-NH2 после воздействия 35% крысиной плазмы на время 0, 1 сутки, 2 сутки и 3 сутки (способ 1). Точность масс-спектрометрии в некоторой степени варьирует за счет интерферирующих ионов и низких концентраций фрагментов; однако идентификация отдельных протеолитических фрагментов возможна.
Фигура 8. Химические структуры метаболитов М1, М2, М3 Ас-06-34-18(TMB)-NH2, идентифицированных после воздействия крысиной плазмы.
Фигура 9. Химическая структура лидера Ас-06-34-18(TMB)-NH2.
Фигура 10. Ферментативный анализ ингибирования калликреина под действием лидера Ас-06-34-18(TMB)-NH2 и его производных со скремблированной 1-ой петлей. Наблюдается резкое снижение аффинности, что подчеркивает важное значение целостности фармакофора WPAR.
Фигура 11. Химические структуры аргинина и его аналогов.
Фигура 12. Химические структуры Trp и потенциальных гидрофобных аналогов.
Фигура 13. Химические структуры Pro и потенциальных аналогов со структурными ограничениями.
Фигура 14. Сравнительное ингибирование калликреина под действием Aze3, NMeArg5 и Ас-06-34-18(TMB)-NH2 с двойной модификацией.
Фигура 15. Химические структуры аланина и его аналогов.
Фигура 16. Сравнительное ингибирование калликреина под действием F2Y4, F2Y2 HR5 и Ас-06-34-18(TMB)-NH2 с двойной модификацией.
Фигура 17. А. Избыточность конкретного мотива в каждой селекции. Последовательности селекции анализировали согласно жесткости селекции. Рассчитывали % конкретного мотива в выходе из селекции конкретной жесткости. В. Связывание конкретных мотивов с человеческим плазматическим калликреином в положениях 2, 3, 4 и 5 (при том, что положения 1, 6, 7, 8, 9 и 10 являются постоянными в 06-34-03)
Подробное описание изобретения
Если не указано иное, то все технические и научные термины, использованные в данном документе, имеют такое же значение, которое обычно понимается специалистами в данной области, такое как имеется в области химии пептидов, культивирования клеток и фагового дисплея, химии нуклеиновых кислот и биохимии. Используются стандартные протоколы для методов молекулярной биологии, генетики и биохимии (см. Sambrook et al., Molecular Cloning: A Laboratory Manual, 3rd ed., 2001, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, NY; Ausubel et al., Short Protocols in Molecular Biology (1999), 4th ed., John Wiley&Sons, Inc.), которые включены в данный документ посредством ссылки.
В том смысле, в котором в данном документе используется термин «пептидный лиганд», он относится к пептиду, который ковалентно связан с молекулярным каркасом. Как правило, такие пептиды содержат две или более реакционноспособных групп, которые способны образовать ковалентные связи с каркасом, и последовательность, стянутую указанными реакционноспособными группами, которая относится в данном документе к петлевой последовательности, поскольку она образует петлю, когда пептид связан с каркасом. В настоящем случае пептиды содержат по меньшей мере три реакционноспособные группы и образуют по меньшей мере две петли на каркасе.
Реакционноспособные группы являются группами, способными к образованию ковалентной связи с молекулярным каркасом. Как правило, реакционноспособные группы находятся в боковых цепях аминокислот в пептиде. Примерами являются аминосодержащие группы, такие как цистеин, лизин и селеноцистеин.
В том смысле, в котором в данном документе используется термин «специфичность», он относится к способности лиганда связываться или взаимодействовать иначе с его мишенью с вытеснением молекул, которые аналогичны мишени. Например, специфичность может относиться к способности лиганда ингибировать взаимодействие фермента человека, но не гомологичного фермента из другого вида. С использованием подхода, описанного в данном документе, специфичность может быть модулирована, т.е. повышена или снижена таким образом, чтобы сделать лиганды более или менее способными к взаимодействию с гомологами или паралогами предполагаемой мишени. Специфичность не является синонимом активности, аффинности или авидности, и активность действия лиганда на его мишени (такая как, например, аффинность связывания или уровень ингибирования) необязательно связаны с его специфичностью.
В том смысле, в котором в данном документе используется термин «активность связывания», он относится к количественной оценке связывания по данным тестов оценки связывания, например, описанных в данном документе. Следовательно, активность связывания относится к количеству пептидного лиганда, которое связывается при данной концентрации мишени.
Полиспецифичность представляет собой способность связываться с двумя или более мишенями. Как правило, связывающиеся пептиды способны связываться с одной мишенью, такой как эпитоп в случае антитела, за счет их конформационных свойств. Однако можно получить пептиды, которые могут связываться с двумя или более мишенями, например, антитела с двойной специфичностью, как это известно в данной области, как указывалось выше. В настоящем изобретении пептидные лиганды могут быть способны к связыванию с двумя или более мишенями и, следовательно, быть полиспецифическими. Предпочтительно, они связываются с двумя мишенями и являются биспецифическими. Связывание может быть независимым, означая, что сайты связывания мишеней в пептиде структурно не блокируются под действием связывания одной или другой мишени. В этом случае обе мишени могут быть связаны независимо. В общем, полагают, что связывание одной мишени будет, по меньшей мере частично, мешать связыванию с другой мишенью.
Существует принципиальная разница между лигандом с двойной специфичностью и лигандом со специфичностью, которая включает две близкие мишени. В первом случае лиганд является специфичным для обеих мишеней по отдельности и взаимодействует с каждой отдельным образом. Например, первая петля в лиганде может быть связана с первой мишенью, а вторая петля со второй мишенью. Во втором случае лиганд не является специфическим, поскольку он не дифференцирует две мишени, например, при взаимодействии с эпитопом мишеней, который является общим для обеих.
В контексте настоящего изобретения возможно, что лиганд, который обладает активностью в отношении, например, мишени и ортолога, является биспецифическим лигандом. Однако в одном варианте осуществления лиганд не является биспецифическим, но обладает менее узкой специфичностью, так что он связывается как с мишенью, так и одним или более ортологами. Как правило, лиганд, который не отобран одновременно к мишени и его ортологу, с меньшей вероятностью является биспецифическим за счет модуляции длины петли.
Если лиганды являются действительно биспецифическими, то в одном варианте осуществления по меньшей мере одна из специфичностей лигандов к мишени будет общей среди отобранных лигандов, и уровень этой специфичности может быть модулирован способами по изобретению. Необязательно должна разделяться вторая или дополнительная специфичность, и не требуется, чтобы она была предметом способов, приведенных в данном документе.
Мишень представляет собой молекулу или ее фрагмент, с которыми пептидные лиганды связываются или взаимодействуют иначе. Несмотря на то, что связывание рассматривается в качестве предварительного условия для проявления активности большинства видов, и может быть активностью самой по себе, предусматриваются другие активности. Таким образом, для настоящего изобретения не требуется оценки связывания непосредственно или опосредованно.
Молекулярный каркас представляет собой любую молекулу, которая способна связывать пептид по многим сайтам с приданием одного или более структурных признаков пептиду. Это не перекрестно-сшивающий линкер в том отношении, что он не только просто заменяет дисульфидную связь; вместо этого он обеспечивает два или более сайта присоединения пептида. Предпочтительно, молекулярный каркас содержит по меньшей мере три сайта присоединения пептида, относящихся к реакционноспособным группам каркаса. Данные группы способны взаимодействовать с реакционноспособными группами в пептиде с образованием ковалентной связи. Предпочтительные структуры молекулярных каркасов описаны ниже.
Скрининг на связывающую активность (или любую другую требуемую активность) проводят с использованием способов, хорошо известных в данной области, например, технологии фагового дисплея. Например, мишени, иммобилизованные на твердой фазе, можно использовать для идентификации или выделения связывающих членов репертуара. Скрининг позволит отобрать члены репертуара согласно требуемым характеристикам.
Термин «библиотека» относится к смеси гетерогенных полипептидов или нуклеиновых кислот. Библиотека состоит из членов, которые не являются идентичными. До такой степени термин «библиотека» является синонимом термина «репертуар». Различия в последовательностях между членами библиотеки ответственны за разнообразие, имеющее место в библиотеке. Библиотека может иметь форму простой смеси полипептидов или нуклеиновых кислот, ил может находиться в форме микроорганизмов или клеток, например, бактерий, вирусов, животных или растительных клеток и тому подобное, трансформированных библиотекой нуклеиновых кислот. Предпочтительно, каждый отдельный микроорганизм или клетка содержит только один или ограниченное число членов библиотеки.
В одном варианте осуществления нуклеиновые кислоты включаются в экспрессионные векторы для обеспечения экспрессии полипептидов, кодированных нуклеиновыми кислотами. Следовательно, в предпочтительном аспекте библиотека может иметь форму микроорганизмов-хозяев, где каждый микроорганизм содержит одну или более копий экспрессионного вектора, содержащего один член библиотеки в форме нуклеиновой кислоты, которая может быть экспрессирована с продукцией ее соответствующего полипептидного члена. Таким образом, популяция микроорганизмов-хозяев имеет потенциальную способность кодировать широкий репертуар генетически различных вариантов полипептидов.
В одном варианте осуществления библиотека нуклеиновых кислот кодирует репертуар полипептидов. Каждый нуклеиновокислотный член библиотеки предпочтительно имеет последовательность, связанную с одним или более другими членами библиотеки. Под термином «близкая последовательность» понимают аминокислотную последовательность, обладающую по меньшей мере 50% идентичностью, например, по меньшей мере 60% идентичностью, например, по меньшей мере 70% идентичностью, например, по меньшей мере 80% идентичностью, например, по меньшей мере 90% идентичностью, например, по меньшей мере 95% идентичностью, например, по меньшей мере 98% идентичностью, например, по меньшей мере 99% идентичностью по меньшей мере с одним другим членом библиотеки. Об идентичности можно судить по смежному сегменту по меньшей мере из 3 аминокислот, например, по меньшей мере из 4, 5, 6, 7, 8, 9 или 10 аминокислот, например, по меньшей мере из 12 аминокислот, например, по меньшей мере из 14 аминокислот, например, по меньшей мере из 16 аминокислот, например, по меньшей мере из 17 аминокислот или полной длины референс-последовательности.
Репертуар представляет собой коллекцию вариантов, в данном случае вариантов полипептидов, которые различаются по их последовательности. Как правило, расположение и природа реакционноспособных групп не будут варьировать, но последовательности, образующие петли между ними, могут быть рандомизированы. Репертуары различаются по размеру, но они должны включать по меньшей мере 102 членов. Могут быть сконструированы репертуары из 1011 или более членов.
В том смысле, в котором в данном документе используется термин «набор полипептидных лигандов», он относится к множеству полипептидных лигандов, которые могут быть подвергнуты селекции описанными способами. Потенциально набор может быть репертуаром, но также он может представлять собой небольшую коллекцию полипептидов, по меньшей мере от 2 до 10, 20, 50, 100 или более полипептидов.
В том смысле, в котором в данном документе используется термин «группа полипептидных лигандов», он относится к двум или более лигандам. В одном варианте осуществления группа лигандов содержит только лиганды, которые разделяют по меньшей мере специфичность к одной мишени. Обычно группа будет состоять по меньшей мере из 2, 3, 4, 5, 6, 7, 8, 9 или 10, 20, 50, 100 или более лигандов. В одном варианте осуществления группа состоит из 2 лигандов.
(А) Конструирование пептидных лигандов
(i) Молекулярный каркас
Молекулярные каркасы описаны, например, в WO 2009/098450 и источниках, цитированных тем, в частности, WO 2004/077062 и WO 2006/078161.
Как отмечалось в вышеприведенных документах, молекулярный каркас может представлять собой небольшую молекулу, такую как небольшая органическая молекула.
В одном варианте осуществления молекулярный каркас может представлять собой природные мономеры, или может быть основан на природных мономерах, таких как нуклеозиды, сахара или стероиды. Например, молекулярный каркас может содержать короткий полимер таких молекул, такой как димер или тример.
В одном варианте осуществления молекулярный каркас представляет собой соединение с известной токсичностью, например, соединение с низкой токсичностью. Примеры подходящих соединений включают холестерины, нуклеотиды, стероиды или существующие лекарственные препараты, такие как тамазепам.
В одном варианте осуществления молекулярный каркас может представлять собой макромолекулу. В одном варианте осуществления молекулярный каркас представляет собой макромолекулу, состоящую из аминокислот, нуклеотидов или углеводов.
В одном варианте осуществления молекулярный каркас содержит реакционноспособные группы, которые способны взаимодействовать с функциональной группой(ами) полипептида с образованием ковалентных связей.
Молекулярный каркас может содержать химические группы, такие как амины, тиолы, спирты, кетоны, альдегиды, нитрилы, карбоновые кислоты, сложные эфиры, алкены, алкины, азиды, ангидриды, сукцинимиды, малеимиды, алкилгалогениды и ацилгалогениды.
В одном варианте осуществления молекулярный каркас может содержать или может состоять из трис(бромметил)бензола, в частности, 1,3,5-трис(бромметил)бензола («ТВМВ») или его производных.
В одном варианте осуществления молекулярный каркас представляет собой 2,4,6-трис(бромметил)мезитилен. Он аналогичен 1,3,5-трис(бромметил)бензолу, но дополнительно содержит три метильные группы, присоединенные к бензольному кольцу. Это имеет преимущество в том отношении, что дополнительные метильные группы могут формировать дополнительные контакты с полипептидом и, следовательно, добавляют дополнительное структурное ограничение.
Молекулярный каркас по изобретению содержит химические группы, которые позволяют функциональным группам полипептида кодированной библиотеки по изобретению образовывать ковалентные связи с молекулярным каркасом. Указанные химические группы выбирают из широкого ряда функциональных групп, включающих амины, тиолы, спирты, кетоны, альдегиды, нитрилы, карбоновые кислоты, сложные эфиры, алкены, алкины, ангидриды, сукцинимиды, малеимиды, азиды, алкилгалогениды и ацилгалогениды.
(ii) Полипептид
Реакционноспособные группы полипептидов могут быть обеспечены боковыми цепями природных или неприродных аминокислот. Реакционноспособные группы полипептидов могут быть выбраны из тиольных групп, аминогрупп, карбоксильных групп, групп гуанидиния, фенольных групп или гидроксильных групп. Реакционноспособные группы полипептидов могут быть выбраны из азида, кетокарбонила, алкина, винила или арилгалогенида. Реакционноспособные группы полипептидов, предназначенные для связывания с молекулярным каркасом, могут представлять собой амино- или карбоксиконец полипептида.
В некоторых вариантах осуществления каждая из реакционноспособных групп полипептида, которая связывается с молекулярным каркасом, представляет собой группу одного типа. Например, каждая реакционноспособная группа может представлять собой остаток цистеина. Дополнительные детали приводятся в WO 2009/098450.
В некоторых вариантах осуществления реакционноспособные группы полипептида, которые связываются с молекулярным каркасом, могут включать два или более различных типов, или могут включать три или более различных типов. Например, реакционноспособные группы могут включать два остатка цистеина и один остаток лизина, или могут включать один остаток цистеина, один остаток лизина и один N-концевой амин.
Цистеин может быть использован, поскольку он обладает тем преимуществом, что его реакционная способность наиболее отличается от других аминокислот. Реакционноспособные группы каркаса, которые могут быть использованы на молекулярном каркасе для взаимодействия с тиольными группами цистеинов, представляют собой алкилгалогениды (или также называемые галогеналканами или галоалканами). Примерами являются бромметилбензол (примером такой реакционноспособной группы является ТВМВ) или йодацетамид. Другими реакционноспособными группами каркаса, которые используются для селективного сочетания соединений с цистеинами в белках, являются малеимиды. Примеры малеимидов, которые можно использовать в качестве молекулярных каркасов в изобретении, включают: трис-(2-малеимидоэтил)амин, трис-(2-малеимидоэтил)бензол, трис-(малеимидо)бензол. Селеноцистеин также представляет собой природную аминокислоту, которая обладает аналогичной реакционной способностью для цистеина и может быть использована для тех же реакций. Таким образом, когда упоминается цистеин, то, как правило, его можно заменить селеноцистеином, если по контексту не предлагается иное.
Лизины (и первичные амины N-конца пептидов) также подходят в качестве реакционноспособных групп для модификации пептидов на фаге посредством присоединения к молекулярному каркасу. Однако они являются более избыточными в фаговых белках по сравнению с цистеинами, и имеется более высокий риск того, что фаговые частицы могут подвергнуться перекрестному сшиванию или потерять их инфекционность. Тем не менее, было установлено, что лизины являются особенно пригодными во внутримолекулярных реакциях (например, когда молекулярный каркас уже связан с фаговым пептидом) для образования второй или следующей связи с молекулярным каркасом. В данном случае молекулярный каркас взаимодействует предпочтительно с лизинами экспонированного пептида (в частности, лизинами, которые находятся в максимальной близости). Реакционноспособные группы каркаса, которые избирательно взаимодействуют с первичными аминами, представляют собой сукцинимиды, альдегиды или алкилгалогениды. В бромметильной группе, которая используется в ряде прилагаемых примеров, электроны бензольного кольца могут стабилизировать катионное переходное состояние. Следовательно, данный конкретный арилгалогенид в 100-1000 раз является более реакционноспособным, чем алкилгалогениды. Примеры сукцинимидов для применения в качестве молекулярного каркаса включают трис-(сукцинимидиламинотриацетат), 1,3,5-бензолтриуксусную кислоту. Примеры альдегидов для применения в качестве молекулярного каркаса включают триформилметан. Примеры алкилгалогенидов для применения в качестве молекулярного каркаса включают 1,3,5-трис(бромметил)-2,4,6-триметилбензол, 1,3,5-трис(бромметил)бензол, 1,3,5-трис(бромметил)-2,4,6-триэтилбензол.
Аминокислоты с реакционноспособными группами, которые связываются с молекулярным каркасом, могут располагаться в любых подходящих положениях в полипептиде. Для оказания влияния на конкретные структуры или образованные петли положения аминокислот, содержащих реакционноспособные группы, могут меняться специалистом в данной области, например, путем манипуляции с нуклеиновой кислотой, кодирующей полипептид для мутирования полученного полипептида. С помощью таких способов можно менять длину петли согласно настоящему изобретению.
Например, полипептид может содержать последовательность AC(X)nC(X)mCG, где Х означает произвольную природную аминокислоту, А - аланин, С - цистеин и G - глицин, и n и m, которые могут быть одинаковыми или различными, являются числами от 3 до 6.
(iii) Реакционноспособные группы полипептида
Молекулярный каркас по изобретению может быть связан с полипептидом посредством функциональных или реакционноспособных групп в полипептиде. Как правило, они образованы боковыми цепями конкретных аминокислот, входящих в состав полипептидного полимера. Такие реакционноспособные группы могут представлять собой боковую цепь цистеина, боковую цепь лизина или N-концевую аминогруппу, или любую другую подходящую реакционноспособную группу. Кроме того, детали можно найти в WO 2009/098450.
Примерами реакционноспособных групп природных аминокислот являются тиольная группа цистеина, аминогруппа лизина, карбоксильная группа аспартата или глутамата, группа гуанидиния аргинина, фенольная группа тирозина или гидроксильная группа серина. Неприродные аминокислоты могут обеспечить широкий ряд реакционноспособных групп, включая азид, кетокарбонил, алкин, винил или арилгалогенид. Аминогруппа и карбоксильная группа конца полипептида также могут служить в качестве реакционноспособных групп для образования ковалентных связей с молекулярным каркасом/молекулярным ядром.
Полипептиды по изобретению содержат по меньшей мере три реакционноспособные группы. Указанные полипептиды также могут содержать четыре или более реакционноспособных групп. Чем больше используется реакционноспособных групп, тем больше петель может образоваться в молекулярном каркасе.
В предпочтительном варианте осуществления получают полипептиды с тремя реакционноспособными группами. Взаимодействие указанных полипептидов с молекулярным каркасом/молекулярным ядром, имеющим трехскладчатую поворотную симметрию, дает один изомер продукта. Получение одного изомера продукта является преимущественным по нескольким причинам. Нуклеиновые кислоты библиотек соединений кодируют только первичные последовательности полипептида, но не изомерное состояние молекул, которые образуются при взаимодействии полипептида с молекулярным ядром. Если может быть образован только один изомер продукта, то приписывание нуклеиновой кислоты к изомеру продукта четко определяется. В том случае, если образуются многочисленные изомеры продукта, то нуклеиновая кислота не может давать информацию о природе изомера продукта, который был выделен в скрининге или при селекции. Образование одного изомера продукта также является преимущественным, если синтезируют конкретный член библиотеки по изобретению. В данном случае химическая реакция полипептида с молекулярным каркасом дает скорее один изомер продукта, а не смесь изомеров.
В еще одном варианте осуществления изобретения получают полипептиды с четырьмя реакционноспособными группами. Взаимодействие указанных полипептидов с молекулярным каркасом/молекулярным ядром, имеющим тетраэдральную симметрию, дает два изомера продукта. Даже если два различных изомера продукта кодируются одной и той же нуклеиновой кислотой, то изомерную природу выделенного изомера можно определить химическим синтезом обоих изомеров, разделением двух изомеров и тестированием обоих изомеров на связывание с лигандом-мишенью.
В одном варианте осуществления изобретения по меньшей мере одна из реакционноспособных групп полипептидов является ортогональной к остальным реакционноспособным группам. Использование ортогональных реакционноспособных групп позволяет направлять указанные ортогональные реакционноспособные группы к специфическим сайтам молекулярного ядра. Стратегии связывания, включающие ортогональные реакционноспособные группы, можно использовать для ограничения числа образовавшихся изомеров продукта. Другими словами, выбором отдельных или различных реакционноспособных групп для одной или более из по меньшей мере трех связей к выбранным для остальных из по меньшей мере трех связей, можно достичь конкретного порядка связывания или направления специфических реакционноспособных групп полипептида к специфическим положениям на молекулярном каркасе.
В еще одном варианте осуществления реакционноспособные группы полипептида по изобретению взаимодействуют с молекулярными линкерами, где указанные линкеры способны взаимодействовать с молекулярным каркасом таким образом, что линкер будет вставлен между молекулярным каркасом и полипептидом в конечном связанном состоянии.
В некоторых вариантах осуществления аминокислоты членов библиотек или наборов полипептидов могут быть замещены любой природной или неприродной аминокислотой. Из этих заменяемых аминокислот исключаются те, которые содержат функциональные группы для перекрестного сшивания полипептидов с молекулярным ядром, так что заменяемыми являются одни последовательности петель. Заменяемые полипептидные последовательности имеют произвольные последовательности, константные последовательности или последовательности с произвольными и константными аминокислотами. Аминокислоты с реакционноспособными группами располагаются в определенных положениях в полипептиде, поскольку положение данных аминокислот определяет размер петли.
В одном варианте осуществления полипептид с тремя реакционноспособными группами имеет последовательность (X)lY(X)mY(X)nY(X)o, где Y представляет собой аминокислоту с реакционноспособной группой, Х является произвольной аминокислотой, m и n представляют собой числа в пределах от 3 до 6, определяющие длину промежуточных полипептидных сегментов, которые могут быть одинаковыми или различными, и l и o являются числами в пределах от 0 до 20, определяющими длину фланкирующих полипептидных сегментов.
Для тиол-опосредованных конъюгаций могут быть использованы альтернативы для присоединения молекулярного каркаса к пептиду посредством ковалентных взаимодействий. Альтернативно данные методы можно использовать для модификации полипептида или присоединения к нему дополнительных групп (таких как небольшие представляющие интерес молекулы, которые отличаются от молекулярного каркаса) после того, как они были отобраны или выделены согласно настоящему изобретению - в данном варианте осуществления присоединение не обязательно является ковалентным и может включать нековалентное присоединение. Данные способы можно использовать вместо (или в комбинации с) методов, опосредованных тиолом, посредством получения фага, который экспонирует белки и пептиды, несущие неприродные аминокислоты с требуемыми химическими реакционноспособными группами, в комбинации с небольшими молекулами, которые несут комплементарную реакционноспособную группу, или включением неприродных аминокислот в полипептид, синтезированный химически или рекомбинантно, когда молекула получена после фазы отбора/выделения. Дополнительные детали можно найти в WO 2009/098450 или в публикации Heinis et al., Nat. Chem. Biol., 2009, 5(7), 502-507.
(iv) Комбинирование петель с образованием полиспецифических молекул
Петли из пептидных лигандов или репертуары пептидных лигандов преимущественно комбинируют секвенированием и синтезом de novo полипептида, включающего комбинированные петли. Альтернативно, можно синтезировать нуклеиновые кислоты, кодирующие такие полипептиды.
В тех случаях, когда репертуары предназначены для комбинирования, в частности, репертуары единичных петель, то нуклеиновые кислоты, кодирующие репертуары, преимущественно расщепляют и вновь лигируют с образованием нового репертуара, содержащего различные комбинации петель из составляющих репертуаров. Фаговые векторы могут включать полилинкеры и другие сайты для рестриктаз, которые могут обеспечить уникальные сайты для разрезания и удаления векторов, с получением требуемых полиспецифических пептидных лигандов. Способы работы с фаговыми библиотеками хорошо известны в отношении антител, и они также могут быть использованы в настоящем случае.
(v) Присоединение эффекторных групп и функциональных групп
Эффекторные и/или функциональные группы могут быть присоединены, например, к N- или C-концу полипептида, или к молекулярному каркасу.
Подходящие эффекторные группы включают антитела и их части или фрагменты. Например, эффекторная группа может включать константную область легкой цепи антитела (CL), домен CH1 тяжелой цепи антитела, домен CH2 тяжелой цепи антитела, домен CH3 тяжелой цепи антитела или любую их комбинацию, в дополнении к одному или более доменов константной области. Эффекторная группа также может включать шарнирную область антитела (такую как область, обычно находящаяся между доменами CH1 и CH2 молекулы IgG).
В дополнительном предпочтительном варианте осуществления данного аспекта изобретения эффекторной группой по настоящему изобретению является Fc-область молекулы IgG. Преимущественно, комплекс пептидный лиганд-эффекторная группа по настоящему изобретению содержит или состоит из слитой конструкции пептидный лиганд-Fc, имеющей tβ период полураспада, составляющий одни сутки или более, двое суток или более, 3 суток или более, 4 суток или более, 5 суток или более, 6 суток или более, или 7 суток или более. Наиболее преимущественно, пептидный лиганд по настоящему изобретению содержит или состоит из слитой конструкции пептидный лиганд-Fc, имеющей tβ период полураспада, составляющий одни сутки или более.
Функциональные группы включают, как правило, связывающие группы, лекарственные препараты, реакционноспособные группы для присоединения других молекул, функциональные группы, которые способствуют захвату макроциклических пептидов в клетки, и тому подобное.
Способность пептидов проникать в клетки позволит пептидам проявлять эффективность против внутриклеточных мишеней. Мишени, которые можно оценить пептидами, обладающими способностью проникать в клетки, включают транскрипционные факторы, внутриклеточные сигнальные молекулы, такие как тирозинкиназы и молекулы, участвующие в апоптозном пути. Функциональные группы, которые способствуют проникновению в клетки, включают пептиды или химические группы, которые добавлены к пептиду или молекулярному каркасу. Пептиды, такие как пептиды, полученные из VP22, HIV-Tat, белка гомеобокс дрозофилы (белка Antennapedia), например, описаны в публикациях Chen and Harrison, Biochemical Society Transactions (2007) Volume 35, part 4, p.821, “Cell-penetrating peptides in drug development: enabling intracellular targets” и “Intracellular delivery of large molecules and small peptides by cell penetrating peptides”, Gupta et al., in Advanced Drug Discovery Reviews (2004) Volume 57, 9637. Примеры коротких пептидов, которые, как было показано, являются эффективными в транслокации через плазматические мембраны, включают проникающий пептид из 16 аминокислот из белка Antennapedia дрозофилы (Derossi et al. (1994) J. Biol. Chem. Volume 269, p.10444, “The third helix of the Antennapedia homeodomain translocates through biological membranes”), «модельный амфипатический пептид» из 18 аминокислот (Oehlke et al. (1998) Biochim. Biophys. Acts, Volume 1414, p.127, “Cellular uptake of an alpha-helical amphipathic model peptide with the potential to deliver polar compounds into the cell interior non-endocytically”) и области, богатые аргинином, ТАТ-белка ВИЧ. Непептидные подходы включают использование небольших молекул миметиков или SMOC, которые можно легко присоединить к биологическим молекулам (Okuyama et al. (2007) Nature Methods, Volume 4, p.153, “Small-molecule mimics of an α-helix for efficient transport of proteins into cells”. Другие химические стратегии, заключающиеся в добавлении групп гуанидиния к молекулам, также повышают проникновение в клетки (Elson-Scwab et al. (2007) J. Biol. Chem., Volume 282, p.13585, “Guanidinylated Neomcyin delivers Large Bioactive Cargo into cells through a heparin Sulphate Dependent Pathway”). Молекулы с низкой молекулярной массой, такие как стероиды, могут быть добавлены к молекулярному каркасу для повышения захвата клетками.
Один класс функциональных групп, которые могут быть присоединены к пептидным лигандам, включает антитела и их связывающие фрагменты, такие как Fab, Fv или однодоменные фрагменты. В частности, можно использовать антитела, которые связываются с белками, способные увеличивать период полураспада пептидного лиганда в условиях in vivo.
Также могут быть включены RGD-пептиды, которые связываются с интегринами, которые находятся на многих клетках.
В одном варианте осуществления конструкция пептидный лиганд-эффекторная группа по изобретению имеет tβ период полураспада, выбранный из группы, состоящей из: 12 ч или более, 24 ч или более, 2 суток или более, 3 суток или более, 4 суток или более, 5 суток или более, 6 суток или более, 7 суток или более, 8 суток или более, 9 суток или более, 10 суток или более, 11 суток или более, 12 суток или более, 13 суток или более, 14 суток или более, 15 суток или более, или 20 суток или более. Преимущественно конструкция пептидный лиганд-эффекторная группа или композиция по изобретению будут иметь tβ период полураспада в пределах 12-60 часов. В еще одном варианте осуществления они будут иметь tβ период полураспада, составляющий сутки или более. В еще одном варианте осуществления они будут иметь tβ период полураспада в пределах 12-26 часов.
Функциональные группы включают лекарственные препараты, такие как цитотоксические агенты для лечения рака. Они включают алкилирующие агенты, такие как цисплатин и карбоплатин, а также оксалиплатин, мехлоретамин, циклофосфамид, хлорамбуцил, ифосфамид; антиметаболиты, включающие аналоги пуринов (азатиоприн и меркаптопурин) или аналоги пиримидинов; растительные алкалоиды и терпеноиды, включающие алкалоиды барвинка, такие как винкристин, винбластин, винорелбин и виндезин; подофиллотоксин и его производные этопозид и тенипозид; таксаны, включающие паклитаксел, первоначально известный как таксол; ингибиторы топоизомеразы, включающие камптотецины: иринотекан и топотекан, и ингибиторы топоизомеразы типа II, включающие амсакрин, этопозид, этопозид фосфат и тенипозид. Дополнительные агенты могут включать противоопухолевые антибиотики, которые включают иммуносупрессор дактиномицин (который используется при трансплантации почек), доксорубицин, эпирубицин, блеомицин и другие.
Возможные эффекторные группы также включают ферменты, например, такие как карбоксипептидаза G2 для применения в терапии фермент/пролекарство, где пептидный лиганд заменяет антитела в ADEPT.
(vi) Синтез
Следует отметить, что после выделения или идентификации представляющего интерес полипептида по настоящему изобретению, затем его последующий синтез может быть упрощен, где это возможно. Таким образом, группы или наборы полипептидов необязательно получают технологией рекомбинантной ДНК. Например, может быть определена последовательность представляющих интерес полипептидов, и их можно получить синтетически стандартными методами с последующим взаимодействием с молекулярным каркасом in vitro. После осуществления этого можно использовать обычную химию, поскольку отпадает необходимость сохранять функциональность или целостность генетически кодированной частицы-носителя, такой как фаг. Это дает возможность обеспечить быстрое крупномасштабное получение растворимого вещества для дальнейших последующих экспериментов или валидации. В этом отношении крупномасштабное получение кандидатов или лидеров, идентифицированных способами по настоящему изобретению, можно провести с использованием обычной химии, такой как описана Timmerman et al.
Таким образом, изобретение также относится к производству полипептидов или конъюгатов, выбранных, как описано в данном документе, где производство включает необязательные дополнительные стадии, которые поясняются ниже. В одном варианте осуществления данные стадии проводят на конечном продукте полипептид/конъюгат, полученном скорее химическим синтезом, а не на фаге.
Необязательно аминокислотные остатки в представляющем интерес полипептиде могут быть замещены при производстве конъюгата или комплекса, например, после первоначальной стадии выделения/идентификации.
Пептиды также можно нарастить с включением, например, другой петли и, следовательно, ввести многочисленные специфичности.
Для наращения пептида его можно просто нарастить химически на его N-конце или С-конце, или внутри петель, используя ортогонально защищенные лизины (и аналоги), с использованием обычного твердофазного синтеза или жидкофазного синтеза. Может быть использована обычная химия белков для введения активируемого N- или C-конца. Альтернативно добавления можно сделать путем конденсации фрагментов или нативного химического лигирования, например, как описано (Dawson P.E., Muir T.W., Clark-Lewis I., Kent, SBH, 1994, Synthesis of Proteins by Native Chemical Ligation, Science, 266:776-779), или с использованием ферментов, например, субтилигазы, как описано (Subtiligase: a tool for semisynthesis of proteins, Chang T.K., Jackson D.Y., Burnier J.P., Wells J.A., Proc. Natl. Acad. Sci. USA, 1994, Dec. 20; 91(26):12544-12548 или Bioorganic & Medicinal Chemistry Letters Tags for labeling protein N-termini with subtiligase for proteomics, Volume 18, Issue 22, 15 November 2008, Pages 6000-6003, Tags for labeling protein N-termini with subtiligase for proteomics; Hikari A.I., Yoshihara, Sami Mahrus and James A. Wells).
Альтернативно, пептиды могут быть наращены или модифицированы дополнительным конъюгированием через дисульфидные связи. Это имеет дополнительное преимущество, позволяющее диссоциировать первому и второму пептиду друг от друга в восстанавливающей окружающей среде клетки. В этом случае молекулярный каркас (например, ТВМВ) может быть добавлен во время химического синтеза первого пептида таким образом, чтобы имело место взаимодействие с тремя группами цистеина; затем может быть присоединен дополнительный цистеин к N-концу первого пептида таким образом, чтобы данный цистеин взаимодействовал только со свободным цистеином второго пептида.
Аналогичные методы можно в равной степени применить для синтеза/сочетания двух бициклических и биспецифических макроциклов, потенциально получив тетраспецифическую молекулу.
Кроме того, добавление других функциональных групп или эффекторных групп можно проводить аналогичным методом с использованием соответствующей химии, сочетанием на N- или С-концах или через боковые цепи. В одном варианте осуществления сочетание проводят таким образом, чтобы не блокировалась активность каждой молекулы.
(vii) Модификация пептидов
Для получения бициклических пептидов (бициклов; пептидов, конъюгированных с молекулярными каркасами) в виде подходящей молекулы, подобной лекарственному препарату, который предназначался бы для инъекционного, ингаляционного, интраназального, внутриглазного, перорального или местного введения, следует учитывать ряд свойств. По меньшей мере, необходимо обеспечить в данном лидерном бицикле следующее:
- стабильность к протеазам, независимо от того, касается это стабильности бицикла к плазматическим протеазам, эпителиальным протеазам («связанным с мембранами»), желудочным и кишечным протеазам, протеазам поверхности легких, внутриклеточным протеазам и тому подобное. Стабильность к протеазам должна поддерживаться у различных видов так, чтобы кандидат лидерного бицикла мог быть разработан на животных моделях, а затем с уверенностью введен людям;
- замещение чувствительных к окислению остатков, таких как триптофан и метионин, аналогами, устойчивыми к окислению, для повышения фармацевтической стабильности молекулы;
- требуемую растворимость, которая является функцией соотношения заряженных и гидрофильных остатков к гидрофобным остаткам, что является важным для состава и всасывания;
- правильный баланс заряженных остатков к гидрофобным остаткам, поскольку гидрофобные остатки оказывают влияние на степень связывания с белками плазмы крови и таким образом концентрацию свободной доступной фракции в плазме крови, в то время как заряженные остатки (в частности аргинины) могут оказать влияние на взаимодействие пептида с фосфолипидными мембранами на поверхности клеток. Оба типа остатков в комбинации могут оказывать влияние на период полураспада, объем распределения и воздействие пептидного препарата, и могут быть удлинены по клинической конечной точке. Кроме того, правильная комбинация и число заряженных остатков к гидрофобным остаткам могут снизить раздражение в месте инъекции (в том случае, когда пептидный препарат вводят подкожно);
- удлиненный период полураспада в зависимости от клинического показания и схемы лечения. Может быть рациональным разработать немодифицированную молекулу для непродолжительного применения при остром течении заболевания или разработать бициклический пептид с химическими модификациями, которые удлиняют период полураспада и, следовательно, они являются оптимальными для лечения хронических заболеваний.
Имеются многочисленные подходы для стабилизации терапевтических пептидов-кандидатов к протеолитическому разложению, и они совпадают с таковыми, используемыми в области пептидомиметиков (см. обзоры Gentilucci et al., Curr. Pharmaceutical Design, (2010), 16, 3185-3203 and Nestor et al., Curr. Medicinal Chem. (2009), 16, 4399-4418).
Они включают:
циклизацию пептида;
N- и С-концевое кэппирование, обычно N-концевое ацетилирование и С-концевое амидирование;
аланиновые сканы для выявления и потенциального удаления сайта(ов) протеолитической атаки;
замещение D-аминокислотами для анализа стерических требований аминокислотных боковых цепей с целью повышения протеолитической стабильности стерическим затруднением и расположенностью D-аминокислот к стабилизации β-поворотных конформаций (Tugyi et al. (2005) PNAS, 102(2), 413-418);
замещение N-метил/N-алкиламинокислотами для придания протеолитической защиты путем непосредственной модификации неустойчивой амидной связи (Fiacco et al., Chembiochem. (2008), 9(14), 2200-2203). N-метилирование также оказывает сильное влияние на углы закручивания пептидной связи, и полагают, что оно способствует проникновению в клетки и пероральной доступности (Biron et al. (2008), Angew. Chem. Int. Ed., 47, 2595-2599);
включение неприродных аминокислот, т.е. использованием:
- изостерических/изоэлектрических боковых цепей, которые не распознаются протеазами, но не оказывают эффекта на целевую активность;
- аминокислотных боковых цепей со структурными ограничениями так, чтобы протеолитический гидролиз соседней пептидной связи был конформационно и стерически затруднен. В частности, это касается аналогов пролина, объемных боковых цепей, Сα-двузамещенных производных (где самым простым производным является Aib, H2N-C(CH3)2-COOH) и циклоаминокислот, где простым соединением является аминоциклопропилкарбоновая кислота).
заменители пептидных связей, и их примеры включают:
- N-алкилирование (см. выше, т.е. CO-NR)
- восстановленные пептидные связи (CH2-NH-)
- пептоиды (N-алкиламинокислоты, NR-CH2-CO)
- тиоамиды (CS-NH)
- азапептиды (CO-NH-NR)
- транс-алкен (RHC=C-)
- ретро-инверсо (NH-CO)
- заменители мочевины (NH-CO-NHR)
модуляцию длины пептидного остова
- т.е. β2/3-аминокислоты (NH-CR-CH2-CO, NH-CH2-CHR-CO);
замены на альфа-углероде в аминокислотах, что затрудняет конформации скелета, самым простым производным является аминоизомасляная кислота (Aib).
Следует явно отметить, что некоторые из этих модификаций могут также служить для преднамеренного повышения активности пептида против мишени или, например, для идентификации сильных заместителей для чувствительных к окислению аминокислот (Trp и Met). Также следует отметить, что лидерный бицикл Ас-06-34-18(ТМВ)-NH2 уже имеет две модификации, которые придают устойчивость к протеолитическому расщеплению, это N/C-концевое кэппирование и (би)циклизация.
(В) Репертуары, ряды и группы полипептидных лигандов
(i) Конструкция библиотек
Библиотеки, предназначенные для отбора, могут быть сконструированы с использованием методов, известных в данной области, например, как описано в WO 2004/077062, или биологических систем, включая фаговые векторные системы, описанные в данном документе. В данной области известны другие векторные системы, и они включают другой фаг (например, фаг лямбда), бактериальные плазмидные экспрессионные векторы, эукариотические клеточные экспрессионные векторы, включающие дрожжевые векторы и тому подобное. Например, см. WO 2009/098450 или публикацию Heinis et al., Nat. Chem. Biol., 2009, 5(7), 502-507.
Небиологические системы, такие как описаны в WO 2004/077062, основаны на подходах обычного химического скрининга. Они просты, но у них отсутствует активность биологических систем, поскольку это невозможно, или, по меньшей мере, очень затруднительно, провести скрининг крупных библиотек пептидных лигандов. Однако они применимы, например, только когда требуется подвергнуть скринингу небольшое количество пептидных лигандов. Скрининг с использованием таких отдельных тестов, однако, может быть длительным по времени, и число уникальных молекул, которые можно тестировать на связывание со специфической мишенью, обычно не превышает 106 химических молекул.
Напротив, биологические методы скрининга или селекции, как правило, позволяют провести оценку большего количества различных молекул. Таким образом, биологические методы могут быть использованы в применении изобретения. В биологических методах молекулы тестируют в одном реакционном сосуде и молекулы с благоприятными свойствами (т.е. связыванием) физически отделяют от неактивных молекул. Имеются стратегии селекции, которые позволяют получать и анализировать одновременно более 1013 отдельных соединений. Примерами методов эффективной аффинной селекции являются фаговый дисплей, рибосомальный дисплей, дисплей мРНК, дрожжевой дисплей, бактериальный дисплей или РНК/ДНК аптамер. Данные биологические методы селекции in vitro являются общими в том отношении, что репертуары лигандов кодируются ДНК или РНК. Они обеспечивают воспроизведение и идентификацию выбранных лигандов секвенированием. Технология фагового дисплея, например, использовалась для выделения антител с очень высокой аффинностью связывания практически к любой мишени.
При использовании биологической системы, после выбора векторной системы, одну или более нуклеиновокислотных последовательностей, кодирующих представляющие интерес полипептиды, клонируют в вектор библиотеки, причем можно получить разнообразие клонированных молекул посредством мутагенеза до экспрессии; альтернативно, кодированные белки можно экспрессировать и выбрать до мутагенеза и провести дополнительные раунды селекции.
Мутагенез нуклеиновокислотных последовательностей, кодирующих структурно оптимизированные полипептиды, проводят стандартными молекулярными методами. Особое применение имеет полимеразная цепная реакция или ПЦР (Mullis and Faloona (1987) Methods Enzymol., 155:335, этот источник включен в данный документ посредством ссылки). ПЦР, в которой используются многочисленные циклы репликации ДНК, катализируемой термостабильной ДНК-зависимой ДНК-полимеразой для амплификации представляющей интерес последовательности-мишени, хорошо известна в данной области. Конструирование различных библиотек антител обсуждалось в публикации Winter et al. (1994) Ann. Rev. Immunology 12, 433-435, и в источниках, цитированных там.
Альтернативно, с учетом короткой длины полипептидов по изобретению, варианты предпочтительно синтезируют de novo и вставляют в подходящие экспрессионные векторы. Синтез пептидов можно провести стандартными методами, известными в данной области, которые были описаны выше. Широко известны автоматические пептидные синтезаторы, такие как Applied Biosystems ABI 433 (Applied Biosystems, Foster City, CA, USA).
(ii) Генетически кодированное разнообразие
В одном варианте осуществления представляющие интерес полипептиды генетически кодированы. Это дает преимущество повышенного разнообразия вместе с простотой манипуляций. Примером библиотеки генетически кодированных полипептидов является библиотека дисплея мРНК. Другим примером является воспроизводимая библиотека пакета генетического дисплея (rgdp), такая как библиотека фагового дисплея. В одном варианте осуществления представляющие интерес полипептиды генетически кодированы в виде библиотеки фагового дисплея.
Таким образом, в одном варианте осуществления комплекс по изобретению включает воспроизводимый пакет генетического дисплея (rgdp), такой как фаговая частица. В данных вариантах осуществления нуклеиновая кислота может быть включена в фаговый геном. В этих вариантах осуществления полипептид может состоять из оболочки фага.
В некоторых вариантах осуществления изобретение можно использовать для получения генетически кодированной комбинаторной библиотеки полипептидов, которые получены трансляцией ряда нуклеиновых кислот в соответствующие полипептиды и молекулы, связывающие указанный молекулярный каркас с указанными полипептидами.
Генетически кодированную комбинаторную библиотеку полипептидов можно получить фаговым дисплеем, дрожжевым дисплеем, рибосомальным дисплеем, бактериальным дисплеем или дисплеем мРНК.
Способы и методологию постановки фагового дисплея можно найти в WO 2009/098450.
В одном варианте осуществления скрининг можно проводить контактированием библиотеки, набора или группы полипептидных лигандов с мишенью и выделением одного или более членов, которые связываются с указанной мишенью.
В еще одном варианте осуществления отдельные члены указанной библиотеки, набора или группы контактируют с мишенью при скрининге, и идентифицируются члены указанной библиотеки, которые связываются с указанной мишенью.
В еще одном варианте осуществления члены указанной библиотеки, набора или группы одновременно контактируют с мишенью, и отбираются члены, которые связываются с указанной мишенью.
Мишень(и) может представлять собой пептид, белок, полисахарид, липид, ДНК или РНК.
Мишень(и) может представлять собой рецептор, лиганд рецептора, фермент, гормон или цитокин.
Мишень может быть прокариотическим белком, эукариотическим белком или белком простейших. Более конкретно, лиганд мишени может представлять собой белок млекопитающих или белок насекомых, или бактериальный белок или грибковый белок, или вирусный белок.
Лиганд мишени может представлять собой фермент, такой как протеаза.
Следует отметить, что изобретение также включает полипептидные лиганды, выделенные в результате скрининга по изобретению. В одном варианте осуществления способ(ы) скрининга по изобретению дополнительно включает стадию: получения количества полипептида, выделенного как способного связываться с указанными мишенями.
Также изобретение относится к пептидным лигандам, содержащим более чем две петли. Например, трициклические полипептиды, соединенные с молекулярным каркасом, могут быть получены присоединением N- и C-концов бициклического полипептида, соединенного с молекулярным каркасом по настоящему изобретению. Таким образом, соединенные N- и C-концы создают третью петлю, создавая трициклический полипептид. Для данного варианта осуществления не требуется проводить его на фаге, а он может быть проведен на конъюгате полипептид-молекулярный каркас, описанном в данном документе. Присоединение N- и C-концов является предметом обычной химии пептидов. В случае необходимости в дополнительном указании, С-конец может быть активирован, и/или N- и C-концы могут быть наращены, например, добавлением цистеина к каждому концу и затем их соединением дисульфидной связью. Альтернативно соединение может быть проведено путем использования области линкера, включенного в N/C-концы. Альтернативно N- и C-концы могут быть соединены обычной пептидной связью. Альтернативно можно использовать любые другие походящие способы соединения N- и C-концов, например, N-C-циклизацию можно провести обычными методами, например, раскрытыми в публикациях Linde et al. Peptide Science 90, 671-682 (2008) “Structure-activity relationship and metabolic stability studies of backbone cyclization and N-methylation of melanocortin peptides” или Hess et al. J. Med. Chem. 51, 1026-1034 (2008) “Backbone cyclic peptidomimetic melanocortin-4 receptor agonist as novel orally administered drug lead for treating obesity”. Одним преимуществом таких трициклических молекул является возможность избежать протеолитического разрушения свободных концов, в частности, под действием экзопротеазы. Другое преимущество трициклического полипептида данной природы заключается в том, что третья петля может быть использована для общих применимых функций, таких как связывание с BSA, вхождение в клетку или эффекты транспорта, мечение или любое другое такое применение. Следует отметить, что данная третья петля обычно не доступна для селекции (поскольку она не продуцируется на фаге, а продуцируется только на конъюгате полипептид-молекулярный каркас) и, таким образом, ее применение для других таких биологических функций по-прежнему остается петлям 1 и 2 для селекции/создания специфичности.
(iii) Выделение фага
Можно использовать любые подходящие способы выделения фага. Обычные методы можно применять в настоящем изобретении. Например, фаг можно выделить фильтрацией или преципитацией, такой как преципитация с ПЭГом; фаговые частицы можно получить и выделить преципитацией с полиэтиленгликолем (ПЭГом), как описано ранее. Детали можно найти в WO 2009/098450.
В случае необходимости в получении дальнейших указаний, можно обратиться к публикации Jespers et al. (Protein Engineering Design and Selection 2004 17(10):709-713. “Selection of optical biosensors from chemisynthetic antibody libraries”). В одном варианте осуществления фаг может быть выделен, как описано в указанном документе. Текст данной публикации специально включен в данный документ посредством ссылки в отношении способа выделения фага; в частности, делается ссылка на раздел материалов и способов, начиная с правой колонки на странице 709 Jespers et al.
Кроме того, фаг можно выделить, как описано в публикации Marks et al. J. Mol. Biol., vol. 222, pp.581-597, которая специально включена в данный документ посредством ссылки в отношении конкретного описания получения/выделения фага.
(iv) Реакционная химия
Настоящее изобретение делает возможным использование химических условий для модификации полипептидов, которые преимущественно сохраняют функцию и целостность генетически кодированного элемента продукта. В частности, когда генетически кодированный элемент представляет собой полипептид, экспонированный на поверхности фага, кодирующего его, химия преимущественно не должна нарушать биологическую целостность фага. В общем, условия приведены в WO 2009/098450.
(С) Применение полипептидных лигандов по изобретению
Полипептидные лиганды, выбранные способом по настоящему изобретению, можно использовать в терапевтических и профилактических применениях in vivo, диагностических применениях in vitro и in vivo, анализе in vitro и применениях в качестве реагента и тому подобное. Лиганды, обладающие выбранными уровнями специфичностями, являются пригодными в применениях, которые включают тестирование на животных, отличных от человека, когда желательна перекрестная реактивность, или в диагностических применениях, где перекрестную реактивность с гомологами или паралогами требуется тщательно контролировать. В некоторых применениях, таких как вакцинные применения, способность вызывать иммунный ответ на заранее определенные уровни антигенов, можно использовать для разработки вакцины против специфических болезней и патогенов.
По существу чистые пептидные лиганды по меньшей мере с 90-95% гомогенностью являются предпочтительными для введения млекопитающему, а с 98-99% или более высокой гомогенностью являются наиболее предпочтительными для фармацевтических применений, особенно, когда млекопитающее является человеком. После очистки, частичной или до требуемой гомогенности, выбранные полипептиды могут быть использованы в диагностических или терапевтических целях (включая экстракорпорально), или при разработке и постановке аналитических методов, иммунофлуоресцентного окрашивания и тому подобное (Lefkovite and Pernis (1979 и 1981) Immunological Methods, Volumes I and II, Academic Press, NY).
Пептидные лиганды по настоящему изобретению, как правило, найдут применение в профилактике, подавлении или лечении воспалительных состояний, аллергических реакций гиперчувствительности, рака, бактериальных или вирусных инфекций, и аутоиммунных расстройств (которые включают, но не ограничиваются ими, диабет типа I, рассеянный склероз, ревматоидный артрит, системную красную волчанку, болезнь Крона и тяжелую миастению).
В настоящей заявке термин «профилактика» включает введение протективной композиции до развития заболевания. «Подавление» относится к введению композиции после индуктивного события, но до появления клинических признаков заболевания. «Лечение» включает введение протективной композиции после того, как симптомы становятся выраженными.
Существуют модельные системы на животных, которые могут быть использованы для скрининга эффективности пептидных лигандов в защите от заболеваний или их лечении. Применение модельных систем на животных облегчается настоящим изобретением, что позволяет разработать полипептидные лиганды, которые перекрестно реагируют с человеческими и животными мишенями, для обеспечения применения животных моделей.
В данной области известны методы тестирования системной красной волчанки (SLE) на чувствительных мышах (Knight et al. (1978) J. Exp. Med., 147:1653; Reinersten et al. (1978) New Eng. J. Med., 299: 515). Тяжелую миастению (MG) тестируют на мышах-самках SJL/J, индуцируя заболевание растворимым белком AchR от других видов (Lindstrom et al. (1988) Adv. Inzn7unol., 42:233). Артрит индуцируют на чувствительных штаммах мышей введением коллагена типа II (Stuart et al. (1984) Ann. Rev. Immunol., 42:233). Описана модель, на которой адъювантный артрит воспроизводят на чувствительных крысах введением микобактериального белка теплового шока (Van Eden et al. (1988) Nature, 331:171). Тиреоидит индуцируют у мышей введением тироглобулина, как описано (Maron et al. (1980) J. Exp. Med., 152:1115). Инсулинозависимый сахарный диабет (IDDM) проявляется в естественных условиях или его можно индуцировать на некоторых штаммах, таких как описано Kanasawa et al. (1984) Diabetologia, 27:113. EAE на мышах и крысах служит в качестве модели рассеянного склероза человека. На данной модели демиелинизирующее заболевание индуцируют введением основного белка миелина (см. Paterson (1986) Textbook of Immunopathology, Mischer et al., eds., Grune and Stratton, New York, pp. 179-213; McFarlin et al. (1973) Science, 179:478 и Satoh et al. (1987) J. Immunol., 138:179).
Как правило, пептидные лиганды по настоящему изобретению будут использоваться в очищенной форме вместе с фармакологически подходящими носителями. Обычно, данные носители включают водные или спиртовые/водные растворы, эмульсии или суспензии, включающие физиологический раствор и/или забуференные среды. Растворители для парентерального введения включают раствор хлорида натрия, раствор декстрозы Рингера, раствор декстрозы и хлорида натрия и лактированный раствор Рингера. Подходящие физиологически приемлемые адъюванты, при необходимости для хранения полипептидного комплекса в суспензии, могут быть выбраны из загустителей, таких как карбоксиметилцеллюлоза, поливинилпирролидон, желатин и альгинаты.
Растворители для внутривенного введения включают жидкость и питательные добавки и электролитные добавки на основе раствора декстрозы Рингера. Также могут присутствовать консерванты и другие добавки, такие как антимикробные агенты, антиоксиданты, хелатообразователи и инертные газы (Mack (1982) Remington’s Pharmaceutical Sciences, 16th Edition).
Пептидные лиганды по настоящему изобретению можно использовать в виде вводимых отдельно композиций или в комбинации с другими агентами. Они могут включать антитела, фрагменты антител и различные иммунотерапевтические лекарственные препараты, такие как циклоспорин, метотрексат, адриамицин или цисплатин, и иммунотоксины. Фармацевтические композиции могут включать «коктейли» (смеси) различных цитотоксических или других агентов в комбинации с выбранными антителами, рецепторами или связывающими белками по изобретению, или даже комбинации выбранных полипептидов по настоящему изобретению, обладающие различными специфичностями, такие как полипептиды, выбранные с использованием различных лигандов мишени, независимо от того, были они объединены до введения или нет.
Путь введения фармацевтических композиций по изобретению может быть любым из путей, обычно известных специалистам в данной области. Для терапии, включая без ограничения иммунотерапию, выбранные антитела, рецепторы или связывающие белки по изобретению можно вводить любому пациенту согласно обычным методам. Введение может быть проведено любым способом, включая парентеральный, внутривенный, внутримышечный, внутрибрюшинный, трансдермальный, пульмонарный путь, или также соответственно прямой инфузией с помощью катетера. Доза и частота введения будет зависеть от возраста, пола и состояния пациента, сопутствующего введения других лекарственных препаратов, противопоказаний и других факторов, которые следует учитывать клиницисту.
Пептидные лиганды по данному изобретению можно лиофилизовать для хранения и восстановить в подходящем носителе перед применением. Было показано, что данный способ является эффективным, и могут быть использованы известные в данной области методики лиофилизации и восстановления. Специалистам в данной области, очевидно, понятно, что лиофилизация и восстановление могут привести к различной степени потери активности, и что уровни применения можно скорректировать для компенсации.
Композиции, содержащие пептидные лиганды по настоящему изобретению или их смесь, можно вводить для профилактического и/или терапевтического лечения. В некоторых терапевтических применениях адекватное количество для достижения по меньшей мере ингибирования, подавления, модуляции, гибели популяции выбранных клеток, или некоторого другого оцениваемого параметра, определяется как «терапевтически эффективная доза». Количества, необходимые для достижения данной дозы, будут зависеть от тяжести заболевания и общего состояния собственной иммунной системы пациента, но обычно они находятся в пределах от 0,005 до 5,0 мг выбранного пептидного лиганда на кг массы тела, при том, что обычно используют дозы от 0,05 до 2,0 мг/кг/дозу. Для профилактических применений композиции, содержащие пептидные лиганды по настоящему изобретению или их смеси, можно вводить в аналогичных или даже более низких дозах.
Композиция, содержащая пептидный лиганд по настоящему изобретению, может быть использована в профилактических и терапевтических целях для изменения, инактивации, гибели или удаления выбранной клеточной популяции у млекопитающего. Кроме того, выбранные репертуары полипептидов, описанных в данном документе, можно использовать экстракорпорально или избирательно in vitro для индукции гибели, истощения или эффективного удаления иным образом клеточной популяции-мишени из гетерогенной смеси клеток. Кровь от млекопитающего можно объединить экстракорпорально с выбранными пептидными лигандами, посредством чего нежелательные клетки гибнут или удаляются иначе из крови с обратным введением млекопитающему с использованием обычных способов.
(D) Мутация полипептидов
Требуемое разнообразие обычно получают изменением выбранной молекулы в одном или более положений. Выбирают положения, предназначенные для изменения, так, чтобы сконструировать библиотеки для каждого отдельного положения в последовательностях петель. Там, где это подходит, одно или более положений можно исключить из процесса селекции, например, когда становится очевидным, что эти положения не доступны для мутации без потери активности.
Затем вариация может быть достигнута рандомизацией, во время которой постоянную аминокислоту замещают любой аминокислотой или ее аналогом, природной или синтетической, с получением очень большого количества вариантов, или замещением постоянной аминокислоты одной или более определенной подгруппой аминокислот с получением более ограниченного числа вариантов.
Сообщалось о различных способах введения такого разнообразия. Также в данной области хорошо известны способы мутации выбранных положений, и они включают применение ошибочно спаренных олигонуклеотидов или вырожденных олигонуклеотидов с использованием или без использования ПЦР. Например, было получено несколько библиотек синтетических антител направленными мутациями в антигенсвязывающих петлях. Такие же методы могут быть использованы в контексте настоящего изобретения. Например, Н3-область человеческого Fab, связывающего столбнячный токсоид, была рандомизирована с получением ряда новых специфичностей связывания (Barbas et al. (1992) Proc. Natl. Acad. Sci. USA, 89:4457). Произвольные или полупроизвольные Н3- и L3-области присоединяли к сегментам V-гена зародышевой линии с получением крупных библиотек с мутированными каркасными областями (Hoogenboom- & Winter (1992) J. Mol. Biol., 227: 381; Barbas et al. (1992) Proc. Natl. Acad. Sci. USA, 89: 4457; Nissim et al. (1994) EMBO J., 13:692; Griffiths et al. (1994) EMBO J., 13:3245; De Kruif et al. (1995) J. Mol. Biol., 248:97). Такое разнообразие было расширено с включением некоторых или всех других антигенсвязывающих петель (Crameri et al. (1996) Nature Med., 2:100; Riechmann et al. (1995) BiolTechnology, 13:475; Morphosys, WO 97/08320, выше).
Однако поскольку полипептиды, используемые в настоящем изобретении, являются значительно более мелкими, чем антитела, то предпочтительным способом является синтез мутантных полипептидов de novo. Выше был описан мутагенез структурированных полипептидов при конструировании библиотек.
Изобретение дополнительно описано ниже со ссылкой на следующие примеры.
Примеры
Материалы и методы
Клонирование фаговых библиотек
Фаговые библиотеки получали согласно методу Heinis et al., Nat. Chem. Biol., 2009, 5(7), 502-507. В методе, описанном Heinis et al., гены, кодирующие полурандомизированный пептид с последовательностью Xaa-Cys-(Xaa)3-Cys-(Xaa)3-, линкер Gly-Gly-Ser-Gly и два домена D1 и D2 без дисульфидных связей (Kather et al., J. Mol. Biol., 2005, 354(3), 666-678) клонировали в правильной ориентации в фаговый вектор fd0D12 с получением «библиотеки 3×3». Гены, кодирующие репертуар пептидов, и два гена 3 доменов получали постадийно в двух последовательных реакциях ПЦР. Во-первых, гены D1 и D2 амплифицировали ПЦР с двумя праймерами prepcr (5’-GGCGGTTCTGGCGCTGAAACTGTTGAAAGTAG-3’) и sfi2fo (5’-GAAGCCATGGCCCCCGAGGCCCCGGACGGAGCATTGACAGG-3’; сайт рестрикции подчеркнут) с использованием вектора fdg3p0ss21 (Kather et al., J. Mol. Biol., 2005, 354(3), 666-678) в качестве матрицы. Во-вторых, ДНК, кодирующую произвольные пептиды, присоединяли в реакции ПЦР с использованием праймера sficx3ba: 5’-TATGCGGCCCAGCCGGCCATGGCANNKTGTNNKNNKNNKTGCNNKNNKNNKNNKTGTNNKGGGCGGTTCTGGCGCTG-3’ (сайт рестрикции подчеркнут) и sfi2fo. Лигирование 55 и 11 мкг Stil-расщепленной плазмиды fd0D12 и продукта ПЦР давало 5,6×108 колоний на чашках 20×20 см 2YT с хлорамфениколом (30 мкг/мл). Колонии соскребали с чашек в среду 2YT с добавлением 15% глицерина и хранили при -80°С. При конструировании библиотек, описанных в данном документе, использовали тот же метод с получением полурандомизированного пептида Pro-Ala-Met-Ala-Cys-(Xaa)3-Cys-(Xaa)3-Cys для библиотеки 3×3, например, и, следовательно, замещали последовательность праймера sficx3ba на: 5’-TATGCGGCCCAGCCGGCCATGGCATGTNNKNNKNNKTGCNNKNNKNNKTGTGGCGGTTCTGGCGCTG-3’. Получали библиотеки с другими длинами петель, следуя той же методологии.
Селекция фаговых библиотек
Стоки фаговых библиотек в глицерине разводили до оптической плотности OD600=0,1 в 500 мл среды 2YT/хлорамфеникол (30 мкг/мл) и фаг культивировали при 30°С в течение ночи (15-16 ч). Фаг выделяли и химически модифицировали, как описано Heinis et al., Nat. Chem. Biol., 2009, 5(7), 502-507, биотинилированный hPK (3 мкг) (IHPKA, из плазмы человека, Innovative Research, Novi, MI, США) инкубировали с 50 мкл предварительно промытых магнитных гранул со стрептавидином (Dynal, M-280 производства Invitrogen, Paisley, UK) в течение 10 мин при комнатной температуре. Гранулы 3 раза промывали перед блокированием 0,5 мл буфера для промывания (10 мМ Трис-Cl, рН 7,4, 150 мМ NaCl, 10 мМ MgCl2, 1 мМ CaCl2), содержащего 1% BSA и 0,1% Твин 20, в течение 30 мин при комнатной температуре и встряхивании. Химически модифицированный фаг (обычно 1010-1011 t.u., растворенный в 2 мл буфера для промывания) одновременно блокировали добавлением 1 мл буфера для промывания, содержащего 3% BSA и 0,3% Твин 20. Затем блокированные гранулы смешивали с блокированным, химически модифицированным фагом и инкубировали в течение 30 минут на вращающемся роторе при комнатной температуре. Гранулы промывали 8 раз буфером для промывания, содержащим 0,1% Твин 20, и дважды буфером для промывания перед инкубацией со 100 мкл 50 мМ глицина, рН 2,2, в течение 5 минут. Элюированный фаг переносили в 50 мкл 1М Трис-Cl, рН 8, для нейтрализации, инкубировали с 30 мл клеток TG1 при OD600=0,4 в течение 90 минут при 37°С и клетки высевали на больших чашках со средой 2YT/хлорамфеникол. Проводили один или два дополнительных раунда пэннинга с использованием аналогичных методов. Во втором раунде селекции покрытые нейтравидином магнитные гранулы использовали для предупреждения обогащения стрептавидин-специфическими пептидами. Покрытые нейтравидином гранулы получали взаимодействием 0,8 мг нейтравидина (Pierce, Rockford, IL, США) с 0,5 мл активированных тозилом магнитных гранул (Dynal, M-280, производства Invitrogen, Paisley, UK) согласно инструкциям изготовителя.
Клонирование и экспрессия человеческого, обезьяньего и крысиного РК
Каталитический домен человеческого, обезьяньего и крысиного РК экспрессировали в клетках млекопитающих в виде неактивного предшественника, содержащего пропептид, соединенный через N-конец посредством сайта расщепления proTEV с каталитическим доменом. Экспрессионный вектор клонировали и белок экспрессировали, активировали и выделяли, как описано следующим образом. Синтетические гены, кодирующие сигнальную последовательность РК, полигистидиновую метку, сайт отщепления proTEV, зрелый каталитический домен РК и стоп-кодон, получали от Geneart (Regensburg, Germany) (Вспомогательные материалы). Готовили плазмидную ДНК, содержащую синтетические гены РК человека, обезьяны (Macaca mulatta) и крысы и гены переносили в экспрессионный вектор млекопитающих pEXPR-IBA42 (IBA Biotechnology, Göttingen, Germany) с использованием пары рестриктаз Xhol и HindIII (Fermentas, Vilnius, Latvia) и ДНК-лигазы Т4 (Fermentas). Лигированные плазмиды трансформировали в синие электрокомпетентные клетки XL-1 (Stratagene, Sante Clara, USA) и высевали на чашках с агаром 2YT, содержащим ампициллин (10 мкг/мл). Получали ДНК из трех экспрессионных векторов (названных mPK, rPK и hPK) и правильные последовательности подтверждали секвенированием ДНК (Macrogen, Seoul, South Korea).
Три ортологичных плазматических калликреина экспрессировали в клетках млекопитающих следующим образом. 50 мл адаптированных к суспензии клеток HEK-293 культивировали в бессывороточной среде ExCell 293 (SAFC Biosciences, St. Louis, MO) в присутствии 4 мМ глутамина и ингибитора гистондеацетилазы вальпроевой кислоты (3,75 мМ) в колбе емкостью 100 мл на орбитальном шейкере при 180 об/мин в термостате ISF-4-W (Kühner A.G, Birsfelden, Switzerland) при 37°С в присутствии 5% СО2. Клетки почек эмбрионов (НЕК-293) с высоким титром клеток (20×106 клеток/мл) (Backliwal et al., Biotechnol. Bioeng., 2008, 99(3), 721-777) трансфицировали тремя плазмидами (300 мкг/мл), используя линейный полиэтиленимин (PEI, Polysciences, Eppenheim, Germany). В конце 7-суточной продуктивной фазы клетки собирали центрифугированием при 2500 об/мин в течение 15 мин при 4°С. Любой дополнительный дебрис удаляли из среды фильтрованием через мембраны PES 0,45 мкм (Filter-top 250 мл с низким связыванием белков ТРР). Белок с полигистидиновой меткой очищали Ni-аффинной хроматографией с использованием смолы Ni-NTA, буфером для промывания (500 мМ NaCl, 25 мМ Na2HPO4, рН 7,4) и элюирующего буфера (500 мМ NaCl, 25 мМ Na2HPO4, рН 7,4, 500 мМ имидазола). Белок частично активировали (50 единицами) proTEV (Promega, Madison, Wisconsin, USA) и дополнительно очищали Ni-аффинной хроматографией и гель-фильтрацией (колонка PD10, 150 мМ NaCl, 0,5 мМ ЭДТА, 50 мМ HEPES, рН 7).
Разработка полипептидов с повышенной связывающей активностью
Рандомизация отдельных положений
Конструирование библиотек: для картирования аминокислот в бициклических пептидах, связывающихся с калликреином, конструировали набор небольших библиотек. Для бицикла, состоящего из 2 петель из 5 остатков, получали 10 библиотек, каждая с рандомизацией в конкретном кодоне в пептидной последовательности. Для каждой библиотеки конструировали олигонуклеотиды для мутирования геномной ДНК фага сайт-направленным мутагенезом. Мутагенез включал рандомизацию представляющего интерес кодона (изменение в NNS) и удаление уникального сайта рестрикции ApaL1 из геномной последовательности матрицы. Продукт мутагенеза выделяли с помощью набора для выделения QiAgen QIAquick PCR с элюированием ультрачистой водой. Каждую библиотеку использовали для трансформирования по отдельности TG1 E. coli электропорацией на приборе BioRad Micropulser (программа Ec1) и с кюветой BioRad длиной 1 мм. После извлечения в течение 1 ч при 37°C в 1 мл среды SOC трансформанты библиотеки культивировали в течение ночи в 25 мл бульона 2TY, содержащего антибиотик только для селективного роста трансформантов библиотеки. Бактерии собирали центрифугированием и ДНК фагов библиотеки выделяли из E. coli с использованием набора QIAgen Plasmid Plus Midi и элюировали дистиллированной водой. Выделенную ДНК расщепляли ApaL1 в течение 2 часов в буфере New England Biolabs 4 для удаления исходного материала. После расщепления ДНК повторно очищали с использованием набора для очистки QIAgen PCR (как описано выше) и использовали для трансформации TG1 (электропорация, как описано выше). После извлечения в течение 1 часа в SOC трансформанты высевали на чашки с агаром LB, содержащим селективный антибиотик, и колонии культивировали в течение ночи при 37°С.
Анализ связывания отдельных клонов: колонии трансформантов библиотеки произвольно собирали и культивировали в виде отдельных культур в бульоне 2TY, содержащем селективный антибиотик. Собранные колонии подвергали секвенированию ДНК с использованием секвенатора QIAgen PyroMark Q96 DNA для установления аминокислотной замены, присутствующей в каждом клоне. После выделения клон с каждой уникальной заменой анализировали на связывание с человеческим плазматическим калликреином следующим образом. Собирали из культуры супернатант, содержащий фаг, и фаг циклизовали трис-бромметилбензолом (TBMB) с использованием методов Heinis et al. (Nature Chemical Biology, vol.5, pp.502-507 (2009)). Выделенный таким способом фаг анализировали на связывание с биотинилированным человеческим плазматическим калликреином с использованием гомогенного планшетного анализа; анализ результатов проводили на ридере для планшетов BMG Labtech Pherastar FS. Определяли средние значения (медианы) количественных данных по связыванию по трем параллельным анализированным пробам и выражали в виде сигнал:фон (где фон представлял собой пробу, анализированную без вещества-мишени). Сигнал:фон выражали в виде % от параллельной исходной пробы. Короткие отрезки, показывающие ошибку, означают стандартное отклонение от среднего значения. Приведенные данные анализа представляют по меньшей мере два независимых опыта. Данные анализа коррелировали с пептидными последовательностями. Замены, отмеченные серым цветом, не тестировали (клон не выделяли при произвольном отборе проб библиотек). Образец не связывающего (произвольного) бицикла анализировали параллельно для установления базовой линии при анализе.
Рандомизация пептидных доменов
Конструирование библиотек: небольшие фаговые библиотеки получали с использованием методов Heinis et al., описанных в разделе «Клонирование фаговых библиотек» выше. Праймер sficx3ba модифицировали таким образом, что фрагмент, кодирующий бицикл, был основан на ДНК-последовательности исходного бицикла 5×5 (5×5: две петли из 5 остатков) только с 4-6 кодонами, рандомизированными к NNS. Рандомизированные кодоны представляли собой кодоны, кодирующие представляющий интерес пептидный домен/мотив.
Анализ связывания отдельных клонов: собирали колонии трансформантов библиотек или колонии, представляющие собой результат селекции, и культивировали в виде отдельных культур в бульоне 2TY, содержащем селективный антибиотик. Собранные колонии подвергали секвенированию ДНК с использованием секвенатора QIAgen PyroMark Q96 DNA для установления аминокислотной замены, присутствующей в клоне, и анализировали на связывание с человеческим плазматическим калликреином следующим образом. Собирали из культуры супернатант, содержащий фаг, и фаг циклизовали трис-бромметилбензолом (TBMB) с использованием методов Heinis et al. (Nature Chemical Biology, vol.5, pp.502-507) (2009)). Выделенный этим способом фаг анализировали на связывание с биотинилированным человеческим плазматическим калликреином, используя гомогенный планшетный анализ связывания; анализ результатов проводили на ридере для планшетов BMG Labtech Pherastar FS. Определяли средние значения (медианы) количественных данных по связыванию по трем параллельным анализированным пробам и выражали в виде сигнал:фон. Приведенные данные анализа представляют по меньшей мере два независимых опыта. Данные анализа коррелировали с пептидными последовательностями.
Синтез и очистка бициклических пептидов
Пептидные последовательности приведены в таблицах 1 и 2. Синтез пептидов был основан на Fmoc-химии с использованием пептидного синтезатора Symphony производства Peptide Instruments. Использовали обычные Fmoc-аминокислоты (Sigma, Merck) со следующими защитными группами боковых цепей: Arg(Pbf); Asn(Trt); Asp(OtBu); Cys(Trt); Glu(OtBu); Gln(Trt); His(Trt); Lys(Boc); Ser(tBu); Thr(tBu): Trp(Boc); Tyr(tBu) (Sigma). Агентом для сочетания был HCTU (Pepceuticals), диизопропилэтиламин (DIPEA, Sigma), который использовали в виде основания, и снятие защиты проводили 20% пиперидином в ДМФА (AGTC). Синтез проводили в объеме 100 мкмоль с использованием 0,37 ммоль/г смолы Fmoc-Rink amide AM (AGTC), Fmoc-аминокислоты использовали в четырехкратном избытке, и основание находилось в четырехкратном избытке по отношению к аминокислотам. Аминокислоты растворяли в концентрации 0,2 М в ДМФА, HCTU в концентрации 0,4 М в ДМФА и DIPEA в количестве 1,6 М в N-метилпирролидине (Alfa Aesar). Время сочетания составляло, как правило, 30 минут, и время снятия защиты равнялось 2×2,5 минут. Fmoc-N-метилглицин (Fmoc-Sar-OH, Merck) сочетали в течение 1 часа, и время снятия защиты и сочетания для последующего остатка соответственно составляло 20 минут и 1 час. После синтеза смолу промывали дихлорметаном и сушили. Отщепление защитных групп боковых цепей и от подложки проводили с использованием 10 мл смеси 95:2,5:2,5:2,5 об./об./об./мас. ТФУК/Н2О/iPr3SiH/дитиотреитол в течение 3 часов. После отщепления израсходованную смолу удаляли фильтрованием и фильтрат добавляли к 35 мл диэтилового эфира, который заранее охлаждали при -80°С. Осадок пептидов центрифугировали, эфирный супернатант отбрасывали и осадок пептидов промывали два раза холодным эфиром. Затем пептиды повторно солюбилизировали 5-10 мл смеси ацетонитрил-вода и лиофилизовали. Небольшой образец отбирали для анализа на чистоту сырого продукта масс-спектрометрией (MALDI-TOF, Voyager DE производства Applied Biosystems). После лиофилизации порошки пептидов собирали 10 мл 6М раствора гидрохлорида гуанидиния в Н2О с добавлением 0,5 мл 1 М дитиотреитрола и наносили на колонку для препаративной ВЭЖХ C8 Luna (Phenomenex). Растворители (Н2О, ацетонитрил) подкисляли 0,1% раствором гептафтормасляной кислоты. Градиент колебался в пределах 30-70% ацетонитрила в течение 15 минут со скоростью потока 15/20 мл/мин, с использованием системы для препаративной ВЭЖХ Gilson. Фракции, содержащие чистый линейный пептид (идентифицировали MALDI), объединяли и модифицировали трис-бромметилбензолом (TBMB, Sigma). Для этого линейный пептид разводили Н2О примерно до 35 мл, добавляли примерно 500 мкл 100 мМ TBMB в ацетонитриле и реакцию начинали добавлением 5 мл 1 М раствора NH4HCO3 в Н2О (рН 8). Реакцию проводили в течение примерно 30-60 минут при комнатной температуре и лиофилизовали после окончания реакции (судили по данным MALDI). После лиофилизации модифицированный пептид очищали, как описано выше, заменив колонку Luna C8 на колонку Germini C18 (Phenomenex) и заменив кислоту на 0,1% раствор трифторуксусной кислоты. Чистые фракции, содержащие правильное модифицированное TMB вещество, объединяли, лиофилизовали и хранили при -20°С.
Неприродные аминокислоты получали из источников, приведенных в таблице 7.
Объемные или аминокислоты со структурными затруднениями (NMe-Ser, NMe-Trp, NorHar, 4PhenylPro, Agb, Agp, NMe-Arg, Pen, Tic, Aib, Hyp, NMe-Ala, NMe-Cys, 4,4-BPAI, 3,3-DPA, Dpg, 1NAI, 2NAI, Aze, 4BenzylPro, Ind) обычно сочетали в течение 1 часа (снятие защиты 20 мин) и 6 часов для остатка, который следовал (снятие защиты 20 минут). HCTU использовали в качестве сочетающего реагента, как описано выше. Объем реакции составлял обычно 50 мкмоль.
Ферментативный анализ
Функциональный ферментативный анализ проводили в 10 мМ Трис HCl, 150 мМ NaCl, 10 мМ MgCl2, 1 мМ CaCl2 и 1 мг/мл BSA (все производства Sigma, UK), рН 7,4, при 25°C в плотных черных 96-луночных планшетах. В кратком изложении, 26,5 пМ человеческого плазматического калликреина (приобретенного у Stratech, UK) или 500 пМ крысиного плазматического калликреина (экспрессированного и очищенного в лаборатории) инкубировали в отсутствие или в присутствии возрастающих концентраций испытуемого пептида в течение 15 минут перед добавлением флуорогенного субстрата Z-Phe-Arg-AMC (Enzo Lifesciences, UK) до конечной концентрации в тесте 100 мкМ в 4% ДМСО. Высвобождение АМС определяли с использованием ридера Pherastar FS (BMG Labtech), при длине волны возбуждения 360 нм и волне эмиссии 460 нм. Рассчитывали скорость линейной фазы реакции, обычно в течение от 5 до 45 минут, с использованием программного обеспечения для анализа данных MARS (BMG labtech). Затем скорость использовали для расчета IC50 и Ki с помощью программы Prism (GraphPad). Использовали четырехпараметрическое уравнение нелинейной регрессии ингибирования для расчета IC50. Уравнение один сайт-Ki использовали для расчета Ki, ограничивая Ki к Km для субстрата, который составлял 150 мкМ. Все значения Ki/IC50 представляют собой среднее значение по меньшей мере двух независимых опытов, и по меньшей мере три для пептидов со значениями Ki ниже, чем 1 нМ.
Пептиды растворяли в виде их солей трифторуксусной кислоты и стоковые растворы обычно готовили на воде. Все растворы центрифугировали и фильтровали (шприцевые фильтры емкостью 20 мкм) перед определением поглощения при 280 нм. Коэффициенты экстинкции определяли на основе содержания Trp/Tyr в пептиде, и этого показателя для ТМВ (ядро ТМВ в составе пептида имеет коэффициент экстинкции примерно 300 М-1см-1). Для пептидов, содержащих неприродные аминокислоты с предполагаемыми хромофорными свойствами (т.е. NorHar, 4PhenylPro, 3Pal, 4Pal, Tic, 4GuanPhe, 4,4-BPAI, 3,3-DPA, 1NAI, 2NAI, 4BenzylPro, Ind), концентрацию определяли взвешиванием порошка и растворением пептида в определенном количестве воды. Их готовили независимо, дважды, для пептидов с Ki для калликреина на уровне 1 нМ или ниже.
Профиль стабильности в плазме крови
Использовали три способа для оценки стабильности бициклов в плазме крови (пептидов, конъюгированных с молекулярными каркасами).
Способ 1:
Разработали быстрый способ оценки стабильности в плазме крови с использованием масс-спектрометрического детектирования (MALDI-TOF, Voyager DE, Applied Biosystems) исходной массы до того времени, пока не наблюдали массу исходного пептида. В частности, 200 мкМ пептида инкубировали в присутствии 35% крысиной или человеческой плазмы (Sera labs, используя цитрат в качестве антикоагулянта) при 37°C, к смеси добавляли 1×PBS (полученный из 10×PBS Stock, Sigma). В различные моменты времени (т.е.. t=0, 3, 24 часа, затем ежедневно до 10 суток) отбирали 2 мкл образца и добавляли к 18 мкл 30 мМ бикарбоната аммония в смеси ацетонитрил:Н2О 1:1. Пробы замораживали при -80°C до времени проведения анализа. Для масс-спектрометрического анализа, с помощью которого определяется примерное окно детектирования пептида, разведенную в смеси ацетонитрил:Н2О пробу, отобранную в определенный момент времени, непосредственно наносили (0,7 мкл) на чашку MALDI. Матрикс (альфа-цианокоричную кислоту, Sigma, приготовленную в виде насыщенного раствора в смеси ацетонитрил:вода 1:1, содержащей 0,1% трифторуксусную кислоту) наносили на образец (1 мкл). Затем при одинаковой интенсивности лазера при MALDI TOF определяли время, пока пептид более не детектировался. Следует отметить, что этот количественный анализ служит для определения относительных изменений в стабильности в плазме крови.
Способ 2:
Для более быстрого получения данных по стабильности пептиды также оценивали в 95% плазме. В данном случае PBS исключали и 1 мМ стоковый раствор пептида (в ДМСО) непосредственно растворяли в плазме крови (т.е. 2,5 мкл стокового раствора в 47,5 мкл плазмы крови) с получением конечной концентрации 50 мкМ. В соответствующие моменты времени отбирали пробы объемом 5 мкл и замораживали при -80°С. Для проведения анализа пробы размораживали, смешивали с 15 мкл смеси ацетонитрил:метанол и центрифугировали при 13k в течение 5 минут. 5 мкл супернатанта, содержащего пептид, аспирировали и смешивали с 30 мМ бикарбоната аммония в смеси ацетонитрил:вода 1:1. Затем 1 мкл данной смеси наносили на чашку MALDI и анализировали, как описано выше. Как отмечалось выше, следует указать, что этот количественный метод служит для детектирования относительных изменений в стабильности в плазме крови.
Способ 3:
Для получения количественных данных о стабильности в плазме крови стоковые растворы пептидов (1 мМ раствор в ДМСО) транспортировали в Biofocus, UK, где проводили анализ. Пептиды разводили до концентрации 100 мкМ водой и разводили 1:20 плазмой (конечная концентрация 5 мкМ с 95% плазмой), отбирали пробы соответствующим образом, осаждали, как описано выше, и проводили количественный анализ Waters Xevo TQ-MS.
Пример 1
Идентификация предпочтительных остатков на связывающую активность
Из примеров пептидов 5×5, приведенных в таблице 4, возможно идентифицировать аминокислоты, которые являются консервативными для пептидов со связывающей активностью. Для определения того, какие остатки являются предпочтительными для связывающей активности, далее исследовали представителей из двух идентифицированных групп пептидов. Это был пептид 06-34, который содержал мотив CXWPARC в первой петле бицикла, и пептид 06-56, который содержал мотив CGGxxNCR через обе петли бицикла. Для каждой пептидной последовательности готовили набор из 10 фаговых библиотек, в которых 9 остатков петель сохраняли постоянными, и другие остатки рандомизировали таким образом, что любую аминокислоту можно было экспрессировать в библиотеке в данном положении (см. подраздел «Рандомизация отдельных положений» - «Конструирование библиотек» в разделе «Методы» выше). Для каждой библиотеки набор из 20 произвольно выбранных колоний фага подвергали скринингу на связывание с человеческим калликреином в тесте оценки связывания фага для идентификации ключевых остатков для связывания с мишенью (см. подраздел «Рандомизация отдельных положений» - «Анализ связывания отдельных клонов» в разделе «Методы» выше). Данные этого опыта показаны на фигурах 4-6.
В отношении пептида 06-34 (фигура 4) становится очевидным, что Arg1 в бицикле может быть замещен множеством различных аминокислот, и связывание с человеческим плазматическим калликреином сохранялось или даже повышалось. В противоположность этому, замена остатков 2, 3, 4, 5 (Trp2, Pro3, Ala4, Arg5) большинством аминокислот существенно снижала сигнал, детектируемой в данном тесте, в котором был установлен жесткий порог отсечения для высокоаффинных связывающих пептидов. Val6 может быть заменен многими различными аминокислотами, и связывающая активность сохранялась или повышалась. Замена других остатков во второй петле указывало, что только Leu10 мог быть замещен множеством различных аминокислот с сохранением активности. Положения 7, 8 и 9 обладали ограниченной способностью к замене, и не было идентифицировано замен, которые бы привели к повышению связывания.
В отношении пептида 06-56 (фигуры 5 и 6) становится очевидным, что глицины в положении 1 и 2 являются в высокой степени предпочтительными остатками для связывания с плазматическим калликреином, какими были аргинин, триптофан и треонин в положениях 6, 8 и 9. Глутамин в положении 4 и треонин в положении 10 могут быть заменены множеством остатков с сохранением высокой связывающей активности. Три остальных остатка - пролин в положении 1, аспарагин в положении 5 и треонин в положении 7 обладают ограниченной способностью к замене.
Анализ аминокислотных замен
По результатам предшествующего анализа становится очевидным, что для пептида 06-34 положение один или положение шесть могут быть заменены рядом аминокислот, и пептид по-прежнему сохраняет активность связывания, равную или даже более высокую по сравнению с исходным пептидом. Для оценки того, насколько данные наблюдения будут сохраняться для выделенных синтетических пептидов, конструировали набор пептидов согласно тому, как представлено на фигуре 4, где Arg заменяли серином, и где Val6 заменяли треонином, метионином или лейцином. Синтезировали также пептиды, для которых использовались различные комбинации данных замен. Данные замены приводили к более высокому сигналу связывания в тесте (таблица 5).
Все вариантные синтетические пептиды обладали примерно равной или повышенной активностью к человеческому плазматическому калликреину в тестах ингибирования фермента по сравнению с исходным пептидом 06-34, указывая на то, что данный тип анализа можно использовать для тонкой корректировки аффинности связывания с мишенью, и он предлагает путь идентификации лидерного пептида-кандидата с очень высокой активностью.
Пептиды также тестировали с крысиным плазматическим калликреином в тестах с выделенным ферментом. Замена Arg1 на Ser1 оказывала незначительное влияние на активность связывания с крысиным калликреином, в то время как замены Val6 на треонин, метионин или лейцин давали пептиды с заметно повышенной активностью в отношении крысиного плазматического калликреина. Активность к человеческому калликреину полностью сохранялась. Таким образом, посредством определения положений, чувствительных к заменам, могут быть идентифицированы пептиды с требуемыми свойствами, такими как перекрестная реакционная способность к ортологу-мишени.
Для демонстрации возможности замены данных двух положений неприродными аминокислотами с целью обеспечения введения функциональных групп или свойств, которые отсутствуют в исходном пептиде, Arg1 и Val6 в пептиде 06-34-03 заменяли аланином или N-метилглицином (саркозином), или N-метилсерином в положении 1, и оценивали на связывание. Примечательно, как показано в таблице 6, положения 1/6 поддаются удалению всей боковой цепи, поскольку пептиды R1A/V6A (06-34-03 Ala1,6) сохраняли полную активность по сравнению с исходным пептидом. Замена остатков 1,6 N-метилглицином (06-34-03 NMeGly1,6) вызывала снижение активности, однако аффинность связывания оставалась на низком наномолярном уровне. Введение N-метилсерина в положение 1 приводило к десятикратной потере активности, но связывание оставалось на пикомолярном уровне. Таким образом, могут быть идентифицированы некоторые положения в бицикле, которые обеспечивают изменения в структуре пептидного остова или боковых цепях, которые могут привести к преднамеренному повышению стабильности к воздействию протеазы, повышенной растворимости, пониженной способности к агрегации и введению ортологичных функциональных групп.
Пример 2
Подробный анализ домена WPAR
Мотив WPAR, идентифицированный в примере 1, анализировали в отношении пептида 06-34-03 для установления альтернатив или усовершенствований мотива WPAR. Конструировали библиотеку, в которой положения 1, 6, 7, 8, 9 и 10 в пептиде 06-34-03 оставляли постоянными и положения 2, 3, 4 и 5 рандомизировали (см. подраздел «Рандомизация пептидных доменов» - «Конструирование библиотек» в разделе «Методы» выше). Селекцию по человеческому плазматическому калликреину проводили при различной жесткости (см. подраздел «Селекция фаговых библиотек» в разделе «Методы» выше). Идентифицировали все выбранные последовательности и анализировали на связывание с мишенью (см. подраздел «Рандомизация пептидных доменов» - «Анализ связывания отдельных клонов» в разделе «Методы» выше). В таблице 17 приведена каждая уникальная последовательность, ее относительная избыточность при селекции (частота) и номер ранга согласно силе связывания с мишенью.
В таблице 17 показано, что мотив WPAR придает наиболее высокое связывание с человеческим плазматическим калликреином, хотя в результате селекции были получены другие последовательности, связывающиеся с калликреином, с высокой избыточностью. Они включают, но не ограничиваются ими: WPSR, WPAR, WSAR, WPFR, WPYR, FPFR и FPFR. Наиболее эффективные и избыточные мотивы в положениях 2, 3, 4 и 5 могут быть обобщены как W/FP×K/R.
В таблице 18(А) показано, что WPAR и WPSR были наиболее избыточными при более жесткой селекции; FPFR & FPYR были избыточными в менее жесткой селекции. Это указывает, что WPAR-подобные последовательности являются более сильными связывающими последовательностями по сравнению с FPFR-подобными последовательностями. Анализ каждого мотива (в отношении пептида 06-34-03) в тесте оценки связывания (таблица 18(В)) выявил, что WPAR в положениях 2, 3, 4 и 5 последовательности 06-34-03 является оптимальной последовательностью для связывания с калликреином.
Пример 3
Оптимизация последовательности вне мотива WPAR
Мотив WPAR и его варианты исследовали в отношении пептида 06-34-03. На фигуре 1 показано, что некоторые положения вне мотива WPAR могут поддерживать связывание с калликреином после замещения другими остатками. Для исследования детерминант связывания с калликреином вне мотива WPAR создавали фаговую библиотеку с постоянной последовательностью WPAR и все другие положения рандомизировали (CxWPARRCxxxxxC), как описано в подразделе «Рандомизация пептидных доменов» - «Конструирование библиотек» в разделе «Методы» выше.
Выделяли 80 произвольных библиотек непосредственно из пула библиотек (без селекции) и анализировали на связывание с калликреином при высокой и низкой жесткости (см. подраздел «Рандомизация пептидных доменов» - «Анализ связывания отдельных клонов» в разделе «Методы» выше). Данные библиотеки, которые содержали произвольные последовательности вне мотива WPAR, показывали слабое связывание или его отсутствие с человеческим плазматическим калликреином (данные не приведены), указывая, что наличие одного мотива WPAR не является достаточным для сохранения определяемого связывания с калликреином: остальная часть последовательности бицикла также должна вносить свой вклад или оказывать влияние на взаимодействие.
Селекцию по человеческому плазматическому калликреину проводили с данной библиотекой для исследования детерминант связывания с калликреином вне мотива WPAR и для выделения оптимальной WPAR-содержащей пептидной последовательности. Было отобрано более 150 последовательностей, и они были подвергнуты скринингу на связывание с человеческим плазматическим калликреином (как описано в разделе «Методы» выше). Последовательности ранжировали по связыванию с калликреином и 50 лучших последовательностей выравнивали в таблице 19. В таблице 19 показано, что остаток в положении 1 не оказывает влияния на связывание с калликреином, но установлен высокий консенсус для гистидина в положении 7 (который подтверждает результаты примера 1 выше). Пептид 06-34-03, полученный в примере 1, представляет собой одну из лучших последовательностей. Состав второй петли показывает четкие тенденции, заключающиеся в том, что наличие мотива WPAR обеспечивает высокое связывание с калликреином.
Наилучшие WPAR-содержащие связывающие последовательности с человеческим плазматическим калликреином имели тенденцию:
C X W P A R C T/L H Q/T D L C
H7, D9 и L10 являются высококонсервативными в WPAR-содержащих последовательностях, связывающихся с калликреином.
Были идентифицированы два мотива внутри второй петли бицикла (положения 6-10):
1. C X W P A R C T H Q/T D L C (положения 6,7 и 10: “THxxL”)
2. C X W P A R C T/L H Q/T D L C (положения 7, 8 и 10: «xHxDL”)
Более 120 идентифицированных последовательностей, связывающихся с человеческим плазматическим калликреином (отобранные последовательности), сгруппировали двумя различными путями согласно происхождению их мотивов «THxxL» или «xHxDL». Для всех групп определяли средний сигнал в тесте оценки связывания с калликреином для отобранных последовательностей в качестве показателя связывания с калликреином для данной группы (таблица 20).
Данные теста оценки связывания с калликреином, приведенные в таблице 20, показывают, что мотивы «THxxL» или «xHxDL» приводят к наиболее высокому связыванию с калликреином при наличии в бициклическом пептиде мотива WPAR. Комбинация из 2 мотивов «THxDL» дает наиболее высокое связывание с человеческим плазматическим калликреином и включает последовательность второй петли «THQDL» в пептиде 06-34-03.
Пример 4
Системный анализ стабильности в плазме крови
Для бицикла, который ингибирует калликреин, разумно получить адекватный профиль стабильности к протеазе так, чтобы он имел низкий клиренс в результате воздействия протеазы в плазме крови или других релевантных средах. В экспрессном сравнительном тесте оценки стабильности в плазме крови (раздел «Методы», способ 1), в котором наблюдается прогрессирующее исчезновение исходного пептида в плазме крови крысы, было установлено, что N-концевой аланин (который присутствовал на время селекции и был первоначально включен в синтетические пептиды лидерных последовательностей) быстро удалялся из всех бициклических последовательностей, тестированных с крысиной и человеческой плазмой крови. Такая деградация отсутствовала при синтезе лидерного кандидата с отсутствием обоих N- и C-концевых аланинов. Для удаления потенциальных сайтов узнавания для амино- и карбоксипептидаз свободный аминоконец, который остается в Cys 1 лидерного кандидата, кэппировали уксусным ангидридом во время синтеза пептидов, приводя к получению молекулы, которая ацетилирована в N-конце. В качестве равноценной меры синтезировали С-концевой цистеин в виде амида, чтобы удалить потенциальный сайт узнавания карбоксипептидаз. Таким образом, бициклические лидерные кандидаты имеют следующую общую последовательность: Ac-C1AA1AA2AAnC2AAn+1AAn+2AAn+3C3(TMB)-NH2, в которой «Ас» относится к N-концевому ацетилированию, «-NH2» относится к С-концевому амидированию, где “С1, С2, С3” относятся к первому, второму и третьему цистеину в последовательности, где “AA1”-“AAn” относятся к положению аминокислоты (природа “AA” определяется отбором, описанным выше) и где “(TMB)” указывает, что пептидная последовательность циклизована ТВМВ или любым другим подходящим реакционноспособным каркасом.
За счет высокой аффинности Ас-06-34-18(ТМВ)-NH2 к человеческому (Ki=0,17 нМ) и крысиному (IC50=1,7 нМ) калликреину заявители выбрали этот бицикл для разработки лидера. С использованием того же экспрессного анализа стабильности в плазме крови, описанного выше, Ас-06-34-18(ТМВ)-NH2 имел окно наблюдаемости примерно 2 суток (раздел «Методы», способ 1), которое равно периоду полураспада в плазме крови крысы, составляющему примерно 2 суток (как определено количественно методом ЖХ/МС, см. ниже, таблица 23, способ 3).
Для идентификации протеолитического сайта(ов) распознавания в Ас-06-34-18(ТМВ)-NH2 пептид тестировали в 35% плазме крови крысы в течение времени (способ 1) и каждую пробу анализировали на прогрессирующее появление пептидных фрагментов, используя масс-спектрометрию MALDI-TOF. Исходная масса Ас-06-34-18(ТМВ)-NH2 составляет 1687 Da. С течением времени (фигура 7) появлялись фрагменты с массами 1548,6 (М1), 1194,5 (М2) и 1107,2 (М3). По последовательности Ас-06-34-18(ТМВ)-NH2 (Ac-C1S1W2P3A4R5C2L6H7Q8D9L10C3-NH2) можно рассчитать, что пик М1 соответствует Ас-06-34-18(ТМВ)-NH2 без Arg5(-R5). Оказалось, что это первоначальное протеолитическое событие, за которым следует удаление 4-аминокислотного сегмента WPAR в Ас-06-34-18(ТМВ)-NH2 (М2, -WPAR) и, наконец, вся первая петля Ас-06-34-18(ТМВ)-NH2 вырезалась (М3, -SWPAR) (фигура 8). По этим данным становится очевидным, что Arg5 в Ас-06-34-18(ТМВ)-NH2 является основным сайтом распознавания плазматической протеазы крысы, который ответственен за деградацию бицикла.
Аланиновые замены и скремблирование первой петли
После установления роли Arg5 в создании сайта распознавания крысиных плазматических протеаз проводили химический синтез производных Ас-06-34-18(ТМВ)-NH2 с целью идентификации кандидатов с более высокой протеолитической стабильностью в плазме крови. По существу, такие модификации не должны оказывать влияния на активность в отношении человеческого или крысиного калликреина. Первоначальное исследование, касающееся роли последовательности WPAR/фармакофор (фигура 9, 10), проводили заменой W2P3 на A2A3 или A2Q3 и скремблированием фрагментов или всей первой петли бицикла. В таблице 8 ниже показаны последовательности и соответствующие аффинности в отношении калликреина.
Судя по этим данным, становится ясным, что одновременное удаление W2P3 резко снижает связывание с калликреином примерно в 100000 раз, эффективно делая молекулу фармакологически инертной. Значение правильной последовательности аминокислот подчеркивается четырьмя скремблированными пептидами (Scram 2-4), поскольку все они показывают существенное снижение аффинности по отношению к калликреину (фигура 10). Любопытно, что все пептиды имеют примерно идентичный профиль стабильности в крысиной плазме крови (от 1 до 2 суток, способ 1), указывая, что распознавание плазматической протеазы базируется на присутствии аргинина (фигура 7), но не его положении внутри последовательности.
Затем получали пять производных Ас-06-34-18(ТМВ)-NH2, в которых W2, P3, A4, R5 и C2 заменяли их соответствующими D-энантиомерными аналогами (таблица 9).
Судя по полученным данным, становится очевидным, что замена A4, R5 и С2 D-аминокислотами повышает стабильность пептидов к воздействию плазматических протеаз. Поскольку вырезание Arg5 протеазами крысиной плазмы является первым событием в разрушении пептидов, то первоначальный гидролиз пептидных связей будет иметь место на N- и/или С-концевой стороне Arg5. Вероятно, что замена аминокислот к каждой стороне Arg5 их D-энантиомерами блокирует гидролиз смежной пептидной связи посредством стерического затруднения. Действительно, это эффект, который наблюдали ранее (Tugyi et al. (2005) PNAS, 102(2), 413-418).
Отрицательное влияние замены D-аминокислотами на аффинность к калликреину во всех случаях является выраженным; потери в активности колеблются в пределах от 300- (D-Arg) до 45000 раз (D-Trp2). Это подчеркивает значение правильного трехмерного расположения данных боковых цепей с пакетом бицикла, связывающимся с калликреином. В равной степени высоким является эффект D-Ala4; в данном случае изменение ориентации одной метильной группы (Ala боковая цепь) приводит к снижению аффинности в 7000 раз.
N-метилирование
Затем остатки в первой петле системно замещали их N-метильными аналогами. N-метилирование служит в качестве непосредственной защиты их пептидной связи; однако за счет отсутствия амидного водорода добавление стерического объема (метильной группы) и изменений в предпочтительных углах закручивания предполагаются потери активности.
Данные обобщаются в таблице 10.
N-метилирование аминокислот в петле 1 оказывает менее выраженное отрицательное действие на активность. В частности, N-метилирование Arg5 по-прежнему приводит к образованию связывающего пептида на наномолярном уровне (20-кратное снижение аффинности по сравнению с пептидом дикого типа), и его стабильность в крысиной плазме превышает время анализа (фрагментации пептида при МС не наблюдали), что делает его привлекательным улучшенным лидерным кандидатом. Как и в случае замен D-аминокислотами, N-метилирование остатков, смежных с Arg5с, придает повышенную стабильность пептиду, в основном за счет стерической интерференции, оказывающей влияние на гидролиз, катализируемый протеазой, N- и/или С-концевых пептидных связей к Arg5. Следует отметить, что Ser1 может быть N-метилирован без существенной потери активности, указывая, что целостность пептидного остова в данном положении не является важной для связывания.
Замены аргинина
С учетом значения Arg5 в распознавании протеаз крысиной плазмы тестировали ряд аргининовых аналогов в лидерном Ас-06-34-18(ТМВ)-NH2. Химические структуры приведены на фигуре 11 и данные по зависимости активности от стабильности приведены в таблице 11.
Удивительно, что все аргининовые аналоги приводили к повышению стабильности пептида за пределами времени аналитического окна, подтверждая значение целостности Arg5 в распознавании плазматической протеазы. При повышении (HomoArg) или снижении длины боковой цепи (Agb, Agp) в обоих случаях имеет место снижение аффинности, однако аналог HomoArg по-прежнему дает очень хороший связывающий пептид (Ki=2,1 нМ) с повышенной стабильностью. Удлинение аминокислотного остова на одну метиленовую группу в Arg5 (так называемая бета-аминокислота), при сохранении той же боковой цепи (β-homoArg), также дает связывающий пептид с повышенной стабильностью, однако ценой достоверного снижения аффинности (Ki=8,2 нМ). При замещении алифатического фрагмента боковой цепи Arg фенильным кольцом имеет место образование резонансно-стабилизированной, объемной и жесткой гуанидил-содержащей боковой цепи (4GuanPhe). Из всех тестированных аналогов Arg 4GuanPhe обладал наиболее высокой аффинностью (2-кратное снижение по сравнению с аналогом дикого типа) на фоне повышенной стабильности в плазме крови. Интересно, что гуанидилфенильная группа в структурном отношении близка к известному низкомолекулярному ингибитору калликреина бензамидину (Stürzebecher et al. (1994), Novel plasma Kallikrein inhibitors of the benzamidine type. Braz. J. Med. Biol. Res. 27(8):1929-1934; Tang et al. (2005), Expression, crystallization, and three-dimensional structure of the catalytic domain of human plasma Kallikrein”. J. Biol. Chem. 280:41077-41089). Кроме того, использовали дериватизованные фенилгуанидины в качестве селективных ингибиторов другой сериновой протеазы, uPA (Sperl et al., (4-aminomethyl)phenylguanidine derivatives as nonpeptidic highly selective inhibitors of human urokinase (2000) Proc. Natl. Acad. Sci. USA, 97(10):5113-5118). Таким образом, пептид Ас-06-34-18(ТМВ)-NH2, содержащий 4GuanPhe5, может рассматриваться в качестве низкомолекулярного ингибитора, чья селективность придается окружающим бициклическим пептидом. Это может стать принципом для получения других основанных на бициклах ингибиторах, когда известный низкомолекулярный ингибитор с низкой селективностью «пересаживается» на бицикл в правильном положении, приводя к получению молекулы с более высокой активностью и селективностью.
Модификация самой Arg гуанидильной группы посредством метилирования (SDMA, NDMA), удаления положительного заряда (Cit, где гуанидильная группа заменяется изостерической, но незаряженной группой мочевины) или делеции Arg одновременно (Δ Arg), оказывает выраженный отрицательный эффект на активность связывания с калликреином. Таким образом, целостность и присутствие гуанидильной группы являются решающими, в то время как природа боковой цепи, связанной с гуанидильной группой или остовом в Arg5, нет. Следует отметить, что Arg5 также может быть заменен лизином, однако вновь со снижением аффинности (см. пептид WPAK).
Подводя итог вышеописанному, данные указывают, что Ас-06-34-18(ТМВ)-NH2 с HomoArg, NMeArg или 4GuanPhe в качестве замены аргинина может представлять собой кандидата с повышенной стабильностью в плазме крови с высокой аффинностью.
Пример 5
Повышение активности лидерного кандидата посредством неприродных модификаций и комбинации с модификациями, повышающими стабильность в плазме крови
Повышение активности данного бициклического кандидата можно осуществить посредством нескольких механизмов. Частично они были указаны в примере 4 и повторно могут быть сформулированы следующим образом:
1. Включение гидрофобных групп, при этом используется гидрофобный эффект и получаются более низкие скорости, так что достигается более высокая аффинность.
2. Включение заряженных групп, при этом используются дальние ионные взаимодействия, что приводит к ускорению скорости и более высокой аффинности (см., например, Schreiber et al., Rapid, electrostatically assisted association of proteins (1966), Nature Struct. Biol. 3, 427-431).
3. Включение дополнительного структурного ограничения в пептид, т.е.
- правильным ограничением боковых цепей аминокислот так, что потеря энтропии является минимальной при связывании мишени
- ограничением углов закручивания остова так, что потеря энтропии является минимальной при связывании мишени
- введением дополнительных циклизаций в молекуле по аналогичным причинам.
(см. обзоры Gentilucci et al., Curr. Pharmaceutical Design, (2010), 16, 3185-3203 и Nestor et al., Curr. Medicinal Chem. (2009), 16, 4399-4418).
Замены триптофана и замены гидрофобным аналогом
Первоначально провели замещение в сайте Trp2 рядом гидрофобных аминокислот для идентификации кандидатов, которые могут заменить чувствительный к окислению триптофан, и для идентификации кандидатов, которые могут приводить к повышению активности (первый пункт выше). Боковые цепи данных аминокислот показаны на фигуре 12, и данные по аффинности обобщены в таблице 12 ниже.
Как и предполагалось, ни одна из модификаций не приводила к повышению стабильности в плазме крови. 2-Нафтилаланин является наиболее близким к Trp2 и обладает активностью, незначительно ниже, чем дикий тип, что делает это хорошим, устойчивым к окислению замещением Trp2. Интересно, что 3,3-DPA2 имеет структуру, которая значительно отличается от Trp, но соответствующий пептид сохраняет высокую активность. Это может указывать на то, что контактирующий «карман» Trp на калликреине может быть использован для обеспечения более высокой аффинности связывания посредством идентификации правильно сконструированной гидрофобной молекулы.
Аналоги пролина
Затем заявители заинтересовались установлением роли Pro3 в фармакофоре WPAR в пептиде Ас-06-34-18(ТМВ)-NH2. Выбрали 4-гидрокси- или 4-фтор-транс(L)-пролин (HyP3, 4FluoPro3) за счет их известного свойства индуцировать дополнительную ригидность и спиральность в пептидном остове (фигура 15, таблица 13). Кроме того, присутствие гидроксила в HyP зондирует доступность пролиновой боковой цепи для растворителя. Значения Ki соответствующих производных были практически идентичны значениям молекулы дикого типа, указывая, что любые воздействия на пептидный остов являются незначительными, но также показывает, что боковая цепь является доступной. Для проведения дальнейших исследований тестировали два дополнительных производных Ас-06-34-18(ТМВ)-NH2, которые содержали объемное удлинение на γ-углероде боковой цепи Pro3 (4фенил-Pro, 4бензил-Pro). Первое производное демонстрирует высокое сохранение активности, в то время как последнее подверглось сильному воздействию, показывая, что боковая цепь Pro является доступной, но ограничивается только отдельными модификациями. Несмотря на стерический объем данных модификаций, стабильность в плазме крови была идентичной стабильности молекулы дикого типа. Таким образом, данные модификации не приводят к повышению селективности в отношении других протеаз.
Для исследования влияния размера пролинового кольца на связывание Pro3 замещали 4-членным аналогом Pro с высокими структурными ограничениями, азетидинкарбоновой кислотой (Aze) и более гибким 6-членным кольцом (пипеколиновой кислотой, Pip). Ас-06-34-18(ТМВ)-NH2 Aze3 связывается с калликреином с наиболее высокой аффинностью из всех производных, известных к настоящему времени, превосходящей таковую для пептида дикого типа в 3 раза (фигура 14). Оказалось, что имеется обратная зависимость между размером кольца и значением Ki, на основании чего можно предположить, что конформационное затруднение в положении 3 Ас-06-34-18(ТМВ)-NH2 является ключом к получению молекулы с высокой связывающей способностью.
Гибкость пролиновой боковой цепи в допущении крупных объемных групп подчеркивается би/трициклическими аналогами пролина Tic, NorHar и Ind (фигура 13). В частности, в последних двух случаях аффинность по-прежнему была высокой и находилась на наномолярном уровне.
Наконец, заявители провели анализ необходимости в полной кольцевой структуре в Pro3. Для этого заявители выбрали аминоизомасляную кислоту (Aib, фигура 13, таблица 13), которая за счет двойного замещения метилом в альфа-углероде имеет сильное структурное влияние на соседние аминокислоты в индукции α и 310 спиральности (Toniolo et al. (1993), Biopolymers, 33, 1061-1072; Karle et al. (1990), Biochemistry, 29, 6747-6756). Примечательно, что такая неприродная, нециклическая аминокислота хорошо допускается на месте Pro3 при Ki, составляющей 1,2 нМ. Таким образом, роль Pro3 в фармакофоре WPAR сводится к приданию структурного ограничения в пептидный остов. Это структурное ограничение может быть повышено за счет использования аналога пролина с уменьшенным размером кольца (см. Aze3). В противоположность этому, пролиновое кольцо может быть замещено относительно эффективно нециклическими, но способствующими образованию структуры аминокислотами, такими как Aib.
Различные аналоги
В таблице 10 показано, что Ser1 в петле 1 пептида Ас-06-34-18(ТМВ)-NH2 может быть N-метилирован с очень незначительным влиянием на активность (значение Ki 0,5 против 0,17 нМ для пептида дикого типа). Заявители попытались определить, насколько данное положение выдерживало крупную двойную замену в Cα в положении 1. Для этого Ser1 заменяли на Dpg (дипропилглицин) (фигура 15). Аффинность данного пептида по отношению к калликреину составляла 1,1 нМ, указывая, что положение 1 является очень гибким в аккомодации практически любого объемного остатка. Таким образом, данное положение в петле 1 может быть использовано для преднамеренного включения требуемых химических функциональных групп или групп, включающих солюбилизирующие аминокислоты, радиоактивные метки, красители-метки, линкеры, сайты конъюгации и т.д.
Также тестировали несколько аналогов аланина в положении 4. Как уже наблюдали для N-метилаланина и D-аланина (таблицы 2, 3), Ala4 был высокочувствительным к стерической ориентации при Cα или к модификации самого пептидного скелета. Два других производных этой группы подтверждают это положение, поскольку элонгация пептидного остова в Ala4 (β-Ala4) резко снижала аффинность (~20 мкМ). Как и предполагалось для D-Ala4, Aib4 снижал аффинность практически в такой же степени (289 нМ, фигура 15 и таблица 14). Примечательно, что удлинение боковой цепи Ala на один метилен (Aba4) приводило к повышению аффинности к калликреину.
Наконец, центральный цистеин (Cys2) заменяли более объемным и более структурно ограниченным аналогом пеницилламином (Pen, фигура 15) в надежде повысить протеолитическую стабильность за счет пониженного пространственного доступа к сайту распознавания протеазы, соседнему Arg5. Действительно, стабильность в крысиной плазме крови была несколько повышена, однако активность достоверно снижалась, что подчеркивает значение полной целостности данного остатка, соединяющегося со структурным каркасом.
Комбинация повышения стабильности в плазме крови и повышения активности неприродными аминокислотами в одном бициклическом лидере
Замены неприродными аминокислотами в пептиде Ас-06-34-18(ТМВ)-NH2, которые сохраняли существенную активность и максимальную стабильность в крысиной плазме крови (как определено способом 1), представляли собой варианты Arg5 гомоаргинин (гомоArg5), 4-гуанидилфенилаланин (4GuanPhe) и N-метиларгинин (NMeArg5). Неприродные замены в пептиде Ас-06-34-18(ТМВ)-NH2, которые повышали активность по сравнению с пептидом дикого типа, представляли собой аналог Pro3 азетидинкарбоновую кислоту (Aze3) и аналог Ala4 2-аминомасляную кислоту (Aba4). Таким образом, Aze3, Aba4 объединяли с повышающими стабильность в плазме крови homoArg5, 4GuanPhe5 и NMeAgg5 для определения того, насколько это приведет к получению кандидатов-пептидов с высокой стабильностью в плазме и повышенной активностью.
В таблицах 15 и 16 приводятся аффинности различных конструкций вместе с данными по стабильности в плазме.
Первое, результаты количественного определения периода полураспада в крысиной плазме крови (4 колонка, таблица 15) пептидов, содержащих аналог аргинина, выявили, что N-метилирование Arg5 оказывало наиболее сильный эффект в защите пептида (t1/2>20 часов), за ним следовали HomoArg5 и GuanPhe5. Возможно, что высокий защитный эффект N-метилирования Arg5 не был удивительным, поскольку при этом непосредственно предупреждался гидролиз пептидной связи. При включении Aze3 в данные соединения аффинность этих пептидов повышалась во всех случаях, что делает Ac-(06-34-18)Aze3 HomoArg5 и Ac-(06-34-18)Aze3 NMeArg5 привлекательными кандидатами для дальнейшей разработки (таблица 15, фигура 16).
Эффект повышения аффинности Aba4 невозможно было воспроизвести в отношении Aze3 и любого из аналогов аргинина, поскольку значения Ki были выше, чем значения, наблюдаемые без Aba4. Таким образом, эффекты повышения активности Aze3 не зависели от типа замены аргинина, в то время как Aba4, вероятно, нет.
Наконец, активность данных пептидов в отношении крысиного калликреина достоверно снижается (таблица 15). Однако данные значения являются относительными и не количественными на данной стадии, поскольку белковый препарат крысиного калликреина не является тривиальным и содержит примеси.
Пример 6
Повышение стабильности в плазме крови бициклического лидера FPYR калликреина, не содержащего Trp, и повышение аффинности введением Aze3
По данным результатов селекции, приведенных в примерах 1-4, заявители установили, что несколько последовательностей, напоминающих Ас-06-34-18(ТМВ)-NH2, имели высокую избыточность, но содержали измененные мотивы WPAR. Это были WPSR и FPYR. Последний представляет особый интерес, поскольку в нем отсутствует чувствительный к окислению триптофан.
Синтезировали бициклы, содержащие WPSR, FPYR, WPYR и FPAR, и сравнивали с исходным пептидом WPAR (таблица 21).
Как и предполагалось, ни один из пептидов не проявлял достоверно отличающейся стабильности в плазме. Замена Trp2 на Phe2 приводит к 40-кратному снижению значения Ki, что подчеркивает необходимость в более объемной боковой цепи Trp2. Однако данное снижение могло компенсироваться замещением Ala4 на Tyr4 (давая мотив FPYR), так что аффинность вновь повышалась практически до значения аффинности последовательности WPAR дикого типа (Ki=0,46 нМ). Таким образом, имеется совместное взаимодействие между остатками в положении 2 и положении 4 бицикла Ас-06-34-18(ТМВ)-NH2. С учетом высокой аффинности связывания с мишенью и отсутствием Trp2 в Ас-06-34-18(ТМВ)-NH2 Phe2Tyr4, этот кандидат исследовали в отношении повышения периода полураспада в крысиной плазме крови, используя подход, описанный в примере выше. Кроме того, заявители исследовали взаимодействие между Phe2 и Tyr4 заменой данных остатков их аналогами, представляющими сбой неприродные аминокислоты.
Замены неприродными аминокислотами Phe2/Tyr4 в Ас-06-34-18(ТМВ)-NH2 Phe2Tyr4
Заявители проводили неполный ряд синтезов, включающих замещения в Phe2 или Tyr4 в лидере Ас-06-34-18(ТМВ)-NH2 Phe2Tyr4. Выбирали неприродные аминокислоты из того же ряда, который показан на фигуре F6, и данные по аффинности приведены в таблице 22.
В данном случае замена любой тестированной аминокислоты в целом хорошо допускалась, независимо от того, является ли боковая цепь гетероароматической (3Pal, 4Pal), ароматической и объемной (1Nal, 2Nal, 4,4-BPal) или циклоалифатической (Cha) группой. 3Pal хорошо допускался в положении 2 (Ki=0,91), который представлял интерес, поскольку Pal содержит ионизируемую группу (которую можно использовать для приготовления состава). Однако оказалось, что исходная комбинация Phe2/Tyr4 оставалась самой активной.
Стабилизация Ас-06-34-18(ТМВ)-NH2 Phe2Tyr4 в крысиной плазме и влияние замены азетидином3
Ас-06-34-18(ТМВ)-NH2 Phe2Tyr4 готовили с заменами гомоаргинином, 4-гуанидилфенилаланином и N-метиларгинином в отсутствие и в присутствии Aze3. HomoArg/4Guanphe хорошо допускался со значениями Ki, почти идентичными таковым для исходного пептида Phe2Tyr2 (таблица 23), и стабильность в крысиной плазме повышалась в 13 раз (t1/2=12,2 часов, таблица 23). Кроме того, значения IC50 для крысиного калликреина были аналогичны значениям исходного пептида, указывая, что это является привлекательным кандидатом для опытов in vivo.
Замена Pro3 на Aze3 в контексте FPYR вновь давала пептиды-кандидаты с повышенной аффинностью, фактически был получен пептид с Ki ниже 1 нМ, который, вероятно, будет иметь период полураспада более 20 часов у крыс (Ac-(06-34-18)Phe2Aze3Tyr4NMeArg5).
Если не указано иное, то любые методы и материалы, аналогичные или эквивалентные описанным в данном документе, можно использовать в практике или тестировании настоящего изобретения. Способы, устройства и материалы, подходящие для таких применений, описаны выше. Все публикации, цитированные в данном документе, включены посредством ссылки в полном объеме для целей описания и раскрытия методологий, реагентов и инструментов, описанных в публикациях, которые могут использоваться в отношении изобретения.
Таблицы
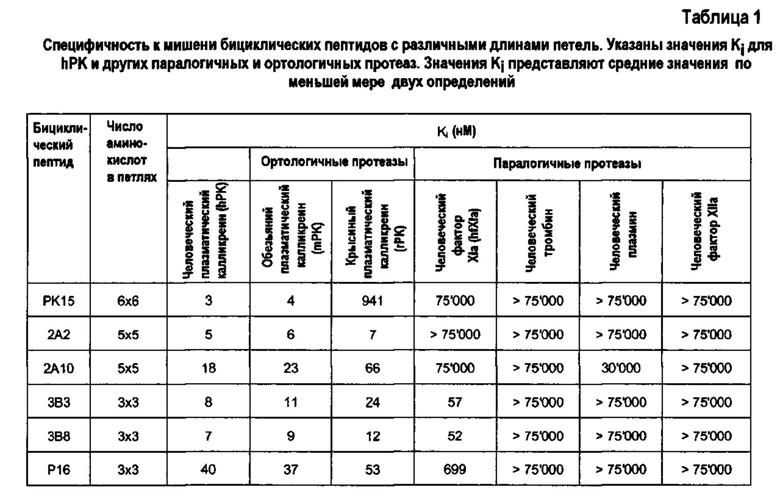
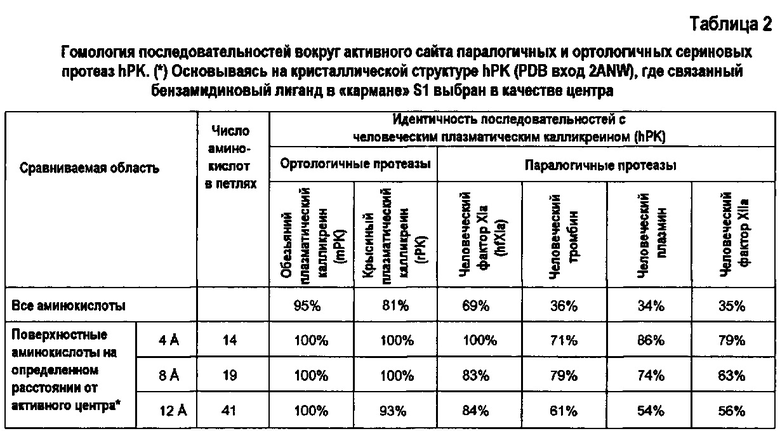

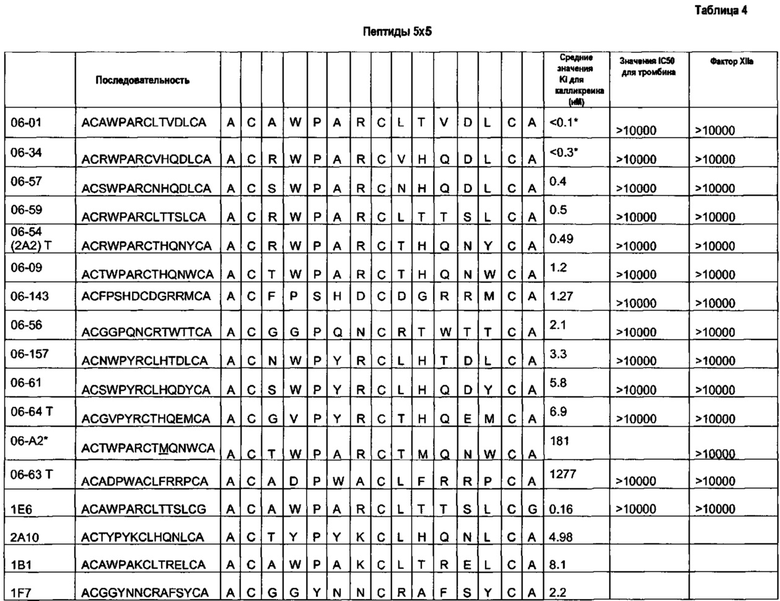
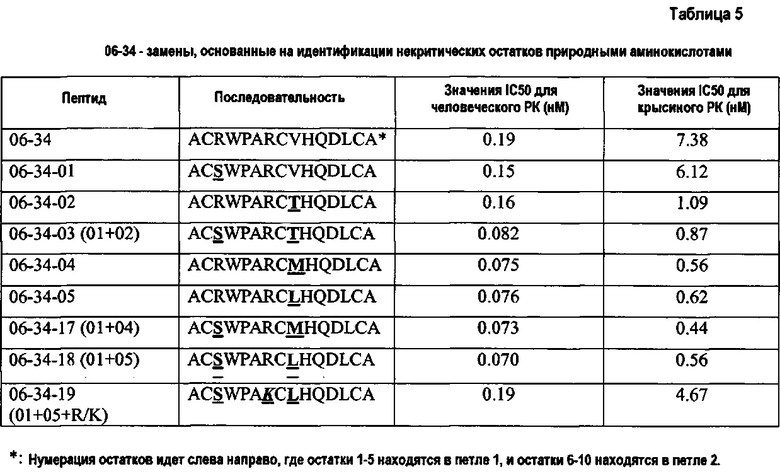

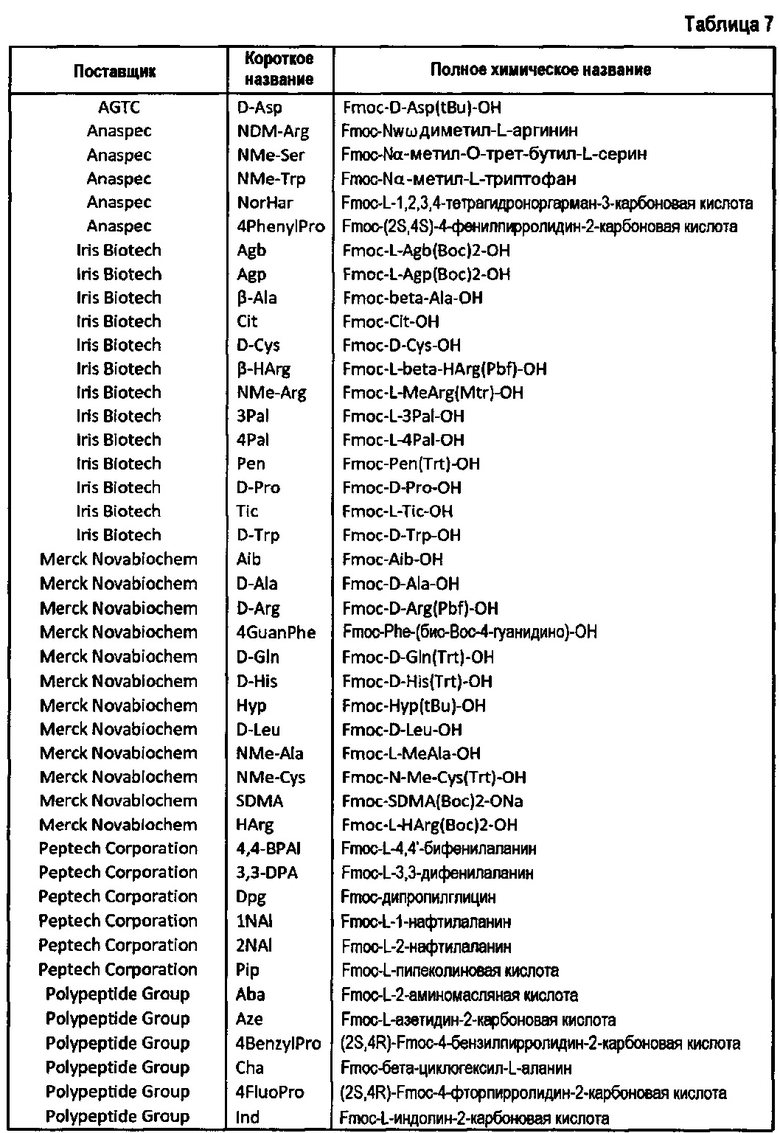
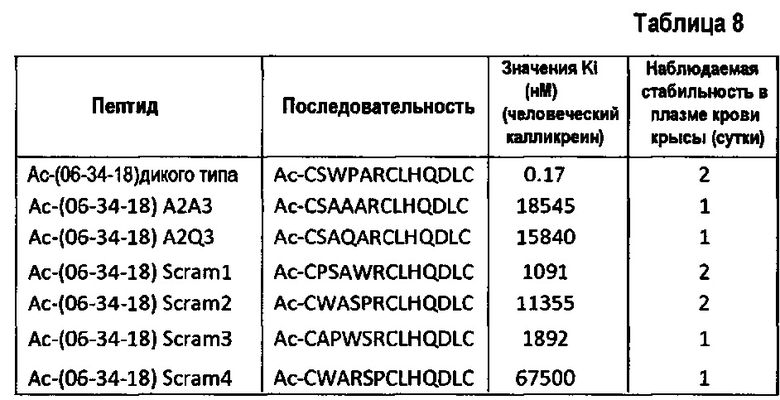
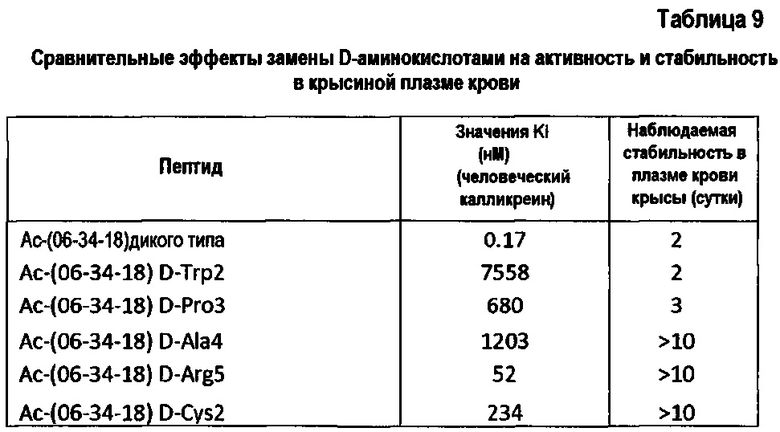
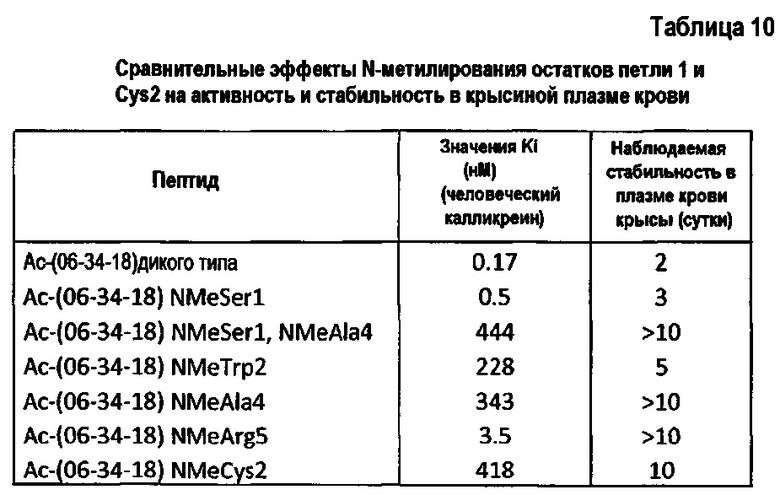
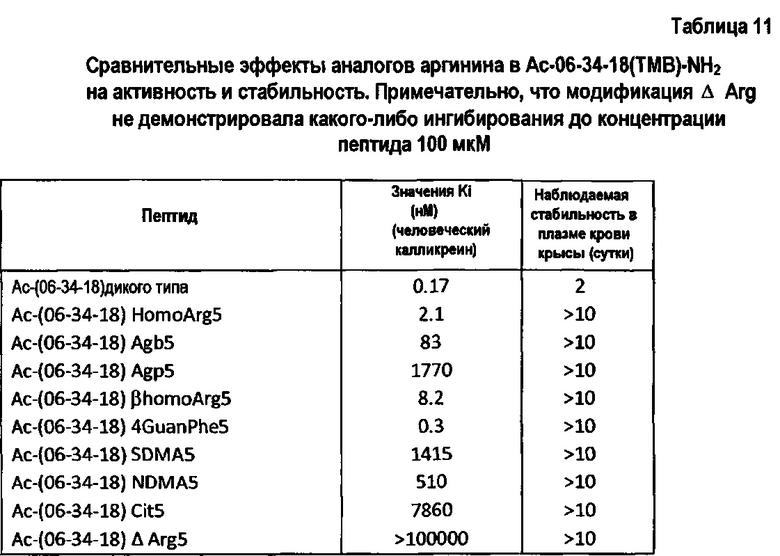
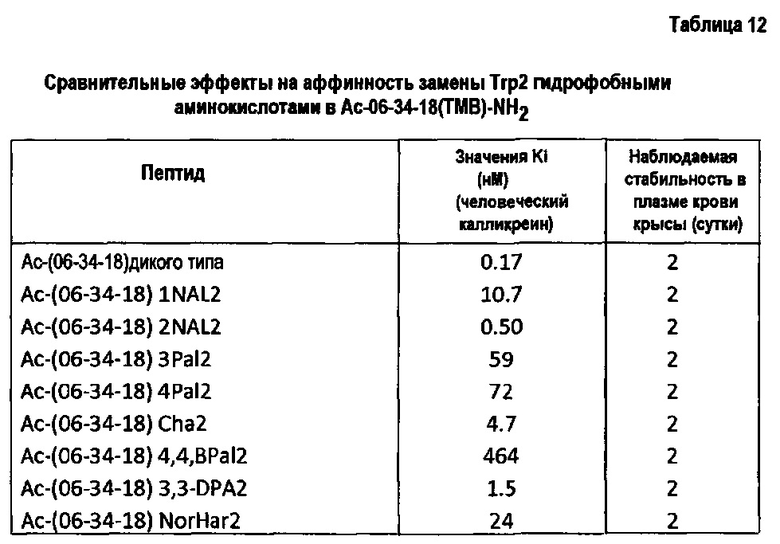
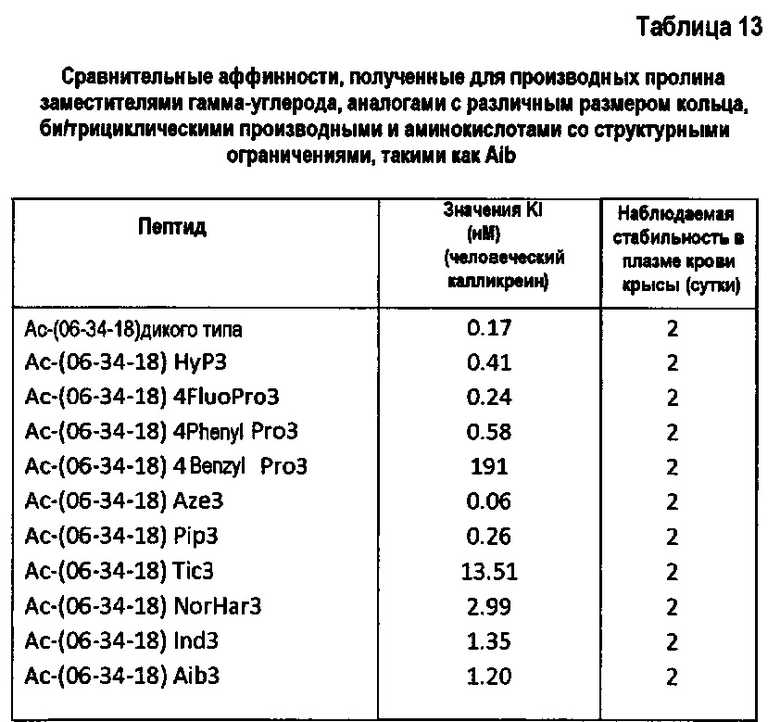
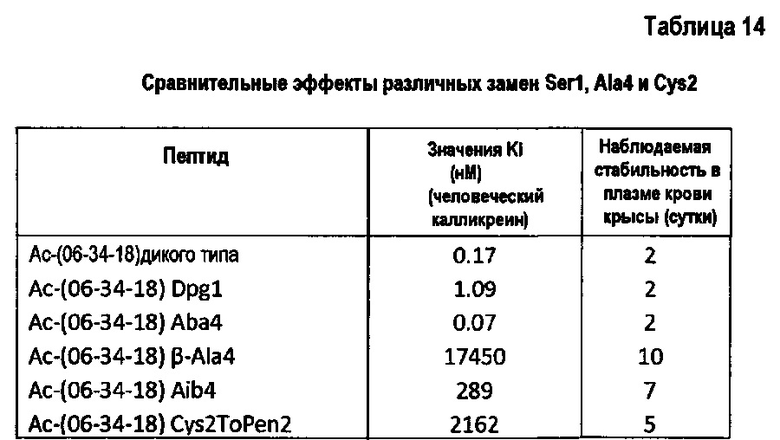
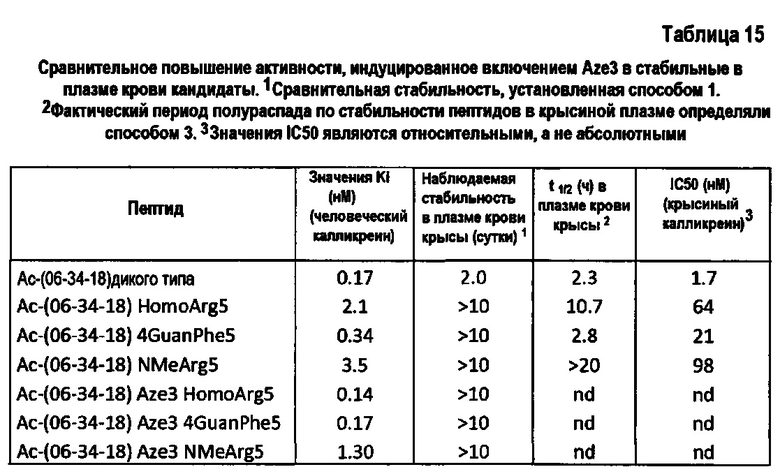
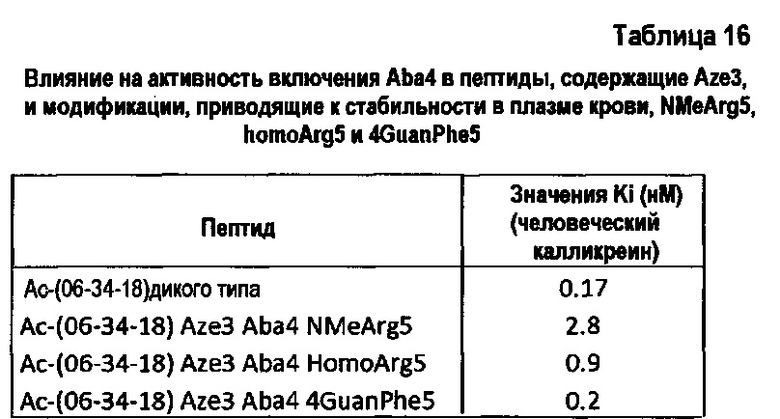
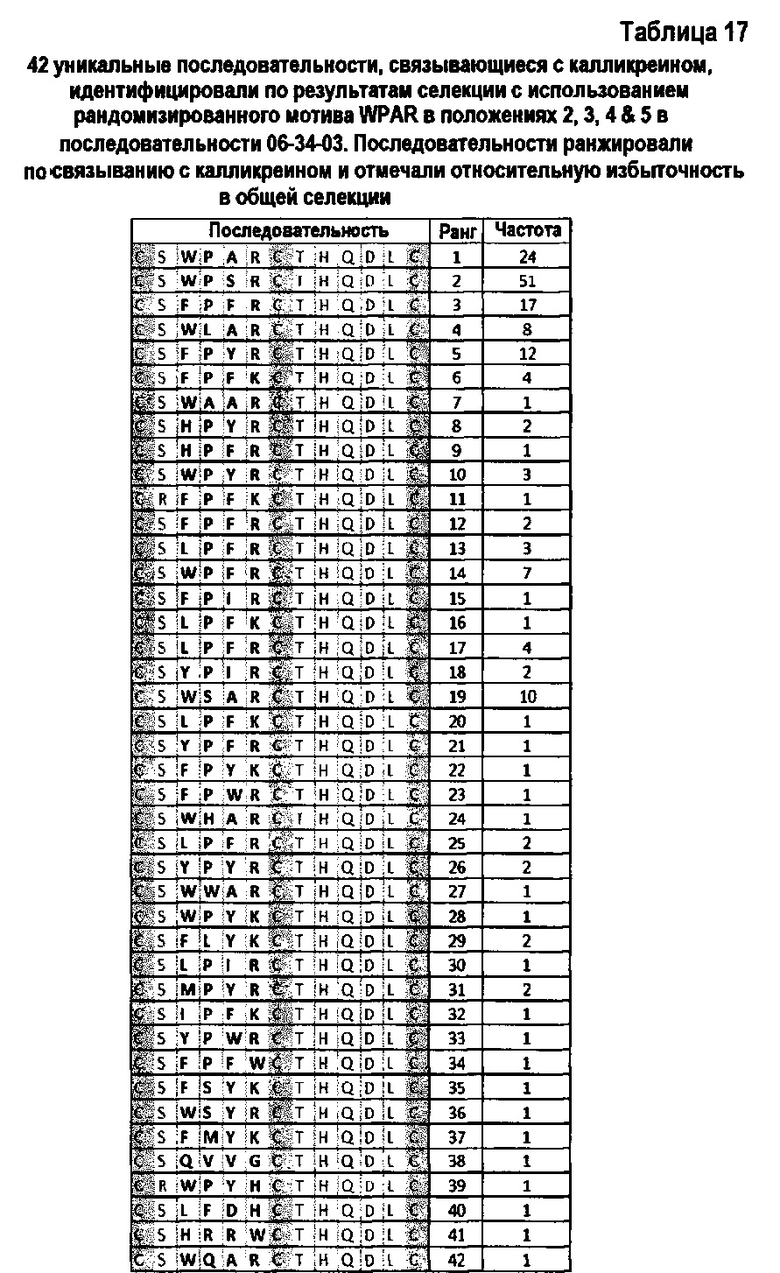
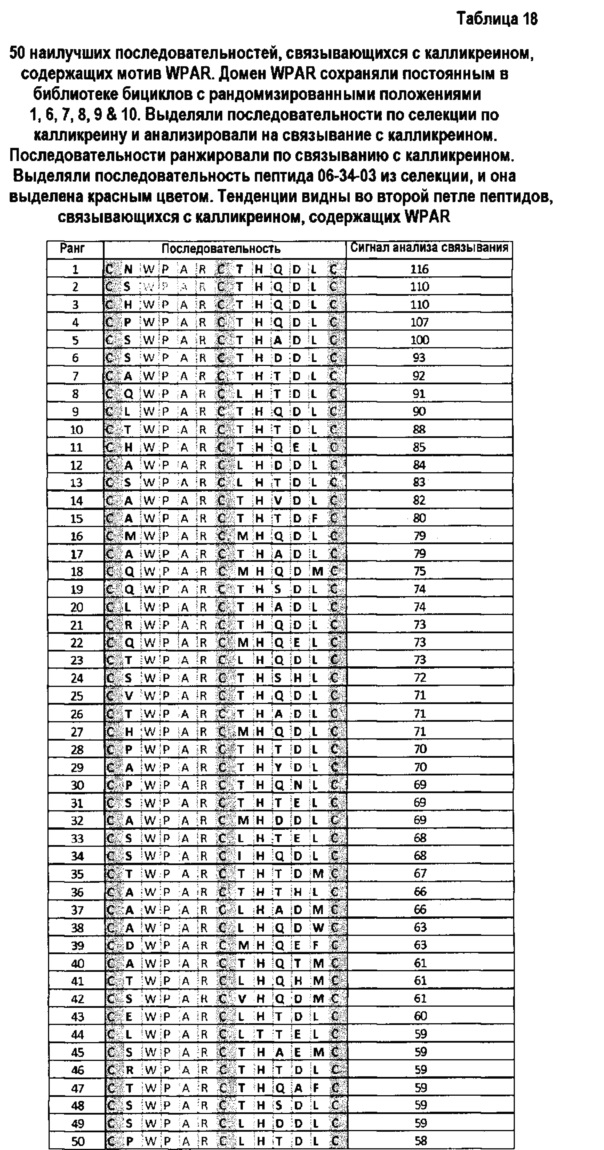
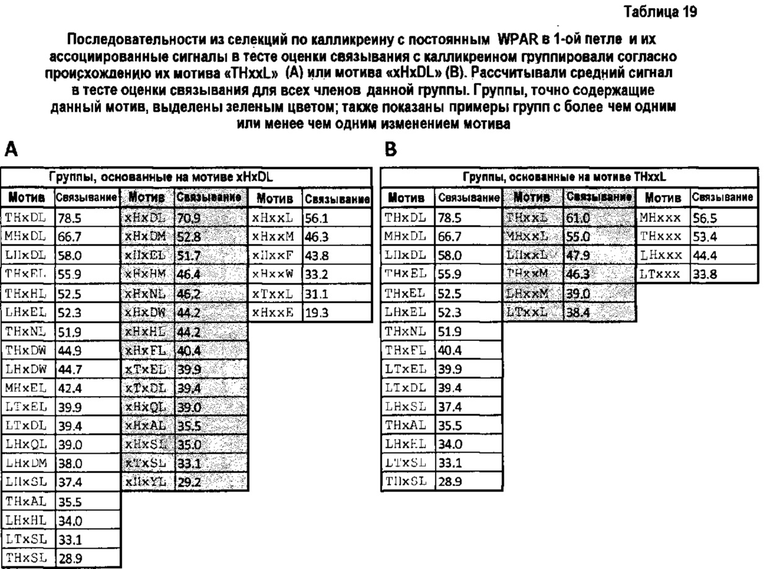
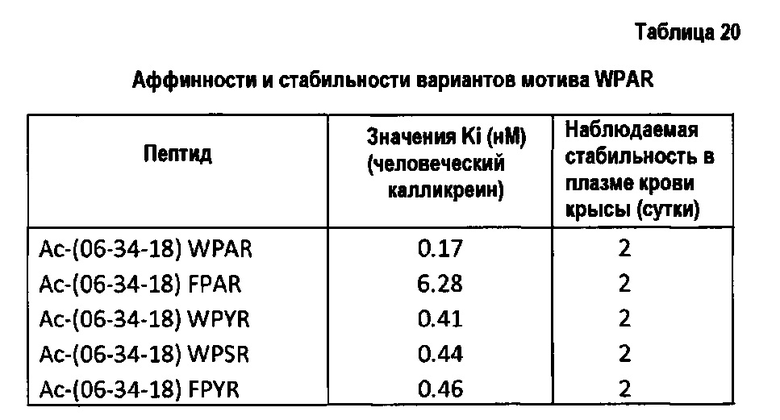
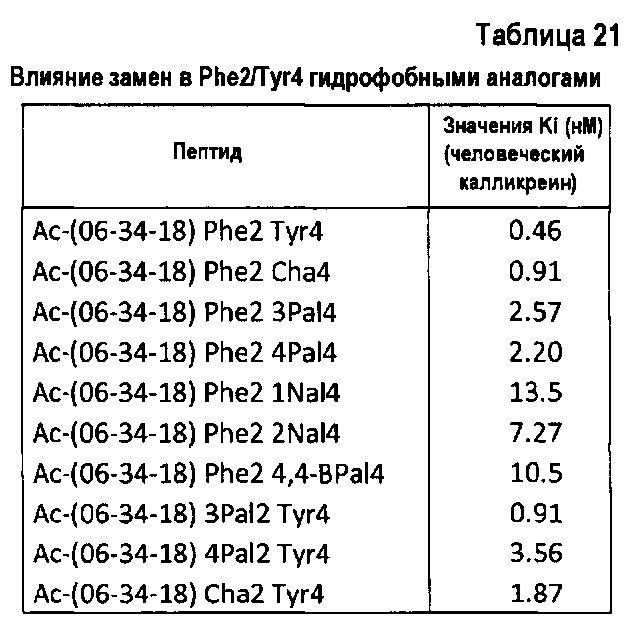
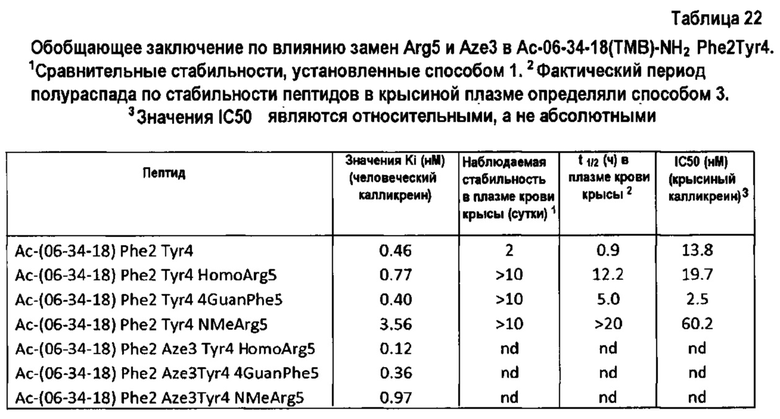
| название | год | авторы | номер документа |
|---|---|---|---|
| МОДУЛЯЦИЯ СПЕЦИФИЧНОСТИ СТРУКТУРИРОВАННЫХ БЕЛКОВ | 2012 |
|
RU2745572C2 |
| МОДУЛЯЦИЯ СПЕЦИФИЧНОСТИ СТРУКТУРИРОВАННЫХ ПОЛИПЕПТИДОВ | 2014 |
|
RU2674070C2 |
| НОВЫЕ ПОЛИПЕПТИДЫ | 2014 |
|
RU2674604C2 |
| БИЦИКЛИЧЕСКИЕ ПЕПТИДНЫЕ ЛИГАНДЫ, СПЕЦИФИЧНЫЕ ДЛЯ МТ1-ММР | 2015 |
|
RU2708459C2 |
| БИЦИКЛИЧЕСКИЕ ПЕПТИДНЫЕ ЛИГАНДЫ, СПЕЦИФИЧНЫЕ ДЛЯ MT1-MMP | 2015 |
|
RU2824959C2 |
| СЛИТЫЕ КОНСТРУКЦИИ ЛЕКАРСТВЕННОГО СРЕДСТВА И КОНЪЮГАТЫ | 2005 |
|
RU2428431C2 |
| ВАРИАНТЫ Fc С ИЗМЕНЕННЫМ СВЯЗЫВАНИЕМ C FcRn | 2008 |
|
RU2529951C2 |
| ВАРИАНТЫ Fc С ИЗМЕНЕННЫМ СВЯЗЫВАНИЕМ С FcRn | 2021 |
|
RU2833597C2 |
| ВАРИАНТЫ Fc С ИЗМЕНЕННЫМ СВЯЗЫВАНИЕМ С FcRn | 2014 |
|
RU2700882C2 |
| КОВАЛЕНТНОЕ МОДИФИЦИРОВАНИЕ ПОЛИПЕПТИДОВ ПОЛИЭТИЛЕНГЛИКОЛЯМИ | 1992 |
|
RU2148586C1 |
























































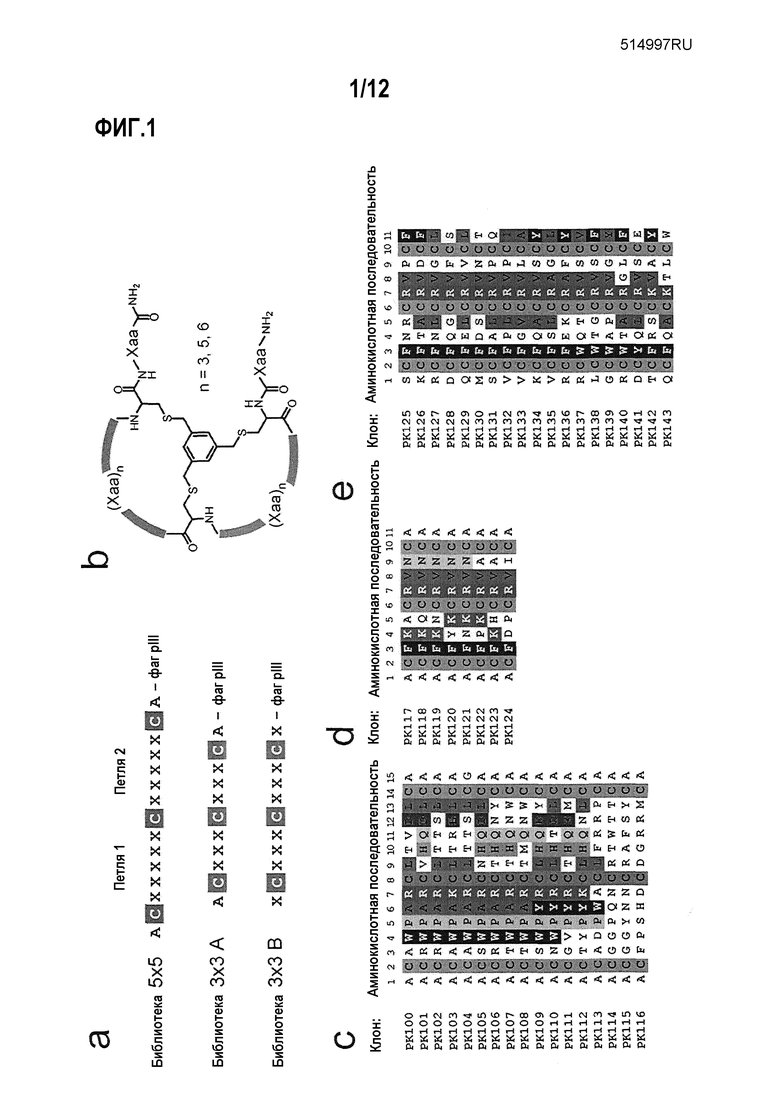
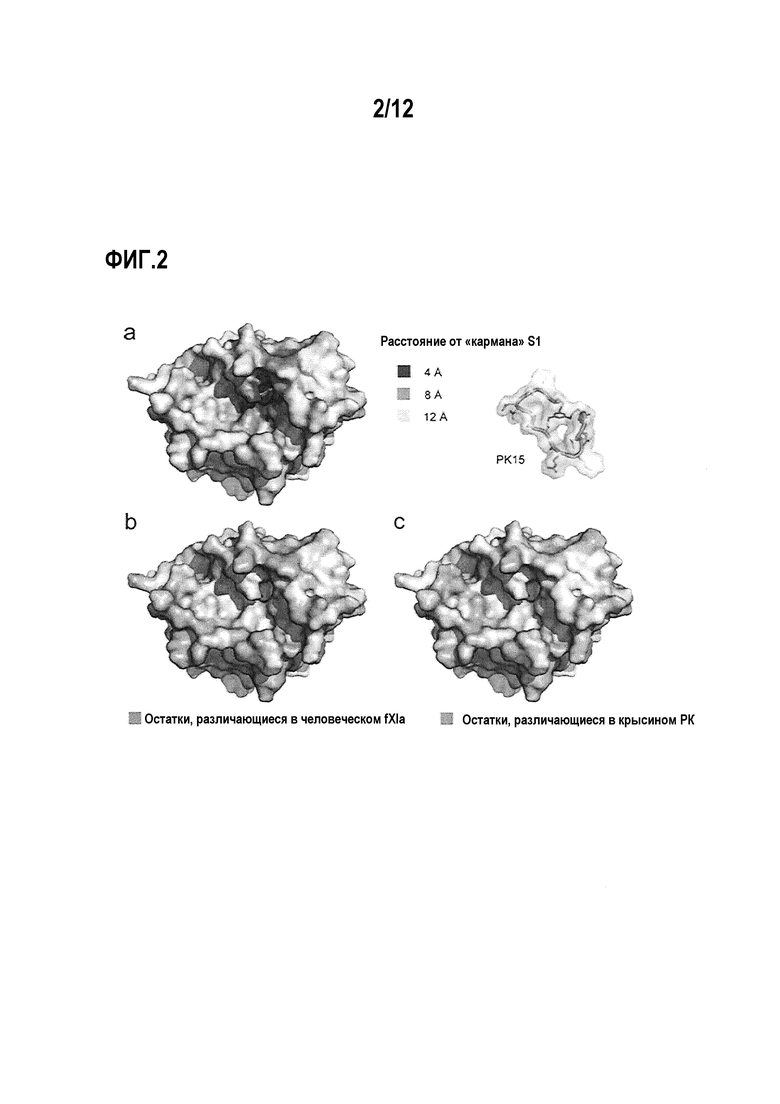
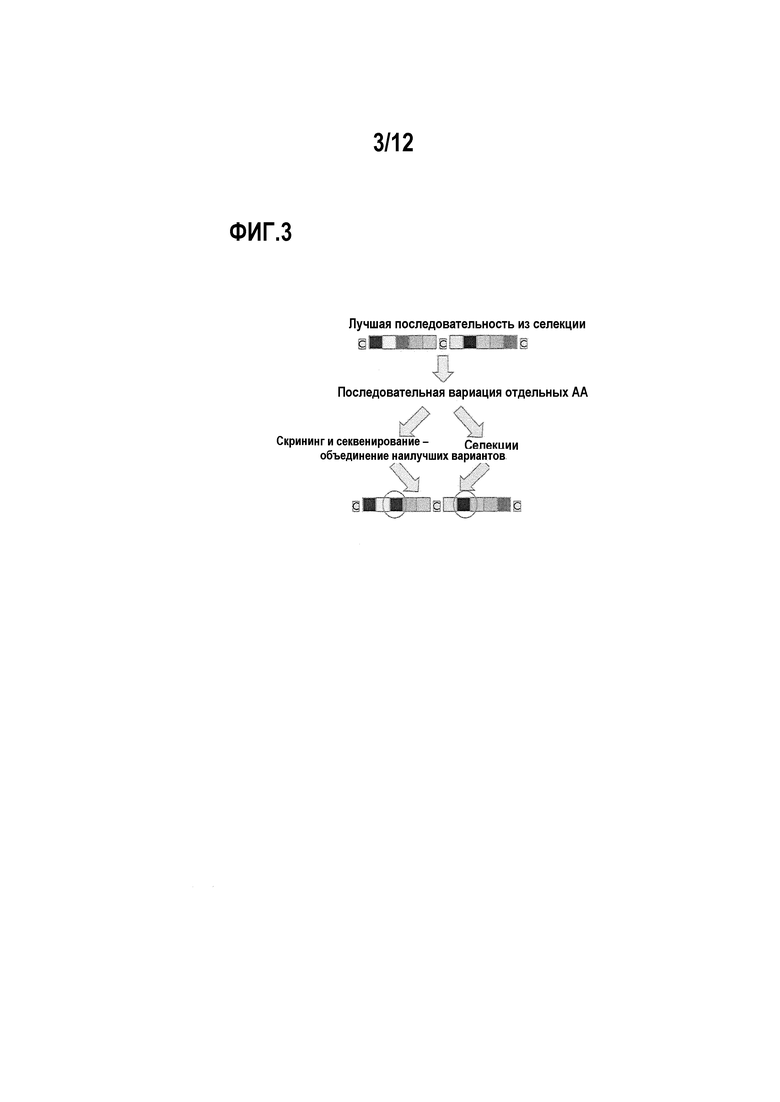
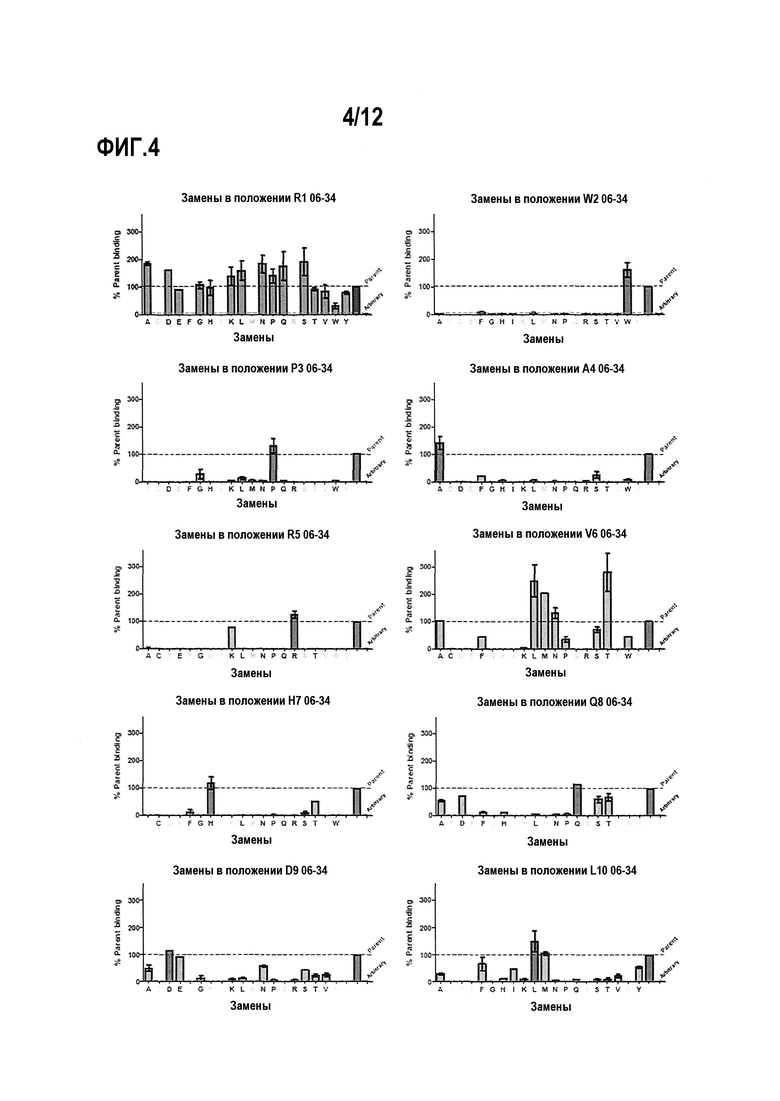
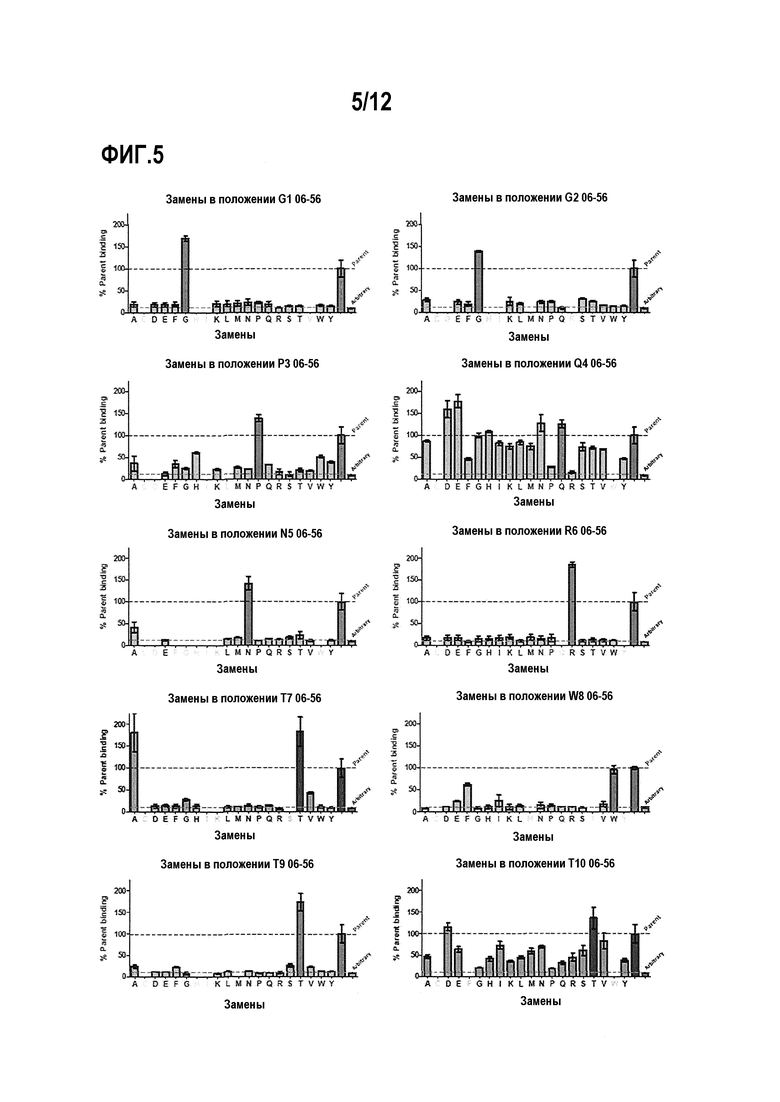
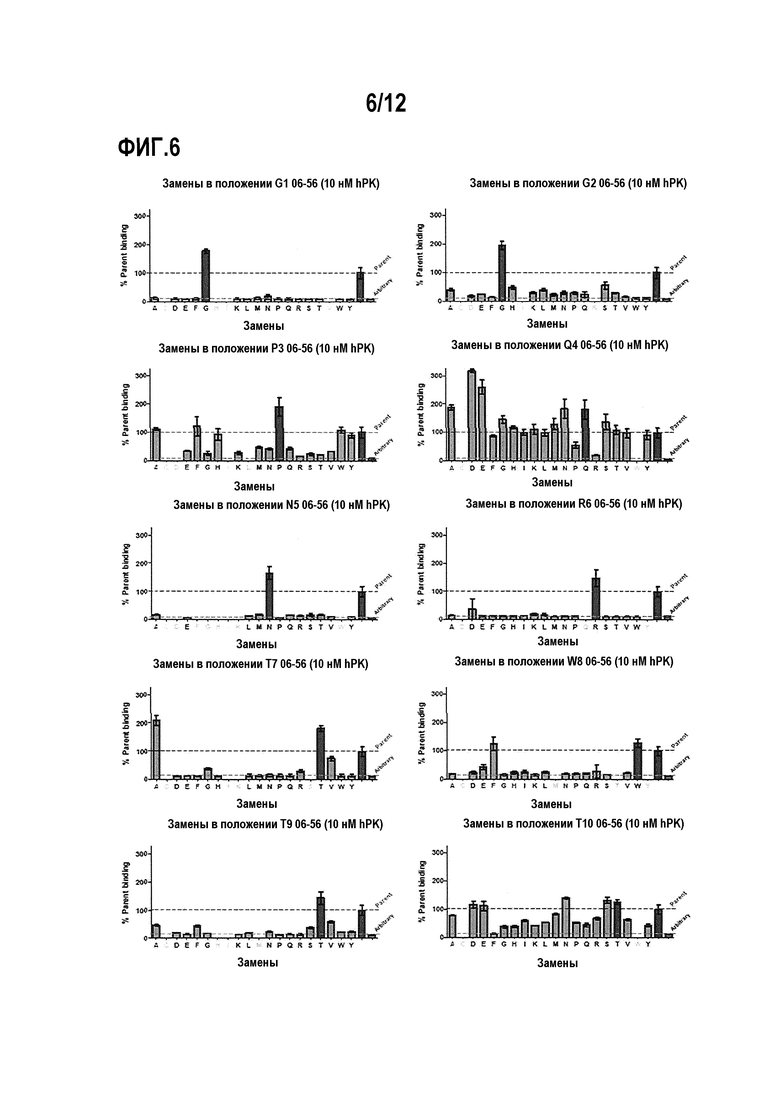
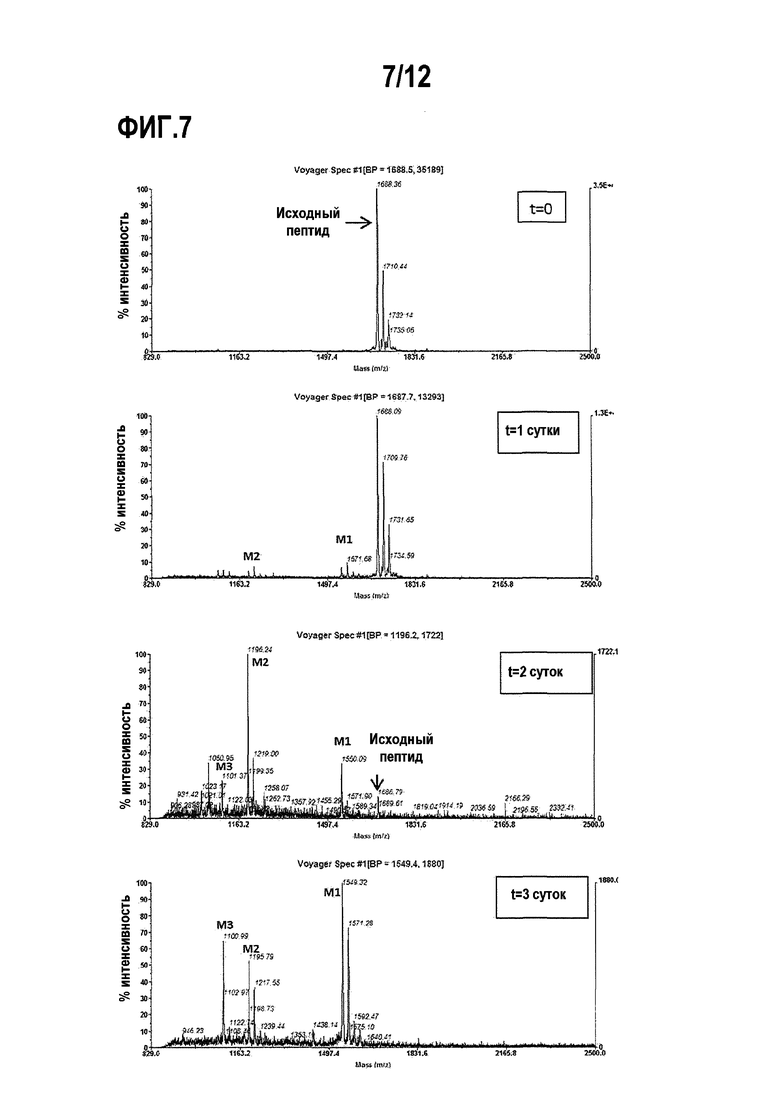
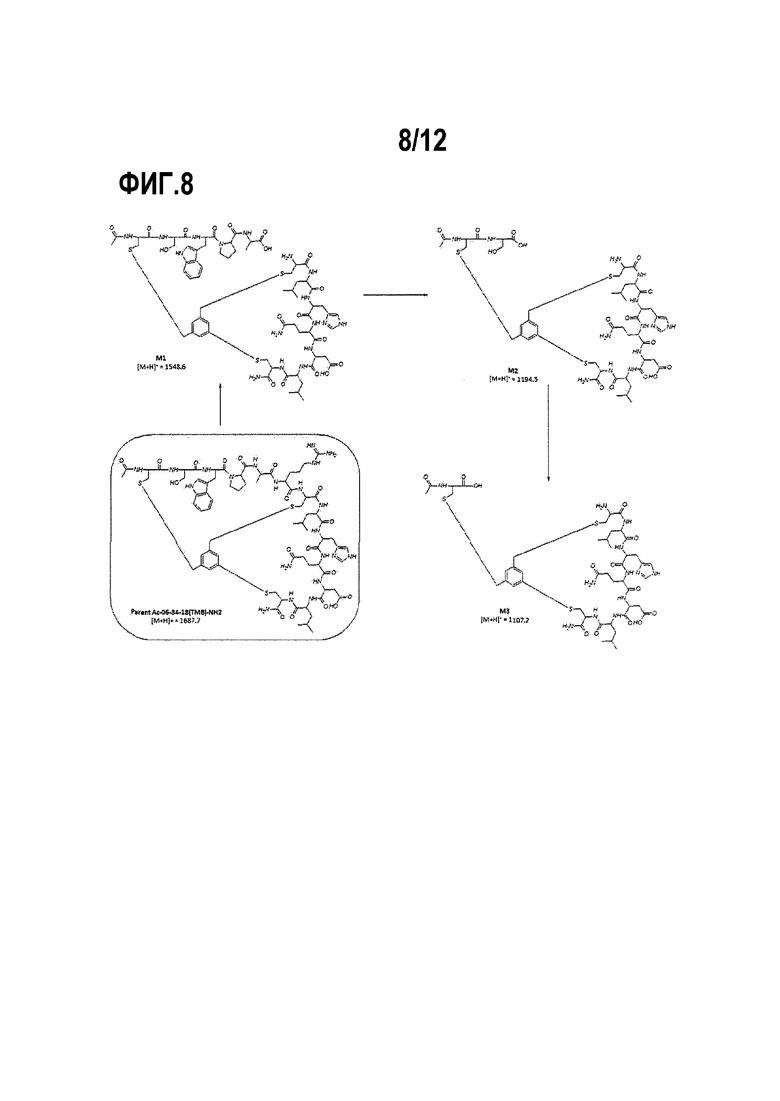
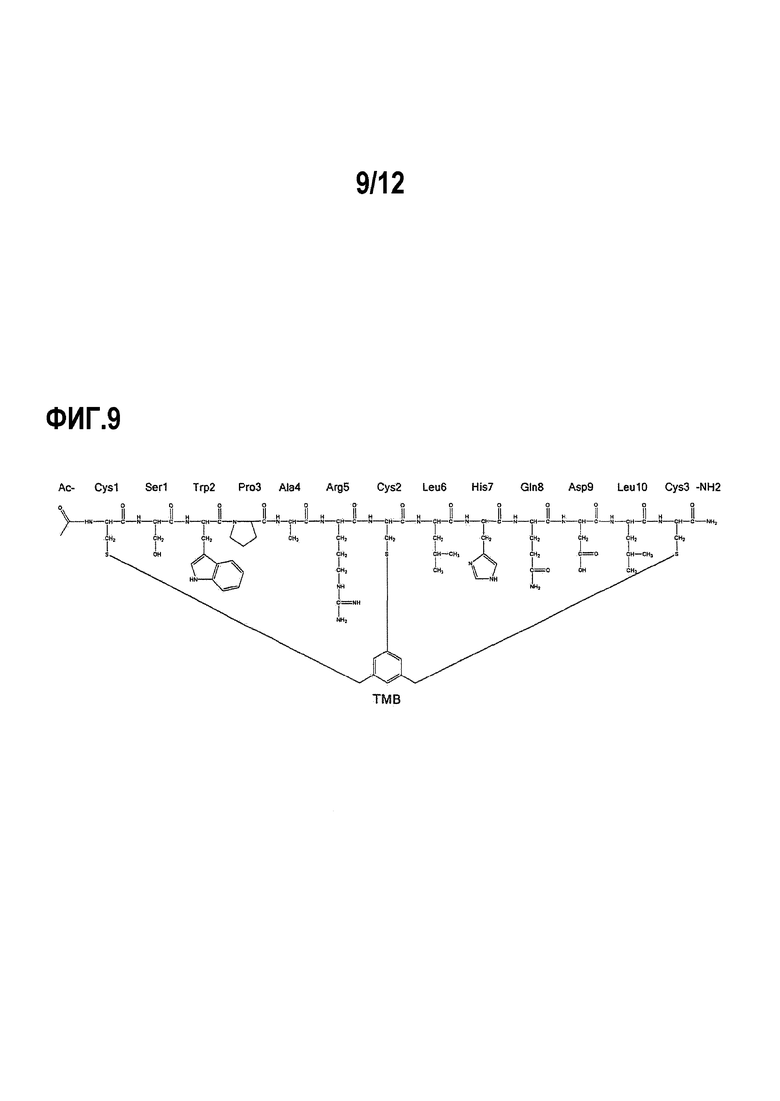
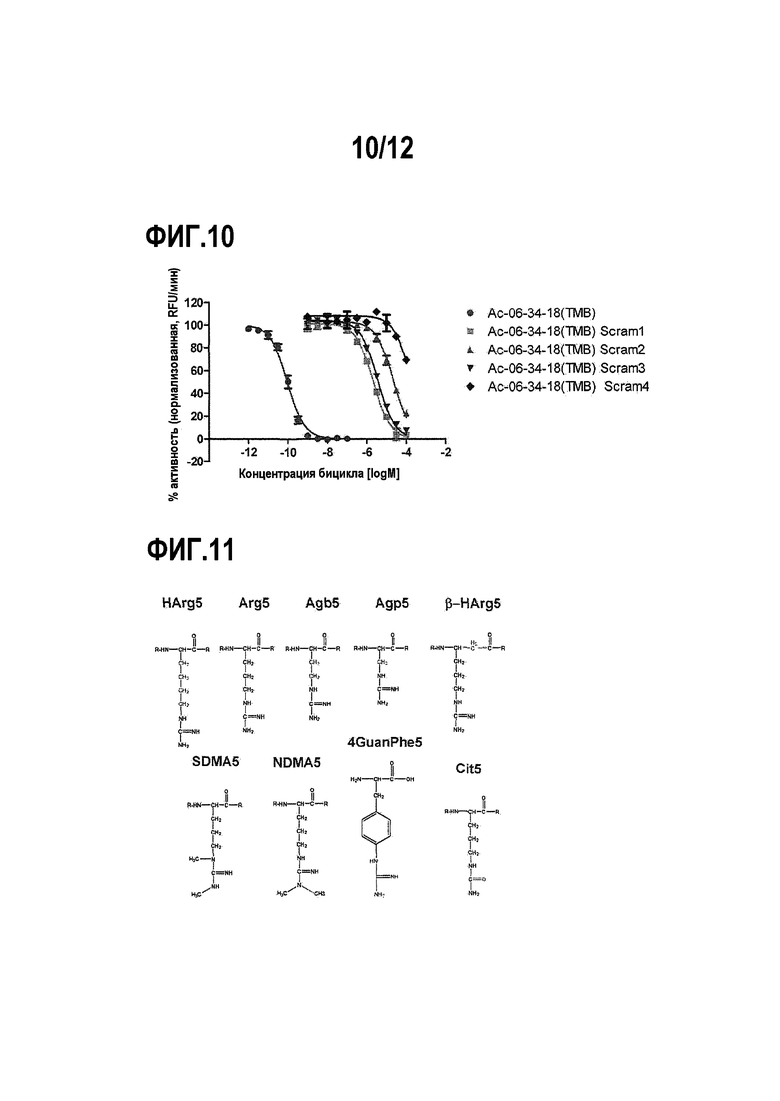

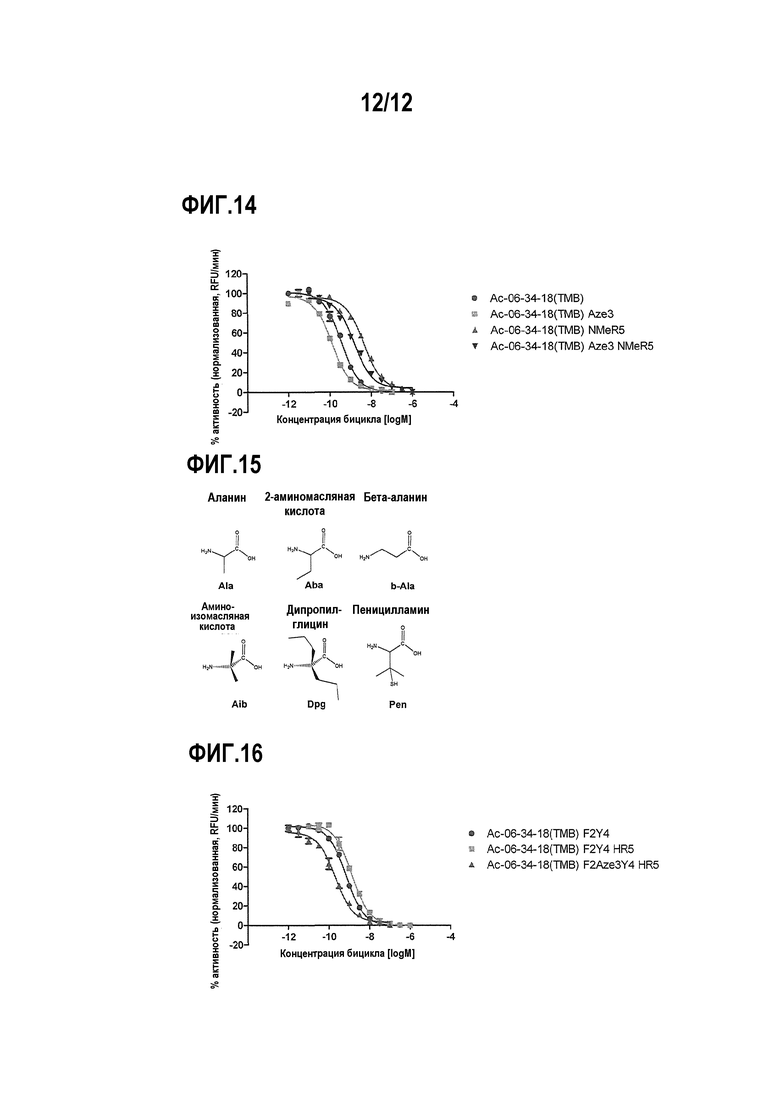
Изобретение относится к области биотехнологии, конкретно к пептидным лигандам человеческого плазматического калликреина, что может быть использовано в медицине. Путем скрининга библиотек мутантных пептидов получают лиганды к человеческому калликреину, библиотеки указанных лигандов и наборы библиотек указанных лигандов, отличающиеся тем, что полученный лиганд содержит аминокислотную последовательность WPAR. Изобретение позволяет получить лиганды к человеческому калликреину с повышенной специфичностью. 4 н. и 11 з.п. ф-лы, 16 ил., 22 табл., 6 пр.
1. Пептидный лиганд, специфичный к человеческому калликреину, содержащий полипептид, включающий три реакционноспособные группы, разделенные двумя последовательностями петель, и молекулярный каркас, который образует ковалентные связи с указанными реакционноспособными группами полипептида таким образом, что две полипептидные петли образуются на указанном молекулярном каркасе, где указанные петли указанного пептидного лиганда содержат три, четыре или пять, но менее шести аминокислот и где указанный полипептид содержит аминокислотную последовательность WPAR.
2. Пептид по п. 1, который включает один из пептидов: ACAWPARCLTVDLCA, ACRWPARCVHQDLCA, ACSWPARCNHQDLCA, ACRWPARCLTTSLCA, ACRWPARCTHQNYCA, ACTWPARCTHQNWCA, ACAWPARCLTTSLCG, ACTWPARCTMQNWCA.
3. Пептидный лиганд по п. 1, где указанные петли пептидного лиганда содержат пять аминокислот, и первая петля содержит мотив GrxWPARGr, где Gr представляет собой реакционноспособную группу.
4. Пептидный лиганд по п. 3, дополнительно содержащий вторую петлю, которая содержит мотив GrT/LHQ/TxLGr.
5. Пептидный лиганд по п. 1, который включает один из полипептидов


6. Пептидный лиганд по п. 4, где х представляет собой S или R.
7. Пептидный лиганд по п. 1, где указанная реакционноспособная группа представляет собой цистеин.
8. Пептидный лиганд по п. 1, который содержит один или более заместителей на основе неприродных аминокислот и устойчив к деградации под действием протеаз.
9. Полипептидный лиганд по п. 8, где указанная модифицированная аминокислота выбрана из N-метиларгинина, гомоаргинина, гидроксипролина и гуанидилфенилаланина, и азетидинкарбоновой кислоты.
10. Пептидный лиганд по п. 9, где указанный полипептид содержит первую петлю, которая включает мотив GrxWPARGr, где Pro замещен азетидинкарбоновой кислотой; и/или R замещен N-метиларгинином; и/или R замещен гомоаргинином; и/или R замещен гуанидилфенилаланином.
11. Способ получения мутантного полипептидного лиганда, специфичного к человеческому калликреину, с получением повышенного уровня активности связывания с мишенью по сравнению с таковой исходного полипептидного лиганда, где указанный исходный полипептидный лиганд содержит полипептид, включающий три реакционноспособные группы, разделенные двумя последовательностями петель, и молекулярный каркас, который образует ковалентные связи с указанными реакционноспособными группами полипептида так, что две полипептидные петли образуются на указанном молекулярном каркасе, где указанный полипептид содержит аминокислотную последовательность WPAR, включающий стадии:
(a) для каждого из двух или более аминокислотных положений в каждой из указанных петлевых последовательностей получение n различных библиотек мутантов, где каждая библиотека состоит из исходных полипептидов, в которых одно из указанных аминокислотных положений в петлевой последовательности мутировано замещением одной из n различных аминокислот, отличных от исходных;
(b) скрининг каждой библиотеки на связывание с исходной мишенью и оценка каждой мутации;
(c) идентификация аминокислотных положений, в которых допускаются мутации;
(d) получение одного или более мутантных полипептидов, содержащих одну или более мутаций, расположенных в аминокислотных положениях, идентифицированных на стадии (с).
12. Способ по п. 11, где стадия (d) включает получение библиотеки, содержащей полипептиды, которые включают мутации в двух или более аминокислотных положениях, идентифицированных на стадии (с), и скрининг библиотеки на полипептиды с повышенным уровнем активности связывания с мишенью.
13. Библиотека полипептидных лигандов, специфичных к человеческому калликреину, где полипептидные лиганды содержат полипептид, включающий три реакционноспособные группы, разделенные двумя последовательностями петель, и молекулярный каркас, который образует ковалентные связи с указанными реакционноспособными группами полипептида таким образом, что две полипептидные петли образуются на указанном молекулярном каркасе, где указанный полипептид содержит аминокислотную последовательность WPAR, где указанная библиотека состоит из m различных мутантов полипептидного лиганда, в которых определенное аминокислотное положение в указанных петлевых последовательностях мутировано замещением одной из m различных аминокислот, где m равно по меньшей мере 2.
14. Набор библиотек полипептидных лигандов, специфичных к человеческому калликреину, где полипептидные лиганды содержат полипептид, включающий три реакционноспособные группы, разделенные двумя последовательностями петель, и молекулярный каркас, который образует ковалентные связи с указанными реакционноспособными группами полипептида таким образом, что две полипептидные петли образуются на указанном молекулярном каркасе, где указанный полипептид содержит аминокислотную последовательность WPAR, где указанный набор включает две или более библиотеки полипептидных лигандов, где каждая из указанных библиотек полипептидных лигандов состоит из m различных мутантов полипептидного лиганда, в которых определенное аминокислотное положение в петлевых последовательностях мутировано замещением одной из m различных аминокислот.
15. Набор библиотек по п. 14, где m равно от 2 до 20.
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| APPEL J.R., Characterization of antigen-antibody interactions using single substitution analogs and mixture-based synthetic combinatorial librarie, J | |||
| Pept | |||
| Res., 1998, v.52, is.5, p.346-355 | |||
| BURGESS K | |||
| et al., DiSSiMiL: Diverse Small Size Mini-Libraries applied to simple and rapid epitope mapping of a monoclonal antibody, J | |||
| Pept | |||
| Res., 2001, v.57, is.1, p.68-76 | |||
| НЕУПОРЯДОЧЕННАЯ БИБЛИОТЕКА ПЕПТИДОВ, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И СПОСОБ ИДЕНТИФИКАЦИИ ПЕПТИДА, СИНТЕЗИРОВАННОГО ТВЕРДОФАЗНЫМ СИНТЕЗОМ | 1991 |
|
RU2145233C1 |
Авторы
Даты
2017-09-28—Публикация
2012-10-08—Подача