Изобретение относится к способам получения оксида алюминия с низким содержанием примесей, используемого для выращивания кристаллов, производства различных видов специальной керамики и огнеупоров.
В большинстве существующих способов получения оксида алюминия, основанных на термическом разложении гидроалюмокарбоната аммония, последний осаждают из растворов соли алюминия в присутствии растворов карбонатов аммония. Эти жидкофазные способы характеризуются повышенной энергоемкостью, значительными материальными потоками, многооперационностью, трудностью отделения осадка гидроалюмокарбоната аммония от раствора, а также связаны с образованием большого количества сточных вод, что снижает их экологичность.
Известен способ получения оксида алюминия (см. пат. 4053579 США, МКИ2 C01F 7/02, С01С 1/26, 1977), включающий добавление к раствору гидрокарбоната аммония с концентрацией 40-270 г/л раствора, содержащего алюминиевую соль, выбранную из группы, включающей хлорид алюминия, нитрат алюминия, сульфат алюминия, аммониевые квасцы и их основные соли, с концентрацией 5-150 г/л в пересчете на Al2O3. Соотношение эквивалентной массы реагентов в пересчете на Al3+/NH4+ составляет 0,07-0,75, при этом скорость добавления раствора алюминиевой соли равна 0,03-1,8 л/ч на 1000 см3 раствора гидрокарбоната аммония, а взаимодействие ведут при температуре 30-35°С и рН 7,5-9,0. Затем полученный гидроалюмокарбонат аммония отстаивают и выдерживают при той же температуре под маточным раствором в течение 15-20 минут для обеспечения роста кристаллов гидроалюмокарбоната аммония. Полученный осадок дважды промывают декантацией, отделяют фильтрацией и сушат при 105-110°С. Термическое разложение гидроалюмокарбоната аммония ведут при 1250-1300°С с получением оксида алюминия со средним размером частиц 0,5 мкм.
Недостатками данного способа являются его многооперационность и низкая интенсивность, обусловленные продолжительным временем смешения реагентов, необходимостью соблюдения большого числа режимных параметров, а также низкой скоростью фильтрации. Кроме того, получаемый гидроалюмокарбонат аммония имеет высокую влажность, что существенно повышает затраты на его последующую сушку. Способ характеризуется значительным объемом материальных потоков и получением большого количества разбавленных растворов солей аммония, что усложняет их утилизацию.
Известен также принятый в качестве прототипа способ получения оксида алюминия (см. пат. 8007760 США, МПК C01F 7/02, С01С 1/26, C01F 7/00 (2006.01), 2011), включающий предварительное получение порошка исходного оксида алюминия, его смешение с твердым карбонатом аммония, предпочтительно гидрокарбонатом аммония, и 5-30% воды с образованием реакционной массы, которую выдерживают при температуре 45-85°С в течение до 12 часов для полного протекания реакции получения гидроалюмокарбоната аммония, который подвергают разложению при температуре 130-320°С и прокалке при 400-800°С в течение 1-16 часов с образованием Al2O3. В качестве сырья для получения исходного оксида алюминия преимущественно используют гидроксид алюминия, получаемый по способу Байера. Полученный наноразмерный оксид алюминия с величиной удельной поверхности 169-502 м2/г дополнительно обрабатывают растворами кислот, чтобы удалить остаточный натрий, содержащийся в исходном оксиде алюминия.
Недостатком известного способа является его многооперационность и низкая интенсивность, обусловленная продолжительным временем синтеза. Кроме того, предварительное получение порошка оксида алюминия и двухстадийная термическая обработка гидроалюмокарбоната аммония требуют высоких энергетических затрат и сложного аппаратурного оформления. Использование гидроксида алюминия, получаемого по способу Байера, требует кислотной промывки его или получаемого оксида алюминия для удаления примеси натрия. Следствием этого является усложнение аппаратурного оформления процесса и значительные объемы кислых сточных вод, что снижает экологичность способа.
Настоящее изобретение направлено на достижение технического результата, заключающегося в интенсификации и снижении энергоемкости способа получения мелкодисперсного оксида алюминия. Техническим результатом является также исключение образования кислых сточных вод, что повышает экологичность способа.
Технический результат достигается тем, что в способе получения оксида алюминия, включающем смешение соединения алюминия и карбоната аммония, взятых в твердом виде, с образованием реакционной массы, содержащей гидроалюмокарбонат аммония, и ее термическую обработку, согласно изобретению, в качестве соединения алюминия берут его нитрат Al(NO3)3⋅9H2O или хлорид AlCl3⋅6H2O, карбонат аммония используют отдельно или в виде его смеси с гидрокарбонатом аммония, при этом количество гидрокарбоната аммония в смеси не превышает 50 мол. %, карбонат аммония или его смесь с гидрокарбонатом аммония берут в количестве 100-130% от стехиометрии на образование гидроалюмокарбоната аммония, смешение исходных компонентов производят в течение 10-30 минут, а термическую обработку реакционной массы ведут при температуре 300-600°С.
На достижение технического результата направлено и то, что перед термической обработкой реакционную массу промывают водой при температуре не выше 40°С до обеспечения величины рН промывной воды не более 7,5.
Сущность изобретения заключается в том, что при смешении кристаллических солей алюминия и карбоната аммония протекают следующие химические реакции:
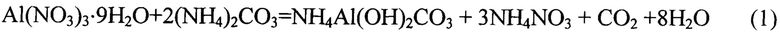
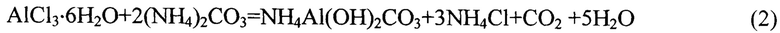
В случае использования смеси карбоната аммония с гидрокарбонатом аммония в дополнение к реакциям (1) и (2) будут протекать следующие химические реакции:
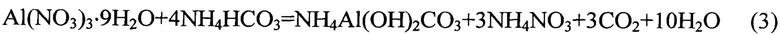

Возможность протекания этих реакций при смешении солей в твердом виде обусловлена наличием слабосвязанной воды в составе кристаллогидратов солей алюминия. Образующийся при этом гидроалюмокарбонат аммония обладает мелкодисперсной структурой, которая сохраняется при его термическом разложении. При промывке реакционной массы перед термическим разложением гидроалюмокарбоната аммония не происходит его гидролитического разложения вследствие наличия в растворе достаточного количества ионов аммония и низкой температуры промывной воды. При смешении твердых солей в отсутствие жидкой фазы гидроалюмокарбонат аммония образуется в малогидратированной форме и поэтому легко выделяется из суспензии фильтрованием.
Существенные признаки заявленного изобретения, определяющие объем правовой защиты и достаточные для получения вышеуказанного технического результата, выполняют функции и соотносятся с результатом следующим образом.
Использование нитрата Al(NO3)3⋅9H2O или хлорида AlCl3⋅6H2O в качестве соединений алюминия обусловлено наличием в них кристаллизационной воды в количестве, необходимом для протекания реакций (1-4) при смешении солей в твердом виде. Кроме того, их использование приводит к образованию нитратов или хлоридов аммония, которые при термическом разложении гидроалюмокарбоната аммония разлагаются или возгоняются, переходя в газовую фазу, и не загрязняют получаемый оксид алюминия.
Использование карбоната аммония или его смеси с гидрокарбонатом аммония позволяет при смешении с соединением алюминия получить гидроалюмокарбонат аммония, обладающий мелкодисперсной структурой, которая сохраняется при его термической обработке. Кроме того, смешение солей в твердом виде позволяет интенсифицировать способ, так как в этом случае их взаимодействие при смешении завершается за 10-30 минут и не требует дополнительной выдержки реакционной массы при повышенной температуре. При этом гидроалюмокарбонат аммония формируется в малогидратированной хорошо фильтруемой форме и легко выделяется из суспензии.
Количество гидрокарбоната аммония в его смеси с карбонатом аммония до 50 мол. % включительно позволяет получить гидроалюмокарбонат аммония без ухудшения его свойств, что расширяет сырьевую базу реагентов. Увеличение количества гидрокарбоната аммония свыше 50 мол. % приводит к получению вязкой пастообразной массы, что снижает технологичность способа.
Использование карбоната аммония или его смеси с гидрокарбонатом аммония в количестве 100-130% от стехиометрии на образование гидроалюмокарбоната аммония позволяет обеспечить полноту протекания взаимодействия. Расход карбоната аммония или его смеси с гидрокарбонатом аммония менее 100% от стехиометрии не обеспечивает полноту взаимодействия реагентов, а расход более 130% является избыточным и не улучшает результат.
Термическая обработка реакционной массы, содержащей гидроалюмокарбонат аммония, при температуре 300-600°С обеспечивает получение мелкодисперсного активного к спеканию оксида алюминия. Проведение обработки при температуре менее 300°С не обеспечивает полного разложения гидроалюмокарбоната аммония до оксида, в то время как температура более 600°С является избыточной и приводит к неоправданному повышению энергоемкости способа.
Совокупность вышеуказанных признаков необходима и достаточна для достижения технического результата изобретения, заключающегося в интенсификации способа и снижении его энергоемкости при получения мелкодисперсного оксида алюминия.
В частном случае осуществления предпочтительны следующие операции и режимные параметры.
Промывка реакционной массы водой при температуре не выше 40°С обеспечивает стабильность гидроалюмокарбоната аммония к гидролитическому разложению в ходе промывки. Значение рН промывной воды 7,5 и менее свидетельствует об отсутствии в составе гидроалюмокарбоната аммония примесей, которые могут присутствовать в исходных реагентах.
Вышеуказанные частные признаки изобретения позволяют осуществить способ в оптимальном режиме с точки зрения интенсификации и снижения энергоемкости получения мелкодисперсного оксида алюминия и исключения образования кислых сточных вод.
Сущность предлагаемого способа может быть более наглядно проиллюстрирована следующими примерами.
Пример 1. 100 г кристаллического нитрата алюминия Al(NO3)3⋅9H2O смешивают с 51,2 г кристаллического карбоната аммония (NH4)2CO3 в лопастном смесителе в течение 10 минут. Расход карбоната аммония составляет 100% от стехиометрии на образование гидроалюмокарбоната аммония. Полученную реакционную массу весом 139,5 г, которая по данным РФА представляет собой смесь гидроалюмокарбоната аммония NH4Al(OH)2CO3 и нитрата аммония, подвергают термической обработке в течение 2 часов при температуре 550°С. В результате получают 13,4 г мелкодисперсного порошка оксида алюминия с удельной поверхностью 512 м2/г и средним размером частиц 2,1 мкм.
Пример 2. 100 г кристаллического хлорида алюминия AlCl3⋅6Н2О смешивают с 95,4 г кристаллического карбоната аммония (NH4)2СО3 в лопастном смесителе в течение 20 минут. Расход карбоната аммония составляет 120% от стехиометрии на образование гидроалюмокарбоната аммония. Полученную реакционную массу весом 177,2 г, которая по данным РФА представляет собой смесь гидроалюмокарбоната аммония, хлорида аммония NH4Cl и карбоната аммония, подвергают термической обработке в течение 2 часов при температуре 300°С. В результате получают 21,1 г мелкодисперсного порошка оксида алюминия с удельной поверхностью 598 м2/г и средним размером частиц 1,8 мкм.
Пример 3. 100 г кристаллического нитрата алюминия Al(NO3)3⋅9H2O смешивают с 37,5 г кристаллического карбоната аммония (NH4)2CO3 и 30,9 г гидрокарбоната аммония NH4HCO3 в лопастном смесителе в течение 15 минут. Содержание NH4HCO3 в смеси карбонатов составляет 50 мол. %, общий расход карбонатов 110% от стехиометрии на образование гидроалюмокарбоната аммония. Полученную реакционную массу весом 148,9 г, которая по данным РФА представляет собой смесь гидроалюмокарбоната аммония, нитрата аммония, карбоната аммония и гидрокарбоната аммония, подвергают термической обработке в течение 2 часов при температуре 600°С. В результате получают 13,2 г мелкодисперсного порошка оксида алюминия с удельной поверхностью 407 м2/г и средним размером частиц 2,7 мкм.
Пример 4. 100 г кристаллического хлорида алюминия AlCl3⋅6H2O смешивают с 78,6 г кристаллического карбоната аммония (NH4)2CO3 и 27,7 г гидрокарбоната аммония NH4HCO3 в лопастном смесителе в течение 30 минут. Содержание NH4HCO3 в смеси карбонатов составляет 30 мол. %, общий расход карбонатов равен 120% от стехиометрии на образование гидроалюмокарбоната аммония. Полученную реакционную массу весом 181,7 г, которая по данным РФА представляет собой смесь гидроалюмокарбоната аммония, хлорида аммония, карбоната аммония и гидрокарбоната аммония, подвергают термической обработке в течение 2 часов при температуре 550°С.
В результате получают 20,9 г мелкодисперсного порошка оксида алюминия с удельной поверхностью 326 м2/г и средним размером частиц 3,1 мкм.
Пример 5. 100 г кристаллического нитрата алюминия Al(NO3)3⋅9H2O смешивают с 66,6 г кристаллического карбоната аммония (NH4)2CO3 в лопастном смесителе в течение 20 минут. Расход карбоната аммония составляет 130% от стехиометрии на образование гидроалюмокарбоната аммония. Полученную реакционную массу весом 154,8 г, которая по данным РФА представляет смесь гидроалюмокарбоната аммония, нитрата аммония NH4NO3 и карбоната аммония, распульповывают в 300 мл воды при температуре 40°С. Образовавшуюся суспензию фильтруют на нутч-фильтре с выделением осадка. Скорость фильтрации составляет 1270 л/(м2⋅ч). Полученный осадок промывают водой при температуре 40°С до обеспечения величины рН промывной воды 7,5. Промытый осадок сушат при 105°С до постоянной массы. Получают 37,4 г сухого осадка, который представляет собой гидроалюмокарбонат аммония. Осадок подвергают термической обработке в течение 2 часов при температуре 550°С. В результате получают 13,3 г мелкодисперсного порошка оксида алюминия с удельной поверхностью 361 м2/г и средним размером частиц 2,5 мкм.
Пример 6. 100 г кристаллического хлорида алюминия AlCl3⋅6H2O смешивают с 78,6 г кристаллического карбоната аммония (NH4)2CO3 и 27,7 г гидрокарбоната аммония NH4HCO3 в лопастном смесителе в течение 30 минут. Содержание NH4CO3 в смеси карбонатов составляет 30 мол. %, общий расход карбонатов равен 120% от стехиометрии на образование гидроалюмокарбоната аммония. Полученную реакционную массу весом 181,7 г, которая по данным РФА представляет собой смесь гидроалюмокарбоната аммония, хлорида аммония, карбоната аммония и гидрокарбоната аммония, распульповывают в 300 мл воды при температуре 30°С. Образовавшуюся суспензию фильтруют на нутч-фильтре с выделением осадка. Скорость фильтрации составляет 1180 л/(м2⋅ч). Полученный осадок промывают водой при температуре 22°С до обеспечения величины рН промывной воды 7,3. Промытый осадок сушат при 105°С до постоянной массы. Получают 57,8 г сухого осадка, который представляет собой гидроалюмокарбонат аммония. Осадок подвергают термической обработке в течение 2 часов при температуре 500°С. В результате получают 20,9 г мелкодисперсного порошка оксида алюминия с удельной поверхностью 234 м2/г и средним размером частиц 3,5 мкм.
Из приведенных Примеров видно, что заявляемый способ позволяет получить в условиях твердофазного процесса мелкодисперсный оксид алюминия с удельной поверхностью 234-598 м2/г, что в 1,2-1,4 раза выше, чем по прототипу. Способ согласно изобретению является менее длительным и энергоемким. Способ исключает образование кислых сточных вод, что повышает его экологичность. Предлагаемый способ относительно прост и может быть реализован с привлечением стандартного технологического оборудования.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОКСИДА АЛЮМИНИЯ | 2014 |
|
RU2577832C1 |
| Способ получения слоистого гидроксида магния и алюминия | 2017 |
|
RU2678007C1 |
| Способ получения корундовой керамики | 2020 |
|
RU2737169C1 |
| Способ получения мелкодисперсного порошка оксида иттрия | 2021 |
|
RU2766414C1 |
| Способ получения нанопористой керамики на основе муллита | 2020 |
|
RU2737298C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРАТА ОКСИДА МЕТАЛЛА | 2008 |
|
RU2375306C1 |
| Комплексный способ получения малоагломерированных высокостехиометричных наноразмерных порошков прекурсора на основе иттрий-алюминиевого граната с оксидами редкоземельных элементов | 2019 |
|
RU2721548C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОСОВМЕСТИМОЙ ПОРИСТОЙ КЕРАМИКИ НА ОСНОВЕ ДИОКСИДА ЦИРКОНИЯ ДЛЯ ЭНДОПРОТЕЗИРОВАНИЯ | 2020 |
|
RU2741918C1 |
| Способ переработки алюминиевых квасцов | 2018 |
|
RU2677204C1 |
| Способ получения алюмината лития | 2022 |
|
RU2793006C1 |
Изобретение может быть использовано при получении оксида алюминия с низким содержанием примесей, используемого для выращивания кристаллов, производства керамики и огнеупоров. Нитрат алюминия Al(NO3)3⋅9H2O или хлорид алюминия AlCl3⋅6H2O смешивают с карбонатом аммония или со смесью карбоната аммония и гидрокарбоната аммония. Количество гидрокарбоната аммония в смеси не превышает 50 мол.%. Смешивание проводят в течение 10-30 минут с образованием реакционной массы, содержащей гидроалюмокарбонат аммония. Карбонат аммония или его смесь с гидрокарбонатом аммония берут в количестве 100-130% от стехиометрии на образование гидроалюмокарбоната аммония. Полученную реакционную массу подвергают термической обработке при температуре 300-600°С с получением оксида алюминия. Изобретение позволяет получить в условиях твердофазного процесса мелкодисперсный оксид алюминия с удельной поверхностью 234-598 м2/г, уменьшить длительность и энергоемкость процесса, исключить образование кислых сточных вод, что повышает экологичность. 1 з.п. ф-лы, 6 пр.
1. Способ получения оксида алюминия, включающий смешение соединения алюминия и карбоната аммония, взятых в твердом виде, с образованием реакционной массы, содержащей гидроалюмокарбонат аммония, и ее термическую обработку, отличающийся тем, что в качестве соединения алюминия берут его нитрат Al(NO3)3⋅9H2O или хлорид AlCl3⋅6H2O, карбонат аммония используют отдельно или в виде его смеси с гидрокарбонатом аммония, при этом количество гидрокарбоната аммония в смеси не превышает 50 мол. %, карбонат аммония или его смесь с гидрокарбонатом аммония берут в количестве 100-130% от стехиометрии на образование гидроалюмокарбоната аммония, смешение исходных компонентов производят в течение 10-30 минут, а термическую обработку реакционной массы ведут при температуре 300-600°С.
2. Способ по п. 1, отличающийся тем, что перед термической обработкой реакционную массу промывают водой при температуре не выше 40°С до обеспечения величины рН промывной воды не более 7,5.
| US 8007760 B2, 30.08.2011 | |||
| Способ получения сорбентов на основе окиси алюминия | 1977 |
|
SU706103A1 |
| US 7947250 B2, 24.05.2011 | |||
| WO 8701365 A, 12.03.1987 | |||
| CN 1369434 A, 18.09.2002 | |||
| JP 58026029 A, 16.02.1983. | |||
Авторы
Даты
2017-10-04—Публикация
2016-10-21—Подача