Предлагаемое изобретение относится к органической химии, в частности, к способу получения 1-алкил-1-азациклоалкадиинов общей формулы (1).

Соединения общей формулы (1) могут быть использованы в качестве универсальных прекурсоров для тонкого органического синтеза [Haraburda Е., Lledó A., Roglans A., Pla-Quintana A. Org. Lett, 2015, 17, 2882; Tanaka K., Nishida G., Sagae H., Hirano M. Synlett, 2007, 9, 1426-1430; Shibata Т., Uchiyama Т., Endo K. Org. Lett, 2009, 11, 3906] и биологически активных соединений [Dembitsky V.M., Levitsky D.O. Nat. Prod. Commun. 2006, 1, 405; Chen J.J., Swope D.M., Dashtipour K., Clin. Ther., 2007, 29, 1825].
Известен способ (Ritter, J.; Gleiter, R. Preparation of 1-azacyclododeca-3,8-diynes and l,6-diazacyclododeca-3,8-diynes. Liebigs Ann. Recueil. 1997, 2113-2118) получения 1-метил-, 1-изо-пропил-1-азациклоалка-3,8-диинов (2a-c) в смеси с макроциклами (3a, b) реакцией азациклизации 1,9-дибромо-2,7-нонадиина или 1,10-дибромо-2,8-декадиина с метил- или изо-пропиламином в присутствии K2CO3 в THF при 40°C в атмосфере аргона:

Известен способ [Epsztein, R.; Goff, N. Le. Synthese de bases de Mannich acetyleniques cycliques. Tetrahedron Lett. 1985, 26, 3203] получения 1-метил-1-азациклодека-3,8-диина (2a) в смеси с макроциклом (3а) и полимером неустановленного строения с выходами 40 и 12% соответственно реакцией внутримолекулярной циклизации N-(метоксиметил)-N-метил-N-(2,7-октадиинил)амина в диоксане в присутствии Cul и N-метилпиперидина в условиях высокого разбавления по схеме:

Таким образом, в литературе отсутствуют сведения о селективном получении 1-алкил-1-азациклоалкадиинов общей формулы (1).
Предлагается новый способ селективного получения 1-алкил-1-азациклоалкадиинов общей формулы (1).
Сущность способа заключается во взаимодействии N-алкил-N,N-бис(этоксиметил)амина общей формулы RN(CH2OEt)2, где R=н-Bu, трет-Bu с α,ω-диацетиленом общей формулы НС≡C-CH2-[CH2]n-CH2-С≡СН, где n=1-4, в присутствии катализатора CuBr2 при мольном соотношении N-алкил-N,N-бис(этоксиметил)амин : α,ω-диацетилен : CuBr2 = 1 : 1 : (0.03-0.07), предпочтительно 1 : 1 : 0.05, в атмосфере аргона при температуре 80°C и атмосферном давлении в толуоле в качестве растворителя в течение 5-7 ч. Выход 1-алкил-1-азациклоалкадиинов (1) составляет 43-56%. Реакция протекает по схеме:
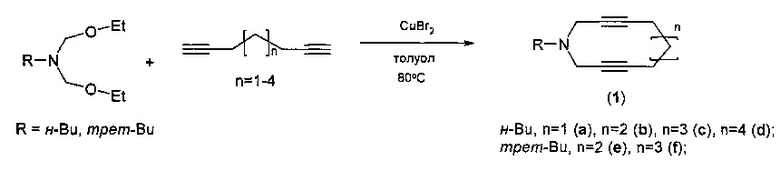
1-Алкил-1-азациклоалкадиины (1) образуются только лишь с участием N-алкил-N,N-бис(этоксиметил)аминов и α,ω-диацетиленов, взятых в мольном соотношении 1:1 (стехиометрические количества), под действием катализатора CuBr2 (5 мол. %). При другом соотношении исходных реагентов или в присутствии других Cu-содержащих катализаторов (CuCl, CuCl2, CuBr) снижается выход целевого продукта (1). Проведение указанной реакции в присутствии катализатора CuBr2 больше 7 мол. % по отношению к 1-алкил-1-азациклоалкадиинам не приводит к существенному увеличению выхода целевого продукта (1). Использование катализатора CuBr2 менее 3% снижает выход (1), что связано, возможно, со снижением каталитически активных центров в реакционной массе. Реакции проводили при температуре 80°C. При температуре выше 80°C (например, 100°C) увеличиваются энергозатраты, а при температуре ниже 80°C (например, 60°C) снижается скорость реакции. Опыты проводили в толуоле, т.к. в нем хорошо растворяются исходные реагенты и целевые продукты.
Существенные отличия предлагаемого способа
В известных способах в качестве исходных реагентов применяются α,ω-дибромоадкадиины (1,9-дибромо-2,7-нонадиин, 1,10-дибромо-2,8-декадиин) или диацетиленовый гем-аминоэфир (N-(метоксиметал)-N-метил-N-(2,7-октадиинил)амин). Известные способы позволяют получать 1-алкил-1-азациклоалкадиины в смеси с диазаалкатетраинами и полимерами в условиях высокого разбавления. В предлагаемом способе в качестве исходных реагентов применяются коммерчески доступные α,ω-диацетилены. Предлагаемый способ позволяет селективно получать индивидуальные 1-алкил-1-азациклоалкадиины общей формулой (1).
Способ поясняется следующими примерами.
Пример 1. В сосуд Шленка, установленный на магнитной мешалке, в атмосфере аргона помещают 0.189 гр (1 ммоль) N,N-бис(этоксиметил)-N-бутиламина, 3 мл толуола и 0.11 гр 1,7-октадиина (1 ммоль), добавляют CuBr2 (0.01 г, 5 мол. %), перемешивают при температуре 80°C в течение 6 ч, отфильтровывают через слой SiO2, промывают хлороформом 3×5 мл, упаривают, целевой продукт очищают методом колоночной хроматографии. Выход 1-бутил-1-аза-3,9-циклоундекадиина (1b) составляет 0.102 г (50%). Другие примеры, подтверждающие способ, приведены в табл. 1.
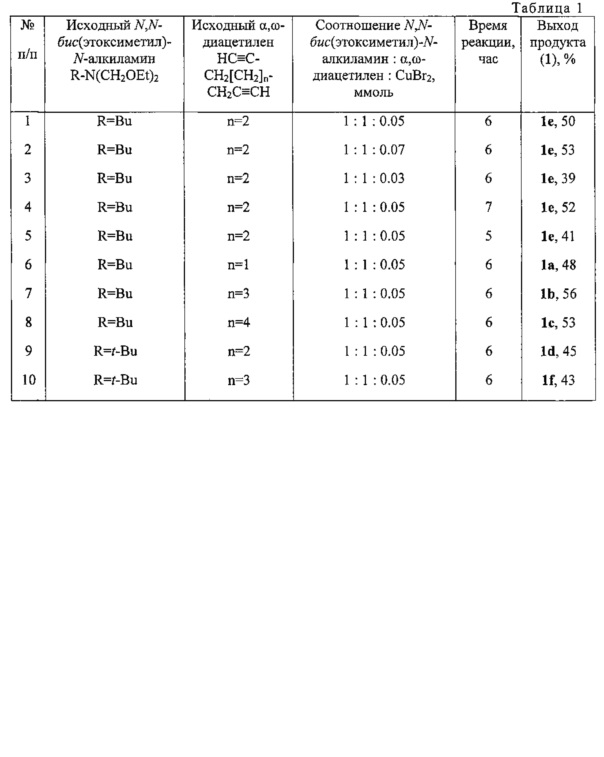
Физико-химические характеристики соединений 1a-1f:* 
1-Бутил-1-аза-3,8-циклодекадиин (1а)

Желтое масло, Rf 0.41 (гексан - EtOAc, 2:1). ИК-спектр: 606 (-C≡C-H), 1076 (-C-N-), 1259 ((-C≡C-H), 1455 (-CH2), 1456 (-CH3), 2204 (-C≡C-), 2262 (-С≡C-), 2861 (CH3), 2930 (CH2) см-1. Спектр ЯМР 1H (400, δ, м.д.): 0.96 (3H, т, J=7.2 Гц, CH3); 1.34-1.49 (4Н, м, CCCH2CH2CH2CC, CH2CH3); 1.75-1.81 (2Н, м, CH2CH2CH3); 2.36-2.39 (4Н, м, CCCH2CH2CH2CC); 2.82 (2Н, т, J=6.8 Гц, NCH2CH2); 3.52 (4Н, с, NCH2CC). Спектр ЯМР 13C (400, δ, м.д.): 14.1 (CH3); 19.9 (CCCH2CH2CH2CC); 20.6 (CH2CH3); 25.9 (CCCH2CH2CH2CC); 29.8 (CH2CH2CH3); 44.8 (N(CH2CC)2); 50.3 (NCH2CH2); 78.3 (NCH2CC); 87.1 (NCH2CC). Масс-спектр (ЭУ, 70 эВ), m/z (Iотн, %): 188 [M-H]+ (8), 174 [М-CH3]+ (8), 160 [М-CH2CH3]+ (8), 146 [М-CHCH2CH3]+ (100), 117 [M-NH(CH2)3CH3]+ (34), 91 [NH(CH2C≡C)2]+ (57). Найдено, %: C 82.59; H 10.21; N 7.34. C13H19N. Вычислено, %: C 82.48; Н 10.12; N 7.40.
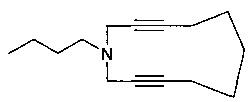
1 -Бутил-1-аза-3,9-циклоундекадиин (1b)

Коричневое масло, Rf 0.56 (гексан - EtOAc, 2:1). ИК-спектр: 613 (-С≡С-Н), 1078, 1142 (-C-N-), 1458 (-CH3), 2250 (-C≡C-), 2856 (CH3), 2924 (CH2) см-1. Спектр ЯМР 1H (δ, м.д.): 0.93 (3H, т, J=6.0 Гц, CH3); 1.33-1.37 (2Н, м, CH2CH3); 1.44-1.47 (2Н, м, CH2CH2CH3); 1.62 (4Н, с, (CCCH2CH2)2); 2.23 (4Н, с, (CCCH2CH2)2); 2.48 (2Н, т, J=6.0 Гц, NCH2CH2); 3.37 (NCH2CC). Спектр ЯМР 13С (δ, м.д.): 14.0 (CH3); 18.3 ((CCCH2CH2)2); 20.7 (CH2CH3); 27.9 ((CCCH2CH2)2); 29.6 (NCH2CH2); 42.6 (NCH2CC); 52.6 (NCH2CH2); 75.3 (NCH2CC); 84.5 (NCH2CC). Масс-спектр (ЭУ, 70 эВ), m/z (Iотн, %): 202 [M-H]+ (9), 174 [М-CH2CH3]+ (9), 160 [М-(CH2)2CH3]+ (100), 91 [NH(CH2C≡C)2]+ (62). Найдено, %: C 82.75; H 10.37; N 6.83. C14H21N. Вычислено, %: C 82.70; H 10.41; N 6.89.
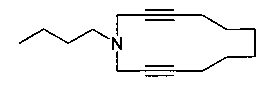
1-Бутил-1-аза-3,10-циклододекадиин (1c)
Желтое масло, Rf 0. 26 (гексан:EtOAc, 2:1). ИК-спектр: 615 (-C≡C-H), 1080, 1141 (-C-N-), 1455 (-CH3), 2250 (-C≡C-), 2858 (CH3), 2926 (CH2) см-1; Спектр ЯМР 1H (δ, м.д.): 0.96 (3H, т, J=6.0 Гц, CH3); 1.28 (2Н, с, CH2CH3); 1.35-1.41 (2Н, м, CH2CH2CH3); 1.46-1.52 (4Н, м, ((CCCH2CH2)2CH2); 1.88-1.91 (2Н, пент, (CCCH2CH2)2CH2); 2.26-2.28 (4Н, м, (CCCH2CH2)3); 2.73-2.78 (2Н, т, J=7.2 Гц, NCH2CH2); 3.53 (NCH2CC). Спектр ЯМР 13С (δ, м.д.): 14.0 (CH3); 17.9 ((СССН2СН2)2CH2); 20.6 (CH2CH3); 24.1 ((CCCH2CH2)2CH2); 24.6 ((CCCH2CH2)2CH2); 29.7 (NCH2CH2); 44.4 (NCH2CC); 50.3 (NCH2CH2); 75.5 (NCH2CC); 84.6 (NCH2CC). Масс-спектр (ЭУ, 70 эВ), m/z (Iотн, %): 217 [M]+ (10), 174 [М-(CH2)2CH3]+ (100), 91 [NH(CH2C≡C)2]+ (29). Найдено, %: C 82.94; H 10.63; N 6.39. C15H23N. Вычислено, %: C 82.89; H 10.67; N 6.44.
1-Бутил-1-аза-3,11-циклотридекадиин (1d)
Коричневое масло, Rf 0.47 (гексан:EtOAc, 1:1). ИК-спектр: 609 (-C≡С-H), 1076, 1143 (-C-N-), 1460 (-CH3), 2259 (-С≡C-), 2859 (CH3), 2932 (CH2) см-1; Спектр ЯМР 1H (δ, м.д.): 0.94 (3H, т, J=7.2 Гц, CH3); 1.35-1.52 (12Н, м, (CCCH2CH2CH2)2, CH2CH2CH3); 2.20 (4Н, с, ((CCCH2CH2CH2)2); 2.48-2.49 (2Н, м, (NCH2CH2)); 3.38 (NCH2CC). Спектр ЯМР 13С (δ, м.д.): 14.0 (CH3); 18.7 ((CCCH2CH2CH2)2); 20.7 (CH2CH3); 28.4 ((CCCH2CH2CH2)2); 24.8 ((CCCH2CH2CH2)2); 29.7 (NCH2CH2); 42.6 (NCH2CC); 52.6 (NCH2CH2); 75.1 (NCH2CC); 84.9 (NCH2CC). Масс-спектр (ЭУ, 70 эВ), m/z (Iотн, %): 231 [M]+ (6), 188 [М-(CH2)2CH3]+ (100), 91 [NH(CH2C≡C)2]+ (29). Найдено, %: C 83.02; H 10.94; N 6.09. C16H25N. Вычислено, %: C 83.06; H 10.89; N 6.05.
1-(Трет-бутил)-1-аза-3,9-циклоундекадиин (1e)

Темно-желтое масло. ИК-спектр: 628 (-C≡C-H), 1108, 1143 (-C-N-), 1457 (-CH3), 2118 (-C≡С-), 2234 (-C≡C-), 2862 (CH3), 2928 (CH2) см-1; Спектр ЯМР 1H (δ, м.д.): 1.19 (9Н, с, CH3); 1.61-1.65 (4Н, м, (C≡CCH2CH2)2); 2.21-2.22 (4Н, м, (C≡CCH2CH2)2); 3.59 (4Н, с, NCH2CC). Спектр ЯМР 13С (δ, м.д.): 18.5 ((CCCH2CH2)2); 27.5 (CH3); 27.9 ((CCCH2CH2)2); 36.7 (NCH2CC); 54.9 (NC(CH3)3); 77.8 (NCH2CC); 84.0 (NCH2CC). Масс-спектр (ЭУ, 70 эВ), m/z (Iотн, %): 203 [M]+ (11), 188 [М-CH3]+ (100), 91 [NH(CH2C≡C)2]+ (31). Найдено, %: C 82.76; H 10.34; N 6.82. C14H21N. Вычислено, %: C 82.70; H 10.41; N 6.89.
1-(Трет-бутил)-1-аза-3,10-циклододекадиин (1f)
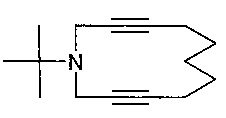
Желтое масло. Спектр ЯМР 1H (δ, м.д.): 1.18 (9Н, с, CH3); 1.50-1.51 (4Н, м, (СССН2СН2)2CH2, (CCCH2CH2)2CH2); 2.18-2.19 (4Н, м, (CCCH2CH2)2CH2), 3.58 (4Н, м, NCH2CC). Спектр ЯМР 13С (δ, м.д.): 18.9 ((CCCH2CH2)2CH2); 27.5 (CH3); 28.0 ((CCCH2CH2)2CH2); 28.4 ((CCCH2CH2)2CH2); 36.7 (NCH2CC); 54.9 (NC(CH3)3); 77.6 (NCH2CC); 84.0 (NCH2CC). Масс-спектр (ЭУ, 70 эВ), m/z (Iотн, %): 217 [М]+ (11), 202 [М-CH3]+ (100), 91 [NH(CH2C≡С)2]+ (26). Найдено, %: C 82.97; H 10.58; N 6.53. C15H23N. Вычислено, %: C 82.89; H 10.67; N 6.44.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ N-АЛКИЛ-N,N-ДИ(АЛКАДИИНИЛ)АМИНОВ | 2015 |
|
RU2626008C2 |
| СПОСОБ ПОЛУЧЕНИЯ N-АЛКИЛ-N,N-БИС[ω-(ПИПЕРИДИН-1-ИЛ)АЛКАДИИН-1-ИЛ]АМИНОВ, ПРОЯВЛЯЮЩИХ ФУНГИЦИДНУЮ АКТИВНОСТЬ | 2019 |
|
RU2734488C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-АЛКИЛ(ФЕНИЛ)-N,N-БИС[4-АЛКОКСИ(ФЕНОКСИ-, БЕНЗИЛОКСИ-, ПРОП-2-ИНИЛОКСИ)-2-БУТИНИЛ]АМИНОВ | 2016 |
|
RU2675505C2 |
| N,N'-ДИ(АЛКАДИИНИЛ)ДИАЗАЦИКЛОАЛКАНЫ И СПОСОБ ПОЛУЧЕНИЯ N,N'-ДИ(АЛКАДИИНИЛ)ДИАЗАЦИКЛОАЛКАНОВ, ПРОЯВЛЯЮЩИХ ФУНГИЦИДНУЮ АКТИВНОСТЬ ПО ОТНОШЕНИЮ К ГРИБАМ Bipolaris sorokiniana и Rhizoctonia solani | 2019 |
|
RU2727138C1 |
| ПРОИЗВОДНЫЕ ПИРИДОКСИНА С НЕЛИНЕЙНЫМИ ОПТИЧЕСКИМИ СВОЙСТВАМИ | 2012 |
|
RU2501801C1 |
| АНТИРЕТРОВИРУСНЫЕ ПРЕПАРАТЫ НА ОСНОВЕ ПРОИЗВОДНЫХ АЗИДОТИМИДИНА | 2014 |
|
RU2561501C1 |
| Соединения фторхинолонового ряда на основе производных пиридоксина, обладающие антибактериальными свойствами | 2019 |
|
RU2713932C1 |
| СПОСОБ ПОЛУЧЕНИЯ 5-АЛКИЛ-1,3,5-ТРИАЗИНАН-2-(ТИ)ОНОВ | 2012 |
|
RU2522446C2 |
| СПОСОБ ПОЛУЧЕНИЯ N-(1,5,3-ДИТИАЗЕПАН-3-ИЛ)КАРБОНОВЫХ КИСЛОТ | 2014 |
|
RU2601310C2 |
| 1-ОМЕГА-АРИЛОКСИАЛКИЛ- И 1-БЕНЗИЛЗАМЕЩЕННЫЕ 2-ИМИНОБЕНЗИМИДАЗОЛИНЫ И ИХ ФАРМАКОЛОГИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, ОБЛАДАЮЩИЕ ПРОТИСТОЦИДНОЙ И АНТИМИКРОБНОЙ АКТИВНОСТЬЮ | 2012 |
|
RU2514196C1 |
Изобретение относится к способу получения 1-алкил-1-азациклоалкадиинов формулы (1)
 . Технический результат: разработан новый селективный способ получения индивидуальных 1-алкил-1-азациклоалкадиинов, которые могут быть использованы в качестве универсальных прекурсоров для тонкого органического синтеза и биологически активных соединений. 1 табл., 1 пр.
. Технический результат: разработан новый селективный способ получения индивидуальных 1-алкил-1-азациклоалкадиинов, которые могут быть использованы в качестве универсальных прекурсоров для тонкого органического синтеза и биологически активных соединений. 1 табл., 1 пр.
Способ получения 1-алкил-1-азациклоалкадиинов общей формулы (1)
 ,
,
отличающийся тем, что N-алкил-N,N-бис(этоксиметил)амин общей формулы RN(CH2OEt)2 (где R= н-Bu, трет-Bu) подвергают взаимодействию с α,ω-диацетиленом общей формулы НС≡С-СН2-(СН2)n-СН2-С≡СН (где n=1-4) в присутствии катализатора CuBr2 при мольном соотношении N-алкил-N,N-бис(этоксиметил)амин : α,ω-диацетилен : CuBr2=1:1:(0.03-0.07) в атмосфере аргона при температуре 80°C и атмосферном давлении в среде толуола в течение 5-7 ч.
| СПОСОБ ПОЛУЧЕНИЯ α,ω-ДИ(АМИНОМЕТИЛ)-АЛКАДИИНОВ | 2008 |
|
RU2440322C2 |
Авторы
Даты
2017-10-09—Публикация
2015-12-24—Подача