Предлагаемое изобретение относится к медицине и может быть использовано в педиатрии, неврологии, неонатологии для определения выраженности ишемического и ишемически-геморрагического поражения головного мозга у недоношенных новорожденных (срок гестации 29-36 недель) и прогнозирования их дальнейшего неврологического развития.
Ведущее место в структуре заболеваний, приводящих к инвалидности, у детей занимают психические расстройства, болезни нервной системы и органов чувств, до 60-70% причин детской инвалидности связаны с перинатальной патологией. Согласно стратегии развития медицинской науки в Российской федерации на период до 2025 года (2012), основными мероприятиями в рамках приоритетного направления по снижению смертности и инвалидизации детей являются разработка современных высокотехнологичных методов диагностики, прогнозирования течения и исходов гипоксических поражений ЦНС для оптимизации их лечения и реабилитации. Диффузионно-взвешенная магнитно-резонансная томография (МРТ) является наиболее объективным методом для подтверждения перинатального гипоксического поражения головного мозга у новорожденных. Особенно важно раннее обнаружение патофизиологических изменений, приводящих к структурным и функциональным повреждениям головного мозга у детей, для подбора комплекса лечебных мероприятий, улучшающих прогноз неврологического развития ребенка.
Известен способ прогнозирования тяжести гипоксического поражения головного мозга у новорожденных по уровню нейроспецифических белков в сыворотке крови иммуноферментного анализа [Голосная Г.С. Нейрохимические аспекты патогенеза гипоксических поражений могза у новорожденных. М.: МЕДПРАКТИКА-М, 2009, с. 128]. Образцы крови отбирают в объеме 1,0 мл из пупочной вены при рождении ребенка, а в последующие сроки из центральных и периферических венозных катетеров. Полученную при центрифугировании сыворотку используют для определения уровня нейроспецифических белков (белка астроцитарной глии S100β, нейротрофических факторов BDNF и CNTF, васкуло-эндотелиального фактора VEGF, маркера апоптоза DK5, активности молекул клеточной адгезии ALCAM и др.). В монографии Г.С. Голосной проведен анализ показателей нейроспецифических белков у недоношенных новорожденных в зависимости от гестационного возраста в раннем и позднем неонатальном периоде, показана их прогностическая значимость в формировании гипоксического поражения головного мозга. Автор отмечает отсутствие до настоящего времени исследований, посвященных нормативным значениям нейротрофических факторов и факторов апоптоза, что является существенным недостатком. Особенно много публикаций посвящены изучению нейроспецифического белка астроцитарной глии S100β, отражающего деструктивные изменения в тканях [Акрамова Х.А. Нейроспецифический белок S100β в прогнозе нарушений раннего неонатального периода у новорожденных. Educatio. 2015, №3 (10), с. 62-64.]. В статье Х.А. Акрамовой выявлена обратная зависимость уровня белка S100β от тяжести асфиксии при рождении у недоношенных новорожденных, показана его роль в прогнозе тяжести поражения головного мозга. Одним из недостатков, затрудняющих диагностику, является повышение уровня белка S100β не только при гипоксическом поражении, но и при внутриутробном инфицировании, нейроинфекции.
За ближайший аналог принят способ, предусматривающий клиническое и нейросонографическое определение проявлений гипоксически-ишемической энцефалопатии у новорожденных различного гестационного возраста [Барашнев Ю.И. Перинатальная неврология. - Москва: издательство Триада-Х, 2011, - 672 с.]. При клиническом обследовании недоношенных новорожденных для церебральной ишемии II степени характерно возбуждение и/или угнетение центральной нервной системы (ЦНС), мышечная гипотония со снижением спонтанной двигательной активности, гипорефлексия, глазные симптомы (продолжительностью 7-21 день), судороги. По данным нейросонографии выявляются повышение сигнальных характеристик мозговой ткани (ишемия), субэпендимальные кровоизлияния - пери- и интравентрикулярные кровоизлияния (ПИВК) 1 степени. В последующем у детей диагностируются минимальные мозговые дисфункции (гиперактивность, гипоактивность, плаксивость, нарушения сна, речевые дисфункции и др.). При клиническом обследовании недоношенных новорожденных для церебральной ишемии III степени характерна прогрессирующая потеря церебральной активности свыше 10 дней (кома), судороги, дисфункция стволовых отделов мозга, декортикация, децеребрация, прогрессирующая внутричерепная гипертензия, вегетативно-висцеральные нарушения со стороны сердечно-сосудистой и дыхательной систем, желудочно-кишечного тракта, почек. По данным нейросонографии выявляются повышение сигнальных характеристик мозговой ткани (ишемия), внутричерепные кровоизлияния - ПИВК, расширение ликворных пространств, кистозная стадия перивентрикулярной лейкомаляции. В последующем диагностируются различные формы детского церебрального паралича, задержка психомоторного развития, симптоматическая эпилепсия. Способ имеет следующие недостатки: при одной и той же выраженности поражения центральной нервной системы в клинической картине (угнетение центральной нервной системы, мышечная гипотония, снижение или угнетение сухожильных и физиологических рефлексов) и на нейросонографии у новорожденных в дальнейшем могут отмечаться различные морфологические изменения; в первые недели жизни даже при выраженном гипоксическом повреждении головного мозга у ребенка структурные изменения на нейросонографии не визуализируются (отсутствуют кисты, расширение ликворных пространств). При выполнении МРТ в стандартных режимах у новорожденных возможно только предположить гипоксически-ишемическое повреждение головного мозга по повышению сигнальных характеристик на Т2-ВИ и понижению на Т1-ВИ, а уточнить распространенность и интенсивность его проявлений допустимо лишь при выполнении МРТ в режиме диффузионно-взвешенных изображений (ДВИ), позволяющему дать количественную оценку выраженности ишемии паренхимы мозга.
Задачи: повышение точности прогнозирования риска развития неврологического дефицита у недоношенных новорожденных в первые 10 дней жизни, улучшение достоверности прогноза их дальнейшего неврологического развития, своевременный подбор соответствующего тяжести поражения головного мозга комплекса лечебных мероприятий.
Сущностью изобретения является то, что у недоношенных новорожденных (срок гестации 29-36 недель) с тяжелыми проявлениями ишемического и ишемически-геморрагического поражения головного мозга при условии выявлении с помощью МРТ в режиме диффузионно-взвешенных изображений на 2-10 сутки жизни среднего значения измеряемого коэффициента диффузии (СЗИКД) белого вещества головного мозга на уровне передних и задних рогов боковых желудочков, тел боковых желудочков обоих полушарий от 1,75×10-3мм2/сек до 1,37×10-3мм2/сек и СЗИКД серого вещества коры лобных долей и чечевицеобразных ядер обоих полушарий от 1,34×10-3мм2/сек до 1,18×10-3мм2/сек прогнозируют отсутствие в дальнейшем стойкого неврологического дефицита и развитие у ребенка функциональных нарушений, что соответствует церебральной ишемии II степени, при условии выявления СЗИКД белого вещества головного мозга от 2,00×10-3мм2/сек до 1,87×10-3мм2/сек, серого вещества головного мозга от 1,47×10-3мм2/сек до 1,35×10-3мм2/сек у новорожденных со сроком гестации 29-33 недели и СЗИКД белого вещества головного мозга от 1,24×10-3мм2/сек до 1,05×10-3мм2/сек, серого вещества головного мозга от 1,06×10-3мм2/сек до 0,93×10-3мм2/сек у новорожденных со сроком гестации 34-36 недель прогнозируют развитие стойкого неврологического дефицита, что соответствует церебральной ишемии III степени.
Технический результат: выполняют МРТ головного мозга в режиме ДВИ (томограф Panorama HFO-Philips, мощностью 1,0 Тесла, FOV - 230×181×131 мм, толщина среза 5 мм, b-фактор от 2 до 5, max b-фактор 800-1000), строят параметрические диффузионные карты для количественной оценки диффузионных свойств воды в ткани. Затем измеряют ИКД, характеризующий уровень перинатальной церебральной ишемии. Способ при использовании позволяет более точно определить выраженность ишемического повреждения мозговой ткани у недоношенных новорожденных и в зависимости от результатов подобрать более адекватную тактику лечения.
Предложенный способ апробирован на базе Детской краевой клинической больницы и краевого перинатального центра г. Краснодара совместно с кафедрой педиатрии с курсом неонатологии ФПК и ППС ГБОУ ВПО Кубанского государственного медицинского университета в 2011-2014 г.г. Исследование проведено у 57 недоношенных новорожденных (срок гестации 29-36 недель) с тяжелыми проявлениями гипоксического поражения головного мозга. Критериями исключения из исследования являлись: 1) со стороны новорожденных - врожденные пороки развития, хромосомные болезни, наследственные ферментопатии, эндокринные заболевания, гемолитическая болезнь новорожденных, токсические и дисметаболические энцефалопатии, респираторный дистресс-синдром, токсико-септические состояния, поражения ЦНС при инфекционных заболеваниях перинатального периода; 2) со стороны матерей - хронические заболевания в стадии декомпенсации, врожденные пороки развития, злокачественные новообразования.
Способ осуществляют следующим образом: проводят клинико-неврологическое обследование новорожденного с проявлениями гипоксического поражения головного мозга, затем в течение первых суток жизни ребенка выполняют нейросонографию для определения структурной патологии (внутричерепные кровоизлияния, изменение эхогенности мозговой ткани, аномалии развития головного мозга) и у детей с тяжелыми проявлениями ишемического и ишемически-геморрагического поражения головного мозга с помощью МРТ на 2-10 сутки жизни проводят количественную оценку выраженности ишемического повреждения и уточняют выявленную по данным нейросонографии структурную патологию. В режиме диффузионно-взвешенных изображений строят параметрические диффузионные карты, затем в аксиальной плоскости производят измерения ИКД белого вещества головного мозга на уровне передних и задних рогов боковых желудочков, тел боковых желудочков обоих полушарий головного мозга. Измерения ИКД серого вещества производят в чечевицеобразных ядрах и в коре лобных долей обоих полушарий. Суммируя результаты измерения ИКД на уровне передних и задних рогов боковых желудочков, тел боковых желудочков обоих полушарий и разделив на число зон измерения, определяют СЗИКД белого вещества. Суммируя результаты измерения ИКД в чечевицеобразных ядрах и в коре лобных долей обоих полушарий и разделив на число зон измерения, определяют СЗИКД серого вещества исследуемых зон головного мозга. По величине ИКД (таблица №1) прогнозируют дальнейшее неврологическое развитие ребенка, отсутствие или формирование у него неврологического дефицита.
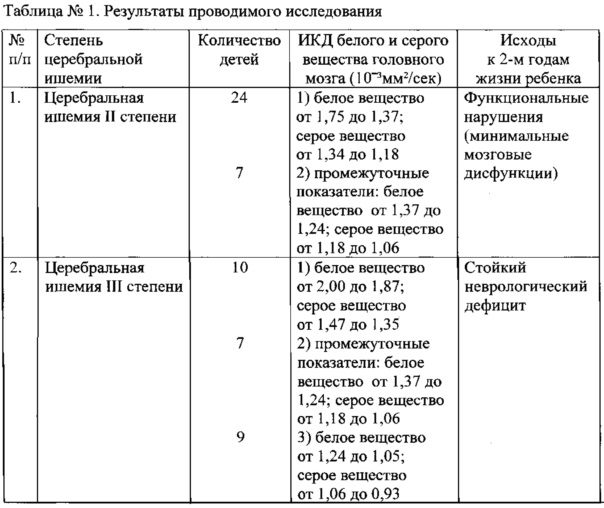
Проводимое исследование позволило выявить детей, составивших группу риска по развитию ДЦП и имеющих промежуточные показатели ИКД белого вещества от 1,37×10-3мм2/сек до 1,24×10-3мм2/сек, серого вещества от 1,18×10-3мм2/сек до 1,06×10-3мм2/сек. Из 14 новорожденных этой группы 7 детей в результате поэтапно проведенной нейрореабилитации имели только функциональные нарушения в возрасте 2-х лет, у 7 детей сформировался стойкий неврологический дефицит.
Анестезиологическое пособие осуществляют с использованием севорана для ингаляционного наркоза с сохранением адекватного дыхания и сердечной деятельности у детей в течение исследования. Безопасность исследования обеспечивают мониторированием частоты сердечных сокращений, частоты дыхания, артериального давления, сатурации.
Примеры применения способа
Пример 1. Ребенок С. родился 27.09.12 г.от III беременности (I беременность - роды срочные 3100 г, II беременность - мед. аборт), протекавшей на фоне угрозы прерывания в 9 недель, дрожжевого кольпита, ОРВИ в 11 недель. Профилактика РДС проведена. Матери 27 лет, роды II преждевременные на 30 неделе, обвитие пуповины вокруг шеи. Вес при рождении - 1600 г, рост - 40 см. Оценка по шкале Апгар 6-7 баллов. Реанимационные мероприятия в родильном зале: санация верхних дыхательных путей (ВДП), лучистое тепло, продленный вдох, NCPAP. Ребенок переведен в реанимационное отделение (РО). Отмечалась вялость, снижение мышечного тонуса, двигательной активности, реакции на внешние раздражители, генерализованные тонико-клонические пароксизмы (купированы введением противосудорожных препаратов). На 8-е сутки переведен в отделение патологии новорожденных (ОПН). Нейросонография от 27.09.12 г. - повышение эхогенности перивентрикулярных областей, киста правого сосудистого сплетения. При выполнении МРТ 05.10.12 г. в стандартных режимах выявлены киста правого сосудистого сплетения, незавершенные процессы миелинизации. В режиме ДВИ определены значения ИКД белого вещества головного мозга: у передних рогов боковых желудочков правого полушария (R) - 1,74×10-3мм2/сек, левого полушария (L) - 1,69×10-3мм2/сек, у задних рогов боковых желудочков R - 1,71×10-3мм2/сек, L - 1,66×10-3мм2/сек, на уровне тел боковых желудочков R - 1,62×10-3мм2/сек, L - 1,65×10-3мм2/сек. ИКД серого вещества головного мозга: кора лобной доли R - 1,33×10-3мм2/сек, L - 1,30×10-3мм2/сек, чечевицеобразные ядра R - 1,25×10-3мм2/сек, L - 1,27×10-3мм2/сек. СЗИКД белого вещества: (1,74+1,69+1,71+1,66+1,62+1,65):6=1,68×10-3мм2/сек. СЗИКД серого вещества: (1,33+1,30+1,25+1,27):4=1,29×10-3мм2/сек. Церебральная ишемия II ст. На 35-е сутки выписан домой в удовлетворительном состоянии. Проведены курсы ноотропных, сосудистых, ФТЛ, массажа 1 раз в 2-3 месяца. При осмотре ребенка в корригированном возрасте 12-ти месяцев, 1,5 и 2 лет моторное развитие соответствует возрасту, выявлены проявления минимальной мозговой дисфункции (ММД), синдром гиперактивности с дефицитом внимания.
Пример 2. Ребенок К. родился 02.12.13 г. от III беременности (I беременность - роды преждевременные на 35 неделе, II беременность - внематочная беременность), протекавшей на фоне токсикоза первой половины. Профилактика РДС проведена. Матери 32 года, роды III преждевременные на 34 неделе, отслойка плаценты, Кесарево сечение. Вес при рождении - 2190 г, рост - 45 см. Оценка по шкале Апгар 5-6 баллов. Реанимационные мероприятия в родильном зале: санация ВДП, искусственная вентиляция легких (ИВЛ) мешком Амбу. По тяжести состояния ребенок переведен в РО. Аппаратная ИВЛ 02.12.13-07.12.13 г. Судорожный синдром купирован, наросла двигательная активность. На 11-е сутки ребенок переведен ОПН. Нейросонография от 02.12.13 г. - повышение эхогенности перивентрикулярных областей, дилатация правого бокового желудочка до 9 мм, правостороннее ПИВК 1 степени. При выполнении МРТ 09.12.13 г. определяется дилатация правого бокового желудочка до 9 мм, правостороннее ПИВК 1 степени, незавершенные процессы миелинизации. В режиме ДВИ определены значения ИКД белого вещества головного мозга: у передних рогов боковых желудочков R - 1,44 × 10-3 мм2/сек, L - 1,39 × 10-3 мм2/сек, у задних рогов боковых желудочков R - 1,37 × 10-3 мм2/сек, L - 1,41 × 10-3 мм2/сек, на уровне тел боковых желудочков R - 1,35 × 10-3 мм2/сек, L - 1,30 × 10-3 мм2/сек. ИКД серого вещества головного мозга: кора лобной доли R - 1,25 × 10-3 мм2/сек, L - 1,21 × 10-3 мм2/сек, чечевицеобразные ядра R - 1,18 × 10-3 мм2/сек, L - 1,16 × 10-3 мм2/сек. СЗИКД белого вещества: (1,44+1,39+1,37+1,41+1,35+1,30):6=1,38×10-3 мм2/сек. СЗИКД серого вещества: (1,25+1,21+1,18+1,16):4=1,20×10-3 мм2/сек. Церебральная ишемия II степени. На 29-е сутки ребенок в удовлетворительном состоянии выписан домой. Проведены курсы ноотропных, нейрометаболиков, ФТЛ, массажа 1 раз в 2-3 месяца. При осмотре ребенка в корригированном возрасте 12-ти месяцев, 1,5 и 2 лет моторное развитие соответствует возрасту. Диагноз: ММД, невротические реакции, задержка речевого развития.
Пример 3. Ребенок 3. родился 09.11.13 г. от IV беременности (I беременность - срочные роды 3200 г, II-III беременность - мед. аборт), протекавшей на фоне угрозы прерывания - прием дюфастона с 5 по 20 неделю, хронической фетоплацентарной недостаточности (стационарное лечение). Профилактика РДС проведена. Матери 30 лет, роды IV преждевременные на 30 неделе. Вес при рождении - 1600 г, рост - 40 см. Оценка по шкале Апгар 4-6 баллов. Реанимационные мероприятия в родильном зале: санация ВДП, ИВЛ мешком Амбу. По тяжести состояния для дальнейшего лечения и выхаживания ребенок переведен в РО. В неврологическом статусе угнетение ЦНС, судорожный синдром. Аппаратная ИВЛ 09.11.13-14.11.13 г. На 14-е сутки переведен в ОПН. Нейросонография от 09.11.13 - перивентрикулярная ишемия, двустороннее ПИВК 2 степени. При выполнении МРТ 14.11.13 г. в стандартных режимах: наружные ликворные пространства, межполушарная щель умеренно расширены, широкие межгирусные пространства, двустороннее ПИВК 2 степени. В режиме ДВИ визуализируется значительное понижение сигнальных характеристик от серого и белого вещества больших полушарий в результате воздействия внутриутробной гипоксии-ишемии. Определены значения ИКД белого вещества головного мозга: у передних рогов боковых желудочков R - 2,00 × 10-3 мм2/сек, L - 2,06 × 10-3 мм2/сек, у задних рогов боковых желудочков R - 2,05 × 10-3 мм2/сек, L - 1,98 × 10-3 мм2/сек, на уровне тел боковых желудочков R - 1,95 × 10-3 мм2/сек, L - 1,94 × 10-3 мм2/сек. ИКД серого вещества головного мозга: кора лобной доли R - 1,49 × 10-3 мм2/сек, L - 1,47 × 10-3 мм2/сек, чечевицеобразные ядра R - 1,45 × 10-3 мм2/сек, L - 1,46 × 10-3 мм2/сек. СЗИКД белого вещества: (2,00+2,06+2,05+1,98+1,95+1,94):6=2,00×10-3 мм2/сек. СЗИКД серого вещества: (1,49+1,47+1,45+1,46):4=1,47×10-3 мм2/сек. Церебральная ишемия III степени. На 35-е сутки ребенок выписан домой. На первом году жизни трижды получал лечение в условиях стационара по поводу микроаспирационного синдрома вследствие псевдобульбарных нарушений, проводились курсы ноотропных, сосудистых, коррекция дозы антиконвульсантов. Осмотрен в корригированном возрасте 12-ти месяцев, 1,5 и 2 лет, диагноз: ДЦП, спастический тетрапарез, грубая задержка психоречевого развития. Симптоматическая эпилепсия.
Пример 4. Ребенок Я. родился 03.04.13 г. от III беременности (I беременность - срочные роды 3000 г, II беременность - срочные роды 2800 г), протекавшей на фоне хронической фетоплацентарной недостаточности, угрозы прерывания в 11, 14 и 26 недель (стационарное лечение), гестоз тяжелой степени. Профилактика РДС проведена. Матери 36 лет, роды III, преждевременные на 31 неделе. Вес при рождении - 1690 г, рост - 42 см. Оценка по шкале Апгар 3-5 баллов. Реанимационные мероприятия в родильном зале: санация ВДП, ИВЛ мешком Амбу. В неврологическом статусе проявления церебральной депрессии, генерализованные тонико-клонические пароксизмы. По тяжести состояния для дальнейшего лечения и выхаживания ребенок переведен в РО. Аппаратная ИВЛ 03.04.13-18.04.13 г. На 20-е сутки переведен в ОПН. Нейросонография от 03.04.13 - перивентрикулярная ишемия, дилатация боковых желудочков до 13 мм, субэпендимальная киста слева. При выполнении МРТ 10.04.13 г. в стандартных режимах: наружные ликворные пространства, межполушарная щель умеренно расширены, широкие межгирусные пространства, дилатация боковых желудочков, субэпендимальная киста слева. В режиме ДВИ визуализируется значительное понижение сигнальных характеристик от серого и белого вещества больших полушарий в результате воздействия внутриутробной гипоксии-ишемии. Определены значения ИКД белого вещества головного мозга: у передних рогов боковых желудочков R - 1,96 × 10-3 мм2/сек, L - 1,89 × 10-3 мм2/сек, у задних рогов боковых желудочков R - 1,90 × 10-3 мм2/сек, L - 1,94 × 10-3 мм2/сек, на уровне тел боковых желудочков R - 1,87 × 10-3 мм2/сек, L - 1,84 × 10-3 мм2/сек. ИКД серого вещества головного мозга: кора лобной доли R - 1,35 × 10-3 мм2/сек, L - 1,39 × 10-3 мм2/сек, чечевицеобразные ядра R - 1,42×10-3мм2/сек, L - 1,47×10-3мм2/сек. СЗИКД белого вещества: (1,96+1,89+1,90+1,94+1,87+1,84):6=1,90×10-3мм2/сек. СЗИКД серого вещества: (1,35+1,39+1,42+1,47):4=1,41×10-3м2/сек. Церебральная ишемия III степени. Ребенок переведен на 30-е сутки жизни в педиатрическое отделение для дальнейшего лечения по поводу микроаспирационного синдрома вследствие псевдобульбарных нарушений, подбора антиконвульсантов. До года каждые 2-3 месяца получал лечение в условиях стационара (ноотропные, сосудистые, коррекция дозы антиконвульсантов). Осмотрен в корригированном возрасте 12-ти месяцев, 1,5 и 2 лет, диагноз: ДЦП, спастический тетрапарез, грубая задержка психоречевого развития. Симптоматическая эпилепсия.
Пример 5. Ребенок М. родился 24.08.12 г.от I беременности, протекавшей на фоне ОРВИ в 15 недель. Матери 24 года, роды I преждевременные на 35 неделе, отслойка плаценты, критическое состояние плода, Кесарево сечение. Вес при рождении - 2390 г, рост - 46 см. Оценка по шкале Апгар 3-4 балла. Реанимационные мероприятия в родильном зале: санация ВДП, ИВЛ мешком Амбу. По тяжести состояния для дальнейшего лечения и выхаживания ребенок переведен в РО. Аппаратная ИВЛ 24.08.12 - 05.09.12 г. В неврологическом статусе выраженное угнетение ЦНС с развитием мозговой комы, судорожного синдрома. На 24-ые сутки переведен в ОПН. Нейросонография от 24.08.12-диффузное гипоксически-ишемическое поражение головного мозга, левостороннее ПИВК 2 степени. При выполнении МРТ 30.08.12 г. на ДВИ определяются зоны повышения сигнальных характеристик от серого и белого вещества больших полушарий, левостороннее ПИВК 2 степени. В режиме ДВИ определены значения ИКД белого вещества головного мозга: у передних рогов боковых желудочков R - 1,19×10-3мм2/сек, L - 1,2510-3мм2/сек, у задних рогов боковых желудочков R - 1,23×10-3мм2/сек, L - 1,20×10-3мм2/сек, на уровне тел боковых желудочков R - 1,14×10-3мм2/сек, L - 1,18×10-3мм2/сек. ИКД серого вещества головного мозга: кора лобной доли R - 1,00×10-3мм2/сек, L - 1,03×10-3мм2/сек, чечевицеобразные ядра R - 0,99×10-3мм2/сек, L - 1,01×10-3мм2/сек. СЗИКД белого вещества: (1,19+1,25+1,23+1,20+1,14+1,18):6=1,20×10-3мм2/сек. СЗИКД серого вещества: (1,00+1,03+0,99+1,01):4 =1,01×10-3мм2/сек. Церебральная ишемия III степени. На 30-ые сутки ребенок переведен в педиатрическое отделение для дальнейшего лечения по поводу микроаспирационного синдрома, подбора антиконвульсантов. Осмотрен в возрасте 12-ти месяцев, 1,5 и 2 лет, диагноз: ДЦП, атонически-астатическая форма, грубая задержка психоречевого развития. Симптоматическая эпилепсия.
Использование способа позволило на ранних этапах выявить у новорожденных показатели ИКД, соответствующие церебральной ишемии III степени, своевременно провести комплекс лечебных мероприятий и уменьшить дальнейший неврологический дефицит. У детей улучшились показатели мышечного тонуса и рефлекторной активности, уменьшились проявления спастичности. Улучшение дальнейшего неврологического развития способствовало повышению качества жизни ребенка.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ прогнозирования риска развития морфологических изменений головного мозга у доношенных новорожденных с перинатальным гипоксически-ишемическим поражением нервной системы | 2020 |
|
RU2737490C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ НЕВРОЛОГИЧЕСКОГО ДЕФИЦИТА У ДОНОШЕННЫХ НОВОРОЖДЕННЫХ С ГИПОКСИЧЕСКИ-ИШЕМИЧЕСКИМ ПОРАЖЕНИЕМ ГОЛОВНОГО МОЗГА | 2014 |
|
RU2565095C1 |
| Способ раннего прогнозирования риска развития двигательных нарушений у недоношенных новорожденных, рожденных с низкой и экстремально низкой массой тела, с перинатальными гипоксически-ишемическими поражениями головного мозга | 2017 |
|
RU2692670C2 |
| Способ прогнозирования возникновения неонатальных судорог у новорожденных из группы высокого перинатального риска | 2019 |
|
RU2722022C1 |
| Способ прогнозирования возникновения ДЦП у детей первых 3-х месяцев жизни с перинатальным поражением ЦНС | 2018 |
|
RU2710218C1 |
| Способ прогнозирования риска развития неврологического дефицита у глубоко недоношенных детей с экстремально и очень низкой массой тела и с функционирующим артериальным протоком | 2024 |
|
RU2835480C1 |
| СПОСОБ ОЦЕНКИ ТЯЖЕСТИ ДЕТСКОГО ЦЕРЕБРАЛЬНОГО ПАРАЛИЧА (ДЦП) И ЗАДЕРЖЕК В ПСИХОРЕЧЕВОМ РАЗВИТИИ (ЗПРР) | 2014 |
|
RU2561290C1 |
| Способ прогнозирования неврологических нарушений у новорожденных с задержкой внутриутробного развития плода | 2016 |
|
RU2629395C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ФОРМИРОВАНИЯ ОККЛЮЗИОННОЙ ПОСТГЕМОРРАГИЧЕСКОЙ ГИДРОЦЕФАЛИИ У НЕДОНОШЕННЫХ ДЕТЕЙ С ЭКСТРЕМАЛЬНО НИЗКОЙ МАССОЙ ТЕЛА ПРИ РОЖДЕНИИ | 2014 |
|
RU2554781C1 |
| Способ антенатального прогнозирования гипоксически-ишемических церебральных нарушений у доношенных новорожденных | 2023 |
|
RU2829429C1 |
Изобретение относится к медицине, педиатрии, неврологии, неонатологии, методам определения выраженности ишемического и ишемически-геморрагического поражения головного мозга у недоношенных новорожденных (срок гестации 29-36 недель), прогнозирования дальнейшего неврологического развития. При выявлении с помощью МРТ в режиме диффузионно-взвешенных изображений на 2-10 сут жизни среднего значения измеряемого коэффициента диффузии (СЗИКД) белого вещества головного мозга на уровне передних и задних рогов боковых желудочков, тел боковых желудочков обоих полушарий от 1,75×10-3 мм2/сек до 1,37×10-3 мм2/сек и СЗИКД серого вещества коры лобных долей и чечевицеобразных ядер обоих полушарий от 1,34×10-3 мм2/сек до 1,18×10-3 мм2/сек прогнозируют отсутствие в дальнейшем стойкого неврологического дефицита и развитие у ребенка функциональных нарушений, что соответствует церебральной ишемии (ЦИ) II степени. При условии выявления СЗИКД белого вещества головного мозга от 2,00×10-3 мм2/сек до 1,87×10-3 мм2/сек, серого вещества головного мозга от 1,47×10-3 мм2/сек до 1,35×10-3 мм2/сек у новорожденных со сроком гестации 29-33 недели и СЗИКД белого вещества головного мозга от 1,24×10-3 мм2/сек до 1,05×10-3 мм2/сек, серого вещества головного мозга от 1,06×10-3 мм2/сек до 0,93×10-3 мм2/сек у новорожденных со сроком гестации 34-36 недель прогнозируют развитие стойкого неврологического дефицита, что соответствует ЦИ III степени. Способ обеспечивает точность, достоверность прогнозирования упомянутого риска и в зависимости от результатов возможность подобрать более адекватную тактику лечения. 5 пр., 1 табл.
Способ прогнозирования риска развития неврологического дефицита у недоношенных новорожденных с гипоксическим поражением головного мозга, отличающийся тем, что при условии выявления с помощью МРТ в режиме диффузионно-взвешенных изображений на 2-10 сутки жизни среднего значения измеряемого коэффициента диффузии (СЗИКД) белого вещества головного мозга на уровне передних и задних рогов боковых желудочков, тел боковых желудочков обоих полушарий от 1,75×10-3 мм2/сек до 1,37×10-3 мм2/сек и СЗИКД серого вещества коры лобных долей и чечевицеобразных ядер обоих полушарий от 1,34×10-3 мм2/сек до 1,18×10-3 мм2/сек прогнозируют отсутствие в дальнейшем стойкого неврологического дефицита и развитие у ребенка функциональных нарушений, что соответствует церебральной ишемии II степени, при условии выявления СЗИКД белого вещества головного мозга от 2,00×10-3 мм2/сек до 1,87×10-3 мм2/сек, серого вещества головного мозга от 1,47×10-3 мм2/сек до 1,35×10-3 мм2/сек у новорожденных со сроком гестации 29-33 недели и СЗИКД белого вещества головного мозга от 1,24×10-3 мм2/сек до 1,05×10-3 мм2/сек, серого вещества головного мозга от 1,06×10-3 мм2/сек до 0,93×10-3 мм2/сек у новорожденных со сроком гестации 34-36 недель прогнозируют развитие стойкого неврологического дефицита, что соответствует церебральной ишемии III степени.
| АКСЕНОВ Д.Б | |||
| Факторы риска развития и прогнозирования неврологической патологии у недоношенных детей с перивентрикулярными кровоизлияниями, дисс.к.м.н., М., 2005 | |||
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ НЕВРОЛОГИЧЕСКОГО ДЕФИЦИТА У ДОНОШЕННЫХ НОВОРОЖДЕННЫХ С ГИПОКСИЧЕСКИ-ИШЕМИЧЕСКИМ ПОРАЖЕНИЕМ ГОЛОВНОГО МОЗГА | 2014 |
|
RU2565095C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ЗАБОЛЕВАНИЙ В ОБЛАСТИ ГИППОКАМПОВ | 2014 |
|
RU2591543C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ВОССТАНОВЛЕНИЯ ДВИГАТЕЛЬНОЙ ФУНКЦИИ У БОЛЬНЫХ В ОСТРОМ ПЕРИОДЕ ИШЕМИЧЕСКОГО ИНСУЛЬТА В БАССЕЙНЕ АРТЕРИЙ КАРОТИДНОЙ СИСТЕМЫ | 2012 |
|
RU2508048C1 |
| US 20110218253 A1, 08.09.2011 | |||
| БЕЛОУСОВА Т.В | |||
| и др | |||
| Перинатальные поражения центральной нервной системы у новорожденных, метод.рек., СПб, 2010, 92 с | |||
| KOSTOVIC I.et al | |||
| Developmental dynamics of radial vulnerability in the cerebral compartments in preterm infants and neonates// Front Neurol | |||
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| RENNIE J.M | |||
| et al | |||
| Advanced magnetic resonance techniques provide more accurate prognostic information than conventional imaging// Dev Med Child Neurol | |||
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
| HARTEMAN J.C | |||
| et al | |||
| Diffusion-weighted imaging changes in cerebral watershed distribution following neonatal encephalopathy are not invariably associated with an adverse outcome// Dev Med Child Neurol | |||
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
Авторы
Даты
2017-11-13—Публикация
2016-08-03—Подача