Изобретение относится к химико-фармацевтической промышленности, медицине, ветеринарии, фармакологии и касается получения мягких лекарственных форм для наружного применения топического действия в виде мазей на гидрофобной основе для лечения ран и ожогов, обладающих антиоксидантной, противовоспалительной, противомикробной и ранозаживляющей активностями.
В качестве действующих фармакологически активных веществ используются продукты комплексной переработки биомассы лиственницы: дигидрокверцетин (ФС 42-3854-99) и лиственничный воск коры (ТУ ОП 9154-004-03533719-2001), а также цинксодержащее производное флавоноида дигидрокверцетина, представляющее собой металлокомплексное соединение дигидрокверцетина, с количественным содержанием ионов цинка 8,8-9,2% [Патент РФ №2553428, 2015 г.].
Дигидрокверцетин - основной компонент флавоноидной фракции из древесины лиственницы, обладающий высокой антиоксидантной, капилляропротекторной, противовоспалительной, гастро-, гепато- и радиопротекторной, гиполипидемической, диуретической и мембранотропной активностями [Биомасса лиственницы: от химического состава до инновационных продуктов / В.А. Бабкин, Л.А. Остроухова, Н.Н. Трофимова; отв. ред. А.А. Семенов; Рос. акад. наук, Сиб. Отд-ние, Иркутский ин-т химии им. А.Е. Фаворского. - Новосибирск: Изд-во СО РАН, 2011. - 236 с.].
Лиственничный воск представляет собой неполярную липидную фракцию из коры лиственницы с температурой плавления 38-44°С, обладающую фармакологической активностью [Бабкин В.А., Иванова Н.В., Остроухова Л.А., Малков Ю.А., Иванова С.З., Попова О.В. Экстракционная переработка коры лиственницы в практически полезные продукты) // Хвойные бореальной зоны. - 2003. - №1. - С. 113-116].
Цинксодержащее производное флавоноида дигидрокверцетина обладает антиоксидантной активностью, превосходящей таковую исходного дигидрокверцетина [Столповская Е.В., Трофимова Н.Н., Бабкин В.А., Костыро Я.А. Биологическая активность комплексов дигидрокверцетина с ионами двухвалентных металлов // V Всеросс. научн. конф. "Новые достижения в химии и химической технологии растительного сырья" / АТУ: материалы. - Барнаул, 2012. - С. 273; Stolpovskaya E.V., Trofimova N.N., Babkin V.A. Research and development of new derivatives based on products of larch wood processing for use in medicine // Traditional medicine: ways of integration with modern healthcare: proceedings of the VI international scientific conference. Ulan-Ude, 2013. P. 51].
Различные виды ран, в том числе и ожоговые, особенно инфицированные, характеризуются развитием окислительного стресса соответствующих тканей, сопровождающегося изменением состава мембран клеток, нарушением их функциональных свойств и активности мембраносвязанных ферментов. Поэтому использование препаратов, обладающих мембранопротекторной и высокой антиоксидантной активностью, является эффективным при лечении данной патологии.
Известно средство для лечения ожогов и ран на основе водного экстракта лиственницы сибирской, получаемого биорезонансным методом [Патент РФ №2470653, 2012]. Данное средство представляет собой комплексный фитопрепарат, в состав которого входят дигидрокверцетин (0,002%), полисахариды, полифенольные соединения, терпеновые сапонины, флавоноиды и эфирные масла. Это средство позиционируется как инъекционная лекарственная форма для внутримышечного применения, хотя в качестве примеров лечения приведено только местное наружное использование в виде внутрираневых впрыскиваний и тампонирований. Недостатками вышеописанного препарата являются:
1. Необходимость соблюдения требований стерильности, что требует дополнительных условий производства, хранения и применения.
2. Ограничение по использованию у потенциальных больных в амбулаторных или домашних условиях в виду отсутствия у последних навыков внутриполостных введений лекарственных препаратов.
Известно еще одно средство для наружного применения в виде гель-бальзама, обладающего широким спектром действия (ранозаживляющая, противовоспалительная, противоотечная активности) [Патент РФ №2381810, 2010]. Оно содержит в своем составе дигидрокверцетин (до 5%), глицерин, льняное или кедровое масло и водный хитозановый гель (80-96%), в рецептуру которого входят препарат наночастиц серебра "Аргоника" (1%), 40 г уксусной кислоты (в пересчете на концентрированную) и 100 г хитозана.
Недостатком гель-бальзама является то, что это средство представляет собой эмульсию по типу масло в воде, которая требует особых условий производства и хранения, при не соблюдении которых возможно ее разрушение, приводящее к потере товарного вида и фармакологической активности.
Наиболее близким аналогом является известный способ лечения термических ожогов с использованием мази, содержащей 3% дигидрокверцетина [Патент РФ №2405536, 2010 г.]. При этом дигидрокверцетин выполняет функцию связующего компонента, стабилизатора, консерванта и действующего начала в процессе заживления ожоговой раны. Недостатком данного способа является то, что в качестве мазевой основы использован нутряной свиной жир, который, как известно, под влиянием кислорода воздуха, света и влаги прогоркает, приобретает кислую реакцию, неприятный запах и раздражающее действие на кожу. К тому же он несовместим с полифенолами [Марченко, Л.Г. Технология мягких лекарственных форм: учеб. пособие / Л.Г. Марченко, А.В. Русак, И.Е. Смехова. - СПб.: Спец. лит., 2004]. Вероятно, описанная в данном источнике рецептура мази готовилась ex tempore, так как никакие подтверждающие данные о ее стабильности в процессе хранения не приводятся. А ведь дигидрокверцетин является растительным полифенолом, который в кислой среде подвергается окислению и требует особых условий хранения.
Поэтому целью данного изобретения является разработка высокоэффективных и удобных в производстве и применении оригинальных фармацевтических композиций в виде мягких лекарственных форм для наружного применения топического действия для лечения различных видов ран, включая инфицированные и ожоговые, обладающих антиоксидантной, противовоспалительной, противомикробной и ранозаживляющей активностями.
Технический результат достигается тем, что средство для лечения ран и ожогов содержит такие действующие фармакологически активные вещества, как дигидрокверцетин или его цинксодержащее металлокомплексное соединение общей формулы ML2(H2O)2, где М - ион цинка, a L - лиганд, представляющий собой депротонированный дигидрокверцетин с количественным содержанием ионов цинка 8,8-9,2% [Трофимова Н.Н., Бабкин В.А., Столповская Е.В. "Способ получения моно- и билигандных комплексов соединений ионов двухвалентных металлов - цинка, меди (II) и кальция с дигидроквецетином, обладающих усиленной антиоксидантной активностью"; Патент РФ №2553428, 2015 г.], [Трофимова Н.Н., Бабкин В.А., Вакульская Т.И., Чупарина Е.В. "Исследование методов синтеза, строения и свойств комплексов флавоноидов с ионами металлов. 1. Синтез и установление строения комплексов и солей дигидрокверцетина с цинком, медью (II) и кальцием в водных растворах" // Химия растительного сырья. - 2012. - №2. - С. 51-62], а также гидрофобную мазевую основу с лиственничным воском.
В качестве основного структурообразователя используется гидрофобная мазевая основа с лиственничным воском следующего состава (мас. %):
которая описана в патенте [Костыро Я.А. и др. Патент 2582984, 2016]. Использование дигидрокверцетина или его цинковой соли совместно с воскообразующей основой для получения нового средства для лечения ран и ожогов способствует получению гомогенной мази (дигидрокверцетин и его цинксодержащее производное обладают гидрофобными свойствами), что обеспечивает высокую биодоступность и эффективность лекарственной формы.
Дигидрокверцетин или его цинксодержащее металлокомплексное производное с количественным содержанием ионов цинка 8,8-9,2% добавляют к основе в количестве от 1 до 10%, поэтому в пересчете на общее процентное содержание количество лиственничного воска в заявляемом средстве составляет 4,5-58,5%, вазелинового или касторового масла - 9,0-81,0%, диметилсульфоксида - 1,0-10,0%, аэросила - 0,01-9,0%.
Таким образом, для достижения технического результата предлагается средство для лечения ран и ожогов, которое содержит дигидрокверцетин или его цинксодержащее соединение, а также гидрофобную основу с лиственничным воском при следующем соотношении компонентов, в мас. %:
Причем гидрофобная основа имеет следующий состав: лиственничный воск 4,5-58,5%, вазелиновое или касторовое масло - 9,0-81,0%, диметилсульфоксид - 1,0-10,0%, аэросил - 0,01-9,0%.
Изучение фармакологической активности фармацевтических композиций на гидрофобной основе с лиственничным воском, содержащих дигидрокверцетин или его цинксодержащее металлокомплексное соединение с количественным содержанием ионов цинка 8,8-9,2%, проводили на модели ожоговой раны [Парамонов Б.А., Чеботарев В.Ю. Методы моделирования термических ожогов кожи при разработке препаратов для местного лечения // Бюл. эксп. биол. и мед. - 2002. - №11. - С. 593-597].
Для этого под кетамин-дроперидол-атропиновым наркозом у крыс линии Wistar весом 220-250 г в области спины воспроизводили термический ожог (на депилированную поверхность воздействовали галогеновой лампой мощностью 300 W на расстоянии 1 см в течение 10 с).
Эксперименты выполнялись в соответствии с нормами гуманного обращения с животными, которые регламентированы «Правилами проведения работ с использованием экспериментальных животных» (Приложение к приказу Министерства здравоохранения СССР от 12.08.1977 г. №755) согласно протоколу, одобренному Комитетом по биомедицинской этике НЦРВХ СО РАМН.
Животным опытных групп сразу после манипуляции и затем на протяжении всего эксперимента наносили исследуемые мази, а крысы контрольной группы оставались без лечения. Выведение животных из эксперимента осуществляли в сроки: 3, 7 и 14 суток.
Для гистологической оценки фармакологической активности фрагменты ожоговой раны фиксировали раствором FineFix. Полученный материал заливали в парафин, готовили срезы толщиной 5 мкм, которые окрашивали по методу Ван-Гизона [Меркулов Г.А. Курс патологогистологической техники - Л.: Медицина, 1969. - 422 с.]. Следующие примеры иллюстрируют изобретение.
Пример 1.
90 г гидрофобной основы с лиственничным воском расплавляли в фарфоровой чашке на водяной бане при температуре не выше 40°С, в расплаве растворяли при перемешивании 10 г дигидрокверцетина. Полученный расплав охлаждали. Гомогенизацию продукта осуществляли до получения однородной по консистенции мази желтого цвета.
Пример 2.
95 г гидрофобной основы с лиственничным воском расплавляли в фарфоровой чашке на водяной бане при температуре не выше 40°С, в расплаве растворяли при перемешивании 5 г цинксодержащего производного дигидрокверцетина. Полученный расплав охлаждали. Гомогенизацию продукта осуществляли до получения однородной по консистенции мази желтого цвета.
Пример 3.
Ранозаживляющая активность
Ранозаживляющую активность исследуемых фармацевтических композиций оценивали планиметрически по методу А.В. Черкасова [Патент СССР (SU) №1675657, 1991]. Результаты эксперимента представлены на рисунке 1.
Так, к 3 суткам эксперимента площадь ожога уменьшилась в 1,7-2 раза во всех группах животных по сравнению с исходным значением (4 см).
На 7 сутки эксперимента данный показатель у группы животных, подвергшихся обработке мазью с цинксодержащим производным дигидрокверцетина на гидрофобной основе с лиственничным воском, оказался существенно меньшим (на 41,4%) по сравнению с контролем, в то время как в группе животных, подвергшихся обработке мазью с дигидрокверцетином на гидрофобной основе с лиственничным воском, площадь ожога была меньше аналогичного показателя в группе контроля всего на 26,0%. К исходу эксперимента (14 сутки) в опытных группах, наблюдалось практически полное заживление термического ожога (сохранялось от 0,5 до 4,0% от исходной площади ожога против 22,3% в группе контроля).
Оценка динамики процессов эпителизации раневого дефекта, состоящих в образовании эпителия в месте повреждения кожи, является важной характеристикой скорости регенерации.
Установлено, что при применении исследуемых фармацевтических композиций достигнута полная эпителизация ожоговой раны к 14 суткам эксперимента (рисунки 2Б и 2В) в опытных группах. В то же время эпителизации в группе контроля (рисунок 2А) не происходит к 14 суткам эксперимента. На гистологических срезах наблюдается созревание грануляционной ткани в ожоговой ране без эпителизации.
Таким образом, в результате проведенных исследований выявлена выраженная ранозаживляющая активность исследуемых фармацевтических композиций, проявляющаяся в ранней эпителизации ожоговой раны по сравнению с контрольной группой животных. При этом мазь с цинксодержащим производным дигидрокверцетина на гидрофобной основе с лиственничным воском существенно по сравнению с мазью с исходным дигидрокверцетином способствует заживлению эпителизацией в 100% случаев.
Пример 4.
Противовоспалительная активность
При оценке противовоспалительной активности исследуемых фармацевтических композиций было показано, что в контрольной группе животных процесс заживления ожоговой раны морфологически соответствует канонам развития воспалительного ответа, при этом даже на 3 сутки сохраняется пик выраженности инфильтрации нейтрофильными лейкоцитами в виде широкой полосы через все слои раны с отеком прилежащих тканей (рисунок 3А).
Применение исследуемых фармацевтических композиций уже к 3 суткам эксперимента позволило существенно уменьшить отек и выраженность нейтрофильной инфильтрации - экссудативную фазу воспаления в области раны. На рисунках 3Б и 3В видна минимальная инфильтрация лейкоцитами ткани дна раны по сравнению с контролем (рисунок 3А), что свидетельствует о противовоспалительном эффекте исследуемых мазей.
При этом исследуемая фармацевтическая композиция с цинксодержащим производным дигидрокверцетина на гидрофобной основе с лиственничным воском существенно по сравнению с мазью с исходным дигидрокверцетином на гидрофобной основе с лиственничным воском способствует уменьшению площади некроза и уменьшению отека в тканях ожоговой раны.
Пример 5.
Противомикробная активность
Помимо хороших ранозаживляющего и противовоспалительного эффектов оригинальные фармацевтические композиции, представляющие собой мази дигидрокверцетина или его цинксодержащего производного на гидрофобной основе с лиственничным воском, обладают и антимикробным действием. Микробиологическая чистота оценивалась при помощи качественного и количественного бактериологического анализа в расчете на 1 г ткани, взятой из глубины ожоговой раны [Клинико-бактериологические методы исследования и антибактериальная терапия ожоговой раневой инфекции (Методические рекомендации) / Ю.В. Филиппович, А.Ю. Варес, В.П. Наабер, В.А. Наумов, Н.Г. Костин, П.В. Мяннико, С.Ш. Уманский, Г.Н. Фирсов, И.Г. Бекергун, С.С. Кузнецова. - Таллин, 1982. - 29 с.].
Результаты проведенных исследований представлены на рисунках 4-6.
Так, исследуемая фармацевтическая композиция с цинксодержащим производным дигидрокверцетина на гидрофобной основе с лиственничным воском существенно (на 1-2 порядка) по сравнению с контролем и мазью с исходным дигидрокверцетином снижает содержание как грам(+), так и грам(-) микроорганизмов и общее количество грибов рода Candida в 1 г ткани ожоговой раны начиная с 3 суток после ожога и поддерживает "бактериологическую чистоту" раны (содержание грам(+), грам(-) микроорганизмов и грибов рода Candida составляет менее 103) в этой группе животных до конца эксперимента.
Содержание грам(+) и грам(-) микроорганизмов, а также грибов рода Candida в опытной группе животных, обработанных мазью с дигидрокверцетином на гидрофобной основе с лиственничным воском, значимо не отличается от аналогичных показателей контрольной группы.
Пример 6.
Антиоксидантная активность
Для изучения механизма ранозаживляющего действия оригинальных фармацевтических композиций для наружного применения, представляющих собой мази дигидрокверцетина или его цинксодержащего производного на гидрофобной основе с лиственничным воском, была проведена оценка показателей оксидантного и антиоксидантного статуса экспериментальных животных путем определения показателей перекисного окисления липидов, а также уровня активности антиоксидантной ферментативной системы в крови крыс.
Оксидантный статус организма экспериментальных животных определяли по накоплению первичных (гидроперекиси липидов - ГПЛ) [Гаврилов В.Б., Мишкорудная М.И. Спектрофотометрическое определение содержания гидроперекисей липидов в плазме крови // Лаб. дело. -1983.- N. 3. - С. 33-35] и конечных продуктов перекисного окисления липидов (малонилдиальдегида - МДА) [Гаврилов В.Б., Гаврилова А.Р., Мажуль Л.М. Анализ методов определение продуктов ПОЛ в сыворотке крови по тесту с ТБК // Вопр. мед. химии. - 1987. - N. 1. - С. 118-122]. Антиоксидантный статус оценивали, исследуя активность супероксиддисмутазы (СОД) [Костюк В.А., Потапович А.И., Ковалева Ж.В. Простой и чувствительный метод определения активности супероксиддисмутазы, основанный на реакции окисления кверцетина // Вопр. мед. химии. - 1990. - N.2. - С. 88-91] и каталазы [Королюк М.А., Иванова Л.И., Майорова И.Г., Токарев В.Е. Метод определения активности каталазы // Лаб. дело. - 1988. - N. 1. - С. 16-19] в эритроцитах крови.
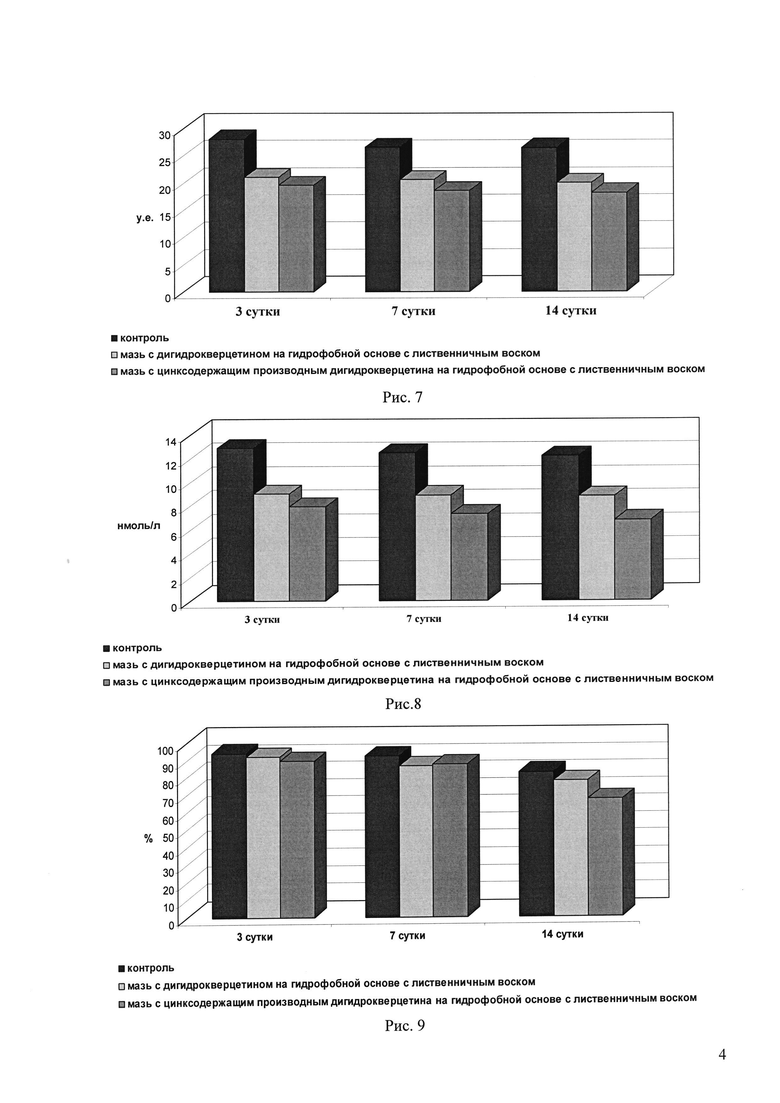
Ожоговая травма вызывает рост продукции радикалов в крови экспериментальных животных, в результате чего в ранние сроки после ожога складываются предпосылки для избыточного накопления пероксидов (рисунок 7).
Это выражалось в повышении количества ГПЛ в эритроцитах крови крыс, особенно в первые сутки после моделирования ожога (до в 1,6 раза в контрольной группе животных и в 1,1-1,2 раза в опытных группах животных, обработанных фармацевтическими композициями с дигидрокверцетином и его цинксодержащим производным, соответственно по сравнению с исходным значением - 18,1 у.е.). Только в экспериментальной группе животных, обработанных мазью с цинксодержащим производным дигидрокверцетина на гидрофобной основе с лиственничным воском, начиная с 7 суток данный показатель приходил в норму. В остальных случаях он оставался на прежнем уровне.
На протяжении всего эксперимента отмечается повышение уровня МДА в эритроцитах крови контрольной группы животных в 1,9-2,0 раза в зависимости от срока по сравнению с исходным значением (6,4 нмоль/л) (рисунок 8). В то время как аналогичный показатель в опытной группе животных, обработанных мазью с дигидрокверцетином, был выше исходного значения в 1,4 раза. В группе животных, обработанных мазью с цинксодержащим производным дигидрокверцетина на гидрофобной основе с лиственничным воском, уровень МДА в эритроцитах крови не превышал исходное значение более чем в 1,2 раза на всем протяжении эксперимента.
Анализ антиоксидантных ферментов эритроцитов крыс при моделировании термического ожога выявил активацию СОД (рисунок 9), при этом отсутствовало достоверное изменение активности каталазы по сравнению с исходным значением данного показателя во всех группах животных.
Ожоговая травма приводит к значительному увеличению СОД-активности в эритроцитах крови во всех группах экспериментальных животных (по сравнению с нормой - 78,8%). Ожог вызывает не только повышение радикал-продуцирующей активности клеток крови, но и развитие дисбаланса в системе антиоксидантной защиты эритроцитов: рост активности СОД без адекватной реакции со стороны пероксидутилизирующего фермента - каталазы.
Таким образом, в результате изучения фармакологической активности оригинальных фармацевтических композиций для наружного применения, представляющих собой мази дигидрокверцетина или его цинксодержащего производного на гидрофобной основе с лиственничным воском, было показано их положительное влияние на процессы перекисного окисления липидов (антиоксидантная активность), лежащее в основе механизма ранозаживляющего действия в эксперименте in vivo на модели термического ожога 2 и 3А степени у крыс.
Исходя из вышесказанного разработанные оригинальные фармацевтические композиции на основе дигидрокверцетина, его цинксодержащего производного и лиственничного воска обладают антиоксидантной, противомикробной, ранозаживляющей и противовоспалительной активностями, особенно в первые сутки после ожога. Это делает заявляемое средство в виде мягких лекарственных форм для наружного применения топического действия перспективным для лечения различных видов ран, в том числе и ожоговых.
| название | год | авторы | номер документа |
|---|---|---|---|
| Средство для профилактики и лечения язвенного колита | 2017 |
|
RU2649119C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ДЛЯ ПРОИЗВОДСТВА МАЗЕЙ, ОБЛАДАЮЩАЯ ПРОТИВОВОСПАЛИТЕЛЬНОЙ И РАНОЗАЖИВЛЯЮЩЕЙ АКТИВНОСТЯМИ, СТИМУЛИРУЮЩАЯ РОСТ ВОЛОСЯНЫХ ФОЛЛИКУЛОВ НА ОСНОВЕ ВОСКА КОРЫ ЛИСТВЕННИЦЫ СИБИРСКОЙ И ГМЕЛИНА. | 2014 |
|
RU2582984C1 |
| Средство для лечения длительно незаживающих ран | 2024 |
|
RU2835678C1 |
| КОМПЛЕКСНОЕ СОЕДИНЕНИЕ ЦИНКА С N-ИЗОПРОПЕНИЛИМИДАЗОЛОМ КАК РАНОЗАЖИВЛЯЮЩЕЕ СРЕДСТВО | 2019 |
|
RU2725634C1 |
| КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ ЦИНКА С N-АЛЛИЛИМИДАЗОЛОМ КАК РАНОЗАЖИВЛЯЮЩИЕ СРЕДСТВА | 2019 |
|
RU2719360C1 |
| ПРОТИВООЖОГОВАЯ КОМПОЗИЦИЯ | 2014 |
|
RU2552790C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ РАН И ОЖОГОВ | 2012 |
|
RU2513186C1 |
| Мазь для лечения поверхностных термических ожогов | 2016 |
|
RU2612260C1 |
| Композиция для лечения заболеваний кожи и косметического использования | 2019 |
|
RU2724342C1 |
| Средство для лечения ожогов | 2024 |
|
RU2825001C1 |



Изобретение относится к химико-фармацевтической промышленности, медицине, ветеринарии, фармакологии и представляет собой средство для лечения ран и ожогов, обладающее антиоксидантной, противовоспалительной, противомикробной и ранозаживляющей активностями, выполненное в мягкой лекарственной форме для наружного применения топического действия в виде гидрофобных мазей, содержащее в качестве действующего фармакологически активного вещества дигидрокверцетин или металлокомплексное соединение дигидрокверцетина с цинком общей формулы ML2(H2O)2, где М - ион цинка, a L - лиганд, представляющий собой депротонированный дигидрокверцетин, в котором количественное содержание ионов цинка составляет 8,8-9,2%, и дополнительно включающее гидрофобную основу с лиственничным воском, причем компоненты в средстве находятся в определенном соотношении, в мас. %. Изобретение обеспечивает эффективное лечение различных видов ран и ожогов и обладает широким спектром терапевтического действия. 2 н.п. ф-лы, 6 пр., 9 ил.
1. Средство для лечения ран и ожогов, обладающее антиоксидантной, противовоспалительной, противомикробной и ранозаживляющей активностями, выполненное в мягкой лекарственной форме для наружного применения топического действия в виде гидрофобных мазей, содержащее в качестве действующего фармакологически активного вещества дигидрокверцетин или металлокомплексное соединение дигидрокверцетина с цинком общей формулы ML2(H2O)2, где М - ион цинка, a L - лиганд, представляющий собой депротонированный дигидрокверцетин, в котором количественное содержание ионов цинка составляет 8,8-9,2%, и дополнительно включающее гидрофобную основу с лиственничным воском при следующем соотношении компонентов в мас. %:
2. Применение средства по п. 1 для лечения ран и ожогов у нуждающегося субъекта.
| МАЗЬ ДЛЯ ЛЕЧЕНИЯ ТЕРМИЧЕСКИХ ОЖОГОВ И СПОСОБ ЛЕЧЕНИЯ С ЕЕ ИСПОЛЬЗОВАНИЕМ | 2008 |
|
RU2405536C2 |
| ИВАНОВА Н.В | |||
| и др | |||
| Характеристические параметры процесса экстракции коры лиственницы этилацетатом //Химия растительного сырья, 2008, стр.39-42 | |||
| КРЕМ ДЛЯ РУК | 2008 |
|
RU2382635C1 |
| NAUMOV AA | |||
| et all | |||
| Beneficial action of the liposomal form of dihydroquercetin on the process of skin regeneration after thermal burn//Tsitologiia, 2010, 52(4):311-6, реферат. | |||
Авторы
Даты
2017-12-04—Публикация
2016-10-18—Подача