Изобретение относится к медицине, в частности, к фармакологии и клинической фармакологии, а именно, к новому применению комплексных соединений цинка производных N-аллилимидазола в качестве соединений, обладающих ранозаживляющим действием. Изобретение может быть использовано в медицине, хирургии, ветеринарии и косметологии при лечении открытых ран, порезов, послеоперационных швов и других повреждений кожи и слизистой, а также для заживления рубцов и шрамов.
Рост бытовых и производственных травм, а также ранений, полученных в ходе военных действий и бытовых конфликтов, определяет проблему лечения раневых повреждений как одну из основных в современной медицине. Поиск фармакологических средств, положительно влияющих на регенеративные процессы в коже, особенно актуален в экстремальной медицине и косметологии.
В настоящее время исследуются разные фармакологические группы лекарственных веществ, обладающих регенерирующими свойствами: гормоны, антисептики, адсорбенты, протеолитические ферменты, препараты на основе неорганических и металлоорганических соединений. Известно использование для заживления ран мазей и гелей: левомеколь, солкосерил, актовегин, метилурацил и др.
В хирургический практике широко применяется 10% метилурациловая мазь, которая обладает противовоспалительным, иммуномодулирующим, регенерирующим, фотозащитным действием, улучшает трофику тканей (Ноздрин В.И., Белоусова Т.А., Яцковский А.Н., 2002). Однако вазелино-ланолиновая основа мази обладает высокой вязкостью и клейкостью, вследствие чего препятствует нормальному водо-, тепло-, газообмену в кожных покровах, а также может вызывать аллергическую реакцию.
Цинксодержащие соединения (цинка оксид, цинка сульфат, цинка гиалуронат и др.) широко применяются в качестве заживляющих средств при пролежнях, свищах, плохо заживающих ранах.
Цинка сульфат, например, обладает антисептическим, вяжущим, подсушивающим, противомикробным действием. Он значительно улучшает процессы ангиогенеза, реэпителизации и ремоделирования тканей (El-Adl, М., Abdelkhalek, N., Mahgoub, Н.A. et al., 2018).
Однако при применении данных средств наблюдаются побочные эффекты в виде легкого жжения, покраснения, кожных высыпаний, ощущения сухости кожи.
Эффективность данных средств вследствие слабого усвоения кожей низкая, что значительно ограничивает их применение.
Известно применение дигидрокверцетина или его цинксодержащего металлокомплексного производного с количественным содержанием ионов цинка 9,2% в качестве действующего вещества в средствах для лечения ран и ожогов и дополнительно включающее гидрофобную основу с лиственничным воском (патент RU 2637440). Однако ранозаживляющее действие данного средства изучалось только на модели ожоговой раны, заживление которой имеет свои патогенетические особенности.
Кроме того, недостатком данного решения является использование гидрофобной основы, которая может препятствовать теплообмену, резорбции веществ, а также выходу жидкости на поверхность раны, что крайне нежелательно при раневом процессе. В ряде случаев возможно аллергическое и сенсибилизирующее действие.
Наиболее близким к предлагаемому решению является применение ацизола (бис(1-винилимидазол)цинкдиацетата) для лечения кожных заболеваний: псориаз, нейродермиты, длительно не заживающие (трофические) язвы и другие дефекты кожи воспалительного характера. Ацизол вследствие антигипоксического эффекта обеспечивает стимуляцию режима оксигенации зоны поражения, что способствует нормализации основных структурных процессов, формирующих эпидермис: пролиферации, дифференцировки и апоптоза (патент RU 2247558). Однако ранозаживляющее действие мазей и растворов на основе ацизола не изучалось.
Технической проблемой, на решение которой направлено заявляемое изобретение, является разработка средства для наружного применения на основе соединений цинка с N-аллилимидазолом, обладающих ранозаживляющим и регенерирующим действием.
Техническим результатом, на достижение которого направлено заявленное изобретение, является сокращение сроков заживления ран и регенерации ткани без образования рубца.
Технический результат достигается за счет применения в качестве ранозаживляющего средства производного N-аллилимидазола - бис(N-аллилимидазол)цинкдиацетата формулы
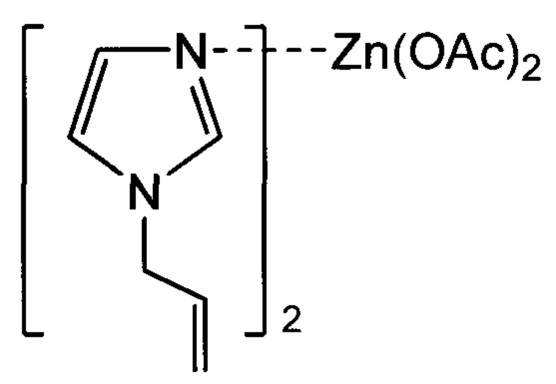
или бис(N-аллил-2-метилимидазол)цинкдиацетата формулы
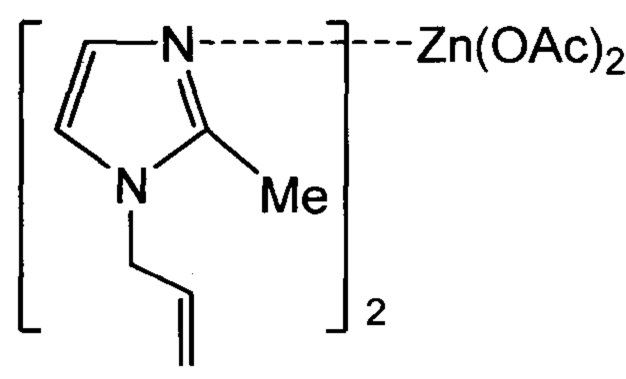 , где Ac - ацетат, Me - метил.
, где Ac - ацетат, Me - метил.
Технический результат также достигается за счет разработки средства для лечения ран для наружного применения, содержащего в качестве действующего вещества производное N-аллилимидазола бис(N-аллилимидазол)цинкдиацетат или бис(N-аллил-2-метилимидазол)цинкдиацетат, и гидрофильную основу, при следующем соотношении компонентов, масс. %:
производное N-аллилимидазола - 0,95-1,05,
основа - остальное.
В качестве основы могут быть использованы производные целлюлозы, полимеры модифицированной акриловой кислоты или полоксамеры.
Средство может быть выполнено в виде геля, крема, мази или любой другой мягкой лекарственной формы.
Лиганд N-аллилимидазол является производным имидазола. Имидазол и его производные участвуют в образовании гетеро- и макроциклов (креатинкиназа, химотрипсин, карбоксипептидаза А, карбоангидраза В и др.). Они играют важную роль в функционировании биологических систем и являются эффективными лекарственными препаратами, широко применяемыми в медицине (циметидин, левамизол, метронидазол, дибазол, метапрот, клонидин, пилокарпин и др.).
Синтез комплекса бис(N-аллилимидазол)цинкдиацетат (шифр ALL) описан ранее (патент РФ №2430090; Parshina L.N., Grishchenko L.A., Smimov V.I. et al., 2019).
Бис(N-аллил-2-метилимидазол)цинкдиацетат (шифр ALL-2) получали при комнатной температуре добавлением ацетата цинка к раствору N-аллил-2-метилимидазола [Zn(OAc)2 : N-аллилимидазол = 1:2.0-4.0] в смеси эфир-ацетон (3:1). К перемешиваемому раствору 1.0 г (8.2 ммоль) N-аллил-2-метилимидазола в 40 мл смеси эфира и ацетона (3:1) в течение 40 мин добавляли небольшими порциями 0.38 г (2.1 ммоль) ацетата цинка. Суспензию перемешивали 2 суток при комнатной температуре. Образовавшийся белый осадок отфильтровывали, промывали эфиром и сушили в вакууме (5-10 мм) 5-6 ч при комнатной температуре. Выход 0.82 г (91%), т.пл. 152-153°С. Полученный комплекс - бис(N-аллил-2-метилимидазол)цинкдиацетат - растворим в воде, этаноле, хлороформе, диметилсульфоксиде, ацетонитриле, этилацетате, хлористом метилене, не растворим в эфире.
Спектр ЯМР 1Н (CDCl3, δ, м.д., J, Гц): 7.29 с (1H, Н4), 6.81 с (1H, Н5), 5.87 м (1H, СН=), 5.27 д (1H,=СНцис, 3J=10.3), 5.05 д (1Н,=CHтранс, 3J=16.8), 4.46 д (2Н, NCH2, 3J=5.2), 2.46 с (3Н, СН3Ас), 2.01 с (3Н, СН3). ИК спектр (KBr, см-1): 434, 525, 556, 617, 673, 760, 780, 911, 1009, 1154, 1248, 1282, 1333, 1384 (ОАссим), 1425, 1480, 1510 (С=Cимидазол, С=Nимидазол), 1546, 1614 (ОАсасим), 2928, 2990, 3045, 3115, 3433.
Найдено (%): С 49.97; Н 6.30 N 12.78. O18H26N4O4Zn. Вычислено (%): С 50.53; Н 6.13; N 13.10.
Предлагаемое средство для лечения ран может быть выполнено в форме геля, крема, мази или любой другой мягкой (вязко-пластичной) лекарственной формы, и может быть изготовлено любым известным способом. При этом специалист в данной области техники может выбрать подходящую гидрофильную основу в зависимости от требуемой лекарственной формы.
В качестве гидрофильной основы - гелеобразующего агента, используемого в гелеобразной форме, - могут выступать производные целлюлозы, либо любой другой коммерчески доступный гелеобразующий агент. Предпочтительными гелеобразующими агентами являются производные целлюлозы, например, метилцеллюлоза, гидроксипропилметилцеллюлоза, карбоксиметилцеллюлоза, натрий карбоксиметилцеллюлоза, гидроксиэтилцеллюлоза, полоксамеры и/или полимеры модифицированной акриловой кислоты, например, карбопол (Carbopol), либо по отдельности, либо в комбинации.
При растворении в воде молекулы гелеобразующего агента меняют свою конфигурацию и увеличивают вязкость жидкости. Для приготовления геля производного целлюлозы, к воде очищенной добавляют навеску водорастворимого производного целлюлозы, оставляют до набухания (обычно 1,5-2 часа), а затем тщательно перемешивают. К полученной гелевой основе добавляют действующее вещество - бис(N-аллилимидазол)цинкдиацетата или бис(N-аллил-2-метилимидазол)цинкдиацетата и перемешивают до его полного растворения в основе. Содержание действующего вещества может составлять от 0,95 до 1,05 масс. %.
В частности, для приготовления 1% геля на основе натрий карбоксиметилцеллюлозы смешивают 0,05 г натрий карбоксиметилцеллюлозы, 0,05 г действующего вещества и 4,90 мл воды.
Было проведено исследование ранозаживляющего действия комплекса цинка с N-аллилимидазолом: ALL [бис(N-аллилимидазол)цинкдиацетат] и ALL-2 [бис(N-аллил-2-метилимидазол)цинкдиацетат] на течение раневого неинфицированного процесса при моделировании линейной кожной раны у крыс. В качестве препаратов сравнения были взяты цинка сульфат 0,5% гель на основе натрий карбоксиметилцеллюлозы, солкосерил гель 10% для наружного применения (ООО «МЕДА Фарма», Россия), метилурацил мазь 10% для местного и наружного применения (АО «Нижфарм», Россия).
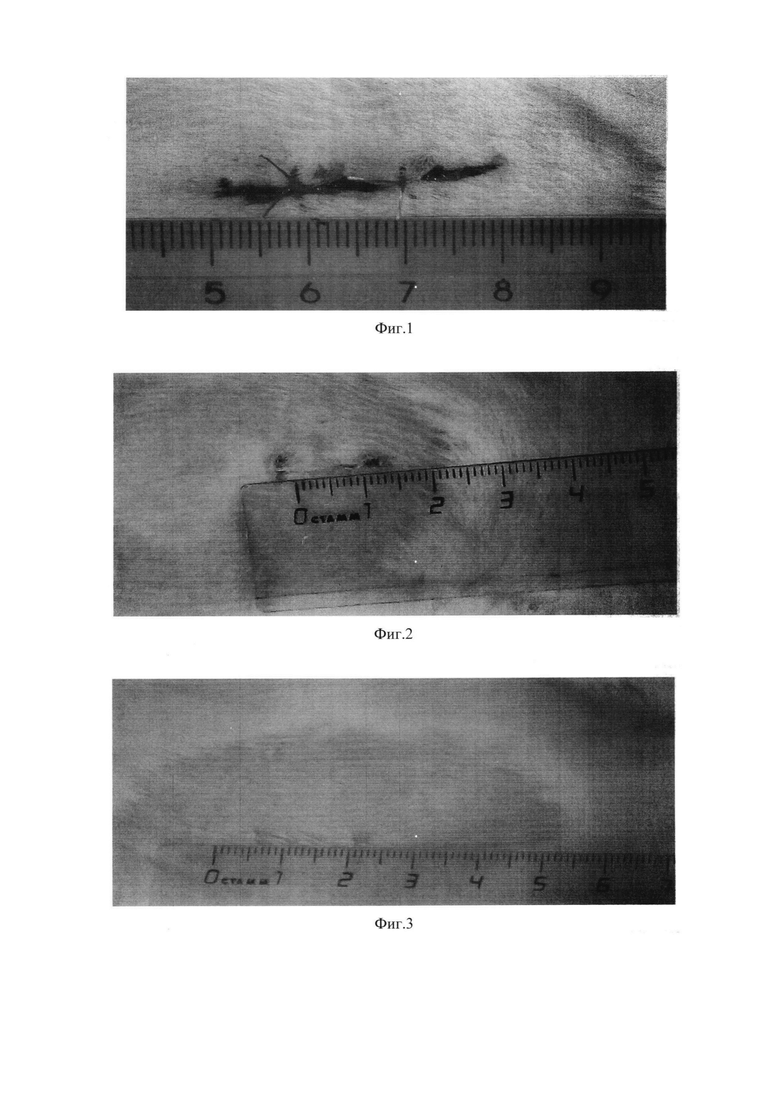
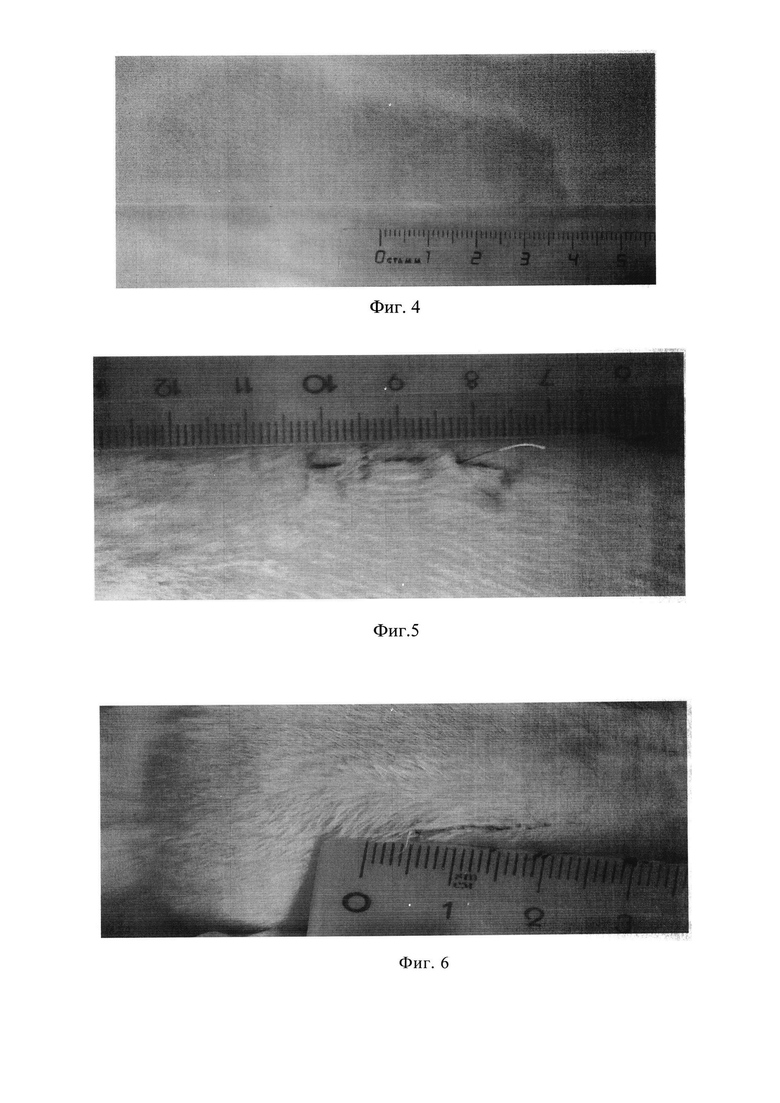
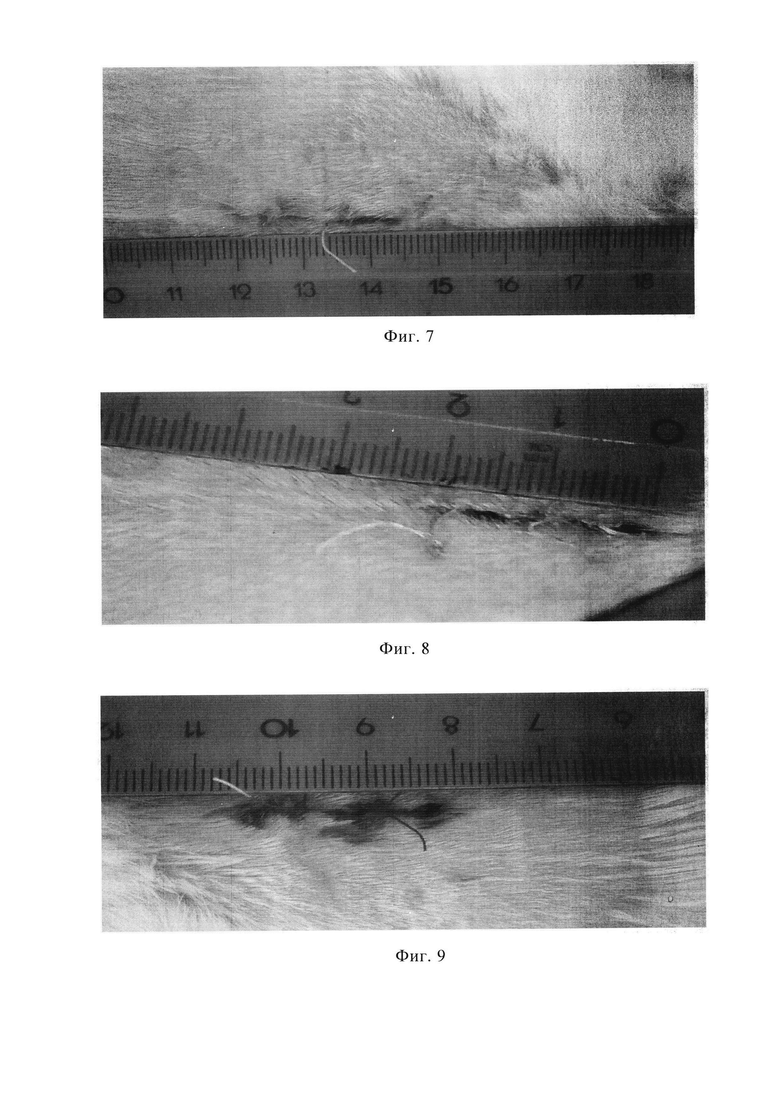
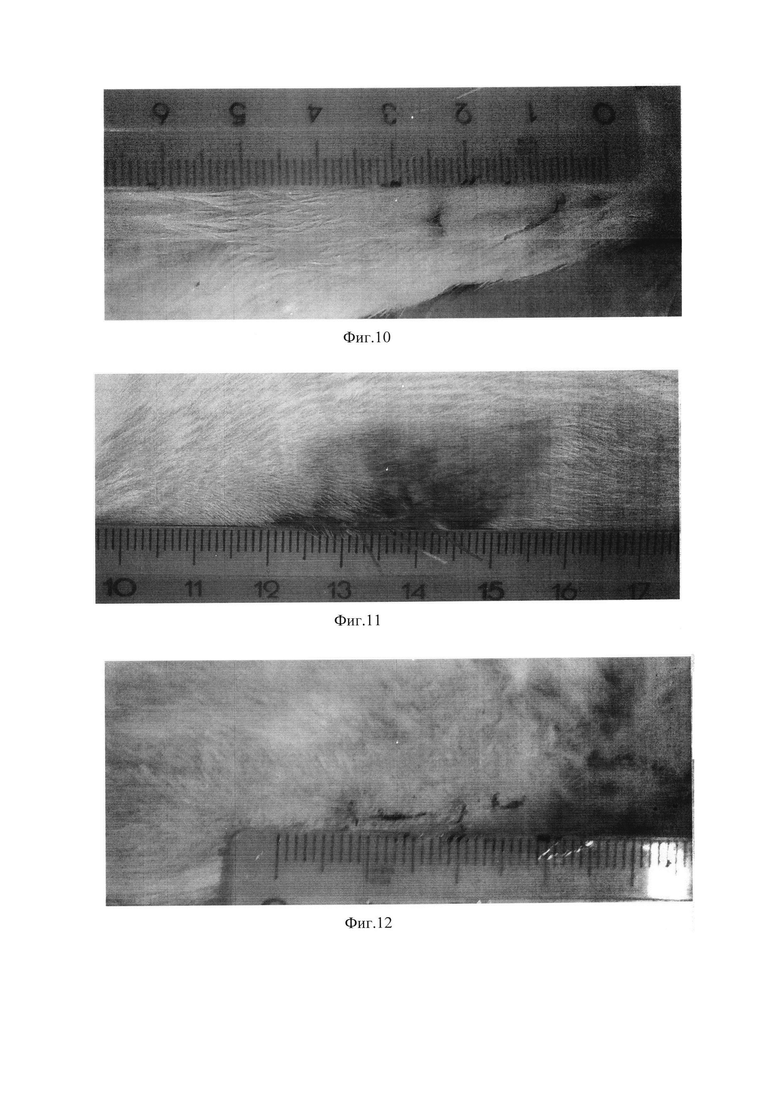
Изобретение иллюстрируется фотографиями, где на Фиг. 1 представлены исходные размеры линейной раны; на Фиг. 2 - размеры линейной раны у животного контрольной группы (8 сутки); на Фиг. 3 - размеры линейной раны у животного опытной группы (ALL, 8 сутки); на Фиг. 4 - размеры линейной раны у животного опытной группы (ALL-2, 8 сутки); на Фиг. 5 - размеры линейной раны у животного интактной группы (6 сутки); на Фиг. 6 - размеры линейной раны у животного интактной группы (7 сутки); на Фиг. 7 - размеры линейной раны у животного опытной группы (солкосерил, 6 сутки); на Фиг. 8 - размеры линейной раны у животного опытной группы (солкосерил, 7 сутки); на Фиг. 9 - размеры линейной раны у животного опытной группы (метилурацил, 6 сутки); на Фиг. 10 - размеры линейной раны у животного опытной группы (метилурацил, 7 сутки); на Фиг. 11 - размеры линейной раны у животного опытной группы (цинка сульфат, 6 сутки); на Фиг. 12 - размеры линейной раны у животного опытной группы (цинка сульфат, 7 сутки).
Исследование проводилось на 42 аутбредных белых крысах-самцах массой 250-370 г, полученных из питомника лабораторных животных «КролИнфо» (Московская область, Орехово-Зуевский район). Животные содержались в виварии в индивидуальных клетках на стандартном рационе питания. Световой режим составлял 12 часов света и 12 часов темноты. Температура воздуха поддерживалась в пределах 18-22°С, относительная влажность - 50-70%.
Все эксперименты проводили с обязательным соблюдением правил Европейской конвенции о защите позвоночных животных, используемых для экспериментов или в иных научных целях (European Convention for the Protection of Vertebrate Animals Used for Experimental and other Scientific Purposes (ETS 123), Strasbourg (1986), а также в соответствии с «Руководством по проведению доклинических исследований лекарственных средств» (Миронов А.Н. [ред.], Т. 1, Гриф и К, Москва, 2012).
Животные были разделены на 7 групп по 6 крыс в каждой: 1 группа - интактные (негативный контроль), 2 группа - контроль (гидрофильная основа), 3-7 группы - опытные. Животные 3 группы получали ALL, 4 группы - ALL-2, 5 группы - сульфат цинка, 6 группы - солкосерил, 7 группы - метилурацил. Модель «линейной раны» воспроизводили на крысах, находящихся под наркозом, вызванным комплексным наркозным средством Телазол™. На участке спины животного, недоступном для вылизывания, удаляли шерсть на ширину 20 мм и длину 50 мм, после чего скальпелем наносили рану длиной 30 мм (размеры раны измерялись с точностью до 1 мм). Затем на равном расстоянии шелковой нитью накладывали 2 шва (Фиг. 1). Для удобства последующего измерения размеров ран швы накладывали с таким расчетом, чтобы эпителий боковых краев раны не соприкасался, и эпителизация проходила от конечных краев раны.
Животным опытных групп сразу после операции наносили на область раны 0,2 г 1% геля цинковых комплексов N-аллилимидазола (в качестве гелевой основы использовали натрий карбоксиметилцеллюлозу) или препараты сравнения. Животным контрольной группы наносили такую же навеску гидрофильной основы. У интактных животных рана заживала «естественным» путем.
Животных размещали в клетках индивидуально. Для оценки динамики заживления раны ежедневно измеряли ее размеры и отмечали состояние кожных покровов. Обработку гелем и препаратами сравнения проводили ежедневно 1 раз в сутки на протяжении 7 дней.
Статистическую обработку полученных данных проводили с использованием t-критерия Стьюдента при помощи пакета статистических программ IBM SPSS Statistics 23. Различия считались статистически значимыми при уровне значимости р≤0,05.
Состояние регенеративных процессов отражает суточное уменьшение размера раны в процессе лечения. Анализ полученных данных показал, что в опытных группах, получавших лечение ALL и ALL-2, начиная с 5 суток лечения наблюдается статистически значимое уменьшение размеров ран по сравнению с контрольными животными. Динамика течения раневого процесса представлена в таблице.
В результате проведенных исследований выявлено более медленное заживление экспериментальной раны у животных контрольной группы. Как видно из таблицы и Фиг. 2, полного заживления к концу срока наблюдения (8 сутки) в данной группе не наблюдалось и составляло 67% от исходной длины раны.
На 8 сутки уменьшение размеров раны в группе опытных животных, получавших ALL-2, составляло 97% по сравнению с исходными размерами.
У животных, получавших лечение ALL, на 8 сутки произошла полная реорганизация раны (Фиг. 3-4). В экспериментальных группах не наблюдали рецидива воспаления, негативных местных и общих реакций.

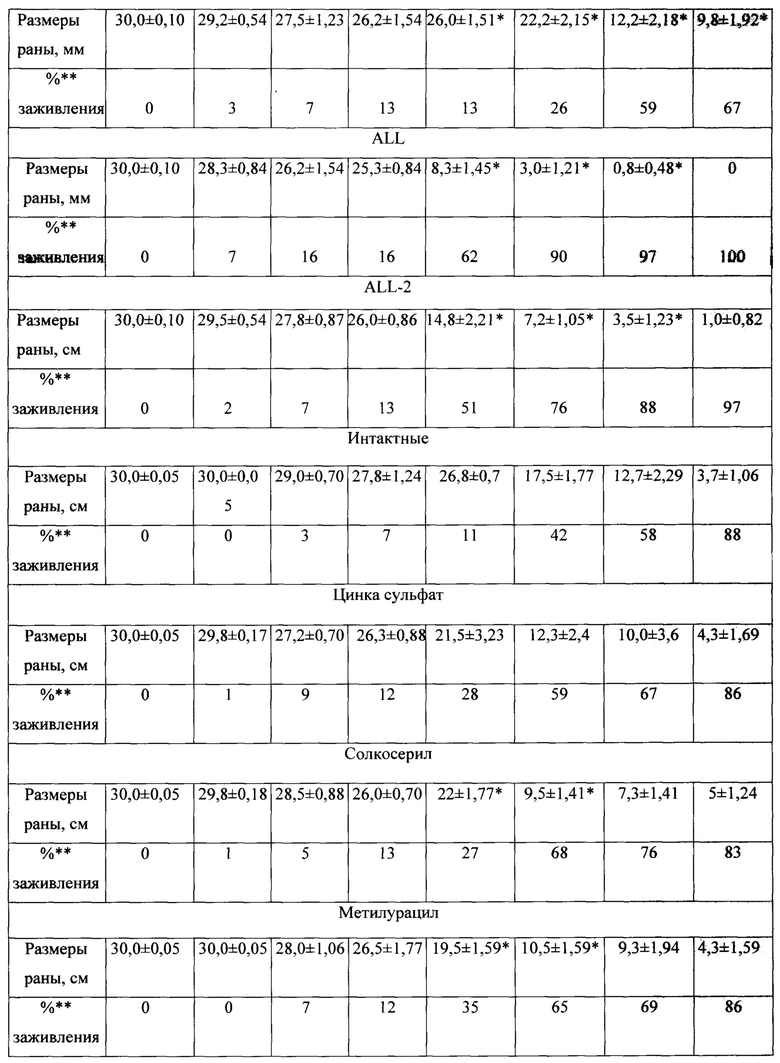
Примечание. Результаты в таблице представлены как средняя величина ± стандартная ошибка среднего (М±m). * - статистически значимые различия (р≤0,05) по отношению к контрольной или интактной группе. ** - % заживления по отношению к исходной длине раны.
У животных, получавших лечение цинка сульфатом, солкосерилом и метилурацилом, заживление ран на 8 сутки наблюдения составило 86, 83 и 86%, соответственно. В группе интактных животных процент заживления составил 88%. Значимые различия между опытными группами и интактными наблюдались на 5 и 6 сутки наблюдения в группе животных, получавших солкосерил и метилурацил. Процент заживления ран в этих группах животных составил 27 и 68% (солкосерил) и 35 и 65% (метилурацил), соответственно. В интактной группе процент заживления ран составил 11 и 42%, соответственно, на 5 и 6 сутки наблюдения (таблица). У животных в области раны отмечалась гиперемия в первые 2-3 суток после проведения операции. Грануляционная ткань имела темно-красный цвет. Корка струпа была грубой, жесткой (Фиг. 5-12).
Полученные результаты свидетельствуют о том, что местное применение 1% геля цинковых комплексов N-аллилимидазолов значительно сокращает сроки заживления неинфицированных ран по сравнению с изученными препаратами сравнения: цинка сульфатом, солкосерилом и метилурацилом.
Выявленное регенерирующее действие представляет интерес для дальнейшего изучения с целью разработки эффективных средств, стимулирующих репаративную регенерацию ран. Дерматотропное действие цинковых комплексов на модели линейных ран реализуется, вероятно, за счет высокой биодоступности, обеспечивающей фармакологическую эффективность, направленную на патогенетические механизмы раневого процесса: устранение гипоксии, улучшение микроциркуляции, нормализацию процессов свободно-радикального окисления и пролиферации клеток.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПЛЕКСНОЕ СОЕДИНЕНИЕ ЦИНКА С N-ИЗОПРОПЕНИЛИМИДАЗОЛОМ КАК РАНОЗАЖИВЛЯЮЩЕЕ СРЕДСТВО | 2019 |
|
RU2725634C1 |
| КОМПЛЕКС АЦЕТАТА ЦИНКА С 3-ГИДРОКСИПИРИДИНОМ, ОБЛАДАЮЩИЙ АНТИГИПОКСИЧЕСКОЙ АКТИВНОСТЬЮ В УСЛОВИЯХ ОСТРОЙ ЭКЗОГЕННОЙ ГИПОКСИИ | 2016 |
|
RU2631496C1 |
| КОМПЛЕКС АЦЕТАТА ЦИНКА С 1-ПРОПАРГИЛИМИДАЗОЛОМ, ОБЛАДАЮЩИЙ АНТИГИПОКСИЧЕСКОЙ АКТИВНОСТЬЮ | 2016 |
|
RU2632682C1 |
| Комбинированная композиция для лечения инфицированных ран различного генеза | 2018 |
|
RU2691144C1 |
| СРЕДСТВО ДЛЯ ЗАЖИВЛЕНИЯ КОЖНЫХ РАН ПЕРВИЧНЫМ НАТЯЖЕНИЕМ | 2004 |
|
RU2270007C2 |
| Способ лечения ран | 2020 |
|
RU2758243C1 |
| Ранозаживляющее средство в виде мази, содержащее хлорид рубидия | 2019 |
|
RU2722127C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ГНОЙНО-ВОСПАЛИТЕЛЬНЫХ ПРОЦЕССОВ МЯГКИХ ТКАНЕЙ И СЛИЗИСТЫХ ОБОЛОЧЕК | 2010 |
|
RU2445083C1 |
| АНТИМИКРОБНОЕ И РАНОЗАЖИВЛЯЮЩЕЕ СРЕДСТВО "УЛЬТРАКОЛ" | 2002 |
|
RU2220724C1 |
| Фармацевтическая субстанция для лечения инфицированных ран различного генеза | 2018 |
|
RU2697869C1 |
Изобретение относится к медицине, в частности к фармакологии и клинической фармакологии, а именно к новому применению бис(N-аллилимидазол)цинкдиацетата формулы
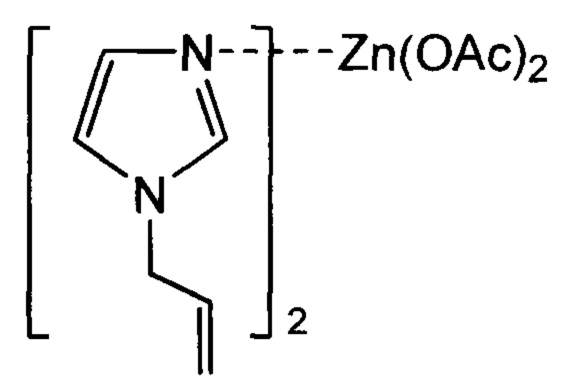
или бис(N-аллил-2-метилимидазол)цинкдиацетата формулы
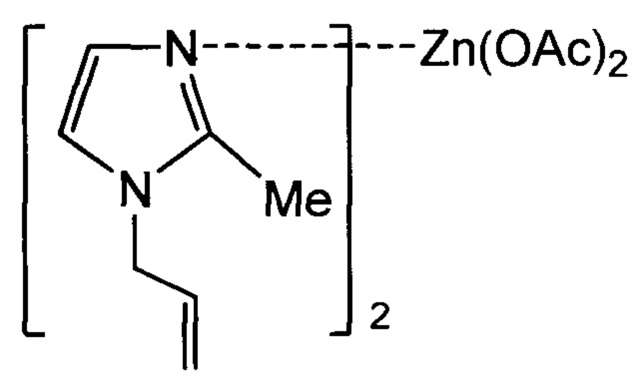 ,
,
где Ас - ацетат, Me - метил, в качестве ранозаживляющего средства. Также предложено средство для лечения ран для наружного применения. Техническим результатом, на достижение которого направлено изобретение, является сокращение сроков заживления ран и регенерации ткани без образования рубца. 2 н. и 2 з.п. ф-лы, 12 ил., 1 табл.
1. Применение бис(N-аллилимидазол)цинкдиацетата формулы
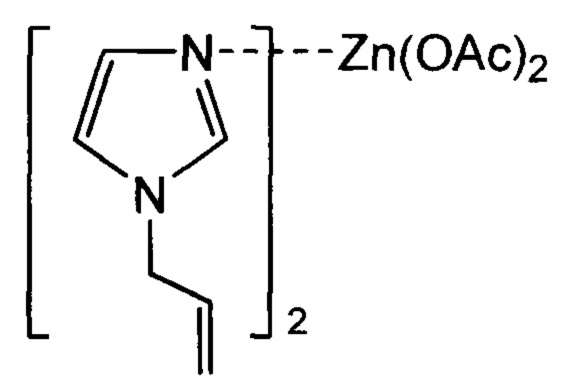
или бис(N-аллил-2-метилимидазол)цинкдиацетата формулы
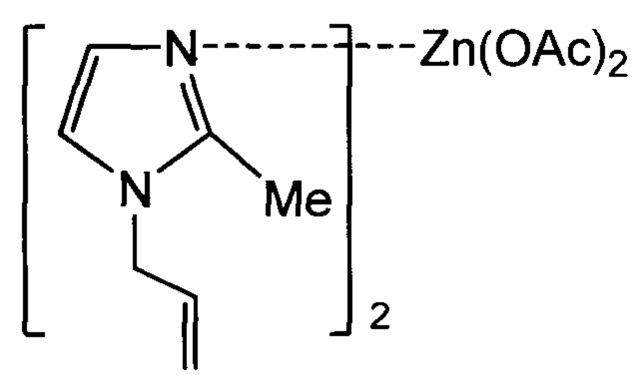 ,
,
где Ас - ацетат, Me - метил,
в качестве ранозаживляющего средства.
2. Средство для лечения ран для наружного применения, содержащее в качестве действующего вещества производное N-аллилимидазола бис(N-аллилимидазол)цинкдиацетат или бис(N-аллил-2-метилимидазол)цинкдиацетат, и гидрофильную основу, при следующем соотношении компонентов, масс. %:
производное N-аллилимидазола 0,95-1,05,
основа остальное.
3. Средство по п. 2, характеризующееся тем, что основа представляет собой производные целлюлозы, полимеры модифицированной акриловой кислоты или полоксамеры.
4. Средство по п. 2, характеризующееся тем, что представляет собой гель, крем, пасту или любую другую мягкую лекарственную форму.
| СРЕДСТВО НА ОСНОВЕ АЦИЗОЛА | 2003 |
|
RU2247558C1 |
| БИС(5-АМИНО-1,4-ДИОКСО-1,2,3,4-ТЕТРАГИДРОФТАЛАЗИН-2-ИЛ)ЦИНК, СПОСОБ ЕГО ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ, ЛЕЧЕБНЫЕ СРЕДСТВА НА ЕГО ОСНОВЕ, СПОСОБ ЛЕЧЕНИЯ КОЖНЫХ ЗАБОЛЕВАНИЙ И СПОСОБ ЛЕЧЕНИЯ ГАСТРИТА | 2013 |
|
RU2577849C2 |
| ПРОИЗВОДНЫЕ 1-АЛЛИЛИМИДАЗОЛА | 2009 |
|
RU2430090C2 |
| Средство для лечения ран и ожогов | 2016 |
|
RU2637440C1 |
Авторы
Даты
2020-04-17—Публикация
2019-10-04—Подача