В данном изобретении раскрыт способ обнаружения и определения (размера и композиции) циркулирующих иммунных комплексов в биологических средах многоступенчатым способом, включающим эксклюзионную хроматографию (ЭХ) и иммуноанализ.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Большинство биотерапевтических средств может индуцировать нежелательные иммунные ответы с возможными последствиями в отношении безопасности и эффективности, где эти ответы варьируют по частоте и тяжести (Buttel, I.C. et al., Biologicals 39 (2011) 100-109; COMMITTEE FOR MEDICINAL PRODUCTS FOR HUMAN USE (CHMP), EMEA Guideline on Immunogenicity Assessment of Biotechnology-derived Therapeutic Proteins, http://www.emea.europa.eu (2007)).
Образование противолекарственных антител (ПЛА) может привести в результате к измененной фармакокинетике, к утрате или снижению эффективности, к нейтрализации природных аналогов, а также к общим иммунным реакциям и реакциям гиперчувствительности, включающим сывороточную реакцию/реакцию гиперчувствительности III типа/заболевание, опосредованное иммунокомплексами (Buttel, I.C. et al., Biologicals 39 (2011) 100-109; COMMITTEE FOR MEDICINAL PRODUCTS FOR HUMAN USE (CHMP), EMEA Guideline on Immunogenicity Assessment of Biotechnology-derived Therapeutic Proteins, http://www.emea.europa.eu (2007)).
Синдром, подобный сывороточной реакции, в результате образования комплексов противолекарственных антител с лекарственным средством (ПЛА-ЛС) является хорошо известным побочным эффектом и описан для ряда биопрепаратов в доклинических исследованиях (Ponce, R. et al., Regul.Toxicol.Pharmacol.54 (2009) 164-182) и в клинической практике (COMMITTEE FOR MEDICINAL PRODUCTS FOR HUMAN USE (CHMP), EMEA Guideline on Immunogenicity Assessment of Biotechnology-derived Therapeutic Proteins, http://www.emea.europa.eu (2007); Dreyfus, D.H. et al., Ann.Allergy Asthma Immunol. 96 (2006) 624-627; Gamarra, R.M., J. Emerg. Med. 30 (2006) 41-44; Goto, S. et al., Int. J. Hematol. 89 (2009) 305-309; Hansel, T.T. et al., Nat.Rev.Drug Discov. 9 (2010) 325-338; Pilette, C. et al., J. Allergy Clin. Immunol. 120 (2007) 972-973; Tamilvanan, S. et al., J. Drug Target 18 (2010) 489-498).
Для имеющихся в продаже лекарственных средств признаки основных реакций, таких как сывороточная реакция или тяжелые аллергические реакции, диагностируют клинически. В тех случаях, когда побочные эффекты следуют за введением вовлеченных моноклональных антител (mAb; от англ. "monoclonal antibody"), эти реакции относят к ответу антител (COMMITTEE FOR MEDICINAL PRODUCTS FOR HUMAN USE (CHMP), EMEA Guideline on Immunogenicity Assessment of Biotechnology-derived Therapeutic Proteins, http://www.emea. europa.eu (2007)). Действительно, можно найти лишь весьма ограниченные данные, где образование ПЛА было исследовано и соотнесено с сигналами, наблюдаемыми клинически (Goto, S. et al., Int. J. Hematol. 89 (2009) 305-309).
С учетом потенциальной серьезности иммуногенности Европейская организация экспертизы лекарственных препаратов (ЕАПС) подчеркивает важность подтверждения и определения образования ПЛА (COMMITTEE FOR MEDICINAL PRODUCTS FOR HUMAN USE (CHMP), EMEA Guideline on Immunogenicity Assessment of Biotechnology-derived Therapeutic Proteins, http://www.emea.europa.eu (2007)).
В характерном случае оценку иммуногенности проводят, используя иммуноанализы, разработанные для обнаружения ПЛА (Mire-Sluis, A.R. et al., J. Immunol. Methods 289 (2004) 1-16; Shankar, G. et al., J. Pharm. Biomed. Anal. 48 (2008) 1267-1281; Koren, E. et al., J. Immunol. Methods 333 (2008) 1-9).
Информация о встречаемости ПЛА, тем не менее, до сих пор не дает возможности глубокого сопоставления с клинической картиной и измененной фармакокинетикой.
Количество и размер образовавшихся комплексов ПЛА с лекарственным средством зависит от нескольких параметров, например, от концентрации/доли ПЛА и лекарственного средства, а также от эпитопа и валентности (Abbas, А.K. and Lichtman, А.Н., Diseases caused by immunity responses: Hypersensitivity and Autoimmunity, in: Saunders (2003); Murphy, K. et al., Janeway's Immunobiology, in: Garland Science, Taylor & Francis Group, LLC (2008)).
Размер и заряд комплекса составляют важную детерминанту клиренса этого комплекса или индукции побочных эффектов. В характерном случае комплексы большего размера выводятся ретикулоэндотелиальной системой, комплексы малого размера обычно не запускают воспаление, в то время как комплексы среднего размера могут фиксировать комплемент, и могут вызвать повреждение ткани (Abbas, А. K. and Lichtman, А.Н., Diseases caused by immunity responses: Hypersensitivity and Autoimmunity, in: Saunders (2003); Murphy, K. et al., Janeway's Immunobiology, in: Garland Science, Taylor & Francis Group, LLC (2008); Mannik, M., Serum Sickness and pathophysiology of immune complexes, in: Clinical Immunology: Principles and Practices, Rich R.R., Fleisher T.A.S.B.D., Shearer W.T., Strober W. (eds.) 1062-1071 (1996); Sicherer, S.H., Leung D.Y.M., Serum Sickness, in: Nelsons textbook of pediatrics, Kliegman R.M., Behrman R.E., Jenson H.B.J., Stanton B.F. (eds.), Saunders Elsevier, pp.985-986 (2007). Кроме того, заряд комплекса является важным фактором для отложения комплексов в тканях (Abbas, А. K. and Lichtman, А.Н., Diseases caused by immunity responses: Hypersensitivity and Autoimmunity, in: Saunders (2003); Mannik, M., Serum Sickness and pathophysiology of immunocomplexes, in: Clinical Immunology: Principles and Practices, Rich R.R., Fleisher T.A.S.B.D., Shearer W.T., Strober W. (eds.) 1062-1071 (1996)).
Для глубокой оценки ответа ПЛА потенциально образуемые комплексы ПЛА-лекарственное средство должны быть охарактеризованы в отношении их размера и заряда. Кроме того, если существует эндогенный аналог лекарственного средства, информация о том, обладают ли образовавшиеся ПЛА перекрестной реактивностью с этими молекулами, и составляют ли эти эндогенные аналоги также часть комплексов, представляет собой ценную информацию. Кроме того, определение структуры антигена/лекарственного средства в иммунокомплексах предоставляет информацию о патогенезе.
Авторами Coyle et al. описано обнаружение и выделение иммунокомплексов в спинномозговой жидкости при рассеянном склерозе (Journal of Neuroimmunology 15 (1987) 97-107). Хроматофокусирование в сочетании с методом твердофазного иммуноферментного анализа (ELISA; от англ. "enzyme-linked immunosorbent analysis"), являющееся чувствительным методом анализа иммунокомплексов, описано Kneba, М., et al. (J. Immunol. Meth. 61 (1983) 233-243). Авторами Matousovic, K., et al. описаны IgA-содержащие иммунокомплексы в моче пациентов с первичной нефропатией IgA-типа (Nephrology Dialysis Transplantation 21 (2006) 2478-2484). Циркулирующие иммунокомплексы у кроликов, переживающих инфекцию вируса чумы, описаны авторами Rattan, В., et al. (Acta Vir. 38 (1994) 105-110). В документе WO 2008/031532 раскрыт анализ антител на лекарственное средство. Авторами Stubenrauch, K., et al. описана оценка общего иммуноанализа толерантности к лекарственному средству с обнаружением иммунокомплексов в образцах сыворотки от яванских макак после введения антител человека (J. Pharm. Biomed. Anal. 52 (2010) 249-254). В документе WO 2011/056590 раскрыты анализы на обнаружение антител к лекарственным средствам, включающим фактор некроза опухоли (TNF; от англ. "tumor necrosis factor"), и аутоантител. Авторами Wang Shui Long et al. описан анализ антител против лекарственного средства (ПЛА) к адалимумабу в сыворотке пациента с использованием нового гомогенного анализа изменения электрофоретической подвижности (Am. J. Gastroent. 105 (Sup I, 2010) S444-S445. В патенте ЕР 2354792 раскрыт способ обнаружения антител против лекарственного средства. Авторами Lambert, Р.Н., et al. описано коллективное исследование Всемирной Организации Здравоохранения (ВОЗ) по оценке восемнадцати способов обнаружения иммунокомплексов в сыворотке (J. Clin. Lab. Immunol. 1 (1978) 1-15). Способы измерения циркулирующих иммунокомплексов описаны авторами LeVinson, S.S. et al. (Clin. Immunol. Newsletter 3 (1987) 39-42).
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Обнаружено, что при способе обнаружения и определения (размера и композиции) циркулирующих иммуннокомплексов, например, комплексов, содержащих ПЛА против данного лекарственного средства, в биологических средах, включающем многоступенчатый способ с использованием эксклюзионной хроматографии (ЭХ) в сочетании по меньшей мере с одним иммуноанализом, может быть установлена корреляция с измененной фармакокинетикой, утратой или снижением эффективности, нейтрализацией природных аналогов, а также с общими иммунными реакциями и реакциями гиперчувствительности, включающими сывороточную реакцию/гиперчувствительность типа III/заболевание, опосредованное иммунокомплексами.
Один аспект, раскрытый в данном изобретении, представляет собой способ анализа/определения циркулирующего иммунокомплекса (ЦИК), образовавшегося in vivo, включающий следующие стадии:
a) эксклюзионную хроматографию (ЭХ) образца, полученного от млекопитающего, которому было введено лекарственное средство по меньшей мере один раз, для определения массы/размера иммунокомплекса,
b) необязательно вторую хроматографию, отличающуюся от ЭХ,
c) по меньшей мере один иммуноанализ, и
d) необязательно анализ на основе масс-спектрометрии,
в результате чего иммунокомплекс определяют посредством корреляции размера иммунокомплекса и результата/считывания данных иммуноанализа или масс-спектрометрического анализа.
Один аспект, раскрытый в данном изобретении, представляет собой способ анализа/определения циркулирующего иммунокомплекса конъюгированного противолекарственного антитела, содержащего (экзогенный) терапевтический полипептид и эндогенное противолекарственное антитело, образовавшегося in vivo, включающий следующие стадии:
a) эксклюзионную хроматографию (ЭХ) образца, полученного от млекопитающего, которому было введено лекарственное средство по меньшей мере один раз, для определения массы/размера иммунокомплекса,
b) необязательно вторую хроматографию, отличающуюся от ЭХ,
c) по меньшей мере один гетерогенный иммуноанализ для определения противолекарственного антитела, и
d) необязательно анализ на основе масс-спектрометрии,
в результате чего иммунокомплекс определяют посредством корреляции размера иммунокомплекса и результата/считывания данных иммуноанализа или масс-спектрометрического анализа,
где терапевтический полипептид представляет собой синтетический или неприродный терапевтический полипептид.
В одном воплощении всех аспектов изобретения образец представляет собой сыворотку или спинномозговую жидкость.
В одном воплощении всех аспектов изобретения иммунокомплекс представляет собой иммунокомплекс, специфичный к лекарственному средству.
Иммунокомплекс, специфичный к лекарственному средству, содержит лекарственное средство вместе с другими молекулами, отличающимися от лекарственного средства.
В одном воплощении всех аспектов изобретения иммуноанализ выбран из группы, включающей анализ на обнаружение противолекарственного антитела, анализ на обнаружение нейтрализующего антитела против лекарственного средства, фармакокинетический анализ (анализ количественного определения лекарственного средства), анализ на изотипирование антитела, анализ на обнаружение перекрестной реактивности ПЛА на эндогенный аналог лекарственного средства (если данное лекарственное средство содержит участок, также встречающийся эндогенно у млекопитающего), анализ связывания комплемента (связанного комплемента или способности к связыванию комплемента), анализ на определение эндогенного аналога лекарственного средства, содержащегося в иммунокомплексе (если данное лекарственное средство содержит участок, также встречающийся эндогенно у млекопитающего).
В одном воплощении всех аспектов изобретения иммуноанализ представляет собой гомогенный иммуноанализ или гетерогенный иммуноанализ. В одном воплощении изобретения иммуноанализ представляет собой радиоиммуноанализ (РИА), либо иммуноферментный анализ (ИФА, ELISA, метод иммуноанализа с ферментным усилением (ИФУ)), либо флуоресцентный поляризационный иммуноанализ (ФПИА), либо люминесцентный иммуноанализ (ЛИА), либо иммунорадиометрический иммуноанализ (ИРМА), либо иммуноанализ с ферментами, иммобилизованными на микрогранулированной смоле (MEIA; от англ. "microbead-enzyme immunoassay"), либо твердофазный иммуноферментный анализ с флуоресцентным усилением (ELFA; от англ. "enzyme-linked fluorescence assay"), либо иммуноферментный анализ, усиленный лектином (LEIA; от англ. lectin-enzyme immunoassay"), либо иммунофлуоресцентный анализ (ИФА), либо электрохемилюминесцентный анализ (ЭХЛИА), либо иммуномагнитный электрохемилюминесцентный анализ (ИМЭХЛ), либо хемилюминесцентный метод дот-анализа на обнаружение тканевых антигенов (CDIA; от англ. "chemiluminescence dot-immunobinding assay"), либо иммунонефелометрический анализ, либо иммунонефелометрический анализ, усиленный частицами.
В одном воплощении изобретения иммуноанализ представляет собой твердофазный иммуноферментный анализ (ELISA; от англ. "enzyme linked immunosorbent assay"), либо электрохемилюминесцентный анализ (ЭХЛИА), либо хемилюминесцентный метод дот-анализа на обнаружение тканевых антигенов (CDIA), либо флуоресцентный поляризационный иммуноанализ (ФПИА), либо иммунонефелометрический анализ, либо иммунонефелометрический анализ, усиленный частицами.
В одном воплощении всех аспектов изобретения вторая хроматография, отличающаяся от ЭХ, представляет собой ионообменную хроматографию (катионо- или анионообменную хроматографию), либо хроматографию с обращенной фазой, либо гидрофильную хроматографию (ГФЛХ), либо гидрофобную хроматографию (ГФБХ), либо гидрофобную хроматографию с переносом заряда (ГФБХ-ПЗ), либо хроматографию с ограниченным доступом вещества (RAMC; от англ. "restricted access material chromatography").
В одном воплощении всех аспектов изобретения эксклюзионная хроматография представляет собой эксклюзионную хроматографию со сбором элюата во фракциях. В одном воплощении изобретения каждую из фракций анализируют в иммуноанализе.
В одном воплощении по меньшей мере одну из фракций эксклюзионной хроматографии дополнительно разделяют с помощью второй хроматографии, отличающейся от ЭХ, со сбором элюата в аликвотах. В одном воплощении изобретения каждую из фракций анализируют в иммуноанализе. В одном воплощении изобретения каждую из фракций эксклюзионной хроматографии анализируют второй хроматографией, отличающейся от ЭХ.
В одном воплощении всех аспектов изобретения фракция представляет собой аликвоту.
В одном воплощении всех аспектов изобретения иммуноанализ представляет собой твердофазный иммуноферментный анализ.
В одном воплощении всех аспектов изобретения по меньшей мере один иммуноанализ представляет собой либо один, либо два, либо три, либо четыре, либо пять, либо шесть иммуноанализов.
В одном воплощении всех аспектов изобретения иммуноанализ представляет собой иммуноанализ противолекарственного антитела.
В одном воплощении всех аспектов изобретения по меньшей мере один из иммуноанализов представляет собой мостиковый твердофазный иммуноферментный анализ.
Положительный мостиковый твердофазный иммуноферментный анализ означает, что противолекарственное антитело составляло часть комплекса ПЛА-ЛС (противолекарственное антитело - лекарственное средство). Обнаружение противолекарственного антитела во фракции высокой молекулярной массы, то есть во фракциях эксклюзионной хроматографии, элюируемых раньше, означает, что противолекарственное антитело составляло часть комплекса, имеющего более высокую молекулярную массу.
В одном воплощении всех аспектов изобретения по меньшей мере один твердофазных иммуноферментных анализов представляет собой комплексный анализ на обнаружение комплексов ПЛА-ЛС. В одном воплощении изобретения комплексный анализ включает иммобилизованное антитело, специфичное к лекарственному средству, и антитело антивидовой специфичности в качестве идентифицирующего антитела.
В одном воплощении всех аспектов изобретения по меньшей мере один из иммуноанализов представляет собой прямой анализ на обнаружение противолекарственных антител, связанных с лекарственным средством, и/или с эндогенным аналогом лекарственного средства. В одном воплощении изобретения этот прямой анализ включает в качестве иммобилизованной молекулы иммобилизованное лекарственное средство или эндогенный аналог лекарственного средства и антитело антивидовой специфичности в качестве идентифицирующего антитела.
В прямом анализе использовано установление равновесия связывания противолекарственного антитела с лекарственным средством и/или его эндогенным аналогом в образце и иммобилизованным лекарственным средством после того, как свободное противолекарственное антитело удалено с помощью эксклюзионной хроматографии.
В одном воплощении всех аспектов изобретения поверхностный слой лекарственного средства представляет собой плотный поверхностный слой лекарственного средства.
За счет плотного поверхностного слоя осуществляют значительный сдвиг этого равновесия в направлении связывания с поверхностно-связанным лекарственным средством (используя авидность противолекарственного антитела).
В одном воплощении всех аспектов изобретения образец инкубируют в иммуноанализе в течение периода времени, составляющего от 16 до 32 часов.
Один аспект, как раскрыто в данном изобретении, представляет собой способ выделения лекарственного средства из комплексов ПЛА-ЛС с целью повышения толерантности лекарственного средства к последовательным анализам ПЛА/иммуноанализам. Аналогично способы, раскрытые в данном изобретении, можно применять для повышения толерантности лекарственного средства к иммуноанализам.
Один аспект, как раскрыто в данном изобретении, представляет собой способ определения комплексов противолекарственное антитело-лекарственное средство (ПЛА-ЛС), образовавшихся in vivo, включает следующие стадии:
a) эксклюзионную хроматографию образца, полученного от млекопитающего, которому было введено лекарственное средство по меньшей мере один раз, для определения массы/размера комплексов ПЛА-ЛС,
b) по меньшей мере один твердофазный иммуноферментный анализ для обнаружения противолекарственных антител,
где иммунокомплекс определяют как
- низкомолекулярный комплекс на основании положительного твердофазного иммуноферментного анализа, имеющий массу от примерно 150 кДа до примерно 400 кДа,
- комплекс средней молекулярной массы на основании положительного твердофазного иммуноферментного анализа, имеющий массу от примерно 400 кДа до примерно 1500 кДа, или
- высокомолекулярный комплекс на основании положительного твердофазного иммуноферментного анализа, имеющий массу от примерно 1500 «Да до примерно 7000 кДа.
Один аспект, как раскрыто в данном изобретении, представляет собой применение способа, раскрытого в данном изобретении, для определения корреляции характеристик иммунокомплекса с измененной фармакокинетикой.
Один аспект, как раскрыто в данном изобретении, представляет собой применение способа, раскрытого в данном изобретении, для определения снижения эффективности лекарственного средства.
Один аспект, как раскрыто в данном изобретении, представляет собой применение способа, раскрытого в данном изобретении, для определения нейтрализации природных аналогов лекарственного средства.
Один аспект, как раскрыто в данном изобретении, представляет собой применение способа, раскрытого в данном изобретении, для определения иммунных реакций и реакций гиперчувствительности к лекарственному средству.
Один аспект, как раскрыто в данном изобретении, представляет собой применение способа, раскрытого в данном изобретении, для определения отложений IgG в гломерулах.
В одном воплощении всех аспектов изобретения иммунная реакция и реакция. гиперчувствительности представляет собой сывороточную реакцию/реакцию гиперчувствительности III типа/заболевание, опосредованное иммунокомплексами.
Один аспект, как раскрыто в данном изобретении, представляет собой применение способа, раскрытого в данном изобретении, для определения присутствия иммунокомплексов, содержащих аутоиммунное антитело.
Один аспект, как раскрыто в данном изобретении, представляет собой применение способа, раскрытого в данном изобретении, для определения присутствия модифицированного/конъюгированного лекарственного средства.
В одном воплощении всех аспектов изобретения лекарственное средство представляет собой антитело человека или гуманизированное антитело.
СВЕДЕНИЯ, ПОДТВЕРЖДАЮЩИЕ ВОЗМОЖНОСТЬ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Определения
Термин "противолекарственное антитело" означает антитело, направленное против антигенного участка лекарственного средства. Данный антигенный участок представляет собой антигенную аминокислотную последовательность лекарственного средства или гликоструктуру лекарственного средства. В одном воплощении изобретения противолекарственное антитело направлено против вторичной модификации лекарственного средства, являющейся результатом рекомбинантного продуцирования лекарственного средства, представляющего собой антитело, в клетках, отличающихся от клеток человека, таких как клетки СНО (клетки яичника китайского хомячка; от англ. "Chinese hamster ovarian cells"), клетки НЕК (клетки мезонефроса человека; от англ. "human embryonic kidney cells") или клетки ВНК (клетки почек новорожденного хомяка; от англ. "baby hamster kidney cells"). Как правило, противолекарственные антитела направлены против антигенного участка лекарственного средства, распознаваемого иммунной системой животного, которому вводят лекарственное средство. Такое противолекарственное антитело представляет собой "специфичное противолекарственное антитело". Лекарственные средства разрабатывают таким образом, чтобы они содержали насколько возможно меньше антигенных областей. Например, лекарственные средства, предназначенные для применения в медицине, могут быть гуманизированы перед применением пациентом-человеком, чтобы свести к минимуму образование иммунного ответа против лекарственного средства. Данный иммунный ответ имел бы форму противолекарственных антител, направленных против участков такого гуманизированного лекарственного средства, не принадлежащих человеку (см., например, Pan, Y., et al., FASEB J. 9 (1995)43-49).
Термин "хромогены" означает флуоресцентные или люминесцентные группы и красители.
Термин "детектируемая метка" означает ферменты, ЯМР-активные группы или металлические частицы, гаптены, такие как, например, дигоскигенин. Детектируемая метка может также представлять собой фотоактивируемую сшиваемую группу, например, азидогруппу или азириновую группу. Хелаты металлов, которые могут быть обнаружены с помощью электрохемилюминесценции, также являются предпочтительными группами, испускающими сигнал, причем, особое предпочтение отдают хелатам рутения, например, хелату (биспиридил)32+рутения. Подходящие группы, меченые рутением, раскрыты, например, в следующих документах: ЕР 0580979, WO 90/05301, WO 90/11511 и WO 92/14138.
Термин "лекарственное средство" означает полипептид, такой как антитело или молекула, отличающаяся от антитела, который можно вводить индивидууму для лечения заболевания. Лекарственные средства (такие как терапевтические полипептиды или терапевтические моноклональные антитела) широко применяют для лечения различных заболеваний, таких как онкологические заболевания (например, гематологические и солидные злокачественные опухоли, включающие неходжкинскую лимфому, рак молочной железы и колоректальный рак), иммунологические заболевания, заболевания центральной нервной системы, сосудистые заболевания или инфекционные заболевания. Такие лекарственные средства описаны, например, в статье Levine, А.Р., et al., Journal of the Royal Society of Medicine 98 (2005) 145-152. Такие лекарственные средства представляют собой, например, антитела против CD20, CD22, HLA-DR, CD33, CD52, EGFR, G250, GD3, HER2, PSMA, CD56, VEGF, VEGF2, СЕА, антигена Levis Y, рецептора интерлейкина (ИЛ)-6 или рецептора IGF-1. Терапевтические антитела также описаны, например, в статье Groner, В., et al., Curr. Mol. Meth. 4 (2004) 539-547; и в статье Harris, М., Lancet Oncol. 5 (2004) 292-302.
Термин "млекопитающее" означает живое существо, принадлежащее к классу позвоночных животных. Термин "млекопитающее" в одном воплощении изобретения означает приматов, кошек, собак, овец, крыс, мышей и кроликов. В одном воплощении изобретения термин "млекопитающее" означает членов семейств отряда приматов, включающих игрунок и тамаринов (семейство игрунковых (Callitrichidae)), обезьян Нового Света (семейство капуцинов (Cebidae)), мартышек (семейство мартышковых (Cercopithecidae)), мышиных и карликовых лемуров (семейство Cheirogaleidae), мадагаскарских руконожек (семейство Daubentoniidae), галаго и сенегальских галаго (семейство Galagonidae), гиббонов и гиббоновых (семейство Hylobatidae), короткохвостого индри, хохлатого индри и их родственников (семейство Indridae), настоящих лемуров (семейство Lemuridae), лори (семейство Loridae), тонкотелых лемуров (семейство Megaladapidae), долгопятов (семейство Tarsiidae), а также их скрещивания. В одном воплощении изобретения млекопитающее выбрано из группы, состоящей из членов семейств игрунок и тамаринов, мартышек, мышиных и карликовых лемуров, гиббонов и гиббоновых, настоящих лемуров, а также их скрещивания. В данном конкретном воплощении изобретения ближайшие родственники людей, высшие приматы, в частности, группа шимпанзе, бонобо, горилл и орангутанов, исключены.
Термин "образец" означает любое количество вещества от млекопитающего, которому введено лекарственное средство. Такие вещества включают, но не ограничены ими, цельную кровь, сыворотку или плазму от такого млекопитающего, являющиеся самыми широко используемыми источниками образцов в рутинной доклинической практике. В одном воплощении изобретения образец представляет собой жидкий образец, такой как слюна, моча, синовиальная жидкость, цельная кровь, плазма или сыворотка. В одном воплощении изобретения образец представляет собой цельную кровь, плазму или сыворотку.
Термин "твердая фаза" означает нетекучее вещество и включает частицы (включая микрочастицы и гранулы), полученные из материалов, таких как полимер, металл (парамагнитные, ферромагнитные частицы), стекло и керамика; гелеобразные вещества, такие как кремнезем, глинозем и полимерные гели; капилляры, которые могут быть получены из полимера, металла, стекла и/или керамики; цеолиты и другие пористые вещества; электроды; микротитрационные планшеты; твердые полоски и кюветы, пробирки или другие контейнеры для спектрофотометрических образцов. Твердофазный компонент анализа отличается от инертных твердых поверхностей, с которыми анализ может находиться в контакте, тем, что "твердая фаза" содержит по меньшей мере одну группировку на его поверхности, предназначенную для взаимодействия с иммобилизованным антителом. Твердая фаза может представлять собой стационарный компонент, такой как пробирка, полоска, кювета или микротитрационный планшет, либо может представлять собой нестационарный компонент, такой как гранулы и микрочастицы. Микрочастицы можно также применять в качестве твердой фазы для гомогенных форматов анализа. Можно использовать разнообразные микрочастицы, дающие возможность либо нековалентного, либо ковалентного присоединения полипептидов и других веществ. Такие частицы включают полимерные частицы, такие как частицы полистирола и поли(метилметкарилат); частицы золота, такие как наночастицы золота и коллоиды золота; и керамические частицы, такие как частицы кремнезема, стекла и оксида металла. См., например, статью Martin, C.R., et al., Analytical Chemistry-News & Features, May 1, 1998, 322A-327A, включенную в данное описание посредством ссылки.
Способ мультиплексного анализа иммунокомплексов
Обнаружено, что при способе обнаружения и определения (размера и композиции) иммунокомплексов, направленных против введенного лекарственного средства, в биологической среде, включающем многоступенчатый способ с использованием эксклюзионной хроматографии (ЭХ) в сочетании с иммуноанализом, может быть установлена корреляция с измененной фармакокинетикой, утратой или снижением эффективности, нейтрализацией природных аналогов, а также общими иммунными реакциями и реакциями гиперчувствительности, включающими сывороточную реакцию/реакцию гиперчувствительности типа III/заболевание, опосредованное иммунокомплексами.
Таким образом, в качестве одного аспекта в данном изобретении раскрыт способ анализа/определения циркулирующих иммунокомплексов (ЦИК), образовавшихся in vivo, включающий эксклюзионную хроматографию образца, полученного от млекопитающего, которому было введено лекарственное средство по меньшей мере один раз, для определения массы/размера иммунокомплексов, необязательно вторую хроматографию, отличающуюся от ЭХ, и по меньшей мере один иммуноанализ, где иммунокомплекс определяют на основании корреляции размера иммунокомплекса и результата/считывания данных иммуноанализа.
Далее в качестве одного аспекта в данном изобретении раскрыт способ определения комплексов противолекарственное антитело-лекарственное средство (ПЛА-ЛС), образовавшихся in vivo, включающий эксклюзионную хроматографию образца, полученного от млекопитающего, которому было введено лекарственное средство по меньшей мере один раз, для определения массы/размера иммунокомплексов ПЛА-ЛС, и по меньшей мере один твердофазный иммуноферментный анализ для обнаружения противолекарственных антител, где иммунокомплекс определяют как низкомолекулярный комплекс на основании положительного твердофазного иммуноферментного анализа и массы от примерно 150 кДа до примерно 400 кДа, как комплекс средней молекулярной массы на основании положительного твердофазного иммуноферментного анализа и массы от примерно 400 кДа до примерно 1500 кДа или как высокомолекулярный комплекс на основании положительного твердофазного иммуноферментного анализа и массы от примерно 1500 кДа до примерно 7000 кДа.
В данном изобретении также раскрыто применение способа, раскрытого в данном изобретении, для определения корреляции с измененной фармакокинетикой, утратой или снижением эффективности, нейтрализацией природных аналогов, а также общими иммунными реакциями и реакциями гиперчувствительности, включающими сывороточную реакцию/реакцию гиперчувствительности типа III/заболевание, опосредованное иммунокомплексами.
Например, после введения лекарственного средства млекопитающему иммунная система этого млекопитающего может распознать введенное лекарственное средство как чужеродное и продуцировать противолекарственные антитела с целью нейтрализации введенного чужеродного вещества. Если лекарственное средство содержит элементы, эндогенные для млекопитающего, противолекарственные антитела могут быть также направлены против этого элемента лекарственного средства, и подобным образом также нацелены на эндогенный аналог у млекопитающего.
Такие события, как иммунный ответ/образование ПЛА/активация комплемента против введенного терапевтического лекарственного средства, могут привести к образованию иммунокомплексов. Образование иммунокомплексов (комплексов ПЛА-ЛС) может привести к измененным фармакокинетическим свойствам или клиническим последствиям, например, к синдромам, подобным сывороточной реакции.
Следующие свойства иммунокомплексов могут быть важными детерминантами индуцированных последующих эффектов:
- Размер комплекса
Образование комплексов большого размера может привести к усиленному клиренсу ретикулоэндотелиальной системой (РЭС).
Образование комплексов среднего размера может привести к фиксации комплемента с последующим отложением в ткани и к "сывороточной реакции".
Образование комплексов малого размера может не обладать выраженным эффектом.
- Заряд комплекса
Катионные иммунокомплексы могут быть отложены на мембранах/ассоциированы с мембранами клеток/тканей (с анионной клеточной поверхностью).
- Полярность комплекса
- Связывание или связывающая способность с C1q.
Таким образом, тщательное определение иммунокомплексов является предпосылкой для корреляции с эффектами in vivo (фармакокинетическими изменениями и/или токсикологическими эффектами).
Отдельная информация, например, о встречаемости противолекарственного антитела (ПЛА), тем не менее, не обеспечивает глубокую корреляцию с клинической картиной и измененной фармакокинетикой.
Количество и размер образовавшихся иммунокомплексов, таких как комплексы противолекарственное антитело-лекарственное средство (комплексы ПЛА-ЛС), зависит от нескольких параметров, например, от концентрации/соотношений, а также от эпитопа и валентности.
Размер комплекса является важной детерминантой клиренса комплекса или индукции побочных эффектов. В характерном случае комплексы большего размера выводятся ретикулоэндотелиальной системой, комплексы малого размера обычно не запускают воспаление, тогда как комплексы среднего размера могут фиксировать комплемент, и могут вызвать повреждение ткани.
Для глубокой оценки иммунного ответа, потенциально образующиеся иммунокомплексы следует определять в отношении их размера. Кроме того, если существует эндогенный аналог лекарственного средства, информация о том, обладают ли образующиеся ПЛА перекрестной реактивностью с этими молекулами, и составляют ли эндогенные аналоги также часть иммунокомплексов, является ценной информацией.
Информация может быть согласована с клинической картиной, такой как измененная фармакокинетика или побочные эффекты вследствие образования иммунокомплексов, и может обеспечить дополнительную информацию, объясняющую различия, например, субъектов, положительных по иммунокомплексам, без какого-либо воздействия и субъектов, положительных по иммунокомплексам, с измененной фармакокинетикой или клиническими последствиями, либо синдромы, подобные сывороточной реакции, только у некоторых субъектов, положительных по иммунокомплексам.
В целях обнаружения образования иммунокомплексов у млекопитающего, которому было введено лекарственное средство, и в целях определения образующихся иммунокомплексов необходим двухступенчатый способ.
Способ, раскрытый в данном изобретении, можно применять для определения любого иммунокомплекса, например, комплексов ПЛА-ЛС, а также аутоиммунокомплексов (аутоиммунных заболеваний, таких как ревматоидный артрит, волчанка и т.д.).
Эксклюзионная хроматография
На первой стадии образовавшиеся иммунокомплексы разделяют в отношении их размера с целью определения предполагаемого числа компонентов в комплексе. Это может быть выполнено с помощью эксклюзионной хроматографии (ЭХ) и фракционирования (в одном воплощении изобретения аликвотирования) элюата.
Исходя из предположения, что противолекарственное антитело относится к классу IgG, и имеет молекулярную массу примерно 150 кДа, и что молекулярная масса терапевтических полипептидов находится в диапазоне от примерно 2,5 кДа (полипептидное лекарственное средство; полипептид, состоящий из 20 аминокислотных остатков) до примерно 250 кДа (лекарственное средство, представляющее собой антитело; полноразмерное терапевтическое антитело класса IgG, содержащее дополнительные слитые эффекторные полипептиды, или мультиспецифическое антитело) стехиометрический комплекс 1:1 противолекарственного антитела и лекарственного средства имеет молекулярную массу, составляющую по меньшей мере примерно 150 кДа в случае низкомолекулярного полипептидного лекарственного средства и вплоть до примерно 400 кДа в случае комплексного лекарственного средства, представляющего собой антитело.
Выбор времени фракционирования определяет информацию о разделении по размеру.
Образец (биологическая среда), который может представлять собой сыворотку, плазму (например, для обнаружения противолекарственного антитела) или синовиальную жидкость (как, например, при ревматоидных заболеваниях), фракционируют, используя эксклюзионную хроматографию. Эксклюзионная хроматография обеспечивает первую информацию: размер аналита (комплекса).
Индивидуальные фракции эксклюзионной хроматографии можно анализировать, используя вторую хроматографию по размеру, такую как разделение ионообменной хроматографией (ИЭХ), чтобы определить заряд комплекса, либо хроматографию с обращенной фазой (ОФ), либо ГФЛХ разделение, чтобы определить полярность комплекса.
Индивидуальные фракции эксклюзионной хроматографии можно анализировать на активность связывания комплемента.
Индивидуальные фракции эксклюзионной хроматографии можно также анализировать, используя твердофазный иммуноферментный анализ (ELISA).
Твердофазный иммуноферментный анализ
Фракционирование элюата эксклюзионной хроматографии дает возможность мультиплексирования анализа ЭХ, поскольку для определения различных комплексов можно проводить различные иммуноанализы, такие как следующие анализы:
- ELISA мостикового типа ("классический скрининговый анализ ПЛА): обнаружение ПЛА во фракции более высокой молекулярной массы указывает на то, что ПЛА составляли часть фракции более высокой молекулярной массы;
- анализ комплексного типа: обнаружение комплексов ПЛА-ЛС, используя иммобилизацию, специфичную к лекарственному средству, и антивидовое обнаружение, представляет собой общий подход для моноклональный антител (mAb) в доклинических исследованиях (см., например, WO 2006/066912, WO 2008/031532, где оба документа включены в настоящее описание посредством ссылки);
- анализ прямого типа: обнаружение ПЛА, которые были связаны с лекарственным средством и/или с эндогенным аналогом путем использования иммобилизованного лекарственного средства и обнаружения антивидовой специфичности.
В одном воплощении изобретения для каждого анализа оценивают специфичную границу отделения фракции путем анализа чистых контрольных или точно предварительно дозированных образцов.
Для определения границы отделения фракции и для полуколичественного сравнения результатов между различными планшетами сигнал ELISA следует считывать после определенного времени (за которым в одном воплощении изобретения следят путем использования положительного контроля на микротитрационном планшете (МТП)).
Иммуноанализы хорошо известны специалистам в данной области техники. Способы выполнения, а также практические применения и методы таких анализов суммированы в соответствующих руководствах. Примерами соответствующих руководств являются следующие руководства: Tijssen, Р., Preparation of enzyme-antibody or other enzyme-macromolecule conjugates (in: "Practice and theory of enzyme immunoassays", Burdon, R.H. and v. Knippenberg, P.H. (eds.), Elsevier, Amsterdam (1990) pp. 221-278), а также различные тома "Methods in Enzymology", Colowick, S.P. and Caplan, N.O. (eds.), Academic Press, dealing with immunological detection methods, в частности, тома 70, 73, 74, 84, 92 и 121).
Принципы различных иммуноанализов раскрыты, например, в статье Hage, D.S., in Anal. Chem. 71 (1999) 294R-304R. Авторами Lu, В., et al., в статье Analyst. 121 (1996) 29R-32R описана ориентированная иммобилизация антител для использования в иммуноанализах. Иммуноанализы, опосредованные авидином-биотином, описаны, например, авторами Wilchek, М. and Bayer, Е.А., Methods Enzymol. 184 (1990) 467-469.
На второй стадии комплексы, разделенные по размеру, определяют на основании их композиции, например, подтверждают присутствие противолекарственных антител и определяют специфичность противолекарственных антител. В одном воплощении изобретения вторая стадия включает по меньшей мере один твердофазный иммуноферментный анализ (ELISA).
В целом ELISA включает иммобилизованную молекулу и меченую молекулу. Иммобилизованная молекула, как правило, иммобилизована/связана на твердой фазе. Меченая молекула, как правило, конъюгирована с детектируемой меткой, где детектируемая метка может представлять собой либо прямо детектируемую метку, либо косвенно детектируемую метку.
Для определения присутствия противолекарственного антитела можно использовать различные форматы ELISA:
- "Сэндвич" ELISA.
В одном воплощении изобретения лекарственное средство, конъюгированное с твердой фазой, используют в качестве иммобилизованной молекулы, а лекарственное средство, конъюгированное с детектируемой меткой, используют в качестве меченой молекулы.
При "сэндвич" ELISA противолекарственное антитело образует мостик между иммобилизованной молекулой и меченой молекулой за счет его бивалентной структуры. Данный формат анализа можно также назвать мостиковым ELISA.
Путем использования мостикового "сэндвич"-анализа ELISA можно обнаружить противолекарственные антитела. Обнаружение ПЛА во фракции ЭХ, охватывающей диапазон масс, отличающийся от его молекулярной массы (например, отличающийся от примерно 300 кДа для комплекса IgG-IgG), указывает на то, что ПЛА составляли часть комплекса более высокой молекулярной массы.
- ELISA комплексного типа.
В одном воплощении изобретения в качестве иммобилизованной молекулы используют антитело, специфичное к лекарственному средству, и в качестве меченой молекулы используют антитело антивидовой специфичности, конъюгированное с детектируемой меткой.
В одном воплощении изобретения в качестве иммобилизованной молекулы используют лекарственное средство, конъюгированное с твердой фазой, и в качестве меченой молекулы используют антитело антивидовой специфичности, конъюгированное с детектируемой меткой.
В одном воплощении изобретения в качестве иммобилизованной молекулы используют антитело антивидовой специфичности, конъюгированное с твердой фазой, и в качестве меченой молекулы используют лекарственное средство, конъюгированное с детектируемой меткой.
В одном воплощении изобретения антитело антивидовой специфичности, конъюгированное с твердой фазой, используют в качестве иммобилизованной молекулы, а антитело, специфичное к лекарственному средству, конъюгированное с детектируемой меткой, используют в качестве меченой молекулы.
В анализе ELISA комплексного типа можно обнаружить комплексы противолекарственное антитело-лекарственное средство.
При доклиническом анализе образца можно использовать иммобилизованное антитело, специфичное к лекарственному средству, и идентифицирующее антитело антивидовой специфичности.
При клиническом анализе образца можно использовать иммобилизованную молекулу, специфичную к лекарственному средству, такую как антиидиотипическое антитело, и идентифицирующее антитело антивидовой специфичности.
Данный анализ предоставляет информацию о том, связано ли ПЛА с лекарственным средством или не связано. Это достигается путем использования различных компонентов комплекса ПЛА-ЛС для иммобилизации комплекса (либо посредством взаимодействия с лекарственным средством, либо с противолекарственным антителом) и для обнаружения иммобилизованного комплекса (либо посредством специфичного взаимодействия с противолекарственным антителом в том случае, когда лекарственное средство использовано для иммобилизации комплекса, либо посредством специфичного взаимодействия с лекарственным средством в случае, когда противолекарственное антитело использовано для иммобилизации комплекса).
Поскольку противолекарственное антитело, как правило, представляет собой полноразмерное антитело, продуцируемое млекопитающим, которому было введено лекарственное средство, это противолекарственное антитело содержит константную область, специфичную для этого млекопитающего. Следовательно, антитела антивидовой специфичности можно использовать для специфичного связывания (иммобилизации или идентификации) противолекарственного антитела независимо от связывающей специфичности противолекарственного антитела, используя присутствие видоспецифичной константной области.
- ELISA прямого типа.
В одном воплощении изобретения лекарственное средство, конъюгированное с твердой фазой, используют в качестве иммобилизованной молекулы, и антитело антивидовой специфичности, конъюгированное с детектируемой меткой, используют в качестве меченой молекулы.
В одном воплощении изобретения эндогенный аналог лекарственного средства, конъюгированный с твердой фазой, используют в качестве иммобилизованной молекулы, и антитело антивидовой специфичности, конъюгированное с детектируемой меткой, используют в качестве меченой молекулы.
Путем использования анализа ELISA прямого типа, включающего иммобилизованный эндогенный аналог лекарственного средства и антивидовые антитела для идентификации противолекарственного антитела, можно обнаружить и определить, связывается ли ПЛА с лекарственным средством или с эндогенным аналогом. Кроме того, возможно определение изотипа антитела противолекарственного антитела путем использования видоспецифичных и подтипоспецифичных антител.
Оценку результатов выполняют как сигнал по отношению к размеру матрицы.
В одном воплощении изобретения образец инкубируют с иммобилизованной молекулой и/или с меченой молекулой в течение периода времени, составляющего от 16 часов до 32 часов.
Анализ ELISA мостикового типа представляет собой способ иммунологического определения иммунокомплекса лекарственного средства (ЛС) и антитела против лекарственного средства (противолекарственного антитела, ПЛА) в образце млекопитающего, используя иммуноанализ двойного мостикового связывания антигена.
Иммунокомплекс далее сокращен как комплекс ПЛА-ЛС.
В одном воплощении изобретения при иммунологическом определении комплекса ПЛА-ЛС в образце используют иммуноанализ двойного мостикового связывания антигена, включающий иммобилизованное антитело и меченое антитело, отличающийся тем, что одно из антител представляет собой антитело, специфично связывающееся с иммуноглобулином (Ig) млекопитающего, а другое антитело представляет собой антитело, специфично связывающееся с лекарственным средством.
В ходе определения образуется комплекс между антителом против Ig млекопитающего, комплексом ПЛА-ЛС и противолекарственным антителом, и количество образовавшегося комплекса соотносят с концентрацией комплекса ПЛА-ЛС, лекарственного средства и/или ПЛА.
В одном воплощении изобретения можно выполнять прямой анализ образца на обнаружение образовавшегося комплекса ПЛА-ЛС. В таком анализе положительные сигналы обнаруживают только в том случае, когда образец содержит и лекарственное средство, и противолекарственные антитела.
В одном воплощении изобретения анализ образца выполняют после предварительной инкубации образца с предопределенным количеством антитела к лекарственному средству. В таком анализе положительные сигналы обнаруживают, если образец содержит противолекарственные антитела, независимо от присутствия/отсутствия лекарственного средства в образце.
В одном воплощении изобретения конъюгация лекарственного средства с его партнером конъюгации происходит за счет химического связывания посредством N-концевых и/или е-аминогрупп (лизина), е-аминогрупп различных лизинов, карбоксильных, сульфгидрильных, гидроксильных и/или фенольных функциональных групп аминокислотного каркаса лекарственного средства и/или сахарных спиртовых групп углеводной структуры лекарственного средства.
В одном воплощении изобретения иммобилизованное антитело или лекарственное средство конъюгировано с твердой фазой за счет пассивной адсорбции, и, следовательно, конъюгировано с твердой фазой по меньшей мере в двух различных сайтах антитела. Пассивная адсорбция описана, например, в книгах Butler, J.E., in "Solid Phases in Immunoassay", page 205-225; Diamandis, E.P. and Christopoulos, Т.K. (Editors): Immunoassays (1996) Academic Press San Diego.
В одном воплощении иммобилизованное антитело или лекарственное средство иммобилизовано за счет специфичной связывающей пары. Такая связывающая пара (первый компонент/второй компонент) представляет собой, например, стрептавидин или авидин/биотин, антитело/антиген (см., например, кн. Hermanson, G.T., et al., Bioconjugate Techniques, Academic Press, 1996), лектин/полисахарид, стероид/стероидсвязывающий белок, гормон/рецептор гормона, фермент/субстрат, IgG/белок А и/или G и т.д. В одном воплощении изобретения иммобилизованное антитело или лекарственное средство конъюгировано с биотином, и иммобилизация происходит посредством иммобилизованного авидина или стрептавидина.
В одном воплощении изобретения меченое антитело конъюгировано с детектируемой меткой. В одном воплощении изобретения меченое антитело конъюгировано за счет специфичной связывающей пары. Такая связывающая пара (первый компонент/второй компонент) представляет собой, например, стрептавидин или авидин/биотин, антитело/антиген (см., например, кн. Hermanson, G.T., et al., Bioconjugate Techniques, Academic Press, 1996), лектин/полисахарид, стероид/стероидсвязывающий белок, гормон/рецептор гормона, фермент/субстрат, IgG/белок А и/или G и т.д. В одном воплощении изобретения меченое антитело конъюгировано посредством дигоксигенина и антитела против дигоксигенина с детектируемой меткой. Альтернативно меченое антитело конъюгировано с электрохемилюминесцентной меткой, такой как комплекс биспиридила рутения.
В одном воплощении изобретения способ предназначен для иммунологического определения антитела против лекарственного средства (противолекарственного антитела, ПЛА) в образце вида обезьян с использованием иммуноанализа двойного мостикового связывания антигена.
В одном воплощении изобретения способ предназначен для иммунологического определения ПЛА в образце млекопитающего с использованием иммуноанализа двойного мостикового связывания антигена, включающего иммобилизованную молекулу и меченую молекулу, отличающегося тем, что либо иммобилизованная молекула, либо меченая молекула представляет собой антитело, специфично связывающееся с IgG млекопитающего, а другая соответствующая молекула представляет собой лекарственное средство.
В одном воплощении изобретения иммунологического определения ПЛА иммобилизованная молекула представляет собой лекарственное средство, и меченая молекула представляет собой антитело против IgG млекопитающего, специфично связывающееся с IgG млекопитающего, от которого выделен/получен образец. В одном воплощении изобретения иммунологического определения ПЛА иммобилизованная молекула представляет собой антитело против IgG млекопитающего, специфично связывающееся с IgG млекопитающего, от которого выделен/получен образец, и меченая молекула представляет собой лекарственное средство. В ходе определения образуется комплекс между лекарственным средством, ПЛА и антителом против IgG млекопитающего, и количество этого образовавшегося комплекса соотносят с концентрацией ПЛА. В одном воплощении изобретения иммунологического определения ПЛА антитело против IgG млекопитающего представляет собой моноклональное антитело (mAb против IgG млекопитающего).
Полипептиды, такие как полипептидные лекарственные средства или лекарственные средства, представляющие собой антитела, содержат ряд химически активных группировок, таких как, например, аминогруппы (лизины, альфа-аминогруппы), тиольные группы (цистины, цистеин и метионин), карбоновокислотные группы (аспарагиновая кислота, глутаминовая кислота) и сахарно-спиртовые группы. Эти группы можно использовать для сочетания с партнером связывания, таким как поверхность, белок, полимер (такой как, например, полиэтиленгликоль (ПЭГ), целлюлоза или полистирол), фермент или член связывающей пары (см., например, Aslam М., and Dent, A., Bioconjuation MacMillan Ref. Ltd. (1999) 50-100).
Одной из наиболее распространенных химически активных групп полипептидов является алифатический е-амин аминокислоты лизина. Как правило, почти все полипептиды содержат часто встречающийся лизин. Амины лизина являются достаточно хорошими нуклеофилами, имеющими значение рН выше 8,0 (pKa=9,18), и, следовательно, легко и чисто взаимодействуют с различными реагентами с образованием стабильных связей. Другой распространенной химически активной группой в полипептидах является тиольный остаток серосодержащей аминокислоты цистина и его восстановленного продукта цистеина (или полуцистина). Цистеин содержит свободную тиольную группу, которая обладает большей нуклеофильностью, чем амины, и, как правило, является наиболее химически активной функциональной группой в белке. Тиолы в целом химически активны при нейтральном значении рН, и, следовательно, могут селективно подвергаться сочетанию с другими молекулами в присутствии аминов. Поскольку свободные сульфгидрильные группы относительно химически активны, в полипептидах, содержащих эти группы, они часто существуют в их окисленной форме в виде дисульфидных групп или дисульфидных связей. В дополнение к цистину и цистеину некоторые полипептиды также имеют аминокислоту метионин, содержащий серу в тиоэфирной связи. В литературе описано использование нескольких тиолатирующих сшивающих реагентов, таких как реагент Трота (2-иминотиолан), сукцинимидил(ацетиотио)ацетат (SATA; от англ. "succinimidyl (acetylthio) acetate") или сульфосукцинимидил-6-[3-(2-пиридилдитио)пропионамидо]гексаноат (Sulfo-LC-SPDP; от англ. "sulfosuccinimidyl 6-[3-(2-pyridyldithio) propionamido] hexanoate"), чтобы обеспечить эффективные пути введения множественных сульфгидрильных групп посредством химически активных аминогрупп. Химически активные сложные эфиры, в частности, N-гидроксисукцинимидные (NHS; от англ. "N-hydroxysuccinimide") эфиры, находятся среди чаще всего используемых реагентов для модификации аминных групп. Оптимум рН для взаимодействия в водной среде составляет рН от 8,0 до 9,0. Изотиоцианаты являются аминмодифицирующими реагентами и образуют тиомочевинные связи с белками. Они взаимодействуют с аминами полипептидов в водном растворе (оптимально при рН от 9,0 до 9,5). Альдегиды взаимодействуют в мягких водных условиях с алифатическими и ароматическими аминами, гидразинами и гидразинами с образованием иминного промежуточного соединения (Шиффова основания). Шиффово основание может быть селективно восстановлено слабыми или сильными восстанавливающими агентами (такими как боргидрид натрия или цианборгидрид натрия) с образованием стабильной алкиламинной связи. Другими реагентами, использованными для модификации аминов, являются ангидриды кислот. Например, диэтилентриаминпентауксусный ангидрид (DTPA; от англ. "diethylenetriaminepentaacetic anhydride") является бифункциональным хелатирующим агентом, содержащим две ангидридные группы, взаимодействующие с аминами. Он может взаимодействовать с N-концевыми и е-аминогруппами белков с образованием амидных связей. Ангидридные кольца размыкаются с образованием мультивалентных плеч, хелатирующих металл, способных прочно связываться с металлом в координационный комплекс.
Другой распространенной химически активной группой в полипептидах являются карбоновые кислоты (аспарагиновая кислота, глутаминовая кислота). Полипептиды содержат карбоновокислотные группы в С-концевом положении и внутри боковых цепей аспарагиновой кислоты и глутаминовой кислоты. Для конъюгации карбоновокислотную группу обычно преобразуют в химически активный сложный эфир путем использования растворимого в воде карбодиимида и подвергают взаимодействию с нуклеофильным реагентом, таким как амин, гидразид или гидразин. Аминсодержащий реагент должен быть слабоосновным, чтобы селективно взаимодействовать с активированной карбоновой кислотой в присутствии других аминов на полипептиде. Сшивание полипептида может происходить, когда рН поднимается выше 8,0.
Периодат натрия можно использовать для окисления спиртовой части сахара в пределах углеводной группировки до альдегида. Каждая альдегидная группа может взаимодействовать с амином, гидразидом или гидразином, как описано для карбоновых кислот.
Тиолоактивные реагенты представляют собой реагенты, сочетающиеся с тиольными группами на полипептидах с образованием продуктов, связанных тиоэфирной связью. Эти реагенты взаимодействуют быстро при значении рН от слабокислого до нейтрального, и, следовательно, могут взаимодействовать селективно в присутствии аминогрупп. Производные галогенацетила, например, йодацетамиды, образуют тиоэфирные связи и являются реагентами для модификации тиола. Реакция происходит на цистеиновых группах, которые либо присутствуют сами по себе, либо являются результатом восстановления дисульфидов в различных положениях полипептида. Следующими полезными реагентами являются малеимиды. Взаимодействие малеимидов с тиолоактивными реагентами является по существу таким же, как с йодацетамидами. Малеимиды взаимодействуют быстро при значении рН от слабокислого до нейтрального.
Амины, гидразиды и гидразины являются реагентами, взаимодействующими с альдегидами и карбоновыми кислотами (образование амидных, гидразоновых или алкиламинных связей). Амины, гидразиды и гидразины можно подвергать сочетанию с карбоновыми кислотами полипептидов после активации карбоксильной группы растворимым в воде карбодиимидом. Аминсодержащий реагент должен быть слабоосновным, чтобы селективно взаимодействовать с карбодиимид-активированным полипептидом в присутствии более высокоосновных е-аминов лизина с образованием стабильной амидной связи. При взаимодействии с альдегидными группами, которые могут быть образованы на полипептидах путем периодатного окисления углеводных остатков на полипептиде, образуется промежуточное Шиффово основание, которое может быть восстановлено до алкиламина посредством взаимодействия этого промежуточного соединения со следующими растворимыми в воде восстанавливающими агентами: цианборгидридом натрия (слабым и селективным) или боргидридом натрия (сильным).
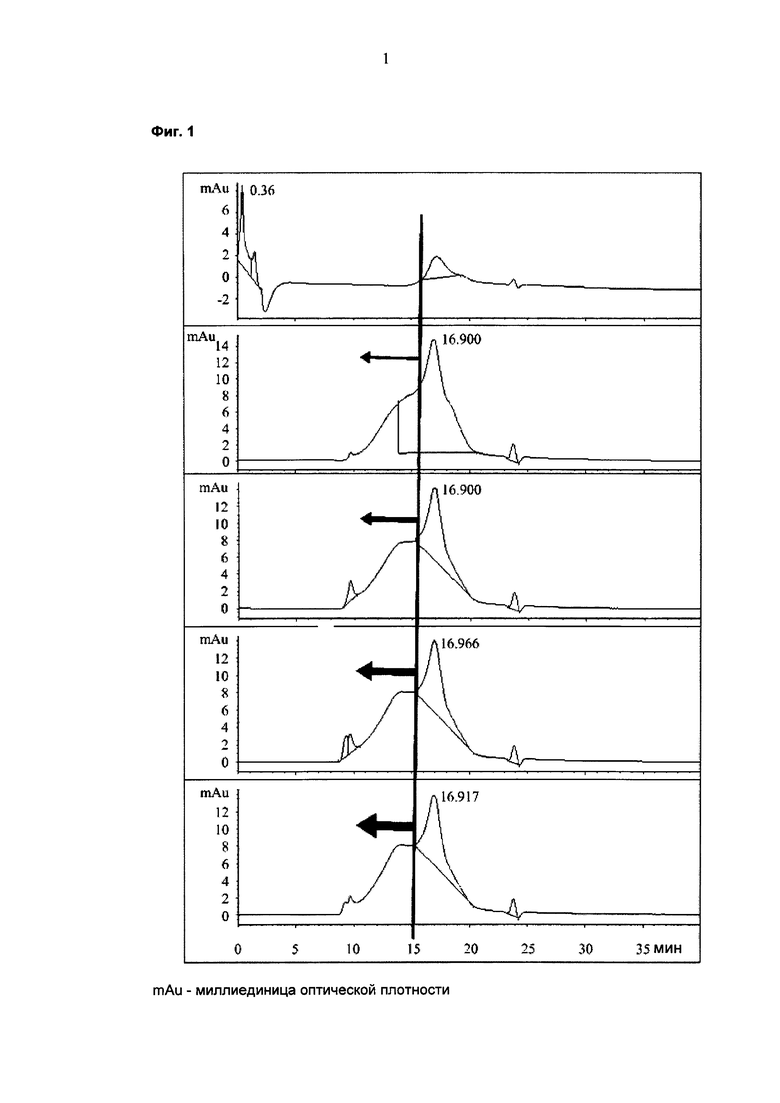
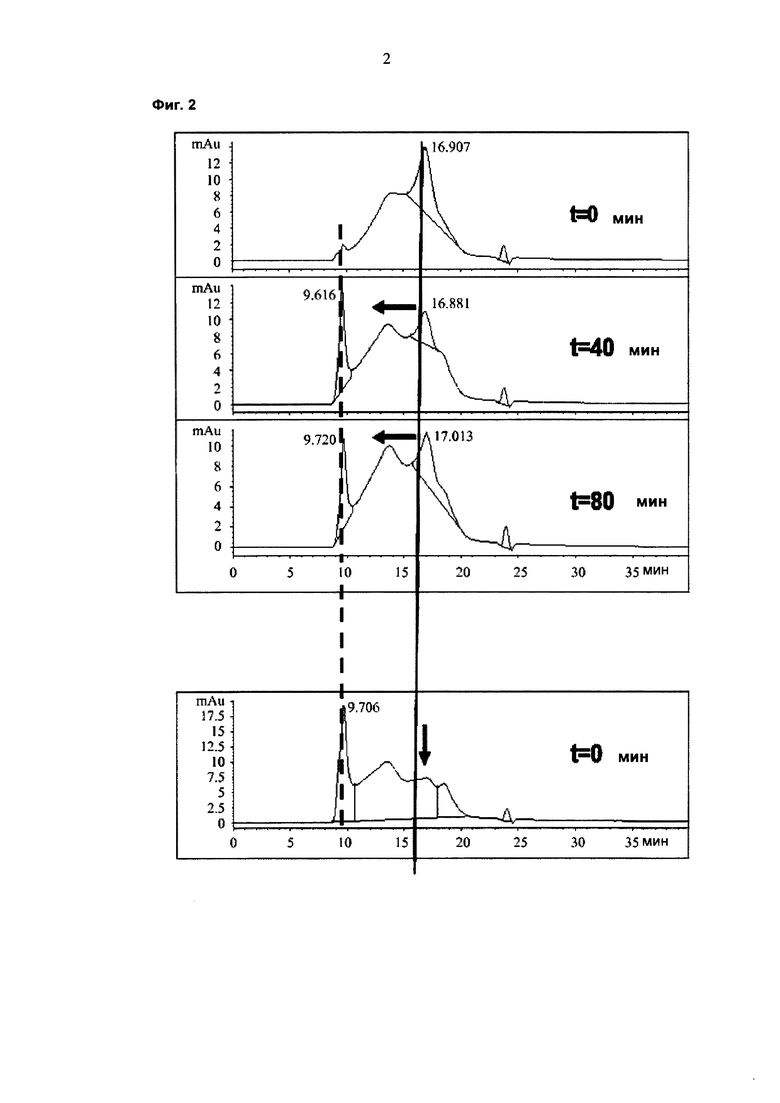
На фиг. 1 показана кинетика образования комплекса лекарственного средства ПЛА-ЛС (1 мг лекарственного средства и 1 мг ПЛА). Видно, что с увеличением времени образуются комплексы более высокого порядка, например, начиная с комплекса 1:1 лекарственное средство: ПЛА через комплекс 1:2 лекарственное средство: ПЛА до комплекса 1:3 лекарственное средство:ПЛА (моменты времени:0 мин, 50 мин, 100 мин, 160 мин, 200 мин). В результате добавления дополнительного количества ПЛА композиция образца может быть сдвинута дальше до более высокомолекулярных комплексов с уменьшением пика мономерного лекарственного средства (фиг. 2).
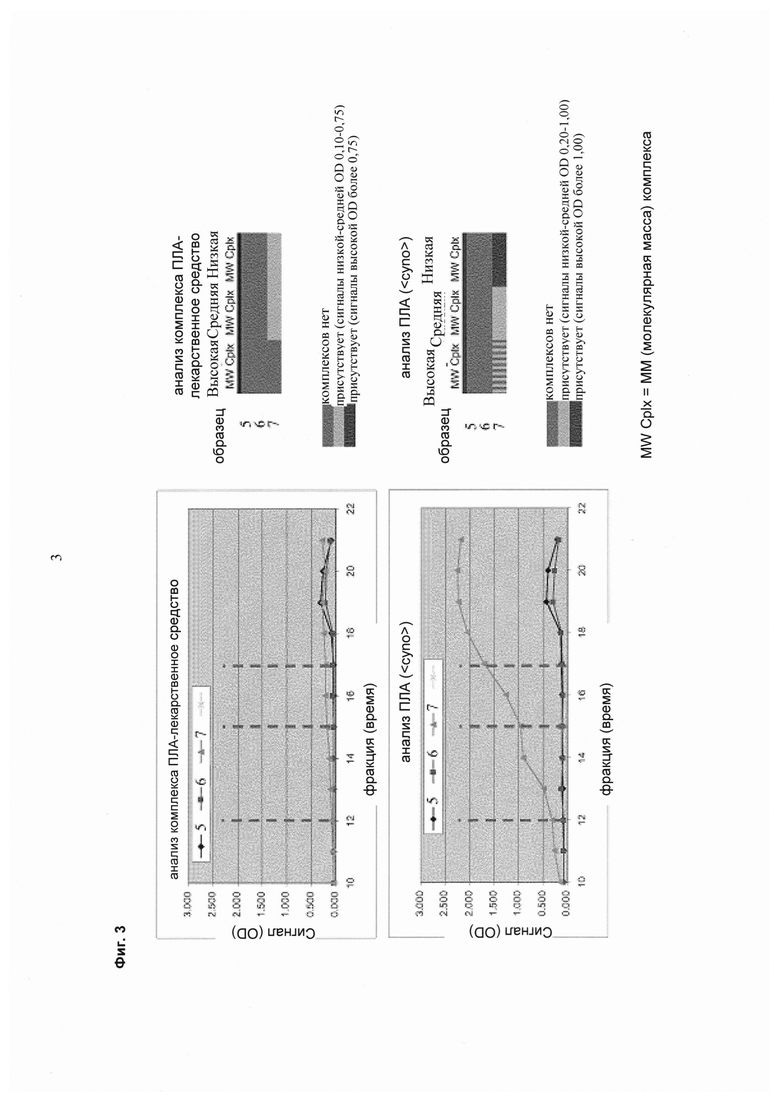
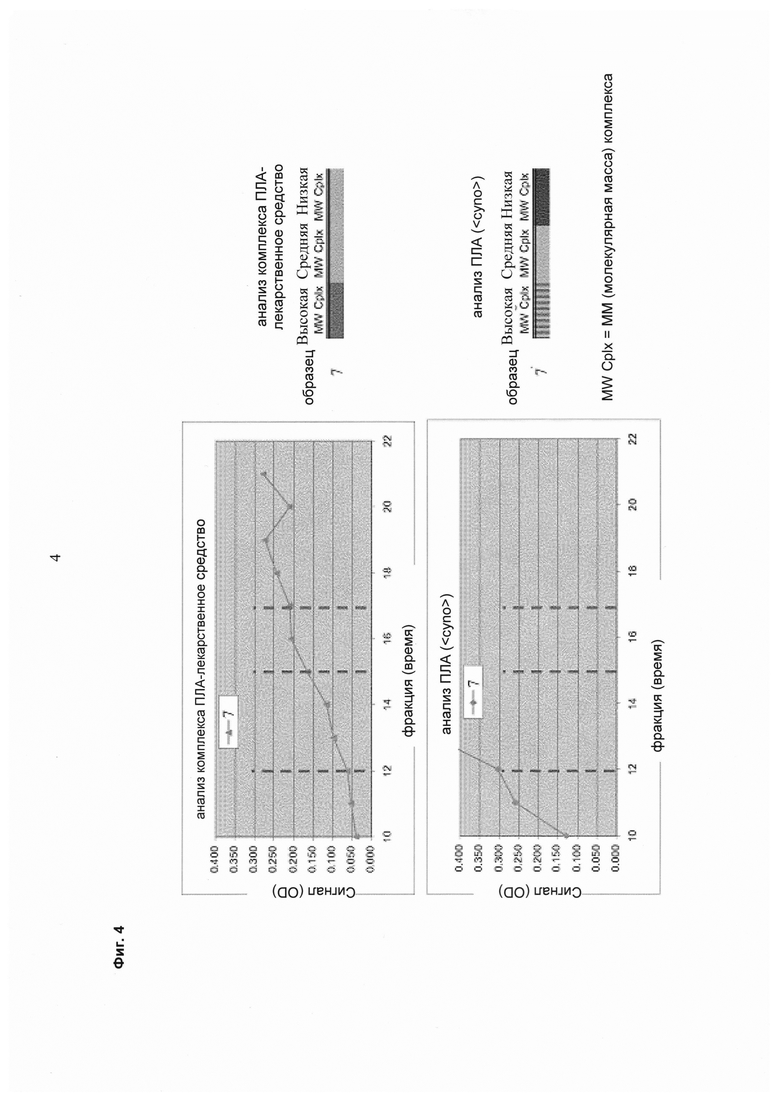
На фиг. 3 показаны иллюстративные преобразованные диаграммы ЭХ (ось Y представляет собой оптическую плотность (OD) ELISA) и результаты ELISA, полученные способом, раскрытым в данном изобретении. На фиг. 4 показано увеличение преобразованной ЭХ образца 201, где ось Y поддерживают постоянной. Таким образом, видно различие в композиции образца.
В данном описании использованы следующие сокращения:
ABTS 2,2'-Азино-ди-[3-этилбензтиазолинсульфонат(6)]диаммоний (от
англ. "2,2'-Azino-di-[3-ethylbenzthiazoline sulfonate (6)] di-ammonium")
Ab Антитело (от англ. "Antibody")
ПЛА Противолекарственные антитела
Bi Биотин
СоА Сертификат анализа (от англ. "Certificate of Analysis")
Конц. Концентрация
СРР Смешанная контрольная плазма яванских макак (от англ. "Cynomdgus monkey pooled blank plasma")
Разв. Разведение
ELISA Твердофазный иммуноферментный анализ
HRP Пероксидаза хрена (от англ. "horseradish peroxidase")
mAb Моноклональное антитело (от англ. "Monoclonal antibody")
МТП Микротитрационный планшет
OD Оптическая плотность (от англ. "Optical density")
ФСБ Фосфатно-солевой буферный раствор
Об/мин Обороты в минуту
КТ Комнатная температура (от+15 до+25°С)
ГУ Готовый к употреблению
СА Стрептавидин
ЭХ Эксклюзионная хроматография.
Приведенные ниже примеры предложены, чтобы помочь пониманию настоящего изобретения, действительный объем которого изложен в прилагаемой формуле изобретения. Понятно, что в описанных ниже методах могут быть произведены модификации без отклонения от сущности изобретения.
ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Фиг. 1. Кинетика образования комплекса лекарственного средства ПЛА-ЛС (1 мг лекарственного средства и 1 мг ПЛА).
Фиг. 2. Кинетика, как показано на фиг.1, с дополнительным добавлением ПЛА.
Фиг. 3. Иллюстративные преобразованные диаграммы ЭХ и результаты ELISA, полученные способом, раскрытом в данном изобретении.
Фиг. 4. Увеличение преобразованной ЭХ, как показано на фиг. 3.
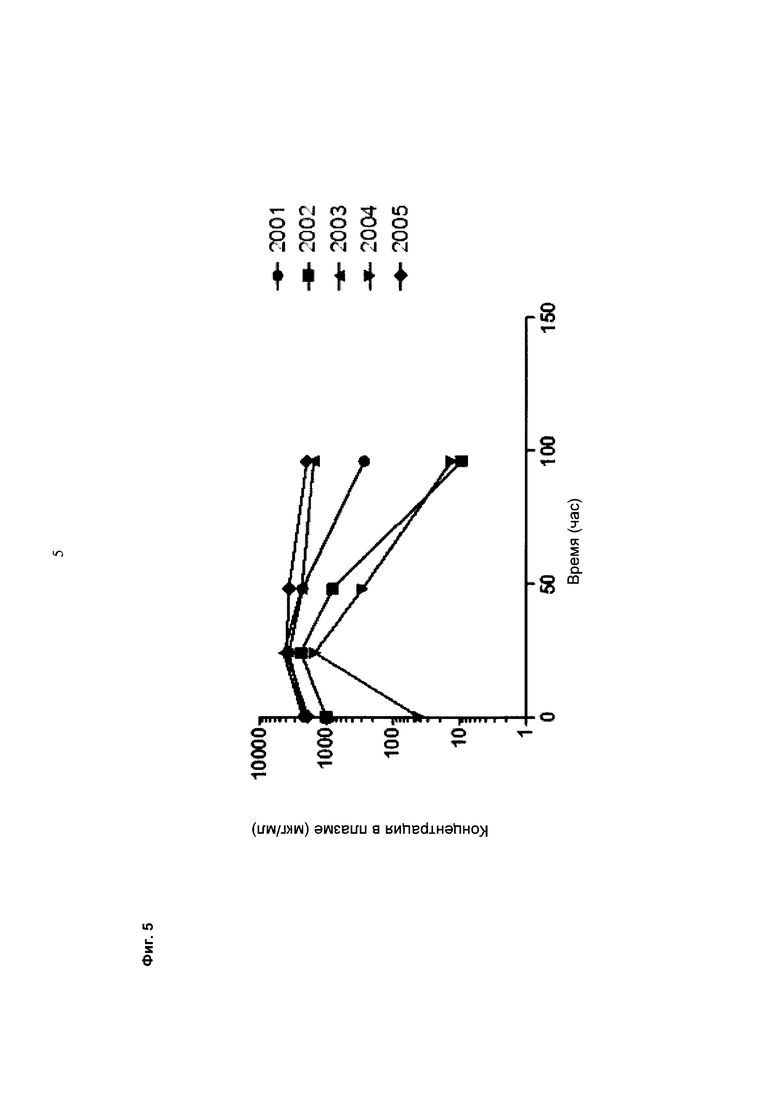
Фиг. 5. Изменение концентрации применяемого лекарственного средства в плазме пяти обезьян (доза=100 мг/кг, повторное применение, применено на сутки 17 исследования).
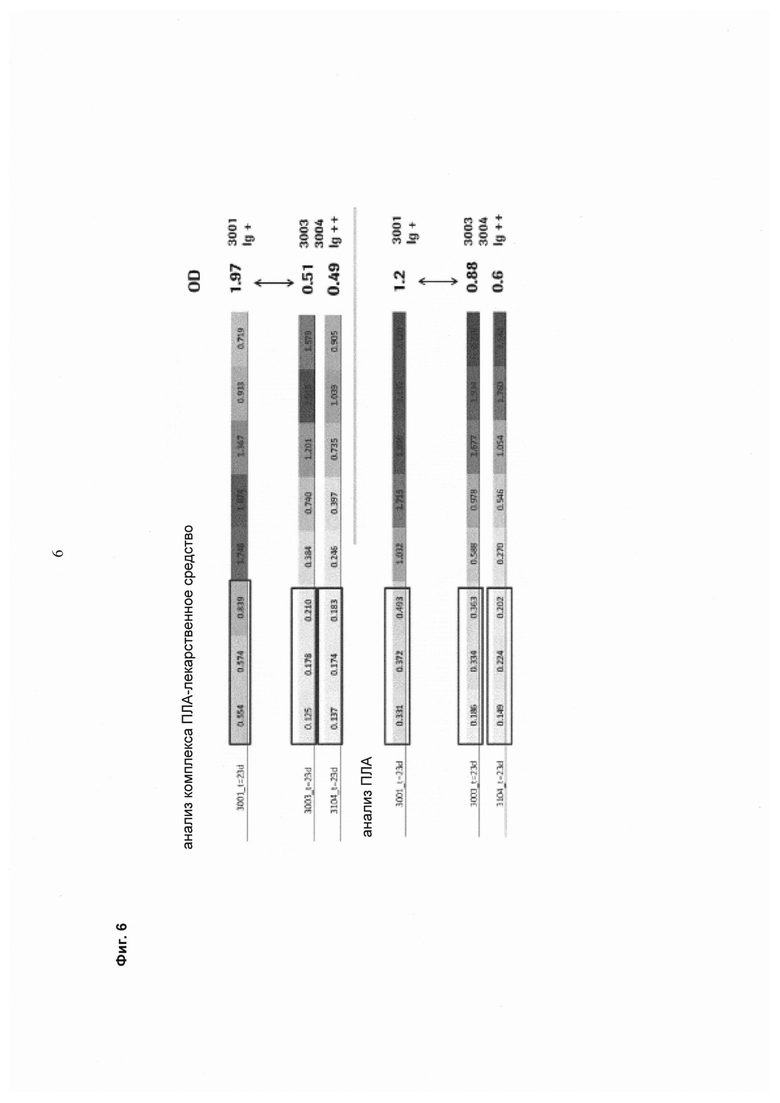
Фиг. 6. Животные с положительным отложением IgG (полуколичественная оценка).
Пример 1
Анализ образцов исследования на яванских макаках
Двадцать семь образцов плазмы, полученных из исследования на яванских макаках, было проанализировано на обнаружение комплексов, содержащих противолекарственные антитела (ПЛА) против введенного лекарственного средства. Кроме того, была проведена оценка размеров комплексов.
Анализ выполняли с использованием двухступенчатого способа, включающего эксклюзионную хроматографию (ЭХ) и твердофазный иммуноферментный анализ (ELISA).
Разделение потенциальных комплексов по размеру было достигнуто с помощью ЭХ с последующим фракционированием элюата ЭХ (1 мин фракции), что обеспечивает мультиплексирование анализа ЭХ, поскольку каждую фракцию можно проанализировать с помощью различных анализов ELISA. Обнаружение ПЛА против введенного лекарственного средства и обнаружение присутствия комплексов ПЛА-ЛС в собранных фракциях было достигнуто с помощью двух различных анализов ELISA. Один из них предназначен для обнаружения ПЛА (определение ПЛА) путем использования биотинилированного лекарственного средства для иммобилизации и идентифицирующего антитела, специфичного против IgG яванского макака, второй анализ предназначен для обнаружения комплексов ПЛА-ЛС путем использования иммобилизованной молекулы, специфичной к лекарственному средству, и идентифицирующего антитела, специфичного против IgG яванского макака.
Образцы плазмы собирали у животных основной группы и группы восстановления. Группа 1: Группа плацебо (образцы 01, 02, 03, 04, 05, 06), группа 2: базовая доза (образцы 07, 08, 09, 10, 11, 12), группа 3: двухкратная базовая доза (образцы 13, 14, 15, 16, 17, 18), группа 4: четырехкратная базовая доза (образцы 19, 20, 21, 22, 23, 24, 25, 26, 27).
Выбор времени фракционирования определяет информацию о разделении по размеру. Размер фракции составлял 1 мин. Результаты анализа ELISA нескольких фракций объединяли, чтобы сконцентрировать информацию до "фракций высокой, средней и низкой молекулярной массы".
Эксклюзионная хроматография (ЭХ):
Образцы плазмы яванских макак разделяли на колонке ЭХ BioSuite 450, 13 мкм с диапазоном молекулярной массы от примерно 20000 до примерно 7000000 Да. Во избежание нежелательного осаждения белков на вершине колонки плазму яванских макак смешивали с этанолом (сравнимым с композицией этанола подвижной фазы) с последующим центрифугированием в течение 1 мин (отношение плазма яванских макак: этанол (95 масс.%) примерно 16:1; 1 мин центрифугирование при 20800 д). Образец 20 мкл впрыскивали на систему высокоэффективной жидкостной хроматографии (ВЭЖХ) (Agilent 1100). Мониторинг записи в канале УФ проводили при длине волны 280 нм. Изократическое разделение проводили в 5% этаноле в фосфатно-солевом буферном растворе (ФСБ) в качестве подвижной фазы (скорость тока 0,5 мл/мин в течение 25 мин, а затем 0,75 мл/мин в течение 13 минут и 0,5 мл/мин в течение последних 2 минут).
Элюат разделения ЭХ фракционировали, чтобы обеспечить обнаружение с помощью ELISA. В одном воплощении изобретения собирали двадцать последовательных фракций с периодом фракции 1 мин, охватывая время элюирования от 9 мин (объем пустот колонки) до 21 мин.
Вычисленная молекулярная масса, относящаяся к соответствующей фракции, приведена в следующей таблице.
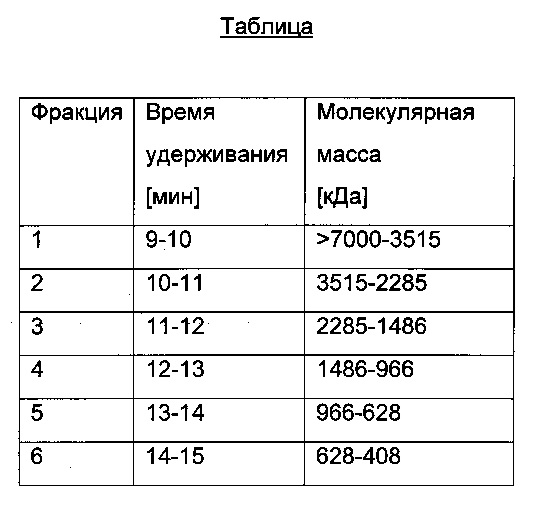
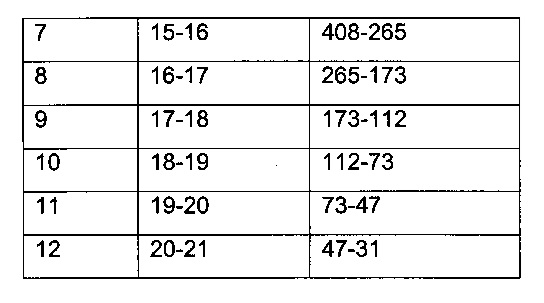
Анализы ПЛА
Обнаружение ПЛА во фракциях ЭХ более высокой молекулярной массы (более 150 кДа, что эквивалентно массе мономера IgG/ПЛА) указывает на то, что ПЛА составляло часть комплекса более высокой молекулярной массы. Обнаружение ПЛА выполняют путем анализа собранной фракции с использованием анализа на ПЛА. Определение размера комплекса основано на времени удерживания ЭХ. Определение композиции комплекса достигается путем анализа присутствия комплексов ПЛА-ЛС (комплексов ПЛА-Лекарственное средство) в соответствующих фракциях.
Для обнаружения комплексов ПЛА и ПЛА-ЛС установлено два последовательных способа ELISA.
Для обнаружения ПЛА лунки микротитрационного планшета, покрытого стрептавидином (СА-МТП), покрывают биотинилированным лекарственным средством (D-Bi (от англ. drug-biotin; с=1 мкг/мл) в течение 1 часа. После того, как покрывающий раствор удален, лунки промывают три раза 1хФСБ, содержащим 0,05% Твин 20, добавляют аликвоту фракции ЭХ и инкубируют в МТП в течение ночи при встряхивании. После отмывки лунок три раза 1хФСБ с 0,05% Твин 20 добавляют дигоксигенилированное антитело против Fc яванского макака (<Cyno Fc>-Dig (от англ. Cynomolgus Fc - digoxygenin, с=0,1 мкг/мл) и инкубируют в течение одного часа при встряхивании. После отмывки лунок три раза 1×ФСБ с 0,05% Твин 20 добавляют (поли) Fab фрагменты антитела против дигоксигенина, конъюгированные с пероксидазой хрена (HRP) (5 мЕд.) и инкубируют в течение одного часа при встряхивании. После отмывки лунок три раза 1×ФСБ с 0,05% Твин 20 добавляют раствор ABTS и следят за развитием окрашивания (длина волны измерения 405 нм; референсная длина волны 490 нм).
Для обнаружения комплекса ПЛА-ЛС лунки СА-МТП покрывают биотинилированным противолекарственным антителом (<drug>-Bi; с=2 мкг/мл) в течение 1 часа при встряхивании. После того, как покрывающий раствор удален, лунки промывают три раза 1хФСБ, содержащим 0,05% Твин 20, добавляют аликвоту фракции ЭХ и инкубируют в МТП в течение часа при встряхивании для обнаружения комплекса. После того, как раствор удален, лунки промывают три раза 1хФСБ, содержащим 0,05% Твин 20, добавляют раствор дигоксигенилированное антитело против Fc яванского макака (<Cyno Fc>-Dig) (с=0,1 мкг/мл) и инкубируют в течение одного часа при встряхивании. После того, как раствор удален, лунки промывают три раза 1хФСБ, содержащим 0,05% Твин 20, и добавляют раствор (поли) Fab фрагментов антитела против дигоксигенина, конъюгированных с HRP (5 мЕд.) и инкубируют в течение одного часа при встряхивании. После отмывки лунок три раза 1хФСБ с 0,05% Твин 20 добавляют раствор ABTS и следят за развитием окрашивания (длина волны измерения 405 нм; референсная длина волны 490 нм).
Предельное значение на основании оптической плотности (OD) сигнала, выше которого результат для фракции ЭХ определяют как положительный по присутствию ПЛА (анализ ПЛА) или комплексов ПЛА-ЛС (анализ ПЛА-ЛС), было определено на основании анализа образцов плацебо исследования.
Результаты анализа ПЛА и анализа ПЛА-ЛС представлены в приведенной ниже таблице (результаты ELISA перечислены в виде значений OD анализа фракций образцов плацебо (верхняя часть: анализ ПЛА; нижняя часть: анализ ПЛА-ЛС)).
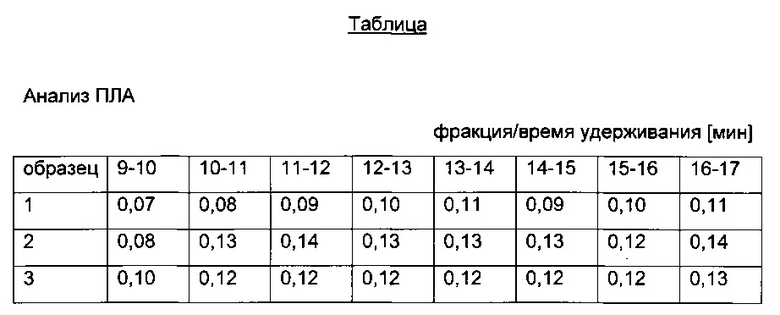
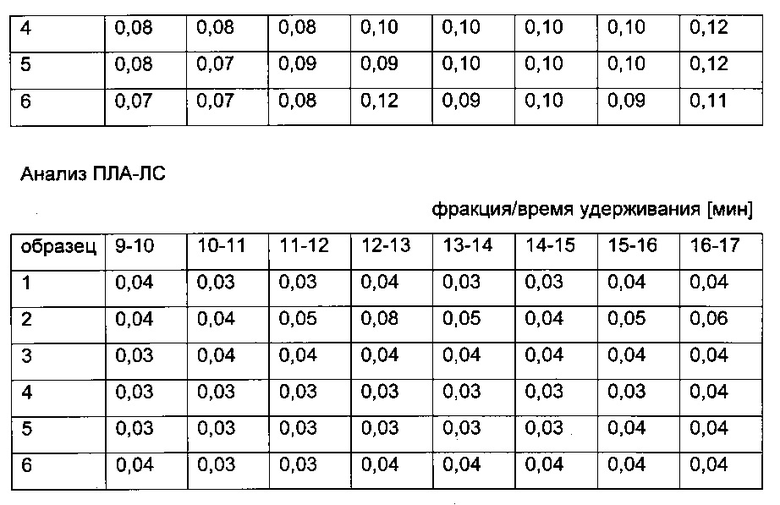
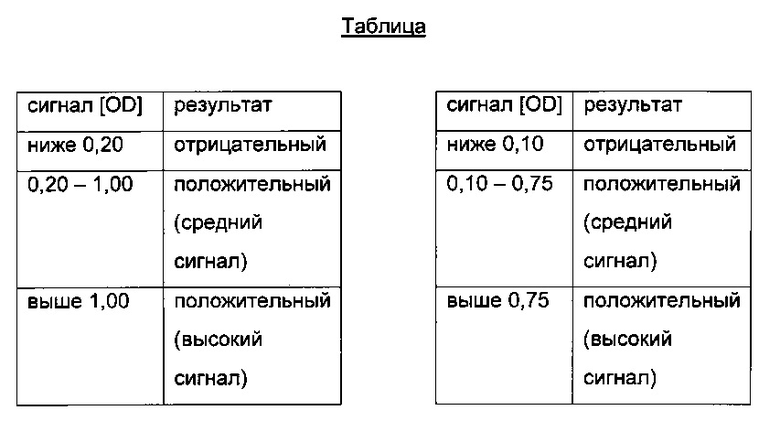
На основании этих данных предельное значение OD было определено для анализа ПЛА как составляющее не менее 0,20, а для анализа ПЛА-ЛС как значение OD, составляющее не менее 0,10, где данные значения представляют собой примерно двукратный средний контрольный сигнал в анализируемых фракциях.
Для дополнительной полуколичественной оценки были определены значения, приведенные в следующей таблице (предельные значения (OD) для анализа ПЛА (слева) и для анализа ПЛА-ЛС (справа)).
Двадцать семь образцов плазмы яванских макак, полученных из исследования, было проанализировано на обнаружение комплексов, содержащих противолекарственные антитела (ПЛА) против введенного лекарственного средства. Кроме того, была проведена оценка размеров комплексов.
Результаты для фракций 1-3 объединены и приведены как фракция комплексов высокой молекулярной массы, для фракций 4-6 как фракция комплексов средней молекулярной массы и для фракций 7-8 как фракция комплексов низкой молекулярной массы. Обзор результатов ELISA анализа фракций образцов исследования приведен в следующей таблице (слева: анализ ПЛА; справа: анализ ПЛА-ЛС; группа 1 представляет собой группу плацебо; группа 2 базовая доза; группа 3 двухкратная базовая доза; группа 4 четырехкратная базовая доза).
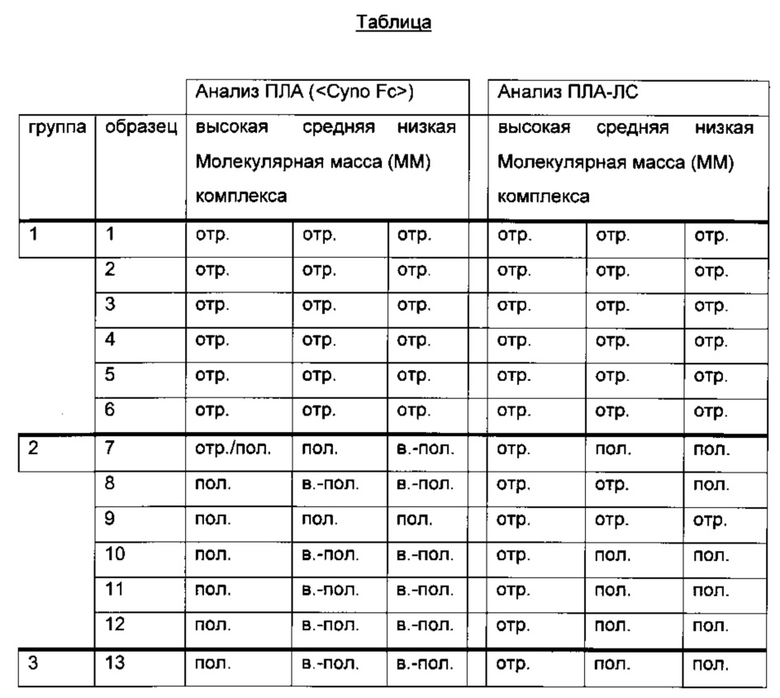
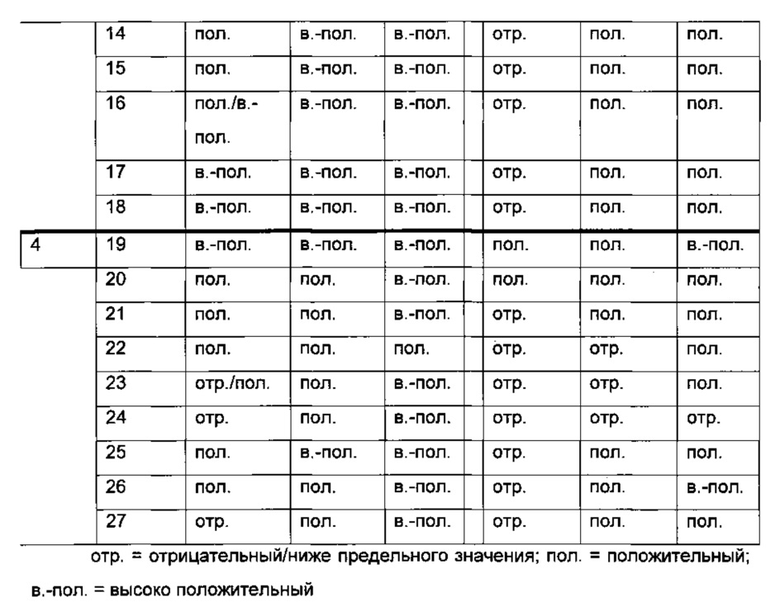
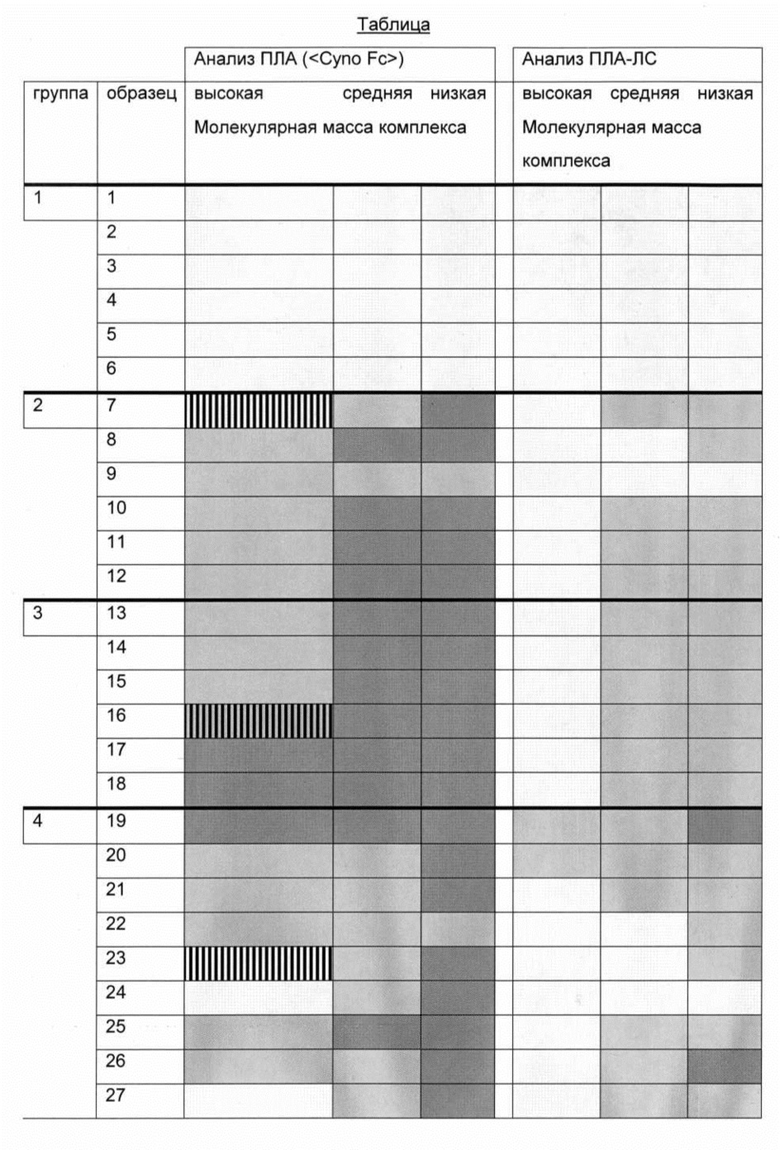

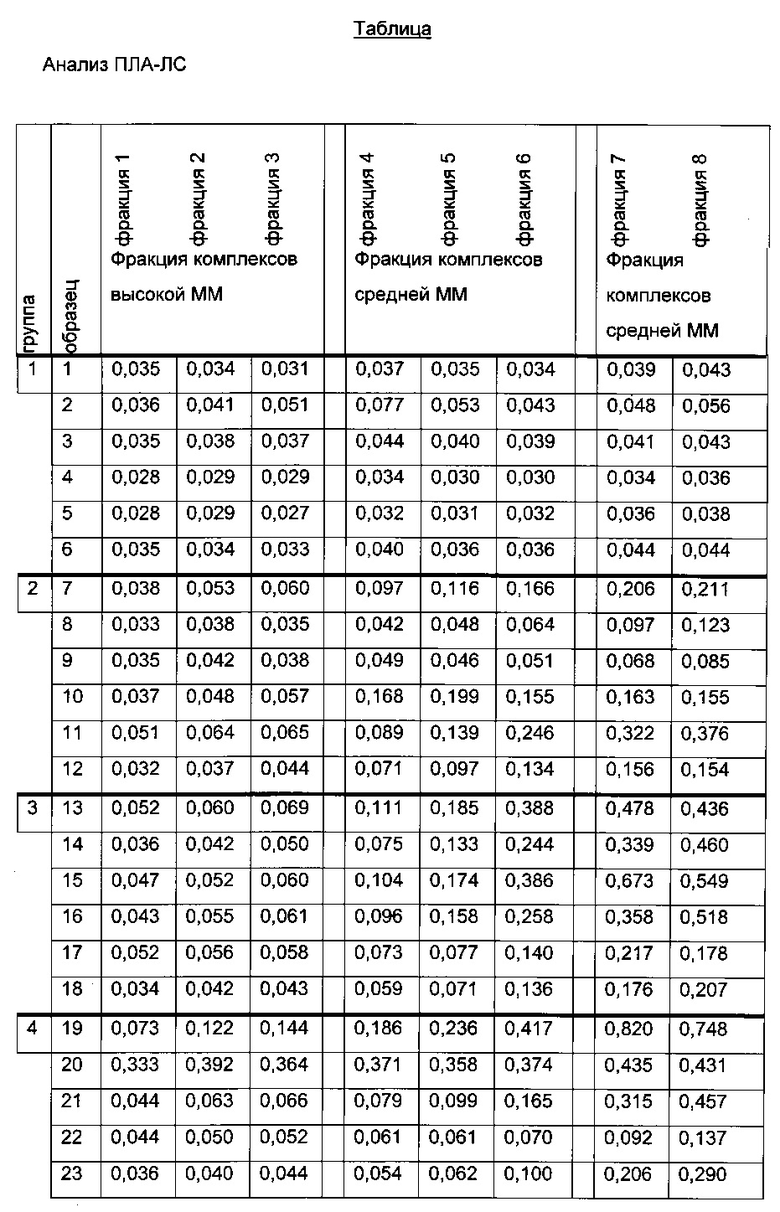
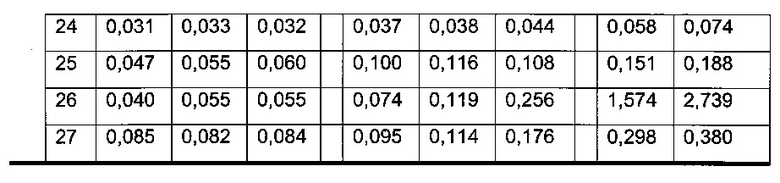
Подробные результаты анализа ELISA фракций образцов исследования, как показано в предыдущей Таблице, приведены в следующей таблице (верхняя часть: анализ ПЛА; нижняя часть: анализ ПЛА-ЛС; группа 1 представляет собой группу плацебо; группа 2 базовая доза; группа 3 двухкратная базовая доза; группа 4 четырехкратная базовая доза).
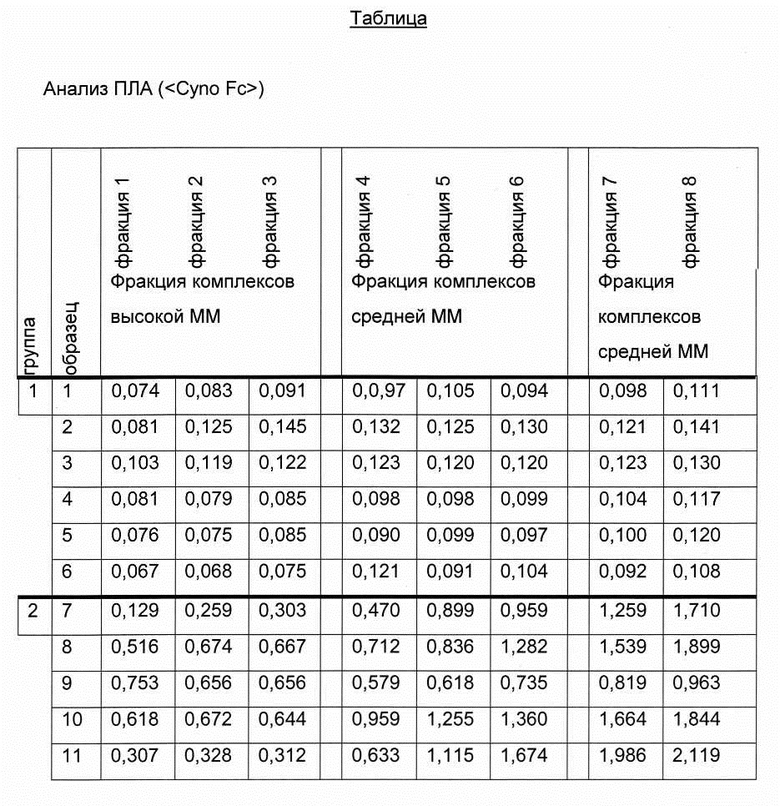
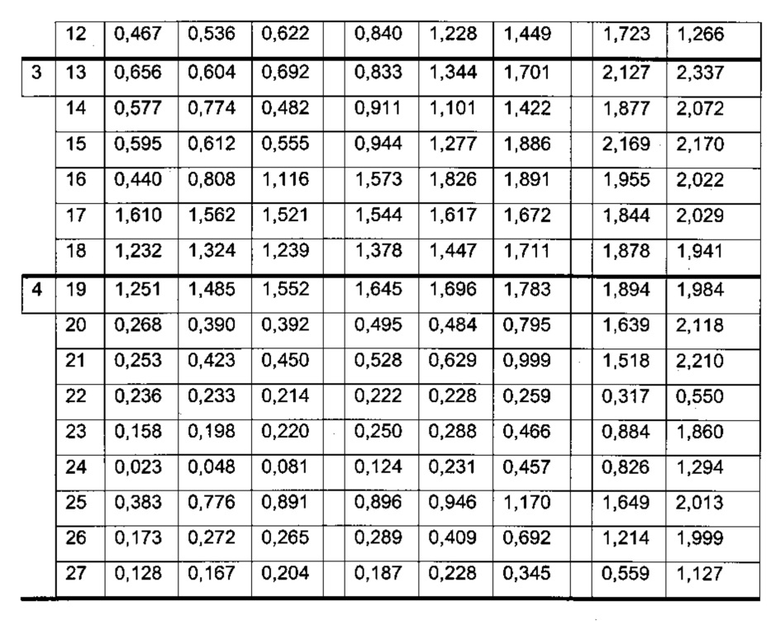
ПЛА против лекарственного средства могут быть обнаружены во всех анализируемых образцах обработанных животных (группа 2-4). Различия между образцами наблюдают в отношении интенсивности сигнала, а также в отношении положительного сигнала во фракциях высокой молекулярной массы. Отрицательные результаты наблюдали в некоторых фракциях следующих образцов: образец 7/фракция 1; образец 23/фракция 1-2, образец 24/фракция 1-4; образец 26/фракция 1; образец 27/фракция 1-3.
Комплексы ПЛА-ЛС могут быть обнаружены во всех, кроме двух образцов (образцы 10, 24) обработанных животных. Различия между образцами наблюдают в отношении интенсивности сигнала. За исключением образца 19 и образца 20 все образцы показали отрицательные результаты во фракциях высокой молекулярной массы (фракции 1-3).
Пример 2
Корреляция анализа ЭХ-ELISA и фармакокинетики Пять образцов плазмы яванских макак собирали перед дозированием и в последующие моменты времени, сутки = 9, 13, 21, 23 (все образцы) и на сутки = 63 (животное 2004, 2005, 3002, 3105) и анализировали на обнаружение комплексов, содержащих противолекарственные антитела (ПЛА) против введенного лекарственного средства. Кроме того, была проведена оценка размеров комплексов с наблюдаемой фармакокинетикой введенного лекарственного средства.
Анализ проводили, используя двухступенчатый способ, включающий эксклюзионную хроматографию (ЭХ) и твердофазный иммуноферментный анализ (анализ ПЛА-ЛС и анализ ПЛА), как описано в Примере 1. Для соотнесения с фармакокинетикой введенного лекарственного средства использовали только результаты анализа ПЛА-ЛС.
Образцы плазмы яванских макак собирали от пяти яванских макак с дозированием лекарственного средства 100 мг/кг.
Из анализа плазмы видно, что у яванских макак номер 2001, 2002 и 2004 можно наблюдать более быстрый сывороточный клиренс по сравнению с яванскими макаками номер 2003 и 2005 (см. фиг. 5).
Элюент разделения ЭХ фракционировали при времени фракции 1 мин, охватывающем время элюирования от 9 мин (объем пустот колонки) до 21 мин. Вычисленную молекулярную массу, относящуюся к соответствующей фракции, используют, как описано в Примере 1 выше.
Предельное значение на основании оптической плотности (OD) сигнала, выше которого результат для фракции ЭХ определяют как положительный по присутствию ПЛА (анализ ПЛА) или комплексов ПЛА-ЛС (анализ ПЛА-ЛС), было определено на основании анализа образцов от исследуемых животных перед дозированием.
Результаты анализа ПЛА и анализа ПЛА-ЛС представлены в следующей таблице (результаты ELISA перечислены как значения OD анализа фракций образцов плацебо (верхняя часть: анализ ПЛА; нижняя часть: анализ ПЛА-ЛС)).
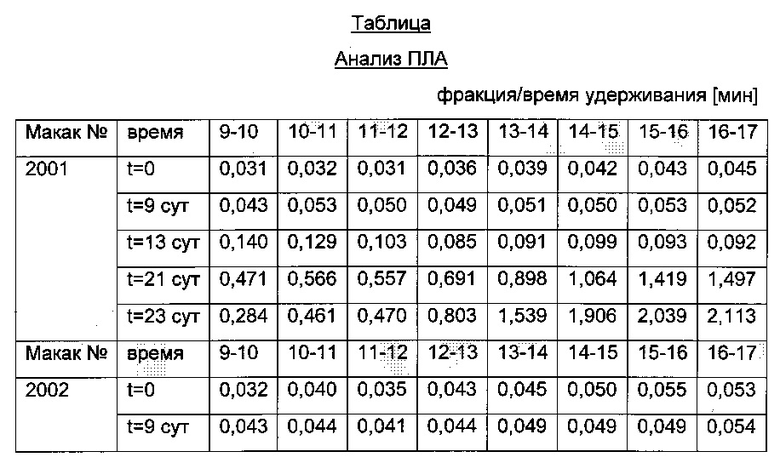
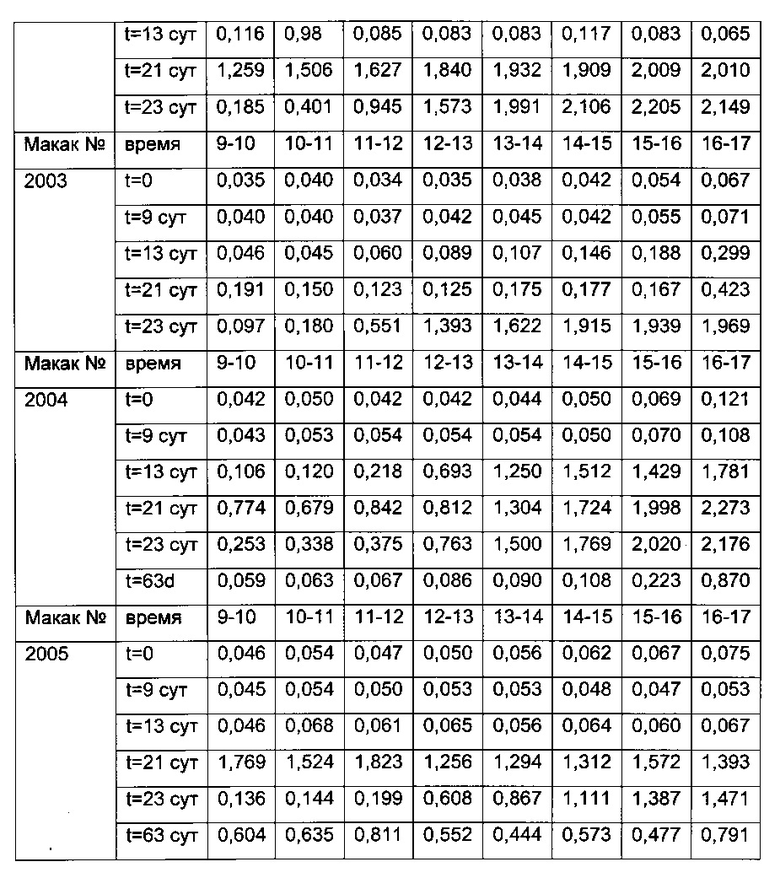
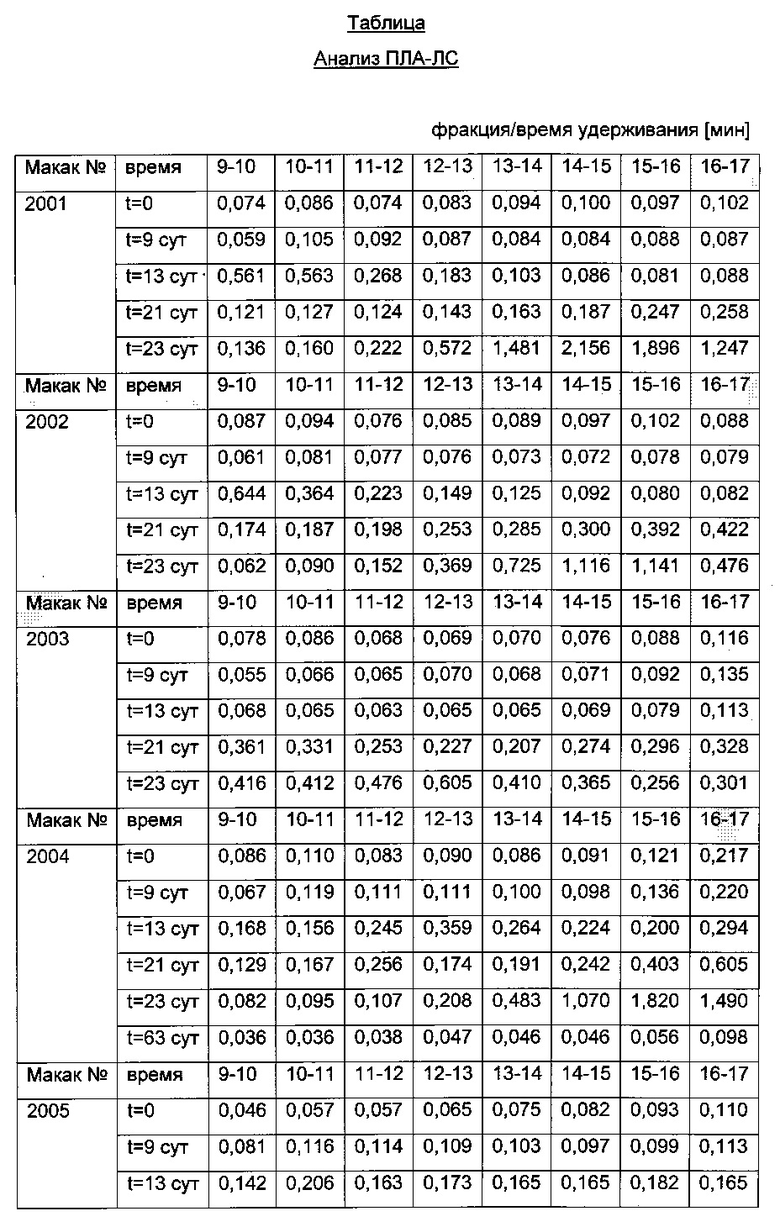
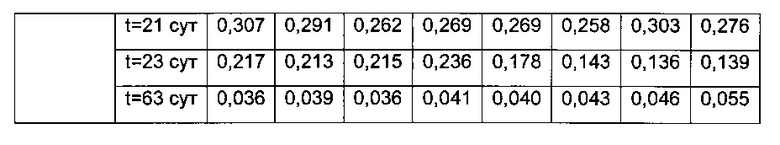
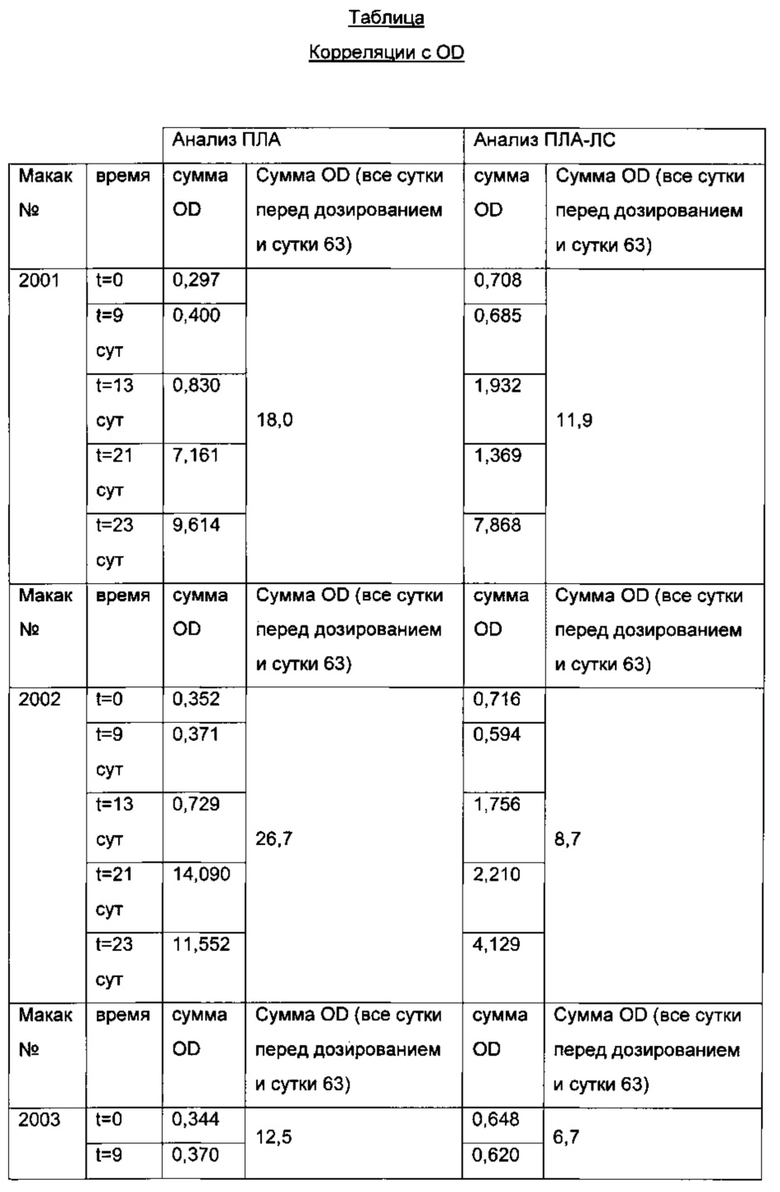
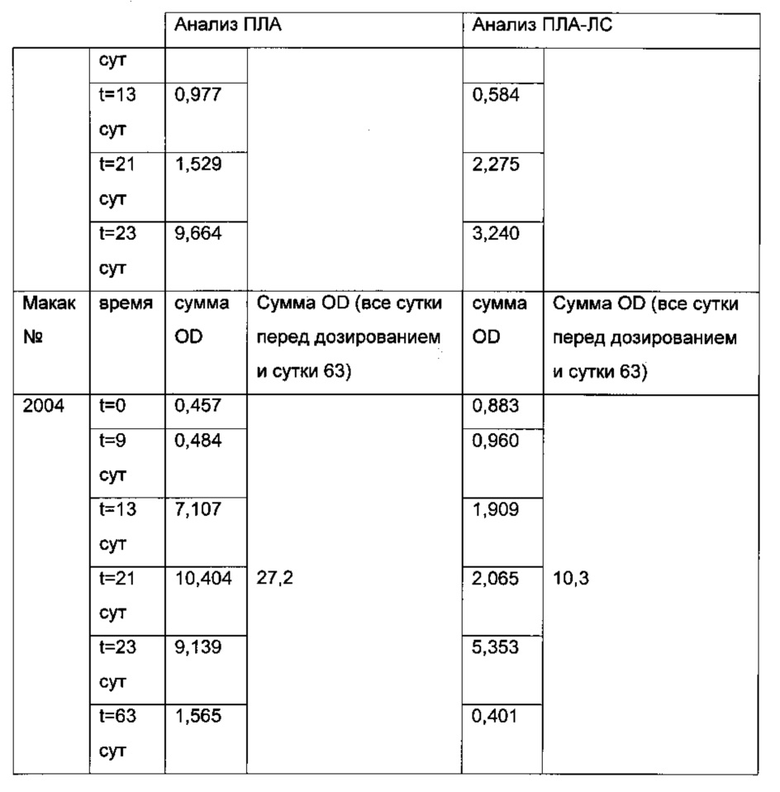
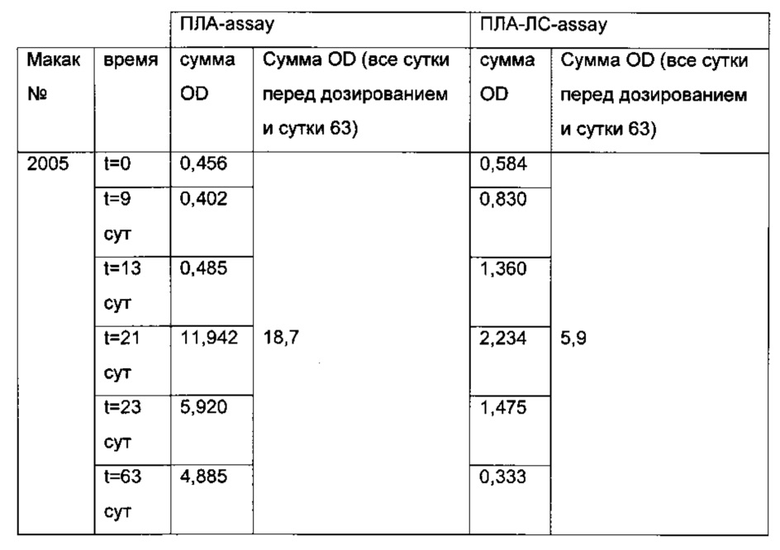
Из фиг. 5 видно, что повышенный клиренс наблюдают для животного 2001, 2002 и 2004. Для этих животных полученная сумма OD (всех суток кроме суток перед дозированием, и суток 63) анализа ПЛА-ЛС составляет 11,9 (животное 2001), 8,7 (животное 2002) и 10,3 (животное 2004). Эти сигналы явно превышают сигналы 6,7 (животное 2003) и 5,9 (животное 2004), которые не показали повышенный клиренс. Следовательно, увеличенные количества комплексов ПЛА-Лекарственное средство указывают на более быстрый плазматический клиренс.
Пример 3
Корреляция анализа ЭХ-ELISA и обнаружение отложений IgG в гломерулах
Для каждого анализа (анализа ПЛА и анализа ПЛА-ЛС) при t=21 сут и t=23 сут и каждой дозируемой группы (Группы А и Группы В) сигналы фракций блоков времени удерживания от 9 мин до 12 мин (блок 1), от 12 мин до 15 мин (блок 2) и от 15 мин до 17 мин (блок 3) суммируют (см. таблицы ниже для анализа ПЛА-ЛС и анализа ПЛА).
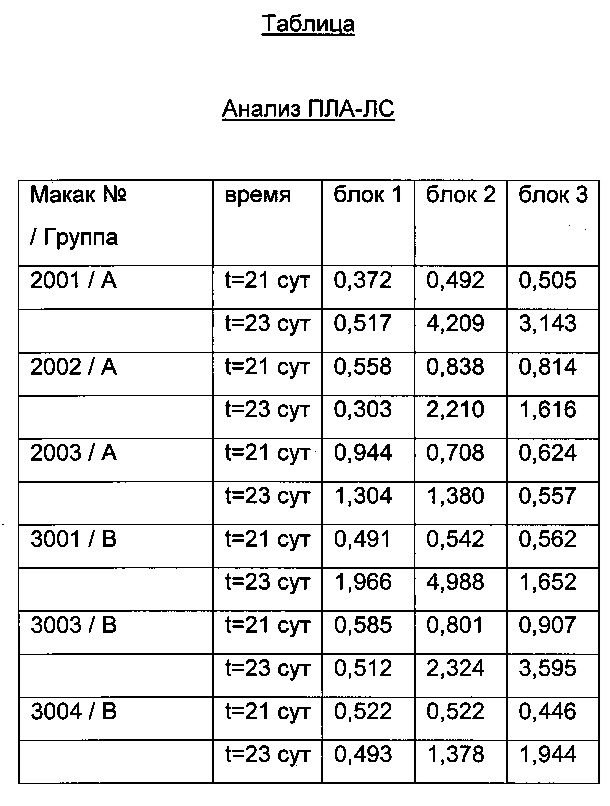
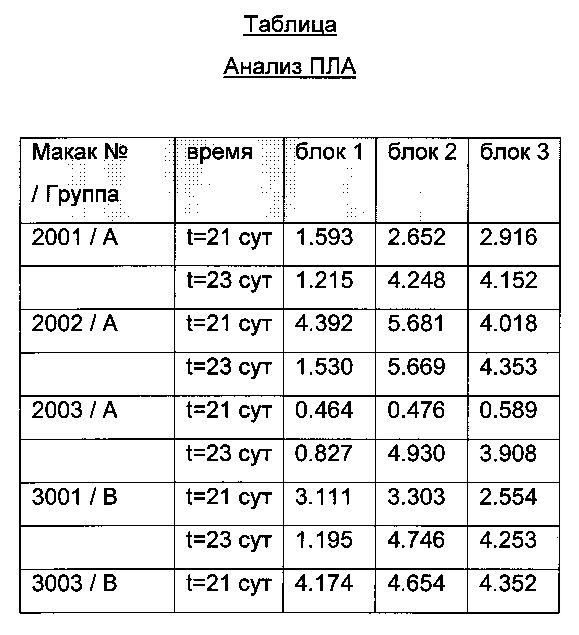
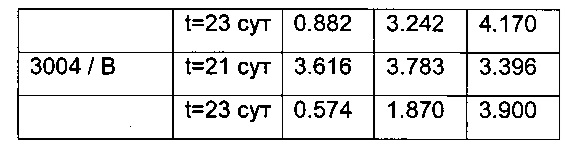
Суммированные сигналы, полученные для момента времени t=23 сут, делят на сигнал, полученный для момента времени t=21 сут ("отношение 1"), что указывает на утрату или повышение сигнала на t=23 сут.
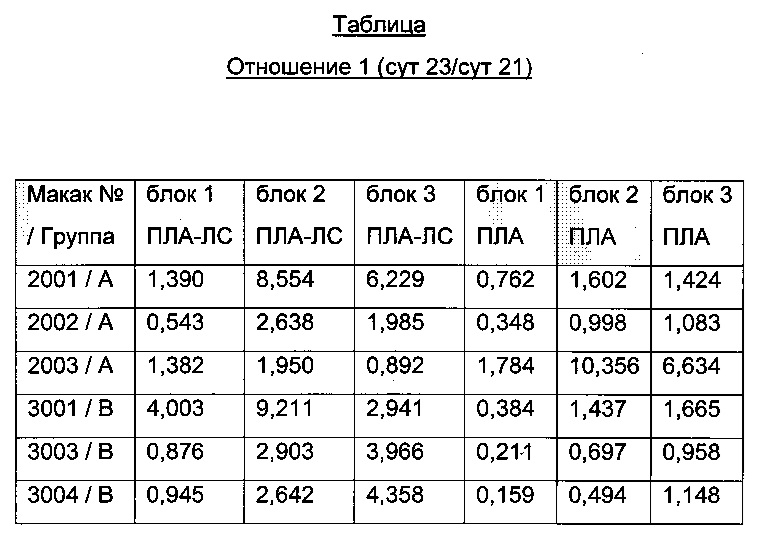
Значения "отношения 1" анализа ПЛА-ЛС делят на значения "отношения 1" анализа ПЛА с получением значений "отношения 2". Высокие значения "отношения 2" в блоке 1 (например, выше 2 или 3) указывает на гломерулярные отложения у животных.
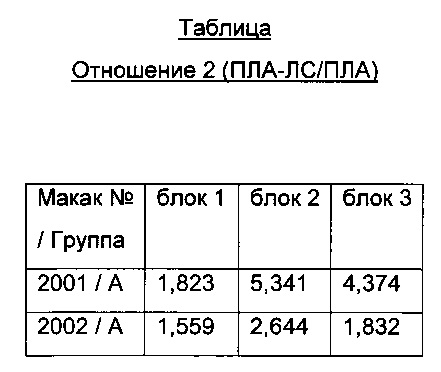
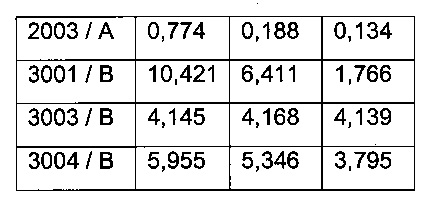
Кроме того, значения "отношения 2" каждой группы и блока дозирования статистически анализируют с помощью F-критерия и Т-критерия (альфа 5%), чтобы дифференцировать, различаются ли значения/среднее блока 1 - блока 3 групп.
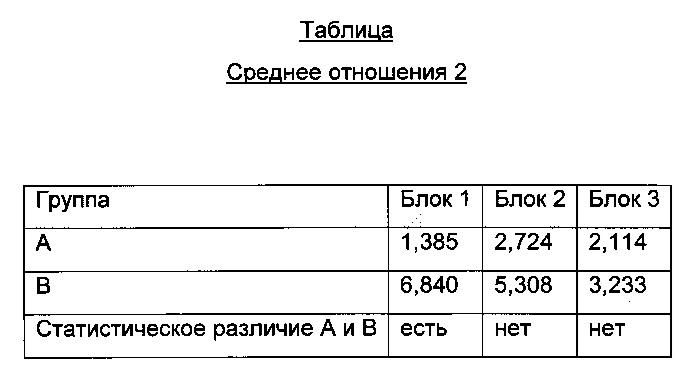
Данные гломерулярных отложений оценивают от "-" для отсутствия отложений до "(+)" слегка видимых гломерулярных отложений до "+" и "++" для положительных образцов с полуколичественным дифференцированием обнаруженных гломерулярных отложений у животных.

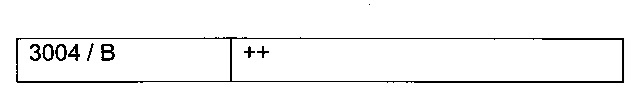
Результаты, приведенные в таблицах выше, показывают корреляцию иммунокомплексов, разделенных с помощью ЭХ, с гломерулярными отложениями у животных. Высокие значения в блоке 1 указывают на гломерулярные отложения у животных. Всех животных группы А оценивают как "-" и "(+)", и всех животных группы В оценивают как "+" и "++". Средние значения этих групп статистически различаются.
Как показано в таблице "Гломерулярные отложения", наблюдали полуколичественную дифференциацию между результатом гломерулярных отложений IgG для животных 3003 и 3004, проявляющих более выраженные отложения.
Как показано в таблицах для анализа ПЛА-Лекарственное средство и анализа ПЛА, сумма сигналов в блоке 1 непрямо пропорциональны результатам гломерулярных отложений (см. также фиг. 6).
Изобретение относится к медицине и касается способа определения циркулирующего конъюгированного противолекарственного антитела, содержащего терапевтический полипептид и эндогенное противолекарственное антитело, образовавшееся in vivo, для установления корреляции измененной фармакокинетики и утраты или снижения эффективности, включающего стадии эксклюзионной хроматографии образца сыворотки или спинномозговой жидкости от млекопитающего, которому введено лекарственное средство по меньшей мере один раз, для определения массы/размера иммунокомплекса, и по меньшей мере одного гетерогенного иммуноанализа на обнаружение конъюгированного противолекарственного антитела. Где терапевтический полипептид представляет собой синтетический или неприродный терапевтический полипептид. Изобретение обеспечивает установление корреляции с измененной фармакокинетикой, утратой или снижением эффективности, нейтрализацией природных аналогов, а также с общими иммунными реакциями и реакциями гиперчувствительности, включающими сывороточную реакцию/гиперчувствительность типа III/заболевание, опосредованное иммунокомплексами. 6 з.п. ф-лы, 3 пр., 6 ил., 15 табл.
1. Способ определения циркулирующего конъюгированного противолекарственного антитела, содержащего терапевтический полипептид и эндогенное противолекарственное антитело, образовавшееся in vivo, для установления корреляции измененной фармакокинетики и утраты или снижения эффективности, включающий следующие стадии:
a) эксклюзионную хроматографию образца сыворотки или спинномозговой жидкости от млекопитающего, которому введено лекарственное средство по меньшей мере один раз, для определения массы/размера иммунокомплекса, и
b) по меньшей мере один гетерогенный иммуноанализ на обнаружение конъюгированного противолекарственного антитела,
где указанная эксклюзионная хроматография представляет собой эксклюзионную хроматографию со сбором элюата во фракциях, при этом каждую из фракций анализируют в иммуноанализе,
где иммунокомплекс определяют на основании корреляции размера иммунокомплекса и считывания данных/результата иммуноанализа,
где терапевтический полипептид представляет собой синтетический или неприродный терапевтический полипептид.
2. Способ по п. 1, отличающийся тем, что по меньшей мере одну из фракций эксклюзионной хроматографии дополнительно разделяют с помощью второй хроматографии, отличающейся от эксклюзионной хроматографии, со сбором элюата во фракциях.
3. Способ по п. 1, отличающийся тем, что по меньшей мере один из иммуноанализов представляет собой мостиковый твердофазный иммуноферментный анализ.
4. Способ по п. 1, отличающийся тем, что по меньшей мере один из иммуноанализов представляет собой комплексный анализ на обнаружение комплексов противолекарственных антител с лекарственным средством (ПЛА-ЛС).
5. Способ по п. 4, отличающийся тем, что комплексный анализ включает иммобилизованное антитело, специфичное к лекарственному средству, и антитело антивидовой специфичности в качестве идентифицирующего антитела.
6. Способ по п. 1, отличающийся тем, что по меньшей мере один из иммуноанализов представляет собой прямой анализ на обнаружение противолекарственных антител, связанных с лекарственным средством.
7. Способ по п. 6, отличающийся тем, что прямой анализ включает в качестве иммобилизованной молекулы иммобилизованное лекарственное средство или эндогенный аналог лекарственного средства и антитело антивидовой специфичности в качестве идентифицирующего антитела.
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| EP 0 834 076 B1, 08.04.1998 | |||
| Колосоуборка | 1923 |
|
SU2009A1 |
Авторы
Даты
2017-12-15—Публикация
2013-03-07—Подача