Изобретение относится к ветеринарии, к диагностике инфекционных болезней, а именно к дифференциации возбудителей бруцеллеза.
Бруцеллез - инфекционная болезнь животных, представляющая большую опасность как для животных, так и для людей.
Существуют различные виды возбудители бруцеллеза. Среди сельскохозяйственных животных наиболее распространены бруцеллы видов abortus и melitensis, опасные как для животных, так и людей.
Принципиально важно, в случае возникновения вспышки бруцеллеза, объективно установить вид возбудителя, так как от этого существенно зависит выбор оптимальной схемы противобруцеллезных мероприятий.
Известно, что для дифференциации возбудителей бруцеллеза в бактериологической диагностике в качестве одного из основных методов используют антивидовые моноспецифические бруцеллезные сыворотки. От уровня их чувствительности зависит надежность видовой дифференциации бруцелл. Кроме того, практически важны простота и безопасность их получения.
Известен принцип получения бруцеллезных моноспецифических (монорецепторных) антивидовых диагностических сывороток по определенной схеме, целью которого является достижение высокого уровня антител за счет многократной гипериммунизации животных-продуцентов (кроликов) культурами вирулентных штаммов бруцелл, с последующей адсорбцией полученных сывороток взвесью бруцелл гетерологичного вида для удаления общих для них антител (Вершилова П.А. Биохимическая и серологическая дифференциация группы Brucella и ее значение в эпидемиологии // Архив биологических наук, 35, сер. Б, 2. М., 1934; Кириллов Л.В. Получение монорецепторных сывороток // Биологические и химиотерапевтические ветеринарные препараты. М., 1963. С. 366-371; Иванов Н.П. Бруцеллез животных и меры борьбы с ним. / Под ред. Т.С. Сайдулдина. - Алматы, 2007. - 433 с.).
Недостатками этого принципа получения бруцеллезных моноспецифических как М-, так и А-сывороток являются высокая себестоимость конечного продукта за счет получения сыворотки только при однократном взятии крови, а также эпидемическая опасность, связанная с использованием в процессе производства живых штаммов бруцелл.
Наиболее близким техническим результатом является способ получения бруцеллезной моноспецифической сыворотки anti-abortus (Патент RU №2375074 (13) С1 от 30.06.2008, А61К 39/00). Способ получения бруцеллезной моноспецифической сыворотки anti-abortus включает внутривенную иммунизацию кроликов разовой дозой в объеме 1 мл смесью (1:1) из взвеси вакцинного штамма В. abortus 19 ВА концентрацией 3,0-5,0×109 м.к. (микробных клеток)/мл, обеззараженной кипячением в течение 60 мин, и взвеси живой культуры того же штамма В. abortus 19ВА концентрацией 3,0-5,0×109 м.к./мл, обескровливание животных, инактивацию сыворотки при 60-65°С в течение 1-1,5 ч, для перекрестной абсорбции используют бакмассу штамма В. melitensis 548, с последующей инкубацией сыворотки при 37°С в течение 2 ч, ее концентрированием путем центрифугирования и добавлением фенола в качестве консерванта.
Недостатками этого способа являются трудоемкость процесса, эпидемическая опасность, связанная с использованием живой культуры бруцелл вида abortus, небольшой объем выхода конечного продукта за счет получения сыворотки от животного-продуцента только при обескровливании.
Техническим результатом предлагаемого способа изготовления бруцеллезной моноспецифической сыворотки anti-abortus является снижение трудоемкости процесса ее изготовления, эпидемической опасности и увеличения выхода конечного продукта.
Техническое решение достигается тем, что способ получения бруцеллезной моноспецифической сыворотки anti-abortus включает иммунизацию кроликов разовой дозой штамма В. abortus 19, получение сыворотки, перекрестную абсорбцию сыворотки бактериальной массой гетерологического вида melitensis с последующей ее инкубацией при 37°С в течение 2 часов, концентрирование сыворотки путем центрифугирования, консервирование и фасовку, иммунизацию кроликов проводят подкожно в область подгрудка суспензией в объеме 1 мл, представляющей собой смесь 200 млн м.к. культуры штамма В. abortus 19, обеззараженной кипячением в течение 60 минут, с адъювантом MONTANIDE™ ISA 61 VG, на 14-16 день проводят пробное крововзятие, а на 21-45 дни осуществляют трехкратное взятие крови и на 60 день обескровливают, для перекрестной адсорбции используют штамм В. melitensis 565, обеззараженный кипячением в течение 60 минут.
Предлагаемый способ изготовления бруцеллезной моноспецифической бруцеллезной диагностической сыворотки anti-abortus позволяет снизить трудоемкость за счет подкожного введения, максимально повысить противоэпидемическую безопасность этого процесса за счет использования обеззараженных культур бруцелл, а минимум четырехкратное взятие крови от каждого кролика позволит в два раза увеличить количество получаемой сыворотки.
В качестве антигенов использовали обеззараженные (инактивированные) кипячением 30 минут культуры бруцелл:
- для гипериммунизации кроликов - взвесь обеззараженной культуры штамма B. abortus 19-200 млн м.к. с добавлением адъюванта MONTANIDE™ ISA 61 VG;
- для адсорбции полученной сыворотки - обеззараженный штамм B. melitensis 565.
Используемые штаммы должны отвечать паспортным данным. Культуру В. abortus 19 высевают на одну из питательных сред: эритрит агар, МППГГА. После 2-3-суточного роста при температуре 37°С бактериальную массу смывают с поверхности питательной среды физиологическим раствором с добавлением 0,5% фенола. Полученную взвесь бруцелл доводят до необходимой концентрации по оптическому стандарту мутности, сливают через двойной марлевый фильтр в колбы и обезвреживают кипячением в течение 60 минут, периодически помешивая. Проверяют на чистоту и стерильность путем засева на питательные среды.
Взвеси культур, используемые в качестве антигенов как при гипериммунизации кроликов, так и для адсорбции полученных сывороток, должны быть стерильными.
В качестве адъюванта применяли французский препарат MONTANIDE™ ISA 61 VG, производитель - фирма «SEPPIC». Готовый к использованию масляный адъювант для ветеринарных вакцин для производства эмульсий «вода в масле» содержит особое обогащенное светлое минеральное масло и высокоочищенное ПАВ, полученное из маннитола и очищенной олеиновой кислоты растительного происхождения. Препарат MONTANID™ISA 61 VG не содержит компонентов животного происхождения. Рецептуры вакцин с MONTANIDE™ ISA 61 VG вызывают сильный и продолжительный иммунный ответ. По сравнению с традиционными масляными эмульсиями суспензия с MONTANIDE™ ISA 61 VG является устойчивой, стабильной и легко вводимой. Для приготовления 100 г вакцины обычно необходимо: MONTANIDE™ ISA 61 VG - 60 г и водной антигенной среды - 40 г. Стабильные эмульсии получаются путем смешивания водной среды в MONTANIDE™ ISA 61 VG, при комнатной температуре или ниже, при интенсивном перемешивании.
При комнатной температуре интенсивно перемешивают на магнитной мешалке взвесь культуры штамма В. abortus 19, обеззараженной (кипячением в течение 60 минут), с добавлением адъюванта MONTANIDE™ ISA 61 VG, в соотношении 40 и 60% соответственно, т.е. для приготовления 10 мл суспензии необходимо 4 мл взвеси - 500 млн м.к./мл и 6 мл адъюванта.
В качестве животных-продуцентов использовали кроликов.
Заявленный результат достигается следующим образом.
Кроликам однократно подкожно в область подгрудка вводят 1 мл суспензии, представляющей собой смесь антигена (200 млн м.к. обеззараженной культуры штамма В. abortus 19) с адъювантом MONTANIDE™ ISA 61 VG. На 14 день проводят пробное крововзятие, а далее, при условии положительной РА с полученной сывороткой и испытуемой живой культурой В. melitensis в разведении не ниже 1:160, осуществляют четырехкратное взятие крови (из ушной вены) в сроки с 21 по 45 день после гипериммунизации, из расчета 16-20 мл крови на 1 кг живой массы. Через 60 дней тотальное взятие крови (производственное кровопускание). Кровь от каждого кролика берут с соблюдением правил асептики и антисептики в отдельную стерильную емкость. После крововзятия емкость с кровью ставят в термостат при 37°С на 3-4 часа для отделения сыворотки, затем помещают в холодильник при 2-8°С на 2-е суток. Сыворотку от каждого кролика сливают отдельно в стерильные сосуды, после чего прогревают в водяной бане при температуре 60-65°С в течение 1-1,5 часов при постоянном перемешивании и добавлением мертиолата натрия до конечной концентрации 1:10000.
Процесс адсорбции полученной штамма anti-abortus сыворотки проводят, используя бактериальную массу обеззараженного кипячением в течение 30 минут штамма В. melitensis 565, полученную путем выращивания на матрицах в течение 72 часов. Бакмассу смывают 0,9% раствором натрия хлорида, центрифугируют в течение 30 минут при частоте вращения 5000 об/мин, осадок собирают и добавляют 0,9% раствор натрия хлорида. Полученную бакмассу, из расчета 3,5-3,7×109 КОЕ на 10 мл сыворотки, добавляют к сыворотке, с последующей инкубацией смеси при 37°С в течение 2 часов, концентрируют сыворотку путем центрифугирования 30 мин при 5000 об/мин и консервируют, например, добавлением мертиолата натрия в конечной концентрации 1:10000, фасуют.
Контроль активности полученной сыворотки осуществляют в РА до адсорбции и после нее, используя в качестве антигенов живые культуры бруцелл видов abortus и melitensis. Сыворотка считается качественной, если РА с ней и антигенами живых культур бруцелл видов melitensis будет положительной в разведениях не ниже 1:160 и отрицательном результате агглютинации живых культур бруцелл видов melitensis в разведениях 1/10 соответственно.
Пробу сыворотки крови из каждой емкости подвергают проверке на стерильность путем высевов на МПА, МПБ, МППБ под вазелиновым маслом и среду Сабуро и на активность в РА, РСК, РБП.
При условии стерильности и получении положительных результатов серологических реакций сыворотку смешивают в одну емкость для составления серии, консервируют, например, мертиолатом натрия качестве консерванта в конечной концентрации 1:10000 и расфасовывают.
Пример 1. Определение оптимальной схемы гипериммунизации кроликов для получения сыворотки бруцеллезной моноспецифической anti-abortus.
В опыте изучена сравнительная эффективность четырех схем получения бруцеллезной моноспецифической сыворотки anti-abortus, для чего из здоровых кроликов, предварительно проверенных на бруцеллез серологическими методами, сформировали 4 группы (по 3 кролика в каждой):
1-я группа - животным вводят однократно внутривенно в объеме 1 мл смесь (1:1) из взвеси вакцинного штамма В. abortus 19 концентрацией 3,0-5,0×109 м.к. (микробных клеток)/мл, обеззараженного кипячением в течение 60 мин, и взвеси живой культуры того же штамма В. abortus 19 концентрацией 3,0-5,0×109 м.к./мл.
2-я группа - животным вводят однократно подкожно в область подгрудка обеззараженную кипячением в течение 60 минут культуру В. abortus 19 в дозе 200 млн м.к. в смеси с адъювантом MONTANIDE™ ISA 61 VG в общем объеме 1 мл.
3-я группа - животным вводят однократно подкожно в область подгрудка обеззараженную кипячением в течение 60 минут культуру В. abortus 19 в дозе 100 млн м.к. в смеси с адъювантом MONTANIDE™ ISA 61 VG в общем объеме 1 мл.
4-я группа - животным вводят однократно подкожно в область подгрудка обеззараженную кипячением в течение 60 минут культуру В. abortus 19 в дозе 300 млн м.к. в смеси с адъювантом MONTANIDE™ ISA 61 VG в общем объеме 1 мл.
Кровь от животных в целях получения сывороток брали на 7, 14, 21, 28, 45, 60 и 90 дни после введения антигенов.
Исследование полученных сывороток проводили в РА с антигенами, приготовленными из В. abortus 544 и B. melitensis 565, согласно общепринятой методике до и после адсорбции.
Перед адсорбцией сыворотки инактивировали при 60-65°С в течение 1-1,5 ч и обезвреживали мертиолатом натрия до конечной концентрации 1:10000.
В дальнейшем проводили адсорбцию полученных сывороток anti-abortus бактериологической массой штамма B. melitensis 565, обеззараженной кипячением в течение 60 минут и добавленной к сыворотке из расчета 3,5-3,7×109 м.к. на 10 мл сыворотки, с последующей инкубацией смеси при 37°С в течение 2 часов, концентрирование путем центрифугирования 30 минут при 5000 об/мин, добавление в качестве консерванта мертиолата натрия до конечной концентрации 1:10000 и фасовку.
Результаты опыта приведены в таблицах 1-7.
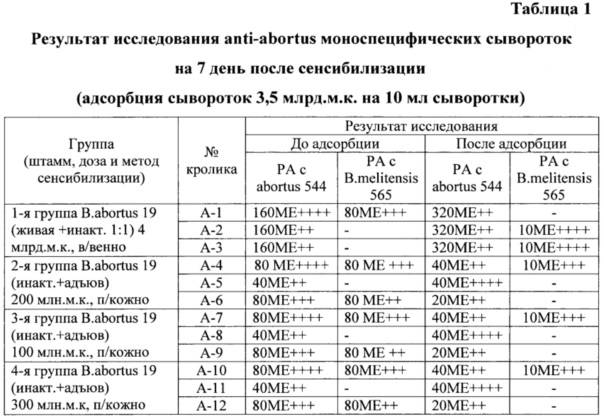
РА с сыворотками крови, полученными от кроликов на 7 день после их сенсибилизации (таблица 1), в первой группе была положительной до адсорбции с антигенами убитых культур бруцелл видов abortus и melitensis в разведении 1:80 - 1:160 и 1:80, а после адсорбции - 1:320 и 0-1:10 соответственно; во второй группе - до адсорбции 1:40 - 1:80 и 0-1:80, а после адсорбции - 1:20 - 1:40 и 0-1:10 соответственно; в третьей группе - до адсорбции 1:40 - 1:80 и 0-1:80 соответственно, а после адсорбции 1:20 - 1:40 и 0-1:10 соответственно; в четвертой группе - до адсорбции 1:40 - 1:80 и 0-1:80 соответственно, а после адсорбции 1:20 - 1:40 и 0-1:10 соответственно.

РА сыворотками крови, полученными от кроликов на 14 день после их сенсибилизации (таблица 2), в первой группе была положительной до адсорбции с антигенами убитых культур бруцелл видов abortus и melitensis в разведении 1:640 - 1:2560 и 1:1280 - 1:2560, а после адсорбции - 1:160 и 1:10-20 соответственно; во второй группе - до адсорбции 1:320 - 1:1280 и 1:80 - 1:1280, а после адсорбции - 1:160 - 1:320 и 0-1:10 соответственно; в третьей группе - до адсорбции 1:80 - 1:320 и 1:80 - 1:320 соответственно, а после адсорбции - 1:20 - 1:160 и 0-1:10 соответственно; в четвертой группе - до адсорбции 1:320 - 1:1280 и 1:160 - 1:1280 соответственно, а после адсорбции 1:160 - 1:320 и 0-1:10 соответственно.

РА с сыворотками крови, полученными от кроликов на 21 день после их сенсибилизации (таблица 3), в первой группе была положительной до адсорбции с антигенами убитых культур бруцелл видов abortus и melitensis в разведении 1:160 - 1:320 и 1:640 - 1:1280, а после адсорбции - 1:160 - 1:1280 и 1:20 соответственно; во второй группе - до адсорбции 1:160 - 1:1280 и 1:80 - 1:1280, а после адсорбции - 1:160 и 0-1:20 соответственно; в третьей группе до адсорбции - 1:80 - 1:160 и 0-1:80 соответственно, а после адсорбции - 1:80 и 0-1:10 соответственно; в четвертой группе - до адсорбции 1:320 - 1:1280 и 1:160 - 1:1280 соответственно, а после адсорбции 1:160 - 1:320 и 0-1:20 соответственно.
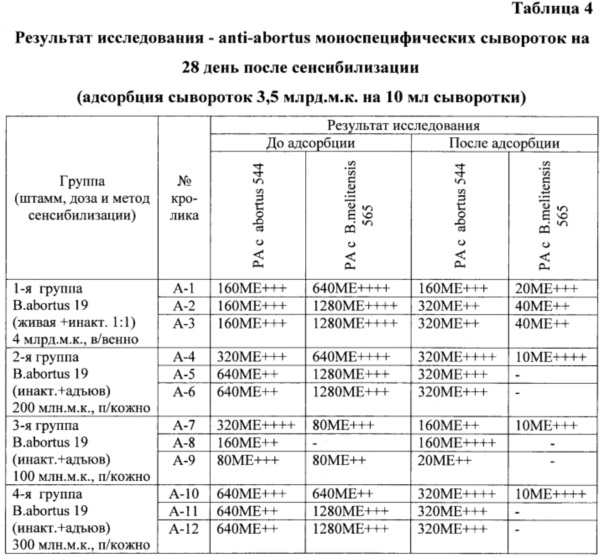
РА с сыворотками крови, полученными от кроликов на 28 день после их сенсибилизации (таблица 4), в первой группе была положительной до адсорбции с антигенами убитых культур бруцелл видов abortus и melitensis в разведении 1:160 и 1:640 - 1:1280, а после адсорбции - 1:160 - 1:320 и 1:20 - 1:40 соответственно; во второй группе - до адсорбции 1:320 - 1:640 и 1:640 - 1:1280, а после адсорбции - 1:320 и 0-1:10 соответственно; в третьей группе - до адсорбции 1:80 - 1:320 и 0-1:80 соответственно, а после адсорбции - 1:20 - 1:160 и 0-1:10 соответственно; в четвертой группе - до адсорбции 1:640 и 1:640 - 1:1280 соответственно, а после адсорбции - 1:320 и 0-1:10 соответственно.
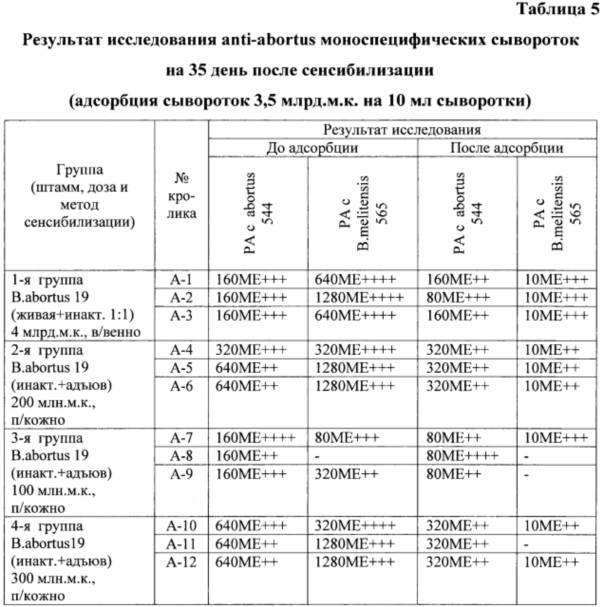
РА с сыворотками крови, полученными от кроликов на 35 день после их сенсибилизации (таблица 5), в первой группе была положительной до адсорбции с антигенами убитых культур бруцелл видов abortus и melitensis в разведении 1:160 и 1:640 - 1:1280, а после адсорбции - 1:80 - 1:160 и 1:10 соответственно; во второй группе - до адсорбции 1:320 - 1:640 и 1:320 - 1:1280, а после адсорбции - 1:320 и 0-1:10 соответственно; в третьей группе - до адсорбции 1:160 и 1:80 - 1:320 соответственно, а после адсорбции - 1:80 и 0-1:10 соответственно; в четвертой группе - до адсорбции 1:640 и 1:320 - 1:1280 соответственно, а после адсорбции - 1:320 и 0-1:10 соответственно.
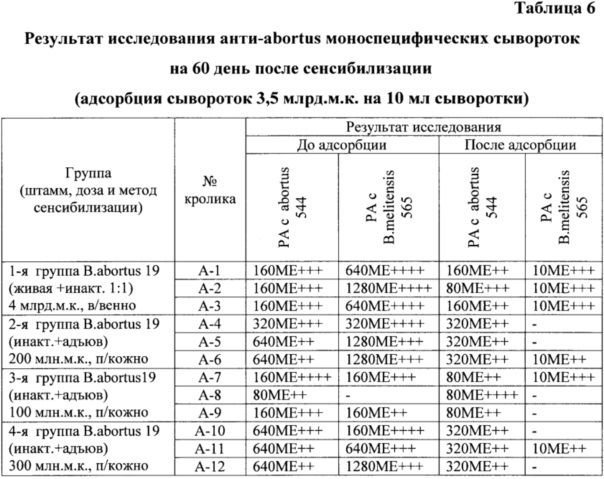
РА с сыворотками крови, полученными от кроликов на 60 день после их сенсибилизации (таблица 6), в первой группе была положительной до адсорбции с антигенами убитых культур бруцелл видов abortus и melitensis в разведении 1:160 и 1:640 - 1:1280, а после адсорбции - 1:80 - 1:160 и 1:10 соответственно; во второй группе до адсорбции - 1:320 - 1:640 и 1:320 - 1:1280, а после адсорбции - 1:320 и 0-1:10 соответственно; в третьей группе до адсорбции - 1:80 - 1:160 и 0-1:160 соответственно, а после адсорбции 1:80 и 0-1:10 соответственно; в четвертой группе до адсорбции - 1:640 и 1:160-1:1280 соответственно, а после адсорбции - 1:320 и 0-1:10 соответственно.
РА с сыворотками крови, полученными от кроликов на 90 день после их сенсибилизации (таблица 7), в первой группе была положительной до адсорбции с антигенами убитых культур бруцелл видов abortus и melitensis в разведении 1:160 - 1:320 и 1:80, а после адсорбции - 1:80 и 1:40 соответственно; во второй группе до адсорбции - 1:160 и 1:320, а после адсорбции - 1:320 и 0-1:10 соответственно, в третьей группе до адсорбции -1:80 и 0-1:80 соответственно, а после адсорбции - 1:-20-40 и 0-1:10 соответственно; в четвертой группе до адсорбции - 1:160 1:320 и 1:320 - 1:640 соответственно, а после адсорбции - 1:320 и 0-1:10 соответственно.
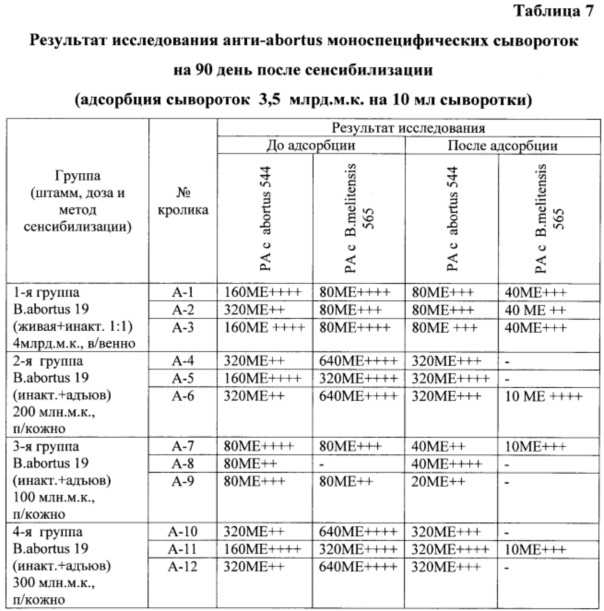
Таким образом, из приведенных данных очевидно, что оптимальной является схема получения бруцеллезной моноспецифической сыворотки anti-abortus, испытанная на животных второй группы, в которой использовалась однократная подкожная гипериммунизация в область подгрудка суспензия инактивированной культуры бруцелл вида anti-abortus в смеси с масляным адъювантом MONTANIDE™ ISA 61 VG. Кроме эпидемической безопасности, ее преимущества заключаются в более высоких ее титрах при получении в отдаленные сроки после гипериммунизации, а значит, в возможности получения значительного объема сыворотки с более высокой активностью за счет многократного (не менее 4-х раз) взятия крови.
Пример 2. Изучение диагностической активности бруцеллезных моноспецифических сывороток anti-abortus, полученных от кроликов, гипериммунизированных по разным схемам, через 6 месяцев их хранения (таблица 8).
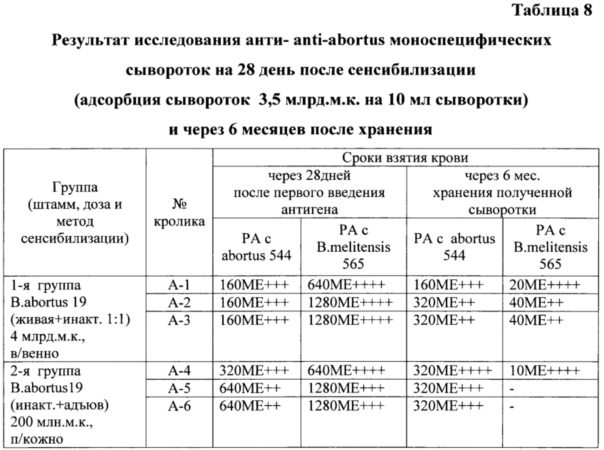
Установлено, что сыворотка, полученная от кроликов по схеме, предусматривающей однократную подкожную, в область подгрудка, гипериммунизацию обеззараженной культурой бруцелл вида anti-abortus в смеси с масляным адъювантом MONTANIDEТМ ISA 61 VG, сохранила свою активность (РА в разведении не ниже 1:160) в течение не менее 6 месяцев после ее получения. Из крови, взятой через 21, 28, 35 и 60 дней после гипериммунизации, в отличие от сыворотки, полученной при однократной внутривенной гипериммунизации смеси 1:1 обеззараженной и живой культурой бруцелл вида abortus без адъюванта, потерявшей активность в более ранние сроки - 28-35 дней.
Предлагаемый способ получения бруцеллезной моноспецифической бруцеллезной диагностической сыворотки anti-abortus позволяет снизить трудоемкость за счет подкожного иммунизации, максимально повысить противоэпидемическую безопасность этого процесса за счет использования обеззараженных культур бруцелл, а также брать кровь от каждого животного минимум четырехкратно, а значит, в два раза повысить количество получаемой сыворотки.
Литература
1. Вершилова П.А. Биохимическая и серологическая дифференциация группы Brucella и ее значение в эпидемиологии // Архив биологических наук, 35, сер. Б, 2. М., 1934.
2. Иванов Н.П. Бруцеллез животных и меры борьбы с ним. / Под ред. Т.С. Сайдулдина. - Алматы, 2007. - 433 с.
3. Кириллов Л.В. Получение монорецепторных сывороток // Биологические и химиотерапевтические ветеринарные препараты. М., 1963. С. 366-371.
4. Патент RU №2375074 (13) от 30.06.2008, А61K 39/00. «Способ получения бруцеллезной моноспецифической сыворотки anti-abortus».
5. Технический бюллетень MONTANIDE™ ISA 61 VG.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения бруцеллёзной моноспецифической сыворотки anti-melitensis | 2016 |
|
RU2613901C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ БРУЦЕЛЛЕЗНОЙ ДИАГНОСТИЧЕСКОЙ СЫВОРОТКИ | 2013 |
|
RU2549434C2 |
| Способ получения R-бруцеллёзной сыворотки на кроликах | 2017 |
|
RU2659948C1 |
| СПОСОБ ПОЛУЧЕНИЯ БРУЦЕЛЛЕЗНОЙ МОНОСПЕЦИФИЧЕСКОЙ СЫВОРОТКИ ANTI-ABORTUS | 2008 |
|
RU2375074C1 |
| АНТИГЕН ПОЛИВАЛЕНТНЫЙ КОРПУСКУЛЯРНЫЙ ДЛЯ ИЗГОТОВЛЕНИЯ ЛЕЧЕБНЫХ И ПРОФИЛАКТИЧЕСКИХ БИОПРЕПАРАТОВ ПРОТИВ БРУЦЕЛЛЕЗА | 2006 |
|
RU2330681C1 |
| СПОСОБ ПОЛУЧЕНИЯ БРУЦЕЛЛЕЗНОГО АНТИГЕНА ДЛЯ РОЗ-БЕНГАЛ ПРОБЫ (РБП) | 2011 |
|
RU2488119C2 |
| ВАКЦИНА ПРОТИВ БРУЦЕЛЛЕЗА КРУПНОГО РОГАТОГО СКОТА | 1997 |
|
RU2108110C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИАГНОСТИЧЕСКОЙ СЫВОРОТКИ ПРОТИВ БРУЦЕЛЛ В L-ФОРМЕ | 2003 |
|
RU2268748C2 |
| ШТАММ БАКТЕРИЙ BRUCELLA MELITENSIS БИОВАРА I, ИСПОЛЬЗУЕМЫЙ ДЛЯ ПОЛУЧЕНИЯ ПОЛИВАЛЕНТНОЙ ГИПЕРИММУННОЙ СЫВОРОТКИ К БРУЦЕЛЛАМ | 1991 |
|
RU2005781C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИАГНОСТИЧЕСКОЙ АГГЛЮТИНИРУЮЩЕЙ СЫВОРОТКИ ПРОТИВ БРУЦЕЛЛ В L-ФОРМЕ | 2003 |
|
RU2242765C1 |
Изобретение относится к ветеринарии и касается способа получения бруцеллезной моноспецифической сыворотки anti-abortus, включающего иммунизацию кроликов разовой дозой штамма В. abortus 19, обескровливание животных, перекрестную абсорбцию сыворотки бактериальной массой гетерологического вида бруцелл с последующей ее инкубацией при 37°C в течение 2 ч, концентрирование сыворотки путем центрифугирования, консервирование и фасовку, где иммунизацию кроликов проводят подкожно в область подгрудка суспензией, представляющей собой смесь культуры штамма В. abortus 19, обеззараженной кипячением, с адъювантом MONTANIDE™ ISA 61 VG, проводят пробное крововзятие, осуществляют трехкратное взятие крови и обескровливают, в качестве гетерологического вида бруцелл для адсорбции используют штамм В. melitensis 565. Изобретение обеспечивает снижение трудоемкости, повышение противоэпидемической безопасности процесса получения сыворотки, увеличение в два раза выхода конечного продукта. 2 пр., 8 табл.
Способ получения бруцеллезной моноспецифической сыворотки anti-abortus, включающий иммунизацию кроликов разовой дозой штамма В. abortus 19, обескровливание животных, перекрестную абсорбцию сыворотки бактериальной массой гетерологического вида бруцелл с последующей ее инкубацией при 37°C в течение 2 ч, концентрирование сыворотки путем центрифугирования, консервирование и фасовку, отличающийся тем, что иммунизацию кроликов проводят подкожно в область подгрудка суспензией в объеме 1 мл, представляющей собой смесь 200 млн м.к. культуры штамма В. abortus 19, обеззараженной кипячением в течение 60 мин, с адъювантом MONTANIDE™ ISA 61 VG, на 14-16 день проводят пробное крововзятие, а на 21-45 дни осуществляют трехкратное взятие крови и на 60 день обескровливают, в качестве гетерологического вида бруцелл для адсорбции используют штамм В. melitensis 565, обеззараженный кипячением в течение 60 мин.
| СПОСОБ ПОЛУЧЕНИЯ БРУЦЕЛЛЕЗНОЙ МОНОСПЕЦИФИЧЕСКОЙ СЫВОРОТКИ ANTI-ABORTUS | 2008 |
|
RU2375074C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ БРУЦЕЛЛЕЗНОЙ ДИАГНОСТИЧЕСКОЙ СЫВОРОТКИ | 2013 |
|
RU2549434C2 |
| KULAKOV Lu | |||
| K., et al., Increased production of the protein antigen of Brucella melitensis in Escherichia coli K-12 cells [Article in Russian] | |||
| Mol Gen Mikrobiol Virusol | |||
| Металлический водоудерживающий щит висячей системы | 1922 |
|
SU1999A1 |
| TABYNOV K., et al., An influenza viral vector Brucella abortus vaccine induces good cross-protection against Brucella melitensis infection in pregnant heifers | |||
| Vaccine | |||
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
Авторы
Даты
2017-12-19—Публикация
2016-04-22—Подача