Изобретение относится к биотехнологии, в частности к вакцине для профилактики бруцеллеза крупного рогатого скота.
Бруцеллез крупного рогатого скота - хроническое зооантропонозное заболевание, распространенное во многих странах мира, наносящее большой экономический ущерб скотоводству и представляющее серьезную опасность здоровью людей.
Основным средством борьбы с бруцеллезом крупного рогатого скота, особенно в зонах его широкого распространения, является вакцинация всего поголовья и своевременное удаление из стада больных животных.
Известна вакцина против бруцеллеза крупного рогатого скота, содержащая антиген из штамма Brucella abortus 19 и сахарозо-желатиновый стабилизатор [1].
Недостатками данной вакцины являются высокая агглютиногенность, так как в крови животных, иммунизированных данной вакциной в течение нескольких месяцев, а иногда и нескольких лет обнаруживают антитела в принятых для диагностики бруцеллеза серологических реакциях, что препятствует выявлению больных животных в вакцинированном стаде. Вакцину нельзя применять для иммунизации стельных коров, так как она вызывает аборты у отдельных животных.
Известна также вакцина против бруцеллеза сельскохозяйственных животных, преимущественно крупного рогатого скота, содержащая инактивированный антиген из штамма Brucella melitensis N "Невский-13", неполный адъювант Фрейнда и физиологический раствор [2].
Недостатком данной вакцины является то, что в крови иммунизированных животных до 90-120 дней сохраняются агглютинирующие и комплеменсвязывающие антитела, улавливаемые в принятых для диагностики бруцеллеза серологических реакциях, которые препятствуют своевременному выявлению и удалению из стада больных бруцеллезом коров.
Целью изобретения является разработка высокоиммуногенной вакцины против бруцеллеза крупного рогатого скота с низкой антигенной активностью.
Цель достигается тем, что вакцина в качестве антигена содержит инактивированную с гидратом окиси алюминия бактериальную массу штамма B.abortus ВГНКИ N КВ 17/100 с концентрацией 300-400х109 бактерий в 1 см3, при следующем соотношении компонентов вакцины, об.%: инактивированная с гидратом окиси алюминия бактериальная масса штамма B.abortus N КВ 17/100 с концентрацией 300х109-400х109 микробных клеток в 1 см3 40-45,0; неполный адъювант Фрейда 50,0-55,0; физиологический раствор остальное.
Для изготовления вакцины используют штамм Brucella abortus ВГНКИ N КВ 17/100.
Штамм B. abortus N КВ 17/100 получен путем целенаправленной селекции по антигенности и иммуногенной активности.
Штамм B. abortus депонирован в коллекции микроорганизмов Всероссийского государственного научно-исследовательского института контроля, стандартизации и сертификации ветеринарных препаратов, регистрационный номер КВ 17/100 ДЕП.
Штамм B. abortus N КВ 17/100 характеризуется следующими признаками и свойствами.
Морфологические признаки.
Бруцеллы штамма - короткие грамотрицательные палочки с закругленными концами, расположенные изолированно, попарно и реже в виде коротких цепочек. Без капсулы, спор не образуют. Размер 1,3-1,5 х 0,6-0,8 мкм.
Культуральные свойства.
Культура штамма хорошо растет в аэробных условиях на плотных и жидких питательных средах, предназначенных для культивирования бруцелл. На плотных питательных средах (4-5 сут инкубирования при 37-38oС) растет в виде круглых, плоских, с нечетко контурированным краем, матовых колоний с диаметром 2,5-3,0 мм. При окрашивании раствором кристаллического фиолетового 1/2000 (по Уайт-Вилсону) 100% колоний окрашиваются как R-форма: фиолетовый центр и светлофиолетовый широкий ободок.
На жидких питательных средах на 2-4 сут инкубирования: легкая опалесценция и узкое пристеночное голубоватое кольцо на границе среды.
Биохимические свойства.
Культура штамма растет на средах содержащих фуксин, тионин в концентрации 1: 50000, бис-трифенилангидрокарбинола оксалат в концентрации 1:100000 (маркер), пенициллин 5ЕД/см3 и не растет на среде, содержащей стрептомицина сульфат 5 мкг/см3. Продуцирует Н2S (6-8 мм). Лизируется фагом Тб.
Агглютинабельные свойства.
Культура штамма агглютинируется R-антибруцеллезной сывороткой и не агглютинируется S-антибруцеллезной сывороткой. Штамм не обладает типоспецифической агглютинабельностью и не агглютинируется А и М монорецепторными сыворотками.
Безвредность.
Штамм безвреден для человека и сельскохозяйственных животных.
Вирулентность.
Остаточная вирулентность: ИД для мышей линии С57 - Блек/6 - 5500 микробных клеток, что соответствует уровню аттенуированных вакцинных штаммов.
Иммуногенность.
Культура штамма защищает от заражения не менее 50% иммунизированных животных.
Пример 1. Штамм Brucella abortus ВГНКИ N КВ 17/100 культивируют на плотной питательной среде или в ферментере на жидкой питательной среде при 37-38oС в течение 72 ч.
Выращенную культуру с плотной питательной среды смывают физиологическим раствором, добавляют 0,3-0,5% формалина и 0,3-0,5% гидрата окиси алюминия, формалин и гидрат окиси алюминия вносят в ферментер сразу после окончания культивирования.
После инактивации бактериальную массу отстаивают, декантируют надосадочную жидкость и устанавливают концентрацию бактериальной массы, равную 300-400х109 микробных клеток в 1 см3. Инактивированную с гидратом окиси алюминия бактериальную массу штамма B.abortus ВГНКИ N КВ 17/100 в количестве 40-45% от объема смешивают с неполным адъювантом Фрейнда в количестве 45-55% от объема с доведением до 100% физиологическим раствором.
Вакцину расфасовывают во флаконы при включенной мешалке. Флаконы закрывают резиновыми пробками, обкатывают металлическими колпачками и этикетируют.
Расфасованную вакцину проверяют на стерильность, безвредность и иммуногенность.
Готовая вакцина представляет собой однородную водно-масляную эмульсию белого цвета с коричневым или серым оттенком. При длительном хранении возможно незначительное отслоение адъюванта над эмульсией, что не влияет на качество вакцины.
Получают 3 серии вакцины, приведенные в табл. 1.
Пример 2. Определяют антигенную активность адъювант-вакцины.
Морских свинок (10-14 голов в группе) иммунизируют адъювант-вакциной из штамма B.abortus ВГНКИ N КВ 17/100 (серии N 1, 2, 3), полученной по примеру 1; адъювант-вакциной из штамма B.melitensis N Н-13, экспериментальной адъювант-вакциной из штамма B.abortus N 16/4 (штамм в R-форме) и живой противобруцеллезной вакциной из штамма B.abortus N 19.
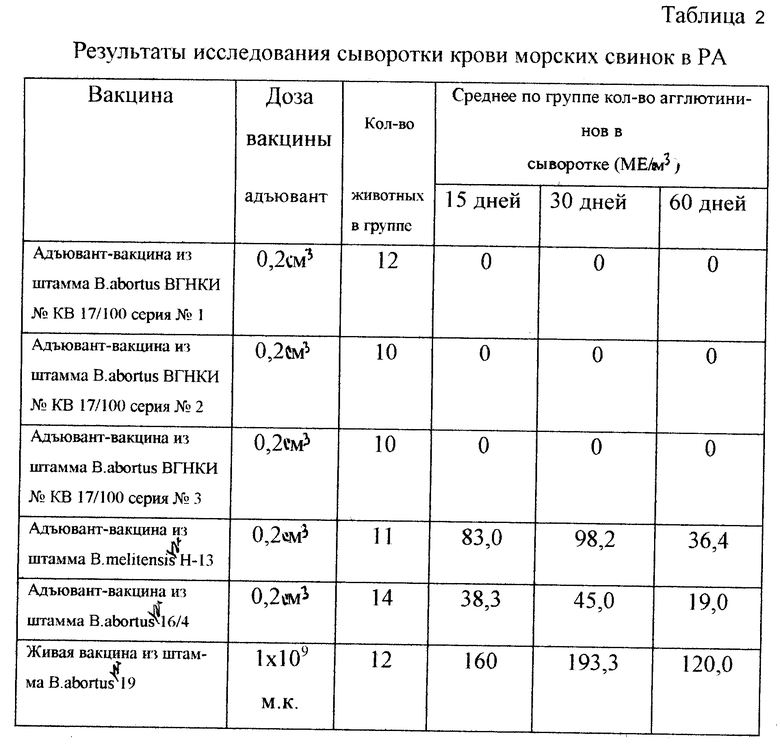
Адъювант-вакцины вводят в дозе 0,2 см3, живую - 1 млрд. микробных клеток в объеме 1 см3 под кожу в область паха. Через 15, 30 и 60 дней после иммунизации у животных берут кровь и исследуют в РА с единым бруцеллезным антигеном (S-антиген). Результаты исследований приведены в табл. 2.
Из табл. 2 следует, что все серии предложенной адъювантвакцины из штамма B. abortus ВГНКИ N КВ 17/100 не индуцируют образования агглютининов в сыворотке крови животных и в отличие от адъювант-вакцин из штаммов B.melitensis N "Невский-13", В. abortus N 16/4 и живой вакцины из штамма В.abortus N 19 являются неагглютиногенными, что дает возможность быстро и своевременно выявлять больных вакцинированных животных в случае их заражения. В то же время среднее количество агглютининов в сыворотке крови морских свинок через 15 дней после иммунизации адъювант-вакцинами из штаммов B.melitensis N "Невский-13" - 83,0, B. abortus N 16/4 - 38,3 МЕ/см3, а живой вакциной из штамма B. abortus N 19 - 160,0 ME/cм3, и в случае заражения больные бруцеллезом животные не могут быть дифференцированы по крайней мере в течение 60 дней от иммунных - незаразившихся, создавая угрозу перезаражения.
Таким образом установлено, что адъювант-вакцина из штамма В.abortus ВГНКИ N КВ 17/100 не индуцирует синтез S-антител в количестве, улавливаемом реакцией агглютинации с единым бруцеллезным антигеном.
Пример 3. Иммуногенную активность новой адъювант-вакцины, полученной по примеру 1 из штамма B.abortus ВГНКИ N 17/100, сравнивают с вакцинами из штаммов B.melitensis N "Невский-13", B.abortus N 16/4 и живой вакциной из штамма B. abortus N 19. Опыт проводят на морских свинках, привитых аналогично примеру 2.
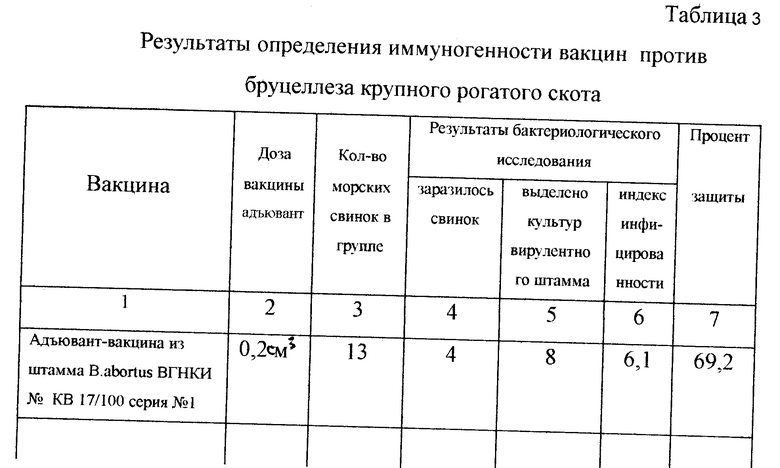
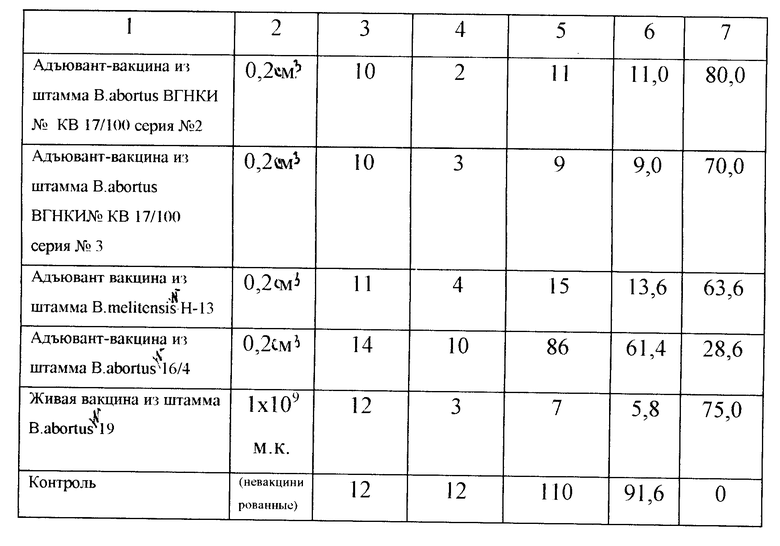
Через 3 мес после прививки морских свинок заражают стандартной культурой контрольного вирулентного штамма В.abortus N 54М/ВГНКИ в дозе 80 микробных клеток (15 ИД50). Спустя 32-35 дней животных убивают и проводят бактериологическое исследование селезенки, печени, костного мозга и лимфатических узлов (всего 10 объектов). Определяют наличие бруцелл вирулентного штамма в лимфатических узлах и внутренних органах животных. Рассчитывают процент защиты (количество незаразившихся животных в процентах от общего их количества в группе) и индекс инфицированности (процентное отношение количества объектов, из которых выделена культура вирулентного штамма, к общему количеству исследованных объектов по группе животных). Результаты исследований приведены в табл. 3.
Таким образом установлено, что адъювант-вакцина из штамма B.abortus ВГНКИ N RD 17/100 всех серий превосходит по иммуногенной активности адъювант-вакцины из штаммов B. melitensis N "Невский-13", B.abortus N 16/4 и не уступает живой вакцине из штамма B.abortus N 19.
Пример 4. Определяют реактогенность адъювант-вакцины из штамма B.abortus ВГНКИ N КВ 17/100 (серия N 1) в опыте на телках трех-четырех месячного возраста в сравнении с адъювант-вакциной из штамма B.meliitensis N "Невский-13". Каждую вакцину вводят 10 телкам под кожу в область подгрудка в дозе 3 см3. У вакцинированных животных ежедневно в течение 10 дней измеряют температуру тела и площадь припухлости в месте введения вакцины.
У животных, иммунизированных адъювант-вакциной из штамма B.abortus ВГНКИ N КВ 17/100, температура тела повышается на 0,8-1,0oС и нормализуется к 5-6 дню после вакцинации, отек в месте введения вакцины не превышает 80 см2 и начинает уменьшаться с 8-10 дня. В группе животных, иммунизированных адъювант-вакциной из штамма B.melitensis N "Невский-13", температура тела повышалась в среднем на 1,2-1,5oС и приходила в норму к 7-9 дню. Отек тканей в месте введения вакцины в среднем 100-120 см3. Заметное уменьшение величины отека отмечают через 15-20 дней после иммунизации.
Таким образом, испытанную вакцину из штамма B.abortus ВГНКИ N КВ 17/100 можно отнести к слабореактогенным масляным адъювантвакцинам.
Пример 5. Определяют антигенные свойства адъювант-вакцины из штамма B. abortus ВГНКИ N КВ 17/100 (серия 2) в опыте на телках трех-четырех месячного возраста. Вакцину вводят под кожу в область подгрудка в дозе 3 см3 42 телкам. Через 15 и 30 дней после иммунизации у животных берут кровь и исследуют в РА и РСК с единым бруцеллезным антигеном (S-антиген).
Все животные иммунизированные адъювант-вакциной не реагируют на бруцеллез. Пример 6. Определяют антигенные свойства адъювант-вакцины из штамма B. abortus ВГНКИ N КВ 17/100 (серия 3) в опыте на телках 14-17-месячного возраста, ранее иммунизированных живой слабоагглютиногенной вакциной из штамма B.abortus N 82. Адъювант-вакцину в дозе 3 см3 вводят под кожу в область подгрудка 70 телкам. Через 15 и 30 дней после иммунизации у животных берут кровь и исследуют на бруцеллез в РА и РСК с единым бруцеллезным антигеном.
Все животные ревакцинированные адъювант-вакциной не реагируют на бруцеллез.
Пример 7. Определяют эффективность адъювант-вакцины из штамма B.abortus ВГНКИ N КВ 17/100 для профилактики бруцеллеза крупного рогатого скота в условиях контролируемого эпизоотологического опыта.
Телок трех-четырех месячного возраста (пример 5) и 14-17-месячного возраста (пример 6), иммунизированных адъювант-вакциной из штамма B.abortus ВГНКИ N КВ 17/100, содержат в условиях хозяйства неблагополучного по бруцеллезу рогатого скота, обеспечивающих контакт с 21 коровой больной бруцеллезом.
Иммунизированные адъювант-вакциной животные не заболевают бруцеллезом в течение шести месяцев, что указывает на высокую эффективность препарата.
Пример 8. Определяют возможность использования адъювант-вакцины из штамма B.abortus ВГНКИ N КВ 17/100 для провокации синтеза специфических антител у больных бруцеллезом коров, не реагирующих в серологических реакциях, принятых для диагностики бруцеллеза. Коров, ранее реагировавших на бруцеллез (в РА и РСК) и утративших титры в серологических реакциях, принятых для диагностики бруцеллеза, иммунизируют адъювант-вакциной из штамма B.abortus КВ 17/100 в дозе 3 см3. Вакцину вводят под кожу в область подгрудка. Через 15 и 3 дней после иммунизации у животных берут кровь и исследую сыворотку в РА и РСК.
После иммунизации животные с хронической формой бруцеллеза положительно реагируют в серологических реакциях в диагностических титрах и идентифицируются как больные.
Таким образом, адъювант-вакцина из штамма B.abortus КВ 17/100 провоцирует появление положительных серологических реакций у нереагирующих на бруцеллез больных животных, что способствует скорейшему выздоровлению больных бруцеллезом животных.
Использование адъювант-вакцины на основе нового штамма B.abortus ВГНКИ N КВ 17/00 в ветеринарной практике позволит повысить эффективность мероприятий по борьбе с бруцеллезом крупного рогатого скота.
| название | год | авторы | номер документа |
|---|---|---|---|
| ШТАММ BRUCELLA ABORTUS, ИСПОЛЬЗУЕМЫЙ ДЛЯ ИЗГОТОВЛЕНИЯ ДИАГНОСТИЧЕСКИХ И ПРОФИЛАКТИЧЕСКИХ БИОПРЕПАРАТОВ ПРОТИВ БРУЦЕЛЛЕЗА ЖИВОТНЫХ | 1997 |
|
RU2130068C1 |
| ШТАММ БАКТЕРИЙ BRUCELLA ABORTUS, ИСПОЛЬЗУЕМЫЙ ДЛЯ ИЗГОТОВЛЕНИЯ ДИАГНОСТИЧЕСКИХ И ПРОФИЛАКТИЧЕСКИХ БИОПРЕПАРАТОВ ПРОТИВ БРУЦЕЛЛЕЗА ЖИВОТНЫХ | 1999 |
|
RU2149183C1 |
| ШТАММ БАКТЕРИЙ BRUCELLA ABORTUS, ИСПОЛЬЗУЕМЫЙ ДЛЯ ОПРЕДЕЛЕНИЯ ИММУНОГЕННОЙ АКТИВНОСТИ ВАКЦИН ПРОТИВ БРУЦЕЛЛЕЗА СЕЛЬСКОХОЗЯЙСТВЕННЫХ ЖИВОТНЫХ | 1999 |
|
RU2149184C1 |
| ВАКЦИНА ПРОТИВ БРУЦЕЛЛЕЗА СЕЛЬСКОХОЗЯЙСТВЕННЫХ ЖИВОТНЫХ | 1992 |
|
RU2026343C1 |
| ВАКЦИНА ПРОТИВ БРУЦЕЛЛЕЗА СЕЛЬСКОХОЗЯЙСТВЕННЫХ ЖИВОТНЫХ | 1992 |
|
RU2026081C1 |
| АССОЦИИРОВАННАЯ ВАКЦИНА ПРОТИВ ЛЕПТОСПИРОЗА И КАМПИЛОБАКТЕРИОЗА КРУПНОГО РОГАТОГО СКОТА | 1992 |
|
RU2021818C1 |
| ВАКЦИНА ПРОТИВ ТРИХОФИТИИ ЖИВОТНЫХ | 1992 |
|
RU2018321C1 |
| ШТАММ ГРИБА TRICHOPHYTON VERRUCOSUM, ИСПОЛЬЗУЕМЫЙ ДЛЯ ИЗГОТОВЛЕНИЯ ВАКЦИНЫ ПРОТИВ ДЕРМАТОФИТОЗОВ ЖИВОТНЫХ | 1994 |
|
RU2074251C1 |
| ВАКЦИНА "МИКРОДЕРМ" ПРОТИВ ДЕРМАТОФИТОЗОВ ЖИВОТНЫХ | 1994 |
|
RU2084240C1 |
| СПОСОБ ДИАГНОСТИКИ БРУЦЕЛЛЕЗА | 1999 |
|
RU2152035C1 |

Вакцина предназначена для профилактики бруцеллеза крупного рогатого скота. Вакцина содержит в качестве антигена инактивированную с гидратом окиси алюминия бактериальную массу штамма B.abortus ВГНКИ N КВ 17/100. Вакцина содержит также неполный адьювант Фрейнда и физиологический раствор. Использование новой вакцины в ветеринарной практике позволяет в 1,5 - 2 раза повысить эффективность противобруцеллезных мероприятий за счет повышения иммуногености и снижения агглютиногенности вакцины. 2 табл.
Вакцина против бруцеллеза крупного рогатого скота, содержащая инактивированный антиген бруцелл, неполный адъювант Фрейнда и физиологический раствор, отличающаяся тем, что она в качестве инактивированного антигена бруцелл содержит инактивированную с гидратом окиси алюминия бактериальную массу штамма Brucella abortus ВГНКИ N КВ 17/100 с концентрацией 300 - 400 • 109 микробных клеток в 1 см3 при следующем соотношении компонентов, об.%:
Инактивированная с гидратом окиси алюминия бактериальная масса штамма Вrucella abortus ВГНКИ N КВ 17/100 с концентрацией 300 - 400 • 109 микробных клеток в 1 см3 - 40 - 50
Неполный адъювант Фрейнда - 45 - 55
Физиологический раствор - Остальноел
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Cyung Y.S., Hall W.T.K | |||
| and Simmons GC | |||
| Способ изготовления электрических сопротивлений посредством осаждения слоя проводника на поверхности изолятора | 1921 |
|
SU19A1 |
| Journal, Vol | |||
| Приспособление для разматывания лент с семенами при укладке их в почву | 1922 |
|
SU56A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| RU, патент, 2026343, кл | |||
| Устройство для сортировки каменного угля | 1921 |
|
SU61A1 |
Авторы
Даты
1998-04-10—Публикация
1997-11-12—Подача