Изобретение относится к области биотехнологии и биохимии и касается репортерной системы, позволяющей с высокой точностью зарегистрировать взаимодействия исследуемых белков в клетке любых животных, растений, грибов и бактерий либо зарегистрировать явление транспортировки белка из одной клетки в другую.
Специфические белковые взаимодействия лежат в основе всех важнейших биологических процессов, включая сложнейшие механизмы воспроизведения генетического материала клетки и передачи сигнала.
Большинство современных методов изучения белок-белковых взаимодействий проводится с использованием биохимических методов in vitro, таких как иммунопреципитация, хроматографическое кофракционирование или система двойной гибридизации в дрожжах. Однако такие подходы не гарантируют абсолютной точности полученных результатов, в особенности, если проводится изучение белок-белковых взаимодействий в клетках млекопитающих. Таким образом, исследования in vivo, не приводящие к разрушению структур клетки и не нарушающие ее метаболизма, позволяют приблизить условия эксперимента к физиологическим и, как следствие, получить более корректные и точные данные.
Взаимодействие белков в клетках может быть детектировано с помощью рекомбинантных репортерных конструкций. Такие репортерные системы представляют собой генетические конструкции, в которых репортерный ген разделен на две функционально неактивные половины. Каждая из частей экспрессируется на разных лентивирусных векторах в одной рамке считывания с одним из исследуемых белков. Если исследуемые белки способны взаимодействовать друг с другом, то их объединение приведет к сближению частей репортерного белка с восстановлением его функциональной активности.
Такие репортерные системы могут применяться при исследовании белок-белковых взаимодействий в различных культурах клеток млекопитающих. Для этого в исследуемые клетки, с помощью процедуры трансфекционного переноса вводятся соответствующие репортерные конструкции. Наиболее распространена процедура транзиторной трансфекции с поддержанием культуры клеток на антибиотике. Однако напрямую уровень экспрессии с плазмид слишком высок, что не соответствует физиологическим условиям. К тому же, высокая концентрация половин репортерных белков неминуемо приведет к их неспецифическому взаимодействию. Таким образом, для применения репортерного подхода детекции белок-белковых взаимодействий требуется создание репортерных векторов, позволяющих проводить их высокоэффективное и контролируемое введение в геном клетки.
В качестве таких векторов могут выступать конструкции на основе лентивирусов (сем. retroviridae - ретровирусы), которые способны эффективно и быстро встраиваться в геном клеток и поддерживать однородную экспрессию введенных в них репортерных кассет.
За последние годы рекомбинантные векторы на основе лентивирусов нашли широкое применение как в фундаментальных исследованиях, так и в медицинской практике. Лентивирусы способны доставлять значительное количество генетического материала в клетку хозяина и обладают уникальной среди ретровирусов способностью реплицироваться в неделящихся клетках, что делает лентивирусы удобным вектором для доставки целевой ДНК.
В частности, перенос генов с использованием лентивирусных векторных конструкций описан в Romano G. Current development of lentiviral-mediated gene transfer. Drug News Perspect. 2005 Mar; 18(2): 128-34; Vigna E, Naldini L. Lentiviral vectors: excellent tools for experimental gene transfer and promising candidates for gene therapy, J Gene Med. 2000 Sep-Oct; 2(5):308-16.
Известна лентивирусная репортерная векторная система для измерения активности ключевых транскрипционных факторов, отражающих функциональное состояние сигнальных путей клетки (патент РФ 2420584). Система содержит маркерный репортерный ген, экспрессия которого находится под контролем специфического промотора, содержащего минимальный промотор цитомегаловируса человека и соответствующий транскрипционному фактору респонсивный элемент, а также ген устойчивости к антибиотикам, которая в качестве маркерного репортерного гена содержит ген бета-галактидазы или EGFP, экспрессия которых находится под контролем промотора, содержащего в качестве р53-респонсивного элемента последовательность SEQ ID NO: 1, включающую шесть копий 20-членного сайта связывания р53 из гена CDKN1A, одну копию высокоаффинного консенсусного сайта связывания p53-CON, сегмент кластера генов рибосомных РНК, содержащего пять сайтов связывания р53, а в качестве гена устойчивости к антибиотикам содержит ген puro.
В международной заявке WO 2006/089001, опубл. 24.08.2006 раскрываются лентивирусные векторы для генотерапии, лечения рака, производства рекомбинантных протеинов, таких как антитела и вакцины, и для других терапевтических целей. Отмечается использование векторных систем для открытия новых белок-белковых взаимодействий в клетках млекопитающих с помощью технологии с двумя гибридами. Лентивирусные векторы, например, включают последовательности хелперов и/или минимально функциональные последовательности LTR, которые могут использоваться для создания высокоэффективных векторов трансдукции. Данное решение может быть указано в качестве ближайшего аналога-прототипа.
Технической задачей, решаемой авторами, являлось создание универсальной лентивирусной репортерной системы для детекции и изучения белок-белковых взаимодействий в живой клетке.
Задача решается описанными плазмидными лентивирусными репортерными конструкциями, содержащими части гена люциферазы, выделенной из светлячка (род. Photinus) Photinus pyralis.
Техническим результатом изобретения является создание системы, позволяющей с высокой точностью зарегистрировать взаимодействия исследуемых белков в клетке либо зарегистрировать явление транспортировки белка из одной клетки в другую.
В основе изобретения лежат разработанные авторами плазмидные лентивирусные ДНК векторы, включающие: в первом случае, промоторный регион цитомегаловируса (CMV), обеспечивающий стабильный уровень экспрессии, сайт для клонирования открытых рамок считывания последовательностей генов целевых белков, N- концевую часть последовательности гена люциферазы Photinus pyralis (SEQ ID NO 1). Во втором случае, сайт для клонирования последовательностей генов целевых белков перемещен на 3'-конец экспрессируемой кассеты, а С- концевая часть люциферазы Photinus pyralis перемещена на 5'-конец (SEQ ID NO 2).
Последовательность конструкции pCMV-MCS-NLuc-NP-Puro

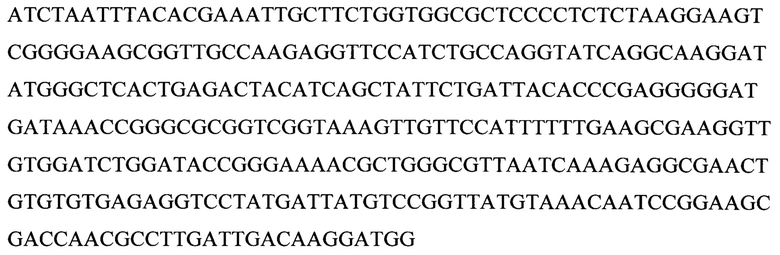
Последовательность конструкции pCMV-CLuc-MCS-NP-Puro

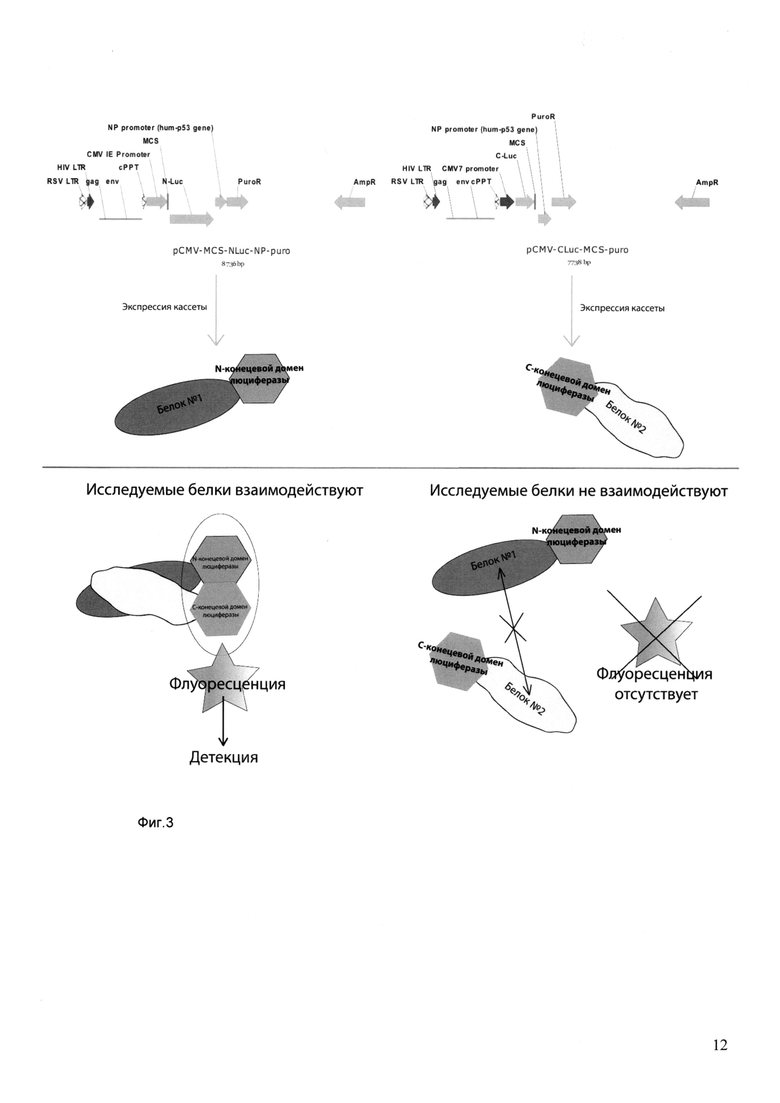
При совместной экспрессии данных генетических конструктов в заданной клеточной системе происходит синтез химерных белковых молекул, состоящих в первом случае из исследуемого белка №1 и N-концевого домена люциферазы, а во втором из исследуемого белка №2 и С-концевого домена люциферазы. Разделенная на два домена люцифераза не обладает ферментативной активностью и не способна катализировать реакцию превращения люциферина в оксилюциферин с выделением фотонов света. При сближении и взаимодействии исследуемых белков произойдет взаимодействие функционально неактивных доменов люциферазы с последующим восстановлением функционально активного фермента. Таким образом, при дальнейшем введении люциферина (субстрат для люциферазы) в клетки станет возможным детектирование излучения фотонов света. С другой стороны, если исследуемые белки окажутся не способны взаимодействовать друг с другом, восстановления люциферазной активности не произойдет и излучения не будет.
Оптическая визуализация позволяет наблюдать за распределением биомолекул и молекулярными событиями в живых клетках, при помощи меток, испускающих фотоны оптического диапазона. Фотоны в таких системах генерируются в процессе явлений флуоресценции или биолюминесценции. Биолюминесценция основывается на химических процессах, при которых освобождающаяся энергия выделяется в форме света. Реакция протекает при окислении молекул субстрата специальным ферментом - люциферазой. Люцифераза имеет очень высокое сродство к своему субстрату, что исключает какие-либо фоновые излучения. К тому же, в клетках млекопитающих нет белков, гомологичных люциферазе, что также полностью исключает возникновение неспецифических реакций. Таким образом, биолюминесценция является наиболее подходящим, высокочувствительным методом визуализации белок-белковых взаимодействий в живых клетках.
Объектом изобретения является репортерная система, которая включает в себя две генетические конструкции (в виде плазмидной ДНК).
Структура плазмид:
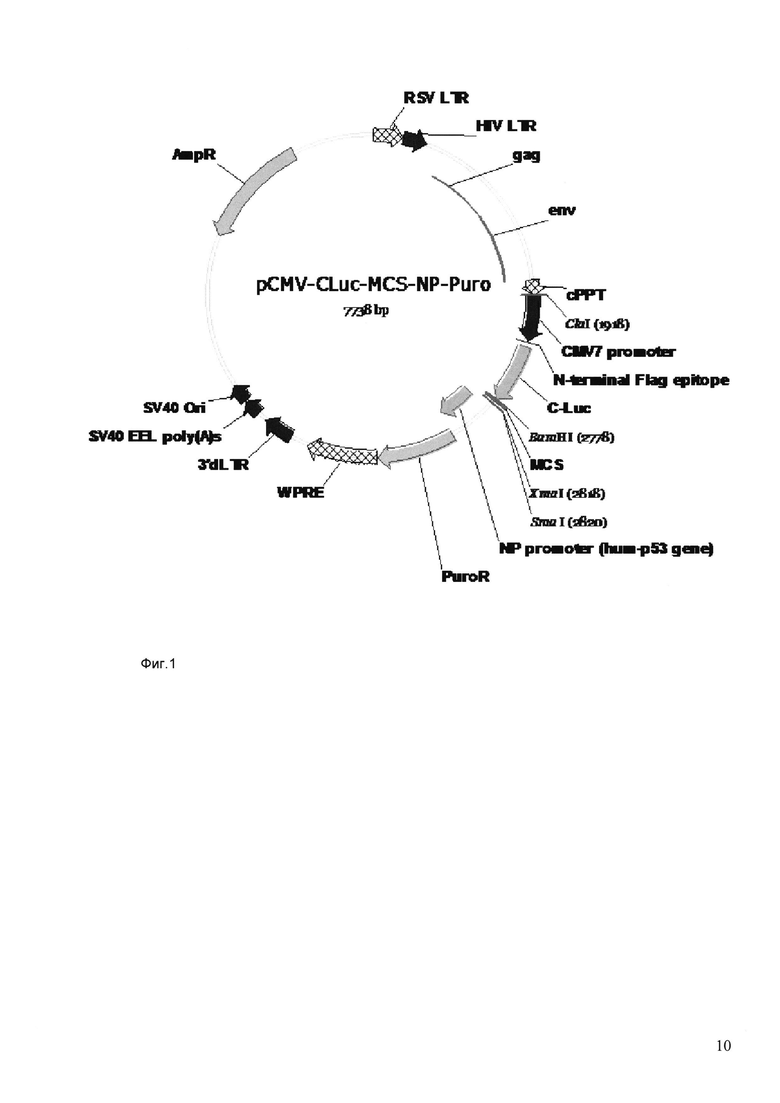
Плазмида №1 (фиг. 1)
- 5' и 3' LTR - длинные концевые повторы, последовательности, используемые вирусом для встраивания собственного генома в геном хозяина, путем гомологичной рекомбинации.
- Центральный полипуриновый тракт (сРРТ) - обеспечивает проникновение целевой последовательности в ядра митотически неактивных клеток.
- Посттранскрипционный регуляторый элемент (WPRE) - регуляторная область, усиливающая экспрессию целевой последовательности.
- Козак - консенсусная последовательность, необходимая для посадки рибосом и инициации трансляции мРНК.
- CMV промотер - промотерный регион цитомегаловируса, обеспечивает высокий уровень транскрипции целевой последовательности
- N-Luc - последовательность N-концевого домена люциферазы светлячка Photinus pyralis
- MCS (multiple cloning site) – сайт, содержащий последовательности узнавания ферментами рестрикции-модификации. По данным сайтам проводится клонирование исследуемых белков.
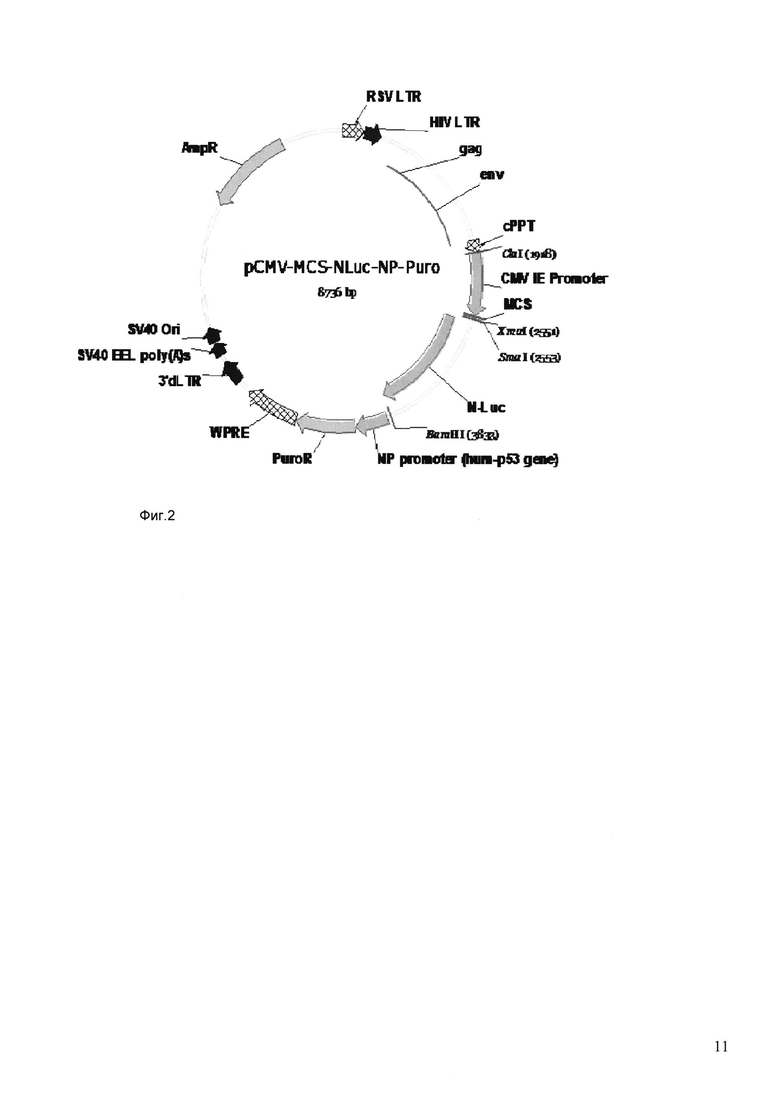
Плазмида №2 (фиг. 2)
Плазмидная ДНК №2 содержит все те же самые последовательности, что и конструкция №1 кроме:
- C-Luc - С-концевой домен люциферазы Photinus pyralis
Для селекции клеток, содержащих интегрированные кассеты, в плазмиды введена последовательность устойчивости к антибиотику - пуромицину.
В качестве целевых белков могут использоваться любые белковые молекулы, взаимодействие которых необходимо проверить в живых клетках, а также белковые молекулы, транслокацию которых из одной клетки в другую необходимо отследить.
На фиг. 1 приведена карта плазмиды 1.
На фиг. 2 приведена карта плазмиды 2.
На фиг. 3 приведена схема работы репортерной системы.
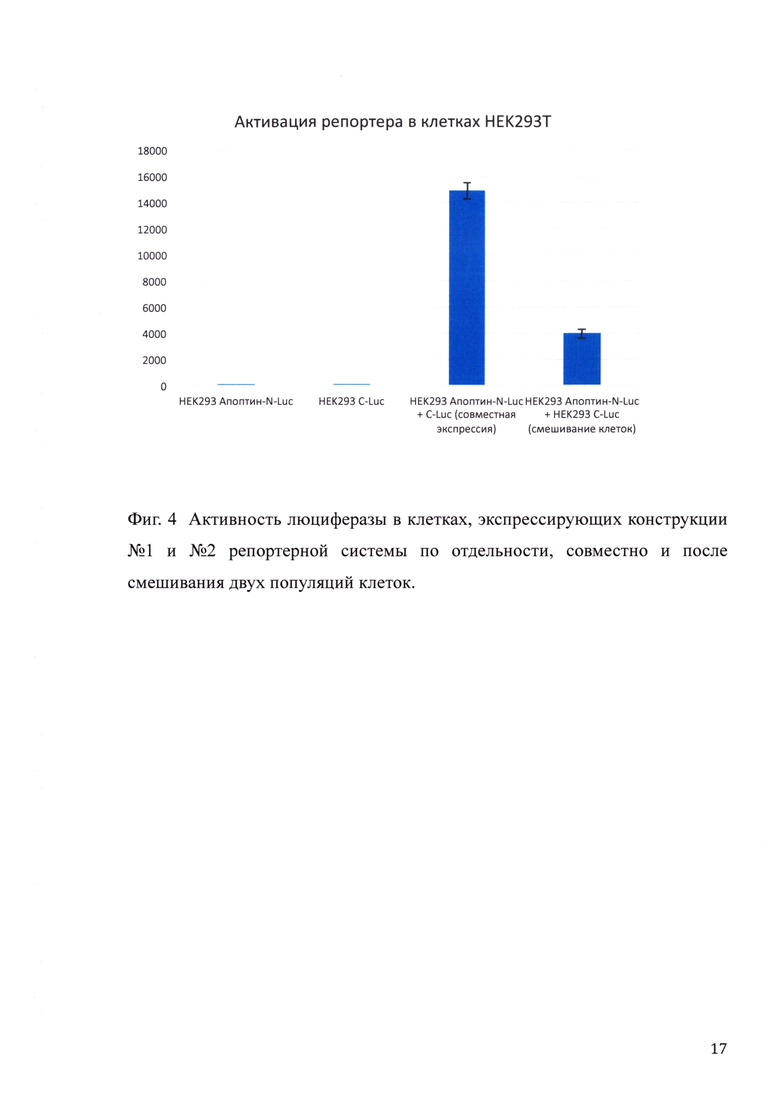
Изобретение, представленное в п. 1 формулы изобретения, было, в частности, протестировано на белке апоптине. Апоптин - неструктурный белок вируса анемии кур, который отвечает за гибель клеток при вирусной инфекции. Изучение цитолитической активности выявило высокую степень избирательности апоптина, поскольку он способен индуцировать апоптоз опухолевых и трансформированных клеток различного видового и органного происхождения, практически не влияя на жизнеспособность нормальных клеток. Известно, что в опухолевых клетках апоптин локализуется преимущественно в ядре, в то время как в нормальных клетках он находится в цитоплазме, нестабилен и быстро деградирует. Для определения возможности межклеточной транслокации онкотоксического белка апоптина использовалась описанная в настоящем изобретении репортерная система на основе люциферазы. Для этого в лентивирусный конструкт №1, перед нуклеотидной последовательностью N-Luc был клонирован ген, кодирующий белок апоптин. Для осуществления секреции и транспортировки апоптина в клетку-реципиент, перед геном апоптина была также встроена последовательность, кодирующая сигнал секреции искусственного происхождения - HMMsp38 и последовательность сигнала трансдукции - ТАТ (трансактиватор транскрипции ВИЧ). Лентивирусные конструкции №1 и №2 вводились в две группы клеток трансформированного эпителия почки человека (клетки НЕК293Т) с помощью наборов для липофекции фирмы Invitrogene (LipofectAMINE Plus). Одновременно с ленивирусными конструкциями вводили три упаковывающие плазмиды: pREV, pGAG и pVSV-G, которые кодируют соответственно обратную транскриптазу, белок GAG вируса иммунодефицита человека (ВИЧ1) и G-белок вируса везикулярного стоматита. Оптимальное соотношение плазмид при трансфекции, дающее максимальные титры рекомбинантных вирионов, определяли экспериментально (вектор:pREV:pGAG:pVSV-G=2:4:2:1). Рекомбинантные вирионы собирали в течение 72 часов с интервалами в 8 часов. Супернатанты объединяли и вирионы осаждали 12% полиэтиленгликолем при 4°С 12 часов с последующим центрифугированием в течение 10 минут при 5000 об/мин. Вирионы затем суспендировали в свежей среде (1/10 от исходного объема) и фильтровали через стерилизующую насадку для шприца. Стерильные вирионы расфасовывали на порции и хранили в заморозке при -70°С. Для введения конструкций в клетки с целью экспрессии целевого белка апоптина были использованы перевиваемые клетки почки эмбриона человека НЕК293Т. Одна группа клеток была инфицирована вирионами, несущими конструкцию с последовательностями, кодирующими N-Luc и апоптин, вторая группа клеток была инфицирована вирионами, несущими конструкцию, кодирующую последовательность C-Luc. Спустя 72 часа обе группы клеток были подвергнуты селекции на антибиотике пуромицине в течение еще 72 часов для элиминации из популяции не получивших конструкции клеток и тем самым обогащения популяции. Далее две группы клеток были смешаны в равных количествах и спустя 24 часа измерена люциферазная активность с помощью набора Luciferase Assay System (Promega). В результате экспрессии конструкции №1 в первой популяции клеток (клетки доноры) происходила наработка белка апоптина, "сшитого" с N-концом люциферазы, его транспорт во внеклеточное пространство с последующим проникновением в акцепторные клетки, содержащие С-конец люциферазы, в результате чего происходило восстановление полноценной люциферазы, способной катализировать окисление субстрата (люциферина) с выделением фотонов света (фиг. 4). Таким образом, с применением настоящего изобретения была показана межклеточная транслокация белка апоптина.
Изобретение относится к области биотехнологии и биохимии, конкретно к векторной конструкции. Описанная репортерная система на основе лентивирусных репортерных конструкций позволяет с высокой точностью зарегистрировать взаимодействия исследуемых белков в клетке животного, растения, гриба и бактерии, а также зарегистрировать явление транспортировки белка из одной клетки в другую. Изобретение основано на двух генетических конструкциях в виде плазмидной ДНК, содержащих части гена люциферазы, выделенной из светлячка (род. Photinus) Photinus pyralis. 2 з.п. ф-лы, 4 ил.
1. Лентивирусная репортерная система для детекции белок-белковых взаимодействий в живой клетке на основе двух генетических конструкций в виде плазмидных ДНК, содержащих части гена люциферазы, выделенной из светлячка (род. Photinus) Photinus pyralis, характеризующаяся тем, что включает:
плазмидный лентивирусный репортерный вектор, в состав которого входят 5' и 3' LTR-длинные концевые повторы, последовательности, используемые вирусом для встраивания собственного генома в геном хозяина путем гомологичной рекомбинации, центральный полипуриновый тракт (сРРТ), посттранскрипционный регуляторный элемент (WPRE), Козак – консенсусная последовательность для посадки рибосом и инициации трансляции мРНК, CMV промотер – промотерный регион цитомегаловируса, C-Luc – последовательность, кодирующая С-концевой домен люциферазы светлячка Photinus pyralis и MCS (multiple cloning site) – сайт, содержащий последовательности узнавания ферментами рестрикции-модификации, куда клонируется ген, кодирующий исследуемый белок;
плазмидный лентивирусный репортерный вектор, в состав которого входят 5' и 3' LTR – длинные концевые повторы, последовательности, используемые вирусом для встраивания собственного генома в геном хозяина путем гомологичной рекомбинации, центральный полипуриновый тракт (сРРТ), посттранскрипционный регуляторный элемент (WPRE), Козак – консенсусная последовательность для посадки рибосом и инициации трансляции мРНК, CMV промотер – промотерный регион цитомегаловируса, N-Luc – последовательность, кодирующая N-концевой домен люциферазы светлячка Photinus pyralis и MCS (multiple cloning site) – сайт, содержащий последовательности узнавания ферментами рестрикции-модификации, куда клонируется ген, кодирующий исследуемый белок.
2. Лентивирусная репортерная система по п. 1, характеризующаяся тем, что в последовательность составляющих ее генетических конструкций включена последовательность гена рас, кодирующего пуромицин-N-ацетил-трансферазу, обеспечивающую устойчивость к селективному антибиотику - пуромицину.
3. Репортерная система по п. 1, характеризующаяся тем, что используется для детекции белок-белковых взаимодействий в клетках и позволяет зарегистрировать с высокой точностью взаимодействия исследуемых белков как внутри клетки, так и между клетками, а также явление транспортировки белка из одной клетки в другую.
| ИДЕНТИФИКАЦИЯ МОЛЕКУЛ, МОДУЛИРУЮЩИХ БЕЛОК-БЕЛКОВОЕ ВЗАИМОДЕЙСТВИЕ | 2008 |
|
RU2476891C2 |
| ЛЕНТИВИРУСНАЯ РЕПОРТЕРНАЯ ВЕКТОРНАЯ СИСТЕМА ДЛЯ ИЗМЕРЕНИЯ АКТИВНОСТИ КЛЮЧЕВЫХ ТРАНСКРИПЦИОННЫХ ФАКТОРОВ, ОТРАЖАЮЩИХ ФУНКЦИОНАЛЬНОЕ СОСТОЯНИЕ СИГНАЛЬНЫХ ПУТЕЙ КЛЕТКИ | 2009 |
|
RU2420584C1 |
| VIGNA E | |||
| et al., Lentiviral vectors: excellent tools for experimental gene transfer and promising candidates for gen therapy | |||
| The journal of gene medicine, 2000, v | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Распределительный механизм для паровых машин | 1921 |
|
SU308A1 |
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| МУТАНТНАЯ ЛЮЦИФЕРАЗА (ВАРИАНТЫ), ДНК, КОДИРУЮЩАЯ УКАЗАННУЮ ЛЮЦИФЕРАЗУ, И ВЕКТОР ДЛЯ ЭКСПРЕССИИ УКАЗАННОГО БЕЛКА | 1996 |
|
RU2210594C2 |
Авторы
Даты
2017-12-21—Публикация
2015-12-29—Подача