Область техники
Настоящее описание относится к способам лечения диабета I типа или диабета II типа у млекопитающих, включающим введение млекопитающему инсулина и соединения феноксипиримидинона или его фармацевтически приемлемых солей, и к их составам.
Предшествующий уровень техники
Диабет представляет собой наиболее распространенное заболевание эндокринной системы и развивается, когда уровень сахара крови в организме постоянно находится выше нормальных значений. Он поражает более 23 миллионов людей только в США. Диабет представляет собой заболевание, объединяющее и неспособность организма создавать инсулин (диабет I типа) и неспособность организма отвечать на действие инсулина (диабет II типа). Он также может развиться во время беременности. Инсулин является одним из основных гормонов, которые регулируют уровень сахара крови и позволяют организму использовать сахар для получения энергии. При развитии диабета II типа симптомы включают необычную жажду, частые мочеиспускания, нарушение зрения или чрезмерную усталость. Диабет I типа развивается из-за разрушения инсулин-продуцирующих клеток поджелудочной железы, бета-клеток, иммунной системой. Люди с диабетом I типа не производят инсулин и должны получать инъекции инсулина для контроля сахара крови. Диабет I типа наиболее часто развивается у людей в возрасте до 20, но может развиться в любом возрасте. Следовательно, соединения и композиции, которые могут быть использованы для лечения диабета I типа и/или II типа, однозначно необходимы.
Сущность изобретения
Настоящее описание обеспечивает способы лечения диабета I типа или диабета II типа у млекопитающего, включающие введение млекопитающему, нуждающемуся в этом, эффективного количества инсулина и эффективного количества соединения по формуле I:
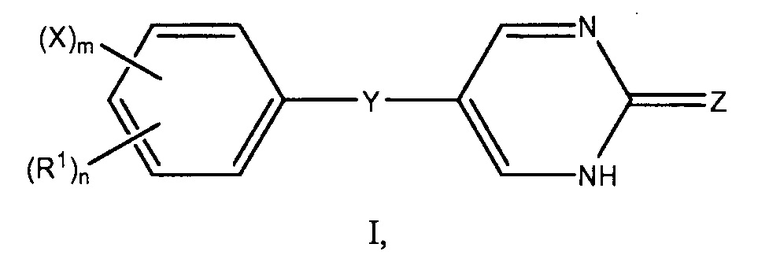
или его фармацевтически приемлемой соли, где: R1 представляет собой алкильную группу; X представляет собой галоген; Y представляет собой O, S, или NH; Z представляет собой O или S; n является целым числом от 0 до 5 и m является 0 или 1, где m + n меньше или равно 5.
Настоящее описание также предоставляет способы лечения диабета I типа или диабета II типа у млекопитающего, включающие введение млекопитающему, нуждающемуся в этом, эффективного количества инсулина и эффективного количества соединения по формуле II:
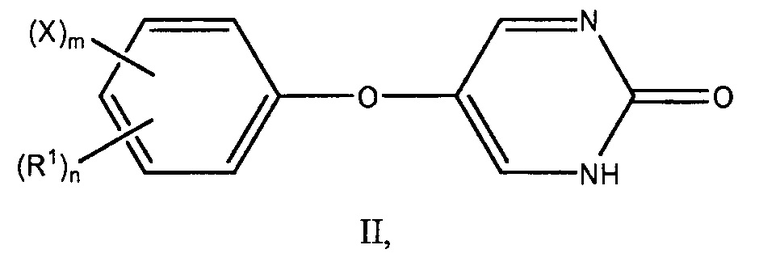
или его фармацевтически приемлемой соли, где: R1 представляет собой алкильную группу; X представляет собой галоген; и n является целым числом от 0 до 5, и m является 0 или 1, где m + n меньше или равно 5.
Настоящее описание также предоставляет способы лечения диабета I типа или диабета II типа у млекопитающего, включающие введение млекопитающему, нуждающемуся в этом, эффективного количества инсулина и эффективного количества соединения по формуле III:
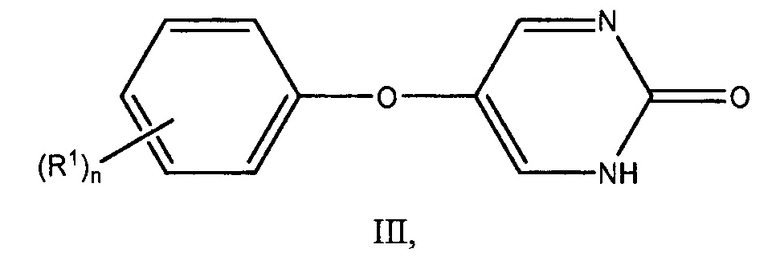
или его фармацевтически приемлемой соли, где: R1 представляет собой алкильную группу; и n является целым числом от 0 до 5.
Настоящее описание также предоставляет способы лечения диабета I типа или диабета II типа у млекопитающего, включающие введение млекопитающему, нуждающемуся в этом, эффективного количества инсулина и эффективного количества соединения по формуле IV:
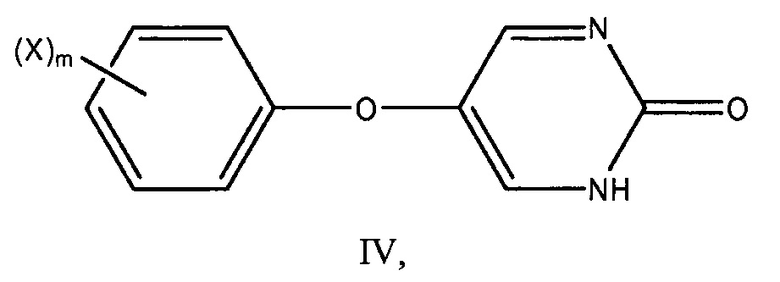
или его фармацевтически приемлемой соли, где: X представляет собой галоген и m равно 0 или 1.
Настоящее описание также предоставляет способы лечения диабета I типа или II типа у млекопитающего, включающие введение млекопитающему, нуждающемуся в этом, эффективного количества инсулина и эффективного количества соединения:
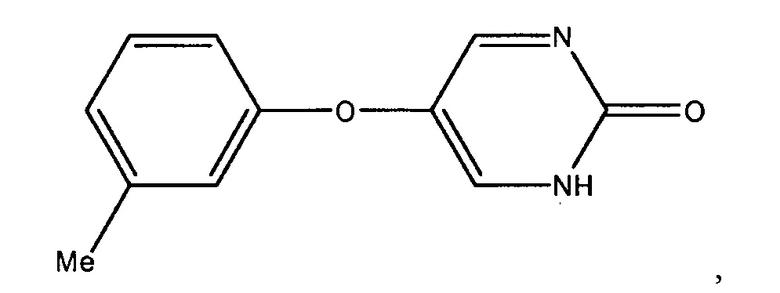
или его фармацевтически приемлемой соли.
Настоящее описание также предоставляет способы лечения диабета I типа или II типа, включающие введение млекопитающему, нуждающемуся в этом, эффективного количества инсулина и эффективного количества соединения:
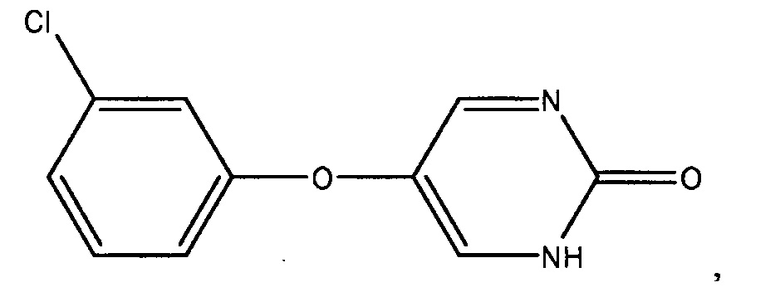
или его фармацевтически приемлемой соли.
Настоящее описание также предоставляет составы для перорального введения в форме таблетки, гелевой капсулы или капсулы, включающей инсулин и от около 1 мг до около 1000 мг соединения:
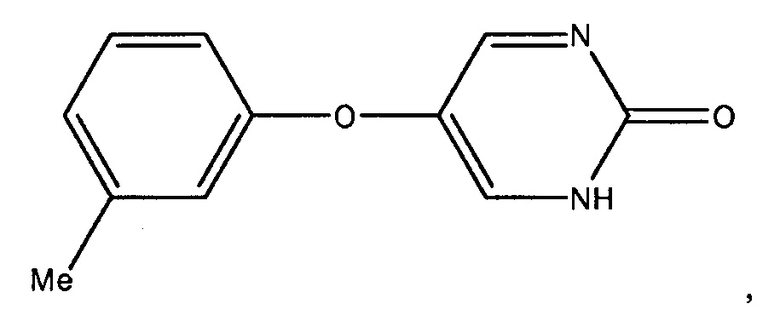
или его фармацевтически приемлемой соли, где состав для перорального введения предназначен для применения в лечении или профилактике диабета I типа или II типа.
Настоящее описание также предоставляет составы для перорального введения в форме таблетки, гелевой капсулы или капсулы, включающей инсулин и от около 1 мг до около 1000 мг соединения:
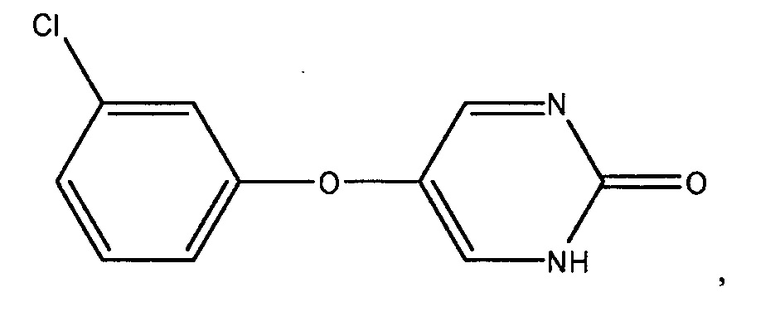
или его фармацевтически приемлемой соли, где состав для перорального введения предназначен для применения в лечении или профилактике диабета I типа или II типа.
Настоящее описание также предоставляет состав, включающий любое одно или более из вышеуказанных соединений феноксипиримидинона, или его фармацевтически приемлемых солей, и инсулин для лечения у млекопитающего диабета I типа или II типа.
Настоящее описание также предоставляет состав, включающий любое одно или более из вышеуказанных соединений феноксипиримидинона, или его фармацевтически приемлемых солей, и инсулин для применения в получении лекарственного препарата для лечения у млекопитающего диабета I типа или диабета II типа.
Настоящее описание также предоставляет применение любого одного или более из вышеуказанных соединений феноксипиримидинона, или их фармацевтически приемлемых солей, и инсулина для лечения у млекопитающего диабета I типа или II типа.
Настоящее описание также предоставляет применение любого одного или более из вышеуказанных соединений феноксипиримидинона или их фармацевтически приемлемых солей, и инсулина для применения в получении лекарственного препарата для лечения у млекопитающего диабета I типа или II типа.
Краткое описание чертежей
На фиг. 1 показаны результаты совместного введения соединения по формуле IV с инсулином, усиливающего снижение глюкозы крови в ответ на действие инсулина. *p<0,05; при сравнении инсулина с совместным введением инсулина/соединения.
На фиг. 2 показаны результаты совместного введения соединения по формуле IV с инсулином, усиливающего снижение глюкозы крови в ответ на действие инсулина. *p<0,05; **p<0,01 при сравнении инсулина с совместным введением инсулина/соединения.
На фиг. 3 показаны результаты введения соединения по формуле IV, потенцирующие и пролонгирующие инсулин-опосредованное снижение глюкозы крови. *p<0,05 при сравнении с лечением отдельно инсулином. ***p<0,001 при сравнении с лечением отдельно инсулином. Данные представлены как среднее +- стандартная ошибка среднего значения. Данные анализировали посредством двухфакторного дисперсионного анализа с последующей поправкой Бонферрони для множественных сравнений.
Описание вариантов осуществления изобретения
Если не указано иначе, все технические и научные термины имеют то же значение, как обычно понимает обычный специалист в области техники, к которой принадлежат описанные варианты осуществления изобретения.
Как используется в настоящем описании, термины "a" или "an" обозначают, что, "по меньшей мере, один" или "один или более" если контекст четко не указывает иного.
Как используется в настоящем описании, термин "около" обозначает, что числовое значение является приблизительным и небольшие вариации существенно не влияют на осуществление описанных вариантов осуществления изобретения. Когда используется числовой предел, если иначе не указано контекстом, "около" обозначает, что числовое значение может варьировать на ±10% и оставаться в рамках описанных вариантов осуществления изобретения.
Как используется в настоящем описании, термин "алкенил" обозначает линейную или разветвленную алкильную группу, имеющую одну или более двойных связей углерод-углерод и 2-20 атомов углерода, включая, но не ограничиваясь этим, этенил, 1-пропенил, 2-пропенил, 2-метил-1-пропенил, 1-бутенил, 2-бутенил, и подобные. В некоторых вариантах осуществления изобретения алкенильная цепь имеет от 2 до 10 атомов углерода в длину, от 2 до 8 атомов углерода в длину, от 2 до 6 атомов углерода в длину, или от 2 до 4 атомов углерода в длину.
Как используется в настоящем описании, термин "алкокси" обозначает линейную или разветвленную -O-алкильную группу из 1-20 атомов углерода, включая, но не ограничиваясь этим, метокси, этокси, н-пропокси, изопропокси, т-бутокси, и подобные. В некоторых вариантах осуществления изобретения алкокси цепь имеет от 1 до 10 атомов углерода в длину, от 1 до 8 атомов углерода в длину, от 1 до 6 атомов углерода в длину, от 1 до 4 атомов углерода в длину, от 2 до 10 атомов углерода в длину, от 2 до 8 атомов углерода в длину, от 2 до 6 атомов углерода в длину или от 2 до 4 атомов углерода в длину.
Как используется в настоящем описании, термин "алкил" обозначает насыщенную углеводородную группу, которая имеет линейную или разветвленную цепь. Алкильная группа может содержать от 1 до 20, от 2 до 20, от 1 до 10, от 2 до 10, от 1 до 8, от 2 до 8, от 1 до 6, от 2 до 6, от 1 до 4, от 2 до 4, от 1 до 3, или 2 или 3 атома углерода. Примеры алкильных групп включают, но не ограничиваются этим, метил (Me), этил (Et), пропил (например, н-пропил и изопропил), бутил (например, н-бутил, т-бутил, изобутил), пентил (например, н-пентил, изопентил, неопентил), гексил, изогексил, гептил, 4,4-диметилпентил, октил, 2,2,4-триметилпентил, нонил, децил, ундецил, додецил, 2-метил-1-пропил, 2-метил-2-пропил, 2-метил-1-бутил, 3-метил-1-бутил, 2-метил-3-бутил, 2-метил-1-пентил, 2,2-диметил-1-пропил, 3-метил-1-пентил, 4-метил-1-пентил, 2-метил-2-пентил, 3-метил-2-пентил, 4-метил-2-пентил, 2,2-диметил-1-бутил, 3,3-диметил-1-бутил, 2-этил-1-бутил, и подобные.
Как используется в настоящем описании, термин "алкинил" обозначает линейную или разветвленную алкильную группу, имеющую одну или более тройных связей углерод-углерод и 2-20 атомов углерода, включая, без ограничения, ацетилен, 1-пропилен, 2-пропилен, и подобные. В некоторых вариантах осуществления изобретения алкинильная цепь имеет от 2 до 10 атомов углерода в длину, от 2 до 6 атомов углерода в длину или от 2 до 4 атомов углерода в длину.
Как используется в настоящем описании, термин "животное" включает, без ограничения, людей и нечеловекообразных позвоночных, таких как дикие, домашние и фермерские животные.
Как используется в настоящем описании, термин "арил" обозначает моноциклические, бициклические или полициклические (например, имеющие 2, 3 или 4 сшитых цикла) ароматические углеводороды. В некоторых вариантах осуществления изобретения арильные группы имеют от 6 до 20 атомов углерода или от 6 до 10 атомов углерода. Примеры арильных групп включают, без ограничения, фенил, нафтил, антраценил, фенантренил, инданил, инденил, тетрагидронафтил и подобные.
Как используется в настоящем описании, термин "арилокси" обозначает -O-арильную группу, где арил определен выше. Арилоксигруппа может быть незамещенной или замещенной одним или двумя подходящими заместителями. Арильным циклом арилоксигруппы может быть моноциклический цикл, где цикл включает 6 атомов углерода, называемый в настоящем описании как "(C6)арилокси."
Как используется в настоящем описании, термин "бензил" обозначает -CH2-фенил.
Как используется в настоящем описании, термин "карбоцикл" обозначает 5- или 6-членное, насыщенное или ненасыщенное циклическое кольцо, необязательно содержащее атомы O, S, или N, как часть кольца. Примеры карбоциклов включают, без ограничения, циклопентил, циклогексил, циклопента-1,3-диен, фенил, и любой из гетероциклов, представленных выше.
Как используется в настоящем описании, термин "носитель" обозначает разбавитель, адъювант или вспомогательное вещество, с которым вводят соединение. Фармацевтические носители могут быть жидкими, такие как вода и масла, включая таковые нефтяного, животного, растительного или синтетического происхождения, такие как арахисовое масло, соевое масло, минеральное масло, кунжутное масло и подобные. Фармацевтическими носителями также может быть солевой раствор, гуммиарабик, желатин, крахмальная паста, тальк, кератин, коллоидный диоксид кремния, мочевина и подобные. Кроме того, могут быть использованы вспомогательные, стабилизирующие, загущающие, смазывающие и красящие средства.
Как используется в настоящем описании, термин "соединение" обозначает все стереоизомеры, таутомеры и изотопы соединений, описанных в настоящем описании.
Как используется в настоящем описании, термины "включающий" (и любая форма включающего, такая как "включать", "включает", и "включенный"), "имеющий" (и любая форма имеющего, такая как "иметь" и "имеет"), "включающий" (и любая форма включающего, такая как "включает" и "включать"), или "содержащий" (и любая форма содержащего, такая как "содержит" и "содержать"), являются включающими или открытыми и не исключают дополнительных, не указанных элементов или стадий метода.
Как используется в настоящем описании, термин "циклоалкил" обозначает неароматические циклические углеводороды, включающие циклические алкильные, алкенильные, и алкинильные группы, которые содержат до 20 образующих цикл атомов углерода. Циклоалкильные группы могут включать моно- или полициклические системы, такие как сшитые системы циклов, кольца с внутренними мостиками, и спиральные системы циклов. В некоторых вариантах осуществления изобретения полициклические системы циклов включают 2, 3 или 4 сшитых цикла. Циклоалкильная группа может содержать от 3 до 15, от 3 до 10, от 3 до 8, от 3 до 6, от 4 до 6, от 3 до 5, или 5 или 6 цикл-образующих атомов углерода. Образующие цикл атомы углерода циклоалкильной группы могут быть необязательно замещены оксо или сульфидо. Примеры циклоалкильной группы включают, но не ограничиваются этим, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил, циклононил, циклопентенил, циклогексенил, циклогексадиенил, циклогептатриенил, норборнил, норпинил, норкарнил, адамантил и подобные. Также включают в определение циклоалкила фрагменты, которые имеют один или более ароматических циклов, сшитых (в общем имеющих связь) с циклоалкильным кольцом, например, бензо- или тиениловые производные пентана, пентена, гексана и подобных (например, 2,3-дигидро-1H-инден-1-ил, или 1H-инден-2(3H)-он-1-ил).
Как используется в настоящем описании, термин "диабет" включает "диабет I типа" и "диабет II типа", и часто сопровождается связанными осложнениями, включающими, например, ожирение и высокий уровень холестерина.
Как используется в настоящем описании, термин "гало" обозначает галогеновые группы, включающие, без ограничения, фтор, хлор, бром и йод.
Как используется в настоящем описании, термин "гетероарил" обозначает ароматический гетероцикл, имеющий до 20 образующих цикл атомов (например, C) и имеющий, по меньшей мере, один член цикла гетероатом (образующий цикл атом), такой как сера, кислород или азот. В некоторых вариантах осуществления изобретения гетероарильная группа имеет, по меньшей мере, один или более гетероатомов, образующих цикл, каждый из которых представляет собой независимо, серу, кислород или азот. В некоторых вариантах осуществления изобретения гетероарильная группа имеет от 3 до 20 образующих цикл атомов, от 3 до 10 образующих цикл атомов, от 3 до 6 образующих цикл атомов или от 3 до 5 образующих цикл атомов. В некоторых вариантах осуществления изобретения гетероарильная группа содержит от 2 до 14 атомов углерода, от 2 до 7 атомов углерода, или 5 или 6 атомов углерода. В некоторых вариантах осуществления изобретения гетероарильная группа содержит 1-4 гетероатома, 1-3 гетероатома, или 1 или 2 гетероатома. Гетероарильные группы включают моноциклические или полициклические системы (например, имеющие 2, 3 или 4 сшитых цикла). Примеры гетероарильных групп включают, но не ограничиваются этим, пиридил, пиримидинил, пиразинил, пиридазинил, триазинил, фурил, хинолил, изохинолил, тиенил, имидазолил, тиазолил, индолил (такие как индол-3-ил), пиррил, оксазолил, бензофурил, бензотиенил, бензтиазолил, изоксазолил, пиразолил, триазолил, тетразолил, индазолил, 1,2,4-тиадиазолил, изотиазолил, бензотиенил, пуринил, карбазолил, бензимидазолил, индолинил, пиранил, оксадиазолил, изоксазолил, триазолил, тиантренил, пиразолил, индолизинил, изоиндолил, изобензофуранил, бензоксазолил, ксантренил, 2H-пирролил, пирролил, 3H-индолил, 4H-хинолизинил, фталазинил, нафтиридинил, хиназолинил, фенантридинил, акридинил, перимидинил, фенантролинил, феназинил, изотиазолил, фенотиазинил, изоксазолил, фуразанил, феноксазинил группы и подобные. Подходящие гетероарильные группы включают 1,2,3-триазол, 1,2,4-триазол, 5-амино-1,2,4-триазол, имидазол, оксазол, изоксазол, 1,2,3-оксадиазол, 1,2,4-оксадиазол, 3-амино-l,2,4-оксадиазол, 1,2,5-оксадиазол, 1,3,4-оксадиазол, пиридин, и 2-аминопиридин.
Как используется в настоящем описании, термин "гетероцикл" или "гетероциклическая структура" обозначает 5-7-членную моно- или бициклическую или 7-10-членную бициклическую систему циклов, любой цикл которой может быть насыщенным или ненасыщенным, и которая состоит из атомов углерода и из одного-трех гетероатомов, выбираемых из N, O и S, и где гетероатомы N и S могут необязательно быть окислены, и гетероатом N может необязательно быть кватернизован, и включающую любую бициклическую группу, в которой любая из вышеописанных гетероциклических структур сшита с бензольным циклом. Особенно применимыми являются циклы, содержащие один кислород или серу, один-три атома азота, или один кислород или серу, в комбинации с одним или двумя атомами азота. Гетероциклическая структура может быть прикреплена к любому гетероатому, что приводит к образованию стабильной структуры. Примеры гетероциклических групп включают, но не ограничиваются пиперидинил, пиперазинил, 2-оксопиперазинил, 2-оксопиперидинил, 2-оксопирролидинил, 2-оксоазепинил, азепинил, пирролил, 4-пипериддонил, пирролидинил, пиразолил, пиразолидинил, имидазолил, имидазолидинил, имидазолидинил, пиридил, пиразинил, пиримидинил, пиридазинил, оксазолил, оксазолидинил, изоксазолил, изоксазолидинил, морфолинил, тиазолил, тиазолидинил, изотиазолил, хинуклидинил, изотиазолидинил, индолил, хинолинил, изохинолинил, бензимидазолил, тиадиазолил, бензопиранил, бензотиазолил, бензоксазолил, фурил, тетрагидрофурил, тетрагидропиранил, тиенил, бензотиенил, тиаморфолинил, тиаморфолинил сульфоксид, тиаморфолинил сульфон, и оксадиазолил. Морфолино представляет собой то же, что и морфолинил.
Как используется в настоящем описании, термин "гетероциклоалкил" обозначает неароматические гетероциклы, имеющие до 20 образующих цикл атомов, включающие циклизованные алкильные, алкенильные, и алкинильные группы, где один или более цикл-образующих атомов углерода замещен гетероатомом, таким как атом O, N, или S. Гетероциклоалкильные группы могут быть моно или полициклическими (например, сшитыми, с мостиками или спиральными системами). В некоторых вариантах осуществления изобретения гетероциклоалкильная группа имеет от 1 до 20 атомов углерода, или от 3 до 20 атомов углерода. В некоторых вариантах осуществления изобретения гетероциклоалкильная группа содержит от 3 до 14 образующих цикл атомов, от 3 до 7 образующих цикл атомов или 5 или 6 образующих цикл атомов. В некоторых вариантах осуществления изобретения гетероциклоалкильная группа имеет от 1 до 4 гетероатомов, от 1 до 3 гетероатомов, или 1 или 2 гетероатома. В некоторых вариантах осуществления изобретения гетероциклоалкильная группа содержит от 0 до 3 двойных связей. В некоторых вариантах осуществления изобретения гетероциклоалкильная группа содержит от 0 до 2 тройных связей. Примеры гетероциклоалкильных групп включают, без ограничения, морфолино, тиоморфолино, пиперазинил, тетрагидрофуранил, тетрагидротиенил, 2,3-дигидробензофурил, 1,3-бензодиоксол, бензо-1,4-диоксан, пиперидинил, пирролидинил, изоксазолидинил, оксазолидинил, изотиазолидинил, пиразолидинил, тиазолидинил, имидазолидинил, пирролидин-2-он-3-ил и подобные. Кроме того, образующие цикл атомы углерода или гетероатомы гетероциклоалкильной группы могут быть необязательно замещены оксо или сульфидо. Например, образующий цикл атом S может быть замещен 1 или 2 оксо (образуя S(O) или S(О)2). Для другого примера, образующий цикл атом C может быть замещен оксо (образуя карбонил). Также включают в определение гетероциклоалкила фрагменты, которые имеют один или более ароматических циклов, сшитые (имеющие связь в общем с) с неароматической гетероциклической структурой, включая, но не ограничиваясь этим, пиридинил, тиофенил, фталидимил, нафталимидил и бензопроизводные гетероциклов, такие как индолен, изоиндолен, изоиндолин-1-он-3-ил, 4,5,6,7-тетрагидротиено[2,3-c]пиридин-5-ил, 5,6-дигидротиено[2,3-c]пиридин-7(4H)-он-5-ил, и 3,4-дигидроизохинолин-1(2H)-он-3ил группы. Образующие цикл атомы углерода и гетероатомы гетероциклоалкильной группы могут быть необязательно замещены оксо или сульфидо.
Как используется в настоящем описании, термин "индивид" или "пациент" используются взаимозаменяемо, обозначая любое животное, включая млекопитающих, таких как мыши, крысы, другие грызуны, кролики, собаки, кошки, свиньи, крупный рогатый скот, овцы, лошади или приматы, такие как человек.
Как используется в настоящем описании, фраза «нуждающийся в этом» обозначает, что животное или млекопитающее определяют как имеющее необходимость в определенном способе или лечении. В некоторых вариантах осуществления изобретения идентификация может обозначать любые средства диагностики. В любом из методов и вариантов лечения, описанных в настоящем описании, животное или млекопитающее может быть нуждающимся в нем.
Как используется в настоящем описании, фраза "целое число от 1 до 5" обозначает 1, 2, 3, 4 или 5.
Как используется в настоящем описании, термин "выделенный" обозначает, что соединения, описанные в настоящем описании, выделяют из других компонентов или (a) натурального источника, такого как растения или клетки, например, бактериальной культуры, или (b) синтетической органической смеси химической реакции, например, обычными методиками.
Как используется в настоящем описании, термин "млекопитающее" обозначает грызуна (например, мышь, крысу или морскую свинку), обезьяну, кошку, собаку, корову, лошадь, свинью или человека. В некоторых вариантах осуществления изобретения млекопитающим является человек.
Как используется в настоящем описании, термин "n-членный", где n является целым числом, обычно описывает количество образующих цикл атомов фрагмента, где количество образующих цикл атомов равно n. Например, пиридин является примером 6-членного гетероарильного цикла и тиофен является примером 5-членного гетероарильного цикла.
Как используется в настоящем описании, фраза «необязательно замещенный» обозначает, что замещение является необязательным и, следовательно, включает и незамещенные, и замещенные атомы, и фрагменты. "Замещенный" атом или фрагмент показывает, что любой водород на обозначенном атоме или фрагменте может быть замещен с выбором из указанных групп заместителей, с условием, что не превосходят нормальную валентность обозначенного атома или фрагмента, и что замена приводит к стабильному соединению. Например, если метиловая группа является необязательно замещенной, тогда 3 атома водорода на атоме углерода могут быть замещены группами-заместителями.
Как используется в настоящем описании, фраза "фармацевтически приемлемый" обозначает такие соединения, материалы, композиции и/или дозируемые лекарственные формы, которые в рамках озвученного медицинского суждения являются подходящими для контакта с тканями людей и животных. В некоторых вариантах осуществления изобретения "фармацевтически приемлемый" обозначает одобренный утверждающим органом Федерального или государственного правления или перечисленный в фармакопее США, или иной общепринятой фармакопее для использования у животных и, точнее, у людей.
Как используется в настоящем описании, фраза "фармацевтически приемлемая соль(и)," включает, но не ограничивается этим, соли кислых или основных групп. Соединения, которые являются основными по природе, способны образовывать большое множество солей с различными неорганическими и органическими кислотами. Кислоты, которые могут быть использованы для получения фармацевтически приемлемых аддитивных солей кислот таких основных соединений, являются таковыми, которые образуют нетоксичные аддитивные соли кислот, т.е. соли, содержащие фармакологически приемлемые анионы, включающие, но не ограниченные, соли серной, тиосерной, лимонной, малеиновой, уксусной, щавелевой кислот; гидрохлорид, гидробромид, гидройодид, нитрат, сульфат, бисульфат, фосфат, кислый фосфат, изоникотинат, борат, ацетат, лактат, салицилат, цитрат, кислый цитрат, тартрат, олеат, таннат, пантотенат, битартрат, аскорбат, сукцинат, малеат, гентисинат, фумарат, глюконат, глюкуронат, сахарат, бензоат, глютамат, метансульфонат, этансульфонат, бензолсульфонат, п-толуолсульфонат, бикарбонат, малонат, мезилат, эзилат, напсидизилат, тозилат, безилат, ортофосфат, трифторацетат и памоат (т.е. 1,1'-метилен-бис-(2-гидрокси-3-нафтоат)). Соединения, которые включают амино-фрагмент, могут образовывать фармацевтически приемлемые соли с различными аминокислотами, в добавление к кислотам, упомянутым выше. Соединения, которые являются кислыми по природе, способны образовывать основные соли с различными фармакологически приемлемыми катионами. Примеры таких солей включают, но не ограничиваются этим, соли щелочных металлов или щелочно-земельных металлов, и в частности, соли кальция, магния, аммония, натрия, лития, цинка, калия и железа. Настоящее изобретение также включает соли четвертичного аммония соединений, описанных в настоящем описании, где соединения имеют один или более фрагментов третичного амина.
Как используется в настоящем описании, термин "фенил" обозначает -C6H5. Фенильная группа может быть незамещенной или замещенной одним, двумя или тремя подходящими заместителями.
Как используется в настоящем описании, термины "профилактика" или "предотвращение" обозначают снижение риска развития определенного заболевания, состояния или расстройства.
Как используется в настоящем описании, термин "очищенный" обозначает, что при выделении изолят содержит, по меньшей мере, 90%, по меньшей мере, 95%, по меньшей мере, 98%, или, по меньшей мере, 99% соединения, описанного в настоящем описании, по массе изолята.
Как используется в настоящем описании, фраза "соли четвертичного аммония" обозначает производные описанных соединений с одним или более фрагментами третичного амина, где, по меньшей мере, один из фрагментов третичного амина в исходном соединении модифицирован путем преобразования фрагмента третичного амина в катион четвертичного аммония посредством алкилирования (и катионы сбалансированы анионами, такими как CI-, CH3COO-, и CF3COO-), например, метилирования или этилирования.
Как используется в настоящем описании, фраза "по существу выделенный" обозначает соединение, которое является, по меньшей мере, частично или почти полностью выделенным из окружения, в котором оно образуется или определяется.
Как используется в настоящем описании, фраза "подходящий заместитель" или "заместитель" обозначает группу, которая не мешает синтетической или фармацевтической применимости соединений, описанных в настоящем описании, или промежуточных продуктов, применимых для их получения. Примеры подходящих заместителей включают, но не ограничиваются этим, C1-С6алкил, C1-С6алкенил, C1-C6алкинил, C5-C6арил, C1-C6алкокси, C3-C5гетероарил, C3-C6циклоалкил, C5-C6арилокси, -CN, -OH, оксо, гало, галоалкил, -NO2, -CO2H, -NH2, -NH(C1-C8алкил), -NH(C1-C8алкил)2, -NH(C6арил), -N(C5-C6арил)2, -CHO, -CO(C1-С6алкил), -CO((C5-C6)арил), -CO2((C1-C6)алкил), и -CO2((C5-C6)арил). Специалист в области техники может легко выбрать подходящий заместитель на основании стабильности и фармакологической и синтетической активности соединений, описанных в настоящем описании.
Как используется в настоящем описании, фраза "терапевтически эффективное количество" обозначает количество активного соединения или фармацевтического средства, которое обеспечивает биологический или медицинский ответ, который ожидает исследователь, ветеринар, врач или другой клиницист в ткани, системе, у животного, индивида или человека. Терапевтический эффект зависит от состояния, которое лечат, или желаемого биологического эффекта. По существу, терапевтическим эффектом может быть уменьшение тяжести симптомов, ассоциированных с расстройством, и/или ингибирование (частичное или полное) прогрессирования расстройства, или улучшение лечения, заживления, профилактика или устранение расстройства или побочных эффектов. Количество, необходимое для получения терапевтического ответа, может быть определено на основании возраста, состояния здоровья, размера и пола пациента. Оптимальные количества также могут быть определены на основании мониторинга ответа пациента на лечение.
Как используется в настоящем описании, термины "лечить", "леченный" или "лечение" обозначают и терапевтическое лечение, и профилактические или превентивные мероприятия, когда у пациента необходимо предотвратить или замедлить (уменьшить) нежелательное физиологическое состояние, расстройство или заболевание или получить полезные или желаемые клинические результаты. Для целей настоящего изобретения полезные или желательные клинические результаты включают, но не ограничиваются этим, облегчение симптомов; уменьшение выраженности состояния, расстройства или заболевания; стабилизацию (т.е. отсутствие ухудшения) состояния, расстройства или заболевания; задержку развития или замедление прогрессирования состояния, расстройства или заболевания; облегчение состояния, расстройства или заболевания или ремиссию (или частичную или полную, определяемую или неопределяемую; облегчение, по меньшей мере, одного измеряемого физического параметра, не обязательно ощущаемое пациентом; или улучшение или коррекцию состояния, расстройства или заболевания. Лечение включает развитие клинически достоверного ответа без избыточного количества побочных эффектов. Лечение также включает продление жизни по сравнению с ожидаемой продолжительностью жизни при отсутствии лечения.
Соединения по описанию определяют в настоящем описании по их химической структуре и/или химическому наименованию. Когда соединение называют и по химической структуре, и по химическому наименованию, и указанные химическая структура и химическое наименование противоречат друг другу, химическая структура является определяющей в сущности соединения.
В различных местах в настоящей спецификации заместители соединений могут быть описаны в группах или в диапазонах. Специфически предназначено, чтобы изобретение включало все и каждую отдельную суб-комбинацию членов таких групп и диапазонов. Например, термин "C1-6 алкил" специфически предназначен для отдельного описания метила, этила, пропила, C4 алкила, C5 алкила, и С6 алкила, линейного и/или разветвленного.
Для соединений, в которых переменная появляется более чем однократно, каждая переменная может быть различным фрагментом, выбираемым из группы формул Маркуша, определяющей переменную. Например, когда описана структура, имеющая две группы R, которые одновременно присутствуют на одном соединении, две группы R могут представлять собой различные фрагменты, выбираемые из групп формул Маркуша, определяемых для R. В другом примере, когда необязательно обозначен множественный заместитель в форме, например, 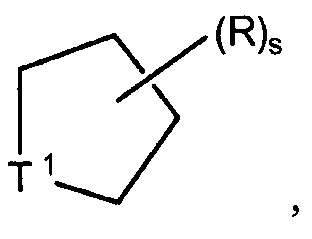 понимают, что заместитель R может появляться на цикле "s” количество раз и R может быть различным фрагментом в каждом положении. Более того, в вышеуказанном примере, когда переменную T1 определяют как включающую водород, например, когда T1 представляет собой CH2, NH, и др., любой H может быть замещен заместителем.
понимают, что заместитель R может появляться на цикле "s” количество раз и R может быть различным фрагментом в каждом положении. Более того, в вышеуказанном примере, когда переменную T1 определяют как включающую водород, например, когда T1 представляет собой CH2, NH, и др., любой H может быть замещен заместителем.
Дополнительно понимают, что определенные характеристики описания, которые, для ясности, описаны в контексте отдельных вариантов осуществления изобретения, также могут быть представлены в комбинации в отдельном варианте осуществления изобретения. Наоборот, различные характеристики описания, которые являются, для краткости, описанными в контексте одного варианта осуществления изобретения, также могут быть представлены отдельно или в любой подходящей суб-комбинации.
Понимают, что настоящее описание охватывает применение, когда применимо, стереоизомеров, диастереомеров и оптических стереоизомеров соединений описания, а также их смесей. Кроме того понимают, что стереоизомеры, диастереомеры и оптические стереоизомеры соединений по описанию и их смеси находятся в рамках описания. В качестве неограничивающего примера, смесь может быть рацематом или смесь может включать неравные пропорции одного определенного стереоизомера относительно другого. Кроме того, соединения могут быть представлены в виде по существу чистых стереоизомеров, диастереомеров и оптических стереоизомеров (таких как эпимеры).
Соединения, описанные в настоящем описании, могут быть асимметричными (например, имеющими один или более стереоцентров). Все стереоизомеры, такие как энантиомеры и диастереомеры, включаются в рамки описания, если не указано иначе. Соединения, которые содержат асимметрически замещенные атомы углерода, могут быть выделены в оптически активных или рацемических формах. В области техники известны способы получения оптически активных форм из оптически активных исходных материалов, такие как разделение рацемических смесей или посредством стереоселективного синтеза. Множество геометрических изомеров олефинов, C=N двойных связей и подобных также могут присутствовать в соединениях, описанных в настоящем описании, и все такие стабильные изомеры охватываются настоящим описанием. Цис и транс геометрические изомеры соединений также включены в рамки описания и могут быть выделены как смесь изомеров или как отдельные изомерные формы. Когда соединение, способное к стереоизомеризму или геометрическому изомеризму, обозначается в его структуре или наименовании без ссылки на специфические R/S или цис/транс конфигурации, понимают, что предусматриваются все такие изомеры.
Разделение рацемических смесей соединений может проводиться любым из множества методов, известных в области техники, включая, например, фракционную рекристаллизацию с использованием хиральной разделяющей кислоты, которая является оптически активной, солеобразующей органической кислотой. Подходящие разделяющие средства для методов фракционной рекристаллизации включают, но не ограничиваются, оптически активные кислоты, такие как D- и L-формы винной кислоты, диацетилвинной кислоты, дибензоилвинной кислоты, миндальной кислоты, яблочной кислоты, молочной кислоты и различных оптически активных камфорсульфоновых кислот, таких как β-камфорсульфоновая кислота. Другие разделяющие средства, подходящие для методов фракционированной кристаллизации включают, но не ограничиваются этим, стереоизомерно чистые формы α-метилбензиламина (например, S- и R-формы, или диастереомерно чистые формы), 2-фенилглицинол, норэфедрин, эфедрин, N-метилэфедрин, циклогексилэтиламин, 1,2-диаминоциклогексан, и подобные. Разделение рацемических смесей также можно проводить посредством элюции на колонке, упакованной с оптически активным разделяющим средством (например, динитробензоилфенилглицин). Подходящие композиции растворителя для элюции могут быть определены специалистом в данной области техники.
Соединения также могут включать таутомерные формы. Таутомерные формы возникают в результате замены одинарной связи соседней двойной связью вместе с сопутствующей миграцией протона. Таутомерные формы включают прототропные таутомеры, которые являются изомерными состояниями протонирования, имеющими одну и ту же эмпирическую формулу и общий заряд. Примеры прототропных таутомеров включают, но не ограничиваются кетон-енольные пары, амид-имидные кислотные пары, пары лактама-лактима, амид-имидные кислотные пары, пары енамина-имина и кольцевые формы, где протон может занимать два или более положения гетероциклической системы, включая, но не ограничиваясь этим, 1H- и 3H-имидазол, 1H-, 2H- и 4H-1,2,4-триазол, 1H- и 2H- изоиндол и 1H- и 2H-пиразол. Таутомерные формы могут находиться в равновесии или быть стерически блокированы в одну форму путем соответствующего замещения.
Соединения также включают гидраты и сольваты, а также безводные и несольватированные формы.
Соединения также могут включать все изотопы атомов, появляющихся в промежуточных или конечных соединениях. Изотопы включают атомы, имеющие то же атомное число, но различные массовые числа. Например, изотопы водорода включают тритий и дейтерий.
В некоторых вариантах осуществления изобретения соединения или их фармацевтически приемлемые соли, по существу выделены. Частичное разделение может включать, например, композицию, обогащенную соединением по описанию. Последующее разделение может включать композиции, содержащие, по меньшей мере, около 50%, по меньшей мере, около 60%, по меньшей мере, около 70%, по меньшей мере, около 80%, по меньшей мере, около 90%, по меньшей мере, около 95%, по меньшей мере, около 97%, или, по меньшей мере, около 99% по массе соединения по описанию, или его фармацевтически приемлемой соли. Способы для выделения соединений и их солей являются обычными в области техники.
Хотя описанные соединения являются подходящими, в соединение могут быть включены другие функциональные группы с возможными подобными результатами. В частности, тиоамиды и тиоэфиры предположительно имеют сходные свойства. Расстояние между ароматическими циклами может влиять на геометрический вид соединений, и указанное расстояние может быть изменено путем включения алифатических цепей различной длины, которые могут быть необязательно замещены или могут включать аминокислоту, бикарбоновую кислоту или диамин. Расстояние между и относительная ориентация мономеров в соединениях также могут быть изменены путем замены амидной связи суррогатом, имеющим дополнительные атомы. Следовательно, замена карбонильной группы дикарбонилом изменяет расстояние между мономерами и свойства дикарбонильной единицы к адаптации анти-расположения двух карбонильных фрагментов и изменения периодичности соединения. Пиромеллитический ангидрид представляет собой еще одну альтернативу простым амидным связям, которая может изменять конформацию и физические свойства соединения. Современные методы твердофазной органической химии (E. Atherton and R. C. Sheppard, Solid Phase Peptide Synthesis A Practical Approach IRL Press Oxford 1989) в настоящее время позволяют синтезировать гомодисперсные соединения с молекулярными массами, достигающими 5000 Дальтон. Другие варианты замещения также равным образом эффективны.
Соединения, описанные в настоящем описании, также включают производные, относящиеся к пролекарствам, которые могут быть получены путем модификации функциональных групп, присутствующих в соединениях таким образом, что модификации отщепляются от исходных соединений или при обычной обработке или in vivo. Примеры пролекарств включают соединения, как описано в настоящем описании, которые содержат один или более молекулярных фрагментов, прикрепленных к гидроксильной, амино, сульфгидрильной или карбоксильной группе соединения и которые при введении пациенту, отщепляются in vivo с образованием свободных гидроксильных, амино, сульфгидрильных или карбоксильных групп, соответственно. Примеры пролекарств включают, но не ограничиваются ими, ацетатные, форматные и бензоатные производные спиртовых и аминовых функциональных групп в соединениях, описанных в настоящем описании. Получение и применение пролекарств обсуждается в T. Higuchi et al, "Pro-drugs as Novel Delivery Systems," Vol. 14 of the A.C.S. Symposium Series, and in Bioreversible Carriers in Drug Design, ed. Edward B. Roche, American Pharmaceutical Association and Pergamon Press, 1987, оба из которых включены в настоящее описание в виде ссылки во всей полноте.
Соединения, содержащие аминную функциональную группу, также могут образовывать N-оксиды. Ссылка в настоящем описании на соединение, которое содержит аминную функциональную группу, также включает N-оксид. Когда соединение содержит несколько аминных функциональных групп, один или более чем один атом азота может быть окислен с образованием N-оксида. Примеры N-оксидов включают N-оксиды третичного амина или атома азота азот-содержащего гетероцикла. N-оксиды могут быть образованы путем обработки соответствующего амина окисляющим средством, таким как перекись водорода или перкислота (например, пероксикарбоновая кислота) (см, Advanced Organic Chemistry, by Jerry March, 4th Edition, Wiley Interscience).
Настоящее изобретение предоставляет соединения по формуле V:
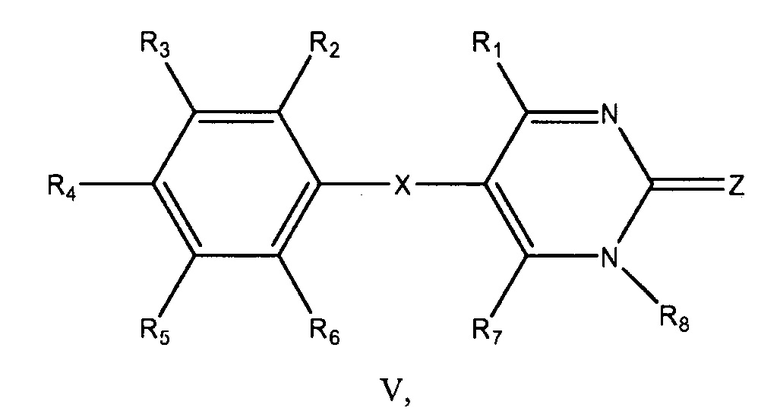
или их фармацевтически приемлемые соли, где каждый из R1, R2, R3, R4, R5, R6, и R7 представляют собой независимо подходящий заместитель; или где каждый из R1, R2, R3, R4, R5, R6, и R7 представляют собой независимо водород, алкокси, алкил, алкенил, алкинил, арил, арилокси, бензил, циклоалкил, галоген, гетероарил, гетероциклоалкил, -CN, -OH, -NO2, -CF3, -CO2H, -CО2алкил, или -NH2;
R8 представляет собой алкил или водород;
X представляет собой O, S, NH, или N-алкил; и
Z представляет собой O или S.
В некоторых вариантах осуществления изобретения R8 представляет собой алкил, такой как метил. В некоторых вариантах осуществления изобретения, R8 представляет собой водород.
В некоторых вариантах осуществления изобретения X представляет собой кислород.
В некоторых вариантах осуществления изобретения Z представляет собой кислород.
В некоторых вариантах осуществления изобретения, по меньшей мере, один из R2-R6 представляет собой алкил, такой как метил. В некоторых вариантах осуществления изобретения, по меньшей мере, один из R2-R6 представляет собой галоген, такой как хлор. В некоторых вариантах осуществления изобретения, по меньшей мере, один из R2-R6 представляет собой -CN. В некоторых вариантах осуществления изобретения, по меньшей мере, один из R2-R6 представляет собой -OH. В некоторых вариантах осуществления изобретения, по меньшей мере, один из R2-R6 представляет собой -NO2. В некоторых вариантах осуществления изобретения, по меньшей мере, один из R2-R6 представляет собой -CF3. В некоторых вариантах осуществления изобретения, по меньшей мере, один из R2-R6 представляет собой -CO2H. В некоторых вариантах осуществления изобретения, по меньшей мере, один из R2-R6 представляет собой -NH2. В некоторых вариантах осуществления изобретения, по меньшей мере, один из R2-R6 представляет собой -алкокси.
В некоторых вариантах осуществления изобретения, R2 представляет собой алкил, такой как метил, и каждый из R1, и R3-R8 представляет собой водород, и X и Z являются O. В некоторых вариантах осуществления изобретения R2 представляет собой галоген, такой как хлор, и каждый из R1, и R3-R8 является водородом, и X и Z являются O. В некоторых вариантах осуществления изобретения R3 представляет собой алкил, такой как метил, и каждый из R1, R2 и R4-R8 представляет собой водород, и X и Z являются O.
В некоторых вариантах осуществления изобретения, R3 представляет собой галоген, такой как хлор, и каждый из R1, R2, и R4-R8 представляет собой водород и X и Z являются O.
В некоторых вариантах осуществления изобретения, R4 представляет собой алкил, такой как метил, и каждый из R1- R3 и R5-R8 представляет собой водород и X и Z являются O.
В некоторых вариантах осуществления изобретения, R4 представляет собой галоген, такой как хлор, и каждый из R1-R3, и R5-R8 представляет собой водород и X и Z являются O.
В некоторых вариантах осуществления изобретения, R5 представляет собой -CF3, и каждый из R1-R4 и R6-R8 представляет собой водород, и X и Z являются O. В некоторых вариантах осуществления изобретения, R5 -NH2, и каждый из R1-R4 и R6-R8 представляет собой водород и X и Z являются O.
В некоторых вариантах осуществления изобретения R6 представляет собой -CF3, и каждый из R1-R5 и R7-R8 представляет собой водород и X и Z являются O. В некоторых вариантах осуществления изобретения R6 представляет собой -NH2 и каждый из R1-R5 и R7-R8 представляет собой водород, и X и Z являются O.
Настоящее описание также предоставляет соединения по формуле I
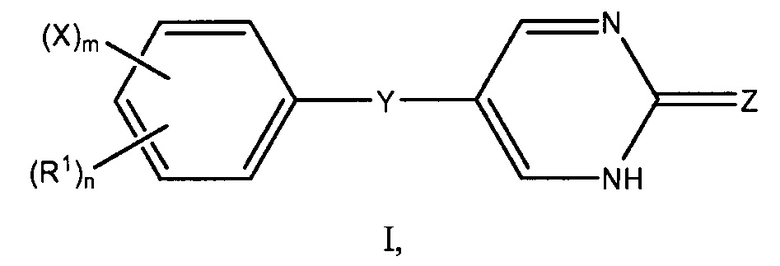
или его фармацевтически приемлемую соль, где:
R1 представляет собой алкильную группу;
X представляет собой галоген;
Y является O, S, или NH;
Z является O или S;
n представляет собой целое число от 0 до 5 и m составляет 0 или 1, где m+n меньше или равно 5. В некоторых вариантах осуществления изобретения алкильная группа является метилом и n равно 1.
В некоторых вариантах осуществления изобретения галогеном является хлор и m составляет 1.
В некоторых вариантах осуществления изобретения Y является O.
В некоторых вариантах осуществления изобретения Z является O.
В некоторых вариантах осуществления изобретения R1 представляет собой метил, Y представляет собой O, Z представляет собой O, n равно 1, и m равно 0. В некоторых вариантах осуществления изобретения R1 находится в мета-положении.
В некоторых вариантах осуществления изобретения X представляет собой хлор, Y представляет собой O, Z представляет собой O, n равно 0, и m равно 1. В некоторых вариантах осуществления изобретения X находится в мета-положении.
Настоящее описание также предоставляет соединения по формуле II:
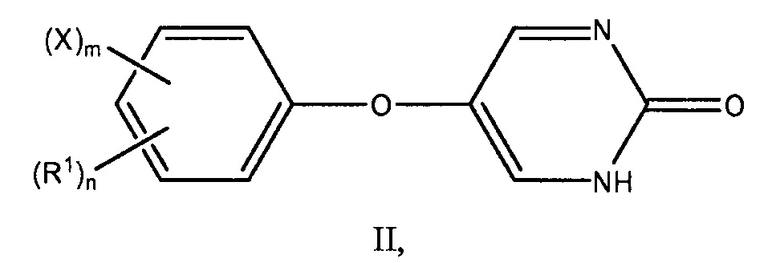
или его фармацевтически приемлемую соль, где:
R1 представляет собой алкильную группу;
X представляет собой галоген; и
n является целым числом от 0 до 5 и m составляет 0 или 1, где m+n меньше или равно 5.
В некоторых вариантах осуществления изобретения алкильной группой является метил и n равно 1.
В некоторых вариантах осуществления изобретения галогеном является хлор и m равно 1.
В некоторых вариантах осуществления изобретения R1 представляет собой метил, n равно 1, и m равно 0. В некоторых вариантах осуществления изобретения, R1 находится в мета-положении.
В некоторых вариантах осуществления изобретения X является хлором, n равно 0, и m равно 1. В некоторых вариантах осуществления изобретения X находится в мета-положении.
Настоящее описание также предоставляет соединения по формуле III:
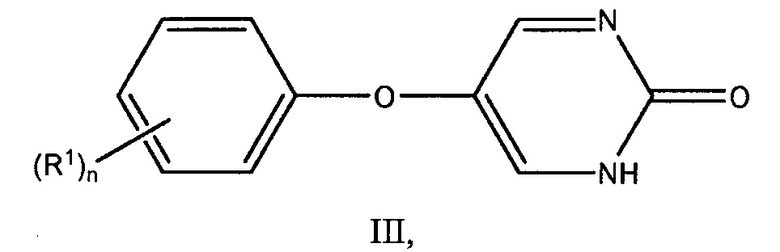
или его фармацевтически приемлемую соль, где:
R1 представляет собой алкильную группу; и
n является целым числом от 0 до 5.
В некоторых вариантах осуществления изобретения, R1 представляет собой метил, n равно 1. В некоторых вариантах осуществления изобретения R1 находится в мета-положении.
Настоящее описание также предоставляет соединения по формуле IV:
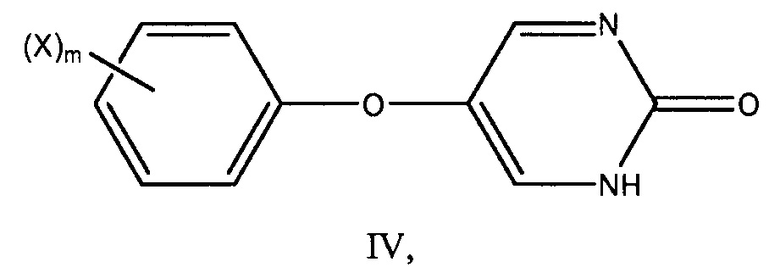
или его фармацевтически приемлемую соль, где:
X представляет собой галоген; и
m является целым числом от 0 до 1.
В некоторых вариантах осуществления изобретения X представляет собой хлор и m равно 1. В некоторых вариантах осуществления изобретения X находится в мета-положении.
Иллюстративные примеры соединений, которые охватываются формулами I-IV, и которые являются применимыми в способах, описанных в настоящем описании, включают, но не ограничиваются:
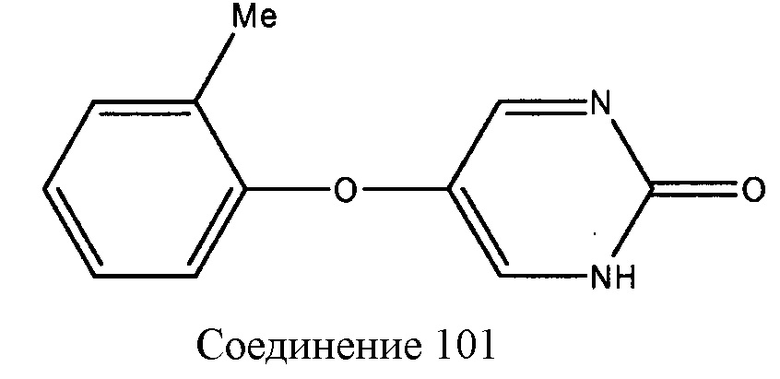
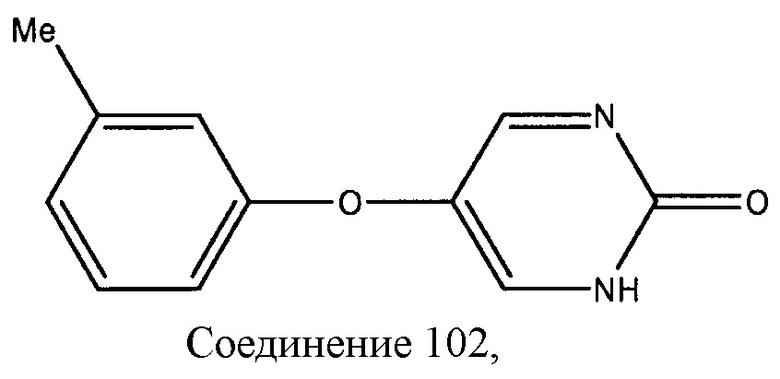
которое также известно как Толимидон, CP-26154, и 2(1H)-Пиримидинон, 5-(3-метилфенокси).
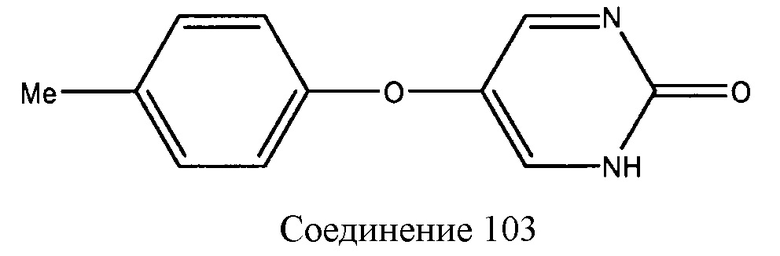
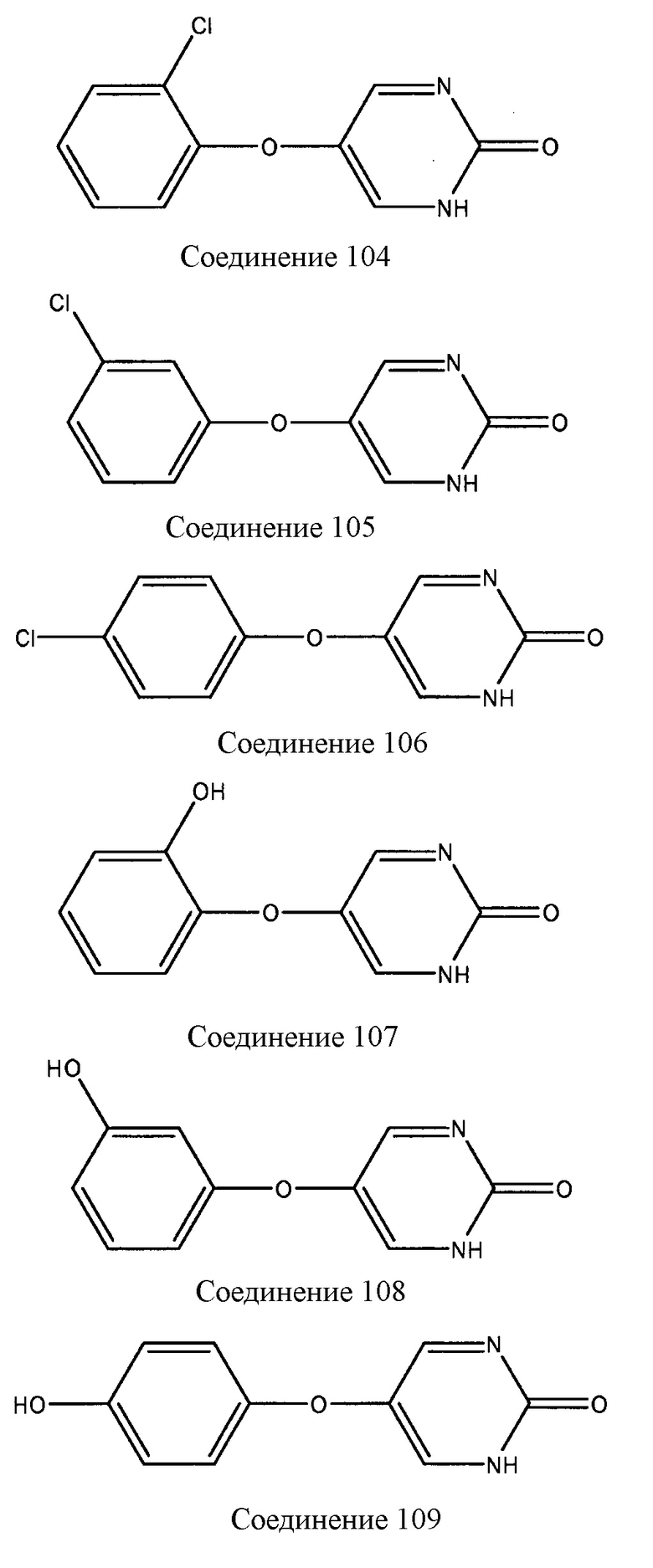
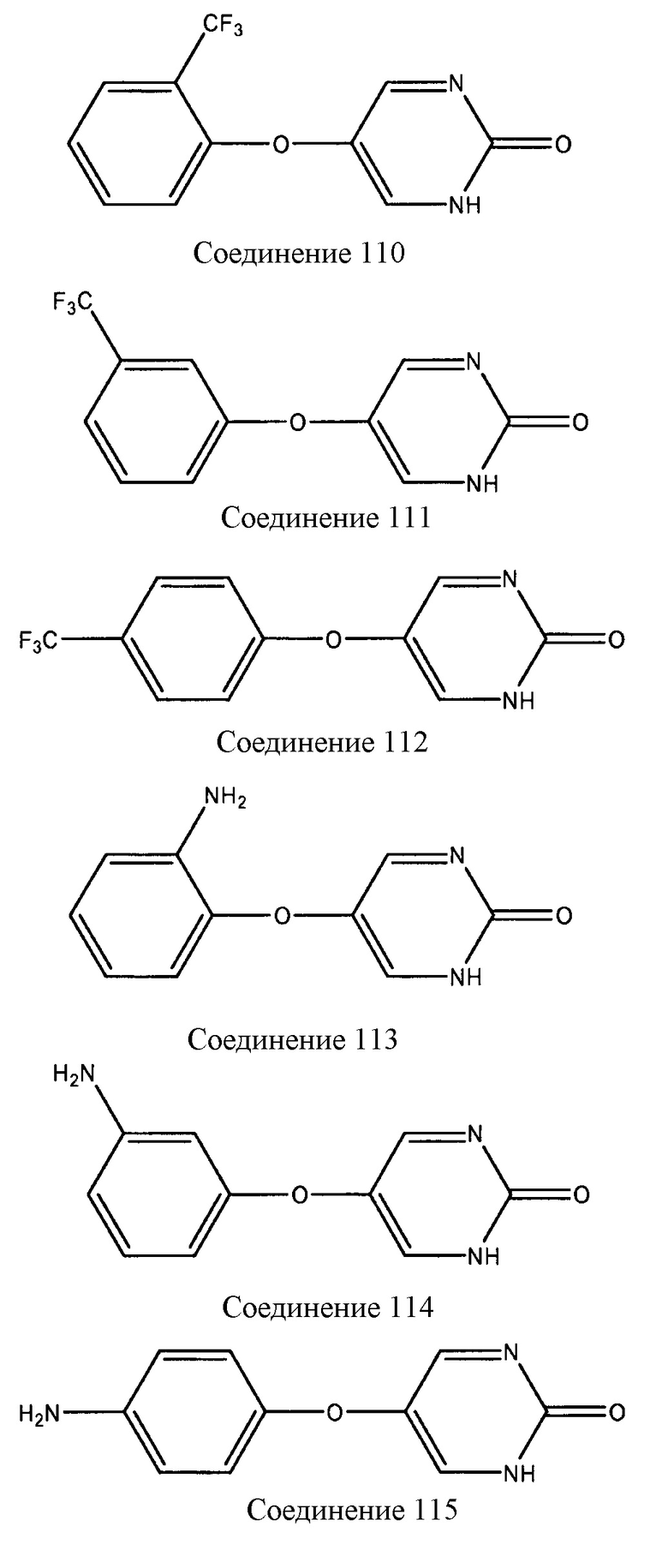
Соединения, описанные в настоящем описании, могут быть синтезированы методиками органической химии, известными обычному специалисту в области техники, например, как описано в патенте США номер 3922345, который включен в настоящее описание в виде ссылки во всей полноте.
Соединения по описанию присутствуют в композициях, включающих инсулин, и их вводят млекопитающим. Подходящие инсулины включают, но не ограничиваются, инъекционный инсулин, чрескожный инсулин, ингаляционный инсулин или их любые комбинации. В качестве альтернативы инсулину могут быть использованы производные, стимуляторы секреции, сенситайзеры или миметики инсулина. Стимуляторы секреции инсулина для использования в комбинации с соединениями по описанию включают, но не ограничиваются этим, форсколин, дибутрил цАМФ и изобутилметилксантин (IBMX).
Существует четыре типа инсулина, которые отличаются по времени начала и продолжительности действия. Инсулины быстрого действия (например, Хумалог) имеют быстрое начало действия (в течение 15 минут) и продолжительность действия до 5 часов и покрывают потребности в пище, потребляемой в момент инъекции. Инсулины короткого действия (например, Хумулин), также имеют быстрое начало действия, покрывают необходимость для приемов пищи, потребляемых в течение часа введения, и имеют продолжительность действия до 8 часов. Инсулины промежуточной продолжительности действия (например, НПХ) имеют отложенное начало действия (1-2 часа) и продолжительность действия до 24 часов. Инсулины длительного действия (например, Лантус, Левемир) имеют отложенное начало действия и продолжительность действия до 36 часов после введения. Такие инсулины обычно вводят в различных комбинациях для регуляции уровня глюкозы крови.
Соединения, описанные в настоящем описании, можно вводить любым обычным образом любым путем, при котором они являются активными. Введение может быть системным, местным или пероральным. Например, введение может быть, без ограничения, парентеральным, подкожным, внутривенным, внутримышечным, интраперитонеальным, чрескожным, пероральным, буккальным, сублингвальным, или глазным путем, или интравагинально, путем ингаляции, депо инъекций или посредством имплантов. Тип введения может зависеть от патогена или целевого микроба. Выбор специфического пути введения может быть осуществлен или отрегулирован клиницистом в соответствии с методами, известными клиницисту, для получения желаемого клинического ответа.
В некоторых вариантах осуществления изобретения может оказаться желательно вводить одно или более соединений, или их фармацевтически приемлемых солей, местно в область, нуждающуюся в лечении. Это может быть достигнуто, например, без ограничения, путем местной инфузии во время хирургического вмешательства, местного нанесения, например, в сочетании с раневой повязкой после операции, путем инъекции, посредством катетера, посредством суппозитория или посредством импланта, где имплант состоит из пористого, непористого или гелеобразного материала, включая мембраны, такие как сиаластические мембраны или волокна.
В некоторых вариантах осуществления изобретения соединения по описанию могут быть использованы в комбинированной терапии с инсулином и, по меньшей мере, одним терапевтическим средством. Соединение по описанию, инсулин и терапевтическое средство могут действовать аддитивно или синергически. В некоторых вариантах осуществления изобретения композицию, включающую соединение по описанию, вводят одновременно или последовательно с введением инсулина и другого терапевтического средства, которое может быть частью той же композиции, что и соединение по описанию, или другой композиции. В другом варианте осуществления изобретения композицию, включающую соединение по описанию, вводят перед или после введения инсулина и другого терапевтического средства. Так как множество заболеваний, в лечении которых применимыми являются соединения по описанию, являются хроническими заболеваниями, в одном варианте осуществления изобретения комбинированная терапия включает периодическое введение композиции, включающей соединение по описанию, инсулина и композиции, включающей другое терапевтическое средство, например, для минимизации токсичности, ассоциированной с определенным терапевтическим средством. Продолжительность введения каждого лекарственного средства или терапевтического агента может составлять, например, один месяц, три месяца, шесть месяцев или год. В определенных вариантах осуществления изобретения, когда композицию по описанию вводят одновременно с инсулином и другим терапевтическим средством, которые потенциально дают нежелательные побочные действия, включающие, но не ограниченные, токсичность, терапевтическое средство можно вводить в дозе, которая находится ниже порога, при котором развиваются побочные эффекты. В некоторых вариантах осуществления изобретения соединения можно вводить в комбинации с инсулином и другими средствами для лечения диабета, средствами для снижения артериального давления и/или средствами для снижения холестерина.
Настоящие композиции можно вводить вместе со статином. Статины для применения в комбинации с соединениями по описанию и инсулином включают, но не ограничиваются, аторвастатин, правастатин, флувастатин, ловастатин, симвастатин и церивастатин.
Настоящие композиции также можно вводить вместе с агонистом PPAR, например, тиазолидиндионом или фибратом. Тиазолидиндионы для применения в комбинации с соединениями по описанию и инсулином включают, но не ограничиваются ими, пиоглитазон, циглитазон, 5-((4-(2-(метил-2-пиридиниламино)этокси)фенил)метил)-2,4-тиазолидиндион, троглитазон, WAY-120,744, энглитазон, AD 5075, дарглитазон, и розиглитазон. Фибраты для применении в комбинации с соединениями по описанию и инсулином включают, но не ограничиваются ими, гемфиброзил, фенофибрат, клофибрат или ципрофибрат. Как упомянуто ранее, терапевтически эффективное количество фибрата или тиазолидиндиона часто имеет токсические побочные эффекты. Соответственно, в некоторых вариантах осуществления изобретения, когда композицию по описанию вводят в комбинации с инсулином и агонистом PPAR, дозировка агониста PPAR ниже, чем таковая, сопровождаемая токсическими побочными эффектами.
Настоящие композиции также можно вводить вместе со смолами, связывающими желчные кислоты. Смолы, связывающие желчные кислоты, для применения в комбинации с соединениями по описанию и инсулином включают, но не ограничиваются ими, холестирамин и гидрохлорид колестипола.
Настоящие композиции также можно вводить вместе с ниацином или никотиновой кислотой.
Настоящие композиции также можно вводить вместе с агонистом RXR. Агонисты RXR для применения в комбинации с соединениями по описанию и инсулином включают, но не ограничиваются ими, LG 100268, LGD 1069, 9-цис ретиноевую кислоту, 2-(1-(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтил)циклопропил)пиридин-5-карбоновую кислоту, или 4-((3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтил)2-карбонил)-бензойную кислоту.
Настоящие композиции также можно вводить вместе со средством против ожирения. Лекарственные средства против ожирения для применения в комбинации с соединениями по описанию и инсулином включают, но не ограничиваются ими, агонисты β-адренергических рецепторов, такие как агонисты β-3 рецепторов, сибутрамин, бупропион, флуоксетин и фентермин.
Настоящие композиции также можно вводить вместе с гормоном. Гормоны для применения в комбинации с соединениями по описанию и инсулином включают, но не ограничиваются ими, тиреоидные гормоны и эстрогены.
Настоящие композиции также можно вводить вместе с тирофостином или его аналогом. Тирофостины для применения в комбинации с соединениями по описанию и инсулином включают, но не ограничиваются этим, тирофостин 51.
Настоящие композиции также можно вводить вместе с лекарственными средствами на основе сульфонилмочевины. Лекарственные средства на основе сульфонилмочевины для применения в комбинации с соединениями по описанию и инсулином включают, но не ограничиваются ими, глизоксепид, глибурид, ацетогексамид, хлорпропамид, глиборнурид, толбутамид, толазамид, глипизид, гликлазид, гликвидон, глигексамид, фенбутамид и толцикламид.
Настоящие композиции также можно вводить вместе с бигуанидом. Бигуаниды для применения в комбинации с соединениями по описанию и инсулином включают, но не ограничиваются ими, метформин, фенформин и буформин.
Настоящие композиции также можно вводить вместе с ингибитором α-глюкозидазы. Ингибиторы α-глюкозидазы для применения в комбинации с соединениями по описанию и инсулином включают, но не ограничиваются ими, акарбозу и миглитол.
Настоящие композиции также можно вводить вместе с агонистом АпоA-I. В одном варианте осуществления изобретения агонист АпоA-I представляет собой Милано-форму АпоA-I (ApoA-IM). В некоторых вариантах осуществления изобретения АпоA-IM для введения в сочетании с соединениями по описанию и инсулином, получают методом патента США № 5721114, выданного Abrahamsen. В некоторых вариантах осуществления изобретения агонист АпоA-I представляет собой пептидный агонист. В некоторых вариантах осуществления изобретения пептидный агонист АпоA-I для введения в сочетании с соединениями по описанию и инсулином представляет собой пептид по патентам США No. 6004925 или 6037323.
Настоящие композиции также можно вводить вместе с аполипопротеином E (АпоE). В некоторых вариантах осуществления изобретения АпоE для введения в сочетании с соединениями по описанию и инсулином получают методом по патенту США No. 5834596.
В некоторых вариантах осуществления изобретения настоящие композиции можно вводить вместе с лекарственным средством, повышающим ЛПВП; усилителем ЛПВП; или регулятором генов аполипопротеина A-I, аполипопротеина A-IV и/или аполипопротеина.
Настоящие композиции можно вводить вместе с известными сердечно-сосудистыми лекарственными средствами. Сердечно-сосудистые лекарственные средства для применения в комбинации с соединениями по описанию и инсулином для предотвращения или лечения сердечно-сосудистых заболеваний включают, но не ограничиваются ими, периферические антиадренергические лекарственные средства, антигипертензивные лекарственные средства центрального действия (например, метилдопа, метилдопа HCl), антигипертензивные прямые вазодилататоры (например, диазоксид, гидралазин HQ), лекарственные средства, действующие на ренин-ангиотензиновую систему, периферические вазодилататоры, фентоламин, средства от стенокардии, сердечные гликозиды, инодилататоры (например, амринон, милринон, эноксимон, феноксимон, имизодан, сульмазол), антиаритмические средства, блокаторы кальциевых каналов, ранитин, бозентан и резулин.
Настоящие композиции можно вводить вместе с лечением облучением или одним или более химиотерапевтическими средствами. Для лечения облучением, облучением могут быть гамма-лучи или рентгеновское излучение. Для общего обзора лучевой терапии см. Hellman, Chapter 12: Principles of Radiation Therapy Cancer, in: Principles and Practice of Oncology, DeVita et al, eds., 2nd. Ed., J.B. Lippencott Company, Philadelphia. Применимые химиотерапевтические средства включают метотрексат, таксол, меркаптопурин, тиогуанин, гидроксимочевину, цитарабин, циклофосфамид, ифосфамид, нитрозомочевины, цисплатин, карбоплатин, митомицин, дакарбазин, прокарбизин, этопозиды, кампатекины, блеомицин, доксорубицин, идарубицин, даунорубицин, дактиномицин, пликамицин, митоксантрон, аспарагиназа, винбластин, винорелбин, паклитаксел и доцетаксел. В некоторых вариантах осуществления изобретения композиция по изобретению дополнительно включает одно или более химиотерапевтических средств и/или ее вводят одновременно с лучевой терапией. В некоторых вариантах осуществления изобретения химиотерапию или лучевую терапию проводят перед или после введения настоящей композиции, например, по меньшей мере, через час, пять часов, 12 часов, день, неделю, месяц или несколько месяцев (например, до трех месяцев) после введения композиции по описанию.
Количество соединения, инсулина и другого терапевтического средства для введения представляет собой количество, которое является терапевтически эффективным. Вводимая дозировка зависит от характеристик пациента, получающего лечение, например, определенного животного, получающего лечение, возраста, массы тела, состояния здоровья, типов сопутствующего лечения, если есть, и частоты введений, и может быть легко определена специалистом в области техники (например, клиницистом). Выбор специфической схемы введения может быть осуществлен или отрегулирован или снижен клиницистом для получения желаемого клинического ответа в соответствии с методами, известными клиницисту.
Количество соединения, описанного в настоящем описании, инсулина и другого терапевтического средства, которое будет эффективным в лечении и/или профилактике определенного заболевания, состояния или расстройства, будет зависеть от природы и выраженности заболевания, состояния или расстройства и может быть определено стандартными клиническими методиками. Кроме того исследования in vitro или in vivo могут необязательно быть использованы для облегчения определения оптимальных диапазонов дозировок. Точная используемая в композициях доза также будет зависеть от пути введения и серьезности расстройства и определяется в соответствии с решением практикующего врача и обстоятельствами каждого пациента. Однако подходящий диапазон дозировок для перорального введения обычно составляет от около 0,001 миллиграмм до около 200 миллиграмм на килограмм массы тела, от около 0,01 миллиграмм до около 100 миллиграмм на килограмм массы тела, от около 0,01 миллиграмм до около 70 миллиграмм на килограмм массы тела, от около 0,1 миллиграмм до около 50 миллиграмм на килограмм массы тела, от 0,5 миллиграмм до около 20 миллиграмм на килограмм массы тела, или от около 1 миллиграмм до около 10 миллиграмм на килограмм массы тела. В некоторых вариантах осуществления изобретения пероральная дозировка составляет около 5 миллиграмм на килограмм массы тела.
В некоторых вариантах осуществления изобретения подходящие диапазоны дозировок для внутривенного (в/в) введения составляют от около 0,01 мг до около 500 мг на кг массы тела, от около 0,1 мг до около 100 мг на кг массы тела, от около 1 мг до около 50 мг на кг масс тела или от около 10 мг до около 35 мг на кг массы тела. Подходящие диапазоны дозировок для других путей введения могут быть рассчитаны на основании вышеуказанных доз, как известно специалисту в области техники. Например, рекомендуемые дозировки для внутрикожного, внутримышечного, интраперитонеального, подкожного, эпидурального, сублингвального, интрацеребрального, интравагинального, трансдермального введения или введения посредством ингаляции находятся в диапазоне от около 0,001 мг до около 200 мг на кг массы тела, от около 0,01 мг до около 100 мг на кг массы тела, от около 0,1 мг до около 50 мг на кг массы тела или от около 1 мг до около 20 мг на кг массы тела. Эффективные дозы могут быть экстраполированы из кривых доза-ответ, полученных в тест-системах in vitro или моделях на животных. Такие модели на животных и системы хорошо известны в области техники.
Соединения, описанные в настоящем описании, могут быть рецептированы для парентерального введения посредством инъекции, например, посредством болюсной инъекции или непрерывной инфузии. Соединения можно вводить посредством непрерывной инфузии подкожно в течение периода от около 15 минут до около 24 часов. Композиции для инъекций могут быть представлены в стандартной лекарственной форме, такой как ампулы, или в многодозовых контейнерах, с добавлением консерванта. Композиции могут принимать такие формы как суспензии, растворы или эмульсии в масляных или водных носителях и могут содержать рецептурные средства, такие как суспендирующие, стабилизирующие и/или диспергирующиие средства. В некоторых вариантах осуществления изобретения инъекции находятся в форме короткодействующих, депо или имплантируемых форм и в форме гранул, вводимых подкожно или внутримышечно. В некоторых вариантах осуществления изобретения парентеральной лекарственной формой является форма раствора, суспензии, эмульсии или сухого порошка.
Для перорального введения соединения, описанные в настоящем описании, могут быть рецептированы путем смешивания соединений с фармацевтически приемлемыми носителями, хорошо известными в области техники. Такие носители позволяют соединениям быть рецептированными в виде таблеток, пилюль, драже, капсул, эмульсий, жидкостей, гелей, сиропов, саше, шариков, порошков, гранул, взвесей, пастилок, водных или масляных суспензий и подобных для перорального потребления пациентом, получающим лечение. Фармацевтические препараты для перорального применения могут быть получены, например, путем добавления твердого вспомогательного вещества, необязательно измельчения полученной смеси и обработки смеси гранул после добавления подходящих добавок, если желательно, для получения ядер таблеток или драже. Подходящие вспомогательные вещества включают, но не ограничиваются ими, наполнители, такие как сахара, включая, без ограничения, лактозу, сахарозу, маннит и сорбит; препараты целлюлозы, такие как, без ограничения, кукурузный крахмал, пшеничный крахмал, рисовый крахмал, картофельный крахмал, желатин, трагакантовая камедь, метилцеллюлоза, гидроксипропилметилцеллюлоза, карбоксиметилцеллюлоза натрия и поливинилпирролидон (PVP). При желании могут быть добавлены дезинтегрирующие средства, такие как, без ограничения, сшитый поливинилпирролидон, агар или альгиновая кислота или ее соль, такая как альгинат натрия.
Вводимые перорально композиции могут содержать одно или более необязательных средств, например, подсластители, такие как фруктоза, аспартам или сахарин; ароматизаторы, такие как мята перечная, винтергриновое масло, или вишня; красители; и консерванты, для обеспечения фармацевтически приятного на вкус препарата. Более того, находясь в форме таблетки или пилюли, композиции могут быть покрыты оболочкой для замедления разложения и абсорбции в желудочно-кишечном тракте, таким образом обеспечивая длительное действие в течение продолжительного периода времени. Селективно проницаемые мембраны, окружающие осмотически активное ведущее соединение, также являются подходящими для перорально вводимых соединений. Пероральные композиции могут включать стандартные носители, такие как маннит, лактоза, крахмал, стеарат магния, сахарин натрия, целлюлоза, карбонат магния и др. Такие носители имеют подходящую фармацевтическую степень чистоты.
Ядра драже могут быть обеспечены подходящими оболочками. С этой целью могут быть использованы концентрированные растворы сахара, которые могут необязательно содержать гуммиарабик, тальк, поливинилпирролидон, гель карбопол, полиэтиленгликоль, и/или диоксид титана, лаковые растворы и подходящие органические растворители или смеси растворителей. Красители или пигменты могут быть добавлены в оболочки таблеток или драже для обозначения или характеристики различных комбинаций доз активных соединений.
Фармацевтические препараты, которые могут быть использованы перорально, включают, но не ограничиваются ими, твердые капсулы, сделанные из желатина, а также мягкие герметичные капсулы, сделанные из желатина и пластификатора, такого как глицерин или сорбит. Твердые капсулы могут содержать активные ингредиенты в смеси с наполнителем, таким как лактоза, вяжущими веществами, такими как крахмалы, и/или смазывающими веществами, такими как тальк или стеарат магния, и необязательно, стабилизаторами. В мягких капсулах активные соединения могут быть растворены или суспендированы в подходящих жидкостях, таких как жирные масла, жидкий парафин или жидкие полиэтиленгликоли. Кроме того, могут быть добавлены стабилизаторы.
Для буккального введения композиции могут принимать форму, например, таблеток или пастилок, рецептированных обычным образом.
Для введения посредством ингаляции соединения, описанные в настоящем описании, могут доставляться в форме аэрозольного спрея из упаковок под давлением или небулайзера с использованием подходящего пропеллента, такого как дихлордифторметан, трихлорфторметан, дихлортетрафторэтан, диоксид углерода или другой подходящий газ. В случае аэрозоля под давлением единица дозирования может быть определена с помощью клапана для введения отмеренного количества. Могут быть рецептированы капсулы и картриджи из, например, желатина для применения в ингаляторе или инсуффляторе, содержащие порошковую смесь соединения и подходящего основания порошка, такого как лактоза или крахмал.
Соединения, описанные в настоящем описании, также могут быть рецептированы в ректальных композициях, таких как суппозитории или микроклизмы с удержанием, например, содержащие обычные основы для суппозиториев, такие как масло какао или другие глицериды. Соединения, описанные в настоящем описании, также могут быть рецептированы в вагинальных композициях, таких как вагинальные кремы, суппозитории, пессарии, вагинальные кольца и внутриматочные устройства.
При трансдермальном введении соединения могут быть нанесены на пластырь или могут применяться при помощи трансдермальных терапевтических систем, которые последовательно используются. В некоторых вариантах осуществления изобретения соединения присутствуют в кремах, растворах, порошках, жидких эмульсиях, жидких суспензиях, полутвердых веществах, мазях, пастах, гелях, желе и пенах, или в пластырях, содержащих любое из них.
Соединения, описанные в настоящем описании, также могут быть рецептированы, как препараты депо. Такие композиции длительного действия можно вводить путем имплантации (например, подкожно или внутримышечно) или посредством внутримышечной инъекции. Депо-инъекции можно вводить с интервалами от около 1 до около 6 месяцев или больше. Следовательно, например, соединения могут быть рецептированы с подходящими полимерными или гидрофобными материалами (например, в виде эмульсии в приемлемом масле) или ионообменными смолами или в виде умеренно растворимых производных, например, в виде умеренно растворимой соли.
В еще одном варианте осуществления изобретения соединения можно вводить в системе контролируемого высвобождения. В одном варианте осуществления изобретения может быть использована помпа (см. Langer, выше; Sefton, CRC Crit. Ref. Biomed. Eng., 1987, 14, 201; Buchwald et al., Surgery, 1980, 88, 507 Saudek et al., N. Engl. J. Med., 1989, 321, 574). В другом варианте осуществления изобретения могут быть использованы полимерные материалы (см. Medical Applications of Controlled Release, Langer and Wise (eds.), CRC Pres., Boca Raton, Fla. (1974); Controlled Drug Bioavailability, Drug Product Design and Performance, Smolen and Ball (eds.), Wiley, New York (1984); Ranger et al., J. Macromol. Sci. Rev. Macromol. Chem., 1983, 23, 61; см. также Levy et al., Science, 1985, 228, 190; During et al., Ann. Neurol., 1989, 25, 351; Howard et al., J. Neurosurg., 1989, 71, 105). В еще одном варианте осуществления изобретения система контролируемого высвобождения может быть помещена вблизи от цели соединений, описанных в настоящем описании, такой как печень, таким образом, требуя только долю системной дозы (см., например, Goodson, in Medical Applications of Controlled Release, supra, vol. 2, pp. 115-138 (1984)). Могут быть использованы другие системы контролируемого высвобождения, обсуждаемые в обзоре Langer, Science, 1990, 249, 1527-1533).
Также известно в области техники, что соединения могут содержаться в таких композициях с фармацевтически приемлемыми разбавителями, наполнителями, дезинтегрирующими веществами, вяжущими веществами, смазывающими веществами, поверхностно-активными веществами, гидрофобными носителями, водорастворимыми носителями, эмульгаторами, буферами, увлажнителями, растворителями, консервантами и подобными. Фармацевтические композиции также могут включать подходящие твердые или гелевые носители или вспомогательные вещества. Примеры таких носителей или вспомогательных веществ включают, но не ограничиваются ими, карбонат кальция, фосфат кальция, различные сахара, крахмалы, производные целлюлозы, желатин и полимеры, такие как полиэтиленгликоли. В некоторых вариантах осуществления изобретения соединения, описанные в настоящем описании, могут быть использованы со средствами, включающими, без ограничения, местные анестетики (например, лидокаин), барьерные устройства (например, GelClair), или ополаскиватели (например, Caphosol).
В некоторых вариантах осуществления изобретения соединения, описанные в настоящем описании, могут быть доставлены в пузырьках, в частности, липосомах (см., Langer, Science, 1990, 249, 1527-1533; Treat et al., in Liposomes in the Therapy of Infectious Disease and Cancer, Lopez-Berestein and Fidler (eds.), Liss, New York, pp. 353-365 (1989); Lopez-Berestein, там же, pp. 317-327; см. в общем там же).
Подходящие композиции включают, но не ограничиваются ими, неабсорбируемые композиции. Подходящие композиции также включают, но не ограничиваются ими, солевой раствор, воду, растворы циклодекстрина и буферные растворы с pH 3-9.
Соединения, описанные в настоящем описании, или их фармацевтически приемлемые соли, могут быть рецептированы с множеством вспомогательных веществ, включающих, без ограничения, очищенную воду, пропиленгликоль, PEG 400, глицерин, DMA, этанол, бензиловый спирт, лимонную кислоту/цитрат натрия (pH3), лимонную кислоту/цитрат натрия (pH5), трис(гидроксиметил)аминометан HCl (pH7,0), 0,9% солевой раствор, и 1,2% солевой раствор и любые их комбинации. В некоторых вариантах осуществления изобретения вспомогательное вещество выбирают из пропиленгликоля, очищенной воды и глицерина.
В некоторых вариантах осуществления изобретения композиция может быть лиофилизирована до твердого вещества, и восстановлена перед применением с помощью, например, воды.
При введении млекопитающим (например, животному при ветеринарном применении или человеку при клиническом применении) соединения можно вводить в выделенной форме.
При введении человеку соединения могут быть стерильными. Вода является подходящим носителем, когда соединение вводят внутривенно. Солевые растворы и водные растворы декстрозы и глицерина также могут быть использованы в качестве жидких носителей, особенно для инъекционных растворов. Подходящие фармацевтические носители также включают вспомогательные вещества, такие как крахмал, глюкоза, лактоза, сахароза, желатин, солод, рис, мука, сел, силикагель, стеарат натрия, моностеарат глицерина, тальк, хлорид натрия, сухое снятое молоко, глицерин, пропилен, гликоль, вода, этанол и подобные. Настоящие композиции, если желательно, также могут содержать минимальные количества увлажняющих или эмульгирующих средств, или буферов рН.
Композиции, описанные в настоящем описании, могут принимать форму раствора, суспензии, эмульсии, таблетки, пилюли, шариков, капсул, капсул, содержащих жидкость, порошок, композиции длительного высвобождения, суппозиториев, аэрозоля, спрея, или любой другой формы, подходящей для применения. Примеры подходящих фармацевтических носителей описаны в Remington's Pharmaceutical Sciences, A.R. Gennaro (Editor) Mack Publishing Co.
В одном варианте осуществления изобретения соединения рецептируют в соответствии с обычными методиками как фармацевтическую композицию, адаптированную для введения людям. Обычно, соединениями являются растворы в стерильном изотоническом водном буфере. Когда необходимо, композиции также могут включать растворитель. Композиции для внутривенного введения могут необязательно включать местные анестетики, такие как лидокаин, для облегчения боли в месте инъекции. Обычно ингредиенты поставляются или отдельно или смешанными вместе в стандартной лекарственной форме, например, в виде сухого лиофилизированного порошка или безводного концентрата в герметично закупоренном контейнере, таком как ампула или саше, с указанием количества активного вещества. Когда соединение необходимо вводить путем инфузии, оно может быть представлено, например, с инфузионной бутылью, содержащей стерильную воду фармацевтической степени чистоты или солевой раствор. Когда соединение вводят посредством инъекции, могут быть обеспечены так ампулы стерильной воды для инъекций или солевого раствора, чтобы ингредиенты можно было смешать перед введением.
Фармацевтические композиции могут находиться в стандартной лекарственной форме. В такой форме композиция может быть разделена на стандартные дозы, содержащие соответствующие количества активного компонента. Стандартной лекарственной формой может быть упакованный препарат, упаковка, содержащая отдельные количества препаратов, например, упакованные таблетки, капсулы и порошки во флаконах или ампулах. Стандартной лекарственной формой также может быть капсула, саше или таблетка как таковая или это может быть соответствующее количество любых из таких упакованных форм.
В некоторых вариантах осуществления изобретения композиция по настоящему изобретению находится в форме жидкости, где активное вещество (т.е. один из номинально амфифильных полимеров или олигомеров, описанных в настоящем описании) присутствует в растворе, в суспензии, в виде эмульсии или в виде раствора/суспензии. В некоторых вариантах осуществления изобретения жидкая композиция находится в форме геля. В других вариантах осуществления изобретения жидкая композиция является водной. В других вариантах осуществления изобретения композиция находится в форме мази.
Подходящие консерванты включают, но не ограничиваются, ртуть-содержащие вещества, такие как фенилртутные соли (например, ацетат, борат и нитрат фенилртути) и тимеросал; стабилизированной диоксид хлора; соединения четвертичного аммония, такие как хлорид бензалкония, бромид цетилтриметиламмония и хлорид цитилпиридина; имидазолидинил мочевина; парабены, такие как метилпарабен, этилпарабен, пропилпарабен и бутилпарабен, и их соли; феноксиэтанол; хлорфеноксиэтанол; феноксипропанол; хлорбутанол; хлоркрезол; фенилэтилэтиловый спирт; EDTA динатрия; и сорбиновая кислота и ее соли.
Необязательно один или более стабилизаторов могут быть включены в композиции для улучшения химической стабильности, когда требуется. Подходящие стабилизаторы включают, но не ограничиваются ими, хелатирующие средства или комплексообразующие средства, такие как, например, средства образующие комплексы с кальцием, этилендиаминтетрауксусная кислота (EDTA). Например, соответствующее количество EDTA или ее соли, например, динатриевой соли, может быть включено в композицию для связывания избытка ионов кальция и предотвращения образования при хранении геля. EDTA или ее соль могут соответствующим образом быть включены в количестве от около 0,01% до около 0,5%. В указанных вариантах осуществления изобретения, содержащих консервант, иной, чем EDTA, EDTA или ее соль, точнее EDTA динатрия, могут быть представлены в количестве от около 0,025% до около 0,1 масс%.
Также в композиции могут быть включены один или более антиоксидантов. Подходящие антиоксиданты включают, но не ограничиваются ими, аскорбиновую кислоту, метабисульфит натрия, бисульфит натрия, ацетилцистеин, поликватерниум-1, хлорид бензалкония, тимеросал, хлорбутанол, метилпарабен, пропилпарабен, фенилэтиловый спирт, эдетат динатрия, сорбиновую кислоту или другие средства, известные специалисту в области техники. Такие консерванты обычно используются в количестве от около 0,01% до около 1,0 масс%.
В некоторых вариантах осуществления изобретения соединения растворяют, по меньшей мере, частично при помощи приемлемого растворителя. Определенные приемлемые неионные поверхностно-активные вещества, например, полисорбат 80, могут быть применимыми в качестве растворителей, как и гликоли, полигликоли, например, полиэтиленгликоль 400 (PEG-400), и эфиры гликоля.
Подходящими растворителями для композиций растворов и растворов/суспензий являются циклодекстрины. Походящие циклодекстрины могут быть выбраны из α-циклодекстрина, β-циклодекстрина, γ-циклодекстрина, алкилциклодекстринов (например, метил-β-циклодекстрина, диметил-β-циклодекстрина, диэтил-β-циклодекстрина), гидроксиалкилциклодекстринов (например, гидроксиэтил-β-циклодекстрина, гидроксипропил-β-циклодекстрина), карбоксиалкилциклодекстринов (например, карбоксиметил-β-циклодекстрина), циклодекстринов сульфоалкилового эфира (например, β-циклодекстрин сульфобутилового эфира), и подобные. Применения циклодекстринов описано в Rajewski et al., Journal of Pharmaceutical Sciences, 1996, 85, 1155-1 159. Приемлемый циклодекстрин может необязательно присутствовать в композиции в концентрации от около 1 до около 200 мг/мл, от около 5 до около 100 мг/мл, или от около 10 до около 50 мг/мл.
В некоторых вариантах осуществления изобретения композиция необязательно содержит суспендирующее средство. Например, в указанных вариантах осуществления изобретения, в которых композиция является водной суспензией или раствором/суспензией, композиция может содержать один или более полимеров в качестве суспендирующих средств. Применимые полимеры включают, но не ограничиваются ими, водорастворимые полимеры, такие как полимеры целлюлозы, например, гидроксипропилметилцеллюлоза, и водонерастворимые полимеры, такие как сшитые полимеры, содержащие карбоксил. Однако в некоторых вариантах осуществления изобретения композиции не содержат существенных количеств твердых частиц, так как антимикробный полимер или олигомерное активное вещество, вспомогательного вещества или оба, в виде твердых частиц, если содержатся, могут вызывать дискомфорт и/или раздражение обрабатываемого глаза.
В композиции могут быть включены одно или более приемлемых средств, регулирующих рН, и/или буферов, включая кислоты, такие как уксусная, борная, лимонная, молочная, фосфорная и соляная кислоты; основания, такие как гидроксид натрия, фосфат натрия, борат натрия, цитрат натрия, ацетат натрия, лактат натрия и трис-гидроксиметиламинометан; и буферы, такие как цитрат/декстроза, бикарбонат натрия и хлорид аммония. Такие кислоты, основания и буферы включают в количестве, необходимом для поддержания pH композиции в приемлемом диапазоне.
Необязательно одно или более приемлемых поверхностно-активных веществ, предпочтительно неионных поверхностно-активных веществ или со-растворителей могут быть включены в композиции для усиления растворимости компонентов композиций или для воздействия на физическую стабильность, или для других целей. Подходящие неионные поверхностно-активные вещества включают, но не ограничиваются ими, глицериды жирных кислот и полиоксиэтилена и растительных масел, например полиоксиэтилен (60) гидрогенизированное касторовое масло; и алкилэфиры и алкилфенилэфиры полиоксиэтилена, например, октоксинол 10, октоксинол 40; полисорбат 20, 60 и 80; поверхностно-активные вещества полиоксиэтилена/полиоксипропилена (например, Pluronic® F-68, F84 и P-103); циклодекстрин; или другие средства, известные специалисту в области техники. Обычно такие со-растворители или поверхностно-активные вещества используются в композициях в количестве от около 0,01% до около 2 масс%.
Одно или более смазывающих средств также могут необязательно быть включены в композиции для обеспечения слезоотделения или в качестве препарата от «сухого глаза». Такие средства включают, но не ограничиваются ими, поливиниловый спирт, метилцеллюлозу, гидроксипропилметилцеллюлозу, поливинилпирролидон и подобные. Понимают, что обеспечение слезоотделения является полезным в настоящем изобретении только когда слезоотделение естественным образом подавлено, для восстановления нормальной степени секреции слезной жидкости. Когда развивается избыточное слезоотделение, время удержания композиции в глазу может быть уменьшено.
Настоящее описание также обеспечивает фармацевтические упаковки или наборы, включающие один или более контейнеров, наполненных одним или более соединениями или композициями, описанными в настоящем описании. Необязательно вместе с такими контейнерами(ом) могут поставляться аннотации в форме, предписанной правительственным агентством, регулирующим производство, применение или продажу фармацевтических препаратов или биологических продуктов, такая аннотация отражает одобрение агентства по производству, применению или продаже для введения людям для лечения состояния, заболевания или расстройства, описанного в настоящем описании. В некоторых вариантах осуществления изобретения набор содержит более чем одно соединение или композицию, описанные в настоящем описании. В некоторых вариантах осуществления изобретения набор включает соединение, описанное в настоящем описании, и инсулин, и необязательно другое терапевтическое средство, в одной инъекционной лекарственной форме, такой как разовая доза в инъекционном устройства, таком как шприц с иглой.
Настоящее описание также обеспечивает методы лечения диабета I типа и/или диабета II типа у млекопитающего, включающие введение млекопитающему, нуждающемуся в этом, эффективного количества инсулина и приемлемого количества одного или более соединений, описанных выше, или их фармацевтически приемлемой соли. В некоторых вариантах осуществления изобретения млекопитающему может быть установлен диагноз диабета I или II типа или предиабета до лечения. В некоторых вариантах осуществления изобретения может не быть формального диагноза; в таких вариантах осуществления изобретения млекопитающее может предположительно иметь диабет I или II типа или предиабет, лечение которого желательно. В некоторых вариантах осуществления изобретения методы могут быть использованы для лечения осложнений ожирения и диабета таких как, например, гиперхолестеринемия, гипертония, ишемическая болезнь сердца, диабетическая нейропатия, диабетическая ретинопатия, эректильная дисфункция и заболевания почек.
В некоторых вариантах осуществления изобретения соединения, описанные в настоящем описании, можно вводить или одновременно или последовательно с инсулином. Следовательно, в некоторых вариантах осуществления изобретения сначала вводят инсулин, а потом соединение, описанное в настоящем описании любой из формул I-V. В некоторых вариантах осуществления изобретения сначала вводят соединение, описанное в настоящем описании любой из формул I-V, а потом инсулин. В некоторых вариантах осуществления изобретения инсулин и соединение, описанное в настоящем описании любой из формул I-V, вводят одновременно. При введении одновременно инсулин и соединение, описанное в настоящем описании любой из формул I-V, могут присутствовать в отдельных фармацевтических композициях или могут быть смешаны в одной фармацевтической композиции, такой как любая из множества композиций, описанных в настоящем описании. В некоторых вариантах осуществления изобретения настоящая схема введения для инсулина может быть использована для введения и инсулина и соединения по любой из формул I-V, описанных в настоящем описании.
В некоторых вариантах осуществления изобретения эффективное количество любого из соединений по формуле I-V составляет от около 0,1 мг/кг до около 100 мг/кг, от около 0,5 мг/кг до около 50 мг/кг, от около 1 мг/кг до около 25 мг/кг, или от около 5 мг/кг до около 20 мг/кг.
Уровень доз и частота инъекций инсулина варьируется в зависимости от типа диабета (тип I или II), состояния чувствительности рецепторов инсулина, возраста и уровня глюкозы крови и определяются для каждого пациента. Начальные дозы для инсулинов являются следующими: инсулины быстрого действия, такие как Хумалог, вводят в начальной дозе 0,5 ЕД/кг/сутки; инсулины короткого действия, такие как Хумулин, вводят в начальной дозе 0,5 ЕД/кг/сутки; инсулины промежуточной продолжительности действия, такие как НПХ, и инсулины длительного действия, такие как Лантус, вводят в начальной дозе 0,2 ЕД/кг/сутки.
В некоторых вариантах осуществления изобретения инсулины быстрого действия, такие как Хумалог, или инсулины короткого действия, такие как Хумулин, вводят (вместе с соединением по формуле I-V) в начальной дозе от около 0,05 ЕД/кг/сутки до около 5 ЕД/кг/сутки, от около 0,1 ЕД/кг/сутки до около 2,5 ЕД/кг/сутки, или от около 0,3 ЕД/кг/сутки до около 0,8 ЕД/кг/сутки. В некоторых вариантах осуществления изобретения инсулины быстрого действия, такие как Хумалог, или инсулины короткого действия, такие как Хумулин, вводят (вместе с соединением по формуле I-V) в начальной дозе около 0,5 ЕД/кг/сутки.
В некоторых вариантах осуществления изобретения инсулины промежуточной продолжительности действия, такие как НПХ, и инсулины длительного действия, такие как Лантус, вводят (вместе с соединением по формуле I-V) в начальной дозе от около 0,01 ЕД/кг/сутки до около 3 ЕД/кг/сутки, от около 0,05 ЕД/кг/сутки до около 0,6 ЕД/кг/сутки или от около 0,1 ЕД/кг/сутки до около 0,3 ЕД/кг/сутки. В некоторых вариантах осуществления изобретения инсулины промежуточной продолжительности действия, такие как НПХ, и инсулины длительного действия, такие как Лантус, вводят (вместе с соединением по формуле I-V) в начальной дозе около 0,02 ЕД/кг/сутки.
С целью более эффективного понимания настоящего описания ниже представлены примеры. Необходимо понимать, что представленные примеры предназначены только для целей иллюстрации и не должны рассматриваться как каким-либо образом ограничивающие заявленные варианты осуществления изобретения. На всем протяжении представленных примеров реакции молекулярного клонирования и другие стандартные методики рекомбинантной ДНК осуществляют в соответствии с методами, описанными в Maniatis et al., Molecular Cloning - A Laboratory Manual, 2nd ed., Cold Spring Harbor Press (1989), с использованием коммерчески доступных реагентов, если не отмечено иначе.
Примеры
Пример 1: Db/db Исследование 1
В настоящем исследовании использовали самцов DbDb Lep-дефицитных мышей (Harlan Laboratories) в возрасте приблизительно 16 недель. Дизайн эксперимента показан в таблице 1.
Дизайн эксперимента 1
Методика: Мышей делили на 4 группы по 6 мышей на группу. Уровень глюкозы крови измеряли с использованием глюкометров Accu-Chek Aviva (Roche Diagnostics). Уровни глюкозы крови измеряли до 72 часов после введения. Глюкометры калибровали перед каждым исследованием. Кровь (5 мкл) получали из надреза хвоста и непосредственно наносили на тест-полоску для определения глюкозы. Уровни глюкозы представляли как мг/дл.
В исследовании 1, животные голодали в течение 4 часов перед введением тестируемых соединений и затем непрерывно голодали до 8-часовой временной точки. Затем животных обеспечивали пищей по потребности до 4-часов перед 28-часовой временной точкой, после которой они голодали до измерения последней временной точки глюкозы крови.
Данные выражали как среднее ± стандартная ошибка среднего значения. Данные анализировали двухфазовым дисперсионным анализом с последующей поправкой Бонферрони для множественных сравнений. N=6/группу.
Результаты: В исследовании 1 мыши db/db в возрасте 16 недель имели уровень глюкозы крови натощак, который в среднем составил 482 мг/дл. Инсулин снижал уровень глюкозы крови в среднем до 166,5 мг/дл через три часа после введения. Уровень глюкозы крови возвращался к исходному уровню у животных, получавших инсулин, через 8 часов. Введение Соединения 102 существенно не влияло на уровень глюкозы крови в любой момент времени после введения. Однако совместное введение Соединения 102 с инсулином удлиняло ответ на инсулин с достоверным снижением глюкозы крови, наблюдаемым до, по меньшей мере, 52 часов после введения. Исторические данные этой лаборатории показали, что db/db мыши в возрасте 16 недель имели уровень инсулина меньший чем или равный 1 нг/мл, по сравнению с пиковым уровнем инсулина у 7 недельных мышей db/db около 10 нг/мл и уровнем инсулина у худых контрольных животных без диабета в среднем около 2-5 нг/мл. Результаты показаны на фиг. 1.
Совместное введение Соединения 102 с инсулином усиливало снижение глюкозы крови в ответ на инсулин. *p<0,05; при сравнении инсулина с совместным введением инсулина/Соединения 102. Небольшое, но статистически недостоверное снижение глюкозы крови в группе лечения Соединением 102 вероятно является результатом низкого уровня продукции инсулина, остающегося у взрослых мышей db/d/b.
Пример 2: Db/db исследование 2
В настоящем исследовании использовали самцов DbDb Lep-дефицитных мышей (Harlan Laboratories) в возрасте приблизительно 18 недель. Дизайн эксперимента показан в таблице 2.
Дизайн эксперимента исследования 2
Методика: Мышей делили на 4 группы по 6 мышей в группе. Уровни глюкозы в крови измеряли с использованием глюкометров Accu-Chek Aviva (Roche Diagnostics). Уровень глюкозы крови измеряли до 72 часов после введения. Глюкометры калибровали перед каждым исследованием. Кровь (5 мкл) получали из надреза хвоста и непосредственно наносили на тест-полоску для определения глюкозы. Уровни глюкозы представляли как мг/дл.
В исследовании 2 животные голодали в течение 4 часов перед каждым измерением глюкозы крови и затем возвращались к питанию по потребности.
Данные представлены как среднее +- стандартная ошибка среднего значения. Данные анализировали двухфазовым дисперсионным анализом с последующей поправкой Бонферрони для множественных сравнений. N=6/группу.
Результаты: Второе исследование проводили для повторения обнаруженных эффектов Соединения 102 в отношении действия инсулина в окно времени 24-72 часа и специфического отслеживания эффекта комбинации инсулина/Соединения 102 на всем протяжении, пока оно не вернется к нормальному уровню (т.е. таковому животных, получавших носитель). Во втором исследовании существовало три отличия от первого: 1) в момент исследования мыши были в возрасте 18 недель, 2) уровень дозы инсулина снижали с 3 до 1,5 ЕД/кг и 3) уровень глюкозы крови измеряли до 72 часов после введения.
В проведенном исследовании уровень глюкозы крови натощак в среднем составил 420 мг/дл. Через двадцать четыре часа после введения инсулина отдельно или введения Соединения 102 отдельно уровень глюкозы крови не отличался от контрольной группы. Однако совместное введение инсулина с Соединением 102 давало достоверное снижение глюкозы крови во временные точки 24, 36 и 48 часов. Уровень глюкозы крови у животных, которым вводили совместно инсулин/Соединение 102, возвращался к исходному уровню через 72 часа. Результаты показаны на фиг. 2.
Совместное введение Соединения 102 с инсулином усиливало снижение глюкозы крови в ответ инсулином. *p<0,05; **p<0,01 при сравнении инсулина с совместным введением инсулина/Соединения 102. Группа, получавшая инсулин, не показала снижения глюкозы крови, так как действие инсулина в норме приводит снижению глюкозы крови в наибольшей степени между 2-4 часами и завершается через 8 часов; настоящее исследование не включало указанный временной период. Немного повышенный уровень глюкозы крови в группе, получавшей инсулин, через 24 и 36 часов представляет собой эффект "рикошета", который часто наблюдают у животных, получающих инсулин.
Пример 3: Исследования со Стрептозоцином
В настоящем исследовании использовали самцов мышей CD-1:ICR (Charles River) в возрасте приблизительно 8 недель. Дизайн эксперимента показан в таблице 3. Введение Стрептозоцина мышам разрушало β-клетки поджелудочной железы и использовалось для получения модели диабета I типа. В ответ на потерю β-клеток поджелудочной железы у мышей развивалась гипергликемия. Такие мыши отвечают на инсулин.
Дизайн эксперимента исследования STZ
Методика:
Введение стрептозоцина: Введение стрептозоцина мышам проводили стандартным методом. Коротко, мышам вводили STZ в дозе 70 мг/кг в дни 1, 3 и 8. Каждому введению предшествовало 18 часовое голодание. Мышам вводили инсулин (0,5 ЕД) в дни 2 и 9. В день 11, измеряли уровень глюкозы крови. Мышей с уровнем глюкозы крови менее чем 300 мг/дл исключали из исследования. Мышей рандомизировали в группы лечения.
Мышам проводили тест на толерантность к инсулину в день 14 после исходного введения STZ. Мышам вводили инсулин (0,35 ЕД п/к) и затем через 30 минут вводили Соединение 102 (100 мг/кг и.п.).
Глюкозу крови измеряли через 5, 15, 30, 60, 90, 120, 180, 240, 360, и 480 минут после введения Соединения 102 или носителя. Кровь собирали из надреза хвоста и в капле крови измеряли уровень глюкозы глюкометром (глюкометры Accu-Chek Aviva; Roche Diagnostics).
Данные представлены как среднее +- стандартная ошибка среднего значения. Данные анализировали двухфазовым дисперсионным анализом с последующей поправкой Бонферрони для множественных сравнений. N=6/группу
Результаты: Введение стрептозоцина повышало уровень глюкозы крови до более чем 500 мг/дл. Такой уровень глюкозы показывал, что β-клетки поджелудочной железы были полностью разрушены. Введение Соединения 102 не влияло на уровень глюкозы крови в любой временной точке до 6 часов после введения. Введение инсулина снижало уровень глюкозы крови с 546 мг/дл (исходно) до 263 мг/дл через 90 минут после введения. Уровень глюкозы крови возвращался к исходному уровню через 4,5 часа после введения.
В комбинации с инсулином Соединение 102 потенцировало эффект инсулина. Соединение 102 вводили через 30 минут после введения инсулина. Соединение 102 увеличивало снижение глюкозы крови, опосредованное инсулином, до 157 мг/дл (по сравнению с 263 мг/дл с инсулином отдельно). Более того уровень глюкозы крови был все еще снижен до 6 часов после введения.
Полученные данные показывают, что Соединение 102 потенцирует и пролонгирует действие инсулина у мышей с диабетом I типа.
Для введения носителя и лечения Соединением 102 у мышей с стрептозоциновым диабетом I типа, мышам вводили Соединение 102 или носитель в момент времени 0. Уровень глюкозы крови измеряли до 6 часов после введения. Соединение 102 не влияло на уровень глюкозы крови у мышей, лишенных инсулина. Для инсулина в комбинации с Соединением 102, инсулин вводили за 30 минут до Соединения 102. Соединение 102 вводили в момент времени 0. Уровень глюкозы крови измеряли до 6 часов после введения. Введение Соединения 102 потенцировало и пролонгировало снижение глюкозы крови, опосредованное инсулином. *p<0,05 при сравнении с лечением инсулином отдельно. ***p<0,001 при сравнении с лечением инсулином отдельно. Данные представлены как среднее ± стандартная ошибка среднего значения. Данные анализировали двухфазовым дисперсионным анализом с последующей поправкой Бонферрони для множественных сравнений. Результаты показаны на фиг. 3.
В проведенных исследованиях совместное введение Соединения 102 с инсулином обеспечивало достоверно пролонгированный ответ снижения глюкозы крови, опосредованного инсулином, у мышей db/db, кроме того, введение Соединения 102 мышам с диабетом I типа, получавшим инсулин, потенцировало и пролонгировало действие инсулина.
Полученные данные предполагают, что Соединение 102 может быть использовано в качестве дополнительной терапии с инсулином для пролонгирования активности инсулина на поздней стадии диабета II типа и при диабете I типа.
Различные модификации изобретения в добавление к описанным в настоящем описании очевидны специалисту в области техники из представленного описания. Такие модификации также попадают в рамки приложенной формулы изобретения. Каждая ссылка (включая, без ограничения, журнальные статьи, патенты США и не-США, публикации патентных заявок, публикации международных патентных заявок, каталожные номера банков генов и подобные), цитируемые в настоящей заявке, включены в настоящее описание в виде ссылки во всей полноте.
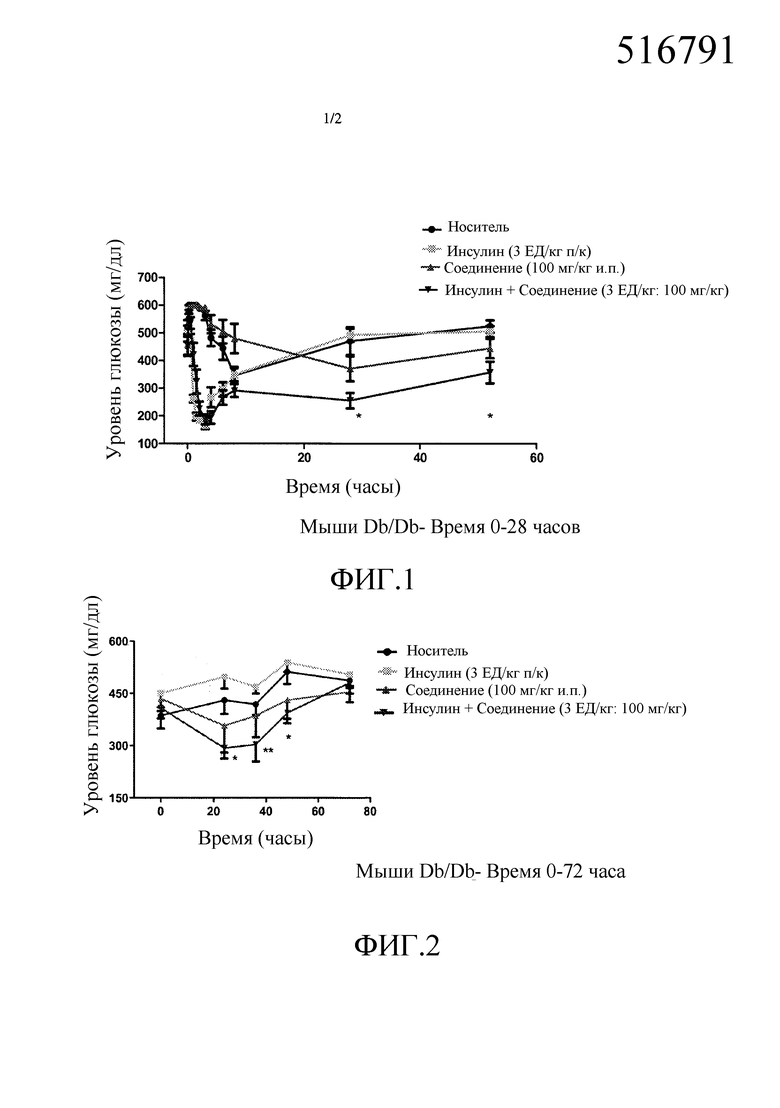
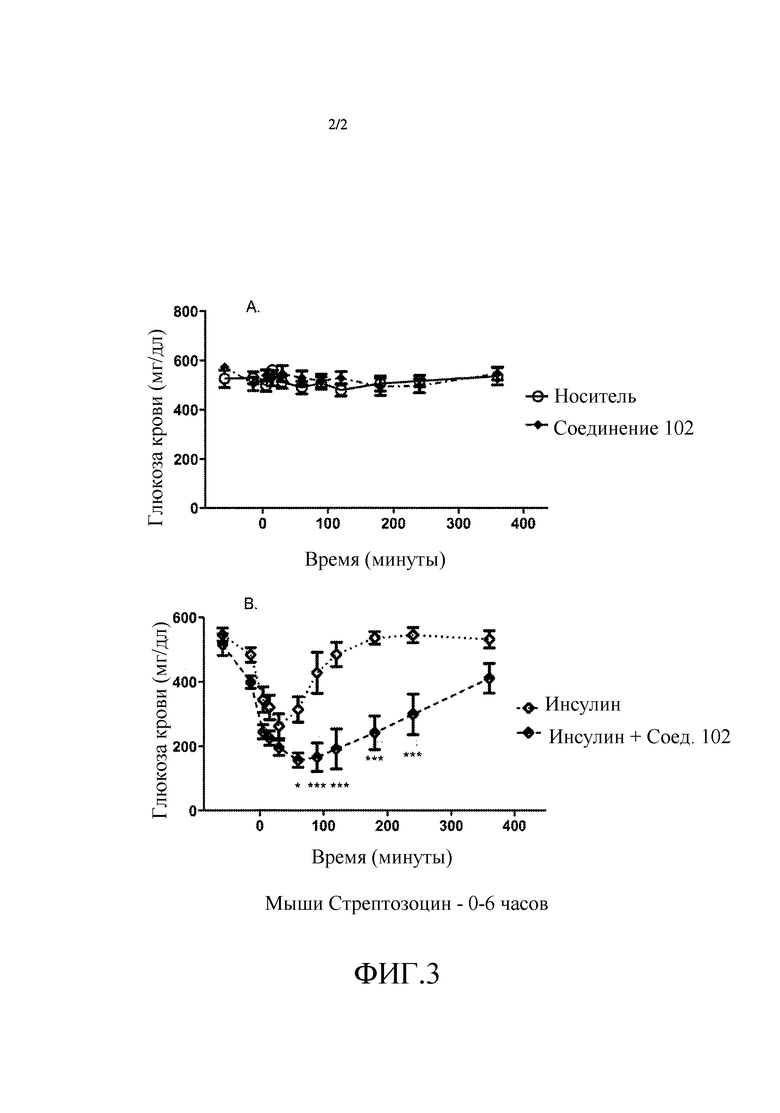
Настоящая группа изобретений относится к медицине, а именно к эндокринологии, и касается лечения диабета 1 и 2 типа. Для этого вводят инсулин в сочетании с эффективным количеством толимидона. Такое сочетанное введение обеспечивает усиление и пролонгирование сахароснижающего действия инсулина за счет способности толимидона модулировать активность Lyn киназ, потенцирующих действие инсулина. 3 н. и 15 з.п. ф-лы, 3 табл, 3 пр.,3 ил.
1. Способ лечения диабета I типа у млекопитающего, включающий последовательное введение млекопитающему, нуждающемуся в этом, эффективного количества инсулина, после чего осуществляют более позднее введение эффективного количества соединения:
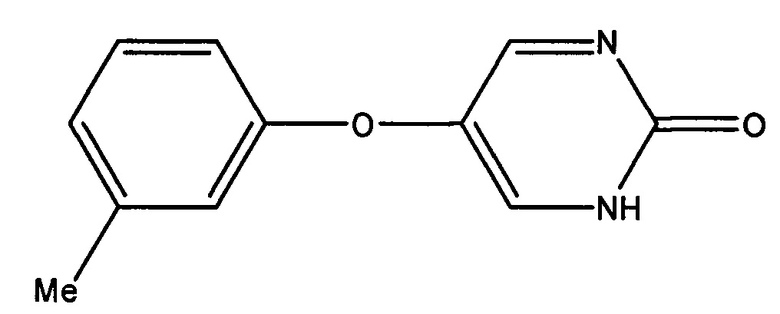
или его фармацевтически приемлемой соли.
2. Способ по п. 1, где млекопитающим является человек.
3. Способ по п. 1, где эффективное количество соединения составляет от около 0,1 мг/кг до около 100 мг/кг.
4. Способ по п. 1, где введение является пероральным.
5. Способ по п. 1, где инсулин выбран из инъекционного инсулина, чрескожного инсулина и ингаляционного инсулина.
6. Способ по п. 1, где инсулин выбран из инсулина быстрого действия, инсулина короткого действия, инсулина промежуточной продолжительности действия и инсулина длительного действия.
7. Способ по п. 6, где эффективное количество инсулина быстрого действия или инсулина короткого действия составляет от около 0,05 ЕД/кг/сутки до около 5 ЕД/кг/сутки, от около 0,1 ЕД/кг/сутки до около 2,5 ЕД/кг/сутки или от около 0,3 ЕД/кг/сутки до около 0,8 ЕД/кг/сутки.
8. Способ по п. 6, где эффективное количество инсулина промежуточной продолжительности действия или инсулина длительного действия составляет от около 0,01 ЕД/кг/сутки до около 3 ЕД/кг/сутки, от около 0,05 ЕД/кг/сутки до около 0,6 ЕД/кг/сутки или от около 0,1 ЕД/кг/сутки до около 0,3 ЕД/кг/сутки.
9. Способ по любому из пп. 1-8, где соединение вводят млекопитающему через 30 минут после введения инсулина.
10. Способ лечения диабета I типа у млекопитающего, включающий введение млекопитающему, нуждающемуся в этом, композиции, содержащей эффективное количество инсулина и эффективное количество соединения:
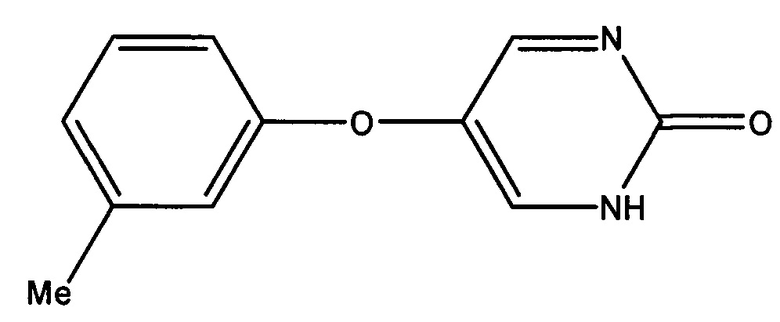
или его фармацевтически приемлемой соли.
11. Способ по п. 10, где млекопитающим является человек.
12. Способ по п. 10, где эффективное количество соединения составляет от около 0,1 мг/кг до около 100 мг/кг.
13. Способ по п. 10, где введение является пероральным.
14. Способ по п. 10, где инсулин выбран из инъекционного инсулина, чрескожного инсулина и ингаляционного инсулина.
15. Способ по п. 10, где инсулин выбран из инсулина быстрого действия, инсулина короткого действия, инсулина промежуточной продолжительности действия и инсулина длительного действия.
16. Способ по п. 15, где эффективное количество инсулина быстрого действия или инсулина короткого действия составляет от около 0,05 ЕД/кг/сутки до около 5 ЕД/кг/сутки, от около 0,1 ЕД/кг/сутки до около 2,5 ЕД/кг/сутки, или от около 0,3 ЕД/кг/сутки до около 0,8 ЕД/кг/сутки.
17. Способ по п. 15, где эффективное количество инсулина промежуточной продолжительности действия или инсулина длительного действия составляет от около 0,01 ЕД/кг/сутки до около 3 ЕД/кг/сутки, от около 0,05 ЕД/кг/сутки до около 0,6 ЕД/кг/сутки или от около 0,1 ЕД/кг/сутки до около 0,3 ЕД/кг/сутки.
18. Композиция для перорального применения для лечения или профилактики диабета I типа в форме таблетки, гелевой капсулы или капсулы, включающая инсулин и от около 1 мг до около 1000 мг соединения:
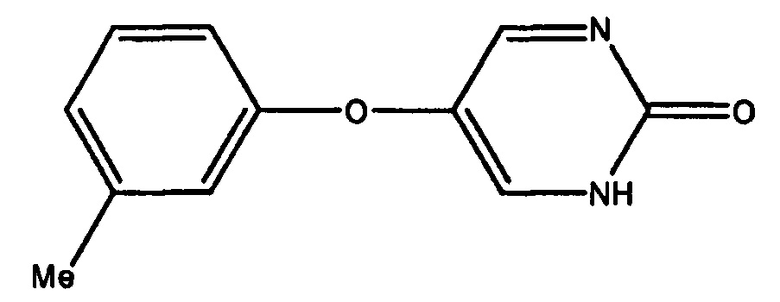
или его фармацевтически приемлемой соли.
| СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА ИНСУЛИНА ДЛЯ ПЕРОРАЛЬНОГО ПРИМЕНЕНИЯ | 2006 |
|
RU2316339C1 |
| US 2007093516 A1 26.04.2007 | |||
| US 20100278804 A1 04.11.2010 | |||
| ВАЛУЕВ Л.И | |||
| и др | |||
| "Пероральный препарат инсулина для регулирования уровня глюкозы в крови" | |||
| Биомедицинская химия, 2009, т.55, вып.2, с.193-200 | |||
| MULLER G | |||
| et al | |||
| Плуг с фрезерным барабаном для рыхления пласта | 1922 |
|
SU125A1 |
| ЩИТОВОЙ ДЛЯ ВОДОЕМОВ ЗАТВОР | 1922 |
|
SU2000A1 |
Авторы
Даты
2018-03-05—Публикация
2012-12-12—Подача