ОБЛАСТЬ ИЗОБРЕТЕНИЯ
[001] Настоящее изобретение обеспечивает пероральные композиции, содержащие белок, усилитель всасывания и ингибитор протеаз, и способ введения указанных композиций.
УРОВЕНЬ ТЕХНИКИ
[002] Благодаря достижениям в области биотехнологии, доступность биологически активных пептидов в фармацевтической промышленности значительно возросла. Тем не менее, ограничивающим фактором при разработке пептидных лекарственных средств является их относительная неэффективность при пероральном введении. Почти все пептидные лекарственные средства вводят парентерально, хотя при парентеральном введении пептидных лекарственных средств часто наблюдают несоблюдение пациентом режима терапии.
[003] Инсулин представляет собой лекарственное средство, которое применяют для лечения пациентов, страдающих диабетом, и представляет собой единственное лекарственное средство для лечения инсулинозависимого сахарного диабета. Сахарный диабет характеризуется патологическим состоянием с полной или относительной недостаточностью инсулина, которая приводит к гипергликемии, и представляет собой одну из основных угроз здоровью человека в 21-м веке. Количество людей, страдающих диабетом, в мире увеличилось до 220 миллионов в 2010 г. и вырастет до 300 миллионов к 2025 г. Диабет I типа связан, главным образом, с неспособностью поджелудочной железы вырабатывать инсулин. При диабете II типа отсутствует восприимчивость организма к действию инсулина.
[004] Приблизительно 20%-30% всех больных диабетом людей ежедневно применяют инъекции инсулина для поддержания уровней глюкозы. Согласно оценке, 10% всех больных диабетом полностью зависят от инъекций инсулина.
[005] На сегодняшний день, единственным путем введения инсулина является инъекция. Ежедневная инъекция инсулина причиняет пациентам значительные страдания. Известно проявление побочных действий, таких как липодистрофия в месте инъекции, липоатрофия, липогипертрофия и эпизодическая гипогликемия. Кроме того, подкожное введение инсулина обычно не обеспечивает точную непрерывную регуляцию метаболизма, которой в норме подвергается инсулин, секретированный поджелудочной железой и поступающий непосредственно в печень через воротную вену.
[006] Настоящее изобретение удовлетворяет потребность в альтернативном решении для введения инсулина и пептидов, таких как инсулин.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[007] В одном варианте реализации настоящее изобретение обеспечивает композицию, включающую белок, имеющий молекулярный вес до 100000 дальтон, ингибитор протеаз и усилитель всасывания, при этом указанный усилитель всасывания усиливает всасывание белка через барьер слизистой оболочки кишечника.
[008] В другом варианте реализации, настоящее изобретение обеспечивает композицию, содержащую белок, имеющий молекулярный вес до 100000 дальтон, ингибитор протеаз и SNAC или SNAD.
[009] В другом варианте реализации, настоящее изобретение обеспечивает способ перорального введения субъекту белка, имеющего молекулярный вес до 100000 дальтон, при этом существенная часть указанного белка сохраняет активность после всасывания через барьер слизистой оболочки кишечника субъекта, указанный способ включает пероральное введение субъекту фармацевтической композиции, включающей белок, ингибитор протеаз и усилитель всасывания, при этом усилитель всасывания усиливает всасывание белка через барьер слизистой оболочки кишечника.
[0010] В другом варианте реализации, настоящее изобретение обеспечивает способ лечения сахарного диабета у субъекта, включающий пероральное введение субъекту фармацевтической композиции, содержащей инсулин, эксенатид или их комбинацию, ингибитор протеаз и усилитель всасывания, при этом усилитель всасывания усиливает всасывание белка через барьер слизистой оболочки кишечника, тем самым осуществляя лечение сахарного диабета.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[001] На Фигуре 1 представлен график, показывающий изменения уровней глюкозы в крови после лечения лекарственными формами согласно настоящему изобретению.
[002] На Фигуре 2 представлен график, показывающий изменения уровней C-пептида в крови после лечения лекарственными формами согласно настоящему изобретению.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0013] Настоящее изобретение обеспечивает композиции, содержащие белок, ингибитор протеаз и усилитель всасывания и способы их применения. В другом варианте реализации, настоящее изобретение обеспечивает композиции, содержащие белок, имеющий молекулярный вес до 100000 дальтон, ингибитор протеаз и усилитель всасывания и способы их применения. В другом варианте реализации, указанный усилитель всасывания усиливает всасывание указанного белка через барьер слизистой оболочки кишечника. В другом варианте реализации, указанный усилитель всасывания усиливает всасывание белка, имеющего молекулярный вес до 100000 дальтон, через барьер слизистой оболочки кишечника.
[0014] В другом варианте реализации, композиции согласно настоящему изобретению содержат активный агент, ингибитор протеаз и носитель. В другом варианте реализации, композиции согласно настоящему изобретению применяют для доставки различных белков через различные биологические, химические и физические барьеры и, в частности, они подходят для доставки белков, которые подвержены деградации под действием окружающей среды. В другом варианте реализации, композиции согласно настоящему изобретению применяют для доставки активных белков через различные биологические, химические и физические барьеры и, в частности, они подходят для доставки активных белков, которые подвержены разложению под действием окружающей среды. В другом варианте реализации, композиции содержат активный белок, SNAC, ингибитор протеаз и EDTA или Na-EDTA. В другом варианте реализации, композиции содержат активный белок, SNAC, ингибитор протеаз и омега-3 жирную кислоту. В другом варианте реализации, композиции содержат активный белок, SNAC, ингибитор протеаз, EDTA или Na-EDTA и омега-3 жирную кислоту. В другом варианте реализации, композиция, описанная в настоящей заявке, представляет собой фармацевтическую композицию для перорального введения. В другом варианте реализации, композиция, описанная в настоящей заявке, представляет собой инкапсулированную пероральную фармацевтическую композицию. В другом варианте реализации, композиция, описанная в настоящей заявке, находится в форме жидкого лекарственного средства для перорального введения. В другом варианте реализации, композиция, описанная в настоящей заявке, находится в форме сухого лекарственного средства для перорального введения (таблетка и т.д.).
[0015] В другом варианте реализации, белок согласно настоящему изобретению имеет молекулярный вес 1000-5000 дальтон. В другом варианте реализации, белок согласно настоящему изобретению имеет молекулярный вес 5000-10000 дальтон. В другом варианте реализации, белок согласно настоящему изобретению имеет молекулярный вес 10000-20000 дальтон. В другом варианте реализации, белок согласно настоящему изобретению имеет молекулярный вес 20000-30000 дальтон. В другом варианте реализации, белок согласно настоящему изобретению имеет молекулярный вес 40000-50000 дальтон. В другом варианте реализации, белок согласно настоящему изобретению имеет молекулярный вес 50000-60000 дальтон. В другом варианте реализации, белок согласно настоящему изобретению имеет молекулярный вес 60000-70000 дальтон. В другом варианте реализации, белок согласно настоящему изобретению имеет молекулярный вес 70000-80000 дальтон. В другом варианте реализации, белок согласно настоящему изобретению имеет молекулярный вес 80000-90000 дальтон. В другом варианте реализации, белок согласно настоящему изобретению имеет молекулярный вес 90000-100000 дальтон. В другом варианте реализации, белок согласно настоящему изобретению имеет молекулярный вес 100000-150000 дальтон.
[0016] В другом варианте реализации, белок имеет молекулярный вес (MW) 1-50 килодальтон (кДа). В другом варианте реализации, молекулярный вес составляет 1-45 кДа. В другом варианте реализации, молекулярный вес составляет 1-40 кДа. В другом варианте реализации, молекулярный вес составляет 1-35 кДа. В другом варианте реализации, молекулярный вес составляет 1-30 кДа. В другом варианте реализации, молекулярный вес составляет 1-25 кДа. В другом варианте реализации, молекулярный вес составляет 1-20 кДа. В другом варианте реализации, молекулярный вес составляет 10-50 кДа. В другом варианте реализации, молекулярный вес составляет 15-50 кДа. В другом варианте реализации, молекулярный вес составляет 20-50 кДа. В другом варианте реализации, молекулярный вес составляет 25-50 кДа. В другом варианте реализации, молекулярный вес составляет 30-50 кДа. В другом варианте реализации, молекулярный вес составляет 35-50 кДа. В другом варианте реализации, молекулярный вес составляет 1-100 кДа. В другом варианте реализации, молекулярный вес составляет 1-90 кДа. В другом варианте реализации, молекулярный вес составляет 1-80 кДа. В другом варианте реализации, молекулярный вес составляет 1-70 кДа. В другом варианте реализации, молекулярный вес составляет 1-60 кДа. В другом варианте реализации, молекулярный вес составляет 10-100 кДа. В другом варианте реализации, молекулярный вес составляет 15-100 кДа. В другом варианте реализации, молекулярный вес составляет 20-100 кДа. В другом варианте реализации, молекулярный вес составляет 25-100 кДа. В другом варианте реализации, молекулярный вес составляет 30-100 кДа. В другом варианте реализации, молекулярный вес составляет 10-80 кДа. В другом варианте реализации, молекулярный вес составляет 15-80 кДа. В другом варианте реализации, молекулярный вес составляет 20-80 кДа. В другом варианте реализации, молекулярный вес составляет 25-80 кДа. В другом варианте реализации, молекулярный вес составляет 30-80 кДа. Каждый из перечисленных вариантов представляет собой отдельный вариант реализации настоящего изобретения.
[0017] В другом варианте реализации, молекулярный вес составляет менее чем 20 кДа. В другом варианте реализации, молекулярный вес составляет менее чем 25 кДа. В другом варианте реализации, молекулярный вес составляет менее чем 30 кДа. В другом варианте реализации, молекулярный вес составляет менее чем 35 кДа. В другом варианте реализации, молекулярный вес составляет менее чем 40 кДа. В другом варианте реализации, молекулярный вес составляет менее чем 45 кДа. В другом варианте реализации, молекулярный вес составляет менее чем 50 кДа. В другом варианте реализации, молекулярный вес составляет менее чем 55 кДа. В другом варианте реализации, молекулярный вес составляет менее чем 60 кДа. В другом варианте реализации, молекулярный вес составляет менее чем 65 кДа. В другом варианте реализации, молекулярный вес составляет менее чем 70 кДа. В другом варианте реализации, молекулярный вес составляет менее чем 75 кДа. В другом варианте реализации, молекулярный вес составляет менее чем 80 кДа. В другом варианте реализации, молекулярный вес составляет менее чем 85 кДа. В другом варианте реализации, молекулярный вес составляет менее чем 90 кДа. В другом варианте реализации, молекулярный вес составляет менее чем 95 кДа. В другом варианте реализации, молекулярный вес составляет менее чем 100 кДа.
[0018] В другом варианте реализации, белок согласно настоящему изобретению представляет собой инсулин. В другом варианте реализации, инсулин для применения в способах и композициях согласно настоящему изобретению представляет собой инсулин человека. В другом варианте реализации, инсулин представляет собой рекомбинантный инсулин. В другом варианте реализации, инсулин представляет собой рекомбинантный инсулин человека. В другом варианте реализации, инсулин представляет собой инсулин быка. В другом варианте реализации, инсулин представляет собой инсулин свиньи. В другом варианте реализации, инсулин представляет собой инсулин кита. В другом варианте реализации, инсулин представляет собой комплексное соединение металла с инсулином (например, комплексное соединение цинка с инсулином, протамин-цинк-инсулин или глобин-цинк-инсулин).
[0019] В другом варианте реализации, инсулин представляет собой эндогенный инсулин. В другом варианте реализации, инсулин представляет собой быстродействующий инсулин. В другом варианте реализации, инсулин представляет собой инсулин ленте. В другом варианте реализации, инсулин представляет собой инсулин семиленте. В другом варианте реализации, инсулин представляет собой инсулин ультраленте. В другом варианте реализации, инсулин представляет собой инсулин НПХ. В другом варианте реализации, инсулин представляет собой инсулин гларгин. В другом варианте реализации, инсулин представляет собой инсулин лизпро. В другом варианте реализации, инсулин представляет собой инсулин аспарт. В другом варианте реализации, инсулин представляет собой комбинацию двух или нескольких из любых перечисленных выше типов инсулина. В другом варианте реализации, инсулин представляет собой любой другой тип инсулина, известный в данной области техники. Каждый из перечисленных вариантов представляет собой отдельный вариант реализации настоящего изобретения.
[0020] В одном варианте реализации, количество инсулина, используемого в способах и композициях согласно настоящему изобретению, составляет 0.5-3 единиц (ед.)/кг массы тела человека. В одном варианте реализации, единицы, используемые для измерения инсулина в способах и композициях согласно настоящему изобретению, представляют собой USP-единицы инсулина. В одном варианте реализации, единицы, используемые для измерения инсулина, представляют собой миллиграммы. В другом варианте реализации, одна международная единица (IU) инсулина эквивалентна 45.5 мг инсулина.
[0021] В другом варианте реализации, указанное количество инсулина составляет 0.1-1 ед./кг. В другом варианте реализации, количество составляет 0.2-1 ед./кг. В другом варианте реализации, количество составляет 0.3-1 ед./кг. В другом варианте реализации, количество составляет 0.5-1 ед./кг. В другом варианте реализации, количество составляет 0.1-2 ед./кг. В другом варианте реализации, количество составляет 0.2-2 ед./кг. В другом варианте реализации, количество составляет 0.3-2 ед./кг. В другом варианте реализации, количество составляет 0.5-2 ед./кг. В другом варианте реализации, количество составляет 0.7-2 ед./кг. В другом варианте реализации, количество составляет 1-2 ед./кг. В другом варианте реализации, количество составляет 1.2-2 ед./кг. В другом варианте реализации, количество составляет 1-1.2 ед./кг. В другом варианте реализации, количество составляет 1-1.5 ед./кг. В другом варианте реализации, количество составляет 1-2.5 ед./кг. В другом варианте реализации, количество составляет 1-3 ед./кг. В другом варианте реализации, количество составляет 2-3 ед./кг. В другом варианте реализации, количество составляет 1 -5 ед./кг. В другом варианте реализации, количество составляет 2-5 ед./кг. В другом варианте реализации, количество составляет 3-5 ед./кг.
[0022] В другом варианте реализации, количество инсулина составляет 0.1 ед./кг. В другом варианте реализации, количество составляет 0.2 ед./кг. В другом варианте реализации, количество составляет 0.3 ед./кг. В другом варианте реализации, количество составляет 0.4 ед./кг. В другом варианте реализации, количество составляет 0.5 ед./кг. В другом варианте реализации, количество составляет 0.6 ед./кг. В другом варианте реализации, количество составляет 0.8 ед./кг. В другом варианте реализации, количество составляет 1 ед./кг. В другом варианте реализации, количество составляет 1.2 ед./кг. В другом варианте реализации, количество составляет 1.4 ед./кг. В другом варианте реализации, количество составляет 1.6 ед./кг. В другом варианте реализации, количество составляет 1.8 ед./кг. В другом варианте реализации, количество составляет 2 ед./кг. В другом варианте реализации, количество составляет 2.2 ед./кг. В другом варианте реализации, количество составляет 2.5 ед./кг. В другом варианте реализации, количество составляет 3 ед./кг.
[0023] В другом варианте реализации, количество инсулина составляет 1-10 ед. В другом варианте реализации, количество составляет 2-10 ед. В другом варианте реализации, количество составляет 3-10 ед. В другом варианте реализации, количество составляет 5-10 ед. В другом варианте реализации, количество составляет 1-20 ед. В другом варианте реализации, количество составляет 2-20 ед. В другом варианте реализации, количество составляет 3-20 ед. В другом варианте реализации, количество составляет 5-20 ед. В другом варианте реализации, количество составляет 7-20 ед. В другом варианте реализации, количество составляет 10-20 ед. В другом варианте реализации, количество составляет 12-20 ед. В другом варианте реализации, количество составляет 10-12 ед. В другом варианте реализации, количество составляет 10-15 ед. В другом варианте реализации, количество составляет 10-25 ед. В другом варианте реализации, количество составляет 10-30 ед. В другом варианте реализации, количество составляет 20-30 ед. В другом варианте реализации, количество составляет 10-50 ед. В другом варианте реализации, количество составляет 20-50 ед. В другом варианте реализации, количество составляет 30-50 ед. В другом варианте реализации, количество составляет 20-100 ед. В другом варианте реализации, количество составляет 30-100 ед. В другом варианте реализации, количество составляет 100-150 ед. В другом варианте реализации, количество составляет 100-250 ед. В другом варианте реализации, количество составляет 100-300 ед. В другом варианте реализации, количество составляет 200-300 ед. В другом варианте реализации, количество составляет 100-500 ед. В другом варианте реализации, количество составляет 200-500 ед. В другом варианте реализации, количество составляет 300-500 ед. В другом варианте реализации, количество составляет 200-1000 ед. В другом варианте реализации, количество составляет 300-1000 ед.
[0024] В другом варианте реализации, количество инсулина составляет 1 ед. В другом варианте реализации, количество составляет 2 ед. В другом варианте реализации, количество составляет 3 ед. В другом варианте реализации, количество составляет 4 ед. В другом варианте реализации, количество составляет 5 ед. В другом варианте реализации, количество составляет 6 ед. В другом варианте реализации, количество составляет 8 ед. В другом варианте реализации, количество составляет 10 ед. В другом варианте реализации, количество составляет 12 ед. В другом варианте реализации, количество составляет 14 ед. В другом варианте реализации, количество составляет 16 ед. В другом варианте реализации, количество составляет 18 ед. В другом варианте реализации, количество составляет 20 ед. В другом варианте реализации, количество составляет 22 ед. В другом варианте реализации, количество составляет 25 ед. В другом варианте реализации, количество составляет 30 ед. В другом варианте реализации, количество составляет 50 ед. В другом варианте реализации, количество составляет 80 ед. В другом варианте реализации, количество составляет 100 ед. В другом варианте реализации, количество составляет 120 ед. В другом варианте реализации, количество составляет 140 ед. В другом варианте реализации, количество составляет 160 ед. В другом варианте реализации, количество составляет 180 ед. В другом варианте реализации, количество составляет 200 ед. В другом варианте реализации, количество составляет 300 ед. В другом варианте реализации, количество составляет 500 ед.
[0025] В другом варианте реализации, указанный белок представляет собой стимулятор секреции инсулина. В другом варианте реализации, белок представляет собой GLP-1. В другом варианте реализации, белок представляет собой аналог GLP-1. В другом варианте реализации, белок представляет собой миметик GLP-1. В другом варианте реализации, белок представляет собой миметик инкретина. В другом варианте реализации, белок имитирует инкретин GLP-1. В другом варианте реализации, белок представляет собой GLP-2. В другом варианте реализации, белок представляет собой аналог GLP-2. В другом варианте реализации, белок представляет собой миметик GLP-2.
[0026] В другом варианте реализации, белок представляет собой эксенатид. В другом варианте реализации, лекарственные формы для перорального применения согласно настоящему изобретению защищают эксенатид от разрушения в желудке. В другом варианте реализации, лекарственная форма, содержащая эксенатид, согласно настоящему изобретению контролирует уровни сахара в крови. В другом варианте реализации, лекарственная форма, содержащая эксенатид, согласно настоящему изобретению помогает контролировать уровни сахара в крови. В другом варианте реализации, лекарственная форма, содержащая эксенатид, согласно настоящему изобретению вызывает продукцию инсулина поджелудочной железой. В другом варианте реализации, лекарственную форму, содержащую эксенатид, согласно настоящему изобретению применяют для лечения диабета 2 типа (инсулинонезависимого). В другом варианте реализации, лекарственную форму, содержащую эксенатид, согласно настоящему изобретению применяют в сочетании с другими лекарственными средствами для лечения диабета.
[0027] В другом варианте реализации, указанное количество эксенатида в лекарственной форме, согласно настоящему описанию, составляет от 10 мкг до 1 мг. В другом варианте реализации, количество эксенатида в лекарственной форме, согласно настоящему описанию, составляет от 10 мкг до 25 мкг. В другом варианте реализации, количество эксенатида в лекарственной форме, согласно настоящему описанию, составляет от 25 мкг до 50 мкг. В другом варианте реализации, количество эксенатида в лекарственной форме, согласно настоящему описанию, составляет от 50 мкг до 60 мкг. В другом варианте реализации, количество эксенатида в лекарственной форме, согласно настоящему описанию, составляет от 60 мкг до 70 мкг. В другом варианте реализации, количество эксенатида в лекарственной форме, согласно настоящему описанию, составляет от 70 мкг до 80 мкг. В другом варианте реализации, количество эксенатида в лекарственной форме, согласно настоящему описанию, составляет от 80 мкг до 90 мкг. В другом варианте реализации, количество эксенатида в лекарственной форме, согласно настоящему описанию, составляет от 90 мкг до 100 мкг. В другом варианте реализации, количество эксенатида в лекарственной форме, согласно настоящему описанию, составляет от 100 мкг до 110 мкг. В другом варианте реализации, количество эксенатида в лекарственной форме, согласно настоящему описанию, составляет от 110 мкг до 125 мкг. В другом варианте реализации, количество эксенатида в лекарственной форме, согласно настоящему описанию, составляет от 125 мкг до 150 мкг. В другом варианте реализации, количество эксенатида в лекарственной форме, согласно настоящему описанию, составляет от 150 мкг до 175 мкг. В другом варианте реализации, количество эксенатида в лекарственной форме, согласно настоящему описанию, составляет от 175 мкг до 200 мкг. В другом варианте реализации, количество эксенатида в лекарственной форме, согласно настоящему описанию, составляет от 200 мкг до 220 мкг. В другом варианте реализации, количество эксенатида в лекарственной форме, согласно настоящему описанию, составляет от 220 мкг до 240 мкг. В другом варианте реализации, количество эксенатида в лекарственной форме, согласно настоящему описанию, составляет от 240 мкг до 260 мкг. В другом варианте реализации, количество эксенатида в лекарственной форме, согласно настоящему описанию, составляет от 260 мкг до 300 мкг.
[0028] В другом варианте реализации, количество эксенатида в лекарственной форме, согласно настоящему описанию, составляет от 300 мкг до 350 мкг. В другом варианте реализации, количество эксенатида в лекарственной форме, согласно настоящему описанию, составляет от 350 мкг до 400 мкг. В другом варианте реализации, количество эксенатида в лекарственной форме, согласно настоящему описанию, составляет от 400 мкг до 450 мкг. В другом варианте реализации, количество эксенатида в лекарственной форме, согласно настоящему описанию, составляет от 450 мкг до 500 мкг. В другом варианте реализации, количество эксенатида в лекарственной форме, согласно настоящему описанию, составляет от 550 мкг до 600 мкг. В другом варианте реализации, количество эксенатида в лекарственной форме, согласно настоящему описанию, составляет от 600 мкг до 700 мкг. В другом варианте реализации, количество эксенатида в лекарственной форме, согласно настоящему описанию, составляет от 700 мкг до 800 мкг. В другом варианте реализации, количество эксенатида в лекарственной форме, согласно настоящему описанию, составляет от 800 мкг до 900 мкг. В другом варианте реализации, количество эксенатида в лекарственной форме, согласно настоящему описанию, составляет от 900 мкг до 1 мг.
[0029] В другом варианте реализации, лекарственную форму, содержащую эксенатид, согласно настоящему описанию, принимают один раз в день. В другом варианте реализации, лекарственную форму, содержащую эксенатид, согласно настоящему описанию, принимают дважды в день. В другом варианте реализации, лекарственную форму, содержащую эксенатид, согласно настоящему описанию, принимают три раза в день. В другом варианте реализации, лекарственную форму, содержащую эксенатид, согласно настоящему описанию, принимают четыре раза в день. В другом варианте реализации, лекарственную форму, содержащую эксенатид, согласно настоящему описанию, принимают пять раз в день. В другом варианте реализации, специалист в данной области техники определяет дозировку лекарственной формы, содержащей эксенатид, согласно настоящему описанию. В другом варианте реализации, специалист в данной области техники определяет ежедневную дозу лекарственной формы, содержащей эксенатид, согласно настоящему описанию. В другом варианте реализации, специалист в данной области техники определяет ежедневную схему приема лекарственной формы, содержащей эксенатид, согласно настоящему описанию.
[0030] В другом варианте реализации, состав, содержащий эксенатид, согласно настоящему описанию, принимают по меньшей мере за 15 минут до приема пищи. В другом варианте реализации, лекарственную форму, содержащую эксенатид, согласно настоящему описанию, принимают по меньшей мере за 30 минут до приема пищи. В другом варианте реализации, лекарственную форму, содержащую эксенатид, согласно настоящему описанию, принимают по меньшей мере за 45 минут до приема пищи. В другом варианте реализации, лекарственную форму, содержащую эксенатид, согласно настоящему описанию, принимают по меньшей мере за 60 минут до приема пищи. В другом варианте реализации, лекарственную форму, содержащую эксенатид, согласно настоящему описанию, принимают по меньшей мере за 75 минут до приема пищи. В другом варианте реализации, лекарственную форму, содержащую эксенатид, согласно настоящему описанию, принимают по меньшей мере за 90 минут до приема пищи. В другом варианте реализации, лекарственную форму, содержащую эксенатид, согласно настоящему описанию, принимают по меньшей мере за 100 минут до приема пищи. В другом варианте реализации, лекарственную форму, содержащую эксенатид, согласно настоящему описанию, принимают по меньшей мере за 120 минут до приема пищи. В другом варианте реализации, лекарственную форму, содержащую эксенатид, согласно настоящему описанию, принимают по меньшей мере за 150 минут до приема пищи. В другом варианте реализации, лекарственную форму, содержащую эксенатид, согласно настоящему описанию, принимают по меньшей мере за 180 минут до приема пищи.
[0031] В другом варианте реализации, лекарственная форма, содержащая эксенатид, согласно настоящему описанию, уменьшает побочные действия, связанные с инъецируемой лекарственной формой, содержащей эксенатид. В другом варианте реализации, лекарственная форма, содержащая эксенатид, согласно настоящему описанию, обеспечивает уменьшение такого побочного эффекта, как тошнота, который связан с инъецируемой лекарственной формой, содержащей эксенатид. В другом варианте реализации, лекарственная форма, состоящая эксенатид, согласно настоящему описанию, не вызывает такого побочного эффекта, как тошнота, который связан с инъецируемой лекарственной формой, содержащей эксенатид.
[0032] В другом варианте реализации, белок представляет собой глюкагон. В другом варианте реализации, белок представляет собой интерферон гамма. В другом варианте реализации, белок представляет собой интерферон альфа. В другом варианте реализации, белок представляет собой гормон роста. В другом варианте реализации, белок представляет собой эритропоэтин. В другом варианте реализации, белок представляет собой гранулоцитарный колониестимулирующий фактор (G-CSF). В другом варианте реализации, белок представляет собой оментин. В другом варианте реализации, белок представляет собой кальцитонин. В другом варианте реализации, белок представляет собой паратиреоидный гормон (ПТГ). В другом варианте реализации, белок представляет собой PYY.
[0033] В другом варианте реализации, белок представляет собой любой другой белок, известный в данной области техники. В другом варианте реализации, белок представляет собой гормон роста. В одном варианте реализации, гормон роста представляет собой соматотропин. В другом варианте реализации, гормон роста представляет собой инсулиноподобный фактор роста (IGF-I). В другом варианте реализации, гормон роста представляет собой любой другой гормон роста, известный в данной области техники.
[0034] В другом варианте реализации, способы и композиции согласно настоящему изобретению применяют для введения сывороточного альбумина человека. Сывороточный альбумин человека, в одном варианте реализации, не считают фармацевтически активным компонентом; тем не менее, его можно применять в контексте настоящего изобретения в качестве терапевтически подходящего носителя активного компонента. Каждый тип белка представляет собой отдельный вариант реализации настоящего изобретения.
[0035] В одном варианте реализации, белок представляет собой фермент. В некоторых вариантах реализации, белок представляет собой рецептор, лиганд, транспортер или запасной белок. В одном варианте реализации, белок представляет собой структурный белок.
[0036] В некоторых вариантах реализации, фермент представляет собой оксидоредуктазу, трансферазу, гидролазу, лиазу, изомеразу или лигазу. В некоторых вариантах реализации, оксидоредуктазы действуют на альдегидную или оксогруппу доноров, на CH-CH группу доноров, на CH-NH(2) группу доноров, на CH-NH группу доноров, NADH или NADPH, на CH-OH группу доноров, на азотные соединения в качестве доноров, на содержащую серу группу доноров, содержащую гем группу доноров, на дифенолы и сходные вещества в качестве доноров, на пероксид в качестве акцептора, на водород в качестве донора, на отдельные доноры с включением молекулярного кислорода, на парные доноры, на супероксид в качестве акцептора, окисляющие ионы металлов, на CH- или CH(2)-группы, на железо-серные белки в качестве доноров, на восстановленный флаводоксин в качестве донора, на фосфор или мышьяк в донорах или на x-H и y-H с образованием связи x-y.
[0037] В некоторых вариантах реализации, трансферазы представляют собой ацилтрансферазы или гликозилтрансферазы. В некоторых вариантах реализации, трансферазы переносят остатки альдегида или кетона. В некоторых вариантах реализации, трансферазы переносят алкильные или арильные группы, отличные от метальных групп. В некоторых вариантах реализации, трансферазы переносят группы, содержащие азот, фосфор, серу или селен.
[0038] В некоторых вариантах реализации, гидролазы представляют собой гликозилазы или действуют на простые эфирные связи, на пептидные связи, на углерод-азотные связи, отличные от пептидных связей, на ангидриды кислот, на углерод-углеродные связи, на галогенидные связи, на связи фосфор-азот, на связи сера-азот, на связи углерод-фосфор, на связи сера-сера или на связи углерод-сера.
[0039] В некоторых вариантах реализации, лиазы представляют собой углерод-углерод-лиазы, углерод-кислород-лиазы, углерод-азот-лиазы, углерод-сера-лиазы, углерод-галогенид-лиазы, фосфор-кислород-лиазы или другие лиазы.
[0040] В некоторых вариантах реализации, изомеразы представляют собой рацемазы или эпимеразы, цис-транс-изомеразы, внутримолекулярные оксидоредуктазы, внутримолекулярные трансферазы, внутримолекулярные лиазы или другие изомеразы.
[0041] В некоторых вариантах реализации, лигазы образуют связи углерод-сера, связи углерод-азот, связи углерод-углерод, фосфорноэфирные связи или связи азот-металл.
[0042] В некоторых вариантах реализации, белки-транспортеры представляют собой аннексины, АТФ-связывающие кассетные транспортеры, гемоглобин, АТФазы, кальциевые каналы, калиевые каналы, натриевые каналы или растворенные носители.
[0043] В некоторых вариантах реализации, запасные белки включают альбумины, лактоглобулины, казеин, овомуцин, ферритин, фосвитин, лактоферрин или вителлогенин. В одном варианте реализации, альбумины включают авидин, овальбумин, сывороточный альбумин, парвальбумин, C-реактивный белок, преальбумин, кональбумин, рицин, лактальбумин, метгемальбумин или транстиретин.
[0044] В некоторых вариантах реализации, структурные белки включают амилоид, коллаген, эластин или фибриллин.
[0045] В некоторых вариантах реализации, белок представляет собой вирусный белок, бактериальный белок, белок беспозвоночного или белок позвоночного. В некоторых вариантах реализации, белок представляет собой рекомбинантный белок. В одном варианте реализации, белок представляет собой рекомбинантный белок. В одном варианте реализации, рекомбинантный белок представляет собой рекомбинантный белок человека.
[0046] Молекулярные массы некоторых из упомянутых выше белков описаны далее: инсулин - 6 килодальтон (кДа); глюкагон - 3.5 кДа; интерферон - 28 кДа, гормон роста - 21.5-47 кДа; сывороточный альбумин человека - 69 кДа; эритропоэтин - 34 кДа; G-CSF - 30-34 кДа. Таким образом, в одном варианте реализации, молекулярные массы данных белков подходят для введения с помощью способов согласно настоящему изобретению.
[0047] Согласно настоящему описанию, ингибитор протеаз защищает белок согласно настоящему изобретению от расщепления. В другом варианте реализации, настоящим изобретением предусмотрено, что ингибитор протеаз защищает инсулин согласно настоящему изобретению от расщепления. В другом варианте реализации, настоящим изобретением предусмотрено, что ингибитор протеаз способствует всасыванию белка в кишечнике субъекта. В другом варианте реализации, настоящим изобретением предусмотрено, что ингибитор протеаз способствует всасыванию инсулина в кишечнике субъекта.
[0048] В другом варианте реализации, серпин представляет собой: альфа-1-антитрипсин, родственный антитрипсину белок, альфа-1-антихимотрипсин, каллистатин, ингибитор белка C, кортизолсвязывающий глобулин, тироксинсвязывающий глобулин, ангиотензиноген, центерин, родственный белку Z ингибитор протеаз, васпин, ингибитор эластазы моноцитов/нейтрофилов, ингибитор активатора плазминогена-2, антиген плоскоклеточной карциномы-1 (SCCA-1), антиген плоскоклеточной карциномы-2 (SCCA-2), маспин, PI-6, мегзин, PI-8, PI-9, бомапин, юкопин, хурпин/хэдпин, антитромбин, кофактор гепарина II, ингибитор активатора плазминогена 1, нексин глии/протеазу нексин I, фактор пигментного эпителия, альфа-2-антиплазмин, ингибитор комплемента 1, 47 кДа белок теплового шока (HSP47), нейросерпин или панцпин.
[0049] В другом варианте реализации, настоящим изобретением предусмотрено, что ингибитор протеаз представляет собой ингибитор трипсина, такой как, но не ограниченный перечисленными: ингибитор трипсина из лимской фасоли, апротинин, ингибитор трипсина из соевых бобов (SBTI) или овомукоид.
[0050] В другом варианте реализации, настоящим изобретением предусмотрено, что ингибитор протеаз представляет собой ингибитор цистеиновых протеаз. В другом варианте реализации, настоящм изобретением предусмотрено, что ингибиторы цистеиновых протеаз согласно настоящему изобретению включают: цистатин, цистатины 1 типа (или стефины), цистатины 2 типа, цистатины C, D, S, SN и SA человека, цистатин E/M, цистатин F, цистатины 3 типа или кининогены.
[0051] В другом варианте реализации, настоящим изобретением предусмотрено, что ингибитор протеаз представляет собой ингибитор треониновых протеаз. В другом варианте реализации, настоящим изобретением предусмотрено, что ингибиторы треониновых протеаз согласно настоящему изобретению включают: Бортезомиб, MLN-519, ER-807446, TMC-95A.
[0052] В другом варианте реализации, настоящим изобретением предусмотрено, что ингибитор протеаз представляет собой ингибитор аспарагиновых протеаз. В другом варианте реализации, настоящим изобретением предусмотрено, что ингибиторы аспарагиновых протеаз согласно настоящему изобретению включают: α2-макроглобулин, пепстатин A, ингибитор аспарагиновых протеаз 11, ингибитор аспарагиновых протеаз 1, ингибитор аспарагиновых протеаз 2, ингибитор аспарагиновых протеаз 3, ингибитор аспарагиновых протеаз 4, ингибитор аспарагиновых протеаз 5, ингибитор аспарагиновых протеаз 6, ингибитор аспарагиновых протеаз 7, ингибитор аспарагиновых протеаз 8, ингибитор аспарагиновых протеаз 9, ингибитор пепсина Dit33, ингибитор аспартильных протеаз или ингибитор 3 протеазы A.
[0053] В другом варианте реализации, настоящим изобретением предусмотрено, что ингибитор протеаз представляет собой ингибитор металлопротеиназ. В другом варианте реализации, настоящим изобретении предусмотрено, что ингибиторы металлопротеиназ согласно настоящему изобретению включают: ингибиторный пептид ангиотензин-1-превращающего фермента, противогеморрагический фактор BJ46a, бета-казеин, ингибитор протеиназы CeKI, ингибитор металлопротеиназы змеиного яда DM43, ингибитор карбоксипептидазы A, smpI, IMPI, ингибитор щелочной протеиназы, латексин, ингибитор карбоксипептидазы, противогеморрагический фактор HSF, тестикан-3, SPOCK3, ингибитор металлопротеиназы 1 TIMP1, ингибитор металлопротеиназы 2 TIMP2, ингибитор металлопротеиназы 3 TIMP3, ингибитор металлопротеиназы 4 TIMP4, предполагаемый ингибитор металлопротеиназы tag-225, тканевый ингибитор металлопротеиназ, кислый белок сыворотки молока (WAP), казаль (kazal), иммуноглобулин или куниц (kunitz) и содержащий домен NTR белок 1.
[0054] В некоторых вариантах реализации, ингибитор протеаз представляет собой суицидный ингибитор, ингибитор переходного состояния или хелатирующий агент. В некоторых вариантах реализации, ингибитор протеаз согласно настоящему изобретению представляет собой: AEBSF-HCl, (эпсилон)-аминокапроновую кислоту, (альфа)-1-антихимотрипсин, противоболевое средство, антитромбин III, (альфа)-1-антитрипсин (ингибитор [альфа]-1-протеиназы), APMSF-HCl (4-амидинофенилметансульфонилфторид), апротинин, бензамидин-HCl, химостатин, DFP (диизопропилфторфосфат), леупептин, PEFABLOC® SC (4-(2-аминоэтил)бензолсульфонилфторида гидрохлорид), PMSF (фенилметилсульфонилфторид), TLCK (1-хлор-3-тозиламидо-7-амино-2-гептанон HCl), TPCK (1-хлор-3-тозиламидо-4-фенил-2-бутанон), пентамидинизетионат, пепстатин, гуанидий, альфа-2-макроглобулин, цинк-хелатирующий агент или йодацетат, цинк. Каждый из перечисленных вариантов представляет собой отдельный вариант реализации настоящего изобретения.
[0055] В другом варианте реализации, количество ингибитора протеаз, используемого в способах и композициях согласно настоящему изобретению, составляет 0.1 мг/единичную дозу. В другом варианте реализации, количество ингибитора протеаз составляет 0.2 мг/единичную дозу. В другом варианте реализации, количество составляет 0.3 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 0.4 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 0.6 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 0.8 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 1 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 1.5 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 2 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 2.5 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 3 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 5 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 7 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 10 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 12 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 15 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 20 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 30 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 50 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 70 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 100 мг/единичную дозу.
[0056] В другом варианте реализации, количество ингибитора протеаз составляет 0.1-1 мг/единичную дозу. В другом варианте реализации, указанное количество ингибитора протеаз составляет 0.2-1 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 0.3-1 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 0.5-1 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 0.1-2 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 0.2-2 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 0.3-2 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 0.5-2 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 1-2 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 1-10 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 2-10 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 3-10 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 5-10 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 1-20 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 2-20 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 3-20 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 5-20 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 10-20 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 10-100 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 20-100 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 30-100 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 50-100 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 10-200 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 20-200 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 30-200 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 50-200 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 100-200 мг/единичную дозу.
[0057] В другом варианте реализации, количество ингибитора протеаз, используемого в способах и композициях согласно настоящему изобретению, составляет 1000 ЕИК (единиц инактиватора калликреина)/единичную дозу. В другом варианте реализации, указанное количество составляет 10 ЕИК/единичную дозу. В другом варианте реализации, указанное количество составляет 12 ЕИК/единичную дозу. В другом варианте реализации, указанное количество составляет 15 ЕИК/единичную дозу. В другом варианте реализации, указанное количество составляет 20 ЕИК/единичную дозу. В другом варианте реализации, указанное количество составляет 30 ЕИК/единичную дозу. В другом варианте реализации, указанное количество составляет 40 ЕИК/единичную дозу. В другом варианте реализации, указанное количество составляет 50 ЕИК/единичную дозу. В другом варианте реализации, указанное количество составляет 70 ЕИК/единичную дозу. В другом варианте реализации, указанное количество составляет 100 ЕИК/единичную дозу. В другом варианте реализации, указанное количество составляет 150 ЕИК/единичную дозу. В другом варианте реализации, указанное количество составляет 200 ЕИК/единичную дозу. В другом варианте реализации, указанное количество составляет 300 ЕИК/единичную дозу. В другом варианте реализации, указанное количество составляет 500 ЕИК/единичную дозу. В другом варианте реализации, указанное количество составляет 700 ЕИК/единичную дозу. В другом варианте реализации, указанное количество составляет 1500 ЕИК/единичную дозу. В другом варианте реализации, указанное количество составляет 3000 ЕИК/единичную дозу. В другом варианте реализации, указанное количество составляет 4000 ЕИК/единичную дозу. В другом варианте реализации, указанное количество составляет 5000 ЕИК/единичную дозу. Каждое количество первого или второго ингибитора протеаз представляет собой отдельный вариант реализации настоящего изобретения.
[0058] В другом варианте реализации, композиции согласно настоящему изобретению содержат вещество, которое усиливает всасывание белка согласно настоящему изобретению через барьер слизистой оболочки кишечника. В другом варианте реализации, композиции согласно настоящему изобретению дополнительно содержат вещество, которое усиливает всасывание инсулина через барьер слизистой оболочки кишечника. В другом варианте реализации, композиции согласно настоящему изобретению дополнительно содержат вещество, которое усиливает всасывание эксенатида через барьер слизистой оболочки кишечника. В другом варианте реализации, композиции согласно настоящему изобретению дополнительно содержат вещество, которое уменьшает деградацию эксенатида в пищеварительной системе. В другом варианте реализации, композиции согласно настоящему изобретению дополнительно содержат вещество, которое уменьшает деградацию эксенатида в желудке. В другом варианте реализации, композиции согласно настоящему изобретению дополнительно содержат вещество, которое уменьшает деградацию эксенатида в кишечнике. Такое вещество в настоящей заявке обозначается термином "усилитель". Согласно настоящему описанию, усилители, применяемые совместно с омега-3 жирными кислотами или ингибитором протеаз, повышают способность белка всасываться в кишечнике. Согласно настоящему описанию, усилители, применяемые совместно с омега-3 жирными кислотами или ингибитором протеаз, повышают способность инсулина всасываться в кишечнике. Согласно настоящему описанию, усилители, применяемые совместно с омега-3 жирными кислотами или ингибитором протеаз, повышают способность эксенатида всасываться в кишечнике.
[0059] В одном варианте реализации, указанный усилитель представляет собой дидеканоилфосфатидилхолин (DDPC). В одном варианте реализации, усилитель представляет собой хелатирующий агент, такой как этилендиаминтетрауксусная кислота (ЭДТА) или этиленгликольтетрауксусная кислота (ЭГТА). В другом варианте реализации, ЭДТА представляет собой ЭДТА натрия. В некоторых вариантах реализации, усилитель представляет собой донор N0. В некоторых вариантах реализации, усилитель представляет собой желчную кислоту, конъюгированную с глицином форму желчной кислоты или соль щелочного металла. В одном варианте реализации, усиление всасывания достигается путем применения комбинации α-галактозидазы и β-маннаназы. В некоторых вариантах реализации, указанный усилитель представляет собой жирную кислоту, такую как капрат натрия. В одном варианте реализации, усилитель представляет собой гликохолат натрия. В одном варианте реализации, усилитель представляет собой салицилат натрия. В одном варианте реализации, усилитель представляет собой н-додецил-β-D-мальтопиранозид. В некоторых вариантах реализации, поверхностно-активные вещества служат усилителями всасывания. В одном варианте реализации, указанный усилитель представляет собой хитозан, такой как N,N,N-триметилхитозана хлорид (ТМС).
[0060] В одном варианте реализации, доноры NO согласно настоящему изобретению включают 3-(2-гидрокси-1-(1-метилэтил)-2-нитрозогидразино)-1-пропанамин, N-этил-2-(1-этилгидрокси-2-нитрозогидразино)-этанамин или S-нитрозо-N-ацетилпеницилламин.
[0061] В другом варианте реализации, желчная кислота представляет собой холевую кислоту. В другом варианте реализации, желчная кислота представляет собой хенодезоксихолевую кислоту. В другом варианте реализации, желчная кислота представляет собой таурохолевую кислоту. В другом варианте реализации, желчная кислота представляет собой таурохенодезоксихолевую кислоту. В другом варианте реализации, желчная кислота представляет собой гликохолевую кислоту. В другом варианте реализации, желчная кислота представляет собой гликохенохолевую кислоту. В другом варианте реализации, желчная кислота представляет собой 3-бета-моногидроксихолевую кислоту. В другом варианте реализации, желчная кислота представляет собой литохолевую кислоту. В другом варианте реализации, желчная кислота представляет собой 5-бета-холановую кислоту. В другом варианте реализации, желчная кислота представляет собой 3,12-диол-7-он-5-бета-холановую кислоту. В другом варианте реализации, желчная кислота представляет собой 3-альфа-гидрокси-12-кетохолевую кислоту. В другом варианте реализации, желчная кислота представляет собой 3-бета-гидрокси-12-кетохолевую кислоту. В другом варианте реализации, желчная кислота представляет собой 12-альфа-3-бета-дигидрохолевую кислоту. В другом варианте реализации, желчная кислота представляет собой урсодезоксихолевую кислоту.
[0062] В одном варианте реализации, указанный усилитель представляет собой неионное поверхностно-активное вещество. В одном варианте реализации, усилитель представляет собой неионный поверхностно-активный агент эфир полиоксиэтилена (например, имеющий значение гидрофильно-липофильного баланса (HLB) от 6 до 19, при этом среднее количество единиц полиоксиэтилена составляет от 4 до 30). В другом варианте реализации, усилитель представляет собой анионный поверхностно-активный агент. В другом варианте реализации, усилитель представляет собой катионный поверхностно-активный агент. В другом варианте реализации, усилитель представляет собой амфолитический поверхностно-активный агент. В одном варианте реализации, цвиттер-ионные поверхностно-активные вещества, такие как ацилкарнитины, служат усилителями всасывания.
[0063] В другом варианте реализации, указанный усилитель всасывания представляет собой эффективный пероральный усилитель всасывания для макромолекулярных лекарственных средств. В другом варианте реализации, усилитель всасывания хорошо растворим в воде. В другом варианте реализации, усилитель всасывания полностью, т.е. более чем на 85%, всасывается в желудочно-кишечном тракте. В другом варианте реализации, усилитель всасывания находится в виде крупной фракции. В другом варианте реализации, усилитель всасывания микронизирован. В другом варианте реализации, усилитель всасывания аморфный. В другом варианте реализации, усилитель всасывания представляет собой N-(5-хлорсалицилоил)-8-аминокаприловую кислоту (5-CNAC). В другом варианте реализации, усилитель всасывания представляет собой N-(10-[2-гидроксибензоил]амино)декановую кислоту (SNAD). В другом варианте реализации, усилитель всасывания представляет собой N-(8-[2-гидроксибензоил]амино)каприловую кислоту (SNAC). В другом варианте реализации, усилитель всасывания представляет собой CNAC, SNAD, SNAC, мононатриевые и/или динатриевые соли перечисленных кислот, этанольные сольваты натриевых солей перечисленных кислот и моногидраты натриевых солей перечисленных кислот, и любые их комбинации. В другом варианте реализации, усилитель всасывания представляет собой 8-(N-2-гидрокси-4-метоксибензоил)-аминокаприловую кислоту (4-MOAC) и фармацевтически приемлемые соли указанной кислоты и/или аморфные и полиморфные формы 4-MOAC. В другом варианте реализации, усилитель всасывания представляет собой N-(8-[2-гидрокси-5-хлорбензоил]-амино)октановую кислоту (также известную как 8-(N-2-гидрокси-5-хлорбензоил)аминокаприловая кислота)) (5-CNAC) и фармацевтически приемлемые соли указанной кислоты, и/или аморфные и полиморфные формы 5-CNAC. В другом варианте реализации, усилитель всасывания представляет собой 4-[(2-гидрокси-4-хлорбензоил)амино]бутаноат (также известный как 4-[(4-хлор-2-гидрокси-бензоил)амино]бутановая кислота) (4-CNAB) и фармацевтически приемлемые соли указанной кислоты, включая мононатриевую соль и/или аморфные и полиморфные формы 4-CNAB.
[0064] В другом варианте реализации, SNAD и ингибитор протеаз согласно настоящему изобретению осуществляют синергичное действие для снижения уровня глюкозы в крови. В другом варианте реализации, SNAC и ингибитор протеаз согласно настоящему изобретению осуществляют синергичное действие для снижения уровня глюкозы в крови.
[0065] В другом варианте реализации, фармацевтические композиции согласно настоящему изобретению содержат эффективное для доставки количество одного или нескольких из усилителей всасывания. В другом варианте реализации, фармацевтические композиции согласно настоящему изобретению содержат количество, достаточное для доставки активного агента, чтобы достигнуть желаемого эффекта.
[0066] В другом варианте реализации, фармацевтические композиции согласно настоящему изобретению содержат количество усилителя всасывания, составляющее от 2.5% до 99.4% по весу. В другом варианте реализации, фармацевтические композиции согласно настоящему изобретению содержат количество усилителя всасывания, составляющее от 2.5% до 10% по весу. В другом варианте реализации, фармацевтические композиции согласно настоящему изобретению содержат количество усилителя всасывания, составляющее от 8% до 15% по весу. В другом варианте реализации, фармацевтические композиции согласно настоящему изобретению содержат количество усилителя всасывания, составляющее от 10% до 20% по весу. В другом варианте реализации, фармацевтические композиции согласно настоящему изобретению содержат количество усилителя всасывания, составляющее от 15% до 30% по весу. В другом варианте реализации, фармацевтические композиции согласно настоящему изобретению содержат количество усилителя всасывания, составляющее от 20% до 40% по весу. В другом варианте реализации, фармацевтические композиции согласно настоящему изобретению содержат количество усилителя всасывания, составляющее от 30% до 50% по весу. В другом варианте реализации, фармацевтические композиции согласно настоящему изобретению содержат количество усилителя всасывания, составляющее от 40% до 60% по весу. В другом варианте реализации, фармацевтические композиции согласно настоящему изобретению содержат количество усилителя всасывания, составляющее от 50% до 70% по весу. В другом варианте реализации, фармацевтические композиции согласно настоящему изобретению содержат количество усилителя всасывания, составляющее от 70% до 99.4% по весу. В другом варианте реализации, количество усилителя всасывания в настоящей композиции представляет собой эффективное для доставки количество, и такое количество можно определить для любого конкретного носителя или биологически, или химически активного агента способами, известными специалистам в данной области техники.
[0067] В другом варианте реализации, усилитель всасывания представляет собой пептид. В другом варианте реализации, усилитель всасывания представляет собой аминокислоту. В другом варианте реализации, усилитель всасывания получают из аминокислот.
[0068] В другом варианте реализации, количество энхансера, используемого в способах и композициях согласно настоящему изобретению, составляет 0.1 мг/единичную дозу. В другом варианте реализации, указанное количество усилителя составляет 0.2 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 0.3 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 0.4 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 0.6 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 0.8 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 1 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 1.5 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 2 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 2.5 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 3 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 5 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 7 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 10 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 12 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 15 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 20 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 30 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 50 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 70 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 100 мг/единичную дозу.
[0069] В другом варианте реализации, указанное количество усилителя составляет 0.1-1 мг/единичную дозу. В другом варианте реализации, указанное количество усилителя составляет 0.2-1 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 0.3-1 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 0.5-1 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 0.1-2 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 0.2-2 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 0.3-2 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 0.5-2 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 1-2 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 1-10 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 2-10 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 3-10 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 5-10 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 1-20 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 2-20 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 3-20 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 5-20 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 10-20 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 10-100 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 20-100 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 30-100 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 50-100 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 10-200 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 20-200 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 30-200 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 50-200 мг/единичную дозу. В другом варианте реализации, указанное количество составляет 100-200 мг/единичную дозу. Каждый тип и количество усилителя представляет собой отдельный вариант реализации настоящего изобретения.
[0070] В некоторых вариантах реализации, омега-3 жирную кислоту можно найти в растительных источниках, таких как семена чии, периллы, льна, грецкий орех, портулак, брусника, облепиха и конопля. В некоторых вариантах реализации, омега-3 жирные кислоты также можно найти в плоде пальмы асаи. В другом варианте реализации, омега-3 жирная кислота обеспечивается в виде синтетической омега-3 жирной кислоты. В одном варианте реализации, омега-3 жирная кислота для способов и композиций согласно настоящему изобретению обеспечивается в композиции в виде рыбьего жира. В другом варианте реализации, омега-3 жирная кислота обеспечивается в виде масла канолы. В другом варианте реализации, омега-3 жирная кислота обеспечиваюется в виде льняного масла. В другом варианте реализации, омега-3 жирная кислота обеспечивается в виде любого другого богатого омега-3 жирной кислотой источника, известного в данной области техники. В другом варианте реализации, омега-3 жирная кислота обеспечивается в виде синтетической омега-3 жирной кислоты. Каждая форма омега-3 жирных кислот представляет собой отдельный вариант реализации настоящего изобретения.
[0071] В другом варианте реализации, омега-3 жирная кислота, применяемая для способов и композиций согласно настоящему изобретению, представляет собой омега-3 полиненасыщенную жирную кислоту. В другом варианте реализации, омега-3 жирная кислота представляет собой DHA - омега-3 полиненасыщенную, 22-углеродную жирную кислоту, также называемую 4, 7, 10, 13, 16, 19-докозагексаеновая кислота. В другом варианте реализации, омега-3 жирная кислота представляет собой альфа-линоленовую кислоту (9,12,15-октадекатриеновую кислоту). В другом варианте реализации, омега-3 жирная кислота представляет собой стеаридоновую кислоту (6,9,12,15-октадекатетраеновую кислоту). В другом варианте реализации, омега-3 жирная кислота представляет собой эйкозатриеновую кислоту (ETA; 11,14,17-эйкозатриеновую кислоту). В другом варианте реализации, омега-3 жирная кислота представляет собой эйкозатетраеновую кислоту (8,11,14,17-эйкозатетраеновую кислоту). В одном варианте реализации, омега-3 жирная кислота представляет собой эйкозапентаеновую кислоту (ЕРА; 5,8,11,14,17-эйкозапентаеновую кислоту). В другом варианте реализации, омега-3 жирная кислота представляет собой эйкозагексаеновую кислоту (также называемую "ЕРА"; 5,7,9,11,14,17-эйкозагексаеновую кислоту). В другом варианте реализации, омега-3 жирная кислота представляет собой докозапентаеновую кислоту (DPA; 7,10,13,16,19-докозапентаеновую кислоту). В другом варианте реализации, омега-3 жирная кислота представляет собой тетракозагексаеновую кислоту (6,9,12,15,18,21-тетракозагексаеновую кислоту). В другом варианте реализации, омега-3 жирная кислота представляет собой любую другую омега-3 жирную кислоту, известную в данной области техники. Каждая омега-3 жирная кислота представляет собой отдельный вариант реализации настоящего изобретения.
[0072] В другом варианте реализации, композиции согласно настоящему изобретению дополнительно содержат покрытие, которое ингибирует расщепление указанной композиции в желудке субъекта. В одном варианте реализации, покрытие ингибирует расщепление композиции в желудке субъекта. В одном варианте реализации, содержащие покрытие дозированные формы согласно настоящему изобретению высвобождают лекарственное средство, когда pH сдвигается в щелочной диапазон. В одном варианте реализации, покрытие представляет собой монослой, при этом в других вариантах реализации покрытие наносится множеством слоев. В одном варианте реализации, покрытие представляет собой биоадгезивный полимер, который избирательно связывается со слизистой оболочкой кишечника и, таким образом, позволяет высвобождение лекарственного средства в месте присоединения. В одном варианте реализации, энтеросолюбильное покрытие представляет собой покрытие кишечнорастворимой пленкой. В некотором варианте реализации, покрытие включает биоразлагаемый полисахарид, хитозан, акватерик водный, аквакоат ECD, азо-полимер, ацетат фталат целлюлозы, ацетат тримеллитат целлюлозы, фталат гидроксипропилметилцеллюлозы, желатин, поливинилацетат фталат, гидрогель, пулсинкап или комбинацию перечисленных покрытий. В одном варианте реализации, pH-чувствительное покрытие будут использовать в соответствии с желательным местом высвобождения и/или профилем, что известно специалисту в данной области техники.
[0073] В одном варианте реализации, указанное покрытие представляет собой энтеросолюбильное покрытие. Способы нанесения энтеросолюбильного покрытия хорошо известны в данной области техники и описаны, например, у Siepmann F, Siepmann J и др., Blends of aqueous polymer dispersions used for pellet coating: importance of the particle size. J Control Release 2005; 105 (3): 226-39; и Huyghebaert N, Vermeire A, Remon JP. In vitro evaluation of coating polymers for enteric coating and human ileal targeting. Int J Pharm 2005; 298 (1): 26-37. Каждый способ представляет собой отдельный вариант реализации настоящего изобретения.
[0074] В другом варианте реализации, в качестве энтеросолюбильного покрытия применяют эудрагит®, акриловый полимер. Применение акриловых полимеров для нанесения покрытия на фармацевтические препараты хорошо известно в данной области техники. Было показано, что акриловые полимеры эудрагит безопасны, и они не всасываются и не метаболизируются организмом, но удаляются из организма.
[0075] В другом варианте реализации, покрытие представляет собой желатиновое покрытие. В другом варианте реализации, микрокапсулирование применяют для защиты инсулина от расщепления в желудке. В другом варианте реализации, покрытие представляет собой желатиновое покрытие. В другом варианте реализации, микрокапсулирование применяют для защиты эксенатида от расщепления в желудке. Способы нанесения желатинового покрытия и микрокапсулирования хорошо известны в данной области техники. Каждый способ представляет собой отдельный вариант реализации настоящего изобретения.
[0076] В другом варианте реализации, покрытие представляет собой пленочное покрытие. В другом варианте реализации, покрытие представляет собой этилцеллюлозу. В другом варианте реализации, покрытие представляет собой дисперсию этилцеллюлозы на водной основе, например, гидроксипропилметилцеллюлозу (HPMC) E15. В другом варианте реализации, покрытие представляет собой устойчивые к желудочной кислоте покрытия, например, полимер, содержащий группы карбоновой кислоты в качестве функциональной группы. В другом варианте реализации, покрытие представляет собой монолитную матрицу. В другом варианте реализации, покрытие представляет собой простой эфир целлюлозы (например, гипромеллозу (HPMC)). Каждый тип покрытия представляет собой отдельный вариант реализации настоящего изобретения.
[0077] В другом варианте реализации, настоящее изобретение обеспечивает композицию, содержащую активный белок согласно настоящему изобретению, ингибитор протеаз и усилитель всасывания. В другом варианте реализации, настоящее изобретение обеспечивает композицию, содержащую активный белок согласно настоящему изобретению, ингибитор протеаз, омега-3 жирную кислоту и усилитель всасывания. В другом варианте реализации, настоящее изобретение обеспечивает композицию, содержащую активный белок согласно настоящему изобретению, ингибитор протеаз, омега-3 жирную кислоту, ЭДТА или Na-ЭДТА и усилитель всасывания.
[0078] В другом варианте реализации, настоящее изобретение обеспечивает, что применение по меньшей мере одного ингибитора протеаз и усилителя всасывания в одной композиции для перорального введения неожиданно существенно повышает биодоступность белка согласно настоящему изобретению. В другом варианте реализации, настоящее изобретение обеспечивает, что применение по меньшей мере одного ингибитора протеаз и усилителя всасывания в одной композиции для перорального введения неожиданно существенно повышает биодоступность инсулина. В другом варианте реализации, настоящее изобретение обеспечивает, что применение по меньшей мере одного ингибитора протеаз и усилителя всасывания в одной композиции для перорального введения неожиданно существенно повышает биодоступность эксенатида.
[0079] В другом варианте реализации, настоящее изобретение обеспечивает, что применение по меньшей мере одного ингибитора протеаз и усилителя всасывания в одной композиции для перорального введения неожиданно существенно повышает биодоступность белка согласно настоящему изобретению. В другом варианте реализации, настоящее изобретение обеспечивает, что применение по меньшей мере одного ингибитора протеаз и усилителя всасывания в одной композиции для перорального введения неожиданно существенно повышает биодоступность инсулина. В другом варианте реализации, настоящее изобретение обеспечивает, что применение по меньшей мере одного ингибитора протеаз и усилителя всасывания в одной композиции для перорального введения неожиданно существенно повышает биодоступность эксенатида.
[0080] В другом варианте реализации, настоящее изобретение обеспечивает, что применение по меньшей мере одного ингибитора протеаз и SNAC в одной композиции для перорального введения неожиданно существенно повышает биодоступность белка согласно настоящему изобретению. В другом варианте реализации, настоящее изобретение обеспечивает, что применение по меньшей мере одного ингибитора протеаз и SNAC в одной композиции для перорального введения неожиданно существенно повышает биодоступность инсулина. В другом варианте реализации, настоящее изобретение обеспечивает, что применение по меньшей мере одного ингибитора протеаз и SNAC в одной композиции для перорального введения неожиданно существенно повышает биодоступность эксенатида.
[0081] В другом варианте реализации, настоящее изобретение обеспечивает, что применение по меньшей мере одного ингибитора протеаз и SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность белка согласно настоящему изобретению. В другом варианте реализации, настоящее изобретение обеспечивает, что применение по меньшей мере одного ингибитора протеаз и SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность инсулина. В другом варианте реализации, настоящее изобретение обеспечивает, что применение по меньшей мере одного ингибитора протеаз и SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность эксенатида.
[0082] В другом варианте реализации, настоящее изобретение обеспечивает, что применение серпина и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность белка согласно настоящему изобретению. В другом варианте реализации, настоящее изобретение обеспечивает, что применение серпина и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность инсулина. В другом варианте реализации, настоящее изобретение обеспечивает, что применение серпина и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность эксенатида. В другом варианте реализации, настоящее изобретение обеспечивает, что применение серпина и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность белка согласно настоящему изобретению.
[0083] В другом варианте реализации, настоящее изобретение обеспечивает, что применение ингибитора трипсина и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность инсулина. В другом варианте реализации, настоящее изобретение обеспечивает, что применение ингибитора трипсина и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность эксенатида. В другом варианте реализации, настоящее изобретение обеспечивает, что применение SBTI или апротинина и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность белка согласно настоящему изобретению. В другом варианте реализации, настоящее изобретение обеспечивает, что применение SBTI или апротинина и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность инсулина. В другом варианте реализации, настоящее изобретение обеспечивает, что применение SBTI или апротинина и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность эксенатида.
[0084] В другом варианте реализации, настоящее изобретение обеспечивает, что применение ингибитора цистеиновых протеаз и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность белка согласно настоящему изобретению. В другом варианте реализации, настоящее изобретение обеспечивает, что применение ингибитора цистеиновых протеаз и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность инсулина. В другом варианте реализации, настоящее изобретение обеспечивает, что применение ингибитора цистеиновых протеаз и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность эксенатида.
[0085] В другом варианте реализации, настоящее изобретение обеспечивает, что применение ингибитора треониновых протеаз и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность белка согласно настоящему изобретению. В другом варианте реализации, настоящее изобретение обеспечивает, что применение ингибитора треониновых протеаз и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность инсулина. В другом варианте реализации, настоящее изобретение обеспечивает, что применение ингибитора треониновых протеаз и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность эксенатида.
[0086] В другом варианте реализации, настоящее изобретение обеспечивает, что применение ингибитора металлопротеиназ и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность белка согласно настоящему изобретению. В другом варианте реализации, настоящее изобретение обеспечивает, что применение ингибитора металлопротеиназ и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность инсулина. В другом варианте реализации, настоящее изобретение обеспечивает, что применение ингибитора металлопротеиназ и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность эксенатида.
[0087] В другом варианте реализации, настоящее изобретение обеспечивает, что применение ингибитора аспарагиновых протеаз и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность белка согласно настоящему изобретению. В другом варианте реализации, настоящее изобретение обеспечивает, что применение ингибитора аспарагиновых протеаз и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность инсулина. В другом варианте реализации, настоящее изобретение обеспечивает, что применение ингибитора аспарагиновых протеаз и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность эксенатида.
[0088] В другом варианте реализации, настоящее изобретение обеспечивает, что применение ингибитора протеаз и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность инсулина у человека на по меньшей мере 10%. В другом варианте реализации, настоящее изобретение обеспечивает, что применение ингибитора протеаз и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность эксенатида у человека на по меньшей мере 10%. В другом варианте реализации, настоящее изобретение обеспечивает, что применение ингибитора протеаз и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность инсулина у человека на по меньшей мере 20%. В другом варианте реализации, настоящее изобретение обеспечивает, что применение ингибитора протеаз и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность эксенатида у человека на по меньшей мере 20%. В другом варианте реализации, настоящее изобретение обеспечивает, что применение ингибитора протеаз и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность инсулина у человека на по меньшей мере 30%. В другом варианте реализации, настоящее изобретение обеспечивает, что применение ингибитора протеаз и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность эксенатида у человека на по меньшей мере 30%. В другом варианте реализации, настоящее изобретение обеспечивает, что применение ингибитора протеаз и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность инсулина у человека на по меньшей мере 40%. В другом варианте реализации, настоящее изобретение обеспечивает, что применение ингибитора протеаз и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность эксенатида у человека на по меньшей мере 40%. В другом варианте реализации, настоящее изобретение обеспечивает, что применение ингибитора протеаз и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность инсулина у человека на по меньшей мере 50%. В другом варианте реализации, настоящее изобретение обеспечивает, что применение ингибитора протеаз и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность эксенатида у человека на по меньшей мере 50%. В другом варианте реализации, настоящее изобретение обеспечивает, что применение ингибитора протеаз и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность инсулина у человека на по меньшей мере 60%. В другом варианте реализации, настоящее изобретение обеспечивает, что применение ингибитора протеаз и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность эксенатида у человека на по меньшей мере 60%. В другом варианте реализации, настоящее изобретение обеспечивает, что применение ингибитора протеаз и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность инсулина у человека на по меньшей мере 70%. В другом варианте реализации, настоящее изобретение обеспечивает, что применение ингибитора протеаз и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность эксенатида у человека на по меньшей мере 70%. В другом варианте реализации, настоящее изобретение обеспечивает, что применение ингибитора протеаз и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность инсулина у человека на по меньшей мере 80%. В другом варианте реализации, настоящее изобретение обеспечивает, что применение ингибитора протеаз и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность эксенатида у человека на по меньшей мере 80%. В другом варианте реализации, настоящее изобретение обеспечивает, что применение ингибитора протеаз и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность инсулина у человека на по меньшей мере 90%. В другом варианте реализации, настоящее изобретение обеспечивает, что применение ингибитора протеаз и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность эксенатида у человека на по меньшей мере 90%. В другом варианте реализации, настоящее изобретение обеспечивает, что применение ингибитора протеаз и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность инсулина у человека на по меньшей мере 100%. В другом варианте реализации, настоящее изобретение обеспечивает, что применение ингибитора протеаз и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность эксенатида у человека на по меньшей мере 100%.
[0089] В другом варианте реализации, настоящее изобретение обеспечивает, что применение апротинина или SBTI и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность инсулина у человека на по меньшей мере 10%. В другом варианте реализации, настоящее изобретение обеспечивает, что применение апротинина или SBTI и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность инсулина у человека на по меньшей мере 20%. В другом варианте реализации, настоящее изобретение обеспечивает, что применение апротинина или SBTI и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность инсулина у человека на по меньшей мере 30%. В другом варианте реализации, настоящее изобретение обеспечивает, что применение апротинина или SBTI и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность инсулина у человека на по меньшей мере 40%. В другом варианте реализации, настоящее изобретение обеспечивает, что применение апротинина или SBTI и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность инсулина у человека на по меньшей мере 50%. В другом варианте реализации, настоящее изобретение обеспечивает, что применение апротинина или SBTI и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность инсулина у человека на по меньшей мере 60%. В другом варианте реализации, настоящее изобретение обеспечивает, что применение апротинина или SBTI и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность инсулина у человека на по меньшей мере 70%. В другом варианте реализации, настоящее изобретение обеспечивает, что применение апротинина или SBTI и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность инсулина у человека на по меньшей мере 80%. В другом варианте реализации, настоящее изобретение обеспечивает, что применение апротинина или SBTI и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность инсулина у человека на по меньшей мере 90%. В другом варианте реализации, настоящее изобретение обеспечивает, что применение апротинина или SBTI и SNAC или SNAD в одной композиции для перорального введения неожиданно существенно повышает биодоступность инсулина у человека на по меньшей мере 100%.
[0090] В другом варианте реализации, настоящее изобретение дополнительно обеспечивает применение дозированных форм с замедленным высвобождением (например, микрокапсулирования для замедленного высвобождения), которые позволяют снизить частоту введения лекарственного средства до одного или двух раз в день. В другом варианте реализации, дозировка инсулина соответственно возрастает, при этом снижается частота введения. В другом варианте реализации, дозировка эксенатида соответственно возрастает, при этом снижается частота введения. Каждый тип покрытия, усилителя всасывания, дозированной формы и т.д., которые препятствуют расщеплению композиции в желудке, представляет собой отдельный вариант реализации настоящего изобретения.
[0091] Способы измерения уровней инсулина хорошо известны в данной области техники. В одном варианте реализации, уровни рекомбинантного инсулина измеряют, применяя набор для радиоиммунологического анализа (RIA) инсулина человека, например, набор, произведенный Linco Research Inc, (Сент-Чарлз, Миссури). В другом варианте реализации, также измеряют уровни C-пептида, чтобы определить относительный вклад эндогенного и экзогенного инсулина в наблюдаемое повышение уровней инсулина. В другом варианте реализации, используют наборы для твердофазного иммуноферментного анализа (ELISA) инсулина. В другом варианте реализации, уровни инсулина измеряют с помощью любого другого способа, известного в данной области. В другом варианте реализации, уровни эксенатида измеряют способом, известным в данной области техники. Каждый из перечисленных вариантов представляет собой отдельный вариант реализации настоящего изобретения.
[0092] В другом варианте реализации, для предотвращения расщепления композиции в желудке применяют дозированные формы, состоящие из множества частиц. В другом варианте реализации, для предотвращения расщепления композиции в желудке применяют дозированные формы, состоящие из множества частиц.
[0093] В другом варианте реализации, настоящее изобретение обеспечивает способ перорального введения субъекту белка с ферментативной активностью, при котором существенная часть белка сохраняет свою ферментативную активность после всасывания через барьер слизистой оболочки кишечника субъекта; указанный способ включает пероральное введение субъекту фармацевтической композиции, содержащей указанный белок, ингибитор протеаз и усилитель всасывания, благодаря чему осуществляется пероральное введение субъекту белка с ферментативной активностью.
[0094] В другом варианте реализации, настоящее изобретение обеспечивает способ перорального введения субъекту белка с ферментативной активностью, при котором существенная часть белка сохраняет свою ферментативную активность после всасывания через барьер слизистой оболочки кишечника субъекта; указанный способ включает пероральное введение субъекту фармацевтической композиции, содержащей указанный белок, ингибитор протеаз и SNAC или SNAD, благодаря чему осуществляется пероральное введение субъекту белка с ферментативной активностью.
[0095] В другом варианте реализации, настоящее изобретение обеспечивает способ перорального введения инсулина субъекту, при котором существенная часть инсулина сохраняет активность после всасывания через барьер слизистой оболочки кишечника субъекта; указанный способ включает пероральное введение субъекту фармацевтической композиции, содержащей инсулин, ингибитор протеаз и SNAC или SNAD, благодаря чему осуществляется пероральное введение субъекту белка с ферментативной активностью. В другом варианте реализации, настоящее изобретение обеспечивает способ перорального введения субъекту эксенатида, при котором существенная часть эксенатида сохраняет активность после всасывания через барьер слизистой оболочки кишечника субъекта; указанный способ включает пероральное введение субъекту фармацевтической композиции, содержащей эксенатид, по меньшей мере один ингибитор протеаз и SNAC или SNAD, благодаря чему осуществляется пероральное введение субъекту белка с ферментативной активностью.
[0096] В другом варианте реализации, настоящее изобретение обеспечивает способ перорального введения субъекту белка с ферментативной активностью, при котором существенная часть белка сохраняет свою ферментативную активность после всасывания через барьер слизистой оболочки кишечника субъекта; указанный способ включает пероральное введение субъекту фармацевтической композиции, содержащей указанный белок, по меньшей мере один ингибитор протеаз, SNAC или SNAD и омега-3 жирную кислоту, благодаря чему осуществляется пероральное введение субъекту белка с ферментативной активностью. В другом варианте реализации, настоящее изобретение обеспечивает способ перорального введения субъекту белка с ферментативной активностью, при котором существенная часть белка сохраняет свою ферментативную активность после всасывания через барьер слизистой оболочки кишечника субъекта; указанный способ включает пероральное введение субъекту фармацевтической композиции, содержащей указанный белок, по меньшей мере один ингибитор протеаз и SNAC или SNAD, ЭДТА (или ее соль) и омега-3 жирную кислоту, благодаря чему осуществляется пероральное введение человеку белка с ферментативной активностью.
[0097] В другом варианте реализации, настоящее изобретение обеспечивает способ перорального введения инсулина субъекту, при котором существенная часть инсулина сохраняет активность после всасывания через барьер слизистой оболочки кишечника субъекта; указанный способ включает пероральное введение субъекту фармацевтической композиции, содержащей инсулин, по меньшей мере один ингибитор протеаз, SNAC или SNAD, омега-3 жирную кислоту и Na-ЭДТА, благодаря чему осуществляется пероральное введение субъекту белка с ферментативной активностью. В другом варианте реализации, настоящее изобретение обеспечивает способ перорального введения субъекту эксенатида, при котором существенная часть эксенатида сохраняет активность после всасывания через барьер слизистой оболочки кишечника субъекта; указанный способ включает пероральное введение субъекту фармацевтической композиции, содержащей эксенатид, по меньшей мере один ингибитор протеаз, SNAC или SNAD, омега-3 жирную кислоту и Na-ЭДТА, благодаря чему осуществляется пероральное введение субъекту белка с ферментативной активностью.
[0098] В другом варианте реализации, настоящее изобретение обеспечивает способ лечения сахарного диабета у человека, включающий пероральное введение субъекту фармацевтической композиции, содержащей инсулин, по меньшей мере один ингибитор протеаз и SNAC или SNAD, тем самым осуществляя лечение сахарного диабета. В другом варианте реализации, настоящее изобретение обеспечивает способ лечения сахарного диабета у человека, включающий пероральное введение субъекту фармацевтической композиции, содержащей инсулин и по меньшей мере один ингибитор протеаз и SNAC или SNAD, и омега-3 жирную кислоту, тем самым осуществляя лечение сахарного диабета. В другом варианте реализации, настоящее изобретение обеспечивает способ лечения сахарного диабета у человека, включающий пероральное введение субъекту фармацевтической композиции, содержащей инсулин и по меньшей мере один ингибитор протеаз и SNAC или SNAD, ЭДТА (или ее соль) и омега-3 жирную кислоту, тем самым осуществляя лечение сахарного диабета.
[0099] В другом варианте реализации, настоящее изобретение обеспечивает способ лечения сахарного диабета у человека, включающий пероральное введение субъекту фармацевтической композиции, содержащей эксенатид, по меньшей мере один ингибитор протеаз и SNAC или SNAD, тем самым осуществляя лечение сахарного диабета. В другом варианте реализации, настоящее изобретение обеспечивает способ лечения сахарного диабета у человека, включающий пероральное введение субъекту фармацевтической композиции, содержащей эксенатид и по меньшей мере один ингибитор протеаз и SNAC или SNAD, и омега-3 жирную кислоту, тем самым осуществляя лечение сахарного диабета. В другом варианте реализации, настоящее изобретение обеспечивает способ лечения сахарного диабета у человека, включающий пероральное введение субъекту фармацевтической композиции, содержащей эксенатид и по меньшей мере один ингибитор протеаз и SNAC или SNAD, ЭДТА (или ее соль) и омега-3 жирную кислоту, тем самым осуществляя лечение сахарного диабета.
[00100] В одном варианте реализации, сахарный диабет представляет собой диабет I типа. В другом варианте реализации, сахарный диабет представляет собой диабет II типа. В другом варианте реализации, сахарный диабет представляет собой инсулинозависимый диабет. В другом варианте реализации, сахарный диабет представляет собой инсулинонезависимый диабет. В другом варианте реализации, сахарный диабет представляет собой любой другой тип диабета, известный в данной области техники. Каждый из перечисленных вариантов представляет собой отдельный вариант реализации настоящего изобретения.
[00101] В одном варианте реализации, введение указанной композиции, содержащей инсулин, осуществляют трижды в день. В другом варианте реализации, введение осуществляют дважды в день. В другом варианте реализации, введение осуществляют четыре раза в день. В другом варианте реализации, введение осуществляют один раз в день. В другом варианте реализации, введение осуществляют более четырех раз в день. Каждый из перечисленных вариантов представляет собой отдельный вариант реализации настоящего изобретения.
[00102] В любом из способов согласно настоящему изобретению можно применять, в различных вариантах реализации, любую из композиций согласно настоящему изобретению.
[00103] В другом варианте реализации, настоящее изобретение обеспечивает композицию для перорального введения инсулина, содержащую белок инсулин, по меньшей мере один ингибитор протеаз и SNAC или SNAD, благодаря которой существенная часть инсулина сохраняет ферментативную активность после всасывания через барьер слизистой оболочки кишечника человека.
[00104] В одном варианте реализации, настоящее изобретение обеспечивает применение белка, по меньшей мере одного ингибитора протеаз и SNAC или SNAD для получения лекарственного средства для перорального введения белка с ферментативной активностью субъекту, благодаря которому существенная часть белка сохраняет свою ферментативную активность после всасывания через барьер слизистой оболочки кишечника субъекта. В одном варианте реализации, настоящее изобретение обеспечивает применение белка, по меньшей мере одного ингибитора протеаз, SNAC или SNAD и омега-3 жирной кислоты для получения лекарственного средства для перорального введения белка с ферментативной активностью субъекту, благодаря которому существенная часть белка сохраняет свою ферментативную активность после всасывания через барьер слизистой оболочки кишечника субъекта. В одном варианте реализации, настоящее изобретение обеспечивает применение белка, по меньшей мере одного ингибитора протеаз, SNAC или SNAD, Na-ЭДТА и омега-3 жирной кислоты для получения лекарственного средства для перорального введения белка с ферментативной активностью субъекту, благодаря которому существенная часть белка сохраняет свою ферментативную активность после всасывания через барьер слизистой оболочки кишечника субъекта.
[00105] В одном варианте реализации, настоящее изобретение обеспечивает применение белка инсулина, по меньшей мере одного ингибитора протеаз и SNAC или SNAD для получения лекарственного средства для лечения сахарного диабета у субъекта. В одном варианте реализации, настоящее изобретение обеспечивает применение белка инсулина, по меньшей мере одного ингибитора протеаз, SNAC или SNAD и омега-3 жирной кислоты для получения лекарственного средства для лечения сахарного диабета у субъекта. В одном варианте реализации, настоящее изобретение обеспечивает применение белка инсулина, по меньшей мере одного ингибитора протеаз, SNAC или SNAD, Na-ЭДТА и омега-3 жирной кислоты для получения лекарственного средства для лечения сахарного диабета у субъекта.
[00106] В одном варианте реализации, настоящее изобретение обеспечивает применение белка эксенатида, по меньшей мере одного ингибитора протеаз и SNAC или SNAD для получения лекарственного средства для лечения сахарного диабета у субъекта. В одном варианте реализации, настоящее изобретение обеспечивает применение белка эксенатида, по меньшей мере одного ингибитора протеаз, SNAC или SNAD и омега-3 жирной кислоты для получения лекарственного средства для лечения сахарного диабета у субъекта. В одном варианте реализации, настоящее изобретение обеспечивает применение белка эксенатида, по меньшей мере одного ингибитора протеаз, SNAC или SNAD, Na-ЭДТА и омега-3 жирной кислоты для получения лекарственного средства для лечения сахарного диабета у субъекта.
[00107] В одном варианте реализации, способы и композиции согласно настоящему изобретению имеют преимущество, состоящее в более близкой имитации физиологической секреции инсулина поджелудочной железой. Когда инсулин секретируется в воротную вену, в печени находится большая концентрация инсулина, чем в периферических тканях. Аналогично, инсулин, который вводят согласно настоящему изобретению, достигает кишечника и всасывается в организм через кишечник и через систему воротной вены печени. Этот путь всасывания, таким образом, имеет сходство с физиологической секрецией инсулина поджелудочной железой, позволяя, в данном варианте реализации, точный контроль уровня глюкозы в крови и метаболической активности печени и периферических органов, контролируемой инсулином. Напротив, когда инсулин вводят пациентам с недостаточным уровнем инсулина, страдающим диабетом, через периферическую венозную систему, концентрация инсулина в воротной вене аналогична таковой в периферическом кровообращении, что приводит к гипоинсулинемии в воротной вене и печени и гиперинсулинемии в периферической венозной системе. Это приводит, в одном варианте реализации, к нарушению пути утилизации глюкозы.
[00108] В другом варианте реализации, различные компоненты композиций согласно настоящему изобретению всасываются с различными скоростями из просвета кишечника в кровоток. Всасывание желчной кислоты, в одном варианте реализации, происходит значительно быстрее, чем всасывание инсулина.
[00109] По этой причине, в другом варианте реализации, использовали схему приема лекарственного средства, включающую прием внутрь пары пилюль с некоторым интервалом времени, например, вторую пилюлю, содержащую более высокую концентрацию усилителя, принимают через определенный промежуток времени (например, через 30 минут) после приема первой пилюли. В другом варианте реализации, некоторые из компонентов микроинкапсулируют для улучшения всасывания инсулина в организме. В другом варианте реализации, некоторые из компонентов микроинкапсулируют для улучшения всасывания эксенатида в организме.
[00110] В одном варианте реализации, протокол лечения согласно настоящему изобретению терапевтический. В другом варианте реализации, протокол профилактический. Каждый из перечисленных вариантов представляет собой отдельный вариант реализации настоящего изобретения.
[00111] В другом варианте реализации, твердые носители/разбавители для применения в способах и композициях согласно настоящему изобретению включают, но не ограничены перечисленными, камедь, крахмал (например, кукурузный крахмал, желатинированный крахмал), сахар (например, лактозу, маннит, сахарозу, декстрозу), целлюлозный материал (например, микрокристаллическую целлюлозу), акрилат (например, полиметилакрилат), карбонат кальция, оксид магния, тальк или смеси перечисленных компонентов.
[00112] В другом варианте реализации, указанные композиции дополнительно содержат связующие вещества (например, акацию, кукурузный крахмал, желатин, карбомер, этилцеллюлозу, гуаровую камедь, гидроксипропилцеллюлозу, гидроксипропилметилцеллюлозу, повидон), дезинтегрирующие агенты (например, кукурузный крахмал, картофельный крахмал, альгиновую кислоту, диоксид кремния, кроскармелозу натрия, кросповидон, гуаровую камедь, натриевую соль гликолята крахмала), буферы (например, Tris-HCl, ацетат, фосфат) с различными pH и ионной силой, вспомогательные вещества, такие как альбумин или желатин, для предотвращения абсорбции поверхностями, детергенты (например, Tween 20, Tween 80, Pluronic F68, соли желчных кислот), поверхностно-активные вещества (например, лаурилсульфат натрия), усилители проницаемости, солюбилизирующие агенты (например, глицерин, полиэтиленглицерин), антиоксиданты (например, аскорбиновую кислоту, метабисульфит натрия, бутилированный гидроксианизол), стабилизаторы (например, гидроксипропилцеллюлозу, гидроксипропилметилцеллюлозу), агенты, повышающие вязкость (например, карбомер, коллоидный диоксид кремния, этилцеллюлозу, гуаровую камедь), подсластители (например, аспартам, лимонную кислоту), консерванты (например, тимеросал, бензиловый спирт, парабены), лубриканты (например, стеариновую кислоту, стеарат магния, полиэтиленгликоль, лаурилсульфат натрия), добавки, повышающие текучесть (например, коллоидный диоксид кремния), пластификаторы (например, диэтилфталат, триэтилцитрат), эмульгаторы (например, карбомер, гидроксипропилцеллюлозу, лаурилсульфат натрия), полимерные покрытия (например, полоксамеры или полоксамины), образующие покрытие и пленку агенты (например, этилцеллюлозу, акрилаты, полиметакрилаты) и/или адъюванты. Каждое из перечисленных выше вспомогательных веществ представляет собой отдельный вариант реализации настоящего изобретения.
[00113] В некоторых вариантах реализации, дозированные формы согласно настоящему изобретению входят в состав формы для достижения профиля немедленного высвобождения, профиля пролонгированного высвобождения или профиля задержанного высвобождения. В некоторых вариантах реализации, определенный профиль высвобождения композиции обеспечивают благодаря применению определенных вспомогательных веществ, которые служат, например, связующими веществами, дезинтегрирующими агентами, наполнителями или материалами покрытия. В одном варианте реализации, разрабатывают состав, содержащий композицию для достижения конкретного профиля высвобождения, что известно специалисту в данной области техники.
[00114] В одном варианте реализации, указанная композиция приготавливается в виде пероральной дозированной формы. В одном варианте реализации, композиция представляет собой твердую пероральную дозированную форму, включающую таблетки, жевательные таблетки или капсулы. В одном варианте реализации, капсулы представляют собой мягкие желатиновые капсулы. В другом варианте реализации, капсулы, согласно настоящему описанию, представляют собой капсулы в твердой оболочке. В другом варианте реализации, капсулы, согласно настоящему описанию представляют собой капсулы в мягкой оболочке. В другом варианте реализации, капсулы согласно настоящему описанию изготовлены из желатина. В другом варианте реализации, капсулы согласно настоящему описанию изготовлены из желатинизирующих веществ растительного происхождения, таких как каррагинаны и модифицированные формы крахмала и целлюлозы.
[00115] В других вариантах реализации, покрытия для контролируемого или продолжительного высвобождения, применяемые в способах и композициях согласно настоящему изобретению, включают получение липофильных депоформул (например, с помощью жирных кислот, восков, масел).
[00116] Указанные композиции также содержат, в другом варианте реализации, включение активного материала внутрь или на поверхность препаратов в виде частиц полимерных соединений, таких как полимолочная кислота, полигликолевая кислота, гидрогели и т.д., или на поверхность липосом, микроэмульсий, мицелл, однослойных или многослойных везикул, теней эритроцитов или сферопластов). Такие композиции будут влиять на агрегатное состояние, растворимость, стабильность, скорость высвобождения in vivo и скорость клиренса in vivo. В другом варианте реализации, композиции активных ингредиентов в форме частиц покрывают полимерами (например, полоксамерами или полоксаминами).
[00117] В другом варианте реализации, указанные композиции, содержащие инсулин и омега-3 жирную кислоту, доставляют в виде везикулы, например, липосомы (см. Langer, Science 249: 1527-1533 (1990); Treat и др., в Liposomes in the Therapy of Infectious Disease and Cancer, Lopez-Berestein и Fidler (ред.), Liss, Нью-Йорк, стр.353-365 (1989); Lopez-Berestein, там же, стр.317-327; см., как правило, там же). В другом варианте реализации, композиции, содержащие эксенатид и омега-3 жирную кислоту, доставляют в виде везикулы, например, липосомы (см. Langer, Science 249: 1527-1533 (1990); Treat и др., в Liposomes in the Therapy of Infectious Disease and Cancer, Lopez-Berestein и Fidler (ред.), Liss, Нью-Йорк, стр.353-365 (1989); Lopez-Berestein, там же, стр.317-327; см., как правило, там же).
[00118] Получение фармацевтических композиций, которые содержат активный компонент, например, с помощью процессов смешивания, гранулирования или таблетирования, хорошо известно в данной области. Активный терапевтический ингредиент часто смешивают с вспомогательными веществами, которые являются фармацевтически приемлемыми и совместимыми с активным ингредиентом. Для перорального введения, указанные активные ингредиенты композиций согласно настоящему изобретению смешивают с вспомогательными веществами, характерными для этого назначения, такими как среды, стабилизаторы или инертные разбавители, и переводят с помощью обычных способов в подходящие формы для введения, такие как таблетки, имеющие покрытие таблетки, твердые или мягкие желатиновые капсулы, водные, спиртовые или маслянистые растворы.
[00119] Каждая из перечисленных выше добавок, вспомогательных веществ, лекарственных форм и способов введения представляет собой отдельный вариант реализации настоящего изобретения.
[00120] В одном варианте реализации, термин "лечение" относится к лечению заболевания. В другом варианте реализации, "лечение" относится к предупреждению заболевания. В другом варианте реализации, "лечение" относится к уменьшению числа случаев заболевания. В другом варианте реализации, "лечение" относится к облегчению симптомов заболевания. В другом варианте реализации, "лечение" относится к индуцированию ремиссии. В другом варианте реализации, "лечение" относится к замедлению прогрессирования заболевания.
РАЗДЕЛ ПОДРОБНОГО ОПИСАНИЯ ЭКСПЕРИМЕНТОВ
ПРИМЕР 1: ПЕРОРАЛЬНЫЕ ЛЕКАРСТВЕННЫЕ ФОРМЫ, СОДЕРЖАЩИЕ ИНСУЛИН. SNAC И ИНГИБИТОРЫ ПРОТЕАЗ МАТЕРИАЛЫ И ЭКСПЕРИМЕНТАЛЬНЫЕ МЕТОДЫ
Лекарственная форма
[00121] Приготавливали составы, содержащие: (1) 6 мг инсулина, 250 мг SNAC, 125 мг SBTI; (2) 6 мг инсулина, 250 мг SNAC, 2.5 мг апротинина, 125 мг SBTI; (3) 6 мг инсулина, 250 мг SNAC, 2.5 мг апротинина, 125 мг SBTI; (4) 6 мг инсулина, 250 мг SNAC. Указанные составы хранили в холодильнике (4°C) до начала дозирования.
РЕЗУЛЬТАТЫ
[00123] В следующем эксперименте, составы, описанные в разделе "Лекарственная форма", принимали перорально 3 здоровых человека. На Фиг.1 показано, что уровни глюкозы в крови значительно снижались и были более стабильны у людей, получавших лечение составами (1) и (3). Данные результаты позволяют предположить, что лекарственные формы, содержащие комбинацию ингибитора протеаз и SNAC, лучше, чем лекарственные формы, содержащие только SNAC. В частности, комбинация SNAC и SBTI лучше, чем любой другой применяемый состав. Важно отметить, что действие SNAC и ингибитора протеаз синергично, так как лекарственные формы, содержащие инсулин и один ингибитор протеаз, не вызывают снижения глюкозы в крови, т.е. не наблюдаются различия в снижении уровней глюкозы в крови в предыдущем эксперименте с теми же лекарственными формами, содержащими один ингибитор протеаз (SBTI или апротинин). Таким образом, результаты, относящиеся к снижению уровней глюкозы в крови с помощью инсулина и комбинации SNAC и по меньшей мере одного ингибитора протеаз, были неожиданными. Лекарственная форма, содержащая SNAC и SBTI, вызывала, благодаря синергичному действию, наиболее сильное снижение уровней глюкозы в крови.
[00124] На Фиг.2 показано, что уровни C-пептида в крови значительно снижались у людей, получавших лечение лекарственной формой (1) и (3). Данные результаты также позволяют предположить, что комбинация SNAC и ингибитора протеаз, такого как SBTI, оказывает синергичное действие на снижение уровней C-пептида в крови.
[00125] Следует подчеркнуть, что не наблюдали снижения уровней С-пептида в предыдущем эксперименте, в котором применяли лекарственные формы, содержащие один ингибитор протеаз (SBTI или апротинин). Таким образом, полученные результаты, относящиеся к снижению уровней С-пептида в крови с помощью инсулина и комбинации ингибиторов протеаз, таких как SBTI и SNAC, были неожиданными.
ПРИМЕР 2: ОПТИМИЗАЦИЯ ИСТОЧНИКА ОМЕГА-3 ЖИРНЫХ КИСЛОТ
[00126] Различные омега-3 жирные кислоты или источники омега-3 жирных кислот (например, перечисленые выше в настоящем описании) сравнивали по их способности предохранять инсулин после перорального введения в способах и композициях согласно настоящему изобретению. Таблетки или капсулы инсулина приготавливали согласно Примерам, приведенным выше, за исключением того, что инсулин растворяли в альтернативном рыбьему жиру источнике. Наиболее эффективный источник омега-3 жирных кислот использовали в последующих Примерах.
ПРИМЕР 3: ОПТИМИЗАЦИЯ ИНГИБИТОРА ПРОТЕАЗ
[00127] Различные ингибиторы протеаз (одинаково нетоксичные или имеющие приемлемый профиль токсичности; например, такие, которые перечислены выше в настоящем описании) сравнивали по их способности предохранять инсулин после перорального введения в способах и композициях согласно настоящему изобретению. Таблетки или капсулы инсулина и/или эксенатида приготавливали согласно Примерам, приведенным выше, за исключением того, что SBTI и/или апротинин заменили альтернативными ингибиторами протеаз. Количества ингибиторов протеаз также варьировали, чтобы определить оптимальные количества. Наиболее эффективный ингибитор протеаз в наиболее эффективном количестве использовали в последующих Примерах.
ПРИМЕР 4: ОПТИМИЗАЦИЯ УСИЛИТЕЛЯ
[00128] Различные усилители (например, перечисленные выше в настоящем описании) сравнивали по их способности способствовать всасыванию инсулина после перорального введения в способах и композициях согласно настоящему изобретению. Таблетки или капсулы инсулина приготавливали согласно Примерам, приведенным выше, за исключением того, что ЭДТА заменили альтернативными усилителями. Количества усилителей также варьировали, чтобы определить оптимальные количества. Наиболее эффективный усилитель в наиболее эффективном количестве использовали в последующих экспериментах.
ПРИМЕР 5: ОПТИМИЗАЦИЯ ТИПА И КОЛИЧЕСТВА ИНСУЛИНА
[00129] Различные типы и количества инсулина, например, перечисленные выше в настоящем описании, сравнивали по их способности регулировать сахар в крови в способах и композициях согласно настоящему изобретению. Таблетки или капсулы инсулина приготавливали согласно Примерам, приведенным выше, за исключением того, что тип и количество инсулина варьировали. Наиболее эффективный тип инсулина в наиболее эффективном количестве использовали в клинических исследованиях.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ПЕРОРАЛЬНОГО ВВЕДЕНИЯ БЕЛКОВ | 2009 |
|
RU2494755C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ПЕРОРАЛЬНОГО ВВЕДЕНИЯ ПРОТЕИНОВ | 2009 |
|
RU2504373C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ПЕРОРАЛЬНОГО ВВЕДЕНИЯ ЭКСЕНАТИДА | 2009 |
|
RU2566063C2 |
| КОМПОЗИЦИИ, СОДЕРЖАЩИЕ РЕКОМБИНАНТНЫЙ ИНГИБИТОР ПРОТЕАЗЫ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2826190C2 |
| МИМЕТИК КАЛЬЦИТОНИНА ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНЕЙ И НАРУШЕНИЙ | 2014 |
|
RU2689551C1 |
| ПРИМЕНЕНИЕ КАЛЬЦИТОНИНА ДЛЯ ЛЕЧЕНИЯ РЕВМАТОИДНОГО АРТРИТА | 2006 |
|
RU2453330C2 |
| ПРИМЕНЕНИЕ КАЛЬЦИТОНИНА ПРИ ОСТЕОАРТРИТЕ | 2004 |
|
RU2368390C2 |
| СПОСОБЫ ИЗГОТОВЛЕНИЯ ЛЕКАРСТВЕННЫХ СОСТАВОВ АЦИКЛОВИРА | 2005 |
|
RU2406504C2 |
| ТВЕРДЫЕ КОМПОЗИЦИИ ДЛЯ ПЕРОРАЛЬНОГО ВВЕДЕНИЯ | 2018 |
|
RU2777206C2 |
| ЛЕЧЕНИЕ ДИАБЕТА И МЕТАБОЛИЧЕСКОГО СИНДРОМА | 2010 |
|
RU2537181C2 |
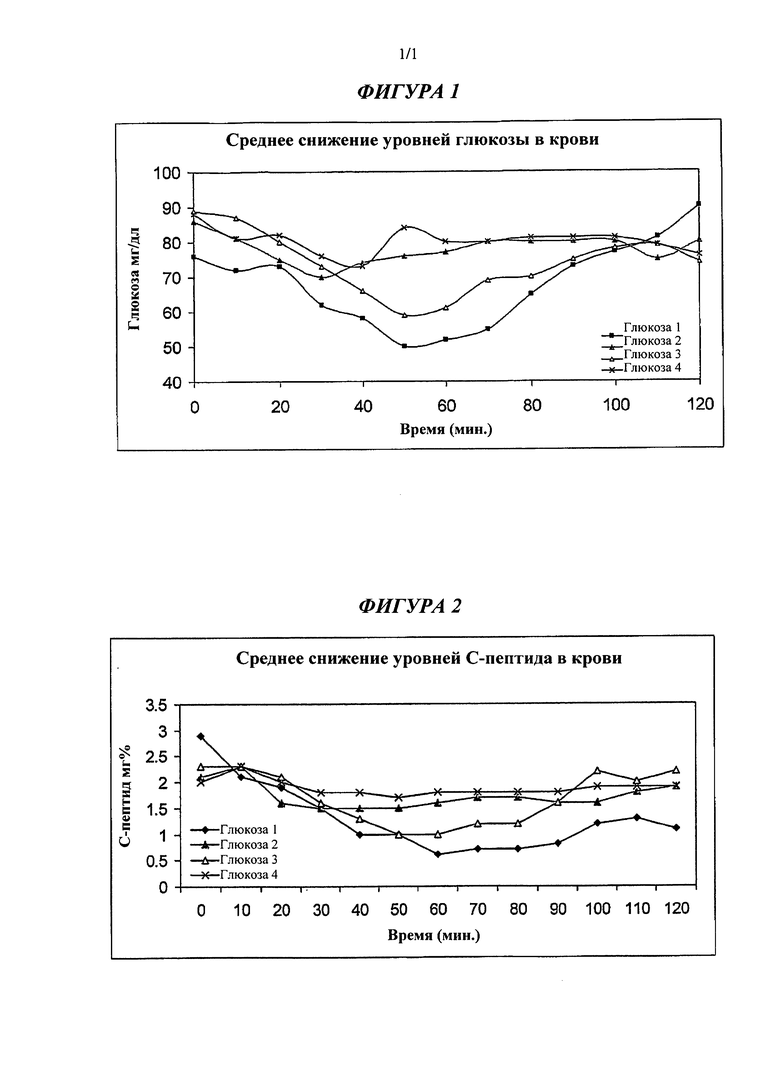
Группа изобретений относится к области фармацевтики и медицины и касается фармацевтической композиции для перорального введения, содержащей паратиреоидный гормон (ПТГ), ингибитор протеаз, усилитель всасывания, выбранный из группы, состоящей из N-(8-[2-гидроксибензоил]амино)каприлата, N-(10-[2-гидроксибензоил]амино)деканоата, соли N-(8-[2-гидроксибензоил]амино)каприлата, соли N-(10-[2-гидроксибензоил]амино)деканоата и комбинации указанных соединений. Заявлен также способ перорального введения ПТГ в композиции. Группа изобретений обеспечивает усиление всасывания ПТГ при пероральном введении. 2 н. и 8 з.п. ф-лы, 5 пр., 2 ил.
1. Фармацевтическая композиция для перорального введения белка субъекту, нуждающемуся в этом, при этом композиция содержит указанный белок, ингибитор протеаз и соединение, выбранное из группы, состоящей из N-(8-[2-гидроксибензоил]амино)каприлата, N-(10-[2-гидроксибензоил]амино)деканоата, соли N-(8-[2-гидроксибензоил]амино)каприлата, соли N-(10-[2-гидроксибензоил]амино)деканоата и комбинации указанных соединений, причем белок представляет собой паратиреоидный гормон (ПТГ) или его часть и имеет молекулярный вес до 100000 Дальтон.
2. Композиция по п. 1, отличающаяся тем, что указанный белок представляет собой рекомбинантный белок.
3. Композиция по п. 1, отличающаяся тем, что указанное соединение представляет собой соль N-(8-[2-гидроксибензоил]амино)каприлата или соль N-(10-[2-гидроксибензоил]амино)деканоата, и указанная соль выбрана из группы, состоящей из мононатриевой соли, динатриевой соли и комбинации указанных солей.
4. Композиция по п. 1, отличающаяся тем, что указанный ингибитор протеаз выбран из группы, состоящей из серпина, суицидного ингибитора, ингибитора переходного состояния, белкового ингибитора протеаз, хелатирующего агента, ингибитора цистеиновых протеаз, ингибитора треониновых протеаз, ингибитора аспарагиновых протеаз и ингибитора металлопротеаз.
5. Композиция по п. 4, отличающаяся тем, что указанный ингибитор протеаз представляет собой серпин, и указанный серпин представляет собой ингибитор трипсина.
6. Композиция по п. 5, отличающаяся тем, что указанный ингибитор протеаз выбран из группы, состоящей из ингибитора трипсина из лимской фасоли, апротинина, ингибитора трипсина из соевых бобов (SBTI) и овомукоида.
7. Композиция по любому из пп. 1-6, дополнительно содержащая омега-3 жирную кислоту.
8. Композиция по любому из пп. 1-6, дополнительно содержащая ЭДТА или ее соль.
9. Композиция по любому из пп. 1-6, дополнительно содержащая покрытие, которое ингибирует расщепление указанной композиции в желудке субъекта; энтеросолюбильное покрытие или желатиновое покрытие.
10. Способ перорального введения белка, имеющего молекулярный вес до 100000 Дальтон, субъекту, не являющемуся человеком, причем белок представляет собой паратиреоидный гормон (ПТГ) или его часть, при этом способ включает пероральное введение указанному субъекту композиции по любому из пп. 1-9.
| US2007087957 A1, 19.04.2007 | |||
| US2002123459A1, 05.09.2002 | |||
| US2008153779 A1, 26.06.2008. |
Авторы
Даты
2018-03-07—Публикация
2013-07-04—Подача