Область техники
Настоящее изобретение относится к новому способу сухого гранулирования для получения композиций метформина, а также его комбинаций с ингибиторами дипептидилпептидазы-4 (DPP-IV). Изобретение дополнительно относится к новой композиции метформина в чистом виде и его комбинациям с ингибиторами DPP-IV.
Предшествующий уровень техники
Сахарный диабет (диабет) представляет собой заболевание, отличающееся высокими уровнями глюкозы в крови, которые происходят в результате нарушений способности организма продуцировать и/или использовать инсулин. Сахарный диабет возникает в тех случаях, когда уровень глюкозы в крови становится выше нормального. Основными типами диабета являются диабет I типа и диабет II типа, а также гестационный диабет. Диабет II типа представляет собой наиболее распространенную форму диабета, воздействующую на 85-90% всех людей, страдающих от данного расстройства. В отношении сахарного диабета II типа заболевание обычно развивается в более позднем возрасте. Секреция инсулина может быть нормальной или даже избыточной (и пациенты II типа, таким образом, в меньшей степени склонны к кетозу), но этого недостаточно для компенсации инсулинорезистентности. Ожирение присутствует у большинства пациентов с диабетом II типа; пациенты, не страдающие ожирением, имеют тенденцию к низкой инсулин-секретирующей способности (хотя не настолько низкой, как в случае диабета I типа), нежели ощутимой инсулинорезистентности. Это тесно связано с сердечно-сосудистым заболеванием.
Метформин представляет собой хорошо известное пероральное противодиабетическое лекарственное средство класса бигуанидов, которое описано в патенте США №3174901. Метформин в настоящее время представлен на рынке в дозировках 500, 850 и 1000 мг под торговой маркой Glucophage® для лечения диабета II типа.
Метформин представляет собой 1,1-диметилбигуанид, имеющий следующую структурную формулу:
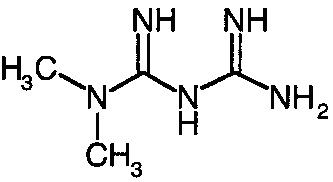
Вилдаглиптин представляет собой ингибитор фермента дипептидилпептидазы-4, фермента, ответственного, наряду с другими функциями, за разрушение гормона внутренней секреции глюкагоноподобного пептида-1 (GLP-1; инсулинотропин), который играет роль в регуляции секреции инсулина. Вилдаглиптин используют в лечении сахарного диабета II типа; его можно добавлять к метформину, сульфонилмочевине или тиазолидиндиону, когда монотерапия с использованием данных соединений является недостаточной.
Вилдаглиптин, имеющий систематическое название (S)-{[(3-Гидроксиадамантан-1-ил)амино]ацетил}пирролидин-2-карбонитрил и следующую структурную формулу, представлен на рынке в дозе 50 мг под торговой маркой Galvus®.
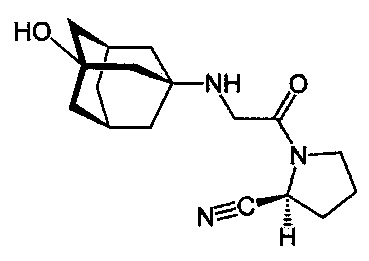
Объединение двух или более чем двух противодиабетических агентов в одну таблетку обеспечивает потенциальный способ доставки комбинированной терапии без увеличения сложности суточных схем пациентов, как описано в EP 02402342. Комбинация вилдаглиптина и метформина представлена на рынке под торговой маркой Eucreas®. Eucreas, объединяет два антигипергликемических агента с комплиментарными механизмами действия для улучшения гликемического контроля у пациентов с диабетом II типа: вилдаглиптин, член класса лекарственных средств, стимулирующих синтез инсулина островками, и метформина гидрохлорид, член класса бигуанидов.
Известно, что свойства сыпучести и прессуемость метформина являются очень неудобными в отношении способа таблетирования. Так как он является высококристаллическим и имеет плохие свойства уплотненности, сложно получать таблетки посредством прямого прессования или сухого гранулирования. В общем, для фармацевтических ингредиентов, которые имеют такие свойства, используют способ влажного гранулирования. Кроме того, метформин представляет собой высокодозное лекарственное средство, которое тяжело прессовать прямо в таблетки. В данном случае проблемы, заключающиеся в большей массе таблеток, возникают при способах сухого гранулирования, так как получающийся порошок требует избыточного количества эксципиентов, и особенно связующих веществ, для получения таблеток, прессованных должным образом.
В US 2003/104049-A1 описан способ сухого смешения для получения композиций метформина с метилцеллюлозой 15 сП (сантипуаз), микрокристаллической целлюлозой и стеаратом магния в разных соотношениях (примеры 1-6). Однако отмечено, что количество эксципиентов, необходимое в композиции, является довольно большим, и также применение смазывающих веществ, таких как стеарат магния, очень ограничено вследствие их неблагоприятных эффектов в отношении более низкой твердости и истираемости (пар. 24). Заявители данной заявки сообщают о том, что, поскольку количество стеарата магния снижено в примерах, твердость и истираемость значительно улучшены. Однако специалисты в данной области техники оценили бы тот факт, что снижение количества смазывающего вещества вызовет неизбежные проблемы, такие как низкая сыпучесть и проблемы прилипания в пуансонах. Вследствие этого все еще существует потребность в композициях метформина, которые имеют хорошую истираемость и твердость без проблем прилипания и плохой сыпучести.
Таким образом, одна из задач настоящего изобретения заключается в обеспечении композиций метформина, которые не имеют проблем, указанных выше.
Другая задача настоящего изобретения заключается в разработке композиций, которые делают способ сухого гранулирования более последовательным и, вследствие этого, пригодным для промышленного производства при поддержании фармацевтической эквивалентности стандартной фармацевтической форме.
Кроме того, класс лекарственных средств ингибиторов дипептидилпептидазы-4 (DPP-4), особенно вилдаглиптин, является гигроскопичным, практически не способным к уплотнению, и имеет проблемы стабильности. Факт того, что вилдаглиптин представляет собой молекулу, чувствительную к влажности, может приводить к проблемам стабильности продукта. Для возможности преодоления данной проблемы авторы изобретения разработали способ сухого гранулирования и конкретную композицию для получения свободно сыпучей, способной к уплотнению композиции, которая приводит к прессованию таблеток, имеющих хорошие свойства, например хорошую твердость, истираемость, и с улучшенной стабильностью вилдаглиптина.
В WO 2007/078726-А2 описаны способы сухой или влажной обработки для получения комбинаций метформина и ингибитора DPP-4, хотя все композиции, описанные в конкретных примерах, приведены, будучи полученными посредством способа влажного гранулирования. В данном документе ничего не говорится о проблемах прессуемости и стабильности, также в нем не описывается конкретная композиция, которую получают посредством прямого или сухого гранулирования. Также в способе сухого гранулирования не рассматривают массу и истираемость таблеток.
В WO 2007/041053-A2 описано получение комбинаций ингибитор DPP-4/метформин, где установлено, что влажное гранулирование может быть более предпочтительным, чем сухое гранулирование, из-за преимуществ, которые оно обеспечивает, таких как прессуемость с лучшей смачиваемостью, уменьшением проблем растворения и дезинтеграции и обеспечением улучшенной однородности состава. Дополнительно установлено, что метформин обычно получают посредством процесса влажного гранулирования с высокой загрузкой лекарственного средства и известно, что его очень сложно обрабатывать традиционными методиками, такими как вальцевание и прямое прессование, из-за плохих свойств уплотненности. Для решения проблем, указанных выше, подходящим эксципиентам, таким как связующие вещества, придают особое значение, тогда как разбавители считают абсолютно необязательными. В качестве предпочтительных способов предлагают влажное гранулирование и гранулирование из расплава наряду со связующими веществами, и также сообщают, что метформин влажной грануляции демонстрирует разрушение вилдаглиптина, составляющее 6,6%, согласно примеру 2. Для композиций метформина, полученных посредством способов сухого гранулирования, конкретных примеров не приведено.
В WO 2011/032912-A1 описана композиция комбинаций метформина и вилдаглиптина или ситаглиптина с немедленным высвобождением, а также способы изготовления таких композиций. Применяют способы прямого прессования и гранулирования из расплава, при которых метформина гидрохлорид используют в виде смеси с 0,5% Aerosil®. Предлагают, чтобы активные вещества обрабатывали в фармацевтическую композицию вместе с более чем 10 мас.% смазывающего вещества, где смазывающее вещество представляет собой полиэтиленгликоль или смесь полиэтиленгликоля с одним или множеством других смазывающих веществ.
Согласно предшествующему уровню техники частицы ингибитора DPP-IV также можно добавлять к внешней фазе гранул метформина, которые смешивают и таблетируют. Однако в отношении ингибитора DPP-IV, загрузка которого составляет 3-4% в конечной композиции, нужно принимать во внимание риск для однородности смеси. Известно, что влажное гранулирование/гранулирование из расплава метформина и ингибитора DPP-IV совместно приводит к проблемам разрушения ингибитора DPP-IV, как упомянуто в WO 2007/041053-А2.
Таким образом, еще одной задачей настоящего изобретения является устранение риска для однородности смеси ингибитора DPP-IV на этапе конечной композиции.
В связи с этим устранение недостатков, связанных с классическими способами влажного гранулирования/гранулирования из расплава/сухого гранулирования при получении прессуемых порошков метформина и ингибиторов DPP-4 для таблеток и обеспечение улучшенных таблеток как таковых, будет являться значительной разработкой в области получения лекарственных средств.
Вследствие этого еще одной задачей настоящего изобретения является устранение сложных и дорогих стадий влажного гранулирования/гранулирования из расплава при получении прессуемых комбинаций метформина и ингибитора DPP-4.
Более конкретно, задачей настоящего изобретения является обеспечение прямого способа получения таких комбинаций посредством модификации эксципиентов и, таким образом, получения таблеток с улучшенным качеством прессуемости, не имеющих проблем прилипания и сыпучести.
Еще одной задачей настоящего изобретения является устранение неблагоприятных эффектов традиционных способов на комбинации метформина и ингибитора DPP-4 для обеспечения улучшенной стабильности.
Задачи настоящего изобретения достигаются посредством использования конкретных разбавителей, то есть комбинации микрокристаллической целлюлозы и безводного двухосновного фосфата кальция в хорошо согласованных количествах.
Подробное описание изобретения
Термин "метформин", в том виде, как он используется в данном документе, относится к метформину или его фармацевтически приемлемой соли. В настоящем контексте "ингибитор DPP-IV" также относится к активным метаболитам и пролекарствам ингибиторов DPP-IV. "Метаболит" представляет собой активное производное ингибитора DPP-IV, которое образуется, когда ингибитор DPP-IV метаболизируется. "Пролекарство" представляет собой соединение, которое либо метаболизируется до ингибитора DPP-IV, либо метабилизируется до такого(их) же метаболита(ов), как ингибитор DPP-IV. В предпочтительных воплощениях указанный ингибитор DPP-IV включает ситаглиптин, вилдаглиптин или саксаглиптин. Наиболее предпочтительно ингибитор DPP-IV представляет собой вилдаглиптин.
Как отмечено в предшествующем уровне техники, метформин и ингибиторы DPP-IV демонстрируют определенные недостатки, что делает сложной их обработку посредством традиционных способов. Сыпучесть, истираемость, прессуемость и стабильность представляют собой главные проблемы, которые нужно решать при разработке новых способов и композиций. Более конкретно, метформин обладает плохой уплотняемостью и сыпучестью, тогда как и метформин и ингибиторы DPP-IV обладают плохой или умеренно плохой стабильностью при применении способа влажного гранулирования из-за чувствительности вилдаглиптина к влажности. Сегрегация представляет собой еще одну проблему ингибиторов DPP-4, которая обычно обусловлена кристаллической структурой данных соединений.
Способы влажного гранулирования, предложенные в предшествующем уровне техники для устранения проблем прессуемости, связанных с метформином, все еще считаются недостаточными для преодоления проблем в отношении стабильности и возможной однородности смеси комбинаций лекарственных средств. С другой стороны, известно, что традиционные способы сухого гранулирования не обеспечивают удовлетворительного решения проблем плохих свойств уплотняемости метформина, и это приводит к увеличению массы получаемых таблеток из-за необходимости использовать избыточное количество эксципиентов.
Принимая во внимание задачи настоящего изобретения, авторы изобретения провели обширное исследование на новых композициях комбинаций метформин/ингибитор DPP-4, которые являются легко прессуемыми и достаточно стабильными, и неожиданно обнаружили, что определенные разбавители, то есть комбинации микрокристаллической целлюлозы (МСС) и безводного двухосновного фосфата кальция (DCPA), являются преимущественными для устранения отмеченных недостатков, например, в способах сухого гранулирования. Отмечают, что МСС и DCPA являются подходящими для обеспечения лучшей уплотняемости и сыпучести метформина в том случае, когда их используют в виде комбинации. Авторы изобретения дополнительно отмечают, что указанные выше полезные эффекты гораздо более заметны, когда отношение метформина к разбавителю (MCC+DCPA) составляет от 2,5 до 25 по массе, даже несмотря на то, что указанный разбавитель, имея гораздо более низкие массовые отношения, как отмечено, является все еще эффективным в отношении успешно прессованных таблеток с хорошей истираемостью и незначительными проблемами прилипания. В данном случае, более низкие количества MCC+DCPA, такие как массовое отношение метформина к разбавителю, составляющее от 15 до 25, являются также эффективными, и такие более низкие количества разбавителей значительно снижают массу таблетки. Вследствие этого отрицательные воздействия смазывающих веществ (то есть стеарата магния), как указано, например, в US 2003/0104049, вызывающих высокую истираемость и твердость, в настоящее время устранены. Кроме того, проблемы стабильности, связанные с влажными способами или избыточными количествами эксципиентов, реагирующими на ингибиторы DPP-4, могут быть также устранены.
Таким образом, согласно первому аспекту настоящего изобретения предложен способ получения композиций метформина в виде таблеток, включающий сухое гранулирование активного вещества с MCC+DCPA. Композиция предпочтительно дополнительно содержит ингибитор DPP-4. В других воплощениях отношение метформина к MCC+DCPA составляет от 2,5 до 25 по массе.
Согласно еще одному аспекту предложена композиция метформина, содержащая комбинацию МСС и DCPA в качестве разбавителей. Соответственно, отношение метформина к (МСС+DCPA) может составлять от 2,5 до 25 по массе.
Как отмечено выше, ингибитор DPP-IV предпочтительно представляет собой вилдаглиптин. Способ по настоящему изобретению, направленный на получение преимущественных композиций в виде таблеток, может включать также дополнительные разбавители, связующие вещества, разрыхлители, смазывающие вещества и скользящие вещества.
Примеры таких дополнительных разбавителей включают маннит, лактозу, сорбит, водный двухосновный фосфат кальция и целлюлозу в порошке. Общее количество разбавителей, добавляемое к способу гранулирования, составляет от 2 до 25%, более предпочтительно от 10 до 20% на основе общей массы композиции.
Для возможности получения таблетки, которая имеет подходящий размер для использования пациентами, то есть которую легко глотать, выбор разбавителя представлял собой ключевой момент. В отношении таблеток, содержащих 1000 мг метформина и 50 мг вилдаглиптина, целевым показателем была масса таблетки от 1200 мг до 1600 мг, которая соответствует от 83,3% до 62,5% загрузке метформина. В первом испытании авторы изобретения оценивали множество эксципиентов, таких как лактоза, в качестве разбавителя, но для достижения достаточного образования гранул посредством сухого гранулирования потребляется большое количество лактозы, следовательно, получают больший размер таблеток. Обнаружено, что микрокристаллическая целлюлоза в комбинации с безводным двухосновным фосфатом кальция давали многообещающие результаты в отношении хороших свойств уплотняемости с более низким процентным содержанием в композиции, и получали таблетки в пределах намеченной массы с достаточной твердостью и истираемостью и без прилипания к пуансонам. Avicel РН101 и Avicel DG используют для нескольких испытаний, и способность к повторному уплотнению сорта DG была значительно лучше, чем сорта РН101, например, для конечных таблеток с Avicel DG получают более высокие значения твердости и желательные профили растворимости. Известно, что Avicel DG представляет собой комбинацию 75% микрокристаллической целлюлозы и 25% безводного двухосновного фосфата кальция и, как отмечают, является полезным для осуществления задач настоящего изобретения как в отношении метформина, так и его комбинации с ингибиторами DPP-4.
Новый способ по настоящему изобретению может также включать одно или более чем одно связующее вещество, подлежащее применению в способе сухого гранулирования. Примеры связующих веществ включают гидроксипропилцеллюлозу (НРС), гидроксипропилметилцеллюлозу (НМРС), гидроксиэтилцеллюлозу, крахмал 1500, поливинилпирролидон (повидон) и коповидон. Предпочтительное связующее вещество представляет собой гидроксипропилцеллюлозу (НРС). Связующие вещества могут находиться в количестве от 1 до 10 мас.%, более предпочтительно от 3 до 5 мас.% от общей массы композиции.
Согласно еще одному воплощению способ по настоящему изобретению может также включать разрыхлитель. Разрыхлитель может представлять собой один или более чем один из модифицированных видов крахмала, модифицированных полимеров целлюлозы или поликарбоновых кислот, таких как поперечно сшитая гидроксиметилцеллюлоза натрия, натрия крахмал гликолят, полакрилин калия, кроскармеллоза натрия и гидроксиметилцеллюлоза кальция (HMC-Ca). Разрыхлитель предпочтительно представляет собой кроскармеллозу натрия и может находиться в количестве от 0,1 до 5 мас.%, более предпочтительно от 0,5 до 2 мас.% от общей массы композиции.
Способ по настоящему изобретению может также включать одно или более чем одно смазывающее вещество и/или скользяще вещество, которые выбраны из группы стеарата магния, стеарата кальция, стеариновой кислоты, стеарилфумарата натрия, гидрогенизированного касторового масла, талька, фумаровой кислоты, видов крахмала и их смеси. Предпочтительным смазывающим веществом является стеарат магния или стеарилфумарат натрия или их смесь. Примеры скользящих веществ включают коллоидный диоксид кремния, фосфат кальция, силикат магния и тальк. Смазывающие вещества и скользящие вещества могут присутствовать в количестве от 0,1 до 5 мас.%, более предпочтительно от 0,5 до 2 мас.% от общей массы композиции. Как упомянуто выше, композиции по настоящему изобретению не имеют недостатков смазывающих веществ, наблюдаемых в традиционных композициях.
Способ по изобретению может дополнительно включать поверхностно-активные вещества или увлажнители. Поверхностно-активное вещество может быть анионными, катионными или нейтральными. Анионные поверхностно-активные вещества включают лаурилсульфат натрия, додекансульфонат натрия, олеилсульфат натрия и лаурат натрия, смешанный со стеаратами и тальком. Катионные поверхностно-активные вещества включают бензалкония хлориды и бромиды алкилтриметиламмония. Нейтральные поверхностно-активные вещества включают глицерил моноолеат, полиоксиэтиленовый дегидрированный сложный эфир сорбита и жирной кислоты, поливиниловый спирт и дегидрированный сложный эфир сорбита.
В предпочтительных воплощениях настоящего изобретения метформин может быть включен в способ сухого гранулирования в форме его соли HCl и присутствует в количестве от 60 до 98 мас.%, более предпочтительно от 70 до 80 мас.% от общей массы композиции. Ингибитор DPP-4 также присутствует в количестве от 1 до 6 мас.%, более предпочтительно от 4 до 5 мас.% от общей массы композиции.
Новый способ по настоящему изобретению обеспечивает хорошую прессуемость ингредиентов в комбинациях, даже в высококонцентрированных лекарственных средствах, содержащих избыточное количество активного вещества, как описано выше. В предпочтительных воплощениях разбавители включают 75% МСС + 25% DCPA, например Avicel DG, для более эффективного решения проблем стабильности композиции и облегчения ее же обработки.
Изобретение ниже в данном документе будет дополнительно определено со ссылкой на конкретные примеры.
Пример I
Получение пероральных таблеток, содержащих метформин HCl и вилдаглиптин
Получение порошковой смеси
Метформин HCl просеивали через сито 850 мкм, также Вилдаглиптин, Avicel DG и НРС просеивали через сито 500 мкм. Затем коллоидный безводный диоксид кремния взвешивали на другие ингредиенты и смешивали. Порошковую смесь затем просеивали через сито 850 мкм и перемешивали.
Комкование
Порошковую смесь прессуют в 900 мг брусочные таблетки с твердостью 50 H. Брусочные таблетки просеивают через сито frewitt 1,0 мм. Кроскармеллозу натрия добавляют и перемешивают и к гранулам добавляют стеарат магния, в то время как конечную смесь продолжают перемешивать.
Таблетирование
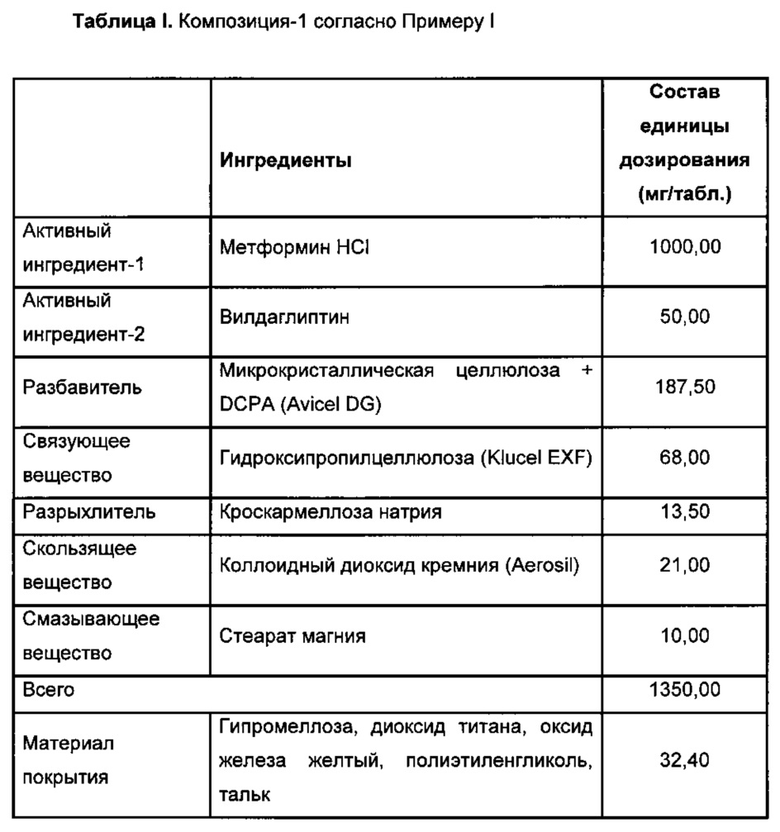
Конечную смесь затем прессовали в таблетки в ротационной машине для таблетирования. В то время как твердость таблеток составляла около 200 H, распадаемость составляла около 16 мин. Таблетки, полученные указанным выше способом, имели следующий состав.
Пленочная оболочка
Получают 15% дисперсию материала покрытия и ядра покрывают до получения увеличения массы приблизительно на 2-3%.
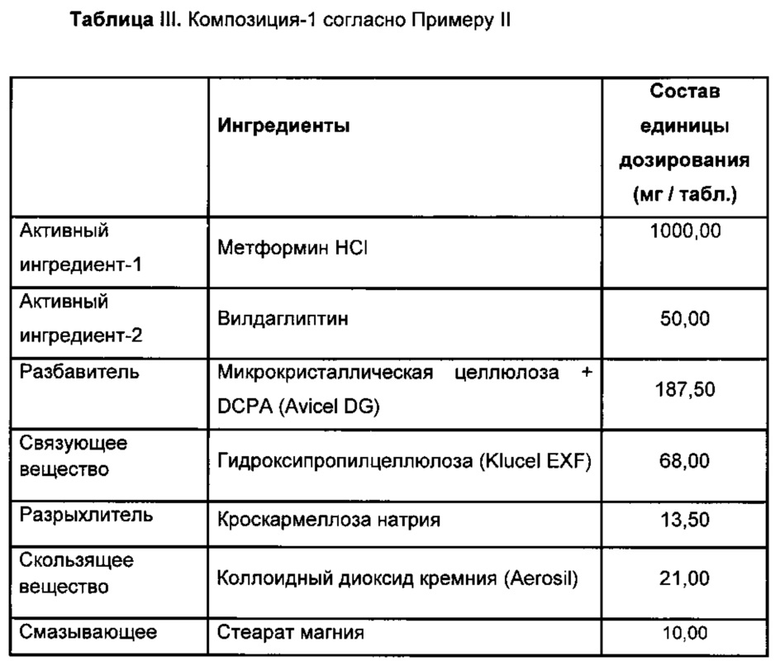
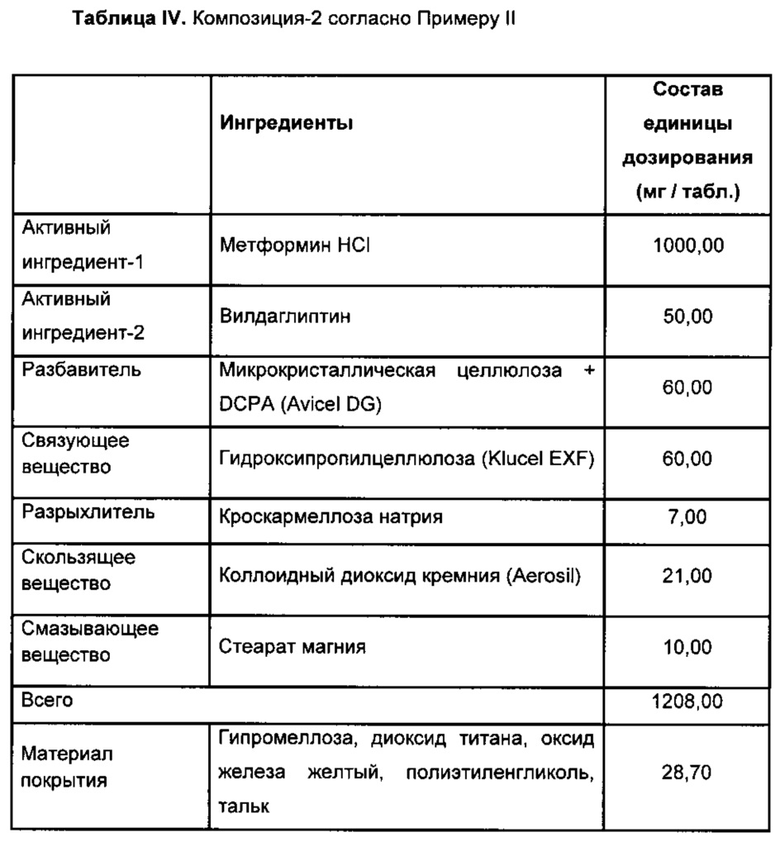
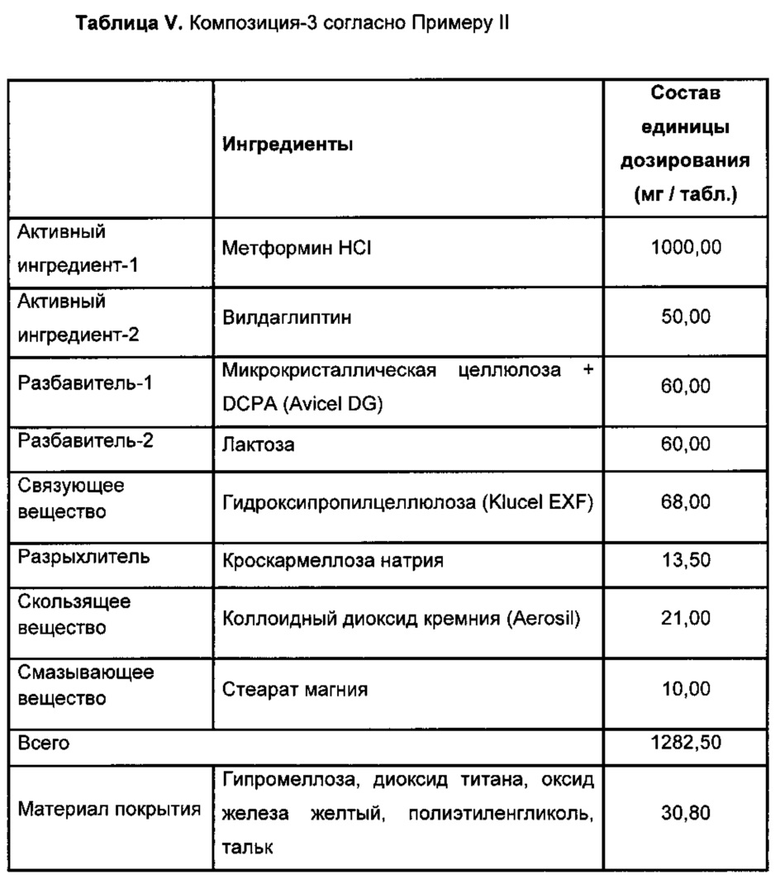
Пример II
Получение пероральных таблеток, содержащих метформин HCI и Вилдаглиптин
Получение порошковой смеси
Метформин HCI просеивали через сито 850 мкм, также Вилдаглиптин, Avicel DG и НРС просеивали через сито 500 мкм. Затем коллоидный безводный диоксид кремния, кроскамеллозу натрия взвешивали на другие ингредиенты и смешивали. Порошковую смесь затем просеивали через сито 850 мкм и перемешивали.
Уплотнение
Порошковую смесь вальцевали в соответствии с гидравлической системой 10 мПа (100 бар), винтовым питателем 40 об/мин, роликовым блоком качения 7 об/мин, тонким гранулятором 25 об/мин, расстоянием между роликами 1,0 мм с использованием сита 1,0 мм.
Таблетирование
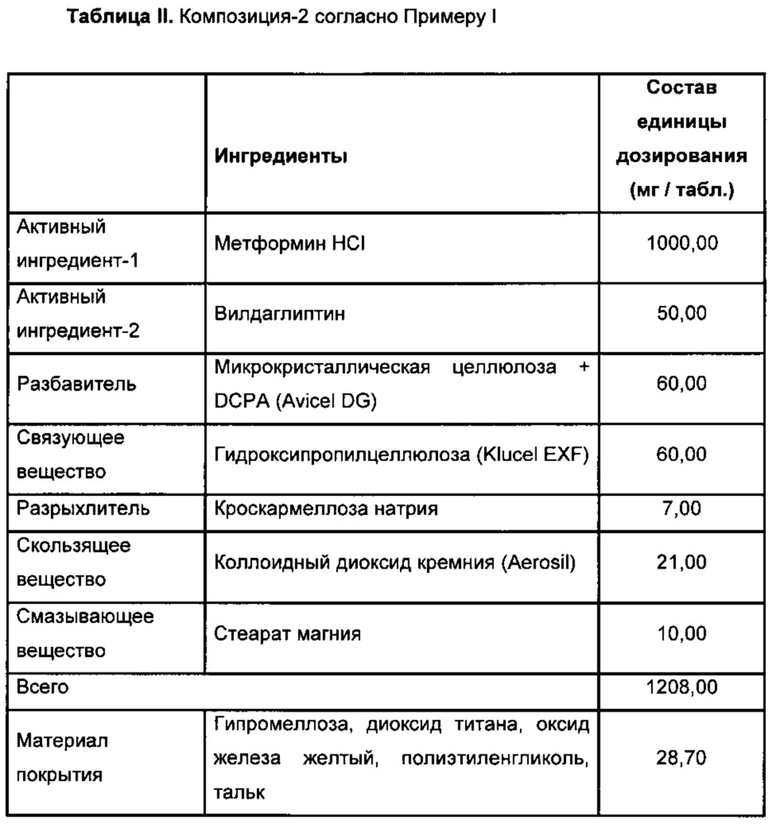
Конечную смесь затем прессовали в таблетки в ротационной машине для таблетирования. В то время как твердость таблеток составляла около 200 Н, распадаемость составляла около 16 мин. Таблетки, полученные указанным выше способом, имели следующий состав.
Пленочная оболочка
Получают 15% дисперсию материала покрытия, и ядра покрывают до получения увеличения массы приблизительно на 2-3%.

Пример III (Сравнительные испытания)
Композиции с разными количествами эксципиентов получали для оценки эффекта каждого разбавителя на сыпучесть, истираемость, твердость и прессуемость получаемых таблеток. Состав композиций указан ниже в Таблице VI.
Как отмечено, композиции 1, 4 и 5 получали с разными количествами Avicel DG, в то время как композиции 2 и 3 получали с лактозой и DCPA, соответственно.
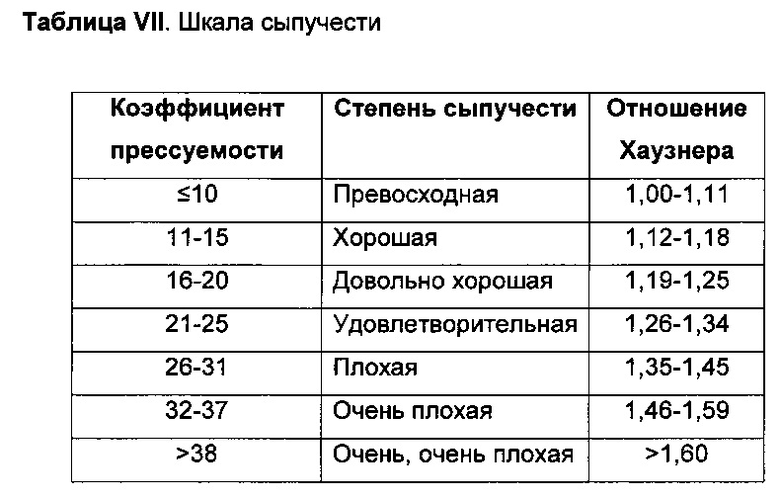
Сыпучесть и истираемость прессованных таблеток, полученных с помощью данных композиций, определяют в соответствии с отношением Хаузнера, которое соответствует отношению насыпной плотности к объемной плотности. В таблице VII, приведенной ниже, показана шкала сыпучести в зависимости от значения отношения Хаузнера.
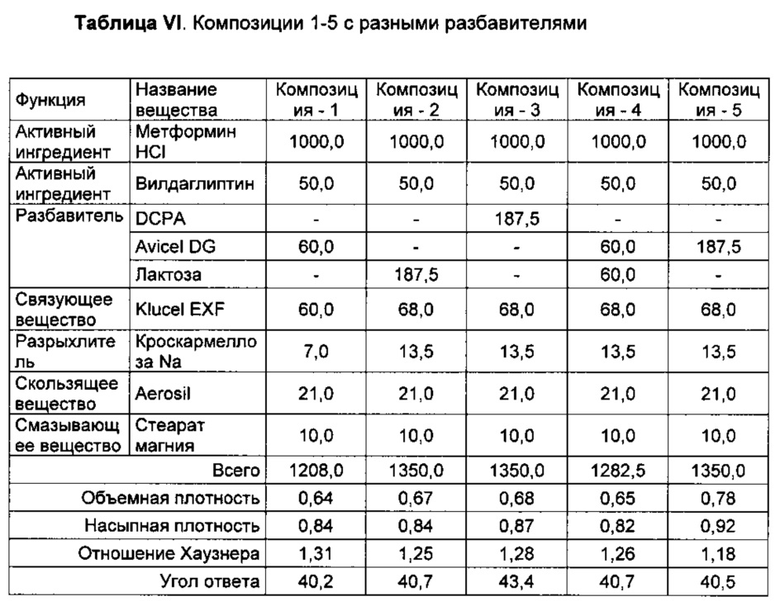
Согласно таблице VI наилучшие результаты получали с композицией -5, в которой содержится относительно более высокое количество Avicel DG. Примечательно, что композиция-2 и композиция-3, имеющие такое же количество лактозы и безводного двухосновного фосфата кальция соответственно, вместо Avicel DG, имели явно более низкие характеристики сыпучести, по сравнению с композицей-5.
Также неожиданно отметили, что Avicel DG улучшает истираемость и прессуемость композиций. Несмотря на то, что более низкие количества Avicel DG вызывают более низкую сыпучесть, авторы изобретения сообщают о том, что истираемость и свойства таблетирования композиций 1 и 4 были все еще приемлемыми, несмотря на тот факт, что стеарат магния, который, как известно, является неблагоприятным по отношению к истираемости, включен во все композиции.
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЙ СОСТАВ | 2006 |
|
RU2483716C2 |
| НОВЫЙ СОСТАВ | 2006 |
|
RU2821230C2 |
| КОМПОЗИЦИЯ И СПОСОБ ПРЯМОГО ПРЕССОВАНИЯ | 2005 |
|
RU2391097C2 |
| КОМПОЗИЦИЯ И СПОСОБ ПРЯМОГО ПРЕССОВАНИЯ | 2005 |
|
RU2766487C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ДИАБЕТА 2 ТИПА | 2010 |
|
RU2533560C2 |
| ТВЕРДАЯ ДОЗИРОВАННАЯ ЛЕКАРСТВЕННАЯ ФОРМА ДЛЯ ОРАЛЬНОГО ВВЕДЕНИЯ, СОДЕРЖАЩАЯ КОМБИНАЦИЮ ВИЛДАГЛИПТИНА И ГЛИКВИДОНА | 2014 |
|
RU2585378C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМБИНАЦИЯ, КОМПОЗИЦИЯ И КОМБИНИРОВАННЫЙ СОСТАВ, СОДЕРЖАЩИЙ АКТИВАТОР ГЛЮКОКИНАЗЫ И ИНГИБИТОР DPP-IV, И СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ И ПРИМЕНЕНИЯ | 2019 |
|
RU2770775C1 |
| ТВЕРДЫЕ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ИНГИБИТОР ИНТЕГРАЗЫ | 2010 |
|
RU2602865C2 |
| ЭКСТРУЗИОННЫЙ СПОСОБ ПРИГОТОВЛЕНИЯ КОМПОЗИЦИЙ, СОДЕРЖАЩИХ ПЛОХО ПРЕССУЮЩИЕСЯ ЛЕКАРСТВЕННЫЕ СОЕДИНЕНИЯ | 2006 |
|
RU2405539C2 |
| Твёрдые лекарственные формы палбоциклиба | 2016 |
|
RU2686840C1 |
Настоящее изобретение относится к новому способу сухого гранулирования для получения композиций метформина в виде таблеток, а также к его комбинации с ингибиторами DPP-4. Способ включает применение в качестве разбавителя фармацевтической композиции метформина смеси микрокристаллической целлюлозы (MCC) и безводного двухосновного фосфата кальция (DCPA). Количество метформина в композиции составляет от 60 до 80 мас.%. Отношение метформина к указанному разбавителю составляет от 2,5 до 25 по массе. В качестве ингибитора дипептидилпептидазы-4 композиция содержит вилдаглиптин. Способ по настоящему изобретению обеспечивает хорошую прессуемость ингредиентов в высококонцентрированных лекарственных средствах, удовлетворительные характеристики сыпучести и истираемости прессованных таблеток. 2 н. и 15 з.п. ф-лы, 7 табл., 3 пр.
1. Способ получения фармацевтической композиции метформина в виде таблеток, включающий сухое гранулирование активного вещества с разбавителем, который представляет собой смесь микрокристаллической целлюлозы и безводного двухосновного фосфата кальция, и связующим веществом, при этом количество метформина составляет от 60 до 80 мас.% от общей массы композиции и отношение метформина к разбавителю составляет от 2,5 до 25 по массе.
2. Способ по п. 1, дополнительно включающий добавление к композиции ингибитора дипептидилпептидазы-4 (DPP-4), который выбирают из группы, состоящей из ситаглиптина, вилдаглиптина и саксаглиптина, с получением комбинации метформина и указанного ингибитора DPP-4.
3. Способ по п. 2, отличающийся тем, что ингибитор DPP-4 представляет собой вилдаглиптин.
4. Способ по п. 1, отличающийся тем, что смесь микрокристаллической целлюлозы и безводного двухосновного фосфата кальция представляет собой Avicel DG.
5. Фармацевтическая композиция в виде таблетки, содержащая гранулы метформина, полученные в результате сухого гранулирования по п. 1, включающие разбавитель, который представляет собой смесь микрокристаллической целлюлозы и безводного двухосновного фосфата кальция, и связующее вещество, при этом количество метформина составляет от 60 до 80 мас.% от общей массы композиции и отношение метформина к разбавителю составляет от 2,5 до 25 по массе.
6. Композиция по п. 5, дополнительно содержащая ингибитор DPP-4, который выбирают из группы, состоящей из ситаглиптина, вилдаглиптина и саксаглиптина.
7. Композиция по п. 6, отличающаяся тем, что ингибитор DPP-4 представляет собой вилдаглиптин.
8. Композиция по п. 5, отличающаяся тем, что смесь микрокристаллической целлюлозы и безводного двухосновного фосфата кальция представляет собой Avicel DG.
9. Композиция по п. 5, дополнительно содержащая один или более чем один эксципиент, выбранный из группы дополнительных разбавителей, связующих веществ, разрыхлителей, смазывающих веществ и скользящих веществ.
10. Композиция по п. 9, отличающаяся тем, что дополнительный разбавитель выбирают из группы, состоящей из маннита, лактозы, сорбита, водного двухосновного фосфата кальция и целлюлозы в порошке.
11. Композиция по п. 5 или 9, отличающаяся тем, что общее количество разбавителей, добавляемое к композиции, составляет от 10 до 25 мас.% от общей массы композиции.
12. Композиция по п. 9, отличающаяся тем, что связующее вещество выбирают из группы гидроксипропилцеллюлозы, гидроксипропилметилцеллюлозы, гидроксиэтилцеллюлозы, крахмала, поливинилпирролидона и коповидона.
13. Композиция по п. 9, отличающаяся тем, что разрыхлитель выбирают из группы модифицированных крахмалов, модифицированных полимеров целлюлозы, поперечно-сшитой гидроксиметилцеллюлозы натрия, натрия крахмал гликолята, полакрилина калия, кроскармеллозы натрия и гидроксиметилцеллюлозы кальция.
14. Композиция по п. 9, отличающаяся тем, что смазывающее вещество и скользящее вещество выбирают из группы стеарата магния, стеарата кальция, стеариновой кислоты, стеарилфумарата натрия, гидрогенизированного касторового масла, талька, коллоидного диоксида кремния, фумаровой кислоты, крахмалов и их смесей.
15. Композиция по п. 6, отличающаяся тем, что количество ингибитора DPP-4 составляет от 1 до 6 мас.% от общей массы композиции.
16. Композиция по п. 5, отличающаяся тем, что смесь композиции содержит следующие ингредиенты, в мас.% от общей массы композиции:
70-80 мас.% метформина HCl;
4-5 мас.% вилдаглиптина;
10-20 мас.% разбавителя;
3-5 мас.% связующего вещества;
0,5-2 мас.% разрыхлителя;
0,5-2 мас.% смазывающего вещества;
0,5-2 мас.% скользящего вещества.
17. Композиция по п. 7, содержащая активные ингредиенты в количествах, соответствующих одной из величин дозировки 500 мг, 850 мг, 1000 мг метформина и 25 мг, 50 мг и 100 мг вилдаглиптина в виде свободных оснований.
| EP 1948149 B1, 16.11.2011 | |||
| Колосоуборка | 1923 |
|
SU2009A1 |
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| ГРАНУЛЫ, ТАБЛЕТКИ И ГРАНУЛИРОВАНИЕ | 2007 |
|
RU2441696C2 |
Авторы
Даты
2018-03-15—Публикация
2013-12-17—Подача