Изобретение относится к способу получения ацетиленидов олова общей формулы
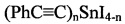
где n=1-4.
Ацетилениды олова находят широкое применение в органическом синтезе. В частности, тетраацелинелиды олова и йодацетилениды олова могут быть использованы для синтеза диарилацетиленов [Levashov A.S. et al. Tetraalkynylstannanes in the Stille cross coupling reaction: a new effective approach to arylalkynes // New J. Chem. 2017. Vol. 41. P. 2910-2918].
Известны способы получения ацетиленидов олова взаимодействием галогенидов олова с ацетиленидами активных металлов (лития, натрия или магния) [Pant B.C., Reiff H.F. Organometallic acetylenes of group iva elements. Synthesis and spectral data of tetrakis(tert-Butylethynyl) derivatives // J. Organomet. Chem. 1968. Vol. 15, №LP. 65-68; Hartbaum C, Roth G., Fischer H. Polynuclear Complexes with Propynylidene C3 -Bridges: General Synthetic Route to Bis-, Tris-, and Tetrakis (ethynylcarbene) Complexes // Eur. J. Inorg. Chem. 1998. Vol. 1998, №2. P. 191-202; Hartmann H., Ahrens J.U. Uber Germanium-acetylen-Verbindungen // Angew. Chemie. WILEY-VCH Verlag GmbH, 1958. Vol. 70, №3. P. 75-75]. Недостатком данных способов является сложность получения исходных ацетиленидов металлов, а также их высокая активность, что затрудняет работу с ними.
Известен способ получения ацетиленидов олова взаимодействием галогенидов олова с 1-алкинами в присутствии хлорида цинка и амина [патент РФ №2317993, МПК C07F 7/22, Левашов А.С., Андреев А.А., Комаров Н.В. Способ получения три- и тетраорганилалкинилолова, заявка №2006126447/04 заявл. 20.07.2006 Россия. Опубликовано 27.02.2008, Бюл. №6]. Недостатком данного способа является использование легкогидролизуемого тетрахлорида олова.
В промышленности оловоорганические соединения наиболее часто получают взаимодействием алкилгалогенидов с металлическим оловом или его сплавами. Например, известен способ получения оловоалкилгалоидных соединений взаимодействиtv оловянно-магниевого сплава (71% Sn и 29% Mg) с парами галоидного алкила, в присутствии инертного разбавителя (пары циклогексана или ксилола) и каталитических количеств уксуснокислой ртути при температуре 170-300°С. При этом, разбавление паров галоидного алкила парами инертного растворителя дает возможность повысить выход оловоалкилгалоидных соединений до 47% и снизить количество диалкилоловодигалогенида (тетраалкилолово в этом случае не образуется), который представляет меньший интерес, чем триалкилоловогалогенид [а.с. №137519, Способ получения оловоалкилгалоидных соединений. Лайне Л.В, Шостаковский М.Ф., Котрелев В.Н., Калинина С.П., Кузнецова Г.И, Борисова А.И. - заявл. 24.08.1960. - БИ №8 за 1961 г.].
Известен способ получения тетраалкилолова взаимодействием порошков олова и магния с алкилхлоридами в присутствии йодида тетрабутиламмония при температуре 160-170°С [Nicholson J.W., Douek J.A. A new route to tetraorganotin compounds // J. Organomet. Chem. 1982. Vol. 233. P. 169-172].
Известен способ получения тетраалкилолова и триалкилхлоролова взаимодействием сплава олова с натрием, содержащим 2% цинка, с алкилхлоридом при температуре 160-170°C с общим выходом 25-30% [Zietz J.R. et al. Synthesis of Higher Alkyltin Compounds from Sodium-Tin Alloys // J. Org. Chem. 1957. Vol. 22. P. 60-62].
Наиболее близким аналогом к предлагаемому техническому решению является способ получения оловоорганических соединений взаимодействием алкилгалогенидов со сплавом олова, содержащим 4-5% меди в органическом растворителе при температуре 160°С в течение 12 часов с выходами до 72% [Zakharkin L.I., Okhlobystin O.Y. The synthesis of organotin compounds from alkyl halies and metallic tin in solvating solvents // Russ. Chem. Bull. 1963. Vol. 12, №12. P. 2027-2029]. В качестве органического растворителя используют диметиловой эфир диэтиленгликоля. Использование других растворителей приводит к резкому снижению выхода или полному отсутствию взаимодействия. Недостатком данного метода является использование высококипящего растворителя, что вызывает сложности при очистке полученных веществ.
Следует отметить, что несмотря на большое количество способов получения оловоорганических соединений прямым синтезом (т.е. взаимодействием металлического олова или его сплавов) и их промышленное применение, до настоящего времени не известны способы получения ацетиленидов олова прямым синтезом.
Техническим результатом предлагаемого способа является получение ацетиленидов олова, снижение температуры взаимодействия, сокращение времени получения конечного продукта и повышение его выхода.
Для достижения технического результата предлагается проводить взаимодействие сплава олова, содержащего 1,5% цинка с 2-йод-1-фенилацетиленом при температуре 130-145°С в среде ароматического или эфирного растворителя в течение 5-8 часов. Взаимодействие протекает по схеме:
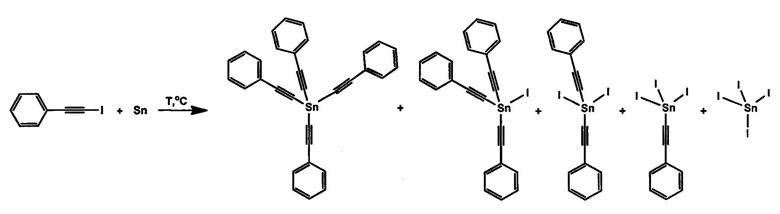
При этом происходит образование тетра(фенилэтинил)олова, трис(фенилэтинил)йодолова, ди(фенилэтинил)дийодолова, фенилэтинилтрийодолова и тетрайодида олова. Тетрайодид олова отделяют фильтрованием, растворитель упаривают в вакууме. Выход ацетиленидов олова составляет 45-85%.
Пример 1. Взаимодействие 2-йод-1-фенилацетилена со сплавом олова, содержащим 1,5% цинка
В ампулу помещают навеску порошка сплава олова с цинком массой 0,1360 г (1,14 моль) и 2-йод-1-фенилацетилен массой 0,5235 г (2,3 ммоль) в 5 мл ксилола. Ампулу запаивают. Реакционную смесь нагревают в ампуле при температуре 145°С в течение 8 часов. Тетрайодид олова отфильтровывают. По результатам анализа методом спектроскопии 119Sn ЯМР в растворе присутствует тетра(фенилэтинил)олово (-332,0 м.д.), трис(фенилэтинил)йодолово (-472,9 м.д.), ди(фенилэтинил)дийодолово (-743,5 м.д.), фенилэтинилтрийодолово (-1177,5 м.д.). Полученный раствор упаривают, суммарный выход оловоацетиленов составил 85%.
Пример 2. Взаимодействие 2-йод-1-фенилацетилена со сплавом олова, содержащим 1,5% цинка
В ампулу помещают навеску порошка сплава олова с цинком массой 0,1360 г (1,14 моль) и 2-йод-1-фенилацетилен массой 0,5235 г (2,3 ммоль) в 5 мл диоксана. Ампулу запаивают. Реакционную смесь нагревают в ампуле при температуре 130°С в течение 8 часов. Тетрайодид олова отфильтровывают. По результатам анализа методом спектроскопии 119Sn ЯМР в растворе присутствует тетра(фенилэтинил)олово (-332,0 м.д.), трис(фенилэтинил)йодолово (-472,9 м.д.), ди(фенилэтинил)дийодолово (-743,5 м.д.), фенилэтинилтрийодолово (-1177,5 м.д.). Полученный раствор упаривают, суммарный выход оловоацетиленов составил 45%.
Пример. 3 Взаимодействие 2-йод-1-фенилацетилена со сплавом олова, содержащим 1,5% цинка
В ампулу помещают навеску порошка сплава олова с цинком массой 0,1360 г (1,14 моль) и 2-йод-1-фенилацетилен массой 0,5235 г (2,3 ммоль) в 5 мл толуола. Ампулу запаивают. Реакционную смесь нагревают в ампуле при температуре 130°С в течение 5 часов. Тетрайодид олова отфильтровывают. По результатам анализа методом спектроскопии 119Sn ЯМР в растворе присутствует тетра(фенилэтинил)олово (-332,0 м.д.), трис(фенилэтинил)йодолово (-472,9 м.д.), ди(фенилэтинил)дийодолово (-743,5 м.д.), фенилэтинилтрийодолово (-1177,5 м.д.). Полученный раствор упаривают, суммарный выход оловоацетиленов составил 66%.
Пример 4. Взаимодействие 2-йод-1-фенилацетилена со сплавом олова, содержащим 1,5% цинка
В ампулу помещают навеску порошка сплава олова с цинком массой 0,1360 г (1,14 моль) и 2-йод-1-фенилацетилен массой 0,5235 г (2,3 ммоль) в 5 мл ксилола. Ампулу запаивают. Реакционную смесь нагревают в ампуле при температуре 140°С в течение 8 часов. Тетрайодид олова отфильтровывают. По результатам анализа методом спектроскопии 119Sn ЯМР в растворе присутствует тетра(фенилэтинил)олово (-332,0 м.д.), трис(фенилэтинил)йодолово (-472,9 м.д.), ди(фенилэтинил)дийодолово (-743,5 м.д.), фенилэтинилтрийодолово (-1177,5 м.д.). Полученный раствор упаривают, суммарный выход оловоацетиленов составил 78%.
Пример 5. Взаимодействие 2-йод-1-фенилацетилена с оловом, не содержащим цинк
В ампулу помещают навеску порошка олова массой 0,1360 г (1,14 моль) и 2-йод-1-фенилацетилен массой 0,5235 г (2,3 ммоль) в 5 мл толуола. Ампулу запаивают. Реакционную смесь нагревают в ампуле при температуре 130°С в течение 150 часов. Тетрайодид олова отфильтровывают. По результатам анализа методом спектроскопии 119Sn ЯМР в растворе присутствует тетра(фенилэтинил)олово (-332,0 м.д.), трис(фенилэтинил)йодолово (-472,9 м.д.), ди(фенилэтинил)дийодолово (-743,5 м.д.), фенилэтинилтрийодолово (-1177,5 м.д.). Полученный раствор упаривают, суммарный выход оловоацетиленов составил 23%.
Как видно из приведенных примеров, реакция протекает в ароматических и эфирных растворителях при температуре 130-145°С. При использовании металлического олова без добавки цинка реакция протекает гораздо медленнее и выход продуктов значительно снижается (пример 5).
Предлагаемый способ является новым, условия протекания реакции обеспечивают снижение температуры взаимодействия, сокращение времени получения конечного продукта и повышение его выхода. Таким образом, заявляемый способ удовлетворяет критерию изобретательский уровень, т.е. заявляемый способ является охраноспособным.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ТРИ- И ТЕТРАОРГАНИЛАЛКИНИЛОЛОВА | 2006 |
|
RU2317993C1 |
| СПОСОБ ПОЛУЧЕНИЯ АЦЕТИЛЕНОВЫХ КЕТОНОВ | 2017 |
|
RU2641697C1 |
| Способ получения комплексных ацетиленидов галлия | 1978 |
|
SU767111A1 |
| Способ получения органооловоацетиленов | 1979 |
|
SU825533A1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИАЛКОКСИДОВ ДИАЛКИЛОЛОВА | 2007 |
|
RU2414474C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-АЛКИНИЛАДАМАНТАНОВ | 2012 |
|
RU2507189C1 |
| СПОСОБ ПОЛУЧЕНИЯ АРОМАТИЧЕСКИХ АЦЕТИЛЕНОВЫХ КЕТОНОВ | 2017 |
|
RU2638839C1 |
| Способ получения иодацетиленовых соединений | 1990 |
|
SU1712350A1 |
| Способ получения полимеров паразамещенных фенилацетиленов | 2021 |
|
RU2796111C1 |
| Бис(N,N-диэтилкарбамат) олова, способ его получения и изготовление пленок оксида олова на его основе | 2020 |
|
RU2762687C1 |
Изобретение относится к способу получения ацетиленидов олова общей формулы (PhC≡C)nSnI4-n, где n=1-4. Способ включает взаимодействие сплава олова с йодпроизводным в среде органического растворителя при нагревании, при этом используют сплав олова с 1,5% цинка. В качестве йодпроизводного используют 2-йод-1-фенилацетилен. Взаимодействие проводят в среде ароматического или эфирного растворителя в течение 5-8 часов при температуре 130-145°C. Изобретение позволяет снизить температуру взаимодействия, сократить время получения конечного продукта и повысить его выход. 5 пр.
Способ получения ацетиленидов олова общей формулы
(PhC≡C)nSnI4-n
где n=1-4,
включающий взаимодействие сплава олова с йодпроизводным в среде органического растворителя при нагревании, отличающийся тем, что используют сплав олова с 1,5% цинка, в качестве йодпроизводного используют 2-йод-1-фенилацетилен, взаимодействие проводят в среде ароматического или эфирного растворителя в течение 5-8 часов при температуре 130-145°C.
| ZAKHARKIN L.I | |||
| et al., The synthesis of organotin compounds from alkyl halies and metallic tin in solvating solvents, Russ | |||
| Chem | |||
| Bull., 1963, v | |||
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| Способ выделения и очищения сульфокислот углеводородных масел | 1924 |
|
SU2027A1 |
| СПОСОБ ПОЛУЧЕНИЯ ТРИ- И ТЕТРАОРГАНИЛАЛКИНИЛОЛОВА | 2006 |
|
RU2317993C1 |
| WRACKMEYER B | |||
| et al., Exchange Reaktions between 1-Alkynyltin Compounds, Studied by 13 C, 29 Si and 119 Sn NMR Multinuclear NMR of Tetrakis(trimethylsilylethynyl)lead and the Crystal Structures of two Tetra-1-alkynyltin Compounds, Main Group Met | |||
| Chem., 1993, v | |||
| Устройство для электрической сигнализации | 1918 |
|
SU16A1 |
| ПРИСПОСОБЛЕНИЕ ДЛЯ АВТОМАТИЧЕСКОЙ БОКОВОЙ СТАБИЛИЗАЦИИ | 1921 |
|
SU445A1 |
Авторы
Даты
2018-03-30—Публикация
2017-06-20—Подача