Область техники, к которой относится изобретение
Настоящее изобретение относится к области медицинских препаратов, применяемых орально для предотвращения туберкулеза. В частности, для задерживания перехода латентной инфекции в активную инфекцию указанной болезни.
Предшествующий уровень техники
Туберкулез - это хроническая инфекционная болезнь, вызванная бактериями, относящимися к группе Micobacterium tuberculosis-complex (MTB-C), в настоящее время включающей бациллы M. tuberculosis, M. bovis, M. microti и M. africanum, M. tuberculosis, являющийся наиболее важным и типичным представителем, что касается туберкулеза человека. Указанная болезнь в первую очередь поражает легкие, хотя в некоторых случаях она может также распространяться в другие органы. Туберкулез может быть фатальным, если не будет подвергаться подходящему лечению.
Согласно отчету за 2011 год Всемирной организации здравоохранения, каждый год в мире регистрируется 9 миллионов новых случаев обнаружения заболевания у людей и сообщается о, примерно, 1,7 миллионов смертей. Также считается, что в мире существует около 2,500 миллионов инфицированных человек и около 100 миллионов новых инфицированных появляется каждый год.
Туберкулез передается по воздуху, так что пациенты с туберкулезной каверной в их легких являются основным источником передачи этой болезни, как описано, например, в J. Grosset, Studies in short-course chemotherapy for tuberculosis. Basis for short-course chemotherapy, Chest, 1981, 80, 719-720, и в J. Grosset Mycobacterium tuberculosis in the Extracellular Compartment: an Underestimated Adversary, Antimicrob. Agents Chemother., 2003, 47, 833-836.
Как описано в указанных работах, пациенты высвобождают путем кашлянья или чихания большое количество микро капель, которые могут переносить бациллы, которые могут входить в альвеолярное пространство человека, который их вдыхает.
После вдыхания бациллы подвергаются фагоцитозу альвеолярными макрофагами и внутри этой клетки бациллы могут расти до количества, вызывающего разрушение клетки. Бациллы подвергаются снова фагоцитозу в межклеточном пространстве новыми макрофагами, и этот процесс повторяется до тех пор, пока однажды они не исчерпываются, и инфекция образуется в прикорневых лимфатических узлах, образуется иммунный ответ, основанный на клеточном иммунитете.
Через примерно 6 недель после инфицирования рост бацилл прекращается, хозяин дает положительный кожный тест на туберкулез, характеризующийся реакцией гиперчувствительности замедленного типа (DTH), и в точках инфекции образуется, так называемый, казеозный некроз.
Одной из основных характеристик инфекции туберкулеза является тот факт, что M. tuberculosis способен оставаться в ткани хозяина годы в форме «латентной» туберкулезной инфекции без развития болезни, но сохраняя свою способность порождать активный туберкулез.
Это латентное состояние инфекции связано с началом, так называемого, казеозного некроза, который образуется в первичных альвеолярных поражениях и в окружающей ткани легких, приводя к разрушению макрофагов, содержащих бациллы, которые размножаются, приводя к плотному некротическому поражению.
Природа этой некротической реакции достоверно не известна, но она связана с реакцией типа DTH. В основном иммунный ответ, который позволяет контролировать популяцию бацилл, является иммунным ответом клеточного типа, руководимым в первую очередь Th1 CD4, то есть он способен вызывать ответ типа DTH и также идентифицировать инфицированные макрофаги и активировать их для разрушения в них бацилл.
Примерно у 10% инфицированных людей, указанный плотный некроз смягчается, что является одним из важных эпизодов в инфекции туберкулеза, так как он происходит тогда, когда инфекция переходит в активный туберкулез, то есть в болезнь туберкулез.
В большинстве случаев смягчение связано с осушением смягченной ткани в направлении бронхиального дерева, образуя туберкулезную каверну и бурный внеклеточный рост бацилл с входом кислорода через отверстие в бронхах. С кашлем этот смягченный казеум, полный бацилл, распространяется в другие части бронхов, легких и вне тела.
Фармакологическое лечение туберкулеза характеризуется как продолжительная терапия, которая осложняет строгое соблюдение лечения, так как в то же время способствует возникновению лекарственной резистентности бактерий.
Считается, что наилучшая стратегия в подавлении туберкулеза основана на превентивном подходе.
Существующая вакцина, которая вводится парентерально, используемая в профилактическом лечении туберкулеза, основана на бактерии штамма, названного BCG (бацилла Кальметта-Герена), ослабленного варианта M. bovis. Однако было замечено, что ее эффективность падает с течением времени, и что она не эффективна в предупреждении болезни у взрослых. В действительности считается, что она защищает только ниши развития фатальной туберкулезной болезни (милиарного туберкулеза или туберкулезного менингита).
Были разработаны другие профилактические лечения туберкулеза, главным образом основанные на других штаммах жизненно ослабленных микобактерий или на бактериальных субъединицах.
Кроме того, профилактические лечения туберкулеза, основные на инактивированных микобактериях, также были изучены в современном состоянии техники с целью получения иммунного ответа, подобного иммунному ответу, полученному с помощью вакцины, основанной на ослабленных микобактериях, то есть, продуцирующих γ-интерферон Th1.
Таким образом, например, статья Opie et al., Protective inoculation against human tuberculosis with heat-killed tubercle bacilli, Am. J. Hyg., 1939, 29, 155-164 описывает клинические испытания, в которых пять доз бацилл M. tuberculosis, инактивированных путем нагревания, вводили внутрикожно с целью создания защиты против болезни.
Также, статья Agger et al., Specific acquired resistance in mice immunized with killed mycobacteria, Scand. J. Immunol., 2002, 56, 443-447 описывает экспериментальное исследование с мышами, вакцинированными тремя введенными подкожно дозами в 1000 мкг бацилл M. tuberculosis, инактивированных нагреванием, с двухнедельным интервалом между каждой дозой, показывая индукцию специфического иммунитета, основанного на Т-клетках.
Другие инактивированные микобактерии были также тестированы на индукцию защиты от туберкулеза, как правило, парентерально.
Например, Gupta et al., Immunogenicity and protective efficacy of “Mycobacterium w” against Mycobacterium tuberculosis in mice Immunized with live versus heat-killed M. w by the aerosol or parenteral route, Infect. Immun., 2009, 77 (1), 223-231 описывают, что вводили живые M. w микобактерии или M. w микобактерии, инактивированные нагреванием. M. w микобактерии, инактивированные нагреванием, вводили подкожно в виде одноразовой дозы и наблюдали иммунный ответ, основанный на индукции Th1 клеток, продуцирующих интерферон.
Чрезвычайно желательно предоставить эффективное профилактическое лечение, применяемое орально, поскольку такой путь применения значительно облегчает применение лекарства и соблюдение лечения.
В этом смысле существуют документы современного состояния техники, которые ссылаются на оральное применение бактерий инактивированных нагреванием микобактерий, Mycobacteriumn vaccae, для обеспечения терапевтического действия на активный туберкулез, в соответствии со схемой лечения, объединенной с лекарствами обычной химиотерапии.
На экспериментальном уровне Hernández-Pando et al., Orally administrated Mycobacterium vaccae modulates expression of immunoregulatory molecules in BALB/mice with pulmonary tuberculosis, Clin. Vaccine Immunol., 2008, 15 (11), 1730-1736, описывают анализ, проведенный на мышах, которым вводили орально 5 доз по 0,1 мкг M. vaccae, инактивированных нагреванием, с 28-дневным интервалом между каждым введением, индуцируя инфицирование M. tuberculosis внутритрахеально через 23 часа после первой дозы. В указанном исследовании было подтверждено, что клеточный иммунный ответ был образован увеличением секреции Th1 клеток, в то время как гуморальный иммунитет упал, как показано уменьшением клеток типа Th2 и фактора роста TGF-бета.
Обычно современное состояние техники предлагает, что желательной является индукция Th1 с последующей продукцией γ интерферона, в то время как Th2 ответ, с последующим производством ИЛ-4, или ответ Th3, который ведет к образованию регуляторных T клеток (Treg), могут производить действие, индуцирующее активный туберкулез.
Это описано, например, у Kursar et al., Cutting Edge: Regulatory T Cells prevent Efficient Clearance of Mycobacterium tuberculosis, J. Immunol., 2007, 178, 2661-2665, где образование регуляторных T клеток (Treg) относят к неспособности CD4 T клеток стерилизовать казеозные поражения и предотвращать латентную инфекцию в мышиной модели экспериментального туберкулеза. Указанная статья предлагает, что разбалансировка, позволяющая дисбаланс между Th1 ответом и Treg ответом в пользу Treg ответа, может быть причиной индукции активного туберкулеза.
Принимая во внимание то, что было описано в современном состоянии техники, продолжает оставаться необходимость предложения эффективного лечения туберкулеза, которое можно проводить орально для предотвращения развития активного туберкулеза и последующего установления патологического состояния болезни как у не инфицированных лиц (профилактическое действие), так и у лиц инфицированных M. tuberculosis, у которых инфекция находится в латентном состоянии (терапевтическое действие).
Цель изобретения
Целью настоящего изобретения является применение инактивированных микобактерий для приготовления медицинского препарата для орального применения для предотвращения туберкулеза.
Описание чертежей
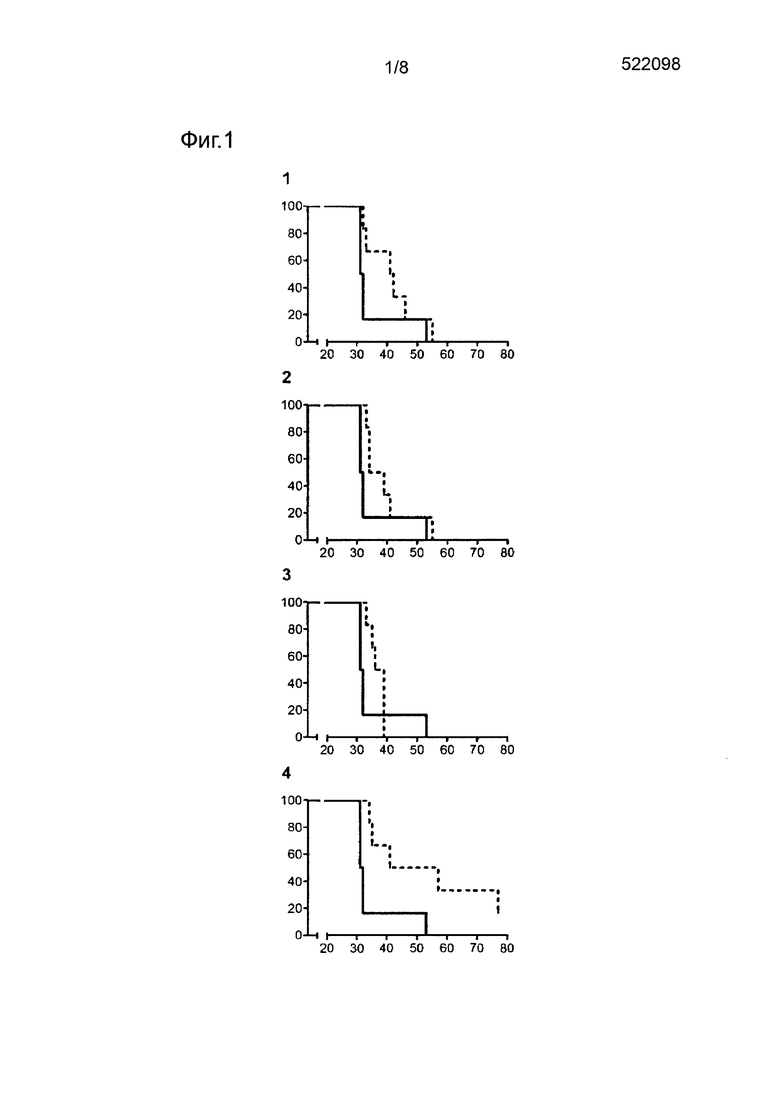
Фигура 1 демонстрирует время выживания, выраженное в днях, представленное на оси X, и процент выживших животных, представленный на оси Y. Контрольная Группа представлена непрерывной линией, а животные Группы 1 представлены прерывистой линией. Животные Группы 1 были подвергнуты оральному лечению инактивированными микобактериями Mycobacterium tuberculosis до инфицирования путем введения 5 доз указанных бацилл, одну каждые 48 часов, начиная за 10 дней до инфицирования. Графики 1, 2, 3 и 4 соответствуют животным Групп 1a, 1b, 1c и 1d соответственно, которым были введены разные количества препарата соответственно в разведениях 1:1, 1:10, 1:100 и 1:1000 (Пример 1).
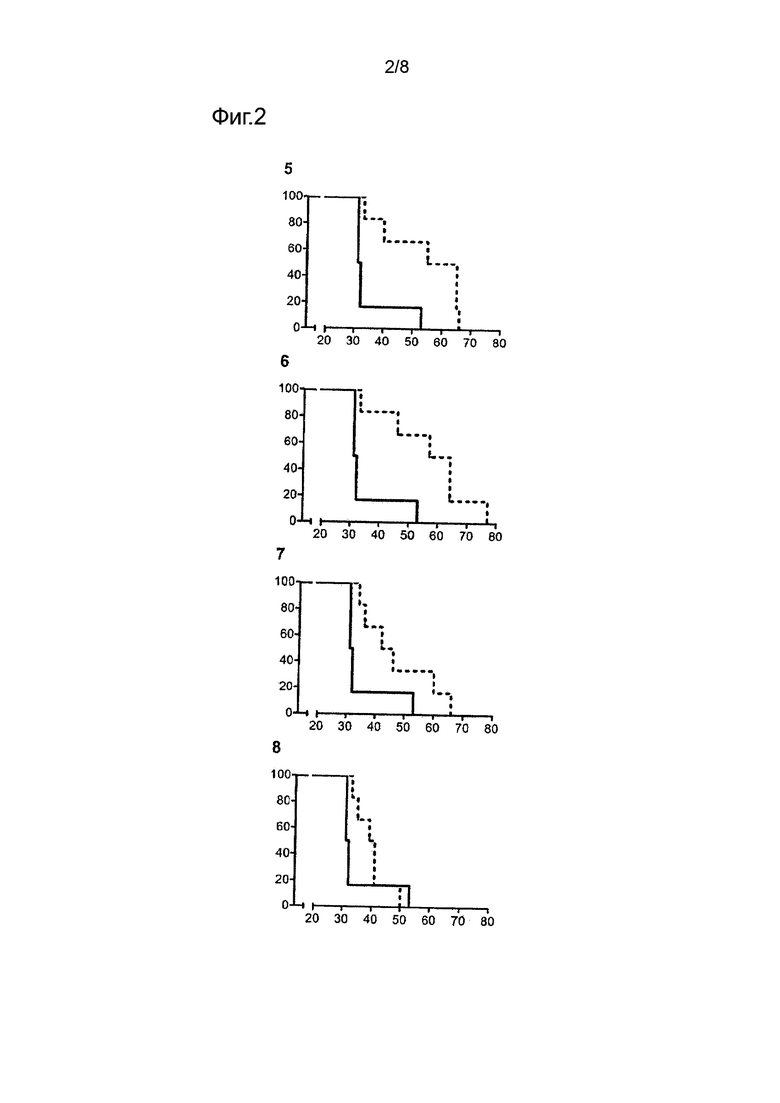
Фигура 2 демонстрирует время выживания, выраженное в днях, представленное на оси X, и процент выживших животных, представленный на оси Y. На этой фигуре Контрольную Группу (непрерывная линия) сравнивают с Группой 2 (прерывистая линия). Животные Группы 2 были подвергнуты оральному лечению инактивированными микобактериями Mycobacterium tuberculosis после инфицирования путем введения 5 доз указанной бациллы, каждые 48 часов, начиная с 11 дня после инфицирования. Графики 5, 6, 7 и 8 соответствуют животным Групп 2a, 2b, 2c и 2d соответственно, которым были введены разные количества препарата, в соответствии с разведениями 1:1, 1:10, 1:100 и 1:1000 (Пример 1).
Фигура 3 демонстрирует время выживания, выраженное в днях, представленное на оси X, и процент выживших животных, представленный на оси Y. На этой фигуре Контрольную Группу (непрерывная линия) сравнивают с животными Группы 1 (прерывистая линия), которые после инфицирования были подвергнуты оральному лечению инактивированными микобактериями M. bovis BCG. (Пример 2).
Фигура 4 демонстрирует время выживания, выраженное в днях, представленное на оси X и процент выживших животных, представленный на оси Y. На этой фигуре Контрольную Группу (непрерывная линия) сравнивают с животными Группы 1 (прерывистая линия), которые были подвергнуты оральному лечению инактивированными микобактериями M. bovis BCG до инфицирования (Пример 3).
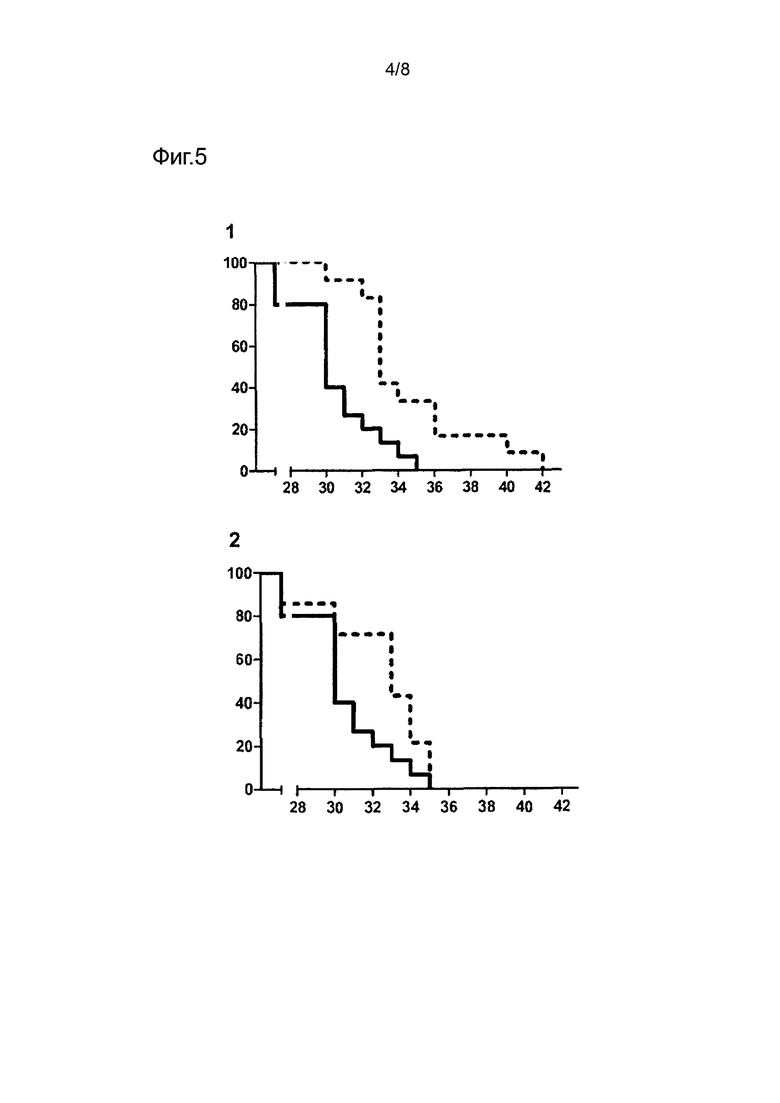
Фигура 5 демонстрирует время выживания, выраженное в днях, представленное на оси X, и процент выживших животных, представленный на оси Y. На графике 1 Контрольную Группу (непрерывная линия) сравнивают с Группой 1 (прерывистая линия), которая была подвергнута лечению оральным введением инактивированных микобактерий Mycobacterium tuberculosis, которое началось до инфицирования. На графике 2 Контрольную Группу (непрерывная линия) сравнивают с Группой 2 (прерывистая линия), которая была подвергнута лечению оральным введением инактивированных микобактерий, которое началось после инфицирования, на графике 2. (Пример 4).
Фигура 6 отображает проценты регуляторных T клеток с CD4+CD25+Foxp3+ фенотипом относительно всех CD4+ T клеток для каждого лечения инактивированными микобактериями M. tuberculosis и контроля, на 3 неделе (график 1) и на 4 неделе (график 2) после инфицирования. Указанный процент регуляторных T клеток отображен на оси Y. Различные группы животных представлены на оси X. Квадраты представляют не леченых животных (Контрольная Группа), треугольники представляют животных Группы 1, леченных до инфицирования (профилактическое действие), и круги представляют животных Группы 2, леченных после инфицирования (терапевтическое действие). Непрерывные горизонтальные линии представляют среднее арифметическое каждой группы (Пример 4).
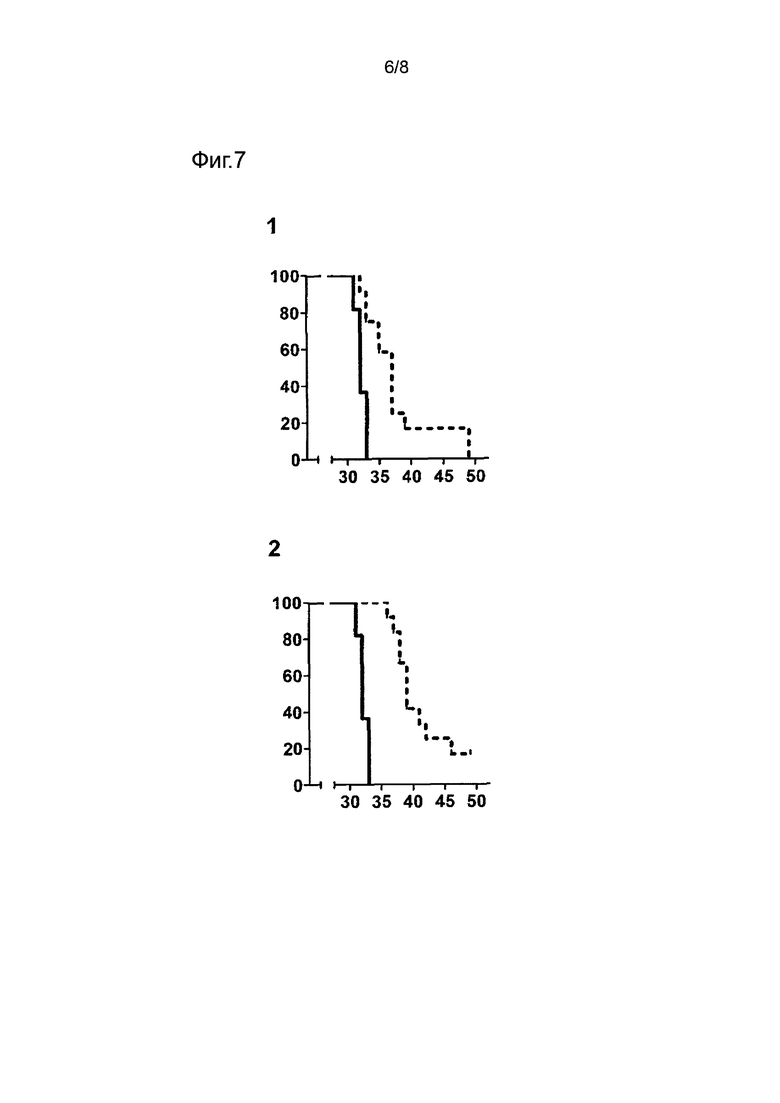
Фигура 7 демонстрирует время выживания, выраженное в днях, представленных на оси X и процент выживших животных, представленный на оси Y. На графике 1 Контрольную Группу (непрерывная линия) сравнивают с Группой 1 (прерывистая линия), которая была подвергнута лечению оральным введением инактивированных микобактерий Mycobacterium kansasii, которое началось до инфицирования (профилактическое действие). На графике 2 Контрольную группу (непрерывная линия) сравнивают с Группой 2 (прерывистая линия), которая была подвергнута лечению оральным введением инактивированных микобактерий Mycobacterium kansasii, которое началось после инфицирования (терапевтическое действие) (Пример 5).
Фигура 8 демонстрирует время выживания, выраженное в днях, представленных на оси X и процент выживших животных, представленный на оси Y. На графике 1 Контрольную Группу (непрерывная линия) сравнивают с Группой 1 (прерывистая линия), которая была подвергнута лечению оральным введением инактивированных микобактерий Mycobacterium fortuitum, которое начиналось до инфицирования (профилактическое действие). На графике 2 Контрольную группу (непрерывная линия) сравнивают с Группой 2 (прерывистая линия), которая была подвергнута лечению оральным введением инактивированных микобактерий Mycobacterium fortuitum, которое началось после инфицирования (терапевтическое действие) (Пример 6).
Фигура 9 демонстрирует время выживания, выраженное в днях, представленных на оси X и процент выживших животных, представленный на оси Y. Животные были заражены и затем лечены противотуберкулезным препаратом RIMSTAR. После лечения RIMSTAR, Группа 1 была подвергнута последующему лечению, образующему толерантность, оральным введением инактивированных микобактерий Mycobacterium fortuitum (противорецидивное действие). Контрольную Группу (непрерывная линия, без лечения, образующего толерантность) сравнивают с Группой 1 (прерывистая линия, с лечением образующим толерантность). Периоды лечения лечением RIMSTAR (черные прямоугольники) и последующим лечением образующим толерантность (белые прямоугольники) указаны на оси X (Пример 7).
Подробное описание изобретения
Целью настоящего изобретения является применение инактивированных микобактерий для приготовления медицинского препарата для предупреждения туберкулеза, где:
- инактивированные микобактерии периодически вводят орально
- интервал между дозами не превышает 5 дней, и
- количество вводимых доз составляет не менее 5.
Иначе, цель настоящего изобретения может быть сформулирована, как инактивированные микобактерии для применения для предотвращения туберкулеза, где:
- микобактерии периодично вводят орально,
- интервал между дозами не превышает 5 дней, и
- количество вводимых доз составляет не менее 5.
Авторы настоящего изобретения разработали новое превентивное лечение туберкулеза, которое основано на введении инактивированных микобактерий, используя схему лечения мульти дозами с ограниченным временным интервалом между введениями.
Авторы наблюдали, что указанное превентивное лечение, примененное до инфицирования M. tuberculosis (профилактическое действие) или после инфицирования (терапевтическое действие), способно предотвратить развитие туберкулеза путем задерживания развития инфекции из латентного состояния в активный туберкулез.
Согласно указанному лечению, периодическое оральное введение мертвых бацилл, предпочтительно в низких дозах и со сниженными интервалами времени между дозами, индуцирует создание толерантности или ответа создающего толерантность, которое неожиданно имеет положительный эффект по задерживанию инфицирования M. tuberculosis, то есть по задерживанию перехода латентной инфекции в активную инфекцию.
Авторы действительно наблюдали, что такое лечение, примененное как до, так и после инфицирования M. tuberculosis, запускает ответ создающий толерантность, характеризующийся увеличением процента регуляторных Т клеток (Treg).
Использование изобретения фокусируется на неинфицированных индивидуумах и индивидуумах, инфицированных M. tuberculosis, у которых инфекция находится в латентном состоянии. Считается, что в случае неинфицированных индивидуумов, превентивное лечение имеет профилактическое действие, в то время как в случае индивидуумов, инфицированных M. tuberculosis, считается, что оно имеет терапевтическое действие.
Особый аспект этого второго случая, то есть превентивное лечение с терапевтическим действием (касающееся инфицированных M. tuberculosis, у которых инфекция находится в латентном состоянии) состоит из тех индивидуумов, у которых предварительно была развита активная форма туберкулеза, и у которых указанная болезнь затем прекратилась, например, с помощью лечения соответствующей противотуберкулезной терапией, туберкулез вследствие этого вернулся обратно в латентное инфекционное состояние. Этот особенный случай превентивного лечения рассматривается как имеющий терапевтическое противорецидивное действие.
Вследствие этого, в случае превентивного лечения с противорецидивным действием, индивидуумов обычно предварительно подвергали фармакологическому лечению противотуберкулезными препаратами. Эти противотуберкулезные препараты хорошо известны специалисту в данной области техники, основными противотуберкулезными препаратами являются, например, изониазид, этамбутол, пиразинамид, рифампицин, стрептомицин; и эти антитуберкулезные препараты второй линии, применяемые в случае возникновения устойчивости, например тиоамиды, (среди прочих протионамид, этионамид), аминогликозиды (среди прочих, амикацин, канамицин), среди прочих циклосерин, рифабутин, рифапентин, флюороквинолоны (моксифлоксацин, левофлоксацин, офлоксацин), PAS, кларитромицин, клофазимид, линезолид или тиоридазин или их смеси.
«Превентивное лечение» обычно понимают как лечение, которое позволяет предохранить индивидуума от болезни.
В этом значении, в контексте изобретения, превентивное лечение является таким лечением, которое способно предотвращать развитие активного туберкулеза посредством задерживания перехода латентной инфекции в активную инфекцию.
«Создание устойчивости» обычно понимается как интенсивная индукция устойчивости посредством биологических или химических веществ, где термин «устойчивость» означает состояние низкого специфического ответа на биологическое или химическое вещество.
Таким образом, в контексте изобретения выражение «индукция ответа создания устойчивости» понимают как способ, при помощи которого состояние отсутствия ответа на специфический антиген индуцируется в иммунной системе хозяина, приводя к подавлению болезни.
Схемы лечения создающего толерантность были описаны в современном уровне техники в контексте других болезней таких как, например атеросклероз. George et al., Suppression of early atherosclerosis in LDL-receptor deficient mice by oral tolerance with h2-glycoprotein I, Cardiovasc. res., 2004, 62, 603-609, описывают использование β2-гликопротеина I для индукции оральной толерантности и подавления раннего атеросклероза, и Harats et al., Oral tolerance with heat shock protein 65 attenuates Mycobacterium tuberculosis-induced and high-fat-diet-driven atherosclerotic lesions, J. Am. Cardiol., 2002, 40, 1333-1338, описывают использование белка 65 теплового шока для индукции оральной толерантности к атеросклеротическим повреждениям.
Инактивированные микобактерии
Род микобактерий принадлежит к семейству Mycobacteriaceae и образуется аэробными бациллами.
Все бациллы, принадлежащие роду микобактерий, являются частью объекта настоящего изобретения, например, среди прочих виды M. abscessus, M. africanum, M. aurum, M. avium, M. avium paratuberculosis, M. avium silvaticum, M. avium hominissuis,, M. bovis, M. bovis BCG, M. chelonae, M. fortuitum, M. gastry, M. goodi, M. gordonae, M. immunogenum, M. haemophilum, M. habana, M. kansasii, M.lentiflavum, M. leprae, M. lepromatosis, M. lufu, M. mageritense, M. malmoense,M. marinum, M. massiliense, M.microti, M. monacense, M. mucogenicum, M. neoaurum, M. peregrinum, M. phlei, M. scrofulaceum, M.smegmatis, M.terrae, M. triviale, M. tuberculosis, M. microti, M. ulcerans, M. vaccae и M. xenopi.
Микобактерии имеют много антигенов общих с M. tuberculosis и являются вследствие этого подходящими для применения в настоящем изобретении. Статья Stanford et Al., Mycobacteria and their world, Int. J. Mycobacteriol., 2012, 3-12, описывает классификацию различных групп антигенов в микобактериях и как они распределены и совпадают у различных видов семейства Mycobacteriaceae.
Инактивированные микобактерии, которые являются частью настоящего изобретения, являются предпочтительно: микобактериями группы, называемой комплекс Mycobacterium tuberculosis (MTB-C), Mycobacterium fortuitum и Mycobacterium kansasii. Другими словами, инактивированные микобактерии предпочтительно выбирают из группы, состоящей из M. tuberculosis, M. bovis, M. africanum и M. microti, M. Bovis BСG, M. fortuitum и M. kansasii.
Инактивированные микобактерии более предпочтительно выбирают из группы, состоящей из M. tuberculosis, M. bovis, M. Bovis BСG, M. fortuitum и M. kansasii.
Инактивированные микобактерии, также называемые как мертвые микобактерии, подразумеваются как такие микобактерии, которые были подвержены физической или химической обработке, трансформирующей живые микобактерии в форму, которая не может реплицироваться.
В рамках настоящего изобретения, подходящими методами для инактивации микобактерий являются, например, обработка формальдегидом, обработка радиацией или обработка нагреванием.
Цель настоящего изобретения - инактивированные микобактерии предпочтительно инактивируют посредством процесса нагревания.
Подходящий способ инактивации микобактерий путем нагревания включает, например, выращивание штамма микобактерий в подходящей культуральной среде, так как они хорошо известны специалисту в данной области техники, среди прочих, такой как агар Миддлбрука 7H10 или 7H11, среда Сотона или среда Проскауэра-Бека. Среду обычно поддерживают до достижения концентрации, составляющей, примерно, между 1×105 и 1×109. единиц образования колоний (CFUs) на мл.
Культуру затем инактивируют нагреванием. Культуру предпочтительно нагревают при температуре между 70°С и 90°С. Период нагревания предпочтительно составляет от 30 минут до 3 часов. Кроме того, посредством использования автоклава, культуру предпочтительно нагревают при температуре в 121°С в течение 20 минут.
Предотвращение туберкулеза
Выражение «предотвращение туберкулеза» относится к предотвращению проявления активного туберкулеза посредством процесса задерживания развития инфекции из латентного состояния в активный туберкулез.
Указанное предотвращение может проводиться у неинфицированных индивидуумов и также у индивидуумов, инфицированных M. Tuberculosis, у которых инфекция находится в латентном состоянии, или потому, что болезнь еще не развилась, или потому, что активная болезнь уже была развита и позже затухла, например благодаря лечению противотуберкулезными лекарствами.
Авторы настоящего изобретения разработали превентивное лечение туберкулеза, которое предотвращает развитие латентной инфекции, таким образом, что развитие твердого казеозного поражения в разжиженное поражение предотвращается, и проявление активного туберкулеза вследствие этого предотвращается.
Авторы настоящего изобретения использовали экспериментальную модель, основанную на использовании C3HeB/FeJ мышей, у которых может быть стимулирована патология легких после инфицирования M. Tuberculosis, аналогичная той, что развивается у людей.
Образование казеозного некроза, который может быть разжижен в ответ на инфицирование M. Tuberculosis, в отличие от того, который возникает в других животных моделях, в которых не развивается указанный некроз, наблюдается у указанных животных, как описано в статье Harper et al., Mouse model of necrotic tuberculosis granulomas develops hypoxic lesions, J. Infect. Dis., 2012, 205, 595-601.
В случае внутривенного инфицирования большой дозой, развитие некроза и поражений у указанных животных такое, что оно может вызвать 100% смертность примерно через четыре недели после инфицирования, как описано в статье Sissons et al., Multigenic control of tuberculosis resistance: analysis of a QTL on mouse chromosome 7 and its synergism with sst1. Genes Immun., 2009, 10, 37-46.
Без намерения быть связанными какой-нибудь теорией, авторы настоящего изобретения считают, что превентивное действие лечения объектом настоящего изобретения происходит благодаря оральному введению частых периодических доз мертвых бацилл, предпочтительно низких доз, благодаря схеме лечения, которая может увеличивать толерантность у субъектов, создавая ответ в котором предпочтительно индуцируются регуляторные Т клетки (Tregs). Указанные клетки связаны с трансформирующим фактором роста бета (TGF-beta), то есть создающий толерантность или Th3 иммунный ответ генерируется в первую очередь, в отличие от обычных систем вакцинации, при которых возникает в основном Th1 иммунный ответ.
Авторы этого изобретения неожиданно обнаружили, что индукция толерантности эффективна для остановки развития инфекции M. tuberculosis, то есть перехода латентной инфекции в активную инфекцию.
Чтобы вызвать этот, создающий толерантность ответ, инактивированные микобактерии должны вводиться периодично и с уменьшенными временными интервалами между каждым введением, то есть не более чем 5 дней; предпочтительно интервал между дозами составляет не более 3 дней; и более предпочтительно, интервал между дозами составляет не более 2 дней.
Лечение по созданию толерантности также требует повторяющееся введение инактивированных микобактерий, число вводимых доз, равняющееся не менее 5; предпочтительно количество вводимых доз равно не менее 7; более предпочтительно количество вводимых доз равно не менее 9 и еще более предпочтительно количество вводимых доз равно не менее 14.
При применении данного изобретения вводится иммунологически эффективное количество инактивированных микобактерий.
Известно, что доза, предназначенная для применения, зависит от возраста и веса индивидуума, которому вводят микобактерии.
Подходящие дозы обычно содержат в пределах между 103 и 1010 инактивированных микобактерий, предпочтительно между 103 и 108 и более предпочтительно между 104 и 108.
Для демонстрации превентивного терапевтического действия на разжижение казеозного поражения схемы дозировок, создающих толерантность, которая является частью настоящего изобретения, C3HeB/FeJ мыши, используемые в модели, описанной выше, были подвергнуты протоколу лечения, по которому было введено орально от 5 до 14 доз инактивированных микобактерий с интервалом между дозами, составляющим от 1 до 3 дней.
Использованная мышиная модель, моделирует превентивную терапию туберкулеза либо, когда лечение проводится до инфицирования, как описано в Примерах 1 и 3-6, или когда лечение начинают после инфицирования M. tuberculosis, как описано в Примерах 1, 2 и 4-6, но указанное лечение проводится на ранних стадиях (до 15 дней после инфицирования, когда у животных уже имеются проявляющиеся поражения, но поражения все еще не развились до сжижения и последующих признаков болезни); или альтернативно, как описано в примере 7, лечение применяется после инфицирования, когда у животных проявились поражения и поражения сжижались, но указанные поражения вернулись в форму небольших поражений, характерных для латентной инфекции.
Основываясь на результатах, полученных в примерах, сделано заключение, что оральное применение инактивированных микобактерий по схемам создающим толерантности как до, так и после инфицирования M. Tuberculosis, увеличивает выживаемость животных, поскольку индукция болезни, то есть переход латентной инфекции в активную инфекцию задерживается.
Таким образом, считается, что использование инактивированных микобактерий в соответствии с настоящим изобретением является подходящим для предотвращения туберкулеза.
Составы
В соответствии с целью настоящего изобретения, инактивированные микобактерии применяют орально.
Указанные микобактерии могут применяться в форме любого фармацевтического препарата, подходящего для орального применения, как хорошо известно специалистам в данной области техники. Для орального применения подходят, например, таблетки, капсулы, растворы, суспензии, взвеси, порошки, гранулы или спрэи.
Микобактерии предпочтительно применяют в форме капсул или таблеток.
Фармацевтические препараты обычно содержат инактивированные микобактерии и не менее одного фармацевтического наполнителя.
Препараты готовят в соответствии с общепринятыми способами, хорошо известными специалисту в данной области техники, такими как те, которые находят в справочниках по фармацевтическим технологиям, таких как книга Remington The science and practice of Pharmacy, 20th edition, Lippincott, Williams & Wilkins, Philadelphia, 2000 [ISBN: 0-683-306472].
Среди фармацевтически приемлемых наполнителей, которые могут быть включены в фармацевтический препарат, находятся, например, вещества, предотвращающие слипание, такие как коллоидный кремнезем, трехосновный фосфат кальция, силикат кальция, силикат магния, трисиликат магния или тальк; разжижители, такие как безводная лактоза, моногидрат лактозы, фосфат кальция, безводный гидрофосфат кальция, кальций гидрофосфат дигидрат, сульфат кальция, карбонат кальция, карбоксиметилцеллюлоза кальция, микрокристаллическая целлюлоза или порошок целлюлозы, ацетат целлюлоза, декстраты, декстрины, декстроза, фруктоза, пальмитостеарат глицерина, каолин, лактитол, карбонат магния, оксид магния, малтитол, мальтодекстрины, мальтоза, полиметакрилаты, прежелатинизированный крахмал, хлорид натрия, крахмал, сахароза; смазывающие вещества, такие как стеарат магния, стеарат кальция, пальмитостеарат глицерина, полоксамеры, оксид магния, бензоат натрия, коллоидный кремнезем, лаурил сульфат натрия, стеарил фумарат натрия, стеариновая кислота, тальк или бегенат глицерина; суспендирующие вещества, такие как ксантановая камедь, камедь циамопсиса, альгиновая кислота, бентонит, карбомеры, карбоксиметилцеллюлоза натрия или кальция, гидроксиэтил целлюлоза, гидроксипропилцеллюлоза, гидроксипропилметилцеллюлоза, гидроксипропил альгинат, микрокристаллическая целлюлоза или порошок целлюлозы, коллоидный безводный кремнезем, декстрины, желатины, каолин, алюмосиликат магния, мальтитол, повидон, эфиры сорбита или трагакант; связующие вещества, такие как трисиликат магния, целлюлоза крахмал, декстрин, декстроза, полидекстроза, мальтоза, мальтодекстрин, этил целлюлоза, метил целлюлоза, полиметакрилаты, тальк, повидон, стеариновая кислота или сахароза; дезагрегирующие вещества такие, как низко замещенная гидроксипропилцеллюлоза, трехосновной фосфат кальция, карбоксиметилцеллюлоза натрия или кальция, кроскармелоза натрия, кросповидон или метилцеллюлоза; покрывающие вещества, такие как хитозан, дибутилфталат, дибутилсебакат, диэтилфталат, диметилфталат, этилцеллюлоза, гидроксиэтилцеллюлоза, гидроксипропилцеллюлоза, гипромеллоза, мальтодекстран, полиметакрилаты, фталат поливинилацетата или триэтилцетрат; диспергирующие вещества такие, как полоксамеры или эфиры сорбитана; подсластители такие, как аспартам, маннитол, сорбитол, сахарин натрия, цикламат натрия, сахароза, декстроза, фруктоза, глюкоза, инулин, изомальтоза, лактитол, мальтоза, мальтол, маннитол, сукралоза, трехалоза, ксилит или тауматин; вкусовые добавки и ароматизаторы, и/или их смеси.
Более полный перечень наполнителей, также как и их физико-химические характеристики и названия коммерческих продуктов, под которыми они продаются, может быть найден в учебнике R.C. Rowe et al., Handbook of Pharmaceutical exсipients, 4th edition, Pharmaceutical Press, London, 2003 [ISBN: 0-85369-472-9].
Следующие примеры стремятся проиллюстрировать изобретение, хотя они не должны быть интерпретированы как лимитирующие его.
Пример 1. Оральное, создающее толерантность, лечение инактивированными бациллами M. tuberculosis, примененное до или после инфицирования (профилактическое или терапевтическое действие)
Клинический штамм M. tuberculosis (TOL-3) из коллекции штаммов Unitat de Tuberculosi Experimental of Institute Germans Trias i Pujol, выращенный в жидкой среде Проскауэр-Бека до достижения экспоненциальной фазы роста и концентрации в 1,7×107 единиц образования колоний (CFUs) на мл, был использован для приготовления инактивированных микобактерий.
Культуру была инактивирована при нагревании при 75°С в течение 2 часов и затем заморожена при 80°С. В дальнейшем она была разведена 50:50 в 10% растворе сахарозы, упакована и лиофилизирована в сосудах в объемах 0,5 мл. Эти сосуды были затем воссозданы 3 мл бидистиллированной воды, в виде разведения 1:1, которое эквивалентно 4,25×105 CFUs.
В анализах, 0,3 мл продукта были применены как при этом разведении 1:1, так и при разведениях 1:10, 1:100 и 1:1000. Эти применения соответствуют нескольким дозам в 4,25×105, 4,25×104, 4,25×103 и 4,25×102 CFUs соответственно.
Эффективность инактивированных микобактерий была проанализирована у 6-8 недельных женских особей мышей C3HeB/FeJ, лишенных специфических патогенов.
Мыши были разделены на три группы по 6 животных в каждой, и каждая из групп была подвержена следующему протоколу создания толерантности.
1) Контрольная Группа: Нелеченые.
2) Группа 1 (доинфекционное лечение): Леченые орально принудительным кормлением 5 дозами продукта, содержащими инактивированные микобактерии, вводимыми каждые 48 часов, начиная за 10 дней до инфицирования. В каждой дозе был введен объем в 0,3 мл, и было проанализировано всего четыре разведения, то есть 1:1, 1:10, 1:100 и 1:1000 (Группы 1а, 1b, 1c и 1d, соответственно).
3) Группа 2 (постинфекционное лечение): Лечили орально принудительным кормлением 5 дозами продукта, содержащими инактивированные микобактерии, вводимыми каждые 48 часов, начиная с 11 дня после инфицирования. В каждой дозе был введен объем в 0,3 мл, и было проанализировано всего четыре разведения, то есть 1:1, 1:10, 1:100 и 1:1000 (Группы 2а, 2b, 2c и 2d, соответственно).
Для инфицирования был использован вирулентный штамм Mycobacterium tuberculosis (H37Rv Pasteur), выращенный в среде Проскауэр-Бека до полулогарифмической фазы роста и хранившийся до использования в аликвотах по 1 мл при температуре -70°С.
Мыши были инфицированы внутривенно, путем введения инокулята с 2×104 жизнеспособных бацилл.
Животных обследовали и взвешивали ежедневно, в соответствии со способом, описанным детально в Таблице 1, до того как состояния животных требовали их умерщвления.
Возможно изменение во внешнем виде или количестве экскрементов
Животное не пьет воду или не ест еду
3: увеличение частоты применения протокола наблюдения до 2 раз/день.
Если оценка 3 получена более чем в одном положении, все оценки 3 становятся оценками 4.
Если одна или больше оценок достигает значения 4, животное умерщвляют.
Полученные результаты изображены графически на фигурах 1 и 2, которые демонстрируют рост выживаемости животных после инфицирования для различных экспериментальных групп. Время выживания, выраженное в днях, представлено на оси X, в то время как процент выживших представлен на оси Y.
На Фигуре 1 Контрольную Группу (непрерывная линяя) сравнивают с животными Группы 1 (прерывистая линия), которые были пролечены до инфицирования. Графики 1, 2, 3 и 4 относятся к животным Групп 1а, 1b, 1c и 1d, соответственно, которым были введены разные количества продукта в соответствии с разведениями 1:1, 1:10, 1:100 и 1:1000.
На Фигуре 2, Контрольную Группу (непрерывная линия) сравнивают с животными Группы 2 (прерывистая линия), которые были пролечены после инфицирования. Графики 5, 6, 7 и 8 относятся к животным Групп 2а, 2b, 2c и 2d, соответственно, которым были введены разные количества продукта в соответствии с разведениями 1:1, 1:10, 1:100 и 1:1000.
Для оценки результата лечения на выживаемость животных кривые выживаемости были сравнены посредством двух способов: анализа по Мантелю-Коксу (или логарифмический ранговый критерий, LR t) и критерия Gehan-Breslow-Wilcoxon (GBW t). В первом способе, предполагается, что риск (смерти/единица от времени) является постоянной в течение всего эксперимента, в то время как второй способ принимает больше в расчет смерти в первые несколько дней (более ранние смерти). Если риск является постоянным, анализ Мантеля-Кокса имеет более высокую статистическую мощность, но если это не так, и существует группа, которая находится на более высоком риске, чем другая, то более подходящим является критерий Gehan-Breslow-Wilcoxon.
Статистически значимые отличия относительно контрольной группы наблюдаются во всех случаях (p<0,05, GBW t). Также существует статистическая значимость для LR t (p<0,05) в лечениях, соответствующих графикам 4, 5, 6 и 7.
Результаты отражают защитный ответ, когда применяли доинфекционную схему лечения с наименьшим разведением (1:1000, Фигура 1, график 4), в то время как защиту при постинфекционной схеме лечения наблюдали при разведениях 1:1, 1:10 и 1:100 (Фигура 2, графики 5, 6 и 7, соответственно), бывшую особенно значительной при схеме лечения с разведением 1:10.
Аутопсии в Контрольной группе отражали очень быстрое прогрессирование между 26 и 36 днями, периода, в течение которого поражения значительно увеличивались в размерах и заканчивались, сливаясь, образуя большие повреждения с некрозами, имеющими внутреннюю кремообразную консистенцию.
Таким образом, можно сделать вывод, что оральное применение образующей толерантность схемы лечения, как до (профилактическое действие), так и после (терапевтическое действие) инфицирования M. Tuberculosis, увеличивает выживаемость животных задерживанием перехода латентной инфекции в активную инфекцию. Поэтому считается, что использование инактивированных микобактерий в соответствии с настоящим изобретением является подходящим в качестве превентивного лечения против туберкулеза.
Пример 2. Оральное, создающее толерантность, лечение инактивированными бациллами M. bovis BCG, примененное после инфицирования (терапевтическое действие).
Терапевтическое средство, использованное в этом примере, было приготовлено из коммерческого штамма M. bovis BCG (SSI), выращенного в жидкой среде Проскауэра и Бека до достижения экспоненциальной фазы роста и концентрации в 1,03×108 колоний образующих единиц (CFUs) на мл. Культура была инактивирована, следуя тому же способу, как описано в Примере 1.
Эффективность инактивированных микобактерий была проанализирована у 6-8 недельных женских особей мышей C3HeB/FeJ, не имеющих специфических патогенов. В каждой дозе был введен объем в 0,3 мл, соответствующий разведению 1:10, которое соответствует 2,575×105 CFUs.
Мыши были разделены на две группы по 12 животных в каждой, и каждая группа была подвержена следующему протоколу создания толерантности:
1) Контрольная группа: Нелеченые
2) Группа 1 (постинфекционное лечение): Леченые орально принудительным кормлением 5 дозами продукта, содержащими инактивированные микобактерии, вводимыми каждые 48 часов, начиная с 12 дня после инфицирования и далее 3 раза в неделю (понедельник, среда и пятница) до конца эксперимента, в соответствии со временем выживаемости каждой мыши.
Для инфицирования был использован вирулентный штамм Mycobacterium tuberculosis (H37Rv Pasteur), выращенный в среде Проскауэра и Бека до логарифмической фазы роста и хранившийся до использования в 1 мл аликвотах при температуре -70°С.
Мыши были инфицированы внутривенно путем введения инокулята живых бактерий в количестве около 2×104.
Животных обследовали и взвешивали ежедневно в соответствии с тем же способом, описанным в Таблице 1 Примера 1, до состояния животного, требующего умерщвления.
Полученные результаты представлены графически на Фигуре 3. Время выживания (в днях) представлено на оси x, в то время как процент выживших представлен на оси Y.
Наблюдается, что Контрольная Группа (сплошная линия) имеет меньший процент выживания, чем леченая Группа 1 (прерывистая линия), наблюдаются существенные различия (логарифмический ранговый критерий, p=0,0147; критерий Gehan-Breslow-Wilcoxon, p=0,0052).
Результаты отражают защитный ответ после продолжительного лечения инфицированных животных. Вследствие этого, можно сделать вывод, что оральное применение образующих толерантность схем приема инактивированных M. bovis BCG после инфицирования M. tuberculosis, увеличивает процент выживания животных за счет задержки индукции болезни. Поэтому считается, что применение инактивированных микобактерий в соответствии с настоящим изобретением является пригодным как превентивное лечение против туберкулеза за счет задержки перехода латентной инфекции в активную инфекцию.
Пример 3. Оральное, создающее толерантность, лечение инактивированными бациллами M. bovis BCG, проводимое до инфицирования (профилактический эффект).
Инактивированные бациллы M. bovis BCG были приготовлены, следуя тому же способу, описанному в Примере 2.
Эффективности инактивированных микобактерий была проанализирована у 6-8 недельных женских особей мышей C3HeB/FeJ, не имеющих специфических патогенов.
Мыши были разделены на две группы по 12 животных в каждой, и каждая группа была подвержена следующему лечению:
1) Контрольная группа: Нелеченая
2) Группа 1 (лечение до инфицирования): Леченые орально принудительным питанием 13 дозами продукта, содержащими инактивированные микобактерии, вводимыми 3 раза в неделю (понедельник, среда, пятница), начиная за 29 дней до инфицирования. В каждой дозе был введен объем в 0,3 мл, соответствующий разведению 1:1000, которое соответствует 2,575×103 CFUs.
Как и в предыдущих примерах, для инфицирования был использован вирулентный штамм Mycobacterium tuberculosis (H37Rv Pasteur), выращенный в среде Проскауэр-Бека до полулогарифмической фазы роста и хранившийся до использования в 1 мл аликвотах при температуре -70°С.
Мыши были инфицированы внутривенно путем введения инокулята с 2×104 жизнеспособных бацилл.
Животных обследовали и взвешивали ежедневно, в соответствии с тем же способом, описанным детально в Таблице 1 Примера 1, до тех пор, пока состояния животных не требовали их умерщвления.
Полученные результаты представлены графически на Фигуре 4. Время выживания (в днях) представлено на оси x, в то время как процент выживших представлен на оси Y.
Наблюдается, что Контрольная Группа (сплошная линия) имеет меньший процент выживания, чем леченая Группа 1 (прерывистая линия), наблюдаются существенные различия на основании логарифмического рангового критерия, (p=0,0020) и критерия Gehan-Breslow-Wilcoxon, (p=0,0019).
Результаты отражают защитный ответ после индукции толерантности путем орального введения инактивированных микобактерий M. bovis BCG до инфицирования M. tuberculosis, констатируя, что указанное лечение в высоком проценте предохраняет от индукции болезни.
Пример 4. Эффективность орального, создающего толерантность, лечения инактивированными бациллами M. tuberculosis, примененного до инфицирования или после инфицирования (профилактическое или терапевтическое действие) и мониторинг индуцированной толерантности путем анализа регуляторных T клеток в селезенке.
Инактивированные бациллы M. Tuberculosis (TOL-3) были приготовлены таким же способом как описано в Примере 1.
Эффективность инактивированных микобактерий была проанализирована у 6-8 недельных женских особей мышей C3HeB/FeJ, не имеющих специфических патогенов.
Мыши были разделены на две группы по 24 животных в каждой, и каждая группа была подвержена следующему лечению:
1) Контрольная группа: Нелеченая
2) Группа 1 (лечение до инфицирования): Леченые орально принудительным питанием 5 дозами продукта, содержащими инактивированные микобактерии, вводимыми каждые 48 часов, начиная за 10 дней до инфицирования, и далее 3 раза в неделю (понедельник, среда и пятница) до конца эксперимента. В каждой дозе был введен объем в 0,3 мл с разведением 1:1000.
3) Группа 2 (лечение после инфицирования): Леченые орально принудительным питанием 5 дозами продукта, содержащими инактивированные микобактерии, вводимыми каждые 48 часов, начиная на 11 день после инфицирования, и далее 3 раза в неделю (понедельник, среда и пятница) до конца эксперимента. В каждой дозе был введен объем в 0,3 мл с разведением 1:10.
Как и в предыдущих примерах, для инфицирования был использован вирулентный штамм Mycobacterium tuberculosis (H37Rv Pasteur), выращенный в среде Проскауэр-Бека до полулогарифмической фазы роста и хранившийся до использования в 1 мл аликвотах при температуре -70°С.
Мыши были инфицированы внутривенно путем введения инокулята с 2×105 жизнеспособных бацилл.
Половина животных в каждой группе (12) была отложена для исследования выживаемости. Животных обследовали и взвешивали ежедневно, в соответствии с тем же способом Примера 1, описанным в Таблице 1, до тех пор, пока состояния животных не требовали их умерщвления.
На Фигуре 5 графики 1 и 2 демонстрируют результаты выживаемости различных экспериментальных групп. Время выживания (в днях) представлено на оси x, в то время как процент выживших животных представлен на оси Y.
На графике 1 Контрольная Группа (сплошная линия) сравнивается с Группой 1 (прерывистая линия), которая была подвержена лечению, которое началось до инфицирования. Наблюдается, что Контрольная Группа имеет более низкий процент выживания, чем леченая группа, со статистически достоверным результатом согласно логарифмическому ранговому критерию, (p=0,0011) и критерию Gehan-Breslow-Wilcoxon, (p=0,0014).
На графике 2 Контрольная Группа (сплошная линия) сравнивается с Группой 2 (прерывистая линия), которая была подвержена лечению, которое началось после инфицирования. Наблюдается, что Контрольная Группа имеет более низкую скорость выживания, чем леченая группа со статистически достоверными результатами согласно логарифмическому ранговому критерию (p=0,004541), в то время как согласно критерию Gehan-Breslow-Wilcoxon различия не являются статистически достоверными.
В обоих случаях можно сделать вывод, что животные леченые инактивированными микобактериями по схеме создания толерантности проживают более длительное время после инфицирования M. Tuberculosis, чем это делают нелеченые животные.
В отношении оставшихся животных в каждой группе (12) половина животных была умерщвлена на 3 неделе (6 животных из группы) и другая половина на 4 неделе (6 животных из группы) для изучения регуляторных T клеток, находящихся среди спленоцитов.
Как описано в статье Faria et al., Oral tolerance, Immunol. Rev., 2005, 206 (1), 232-259, регуляторные T клетки являются группой T клеток, которые являются ключевыми в индукции оральной толерантности, определенные как популяция, вовлеченная в регуляцию иммунного ответа, и они экспрессируют мембранные маркеры CD4 и CD5.
Статья 2003 Hori et al., Control of regulatory T cell development by the transcription factor Foxp3, Science, 2003, 299 (5609), 1057-61, описывает, что транскрипционный фактор Foxp3 является ключевым для развития регуляторных T клеток. По этой причине считается, что T клетки с CD4+CD25+Foxp3+ фенотипом обладают регуляторной функцией.
Животные были умерщвлены путем смещения шейных позвонков после анестезии ингаляцией изофлюраном. Селезенки были вынуты и спленоциты были получены путем механической дезагрегации, фильтрации через клеточный фильтр (BD Falcon Cell Strainer, нейлон, 40 мкм) и лизисом эритроцитов. CD4 и CD25 мембран сплиноцитов и внутриклеточный Foxp3 были помечены с помощью набора для меченья регуляторных T клеток (eBioscience) и проанализированы проточной цитометрией (BD LSR-Fortessa клеточный анализатор). Результаты были обработаны программным обеспечением BD FACSdiva analysis.
Фигура 6 демонстрирует проценты регуляторных T клеток, T клеток с CD4+CD25+Foxp3+ фенотипом по отношению к общему количеству CD4+ T клеток, при различных лечениях и в контроле, на 3 неделе (График 1) и на 4 неделе (график 2) после инфицирования. Процент регуляторных T клеток представлен на Y оси. Различные типы лечений и контроль представлены на оси X.
Квадраты представляют нелеченых животных (Контрольная группа), треугольники представляют животных из Группы 1, леченых до инфицирования, и круги представляют животных из Группы 2, леченых после инфицирования. Непрерывные горизонтальные линии представляют среднее арифметическое значение каждой группы.
Наблюдается, что в действительности существует увеличение процента регуляторных T клеток между неделями 3 и 4 только в группах, леченных в соответствии со схемой лечения создания толерантности, не смотря на то, когда она было начата до или после инфицирования M. Tuberculosis.
Пример 5. Оральное, создающее толерантность, лечение инактивированными бациллами M. kansasii, проводимое до или после инфицирования (профилактическое или терапевтическое действие)
Mycobacterium kamsasii являются медленно растущими, не туберкулезными микобактериями. Клинический штамм M. kamsasii (TOL) из коллекции штаммов Unitat Tuberculosi Experimental of Institue Germans Trias i Pujol выращивали в жидкой среде Проскауэра-Бека до достижения экспоненциальной фазы роста и концентрация 8,07×104 колоний образующих единиц (CFUs) на мл была использована для приготовления инактивированных микобактерий.
Культура была инактивирована автоклавированием при 121°С в течение 20 минут и затем заморожена при -80°С. Впоследствии она была разведена 50:50 в 10% растворе сахарозы, упакована во флаконы в 2 мл объемах и хранилась при -80°С.
Эффективность инактивированных микобактерий была проанализирована у 6-8 недельных женских особей мышей C3HeB/FeJ, не имеющих специфических патогенов.
В каждой дозе был введен объем в 0,3 мл, соответствующий разведению 1:10, что соответствует 1,42×104 CFUs.
Мыши были разделены на группы по 12 животных в каждой, и к каждой группе был применен следующий протокол образования толерантности:
1) Контрольная группа: Нелеченая
2) Группа 1 (лечение до инфицирования): Леченые орально принудительным питанием 13 дозами продукта, содержащими инактивированные микобактерии, вводимыми 3 раза в неделю (понедельник, среда и пятница). Группы были инфицированы через 24 часа после введения последней дозы.
3) Группа 2 (лечение после инфицирования): через 15 дней после инфицирования группы были лечены орально принудительным питанием 13 дозами продукта, содержащими инактивированные микобактерии, вводимые 3 раза в неделю (понедельник, среда и пятница).
Для инфицирования использовали вирулентный штамм Mycobacterium tuberculosis (H37Rv Pasteur), выращенный в среде Проскауэра-Бека до полулогарифмической фазы роста и хранившийся до использования в 1 мл аликвотах при температуре -70°С.
Мыши были инфицированы внутривенно путем введения инокулята с около 2×104 жизнеспособных бацилл.
Животных наблюдали и взвешивали ежедневно в соответствии с таким же способом, описанным в Таблице 1 Примера 1 до состояния животного требующего умерщвления.
Фигура 7, графики 1 и 2 показывают результаты выживших в различных группах. Время выживания (в днях) представлено на оси X, в то время как процент выживших представлен на оси Y.
График 1 относится к профилактическому лечению, сравнению Контрольной Группы с Группой 1, которая была подвергнута лечению, которое началось до инфицирования. Наблюдается, что Контрольная Группа (непрерывная линия) имеет более низкий процент выживания, чем Группа 1 (прерывистая линия), наблюдаются существенные различия (логарифмический ранговый критерий, p<0,0001; критерий Gehan-Breslow-Wilcoxon, p<0,0001).
График 2 относится к терапевтическому лечению, сравнению Контрольной Группы с Группой 2, которая была подвергнута лечению, которое началось после инфицирования. Наблюдается, что Контрольная Группа (непрерывная линия) имеет более низкий процент выживания, чем леченая Группа 2 (прерывистая линия), наблюдаются существенные различия (логарифмический ранговый критерий, p<0,0001; критерий Gehan-Breslow-Wilcoxon, p<0,0001).
В обоих случаях, результаты отражают защитный ответ. Поэтому можно сделать вывод, что оральное лечение схемами создания толерантности медленно растущими, нетуберкулезными инактивированными микобактериями (M. kansasii), применяемое до или после инфицирования M. tuberculosis, повышает процент выживания животных за счет задержки индукции заболевания. Поэтому считается, что использование инактивированных микобактерий в соответствии с настоящим изобретением подходит в качестве превентивного лечения туберкулеза за счет задержки перехода латентной инфекции в активную инфекцию.
Пример 6. Оральное, создающее толерантность, лечение инактивированными бациллами M. fortuitum, проводимое до или после инфицирования (профилактическое или терапевтическое действие)
Mycobacterium fortuitum являются быстро растущими, не туберкулезными микобактериями. Штамм окружающей среды M. fortuitum (Manresa strain) из коллекции штаммов Unitat Tuberculosi Experimental of Institue Germans Trias i Pujol, выращенный на твердой среде Миддлбрука 7H9 до достижения концентрация 2×109 колоний образующих единиц (CFUs) на мл, был использован для приготовления инактивированных микобактерий.
Культура была инактивирована автоклавированием при 121°С в течение 20 минут и затем заморожена при -80°С. Впоследствии она была разведена 50:50 в 10% растворе сахарозы, упакована во флаконы в 2 мл объемах и хранилась при -80°С.
Эффективность инактивированных микобактерий была проанализирована у 6-8 недельных женских особей мышей C3HeB/FeJ, не имеющих специфических патогенов.
В каждой дозе был введен объем в 0,3 мл, соответствующий разведению 1:1000, что соответствует 6×105 CFUs.
Мыши были разделены на 3 группы по 12 животных в каждой, и к каждой группе был применен следующий протокол создания толерантности:
1) Контрольная группа: Нелеченая
2) Группа 1 (лечение до инфицирования): Леченые орально принудительным питанием 10 дозами продукта, содержащими инактивированные микобактерии, вводимыми 5 раз в неделю (с понедельника по пятницу). Группы были инфицированы через 24 часа после введения последней дозы.
3) Группа 2 (лечение после инфицирования): леченые орально принудительным питанием 10 дозами продукта, содержащими инактивированные микобактерии, вводимыми 5 раз в неделю (с понедельника по пятницу), начиная лечение через 5 дней после инфицирования.
Для инфицирования был использован вирулентный штамм Mycobacterium tuberculosis (H37Rv Pasteur), выращенный в среде Проскауэра-Бека до полулогарифмической фазы роста и хранившийся до использования в 1 мл аликвотах при температуре -70°С.
Мыши были инфицированы внутривенно путем введения инокулята с около 2×105 жизнеспособных бацилл.
Животных наблюдали и взвешивали ежедневно в соответствии с таким же способом, описанным в Таблице 1 Примера 1 до состояния животного требующего умерщвления.
Фигура 8, графики 1 и 2 показывают результаты выживания различных групп. Время выживания (в днях) представлено на оси X, в то время как процент выживших представлен на оси Y.
Результаты, полученные с точки зрения профилактического лечения показаны на графике 1. Наблюдается, что Контрольная Группа (непрерывная линия) имеет более низкий процент выживания, чем леченая Группа 1 (прерывистая линия), наблюдаются существенные различия (логарифмический ранговый критерий, p<0,0001; критерий Gehan-Breslow-Wilcoxon, p<0,0001).
Результаты, полученные с точки зрения терапевтического лечения, показаны на графике 2. Наблюдается, что Контрольная Группа (непрерывная линия) имеет более низкий процент выживания, чем леченая Группа 2 (прерывистая линия), наблюдаются существенные различия (логарифмический ранговый критерий, p<0,0001; критерий Gehan-Breslow-Wilcoxon, p<0,0001).
В обоих случаях, результаты отражают защитный ответ. Поэтому можно сделать вывод, что оральное применение схем лечения, создающего толерантность, быстрорастущими, нетуберкулезными инактивированными микобактериями (M. fortuitum) до или после инфицирования M. tuberculosis, повышает процент выживания животных за счет задерживания индукции заболевания. Поэтому считается, что использование инактивированных микобактерий в соответствии с настоящим изобретением подходит в качестве превентивного лечения туберкулеза за счет задержки перехода латентной инфекции в активную инфекцию.
Пример 7. Оральное, создающее толерантность, лечение инактивированными бациллами M. fortuitum, проводимое после лечения экспериментального активного туберкулеза (действие против рецидива)
Инактивированные бациллы Mycobacterium fortuitum (Manresa strain) были приготовлены тем же способом, описанным в Примере 6.
Эффективность инактивированных микобактерий была проанализирована у 6-8 недельных женских особей мышей C3HeB/FeJ, не имеющих специфических патогенов.
В каждой дозе был введен объем в 0,3 мл, соответствующий разведению 1:100, что соответствует 6×106 CFUs.
В данном случае, эффективность превентивного лечения, создающего толерантность, в соответствии с настоящим изобретением была изучена с точки зрения противорецидивного действия, то есть после того как у животных развивалась активная фаза туберкулеза и после того как они были пролечены противотуберкулезными препаратами.
Поэтому в начале эксперимента, мыши были внутривенно инфицированы путем введения инокулята с около 2×105 жизнеспособных бацилл.
Как и в предыдущих примерах, для инфицирования был использован вирулентный штамм Mycobacterium tuberculosis (H37Rv Pasteur), выращенный в среде Проскауэра-Бека до полулогарифмической фазы роста и хранившийся до использования в 1 мл аликвотах при температуре -70°С.
Животных наблюдали и взвешивали ежедневно в соответствии с таким же способом, описанным в Таблице 1 Примера 1, до состояния животного требующего умерщвления.
В это время (21 день), было начато лечение, 5 дней в неделю, с использованием комбинации антибиотиков, содержащихся в коммерческом препарате, именуемом RIMSTAR (изониазид, этамбутол, пиразинамид и рифампицин), отрегулированное по весу животного. Последнюю дозу вводили на 60 день.
Мыши были затем разделены на 3 группы по 12 животных в каждой, и к каждой группе был применен следующий протокол создания толерантности:
1) Контрольная Группа: без лечения, создающего толерантность.
2) Группа 1: Леченые орально принудительным питанием 14 дозами продукта, содержащими инактивированные микобактерии, вводимыми 7 раз в неделю (с понедельника по воскресенье), начиная указанное лечение, создающее толерантность, через 72 часа после окончания лечения активного туберкулеза препаратом RIMSTAR (63 день) и введением последней дозы на 76 день.
Результаты, полученные с точки зрения лечения против рецидива, графически представлены на Фигуре 9. Время выживания (в днях) представлено на оси X, в свою очередь процент выживших представлен на оси Y. Кроме того, на временной X оси период лечения препаратом RIMSTAR указан черными треугольниками, и период лечения, создающего толерантность, Группы 1 указан белыми треугольниками.
Наблюдается, что Контрольная Группа (непрерывная линия) имеет более низкий процент выживания, чем леченая Группа 1 (прерывистая линия),
Результаты отражают защитный ответ, и, таким образом, можно сделать вывод, что после получения лечения активного туберкулеза оральное применение схем создающего толерантность лечения микобактериями предотвращает рецидив.
| название | год | авторы | номер документа |
|---|---|---|---|
| ОБНАРУЖЕНИЕ ТУБЕРКУЛЕЗА И ЗАРАЖЕНИЯ ТУБЕРКУЛЕЗНЫМИ МИКОБАКТЕРИЯМИ С ИСПОЛЬЗОВАНИЕМ НВНА | 2005 |
|
RU2426128C2 |
| ВАКЦИНЫ РЕКОМБИНАНТНЫХ ВНУТРИКЛЕТОЧНЫХ ПАТОГЕНОВ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2001 |
|
RU2266132C2 |
| ПРЕПАРАТЫ, СОДЕРЖАЩИЕ АНТИТЕЛА ЧЕЛОВЕКА, ПРИМЕНЯЕМЫЕ В ЛЕЧЕНИИ МИКОБАКТЕРИАЛЬНЫХ ИНФЕКЦИЙ | 2003 |
|
RU2350352C2 |
| ПРОТИВОТУБЕРКУЛЕЗНАЯ ВАКЦИНА | 2007 |
|
RU2443773C2 |
| ИММУНОТЕРАПЕВТИЧЕСКОЕ СРЕДСТВО, ПРЕДНАЗНАЧЕННОЕ ДЛЯ ПЕРВИЧНОЙ ПРОФИЛАКТИКИ ТУБЕРКУЛЕЗА | 2009 |
|
RU2544125C2 |
| КОМПОЗИЦИИ ДЛЯ ПРИМЕНЕНИЯ В КАЧЕСТВЕ ПРОФИЛАКТИЧЕСКОГО СРЕДСТВА ДЛЯ ПАЦИЕНТОВ С РИСКОМ ТУБЕРКУЛЕЗНОЙ ИНФЕКЦИИ ИЛИ В КАЧЕСТВЕ ВТОРИЧНЫХ СРЕДСТВ ДЛЯ ЛЕЧЕНИЯ ПАЦИЕНТОВ С ТУБЕРКУЛЕЗНОЙ ИНФЕКЦИЕЙ | 2019 |
|
RU2778094C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ЛЕЧЕНИЯ АКТИВНОЙ ИНФЕКЦИИ MYCOBACTERIUM TUBERCULOSIS | 2013 |
|
RU2659149C2 |
| ЛИПОСОМНЫЙ ПРЕПАРАТ, ПРЕДНАЗНАЧЕННЫЙ ДЛЯ ЛЕЧЕНИЯ ИЛИ ПРЕДУПРЕЖДЕНИЯ ТУБЕРКУЛЕЗА | 2012 |
|
RU2648842C2 |
| ПРОТИВОТУБЕРКУЛЕЗНОЕ СРЕДСТВО | 2017 |
|
RU2756208C2 |
| ПРОФИЛАКТИЧЕСКАЯ ВАКЦИНА ОТ ТУБЕРКУЛЕЗА | 2007 |
|
RU2526910C2 |




Изобретение относится к медицине. Предложен способ предотвращения туберкулеза оральным периодическим введением инактивированных микобактерий, причём интервал между дозами не превышает 5 дней, количество доз не менее 5. Технический результат: механизм создания толерантности к инфицированию туберкулезными бациллами характеризуется увеличением доли регуляторных Т-клеток (Treg); при этом обеспечен защитный ответ за счёт задержки индукции заболевания при инфицировании микобактериями и предотвращается рецидив пролеченной активной фазы туберкулёза. Инактивированные бактерии могут быть использованы по вышеупомянутой схеме лечения для задержки развития инфекции из латентного состояния в активный туберкулез. 14 з.п. ф-лы, 9 ил., 7 пр.
1. Способ предотвращения туберкулеза, включающий введение инактивированных микобактерий, где
- микобактерии периодически вводятся орально,
- интервал между дозами не превышает 5 дней, и
- количество введенных доз равно как минимум 5.
2. Способ по п.1, где инактивированные микобактерии выбирают из группы, состоящей из M. tuberculosis, M. Bovis, M. africanum и M. microti, M.bovis BCG, M. fortuitum, и M. kansasii.
3. Способ по п.2, где инактивированные микобактерии выбирают из M. tuberculosis, M. Bovis, M.bovis BCG, M. fortuitum, и M. kansasii.
4. Способ по любому из пп.1-3, где микобактерии инактивируют путем процесса нагревания.
5. Способ по любому из пп.1-3, где интервал между дозами равен не более 3 дней.
6. Способ по п.5, где интервал между дозами равен не более 2 дней.
7. Способ по любому из пп.1-3, где количество вводимых доз равно как минимум 7.
8. Способ по п.7, где количество вводимых доз равно как минимум 9.
9. Способ по любому из пп.1-3, где каждая доза содержит между от 103 до 1010 инактивированных микобактерий.
10. Способ по любому из пп.1-3, где микобактерии вводят в виде фармацевтической композиции, содержащей инактивированные микобактерии и не менее одного фармацевтически приемлемого наполнителя.
11. Способ по п.10, где фармацевтическая композиция находится в форме капсул.
12. Способ по п.10, где фармацевтический препарат находится в форме таблеток.
13. Способ по любому из пп.1-3, где он вводится индивидууму, инфицированному M. Tuberculosis, у которого инфекция находится в латентном состоянии.
14. Способ по п.13, где у индивидуума была в прошлом развита активная форма туберкулеза.
15. Способ по любому из пп.1-3, где он вводится индивидууму, не инфицированному M. Tuberculosis.
| YEBOAH KG et al | |||
| Evaluation of albumin microspheres as oral delivery system for Mycobacterium tuberculosis vaccines | |||
| J.Microencapsul | |||
| Колосоуборка | 1923 |
|
SU2009A1 |
| BUTOV DA et al | |||
| Phase IIb randomized trial of adjunct immunotherapy in patients with first-diagnosed tuberculosis, relapsed and multi-drug-resistant (MDR) TB | |||
| J.Immune Based Ther Vaccines | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| МЕДУНИЦЫН Н.В.,Вакцинология, М., 2010, Триада-Х, с.385 раздел Вакцина стафилококковая сухая, с.387 раздел Бронхомунал | |||
| RU 2006116429 A, 10.12.2007 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| DLUGOVITZKY D | |||
| et al | |||
| Immunotherapy with oral, heat-killd, Mycobacterium vaccae in patients with moderate to advanced pulmonary tuberculosis | |||
| Immunotherapy | |||
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
Авторы
Даты
2018-06-15—Публикация
2013-06-13—Подача