Уровень техники
Сорго (Sorghum spp.) - род растений, включающий приблизительно 20 видов трав. Это местные растения тропического и субтропического регионов Восточной Африки, и их выращивают на каждом континенте ради зерна, потребляемого человеком и животными, а также используют в качестве корма для животных и для производства алкогольных напитков. Поскольку эти растения не содержат плотен, сорго могут употреблять люди, страдающие глютеновой болезнью.
Сорго более устойчивы к засухе и избыточному содержанию влаги в почве, чем большинство зерновых культур. Они способны расти должным образом при различных почвенных и погодных условиях. Также, они благоприятно реагируют на орошение, требуя не менее 250 мм за время жизненного цикла, с оптимальным орошением колеблющимся в пределах 400-550 мм.
Почва должна содержать подходящее количество влаги во время посева для того чтобы достичь быстрого и равномерного всхождения и, таким образом, хорошей посадки культур. Наибольшая потребность в воде начинается через 30 дней после всхождения и продолжается до заполнения зерен, наиболее важными стадиями являются образование метелки и цветение, т.к. недостаток воды в это время приведет к уменьшению размера урожая.
Далее, сорго обладает способностью находиться в состоянии покоя во время периодов засухи и продолжать рост во время благоприятных периодов, хотя такие стрессовые ситуации могут сказываться на продуктивности.
Сорго требуются высокие температуры для нормального развития, и, следовательно, они более чувствительны к низким температурам, чем другие сельскохозяйственные культуры. Температура почвы не менее 18°С требуется для прорастания семян; и фактический активный рост растения не достигается до достижения температуры в 15°С, оптимальная температура около 32°С.
Синтаза ацетогидроксикисллот (AHAS) - первый из ферментов, катализирующих синтез разветвленноцепочечных аминокислот валина, лейцина и изолейцина. AHAS является мишенью некоторых гербицидов, таких как сульфонилмочевины, имидазолиноны, триазолопиримидины и пиримидилоксибензоаты. Два первых семейства гербицидов широко используются в современном сельском хозяйстве в связи с их низкой токсичностью и высокой эффективностью против сорняков.
Семейство гербицидов имидазолинонов включает в свой состав имазетапир, имазаквин и имазапир.
Сульфонилмочевины присутствующие на рынке включают, например: метсульфурон-метил, хлоросульфурон, никосульфурон, циносульфурон, имидасульфурон, галосульфурон, римсульфурон, трисульфурон-метил и трибенурон-метил.
Однако, существуют растения устойчивые к гербицидам из семейств имидазолинонов и/или сульфонилмочевин; например, такие виды как Zea mays, Arabidopsis thaliana, Brassica napus, Glycine max, Nicotiana tabacum и Oryza sativa (Sebastian et al., (1989) Crop Sci., 29: 1403-1408; Swanson et al., 1989 Theor. Appl. Genet. 78: 525-530; Newhouse et al., (1991) Theor. Appl. Genet., 83: 65-70; Sathasivan et al., (1991) Plant Physiol., 97: 1044-1050; Mourand et al., (1993) J. Heredity 84: 91-96; патент США №5545822). Была описана точечная мутация подсолнуха, в большой субъединице AHAS, которая придает устойчивость к гербицидам типа имидазолинонов (WO 2007/0118920).
Растения устойчивые к гербицидам типов имидазолинонов или сульфонилмочевин так же были обнаружены. Эти растения приобрели устойчивость естественным образом и были использованы для скрещивания, что привело к гербицид-устойчивым сортам. После анализа устойчивых растений, была определена точечная мутация в белке AHAS подсолнуха приведшая к замене аминокислоты Ala на Val (White et al., (2003) Weed Sel, 51: 845-853).
Кроме того, в патентах США №4761373; 5331107; 5304732; 6211438; 6211439; и 6222100 раскрыты растения устойчивые к имидазолиноновым гербициды. Все эти патенты, как правило, описывают использование измененного гена AHAS, чтобы добиться устойчивости к гербицидам у растений, и, в особенности, раскрывают некоторые имидазолинон-устойчивые линии кукурузы. В патенте США №5731180 и патенте США №5767361 обсуждается выделенный ген, имеющий одну аминокислотную замену в аминокислотной последовательности AHAS однодольных дикого типа, которая приводит к имидазолинон-специфической устойчивости.
В патентных документах WO 2006/007373 и WO 2006/060634 раскрыты мутации, придающие устойчивость к гербицидам имидазолинонового типа растениям пшеницы.
В публикации "Amino acids conferring herbicide resistance in tobacco acetohydroxyacid synthase" описана другая точечная мутация AHAS, которая придает устойчивость к гербицидам (GΜ Crops 1:2, 62-67; February 16, 2010).
В патентном документе US 20100115663 есть ссылка на гербицид-устойчивые растения сорго, полученные изменением генов ацетил-СоА карбоксилазы. Так же раскрыты растения сорго, устойчивые к гербициду динитроанилину (US 20100205686) и растения сорго, устойчивые к гербициду ацетолактат синтаза (WO 2008/073800).
Сущность изобретения
Растения сорго, описанные в настоящем изобретении, проявляют повышенную устойчивость к гербицидам, например, гербицидам, мишенью которых является фермент AHAS, среди прочего, имидазолинонам и сульфонилмочевинам, по сравнению с растениями сорго дикого типа. В частности, растение сорго (Sorghum bicolor), описанное в настоящем изобретении, содержит в составе своего генома по меньшей мере один полинуклеотид, который кодирует большую субъединицу AHAS, имеющую замену аланина на треонин в 93 положении большой субъединицы AHAS сорго или эквивалентном положении, где названное растение имеет повышенную устойчивость к одному или более гербицидам, таким как гербициды, отобранные из группы имидазолинонов, по сравнению с растением сорго дикого типа. Растение сорго может содержать в составе своего генома, одну, две, три или более копий полинуклеотида, кодирующего мутированную большую субъединицу AHAS сорго или полипептид AHAS сорго, описанный в настоящем исследовании. В этой связи, растение сорго может быть устойчивым к любому гербициду, способному ингибировать ферментативную активность AHAS, то есть, растение сорго может быть устойчивым к гербицидам имидазолинонового типа, таким как, без ограничений, имазетапир, имазапир и имазапик или к гербицидам группы сульфонилмочевин, таким как, без ограничений, хлоросульфурон, метсульфурон-метил, сульфометурон-метил, хлоримурон-этил, тиофенсульфурон-метил, трибенурон-метил, бенсульфурон-метил, никосульфурон, этаметсульфурон-метил, римсульфурон, трифлусульфурон-метил, триасульурон, примисульфурон-метил, циносульфурон, амидосульфурон, флюзасульфурон, имазосульфурон, пиразосульфурон-этил и галосульфурон.
В предпочтительном варианте осуществления, растением сорго, описанное в настоящем изобретении, которое устойчиво к гербицидам, принадлежащим группе имидазолинонов или сульфонилмочевин, является линия сорго, названная VT11-11331-ВК, семена которой были депонированы в коллекции NCIMB с номером доступа NCIMB 41870, 12 октября 2011 г, в соответствии с Будапештским Договором. Мутированное растение VT11-11331-BK, его части и его семена содержат в своем геноме мутированный ген AHAS, содержащий полинуклеотид, имеющий нуклеотидную последовательность представленную в SEQ ID No. 1, и кодирующий полипептид или большую субъединицу AHAS, имеющую последовательность представленную в SEQ ID No. 2. Аминокислотная последовательность SEQ ID No. 2, соответствующая большой субъединице AHAS отличается на одну аминокислоту от аминокислотной последовательности дикого типа большой субъединицы AHAS сорго (SEQ ID No. 3), названная разница представляет собой замену аланина на треонин в 93 положении большой субъединице AHAS сорго или в эквивалентных положениях.
Зародышевая плазма гербицид-устойчивого растения сорго настоящего изобретения может быть использована для введения признака устойчивости другим сортам сорго путем интрогрессии. Растения сорго настоящего изобретения включают в себя потомство и семена растений, содержащие полинуклеотид, где названный полинуклеотид кодирует большую субъединицу AHAS и имеет замену аланина на треонин в 93 положении названной большой субъединице AHAS сорго или в эквивалентных положениях, где названное растение демонстрирует повышенную устойчивость к одному или нескольким имидазолиноновым и/или сульфонилмочевиновым гербицидам по сравнению с растением сорго дикого типа. В предпочтительном варианте осуществления, гербицид-устойчивое растение сорго имеет признаки устойчивости как у NCIMB 41870, и может быть растением, описанные в NCIMB 41870, потомством растения NCIMB 41870, мутантом растения NCIMB 41870, потомство растения-мутанта NCIMB 41870. Растение может быть трансгенным или не трансгенным и принадлежать к любому виду растений, пригодному для сельскохозяйственного использования или других использований, например в качестве декоративного растения.
Далее предлагается семя сорго, содержащее своем геноме по меньшей мере один полинуклеотид, где названный полинуклеотид кодирует полипептид, имеющий замену аланина на треонин в 93 положении большой субъединицы белка AHAS сорго. Семя прорастает и порождает растение, имеющие устойчивость к одному или более гербицидам группы имидазолинонов по сравнению с растением сорго дикого типа. В предпочтительном варианте осуществления названным семенем является депонированное как NCIMB 41870.
Далее предлагается способ идентификации растения, устойчивого к гербицидам группы имидазолинонов или сульфонилмочевин, включающий:
(а) обеспечение образца нуклеиновой кислоты из растения сорго;
(б) амплифицирование участка, соответствующего гену AHAS из растения сорго, присутствующего в названном образце нуклеиновой кислоты;
(в) идентификацию растения сорго устойчивого к гербицидам группы имидазолинонов на основании наличия по меньшей мере одной мутации в названном амплифицированном образце нуклеиновой кислоты, которая придает устойчивость к имидазолиноновым гербицидам. В предпочтительном варианте осуществления, отбираются растения, содержащие по меньшей мере одну мутацию в AHAS, такую как мутация в NCIMB 41870, где названная, по меньшей мере одна, мутация в гене AHAS, который кодирует полипептид или большую субъединица AHAS, содержит Ala93Thr замену по сравнению аминокислотной последовательностью AHAS сорго дикого типа. Растение может быть однодольным или двудольным. Предпочтительно, растение является растением, представляющим сельскохозяйственный интерес, таким как сорго, рис, кукуруза, соя, пшеница, овес, ячмень, рожь, лен, хлопок, сахарный тростник, подсолнух или тому подобные. В способ определения может использоваться SNP маркер, специфичный к точечной мутации.
В настоящем изобретении предлагается способ для контроля за сорняками прорастающими в непосредственной близости от сельскохозяйственных растений, например растений сорго, где названные растения сорго являются устойчивыми к гербицидам, таким как гербициды из групп имидазолинонов и/или сульфонилмочевин. В предпочтительном варианте осуществления гербицидом является имидазолиноновый гербицид. Имидазолиноновым гербицидом может быть имазетапир, имазапик или имазапир. Растение может проявлять признаки устойчивости такие как в NCIMB 41870, и оно может быть производным, мутантом, или потомством одного из этих растений.
Настоящее изобретение предлагает полипептид содержащий, без ограничений, одну или более из следующих нуклеотидных последовательностей:
- последовательность представленную в SEQ ID No. 1,
- нуклеотидную последовательность, кодирующую полипептид из SEQ ID No. 2,
- нуклеотидную последовательность, кодирующую полипептид, имеющий по меньшей мере 95% идентичность последовательности с аминокислотной последовательностью из SEQ ID No. 2, где полипептид имеет гербицид-устойчивую AHAS-активность;
- нуклеотидную последовательность имеющую по меньшей мере 85% идентичность с нуклеотидной последовательностью, представленной в SEQ ID No. 1, где нуклеотидная последовательность кодирует полипептид, содержащий большую субъединицу AHAS и имеющий гербицид-устойчивую AHAS-активность,
или последовательности, комплементарные вышеперечисленным.
Предпочтительно полинуклеотид кодирует полипептид большой субъединицы AHAS, содержащий замену Ala93Thr.
Настоящее изобретение так же предлагает экспрессионную кассету, содержащую по меньшей мере один полинуклеотид, имеющий следующую нуклеотидную последовательность: SEQ ID No. 1, нуклеотидную последовательность, кодирующую полипептид, представленный в SEQ Ш No. 2, нуклеотидную последовательность, кодирующую полипептид, имеющий по меньшей мере 95% идентичность последовательности с аминокислотной последовательностью из SEQ ID No. 2, где полипептид имеет гербицид-устойчивую AHAS-активность; нуклеотидную последовательность, имеющую по меньшей мере 85% идентичность с нуклеотидной последовательностью, представленной в SEQ ID No. 1, где нуклеотидная последовательность кодирует полипептид, содержащий большую субъединицу AHAS и имеющий гербицид-устойчивую AHAS-активность, или последовательность, комплементарную вышеперечисленным. Предпочтительно, полинуклеотид кодирует полипептид большой субъединицы AHAS, содержащий Ala93Thr замену; названные последовательности являются функционально связанными с нуклеотидной последовательностью для осуществления экспрессии, например одним или более промотором, энхансером или другой известной регуляторной последовательностью. Промотор может быть промотором для экспрессии в растениях, растительных тканях, хлоропластах, животных, бактериальных клетках, клетках грибов или дрожжей.
Настоящее изобретение предлагает вектор для трансформации, содержащий по меньшей мере один полинуклеотид, имеющий одну из следующих нуклеотидных последовательностей: а) нуклеотидную последовательность, представленную в SEQ ID No. 1, б) нуклеотидную последовательность, кодирующую полипептид, представленный в SEQ ID No. 2, в) нуклеотидную последовательность, кодирующую полипептид, имеющий по меньшей мере 95% идентичность последовательности с аминокислотной последовательностью из SEQ ID No. 2, где полипептид имеет гербицид-устойчивую AHAS-активность, г) нуклеотидную последовательность, имеющую по меньшей мере 85% идентичность с нуклеотидной последовательностью, представленной в SEQ ID No. 1, где нуклеотидная последовательность кодирует полипептид содержащий большую субъединицу AHAS и имеющий гербицид-устойчивую AHAS-активность; далее, содержащий функционально связанные последовательности управляющие экспрессией нуклеотидной последовательности, и селектируемые маркеры. Вектор может быть использован для трансформации бактерий, грибов, дрожжей, растительных клеток и животных клеток, будучи адаптированным для каждого конкретного случая.
Настоящее изобретение предлагает трансформированное растение, содержащее в своем геноме по меньшей мере один промотор, интегрированный в геном и функционально связанный с полинуклеотидом, отобранным из последовательностей: а) нуклеотидной последовательности, представленной в SEQ ID No. 1, б) нуклеотидной последовательности, кодирующей полипептид, представленный в SEQ ID No. 2; в) нуклеотидной последовательности, кодирующей полипептид, имеющий по меньшей мере 95% идентичность последовательности с аминокислотной последовательностью из SEQ ID No. 2, где полипептид имеет гербицид-устойчивую AHAS-активность; г) нуклеотидной последовательности, имеющей по меньшей мере 85% идентичность с нуклеотидной последовательностью, представленной в SEQ ID No. 1, где нуклеотидная последовательность кодирует полипептид содержащий большую субъединицу AHAS и имеющий гербицид-устойчивую AHAS-активность; д) нуклеотидной последовательности, полностью комплементарная одной из нуклеотидных последовательностей от (а) до (г), где вектор далее содержит селектируемый ген и по меньшей мере один промотор, функционально связанный с нуклеотидной последовательностью, которая управляет экспрессией названной нуклеотидной последовательности. Промотором является промотор, управляющий экспрессией полипептида в растениях, например в растительных тканях или хлоропластах. Трансформированные растения могут быть однодольными, например сорго, кукурузой, рисом или пшеницей; двудольными, например подсолнухом, Arabidopsis, табаком или масличным рапсом. Трансформированное растение более устойчиво к гербицидам (имидазолинонам и сульфонилмочевинам) по сравнению с таким же растением дикого типа когда к обоим применяются равные количества названных гербицидов.
Настоящее изобретение так же предлагает способ для получения гербицид-устойчивых растений или растений, имеющих повышенную устойчивость к гербициду, названный способ включает в себя следующие шаги i) трансформация растительной клетки экспрессионной кассетой, содержащей полинуклеотид ii) регенерация растительной клетки для получения гербицид-устойчивого растения, названный полинуклеотид содержит по меньшей мере одну из следующих нуклеотидных последовательностей: а) нуклеотидную последовательность представленную в SEQ ID No. 1, б) нуклеотидную последовательность, кодирующую полипептид, представленный в SEQ ID No. 2, в) нуклеотидную последовательность, кодирующую полипептид, имеющий по меньшей мере 95% идентичность последовательности с аминокислотной последовательностью из SEQ ID No. 2, где полипептид имеет гербицид-устойчивую AHAS-активность, г) нуклеотидную последовательность, имеющую по меньшей мере 85% идентичность с нуклеотидной последовательностью, представленной в SEQ ID No. 1, где нуклеотидная последовательность кодирует полипептид содержащий большую субъединицу AHAS и имеющий гербицид-устойчивую AHAS-активность и д) нуклеотидную последовательность полностью комплементарную одной из нуклеотидных последовательностей от (а) до (г). ДНК экспрессионная кассета содержит по меньшей мере один промотор для управления экспрессией полипептида в растениях, например в растительных тканях или в хлоропластах. Трансформированные растения могут быть однодольными, например сорго, кукурузой, рисом или пшеницей; двудольными, например подсолнухом, Arabidopsis, табаком, соей или масличным рапсом. Трансформированное растение устойчиво к гербицидам (имидазолинонам и сульфонилмочевинам) по сравнению с таким же растением дикого типа когда к обоим применяются равные количества названных гербицидов. Растение содержит большую субъединицу AHAS, устойчивую к гербицидам.
Описание графического материала
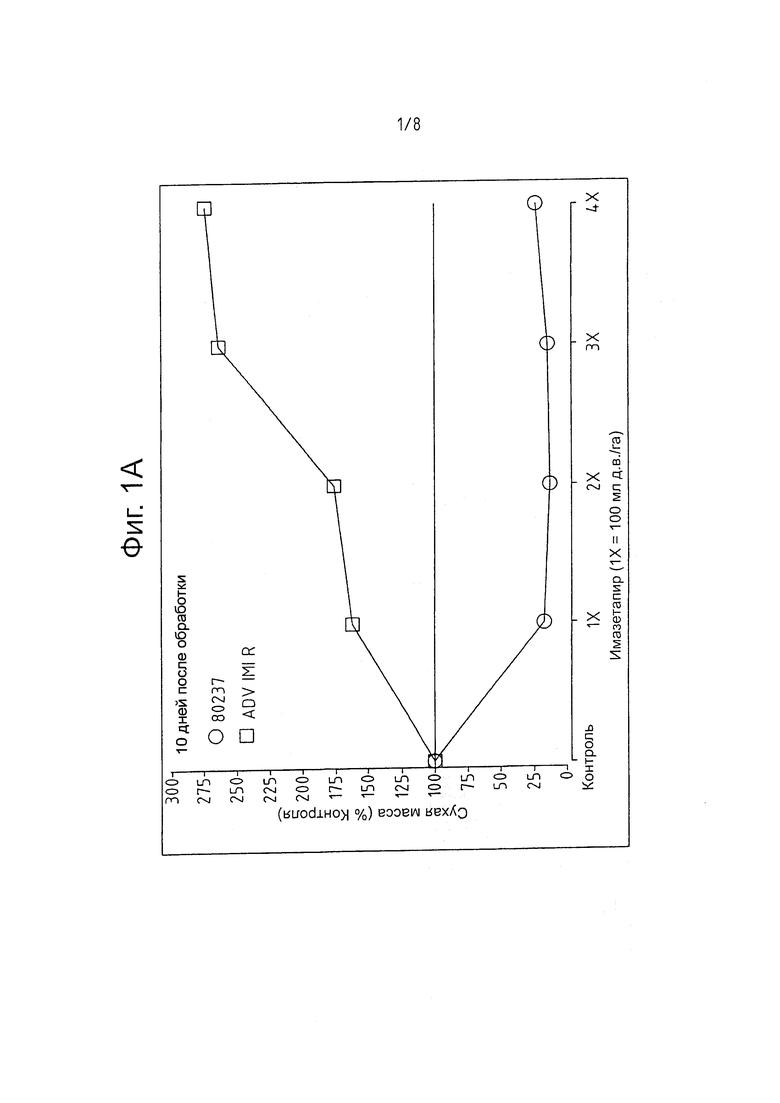
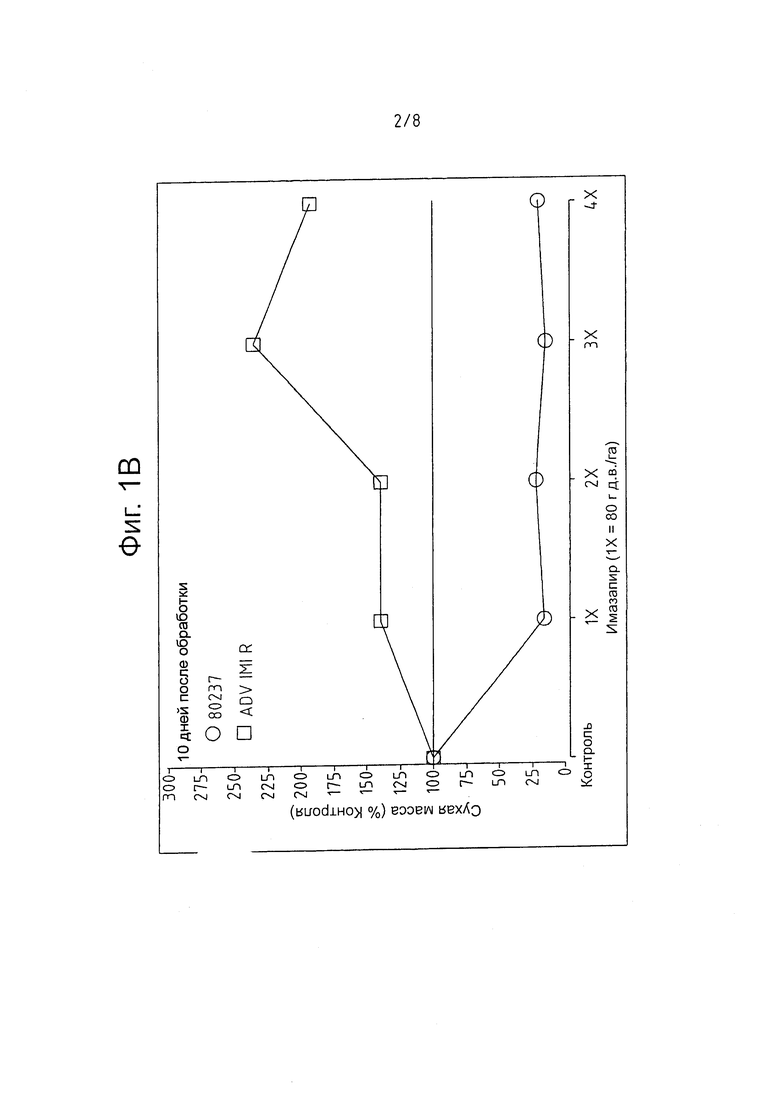
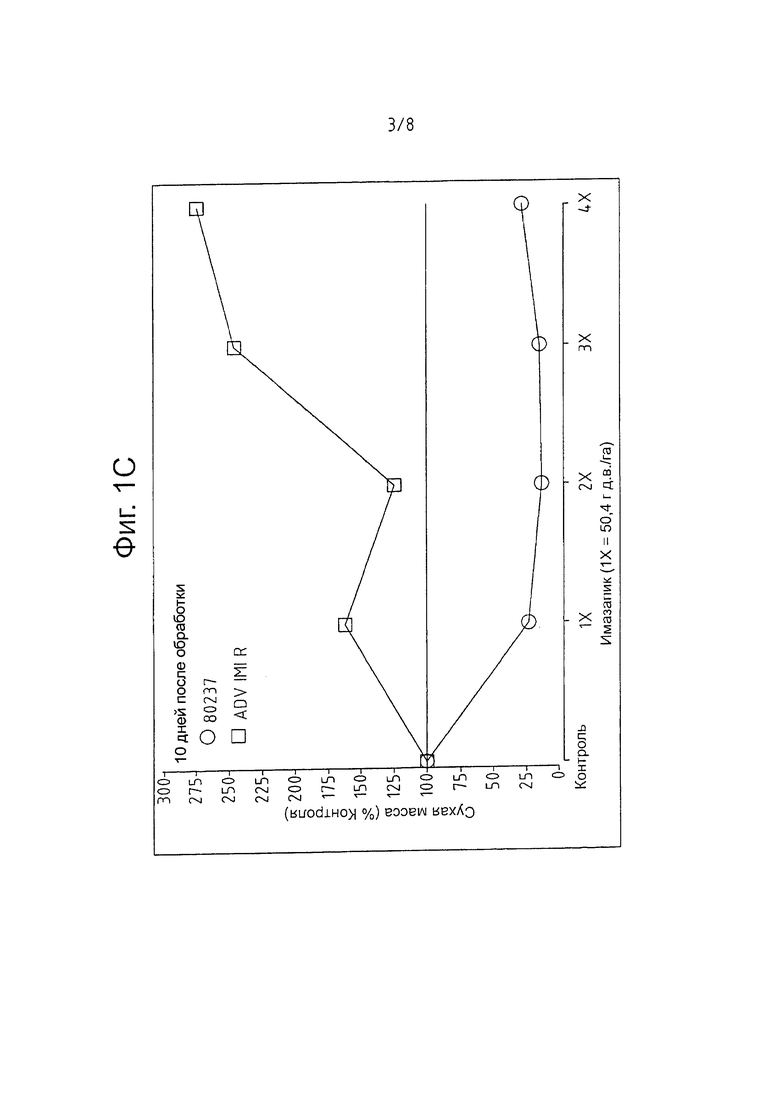
На фигуре 1 представлены кривые дозовой зависимости имидазолинон-устойчивых мутантных линий сорго (ADV-IMI-R) и исходной эндогамной линии сорго 80237 или линии дикого типа. Испытывали гербициды: имазетапир, имазапир и имазапик при расходах 0 (контроль), 1X, 2Х, 3Х, and 4Х. Гербицидное действие определяли как процент сухой массы (DM) надземных тканей по сравнению с необработанным контролем; каждое значение является средним трех измерений.
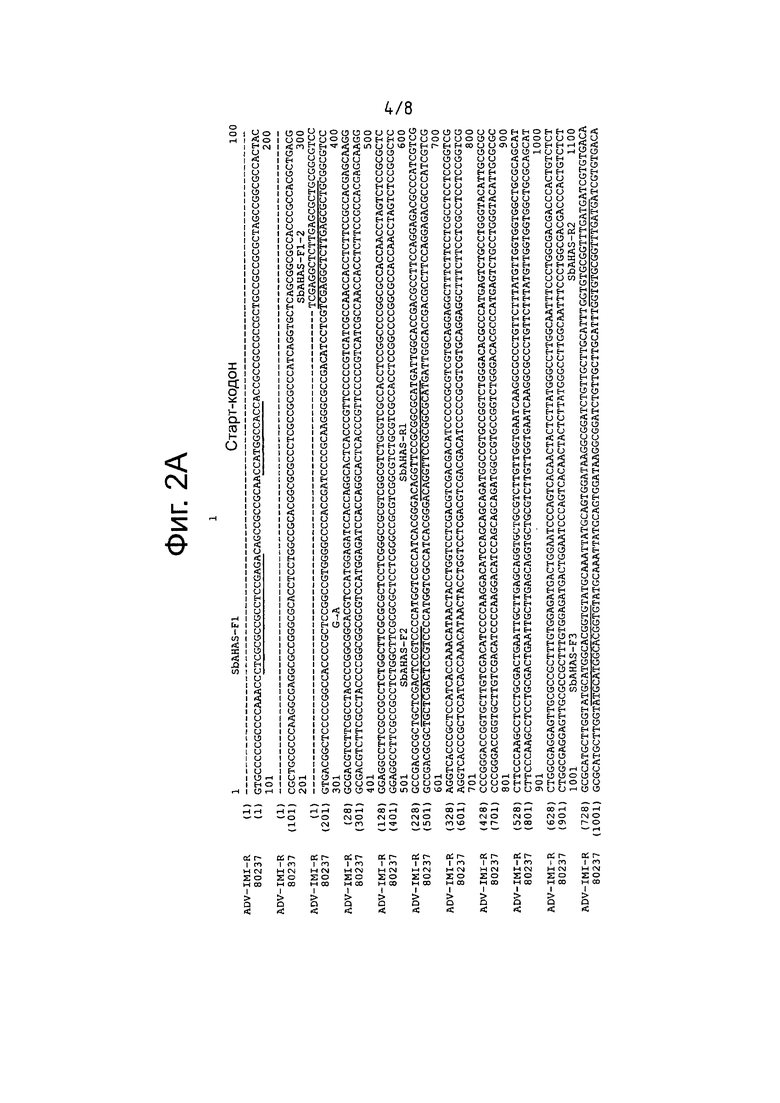
На фигуре 2 представлено выравнивание мутантной нуклеотидной последовательности ADV-IMI-R AHAS и последовательности исходной эндогамной линии сорго 80237 или линии дикого типа. Замена нуклеотида G на А указана в положении +277, что различает обе последовательности. Подчеркнуты различные праймеры, использованные для амплифицирования перекрывающихся последовательностей ампликонов.
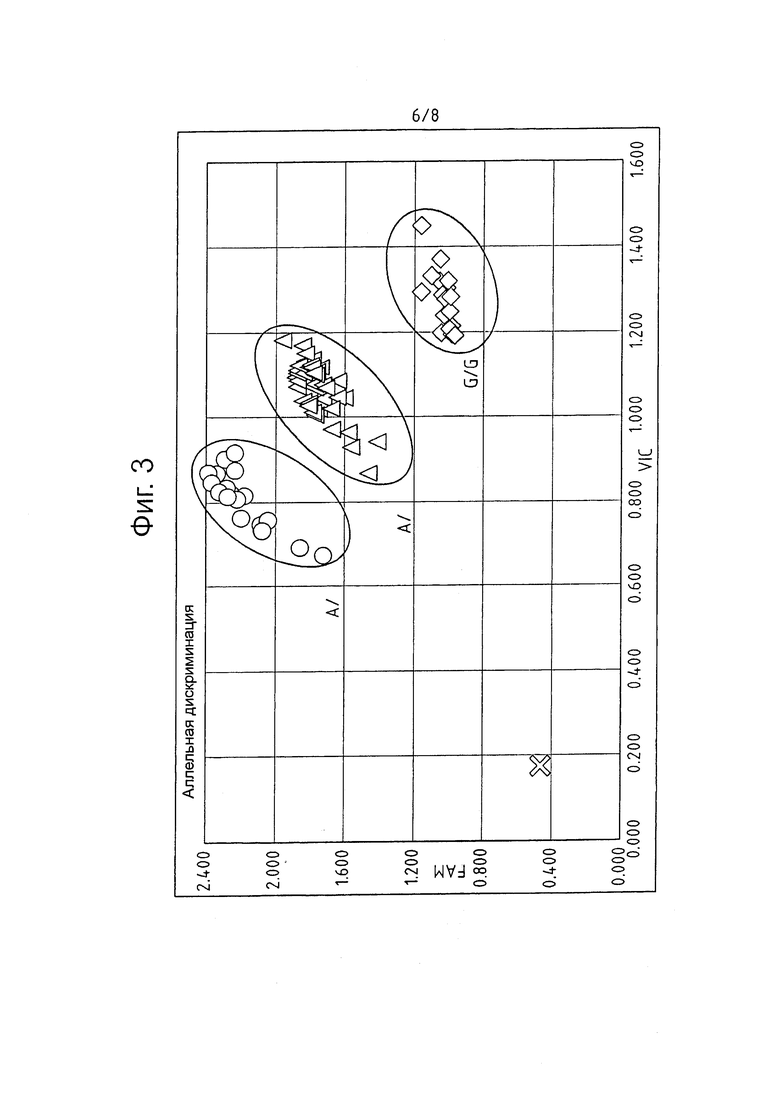
На фигуре 3 представлены результаты генотипирования с помощью SNP по признаку G/A в кодоне 93 гена AHAS сорго. Специфический SNP-SbAHAS маркер анализировали в генотипе 177 растений поколения F2 от ADV-IMI-R × F2 90523. Были однозначно выделены три группы и отмечены точками (•), соответствующие гомозиготным растениям с мутантной аллелью (А/А), треугольниками (▲), соответствующие гетерозиготным растениям (A/G) и ромбами (♦), соответствующие гомозиготным растениям с аллелью дикого типа (G/G).
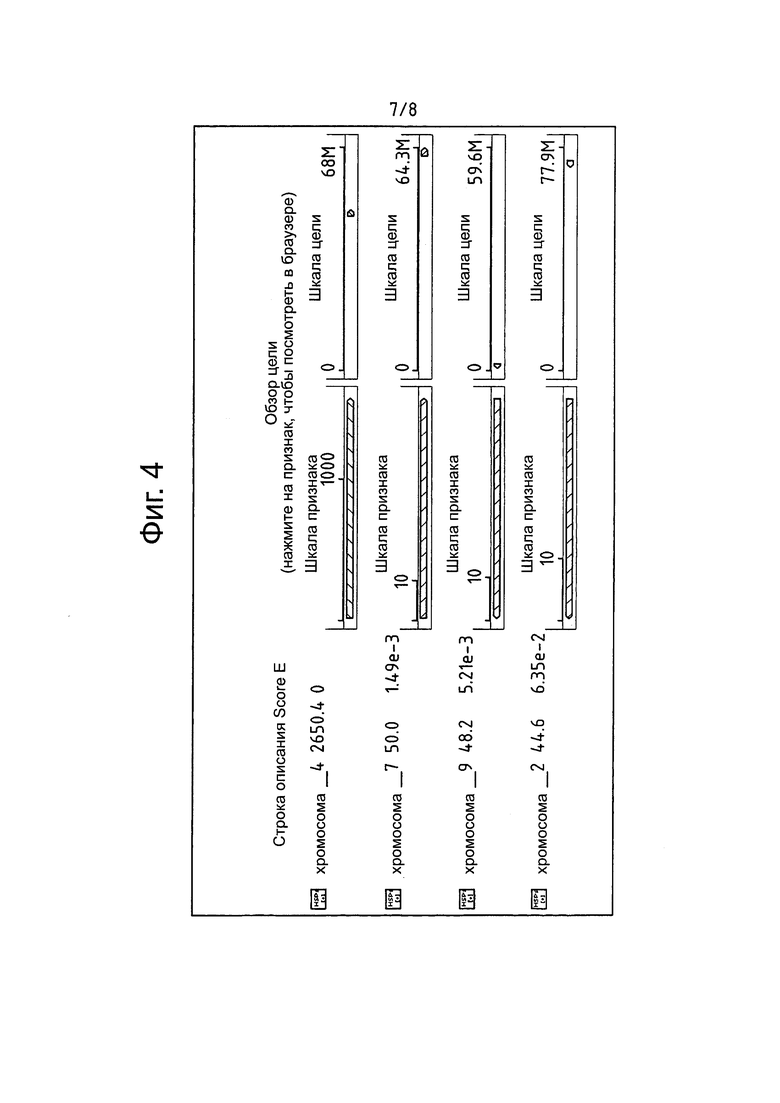
На фигуре 4 представлены результаты, полученные при совмещении нуклеотидной последовательности гена AHAS сорго (номер доступа GM663363.1) с геномной последовательностью сорго (Sorghum bicolor) депонированной в базе данных нуклеотидных последовательностей Phytozome (http://www.phytozome.net/search.php). Это совмещение показало, что последовательность AHAS GM663363.1 имеет сильно выраженную гомологию (величина е=0) с последовательностью AHAS, расположенной на хромосоме 4 генома сорго, это свидетельствует о том, что исследуемый ген находится в этой группе сцепления.
На фигуре 5 представлена карта сцепления хромосомы 4 S. bicolor. Расстояние между соседними маркерами выражены в сантиморганах (сМ). Указано положение на хромосоме SNP-SbAHAS и устойчивости к имазетапиру со ссылкой на 7 SSR в хромосоме 4 генотипа 177 растений F2. Карты была построена с помощью JoinMap, с использованием параметров по умолчанию - LOD=3 и максимальное расстояние Косамби 50 сМ.
Подробное описание настоящего изобретения
Для того, чтобы получить гербицид-устойчивые растения, растения эндогамной линии 80237 сорго (Sorghum bicolor) обрабатывали водным раствором этилметансульфоната (EMS). Обработанные семена высаживали и оставляли для свободного опыления. Отбирали двести семьдесят три M1 растения и два семени каждого растения высаживали в питомник, таким образом получая всего 546 М2 растений. Пыльцу одного растения из каждой пары собирали и использовали для опыления другого растения из этой пары. Собирали М3 семена, полученные от каждого из 273 опыленных М2 растений. М3 потомством было засажено всего 273 бороздки. Пятьдесят растений из каждой М3 бороздки опрыскивали 100 мл л д.в./га имазетапира. Шестьдесят восемь растений в бороздках показали нормальный рост и отсутствие симптомов после применения гербицида и рассматривались как устойчивые к гербициду и были определены как VT09-9754. Определяли генеалогию устойчивых растений из бороздок и обозначали их как 80237EMS2-192 (в дальнейшем в этом документе именуемые как ADV-IMI-R). Гербицид-устойчивые М7 мутантные растения и семена, селекционированные из исходных ADV-IMI-R мутантов (обозначенных VT11-11331-BK), были получены и депонированы в собрание NCIMB с номером доступа NCIMB 41870, в соответствии с Будапештским Договором, 12 октября 2011 г.
Настоящее изобретение не ограничено растением сорго, мутированным с помощью EMS. В рамках настоящего изобретения находятся растения сорго, полученные другими способами мутации, например способами, такими как радиоактивными и химическими мутагенами. Гербицид-устойчивые мутантные растения могут так же быть получены с помощью способа селективного давления на клетки, культивируемые с гербицидом и селектированием устойчивых клеток для образования гербицид-устойчивого растения. Тонкости способов мутирования и селекции можно найти в "Principles of Cultivar Development" Fehr, 1993, Macmillan Publishing Company, раскрытие которой включено в настоящей документ в качестве ссылки.
Далее, эффект от опрыскивания гербицидом мутантных имидазолинон-устойчивых растений ADV-IMI-R (исходная мутация) сравнивали с реакцией эндогамной линии сорго 80237 (элитная линия в собственности Advanta). С этой целью, растения в поле обрабатывали тремя гербицидами, принадлежащими семейству имидазолинонов: имазетапиром, имазапиром и имазапиком. Испытывали четыре различных расхода: 1X, 2Х, 3Х и 4Х для каждого из гербицидов. Рекомендуемая норма расхода (IX) для каждого гербицида приведена в Таблице 1.

Через десять дней после опрыскивания, определяли сухую массу (DM) надземных тканей всех растений. Результаты представлены на Фигуре 1.
Реакцию ADV-IMI-R мутанта, описанного в настоящем изобретении, сравнивали с реакцией эндогамной линии сорго 80237. В Таблице 2 приведены эффекты различных расходов имазетапира, имазапира и имазапика, выраженные в процентах от сухой массы по сравнению с необработанным контролем (DM % Контроля). Раскрываемые значения являются средним от трех экспериментов.
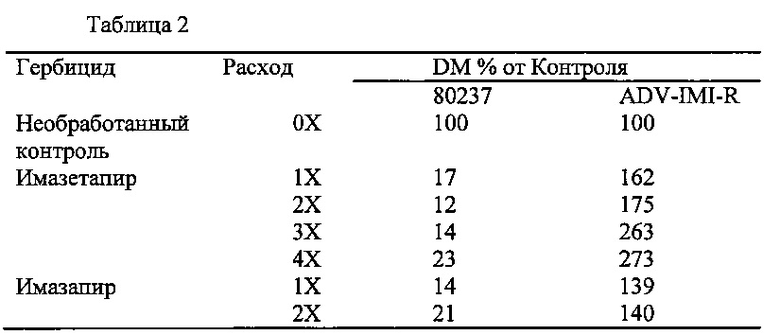

Из представленных результатов видно, что ADV-IMI-R мутант, описанный в настоящем изобретении, устойчив к трем испробованным гербицидам группы имидазолинонов даже при расходах в 4Х. С другой стороны, исходная эндогамная линия сорго 80237 очевидно чувствительная ко всем гербицидам, даже когда применялась рекомендуемая норма расхода (1X).
Как можно увидеть, гербицид-устойчивые растения сорго, описанные в настоящем изобретении устойчивы к гербицидам группы имидазолинонов, таким как, имазетапир, имазапик или имазапир.
Имидазолинон-устойчивые растения сорго могут быть опрыскиваемы количествами гербицидов любой известной группы имидазолинонов, которые в 4 раза превышают рекомендуемые к использованию дозировки. Устойчивое растение может иметь, например, признаки устойчивости, наблюдаемые в растениях из семян NCIMB 41870, или это может быть растение, полученное из них, потомство или другие растения, содержащие в составе своего генома по меньшей мере один полинуклеотид, кодирующий полипептид, имеющий замену аланина на треонин в 93 положении в белке AHAS сорго или в эквивалентном положении, где названное имеет повышенную устойчивость к одному или более гербицидам группы имидазолинонов по сравнению с растением сорго дикого типа.
Далее, для специалиста известно, что такие аминокислотные положения могут отличаться в зависимости от того добавлены аминокислоты или убраны, например, с N-концевой части аминокислотной последовательности. Под "эквивалентным положением" имеется в виду положение, находящиеся в границах того же самого консервативного участка, что и приведенное в пример положение аминокислоты.
В настоящем изобретении термины "устойчиво" к гербициду и "толерантно" к гербициду имеют одинаковое значение и равноценный масштаб когда применяются в отношении гербицидов, таких как имидазолиноны или сульфонилмочевины.
Настоящее изобретение предлагает растения, клетки растений, растительные ткани демонстрирующие устойчивость к эффективным количествам гербицидов. Под "эффективными количествами" имеются в виду количества гербицида, способные ингибировать рост растений дикого типа, растительных клеток или тканей, но которые не оказывают серьезного воздействия устойчивые растения, клетки растений или ткани растений. Эффективным количеством гербицида является рекомендуемая норма расхода для устранения сорняков. Растение дикого типа, клетка или ткань - такие, не имеют признаков устойчивость к гербицидам, например, гербицидам, принадлежащим к группе имидазолинонов или сульфонилмочевин. Термин "растение" охватывает растение в любой стадии, или части растений, где названными частями растений могут быть семена, листья, цветы, стебли, ткани или органы, хорошо известные опытному ботанику.
Для того, чтобы определить мутацию, секвенировали мутированный ген AHAS сорго, описанный в настоящем изобретении, который кодирует полипептид, имеющий активность синтазы ацетогидроксикислот, где названный полипептид AHAS или большая субъединица AHAS являются гербицид-устойчивыми.
Сравнение последовательности ДНК гена AHAS из мутированных растений с последовательностью ДНК гена AHAS из растений сорго дикого типа выявило точечную мутацию, которая представляет собой замену нуклеотида G в нуклеотидном положении +277 на А, что отличает исходную линию сорго 80237 (дикого типа) от ADV-IMI-R мутанта, описанного в настоящем изобретении. Когда аминокислотные последовательности AHAS из линий мутанта дикого типа были выведены, было отмечено, что нуклеотидная замена (GCG на ACG в SEQ ID No. 1) кодировала мутированный полипептид в кодоне 93 и приводила к замене аланина на треонин (Ala93Thr) в полипептиде (SEQ ID No. 2), имеющем активность синтазы ацетогидроксикислот и соответствующем большой субъединице белка AHAS сорго мутированной линии ADV-IMI-R.
В объем настоящего изобретения входят растения, части растений, семена, их потомство, трансгенные растения или что-либо подобное, содержащие полинуклеотид, кодирующий полипептид, имеющий замену аланин-на-треонин (Ala93Thr) в положении 93 названного полипептида или в эквивалентном положении другого фермента AHAS, принадлежащего другому виду.
В объем настоящего изобретения входят полинуклеотид или полипептид, имеющие идентичность последовательности по меньшей мере 85%, 95% или 98%. Процент идентичности последовательности определяется выравниванием двух аминокислотных последовательностей или двух нуклеотидных последовательностей. Процент выравнивания между двумя последовательностями может быть рассчитан, например, с использованием следующей формулы:
(количество идентичных положений/суммарное количество перекрывающихся положений)×100
Процент выравнивания между двумя последовательностями определяется с использованием различных математических алгоритмов, например, алгоритмов, включенных в программы NBLAST и XBLAST из Altschul et al, (1990) J. Mol. Biol. 215: 403. При использовании программ BLAST, Gapped BLAST и PSI-Blast, могут быть использованы исходные параметры соответствующих программ (например, XBLAST и NBLAST). Смотри http://wvvw.ncbi.nlm.nih.gov. Другим предпочтительным, не ограничительным примером математического алгоритма, используемого для сравнения последовательностей является алгоритм Myers и Miller (1988) CABIOS 4:11-17. Такой алгоритм включен в программу ALIGN (версия 2.0), которая является частью программного обеспечения для выравнивания последовательностей GCG sequence allignment. При использовании программы ALIGN для сравнения аминокислотных последовательностей, таблица весов замен остатков РАМ 120, штраф за удлинение разрыва 12 и штраф за разрыв 4 могут быть использованы. Выравнивание так же может быть проведено визуальным осмотром.
Настоящее изобретение включает в свой состав полинуклеотиды и белки, придающие устойчивость к гербицидам. Должно быть понятно, что когда говорится о гербицид-устойчивом полинуклеотиде, имеется в виду полинуклеотид, кодирующий гербицид-устойчивый белок AHAS. Гербицид-устойчивые белки AHAS могут быть естественными или мутантными и они придают устойчивость к гербицидам, принадлежащим к группе имидазолинонов или сульфонилмочевин.
Наследование устойчивости к имидазолинонам, например имазетапиру, исследовали в расщепляющейся F2 популяции сорго, порожденной скрещиванием имазетапир-чувствительной линии с ADV-IMI-R мутантом. F2 растения, полученные таким образом, опрыскивали имазетапиром (Pivot®, BASF) с расходом 3Х, в течение 20 дней в стадии V6 после всхождения, фенотипические симптомы оценивали через 10 дней после обработки. Полученные результаты представлены в Таблице 3. 
Из результатов видно, что растения F2 популяции могут быть классифицированы на основании внешних симптомов, в соответствии фенотипической оценкой, что позволило объединить отдельные особи в три фенотипические категории: растения без повреждений, хлоротические растения и погибшие растения.
Секвенирование показало, что гербицид-устойчивый мутант сорго, описанный в настоящем изобретении имел точечную мутация в полипептиде, имеющем активность синтазы ацетогидроксикислот или в большой субъединице белка AHAS. Нуклеотидная последовательность, представленная в SEQ ID No. 1, демонстрирует, что нуклеотид G заменен на А в нуклеотидном положении +277 (соответствующем кодону 93), что отличает исходную эндогамную линию сорго 80237 (чувствительную к гербицидам) от индуцированного мутанта ADV-IMI-R, описанного в настоящем изобретении. Этот молекулярный маркер был назван SNP-SbAHAS.
Для определения применимости SNP-SbAHAS маркера для определения потенциально гербицид-устойчивых растений, частей растений или семян, исследовали 177 растений популяции F2, полученной скрещиванием гербицид-устойчивого мутанта ADV-IMI-R (отбор VT09-9754-48-6-BK) с гербицид-чувствительной эндогамной линией 90523 (в данном документе называемая популяцией ADV-IMI-R × 90523 F2). На Фигуре 3 в качестве примера приведена дискриминация аллелей некоторых растений из популяции F2. Два исследованных контроля были классифицированы в предсказанные группы (ADV-IMI-R мутант и линия дикого типа 90523, гомозиготные устойчивые и гомозиготные чувствительные, соответственно). Полученные данные подтверждают, что молекулярный маркер SNP-SbAHAS применим для различение трех аллельных в нуклеотидном положении +277 полинуклеотида, кодирующего полипептид, имеющий активность синтазы ацетогидроксикислот или большую субъединица белка AHAS сорго.
Средние специалисты в данной области могут, в свете открытия SNP-SbAHAS маркера и его применения, определить гербицид-устойчивые растения, например к таким как гербициды, принадлежащие группе имидазолинонов и/или сульфонилмочевин, например, имазетапиру, имазапику или другим. Способом идентификации может быть, помимо способа, описанного в настоящем документе, любой другой известный способ, смотри, например ASA (Soleimani et al., (2003) Plant Mol Biol Rep 21: 281-288), PAMSA (Gaudet et al., (2007) Plant Mol Biol Rep 25: 1-9), SSCP (Germano and Klein (1999) Theor Appl Genet 99: 37-49) или TaqMan® (Jones et al., (2008) Pest Management Science 64: 12-15).
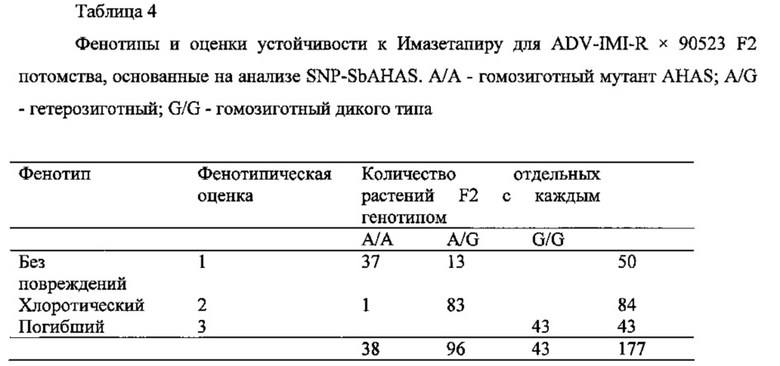
Корреляция между устойчивым фенотипов и количеством мутантных аллелей исследовали с помощью SNP-SbAHAS маркера. Для этой цели, хлоротический и погибший фенотипы отдельных растений из F2 потомства (ADV-IMI-R × 90523) изучали после опрыскивания имазетапиром. Наряду с этим, изучали генотип SNP-SbAHAS маркера. Полученные результаты представлены в Таблице 4. Корреляцию между молекулярным маркером SNP-SbAHAS и устойчивостью к имазетапиру (определенной как фенотипическая оценка) определяли с использованием теста на взаимную независимость их квадрат. В результате теста было получено значение вероятности р=1.948 с-46, указывающее на высоко-значимую корреляцию между индуцированной мутацией в гене AHAS (генотипирование с использованием специфического маркера SNP-SbAHAS) и устойчивостью к имазетапиру, в соответствие с совместным разделением фенотипа и генотипа.
Далее, было выполнено генетическое картирование гербицид-устойчивости и специфического SNP-SbAHAS маркера. На основании последовательности AHAS сорго, раскрытой в GenBank (номер доступа GM663363.1, SEQ ID No. 4), выполняли анализ BLAST для сравнения последовательности ДНК Sorghum bicolor с базой данных Phytozome (http://www.phytozome.net/search.php). Полученные результаты, представленные на Фигуре 4, указывают, что последовательность AHAS, ассоциированная с устойчивостью к гербицидам, принадлежащим группе имидазолинонов расположена на хромосоме 4 генома Sorghum bicolor. На основании полученной информации была проведена процедура фингерпринтинга (генотипирования) для мутированной линии ADV-IMI-R, описанной в настоящем изобретении и эндогамной линии 90253, с использованием различным молекулярный маркеров ДНК SSR-типа. Семь полиморфных SSR, расположенных на хромосоме 4, были отобраны для генотипирования (Mace, ES et al., А consensus genetic тар of sorghum that integrates multiple component maps and high-throughput Diversity Array Technology (DArT) markers, BMC Plant Biology, 2009, 9: 13; Srinivas, G et al., Exploration and mapping of microsatellite markers from subtracted drought stress ESTs in Sorghum bicolor (L.), Moench. Theor. Appl. Genet. 2009, 118: 703-717; Ramu, Ρ et al., In silico mapping of important genes and markers available in the public domain for efficient sorghum breeding, Mol Breeding 2010, 26: 409-418; http://www.lbk.ars. usda.gov/psgd/sorghum/2009SorghumSEAMs_LBKARS.xls).
Имея результаты вышеописанной процедуры было возможно генетически картировать как SNP-SbAHAS маркер, так и устойчивый фенотип, что указывает на расположение устойчивости к имидазолинонам и специфического SNP-SbAHAS маркера на хромосоме 4 между ранее идентифицированными SSR в хромосоме 4 Sorghum bicolor (Фигура 5).
Полинуклеотид, описанный в настоящем изобретении (SEQ ID No. 1) может быть введен в растения для получения трансгенных растений. Существуют различные способы введения полинуклеотида в растения, в частности в растения, представляющие сельскохозяйственный интерес, например кукурузу, сою, сорго, пшеницу, сахарный тростник, лен, подсолнух или другие растения; овощи, деревья или декоративные растения. Способы для введения полинуклеотидов для получения трансгенных растений хорошо известны в этой области техники, и так же могут быть использованы рекомбинантные способы.
Существуют различные способы трансформации растений, например с использованием векторов (An, G. et al., (1986) Plant Pysiol, 81: 301-305; Fry, J., et al., (1987) Plant Cell Rep., 6: 321-325; Block, M. (1988) Theor. Appl Genet., 76: 767-774; Hinchee, et al., (1990) Stadler. Genet. Symp, 203212.203-212; Barcelo, et al., (1994) Plant J., 5: 583-592; Becker, et al., (1994) Plant J., 5: 299-307; Borkowska et al., (1994) Acta Physiol Plant., 16: 225-230; Christou, et al., (1992) Trends Biotechnol, 10: 239-246; D'Halluin, et al, (1992) Bio/Technol., 10: 309-314; Dhir, et al., (1992) Plant Physiol, 99: 81-88; Casas et al., (1993) Proc. Nat. AcadSci. USA 90: 11212-11216; Dong, J.A. and Mchughen, A. (1993) Plant Sci., 91: 139-148; Golovkin, et al., (1993) Plant Sci., 90: 41-52; Guo Chin Sci., Bull, 38: 2072-2078; Asano, et al., (1994) Plant Cell Rep., 13; Christou, P. (1994) Agro. Food. Ind. Hi Tech., 5: 17-27; Eapen et al., (1994) Plant Cell Rep., 13: 582-586; Hartman, et al., (1994) Bio-Technology 12: 919923; Christou, P. (1993) In Vitro Cell. Dev. Biol-Plant; 29P: 119-124; Davies, et al., (1993) Plant Cell Rep, 12: 180-183; Ritala, et al., (1994) Plant. Mol. Biol. 24:317-325; and Wan, Y.C. and Lemaux, P.G. (1994) Plant Physiol, 104:3748).
Некоторые способы трансформации растений и генно-инженерные приемы описаны в Sambrook, et al., (1989) Molecular cloning, A laboratory manual, Cold Spring Harbor Press, Plainview, N.Y.; Ausubel FM, et al., Current Protocols in Molecular Biology, John Wiley & Sons, New York, N. Y.
Вектор может так же быть введен с использованием приемов баллистического ускорения частиц, таких как описанные в патенте США №4945050 и в Casas el. al., Proc. Natl. Sel, USA, 90: 11212, 1993
Растения, трансформированные, например, полинуклеотидом, описанным в настоящем изобретении, экспрессируют гербицид-устойчивые белки AHAS проявляют признаки устойчивости к гербицидам, таким как имидазолиноны и/или сульфонилмочевин. Под "гербицид-устойчивыми белками AHAS" имеются в виду белки, имеющие AHAS активность, которая выше AHAS активности дикого типа в присутствии гербицидов, влияющих на AHAS активность, в концентрациях в которых гербицид влияет на AHAS активность белка AHAS дикого типа.
Полинуклеотидная последовательность, описанная в настоящем изобретении может быть включена в состав экспрессионной кассеты для экспрессирования устойчивых белков AHAS в целевых растениях, например, представляющих сельскохозяйственный интерес. Кассета содержит регуляторную последовательность, функционально связанную, например, с по меньшей мере одним промотором. Промоторы хорошо известны в данной области техники, и могут быть, например, конститутивными, индуцируемыми, тканеспецифичными, хлоропласт-специфичными промоторами, все из которых являются функциональными в растениях. Далее, кассета содержит последовательности терминации транскрипции, известные в данной области техники. Кассета может содержать различные регуляторные последовательности для того, чтобы улучшать эффективность экспрессии гербицид-устойчивых AHAS полинуклеотидов, например энхансеры, такие как интроны, вирусные последовательности или что-либо в этом роде; или кассеты могут содержать другие последовательности полинуклеотидов, представляющие интерес, отличающиеся от полинуклеотида, описанного в настоящем изобретении, связанные с названные полинуклеотидом или нет; или лидерные последовательности.
Промоторы включают в себя, но не ограничены, конститутивными, индуцируемыми, ткане- или органелла-специфичными промоторами, таким как 35S промотор, индуцируемым раной или химически индуцируемым промотором, промотором генов теплового шока, тетрациклин-индуцируемьгм промотором или каким-либо другим промотором (Chao et. al. 1999, Plant Physiol, 120: 979; патенты США 5187267 и США 5057422.
Среднему специалисту в данной области техники так же известны подходящие терминаторы транскрипции, которые могут быть использованы в растениях, смотри, например, Odell, et al., 1985, Nature 313: 810; Sanfacon, et. al., Genes Dev., 5: 141, 1990; Munroe, et al., 1990 Gene 91: 151; Rosenberg et al., 1987, Gene 56: 125; Joshi, et al., Nucleic Acid Res., 15: 9627, 1987.
"Функционально связанный" предназначено для обозначения функциональной связи между промотором и второй последовательностью. Последовательность промотора инициирует и опосредует транскрипцию последовательности ДНК, соответствующей второй последовательности. Термин "функционально связанный" означает, что связанные последовательности нуклеиновой кислоты являются непрерывными и, когда необходимо объединение двух белок-кодирующих участков, непрерывными и в одной рамке считывания. Кассетой может быть несколько экспрессионных кассет.
Полинуклеотид, описанный в настоящем изобретении, может быть присоединен к другим полинуклеотидам в виде слитых полинуклеотидов или раздельных. Другие полинуклеотиды могут кодировать, например, гербицид-устойчивые, устойчивые к насекомым или другие части растений хорошо известные среднему специалисту в данной области техники.
Для улучшения экспрессии в растениях, полинуклеотид, описанный в настоящем изобретении может быть модифицирован, например введением кодонов, предпочтительных для растений, удалением последовательностей, таких как интроны или вредоносные последовательности. Так же, в рамках настоящего изобретения находится полинуклеотид, кодирующий устойчивый AHAS полипептид, описанный в настоящем изобретении, который был мутирован, и имеет, например, делеции или вставки, или другие мутации, отличные от описанной в настоящем документе. Под "мутированным полинуклеотидом" имеется в виду полинуклеотид, имеющий постоянные изменения в своей нуклеотидной последовательности.
Полинуклеотид, описанный в настоящем изобретения может быть изменен заменами, делениями, усечениями и вставками. Способы для таких манипуляций обычно известны в данной области техники. Способы мутагенеза и изменения нуклеотидных последовательностей хорошо известны в данной области техники (Kunkel (1985) Proc. Natl. Acad Set, USA 82: 488-492; Kunkel et al., (1987) Methods in Enzymol, 154: 367-382; Walker and Gaastra, eds., (1983) Techniques in Molecular Biology (MacMillan Publishing Company, New York) и ссылки противопоставленные в перечисленных публикациях. Аминокислотные замены, которые не влияют на биологическую активность исследуемого белка, можно найти в Dayhoff et al., (1978) Atlas of Protein Sequence and Structure (Natl. Biomed. Res. Found., Washington, D.C.), включенный в настоящую заявку в качестве посредством ссылки.
ДНК, содержащая полинуклеотид AHAS, описанный в настоящем изобретении может быть введена в различные растения как часть вектора. Выбор подходящего вектора зависит от предполагаемого способа трансформации и растения, которое собираются трансформировать. Средним специалистам в данной области техники хорошо известны различные векторы, например, Ti и/или Ri. Т-ДНК так же используется в качестве фланкирующих участков для интегрирующихся Ti или Ri векторов (WO 84/02913, Herrera-Estrella et al., 1983, Nature 303: 209; Horsch et al., 1984, Science 223: 496; Fraley et. al., 1983, Proc. Natl. Acad. Sci, USA 80:4803.
Вектор может содержать экспрессионную кассету и другие нуклеотидные последовательности, например селектируемые маркеры, такие как маркеры, придающие устойчивость к антибиотикам или гербицидам, и последовательности, запускающие экспрессию данных полинуклеотидов в растениях, например, полипептида большой субъединицы AHAS из SEQ ID No. 2.
Вектор, содержащий полинуклеотид, кодирующий устойчивые полипептиды AHAS, описанные в настоящем изобретении, может быть использован для получения трансгенного растения, которое устойчиво к гербицидам типов имидазолинонов и сульфонилмочевин. Трансформированные растения могут быть любыми типами растений, такими как двудольные и однодольные, среди которых, без ограничений, растениями, представляющими сельскохозяйственный интерес, такими как, сорго (Sorghum bicolor, Sorghum vulgare), кукуруза (Zea mays), Brassica sp.(например, В. napus, В. rapa, В. juncea), люцерна (Medicago sativa), рис (Oryza sativa), рожь (Secale cereale), просо (Pennisetum glaucum), (Panicum miliaceum), (Setaria itálica), (Eleusine coracand), подсолнух (Helianthus annuus), пшеница (Triticum aestivum, T. Turgidum ssp.durum), соя (Glycine max), табак (Nicotiana tabacum), земляной орех (Arachis hypogaea), хлопок (Gossypium barbadense, Gossypium hirsutum), сладкий картофель (Ipomoea batatus), маниок (Manihot esculenta), кофе (Coffea spp.), кокос (Cocos nucífera), сафлор (Carthamus tinctorius), ананас (Ananas comosus), цитрусовые (Citrus spp.), шоколадное дерево (Theobroma cacao), чайный куст (Camellia sinensis), банановое дерево (Musa spp.), авокадо (Persea americana), маслина европейская (Olea europaea), анакард (Anacardium occidentale), миндальное дерево (Prunus amygdalus), сахарная свекла (Beta vulgaris), картофель (Solanum tuberosum), сахарный тростник (Saccharum spp.), овощи, декоративные растения и деревья. Предпочтительно, растением, настоящего изобретения является сорго.
Настоящее изобретение лучше проиллюстрировано в следующих примерах, которые не следует толковать как ограничивающие его объем. Наоборот, необходимо четко понимать, что другие варианты осуществления, модификации и эквиваленты настоящего изобретения могут быть осуществлены после прочтения настоящего описания, и могут быть предложены кем-либо из средних специалистов в данной области техники без отступления от существа и объема настоящего изобретения и/или объема притязаний прилагаемой формулы изобретения.
ПРИМЕРЫ
ПРИМЕР 1
Мутагенез эндогамной линии сорго 80237 и отбор имидазолинон-устойчивого мутанта 80237EMS2-192
Тридцать две тысячи предварительно пророщенных семян сорго эндогамной линии 80237 погружали в водный раствор 0.05% об/об этилметансульфоната (EMS) на 16 часов. Обработанные семена высаживали на экспериментальной станции Advanta Seeds в Venado Tuerto, Province of Santa Fe, Argentina, опытный участок No. 1 (33° 41' 47" S; 61° 58' 45" W) 21 декабря 2007 г и оставляли для свободного опыления.
Всего 273 M1 растения были отобраны и два семени от каждого растения высаживали 23 мая 2008 г, на экспериментальной станции Advanta Seeds в Oran, Province of Salta, Argentina (22° 49' 37" S; 64° 20' 14" W) в питомник и всего получили 546 М2 растений. Пыльца одного растения из каждой пары была собрана и использована для опыления другого растения из этой пары. МЗ семена, полученные от каждого из 273 опыленных М2 растений были собраны. Всего 273 бороздки М3 потомства были высажены 16 декабря 2008 г, в Venado Tuerto и 50 растений из каждой МЗ бороздки опрыскивали 100 мл л д.в./га имазетапира 23 декабря 2008 г. Шестьдесят восемь растений в бороздках показали нормальный рост и отсутствие симптомов после применения гербицида и рассматривались как устойчивые к гербициду и были определены как VT09-9754. Определяли генеалогию устойчивых растений из бороздок и обозначали их как 80237EMS2-192 (в дальнейшем в этом документе именуемые как ADV-IMI-R).
Генерационная история приведена в Таблице 5.


ПРИМЕР 2
Исследование частоты ответа на обработку имидазолинонами устойчивых ADV-IMI-R мутантов по сравнению с исходной эндогамной линией сорго 80237
Растения линии сорго 80237 (элитная линия в собственности Advanta) и имидазолинон-устойчивого мутанта ADV-IMI-R (исходная мутация) опрыскивали в поле тремя гербицидами, принадлежащими семейству имидазолинонов: имазетапиром, имазапиром и имазапиком. Испытывали четыре различных расхода каждого гербицида: 1X, 2Х, 3Х и 4Х (1X является рекомендуемым расходом) (см. вышеприведенную Таблицу 1):
Полевые эксперименты проводили в Venado Tuerto, высадку производили 1 декабря 2010 г. Растения опрыскивали гербицидом через 20 дней после всхождения (стадия V6). Все применения сравнивали с необработанными контролями. Схема опыта состояла из опытных участков, разделенных на три реплики (основной опытный участок: обработка гербицидом; под-участок: линия).
Через десять дней после опрыскивания, определяли сухую массу (DM) надземных тканей всех растений. Реакцию на гербицид вычисляли в процентах DM в надземных тканях соответствующего необработанного контроля.
Таким образом, чувствительность каждой линии к гербициду / для каждого расхода j выражали как:
DMij % от Контроля=(DMij/100)/DM Контроля
DMij % от Контроля является средним значением 3 экспериментов для каждого применения в каждой линии.
ПРИМЕР 3
Секвенирование гена AHAS сорго, кодирующего мутированный полипептид, описанный в настоящем изобретении, имеющий активность синтазы ацетогидроксикислот и который является имидазолинон-устойчивым
Секвенирование проводили на ткани листа мутанта ADV-IMI-R (VT11-11331-BK отбор) и эндогамной линии дикого типа 80237. Выделяли геномную ДНК и растворяли в воде в конечной концентрации 100 нг/мкл. При секвенировании гена синтазы ацетогидроксикислот (AHAS) из мутанат ADV-IMI-R и линии сорго 80237, были сконструированы специфические праймеры для амплификации полимеразной цепной реакцией (PCR), на основании последовательности AHAS сорго, раскрытой в GenBank с номером доступа GM663363.1. Праймеры были сконструированы таким образом, чтобы образовать 5 перекрывающихся участков ДНК (ампликонов), представляющих полную кодирующую последовательность AHAS. Последовательности сконструированных праймеров приведены ниже:

PCR смесь имела конечный объем 25 мкл и следующие компоненты: 1X реакционный буфер (Invitrogen), 0,2 мМ дНТФ (GE Healthcare), 2,5 мМ MgCl2 (Invitrogen), 0,2 мкМ каждого праймера, 0,5 мкл Platinum Taq (5 ед/мкл) (Invitrogen) и 100 нг геномной ДНК. PCR реакцию проводили в GeneAmp PCR System 9700 амплификаторе (Perkin-Elmer) и условия амплификации были следующими: этап начальной денатурации при 94°С в течение 1 мин, далее 35 циклов 94°С в течение 45 сек, 57°С в течение 45 сек и 72°С в течение 70 сек, и окончательного этапа элонгации при 72°С в течение 10 мин.
Продуктов амплификации не было получено при использовании праймеров SbAHAS-F1 и SbAHAS-R1, как с продуктами ADV-IMI-R, так и с исходной линией сорго 80237.
Для преодоления этой трудности, были сконструированы два новых праймера для образования шестого ампликона:
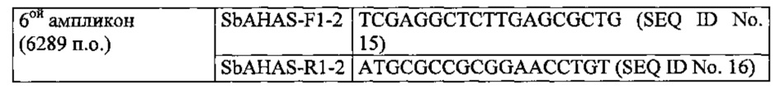
Для получения 6го ампликона использовали те же самые условия PCR, как и описанные выше.
Два мкл каждого ДНК продукта, полученного при амплификации с помощью PCR исследовали с помощью электрофореза в агарозном геле для определения размера фрагментов и приблизительной концентрации ДНК на основании маркеров молекулярной массы Low DNA Mass Ladder (Invitrogen). Оставшиеся продукты PCR очищали с использованием Wizard® SV геля (Promega) и PCR Clean-Up System (Promega). Очищенную ДНК секвенировали с использованием BigDye® Terminator v3.1 Cycle Sequencing System (Applied Biosystems), в соответствии с инструкцией производителя.
Файлы полученные при секвенировании синтазы ацетогидроксикислот, полученные с каждым ампликоном, объединяли с помощью САР3 Sequence Assembly Program (http://pbil.univ-lyonl.fr/cap3.php). Полученную последовательность ДНК гена синтазы ацетогидроксикислот выравнивали с использованием программы Clustal W версии 2.1 Qittp://www.clustal.org).
ПРИМЕР 4
Наследование устойчивость к имазетапиру в изолированной популяции сорго F2, полученной при скрещивании имазетапир-чувствительной линии с устойчивым мутантм ADV-IMI-R
Проводили целенаправленное скрещивание линии сорго 90523 (элитная линия в собственности Advanta, чувствительная к имидазолинонам) и имидазолинон-устойчивого мутанта ADV-IMI-R (VT09-9754-48-6-BK отбор). Полученные F1 растения самоопылялись, и F2 семена были собраны. F2 семена высаживали в поле в Venado Tuerto, в октябре 2010 г. F2 растения (177 растений) опрыскивали имазетапиром (Pivot®, BASF) при расходе 3Х (где 1X - расход, рекомендуемый производителем для коммерческого использования, что является эквивалентом 100 мл д.в./га). Перед опрыскиванием, собирали ткань листьев каждого из 177 F2 растений как ADV-IMI-R мутанта (VT09-9754-48-6-ВК отбор), так и линии дикого типа 90523, для выделения геномной ДНК, последнюю растворяли в воде до конечной концентрации 100 нг/мкл для использования при генотипировании.
Гербицид распыляли через 20 дней после всхождения (стадия V6). Растения оценивали через десять дней после опрыскивания и гербицидное действие объединяли в три группы с помощью визуальной оценки симптомов, в соответствии со следующей фенотипической оценкой:
- 1 = без повреждений
- 2 = хлоротический
- 3 = погибший
ПРИМЕР 5
Создание ДНК маркеров, специфичных к SNP-SbAHAS
Одиночная точечная мутация в гене AHAS, заменяющая нуклеотид G на А в нуклеотидном положении +277 (кодон 93), отличает исходную эндогамную линию сорго 80237 (гербицид-чувствительную) от индуцированного мутанта ADV-IMI-R. Молекулярный маркер (называемый в настоящем документе SNP-SbAHAS) был сконструирован с использованием следующей группы двояко-меченных праймеров и зондов:

Генотипирование проводили с помощью аллельного дискриминантного анализа с использованием PCR в режиме реального времени на АВ 7500 амплификаторе (Applied Biosystems, Foster City, CA, US). PCR реакционная смесь была приготовлена в конечном объеме 25 мкл и содержала: 12,5 мкл 2Х Perfecta® qPCR Supermix (Quanta Biosciences, Gaithersburg, MD, US), 0,08 мкМ праймеров (прямого и обратного), 0,4 мкМ зондов (1 и 2), 10 мкл геномной ДНК и ДНКаза-свободную воду до конечного объема. Условия амплификации: один начальный этап денатурации при 95°С в течение 10 мин, далее 50 денатурирующих циклов при 92°С в течение 15 сек и гибридизации/удлинения при 60°С в течение 1 мин. Результаты, полученные с помощью аллельного дискриминантного анализа подробно разбирали после амплификации с использованием АВ Sequence Detection System (SDS) 7500 1.4 программного продукта (Applied Biosystems, Foster City, CA, US).
ПРИМЕР 6
Корреляция устойчивости к гербициду с мутацией AHAS в мутантах ADV-IMI-R Отдельные особи F2 потомства, полученные при скрещивании ADV-IMI-R × 90523 оценивали фенотипически (без повреждений, хлороидные и погибшие) после опрыскивания имазетапиром (используя способ, описанный в Примере 4) и потом классифицировали генотипированием с использованием молекулярного маркера SNP-SbAHAS, который специфичен к индуцированной в AHAS (используя способ, описанный в Примере 5).
ПРИМЕР 7
Генетическое картирование устойчивость к гербициду и специфического SNP-SbAHAS маркера
Устойчивость к гербициду и специфический SNP-SbAHAS маркер генетически картировали. На основании последовательности AHAS сорго, раскрытой в GenBank (номер доступа GM663363.1, проводили анализ BLAST, сравнивая названную последовательность с геномной последовательностью ДНК Sorghum bicolor, депонированной в базе данных Phytozome (bttp://vvww.phvtozome.net/search.php).
Генотипирование (фингерпринтинг) мутированной ADV-IMI-R линии и эндогамной линии 90253 проводили с использованием группы молекулярных маркеров SSR типа. Семь полиморфных SSR, находящихся на хромосоме 4 генома Sorghum bicolor были отобраны для генотипирования (Mace, ES et al., A consensus genetic тар of sorghum that integrates multiple component maps and high-throughput Diversity Array Technology (DArT) markers, BMC Plant Biology, 2009, 9:13; Srinivas, G et al., Exploration and mapping of microsatellite markers from subtracted drought stress ESTs in Sorghum bicolor (L.), Moench. Theor. Appl. Genet. 2009, 118: 703-717; Ramu, P et al., In silico mapping of important genes and markers available in the public domain for efficient sorghum breeding, Mol Breeding 2010, 26: 409-418; http://ww.lbk.ars.usda.gov/psgd/sorghum/2009SorghumSEAMs_LBKARS.xls).
7 отобранный полиморфных SSR представлены ниже:

Полученные PCR фрагменты от каждой из исследованных SSR разделяли с помощью капиллярного электрофореза с использованием автоматического секвенатора ABI3130×1 (Applied Biosystems). Генотипирование этих 7 SSR проводили в 177 отдельных растениях F2 потомство, полученных при скрещивании ADV-IMI-R × 90523. В дополнение, те же самые 177 растений F2 потомства, исследовали на наличие SNP-SbAHAS маркера, специфичного к индуцированной мутации в гене AHAS. Полученные результаты классифицировали в соответствии с фенотипической оценкой после применения имазетапира на растения F2 потомства и анализировали и использованием компьютерной программы JoinMap (Van Ooijen, JW and Voorips, RE, JoinMap 3.0 Software for the calculation of genetic linkage maps, Plant Research International, 2001, Wageningen, The Netherlands).




















Изобретение относится к области биохимии, в частности к мутантному растению сорго, содержащему в своем геноме по меньшей мере один полинуклеотид, где указанный полинуклеотид кодирует полипептид, имеющий замену аланина на треонин в положении 93 большой субъединицы белка AHAS сорго, причем указанное растение имеет повышенную устойчивость к одному или более имидазолиноновым гербицидам, к его семени, а также к способу его получения и способу его идентификации. Также раскрыт полинуклеотид, обладающий активностью устойчивости к гербицидам AHAS, и экспрессионная кассета, клетка, вектор экспрессии, его содержащие. Изобретение также относится к способу борьбы с сорняками в непосредственной близости от вышеуказанного растения сорго. Изобретение позволяет эффективно получать растение сорго с повышенной устойчивостью к одному или более имидазолиноновым гербицидам. 10 н. и 10 з.п. ф-лы, 5 ил., 5 табл., 6 пр.
1. Мутантное растение сорго, содержащее в своем геноме по меньшей мере один полинуклеотид, где указанный полинуклеотид кодирует полипептид, имеющий замену аланина на треонин в положении 93 большой субъединицы белка AHAS сорго, причем указанное растение имеет повышенную устойчивость к одному или более имидазолиноновым гербицидам по сравнению с растением сорго дикого типа, где имидазолиноновый гербицид, в частности, отбирают из группы, состоящей из имазетапира, имазапира и имазапика, и где по меньшей мере один полинуклеотид характеризуется SEQ ID No. 1, кодирующей полипептид, характеризующийся SEQ ID No. 2.
2. Растение сорго по п. 1, где указанное растение сорго с повышенной устойчивостью к одному или более гербицидам может быть использовано для внедрения черты устойчивости в другое растение сорго путем интрогрессии.
3. Растение сорго по п. 1, где указанное растение является трансгенным.
4. Растение сорго по п. 1, где указанное растение не является трансгенным.
5. Растение сорго по п.1, где растение сорго содержит в своем геноме по меньшей мере один полинуклеотид, кодирующий полипептид, имеющий замену аланина на треонин в положении 93 большой субъединицы белка AHAS сорго, и отобрано из группы, состоящей из мутантного растения, такого как NCIMB 41870, полученного путем мутагенеза с использованием этилметансульфоната, потомства растения NCIMB 41870, мутанта растения NCIMB 41870 и потомства мутанта NCIMB 41870, где гербицид принадлежит, в частности, к группе имидазолинонов, где NCIMB 41870 является мутантным растением, депонированным в коллекции NCIMB с номером доступа NCIMB 41870 12 октября 2011 г.
6. Растение сорго по п. 5, где указанное растение является трансгенным.
7. Растение сорго по п. 5, где указанное растение является нетрансгенным.
8. Мутантное семя сорго, содержащее в своем геноме по меньшей мере один полинуклеотид, где указанный полинуклеотид кодирует полипептид, имеющий замену аланина на треонин в положении 93 большой субъединицы белка AHAS сорго, где указанное семя порождает растение сорго, имеющее повышенную устойчивость к одному или более гербицидам из группы имидазолинонов по сравнению с растением сорго дикого типа, где по меньшей мере один полинуклеотид характеризуется SEQ ID No. 1, кодирующей полипептид, охарактеризованный SEQ ID No. 2.
9. Способ идентификации гербицид-устойчивого растения сорго, включающий:
a) получение образца нуклеиновой кислоты из растения сорго;
b) амплификацию участка, соответствующего гену AHAS, присутствующему в указанном образце нуклеиновой кислоты из растения сорго ;
c) идентификацию гербицид-устойчивого растения, основанную на присутствии по меньшей мере одной мутации в амплифицированном образце нуклеиновой кислоты, где указанное гербицид-устойчивое растение сорго устойчиво к одному или более имидазолиноновым гербицидам, в частности, выбранным из группы, состоящей из имазетапира, имазапира и имазапика, где указанная по меньшей мере одна мутация содержит замену Ala93Thr в положении 93 кодируемого полипептида, где указанный полипептид имеет активность синтазы ацетогидроксикислот, и/или
где образец нуклеиновой кислоты характеризуется SEQ ID No. 1, и/или где полипептид характеризуется SEQ ID No. 2.
10. Способ по п. 9, где указанное растение является однодольным.
11. Способ по п. 9, где указанное растение является трансгенным растением.
12. Способ по п. 9, где указанное растение является нетрансгенным растением.
13. Способ борьбы с сорняками в непосредственной близости от растений сорго, включающий нанесение эффективного количества имидазолинового гербицида на сорняки и возделываемые растения, где имидазолиноновый гербицид, в частности, отбирают из группы, включающей имазетапир, имазапик и имазапир, и где возделываемое растение, в частности, отбирают из группы, состоящей из:
a) растения сорго по п.1;
b) потомства, производного или мутанта растения сорго a),
где указанное потомство, производное или мутант содержат в своем геноме по меньшей мере один полинуклеотид, который кодирует полипептид, имеющий замену аланина на треонин в положении 93 большой субъединицы белка AHAS сорго, как показано в SEQ ID NO:1.
14. Полинуклеотид, имеющий нуклеотидную последовательность, отобранную из группы, состоящей из:
a) нуклеотидной последовательности, представленной в SEQ ID No. 1,
b) нуклеотидной последовательности, кодирующей полипептид, представленный в SEQ ID No. 2;
c) нуклеотидной последовательности, кодирующей полипептид, имеющий по меньшей мере 95% идентичность последовательности с аминокислотной последовательностью SEQ ID No. 2, где полипептид имеет замену Ala93Thr в большой субъединице белка AHAS сорго и активность устойчивости к гербицидам AHAS;
d) нуклеотидной последовательности, имеющей по меньшей мере 85% идентичность с нуклеотидной последовательностью, представленной в SEQ ID No. 1, где нуклеотидная последовательность кодирует полипептид, содержащий большую субъединицу AHAS и имеющий замену Ala93Thr в большой субъединице белка AHAS сорго и активность устойчивости к гербицидам AHAS,
где указанный полинуклеотид кодирует полипептид, имеющий замену Ala93Thr в большой субъединице белка AHAS сорго.
15. Экспрессионная кассета, содержащая нуклеотидную последовательность по п. 14 и по меньшей мере один промотор, который управляет экспрессией полинуклеотида, где промотор, в частности, отбирают из группы, включающей промотор для экспрессии в клетках растений, бактерий, грибов, животных и простейших.
16. Клетка, трансформированная экспрессионной кассетой по п. 15, где указанная клетка, в частности, отбирается из группы, включающей клетку бактерий, грибов, дрожжей, растений и животных, и где клетка устойчива к имидазолиноновым гербицидам.
17. Вектор экспрессии, содержащий полинуклеотид, который содержит нуклеотидную последовательность, которую отбирают из группы, включающей:
a) нуклеотидную последовательность, представленную в SEQ ID No. 1,
b) нуклеотидную последовательность, кодирующую полипептид, представленный в SEQ ID No. 2;
c) нуклеотидную последовательность, кодирующую полипептид, имеющий по меньшей мере 95% идентичность последовательности с аминокислотной последовательностью SEQ ID No. 2, где полипептид имеет активность AHAS устойчивости к гербицидам;
d) нуклеотидную последовательность, имеющую по меньшей мере 85% идентичность с нуклеотидной последовательностью, представленной в SEQ ID No. 1, где нуклеотидная последовательность кодирует полипептид, содержащий большую субъединицу AHAS и имеющий активность AHAS устойчивости к гербицидам;
где полинуклеотид кодирует полипептид, имеющий замену Ala93Thr в большой субъединице белка AHAS сорго, в частности, для применения для экспрессии полинуклеотида в клетках, которые отбирают из группы, включающей клетки бактерий, грибов, дрожжей, растений и животных.
18. Трансформированное растение сорго, где указанное растение содержит вектор по п.17, где трансформированное растение сорго устойчиво к гербицидам имидазолинонового типа, и
где вектор далее содержит селектируемый ген и по меньшей мере один промотор, функционально связанный с нуклеотидной последовательностью, способной управлять экспрессией указанной нуклеотидной последовательности, где промотор, в частности, отбирают из группы, включающей тканеспецифичный промотор и хлоропласт-специфичный промотор.
19. Способ для получения растения сорго с повышенной устойчивостью к имидазолиноновым гербицидам по сравнению с растением сорго дикого типа, где имидазолиноновый гербицид, в частности, отбирают из группы, включающей имазетапир, имазапик и имазапир, где указанный способ включает:
i) трансформирование растительной клетки сорго экспрессионной кассетой или вектором, содержащим полинуклеотид, имеющий нуклеотидную последовательность, отбираемую из группы, включающей:
a) нуклеотидную последовательность, представленную в SEQ ID No. 1;
b) нуклеотидную последовательность, кодирующую полипептид, представленный в SEQ ID No. 2;
c) нуклеотидную последовательность, кодирующую полипептид, имеющий по меньшей мере 95% идентичность последовательности с аминокислотной последовательностью из SEQ ID No. 2, где полипептид имеет активность устойчивости к гербицидам AHAS; и
d) нуклеотидную последовательность, имеющую по меньшей мере 85% идентичность с нуклеотидной последовательностью, представленной в SEQ ID No. 1, где нуклеотидная последовательность кодирует полипептид, содержащий большую субъединицу AHAS и имеющий активность AHAS устойчивости к гербицидам;
где полинуклеотид кодирует полипептид, имеющий замену Ala93Thr в большой субъединице белка AHAS сорго,
ii) регенерацию растительной клетки для получения растения сорго с повышенной устойчивостью к имидазолиноновым гербицидам по сравнению с растением сорго дикого типа,
где экспрессионная кассета далее содержит по меньшей мере один промотор, в частности, растительный тканеспецифичный промотор или хлоропласт-специфичный промотор, функционально связанный с полинуклеотидом, где указанный промотор способен управлять экспрессией указанного полинуклеотида.
20. Способ по п. 19, где указанное растение имеет повышенную устойчивость к гербициду по сравнению с нетрансформированным растением.
| WO 2010037061 A1, 01.04.2010 | |||
| WO 2008124431 A1, 16.10.2008 | |||
| WO 2008124495 A2, 16.10.2008 | |||
| РАСТЕНИЯ ПШЕНИЦЫ С ПОВЫШЕННОЙ УСТОЙЧИВОСТЬЮ К ИМИДАЗОЛИНОНОВЫМ ГЕРБИЦИДАМ | 2002 |
|
RU2337532C2 |
Авторы
Даты
2018-06-21—Публикация
2012-04-05—Подача