Изобретение относится к катализатору и процессам каталитической окислительной конверсии углеводородов и гидрирования оксидов углерода и углеводородов. В частности, такие реакции, как паровая, углекислотная конверсии, парциальное окисление или автотермический риформинг углеводородов с получением синтез-газа, лежат в основе большинства крупнотоннажных процессов химической и нефтехимической промышленности.
Усовершенствование катализаторов и оптимизация параметров проведения этих процессов всегда имели стратегическое значение, способствуя ресурсо- и энергосбережению.
В последнее время большое внимание также стало уделяться проблеме утилизации оксидов углерода, в первую очередь улавливанию и вовлечению в оборот углекислого газа - одного из основных парниковых газов, приводящих к глобальному потеплению. Каталитическая конверсия СО2 в топливо (например, получение синтетического природного газа, метанола, диметилового эфира, синтез-газа) рассматривается как перспективный подход по его утилизации. В частности, каталитическая конверсия может применяться при переработке биогаза, одновременно содержащего метан и углекислый газ. В этой связи разработка активных, селективных и стабильных гетерогенных катализаторов, позволяющих минимизировать капитальные затраты и операционные издержки при проведении вышеперечисленных процессов, является крайне важной задачей.
В настоящее время известны катализаторы и способы проведения каталитических реакций окислительной конверсии углеводородов с применением нанесенных рутениевых, платиновых, родиевых, кобальтовых, никелевых катализаторов (Р.K. Cheekatamarla, C.M. Finnerty, Reforming catalysts for hydrogen generation in fuel cell applications // Journal of Power Sources, V. 160 Is. 1,2006, 490-499; EP 1586 535 A2; CN 102949994 (A); US 7449168, B01J 23/78, C01B 3/26, 11.11.2009). Недостатками известных катализаторов являются невысокая активность, зауглероживание катализаторов и спекание дисперсных металлических частиц в условиях протекания каталитической реакции.
Известны также катализаторы и способы проведения гидрирования оксидов углерода и углеводородов (RU 2409878, Н01М 8/06, 20.01.2011; SU №780881, B01J 37/02, 1980). В частности, известны способы каталитической конверсии углекислого газа, где в качестве катализатора используются переходные металлы, например, Ru, Rh, Pt, Ni, Co, нанесенные на оксид алюминия (О.В. Крылов, А.Х. Мамедов, Гетерогенно-каталитические реакции диоксида углерода // Успехи химии, 1995, том 64, номер 9, страницы 935-959). Недостатками известных катализаторов являются невысокая конверсия углекислого газа, зауглероживание и снижение активности.
В основном, эти недостатки вызваны структурой используемого в катализаторах носителя, обычно представляющего собой агломераты из сферически подобных наноразмерных частиц, которые не обеспечивают сохранение высокой дисперсности, оптимального фазового состава нанесенных металлических частиц в процессе приготовления катализатора и в условиях протекания каталитических реакций.
В качестве прототипа был выбран 5 вес. % Rh/Al2O3 катализатор (J. Yu, Z. Zhang, F. Dallmann, J. Zhang, D. Miao, H. Xu, A. Goldbach, R. Dittmeyer, Facile synthesis of highly active Rh/Al2O3 steam reforming catalysts with preformed support by flame spray pyrolysis // Applied Catalysis B: Environmental 198 (2016) 171-179).
Недостатками являются невысокая конверсия углекислого газа, зауглероживание и снижение активности.
Задачей, на решение которой направлено настоящее изобретение, является повышение эффективности каталитической окислительной конверсии углеводородов и гидрирования оксидов углерода и углеводородов за счет разработки более эффективных катализаторов.
Технический результат - высокая активность, стабильность катализатора при проведении данных каталитических процессов.
Задача решается благодаря использованию катализатора, содержащего в качестве активного компонента переходные металлы Периодической системы, преимущественно не менее одного переходного металла, выбранного из VIII группы Периодической системы, в количестве не менее 0,01 мас. %, и носителя, представляющего собой монокристаллические нановолокна оксида алюминия, преимущественно имеющих диаметр более 3 нм и длину более 100 нм (US Patent Application 2013/0192517 A1, C30B 9/00, 01.08.2013), которые в своем составе могут содержать переходные металлы и лантаноиды.
Задача решается также способом приготовления катализатора окислительной конверсии углеводородов и гидрирования оксидов углерода и углеводородов нанесением комплексных соединений переходных металлов, преимущественно не менее одного переходного металла, выбранного из VIII группы Периодической системы, в количестве не менее 0,01 мас. %, на носитель, представляющий собой монокристаллические нановолокна оксида алюминия, преимущественно имеющие диаметр более 3 нм и длину более 100 нм, которые в своем составе могут содержать переходные металлы и лантаноиды.
Задача решается также способом окислительной конверсии углеводородов в присутствии катализатора, описанного выше, при температуре выше 20°С, при давлении выше 0,1 атм. В качестве окислителя преимущественно используют воду, и/или углекислый газ, и/или кислород, который может находиться в смеси с азотом, в качестве основных продуктов реакции могут образовываться водород, вода, монооксид углерода, углекислый газ, метан.
Задача решается также способом гидрирования оксидов углерода и углеводородов в присутствии катализатора, описанного выше, при температуре выше 20°С, при давлении выше 0,1 атм. Для проведения гидрирования преимущественно используют водород, а основным продуктом является метан.
На прототипе при 650°С даже при потоке 196000 см3г-1ч-1 не достигалось равновесное распределение продуктов и конверсия метана в ходе проведения реакции паровой конверсии метана. На катализаторе, приготовленном по примеру 2, достигалось равновесное распределение продуктов при потоках до 270000 см3г-1ч-1. Результат достигается за счет высокой активности и стабильности катализатора, что иллюстрируется примерами 11 и 12.
Сущность изобретения иллюстрируется следующими примерами по приготовлению катализаторов и примерами, описывающими результаты испытаний катализаторов в окислительной конверсии углеводородов и гидрирования оксидов углерода и углеводородов.
I. Приготовление катализаторов
Пример 1.
Получение образца 0.3 мас. % Rh/Нановолокна оксида алюминия.
0,100 г нитрата родия (III) гидрата растворяют в 75 мл воды, далее в раствор помещают 10 г нановолокон оксида алюминия, высушивают при 110°С и прокаливают при 400°С.
Пример 2.
Получение образца 37 мас. % Ni/Нановолокна оксида алюминия.
5,7 г [Ni(NO3)2⋅6H2O] и 1,2 г глицина растворяют в 15 мл воды. В полученный раствор помещают 2 г нановолокон оксида алюминия, после чего на 30 мин помещают в печь, разогретую до 400°С. Далее восстанавливают при 700°С в токе 10%Н2 в Ar в течение 4 ч.
Пример 3.
Получение образца 37 мас. % Ni/Нановолокна оксида алюминия с содержанием церия.
5,7 г [Ni(NO3)2⋅6H2O] и 1,2 г глицина растворяют в 15 мл воды. В полученный раствор помещают 2 г нановолокон оксида алюминия, содержащие в своем составе 0,1 мас. % церия, после чего на 30 мин помещают в печь, разогретую до 400°С. Далее восстанавливают при 500°С в токе 10%Н2 в Ar в течение 4 ч.
Пример 4.
Получение образца 20 мас. % Ni/Нановолокна оксида алюминия.
2,7 г [Ni(NO3)2⋅6H2O] растворяют в 15 мл воды. В полученный раствор помещают 2 г нановолокон оксида алюминия, после чего на 30 мин помещают в печь, разогретую до 400°С. Далее восстанавливают при 500°С в токе 10%Н2 в Ar в течение 4 ч.
Пример 5.
Получение образца 15 мас. % Ni/Нановолокна оксида алюминия с содержанием хрома.
1,8 г [Ni(NO3)2⋅6H2O] растворяют в 50 мл воды. В полученный раствор помещают 2 г нановолокон оксида алюминия, содержащие 1 мас. % хрома, и по каплям прикапывают 17 мл 1 моль/л раствора гидроксида натрия. После этого нановолокна извлекают из раствора и на 30 мин помещают в печь, разогретую до 400°С. Далее восстанавливают при 500°С в токе 10%H2 в Ar в течение 4 ч.
Пример 6.
Получение образца 0.3 мас. % Pt-0.3 мас. %Со/Нановолокна оксида алюминия.
0,080 г гексахлороплатината натрия и 0,10 г нитрата кобальта (II) растворяют в 75 мл воды, далее в раствор помещают 10 г нановолокон оксида алюминия, высушивают при 110°С и прокаливают при 400°С.
II. Испытание катализаторов
Пример 7.
Окислительная конверсия углеводородов иллюстрируется на примере паровой конверсии метана. Процесс проводят с катализатором, приготовленным в соответствии с примером 2, при температуре 650°С, при скорости 135000 см3г-1ч-1 и атмосферном давлении. Реакционная газовая смесь состоит из: 33.3 об. % СН4 и 66.7 об. % H2O. Полученные результаты приведены в таблице 1.

Пример 8.
Процесс гидрирования углекислого газа в присутствии метана проводят с катализатором, приготовленным в соответствии с примером 3, при температуре 410°С, при скорости 34000 см3г-1ч-1 и атмосферном давлении. Реакционная газовая смесь состоит из: 8,2 об. % CO2, 38,2 об. % Н2, 2 об. % СН4, 51,6 об. % N2. Полученные результаты приведены в таблице 2.

Пример 9.
Процесс гидрирования углекислого газа проводят с катализатором, приготовленным в соответствии с примером 3, при температуре 395°С, при скорости 34000 см3г-1ч-1 и атмосферном давлении. Реакционная газовая смесь состоит из: 8,2 об. % СО2, 38,2 об. % Н2, 53,6 об. % N2 Полученные результаты приведены в таблице 3.
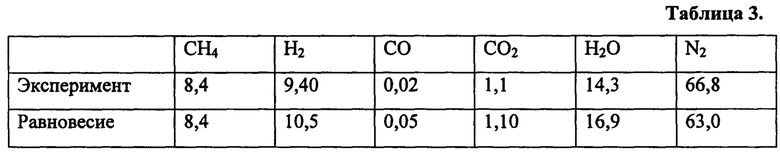
Пример 10.
Процесс гидрирования пропана проводят с катализатором, приготовленным в соответствии с примером 3, при температуре 400°С, при скорости 25000 см3г-1ч-1 и атмосферном давлении. Реакционная газовая смесь состоит из: 10 об. % C3H8, 50 об. % СН4, 30 об. % Н2, 10 об. % N2. Полученные результаты приведены в таблице 4.
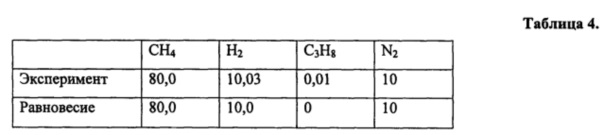
Таким образом, как видно из примеров и таблиц, предлагаемое изобретение позволяет эффективно осуществлять процессы окислительной конверсии углеводородов и гидрирования оксидов углерода и углеводородов.
Пример 11, который доказывает достижение высокой стабильности катализатора по сравнению с прототипом
Пример 11.
Стабильность катализатора иллюстрируется на примере паровой конверсии метана в течение 90 ч. Процесс проводят с катализатором, приготовленным в соответствии с примером 2, при температуре 650°С, при скорости 135000 см3г-1ч-1 и атмосферном давлении. Реакционная газовая смесь состоит из: 33.3 об. % СН4 и 66.7 об. % H2O Полученные результаты приведены в таблице 5.
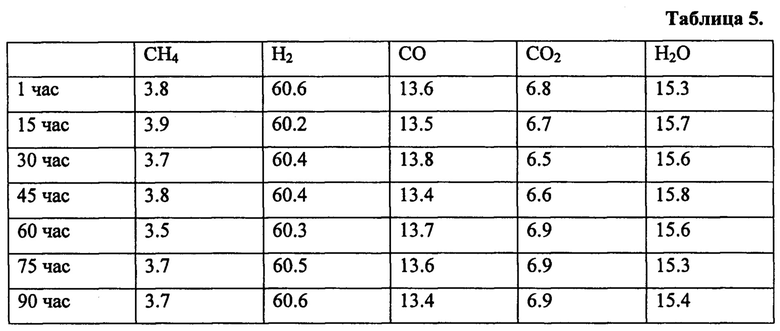
Примеры 12 и 13 доказывают высокую активность катализатора в гидрировании оксидов углерода
Пример 12.
Процесс гидрирования моноксида углерода проводят с катализатором, приготовленным в соответствии с примером 3, при температуре 300°С, при скорости 29000 см3г-1ч-1 и атмосферном давлении. Реакционная газовая смесь состоит из: 2 об. % СО, 98 об. % Н2. Полученные результаты приведены в таблице 6.
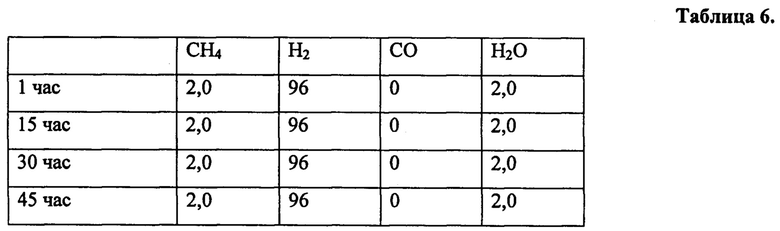
Пример 13.
Процесс гидрирования моноксида и диоксида углерода проводят с катализатором, приготовленным в соответствии с примером 3, при температуре 300°С, при скорости 29000 см3г-1ч-1 и атмосферном давлении. Реакционная газовая смесь состоит из: 1 об. % СО, 1 об. % CO2, 98 об. % Н2. Полученные результаты приведены в таблице 7.
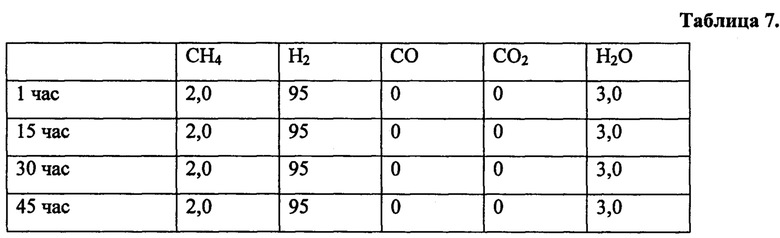
Таким образом, как видно из примеров и таблиц, предлагаемое изобретение позволяет эффективно осуществлять процессы окислительной конверсии углеводородов и гидрирования оксидов углерода и углеводородов.
| название | год | авторы | номер документа |
|---|---|---|---|
| КАТАЛИЗАТОР СИНТЕЗА УГЛЕВОДОРОДОВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2009 |
|
RU2422200C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ОКСИДНО-ПОЛИМЕТАЛЛИЧЕСКИХ КАТАЛИЗАТОРОВ НА ОСНОВЕ ЖАРОПРОЧНЫХ СПЛАВОВ ДЛЯ ПАРЦИАЛЬНОГО ОКИСЛЕНИЯ УГЛЕВОДОРОДОВ В СИНТЕЗ-ГАЗ | 2013 |
|
RU2552639C1 |
| КАТАЛИЗАТОР И СПОСОБ УГЛЕКИСЛОТНОЙ КОНВЕРСИИ ЛЕГКИХ УГЛЕВОДОРОДОВ | 2007 |
|
RU2351392C1 |
| КАТАЛИЗАТОР ДЛЯ ПАРОВОЙ КОНВЕРСИИ УГЛЕВОДОРОДОВ И СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ | 1993 |
|
RU2054963C1 |
| КАТАЛИЗАТОР ДЛЯ СИНТЕЗА УГЛЕВОДОРОДОВ ИЗ СО И H И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2009 |
|
RU2414296C1 |
| СПОСОБ ПОЛУЧЕНИЯ СИНТЕЗ-ГАЗА ВЫСОКОТЕМПЕРАТУРНЫМ КАТАЛИТИЧЕСКИМ ОКИСЛИТЕЛЬНЫМ ПРЕВРАЩЕНИЕМ МЕТАНА | 2015 |
|
RU2594161C1 |
| СПОСОБ ПОЛУЧЕНИЯ КАТАЛИЗАТОРА ДЛЯ ГЛУБОКОГО ОКИСЛЕНИЯ CO И УГЛЕВОДОРОДОВ И КАТАЛИЗАТОР, ПОЛУЧЕННЫЙ ЭТИМ СПОСОБОМ | 2010 |
|
RU2434678C1 |
| Никельсодержащий углерод-графеновый катализатор гидрирования и способ его получения | 2020 |
|
RU2748974C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА КОНВЕРСИИ УГЛЕВОДОРОДОВ | 1998 |
|
RU2141383C1 |
| КАТАЛИЗАТОР, СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ И СПОСОБ ПОЛУЧЕНИЯ СИНТЕЗ-ГАЗА | 2005 |
|
RU2292237C1 |
1. Катализатор окислительной конверсии углеводородов и гидрирования оксидов углерода и/или углеводородов, содержащий в качестве активного компонента переходные металлы Периодической системы и носитель, отличающийся тем, что в качестве носителя он содержит монокристаллические нановолокна оксида алюминия, имеющие диаметр более 3 нм и длину более 100 нм.
2. Катализатор по п. 1, отличающийся тем, что он содержит активный компонент в количестве не менее 0,01 мас. %.
3. Способ приготовления катализатора окислительной конверсии углеводородов и гидрирования оксидов углерода и/или углеводородов нанесением активного компонента - переходных металлов Периодической системы на носитель, отличающийся тем, что катализатор готовят нанесением комплексных соединений переходных металлов на монокристаллические нановолокна оксида алюминия, имеющие диаметр более 3 нм и длину более 100 нм.
4. Способ приготовления катализатора по п. 3, отличающийся тем, что активный компонент наносят в количестве не менее 0,01 мас. %.
5. Способ окислительной конверсии углеводородов в присутствии катализатора, отличающийся тем, что в качестве катализатора используют катализатор по пп. 1, 2 или приготовленный по пп. 3, 4.
6. Способ по п. 5, отличающийся тем, что в качестве окислителя используют воду и/или углекислый газ и/или кислород.
7. Способ по п. 5, отличающийся тем, что в качестве окислителя используют кислород в смеси с азотом.
8. Способ по п. 5, отличающийся тем, что в качестве основных продуктов реакции образуются водород и/или вода и монооксид углерода и/или углекислый газ и/или метан.
9. Способ по п. 5, отличающийся тем, что процесс проводят при температуре выше 20°С.
10. Способ по п. 5, отличающийся тем, что процесс проводят при давлении выше 0,1 атм.
11. Способ гидрирования монооксида углерода и/или диоксида углерода и/или углеводородов в присутствии катализатора, отличающийся тем, что в качестве катализатора используют катализатор по пп. 1, 2 или приготовленный по пп. 3, 4.
12. Способ по п. 11, отличающийся тем, что для проведения гидрирования используют водород.
13. Способ по п. 11, отличающийся тем, что основным продуктом гидрирования является метан.
14. Способ по п. 11, отличающийся тем, что процесс проводят при температуре выше 20°С.
15. Способ по п. 11, отличающийся тем, что процесс проводят при давлении выше 0,1 атм.
| RU 2012141952 А, 10.04.2014 | |||
| WO 2014011646 A1, 16.01.2014 | |||
| US 2013192517 A1, 01.08.2013 | |||
| 1971 |
|
SU409878A1 | |
| КАТАЛИЗАТОР ДЛЯ СИНТЕЗА УГЛЕВОДОРОДОВ ИЗ СО И H И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2009 |
|
RU2414296C1 |
| НАНЕСЕНИЕ И ЗАКРЕПЛЕНИЕ НАНОАКТИВНОГО МАТЕРИАЛА | 2010 |
|
RU2579144C2 |
| Катализатор для гидрирования ароматических углеводородов и очистки газов от кислорода и окиси углерода и способ его получения | 1979 |
|
SU780881A1 |
| Маркова Е.Б | |||
| и др | |||
| Исследование нановолокнистых катализаторов на основе оксидов алюминия и титана в реакции крекинга пропана | |||
| Бутлеровские чтения, 2013, т | |||
| Нивелир для отсчетов без перемещения наблюдателя при нивелировании из средины | 1921 |
|
SU34A1 |
| Способ приготовления пищевого продукта сливкообразной консистенции | 1917 |
|
SU69A1 |
Авторы
Даты
2018-06-28—Публикация
2016-06-15—Подача