ОБЛАСТЬ ТЕХНИКИ
[0001] В настоящем изобретении предложены пролекарства соединений, содержащие донор оксида азота и катализаторы разложения активных форм кислорода (АФК), а также их фармацевтические композиции.
УРОВЕНЬ ТЕХНИКИ
[0002] В патентах США №№6448267, 6455542 и 6759430 раскрыты, наряду с прочим, 1-пирролидинилокси-, 1-пиперидинилокси- и 1-азепанилоксипроизводные, содержащие донор оксида азота и поглотитель О2-, способные выступать в качестве источников оксида азота и в качестве катализаторов разложения АФК, их получение и применение для лечения различных состояний, связанных с окислительным стрессом или эндотелиальной дисфункцией, таких как сахарный диабет и сердечно-сосудистые заболевания.
[0003] В публикации международной заявки № WO 2012/093383 раскрыты способы и композиции для лечения сепсиса и состояний, связанных с ним, с применением соединений, раскрытых в патентах США №№6448267, 6455542 и 6759430; в публикации международной заявки WO 2011/092690 раскрыты способы и композиции для предотвращения, лечения и контролирования легочной артериальной гипертензии (ЛАГ) с применением этих соединений; в публикации международной заявки WO 2013/005216 раскрыты способы и композиции для предотвращения и лечения ишемически-реперфузионного повреждения почки; и в публикации международной заявки WO 2013/190497 раскрыты способы и композиции для лечения ингаляционного поражения легких хлором (ИПЛХ). Полное содержание каждого и всех указанных патентов и патентных публикаций включено в настоящее описание посредством ссылки, как если бы оно было полностью раскрыто в настоящем описании.
[0004] Как показано в публикации международной заявки WO 2013/005216, соединения, раскрытые в патентах США №№6448267, 6455542 и 6759430, в частности 3-нитратометил-2,2,5,5-тетраметилпирролидинилокси, обозначенное в настоящем описании как R-100, которое конкретно проиллюстрировано в указанных публикациях международных заявок, относящихся к лечению сепсиса, ЛАГ, ишемически-реперфузионного повреждения почки и ИПЛХ, в значительной степени не растворимы в воде, но растворимы в некоторых органических растворителях, таких как диметилсульфоксид (ДМСО), или, в качестве альтернативы, если их приготовить в виде комплексов включения с гидроксиалкилциклодекстрином, таким как гидроксипропилциклодекстрин (HPCD). Включение таких органических растворителей в фармацевтические композиции потенциально вызывает токсичность и, таким образом, его предпочтительно избегать. HPCD относительно хорошо переносится, но для того чтобы полностью растворить соединение R-100, HPCD следует смешивать с R-100 в соотношении >20:1 (HPCD:R-100). Верхний предел безопасности при клиническом применении HPCD неизвестен, но самое большое его суточное количество, одобренное для применения у человека внутривенно, составляет 7 граммов. Учитывая минимально применимое для растворения отношение R-100 к HPCD, составляющее 20:1, и ограничение по HPCD, составляющее 7 граммов в сутки, максимальное количество R-100, доставляемого в таких составах для внутривенного введения, будет составлять 350 мг ежедневно.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0005] Чтобы преодолеть представленные выше ограничения, были получены пролекарства соединения R-100, например 2,2,5,5-тетраметил-3-(нитрооксиметил)пирролидин-1-илацетат, обозначенные в настоящем описании как R-107. Как было неожиданно обнаружено, R-107 представляет собой стабильное масло до того, как его подвергают воздействию плазмы, после которого оно легко превращается в соответствующее 1-пирролидининоксипроизводное R-100. R-107 имеет плотность 1,12 мг/мл и может быть введено либо в чистом виде, либо разбавленным, например, в полиэтиленгликоле (ПЭГ)-400, различными способами, включая внутривенный, внутримышечный, подкожный и местный, например, к коже, ранам, язвам, полости рта, влагалищу и анальному каналу.
[0006] В одном аспекте согласно настоящему изобретению, таким образом, предложено соединение общей формулы I:
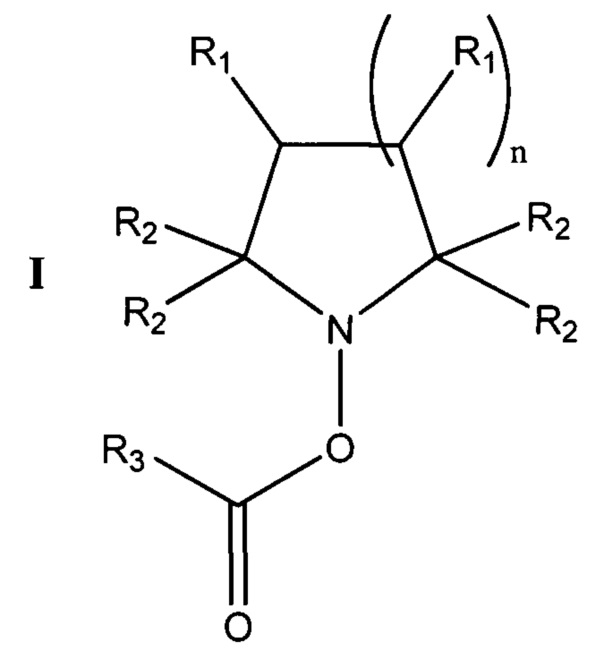
или его энантиомер, диастереомер, рацемат, или фармацевтически приемлемая соль или сольват,
где
каждый R1 независимо выбран из Н, -ОН, -COR4, -COOR4, -OCOOR4, -OCON(R4)2, -(C1-C16)алкилен-COOR4, -CN, -NO2, -SH, -SR4, -(C1-C16)алкила, -O-(С1-С16)алкила, -N(R4)2, -CON(R4)2, -SO2R4, -SO2NHR4, -S(=O)R4 или группы-донора оксида азота, имеющей формулу -Х1-Х2-Х3, в которой X1 отсутствует или выбран из -О-, -S- или -NH-; Х2 отсутствует или представляет собой (С1-С20)алкилен, необязательно замещенный одной или более группами -ONO2; и Х3 представляет собой -NO или -ONO2 при условии, что по меньшей мере одна группа R1 представляет собой группу-донор оксида азота;
каждый R2 независимо выбран из (C1-C16)алкила, (C2-С16)алкенила или (С2-С16)алкинила;
каждый R3 выбран из (С1-C10)алкила, (С3-C10)циклоалкила, (C6-С14)арила или 4-12-членного гетероциклила, каждый из которых может быть необязательно замещен посредством -ОН, -COR5, -COOR5, -(Cl-C8)алкилен-COOR5, -CN, -NO2, -(С1-С8)алкила, -О-(С1-С8)алкила, -N(R5)2, -CON(R5)2, -SO2R5, -SO2NHR5 или -S(=O)R5;
каждый R4 независимо выбран из Н, (С1-С8)алкила, (С3-C10)циклоалкила, (C6-С14)арила или 4-12-членного гетероциклила, каждый из которых не является Н и может быть необязательно замещен посредством -ОН, -COR5, -COOR5, -OCOOR5, -OCON(R5)2, -(C1-C8)алкилен-COOR5, -CN, -NO2, -SH, -SR5, -(С1-С8)алкила, -O-(С1-С8)алкила, -N(R5)2, -CON(R5)2, -SO2R5, -SO2NHR5 или -S(=O)R5;
каждый R5 независимо выбран из Н, (С1-С8)алкила, (С3-C10)циклоалкила, (C6-С14)арила или 4-12-членного гетероциклила; и
n представляет собой целое число от 1 до 3.
[0007] В другом аспекте согласно настоящему изобретению предложена фармацевтическая композиция, содержащая соединение общей формулы I, определенное выше, или его энантиомер, диастереомер, рацемат, или фармацевтически приемлемую соль или сольват, и фармацевтически приемлемый носитель. Соединения и фармацевтические композиции согласно настоящему изобретению являются подходящими для предотвращения, лечения и контролирования заболевания, расстройства или состояния, связанных с окислительным стрессом или эндотелиальной дисфункцией.
[0008] В другом аспекте настоящее изобретение относится к соединению общей формулы I, определенному выше, или его энантиомеру, диастереомеру, рацемату, или фармацевтически приемлемой соли или сольвату для применения для предотвращения, лечения или контролирования заболевания, расстройства или состояния, связанных с окислительным стрессом или эндотелиальной дисфункцией.
[0009] В еще одном аспекте настоящее изобретение относится к применению соединения общей формулы I, определенного выше, или его энантиомера, диастереомера, рацемата, или фармацевтически приемлемой соли или сольвата для получения фармацевтической композиции для предотвращения, лечения и контролирования заболевания, расстройства или состояния, связанных с окислительным стрессом или эндотелиальной дисфункцией.
[0010] В еще одном аспекте настоящее изобретение относится к способу предотвращения, лечения и контролирования заболевания, расстройства или состояния, связанных с окислительным стрессом или эндотелиальной дисфункцией у нуждающегося в этом индивидуума, включающему введение указанному индивидууму эффективного количества соединения общей формулы I, определенного выше, или его энантиомера, диастереомера, рацемата, или фармацевтически приемлемой соли или сольвата.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0011] На фиг. 1A-1F показаны приведенные в качестве иллюстрации микрофотографии, демонстрирующие окрашенные гематоксилином/эозином участки легких, взятых у мышей, подвергнутых имитационной операции (1А, 1B); животных, обработанных Cl2 и HPCD (1С); животных, обработанных Cl2 и солевым раствором (1D); животных, обработанных Cl2 и R-100, 80 мг/кг/дозу, IP (IE); животных, обработанных Cl2 и R-107, 100 мг/кг/дозу, IP (IF), как описано в примере 16.
[0012] На фиг. 2 представлено, что соединение R-107 (100 мг/кг на одну дозу), а также соответствующее ему 1-пирролидинилоксисоединение, R-100 (80 мг/кг/дозу), при введении через 2 и 6 часов после 60-минутного воздействия Cl2 (400 ppm), содержащим воздух, существенно снизили ИПЛХ у мышей через 24 часа после воздействия, на что указывают улучшенные гистологические оценки.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0013] В одном аспекте согласно настоящему изобретению предложены производные 1-пирролидинил-, 1-пиперидинил- и 1-азепанил(сложного эфира) общей формулы I, определенной выше, содержащие от одной до четырех групп-доноров оксида азота и катализатор разложения АФК, например поглотитель супероксидного аниона (O2-). Соединения согласно настоящему изобретению фактически представляют собой пролекарства соответствующих гидроксиламиновых или N-гидроксильных (N-OH) соединений после гидролиза сложноэфирной связи (O-C(O)R3), и эти соединения гидроксиламина затем окисляются in vivo до их соответствующих нитроксидных производных, в частности 1-пирролидинилокси-, 1-пиперидинилокси- и 1-азепанилоксипроизводных описанных в вышеуказанных патентах США №№6448267, 6455542 и 6759430. Соединения согласно настоящему изобретению, таким образом, как ожидается, являются эффективными для всех клинических показаний, при которых вышеупомянутые 1-пирролидинилокси-, 1-пиперидинилокси- и 1-азепанилоксипроизводные являются полезными.
[0014] Термин "алкил", применяемый в настоящем описании, как правило, означает прямой или разветвленный насыщенный углеводородный радикал, содержащий 1-16 атомов углерода, и включает, например, метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, изобутил, трет-бутил, н-пентил, изоамил, 2,2-диметилпропил, н-гексил, н-гептил, н-октил, н-нонил, н-децил, н-ундецил, н-додецил, н-тридецил, н-тетрадецил, н-пентадецил, н-гексадецил и т.п. Предпочтительными являются (С1-С8)алкильные группы, более предпочтительны (C1-C4)алкильные группы, наиболее предпочтительны метил и этил. Термины "алкенил" и "алкинил", как правило, означают прямые или разветвленные углеводородные радикалы, содержащие 2-16 атомов углерода и 1 двойную или тройную связь, соответственно, и включают этенил, пропенил, 3-бутен-1-ил, 2-этенбутил, 3-октен-1-ил, 3-ноненил, 3-деценил и т.п., а также пропинил, 2-бутин-1-ил, 3-пентин-1-ил, 3-гексинил, 3-октинил, 4-децинил и т.п. Предпочтительными являются C2-C6 алкенильные и алкинильные радикалы, более предпочтительны С2-С4 алкенил и алкинил.
[0015] Термин "алкилен", как правило, означает двухвалентный прямой или разветвленный углеводородный радикал, содержащий 1-20 атомов углерода, и включает, например, метилен, этилен, пропилен, бутилен, 2-метилпропилен, пентилен, 2-метилбутилен, гексилен, 2-метилпентилен, 3-метилпентилен, 2,3-диметилбутилен, гептилен, октилен и т.д. Предпочтительными являются (С1-С8)алкилены, более предпочтительны (C1-C4)алкилены, наиболее предпочтительны (С1-С2)алкилены.
[0016] Термин "циклоалкил", применяемый в настоящем описании, означает циклическую или бициклическую группу углеводородного радикала, содержащую 3-10 атомов углерода, такую как циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил, адамантил, бицикло[3,2,1]октил, бицикло[2,2,1]гептил и т.п. Предпочтительными являются (С5-C10)циклоалкилы, более предпочтительны (С5-С7)циклоалкилы.
[0017] Термин "арил" означает ароматическую карбоциклическую группу, содержащую 6-14 атомов углерода, состоящих из одного или нескольких колец либо конденсированных, либо связанных ковалентной связью, таких как, но не ограничиваясь ими, фенил, нафтил, фенантрил и бифенил.
[0018] Термин "гетероциклическое кольцо" означает моно- или полициклическое неароматическое кольцо из 4-12 атомов, содержащее по меньшей мере один атом углерода и от одного до трех гетероатомов, выбранных из серы, кислорода или азота, при этом указанные кольца могут быть насыщенными или ненасыщенными, то есть содержащими по меньшей мере одну ненасыщенную связь. Предпочтительными являются 5- или 6-членные гетероциклические кольца. Термин "гетероциклил", используемый в настоящем описании, относится к любому одновалентному радикалу, полученному из гетероциклического кольца, определенного в настоящем описании, путем удаления водорода от любого атома кольца. Примеры таких радикалов включают, но не ограничиваются ими, пиперидино, 4-морфолинил или пирролидинил.
[0019] Термин "группа-донор оксида азота" в контексте настоящего описания относится к любой группе формулы -Х1-Х2-Х3, где X1 может отсутствовать или выбран из -О-, -S- or -NH-; Х2 может отсутствовать или представляет собой (С1-С20)алкилен, необязательно замещенный одной или более группами -ONO2; и Х3 представляет -NO или -ONO2. Конкретные группы-доноры оксида азота представляют собой группы, в которых X1 отсутствует или представляет собой -О-; Х2 отсутствует или представляет собой -(C1-С6)алкилен, предпочтительно -(С1-С3)алкилен, более предпочтительно метилен; Х3 представляет собой -NO или -ONO2, предпочтительно -ONO2, и указанный алкилен необязательно замещен, как определено выше в настоящем описании. В соответствии с настоящим изобретением соединение общей формулы I может содержать одну группу-донор оксида азота или более одной идентичных или различных групп-доноров оксида азота.
[0020] В некоторых вариантах реализации соединение согласно настоящему изобретению представляет собой соединение общей формулы I, где каждый R1 независимо представляет собой Н, -COOR4, -CON(R4)2 или группу-донор оксида азота; и R4 представляет собой Н.
[0021] В некоторых вариантах реализации соединение согласно настоящему изобретению представляет собой соединение общей формулы I, где каждый R2 независимо представляет собой (С1-С8)алкил, предпочтительно (C1-C4)алкил, более предпочтительно метил или этил. В конкретных таких вариантах реализации группы R2 идентичны.
[0022] В некоторых вариантах реализации соединение согласно настоящему изобретению представляет собой соединение общей формулы I, где R3 представляет собой (C1-C8)алкил, предпочтительно (С1-С3)алкил, который необязательно замещен, предпочтительно по концевому атому углерода, посредством -ОН, -N(R5)2 или -COOR5, где каждый R5 независимо представляет собой (C1-C8)алкил, предпочтительно (C1-С2)алкил или Н. В конкретных таких вариантах реализации R3 представляет собой (C1-С8)алкил, предпочтительно (С1-С3)алкил, (С1-С8)алкилен-ОН, предпочтительно (C1-С3)алкилен-ОН, (Cl-C8)алкилен-N(R5)2, предпочтительно (C1-C3)алкилен-N(R5)2 или (C1-C8)алкилен-COOR5, предпочтительно (С1-С3)алкилен-COOR5.
[0023] В некоторых вариантах реализации соединение согласно настоящему изобретению представляет собой соединение общей формулы I, где в указанной группе-доноре оксида азота X1 отсутствует или представляет собой -О-; Х2 отсутствует или представляет собой (С1-С20)алкилен, предпочтительно -(С1-С6)алкилен, более предпочтительно -(С1-С3)алкилен, наиболее предпочтительно метилен; Х3 представляет собой -NO или -ONO2, предпочтительно -ONO2; и указанный алкилен необязательно замещен посредством одной или более групп -ONO2.
[0024] В некоторых вариантах реализации соединение согласно настоящему изобретению представляет собой соединение общей формулы I, где каждый R1 независимо представляет собой Н, -COOR4, -CON(R4)2 или группу-донор оксида азота; каждый R2 независимо представляет собой (С1-С8)алкил, предпочтительно (C1-C3)алкил, более предпочтительно метил или этил; R3 представляет собой (С1-С8)алкил, предпочтительно (С1-С3)алкил, который необязательно замещен, предпочтительно по концевому атому углерода, посредством -ОН, -N(R5)2, или -COOR5; R4 представляет собой Н; каждый R5 независимо представляет собой (С1-С8)алкил, предпочтительно (С1-С2)алкил, или Н; и в указанной группе-доноре оксида азота X1 отсутствует или представляет собой -О-; Х2 отсутствует или представляет собой (С1-С20)алкилен, предпочтительно -(С1-С6)алкилен, более предпочтительно -(С1-С3)алкилен, наиболее предпочтительно метилен; Х3 представляет собой -NO или -ONO2, предпочтительно -ONO2; и указанный алкилен необязательно замещен посредством одной или более групп -ONO2.
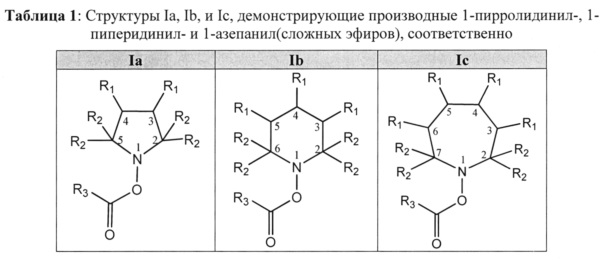
[0025] В некоторых вариантах реализации соединение согласно настоящему изобретению представляет собой соединение общей формулы I, где R1-R5 и каждая группа-донор оксида азота независимо выбраны из вариантов, определенных посредством любого из вышеуказанных вариантов реализации; и n составляет 1, 2 или 3, то есть производное 1-пирролидинил(сложного эфира) формулы Ia, производное 1-пиперидинил(сложного эфира) формулы Ib или производное 1-азепанил(сложного эфира) формулы Ic (см. таблицу 1).
[0026] В некоторых частных вариантах реализации соединение согласно настоящему изобретению представляет собой соединение формулы Ia из таблицы 1, где либо атом углерода в положении 3 пирролидинового кольца, либо атом углерода в положении 4 пирролидинового кольца, либо оба из них, каждый связан с группой-донором оксида азота. Более конкретными такими вариантами реализации являются варианты, в которых каждая из групп-доноров оксида азота независимо имеет формулу -(С1-С6)алкилен-ONO2, предпочтительно -(С1-С3)алкилен-ONO2, более предпочтительно -CH2-ONO2, или -O-(C1-С6)алкилен-ONO2, где указанный алкилен необязательно замещен посредством одной или более групп -ONO2, или представляет собой -ONO2.
[0027] В других частных вариантах реализации соединение согласно настоящему изобретению представляет собой соединение формулы Ib в таблице 1, где каждый из одного, двух или трех атомов углерода в положениях 3-5 пиперидинового кольца связан с группой-донором оксида азота, то есть (i) каждый атом углерода в положении 3 пиперидинового кольца и необязательно один или более атомов углерода в положениях 4 или 5 пиперидинового кольца связаны с группой-донором оксида азота; (ii) каждый атом углерода в положении 4 пиперидинового кольца и необязательно один или более атомов углерода в положениях 3 или 5 пиперидинового кольца связаны с группой-донором оксида азота; или (iii) каждый атом углерода в положении 5 пиперидинового кольца и необязательно один или более атомов углерода в положениях 3 или 4 пиперидинового кольца связаны с группой-донором оксида азота. Более конкретными такими вариантами реализации являются варианты, в которых каждая из групп-доноров оксида азота независимо имеет формулу -(С1-С6)алкилен-ONO2, предпочтительно -(С1-С3)алкилен-ONO2, более предпочтительно -CH2-ONO2, или -O-(С1-С6)алкилен-ONO2, где указанный алкилен необязательно замещен посредством одной или более групп -ONO, или представляет собой -ONO2.
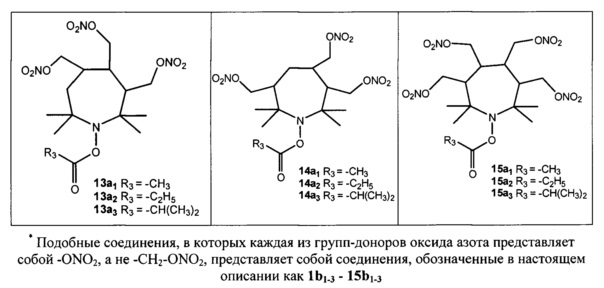
[0028] В других частных вариантах реализации соединение согласно настоящему изобретению представляет собой соединение формулы 1 с в таблице 1, в котором каждый из одного, двух, трех или четырех атомов углерода в положениях 3-6 азепанового кольца связан с группой-донором оксида азота, то есть (i) каждый атом углерода в положении 3 азепанового кольца и необязательно один или более атомов углерода в положениях 4-6 азепанового кольца связаны с группой-донором оксида азота; (ii) каждый атом углерода в положении 4 азепанового кольца и необязательно один или более атомов углерода в положениях 3, 5 или 6 азепанового кольца связаны с группой-донором оксида азота; (iii) каждый атом углерода в положении 5 азепанового кольца и необязательно один или более атомов углерода в положениях 3, 4 или 6 азепанового кольца связаны с группой-донором оксида азота; или (iv) каждый атом углерода в положении 6 азепанового кольца и необязательно один или более атомов углерода в положениях 3-5 азепанового кольца связаны с группой-донором оксида азота. Более конкретными такими вариантами реализации являются варианты, в которых каждая группа-донор оксида азота независимо имеет формулу -(С1-С6)алкилен-ONO2, предпочтительно -(С1-С3)алкилен-ONO2, более предпочтительно -CH2-ONO2, или -O-(С1-С6)алкилен-ONO2, где указанный алкилен необязательно замещен посредством одной или более групп -ONO2, или представляет собой -ONO2.
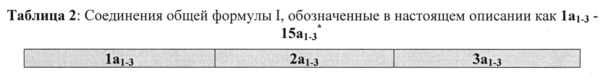
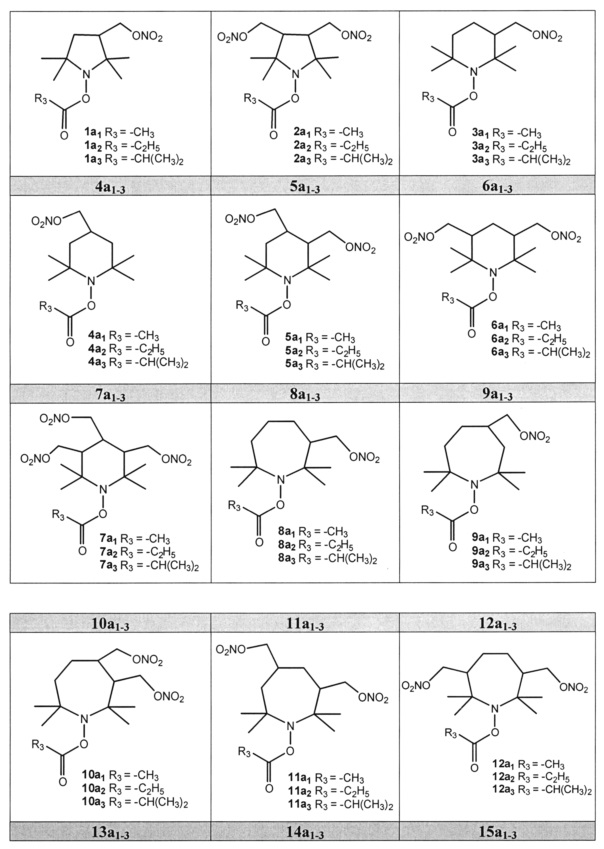
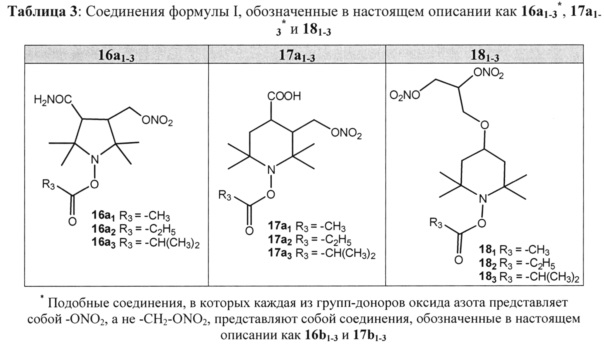
[0029] Конкретные соединения общих формул Ia, Ib, и Ic, представленных в настоящем описании, в которых каждая из групп R1 независимо представляет собой либо Н, либо группу-донор оксида азота -CH2-ONO2, и R3 представляет собой метил, этил или изопропил, представляют собой соединения, обозначенные в настоящем описании жирным шрифтом как 1а1-3-15a1-3 (соединение 1a1 также обозначено как R-107), и их полные химические структуры приведены в таблице 2. Подобные соединения, в которых каждая из групп-доноров оксида азота представляет собой -ONO2, а не -CH2-ONO2, представляют собой соединения, обозначенные в настоящем описании жирным шрифтом как 1b1-3-15b1-3. Другие конкретные соединения общих формул Ia и Ib, представленных в настоящем описании, в которых одна группа R1 представляет собой группу-донор оксида азота -CH2-ONO2, другая группа R1 не является Н, и R3 представляет собой метил, этил или изопропил, представляют собой соединения, обозначенные в настоящем описании жирным шрифтом как 16a1-3 и 17а1-3, и их полные химические структуры приведены в таблице 3. Подобные соединения, в которых группа-донор оксида азота представляет собой -ONO2, а не -CH2-ONO2, представляют собой соединения, обозначенные в настоящем описании жирным шрифтом как 16b1-3 и 17b1-3. Другие конкретные соединения общей формулы Ib, представленной в настоящем описании, в которых одна группа R1 представляет собой группу-донор оксида азота -O-CH2-CH(ONO2)CH2-ONO2, другие группы R1 представляют собой Н, и R3 представляет собой метил, этил или изопропил, представляют собой соединения, обозначенные в настоящем описании жирным шрифтом как 181-3, и их полные химические структуры приведены в таблице 3.
[0030] В конкретных вариантах реализации соединение согласно настоящему изобретению представляет собой соединение формулы Ia, то есть соединение общей формулы I, в которой n составляет 1, где каждый R2 представляет собой метил; R3 представляет собой метил, этил или изопропил; и (i) группа R1, связанная с атомом углерода в положении 3 пирролидинового кольца, представляет собой группу-донор оксида азота -CH2-ONO2; и группа R1, связанная с атомом углерода в положении 4 пирролидинового кольца, представляет собой Н, то есть 2,2,5,5-тетраметил-3-(нитрооксиметил)пирролидин-1-илацетат, 2,2,5,5-тетраметил-3-(нитрооксиметил)пирролидин-1-илпропионат и 2,2,5,5-тетраметил-3-(нитрооксиметил)пирролидин-1-илизобутират (соединения 1a1, 1а2 и 1а3, соответственно); (i) группа R1, связанная с атомом углерода в положении 3 пирролидинового кольца, представляет собой группу-донор оксида азота -ONO2; и группа R1, связанная с атомом углерода в положении 4 пирролидинового кольца, представляет собой Н, то есть 2,2,5,5-тетраметил-3-(нитроокси)пирролидин-1-илацетат, 2,2,5,5-тетраметил-3-(нитроокси)пирролидин-1-илпропионат и 2,2,5,5-тетраметил-3-(нитроокси)пирролидин-1-илизобутират (соединения, обозначенные в настоящем описании как 1b1, 1b2 и 1b3, соответственно); (iii) каждая из групп R1, связанная с атомом углерода в положениях 3 и 4 пирролидинового кольца, представляют собой группу-донор оксида азота -CH2-ONO2, то есть 2,2,5,5-тетраметил-3,4-бис(нитрооксиметил)пирролидин-1-илацетат, 2,2,5,5-тетраметил-3,4-бис(нитрооксиметил)пирролидин-1-илпропионат и 2,2,5,5-тетраметил-3,4-бис(нитрооксиметил)пирролидин-1-илизобутират (соединения, обозначенные в настоящем описании как 2a1, 2а2 и 2а3, соответственно); или (iv) каждая из групп R1, связанная с атомом углерода в положениях 3 и 4 пирролидинового кольца, представляют собой группу-донор оксида азота-ONO2, то есть 2,2,5,5-тетраметил-3,4-бис(нитроокси)пирролидин-1-илацетат, 2,2,5,5-тетраметил-3,4-бис(нитроокси)пирролидин-1-илпропионат и 2,2,5,5-тетраметил-3,4-бис(нитроокси)пирролидин-1-илизобутират (соединения, обозначенные в настоящем описании как 2b1, 2b2 и 2b3, соответственно).
[0031] В других конкретных вариантах реализации соединение, согласно настоящего изобретению, представляет собой соединение формулы Ib, то есть соединение общей формулы I, где n составляет 2, в котором каждый R2 представляет собой метил; R3 представляет собой метил, этил или изопропил; и (i) группа R1, связанная с атомом углерода в положении 3 пиперидинового кольца, представляет собой группу-донор оксида азота -CH2-ONO2; и каждая из групп R1, связанных с атомами углерода в положениях 4 и 5 пиперидинового кольца, представляет собой Н, то есть 2,2,6,6-тетраметил-3-(нитрооксиметил)пиперидин-1-илацетат, 2,2,6,6-тетраметил-3-(нитрооксиметил)пиперидин-1-илпропионат и 2,2,6,6-тетраметил-3-(нитрооксиметил)пиперидин-1-илизобутират (соединения, обозначенные в настоящем описании как 3a1, 3а2 и 3а3, соответственно); (ii) группа R1, связанная с атомом углерода в положении 3 пиперидинового кольца, представляет собой группу-донор оксида азота -ONO2; и каждая из групп R1, связанных с атомами углерода в положениях 4 и 5 пиперидинового кольца, представляют собой Н, то есть 2,2,6,6-тетраметил-3-(нитроокси)пиперидин-1-илацетат, 2,2,6,6-тетраметил-3-(нитроокси)пиперидин-1-илпропионат и 2,2,6,6-тетраметил-3-(нитроокси)пиперидин-1-илизобутират (соединения, обозначенные в настоящем описании как 3b1, 3b2 и 3b3, соответственно); (iii) группа R1, связанная с атомом углерода в положении 4 пиперидинового кольца, представляет собой группу-донор оксида азота -CH2-ONO2; каждая из групп R1, связанных с атомами углерода в положениях 3 и 5 пиперидинового кольца, представляют собой Н, то есть 2,2,6,6-тетраметил-4-(нитрооксиметил)пиперидин-1-илацетат, 2,2,6,6-тетраметил-4-(нитрооксиметил)пиперидин-1-илпропионат и 2,2,6,6-тетраметил-4-(нитрооксиметил)пиперидин-1-илизобутират (соединения, обозначенные в настоящем описании как 4a1, 4а2 и 4а3, соответственно); (iv) группа R1, связанная с атомом углерода в положении 4 пиперидинового кольца, представляет собой группу-донор оксида азота -ONO2; и каждая их групп R1, связанных с атомами углерода в положениях 3 и 5 пиперидинового кольца, представляют собой Н, то есть 2,2,6,6-тетраметил-4-(нитроокси)пиперидин-1-илацетат, 2,2,6,6-тетраметил-4-(нитроокси)пиперидин-1-илпропионат и 2,2,6,6-тетраметил-4-(нитроокси)пиперидин-1-илизобутират (соединения, обозначенные в настоящем описании как 4b1, 4b2 и 4b3, соответственно); (v) каждая из групп R1, связанных с атомами углерода в положениях 3 и 4 пиперидинового кольца, представляют собой группу-донор оксида азота -CH2-ONO2; и группа R1, связанная с атомом углерода в положении 5 пиперидинового кольца, представляет собой Н, то есть 2,2,6,6-тетраметил-3,4-бис(нитрооксиметил)пиперидин-1-илацетат, 2,2,6,6-тетраметил-3,4-бис(нитрооксиметил)пиперидин-1-илпропионат и 2,2,6,6-тетраметил-3,4-бис(нитрооксиметил)пиперидин-1-илизобутират (соединения, обозначенные в настоящем описании как 5a1, 5а2 и 5а3, соответственно); (vi) каждая из групп R1, связанных с атомами углерода в положениях 3 и 4 пиперидинового кольца, представляет собой группу-донор оксида азота -ONO2; и группа R1, связанная с атомом углерода в положении 5 пиперидинового кольца, представляет собой Н, то есть 2,2,6,6-тетраметил-3,4-бис(нитроокси)пиперидин-1-илацетат, 2,2,6,6-тетраметил-3,4-бис(нитроокси)пиперидин-1-илпропионат и 2,2,6,6-тетраметил-3,4-бис(нитроокси)пиперидин-1-илизобутират (соединения, обозначенные в настоящем описании как 5b1, 5b2 и 5b3, соответственно); (vii) каждая из групп R1, связанных с атомами углерода в положениях 3 и 5 пиперидинового кольца, представляют собой группу-донор оксида азота -CH2-ONO2; и группа R1, связанная с атомом углерода в положении 4 пиперидинового кольца, представляет собой Н, то есть 2,2,6,6-тетраметил-3,5-бис(нитрооксиметил)пиперидин-1-илацетат, 2,2,6,6-тетраметил-3,5-бис(нитрооксиметил)пиперидин-1-илпропионат и 2,2,6,6-тетраметил-3,5-бис(нитрооксиметил)пиперидин-1-илизобутират (соединения, обозначенные в настоящем описании как 6a1, 6а2 и 6а3, соответственно); (viii) каждая из групп R1, связанных с атомами углерода в положениях 3 и 5 пиперидинового кольца, представляет собой группу-донор оксида азота -ONO2; и группа R1, связанная с атомом углерода в положении 4 пиперидинового кольца, представляет собой Н, то есть 2,2,6,6-тетраметил-3,5-бис(нитроокси)пиперидин-1-илацетат, 2,2,6,6-тетраметил-3,5-бис(нитроокси)пиперидин-1-илпропионат и 2,2,6,6-тетраметил-3,5-бис(нитроокси)пиперидин-1-илизобутират (соединения, обозначенные в настоящем описании как 6b1, 6b2 и 6b3, соответственно); (ix) каждая из групп R1, связанных с атомами углерода в положениях 3 и 5 пиперидинового кольца, представляет собой группу-донор оксида азота -CH2-ONO2, то есть 2,2,6,6-тетраметил-3,4,5-трис(нитрооксиметил)пиперидин-1-илацетат, 2,2,6,6-тетраметил-3,4,5-трис(нитрооксиметил)пиперидин-1-илпропионат и 2,2,6,6-тетраметил-3,4,5-трис(нитрооксиметил)пиперидин-1-илизобутират (соединения, обозначенные в настоящем описании как 7а1, 7а2 и 7а3, соответственно); или (х) каждая из групп R1, связанных с атомами углерода в положениях 3 и 5 пиперидинового кольца, представляет собой группу-донор оксида азота -ONO2, то есть 2,2,6,6-тетраметил-3,4,5-трис(нитроокси)пиперидин-1-илацетат, 2,2,6,6-тетраметил-3,4,5-трис(нитроокси)пиперидин-1-илпропионат и 2,2,6,6-тетраметил-3,4,5-трис(нитроокси)пиперидин-1-илизобутират (соединения, обозначенные в настоящем описании как 7b1, 7b2 и 7b3, соответственно).
[0032] В других конкретных вариантах реализации соединение, применяемое в соответствии со способом согласно настоящему изобретению, представляет собой соединение формулы Ic, то есть соединение общей формулы I, где n составляет 3, где каждый R2 представляет собой метил; R3 представляет собой метил, этил или изопропил; и (i) группа R1, связанная с атомом углерода в положении 3 азепанового кольца, представляет собой группу-донор оксида азота -CH2-ONO2; и каждая из групп R1, связанных с атомами углерода в положениях 4-6 азепанового кольца, представляет собой Н, то есть 2,2,7,7-тетраметил-3-(нитрооксиметил)азепан-1-илацетат, 2,2,7,7-тетраметил-3-(нитрооксиметил)азепан-1-илпропионат и 2,2,7,7-тетраметил-3-(нитрооксиметил)азепан-1-илизобутират (соединения, обозначенные в настоящем описании как 8a1, 8а2 и 8а3, соответственно); (ii) группа R1, связанная с атомом углерода в положении 3 азепанового кольца, представляет собой группу-донор оксида азота -ONO2; и каждая из групп R1, связанных с атомами углерода в положениях 4-6 азепанового кольца, представляет собой Н, то есть 2,2,7,7-тетраметил-3-(нитроокси)азепан-1-илацетат, 2,2,7,7-тетраметил-3-(нитроокси)азепан-1-илпропионат и 2,2,7,7-тетраметил-3-(нитроокси)азепан-1-илизобутират (соединения, обозначенные в настоящем описании как 8b1, 8b2 и 8b3, соответственно); (iii) группа R1, связанная с атомом углерода в положении 4 азепанового кольца, представляет собой группу-донор оксида азота -CH2-ONO2; и каждая из групп R1, связанных с атомами углерода в положениях 3, 5 и 6 азепанового кольца, представляет собой Н, то есть 2,2,7,7-тетраметил-4-(нитрооксиметил)азепан-1-илацетат, 2,2,7,7-тетраметил-4-(нитрооксиметил)азепан-1-илпропионат и 2,2,7,7-тетраметил-4-(нитрооксиметил)азепан-1-илизобутират (соединения, обозначенные в настоящем описаний как 9a1, 9а2 и 9а3, соответственно); (iv) группа R1, связанная с атомом углерода в положении 4 азепанового кольца, представляет собой группу-донор оксида азота -ONO2; и каждая из групп R1, связанных с атомами углерода в положениях 3, 5 и 6 азепанового кольца, представляет собой Н, то есть 2,2,7,7-тетраметил-4-(нитроокси)азепан-1-илацетат, 2,2,7,7-тетраметил-4-(нитроокси)азепан-1-илпропионат и 2,2,7,7-тетраметил-4-(нитроокси)азепан-1-илизобутират (соединения, обозначенные в настоящем описании как 9b1, 9b2 и 9b3, соответственно); (v) каждая из групп R1, связанных с атомами углерода в положениях 3 и 4 азепанового кольца, представляет собой группу-донор оксида азота -CH2-ONO2; и каждая из групп R1, связанных с атомами углерода в положениях 5 и 6 азепанового кольца, представляет собой Н, то есть 2,2,7,7-тетраметил-3,4-бис(нитрооксиметил)азепан-1-илацетат, 2,2,7,7-тетраметил-3,4-бис(нитрооксиметил)азепан-1-илпропионат и 2,2,7,7-тетраметил-3,4-бис(нитрооксиметил)азепан-1-илизобутират (соединения, обозначенные в настоящем описании как 10a1, 10а2 и 10а3, соответственно); (vi) каждая из групп R1, связанных с атомами углерода в положениях 3 и 4 азепанового кольца, представляет собой группу-донор оксида азота -ONO2; и каждая из групп R1, связанных с атомами углерода в положениях 5 и 6 азепанового кольца, представляет собой Н, то есть 2,2,7,7-тетраметил-3,4-бис(нитроокси)азепан-1-илацетат, 2,2,7,7-тетраметил-3,4-бис(нитроокси)азепан-1-илпропионат и 2,2,7,7-тетраметил-3,4-бис(нитроокси)азепан-1-илизобутират (соединения, обозначенные в настоящем описании как 10b1, 10b2 и 10b3, соответственно); (vii) каждая из групп R1, связанных с атомами углерода в положениях 3 и 5 азепанового кольца, представляет собой группу-донор оксида азота -CH2-ONO2; и каждая из групп R1, связанных с атомами углерода в положениях 4 и 6 азепанового кольца, представляет собой Н, то есть 2,2,7,7-тетраметил-3,5-бис(нитрооксиметил)азепан-1-илацетат, 2,2,7,7-тетраметил-3,5-бис(нитрооксиметил)азепан-1-илпропионат и 2,2,7,7-тетраметил-3,5-бис(нитрооксиметил)азепан-1-илизобутират (соединения, обозначенные в настоящем описании как 11a1, 11а2 и 11а3, соответственно); (viii) каждая из групп R1, связанных с атомами углерода в положениях 3 и 5 азепанового кольца, представляет собой группу-донор оксида азота -ONO2; и каждая из групп R1, связанных с атомами углерода в положениях 4 и 6 азепанового кольца, представляет собой Н, то есть 2,2,7,7-тетраметил-3,5-бис(нитроокси)азепан-1-илацетат, 2,2,7,7-тетраметил-3,5-бис(нитроокси)азепан-1-илпропионат и 2,2,7,7-тетраметил-3,5-бис(нитроокси)азепан-1-илизобутират (соединения, обозначенные в настоящем описании как 11b1, 11b2 и 11b3, соответственно); (ix) каждая из групп R1, связанных с атомами углерода в положениях 3 и 6 азепанового кольца, представляет собой группу-донор оксида азота -CH2-ONO2; и каждая из групп R1, связанных с атомами углерода в положениях 4 и 5 азепанового кольца, представляет собой Н, то есть 2,2,7,7-тетраметил-3,6-бис(нитрооксиметил)азепан-1-илацетат, 2,2,7,7-тетраметил-3,6-бис(нитрооксиметил)азепан-1-илпропионат и 2,2,7,7-тетраметил-3,6-бис(нитрооксиметил)азепан-1-илизобутират (соединения, обозначенные в настоящем описании как 12a1, 12а2 и 12а3, соответственно); (х) каждая из групп R1, связанных с атомами углерода в положениях 3 и 6 азепанового кольца, представляет собой группу-донор оксида азота -ONO2; и каждая из групп R1, связанных с атомами углерода в положениях 4 и 5 азепанового кольца, представляет собой Н, то есть 2,2,7,7-тетраметил-3,6-бис(нитроокси)азепан-1-илацетат, 2,2,7,7-тетраметил-3,6-бис(нитроокси)азепан-1-илпропионат и 2,2,7,7-тетраметил-3,6-бис(нитроокси)азепан-1-илизобутират (соединения, обозначенные в настоящем описании как 12b1, 12b2 и 12b3, соответственно); (xi) каждая из групп R1, связанных с атомами углерода в положениях 3-5 азепанового кольца, представляет собой группу-донор оксида азота -CH2-ONO2; и группа R1, связанная с атомом углерода в положении 6 азепанового кольца, представляет собой Н, то есть 2,2,7,7-тетраметил-3,4,5-трис(нитрооксиметил)азепан-1-илацетат, 2,2,7,7-тетраметил-3,4,5-трис(нитрооксиметил)азепан-1-илпропионат и 2,2,7,7-тетраметил-3,4,5-трис(нитрооксиметил)азепан-1-илизобутират (соединения, обозначенные в настоящем описании как 13a1, 13а2 и 13а3, соответственно); (xii) каждая из групп R1, связанных с атомами углерода в положениях 3-5 азепанового кольца, представляет собой группу-донор оксида азота -ONO2; и группа R1, связанная с атомом углерода в положении 6 азепанового кольца, представляет собой Н, то есть 2,2,7,7-тетраметил-3,4,5-трис(нитроокси)азепан-1-илацетат, 2,2,7,7-тетраметил-3,4,5-трис(нитроокси)азепан-1-илпропионат и 2,2,7,7-тетраметил-3,4,5-трис(нитроокси) азепан-1-илизобутират (соединения, обозначенные в настоящем описании как 13b1, 13b2 и 13b3, соответственно); (xiii) каждая из групп R1, связанных с атомами углерода в положениях 3, 4 и 6 азепанового кольца, представляет собой группу-донор оксида азота -CH2-ONO2; и группа R1, связанная с атомом углерода в положении 5 азепанового кольца, представляет собой Н, то есть 2,2,7,7-тетраметил-3,4,6-трис(нитрооксиметил)азепан-1-илацетат, 2,2,7,7-тетраметил-3,4,6-трис(нитрооксиметил) азепан-1-илпропионат и 2,2,7,7-тетраметил-3,4,6-трис(нитрооксиметил)азепан-1-илизобутират (соединения, обозначенные в настоящем описании как 14a1, 14а2 и 14а3, соответственно); (xiv) каждая из групп R1, связанных с атомами углерода в положениях 3, 4 и 6 азепанового кольца, представляет собой группу-донор оксида азота -ONO2; и группа R1, связанная с атомом углерода в положении 5 азепанового кольца, представляет собой Н, то есть 2,2,7,7-тетраметил-3,4,6-трис(нитроокси)азепан-1-илацетат, 2,2,7,7-тетраметил-3,4,6-трис(нитроокси)азепан-1-илпропионат и 2,2,7,7-тетраметил-3,4,6-трис(нитроокси)азепан-1-илизобутират (соединения, обозначенные в настоящем описании как 14b1, 14b2 и 14b3, соответственно); (xv) каждая из групп R1, связанных с атомами углерода в положениях 3-6 азепанового кольца, представляет собой группу-донор оксида азота -CH2-ONO2, то есть 2,2,7,7-тетраметил-3,4,5,6-тетракис(нитрооксиметил) азепан-1-илацетат, 2,2,7,7-тетраметил-3,4,5,6-тетракис (нитрооксиметил)азепан-1-илпропионат и 2,2,7,7-тетраметил-3,4,5,6-тетракис (нитрооксиметил)азепан-1-илизобутират (соединения, обозначенные в настоящем описании как 15a1, 15а2 и 15а3, соответственно); или (xvi) каждая из групп R1, связанных с атомами углерода в положениях 3-6 азепанового кольца, представляет собой группу-донор оксида азота -ONO2, то есть 2,2,7,7-тетраметил-3,4,5,6-тетракис(нитроокси)азепан-1-илацетат, 2,2,7,7-тетраметил-3,4,5,6-тетракис(нитроокси)азепан-1-илпропионат и 2,2,7,7-тетраметил-3,4,5,6-тетракис(нитроокси)азепан-1-илизобутират (соединения, обозначенные в настоящем описании как 15b1, 15b2 и 15b3, соответственно).
[0033] В других конкретных вариантах реализации соединение согласно настоящему изобретению представляет собой соединение формулы Ia, где каждый R2 представляет собой метил; R3 представляет собой метил, этил или изопропил; и (i) группа R1, связанная с атомом углерода в положении 3 пирролидинового кольца, представляет собой группу-донор оксида азота -CH2-ONO2; и группа R1, связанная с атомом углерода в положении 4 пирролидинового кольца, представляет собой -CONH2, то есть 2,2,5,5-тетраметил-3-(нитрооксиметил)-4-карбамоил-пирролидин-1-илацетат, 2,2,5,5-тетраметил-3-(нитрооксиметил)-4-карбамоил-пирролидин-1-илпропионат и 2,2,5,5-тетраметил-3-(нитрооксиметил)-4-карбамоил-пирролидин-1-илизобутират (соединения, обозначенные в настоящем описании как 16а1, 16а2 и 16а3, соответственно); или (ii) группа R1, связанная с атомом углерода в положении 3 пирролидинового кольца, представляет собой группу-донор оксида азота -ONO2; и группа R1, связанная с атомом углерода в положении 4 пирролидинового кольца, представляет собой -CONH2, то есть 2,2,5,5-тетраметил-3-(нитроокси)-4-карбамоил-пирролидин-1-илацетат, 2,2,5,5-тетраметил-3-(нитроокси)-4-карбамоил-пирролидин-1-илпропионат и 2,2,5,5-тетраметил-3-(нитроокси)-4-карбамоил-пирролидин-1-илизобутират (соединения, обозначенные в настоящем описании как 16b1, 16b2 и 16b3, соответственно).
[0034] В других конкретных вариантах реализации соединение согласно настоящему изобретению представляет собой соединение формулы Ib, где каждый R2 представляет собой метил; R3 представляет собой метил, этил или изопропил; и (i) группа R1, связанная с атомом углерода в положении 3 пиперидинового кольца, представляет собой группу-донор оксида азота -CH2-ONO2; группа R1, связанная с атомом углерода в положении 4 пиперидинового кольца, представляет собой -СООН; и группа R1, связанная с атомом углерода в положении 5 пиперидинового кольца, представляет собой Н, то есть 2,2,6,6-тетраметил-3-(нитрооксиметил)-4-карбоксипиперидин-1-илацетат, 2,2,6,6-тетраметил-3-(нитрооксиметил)-4-карбоксипиперидин-1-илпропионат и 2,2,6,6-тетраметил-3-(нитрооксиметил)-4-карбоксипиперидин-1-ил-изобутират (соединения, обозначенные в настоящем описании как 17a1, 17а2 и 17а3, соответственно); или (ii) группа R1, связанная с атомом углерода в положении 3 пиперидинового кольца, представляет собой группу-донор оксида азота -ONO2; группа R1, связанная с атомом углерода в положении 4 пиперидинового кольца, представляет собой -СООН; и группа R1, связанная с атомом углерода в положении 5 пиперидинового кольца, представляет собой Н, то есть 2,2,6,6-тетраметил-3-(нитроокси)-4-карбоксипиперидин-1-илацетат, 2,2,6,6-тетраметил-3-(нитроокси)-4-карбоксипиперидин-1-илпропионат и 2,2,6,6-тетраметил-3-(нитроокси)-4-карбоксипиперидин-1-илизобутират (соединения, обозначенные в настоящем описании как 17b1, 17b2 и 17b3, соответственно).
[0035] В еще одном конкретном варианте реализации соединение согласно настоящему изобретению представляет собой соединение формулы Ib, где каждый R2 представляет собой метил; R3 представляет собой метил, этил или изопропил; группа R1, связанная с атомом углерода в положении 4 пиперидинового кольца, представляет собой группу-донор оксида азота -O-CH2-CH(ONO2)CH2-ONO2; и каждая их групп R1, связанных с атомом углерода в положениях 3 и 5 пиперидинового кольца, представляет, собой Н, то есть 2,2,6,6-тетраметил-4-(2,3-бис(нитроокси)пропилокси)-пиперидин-1-илацетат, 2,2,6,6-тетраметил-4-(2,3-бис(нитроокси)пропилокси)-пиперидин-1-илпропионат и 2,2,6,6-тетраметил-4-(2,3-бис(нитроокси)пропилокси)-пиперидин-1-илизобутират (соединения, обозначенные в настоящем описании как 181, 182 и 183, соответственно).
[0036] Соединения согласно настоящему изобретению могут быть синтезированы в соответствии с любой технологией или методикой, известной в данной области техники, например, как описано далее в разделе «Примеры» по отношению к соединениям 1a1, 1а2 и 1а3.
[0037] Соединения общей формулы I могут иметь один или более центров симметрии и, соответственно, могут существовать в виде энантиомеров, например оптических изомеров (R, S, или рацемата, где определенный энантиомер может иметь оптическую чистоту 90%, 95%, 99% или более) и в виде диастереоизомеров. А именно, указанные хиральные центры могут быть, например, в каждом углеродном атоме производного 1-пирролидинил(сложного эфира), производного 1-пиперидинил(сложного эфира); и производного 1-азепанил(сложного эфира) общих формул Ia, Ib и Ic, соответственно. Следует понимать, что настоящее изобретение охватывает все выше обозначенные энантиомеры, изомеры и их смеси, а также фармацевтически приемлемые соли и сольваты.
[0038] Оптически активные формы соединений общей формулы I могут быть получены с использованием любого способа, известного в данной области техники, например путем разделения рацемической формы методами перекристаллизации, путем хирального синтеза, путем экстракции хиральными растворителями или путем хроматографического разделения с использованием хиральной стационарной фазы. Неограничивающий пример способа получения оптически активных веществ представляет собой перенос через хиральные мембраны, то есть метод, согласно которому рацемат находится в контакте с барьером в виде тонкой мембраны, причем перепад концентраций или давления вызывает преимущественный перенос через мембранный барьер, и разделение происходит в результате нерацемической хиральной природы мембраны, которая пропускает только один энантиомер рацемата. Также может быть использована хиральная хроматография, которая включает хроматографию с псевдодвижущимся слоем. На рынке имеется широкое разнообразие хиральных стационарных фаз.
[0039] Соединения согласно настоящему изобретению представляют собой пролекарства соответствующих 1-пирролидинилокси-, 1-пиперидинилокси- и 1-азепанилоксипроизводных, описанных в патентах США №№6448267, 6455542 и 6759430, и, таким образом, как ожидается, они будут эффективны для всех клинических показаний, при которых эти соединения являются полезными, например, для предотвращения, лечения или контролирования любого состояния, связанного с окислительным стрессом или эндотелиальной дисфункцией. Такие состояния включают, без ограничений, ишемически-реперфузионное повреждение сетчатки; острую переднюю ишемическую оптическую невропатию; закупорку центральной ретинальной артерии; гемолитические заболевания, включая сфероцитоз, дефицит глюкозо-6-фосфатдегидрогеназы (G6PD), серповидно-клеточную болезнь, талассемии и ночную пароксизмальную гемоглобинурию; сахарный диабет, включая диабетические раны и диабетическую ретинопатию, нефропатию и сердечнососудистое заболевание; сердечно-сосудистые заболевания, такие как ишемическая болезнь сердца, стенокардия, ишемически-реперфузионное повреждение миокарда и инфаркт, острое и хроническое ишемически-реперфузионное повреждение конечности, застойная сердечная недостаточность (ЗСН), атеросклероз, аритмии сердца при гипертензии периферических артерий, идиопатическая легочная гипертензия, легочная гипертензия, связанная с идиопатическим легочным фиброзом, легочная гипертензия, связанная с гемолитическим заболеванием, первичная легочная гипертензия новорожденных, легочная гипертензия на фоне врожденной диафрагмальной грыжи и аспирации мекония; легочную гипертензию на фоне врожденного заболевания сердца; легочную гипертензию на фоне недостаточности митрального клапана, дефекта межпредсердной или межжелудочковой перегородки; контраст-индуцированную нефропатию; астму; травму; гиповолемический, нейрогенный или септический шок; идиопатическую эректильную дисфункцию; эректильную дисфункцию на фоне нервосберегающей радикальной простатэктомии; ингаляционное поражение легких вызванное токсическим агентом; ингаляционное поражение легких хлором; нейротоксичность; нейродегенеративные и неврологические расстройства, включая болезни Альцгеймера и Паркинсона, боковой амиотрофический склероз, рассеянный склероз, судорожные расстройства (с припадками), деменцию при СПИДе и расстройства, которые затрагивают процессы обучения и память; глаукому и внутриглазную гипертензию; нарушения желудочной секреции, расслабление и перистальтику желудочно-кишечного тракта (включая сфинктеры); нефропатию лекарственного генеза и вызванная заболеванием; патологические (преждевременные) и физиологические маточные сокращения; ухудшение клеточной защиты; заболевания, вызванные эндотелиальной дисфункцией; резистентность к инсулину при диабете; гипертензию, вызванную беременностью; цереброваскулярные заболевания; нарушения агрегации; или женскую половую дисфункцию, включая вагинальную сухость.
[0040] Соединения согласно настоящему изобретению обеспечивают возможность доставки соединений, в которые они превращаются в физиологических условиях, в более концентрированном жидком виде, что, в частности, показано в отношении соединения R-107, которое, под воздействием плазмы, превращается в R-100 (пример 4 далее). Возможность доставки меньших объемов последнего может быть выгодна в тех клинических ситуациях, когда объем введения ограничен, например, при ЗСН, при внутримышечных и подкожных инъекциях и всех видах местного применения. Было также обнаружено при осуществлении настоящего изобретения на практике, что соединения согласно настоящему изобретению превращаются в (и высвобождают) соответствующие 1-пирролидинилокси-, 1-пиперидинилокси- и 1-азепанилоксипроизводные в течение определенного периода времени в биологических растворах и тканях. Таким образом, эти соединения тем самым обеспечивают замедленное высвобождение соответствующих 1-пирролидинилокси-, 1-пиперидинилокси- и 1-азепанилоксипроизводных, что отражается в их более низкой средней максимальной концентрации (Cmax) в крови. Это может быть предпочтительным в тех случаях, когда нежелательно быстрое введение указанных соединений и предпочтительно замедленное высвобождение.
[0041] В другом аспекте настоящее изобретение относится к фармацевтической композиции, содержащей соединение общей формулы I, определенное выше, или его энантиомер, диастереомер, рацемат, или фармацевтически приемлемую соль или сольват, также обозначенные в настоящем описании как активный агент, и фармацевтически приемлемый носитель. Конкретные такие фармацевтические композиции содержат, в качестве активного агента, соединение, выбранное из соединений, приведенных выше в таблицах 2-3, например соединение 1a1, 1а2 или 1а3, или его энантиомер, диастереомер, рацемат, или фармацевтически приемлемую соль или сольват.
[0042] Фармацевтические композиции согласно настоящему изобретению являются подходящими для предотвращения, лечения и контролирования заболевания, расстройства или состояния, связанных с окислительным стрессом или эндотелиальной дисфункцией.
[0043] В WO 2012/093383 раскрыты способы и композиции для лечения сепсиса и связанных с ним состояний с применением 1-пирролидинилокси-, 1-пиперидинилокси- и 1 -азепанилоксипроизводных, раскрытых в патентах США №№6448267, 6455542 и 6759430, с приведением R-100 в качестве конкретного примера. В приведенных ниже примерах 5 и 6 описаны протоколы, в которых показана эффективность R-107 в качестве терапевтического агента на мышах, которых подвергали воздействию летальной дозы липополисахарида (ЛПС) Е. coli, и в отношении функции легких у овец, страдающих септической пневмонией, вызванной Pseudomonas aeruginosa.
[0044] В некоторых вариантах реализации фармацевтическую композицию согласно настоящему изобретению, таким образом, применяют для лечения сепсиса, в частности вызванного микроорганизмами или их продуктами, и связанных с ним состояний. Сепсис может быть вызван грамотрицательными бактериями, например Escherichia coli, Pseudomonas aeruginosa, видами Serratia, видами Salmonella, видами Shigella, видами Enterobacter, видами Citrobacter, видами Proteus и видами Klebsiella; грамположительными кокками, например видами Pneumococcus, видами Enterococcus, видами Staphylococcus и видами Streptococcus; некоторыми грибами и дрожжами, видами риккетсий, видами плазмоидиев, видами Clostridium, или вирусами; или токсинами грамположительных бактерий, включая токсины, вызывающие синдром токсического шока. В таких конкретных вариантах реализации лечение соединениями или фармацевтическими композициями согласно настоящему изобретению направлено на ингибирование развития связанной с сепсисом коагулопатии.
[0045] Термин "лечение", используемый в настоящем описании в отношении сепсиса и связанных с ним состояний относится к введению активного агента после появления симптомов сепсиса, независимо от причины этого патологического состояния. В соответствии с настоящим изобретением введение указанного активного агента для лечения сепсиса и связанных с ним состояний направлено на ингибирование, например ограничение или уменьшение, патологических состояний, возникающих вследствие системной инфекции, наиболее конкретно вследствие легочной артериальной гипертензии, из-за легочного шунта и вследствие снижения податливости легкого к растяжению, и в некоторых случаях - также развития связанной с сепсисом коагулопатии.
[0046] В публикации международной заявки WO 2011/092690 раскрыты способы и композиции для предотвращения, лечения или контролирования легочной артериальной гипертензии (ЛАГ) с применением 1-пирролидинилокси, 1-пиперидинилокси и 1-азепанилоксипроизводных, раскрытых в патентах США №№6448267, 6455542 и 6759430, в которых R-100 приведено в качестве конкретного примера. В приведенных ниже примерах 7-9 описаны протоколы, в которых показана эффективность R-107 в качестве терапевтического агента в модели ЛАГ у крыс и при реструктурировании сосудов в легких, вызванном монокроталином (MKT), в модели легочной гипертензии у новорожденных ягнят и в модели периферической артериальной гипертензии у карликовых свиней, соответственно.
[0047] В некоторых вариантах реализации фармацевтическую композицию согласно настоящему изобретению, таким образом, применяют для предотвращения, лечения или контролирования ЛГ, в частности ЛАГ, причем ЛГ связана с заболеванием левого отдела сердца, ЛГ связана с заболеванием легких и/или гипоксемией, или ЛГ вызвана хроническим тромботическим и/или эмболическим заболеванием. Фармацевтическую композицию согласно настоящему изобретению можно применять для лечения любой формы ЛГ, включая, но не ограничиваясь ими, легкую форму, например связанную с увеличением среднего легочного артериального давления (СЛАД) в состоянии покоя до 30, более предпочтительно 20-30, мм рт.ст.; среднюю форму, например связанную с увеличением СЛАД в состоянии покоя до 30-39 мм рт.ст.; и тяжелую форму, например связанную с увеличением СЛАД в состоянии покоя до 40 мм рт.ст. или более.
[0048] ЛАГ может представлять собой идиопатическую ЛАГ; наследственную ЛАГ; ЛАГ, связанную с коллагенозным заболеванием сосудов; ЛАГ, связанную с врожденными сердечными расстройствами; ЛАГ, связанную с ВИЧ-инфекцией; ЛАГ, связанную с венозными или капиллярными заболеваниями; ЛАГ, связанную с расстройствами щитовидной железы, болезнью накопления гликогена, болезнью Гоше, гемоглобинопатией или миелопролиферативными нарушениями; ЛАГ, связанную с повреждением от ингаляции дыма, либо от сочетания ингаляции дыма и ожога; ЛАГ, связанную с аспирацией; ЛАГ, связанную с вентиляторным повреждением; ЛАГ, связанную с пневмонией; ЛАГ, связанную с респираторным дистресс-синдромом взрослых; персистирующую ЛГ новорожденных; респираторный дистресс-синдром недоношенных новорожденных; аспирацию мекония у новорожденных; диафрагмальную грыжу новорожденных; гемангиоматоз легочных капилляров или легочную вено-окклюзионную болезнь. Заболевание левого отдела сердца может представлять собой левостороннее заболевание предсердия, или заболевание желудочка, или заболевания клапанов. Заболевание легкого может представлять собой хроническую обструктивную болезнь легких; интерстициальное заболевание легких; нарушение дыхания во сне; альвеолярное расстройство гиповентиляции; хроническое нахождение на большой высоте или развивающуюся легочную аномалию. Хроническое тромботическое и/или эмболическое заболевание может представлять собой тромбоэмболическую обструкцию дистальных или проксимальных легочных артерий или нетромботическую эмболию легких, например, опухолевыми клетками или паразитами.
[0049] Многие из заболеваний, расстройств или состояний, перечисленных выше, могут быть связаны с повышенным риском ЛГ, причем конкретные примеры включают врожденное заболевание сердца, например синдром Эйзенменгера; заболевание левого отдела сердца; заболевание легочных вен, например сужение фиброзной ткани или окклюзию легочных вен и венул; заболевание легочных артерий; заболевания, вызывающие альвеолярную гипоксию; фиброзные заболевания легких; синдром Вильямса; пациентов с поражением от внутривенного употребления наркотиков; легочный васкулит, такой как синдромы Вегенера, Гудпасчера и Черджа-Стросс; эмфизему; хронический бронхит; кифосколиоз; кистозный фиброз; расстройства, представляющие собой гипервентиляцию вследствие ожирения и апноэ во сне; легочный фиброз; саркоидоз; силикоз; КРПСТ (кальциноз кожи, синдром Рейно; расстройство моторики пищевода; склеродактилия и телеангиэктазия) и другие заболевания соединительной ткани. Например, субъект с мутацией костного морфогенетического белка-рецептора Е (РКМБ2) имеет пожизненный риск приобретения наследственной легочной артериальной гипертензии 10-20%, а субъекты с наследственной геморрагической телеангиэктазией, в частности субъекты, содержащие мутации в гене активин-рецептороподобной киназы (ALK1), были также определены как подверженные риску заболевания идиопатической легочной артериальной гипертензией. Факторы риска и диагностические показатели ЛГ описаны в источнике McGoon et ah, Chest, 2004, 126, 14S-34S.
[0050] Термины "лечение" и "предотвращение", применяемые в настоящем описании в отношении ЛГ, относятся к введению активного агента после появления симптомов ЛГ в любой его форме, или до появления симптомов, в частности пациентам, имеющим риск в отношении ЛГ, соответственно. Термин "контролирование", применяемый в настоящем описании в отношении ЛГ, относится к предотвращению повторного возникновения ЛГ у пациентов, ранее страдавших ЛГ.
[0051] В WO 2013/005216 раскрыты способы и композиции для предотвращения и лечения ишемически-реперфузионного повреждения почки с применением 1-пирролидинилокси, 1-пиперидинилокси и 1-азепанилоксипроизводных, описанных в патентах США №№6448267, 6455542 и 6759430, в которых R-100 приведено в качестве конкретного примера. В приведенном ниже примере 10 описан протокол, в котором показана эффективность R-107 в качестве терапевтического агента в модели ишемически-реперфузионного повреждения почки у крыс. В конкретных вариантах реализации фармацевтическую композицию согласно настоящему изобретению, таким образом, применяют для предотвращения или лечения ишемически-реперфузионного повреждения почки.
[0052] Термин "ишемия почки" относится к дефициту кровотока в одной или обеих почках или нефронах, как правило, из-за функционального сужения или существующей обструкции кровеносного сосуда или хирургического удаления почки. Ишемия почки может быть результатом различных заболеваний, включая, но не ограничиваясь ими, геморрагический шок, септический шок, асфиксию, также известную как удушье, остановку сердечной деятельности, также известную как остановка сердца или остановка кровообращения, остановку дыхания, респираторную недостаточность, кардиогенный шок, аневризму аорты, оперативное вмешательство при аневризме аорты, гипотензию, обезвоживание, спинальный шок, травму, пересадку трупной почки, пересадку почки от живого донора, пересадку печени, заболевание печени, ишемию почки, обусловленную действием лекарственного средства, гидронефроз, обструкцию уретры, операцию в условиях искусственного кровообращения, введение радиоконтрастного агента, эндоваскулярную катетеризацию почечной артерии, реноваскулярный стеноз, тромбоз почечных артерий, обструкцию мочеточника, гипоксию и гипоксемию. Термин "ишемически-реперфузионное повреждение почки" относится к поражению, причиненному почке (-ам), когда кровоснабжение возвращается в ткань после периода ишемии почки. Ишемически-реперфузионное повреждение почки характеризуется нарушением функции почки и тубулярными повреждениями и рассматривается как основная причина острой почечной недостаточности, которая также может иметь отношение к развитию и прогрессированию некоторых форм хронической почечной недостаточности. В общем, отсутствие кислорода и питательных веществ в крови в течение ишемического периода создает состояние, при котором восстановление циркуляции приводит к воспалению и окислительному повреждению через возбуждение окислительного стресса, а не к восстановлению нормальной функции.
[0053] Термин "лечение", применяемый в настоящем описании в отношении ишемически-реперфузионного повреждения почки, относится к введению активного агента после появления симптомов ишемически-реперфузионного повреждения почки, например, после восстановления притока крови к ишемически пораженной ткани, независимо от причины, вызвавшей ишемию почки. Термин "предотвращение", применяемый в настоящем описании в отношении ишемически-реперфузионного повреждения почки, относится к введению указанного активного агента до появления симптомов, например либо до наступления ишемии почки, либо после наступления ишемии почки, но до реперфузии, и в основном относится к случаям, в которых ишемия и/или реперфузия почки связаны с хирургическим вмешательством, например с оперативным вмешательством при аневризме аорты, пересадкой трупной почки, пересадкой почки от живого донора, пересадкой печени, операцией в условиях искусственного кровообращения или эндоваскулярной катетеризацией почечной артерии. В соответствии с настоящим изобретением, введение указанного активного агента либо для лечения, либо для предотвращения ишемически-реперфузионного повреждения почки направлено на ингибирование, например ограничение или сокращение, дисфункции почки, инфильтрации полиморфноядерных нейтрофилов в паренхиму почки и гистологического нарушения, например тубулярного некроза.
[0054] В приведенных ниже примерах 11-12 описаны протоколы, в которых показана эффективность R-107 в качестве терапевтического агента в моделях ишемически-реперфузионного повреждения сетчатки у мышей и свиней. В некоторых вариантах реализации фармацевтическую композицию согласно настоящему изобретению, таким образом, применяют для лечения ишемически-реперфузионного повреждения сетчатки.
[0055] Термин "ишемия сетчатки" относится к состояниям, при которых кровоснабжение клеток сетчатки нарушается, что приводит к дефициту подачи кислорода к ткани сетчатки. Термин "ишемически-реперфузионное повреждение сетчатки" относится к состояниям, при которых ишемия сетчатки сопровождется улучшенным кровотоком (так называемой "реперфузией"), которая, таким образом, увеличивает образование окислителя и, следовательно, индуцирует повреждение ткани.
[0056] Термин "лечение", применяемый в настоящем описании в отношении ишемически-реперфузионного повреждения сетчатки, относится к введению активного агента после появления симптомов ишемически-реперфузионного повреждения сетчатки, например после восстановления притока крови к ишемически пораженной ткани, независимо от причины, вызвавшей ишемию сетчатки. В соответствии с настоящим изобретением, введение указанного активного агента для лечения ишемически-реперфузионного повреждения сетчатки направлено на ингибирование, например ограничение или уменьшение, степени повреждения сетчатки и в конечном итоге потери зрения.
[0057] В приведенном ниже примере 13 описан протокол, в котором показана эффективность R-107 в качестве терапевтического агента в крысиной модели ишемически-реперфузионного повреждения миокарда. В некоторых вариантах реализации фармацевтическую композицию, согласно настоящему изобретению, таким образом, применяют для предотвращения или лечения ишемически-реперфузионного повреждения миокарда.
[0058] Термин "ишемия миокарда" относится к состояниям, при которых существует несоответствие между притоком кислорода и потребностью миокарда в кислороде. Термин "ишемически-реперфузионное повреждение миокарда" относится к ситуациям, когда реваскуляризация подверженной ишемии области сердца сопровождается увеличением потока свободных радикалов с последующим развитием повреждения ткани миокарда.
[0059] Термин "лечение", применяемый в настоящем описании в отношении ишемически-реперфузионного повреждения миокарда, относится к введению активного агента после проявления симптомов ишемически-реперфузионного повреждения миокарда, например после восстановления притока крови к ишемически пораженной ткани, независимо от причины, вызвавшей миокардиальную ишемию. Термин "предотвращение", применяемый в настоящем описании ишемически-реперфузионного повреждения миокарда, относится к введению указанного активного агента до появления симптомов, например либо до начала ишемии миокарда, либо после, но до реперфузии, и в основном относится к случаям, вызванным срочной терапевтической реваскуляризационной процедурой, такой как ангиопластика или тромболиз. В соответствии с настоящим изобретением, введение указанного активного агента либо для лечения, либо для предотвращения ишемически-реперфузионного повреждения миокарда, направлено на ингибирование, то есть на ограничение или уменьшение степени нежизнеспособности миокарда и появления аритмии.
[0060] В приведенном ниже примере 14 описан протокол, в котором показана эффективность R-107 в качестве терапевтического агента в модели острого ишемически-реперфузионного повреждения конечности у карликовых свиней. В некоторых вариантах реализации фармацевтическую композицию согласно настоящему изобретению, таким образом, применяют для предотвращения или лечения ишемически-реперфузионного повреждения конечности.
[0061] Термин "ишемия конечности" относится к несоответствию притока кислорода к конечности и потребностью конечности в кислороде. Термин "ишемически-реперфузионное повреждение конечности" относится к повреждению, произошедшему в результате резкого восстановления кровотока в ранее ишемизированной конечности.
[0062] Термин "лечение", применяемый в настоящем описании в отношении ишемически-реперфузионного повреждения конечности, относится к введению активного агента после появления симптомов ишемически-реперфузионного повреждения конечности, например после восстановления притока крови к ишемически пораженной ткани, независимо от причины, вызвавшей ишемию конечности. Термин "предотвращение", применяемый в настоящем описании в отношении ишемически-реперфузионного повреждения конечности, относится к введению указанного активного агента до появления симптомов, то есть, либо до наступления ишемии конечности, либо после наступления ишемии конечности, но до реперфузии, и в основном относится к случаям, в котором восстановление кровотока в пораженной конечности происходит в течение 6-12 часов острой ишемии. В соответствии с настоящим изобретением, введение указанного активного агента либо для лечения, либо для предотвращения ишемически-реперфузионного повреждения конечности, направлено на ингибирование, то есть ограничение или уменьшение повреждения мышц, мышечной слабости, некроза конечности и гангрены, ампутации конечности, миоглобинурии, почечной недостаточности, синдрома сдавливания, гиперкалиемии, острого респираторного дистресс-синдрома и циркуляторного шока.
[0063] В приведенном ниже примере 15 описан протокол, в котором показана эффективность R-107 в качестве терапевтического агента в модели контраст-индуцированной нефропатии у крыс. В некоторых вариантах реализации фармацевтическую композицию согласно настоящему изобретению, таким образом, применяют для предотвращения или лечения контраст-индуцированной нефропатии.
[0064] Термин "контраст-индуцированная нефропатия" относится к нарушению морфологии и функции почки в результате резкого введения рентгеноконтрастного красителя для проведения ангиографии, причем указанная нефропатия, как правило, происходит на фоне заболевания почки, о чем свидетельствует снижение скорости клубочковой фильтрации и тубулярной функции и повышение уровня азота мочевины в сыворотке крови (АМК) и/или креатинина.
[0065] Термины "лечение" и "предотвращение", применяемые в настоящем описании контраст-индуцированной нефропатии, относятся к введению активного агента после появления симптомов контраст-индуцированной нефропатии или до появления симптомов, соответственно. В соответствии с настоящим изобретением, введение указанного активного агента, либо для лечения, либо для предотвращения контраст-индуцированной нефропатии, направлено на обеспечение жизнеспособности почки, что отражается посредством морфологической оценки и функциональных показателей клубочковой фильтрации в почках и поведения почечных канальцев, таких как АМК и креатинин сыворотки крови.
[0066] В WO 2013/190497 раскрыты способы и композиции для лечения ингаляционного поражения легких хлором (ИПЛХ) с применением, наряду с прочим, 1-пирролидинилокси-, 1-пиперидинилокси- и 1-азепанилоксипроизводных, раскрытых в патентах США №№6448267, 6455542 и 6759430, в которых R-100 приведено в качестве конкретного примера. В приведенном ниже примере 16 показана эффективность R-107 в качестве терапевтического агента в модели при воздействии хлором у мышей.
[0067] В некоторых вариантах реализации фармацевтическую композицию согласно настоящему изобретению, таким образом, применяют для лечения воспалительного заболевания легкого, вызванного вдыханием токсического агента или раздражителя. В одном конкретном варианте реализации такой токсический агент представляет собой Сl2, и фармацевтическую композицию применяют для лечения ИПЛХ. В других конкретных вариантах реализации такой токсический агент представляет собой боевой химический агент - фосген или дифосген, или раздражителем является дым.
[0068] Термин "лечение", применяемый в настоящем описании в отношении воспалительных заболеваний легкого, вызванных вдыханием токсического агента или раздражителя, относится к введению активного агента после воздействия указанного токсического агента или раздражителя и после появления симптомов указанного воспалительного заболевания, для уменьшения действия указанных токсического агента или раздражителя в отношении легких. В соответствии с настоящим изобретением, введение указанного активного агента для лечения ИПЛХ направлено на снижение отека легких и легочного шунта, уменьшение инфильтрации полиморфноядерных нейтрофилов (ПМН) в легочную паренхиму, подавление снижения податливости легкого к растяжению, улучшение обеспечения кислородом и уменьшение задержки углекислого газа.
[0069] В приведенном ниже примере 17 описан протокол, в котором показана эффективность R-107 в качестве терапевтического агента в модели эректильной дисфункции у крыс. В некоторых вариантах реализации фармацевтическую композицию согласно настоящему изобретению применяют, таким образом, для лечения эректильной дисфункции.
[0070] Термин "эректильная дисфункция" относится к неспособности субъекта мужского пола проявлять эрекцию, позволяющую надежно и эффективно проникать во влагалище. Термин "лечение", применяемый в настоящем описании в отношении эректильной дисфункции, относится к введению активного агента после появления симптомов эректильной дисфункции. В соответствии с настоящим изобретением, введение указанного активного агента для лечения эректильной дисфункции направлено на улучшение качества эрекции и, тем самым, облегчение успешного проникновения во влагалище.
[0071] Фармацевтическая композиция согласно настоящему изобретению может быть представлена в виде различных составов, например, в фармацевтически приемлемой форме и/или в форме соли, а также в различных дозах.
[0072] В одном варианте реализации фармацевтическая композиция согласно настоящему изобретению содержит нетоксичную фармацевтически приемлемую соль соединения общей формулы I. Подходящие фармацевтически приемлемые соли включают соли, полученные посредством добавления кислоты, такие как, не ограничиваясь ими, мезилатная соль, малеатная соль, фумаратная соль, тартратная соль, гидрохлоридная соль, гидробромидная соль, эзилатная соль, n-толуолсульфонатная соль, бензолсульфонатная соль, бензоатная соль, ацетатная соль, фосфатная соль, сульфатная соль, цитратная соль, карбонатная соль и сукцинатная соль. Дополнительные фармацевтически приемлемые соли включают соли аммония (NH4+) или органического катиона, полученного из амина, имеющего формулу R4N+, где каждый из R независимо выбран из Н, C1-C-, предпочтительно C1-С6 алкила, такого как метил, этил, пропил, изопропил, н-бутил, втор-бутил, изобутил, трет-бутил, н-пентил, 2,2-диметилпропил, н-гексил и т.п., фенила или гетероарила, такого как пиридил, имидазолил, пиримидинил и т.п., или два R совместно с атомом азота, к которому они присоединены, образуют 3-7 членное кольцо, необязательно содержащее дополнительный гетероатом, выбранный из N, S и О, такое как пирролидин, пиперидин и морфолин. Кроме того, когда соединения общей формулы I содержат кислотную группу, подходящие фармацевтически приемлемые соли могут включать соли металлов, такие как соли щелочных металлов, например соли лития, калия или натрия, и соли щелочноземельных металлов, например соли кальция или магния.
[0073] Другие фармацевтически приемлемые соли включают соли катионного липида или смесей катионных липидов. Катионные липиды часто смешивают с нейтральными липидами перед их применением в качестве средств доставки. Нейтральные липиды включают, но не ограничиваются ими, лецитины; фосфатидилэтаноламин; диацилфосфатидилэтаноламин, такой как диолеоилфосфатидилэтаноламин, дипальмитоилфосфатидилэтаноламин, пальмитоилолеоилфосфатидилэтаноламин и дистеароилфосфатидилэтаноламин; фосфатидилхолин; диацилфосфатидилхолины, такие как диолеоилфосфатидилхолин, дипальмитоилфосфатидихолин, пальмитоилолеоилфосфатидилхолин и дистеароилфосфатидилхолин; фосфатидил глицерин; диацилфосфатидилглицерины, такие как диолеилфосфатидилглицерин, дипальмитоилфосфатидилглицерин и дистереарилфосфатидилглицерин; фосфатидилсерин; диацилфосфатидилсерины, такие как диолеоил- или дипальмитоилфосфатидилсерин; и дифосфатидилглицерины; сложные эфиры жирных кислот; сложные эфиры глицерина; сфинголипиды; кардиолипин; цереброзиды; церамиды; и их смеси. Нейтральные липиды также содержат холестерин и другие 3β-гидроксистерины.
[0074] Примеры соединений катионных липидов содержат, но не ограничиваются ими, Липофектин (Lipofectin®, Life Technologies, Берлингтон, Онтарио) (состав 1:1 (масс./масс.) катионного липида N-[1-(2,3-диолеилокси)пропил]-N,N,N-триметиламмония хлорида и диолеоилфосфатидилэтаноламина); Липофектамин (Lipofectamine™, Life Technologies, Берлингтон, Онтарио) (состав 3:1 (масс./масс.) поликатионного липида 2,3-диолеилокси-N- [2(спериминкарбоксамидо)этил]-N,N-диметил-1-пропанамин-ийтрифторацетата и диолеоилфосфатидилэтаноламина), Липофектамин плюс (Lipofectamine Plus, Life Technologies, Берлингтон, Онтарио) (Lipofectamine и реагент Plus), Липофектамин 2000 (Lipofectamine 2000, Life Technologies, Берлингтон, Онтарио) (катионный липид), Эффектен (Effectene, Qiagen, Миссисога, Онтарио) (нелипосомный липидный состав), Метафектин (Metafectene, Biontex, Мюнхен, Германия) (поликатионный липид), Эу-фектины (Eu-fectins, Promega Biosciences, Сан-Луис Обиспо, Калифорния) (этанольные катионные липиды №1-12: C52H106N6O4⋅4CF3CO2H, C88H178N8O4S2⋅4CF3CO2H, C40H84NO3P⋅CF3CO2H, C50H103N7O3⋅4CF3CO2H, C55H116N8O2⋅6CF3CO2H, C49H102N6O3⋅4CF3CO2H, C44H89N5O3⋅2CF3CO2H, C100H206N12O4S2⋅8CF3CO2H, C162H330N22O9⋅13CF3CO2H, C43H88N4O2⋅2CF3CO2H, C43H88N4O3⋅2CF3CO2H, C41H78NO8P); Цитофектин (Cytofectene, Bio-Rad, Геркулес, Калифорния) (смесь катионного липида и нейтрального липида), ДжинПОРТЕР (GenePORTER®, Gene Therapy Systems, Сан-Диего, Калифорния) (состав нейтрального липида (Dope) и катионного липида) и ФуДЖИН 6 (FuGENE 6, Roche Molecular Biochemicals, Индианаполис, Индиана) (нелипосомальный реагент на основе мультикомпонентного липида).
[0075] Фармацевтически приемлемые соли согласно настоящему изобретению могут быть получены обычными способами, например путем реакции основной формы активного агента, то есть соединения общей формулы I, с одним или более эквивалентами соответствующей кислоты в растворителе или среде, в которой соль нерастворима, или в таком растворителе, как вода, которую удаляют под вакуумом или посредством сублимационной сушки, или путем обмена аниона/катиона существующей соли на другой анион/катион на соответствующей ионообменной смоле.
[0076] Настоящее изобретение включает сольваты соединений общей формулы I, а также их соли, например гидраты.
[0077] Фармацевтические композиции, предложенные в настоящем изобретении, могут быть получены с помощью обычных методик, например, как описано в источнике Remington: The Science and Practice of Pharmacy, 19th Ed., 1995. Композиции могут быть приготовлены, например, путем однородного и равномерного приведения активного агента в ассоциацию с жидким носителем, тонко измельченным твердым носителем или с ними обоими и, если необходимо, последующего формования продукта с получением желаемого состава. Композиции могут быть в жидкой, твердой или полутвердой формах и могут также содержать фармацевтически приемлемые наполнители, носители, разбавители или адъюванты и другие инертные ингредиенты и вспомогательные вещества. В одном варианте реализации фармацевтическая композиция согласно настоящему изобретению приготовлена в виде наночастиц.
[0078] Композиции могут быть приготовлены для любого подходящего способа введения, но предпочтительно они приготовлены для парентерального введения, например внутривенного, внутриартериального, внутримышечного, внутрибрюшинного, интратекального, внутриплеврального, внутритрахеального, подкожного или местного введения, а также для ингаляций. Фармацевтические композиции, приготовленные для внутримышечных инъекций, могут подходить, в частности, для неотложного применения, такого как при ИПЛХ; и фармацевтические композиции, приготовленные для местного введения, могут подходить, в частности, для лечения кожных язв и ран, повышенного внутриглазного давления и увеита (путем нанесения на роговицу), эректильной дисфункции (путем нанесения на половой член), а также для увеличения количества генитальной смазки (путем вагинального применения). Дозировка зависит от состояния пациента и будет определяться по усмотрению практикующего врача.
[0079] Фармацевтическая композиция согласно настоящему изобретению может быть представлена в форме стерильной водной или масляной суспензии для инъекций, которая может быть получена в соответствии с известным методом при использовании подходящих диспергирующих, смачивающих или суспендирующих агентов. Стерильный препарат для инъекций может также представлять собой стерильный инъецируемый раствор или суспензию в нетоксичном парентерально приемлемом разбавителе или растворителе. Приемлемые переносящие среды (vehicles) и растворители, которые могут быть использованы, включают, но не ограничиваются ими, воду, раствор Рингера, полиэтиленгликоль (ПЭГ), 2-гидроксипропил-β-циклодекстрин (HPCD), Твин-80 и изотонический раствор хлорида натрия.
[0080] Фармацевтические композиции в соответствии с настоящим изобретением, в том случае, если они приготовлены для ингаляции, могут быть введены с использованием любого подходящего устройства, известного в данной области техники, таких как дозирующие аэрозольные ингаляторы, распылители жидкостей, ингаляторы сухого порошка, опрыскиватели, паровые ингаляторы, электрогидродинамические аэрозольные распылители и тому подобные.
[0081] Фармацевтические композиции в соответствии с настоящим изобретением, в том случае, если они приготовлены введения, отличного от парентерального, могут быть в форме, подходящей для перорального применения, например, в виде таблеток, пастилок (troches), таблеток для рассасывания (lozenges), водных или масляных суспензий, диспергируемых порошков или гранул, эмульсий, твердых или мягких капсул, сиропов или эликсиров.
[0082] Фармацевтические композиции, предназначенные для перорального введения, должны быть приготовлены таким образом, чтобы ингибировать высвобождение активного агента в желудке, то есть должны задерживать высвобождение активного агента до тех пор, пока по меньшей мере часть лекарственной формы не пройдет через желудок, для того чтобы избежать повышенной кислотности содержимого желудка в результате гидролиза активного агента до его в значительной степени не растворимой в воде формы, например соответствующего 1-пирролидинилокси-, 1-пиперидинилокси- или 1-азепанилоксипроизводного. Такими конкретными композициями являются композиции, в которых активный агент покрыт полимером рН-зависимого кишечнорастворимого покрытия. Примеры полимеров рН-зависимого кишечнорастворимого покрытия включают, но не ограничиваются ими, Эудрагит S (Eudragit® S) (поли(метакриловая кислота, метилметакрилат), 1:2), Эудрагит L 55 (Eudragit® L 55) (поли(метакриловая кислота, этилакрилат), 1:1), Колликоат (Kollicoat®) (поли(метакриловая кислота, этилакрилат), 1:1), фталат гидроксипропилметилцеллюлозы (ГПМЦФ), альгинаты, карбоксиметилцеллюлозу и их комбинации. Указанный полимер рН-зависимого кишечнорастворимого покрытия может присутствовать в композиции в количестве от примерно 10% до примерно 95% по массе от общей массы композиции.
[0083] Фармацевтические композиции, предназначенные для перорального введения, могут быть получены в соответствии с любым способом, известным в данной области техники для получения фармацевтических композиций, и могут дополнительно содержать один или более агентов, выбранных из подсластителей, ароматизаторов, красителей и консервантов, для обеспечения фармацевтически привлекательных и приятных на вкус препаратов. Таблетки содержат активный ингредиент в смеси с нетоксичными фармацевтически приемлемыми вспомогательными веществами, подходящими для получения таблеток. Такими вспомогательными веществами могут быть, например, инертные разбавители, такие как карбонат кальция, карбонат натрия, лактоза, фосфат кальция или фосфат натрия; гранулирующие и разрыхляющие агенты, например кукурузный крахмал или альгиновая кислота; связующие агенты, например крахмал, желатин или аравийская камедь; и смазывающие агенты, например стеарат магния, стеариновая кислота или тальк. Таблетки могут быть либо не содержать покрытия, либо содержать покрытие, нанесенное с применением известных методов для замедления дезинтеграции и всасывания в желудочно-кишечном тракте и, тем самым, обеспечения замедленного действия в течение длительного периода. Например, может быть использовано вещество для задержки во времени, такое как глицерилмоностеарат или глицерилдистеарат. Таблетки могут быть также покрыты с применением методов, описанных в патентах США №№4256108, 4166452 и 4265874, с получением осмотических терапевтических таблеток для контролируемого высвобождения. Фармацевтическая композиция согласно настоящему изобретению может быть также представлена в форме эмульсий масло-в-воде.
[0084] Фармацевтические композиции согласно настоящему изобретению могут быть приготовлены для контролируемого высвобождения активного агента. Такие композиции могут быть приготовлены в виде матрицы с контролируемым высвобождением, например в виде таблеток с матрицей с контролируемым высвобождением, в которых высвобождение растворимого активного агента регулируют путем активного диффундирования через гель, образованный после набухания гидрофильного полимера, приведенного в контакт с растворяющей жидкостью (in vitro) или жидкостью желудочно-кишечного тракта (in vivo). Было описано множество полимеров, способных к образованию такого геля, например производные целлюлозы, в частности простые эфиры целлюлозы, такие как гидроксипропилцеллюлоза, гидроксиметилцеллюлоза, метилцеллюлоза или метилгидроксипропилцеллюлоза, и среди различных коммерческих видов этих простых эфиров присутствуют такие, которые обладают достаточно высокой вязкостью. В других конфигурациях композиции содержат активное вещество, приготовленное для контролируемого высвобождения в микроинкапсулированной лекарственной форме, в которой мелкие капли активного агента окружены покрытием или мембраной с образованием частиц в диапазоне от нескольких микрометров до нескольких миллиметров.
[0085] Другой предполагаемый состав представляет собой системы депо на основе биоразлагаемых полимеров, в которых по мере разложения полимера активный ингредиент медленно высвобождается. Наиболее распространенным классом биоразлагаемых полимеров являются гидролитически лабильные полиэфиры, полученные из молочной кислоты, гликолевой кислоты или комбинаций этих двух молекул. Полимеры, полученные из таких индивидуальных мономеров, содержат поли(D,L-лактид) (ПЛА), поли(гликолид) (ПГА), и сополимер D,L-лактида и гликолида (ПЛГ).
[0086] В другом аспекте настоящее изобретение относится к соединению общей формулы I, определенному выше, или его энантиомеру, диастереомеру, рацемату, или фармацевтически приемлемой соли или сольвату, для применения для предотвращения, лечения или контролирования заболевания, расстройства или состояния, связанных с окислительным стрессом и эндотелиальной дисфункцией.
[0087] В еще одном аспекте настоящее изобретение относится к применению соединения общей формулы I, определенного выше, или его энантиомера, диастереомера, рацемата, или фармацевтически приемлемой соли или сольвата, для получения фармацевтической композиции для предотвращения, лечения или контролирования заболевания, расстройства или состояния, связанных с окислительным стрессом и эндотелиальной дисфункцией.
[0088] В еще одном аспекте настоящее изобретение относится к способу предотвращения, лечения или контролирования заболевания, расстройства или состояния, связанных с окислительным стрессом и эндотелиальной дисфункцией у нуждающегося в этом индивидуума, включающему введение указанному индивидууму эффективного количества соединения общей формулы I, определенного выше, или его энантиомера, диастереомера, рацемата, или фармацевтически приемлемой соли или сольвата.
[0089] В одном частном варианте реализации способ согласно настоящему изобретению предназначен для лечения ИПЛХ.
[0090] Настоящее изобретение будет проиллюстрировано следующими примерами, не имеющими ограничительного характера.
ПРИМЕРЫ
Экспериментальная часть
Синтез 3-нитрооксиметилпроксила
[0091] Суспензию 3-карбоксипроксила (77,5 г, 0,416 моль) в сухом тетрагидрофуране (ТГФ, 500 мл) охлаждали до 0°C. К суспензии медленно добавляли алюмогидрид лития (2М раствор в ТГФ, 160 мл, 0,32 моль) в течение 4 часов в атмосфере азота. В процессе добавления температуру поддерживали ниже 5°C. После завершения добавления реакционную смесь перемешивали при 0-5°C в течение 30 минут и затем при комнатной температуре в течение 3 часов. Реакционную смесь затем снова охлаждали до 0°C. Небольшими порциями медленно в течение 1 часа добавляли твердый сульфат натрия декагидрат (52 г). Суспензию перемешивали еще в течение 1 часа. Суспензию разбавили этилацетатом (1 литр) и фильтровали. Остаток на фильтре промывали этил ацетатом (500 мл), и концентрировали фильтрат на роторном испарителе. Осадок, полученный после концентрирования, суспендировали в 30% этилацетате-гексане (500 мл), и отделенное твердое вещество отфильтровывали и промывали 30% этилацетат-гексаном и сушили под вакуумом с получением 3-гидроксиметилпроксила в виде твердого вещества желтого цвета (56,320 г). Данный материал использовали без очистки для следующей реакции. Концентрированную азотную кислоту (90% раствор, 100 мл) охлаждали до 0°C с использованием ледяной бани в чаше вместимостью 2 литра. К азотной кислоте медленно добавляли концентрированную серную кислоту (100 мл) при 0°C в течение 15 минут. Смесь перемешивали при 0-5°C в течение 15 минут. Добавляли 3-гидроксиметилпроксил (50 г, 0,29 моль) небольшими порциями в течение 2 часов. После добавления смесь перемешивали при 0-5°C в течение 1 часа и гасили дробленым льдом (~1 кг). Затем смесь подщелачивали путем медленного добавления твердого карбоната калия (460 г) в течение 1 часа при 0°C. Подщелоченную смесь перемешивали при комнатной температуре в течение 30 минут. Твердое вещество отделяли фильтрованием и промывали водой (1 литр). Твердое вещество повторно суспендировали в воде (400 мл) с добавлением этилацетата (400 мл), и полученную двухфазную смесь переносили в делительную воронку. Этилацетатный слой собирали. Водный слой снова подвергали экстракции этилацетатом (400 мл). Объединенный органический экстракт сушили на безводном сульфате натрия и фильтровали. Фильтрат концентрировали на роторном испарителе. Осадок растворяли этилацетатом и растирали с гексаном. Выделенное твердое вещество концентрировали путем фильтрования с получением 3-нитрооксиметилпроксила в виде бледно-желтого твердого вещества (39,7 г). МС (ЭР+): m/z 218,3 (М+1).
Синтез (1-гидрокси-2,2,5,5-тетраметилпирролидин-3-ил)метилнитрата гидрохлорида
[0092] Суспензию 3-нитрооксиметилпроксила (10,0 г, 0,046 моль) в этаноле (100 мл) медленно обрабатывали 4 М раствором соляной кислоты в диоксане (0,1 моль) при комнатной температуре. Реакционную смесь затем перемешивали в течение 2 часов и концентрировали на роторном испарителе. Добавляли сухой эфир, и выделенное твердое вещество фильтровали и сушили под вакуумом с получением (1-гидрокси-2,2,5,5-тетраметилпирролидин-3-ил)метилнитратагидрохлорида в виде белого вещества в твердой фазе (11,050 г). +Н ЯМР (ДМСО-d6): δ 1,19-1,51 (m, 12Н), 2,02 (m, 1H), 2,48-2,52 (m, 1H), 3,45 (m, 1Н), 4,56-4,66 (m, 2Н), 11,52 (bs, 1H), 11,86 (bs, 1Н). МС (ЭР+): m/z 219,3 (М+1).
Пример 1. Синтез [1-(ацетилокси)-2,2,5,5-тетраметилпирролидин-3-ил]метилнитрата, 1a1 (R-107)
[0093] 1-Гидрокси-2,2,5,5-тетраметилпирролидин-3-ил)метилнитрат гидрохлорид (4,0 г, 0,0157 моль) растворяли в ТГФ (40 мл) и обрабатывали триэтиламином (4,5 мл) и уксусным ангидридом (2 мл) при комнатной температуре в течение 1 часа. Реакционную смесь концентрировали и растворяли в этилацетате и воде (50 мл каждого). Органический слой собирали и сушили над сульфатом натрия. Затем его концентрировали, и осадок очищали на колонке с силикагелем с использованием 0-20% этилацетат-гексана с получением (1-ацетокси-2,2,5,5-тетраметилпирролидин-3-ил)метилнитрата в виде бледно-желтого масла (4,1 г). 1Н ЯМР (CDCl3): δ 1,10 (s, 3H), 1,15 (s, 3H), 1,18 (s, 3H), 1,21 (s, 3H), 1,59-1,65 (m, 1H), 1,88-1,93 (dd, J=7 и 12 Гц, 1H), 2,11 (s, 3H), 2,37-2,41 (m, 1H), 4,36-4,51 (m 2H).
Пример 2. Синтез [(1-пропаноилокси-2,2,5,5-тетраметилпирролидин-3-ил)]метилнитрата, 1a2
[0094] 1-Гидрокси-2,2,5,5-тетраметилпирролидин-3-ил)метилнитрат гидрохлорид (1,0 г, 0,004 моль) растворяли в ТГФ (20 мл) и обрабатывали триэтиламином (3 экв) и пропионовым ангидридом (2 экв.) при комнатной температуре в течение 1 часа. Реакционную смесь концентрировали и растворяли в этилацетате и воде (50 мл каждого). Органический слой собирали и сушили над сульфатом натрия. Затем его концентрировали, и осадок очищали на колонке с силикагелем с использованием 0-20% этилацетат-гексана с получением (1-пропаноилокси-2,2,5,5-тетраметилпирролидин-3-ил)метилнитрата в виде бледно-желтого масла (1,010 г). 1Н ЯМР (CDCl3): δ 1,09 (s, 3H), 1,16 (s, 3H), 1,17 (s, 3H), 1,18-1,21 (m, 6Н), 1,58-1,65 (m, 1Н), 1,85-1,92 (dd, J=7,5 и 12,9 Гц, 1H), 2,33-2,41 (m, 2Н), 2,37-2,41 (m, 1H), 4,34-4,50 (m 2Н).
Пример 3. Синтез [1-(2-метилпропаноилокси-2,2,5,5-тетраметилпирролидин-3-ил)]метилнитрата, 1а3
[0095] 1-Гидрокси-2,2,5,5-тетраметилпирролидин-3-ил)метилнитрат гидрохлорид (1,04 г, 0,004 моль) растворяли в ТГФ (20 мл) и обрабатывали триэтиламином (3 экв.) и ангидридом изобутановой кислоты (1,5 экв.) при комнатной температуре в течение 30 минут. Реакционную смесь концентрировали и растворяли в этилацетате и воде (50 мл каждого). Органический слой собирали и сушили над сульфатом натрия. Затем его концентрировали, и остаток очищали на колонке с силикагелем с использованием 25% этилацетат-гексана с получением [1-(2-метилпропаноилокси-2,2,5,5-тетраметилпирролидин-3-ил)]метинитрата в виде бледно-желтого масла (1,0 г). 1H ЯМР (CDCl3): δ 1,10-1,22 (m, 18H), 1,61 (dd, J=12 Hz, 1H), 1,85-1,92 (dd, J=7,5 и 12 Гц, 1H), 2,33-2,43 (m, 1H), 2,57-2,67 (m, 1H), 4,38-4,51 (m, 2H).
Пример 4. R-107 в физиологических условиях преобразуется в R-100
[0096] В исследованиях in vivo 2,2,5,5-тетраметил-3-(нитрооксиметил)пирролидин-1-илацетат (R-107) инкубировали в плазме мыши или крысы при 37°C и концентрации 4 мМ, и измеряли посредством ВЭЖХ относительные концентрации этого соединения, а также его соответствующего гидроксиламина, (1-гидрокси-2,2,5,5-тетраметилпирролидин-3-ил)метилнитрата (R-105), и 3-нитратометил-2,2,5,5-тетраметилпирролидинилокси (R-100). В таблице 4 показаны относительные концентрации каждого соединения в плазме мыши и крысы по прошествии 0,1, 1,5 и 20 часов, свидетельствующие о том, что R-107 в действительности представляет собой пролекарство его соответствующего гидроксиламинового соединения после гидролиза сложноэфирной связи (O-C(O)R3 в общей формуле I), где гидроксиламиновое соединение затем окисляется in vivo до его соответствующего нитроксильного производного R-100.
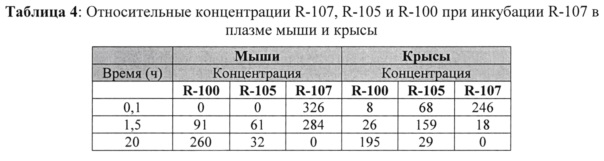
[0097] В следующих двух экспериментах изучали фармакокинетику высвобождения in vivo R-100 из R-107 через R-105, который является восстановленной формой R-100, в соответствии с протоколом, приведенным в настоящем описании.
Методы и стандарты
[0098] Аликвоты (100 мкл) плазмы, полученной из овец или свиней, обработанных R-107, размораживали, и к каждым 100 мкл образца добавляли 200 мкл ледяного этанола для осаждения белка. Затем образцы перемешивали на вортексе, помещали на лед на 10 минут и затем центрифугировали при комнатной температуре в течение 15 минут. Первые 100 мкл надосадочной жидкости из каждого центрифугированного образца отобрали и поместили в маркированную микровиалу для ВЭЖХ, в которую добавляли 300 мкл ПФА (подвижная фаза А для ЖХ), и затем содержимое виалы перемешивали и подвергали анализу посредством жидкостной хроматомасс-спектрометрии (выдерживая при 4°C). Измеряли концентрацию R-107 в этом образце, а также концентрацию R105. Вторые 100 мкл надосадочной жидкости из каждого центрифугированного образца вносили в маркированную микровиалу для ВЭЖХ, в которую добавляли 300 мкл ПФА и 2 мкл восстанавливающего раствора (аскорбиновая кислота, 1,0 мг/мл в воде). Содержимое этих виал перемешивали на вортексе; инкубировали при 50°C в течение 1 часа при осторожном встряхивании и затем охлаждали до 4°C и подвергали анализу посредством жидкостной хроматомасс-спектрометрии. Этот образец анализировали в отношении R105, то есть восстановленной формы R-100, и измеренное таким образом количество представляет собой сумму количеств R-100 и R-105, первоначально присутствующих в плазме. Концентрация R-100 может быть вычислена по разности между R-105 во втором образце и R-105 в первом образце. Однако было выявлено, что концентрации R-105 низкие (составляют приблизительно 10% или меньше от концентраций R-100) и поэтому результаты, представленные ниже для R-100 не корректировали в отношении R-105.
[0099] Наборы стандартов (R-100, R-105 и R-107) были индивидуально подготовлены методом добавок в свиной плазме. Аликвоты этих проб 100 мкл с добавками плазмы, после разморозки, включили в вышеобозначенные протоколы экстракции.
Методы анализа
[00100] Анализ проводили с помощью прибора Agilent для ВЭЖХ с направлением колоночного элюата через перепускной клапан в источник АВ Sciex ‘Qstar Elite’ Hybrid TOF, масс-спектрометр с высоким разрешением. Колонка для ЖХ: Phenomenex Kinetex CI8 2,6u 100A, 2,1×50 мм. Подвижная фаза А для ЖХ: H2O с 0,02% трифторуксусной кислотой (ТФУК), 0,1% муравьиной кислотой (HOF); фаза В: ацетонитрил (ACN) с 0,02% ТФУК, 0,1%) HOF. Скорость потока подвижной фазы =500 мкл/мин. Размер впрыска: 8 мкл, через авто дозатор Agilent 1100 u-WPS.
[00101] В таблицах 5 и 6 приведены количества R-107 и R-100, измеренные в плазме крови овцы (35 кг) в заданные моменты времени после, соответственно, внутривенного или внутримышечного введения чистого R-107 (0,8 мл, 880 мг, 25 мг/кг) в течение 10 минут. Для сравнения в таблице 7 показаны количества R-100, измеренные в заданные моменты времени после внутривенного введения R-100 в гидроксипропил-бета-циклодекстрине (HPCD) (20 мг/мл) в болюсной дозе 20 мг/кг (отношение молекулярных масс R-107:R-100 составляет 269:217, поэтому дозировки 25 мг/кг R-107 и 20 мг/кг R-100 приблизительно эквимолярны).

[00102] В таблице 8 приведены количества R-107 и R-100, измеренные в плазме свиньи (10 кг) в заданные моменты времени после внутривенного введения чистого R-107 (0,8 мл, 880 мг, 88 мг/кг) в течение 6 минут; в таблице 9 приведены количества R-107 и R-100, измеренные в плазме свиньи (10 кг) в заданные моменты времени после внутривенного введения R-107, разбавленного 4 частями ПЭГ400 (0,8 мл, 176 мг, 18 мг/кг) в течение 6 минут; в таблице 10 приведены количества R-107 и R-100, измеренные в плазме свиньи (10 кг) в заданные моменты времени после перорального введения чистого R-107 (0,8 мл, 880 мг, 88 мг/кг; в виде перорально вводимой капсулы).
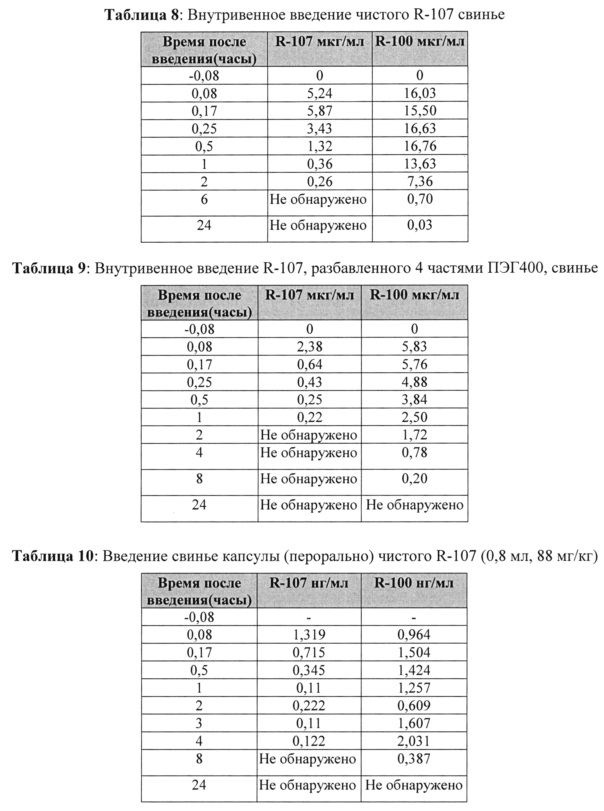
Пример 5. R-107 эффективно в модели сепсиса у мышей
[00103] В данном исследовании мышей линии Balb/c подвергали действию летальной дозы липополисахарида Е. coli (ЛПС; 10 мг/кг внутрибрюшинно) и обрабатывали R-107 (0, 20, 40 или 80 мг/кг/в день, дважды в сутки внутрибрюшинно), давая первую дозу спустя 1 час после введения ЛПС, и сравнивали смертность животных, обработанных только ЛПС (контрольной группы) со смертностью животных, получавших различные дозы R-107.
[00104] В сопутствующем исследовании производили отбор образцов тканей и сыворотки для анализа в момент времени 16 часов, т.е. спустя 15 часов после первого введения и 3 часа после второго введения R-107, и измеряли уровни креатинина, аспартаттрансаминазы (ACT), аланинтрансаминазы (АЛТ), билирубина, амилазы, липазы и щелочной фосфатазы (ЩФ), которые связаны с функционированием почки, поджелудочной железы и печени.
[00105] Аналогичные исследования могут быть проведены в отношении соединений общей формулы I, отличных от R-107.
Пример 6. R-107 эффективно в модели септической пневмонии у овец
[00106] В данном исследовании использована модель овцы, страдающей септической пневмонией, вызванной Pseudomonas aeruginosa (PSA), и вызванной ей дисфункцией легких. Для долговременного исследования овцам породы меринос оперативным путем устанавливают Swan-Ganz®, т.е., катетеры легочной и бедренной артерий, и случайным образом распределяют овец между группами, получающими либо контрольный носитель, либо лечение R-107. У них вызывают травму от ингаляции дыма (48 вдохов хлопкового дыма), и через бронхоскоп вводят овцам в легкое под общим наркозом 2,4×1011 колониеобразующих единиц (КОЕ) PSA. Животным из группы лечения внутривенно вводят R-107 в общей дозе 80 мг/кг по схеме дважды в сутки. Для поддержания гематокрита (hct) на исходном уровне ±3% осуществляют внутривенную титрацию лактатного раствора Рингера. Измерения осуществляют в начальный момент и каждые 3 часа в течение 24-часового периода исследования. Данные выражают в виде среднее ± стандартная ошибка среднего (СОС). Используют следующие методы статистического анализа: двухфакторный ANOVA и апостериорное сравнение Бонферрони. Значение р<0,05 считается статистически значимым.
[00107] Аналогичные исследования могут быть проведены в отношении соединений общей формулы I, отличных от R-107.
Пример 7. Влияние R-107 на вызванные монокроталином (MKT) изменения общего и легочного артериального давления и на MKT-индуцированное реструктурирование сосудов в легких
[00108] В данном исследовании взрослых самцов крыс линии Sprague-Dawley (250-350 г) (3 группы) подвергают однократному подкожному введению монокроталина (MKT; 60 мг/кг), растительного яда, который позволяет получить хорошо изученную экспериментальную модель легочной гипертензии, либо эквивалентного объема солевого раствора (2 мл/кг; носитель, контроль). По истечении 38-дневного периода, в течение которого у крыс развивается тяжелая форма ЛГ, начинают дозирование R-107 в течение 10 дней по следующей схеме: группа 1 (имитирующие животные) не получает MKT и получает контрольный носитель в питьевой воде; группа 2 получает контрольный носитель в питьевой воде; группа 3 получает R-107 (80-160 мг/кг/в день, внутрибрюшинно дважды в сутки). По завершении 10-дневного периода дозирования животных подвергают анестезии, снабжают измерительными приборами и измеряют гемодинамические параметры в состоянии покоя.
[00109] После умерщвления нижнюю долю правого легкого фиксируют в растворе формалина, после парафинизации 5-мм срезы окрашивают гематоксилином и эозином и исследуют под микроскопом Dialux 22 Leitz (Wetziar, Германия). Степень фиброза легких оценивают на срезах, окрашенных красителем Masson Trichrome. С целью морфометрической оценки исследуют все три доли правого легкого. В каждой доле подсчитывают сосуды среднего и малого размера, в которых наблюдаются отек и воспалительные клетки. Результаты выражают в виде процентной доли сосудов, демонстрирующих признаки заболевания, по отношению к общему числу сосудов, посчитанных на срезах. Долю сосудов, в оболочке которых наблюдается утолщение слоя гладкой мускулатуры, также выражают в процентах относительно общего числа подсчитанных сосудов.
[00110] Аналогичные исследования могут быть проведены в отношении соединений общей формулы I, отличных от R-107.
Пример 8. R-107 эффективно в модели легочной гипертензии новорожденных у овец
[00111] В данном исследовании проспективное плацебо-контролируемое рандомизированное исследование с повышением дозы проводят на анестезированных новорожденных ягнятах с расслабленной мускулатурой, находящихся под искусственной вентиляцией легких, у которых путем перевязывания артериального протока in utero была индуцирована легочная гипертензия новорожденных (ПЛГН). Для этой клинически значимой, являющейся «золотым стандартом» модели характерна тяжелая ГЛА, которая слабо реагирует на ингаляцию оксида азота (иNO), что отражает отсутствие реакции на терапию иNO у 30-50% больных клинической ПЛГН. R-107 (0, 0,3, 1,0 и 3,0 мг/кг/ч ВВ; n=6 в группе) сравнивают с иNO (40 ppm; n=6) в течение 6 часового периода наблюдений. О реакции на лечение и появлении «рикошетной» гипертензии легочной артерии после отмены лечения судят, наблюдая за гемодинамическими параметрами. Для построения фармакодинамического профиля активность R-107 соотносят с его концентрацией в плазме.
[00112] Аналогичные исследования могут быть проведены в отношении соединений общей формулы I, отличных от R-107.
Пример 9. R-107 эффективно в модели периферийной гипертензии у карликовых свиней
[00113] Для тестирования эффективности R-107 при периферийной гипертензии (АГ), проводят 3 серии гемодинамических исследований на находящихся в сознании и подвижных карликовых свиньях (n=5), снабженных измерительным оборудованием с телеметрической передачей данных, у которых АГ является вторичной по отношению к одностороннему реноваскулярному стенозу эндоваскулярного происхождения. Карликовых свиней обрабатывают R-107 путем введения пероральных капсул с кишечнорастворимой оболочкой.
[00114] В серии А устанавливают корреляцию между фармакокинетическим профилем и гемо динамическим эффектом однократного введения R-107 (3, 10, 20, 30 мг/кг) с однонедельным периодом вымывания перед каждым следующим уровнем дозы. Наблюдение за животными осуществляют в течение 24 часов, чтобы непрерывно собирать данные о гемодинамике и промежуточных концентрациях R-107 и его метаболитов в плазме (0, 0,25, 0,5, 0,75, 1, 2, 4, 6, 8, 12, 16, 20, и 24 часа). В серии В производят оценку двух дозировок R-107, оказавшихся наиболее эффективными в серии А, для чего проводят исследование повторных доз R-107, вводимых каждые 6 часов (q6h) в течение 3 суток. Между гемодинамическими эффектами R-107 и пиковыми и остаточными концентрациями R-107 и его метаболитов в плазме, измеряемыми каждые 6 часов, проводят корреляцию. В серии С, используя оптимальную дозу, определенную в серии В, оценивают появление тахифилаксии к R-107 в двухнедельном исследовании повторных доз (q6h), с проведением корреляции между гемодинамикой и фармакокинетическими параметрами в плазме аналогично серии В.
[00115] Аналогичные исследования могут быть проведены в отношении соединений общей формулы I, отличных от R-107.
Пример 10. R-107 эффективно в модели ишемически-реперфузионного повреждения почки у крыс.
[00116] В данном исследовании действие R-107 в дозе 80 мг/кг тестируют на хорошо изученной модели почечной ишемии и реперфузии у крыс. Самцов крыс линии Sprague-Dawley помещают на нагревательный мат с термостатическим контролем и поддерживают температуру их тел на уровне 38±1°C с помощью ректального зонда, соединенного с гомеотермическим одеялом. Для поддержания проходимости дыхательных путей и облегчения самостоятельного дыхания проводят трахеотомию. Проводят срединную лапаротомию и канюлируют мочевой пузырь. Локализуют обе почки и аккуратно выделяют почечные ножки, содержащие артерию, вену и нерв, идущие к каждой почке.
[00117] Состоянию крыс (в группах 2 и 3) дают стабилизироваться в течение 30 минут перед тем, как их подвергают 30-минутной двусторонней почечной окклюзии с использованием артериальных зажимов для пережатия почечных ножек. Реперфузия начинается с удалением артериальных зажимов (контрольные животные). Окклюзию подтверждают визуально по изменению цвета почки в сторону более бледного оттенка, а реперфузию - по покраснению. Других крыс (группа 1), над которыми провели те же хирургические процедуры, что и над контрольными животными, но не проводили двустороннее пережимание почек, подвергают имитационной операции (имитационно оперированные) и в течение всего эксперимента держат под наркозом. По окончании всех экспериментов животных убивают посредством передозировки натрия тиопентона.
[00118] По завершении хирургических процедур животных случайным образом помещают в группу 1: имитационную (без ишемии); группу 2: (ишемия-реперфузия, И/Р); и группу 3: (ишемия-реперфузия, И/Р и терапия R-107). В течение следующих периодов у крыс собирают мочу: (i) между 2 часами до ишемизации и 30 минутами до ишемизации; (ii) от наступления реперфузии до 1,5 часов после наступления реперфузии; (iii) от 1,5 часов после наступления реперфузии до 3,0 часов после наступления реперфузии; (iv) от 3 часов после наступления реперфузии до 4,5 часов после наступления реперфузии; и (v) от 4,5 часов после наступления реперфузии до 6,0 часов после наступления реперфузии. Образцы артериальной крови забирают спустя 0, 1,5 часа, 3,0 часа, 4,5 часа и 6,0 часов после наступления реперфузии. R-107 (80 мг/кг; группа 3) вводят путем 10-минутной внутривенной инфузии начиная с 20 минут после наступления ишемии.
[00119] По окончанию периода реперфузии образцы крови (1 мл) отбирают из сонной артерии в пробирки S1/3, содержащие гель для отделения сыворотки и центрифугируют образцы (6000 об/мин в течение 3 минут), чтобы отделить плазму. Биохимические параметры всех образцов плазмы анализируют не позднее 24 часов после их отбора. В течение периода реперфузии собирают образцы мочи и регистрируют объем образовавшейся мочи. Измеряют концентрацию Na+ в моче и вместе с данными о концентрации Na+ в плазме используют для расчета по стандартной формуле фракционной экскреции натрия (ФЭNa), которую используют в качестве индикатора функционирования почечных канальцев. В качестве индикаторов нарушения функции клубочков измеряют концентрации креатинина в плазме и моче. Клиренс креатинина рассчитывают по формуле UV/P, где U - концентрация креатинина в моче, V - объем мочи, отделяемой в минуту и Р - креатинин в сыворотке. Концентрацию липокалина, ассоциированного с желатиназой нейтрофилов (NGAL), в плазме оценивают так, как указано в коммерческом наборе. Концентрацию NGAL в моче оценивают так, как указано в коммерческом наборе.
[00120] Активность миелопероксидазы (МПО) в почках используют в качестве индикатора инфильтрации полиморфноядерных клеток (ПМЯ) по ранее описанному методу. Вкратце: по окончании экспериментов почечную ткань взвешивают и гомогенизируют в растворе, содержащем 0,5% (масс./об.) гексадецилтриметиламмония бромида, растворенного в буфере, содержащем 10 мМ фосфата калия (рН 7,4), и центрифугируют в течение 30 минут при 20000 g и 4°C. Затем отбирают аликвоту супернатанта и добавляют к реакционной смеси, содержащей 1,6 мМ тетраметилбензидина и 0,1 мМ пероксида водорода (Н2О2). Измеряют скорость изменения оптического поглощения при длине волны 650 нм на спектрофотометре. Активность МПО определяют как количество фермента, необходимое для разрушения 1 миллимоля Н2О2 при 37°C и выражают в Ед на грамм влажной ткани.
[00121] В качестве индикатора перекисного окисления липидов определяют уровень малонового диальдегида (МДА) в почках, следуя протоколу, описанному ранее. Вкратце: почечную ткань взвешивают и гомогенизируют в растворе, содержащем 1,15% (масс./об.) KCl. Затем отбирают аликвоту гомогената объемом 100 мл и добавляют ее к реакционной смеси, содержащей 200 мл 8,1% (масс/об.) лаурилсульфата, 1,5 мл 20% (об./об.) уксусной кислоты (рН 3,5), 1,5 мл 0,8% (масс./об.) тиобарбитуровой кислоты и 700 мл дистиллированной воды. Затем образцы греют в течение 1 часа при 95°C и центрифугируют при 3000×g в течение 10 минут. Измеряют оптическое поглощение супернатанта при 650 нм на спектрофотометре. Уровни МДА выражают в мкМ на 100 мг влажной ткани.
[00122] После умерщвления делают срез почек толщиной 5 мкм, помещают в формалин и подвергают процедуре воскования. Нарезают пятимиллиметровые кусочки и окрашивают гематоксилином и эозином. Делают полуколичественную гистологическую оценку некроза канальцев с использованием модификации метода, взятого из источника McWhinnie et al., Tissue Antigens, 1987, 29(4), 214-223. С помощью 20-кратного объектива исследуют случайные кортикальные поля. Для определения числа линейных пересечений, включающих профили канальцев, используют градуировочную решетку (25 квадратов). Для каждой почки исследуют сто пересечений и присваивают каждому профилю канальца, включающему пересечение, оценку от 0 до 3: 0= нормальная гистология; 1= набухание канальцевых клеток, утрата щеточной каймы, конденсация ядер, такая, что до одной трети профиля канальца теряет ядра; 2= то же, что и для рейтинга 1, но утрата ядер наблюдается в более, чем одной трети и менее, чем в двух третях профиля канальца; 3= более, чем в двух третях профиля канальца наблюдается потеря ядер. Суммарную оценку каждой почки рассчитывают путем сложения всех 100 оценок.
[00123] Аналогичные исследования могут быть проведены в отношении соединений общей формулы I, отличных от R-107.
Пример 11. R-107 эффективно в модели ишемически-реперфузионного повреждения сетчатки у мышей
[00124] В данном исследовании проверяют эффективность R-107 в модели подострого ишемически-реперфузионного повреждения сетчатки у мышей с использованием самцов мыши линии C57BL/6 (n=10 в группе). Вкратце: переднюю камеру правого глаза канюлируют иглой 30 размера, соединенной с линией для инфузии стерильного солевого раствора. Путем поднятия резервуара с солевым раствором внутриглазное давление (ВГД) повышают до 110 мм рт.ст. Левый глаз подвергают имитационной операции, при которой иглу вставляют в переднюю камеру, не повышая ВГД. Введение R-107 (30 мг/кг/сутки внутрибрюшинно дважды в сутки) начинают непосредственно перед реперфузией. Для сравнения с лекарственной терапией используют 2 контрольных носителя (нормальный солевой раствор и HPCD). Далее обработку повторяют дважды в сутки до момента умерщвления. Результат данных фармакологических исследований оценивают количественно, используя терминальное дезоксиуридиновое мечение концов (TUNEL) для измерения гибели клеток сетчатки (спустя 3 суток), конфокальную визуализацию количественной характеристики выживания нейронов в слое ганглиозных клеток (спустя 7 суток) и электроретинограммы для измерения функционирования нейронов сетчатки (спустя 21 сутки).
[00125] Аналогичные исследования могут быть проведены в отношении соединений общей формулы I, отличных от R-107.
Пример 12. R-107 эффективно в модели острой ишемически-реперфузионного повреждения сетчатки у свиней
[00126] В данном исследовании свиную модель острой ишемически-реперфузионного повреждения сетчатки (n=6 в группе) создают путем уравновешивания с помощью приподнятого резервуара с солевым раствором, создающего статическое ВГД 90 мм рт.ст. в течение 90 мин. Задача №1: Микроваскулярная чувствительность: Изучение ответа на парэнтеральную дозу R-107 (0, 10, 30, 80 мг/кг/сутки ВВ дважды в сутки) начинают за 10 минут до реперфузии. Через 1 час после реперфузии капилляры сетчатки извлекают и канюлируют для анализа васкулярной чувствительности к эндотелий-зависимым и независимым вазодилатантам ex vivo. Задача №2: Функция и морфология сетчатки: R-107 вводят за 10 минут до реперфузии 10 (в дозе, определенной на этапе задачи №1) и судят о его эффективности по электроретинограмме (на 1, 2, 7 сутки после реперфузии), гистологии сетчатки, ее ультраструктуре и концентрации лекарства (на 7 сутки).
[00127] Аналогичные исследования могут быть проведены в отношении соединений общей формулы I, отличных от R-107.
Пример 13. R-107 эффективно в модели ишемически-реперфузионного повреждения миокарда у крыс
[00128] С целью проверки эффективности R-107 при ишемически-реперфузионной травме миокарда, старым самцам крыс линии Sprague-Dawley вводят дозы R-107 (0, 10, 30, 80 мг/кг ВВ) за 10 минут до окончания 30-минутного периода ишемии, вызванного окклюзией передней межжелудочковой ветви (ПМВ) коронарной артерии. Наблюдение за функцией сердца осуществляют с помощью катетера Millar для определения частоты пульса (ЧП), систолического и диастолического кровяного давления (КД), систолического давления в левом желудочке (ЛЖ), конечного диастолического давления в левом желудочке (КДД ЛЖ), ±dP/dt, петли давление-объем (ДО) и тау (τ). Спустя 3 часа после ишемии кровь и миокард анализируют на наличие морфологических, гистохимических и биоаналитических признаков повреждения. Количественно измеряют площадь некроза в % от площади, подверженной риску (ППР) и величину зоны невосстановленного кровотока.
[00129] Аналогичные исследования могут быть проведены в отношении соединений общей формулы I, отличных от R-107.
Пример 14. R-107 эффективно в модели ишемически-реперфузионного повреждения конечности у карликовых свиней
[00130] В данном исследовании проверяют эффективность R-107 при ишемически-реперфузионной травме конечности (ИТК). При этой обширной модели острой ИТК у животных (n=6 карликовых свиней в группе), вызываемой путем окклюзии бедренной артерии с помощью эндоваскулярного баллона в течение 6 часов, парентеральное введение R-107 (0, 10, 30, 80 мг/кг/сутки трижды в сутки) начинают за 10 минут до реперфузии путем прямой инфузии в артерию, за которой в дальнейшем следует внутривенная инфузия. На 7, 14 и 21 сутки после реперфузии проводят корреляцию между перфузией конечности (измеренной путем допплерографии кровотока) и скоростью проводимости нерва (НТС, измеряемой электромиографически, ЭМГ), силой мышц (определяемой по давлению стопы на поверхность для ходьбы) и одновременно измеряемыми концентрациями R-107 в плазме.
[00131] Аналогичные исследования могут быть проведены в отношении соединений общей формулы I, отличных от R-107.
Пример 15. R-107 эффективно в модели контраст-индуцированной нефропатии у крыс
[00132] С целью проверки эффективности R-107 при контраст-индуцированной нефропатии (КИН), проводят одинарное слепое исследование КИН на крысах линии Sprague-Dawley (n=10 в группе), подвергнутых дегидратации, ингибированию простагландинсинтетазы и внутривенному введению контрастного препарата (КП). Группу животных с имитационной травмой сравнивают с лечением обработанных КП здоровых крыс с помощью R-107 (10, 20, 40 мг/кг/сутки в 5% декстрозе, дважды в сутки ВВ), N-ацетилцистеина (НАЦ, 100 мг/кг/сутки в 5% декстрозе, дважды в сутки), или контрольного носителя (гидроксипропилциклодекстрин, HPCD), которое начинают за 10 мин до введения КП и продолжают в течение 48 часов. Через 48 часов у крыс оценивают функцию почек (отношение азота мочевины крови к креатинину, АМК : креатинин) и параметры, отражающие повреждение почек, включая высвобождение белков в кровь (NGAL; молекула травмы почек-1, KIM-1), экспрессию провоспалительных факторов транскрипции (деградацию цитоплазматического IkBa, ядерную транслокацию р65), гистологические повреждения (окрашивание гематоксилином и эозином), разбухание митохондрий (электронной микроскопией), повреждения ядер и репарацию ДНК (активация PARP и нитрозативный стресс, определяемый по иммунореактивности тканей к поли(АДФ-рибозе) и 3-нитротирозину (3-НТ).
[00133] С тем, чтобы лучше смоделировать группу больных с наибольшим риском КИН, производят дальнейшую оценку оптимальной дозы, применяя тот же подход и дизайн эксперимента, что и ранее, но на крысах Sprague-Dawley с диабетом, вызванным инъекцией стрептозотоцина (СТЗ; 60 мг/кг ВВ) 2 неделями ранее. Контрольная группа крыс с СТЗ-индуцированным диабетом получает контрольный носитель. Если эффективность R-107 в диабетической группе оказывается меньше, чем на здоровых крысах, производят оценку дополнительных групп при более высоких дозах R-107, с тем, чтобы получить оптимальный эффект в данной клинически значимой модели диабета и КИН. Наконец, мы исследовали, возможно ли достичь дальнейшего улучшения в ситуации диабета, комбинируя введение R-107 с агрессивным восполнением ОЦК, на основании существующего в настоящее время единого врачебного мнения о том, что усиленная гидратация облегчает КИН. Диабетические крысы в группе усиленной гидратации одновременно с введением R-107 получали болюсные ВВ дозы 10 мл/кг нормального солевого раствора (ФР). Контрольная группа получала только ВВ ФР.
[00134] Аналогичные исследования могут быть проведены в отношении соединений общей формулы I, отличных от R-107.
Пример 16. R-107 эффективно в мышиной модели воздействия С12
[00135] В данном исследовании тестируют эффект R-107 при лечении вызванного хлором поражения легких. Мышей линии Balb/c обрабатывают в цилиндрической стеклянной камере, которую непрерывно в течение 60 минут продувают со скоростью 2 литра в минуту увлажненным газом, подаваемым из калиброванного цилиндра, содержащего воздух и 400 ppm Cl2. По окончании 30-минутной обработки камеру открывают, мышей извлекают и немедленно помещают в клетки с комнатным воздухом. Спустя два и шесть часов после завершения обработки Cl2 мышам внутрибрюшинно (ВБ) вводят различные дозы R-107. Через 24 часа после воздействия содержащего Cl2 воздуха, делают срединный разрез от шеи до лобка, чтобы получить доступ к грудной клетке и брюшной полости. Непосредственно перед умерщвлением отбирают образцы крови из нижней полой вены, сердечно-легочный блок быстро удаляют и вымывают кровь из легких через легочную артерию с помощью 20 мл нормального солевого раствора. Легкие отделяют от тканей средостения и используют для биохимического анализа и гистологического исследования (окрашивание гематоксилин и эозином). Для выставления оценок используют следующие морфологические критерии: 0 баллов - нормальное легкое; 1 балл - минимальный отек или инфильтрация стенок альвеол или бронхиол; 3 балла - умеренный отек и инфильтрация воспалительных клеток без явных повреждений архитектуры легкого; 4 балла - значительная инфильтрация воспалительных клеток с явным повреждением архитектуры легкого. Аналогичные исследования могут быть проведены в отношении соединений общей формулы I, отличных от R-107.
[00136] В одном из исследований эффект R-107 при лечении ИПЛХ исследовали в соответствии с вышеописанным протоколом. Самцов мышей линии Balc/с разделяли на 5 следующих групп: (i) имитация (n=5); (ii) носитель, HPCD (n=5); (iii) носитель, ПЭГ-400 (n=5); (iv) R-100, приготовленное в HPCD, 80 мг/кг/дозу, всего 160 мг/кг/день, ВБ (n=10); и (v) R-107, приготовленное в ПЭГ-400, 100 мг/кг/дозу, всего 200 мг/кг/день, ВБ (n=10). На фиг. 1A-1F представлены приведенные в качестве иллюстрации микрофотографии, на которых изображены окрашенные гематоксилином и эозином срезы легких, взятых у мышей, подвергнутых имитационной операции (1А, 1B), животных, обработанных Cl2 и HPCD (1С), животных, обработанных Cl2 и солевым раствором (1D), животных, обработанных Cl2 и R-100 (1Е) и животных, обработанных Cl2 и R-107 (1F). Фиг. 2 показывает, что R-107, так же, как и соответствующее ему 1-пирролидинилоксисоединение, R-100, при введении спустя 2 и 6 часов после 60-минутного воздействия воздуха, содержащего Cl2, значительно облегчали ИПЛХ у мышей через 24 часа после воздействия, на что указывают улучшенные гистологические оценки.
[00137] В другом исследовании, проведенном в соответствии с описанным выше протоколом, самцов мыши линии Balc/с разделили на следующие 5 групп: (i) имитация (n=2); (ii) носитель, оливковое масло (n=4); (iii) R-107, приготовленное в оливковом масле, 10 мг/кг/дозу, всего 20 мг/кг/день, IP (n=4); (iv) R-107, приготовленное в масле, 30 мг/кг/дозу, всего 60 мг/кг/день, IP (n=4); и (v) R-107, приготовленное в масле, 80 мг/кг/дозу, всего 160 мг/кг/день, ВБ (n=4). Лекарство вводили спустя 2 и 6 часов после 60-минутного воздействия воздуха, содержащего Cl2 (400 ppm), через 24 часа мышей умерщвляли, и проводили гистологическое исследование легких. В таблице 11 показано, что R-107 дозозависимым образом облегчало ИПЛХ у мышей через 24 часа после воздействия, на что указывают улучшенные гистологические оценки.
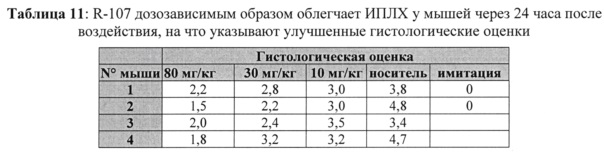
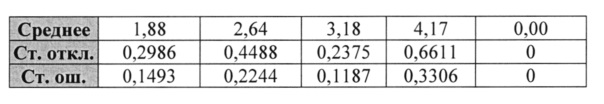
Пример 17. R-107 эффективно в модели эректильной дисфункции у крыс
[00138] Для проверки эффективности R-107 при эректильной дисфункции (ЭД) проводят проспективное плацебо-контролируемое рандомизированное одинарное слепое исследование ЭД на анестезированных крысах линии Sprague-Dawley (n=10 в группе). Группу имитационного повреждения сравнивают с обработкой R-107 (80 мг/кг/день дважды в сутки ВВ), которую начинают за 10 минут до сдавливающего повреждения кавернозных нервов пениса и продолжают в течение 1 недели. Через 1 неделю крыс подвергают оценке нейрогенно-опосредованного эректильного ответа in vivo. По завершении физиологической оценки крыс умерщвляют и забирают ткани для биохимического и морфологического анализов и анализа воспаления. Сдавливающее повреждение создают следующим образом: после внутрибрюшинного введения пентобарбитала натрия (50 мг/кг) в качестве наркоза, брюшко бреют, обрабатывают раствором йода и делают нижнесрединную лапаротомию. Оголяют предстательную железу и идентифицируют и изолируют идущие заднелатерально кавернозные нервы. Над группой имитации дальнейших хирургических манипуляций не производят. В остальных группах создают сдавливающее повреждение в течение 3 минут, используя кровоостанавливающий зажим. Затем брюшные полости всех крыс зашивают в 2 слоя. Спустя 1 неделю после хирургического вмешательства всех крыс подвергают исследованию нейрогенно-опосредованного эректильного ответа in vivo. Крыс анестезируют пентобарбиталом (50 мг/кг ВБ) и помещают на терморегулируемый хирургический стол. Трахею канюлируют с помощью полиэтиленовой трубки РЕ-240 для поддержания дыхательного пути раскрытым и животные дышат комнатным воздухом, обогащенным смесью 95% O2/5% CO2. Сонную артерию канюлируют трубкой РЕ-50, чтобы непрерывно измерять системное кровяное давление (САД) с помощью преобразователя Statham, соединенного с системой сбора данных и подключенного к компьютеру. Иглу размера 25, заполненную гепарином (250 Ед/мл) и подсоединенную к трубке РЕ-50, вставляют в правую ножку и подключают к преобразователю давления, чтобы обеспечить непрерывное измерение интракавернозного давления (ИКД). В области, заднелатеральной относительно простаты, на стороне 1 идентифицируют кавернозный нерв (КН) и помещают вокруг него электрический стимулятор с двухполюсным зацепом из нержавеющей стали. КН подвергают стимуляции с помощью стимулятора с квадратным импульсом (Grass Instruments, Куинси, Массачусетс). Стимуляцию КН (СКН) с частотой 15 Гц и шириной импульса 30 с делают каждой крысе. В данном протоколе для достижения значительного и устойчивого эректильного ответа использована СКН при 2,5, 5 и 7,5 В. Продолжительность стимуляции составляет 1 минуту с периодом отдыха между последовательными СКН, составляющим 3-5 минут. Суммарный эректильный ответ, или суммарное ИКД определяют по площади под графиком в мм рт.ст. в секунду от начала СКН до возвращения ИКД к исходному значению, или давлению до стимуляции. Чтобы контролировать колебания САД, определяют соотношение ИКД/САД в момент максимального эректильного ответа.
[00139] Аналогичные исследования могут быть проведены в отношении соединений общей формулы I, отличных от R-107.


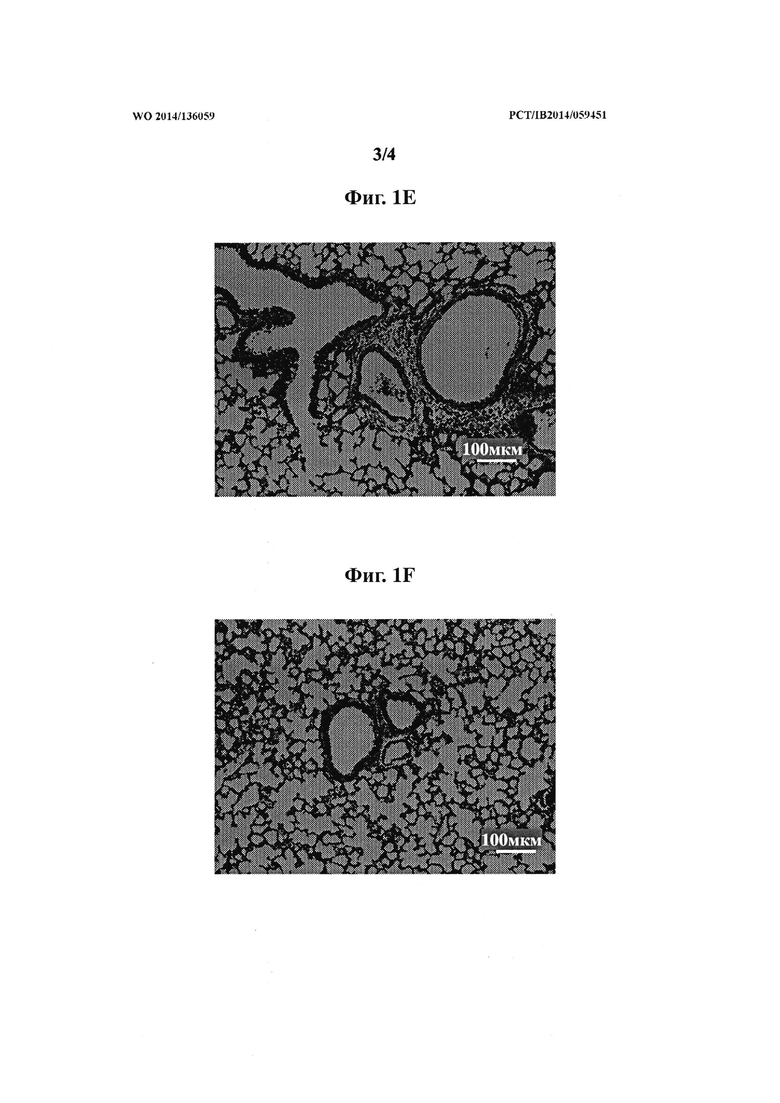
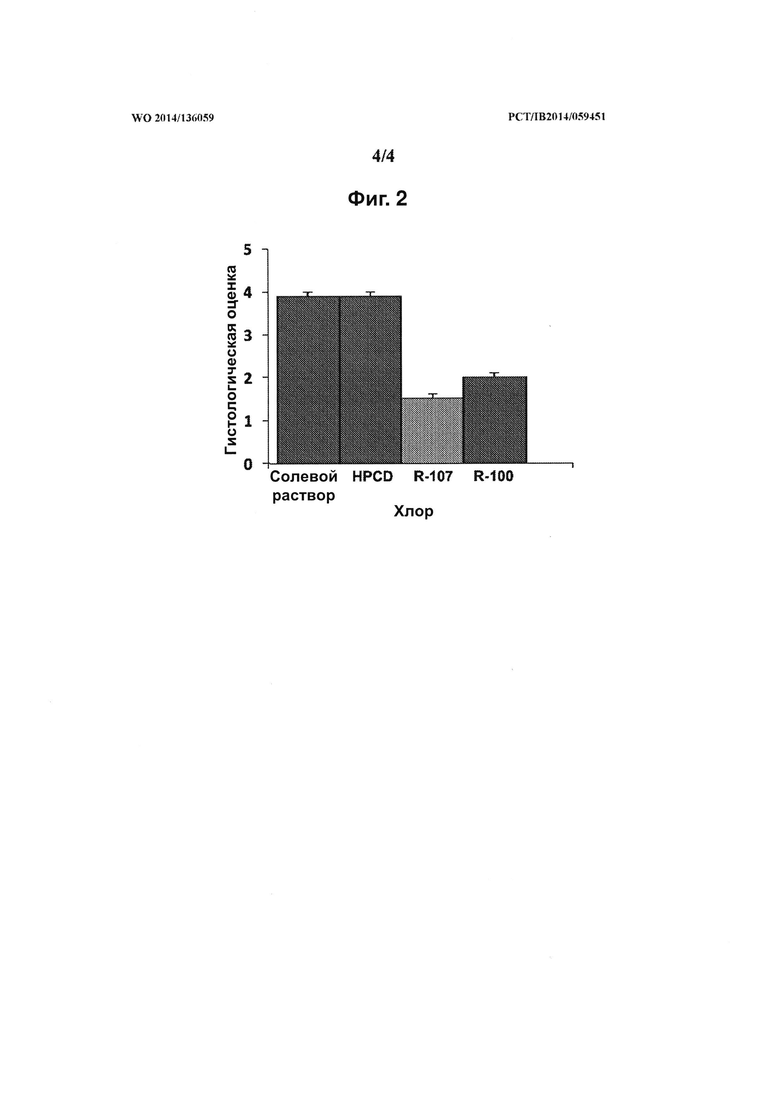
Изобретение относится к пролекарствам соединений, содержащим донор оксида азота и катализатор разложения активных форм кислорода (АФК), в частности 1-пирролидинилокси-, 1-пиперидинилокси- и 1-азепанилоксипроизводные, и содержащим их фармацевтические композиции. Указанные соединения и фармацевтические композиции являются подходящими для предотвращения, лечения или контролирования заболеваний, расстройств или состояний, связанных с окислительным стрессом или эндотелиальной дисфункцией. 4 н. и 13 з.п. ф-лы, 7 ил., 11 табл., 17 пр.
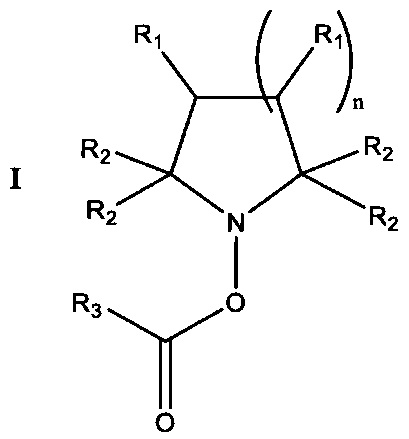
1. Соединение общей формулы I:
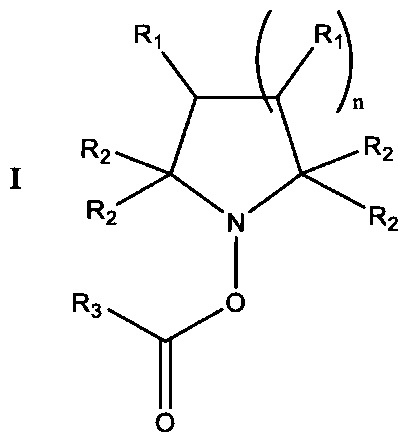
или его энантиомер, диастереомер, рацемат или фармацевтически приемлемая соль,
где
каждый R1 независимо выбран из Н, -COOR4, CON(R4)2 или группы-донора оксида азота, имеющей формулу -Х1-Х2-Х3, где X1 отсутствует или представляет собой -О; X2 отсутствует или представляет собой (С1-C20)алкилен, необязательно замещенный одной или более группами -ONO2; и X3 представляет собой -NO или -ONO2, при условии, что по меньшей мере одна группа R1 представляет собой группу-донор оксида азота;
каждый R2 независимо представляет собой (C1-С8)алкил;
R3 представляет собой (С1-С8)алкил или -N(R5)2;
каждый R4 представляет собой Н;
каждый R5 представляет собой Н или (C1-C8)алкил; и
n представляет собой целое число, равное 1, 2 или 3.
2. Соединение по п. 1, в котором R2 идентичны.
3. Соединение по п. 1 или 2, в котором (i) n составляет 1; и один или два атома углерода в положениях 3 или 4 пирролидинового кольца связаны с группой-донором оксида азота, имеющей формулу -Х1-Х2-Х3; (ii) n составляет 2; и один или более атомов углерода в положениях 3-5 пиперидинового кольца связаны с группой-донором оксида азота, имеющей формулу -Х1-Х2-Х3; или (iii) n составляет 3; и один или более атомов углерода в положениях 3-6 азепанового кольца связаны с группой-донором оксида азота, имеющей формулу -Х1-Х2-Х3.
4. Соединение по п. 3, отличающееся тем, что указанное соединение содержит две, три или четыре идентичных или разных групп-доноров оксида азота, имеющих формулу -Х1-Х2-Х3.
5. Соединение по п. 3, отличающееся тем, что каждая из указанных групп-доноров оксида азота, имеющих формулу -Х1-Х2-Х3, независимо представляет собой -ONO2, -(С1-C6)алкилен-ONO2 или -O-(С1-С6)алкилен-ONO2, где указанный алкилен необязательно замещен одной или более группами -ONO2.
6. Соединение по п. 5, в котором n составляет 1; каждый R2 представляет собой метил; R3 представляет собой метил, этил или изопропил; и
(i) R1, связанный с атомом углерода в положении 3 пирролидинового кольца, представляет собой -СН2-ONO2; и R1, связанный с атомом углерода в положении 4 пирролидинового кольца, представляет собой Н;
(ii) R1, связанный с атомом углерода в положении 3 пирролидинового кольца, представляет собой -ONO2; и R1, связанный с атомом углерода в положении 4 пирролидинового кольца, представляет собой Н;
(iii) каждый из R1, связанных с атомами углерода в положениях 3 и 4 пирролидинового кольца, представляет собой CH2-ONO2; или
(iv) каждый из R1, связанных с атомами углерода в положениях 3 и 4 пирролидинового кольца, представляет собой ONO2.
7. Соединение по п. 5, в котором n составляет 2; каждый R2 представляет собой метил; R3 представляет собой метил, этил или изопропил; и
(i) R1, связанный с атомом углерода в положении 3 пиперидинового кольца, представляет собой -СН2-ONO2; и каждый из R1, связанных с атомами углерода в положениях 4 и 5 пиперидинового кольца, представляет собой Н;
(ii) R1, связанный с атомом углерода в положении 3 пиперидинового кольца, представляет собой -ONO2; и каждый из R1, связанных с атомами углерода в положениях 4 и 5 пиперидинового кольца, представляет собой Н;
(iii) R1, связанный с атомом углерода в положении 4 пиперидинового кольца, представляет собой -CH2-ONO2; и каждый из R1, связанных с атомами углерода в положениях 3 и 5 пиперидинового кольца, представляет собой Н;
(iv) R1, связанный с атомом углерода в положении 4 пиперидинового кольца, представляет собой -ONO2; и каждый из R1, связанных с атомами углерода в положениях 3 и 5 пиперидинового кольца, представляет собой Н;
(v) каждый из R1, связанных с атомами углерода в положениях 3 и 4 пиперидинового кольца, представляет собой -CH2-ONO2; и R1, связанный с атомом углерода в положении 5 пиперидинового кольца, представляет собой Н;
(vi) каждый из R1, связанных с атомами углерода в положениях 3 и 4 пиперидинового кольца, представляет собой -ONO2; и R1, связанный с атомом углерода в положении 5 пиперидинового кольца, представляет собой Н;
(vii) каждый из R1, связанных с атомами углерода в положениях 3 и 5 пиперидинового кольца, представляет собой -CH2-ONO2; и R1, связанный с атомом углерода в положении 4 пиперидинового кольца, представляет собой Н;
(viii) каждый из R1, связанных с атомами углерода в положениях 3 и 5 пиперидинового кольца, представляет собой -ONO2; и R1, связанный с атомом углерода в положении 4 пиперидинового кольца, представляет собой Н;
(ix) каждый из R1, связанных с атомами углерода в положениях 3, 4 и 5 пиперидинового кольца, представляет собой -СН2-ONO2; или
(х) каждый из R1, связанных с атомами углерода в положениях 3, 4 и 5 пиперидинового кольца, представляет собой -ONO2.
8. Соединение по п. 5, в котором n составляет 3; каждый R2 представляет собой метил; R3 представляет собой метил, этил или изопропил; и
(i) R1, связанный с атомом углерода в положении 3 азепанового кольца, представляет собой -CH2-ONO2; и каждый из R1, связанных с атомами углерода в положениях 4, 5 и 6 азепанового кольца, представляет собой Н;
(ii) R1, связанный с атомом углерода в положении 3 азепанового кольца, представляет собой -ONO2; и каждый из R1, связанных с атомами углерода в положениях 4, 5 и 6 азепанового кольца, представляет собой Н;
(iii) R1, связанный с атомом углерода в положении 4 азепанового кольца, представляет собой -СН2-ONO2; и каждый из R1, связанных с атомами углерода в положениях 3, 5 и 6 азепанового кольца, представляет собой Н;
(iv) R1, связанный с атомом углерода в положении 4 азепанового кольца, представляет собой -ONO2; и каждый из R1, связанных с атомами углерода в положениях 3, 5 и 6 азепанового кольца, представляет собой Н;
(v) каждый из R1, связанных с атомами углерода в положениях 3 и 4 азепанового кольца, представляет собой -CH2-ONO2; и каждый из R1, связанных с атомами углерода в положениях 5 и 6 азепанового кольца, представляет собой Н;
(vi) каждый из R1, связанных с атомами углерода в положениях 3 и 4 азепанового кольца, представляет собой -ONO2; и каждый из R1, связанных с атомами углерода в положениях 5 и 6 азепанового кольца, представляет собой Н;
(vii) каждый из R1, связанных с атомами углерода в положениях 3 и 5 азепанового кольца, представляет собой -CH2-ONO2; и каждый из R1, связанных с атомами углерода в положениях 4 и 6 азепанового кольца, представляет собой Н;
(viii) каждый из R1, связанных с атомами углерода в положениях 3 и 5 азепанового кольца, представляет собой -ONO2; и каждый из R1, связанных с атомами углерода в положениях 4 и 6 азепанового кольца, представляет собой Н;
(ix) каждый из R1, связанных с атомами углерода в положениях 3 и 6 азепанового кольца, представляет собой -СН2-ONO2; и каждый из R1, связанных с атомами углерода в положениях 4 и 5 азепанового кольца, представляет собой Н;
(х) каждый из R1, связанных с атомами углерода в положениях 3 и 6 азепанового кольца, представляет собой -ONO2; и каждый из R1, связанных с атомами углерода в положениях 4 и 5 азепанового кольца, представляет собой Н;
(xi) каждый из R1, связанных с атомами углерода в положениях 3, 4 и 5 азепанового кольца, представляет собой -CH2-ONO2; и R1, связанный с атомом углерода в положении 6 азепанового кольца, представляет собой Н;
(xii) каждый из R1, связанных с атомами углерода в положениях 3, 4 и 5 азепанового кольца, представляет собой -ONO2; и R1, связанный с атомом углерода в положении 6 азепанового кольца, представляет собой Н;
(xiii) каждый из R1, связанных с атомами углерода в положениях 3, 4 и 6 азепанового кольца, представляет собой -CH2-ONO2; и R1, связанный с атомом углерода в положении 5 азепанового кольца, представляет собой Н;
(xiv) каждый из R1, связанных с атомами углерода в положениях 3, 4 и 6 азепанового кольца, представляет собой -ONO2; и R1, связанный с атомом углерода в положении 5 азепанового кольца, представляет собой Н;
(xv) каждый из R1, связанных с атомами углерода в положениях 3, 4, 5 и 6 азепанового кольца, представляет собой -CH2-ONO2; или
(xvi) каждый из R1, связанных с атомами углерода в положениях 3, 4, 5 и 6 азепанового кольца, представляет собой -ONO2.
9. Соединение по п. 5, в котором n составляет 1; каждый R2 представляет собой метил; R3 представляет собой метил, этил или изопропил; и
(i) R1, связанный с атомом углерода в положении 3 пирролидинового кольца, представляет собой -CH2-ONO2; и R1, связанный с атомом углерода в положении 4 пирролидинового кольца, представляет собой -CONH2; или
(ii) R1, связанный с атомом углерода в положении 3 пирролидинового кольца, представляет собой -ONO2; и R1, связанный с атомом углерода в положении 4 пирролидинового кольца, представляет собой -CONH2.
10. Соединение по п. 5, в котором n составляет 2; каждый R2 представляет собой метил; R3 представляет собой метил, этил или изопропил; и
(i) R1, связанный с атомом углерода в положении 3 пиперидинового кольца, представляет собой -СН2-ONO2; R1, связанный с атомом углерода в положении 4 пиперидинового кольца, представляет собой -СООН; и R1, связанный с атомами углерода в положении 5 пиперидинового кольца, представляет собой Н; или
(ii) R1, связанный с атомом углерода в положении 3 пиперидинового кольца, представляет собой -ONO2; R1, связанный с атомом углерода в положении 4 пиперидинового кольца, представляет собой -СООН; и R1, связанный с атомами углерода в положении 5 пиперидинового кольца, представляет собой Н.
11. Соединение по п. 5, в котором n составляет 2; каждый R2 представляет собой метил; R3 представляет собой метил, этил или изопропил; R1, связанный с атомом углерода в положении 4 пиперидинового кольца, представляет собой -O-CH2-СН(ONO2)СН2-ONO2; и каждый из R1, связанных с атомами углерода в положениях 3 или 5 пиперидинового кольца, представляет собой Н.
12. Соединение по п. 6, выбранное из 2,2,5,5-тетраметил-3-(нитрооксиметил)пирролидин-1-илацетата, 2,2,5,5-тетраметил-3-(нитрооксиметил)пирролидин-1-илпропионата или 2,2,5,5-тетраметил-3-(нитрооксиметил)пирролидин-1-илизобутирата, или их энантиомера, диастереомера, рацемата или фармацевтически приемлемой соли.
13. Фармацевтическая композиция для предотвращения, лечения или контролирования заболевания, расстройства или состояния, связанного с окислительным стрессом или эндотелиальной дисфункцией, содержащая соединение по любому из пп. 1-12 или его энантиомер, диастереомер, рацемат или фармацевтически приемлемую соль и фармацевтически приемлемый носитель, где указанное заболевание, расстройство или состояние, связанное с окислительным стрессом или эндотелиальной дисфункцией, представляет собой ишемически-реперфузионное повреждение сетчатки; острую переднюю ишемическую оптическую невропатию; закупорку центральной ретинальной артерии; гемолитические заболевания, включая сфероцитоз, дефицит глюкозо-6-фосфатдегидрогеназы (G6PD), серповидно-клеточную болезнь, талассемию и ночную пароксизмальную гемоглобинурию; сахарный диабет, включая диабетические раны и диабетическую ретинопатию, нефропатию и сердечно-сосудистое заболевание; сердечно-сосудистые заболевания, такие как ишемическая болезнь сердца, стенокардия, ишемически-реперфузионное повреждение миокарда и инфаркт, острое и хроническое ишемически-реперфузионное повреждение конечности, застойная сердечная недостаточность (ЗСН), атеросклероз, аритмии сердца при гипертензии периферических артерий, идиопатическая легочная гипертензия, легочная гипертензия, связанная с идиопатическим легочным фиброзом, легочная гипертензия, связанная с гемолитическим заболеванием, первичная легочная гипертензия новорожденных, легочная гипертензия на фоне врожденной диафрагмальной грыжи и аспирации мекония; легочная гипертензия на фоне врожденного заболевания сердца; легочную гипертензию на фоне недостаточности митрального клапана, дефекта межпредсердной или межжелудочковой перегородки; контраст-индуцированную нефропатию; астму; травму; гиповолемический, нейрогенный или септический шок; идиопатическую эректильную дисфункцию; эректильную дисфункцию на фоне нервосберегающей радикальной простатэктомии; ингаляционное поражение легких, вызванное токсическим агентом; ингаляционное поражение легких хлором; нейротоксичность; нейродегенеративные и неврологические расстройства, включая болезни Альцгеймера и Паркинсона, боковой амиотрофический склероз, рассеянный склероз, судорожные расстройства (с припадками), деменцию при СПИДе и расстройства, которые затрагивают процессы обучения и память; глаукому и внутриглазную гипертензию; нарушения желудочной секреции, расслабление и перистальтику желудочно-кишечного тракта (включая сфинктеры); нефропатию лекарственного генеза и вызванную заболеванием; патологические (преждевременные) и физиологические маточные сокращения; ухудшение клеточной защиты; заболевания, вызванные эндотелиальной дисфункцией; резистентность к инсулину при диабете; гипертензию, вызванную беременностью; цереброваскулярные заболевания; нарушения агрегации или женскую половую дисфункцию, включая вагинальную сухость.
14. Фармацевтическая композиция по п. 13, отличающаяся тем, что указанное соединение представляет собой 2,2,5,5-тетраметил-3-(нитрооксиметил)пирролидин-1-илацетат; 2,2,5,5-тетраметил-3-(нитрооксиметил)пирролидин-1-илпропионат; или 2,2,5,5-тетраметил-3-(нитрооксиметил)пирролидин-1-илизобутират, или их энантиомер, диастереомер, рацемат или фармацевтически приемлемую соль.
15. Фармацевтическая композиция по п. 13, приготовленная для внутривенного, внутриартериального, внутримышечного, внутрибрюшного, интратекального, внутриплеврального, внутритрахеального, подкожного, местного или перорального введения, или для введения путем ингаляции.
16. Применение соединения по любому из пп. 1-12 или его энантиомера, диастереомера, рацемата или фармацевтически приемлемой соли для получения фармацевтической композиции для предотвращения, лечения или контролирования заболевания, расстройства или состояния, связанного с окислительным стрессом или эндотелиальной дисфункцией, где указанное заболевание, расстройство или состояние, связанное с окислительным стрессом или эндотелиальной дисфункцией, представляет собой ишемически-реперфузионное повреждение сетчатки; острую переднюю ишемическую оптическую невропатию; закупорку центральной ретинальной артерии; гемолитические заболевания, включая сфероцитоз, дефицит глюкозо-6-фосфатдегидрогеназы (G6PD), серповидно-клеточную болезнь, талассемию и ночную пароксизмальную гемоглобинурию; сахарный диабет, включая диабетические раны и диабетическую ретинопатию, нефропатию и сердечно-сосудистое заболевание; сердечно-сосудистые заболевания, такие как ишемическая болезнь сердца, стенокардия, ишемически-реперфузионное повреждение миокарда и инфаркт, острое и хроническое ишемически-реперфузионное повреждение конечности, застойная сердечная недостаточность (ЗСН), атеросклероз, аритмии сердца при гипертензии периферических артерий, идиопатическая легочная гипертензия, легочная гипертензия, связанная с идиопатическим легочным фиброзом, легочная гипертензия, связанная с гемолитическим заболеванием, первичная легочная гипертензия новорожденных, легочная гипертензия на фоне врожденной диафрагмальной грыжи и аспирации мекония; легочная гипертензия на фоне врожденного заболевания сердца; легочную гипертензию на фоне недостаточности митрального клапана, дефекта межпредсердной или межжелудочковой перегородки; контраст-индуцированную нефропатию; астму; травму; гиповолемический, нейрогенный или септический шок; идиопатическую эректильную дисфункцию; эректильную дисфункцию на фоне нервосберегающей радикальной простатэктомии; ингаляционное поражение легких, вызванное токсическим агентом; ингаляционное поражение легких хлором; нейротоксичность; нейродегенеративные и неврологические расстройства, включая болезни Альцгеймера и Паркинсона, боковой амиотрофический склероз, рассеянный склероз, судорожные расстройства (с припадками), деменцию при СПИДе и расстройства, которые затрагивают процессы обучения и память; глаукому и внутриглазную гипертензию; нарушения желудочной секреции, расслабление и перистальтику желудочно-кишечного тракта (включая сфинктеры); нефропатию лекарственного генеза и вызванную заболеванием; патологические (преждевременные) и физиологические маточные сокращения; ухудшение клеточной защиты; заболевания, вызванные эндотелиальной дисфункцией; резистентность к инсулину при диабете; гипертензию, вызванную беременностью; цереброваскулярные заболевания; нарушения агрегации или женскую половую дисфункцию, включая вагинальную сухость.
17. Способ предотвращения, лечения или контролирования заболевания, расстройства или состояния, связанного с окислительным стрессом или эндотелиальной дисфункцией, у нуждающегося в этом индивидуума, включающий введение указанному индивидууму эффективного количества соединения по любому из пп. 1-12, или его энантиомера, диастереомера, рацемата или фармацевтически приемлемой соли, где указанное заболевание, расстройство или состояние, связанное с окислительным стрессом или эндотелиальной дисфункцией, представляет собой ишемически-реперфузионное повреждение сетчатки; острую переднюю ишемическую оптическую невропатию; закупорку центральной ретинальной артерии; гемолитические заболевания, включая сфероцитоз, дефицит глюкозо-6-фосфатдегидрогеназы (G6PD), серповидно-клеточную болезнь, талассемию и ночную пароксизмальную гемоглобинурию; сахарный диабет, включая диабетические раны и диабетическую ретинопатию, нефропатию и сердечно-сосудистое заболевание; сердечно-сосудистые заболевания, такие как ишемическая болезнь сердца, стенокардия, ишемически-реперфузионное повреждение миокарда и инфаркт, острое и хроническое ишемически-реперфузионное повреждение конечности, застойная сердечная недостаточность (ЗСН), атеросклероз, аритмии сердца при гипертензии периферических артерий, идиопатическая легочная гипертензия, легочная гипертензия, связанная с идиопатическим легочным фиброзом, легочная гипертензия, связанная с гемолитическим заболеванием, первичная легочная гипертензия новорожденных, легочная гипертензия на фоне врожденной диафрагмальной грыжи и аспирации мекония; легочная гипертензия на фоне врожденного заболевания сердца; легочную гипертензию на фоне недостаточности митрального клапана, дефекта межпредсердной или межжелудочковой перегородки; контраст-индуцированную нефропатию; астму; травму; гиповолемический, нейрогенный или септический шок; идиопатическую эректильную дисфункцию; эректильную дисфункцию на фоне нервосберегающей радикальной простатэктомии; ингаляционное поражение легких, вызванное токсическим агентом; ингаляционное поражение легких хлором; нейротоксичность; нейродегенеративные и неврологические расстройства, включая болезни Альцгеймера и Паркинсона, боковой амиотрофический склероз, рассеянный склероз, судорожные расстройства (с припадками), деменцию при СПИДе и расстройства, которые затрагивают процессы обучения и память; глаукому и внутриглазную гипертензию; нарушения желудочной секреции, расслабление и перистальтику желудочно-кишечного тракта (включая сфинктеры); нефропатию лекарственного генеза и вызванную заболеванием; патологические (преждевременные) и физиологические маточные сокращения; ухудшение клеточной защиты; заболевания, вызванные эндотелиальной дисфункцией; резистентность к инсулину при диабете; гипертензию, вызванную беременностью; цереброваскулярные заболевания; нарушения агрегации или женскую половую дисфункцию, включая вагинальную сухость.
| WO 2013005216 A1, 10.01.2013 | |||
| WO 2012093383 A1, 12.07.2012 | |||
| WO 1999037616 A1, 29.07.1999 | |||
| WO 2011092690 A1, 04.08.2011 | |||
| МНОГОФУНКЦИОНАЛЬНЫЕ ПРОИЗВОДНЫЕ НИТРОКСИДА И ИХ ПРИМЕНЕНИЕ | 2011 |
|
RU2597265C2 |
Авторы
Даты
2018-06-29—Публикация
2014-03-05—Подача