Изобретение относится к области медицины, в частности к медицинской диагностике и может быть использовано для прогнозирования риска потери плода в семейной паре при наличии урогенитальной инфекции у мужчин.
В условиях персистирующей вирусно-бактериальной урогенитальной инфекции происходит качественное изменение течения инфекционного процесса, так как возбудители, взаимодействуя друг с другом, могут существенно менять свои патогенные свойства, вследствие чего, клиническая картина приобретает определенные особенности и существенно меняется от таковой, присущей отдельным моноинфекциям. Как известно, при вирусе простого герпеса (ВПГ-2) происходят выраженные нарушения интерферонового и цитокинового статусов больных [7]. Бессимптомное персистирование С. trachomatis, может приводить к «запуску» иммунного ответа организма с реакцией замедленной гиперчувствительности, что является одним из ведущих факторов в генезе мужского бесплодия, а в ассоциации с хламидиями ВПГ-2 оказывает роль в развитии неопластических процессов предстательной железы [1; 2; 6; 8; 13; 17].
Известно, что фактор некроза опухоли - ФНОα подает сигнал смерти через рецептор ФНОα 1 типа (р55) и Fas-антиген (Аро-1, CD95+), инициирующие взаимодействие смертельных доменов рецептора с адаптерными протеинами FADD (FasR-associated death domain) и TRADD (ФНОR-associated death domain) и каспазой-8 [4; 10]. Низкое содержание ФНОα, необходимого для запуска апоптогенного сигнала, косвенно свидетельствует о нарушении апоптоза. Дефект апоптоза является одной из причин сохранения жизнеспособности инфицированных вирусом клеток, что приводит к хронизации процесса [9, 12]. Этому способствует также и недостаточная выработка интерлейкина - ИЛ-2 [11]. Дефицит ФНОα и ИЛ-2 может свидетельствовать о недостаточной противовирусной активности клеточного иммунитета, что способствует длительной персистенции вирусов. Давно известно, что ФНО подавляет хламидийную инфекцию и играет важную роль в ранней элиминации хламидий, не связанной с интерфероном-ИФНγ [5]. Хламидийная инфекция поддерживает персистенцию ВПГ-2 вследствие накопления NADPH, снижения образования восстановленного глутатиона и повышения окислительных процессов [13]. Повышение содержания hsp60 при урогенитальном хламидиозе способствует появлению цитокинов воспаления, индуцирует синтез металлопротеиназ (ММП) и окисление липопротеинов [3]. Активность ММП зависит от уровня экспрессии их генов и от наличия активаторов и ингибиторов [16]. ММП могут принимать участие в элиминации инфекции, но усиление экспрессии этих ферментов может также привести к деградации межклеточного матрикса и образованию рубцов [16], а их тканевые ингибиторы (ТИМП) способствуют образованию фиброза. R. Jha et al. (2011) [18] показали, что ИЛ-22 и ИЛ-17 могут совместно индуцировать продукцию провоспалительных цитокинов, нейтрофильных хемокинов и антимикробных молекул. Например, ИЛ-22 и ИЛ-17 увеличивают производство S100A8 (calgranulin А) и S100A9 (calgranulin В), которые образуют гетеродимерный комплекс - calprotectin (индуцирует хемотаксис нейтрофилов и выступает в качестве антимикробного петида - alarmin, мощно усиливая воспаление).
R.M. Johnson et al. (2014) [15] обнаружили, что при урогенитальном хламидиозе CD4+ Т-хелперы 1 типа опосредуют защитный иммунитет, в то время как ответы CD8+Т-клеток связаны с рубцеванием и бесплодием. Спаечный процесс опосредуется CD8+Т-клетками и связан с продукцией ФНОα. Авторы указывают, что два из пяти клонов CD8+ производили ИЛ-13 в дополнение к ИЛ-2, ФНОα, ИЛ-10 [15]. K.L. Asquith et al. (2011) [14] в своем исследовании показали, что высокий уровень ИЛ-13 может способствовать восприимчивости к хламидийной инфекции и усилению воспаления.
На сегодняшний день лабораторные исследования в диагностике невынашивания беременности имеют одно из первостепенных значений. Известны несколько способов диагностики риска потери плода на этапе прегравидарной подготовки.
Известен способ прогнозирования невынашивания беременности ранних сроков инфекционного генеза (патент RU 2444734). Согласно способу, определяют уровень растворимой формы рецептора sFlt-1 в сыворотке крови беременной в 1 триместре. При его величине, равной 0,389 нг/мл или ниже, прогнозируют прерывание беременности. Способ позволяет снизить угрозу перинатальных потерь за счет своевременного выявления беременных группы риска и начала адекватных лечебных мероприятий. Недостатком данного способа является определение риска потери плода в состоянии беременности.
Известен способ раннего прогнозирования невынашивания беременности (RU 2592204). Согласно способу, выделяют РНК из эпителиальных клеток цервикального канала у женщин, с проведением обратной транскрипции с получением мДНК, определение экспрессии
CASP-3α (отн. ед.) и СОХ-2 с помощью количественной полимеразной цепной реакции и расчет y1 и у2 по уравнениям линейной дискриминантной функции следующего вида:
у1 = -0,8383+155,755*х1+27,2986*х2,
у2 = -207,714+3007,030*х1+533,609*х2,
где x1 - уровень экспрессии мРНК CASP-3α (отн. ед.),
х2 - уровень экспрессии мРНК СОХ-2 (отн. ед.).
Прогнозируют развитие невынашивания беременности ранних сроков, если y1 больше y2. Прогнозируют прогрессирование беременности в случае, если y2 больше, чем y1. Предложенное изобретение позволяет эффективно прогнозировать невынашивание беременности в 92,10% случаев. Применение данного способа позволяет своевременно реализовывать необходимые лечебно-профилактические мероприятия по предупреждению невынашивания беременности. Недостатком данного способа является сложность расчетов и определение риска невынашивания на ранних сроках беременности.
Известен способ диагностики мужского фактора невынашивания беременности в первом триместре (RU 2268464). Согласно способу, определяют качественно-количественные характеристики эякулята. Проводят исследование эякулята при помощи проточной цитофлуорометрии. В качестве флуорохрома используют этидия бромид. Анализируют гистограммы, отражающие распределение клеток по малоугловому светорассеянию и по интенсивности флуоресценции ДНК в красной области спектра (λ=620 нм). В гистограммах, отражающих распределение клеток по малоугловому светорассеянию, определяют процентное содержание в эякуляте клеток доминирующей популяции, коэффициент вариации светорассеяния в этой популяции. В гистограммах, отражающих распределение клеток по интенсивности флюоресценции ДНК, определяют коэффициент вариации интенсивности флуоресценции в доминирующей популяции. С помощью математической обработки полученных результатов выведено решающее правило определения диагностического индекса (MF). Получив MF>0, диагностируют мужской фактор риска прерывания беременности в первом триместре, при MF<0 считают мужской фактор несущественным. Способ обеспечивает эффективность и специфичность диагностики прогноза мужского фактора невынашивания беременности. Способ диагностики мужского фактора невынашивания беременности в первом триместре путем исследования эякулята, отличающийся тем, что оценивают морфологию сперматозоидов, определяя содержание в эякуляте сперматозоидов с нормальной морфологией в процентном и количественном отношениях и гистограммы проточной цитофлуорометрии эякулята и вычисляют диагностический индекс по формуле:
MF = 1,203-0,043⋅N1+0,005⋅N2-0,013⋅N3-0,026⋅N4+0,054⋅N5+0,027⋅N6,
MF - диагностический индекс (male factor);
N1 - содержание в эякуляте сперматозоидов с нормальной морфологией, %;
N2 - количество в эякуляте сперматозоидов с нормальной морфологией, млн;
N3 - концентрация сперматозоидов с нормальной морфологией, млн/мл;
N4 - содержание клеток доминирующей популяции в гистограмме малоуглового светорассеяния, %;
N5 - коэффициент вариации светорассеяния доминирующей популяции в гистограмме малоуглового светорассеяния;
N6 - коэффициент вариации интенсивности флуоресценции ДНК в доминирующей популяции,
при MF более 0 диагностируют мужской фактор невынашивания беременности, если же MF менее 0, считают мужской фактор несущественным в невынашивании беременности в первом триместре. Недостатком данного исследования считаем отсутствие комплексного подхода в определении мужского фактора невынашивания беременности и определение качественно-количественных характеристик эякулята после оплодотворения.
Известен способ прогнозирования угрозы невынашивания беременности в 1 и 2 триместрах при урогенитальной инфекции (RU 2341799). Согласно этому способу, у беременных женщин с выявленной урогенитальной инфекцией в 1 и 2 триместрах определяют уровень интерлейкина 12 (ИЛ-12) в слизи цервикального канала. При значении уровня ИЛ-12 выше 102,0 пг/мл прогнозируют высокий риск невынашивания беременности в 1 и 2 триместрах. Использование способа позволяет повысить чувствительность прогнозирования угрозы невынашивания беременности в 1 и 2 триместрах у беременных с урогенитальной инфекцией, что дает возможность назначить своевременные лечебные мероприятия в период беременности. Недостатком данного способа считаем отсутствие анализа уровня ИЛ-12 у мужчин в семейных парах, так как при урогенитальной инфекции диагностика и лечение осуществляется в паре.
Известен способ прогнозирования результата лечения бесплодия и невынашивания у женщин в зависимости от иммунологических и иммуногенетических показателей (отозванная заявка RU 2013134051). Согласно способу, определяют особенности генотипа HLA партнеров и доноров лимфоцитов, отличающихся необходимостью типирования по HLA доноров для проведения лимфоцитотерапии на фоне высокого уровня NK-клеток у реципиента, что улучшает прогноз, так как позволяет обеспечить иммунизацию по максимальному количеству генов, и определения зон прогноза с помощью мультифакторного дискриминантного анализа, при котором рассчитываются значения канонических дискриминантных функций F1 и F2 для пары с HLA-совместимостью в анамнезе, позволяющие отнести пару в 1, 2-ю или 3-ю зоны на территориальной карте и определяющие прогностический индекс Р, при Р>1,461, пара относится к первой зоне - благоприятный прогноз наступления беременности, при Р<-1,237, пара в третьей зоне - прогноз неблагоприятный, при Р в диапазоне >-1,237, но <1,461, пара относится к 2-й зоне на территориальной карте прогноз условно благоприятный (достижение беременности только методами вспомогательных репродуктивных технологий). Недостатком данного метода считаем определение наступления беременности, но не положительного ее исхода.
Наиболее близким к заявляемому способу является способ прогнозирования исхода беременности у женщин с угрожающим выкидышем ранних сроков (Патент РФ №2103686). Согласно этому способу прогнозируют исход беременности у женщин с угрожающим выкидышем ранних сроков (до 12 недель) по сперме отца ребенка. Эта цель достигается тем, что прогнозирование исхода беременности у женщин с угрожающим выкидышем ранних сроков осуществляется путем количественного определения плацентарного альфа-2 микроглобулина (ПАМГ-2) в сперме мужа, и при его содержании менее или равном 8 мкг/мл, прогнозируют самопроизвольный выкидыш. При уровне ПАМГ-2 в сперме 16-64 мкг/мл прогнозируют донашивание беременности. Данный способ рассчитан на выявление риска потери плода, но реализуется при наличии только одного учитываемого фактора.
Ни один из указанных способов не ставит задачу ранней диагностики риска потери плода семейной пары при наличии урогенитальной инфекции у мужчины на этапе подготовки к беременности с помощью определения в сыворотке венозной крови и эякуляте про- и противовоспалительных цитокинов и показателей, характеризующих состояние межклеточного матрикса (ММП и ТИМП).
Задачей настоящего изобретения является создание способа ранней диагностики риска потери плода в семейной паре при наличии урогенитальной инфекции у мужчин на этапе прегравидарной подготовки, позволяющего выявить наиболее достоверные критерии риска возникновения репродуктивных потерь и в короткие сроки определить тактику профилактики и лечения невынашивания беременности в семейной паре.
Для решения поставленной задачи разработан способ ранней диагностики риска потери плода в семейной паре при наличии урогенитальной инфекции у мужчин, согласно которому, на этапе прегравидарной подготовки, у пациента определяют уровни ФНОα, ИЛ-17, ИЛ-13 и ТИМП-2 в сыворотке венозной крови, а также ФНОα, ИЛ-13 и ММП-8 в эякуляте с помощью твердофазного иммуноферментного анализа, и в случае выявления: в сыворотке венозной крови ФНОα более 12,0 пг/мл, ИЛ-17 выше 8,5 пг/мл, ИЛ-13 выше 100,0 пг/мл и ТИМП-2 ниже 110,0 нг/мл и в эякуляте ФНОα выше 5,0 пг/мл, ИЛ-13 выше 55,0 пг/мл и ММП-8 выше 10,0 нг/мл диагностируют высокий риск потери плода.
Технический результат изобретения заключается в том, что выявлены достоверные критерии ранней диагностики репродуктивных потерь в семейной паре при наличии хронического уретрита у мужчин на этапе планирования беременности, а именно: высокие уровни ФНОα, ИЛ-17, ИЛ-13 и низкие значения ТИМП-2 в сыворотке венозной крови, а также высокие уровни ФНОα, ИЛ-13 и ММП-8 в эякуляте. Это позволяет в короткие сроки прогнозировать наличие риска потери плода на этапе прегравидарной подготовки семейной пары и принять необходимую стратегию профилактики и лечения синдрома потери плода в семейной паре.
Для разработки заявляемого способа были проведены соответствующие исследования. В исследовании приняло участие 102 пациента мужского пола в возрасте 26-44 лет, средний возраст 33,07±0,69 года. Все пациенты оформляли договор о личном согласии на прохождение всех этапов исследования.
Выполнена комплексная оценка биохимических, вирусологических, бактериологических, бактериоскопических, цитокиновых, показателей межклеточного матрикса, у пациентов с хроническим уретритом. Выявлены наиболее ценные для риска развития репродуктивных потерь маркеры (цитокины, ММП и ТИМП) и установлен их достоверный уровень для определения раннего прогнозирования риска потери плода.
Определение уровня ФНОα было выполнено с помощью постановки реакций со специфическими реактивами фирмы «R&D Diagnostic. Inc» (США), методом сэндвич - варианта твердофазного иммуноферментного анализа. Количественную оценку результатов проводили методом построения калибровочной кривой, отражающей зависимость оптической плотности от концентрации антитела. Учет результатов производили с помощью иммуноферментного анализатора (Multiscan, Финляндия). Расчет количества ФНОα проводили путем построения калибровочной кривой с помощью компьютерной программы Excel. Содержание цитокина выражали в пикограммах на миллилитр (пг/мл), чувствительность применяемого метода составила 1 пг/мл. Концентрация ИЛ-17 оценивалась в сыворотке крови количественным методом твердофазного ИФА наборами ИЛ-17 (R&D Diagnostic. Inc, США). Содержание ИЛ-17 выражали в пикограммах на миллилитр (пг/мл), чувствительность применяемого метода составила 1 пг/мл. Концентрация ИЛ-13 оценивалась в сыворотке крови количественным методом твердофазного ИФА наборами ИЛ-13 (R&D Diagnostic. Inc, США). Содержание ИЛ-13 выражали в пикограммах на миллилитр (пг/мл), чувствительность применяемого метода составила 1 пг/мл. За контрольные значения принимались результаты аналогичных тестов, проведенных в группе здоровых людей. Концентрация ТИМП-2 оценивалась в сыворотке крови количественным методом твердофазного ИФА наборами ТИМП-2 (R&D Diagnostic. Inc, США). Содержание тканевого ингибитора матриксной металоопротеиназы-2 выражали в нанограммах на миллилитр (нг/мл), чувствительность применяемого метода составляла 0,08 нг/мл. Концентрация ММП-8 оценивалась в сыворотке крови количественным методом твердофазного ИФА наборами ММП-8 (R&D Diagnostic. Inc, США). Содержание матриксной металоопротеиназы-8 выражали в нанограммах на миллилитр (нг/мл), чувствительность применяемого метода составляла 1 нг/мл. За контрольные значения принимались результаты аналогичных тестов, проведенных в группе здоровых людей. Статистическую обработку полученных данных проводили с помощью пакета программ «Statistica-6». Данные представляли в виде медианы и двух квартилей (Me, Q25, Q75). Межгрупповые (между группами хронического уретрита в зависимости от этиологического фактора) различия оценивали с помощью критерия Манна - Уитни в рамках прикладной программы SPSS v.16. Для проверки взаимосвязи или независимости между величинами определяли критерий χ2. Уровень доверительной вероятности был задан равным 95%, т.е. нулевые гипотезы отвергались в том случае, когда достигнутый уровень значимости Р используемого статистического критерия принимал значения менее 5%.
Для выявления предикторов потери плода на этапе прегравидарной подготовки выполняли следующее: у пациентов с хроническим уретритом осуществлялся забор венозной крови и эякулята до лечения для лабораторного определения уровней цитокинов и показателей межклеточного матрикса.
Полученные результаты представлены в таблице 1, 2.
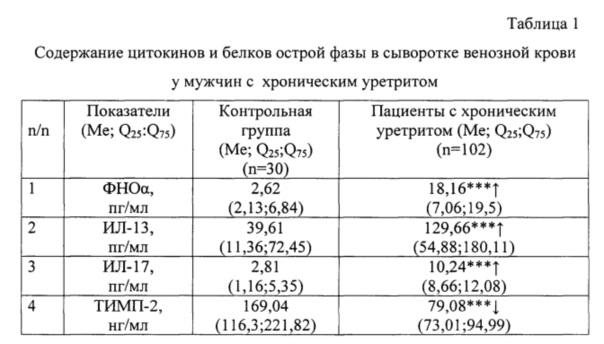
Примечание: статистическая достоверность различий между группами: с группой контроля: р<0,05 - *; р<0,01 - **; р<0,001 - ***; между группами пациентов с хроническим уретритом в зависимости от этиологии: р<0,05 - #; р<0,01 - ##; р<0,001 - ###, где 1, 2, 3 - исследуемые группы
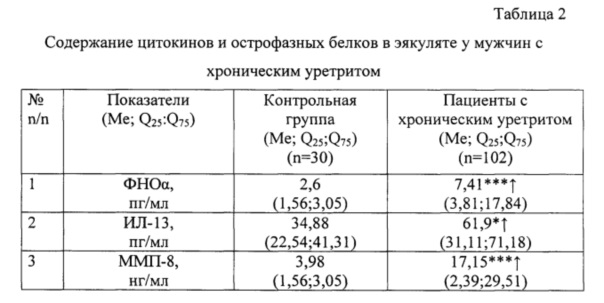
Примечание: статистическая достоверность различий между группами: с группой контроля: р<0,05 - *; р<0,01 - **; р<0,001 - ***; между группами пациентов с хроническим уретритом в зависимости от этиологии: р<0,05 - #; р<0,01 - ##; р<0,001 - ###, где 1, 2, 3 - исследуемые группы
По результатам исследования при разработке заявляемого способа были выявлены предикторы потери плода в семейной паре при наличии урогенитальной инфекции у мужчин в период прегравидарной подготовки. Вывод о риске невынашивания беременности в семейной паре у мужчин с хроническим уретритом делают в случае выявления изменения уровней (табл. 1, 2): ФНОα более 12,0 пг/мл, ИЛ-17 выше 8,5 пг/мл, ИЛ-13 выше 100,0 пг/мл и ТИМП-2 ниже 110,0 нг/мл в сыворотке венозной крови и уровней ФНОα выше 5,0 пг/мл, ИЛ-13 выше 55,0 пг/мл и ММП-8 выше 10,0 нг/мл, что свидетельствует о высоком риске потери плода.
Таким образом, предложен новый достоверный способ ранней диагностики риска потери плода в семейной паре при наличии урогенитальной инфекции у мужчин.
По мнению авторов, заявляемое техническое решения соответствует критериям «новизна» и «изобретательский уровень», поскольку его существенные признаки не только не известны из уровня техники, но для специалиста предлагаемое решение явным образом не следует из уровня техники. Заявляемое техническое решения соответствует критерию «промышленная применимость», поскольку может быть применимо в здравоохранении.
Не известен способ раннего прогнозирования риска потери плода на этапе прегравидарной подготовки в семейной паре при наличии урогенитальной инфекции у мужчин. По наличию изменения концентраций ФНОα, ИЛ-17, ИЛ-13 и ТИМП-2 в сыворотке венозной крови, а также ФНОα, ИЛ-13 и ММП-8 в эякуляте. Для проверки взаимосвязи или независимости (χ2) между предлагаемыми показателями при хроническом вирусном уретрите в сыворотке венозной крови между гиперпродукцией ФНОα у исследуемых пациентов и риском потери плода установлен уровень значимости 0,05% (χ2=3,21, р<0,05), между избытком ИЛ-17 (χ2=4,11, р<0,05), ИЛ-13 выше 100,0 пг/мл (χ2=5,09, р<0,01) и дефицитом ТИМП-2 (χ2=3,48, р<0,05) в сыворотке венозной крови с риском потери плода на этапе прегравидарной подготовки при наличии урогенитальной инфекции у мужчин. Кроме этого, определение χ2 подтверждает тесную связь повышения уровней ФНОα (χ2=3,47, р<0,01), ИЛ-13 (χ2=4,22, р<0,05) и ММП-8 (χ2=5,08, р<0,01) и риском потери плода в эякуляте, то есть выявлена достоверная связь увеличения ФНОα выше 5,0 пг/мл, ИЛ-13 выше 55,0 пг/мл и ММП-8 выше 10,0 нг/мл.
Клинический пример №1.
Больной В, 35 лет, ИБ № М-24, дата поступления: 01.12.2014
Поступил с жалобами боли в области промежности во время полового акта, пузырьковые высыпания в правой паховой области.
Диагноз при поступлении: Генитальный герпес, стадия обострения.
Из анамнеза: потеря плода у супруги на 16 неделе беременности (2013 г.)
По данным лабораторной диагностики (03.12.2014): anti HSV Ig G - полож.
(кп = 8,4), Авидность 52%, ПЦР-мазок Герпес I/II типа - обнаружено.
УЗИ предстательной железы (02.12.2014): умеренные диффузные изменения предстательной железы.
Спермограмма (05.12.2014): Тератозооспемия.
До лечения (02.12.2014), согласно предлагаемому способу, определили содержание цитокинов и медиаторов межклеточного взаимодействия путем иммуноферментного анализа:
- сыворотка венозной крови: ФНОα 15,4 пг/мл, ИЛ-2 39,47 пг/мл, ИЛ-2sR 42,12 пг/мл, ИЛ-17 11,36 пг/мл, ИЛ-13 125,0 пг/мл, ТИМП-2 76,5 нг/мл;
- эякулят: ФНОα 8,41 пг/мл, ИЛ-13 61,37 пг/мл, ММП-8 12,5 нг/мл.
Диагноз: Генитальный герпес. Хронический вирусный уретрит. Тератозооспермия. Бесплодие II.
На основании результатов обследования своевременно была назначена противовирусная и иммуномодулирующая терапия, позволившая избежать потери новой беременности в супружеской паре.
Итак, применение предлагаемого способа позволяет повысить точность и эффективность диагностики риска потери плода на этапе подготовки к беременности, что позволит своевременно назначить комплекс лечебно-профилактических мероприятий и сохранить беременность в семейной паре.
Клинический пример №2.
Больной А, 29 лет, ИБ № М-72, дата поступления: 12.10.2015
Поступил с жалобами выделения из уретры и дискомфорт во время акта мочеиспускания.
Диагноз при поступлении: Уретрит инфекционного генеза, подострое течение.
Из анамнеза: потеря 2-х беременностей у супруги на сроке 6 и 8 недель (2012, 2013 гг.).
По данным лабораторной диагностики (11.10.2015): anti HSV Ig G - полож.
(кп = 9,4), Авидность 35%, ПЦР-мазок Герпес I/II типа - обнаружено. ПЦР (12.10.2015) положит., обнаружены Chlamydia trachomatis МОМР+pgp3 - IgG 1:32, Chlamydia trachomatis HSP60 - IgG 1:4.
УЗИ предстательной железы (12.10.2015): умеренные диффузные изменения предстательной железы. Парауретрит.
Спермограмма (12.10.2015): Олигоспермия. Тератозооспемия.
До лечения (15.10.2015), согласно предлагаемому способу, определили содержание цитокинов и медиаторов межклеточного взаимодействия путем иммуноферментного анализа:
- сыворотка венозной крови: ФНОα 14,2 пг/мл, ИЛ-2 41,02 пг/мл, ИЛ-2sR 43,12 пг/мл, ИЛ-17 10,59 пг/мл, ИЛ-13 119,58 пг/мл, ТИМП-2 74,56 нг/мл; - эякулят: ФНОα 7,99 пг/мл, ИЛ-13 60,09 пг/мл, ММП-8 13,07 нг/мл.
Диагноз: Хронический вирусно-бактериальный уретрит (ВПГ, Хламидиоз). Олигоспермия. Тератозооспермия. Бесплодие II.
На основании результатов обследования своевременно была назначена противовирусная, антибактериальная и иммуномодулирующая терапия, позволившая избежать потери новой беременности в супружеской паре.
Применение предлагаемого способа позволяет повысить точность и эффективность диагностики риска потери плода на этапе подготовки к беременности, что позволит своевременно назначить комплекс лечебно-профилактических мероприятий и сохранить беременность в семейной паре.
Источники информации
1. Абрамова, Т.В. Новые возможности терапии генитального герпеса Мерцалова / Т.В. Абрамова, И.Б. Мерцалова // Terra Medica. - 2012. - №1. - C. 26-33.
2. Азовцева, О.В. Иммунологические изменения при урогенитальном герпесе / О.В. Азовцева // Вестник Кыргызско-Российского славянского университета. - 2013. - Т. 13, №6. - С. 124-128.
3. Гудков, Р.В. Клинико-паразитологическое обоснование рациональной терапии у мужчин с хламидийно-трихомонадной микст-инфекцией : дис. … канд. мед. наук: 14.01.09: 03.02.11 / Гудков Р. В. [Военно-медицинская академия имени С.М. Кирова]. - СПб., 2012. - 555 с.
4. Клиническая иммунология / ред. А.В. Караулов. - М.: Мед. информ. агентство, 2002. - 604 с.
5. Мавров, Г.И. Роль цитокинов в патогенезе хламидиоза / Г.И. Мавров, Г.П. Чинов /  журнал
журнал 
 - 2004. - №1. - С. 53-59
- 2004. - №1. - С. 53-59
6. Новые диагностические и прогностические маркеры при герпетической и хламидийно-герпетической инфекции / Н.С. Чепурнова, Е.В. Маркелова, М.С. Тулупова, Л.Г. Волчкович // Тихоокеанский медицинский журнал. - 2016. - №4. - С. 57-60.
7. Показатели интерферонового статуса и цитокинового профиля у больных с острой и хронической сочетанной формами герпетической инфекции / А.В. Мельниченко, М.В. Мезенцева, Р.Я. Подчерняева и др. // Медицинская иммунология. - 2011. - Т. 13, №4-5. - С. 411-412.
8. Сенчукова, С.Р. Патологический микробиоценоз у пациентов с рецидивирующим генитальным герпесом / С.Р. Сенчукова // Фундаментальные исследования. - 2013. - №9. - С. 127-131.
9. Уджуху, В.Ю. Лавомакс - новые возможности иммуномодулирующей терапии генитального герпеса / В.Ю. Уджуху, А.А. Кубылинский // Вестник дерматологии и венерологии. - 2011. - №4. - С. 108-110.
10. Ярилин, А.А. Иммунология / А.А. Ярилин - М.: ГЭОТАР-Медиа, 2010. - 752 с.
11. Bryant-Hudson, R.M. PD-L1-expressing dendritic cell contribute to viral resisrance during acute HSV-1 infection / R.M. Bryant-Hudson, D.J.J. Carr // Clinical and Developmental Immunology. - 2012. - 9 p.
12. HSV immune complex (HSV-IgG: IC) and HSV-DNA elicit the production of angiogenic factor VEGF and MMP-9 / K. Hayashi, L.С. Hooper, B. Detrick, J.J. Hooks // Arch Virol. - 2009. - V. 154, №2. - P. 219-226.
13. Imbalanced Oxidative Stress Causes Chlamydial Persistence during NonProductive Human Herpes Virus Co-Infection / B.K. Prusty, L. Bohme, B. Bergmann et al. // PLOS ONE. - 2012. - V. 7, №10. - P. 1-17.
14. Interleukin-13 promotes susceptibility to chlamydial infection of the respiratory and genital tracts / K.L. Asquith, J.C. Horvat, G.E. Kaiko et al. // Plos Pathogens. - 2011. - V. 7 (5). - P. e1001339. DOI:10.1371/journal.ppat.1001339
15. Johnson, R.M. An atypical CD8 T-cell response to Chlamydia muridarum genital tract infections includes T cells that produce interleukin-13 / R.M. Johnson, M.S. Kerr, J.E. Slaven // Immunology. - 2014. - V. 142. - P. 248-257.
16. Role of matrix metalloproteinase-7 in the modulation of a Chlamydia trachomatis infection / P. Sukumar, P. Schmidt, E. Peterson, L. Wilson // Blackwell Publishing Ltd, Immunology. - 2005. - V. 117. - P. 213-219.
17. Seminal Levels of IL-10, IL-12, and IL-17 in Men with Asymptomatic Chlamydia Infection / H. Hakimi, M.M. Akhondi, M.R. Sadeghi et al. // Inflammation. - 2014. - V. 37, №1. - P. 122-126.
18. Spontaneous secretion of interleukin-17 and -22 by human cervical cells in Chlamydia trachomatis infection. / R. Jha. P. Srivastava, S. Salhan et al. // Microbes And Infection. - 2011. - V. 13 (2). - P. 167-78. DOI: 10.1016/j.micinf.2010.10.012
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ прогнозирования неразвивающейся беременности, ассоциированной с хромосомными аномалиями эмбриона | 2021 |
|
RU2760499C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ВИРУСНОГО ИНФИЦИРОВАНИЯ СПЕРМАТОЗОИДОВ | 2020 |
|
RU2738798C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ НЕВЫНАШИВАНИЯ БЕРЕМЕННОСТИ ИНФЕКЦИОННОГО ГЕНЕЗА НА РАННИХ СРОКАХ ГЕСТАЦИИ | 2016 |
|
RU2627472C1 |
| Способ диагностики хламидийной урогенитальной инфекции у мужчин | 2018 |
|
RU2683024C1 |
| Способ профилактики постинфекционных репродуктивных нарушений | 2018 |
|
RU2686302C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ РЕПРОДУКТИВНЫХ НАРУШЕНИЙ | 2012 |
|
RU2495431C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ УГРОЗЫ ПРЕРЫВАНИЯ БЕРЕМЕННОСТИ ПРИ УРОГЕНИТАЛЬНОЙ ИНФЕКЦИИ | 2004 |
|
RU2281504C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ НЕВЫНАШИВАНИЯ БЕРЕМЕННОСТИ В РАННИЕ СРОКИ | 2012 |
|
RU2501017C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ УГРОЗЫ ПРЕРЫВАНИЯ БЕРЕМЕННОСТИ С РАННИХ СРОКОВ ГЕСТАЦИИ | 2005 |
|
RU2285926C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ НЕВЫНАШИВАНИЯ ВО ВТОРОМ ТРИМЕСТРЕ БЕРЕМЕННОСТИ | 2007 |
|
RU2340899C1 |
Изобретение относится к области медицины и представляет собой способ ранней диагностики риска потери плода в семейной паре при наличии урогенитальной инфекции у мужчин, характеризующийся тем, что на этапе прегравидарной подготовки у пациента определяют следующие показатели: уровни ФНОα, ИЛ-17, ИЛ-13 и ТИМП-2 в сыворотке венозной крови, а также ФНОα, ИЛ-13 и ММП-8 в эякуляте с помощью твердофазного иммуноферментного анализа, и в случае выявления: в сыворотке венозной крови ФНОα более 12,0 пг/мл, ИЛ-17 выше 8,5 пг/мл, ИЛ-13 выше 100,0 пг/мл и ТИМП-2 ниже 110,0 нг/мл и в эякуляте ФНОα выше 5,0 пг/мл, ИЛ-13 выше 55,0 пг/мл и ММП-8 выше 10,0 нг/мл диагностируют высокий риск потери плода. Осуществление изобретения позволяет в короткие сроки прогнозировать наличие риска потери плода на этапе прегравидарной подготовки семейной пары и принять необходимую стратегию профилактики и лечения синдрома потери плода в семейной паре. 2 табл., 2 пр.
Способ ранней диагностики риска потери плода в семейной паре при наличии урогенитальной инфекции у мужчин, характеризующийся тем, что на этапе прегравидарной подготовки у пациента определяют следующие показатели: уровни ФНОα, ИЛ-17, ИЛ-13 и ТИМП-2 в сыворотке венозной крови, а также ФНОα, ИЛ-13 и ММП-8 в эякуляте с помощью твердофазного иммуноферментного анализа, и в случае выявления: в сыворотке венозной крови ФНОα более 12,0 пг/мл, ИЛ-17 выше 8,5 пг/мл, ИЛ-13 выше 100,0 пг/мл и ТИМП-2 ниже 110,0 нг/мл и в эякуляте ФНОα выше 5,0 пг/мл, ИЛ-13 выше 55,0 пг/мл и ММП-8 выше 10,0 нг/мл, диагностируют высокий риск потери плода.
| МАРКЕЛОВА Е.В | |||
| и др | |||
| Фактор некроза опухоли - α, состояние психоэмоционального статуса и сперматогенеза у мужчин с хроническим вирусно-бактериальным уретритом в супружеских парах с синдромом потери плода // Современные проблемы науки и образования | |||
| Токарный резец | 1924 |
|
SU2016A1 |
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ИСХОДА БЕРЕМЕННОСТИ У ЖЕНЩИН С УГРОЖАЮЩИМ ВЫКИДЫШЕМ РАННИХ СРОКОВ | 1994 |
|
RU2103686C1 |
| ОВЧИННИКОВ Р.И | |||
| и др | |||
| Походная разборная печь для варки пищи и печения хлеба | 1920 |
|
SU11A1 |
| КОЛПАЧЕК ДЛЯ ПАРОПЕРЕГРЕВАТЕЛЬНЫХ ЭЛЕМЕНТОВ | 1923 |
|
SU634A1 |
Авторы
Даты
2018-07-06—Публикация
2017-05-04—Подача