Перекрестная ссылка
Настоящая заявка заявляет приоритет по предварительной заявке на патент США с регистрационным номером US 61/523862, поданной 16 августа 2011 г., которая включена посредством ссылки во всей своей полноте.
Область изобретения
Настоящее раскрытие относится к фармацевтической комбинации антитела к CD19 и аналога пурина для лечения неходжкинской лимфомы, хронического лимфоцитарного лейкоза и/или острого лимфобластного лейкоза.
Предпосылки изобретения
В-клетки являются лимфоцитами, которые играют большую роль в гуморальном иммунном ответе. Они образуются в костном мозге большинства млекопитающих и составляют 5-15% от пула циркулирующих в крови лимфоидных клеток. Основной функцией В-клеток является выработка антител к различным антигенам, и они являются существенным компонентом адаптивной иммунной системы.
Из-за их критически важной роли в регуляции иммунной системы дисрегуляция В-клеток ассоциирована с различными нарушениями, такими как формы лимфомы и лейкоза. Они включают неходжкинскую лимфому (NHL), хронический лимфолейкоз (CLL) и острый лимфобластный лейкоз (ALL).
NHL является гетерогенным злокачественным заболеванием, возникающим в лимфоцитах. В Соединенных Штатах Америки (США) заболеваемость оценивается в 65000 человек в год при смертности, составляющей около 20000 человек в год (Американское онкологическое общество, 2006 г., и обзор статистики онкологических заболеваний SEER). Заболевание может иметь место в любом возрасте, обычно проявление начинается у взрослых старше 40 лет, при этом с возрастом заболеваемость возрастает.NHL характеризуется клональной пролиферацией лимфоцитов, которые накапливаются в лимфатических узлах, крови, костном мозге и селезенке, хотя может быть вовлечен любой основной орган. Существующей системой классификации, применяемой патологоанатомами и клиницистами, является классификация опухолей Всемирной организации здравоохранения (WHO), по которой подразделяет NHL на новообразования из предшественников В-клеток или Т-клеток и зрелых таковых. В PDQ в настоящее время NHL подразделены на медленно прогрессирующие и агрессивные формы для внесения в реестр клинических испытаний. Группа медленно прогрессирующих форм NHL включает главным образом фолликулярные подтипы, мелкоклеточную лимфоцитарную лимфому, MALT-лимфому (из лимфоидной ткани, ассоциированной со слизистыми оболочками) и лимфому маргинальной зоны; медленно прогрессирующие формы охватывают около 50% пациентов с впервые диагностированной В-клеточной NHL. Агрессивные формы NHL охватывают пациентов с гистологическими диагнозами первичная диффузная крупноклеточная В-клеточная лимфома (DLBL, DLBCL или DLCL) (40% всех пациентов, у которых была впервые диагностирована NHL, имеют диффузную крупноклеточную лимфому), лимфома Беркитта и мантийноклеточная лимфома. Клиническое течение NHL сильно варьирует. Основным фактором, определяющим клиническое течение, является гистологический подтип. Большинство медленно прогрессирующих типов NHL считаются неизлечимыми заболеваниями. Пациенты изначально отвечают либо на химиотерапию, либо на терапию с помощью антител, но большинство будут иметь рецидив.
Исследования, проведенные до настоящего времени, не продемонстрировали улучшения выживаемости при раннем вмешательстве. У пациентов с бессимптомным течением приемлемой является тактика "наблюдения и выжидания", пока у пациента не появятся симптомы или темпы заболевания не будут представляться ускоряющимися. Со временем заболевание может преобразоваться в более агрессивную гистологическую форму. Медианная выживаемость составляет от 8 до 10 лет, и пациенты с медленно прогрессирующей формой часто получают 3 или более курса лечения в ходе фазы лечения их заболевания. Первоначальным лечением пациентов с симптомами медленно прогрессирующей NHL исторически была комбинированная химиотерапия. Наиболее часто применяемые средства включают циклофосфамид, винкристин и преднизон (CVP) или циклофосфамид, адриамицин, винкристин, преднизон (CHOP). Примерно от 70% до 80% пациентов будут отвечать на первоначальную химиотерапию, продолжительность ремиссий составляет приблизительно 2-3 года. В конечном счете, у большинства пациентов отмечается рецидив. Обнаружение и клиническое применение антитела к CD20, ритуксимаба, обеспечивает значительные улучшения показателя ответа и коэффициента выживаемости. Современным стандартом лечения для большинства пациентов является применение комбинаций ритуксимаб+CHOP (R-CHOP) или ритуксимаб+CVP (R-CVP). Интерферон одобрен для первоначального лечения NHL в комбинации с алкилирующими средствами, но имеет ограниченное применение в США. Терапия с помощью ритуксимаба показала свою эффективность в отношении нескольких типов NHL и в настоящее время одобрена в качестве первой линии терапии как для медленно прогрессирующей (фолликулярной лимфомы), так и для агрессивной NHL (диффузной крупноклеточной В-клеточной лимфомы). Тем не менее, существуют значительные ограничения для моноклонального антитела к CD20 (mAb), в том числе первичная резистентность (50% ответ у пациентов с медленно прогрессирующей формой, у которых отмечается рецидив), приобретенная резистентность (50% показатель ответа при повторном лечении), редкие случаи полного ответа (2% показатель полного ответа в группе пациентов, у которых отмечается рецидив) и картина длительного рецидива. Наконец, многие В-клетки не экспрессируют CD20 и, таким образом, многие В-клеточные нарушения не поддаются лечению путем терапии с помощью антител к CD20.
В дополнение к NHL, существует несколько типов лейкозов, возникающих в результате дисрегуляции В-клеток. Хронический лимфоцитарный лейкоз (также известный как "хронический лимфолейкоз" или "CLL") представляет собой тип лейкоза у взрослых, вызываемый аномальным накоплением В-лимфоцитов. При CLL злокачественные лимфоциты могут выглядеть нормальными и зрелыми, но они не в состоянии эффективно справляться с инфекцией. CLL является наиболее распространенной формой лейкоза у взрослых. У мужчин в два раза больше шансов на развитие CLL, чем у женщин. Тем не менее, ключевым фактором риска является возраст. Более 75% новых случаев диагностируют у пациентов старше 50 лет. Более 10000 случаев диагностируют ежегодно, и смертность составляет почти 5000 человек в год (Американское онкологическое общество, 2006 г., и обзор статистики онкологических заболеваний SEER). CLL является неизлечимым заболеванием, но в большинстве случаев прогрессирует медленно. Многие люди с CLL ведут нормальный и активный образ жизни в течение многих лет. Из-за его медленного начала, как правило, лечение CLL на ранней стадии не проводят, поскольку считается, что ранее вмешательство при CLL не улучшает время выживания и качество жизни. Вместо этого происходит отслеживание состояния с течением времени. Первоначальное лечение CLL варьирует в зависимости от точного диагноза и прогрессирования заболевания. Существуют десятки средств, применяемых для терапии CLL. Режимы комбинированной химиотерапии, такие как FCR (флударабин, циклофосфамид и ритуксимаб) и BR (бендамустин и ритуксимаб), эффективны как при впервые диагностированном, так и при рецидивирующем CLL. Аллогенная трансплантация костного мозга (стволовых клеток) редко применяется в качестве первой линии терапии CLL из-за ее опасности.
Другой тип лейкоза представляет собой острый лимфобластный лейкоз (ALL), известный также как острый лимфоцитарный лейкоз. ALL характеризуется перепроизводством и непрерывным размножением злокачественных и незрелых белых кровяных телец (также известных как лимфобласты) в костном мозге. "Острый" относится к недифференцированному, незрелому состоянию циркулирующих в крови лимфоцитов ("бластов") и к тому, что болезнь быстро прогрессирует, при этом ожидаемая продолжительность жизни в отсутствие ее лечения составляет от нескольких недель до нескольких месяцев. ALL наиболее распространен в детском возрасте с пиком заболеваемости в 4-5-летнем возрасте. Дети в возрасте 12-16 лет чаще умирают от него, чем другие. В настоящее время по меньшей мере 80% случаев ALL в детском возрасте считаются излечимыми. Около 4000 случаев диагностируют ежегодно, и смертность составляет почти 1500 человек в год (Американское онкологическое общество, 2006 г., и обзор статистики онкологических заболеваний SEER).
Молекула CD19 человека является структурно обособленным рецептором клеточной поверхности, экспрессируемым на поверхности В-клеток человека, в том числе, но без ограничений, пре-В-клеток, В-клеток на ранней стадии развития (т.е. незрелых В-клеток), зрелых В-клеток, прошедших терминальную дифференцировку в плазматические клетки, и злокачественных В-клеток. CD19 экспрессируется в большинстве случаев при пре-В-клеточном остром лимфобластном лейкозе (ALL), неходжкинской лимфоме, В-клеточном хроническом лимфоцитарном лейкозе (CLL), пролимфоцитарном лейкозе, злокачественном ретикулоэндотелиозе, остром недифференцированном лимфоцитарном лейкозе и некоторых формах острого лимфобластного лейкоза с нулевым фенотипом (Nadler et al., J.Immunol., 131:244-250(1983), Loken et al., Blood, 70:1316-1324 (1987), Uckun et al., Blood, 71:13-29 (1988), Anderson et al., 1984. Blood, 63:1424-1433 (1984), Scheuermann, Leuk. Lymphoma, 18:385-397(1995)). Экспрессия CD19 в плазматических клетках дополнительно позволяет предположить, что он может экспрессироваться в дифференцированных В-клетках опухолей, таких как множественная миелома, плазмоцитома, опухоль при болезни Вальденстрема (Grossbard et al., Br. J. Haematol, 102:509-15 (1998); Treon el al., Semin. Oncol, 30:248-52(2003)).
Таким образом, антиген CD19 является мишенью для иммунотерапии при лечении неходжкинской лимфомы (в том числе каждого из подтипов, описанных в данном документе), хронического лимфоцитарного лейкоза и/или острого лимфобластного лейкоза. CD19 также был предложен в качестве мишени для иммунотерапии при лечении аутоиммунных нарушений в WO2000074718, включенном посредством ссылки во всей своей полноте.
Были показаны некоторые методы терапии в отношении CD19. Т-клетки, экспрессирующие химерный рецептор антигена CD19 (CAR), в том числе молекулы CD3-ζ и CD28, вводили пациенту, имеющему фолликулярную лимфому. Kochenderfer et al., Eradication of В lineage cell and regression of lymphoma in a patient treated with autologous T cells genetically engineered to recognize CD19, Blood, vol. 116, no: 20 (ноябрь 2010 г.). В Sadelain et al., The promise and potential pitfalls of chimeric antigen receptors, Current Opinion in Immunology, Elsevier, vol. 21, no. 2, 2 апреля 2009 г., включенном посредством ссылки во всей своей полноте, также описаны химерные рецепторы антигена CD19 (CAR). В Rosenberg et al, Treatment of В cell Malignancies with T cells expressing an anti-CD19 chimeric receptor: Assessment of the Impact of Lymphocyte Depletion Prior to T cell Transfer (сентябрь 2008 г.), www.gemcris.od.nih.gov/Abstracts/940_s.pdf (загружено 13 января 2012 г.), включенном посредством ссылки во всей своей полноте, описаны химерные рецепторы антигена CD19 (CAR), применяемые с флударабином. См. также Eshhar et al., Proceedings of the National Academy of Sciences of USA, National Academy of Science, Washington, D.C:. vol. 90, no.2 (15 января 1993 г. ). Ни у Kochenderfer и соавт., ни у Sadelain и соавт., ни у Rosenberg и соавт., ни у Eshhar и соавт., однако, не описано антитело, специфичное к CD19, в комбинации с флударабином, приводимой в качестве примера в данном документе.
Флударабин в качестве средства терапии при лечении CLL был описан в Montserrat et al., Chronic lymphocytic leukemia treatment, Blood Review, Churchill Livingstone, vol. 7, no. 3 (1 сентября 1993 г.), но там не предлагается антитело, специфичное к CD19, в комбинации с флударабином, приводимой в качестве примера в данном документе.
Применение антитела к CD19 при В-клеточных нарушениях обсуждается в US 2011104150, включенном посредством ссылки во всей своей полноте, наряду с поверхностным упоминанием флударабина в длинном списке возможных компонентов комбинаций, но этого недостаточно как для того, чтобы изложить идею антитела, приводимого в качестве примера, так и для того, чтобы предположить синергические эффекты комбинации при лечении неходжкинской лимфомы, хронического лимфоцитарного лейкоза и/или острого лимфобластного лейкоза, приводимой в качестве примера в данном документе.
Применение антитела к CD19 при формах неспецифической В-клеточной лимфомы обсуждается в WO 2007076950, включенном посредством ссылки во всей своей полноте, наряду с поверхностным упоминанием флударабина в длинном списке возможных компонентов комбинаций, но этого недостаточно как для того, чтобы изложить идею антитела, приводимого в качестве примера, так и для того, чтобы предположить синергические эффекты комбинации при лечении неходжкинской лимфомы, хронического лимфоцитарного лейкоза и/или острого лимфобластного лейкоза, приводимой в качестве примера в данном документе.
Применение антитела к CD19 при формах лейкоза и лимфомы обсуждается в WO 2005012493, включенном посредством ссылки во всей своей полноте, наряду с поверхностным упоминании флударабина в длинном списке возможных компонентов комбинаций, но этого недостаточно как для того, чтобы изложить идею антитела, приводимого в качестве примера, так и для того, чтобы предположить синергические эффекты комбинации при лечении неходжкинской лимфомы, хронического лимфоцитарного лейкоза и/или острого лимфобластного лейкоза, приводимой в качестве примера в данном документе.
Применение антитела к CD19 при CLL, NHL и ALL описано в Scheuermann et al., CD19 Antigen in Leukemia and Lymphoma Diagnosis and Immunotherapy, Leukemia and Lymphoma. Vol. 18, 385-397 (1995), включенном посредством ссылки во всей своей полноте, но этого недостаточно для того, чтобы предложить комбинацию, приводимую в качестве примера в данном документе.
Дополнительные антитела, специфичные к CD19, описаны в WO 2005012493 (US7109304), WO 2010053716 (US 12/266999) (Immunomedics); WO 2007002223 (US US8097703) (Medarex); WO 2008022152 (12/377251) и WO 2008150494 (Xencor), WO 2008031056 (US 11/852106) (Medimmune); WO 2007076950 (US 11/648505) (Merck Patent GmbH); WO 2009/052431 (US 12/253895) (Seattle Genetics) и WO 2010095031 (12/710442) (Glenmark Pharmaceuticals), все из которых включены посредством ссылки во всей своей полноте.
Комбинации антител, специфичных к CD19, и других средств описаны в WO 2010151341 (US 13/377514) (The Feinstein Institute); US 5686072 (University of Texas) и WO 2002022212 (PCT/US 01/29026) (IDEC Pharmaceuticals), все из которых включены посредством ссылки во всей своей полноте.
Ясно, что, несмотря на недавний прогресс в обнаружении и разработке противораковых средств, многие формы рака, в которые вовлечены опухоли, экспрессирующие CD19, все еще имеют неблагоприятный прогноз. Таким образом, существует потребность в улучшенных композициях и способах для лечения таких форм рака.
Краткое описание
Ни в отдельности, ни в комбинации в известном уровне техники не предполагаются синергические эффекты комбинации антитела, приводимого в качестве примера, и флударабина при лечении неходжкинской лимфомы, хронического лимфоцитарного лейкоза и/или острого лимфобластного лейкоза.
В одном аспекте настоящее раскрытие относится к синергической комбинации антитела, специфичного к CD19, и аналога пурина. Такие комбинации применимы при лечении В-клеточных злокачественных заболеваний, таких как неходжкинская лимфома, хронический лимфоцитарный лейкоз и/или острый лимфобластный лейкоз.
Модели in vitro и in vivo, как полагают, свидетельствуют о том, как определенное соединение или комбинация соединений будет вести себя в организме человека. Кроме того, когда соединения комбинируют in vitro или in vivo, ожидается, что комбинация имеет только аддитивные эффекты. К удивлению, авторы настоящего изобретения обнаружили, что комбинация конкретного антитела, специфичного к CD19, и флударабина опосредует специфическое уничтожение клеток из клеточной линии МЕС-1 хронического В-клеточного лейкоза на синергическом уровне по сравнению с антителом и флударабином в отдельности. Эта модель in vitro свидетельствует о том, как комбинация будет действовать при лечении хронического лимфолейкоза (CLL) у людей. Кроме того, и также неожиданно, авторы изобретения обнаружили, что комбинация конкретного антитела, специфичного к CD19, и флударабина как синергически ингибирует рост опухоли, так и синергически увеличивает медианную выживаемость в моделях лимфомы Беркитта на мышах с SCID по сравнению с антителом и флударабином в отдельности. Эти модели in vivo свидетельствуют о том, как комбинация будет действовать при лечении неходжкинской лимфомы у людей. Таким образом, комбинация антитела к CD19, приводимого в качестве примера, и флударабина проявляла синергическое поведение в моделях, соответствующих NHL и CLL. Поскольку как NHL, так и CLL являются В-клеточными нарушениями, и CD19 экспрессируется на высоком уровне в В-клетках, то комбинация, приводимая в качестве примера, будет иметь тот же механизм действия, а также должна проявлять синергическое поведение при лечении других В-клеточных нарушений, например, ALL.
Таким образом, комбинация антитела, приводимого в качестве примера, специфичного к CD19, и флударабина будет эффективной при лечении неходжкинской лимфомы, хронического лимфоцитарного лейкоза и/или острого лимфобластного лейкоза у людей. Кроме того, антитело, специфичное к CD19, приводимое в качестве примера в данном описании, уже участвовало в клинических испытаниях, где такие комбинации могут быть подтверждены при участии людей.
Поскольку механизмы действия флударабина и других аналогов пурина являются сходными ввиду того, что аналоги пурина препятствуют синтезу нуклеиновых кислот, считают, что синергия также будет наблюдаться при лечении людей, имеющих неходжкинскую лимфому, хронический лимфоцитарный лейкоз и/или острый лимфобластный лейкоз, с помощью комбинации антитела к CD19, приводимого в качестве примера, и аналога пурина, отличного от флударабина.
Поскольку антитело к CD19, приводимое в качестве примера, и другие антитела к CD19 связываются с CD19, считают, что синергия также будет наблюдаться при лечении людей, имеющих неходжкинскую лимфому, хронический лимфоцитарный лейкоз и/или острый лимфобластный лейкоз, при помощи комбинации любого антитела к CD19 и аналога пурина, например, флударабина.
Поскольку антитело к CD19, приводимое в качестве примера, связывается с конкретным эпитопом CD19, считают, что антитела, участвующие в перекрестной конкуренции с антителом, приводимым в качестве примера, или связывающиеся с тем же эпитопом, что и антитело, приводимое в качестве примера, также должны проявлять синергическое поведение при лечении людей, имеющих неходжкинскую лимфому, хронический лимфоцитарный лейкоз и/или острый лимфобластный лейкоз, в комбинации с аналогом пурина, например, флударабином.
Один аспект настоящего изобретения включает синергическую комбинацию антитела, специфичного к CD19, которое содержит HCDR1-участок с последовательностью SYVMH (SEQ ID NO: 1), HCDR2-участок с последовательностью NPYNDG (SEQ ID NO: 2), HCDR3-участок с последовательностью GTYYYGTRVFDY (SEQ ID NO: 3), LCDR1-участок с последовательностью RSSKSLQNVNGNTYLY (SEQ ID NO: 4), LCDR2-участок с последовательностью RMSNLNS (SEQ ID NO: 5) и LCDR3-участок с последовательностью MQHLEYPIT (SEQ ID NO: 6), и флударабина. В предпочтительных аспектах комбинацию применяют при лечении неходжкинской лимфомы, хронического лимфоцитарного лейкоза и/или острого лимфобластного лейкоза.
Описание графических материалов
На фигуре 1 показаны цитотоксические эффекты MOR208 и флударабина в отдельности и в комбинации в отношении клеток МЕС-1.
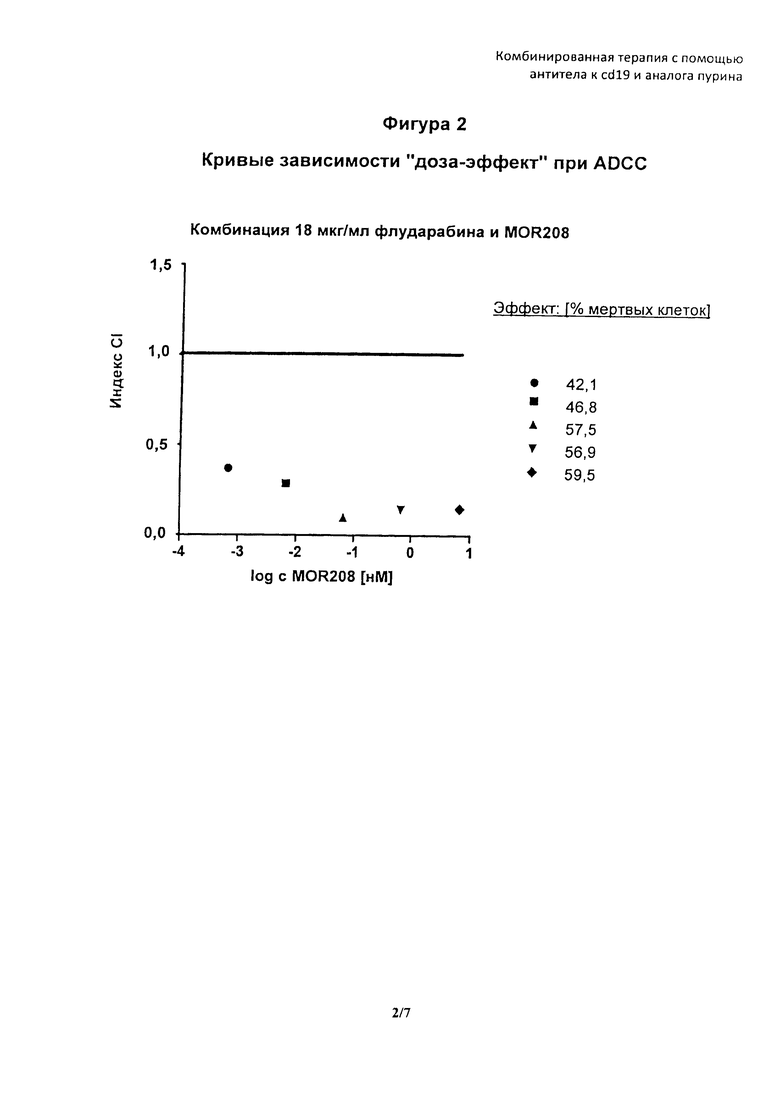
На фигуре 2 показаны кривые зависимости "доза-эффект" для комбинации MOR208 и флударабина в клетках МЕС-1 при ADCC.
На фигуре 3 показаны аминокислотные последовательности вариабельных доменов MOR208.
На фигуре 4 показаны аминокислотные последовательности Fc-областей MOR208.
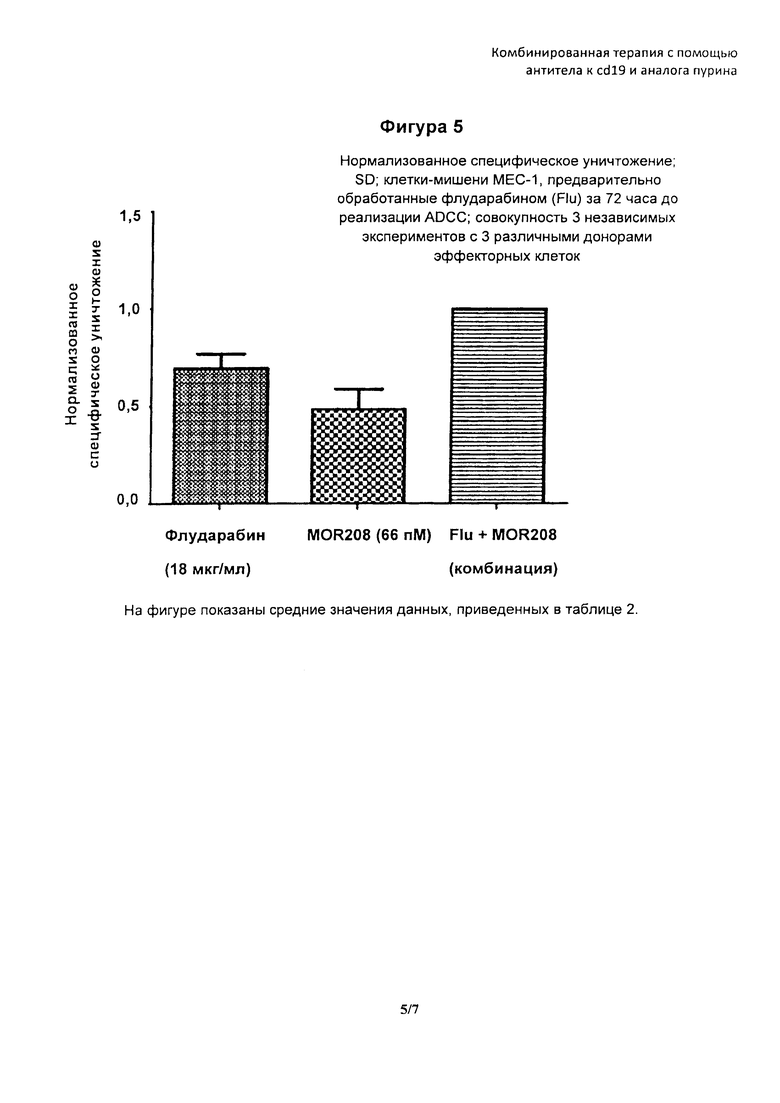
На фигуре 5 показано нормализованное специфическое уничтожение клеток-мишеней МЕС-1, предварительно обработанных флударабином (FLU) за 72 часа до этого. Данные представляют совокупность 3 независимых экспериментов с 3 различными донорами эффекторных клеток.
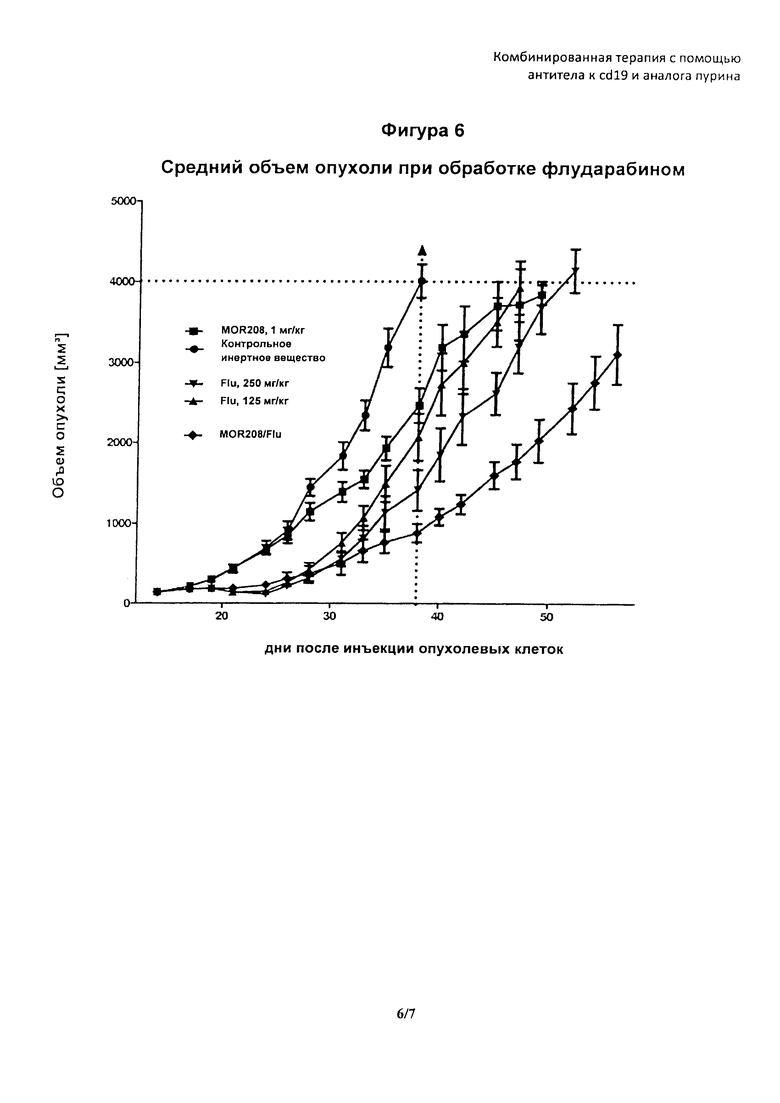
На фигуре 6 показан средний темп роста опухоли в группах MOR208, FLU и комбинации (MOR208/FLU) в модели на мышах с SCID, описываемой в примере 2.
На фигуре 7 показано медианное время выживания в группах MOR208, FLU и комбинации (MOR208/FLU) в модели на мышах с SCID, описываемой в примере 3.
Подробное описание настоящего изобретения
"Синергия", "синергизм" или "синергический" означает эффект, превышающий ожидаемый аддитивный эффект комбинации. "Синергия", "синергизм" или "синергический" эффект комбинации определены в данном документе способами Chou и соавт., Clarke и соавт.и/или Webb и соавт. См. Ting-Chao Chou, Theoretical Basis, Experimental Design, and Computerized Simulation of Synergism and Antagonism in Drug Combination Studies, Pharmacol Rev 58:621-681 (2006), включенный посредством ссылки во всей своей полноте. См. также Clarke et al., Issues in experimental design and endpoint analysis in the study of experimental cytotoxic agents in vivo in breast cancer and other models, Breast Cancer Research and Treatment 46:255-278 (1997), включенный посредством ссылки во всей своей полноте. См. также Webb, J. L. (1963) Enzyme and Metabolic Inhibitors, Academic Press, New York, включенный посредством ссылки во всей своей полноте.
Выражение "антитело" означает моноклональные антитела, в том числе любой изотип, такой как IgG, IgM, IgA, IgD и IgE. Антитело IgG состоит из двух идентичных тяжелых цепей и двух идентичных легких цепей, соединенных дисульфидными связями. Каждая тяжелая и легкая цепь содержит константную область и вариабельную область. Каждая вариабельная область содержит три сегмента, называемых "участками, определяющими комплементарность" ("CDR") или "гипервариабельными участками", которые в первую очередь отвечают за связывание с эпитопом антигена. Они называются CDR1, CDR2 и CDR3 и пронумерованы последовательно с N-конца. Более высококонсервативные части вариабельных областей за пределами CDR называются "каркасными областями". "Фрагмент антитела" означает Fv-, scFv-, dsFv-, Fab-, Fab'-, F(ab')2-фрагмент или другой фрагмент, содержащий по меньшей мере одну вариабельную область тяжелой цепи или вариабельную область легкой цепи, при этом каждая из них содержит CDR и каркасные области.
Аналог пурина представляет собой антиметаболит, который имитирует структуру пуринов, участвующих в метаболизме, тем самым препятствуя синтезу нуклеиновых кислот.Флударабин, например, может быть включен в РНК и ДНК посредством замены пуриновых нуклеотидов аденина и гуанина. Аналоги пурина ингибируют рост быстро пролиферирующих клеток лица, например, раковых клеток, клеток костного мозга или клеток, присутствующих в желудочно-кишечном тракте. Аналоги пурина включают меркаптопурин, азатиоприн, тиогуанин и флударабин.
Меркаптопурин применяют в лечении форм острого лейкоза, форм лимфомы, ревматоидного артрита и воспалительных заболеваний кишечника, таких как болезнь Крона и неспецифический язвенный колит, соответственно. Меркаптопурин имеет следующую структуру:

Азатиоприн является основным иммунодепрессивным цитотоксическим веществом. Его широко применяют в трансплантации для контроля реакции отторжения. Он подвергается неферментативному расщеплению до 6-меркаптопурина, который действует как аналог пурина и ингибитор синтеза ДНК. Предупреждая клональную экспансию лимфоцитов в индуктивной фазе иммунного ответа, он воздействует как на клеточный, так и гуморальный иммунитет. Он также успешно подавляет аутоиммунную реакцию. Азатиоприн имеет следующую структуру:
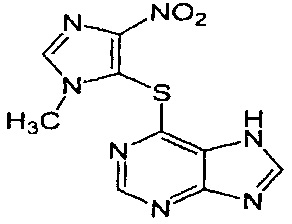
Тиогуанин применяют в ходе ранней и/или поздней интенсификационной терапии детского острого лимфобластного лейкоза (ALL), тогда как 6-меркаптопурин применяют главным образом в другой момент времени при терапии, а именно в ходе поддерживающего лечения ALL. Тиогуанин имеет следующую структуру:

Флударабин или фосфат флударабина (Fludara®) представляет собой химиотерапевтическое лекарственное средство, применяемое при лечении хронического лимфоцитарного лейкоза и медленно прогрессирующей неходжкинской лимфомы. Флударабин является аналогом пурина. Флударабин ингибирует синтез ДНК, препятствуя действию рибонуклеотидредуктазы и ДНК-полимеразы, и является специфичным для S-фазы (поскольку эти ферменты обладают высокой активностью при репликации ДНК). Флударабин имеет следующую структуру:
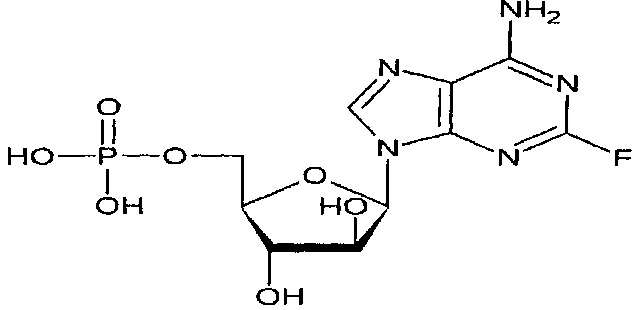
"FLU", применяемое в данном документе, означает флударабин.
"VH" относится к вариабельной области тяжелой цепи иммуноглобулина в антителе или фрагменте антитела. "VL" относится к вариабельной области легкой цепи иммуноглобулина в антителе или фрагменте антитела.
Выражение "CD19" относится к белку, известному как CD19, имеющему следующие синонимы: В4, В-лимфоцитарный антиген CD19, В-лимфоцитарный поверхностный антиген В4, CVID3, дифференцировочный антиген CD19, MGC12802 и Т-клеточный поверхностный антиген Leu-12.
CD19 человека имеет аминокислотную последовательность

"MOR208" представляет собой антитело к CD19. Аминокислотная последовательность вариабельных доменов представлена на фигуре 3. Аминокислотная последовательность Fc-областей тяжелой и легкой цепей MOR208 представлена на фигуре 4. "MOR208" и "XmAb 5574" применяют в качестве синонимов для описания антитела, показанного на фигурах 3 и 4. Антитело MOR208 описано в заявке на патент США с регистрационным номером 12/377251, включенной посредством ссылки во всей своей полноте.
Дополнительные антитела, специфичные к CD19, описаны в патенте США №7109304 (Immunomedics), включенном посредством ссылки во всей своей полноте; заявке на патент США с регистрационным номером 11/917750 (Medarex), включенной посредством ссылки во всей своей полноте; заявке на патент США с регистрационным номером 11/852106 (Medimmune), включенной посредством ссылки во всей своей полноте; заявке на патент США с регистрационным номером 11/648505 (Merck Patent GmbH), включенной посредством ссылки во всей своей полноте; патенте США №7968687 (Seattle Genetics), включенном посредством ссылки во всей своей полноте; и заявке на патент США с регистрационным номером 12/710442 (Glenmark Pharmaceuticals), включенной посредством ссылки во всей своей полноте.
"Fc-область" означает константную область антитела, которое у человека может принадлежать к подклассам IgG1, 2, 3, 4 или другим. Последовательности Fc-областей человека доступны в IMGT, Human IGH C-REGIONs, на http://www.imgt.org/IMGTrepertoire/Proteins/protein/human/IGH/IGHC/Hu_IGHCallgenes.html (загружено 16 мая 2011 г.).
"RefmAb33" представляет собой антитело, аминокислотная последовательность которого выглядит следующим образом.
Тяжелая цепь, содержащая Fc-область:

Легкая цепь, содержащая Fc-область:

RefmAb33 является специфичным к RSV и применяется в качестве изотипического контроля, так как оно содержит ту же Fc-область, что и MOR208.
"Комбинация" означает более одного объекта, например, соединение, такое как антитело, и флударабин.
Настоящее раскрытие также относится к комбинациям, фармацевтическим препаратам и фармацевтическим композициям, содержащим описанные комбинации. Два компонента синергической комбинации согласно настоящему изобретению, например, антитело, специфичное к CD19, и флударабин, можно вводить вместе, одновременно или раздельно. При введении вместе два компонента могут быть составлены в одной фармацевтической композиции, которая может содержать фармацевтически приемлемый носитель или наполнитель. Альтернативно, два компонента могут также быть составлены в различных фармацевтических композициях. В этом случае два компонента можно вводить одновременно или последовательно. В одном из вариантов осуществления флударабин вводят перед введением антитела, специфичного к CD19, например, MOR208, и/или отдельно от него.
Фармацевтическая композиция содержит активное средство, например, антитело для терапевтического применения у людей. Фармацевтическая композиция может содержать приемлемые носители или наполнители.
"Вводимый" или "введение" включает, но без ограничений, доставку инъекционной формы, такую как, например, посредством внутривенного, внутримышечного, внутрикожного или подкожного пути введения или пути введения через слизистые оболочки, например, в виде назального спрея, или аэрозоля для ингаляции, или в качестве раствора, принимаемого внутрь, капсулы или таблетки.
"Терапевтически эффективное количество" соединения или комбинации относится к количеству, достаточному для лечения, облегчения или частичного подавления клинических проявлений данного заболевания или нарушения и его осложнений. Количество, которое является эффективным для конкретной терапевтической цели, будет зависеть от тяжести заболевания или повреждения, а также от веса и общего состояния субъекта. Следует понимать, что определение соответствующей дозировки может быть достигнуто с применением стандартных экспериментов путем построения матрицы значений и тестирования различных точек в матрице, все из которых находятся в пределах обычных профессиональных навыков квалифицированного врача или ученого-клинициста.
"CDR" в данном документе определены либо по Chothia и соавт., либо по Kabat и соавт. См. Chothia С, Lesk AM. (1987) Canonical structures for the hypervariable regions of immunoglobulins. J Mol Biol., 196(4):901-17, включенный посредством ссылки во всей своей полноте. См. Kabat Е.А., Wu Т.Т., Perry Н.М., Gottesman K.S. and Foeller C. (1991). Sequences of Proteins of Immunological Interest. 5th edit., NIH Publication no. 91-3242, US Dept. of Health and Human Services, Washington, DC, включенный посредством ссылки во всей своей полноте.
"Участвует в перекрестной конкуренции" означает способность антитела или другого связывающего средства препятствовать связыванию других антител или связывающих средств с CD19 в стандартном анализе конкурентного связывания. Способность или степень, в которой антитело или другое связывающее средство способно препятствовать связыванию другого антитела или связывающей молекулы с CD19 и, следовательно, как можно сказать, участвовать в перекрестной конкуренции согласно настоящему изобретению, может быть определена с помощью стандартных анализов конкурентного связывания. В один подходящий анализ вовлечено применение технологии Biacore (например, с помощью прибора BIAcore 3000 (Biacore, Уппсала, Швеция)), который может измерить степень взаимодействия при помощи технологии поверхностного плазмонного резонанса. В другом анализе для измерения перекрестной конкуренции применяется подход на основе ELISA. Процесс "связывания с эпитопом" антител с высокой производительностью, основанный на их перекрестной конкуренции, описан в международной заявке на патент №WO 2003/48731.
Выражение "эпитоп" включает любую детерминанту белка, способную к специфическому связыванию с антителом или иному взаимодействию с молекулой. Эпитопы-детерминанты обычно состоят из химически активных поверхностных группировок молекул, таких как аминокислоты или углеводные или сахарные боковые цепи, и могут иметь конкретные характеристики трехмерных структур, а также конкретные характеристики зарядов. Эпитоп может быть "линейным" или "конформационным". Выражение "линейный эпитоп" относится к эпитопу, в котором все точки взаимодействия между белком и взаимодействующей молекулой (такой как антитело) возникают линейно на всем протяжении первичной аминокислотной последовательности белка (непрерывной). Выражение "конформационный эпитоп" относится к эпитопу, в котором прерывистые аминокислотные последовательности объединяются в трехмерную конформацию. В конформационном эпитопе точки взаимодействия возникают на аминокислотных остатках белка, которые отделены друг от друга.
"Связывается с тем же эпитопом" означает способность антитела или другого связывающего средства связываться с тем же эпитопом CD19, что и антитело, приводимое в качестве примера. Эпитопы для антитела, приводимого в качестве примера, и других антитела к CD 19 можно определить при помощи стандартных методик картирования эпитопов. Методики картирования эпитопов, хорошо известные в данной области техники, включают описанные в Epitope Mapping Protocols in Methods in Molecular Biology, Vol. 66 (Glenn E. Morris, Ed., 1996) Humana Press, Totowa, New Jersey. К примеру, линейные эпитопы можно определить путем, например, параллельного синтеза большого количества пептидов на твердых подложках, при этом пептиды соответствуют частям белковой молекулы, и введения пептидов в реакцию с антителами, при том что пептиды все еще прикреплены к подложкам. Такие способы известны в данной области техники и описаны, например, в патенте США №4708871; Geysen et al., (1984) Proc. Natl. Acad. Sci. USA 3:3998-4002; Geysen et al., (1985) Proc. Natl. Acad. Sci. USA 82:78-182; Geysen et al., (1986) Mol. Immunol. 23:709-715. Аналогично, конформационные эпитопы легко идентифицировать путем определения пространственной конформации аминокислот, такого как, например, с помощью водородно-дейтериевого обмена, рентгеновской кристаллографии и двумерного ядерного магнитного резонанса. См., например, Epitope Mapping Protocols, выше. Антигенные участки белков также можно идентифицировать при помощи стандартных графиков антигенности и гидрофобности, таких как рассчитываемые при помощи, например, программы из системы программного обеспечения Omiga версии 1.0, доступной от Oxford Molecular Group.В этой компьютерной программе используют способ Хоппа-Вудса, Норр et al., (1981) Proc. Natl. Acad. Sci USA 78:3824-3828; для определения профилей антигенности и методику Кайта-Дулитла, Kyte et al., (1982) J.Mol. Biol. 157:105-132; для графиков гидрофобности.
Варианты осуществления
Один аспект настоящего раскрытия включает комбинацию антитела, специфичного к CD19, и аналога пурина для применения в лечении неходжкинской лимфомы, хронического лимфоцитарного лейкоза и/или острого лимфобластного лейкоза. В вариантах осуществления комбинация является синергической.
В данном документе комбинация антитела к CD19, приводимого в качестве примера, и флударабина проявляла синергическое поведение в моделях in vitro и in vivo, соответствующих NHL и CLL. Поскольку как NHL, так и CLL представляют собой В-клеточные нарушения, и CD19 экспрессируется на высоком уровне в В-клетках, то комбинация, приводимая в качестве примера, должна иметь такой же механизм действия и должна также проявлять синергическое поведение при лечении других В-клеточных нарушений, например, ALL. Таким образом, комбинация антитела, приводимого в качестве примера, специфичного к CD19, и флударабина будет эффективной при лечении неходжкинской лимфомы, хронического лимфоцитарного лейкоза и/или острого лимфобластного лейкоза у людей.
Поскольку механизмы действия флударабина и других аналогов пурина являются сходными в том отношении, что аналоги пурина препятствуют синтезу нуклеиновых кислот, считают, что синергия также будет наблюдаться при лечении людей, имеющих неходжкинскую лимфому, хронический лимфоцитарный лейкоз и/или острый лимфобластный лейкоз, с помощью комбинации антитела к CD19, приводимого в качестве примера, и аналога пурина, отличного от флударабина, например, меркаптопурина, азатиоприна и тиогуанина.
Поскольку антитело к CD19, приводимое в качестве примера, и другие антитела к CD19 связываются с антигеном CD19, считают, что синергия также будет наблюдаться при лечении людей, имеющих неходжкинскую лимфому, хронический лимфоцитарный лейкоз и/или острый лимфобластный лейкоз, с помощью комбинации любого антитела к CD19 и аналога пурина, где антитело к CD19, например, описано в заявке на патент США с регистрационным номером 12/377251 (Xencor), WO 2005012493, WO 2010053716 (Immunomedics); WO 2007002223 (Medarex); WO 2008022152 (Xencor); WO 2008031056 (Medimmune), WO 2007/076950 (Merck Patent GmbH); WO 2009/052431 (Seattle Genetics) и WO 2010095031 (Glenmark Pharmaceuticals), все из которых включены посредством ссылки во всей своей полноте.
В вариантах осуществления антитело, специфичное к CD19, включает в себя антитело, участвующее в перекрестной конкуренции с антителом, содержащим HCDR1-участок с последовательностью SYVMH (SEQ ID NO: 1), HCDR2-участок с последовательностью NPYNDG (SEQ ID NO: 2), HCDR3-участок с последовательностью GTYYYGTRVFDY (SEQ ID NO: 3), LCDR1-участок с последовательностью RSSKSLQNVNGNTYLY (SEQ ID NO: 4), LCDR2-участок с последовательностью RMSNLNS (SEQ ID NO: 5) и LCDR3-участок с последовательностью MQHLEYPIT (SEQ ID NO: 6).
В вариантах осуществления антитело, специфичное к CD19, включает в себя антитело, связывающееся с тем же эпитопом, что и антитело, содержащее HCDR1-участок с последовательностью SYVMH (SEQ ID NO: 1), HCDR2-участок с последовательностью NPYNDG (SEQ ID NO: 2), HCDR3-участок с последовательностью GTYYYGTRVFDY (SEQ ID NO: 3), LCDR1-участок с последовательностью RSSKSLQNVNGNTYLY (SEQ ID NO: 4), LCDR2-участок с последовательностью RMSNLNS (SEQ ID NO: 5) и LCDR3-участок с последовательностью MQHLEYPIT (SEQ ID NO: 6).
В вариантах осуществления антитело, специфичное к CD19, содержит HCDR1-участок с последовательностью SYVMH (SEQ ID NO: 1), HCDR2-участок с последовательностью NPYNDG (SEQ ID NO: 2), HCDR3-участок с последовательностью GTYYYGTRVFDY (SEQ ID NO: 3), LCDR1-участок с последовательностью RSSKSLQNVNGNTYLY (SEQ ID NO: 4), LCDR2-участок с последовательностью RMSNLNS (SEQ ID NO: 5) и LCDR3-участок с последовательностью MQHLEYPIT (SEQ ID NO: 6).
В вариантах осуществления антитело, специфичное к CD19, содержит вариабельный домен тяжелой цепи с последовательностью

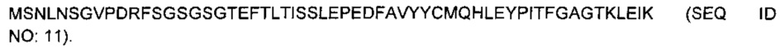
В вариантах осуществления антитело, специфичное к CD19, содержит константный домен тяжелой цепи с последовательностью

В вариантах осуществления антитело, специфичное к CD19, содержит константный домен легкой цепи с последовательностью
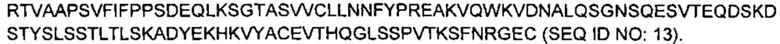
В вариантах осуществления аналог пурина представляет собой флударабин.
В вариантах осуществления компоненты комбинации, антитело, специфичное к CD19 и флударабин, вводят раздельно. В одном из вариантов осуществления флударабин вводят перед введением антитела, специфичного к CD19.
В вариантах осуществления комбинация представляет собой фармацевтическую композицию. В вариантах осуществления композиция содержит приемлемый носитель. В вариантах осуществления комбинацию вводят в эффективном количестве.
В одном из аспектов синергическая комбинация антитела, специфичного к CD19, содержащего HCDR1-участок с последовательностью SYVMH (SEQ ID NO: 1), HCDR2-участок с последовательностью NPYNDG (SEQ ID NO: 2), HCDR3-участок с последовательностью GTYYYGTRVFDY (SEQ ID NO: 3), LGDR1-участок с последовательностью RSSKSLQNVNGNTYLY (SEQ ID NO: 4), LCDR2-участок с последовательностью RMSNLNS (SEQ ID NO: 5) и LCDR3-участок с последовательностью MQHLEYPIT (SEQ ID NO: 6), и флударабина способна опосредовать уничтожение клеток МЕС-1 благодаря ADCC в присутствии выделенных РВМС человека при эффективности, по меньшей мере в два раза, в три раза, в четыре раза или в пять раз лучшей, чем таковая для флударабина в отдельности.
Один из аспектов настоящего раскрытия включает синергическую комбинацию антитела, специфичного к CD19, содержащего HCDR1-участок с последовательностью SYVMH (SEQ ID NO: 1), HCDR2-участок с последовательностью NPYNDG (SEQ ID NO: 2), HCDR3-участок с последовательностью GTYYYGTRVFDY (SEQ ID NO: 3), LCDR1-участок с последовательностью RSSKSLQNVNGNTYLY (SEQ ID NO: 4), LCDR2-участок с последовательностью RMSNLNS (SEQ ID NO: 5) и LCDRS-участок с последовательностью MQHLEYPIT (SEQ ID NO: 6), и флударабина для лечения неходжкинской лимфомы, фонического лимфоцитарного лейкоза и/или острого лимфобластного лейкоза. В вариантах осуществления неходжкинская лимфома выбрана из группы, состоящей из фолликулярной лимфомы, мелкоклеточной лимфоцитарной лимфомы, лимфомы из лимфоидной ткани, ассоциированной со слизистыми оболочками, лимфомы маргинальной зоны, диффузной крупноклеточной В-клеточной лимфомы, лимфомы Беркитта и мантийноклеточной лимфомы.
Другой аспект включает способ лечения неходжкинской лимфомы, хронического лимфоцитарного лейкоза и/или острого лимфобластного лейкоза у лица, нуждающегося в этом, каковой способ включает введение антитела, специфичного к CD19, и аналога пурина. 3 вариантах осуществления способа антитело, специфичное к CD19, содержит HCDR1-участок с последовательностью SYVMH (SEQ ID NO: 1), HCDR2-участок с последовательностью NPYNDG (SEQ ID NO: 2), HCDR3-участок с последовательностью GTYYYGTRVFDY (SEQ ID NO: 3), LCDR1-участок с последовательностью RSSKSLQNVNGNTYLY (SEQ ID NO: 4), LCDR2-участок с последовательностью RMSNLNS (SEQ ID NO: 5) и LCDR3-участок с последовательностью MQHLEYPIT (SEQ ID NO: 6). В вариантах осуществления способа аналог пурина представляет собой флударабин.
Примеры
Пример 1. Ингибирование пролиферации клеток МЕС-1 при помощи MOR208 и флударабина в отдельности и в комбинации
Материалы
Клетки МЕС-1: линия клеток хронического В-клеточного лейкоза DSMZ# АСС497; среда для клеток: среда Дульбекко, модифицированная по способу Исков (IMDM), с GlutaMAX™, Invitrogen, №по каталогу 31980-048, 20% FCS; РВМС: RPMI1640 со стабильным глутамином, PAN Biotech GmbH, №по каталогу Р04-13500, дополненная 10% FCS; Biocoll: Biochrome AG, №по каталогу L6115, №партии 1050Т; флударабин: Bayer, 25 мг/мл в бидистилированной H2O, №партии 9100ST; и RefmAb33 (антитело к RSV) с такой же Fc-областью, что и у MOR208.
Способы
Цитотоксичность MOR208 и флударабина в отдельности и в комбинации тестировали на клетках МЕС-1. FLU представляет собой аналог пурина, следовательно, действует посредством прямой цитотоксичности в отношении клеток МЕС-1. MOR208 нацеливается на CD19 и дополнительно действует благодаря ADCC, уничтожая клетки МЕС-1. Для Уничтожение клеток МЕС-1 измеряли для следующих групп: FLU при 18 мкг/мл; MOR208 при 66 пМ и комбинация MOR208 при 66 пМ и FLU при 18 мкг/мл. Эти концентрации были выбраны, поскольку они близки к ЕС50 для MOR208 и FLU или равны таковой.
В группе FLU и группе комбинации MOR208+FLU клетки МЕС-1 предварительно инкубировали с FLU за 72 часа до измерений в анализе ADCC. Клетки МЕС-1 окрашивали при помощи 1 мг/мл кальцеина AM, затем подсчитывали и доводили до 2×105/мл. РВМС подсчитывали и доводили до 6×106/мл. Анализы ADCC выполняли следующим образом: применяли 96-луночные планшеты, в каждую лунку добавляли 100 мкл клеточной суспензии клеток МЕС-1, затем в каждую лунку добавляли 100 мкл клеточной суспензии РВМС, в результате чего соотношение Е:Т составило 30:1. Антитела разводили в среде до 1 мкг/мл. Клетки центрифугировали и ресуспендировал и. К дебрису, содержащему клетки-мишени и эффекторные клетки, добавляли 100 мкл раствора антитела или соответствующего контрольного раствора. Смесь инкубировали в течение 4 часов в CO2-инкубаторе при 37°С. Измерения ADCC проводили следующим образом: раствор инкубированных клеток (~ 100 мкл) помещали в пробирки для FACS, и в каждую пробирку добавляли 200 мкл буфера для FACS (DPBS+3% FCS) и 0,5 мкл исходного раствора PI. Применяли FACS-Calibur. Мертвые клетки МЕС-1 окрашивали йодидом пропидия.
В таблице 1 и на фигуре 1 представлены необработанные данные.

Значения представляют % мертвых клеток. В каждом эксперименте представлены РВМС от различных доноров. Контроль, применяемый для экспериментов 1 и 2, представлял собой RefMab33. Контроль, применяемый для эксперимента 3, представлял собой РВМС в отдельности.
В таблице 2 представлены необработанные данные из таблицы 1, нормализованные к значениям специфического уничтожения, и результаты расчетов индекса Чоу, выполненные для определения синергизма.

Значения, представленные в таблице 2, рассчитывали следующим образом: 1) из необработанных данных (% мертвых клеток), представленных в таблице 1, вычитали фоновые (контрольные) значения, в результате чего получали значения специфического уничтожения для каждой группы лечения; затем 2) значения специфического уничтожения нормализовали путем установления значения для комбинации MOR208+FLU на 1. Средние значения из таблицы 2 изображены на фигуре 5. Типичные кривые зависимости "доза-эффект" при ADCC, применяемые при расчете фактора Чоу для комбинации MOR208+FLU, представлены на фигуре 2.
Расчеты индекса Чоу (CI) выполняли для того, чтобы определить синергию комбинации антитела к CD19, приводимого в качестве примера, и флударабина по сравнению с MOR208 и FLU в отдельности. Расчеты описаны в Ting-Chao Chou, Theoretical Basis, Experimental Design, and Computerized Simulation of Synergism and Antagonism in Drug Combination Studies, Pharmacol Rev 58:621-681 (2006), включенном посредством ссылки во всей своей полноте, и Chou ТС, Talalay Р, Quantitative analysis of dose-effect relationships: the combined effects of multiple drugs or enzyme inhibitors. Adv Enzyme Regul 22: 27-55 (1984), включенном посредством ссылки во всей своей полноте. Способы по Chou-Talalay осуществляют при помощи способа изоболограмм с CI.
Уравнение медианного эффекта
Модели эффектов ингибитора (например, лекарственного средства) выражаются с помощью уравнения медианного эффекта Fa/Fu=(D/D50)^m, где D означает дозу, Fa и Fu означают доли системы, подвергающиеся и не подвергающиеся воздействию дозы D (Fa+Fu=1); D50 означает дозу, вызывающую медианный эффект (например, IC50, ED50, LD50). Константа т определяет форму кривой зависимости "доза-эффект". Применяли программное обеспечение Excel Fit, чтобы выполнить расчет параметров линейной регрессии для оценки параметров т и D50.
Эффекты комбинации в отношении клеток МЕС-1 измеряли как % гибели клеток, как описано выше. Доля Fu определяется как соотношение % гибели клеток в линии клеток, подвергнутой обработке, и % гибели клеток в линии клеток, подвергнутой воздействию контроля. Иными словами:
Fu=% гибели клеток (линия клеток, подвергнутая обработке)/% гибели клеток (линия клеток, не подвергнутая обработке)
Таким образом, % гибели клеток в линии клеток является константой D50 в уравнении медианного эффекта, которую можно оценить с помощью линейной регрессии, описанной выше.
Способ изоболограмм с CI
Способ изоболограмм с CI обеспечивает количественную оценку синергизма лекарственных препаратов. Показатель аддитивности (CI) оценивают на основании данных о зависимости "доза-эффект" при монотерапии и комбинированном применении лекарственных средств. Значение CI менее 1 указывает на синергизм; CI=1 указывает на аддитивный эффект; и CI>1 указывает на антагонизм. Взаимодействие лекарственных средств (синергизм или антагонизм) тем более явно выражено, чем дальше значение CI отстоит от 1.
Формально, показатель аддитивности (CI) при комбинированном применении лекарственных средств определяют как CI=D1/Dx1+D2/Dx2. Здесь и D2 означают дозы лекарственного средства 1 и лекарственного средства 2 в комбинации, соответственно; a Dx1 и Dx2 означают дозы при лечении только лекарственным средством 1 и только лекарственным средством 2, которые дадут тот же эффект, что и комбинация. Дозы Dx1 и Dx2 должны быть оценены на основании о зависимости "доза-эффект" при монотерапии. По большому счету, уравнение медианного эффекта соответствует данным для каждого лекарственного средства. На основании уравнения медианного эффекта для лекарственного средства можно оценить дозу (т.е. D), необходимую для вызова эффекта (т.е. Fa, Fu). Чем дальше от линии аддитивного взаимодействия находится точка, чем больше разница между CI и 1, тем сильнее эффект (синергический или антагонистический).
Результаты
Как представлено в таблице 2, значения индекса Чоу указывают на отчетливо выраженный синергизм комбинации MOR208 и флударабина при специфическом уничтожении клеток МЕС-1 по сравнению с MOR208 и флударабином в отдельности. Этот вывод основан на расчетах индекса Чоу, составляющего 0,03, 0,3 и 0,3 в каждом из трех экспериментов, соответственно, при среднем значении 0,21, где CI<1 указывает на синергизм. Таким образом, комбинация MOR208 и флударабина также проявляет синергическое поведение при лечении неходжкинской лимфомы (NHL), хронического лимфолейкоза (CLL) и/или острого лимфобластного лейкоза (ALL) у людей.
Чтобы подтвердить результаты вышеприведенных расчетов индекса Чоу, оценивали статистическую значимость нормализованных данных из таблицы 2 при помощи критерия множественного сравнения Бонферрони. См. James, et al, Antibody-mediated B-cell depletion before adoptive immunotherapy with T cells expressing CD20-specific chimeric T-cell receptors facilitates eradication of leukemia in immunocompetent mice, Blood, 114(27):5454-63 (электронная публикация 30 октября 2009 г.), включенный посредством ссылки во всей своей полноте. Результаты представлены в таблице 3.
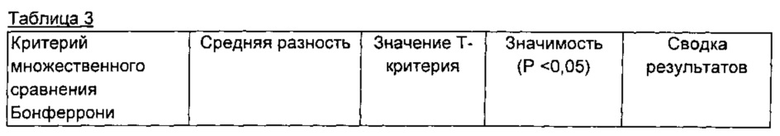
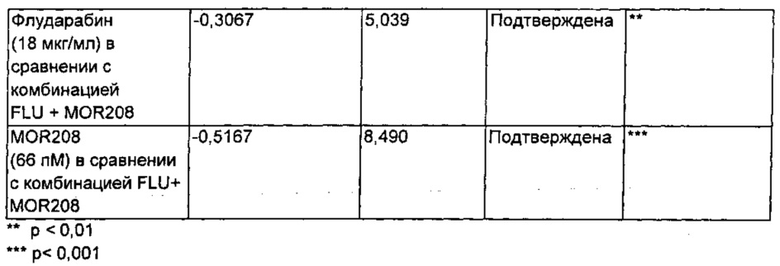
Результаты
Как представлено в таблице 3, критерий множественного сравнения Бонферрони показывает, что комбинированное лечение с помощью FLU+MOR208 является статически более эффективной при специфическом уничтожении клеток МЕС-1, чем лечение при помощи FLU и MOR208 в отдельности.
Пример 2. MOR208 и FLU в отдельности и в комбинации в модели роста опухоли при подкожной (SC) имплантации клеток RAMOS В-клеточной лимфомы Беркитта человека.
Материалы
Клетки RAMOS лимфомы Беркитта человека (№в АТСС CRL-1596, №партии 39531381); контрольное инертное вещество: 0,9% хлорид натрия, 25 мг/мл маннит, pH 7,0; мыши с SCID (Университет Аделаиды, Уэйт Кампус, Аррбрей, Южная Австралия, Австралия, линия C.B.-17-Igh-1b-Prkdcscid).
Способы
Самкам мышей С. В-17 с SCID в возрасте шести-семи недель подкожно имплантировали клетки RAMOS (~5×106 клеток/мышь). Через 14 дней после инокуляции мышей разделили на десять групп по восемь животных в каждой, где каждая группа характеризовалась относительно одинаковыми объемами опухолей. Лечение началось в день 14. Режимы лечения приведены в таблице 4. Продолжительность исследования составляла 63 дня.

MOR208, флударабин и инертное вещество вводили в объеме 0,1 мл/10 г массы тела. Исходным регистрируемым показателем был темп роста опухоли, в частности, объем опухоли в день 38 исследования. Вес опухоли рассчитывали при помощи уравнения (I×w2)/2, где I и w обозначают наибольший и наименьший размеры, данные о которых собирали при каждом измерении.
Результаты представлены в таблице 5, и средние значения изображены на фигуре 6.
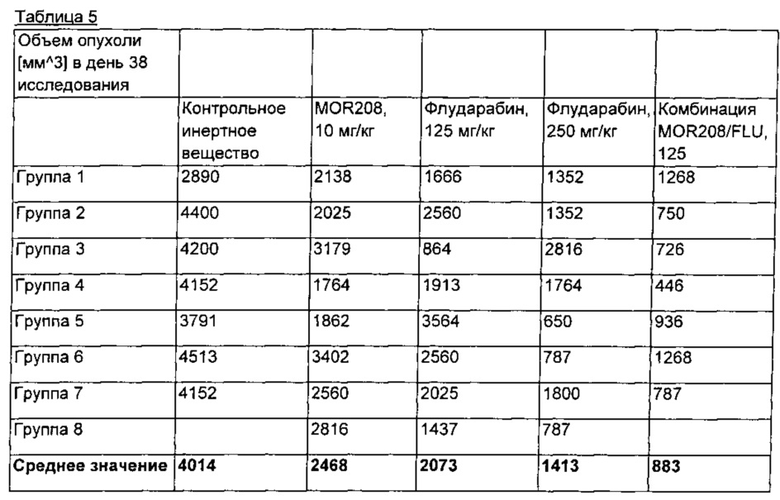
В дополнение к конечному результату для объема опухоли в 38 день исследования оценивали параметры 1) уменьшения темпа роста опухоли [%] в день 38 и 2) увеличения времени, необходимого для достижения объема опухоли, составляющего 4000 мг [%]. Результаты представлены в таблице 6.

Оба конечных результата, представленных в таблице 6, оценивали при помощи метода частичного продукта (FPC), чтобы определить, существует ли синергизм при лечении с помощью комбинации MOR208 и FLU по сравнению с MOR208 и FLU в отдельности. Если эффективность в группе комбинированного лечения превышает таковую по FPC, то синергизм существует.Значение по методу частичного продукта рассчитывали по формуле 1-[(1-А)*(1-В)]=fpc (%), как описано в Webb, J.L. (1963) Enzyme and Metabolic Inhibitors, Academic Press, New York, включенном посредством ссылки во всей своей полноте. После выполнения расчетов значения по FPC полученное значение по FPC и значения из таблицы 6 нормализовали путем установления значения по FPC на 1. Результаты этих расчетов представлены в таблице 7.
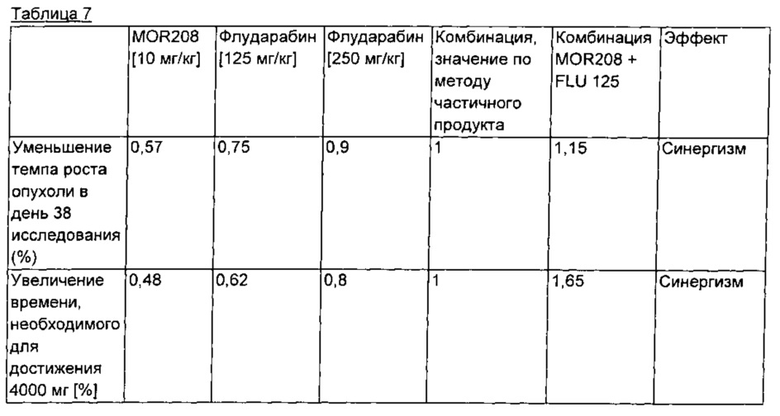
Результаты
Оба конечных результата представляют собой меру ингибирования роста опухоли, и при обоих конечных результатах, уменьшении темпа роста опухоли (%) в день 38 исследования и увеличении времени (%), необходимого для достижения 4000 мг, комбинация MOR208+FLU125 проявляла отчетливо выраженный синергизм по сравнению с MOR208 и FLU125 в отдельности.
Чтобы подтвердить результаты вышеприведенных расчетов значений по FPC, оценивали статистическую значимость данных о среднем объеме опухоли [мм^3] в день 38 исследования (представленных в таблице 5) при помощи критерия множественного сравнения Бонферрони. Результаты представлены в таблице 8.
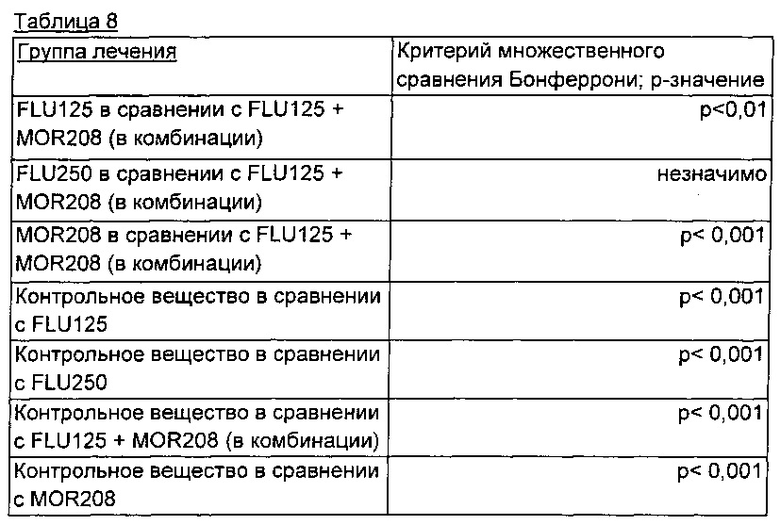
Значение р<0,05 указывает на статистическую значимость. Результаты
Как представлено в таблицах 5 и 6, комбинация MOR208 и флударабина, 125 мг/кг, по всем параметрам была более эффективной в ингибировании роста опухолей in vivo, чем MOR208 или флударабин в отдельности. Было подтверждено, что это увеличение эффективности комбинации MOR208 и флударабина, 125 мг/кг, в ингибировании роста опухоли in vivo по сравнению как с MOR208, так и с флударабином в отдельности является статистически значимым, как представлено в таблице 8. Кроме того, рассчитанное значение по методу частичного продукта показывает отчетливо выраженный синергизм комбинации MOR208 и флударабина, 125 мг/кг, при ингибировании роста опухоли in vivo по сравнению с MOR208 или флударабином в отдельности, как представлено в таблице 7. Таким образом, комбинация MOR208 и флударабина также будет проявлять синергическое поведение при лечении неходжкинской лимфомы (NHL), хронического лимфолейкоза (CLL) и острого лимфобластного лейкоза (ALL) у людей.
В дополнение, комбинация MOR208 и флударабина, 125 мг/кг, была более эффективной в ингибировании роста опухолей in vivo, чем более высокая доза флударабина, 250 мг/кг, в отдельности. Поскольку флударабин продемонстрировал значительные побочные эффекты при более высоких дозах, этот результат показывает, что более безопасной, более эффективной альтернативой высокой дозе флударабина является комбинация MOR208 и флударабина.
Пример 3. MOR208 и флударабин в отдельности и в комбинации в опухолевых клетках RAMOS неходжкинской лимфомы человека у мышей с SCID, модель выживаемости
Материалы
Циклофосфамид (Fluka, Бухс, Швейцария, №партии 07551661); контрольное инертное вещество: 0,9% хлорид натрия, 25 мг/мл маннит, рН 7,0; мыши с SCID (Университет Аделаиды, Уэйт Кампус, Аррбрей, Южная Австралия, Австралия, линия C.B.-17-lgh-1b-Prkdcscid); клетки RAMOS лимфомы человека (№в АТСС CRL-2638).
Способы
Мышей с SCID предварительно обрабатывали циклофосфамидом (18 мг/кг, i.p., два раза в день) в течение двух дней перед инокуляцией клеток RAMOS (день -5 и -4). В день инокуляции (день -3) мышей разделили на десять групп по восемь животных в каждой, и каждой мыши внутривенно инокулировали 1 х 106 клеток RAMOS в хвостовую вену. Режим дозирования для каждой группы представлен в таблице 9, и он вступал в силу в день 0. Продолжительность исследования составляла три недели.

Регистрируемым показателем было медианное время выживания в днях. Чтобы оценить, являлся ли синергическим эффект комбинации по сравнению с таковым в группах лечения отдельными препаратами, применяли способы по Clarke и соавт.
Синергизм по Clarke и соавт.
Способ описан в Issues in experimental design and endpoint analysis in the study of experimental cytotoxic agents in vivo in breast cancer and other models, Breast Cancer Research and Treatment 46:255-278 (1997), включенном посредством ссылки во всей своей полноте.
Данные анализируют следующим образом:
Антагонистический эффект (АВ)/С<(А/С)×(В/С)
Аддитивный эффект (АВ)/С=(А/С)×(В/С)
Синергический эффект (АВ)/С>(А/С)×(В/С)
где А представляет собой лечение с помощью MOR208; В представляет собой лечение с помощью FLU в отдельности; С представляет собой ответ на лечение инертным веществом; АВ представляет собой комбинацию методов лечения А и В. Медианное время выживания в днях для каждой исследуемой группы и анализ по Clarke и соавт. представлены в таблице 10.
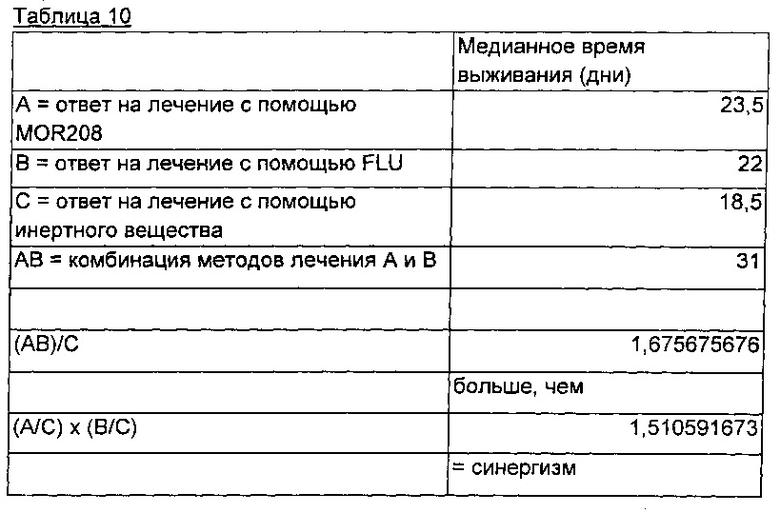
Результаты
Комбинация MOR208 и FLU показала отчетливо выраженный синергизм, определенный по медианной выживаемости, по сравнению с MOR208 и FLU в отдельности.
Чтобы подтвердить результаты вышеприведенных расчетов синергического эффекта, медианное время выживания в днях для комбинации MOR208 и флударабина, 125 мг/кг, сравнили с таковым для MOR208 и флударабина в отдельности при помощи критерия Мантеля-Хензеля [Р-значение] и критерия Гехана-Уилкоксона [Р-значение]. Результаты представлены в таблице 11.

Результаты
В таблице 10 показано, что комбинация MOR208 и флударабина, 125 мг/кг,
синергически увеличивала медианное время выживания в модели лимфомы Беркитта на мышах с SCID по сравнению как с MOR208, так и с флударабином в отдельности. Было подтверждено, что это увеличение медианного времени выживания для комбинации MOR208 и флударабина, 125 мг/кг, in vivo по сравнению как с MOR208, так и с флударабином в отдельности является статистически значимым, как показано в таблице 11. Таким образом, комбинация MOR208 и флударабина будет также проявлять синергическое поведение при лечении неходжкинской лимфомы (NHL), хронического лимфолейкоза (CLL) и острого лимфобластного лейкоза (ALL) у людей.
В дополнение, комбинация MOR208 и флударабина, 125 мг/кг, была более эффективной в увеличении медианного времени выживания in vivo, чем более высокая доза флударабина, 250 мг/кг, в отдельности. Поскольку флударабин продемонстрировал значительные побочные эффекты при более высоких дозах, несмотря на его эффективность, этот результат показывает, что более безопасной, более эффективной альтернативой высокой дозе флударабина является комбинация MOR208 и флударабина.
Следует понимать, что описание, конкретные примеры и данные, хотя и указывают на иллюстративные варианты осуществления, предоставлены с целью иллюстрации и не предназначены для ограничения настоящего изобретения. Различные изменения и модификации в пределах настоящего изобретения станут очевидными для специалиста в данной области из обсуждения, раскрытия и данных, содержащихся в данном документе, и, таким образом, считаются частью настоящего изобретения.




Изобретение относится к области биохимии, в частности к применению антитела, специфичного к CD19 и флударабина для получения синергетической комбинации для лечения неходжкинской лимфомы, хронического лимфоцитарного лейкоза и/или острого лимфобластного лейкоза. Изобретение позволяет эффективно лечить неходжкинскую лимфому, хронический лимфоцитарный лейкоз и/или острый лимфобластный лейкоз. 6 з.п. ф-лы, 7 ил., 11 табл., 3 пр.
1. Применение антитела, специфичного к CD19 и содержащего HCDR1-участок, включающий последовательность SYVMH (SEQ ID NO: 1), HCDR2-участок, включающий последовательность NPYNDG (SEQ ID NO: 2), HCDR3-участок, включающий последовательность GTYYYGTRVFDY (SEQ ID NO: 3), LCDR1-участок, включающий последовательность RSSKSLQNVNGNTYLY (SEQ ID NO: 4), LCDR2-участок, включающий последовательность RMSNLNS (SEQ ID NO: 5), и LCDR3-участок, включающий последовательность MQHLEYPIT (SEQ ID NO: 6), и флударабина для получения синергетической комбинации для лечения неходжкинской лимфомы, хронического лимфоцитарного лейкоза и/или острого лимфобластного лейкоза.
2. Применение по п. 1, где антитело содержит вариабельный домен тяжелой цепи с последовательностью EVQLVESGGGLVKPGGSLKLSCAASGYTFTSYVMHWVRQAPGKGLEWIGYINPYNDGTKYNEKFQGRVTISSDKSISTAYMELSSLRSEDTAMYYCARGTYYYGTRVFDYWGQGTLVTVSS (SEQ ID NO: 10) и вариабельный домен легкой цепи с последовательностью DIVMTQSPATLSLSPGERATLSCRSSKSLQNVNGNTYLYWFQQKPGQSPQLLIYRMSNLNSGVPDRFSGSGSGTEFTLTISSLEPEDFAVYYCMQHLEYPITFGAGTKLEIK (SEQ ID NO: 11).
3. Применение по п. 1, где антитело содержит константный домен тяжелой цепи с последовательностью
ASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPDVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTFRVVSVLTVVHQDWLNGKEYKCKVSNKALPAPEEKTISKTKGQPREPQVYTLPPSREEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPMLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK (SEQ ID NO: 12).
4. Применение по п. 1, где указанное антитело, специфичное к CD19, и флударабин вводятся раздельно.
5. Применение по п. 1, где флударабин вводится перед введением антитела, специфичного к CD19.
6. Применение по п. 1, где комбинация способна опосредовать уничтожение клеток МЕС-1 благодаря ADCC в присутствии выделенных РВМС человека при эффективности, по меньшей мере в два раза лучшей, чем таковая для флударабина в отдельности.
7. Применение по любому из пп. 1-6 в лечении неходжкинской лимфомы, отличающееся тем, что неходжкинская лимфома выбрана из группы, состоящей из фолликулярной лимфомы, мелкоклеточной лимфоцитарной лимфомы, лимфомы из лимфоидной ткани, ассоциированной со слизистыми оболочками, лимфомы маргинальной зоны, диффузной крупноклеточной В-клеточной лимфомы, лимфомы Беркитта и мантийноклеточной лимфомы.
| US 2010272723 A1, 28.10.2010 | |||
| HORTON H.M | |||
| et al., Potent In vitro and In vivo Activity of an Fc-Engineered Anti-CD19 Monoclonal Antibody against Lymphoma and Leukemia, Cancer Research, 2008, Vol.68, N | |||
| Способ изготовления электрических сопротивлений посредством осаждения слоя проводника на поверхности изолятора | 1921 |
|
SU19A1 |
| Комбинированный котел | 1925 |
|
SU4107A1 |
| US 2011165152 A1, 07.07.2011. | |||
Авторы
Даты
2018-08-17—Публикация
2012-08-14—Подача