В целом изобретение относится к соединениям 5-азаиндазола для лечения расстройств, опосредованных ингибиторами киназы Pim (Pim-1, Pim-2 и/или Pim-3), таким образом полезным в качестве терапевтических средств от рака. Изобретение также относится к композициям, а именно фармацевтическим композициям, включающим эти соединения, и способам применения их, отдельно или в сочетании, для лечения разных форм рака и гиперпролиферативных заболеваний, а также способам применения соединений в in vitro, in situ и in vivo диагностике или лечении клеток млекопитающих или связанных патологических состояний.
Киназы Pim представляют собой семейство трех в высокой степени связанных серии и треонин протеинкиназ, кодированных генами Pim-1, Pim-2 и Pim-3. Названия генов происходят от фразы Proviral Insertion, Moloney, частых сайтов интеграции для вируса мышиной лейкемии Молони, где включения приводят к сверхэкспрессии киназ Pim и либо впервые обнаруженных Т-клеточных лимфом, либо сильному ускорению онкогенеза на трансгенной модели Мус-обусловленной лимфомы (Cuypers et al. (1984) Cell, vol. 37 (1) pp. 141-50; Selten et al. (1985) EMBO J. vol. 4 (7) pp. 1793-8; van der Lugt et al. (1995) EMBO J. vol. 14 (11) pp. 2536-44; Mikkers et al. (2002) Nature Genetics, vol. 32 (1) pp. 153-9; van Lohuizen et al. (1991) Cell, vol. 65 (5) pp. 737-52). Эти эксперименты демонстрируют синергизм с онкогеном с-Мус и указывают на то, что ингибирование киназ Pim может приносить терапевтическую пользу.
Мышиная генетика подтверждает, что противодействующие киназы Pim могут иметь приемлемый профиль безопасности; мышиный нокаут Pim 1 -/-; Pim-2 -/-, Pim-3 -/- является жизнеспособным, хотя немного меньше, чем у однопометных животных дикого типа (Mikkers et al. (2004) Mol Cell Biol vol. 24 (13) pp. 6104-154). Три гена дают начало шести изоформам белка, включая домен протеинкиназ, и очевидно без различимых регулирующих доменов. Все шесть изоформ являются постоянно активными протеинкиназами, которые не требуют посттрансляционной модификации активности, таким образом киназы Pim регулируются главным образом на транскрипционном уровне (Qian et al. (2005) J Biol Chem, vol. 280 (7) pp. 6130-7). Экспрессия киназы Pim является высоко индуцируемой цитокинами и рецепторами фактора роста, и Pims представляют собой непосредственные транскрипционые мишени белков Stat, включая Stat3 и Stat5. Например Pim-1Необходим для др130-опосредованного сигнала пролиферации Stat3 (Aksoy et al. (2007) Stem Cells, vol. 25 (12) pp. 2996-3004; Hirano et al. (2000) Oncogene vol. 19 (21) pp. 2548-56; Shirogane et al. (1999) Immunity vol. 11 (6) pp. 709-19).
Киназы Pim действуют на клеточную пролиферацию и пути существования параллельно PI3k/Akt/mTOR сигнальной оси (Hammerman et al. (2005) Blood vol. 105 (11) pp. 4477-83). В действительности некоторые мишени фосфорилирования оси PI3k, включая Bad и elF4E-BP1, являются регуляторами роста клеток и апоптоза и также представляют собой мишени фосфорилирования киназ Pim (Fox et al. (2003) Genes Dev vol. 17 (15) pp. 1841-54; Macdonald et al. (2006) Cell Biol vol. 7 pp. 1; Aho et al. (2004) FEBS Letters vol. 571 (1-3) pp. 43-9; Tamburini et al. (2009) Blood vol. 114 (8) pp. 1618-27). Киназа Pim может воздействовать на клеточное выживание, поскольку фосфорилирование Bad увеличивает активность Bcl-2 и, следовательно, активирует клеточное выживание. Подобным образом фосфорилирование elF4E-BP1 под действием mTOR или киназ Pim вызывает ослабление elF4E, активируя трансляцию мРНК и клеточный рост. Кроме того, установлено, что Pim-1 активирует развитие клеточного цикла через фосфорилирование CDC25A, р21 и Cdc25C (Mochizuki et al. (1999) J Biol Chemvol. 274 (26) pp. 18659-66; Bachmann et al. (2006) Int J Biochem Cell Biol vol. 38 (3) pp. 430-43; Wang et al. (2002) Biochim Biophys Acta vol. 1593 (1) pp. 45-55).
Киназы Pim демонстрируют синергизм на моделях трансгенных мышей с с-Мус-обусловленными и Akt-обусловленными опухолями (Verbeek et al. (1991) Mol Cell Biol vol. 11 (2) pp. 1176-9; Allen et al. Oncogene (1997) vol. 15 (10) pp. 1133-41; Hammerman et al. (2005) Blood vol. 105 (11) pp. 4477-83). Киназы Pim включены в трансформирующую активность онкогенов, установленных при остром миелобластном лейкозе (ОМЛ), включая Flt3-ITD, BCR-abl и Tel-Jak2. Экспрессия этих онкогенов в клетках BaF3 приводит к повышающей регуляции экспрессии Pim-1 и Pim-2, вызывающей независимый рост IL-3, и последующее ингибирование Pim приводит к апоптозу и угнетению роста клеток (Adam et al. (2006) Cancer Research 66 (7):3828-35). Также сверхэкспрессия и дисрегуляция Pim упоминаются в качестве частого явления при многих гемопоэтических раках, включая лейкозы и лимфомы (Amson et al. (1989) Proc Natl Acad Sci USA 86 (22):8857-61); Cohen et al. (2004) Leuk Lymphoma 45 (5):951-5; Huttmann et al. (2006) Leukemia 20 (10): 1774-82), а также множественную миелому (Claudio et al. (2002) Blood 100 (6):2175-86). Было показано, что Pim 1 сверхэкспрессирован и коррелирует с развитием рака предстательной железы (Cibull et al. (2006) J Clin Pathol 59 (3):285-8; Dhanasekaran et al. (2001) Nature vol. 412 (6849):822-6). Экспрессия Pim 1 увеличивается в мышиных моделях с развитием заболевания (Kim et al. (2002) Proc Natl Acad Sci USA 99 (5):2884-9). Сообщалось, что Pim-1 представляет собой наиболее сверхэкспрессированную мРНК в подгруппе образцов опухоли предстательной железы человека, которые имеют с-Мус-обусловленную генную сигнатуру (Ellwood-Yen et al. (2003) Cancer Cell 4(3):223-38). Также было показано, что Pim-3 сверхэкспрессирован и выполняет функциональную роль при раке поджелудочной железы и гепатоцеллюлярной карциноме (Li et al. (2006) Cancer Research 66 (13):6741-7; Fujii et al. (2005) Int J Cancer 114 (2):209-18).
Кроме терапевтических и диагностических применений в онкологии, киназы Pim могут играть роль в нормальной функции иммунной системы, и ингибирование Pim может быть лечебным для ряда разных иммунологических патологий, включая воспалительные, аутоиммунные состояния, аллергию и угнетение иммунитета при трансплантации органа (Aho et al. (2005) Immunology 116 (1):82-8).
Изобретение относится к соединениям 5-азаиндазола для лечения заболеваний, опосредованных соединениями формулы I ингибиторов киназы Pim (Pim-1, Pim-2 и/или Pim-3).
Соединения формулы I имеют структуру пиразоло[4,3-с]пиридина (5-азаиндазола):
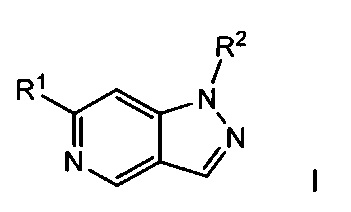
и их стереоизомеры, геометрические изомеры, таутомеры и фармацевтически приемлемые соли. Разные заместители, включая R1 и R2, являются такими, как определено в этом документе.
Одним аспектом изобретения является фармацевтическая композиция, включающая соединение формулы I и фармацевтически приемлемый носитель, скользящее вещество, разбавитель или эксципиент. Кроме того, фармацевтическая композиция может включать химиотерапевтическое средство.
Изобретение включает способ лечения заболевания или расстройства, опосредованного киназой Pim, согласно которому вводят терапевтически эффективное количество соединения формулы I пациенту с заболеванием или расстройством, выбранным из рака, иммунологических нарушений, сердечнососудистого заболевания, вирусной инфекции, воспаления, расстройств обмена веществ / эндокринной функции и неврологических нарушений. Кроме того, согласно способу вводят дополнительный терапевтический агент, выбранный из химиотерапевтического средства, противовоспалительного агента, иммуномодулирующего средства, нейротропного фактора, средства для лечения сердечно-сосудистого заболевания, средства для лечения заболевания печени, противовирусного вещества, средства для лечения заболеваний крови, средства для лечения диабета и средства для лечения иммунодефицитных состояний.
Изобретение включает применение соединения формулы I при изготовлении лекарства для лечения рака, иммунологических нарушений, сердечно-сосудистого заболевания, вирусной инфекции, воспаления, расстройств обмена веществ / эндокринной функции и неврологических нарушений, где лекарство опосредует киназу Pim.
Изобретение включает набор для лечения состояния, опосредованного киназой Pim, содержащий: а) первую фармацевтическую композицию, включающую соединение формулы I; и b) инструкции по применению.
Изобретение включает соединение формулы I для применения в качестве лекарства и для применения в лечении заболевания или расстройства, выбранного из рака, иммунологических нарушений, сердечно-сосудистого заболевания, вирусной инфекции, воспаления, расстройств обмена веществ / эндокринной функции и неврологических нарушений, и опосредованного киназой Pim.
Изобретение включает способы получения соединения формулы I.
Теперь подробно будет сделана ссылка на конкретные воплощения изобретения, примеры которых проиллюстрированы в прилагаемых структурах и формулах. Хотя изобретение будет описано вместе с перечисленными воплощениями, подразумеваться, что они не ограничивают изобретение до этих воплощений. Наоборот, подразумевается, что изобретение охватывает все альтернативы, модификации и эквиваленты, которые могут быть включены в объем настоящего изобретения, как определено формулой изобретения. Квалифицированный специалист в данной области техники определит многие способы и вещества, подобные или эквивалентные тем, что описаны в этом документе, которые могут быть использованы при применении настоящего изобретения. Настоящее изобретение никоим образом не ограничено описанными способами и веществами. В том случае, если одна или более включенных публикаций, патентов и подобных материалов отличаются или противоречат этой заявке, включая, но не ограничиваясь этим, определяемые термины, использование терминов, описанные методики или подобное, данная заявка имеет преимущество. Если не указано иное, то все технические и научные термины, используемые в этом документе, имеют такие же 3Начения, которые обычно понимает под ними один из специалистов в области техники, к которой данное изобретение относится. Несмотря на то, что способы и вещества, подобные или эквивалентные тем, что описаны в этом документе, можно использовать на практике или проверяя изобретение, ниже описаны подходящие способы и вещества. Все публикации, заявки на патент, патенты и другие ссылочные материалы, упомянутые в этом документе, включены в него полностью путем ссылки на них. Используемая в данной заявке номенклатура основывается на систематической номенклатуре ИЮПАК, если не указано иное.
При указании числа заместителей термин "один или более чем один" относится к диапазону от одного заместителя до максимально возможного числа замещений, т.е. замены одного водорода вплоть до замены всех водородов заместителями. Термин "заместитель" обозначает атом или группу атомов, замещающую атом водорода в исходной молекуле. Термин "замещенный" обозначает, что определенная группа несет один или более чем один заместитель. Когда группа может иметь несколько заместителей и определен ряд возможных заместителей, тогда заместители выбирают независимо, и не обязательно они будут одинаковыми. Термин "незамещенный" означает, что определенная группа не имеет заместителей. Термин "возможно замещенный" означает, что определенная группа не замещена или замещена одним или более чем одним заместителем, независимо выбранным из группы возможных заместителей. При указании числа заместителей термин "один или более чем один" означает от одного заместителя до максимально возможного числа замещений, т.е. замены одного водорода или более чем одного, так, например, двух, трех или четырех, включая замещение всех водородов заместителями.
Термин "алкил", как используется в этом документе, относится к насыщенному линейному или разветвленному одновалентному углеводородному радикалу от одного до двенадцати атомов углерода (C1-C12), где алкильный радикал возможно независимо замещен одним или более чем одним заместителем, описанным ниже. В другом воплощении алкильный радикал имеет от одного до восьми атомов углерода (С1-С8) или от одного до шести атомов углерода (C1-С6). Примеры алкильных групп включают, но не ограничиваются этим, метил (Me, -СН3), этил (Et, -СН2СН3), 1-пропил (n-Рr, н-пропил, -СН2СН2СН3), 2-пропил (i-Pr, изопропил, -СН(СН3)2), 1-бутил (n-Bu, н-бутил, -СН2СН2СН2СН3), 2-метил-1-пропил (i-Bu, изобутил, -СН2СН(СН3)2), 2-бутил (s-Bu, втор-бутил, -СН(СН3)СН2СН3), 2-метил-2-пропил (t-Bu, трет-бутил, -С(СН3)3), 1-пентил (н-пентил, -СН2СН2СН2СН2СН3), 2-пентил (-СН(СН3)СН2СН2СН3), 3-пентил (-СН(СН2СН3)2), 2-метил-2-бутил (-С(СН3)2СН2СН3), 3-метил-2-бутил (-СН(СН3)СН(СН3)2), 3-метил-1-бутил (-СН2СН2СН(СН3)2), 2-метил-1-бутил (-СН2СН(СН3)СН2СН3), 1-гексил (-СН2СН2СН2СН2СН2СН3), 2-гексил (-СН(СН3)СН2СН2СН2СН3), 3-гексил (-СН(СН2СН3)(СН2СН2СН3)), 2-метил-2-пентил (-С(СН3)2СН2СН2СН3), 3-метил-2-пентил (-СН(СН3)СН(СН3)СН2СН3), 4-метил-2-пентил (-СН(СН3)СН2СН(СН3)2), 3-метил-3-пентил (-С(СН3)(СН2СН3)2), 2-метил-3-пентил (-СН(СН2СН3)СН(СН3)2), 2,3-диметил-2-бутил (-С(СН3)2СН(СН3)2), 3,3-диметил-2-бутил (-СН(СН3)С(СН3)3, 1-гептил, 1-октил и подобные.
Термин "алкилен", как используется в этом документе, относится к насыщенному линейному или разветвленному двухвалентному углеводородному радикалу от одного до двенадцати атомов углерода (С1-С12), где радикал алкилена возможно независимо замещен одним или более чем одним заместителем, описанным ниже. В другом воплощении радикал алкилена имеет от одного до восьми атомов углерода (C1-C8) или от одного до шести атомов углерода (C1-С6). Примеры алкиленовых групп включают, но не ограничиваются этим, метилен (-СН2-), этилен (-СН2СН2-), пропилен (-СН2СН2СН2-) и подобные.
Термин "алкенил" относится к линейному или разветвленному одновалентному углеводородному радикалу от двух до восьми атомов углерода (С2-С8) с по меньшей мере одним центром ненасыщенности, т.е. углерод-углерод, sp2 двойной связью, где радикал алкенила возможно независимо замещен одним или более чем одним заместителем, описанным в этом документе, и включает радикалы, имеющие "цис" и "транс" конфигурации, или альтернативно "Е" и "Z" конфигурации. Примеры включают, но не ограничиваются этим, этиленил или винил (-СН=СН2), аллил (-СН2СН=СН2) и подобные.
Термин "алкенилен" относится к линейному или разветвленному двухвалентному углеводородному радикалу от двух до восьми атомов углерода (С2-С8) с по меньшей мере одним центром ненасыщенности, т.е. углерод-углерод, sp2 двойной связью, где радикал алкенилена возможно независимо замещен одним или более чем одним заместителем, описанным в этом документе, и включает радикалы, имеющие "цис" и "транс" конфигурации, или альтернативно "Е" и "Z" конфигурации. Примеры включают, но не ограничиваются этим, этиленилен или винилен (-СН=СН-), аллил (-СН2СН=СН-) и подобные.
Термин "алкинил" относится к линейному или разветвленному одновалентному углеводородному радикалу от двух до восьми атомов углерода (С2-С8) с по меньшей мере одним центром ненасыщенности, т.е. углерод-углерод, sp тройной связью, где радикал алкинила возможно независимо замещен одним или более чем одним заместителем, описанным в этом документе. Примеры включают, но не ограничиваются этим, этинил (-С≡СН), пропинил (пропаргил, -СН2С≡СН) и подобные.
Термин "алкинилен" относится к линейному или разветвленному двухвалентному углеводородному радикалу от двух до восьми атомов углерода (С2-С8) с по меньшей мере одним центром ненасыщенности, т.е. углерод-углерод, sp тройной связью, где радикал алкинилена возможно независимо замещен одним или более чем одним заместителем, описанным в этом документе. Примеры включают, но не ограничиваются этим, этинилен (-С≡С-), пропинилен (пропаргилен, -СН2С≡С-) и подобные.
Термины "карбоцикл", "карбоциклил", "карбоциклическое кольцо" и "циклоалкил" относятся к одновалентному неароматическому насыщенному или частично ненасыщенному кольцу, имеющему от 3 до 12 атомов углерода (С3-С12) в виде моноциклического кольца, или от 7 до 12 атомов углерода в виде бициклического кольца. Бициклические карбоциклы, имеющие от 7 до 12 атомов, могут быть классифицированы, например, как бицикло [4,5], [5,5], [5,6] или [6,6] система, и бициклические карбоциклы, имеющие 9 или 10 кольцевых атомов, могут быть классифицированы как бицикло [5,6] или [6,6] система, или как мостиковые системы, такие как бицикло[2.2.1]гептан, бицикло[2.2.2]октан и бицикло[3.2.2]нонан. Также в объем данного определения включены спиро-группировки. Примеры моноциклических карбоциклов включают, но не ограничиваются этим, циклопропил, циклобутил, циклопентил, 1-циклопент-1-енил, 1-циклопент-2-енил, 1-циклопент-3-енил, циклогексил, 1-циклогекс-1-енил, 1-циклогекс-2-енил, 1-циклогекс-3-енил, циклогексадиенил, циклогептил, циклооктил, циклононил, циклодецил, циклоундецил, циклододецил и подобные. Группы карбоциклила возможно независимо замещены одним или более чем одним заместителем, описанным в этом документе.
"Арил" означает одновалентный ароматический углеводородный радикал с 6-20 атомами углерода (С6-С20), полученный при удалении одного атома водорода от одного атома углерода исходной ароматической кольцевой системы. Некоторые арильные группы изображены в примерных структурах в виде "Аr". Арил включает бициклические радикалы, содержащие ароматическое кольцо, конденсированное с насыщенным, частично ненасыщенным кольцом или ароматическим карбоциклическим кольцом. Типичные арильные группы включают, но не ограничиваются этим, радикалы, полученные из бензола (фенил), замещенных бензолов, нафталина, антрацена, бифенила, инденила, инданила, 1,2-дигидронафталина, 1,2,3,4-тетрагидронафтила и подобные.
Арильные группы возможно независимо замещены одним или более чем одним заместителем, описанным в этом документе.
"Арилен" означает двухвалентный ароматический углеводородный радикал с 6-20 углеродными атомами (С6-С20), полученный при удалении двух атомов водорода от двух атомов углерода исходной ароматической кольцевой системы. Некоторые группы арилена изображены в примерных структурах в виде "Аr". Арилен включает бициклические радикалы, содержащие ароматическое кольцо, конденсированное с насыщенным, частично ненасыщенным кольцом или ароматическим карбоциклическим кольцом. Обычные группы арилена включают, но не ограничиваются этим, радикалы, полученные из бензола (фенилен), замещенных бензолов, нафталина, антрацена, бифенилена, инденилена, инданилена, 1,2-дигидронафталина, 1,2,3,4-тетрагидронафтила и подобных. Группы арилена возможно замещены одним или более чем одним заместителем, описанным в этом документе.
Термины "гетероцикл", "гетероциклил" и "гетероциклическое кольцо" используются в этом документе взаимозаменяемо и относятся к насыщенному или частично ненасыщенному (т.е. имеющему одну или более чем одну двойную и/или тройную связь внутри кольца) карбоциклическому радикалу от 3 до приблизительно 20 кольцевых атомов, в котором по меньшей мере один кольцевой атом представляет собой гетероатом, выбранный из азота, кислорода, фосфора и серы, оставшиеся кольцевые атомы представляют собой С, где один или более кольцевых атомов возможно независимо замещены одним или более чем одним заместителем, описанным ниже. Гетероцикл может представлять собой моноцикл, имеющий от 3 до 7 кольцевых членов (2 до 6 атомов углерода и 1 до 4 гетероатомов, выбранных из N, О, Р. и S) или бицикл, имеющий от 7 до 10 кольцевых членов (4 до 9 атомов углерода и 1 до 6 гетероатомов, выбранных из N, О, Р и S), например: бицикло [4,5], [5,5], [5,6] или [6,6] система. Гетероциклы описаны в Paquette, Leo A.; "Principles of Modern Heterocyclic Chemistry" (W.A. Benjamin, New York, 1968), особенно Главы 1, 3, 4, 6, 7 и 9; "The Chemistry of Heterocyclic Compounds, A series of Monographs" (John Wiley & Sons, New York, 1950 по наст, время), в частности Тома 13, 14, 16, 19 и 28; и J. Am. Chem. Soc. (1960) 82:5566. Также "гетероциклил" включает радикалы, где радикалы гетероцикла конденсированы с насыщенным, частично ненасыщенным кольцом или ароматическим карбоциклическим или гетероциклическим кольцом. Примеры гетероциклических колец включают, но не ограничиваются этим, морфолин-4-ил, пиперидин-1-ил, пиперазинил, пиперазин-4-ил-2-он, пиперазин-4-ил-3-он, пирролидин-1-ил, тиоморфолин-4-ил, 8-диоксотиоморфолин-4-ил, азокан-1-ил, азетидин-1-ил, октагидропиридо[1,2-а]пиразин-2-ил, [1,4]диазепан-1-ил, пирролидинил, тетрагидрофуранил, дигидрофуранил, тетрагидротиенил, тетрагидропиранил, дигидропиранил, тетрагидротиопиранил, пиперидине-, морфолино, тиоморфолино, тиоксанил, гомопиперазинил, азетидинил, оксетанил, тиетанил, гомопиперидинил, оксепанил, тиепанил, оксазепинил, диазепинил, тиазепинил, 2-пирролинил, 3-пирролинил, индолинил, 2Н-пиранил, 4Н-пиранил, диоксанил, 1,3-диоксоланил, пиразолинил, дитианил, дитиоланил, дигидротиенил, пиразолидинилимидазолинил, имидазолидинил, 3-азабицикло[3.1.0]гексанил, 3-азабицикло[4.1.0]гептанил, азабицикло[2.2.2]гексанил, 3Н-индолил хинолизинил и N-пиридилмочевины. Также спиро-группировки включены в объем данного определения. Примеры гетероциклической группы, где 2 кольцевых атома замещены оксо (=O) группировками, представляют собой пиримидинонил и 1,1-диоксо-тиоморфолинил. Группы гетероцикла в данном документе возможно независимо замещены одним или более чем одним заместителем, описанным в этом документе.
Термин "гетероарил" относится к одновалентному ароматическому радикалу из 5-, 6- или 7-членных колец и включает конденсированные кольцевые системы (по меньшей мере одна из которых ароматическая) с 5-20 атомами, содержащие один или более чем один гетероатом, независимо выбранный из азота, кислорода и серы. Примерами гетероарильных групп являются пиридинил (включая например 2-гидроксипиридинил), имидазолил, имидазопиридинил, пиримидинил (включая например 4-гидроксипиримидинил), пиразолил, триазолил, пиразинил, тетразолил, фурил, тиенил, изоксазолил, тиазолил, оксадиазолил, оксазолил, изотиазолил, пирролил, хинолинил, изохинолинил, тетрагидроизохинолинил, индолил, бензимидазолил, бензофуранил, циннолинил, индазолил, индолизинил, фталазинил, пиридазинил, триазинил, изоиндолил, птеридинил, пуринил, оксадиазолил, триазолил, тиадиазолил, тиадиазолил, фуразанил, бензофуразанил, бензотиофенил, бензотиазолил, бензоксазолил, хиназолинил, хиноксалинил, нафтиридинил и фуропиридинил. Гетероарильные группы возможно независимо замещены одним или более чем одним заместителем, описанным в этом документе.
Группы гетероцикла или гетероарила могут быть углерод (углерод-соединенные) или азот (азот-соединенные) связанными, когда такое возможно. Например и без ограничения углерод-связанные гетероциклы или гетероарилы связаны в положении 2, 3, 4, 5 или 6 пиридина, положении 3, 4, 5 или 6 пиридазина, положении 2, 4, 5 или 6 пиримидина, положении 2, 3, 5 или 6 пиразина, положении 2, 3, 4 или 5 фурана, тетрагидрофурана, тиофурана, тиофена, пиррола или тетрагидропиррола, положении 2, 4 или 5 оксазола, имидазола или тиазола, положении 3, 4 или 5 изоксазола, пиразола или изотиазола, положении 2 или 3 азиридина, положении 2, 3 или 4 азетидина, положении 2, 3, 4, 5, 6, 7 или 8 хинолина или положении 1, 3, 4, 5, 6, 7 или 8 изохинолина.
Например и без ограничения азот-связанные гетероциклы или гетероарилы связаны в положении 1 азиридина, азетидина, пиррола, пирролидина, 2-пирролина, 3-пирролина, имидазола, имидазолидина, 2-имидазолина, 3-имидазолина, пиразола, пиразолина, 2-пиразолина, 3-пиразолина, пиперидина, пиперазина, индола, индолина, 1Н-индазола, положении 2 изоиндола или изоиндолина, положении 4 морфолина и положении 9 карбазола или В-карболина.
Термины "лечить" и "лечение" относятся как к терапевтическому лечению, так и профилактическим или предупредительным мерам, когда у объекта должно быть предотвращено или замедлено (уменьшено) нежелательное физиологическое изменение или заболевание, такое как развитие или распространение рака. Применительно к этому изобретению полезные или желательные клинические результаты включают, но не ограничиваются этим, облегчение симптомов, снижение степени заболевания, стабилизированное (т.е. не ухудшающееся) состояние заболевания, задержку или замедление развития болезни, улучшение или временное облегчение болезненного состояния и ремиссию (либо частичную, либо полную), либо поддающиеся обнаружению, либо не обнаруживаемые. Также "лечение" может означать продление жизни по сравнению с предполагаемой продолжительностью жизни, если лечения не было. Нуждающиеся в лечении включают тех, у кого уже есть состояние или заболевание, а также тех, кто предрасположен к состоянию или заболеванию, или тех, у кого состояние или заболевание следует предотвратить.
Фраза "терапевтически эффективное количество" означает количество соединения по настоящему изобретению, которое (1) лечит или предотвращает конкретное заболевание, состояние или расстройство, (2) ослабляет, улучшает или устраняет один или более симптомов конкретного заболевания, состояния или расстройства, или (3) предотвращает или замедляет наступление одного или более симптомов конкретного заболевания, состояния или расстройства, описанных в этом документе. В случае рака терапевтически эффективное количество лекарства может уменьшать количество раковых клеток; уменьшать размер опухоли; ингибировать (т.е. замедлять до некоторой степени и предпочтительно останавливать) проникновение раковых клеток в периферические органы; ингибировать (т.е. замедлять до некоторой степени и предпочтительно останавливать) метастаз опухоли; ингибировать до некоторой степени рост опухоли; и/или облегчать до некоторой степени один или более симптомов, связанных с раком. В тех случаях, когда лекарство может предотвращать рост и/или убивать существующие раковые клетки, оно может быть цитостатическим и/или цитотоксическим. При лечении рака эффективность поддается измерению, например, при оценке времени до прогрессирования заболевания (ТТР от time to disease progression) и/или определении частоты ответа (RR от response rate).
Термин "рак" относится или описывает физиологическое состояние у млекопитающих, которое обычно характеризуется нерегулируемым ростом клеток. "Опухоль" включает один или более чем один вид раковых клеток. Примеры рака включают, но не ограничиваются этим, карциному, лимфому, бластому, саркому и лейкоз или лимфонеоплазии. Более определенные примеры подобных раков включают плоскоклеточный рак (например эпителиальный плоскоклеточный рак), рак легкого, включая мелкоклеточный рак легкого, немелкоклеточный рак легкого ("НМРЛ"), аденокарциному легкого и сквамозную карциному легкого, рак брюшной полости, гепатоцеллюлярный рак, желудочный рак или рак желудка, включая рак желудочно-кишечного тракта, рак поджелудочной железы, глиобластому, рак шейки матки, рак яичников, рак печени, рак мочевого пузыря, гепатому, рак молочной железы, рак толстой кишки, рак прямой кишки, колоректальный рак, эндометриальную или маточную карциному, карциному слюнных желез, рак почки или почечный рак, рак предстательной железы, рак вульвы, рак щитовидной железы, печеночную карциному, карциному анального канала, карциному полового члена, а также рак головы и шеи.
"Химиотерапевтическое средство" представляет собой химическое соединение, полезное в лечении рака независимо от механизма действия. Виды химиотерапевтических средств включают, но не ограничиваются этим: алкилирующие агенты, антиметаболиты, растительные алкалоиды веретенного яда, цитотоксические/противоопухолевые антибиотики, ингибиторы топоизомеразы, антитела, фотосенсибилизаторы и ингибиторы киназы. Химиотерапевтические средства включают соединения, используемые в "таргетной терапии" и традиционной химиотерапии. Примеры химиотерапевтических средств включают: эрлотиниб (TARCEVA®, Genentech/OSI Pharm.), доцетаксел (TAXOTERE®, Sanofi-Aventis), 5-FU (фторурацил, 5-фторурацил, CAS №51-21-8), гемцитабин (GEMZAR®, Lilly), PD-0325901 (CAS №391210-10-9, Pfizer), цисплатин (цис-диамин, дихлорплатина (II), CAS №15663-27-1), карбоплатин (CAS №41575-94-4), паклитаксел (TAXOL®, Bristol-Myers Squibb Oncology, Princeton, N.J.), трастузумаб (HERCEPTIN®, Genentech), темозоломид (4-метил-5-оксо-2,3,4,6,8-пентазабицикло[4.3.0]нона-2,7,9-триен-9-карбоксамид, CAS №85622-93-1, TEMODAR®, TEMODAL®, Schering Plough), тамоксифен ((Z)-2-[4-(1,2-дифенилбут-1-енил)фенокси]-N,N-диметилэтанамин, NOLVADEX®, ISTUBAL®, VALODEX®) и доксорубицин (ADRIAMYCIN®), Akti-1/2, HPPD и рапамицин.
Больше примеров химиотерапевтических средств включает: оксалиплатин (ELOXATIN®, Sanofi), бортезомиб (VELCADE®, Millennium Pharm.), сутент (SUNITINIB®, SU11248, Pfizer), летрозол (FEMARA®, Novartis), иматиниба мезилат (GLEEVEC®, Novartis), XL-518 (ингибитор МЕК, Exelixis, WO 2007/044515), ARRY-886 (ингибитор МЕК, AZD6244, Array BioPharma, Astra Zeneca), SF-1126 (ингибитор PI3K, Semafore Pharmaceuticals), BEZ-235 (ингибитор PI3K, Novartis), XL-147 (ингибитор PI3K, Exelixis), PTK787/ZK 222584 (Novartis), фулвестрант (FASLODEX® AstraZeneca), лейковорин (фолиновая кислота), рапамицин (сиролимус, RAPAMUNE®, Wyeth), аналог рапамицина, ингибитор mTOR, такой как эверолимус, ингибитор МЕК (GDC-0973), ингибитор Bcl-2, такой как навитоклакс, (АВТ-263) или АВТ-199), лапатиниб (TYKERB®, GSK572016, Glaxo Smith Kline), лонафарниб (SARASAR™, SCH 66336, Schering Plough), сорафениб (NEXAVAR®, BAY43-9006, Bayer Labs), гефитиниб (IRESSA®, AstraZeneca), иринотекан (CAMPTOSAR®, CPT-11, Pfizer), типифарниб (ZARNESTRA™, Johnson & Johnson), ABRAXANE™ (без Хемофора), альбуминовые нанокомпозиции паклитаксела (American Pharmaceutical Partners, Schaumberg, II), вандетаниб (rINN, ZD6474, ZACTIMA®, AstraZeneca), хлорамбуцил, AG1478, AG1571 (SU 5271; Sugen), темсиролимус (TORISEL®, Wyeth), пазопаниб (GlaxoSmithKline), канфосфамид (TELCYTA®, Telik), тиотепа и циклофосфамид (CYTOXAN®, NEOSAR®); алкилсульфонаты, такие как бусульфан, импросульфан и пипосульфан; азиридины, такие как бензодопа, карбоквон, метуредопа и уредопа; этиленимины и метиламеламины, включая альтретамин, триэтиленмеламин, триэтиленфосфорамид, триэтилентиофосфорамид и триметиломеламин; ацетогенины (особенно буллатацин и буллатацинон); камптотецин (включая синтетический аналог топотекана); бриостатин; каллистатин; СС-1065 (включая его синтетические аналоги адоцелезин, карцелезин и бицелезин); криптофицины (особенно криптофицин 1 и криптофицин 8); доластатин; дуокармицин (включая синтетические аналоги, KW-2189 и СВ1-ТМ1); элеутеробин; панкратистатин; саркодиктин; спонгистатин; азотистый иприт, такой как хлорамбуцил, хлорнафазин, хлорфосфамид, эстрамустин, ифосфамид мехлоретамин, гидрохлорид оксида мехлоретамина, мелфалан, новембицин, фенестерин, преднимустин, трофосфамид, урацилиприт; нитрозомочевины, такие как кармустин, хлорзотоцин, фотемустин, ломустин, нимустин и ранимнустин; антибиотики, такие как ендииновые антибиотики (например калихеамицин, калихеамицин гамма11, калихеамицин омегаИ (Angew Chem. Intl. Ed. Engl. (1994) 33:183-186); динемицин, динемицин А; бисфосфонаты, такие как клодронат, эсперамицин; а также неокарзиностатин хромофор и родственные хромопротеиновые хромофоры ендииновых антибиотиков), аклациномизины, актиномицин, антрамицин, азасерин, блеомицины, кактиномицин, карабицин, карминомицин, карзинофилин, хромомицины, дактиномицин, даунорубицин, деторубицин, 6-диазо-5-оксо-L-норлейцин, морфолино-доксорубицин, цианоморфолино-доксорубицин, 2-пирролино-доксорубицин и дезоксидоксорубицин), эпирубицин, эзорубицин, идарубицин, неморубицин, марселломицин, митомицины, такие как митомицин С, микофеноловая кислота, ногаламицин, оливомицины, пепломицин, порфиромицин, пуромицин, квеламицин, родорубицин, стрептонигрин, стрептозоцин, туберцидин, убенимекс, зиностатин, зорубицин; антиметаболиты, такие как метотрексат и 5-фторурацил (5-FU); аналоги фолиевой кислоты, такие как деноптерин, метотрексат, птероптерин, триметрексат; аналоги пурина, такие как флударабин, 6-меркаптопурин, тиамиприн, тиогуанин; аналоги пиримидина, такие как анцитабин, азацитидин, 6-азауридин, кармофур, цитарабин, дидеоксиуридин, доксифлуридин, эноцитабин, флоксуридин; андрогены, такие как калустерон, пропионат дромостанолона, эпитиостанол, мепитиостан, тестолактон; ингибиторы коры надпочечников, такие как аминоглутетимид, митотан, трилостан; производная фолиевой кислоты, такая как фолиновая кислота; ацеглатон, альдофосфамид гликозид; аминолевулиновая кислота; энилурацил; амсакрин; бестрабуцил; бисантрен; эдатраксат; дефофамин; демеколцин; диазиквон; элфорнитин; ацетат эллиптиния; эпотилон; этоглуцид; нитрат галлия, гидроксимочевина; лентинан; лонидамин; мейтансиноиды, такие как мейтансин и ансамитоцины; митогуазон; митоксантрон; мопиданмол; нитраерин; пентостатин; фенамет; пирарубицин; лосоксантрон; подофиллиновая кислота; 2-этилгидразид; прокарбазин; полисахаридный комплекс PSK® (JHS Natural Products, Eugene, OR); разоксан; ризоксин; сизофиран; спирогерманий; тенуазоновая кислота; триазиквон; 2,2',2''-трихлортриэтиламин; трихотецены (особенно токсин Т-2, верракурин А, роридин А и ангуидин); уретан; виндесин; дакарбазин; манномустин; митобронитол; митолактол; пипоброман; гацитозин; арабинозид ("Аrа-С"); циклофосфамид; тиотепа; 6-тиогуанин; меркаптопурин; метотрексат; аналоги платины, такие как цисплатин и карбоплатин, винбластин, этопозид (VP-16); ифосфамид; митоксантрон; винкристин; винорелбин (NAVELBINE®); новантрон; тенипозид; эдатрексат; дауномицин; аминоптерин; капецитабин (XELODA®, Roche); ибандронат; СРТ-11; ингибитор топоизомеразы RFS 2000; дифторметилорнитин (ДФМО); ретиноиды, такие как ретиноевая кислота; и фармацевтически приемлемые соли, кислоты и производные любых из вышеперечисленных веществ.
Также в определение "химиотерапевтического средства" включены: (i) антигормональные средства, которые действуют как регуляторы или ингибиторы действия гормонов на опухоли, такие как антиэстрогены и селективные модуляторы рецепторов эстрогенов (SERMs от selective estrogen receptor modulators), включая например тамоксифен (включая NOLVADEX®; цитрат тамоксифена), ралоксифен, дролоксифен, 4-гидрокситамоксифен, триоксифен, кеоксифен, LY117018, онапристон и FARESTON® (цитрат торемифина); (и) ингибиторы ароматазы, которые ингибируют фермент ароматазу, который регулирует выработку эстрогена в надпочечных железах, такие как например 4(5)-имидазолы, аминоглутетимид, MEGASE® (ацетат мегестрола), AROMASIN® (эксеместан; Pfizer), форместанин, фадрозол, RIVISOR® (ворозол), FEMARA® (летрозол; Novartis) и ARIMIDEX® (анастрозол; AstraZeneca); (iii) антиандрогены, такие как флутамид, нилутамид, бикалутамид,. лейпролид и госерелин; а также троксацитабин (1,3-диоксолановый аналог нуклеозид-цитозина); (iv) ингибиторы протеинкиназ, такие как ингибиторы МЕК (WO 2007/044515); (v) ингибиторы липидкиназ; (vi) антисмысловые олигонуклеотиды, особенно те, которые ингибируют экспрессию генов в сигнальных путях, участвующих в аберрантной пролиферации клеток, например, РКС-альфа, Raf и H-Ras, такие как облимерсен (GENASENSE®, Genta Inc.); (vii) рибозимы, такие как ингибиторы экспрессии ФРЭС (VEGF) (например ANGIOZYME®) и ингибиторы экспрессии HER2; (viii) вакцины, такие как вакцины генной терапии, например ALLOVECTIN®, LEUVECTIN® и VAX ID®; PROLEUKIN® rlL-2; ингибиторы топоизомеразы 1, такие как LURTOTECAN®; ABARELIX® rmRH; (ix) антиангиогенные средства, такие как бевацизумаб (AVASTIN®, Genentech); и фармацевтически приемлемые соли, кислоты и производные любых из вышеперечисленных веществ.
Также в определение "химиотерапевтического средства" включены лекарственные средства на основе антител, такие как алемтузумаб (САМРАТН®), бевацизумаб (AVASTIN®, Genentech); цетуксимаб (ERBITUX®, Imclone); панитумумаб (VECTIBIX®, Amgen), ритуксимаб (RITUXAN®, Genentech/Biogen Idee), пертузумаб (OMNITARG™, 2C4, Genentech), трастузумаб (HERCEPTIN®, Genentech) и тозитумомаб (BEXXAR®, Corixa, GlaxoSmithKline).
Гуманизированные моноклональные антитела с лечебной возможностью в качестве химиотерапевтических средств в сочетании с соединениями формулы I по изобретению включают: алемтузумаб, аполизумаб, азелизумаб, атлизумаб, бапинейзумаб, бевацизумаб, биватузумаб мертансин, кантузумаб мертансин, цеделизумаб, цертолизумаб пегол, цидфуситузумаб, цидтузумаб, даклизумаб, экулизумаб, эфализумаб, эпратузумаб, эрлизумаб, фелвизумаб, фонтолизумаб, гемтузумаб озогамицин, инотузумаб озогамицин, ипилимумаб, лабетузумаб, лебрикизумаб, линтузумаб, матузумаб, меполизумаб, мотавизумаб, мотовизумаб, натализумаб, нимотузумаб, ноловизумаб, нумавизумаб, окрелизумаб, омализумаб, паливизумаб, пасколизумаб, пекфуситузумаб, пектузумаб, пертузумаб, пекселизумаб, раливизумаб, ранибизумаб, ресливизумаб, реслизумаб, ресивизумаб, ровелизумаб, руплизумаб, сибротузумаб, сиплизумаб, сонтизумаб, такатузумаб тетраксетан, тадоцизумаб, тализумаб, тефибазумаб, тоцилизумаб, торализумаб, трастузумаб, тукотузумаб, целмолейкин, тукуситузумаб, умавизумаб, уртоксазумаб и висилизумаб.
"Метаболит" представляет собой продукт, полученный в ходе метаболизма в теле определенного соединения или его соли. Метаболиты соединения можно определить, используя общепринятые методики, известные в данной области техники, и их активность определяют, используя тесты, такие как те, что описаны в этом документе. Подобные продукты могут быть получены, например, в ходе окисления, восстановления, гидролиза, амидирования, дезамидирования, этерификации, деэтерификации, ферментативного расщепления и т.п.вводимого соединения. Таким образом изобретение включает метаболиты соединений по изобретению, включая соединения, полученные в ходе способа, согласно которому приводят в соприкосновение соединение формулы I по данному изобретению с млекопитающим в течение периода времени, достаточного для выхода продукта обмена веществ.
Термин "листок-вкладыш" используют применительно к инструкциям, обычно включенным в серийные упаковки лекарственных средств, которые содержат информацию о показаниях, способе применения, дозировке, введении, противопоказаниях и/или предупреждения, касающиеся использования подобных лекарственных средств.
Термин "хиральный" относится к молекулам, которые обладают свойством неналожения зеркального изображения друг друга, при этом термин "ахиральный" относится к молекулам, которые являются налагающимися зеркальными изображениями друг друга.
Термин "стереоизомеры" относится к соединениям, которые обладают одинаковым химическим строением, но отличаются расположением атомов или групп в пространстве.
"Диастереомер" относится к стереоизомеру с двумя или более центрами хиральности, и их молекулы не являются зеркальными изображениями друг друга. Диастереомеры обладают разными физическими свойствами, например, температурами плавления, температурами кипения, спектральными свойствами и реакционными способностями. Смеси диастереомеров можно разделить аналитическими способами с высоким разрешением, такими как электрофорез и хроматография.
"Энантиомеры" относятся к двум стереоизомерам соединения, которые являются неналагающимися зеркальными изображениями друг друга.
Стереохимические определения и обозначения, используемые в этом документе, как правило соответствуют S.P. Parker, Ed., McGraw-Hill Dictionary of Chemical Terms (1984) McGraw-Hill Book Company, New York; и Eliel, E. and Wilen, S., "Stereochemistry of Organic Compounds", John Wiley & Sons, Inc., New York, 1994. Соединения по изобретению могут содержать асимметрические или хиральные центры, и, следовательно, существовать в разных стереоизомерных формах. Предполагается, что все стереоизомерные формы соединений по изобретению, включая, но не ограничиваясь этим, диастереомеры, энантиомеры и атропоизомеры, а также их смеси, такие как рацемические смеси, находятся в объеме настоящего изобретения. Многие органические соединения существуют в оптически активных формах, т.е. они обладают способностью вращать плоскость плоскополяризованного света. При описании оптически активного соединения приставки D и L или R и S используют для обозначения абсолютной конфигурации молекулы относительно ее хирального центра(ов). Приставки d и I или (+) и (-) используют для обозначения направления вращения плоскополяризованного света соединением, (-) или I означает, что соединение является левовращающим. Соединение с приставкой (+) или d является правовращающим. Для приведенной химической структуры эти стереоизомеры являются идентичными, кроме того, что они представляют собой зеркальные изображения друг друга. Также определенный стереоизомер может называться энантиомером, и смесь подобных изомеров часто называют энантиомерной смесью. Смесь 50:50 энантиомеров называется рацемической смесью или рацематом, который может встречаться, когда отсутствует стереоселекция или стереоспецифичность в химической реакции или способе. Термины "рацемическая смесь" и "рацемат" относятся к эквимолярной смеси двух энантиомерных частиц без оптической активности. Энантиомеры можно выделить из рацемической смеси в ходе хирального способа разделения, такого как сверхкритическая флюидная хроматография (СФХ). Присваивание конфигурации хиральным центрам разделенных энантиомеров может быть предварительным и изображено в структурах таблиц 1 и 2 в качестве иллюстрации, при этом стереохимическое определение предполагает, например, кристаллографические данные рентгеновского анализа.
Термин "таутомер" или "таутомерная форма" относится к структурным изомерам разной энергии, которые взаимопревращаются через низкоэнергетический барьер. Например, протонные таутомеры (также известные как прототропные таутомеры) включают взаимопревращения в ходе перемещения протона, такие как кето-енольная и имин-енаминная изомеризации. Валентные таутомеры включают взаимопревращения в ходе перегруппировки некоторых из связывающих электронов.
Термин "фармацевтически приемлемые соли" обозначает соли, которые не биологически или иным образом нежелательны. Фармацевтически приемлемые соли включают соли добавления как кислоты, так и основания. Фраза "фармацевтически приемлемые" указывает на то, что вещество или композиция должна быть совместима химически и/или токсикологически с другими компонентами, составляющими препарат, и/или млекопитающим, получающим вместе с этим лечение.
Термин "фармацевтически приемлемые кислотно-аддитивные соли" обозначает те фармацевтически приемлемые соли, что образованы с неорганическими кислотами, такими как соляная кислота, бромисто-водородная кислота, серная кислота, азотная кислота, угольная кислота, фосфорная кислота, и органическими кислотами, выбранными из алифатических, циклоалифатических, ароматических, аралифатических, гетероциклических, карбоновых и сульфоновых классов органических кислот, таких как муравьиная кислота, уксусная кислота, пропионовая кислота, гликолевая кислота, глюконовая кислота, молочная кислота, пировиноградная кислота, щавелевая кислота, яблочная кислота, малеиновая кислота, малоновая кислота, янтарная кислота, фумаровая кислота, винная кислота, лимонная кислота, аспарагиновая кислота, аскорбиновая кислота, глутаминовая кислота, антраниловая кислота, бензойная кислота, циннаминовая кислота, миндальная кислота, эмбоновая кислота, фенилуксусная кислота, метансульфоновая кислота "мезилат", этансульфоновая кислота, п-толуолсульофновая кислота и салициловая кислота.
Термин "фармацевтически приемлемая соль присоединения основания" обозначает те фармацевтически приемлемые соли, что образованы с органическим или неорганическим основанием. Примеры приемлемых неорганических оснований включают соли натрия, калия, аммония, кальция, магния, железа, цинка, меди, марганца и алюминия. Соли, образованные фармацевтически приемлемыми органическими нетоксичными основаниями, включают соли первичных, вторичных и третичных аминов, замещенных аминов, включая встречающиеся в природе замещенные амины, циклических аминов и основных ионообменных смол, таких как смолы на основе изопропиламина, триметиламина, диэтиламина, триэтиламина, трипропиламина, этаноламина, 2-диэтиламиноэтанола, триметамина, дициклогексиламина, лизина, аргинина, гистидина, кофеина, прокаина, гидрабамина, холина, бетаина, этилендиамина, глюкозамина, метилглюкамина, теобромина, пуринов, пиперазина, пиперидина, N-этилпиперидина и полиамина.
"Сольват" относится к ассоциации или комплексу одной или более чем одной молекулы растворителя и соединения по изобретению. Примеры растворителей, которые образуют сольваты, включают, но не ограничиваются этим, воду, изопропанол, этанол, метанол, ДМСО, этилацетат, уксусную кислоту и этаноламин.
Термин "ЕС50" является "полумаксимальной эффективной концентрацией" и обозначает концентрацию в плазме конкретного соединения, необходимую для получения 50% от максимума конкретного эффекта in vivo.
Термин "Ki" представляет собой константу ингибирования и обозначает абсолютную связывающую способность конкретного ингибитора к рецептору. Ее измеряют, используя анализы конкурентного связывания, и она равна концентрации, при которой конкретный ингибитор будет занимать 50% рецепторов при отсутствии конкурирующего лиганда (например радиолиганда). 3начения Ki можно превратить логарифмически в значения pKi (-log Ki), при этом верхние значения указывают на экспоненциально большую эффективность.
Термин "ИК50" представляет собой полумаксимальную концентрацию ингибирования и обозначает концентрацию конкретного соединения, необходимую для 50% ингибирования биологического процесса in vitro. 3начения ИК50 можно преобразовать посредством логарифмирования до значений рИК50 (-log ИК50), при этом верхние значения указывают на экспоненциально большую эффективность. 3начение ИК50 не является абсолютным значением, а зависит от экспериментальных условий, например, используемых концентраций, и может быть преобразовано в абсолютную константу ингибирования (Ki) при использовании уравнения Ченга-Прусоффа (Biochem. Pharmacol. (1973) 22:3099).
Термины "соединение по этому изобретению" и "соединения по настоящему изобретению", и "соединения формулы I" включают соединения формул I и их стереоизомеры, геометрические изомеры, таутомеры, сольваты, метаболиты и фармацевтически приемлемые соли, и пролекарства.
Также подразумевается, что любая приведенная в данном документе формула или структура, включая соединения формулы I, представляет собой гидраты, сольваты и полиморфы подобных соединений, и их смеси.
Также подразумевается, что любая приведенная в данном документе формула или структура, включая соединения формулы I, представляет собой немеченные формы, а также изотопно меченные формы соединений. Изотопно меченные соединения имеют структуры, изображенные с помощью формул, приведенных в данном документе, за исключением того, что один или более чем один атом заменен на атом, имеющий определенную атомную массу или массовое число. Примеры изотопов, которые могут быть включены в соединения по изобретению, включают изотопы водорода, углерода, азота, кислорода, фосфора, фтора и хлора, такие как, но не ограничиваясь этим 2Н (дейтерий, D), 3Н (тритий), 11С, 13С, 14С, 15N, 18F, 31Р, 32Р, 35S, 36Cl и 125I. Разные изотопно меченные соединения по настоящему изобретению, например те, в которые включены радиоактивные изотопы, такие как 3Н, 13С и 14С. Подобные изотопно меченные соединения можно использовать в изучениях обмена веществ, кинетических изучениях реакций, методах детектирования или воспроизведения изображений, таких' как позитронно-эмиссионная томография (ПЭТ) или однофотонная эмиссионная компьютерная томография (ОФЭКТ), включая анализы распределения в тканях лекарства или вещества, или в радиоактивном лечении пациентов. Меченные или замещенные дейтерием терапевтические соединения по изобретению могут иметь улучшенные свойства DMPK (от drug metabolism and pharmacokinetics, метаболизма лекарственных веществ и фармакокинетики), это касается распределения, метаболизма и выведения (ADME). Замещение тяжелыми изотопами, такими как дейтерий, может давать определенные терапевтические преимущества, возникающие в результате большей метаболической устойчивости, например, увеличенный in vivo период полураспада или потребности в пониженной дозировке. 18F меченное соединение можно использовать в изучениях ПЭТ или ОФЭКТ. Как правило, изотопно меченные соединения по этому изобретению и их пролекарства могут быть получены при проведении процедур, раскрытых на схемах или в примерах и получениях, описанных ниже, в ходе замещения общедоступным изотопно меченным реагентом неизотопно меченного реагента. Кроме того, замещение тяжелыми изотопами, особенно дейтерием (т.е. 2Н или D), может давать определенные терапевтические преимущества, возникающие в результате большей метаболической устойчивости, например, увеличенный in vivo период полураспада или потребности в пониженной дозировке, или улучшение терапевтического индекса. Понятно, что дейтерий в данном случае считается заместителем соединения формулы (I). Концентрацию подобного тяжелого изотопа, особенно дейтерия, можно определить по фактору изотопного обогащения. Подразумевается, что в соединениях по этому изобретению любой атом, особо не обозначенный как конкретный изотоп, является любым стабильным изотопом данного атома. Если не указано иное, то, когда положение особо обозначено как "Н" или "водород", тогда подразумевается, что положение является водородом в своем распространенным в природе изотопном составе. Таким образом, имеют в виду, что в соединениях по данному изобретению любой атом, особо обозначенный как дейтерий (D), является дейтерием.
Соединения 5-азаиндазола
Согласно настоящему изобретению предложены соединения 5-азаиндазола формулы I, включая формулы Ia-i, и их фармацевтические препараты, которые потенциально полезны в лечении заболеваний, состояний и/или расстройств, регулируемых киназами Pim.
Соединения формулы I имеют структуру:
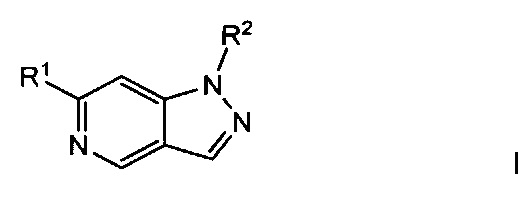
и их стереоизомеры, геометрические изомеры, таутомеры и фармацевтически приемлемые соли, где:
R1 представляет собой пятичленный или шестичленный гетероарил, возможно замещенный одной или более чем одной группой, независимо выбранной из F, Cl, Br, -CN, -NO2, ОН, C1-C12 алкила, -NH(C1-C12 алкил), -N(C1-С12 алкил)2, -O(C1-C12 алкил), -S(C1-C12 алкил), -S(O)2(C1-C12 алкил), -S(O)2N(C1-C12 алкил)2, -(C1-C12 алкилен)-(С3-С12 карбоциклил), -(C1-C12 алкилен)-(С2-С20 гетероциклил), -(С2-С8 алкенилен)-(С3-С12 карбоциклил), -(С2-С8 алкенилен)-(С2-С20 гетероциклил), С6-С20 арила, -(С6-С20 арилен)-(С2-С20 гетероциклил), -(С6-С20 арилен)-(С1-C12 алкилен)-(С2-С20 гетероциклил), С3-С12 карбоциклила, С2-С20 гетероциклила и C1-C20 гетероарила, где алкил, алкенил, алкинил, алкилен, карбоциклил, гетероциклил, арил и гетероарил возможны замещены одной или более чем одной группой, независимо выбранной из F, Cl, Br, I, -СН3, -СН2СН3, -СН(СН3)2) -СН2СН(СН3)2, -CH2NH2, -CH2CH2NH2, -CH2CHCH2NH2, -CH2CH(CH3)NH2, -CH2OH, -CH2CH2OH, -С(СН3)2ОН, -СН(ОН)СН(СН3)2, -С(СН3)2СН2ОН, -CH2CH2SO2CH3, -CN, -CHF2, -CF3, -CO2H, -СОСН3, -СO2СН3, -СO2С(СН3)3, -СОСН(ОН)СН3, -CONH2, -CONHCH3, -CON(CH3)2, -C(CH3)2CONH2, -NO2, -NH2, -NHCH3, -N(CH3)2, -NHCOCH3, -N(CH3)COCH3, -NHS(O)2CH3, -N(CH3)C(CH3)2CONH2, -N(CH3)CH2CH2S(O)2CH3, =O, -OH, -OCH3, -OCH2CH3, -S(O)2N(CH3)2, -SCH3, -CH2OCH3, -S(O)2CH3, циклопропила, циклобутила, циклопентила, циклогексила, циклогептила, азетидинила, азепанила, оксетанила, пирролидинила, пиперазинила, пиперидинила, (пиперидин-4-илэтил), пиранила, (пиперидин-4-илметил), морфолинометила и морфолино; и
R2 представляет собой фенил или шестичленный гетероарил, где фенил или шестичленный гетероарил возможно замещен одной или более чем одной группой, независимо выбранной из F, Cl, Br, -CN, -NO2, ОН, С1-С12 алкила, -NH(C1-G12 алкил), -N(C1-C12 алкил)2, -O(C1-C12 алкил), -S(C1-C12 алкил), -S(O)2(C1-C12 алкил), -S(O)2N(C1-C12 алкил)2, -(C1-C12 алкилен)-(С3-С12 карбоциклил), -(C1-C12 алкилен)-(С2-С20 гетероциклил), -О(С2-С20 гетероциклил), -NH(C2-C20 гетероциклил), -N(C1-C12 алкил)(С2-С20 гетероциклил), -(С2-С8 алкенилен)-(С3-С12 карбоциклил), -(С2-С8 алкенилен)-(С2-С20 гетероциклил), С6-С20 арила, -(С6-С20 арилен)-(С2-С20 гетероциклил), -(С6-С20 арилен)-(C1-С12 алкилен)-(С2-С20 гетероциклил), С3-С12 карбоциклила, С2-С20 гетероциклила и C1-C20 гетероарила, где алкил, алкенил, алкинил, алкилен, карбоциклил, гетероциклил, арил и гетероарил возможно замещены одной или более чем одной группой, независимо выбранной из F, Cl, Br, I, -СН3, -СН2СН3, -СН(СН3)2, -СН2СН(СН3)2, -CH2NH2, -CH2CH2NH2, -CH2CHCH2NH2, -CH2CH(CH3)NH2), -CH2OH, -CH2CH2OH, -С(СН3)2ОН, -СН(ОН)СН(СН3)2, -С(СН3)2СН2ОН, -CH2CH2SO2CH3, -CN, -CHF2, -CF3, -CO2H, -СОСН3, -CO2CH3, -СO2С(СН3)3, -СОСН(ОН)СН3, -CONH2, -CONHCH3, -CON(CH3)2, -C(CH3)2CONH2, -NO2, -NH2, -NHCH3, -N(CH3)2, -NHCOCH3, -N(CH3)COCH3, -NHS(O)2CH3, -N(CH3)C(CH3)2CONH2, -N(CH3)CH2CH2S(O)2CH3, =O, -OH, -OCH3, -OCH2CH3, -S(O)2N(CH3)2, -SCH3, -CH2OCH3, -S(O)2CH3, циклопропила, циклобутила, циклопентила, циклогексила, циклогептила, азетидинила, азепанила, оксетанила, пирролидинила, пиперазинила, пиперидинила, (пиперидин-4-илэтил), пиранила, (пиперидин-4-илметил), морфолинометила и морфолино.
Примерные воплощения соединений формулы I включают те, где R1 выбран из структур:
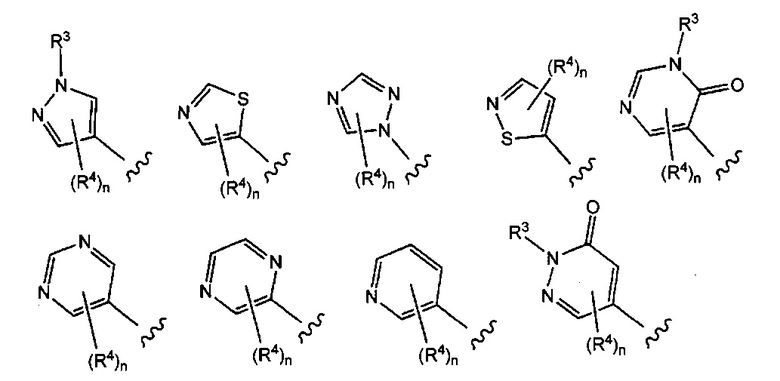
где волнистая линия указывает на место присоединения;
R3 выбран из Н, -СН3, -СН2СН3, -СН(СН3)2, -С(СН3)3, -СН2СН(СН3)2, -CH2NH2, -CH2NHCH3, -CH2CH2NH2, -CH2CHCH2NH2, -CH2CH(CH3)NH2, -CH2OH, -CH2CH2OH, -C(CH3)2OH, -CH(OH)CH(CH3)2, -C(CH3)2CH2OH, -CH2CH2SO2CH3, -CN, -CF3, -CO2H, -COCH3, -CO2CH3, -CO2C(CH3)3, -COCH(OH)CH3, -CONH2, -CONHCH3, -CON(CH3)2, -C(CH3)2CONH2, -S(O)2N(CH3)2, -SCH3, -CH2OCH3, -S(O)2CH3, циклопропила, циклобутила, циклопентила, циклогексила, циклогептила и оксетанила;
R4 независимо выбран из F, Cl, Br, I, -СН3, -СН2СН3, -СН(СН3)2, -С(СН3)3, -СН2СН(СН3)2, -CH2NH2, -CH2NHCH3, -CH2CH2NH2, -CH2CHCH2NH2, -CH2CH(CH3)NH2, -CH2OH, -CH2CH2OH, -C(CH3)2OH, -CH(OH)CH(CH3)2, -C(CH3)2CH2OH, -CH2CH2SO2CH3, -CN, -CF3, -CO2H, -COCH3, -CO2CH3, -CO2C(CH3)3, -COCH(OH)CH3, -CONH2, -CONHCH3, -CON(CH3)2, -C(CH3)2CONH2, -NO2, -NH2, -NHCH3, -N(CH3)2, -NHCH2CHF2, -NHCH2CF3, -NHCOCH3, -N(CH3)COCH3, -NHC(O)OCH2CH3, -NHC(O)OCH2Cl3, -NHC(O)OC6H5, -NHS(O)2CH3, -N(CH3)C(CH3)2CONH2, -N(CH3)CH2CH2S(O)2CH3, =O, -OH, -OCH3, -S(O)2N(CH3)2, -SCH3, -CH2OCH3, -S(O)2CH3, циклопропила, циклобутила, циклопентила, циклогексила, циклогептила, азетидинила, азепанила, оксетанила, пирролидинила, пиперазинила, пиперидинила, (пиперидин-4-илэтил), пиранила, (пиперидин-4-илметил), морфолинометила и морфолино;
и n представляет собой 0, 1, 2 или 3.
Примерные воплощения соединений формулы I включают те, где R2 представляет собой шестичленный гетероарил, имеющий структуру:
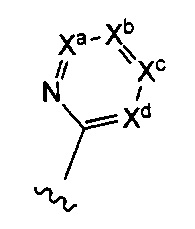
где волнистая линия указывает на точку присоединения;
Ха представляет собой N или CRa;
Хb представляет собой N или CRb;
Xc представляет собой N или CRc;
Xd представляет собой N или CRd;
где 0 или 1 Ха, Хb, Xc и Xd представляет собой N;
Ra, Rb, Rc и Rd независимо выбраны из Н, С2-С20 гетероциклила и -NH(C2-С20 гетероциклил), где гетероциклил возможно замещен одной или более чем одной группой, выбранной из F, Cl, Br, I, -СН3, -СН2СН3, -СН(СН3)2, -С(СН3)3, -СН2СН(СН3)2, -CH2NH2, -CH2NHCH3, -CH2CH2NH2, -CH2CHCH2NH2, -CH2CH(CH3)NH2, -CH2OH, -CH2CH2OH, -C(CH3)2OH, -CH(OH)CH(CH3)2, -C(CH3)2CH2OH, -CH2CH2SO2CH3, -CN, -CF3, -CO2H, -COCH3, -CO2CH3, -CO2C(CH3)3, -COCH(OH)CH3, -CONH2, -CONHCH3, -CON(CH3)2, -C(CH3)2CONH2, -NO2, -NH2, -NHCH3, -N(CH3)2, -NHCH2CHF2, -NHCH2CF3, -NHCOCH3, -N(CH3)COCH3, -NHC(O)OCH2CH3, -NHC(O)OCH2Cl3, -NHC(O)OC6H5, -NHS(O)2CH3, -N(CH3)C(CH3)2CONH2, -N(CH3)CH2CH2S(O)2CH3, =O, -OH, -OCH3, -S(O)2N(CH3)2, -SCH3, -CH2OCH3, -S(O)2CH3, циклопропила, циклобутила, циклопентила, циклогексила, циклогептила, азетидинила, азепанила, оксетанила, пирролидинила, пиперазинила, пиперидинила, (пиперидин-4-илэтил), пиранила, (пиперидин-4-илметил), морфолинометила и морфолино;
или где Ха представляет собой CRa, и Хb представляет собой CRb, и Ra и Rb образуют шестичленное кольцо.
Примерные воплощения соединений формулы I включают те, где R2 выбран из структур:
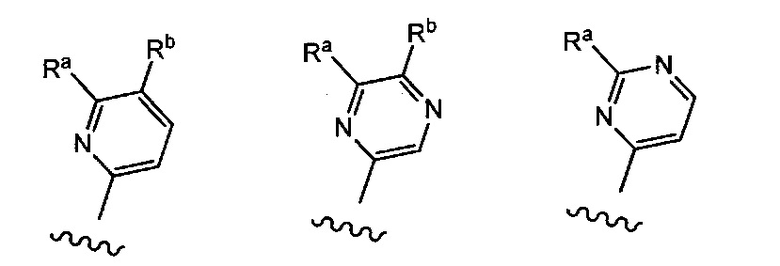
Примерные воплощения соединений формулы I включают те, где R2 выбран из структур:
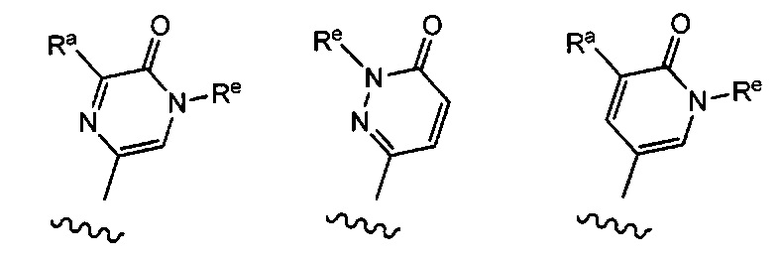
где Re выбран из Н, -СН3, -СН2СН3, -СН(СН3)2, -С(СН3)3, -СН2СН(СН3)2, -CH2NH2, -CH2NHCH3, -CH2CH2NH2, -CH2CHCH2NH2, -CH2CH(CH3)NH2, -CH2OH, -CH2CH2OH, -C(CH3)2OH, -CH(OH)CH(CH3)2, -C(CH3)2CH2OH, -CH2CH2SO2CH3, -CN, -CF3, -CO2H, -COCH3, -CO2CH3, -CO2C(CH3)3, -COCH(OH)CH3, -CONH2, -CONHCH3, -CON(CH3)2, -C(CH3)2CONH2, -S(O)2N(CH3)2, -SCH3, -CH2OCH3, -S(O)2CH3, циклопропила, циклобутила, циклопентила, циклогексила, циклогептила и оксетанила.
Примерные воплощения соединений формулы I включают те, где Ra представляет собой гетероциклил, выбранный из структур:
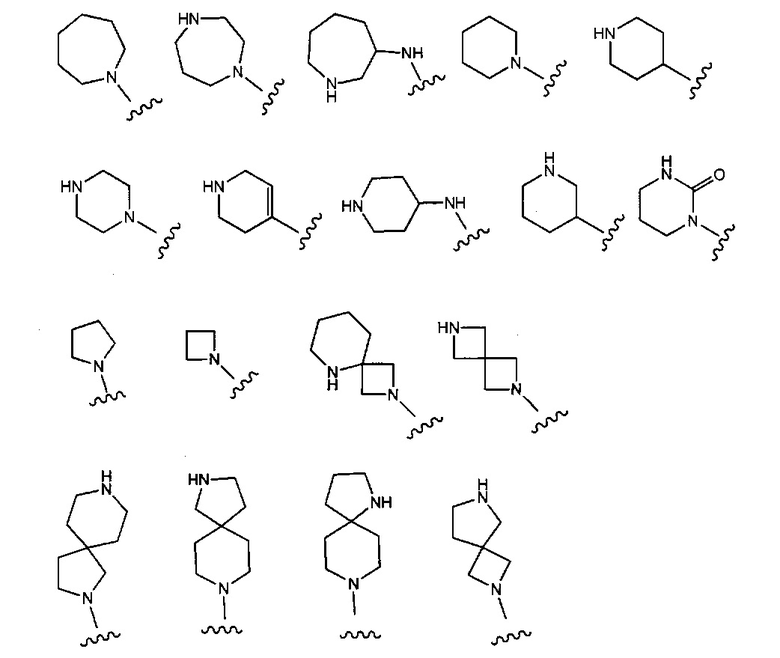
где гетероциклил возможно замещен одной или более чем одной группой, независимо выбранной из F, -ОН, -ОСН3, =O, -NH2, -СН3, -СН2СН3 и оксетан-3-ила.
Примерные воплощения соединений формулы I включают те, где R2 представляет собой фенил, возможно замещенный одной или более чем одной группой, выбранной из F, Cl, Вr, -СН3 и -NH2.
Примерные воплощения соединений формулы I включают структуру формулы Iа:
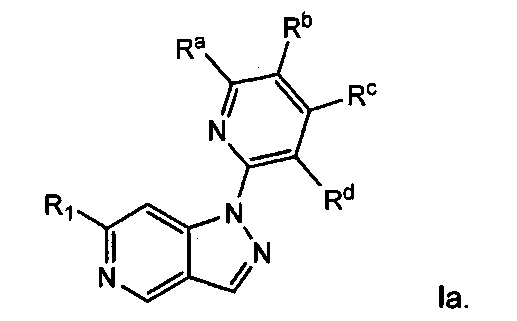
Примерные воплощения соединений формулы I включают структуру формулы Ib:
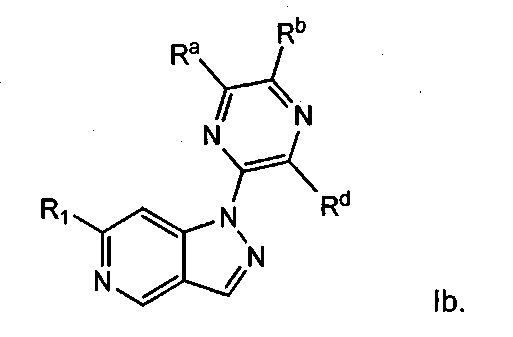
Примерные воплощения соединений формулы I включают структуру формулы Iс:
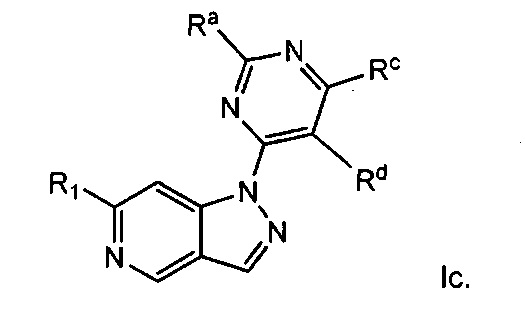
Примерные воплощения соединений формулы I включают структуру формулы Id:
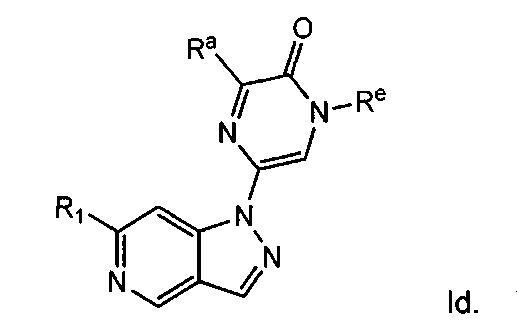
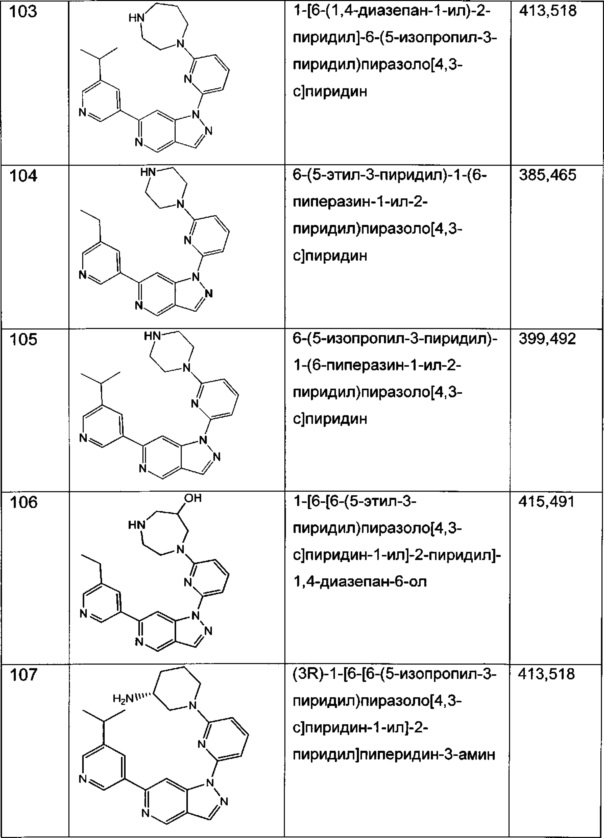
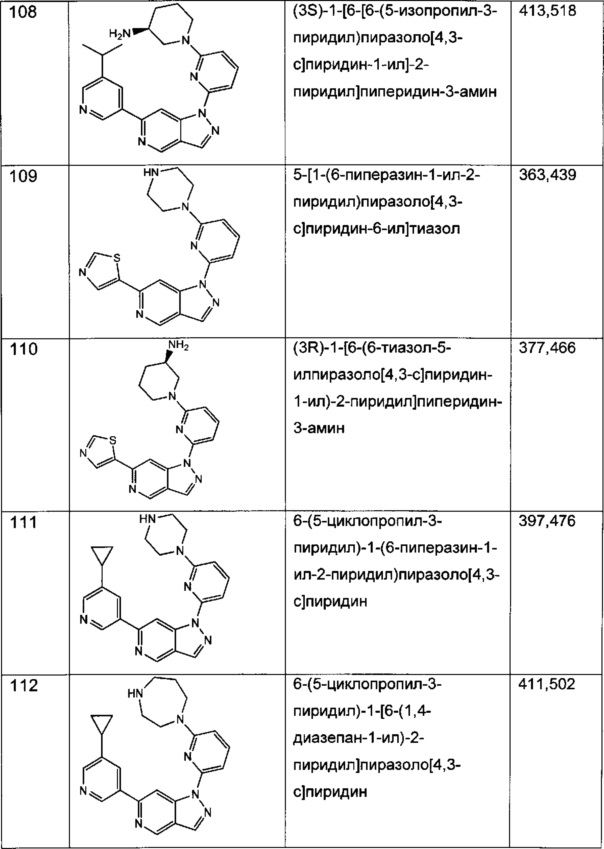
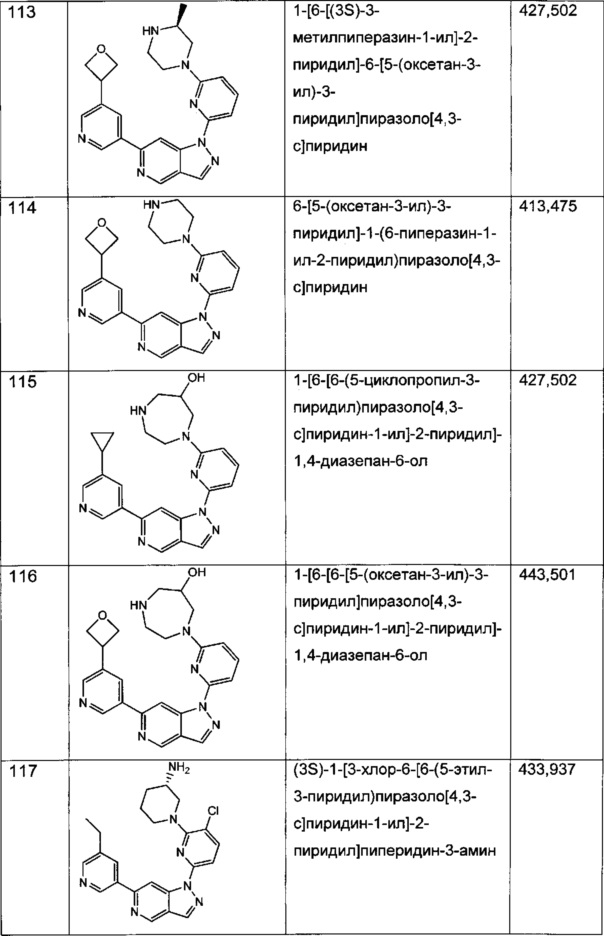
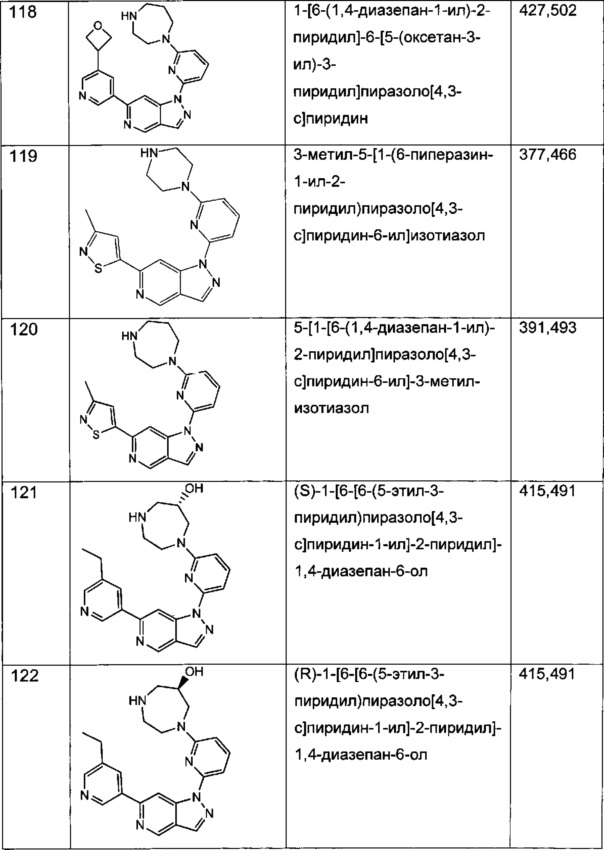
Примерные воплощения соединений формулы I включают соединения таблиц 1 и 2.
Оценка биологического действия
Определение активности соединения формулы I в отношении киназы Pim возможно осуществить целым рядом способов прямого и косвенного обнаружения. Конкретные примерные соединения, описанные в этом документе, анализировали на их активность связывания киназы Pim, включая изоформы Pim-1, Pim-2 и Pim-3, (пример 901) и in vitro активность в отношении опухолевых клеток (пример 902). Конкретные примерные соединения по изобретению имели 3Начения ИК50 активности связывания Pim меньше чем приблизительно 1 микромолярная (мкМ). Конкретные соединения по изобретению имели 3Начения ЕС50 активности в отношении опухолевых клеток меньше чем приблизительно 1 микромолярная (мкМ). Соединения формулы I, имеющие Ki/ИK50/EC50 меньше чем 1 мкМ согласно анализам, описанным в примерах 901 и 902, можно использовать терапевтически в качестве ингибиторов киназы Pim (Pim-1, Pim-2 и/или Pim-3).
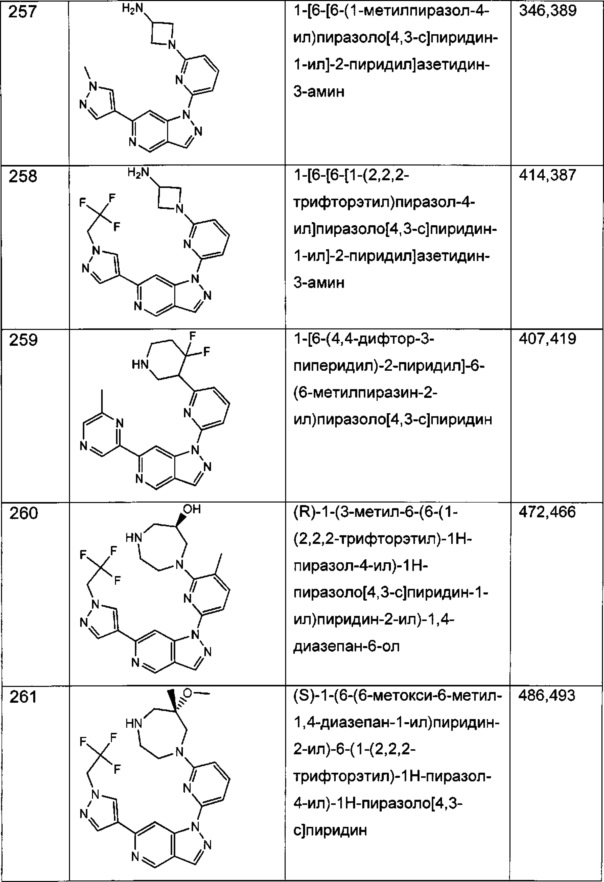
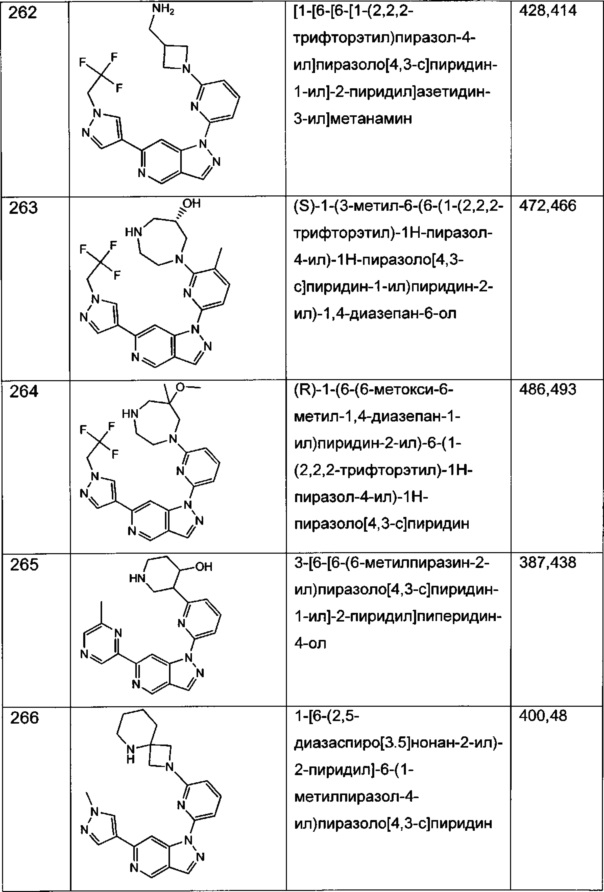
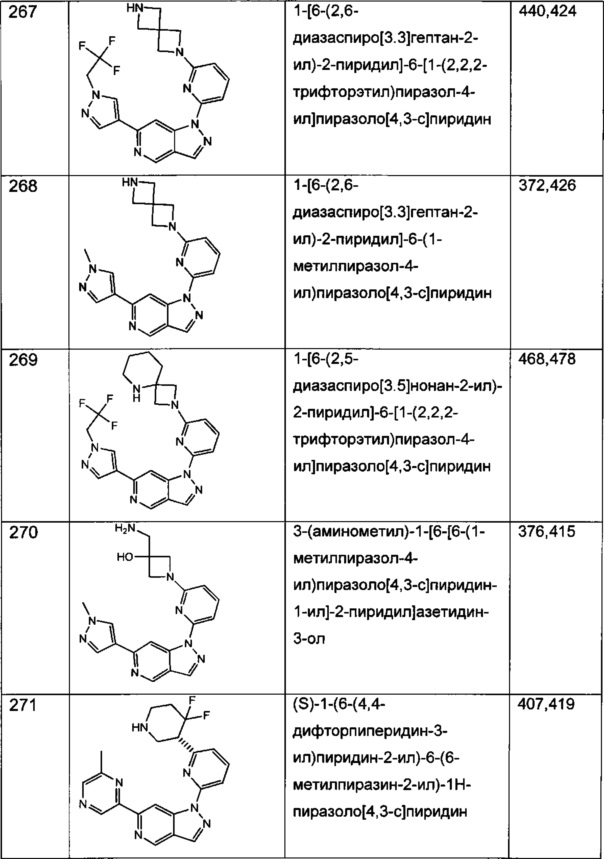
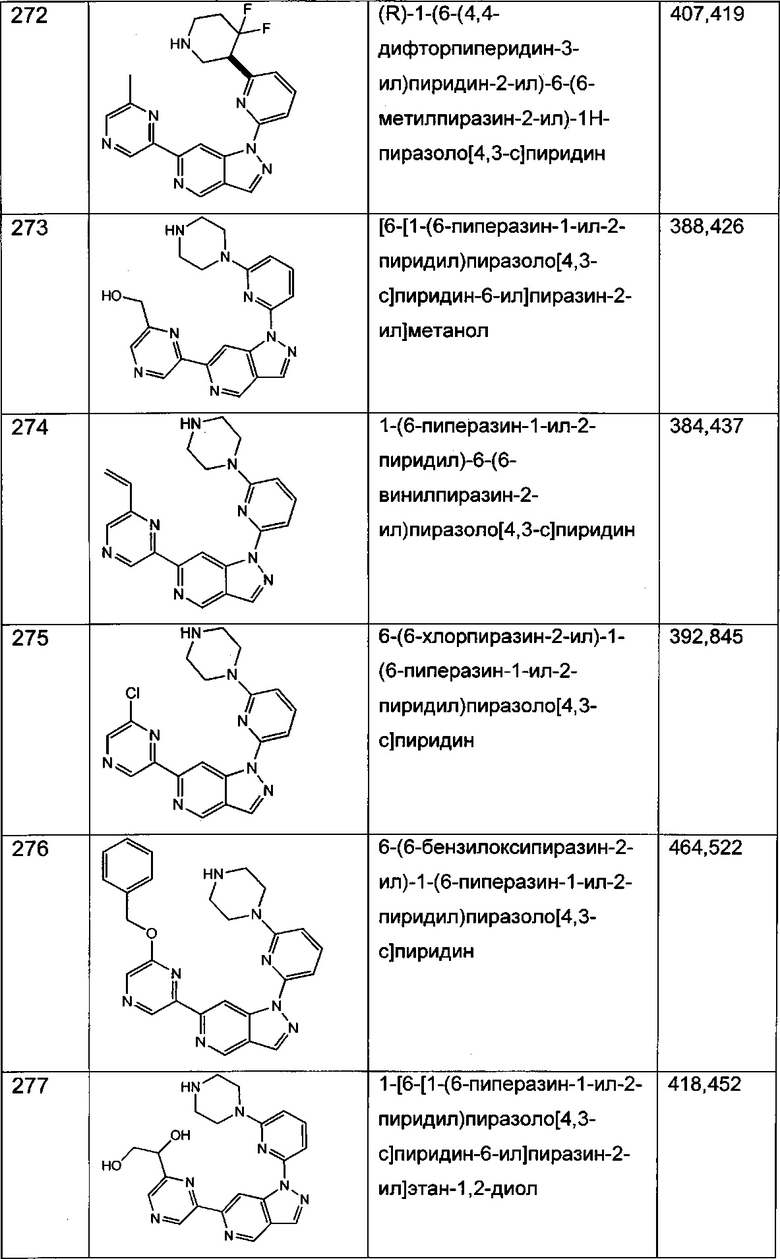
Примерные соединения формулы I приведены в таблицах 1 и 2, охарактеризованы и проверены на ингибирование киназы Pim способами по данному изобретению, и имеют следующие структуры и соответствующие названия (ChemBioDraw Ultra, Version 11.0, CambridgeSoft Corp., Cambridge MA).
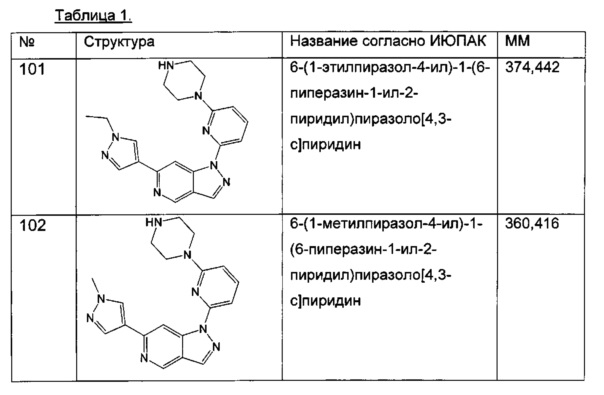
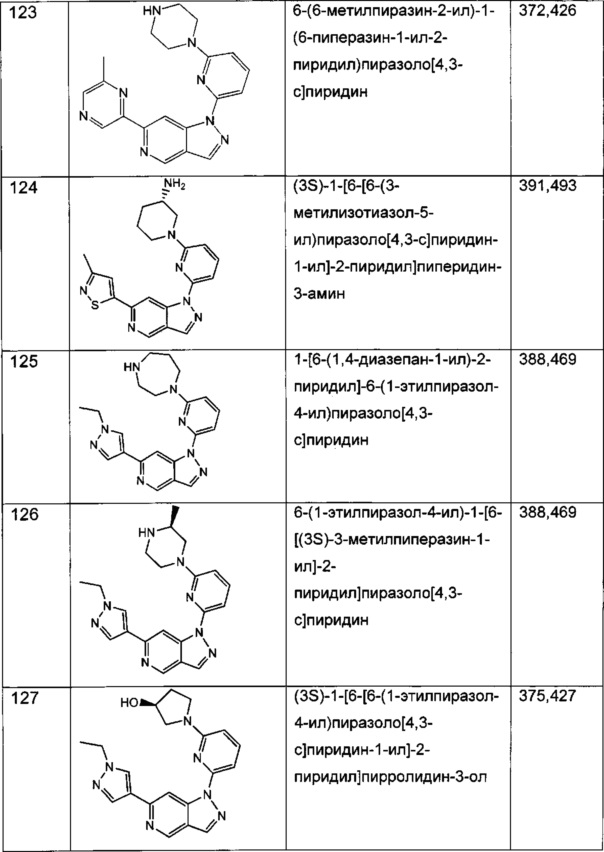
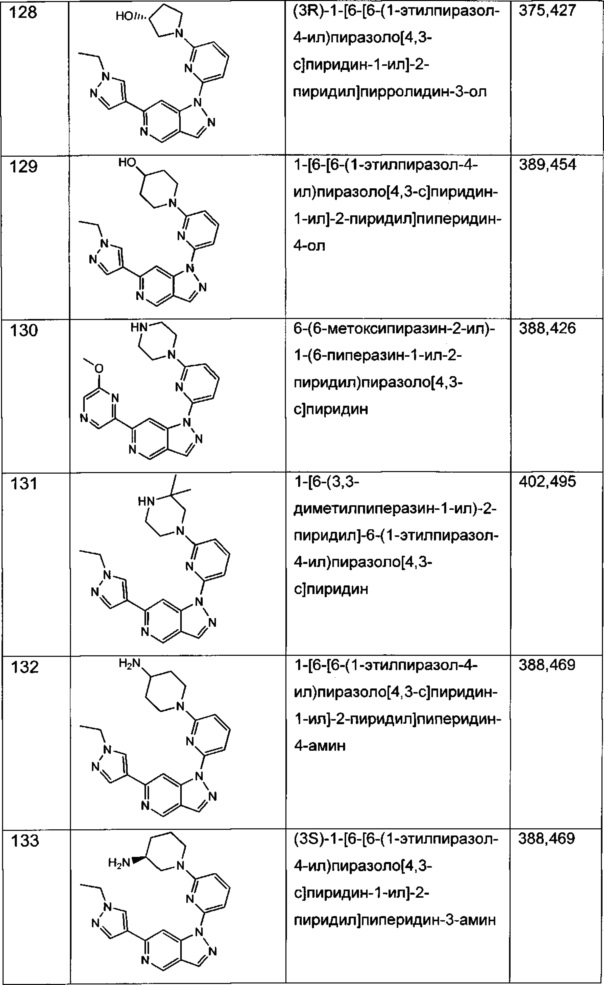
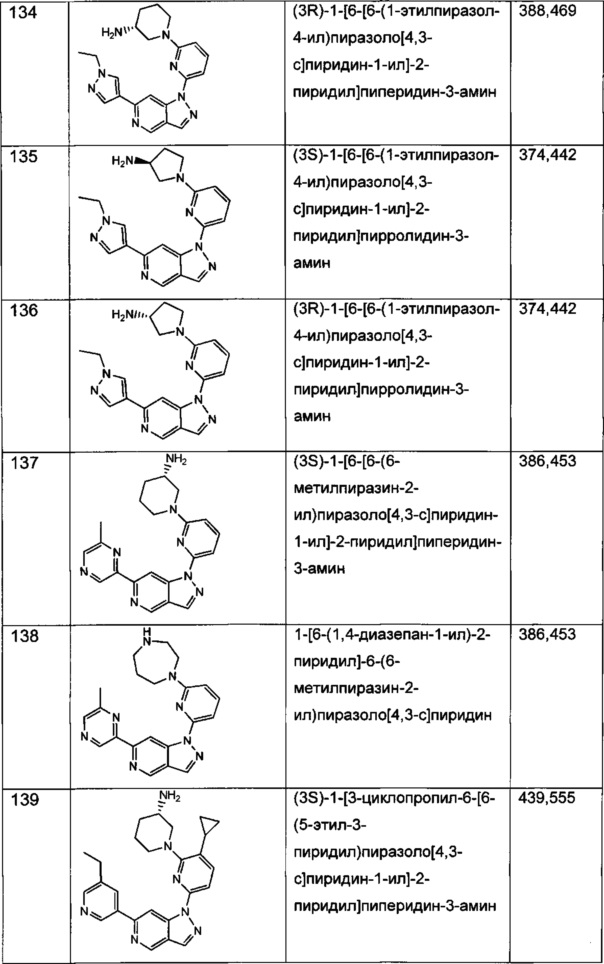
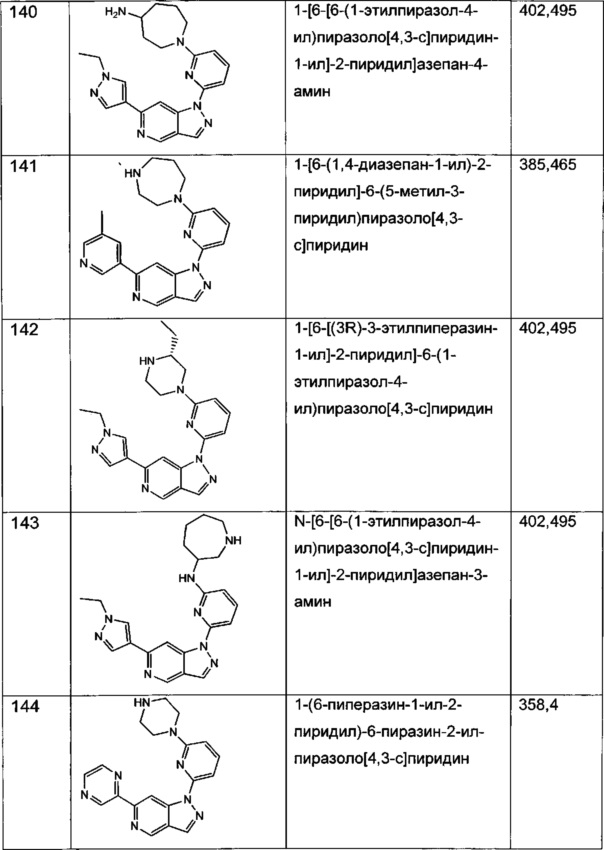
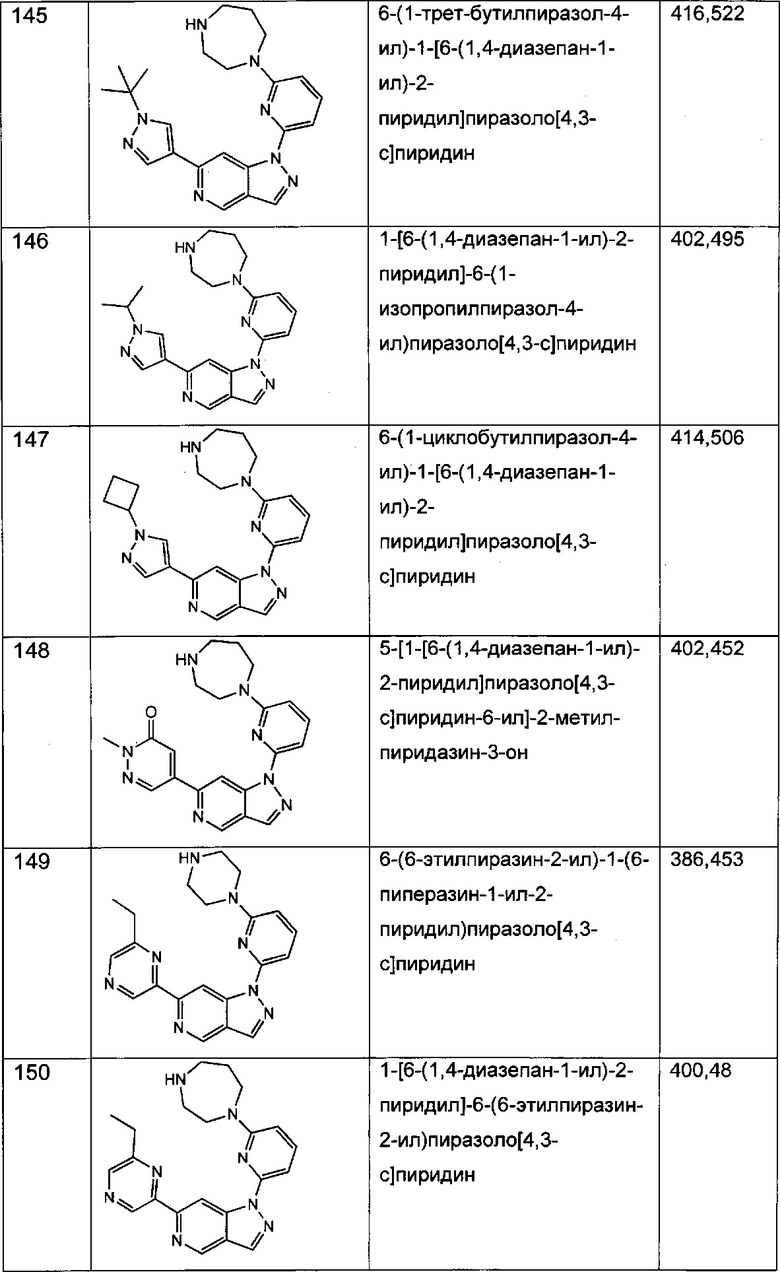
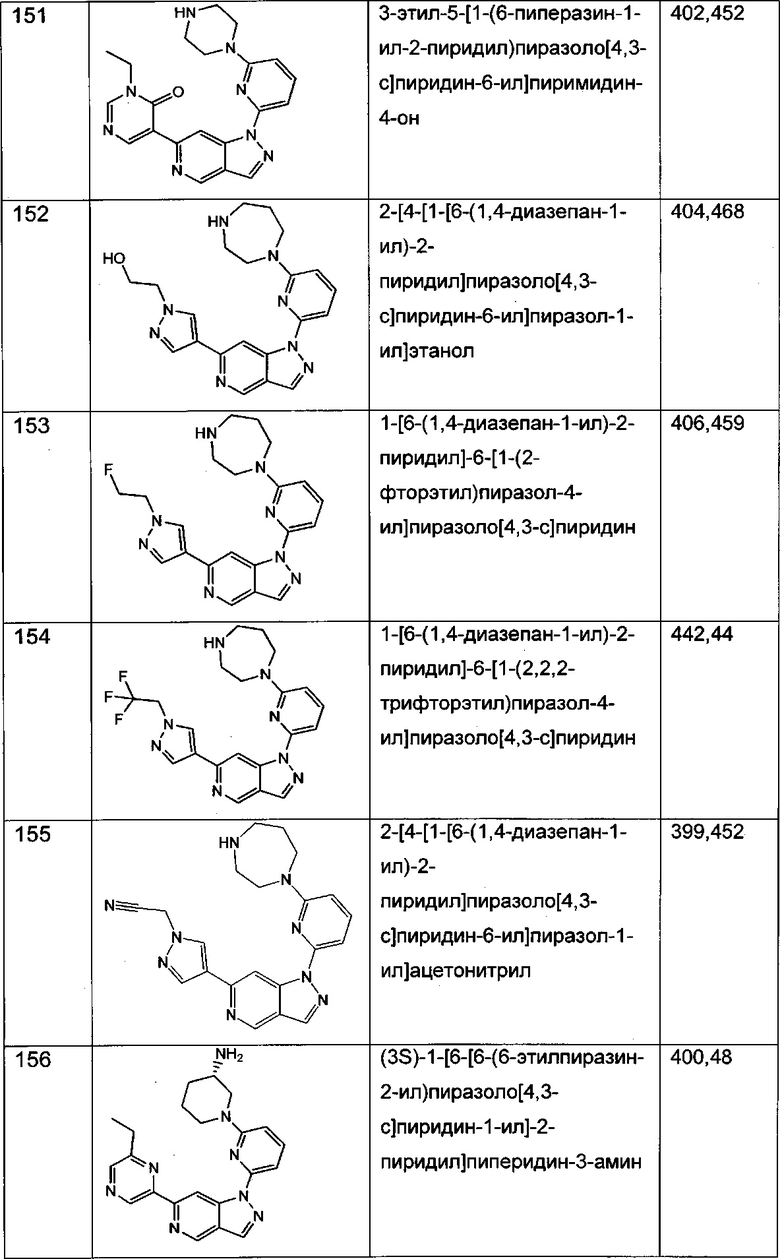
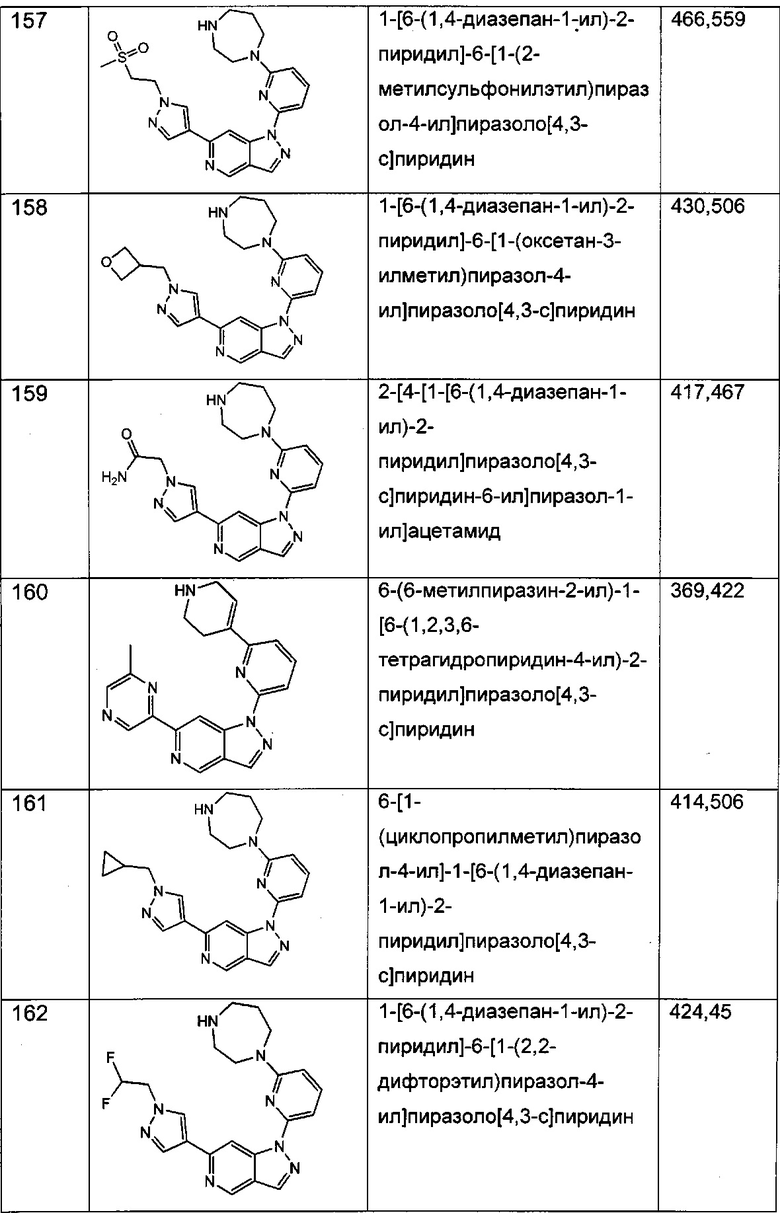
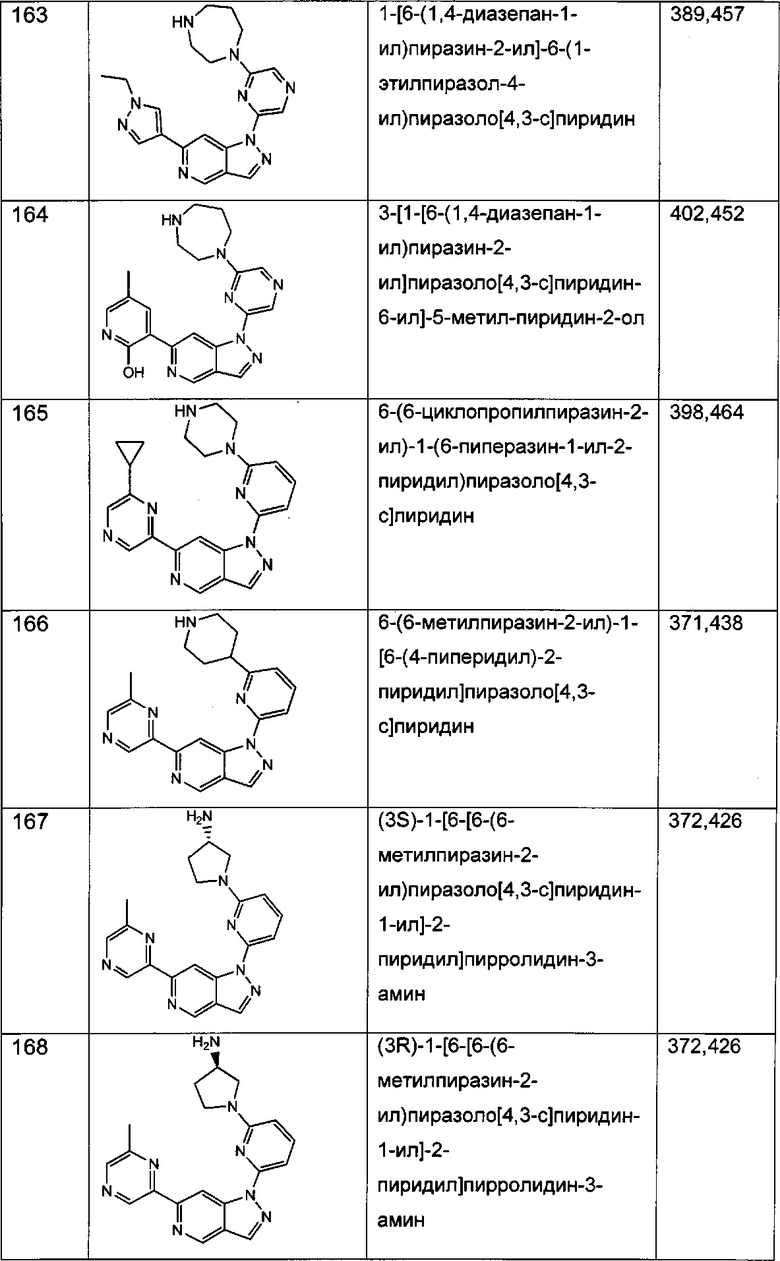
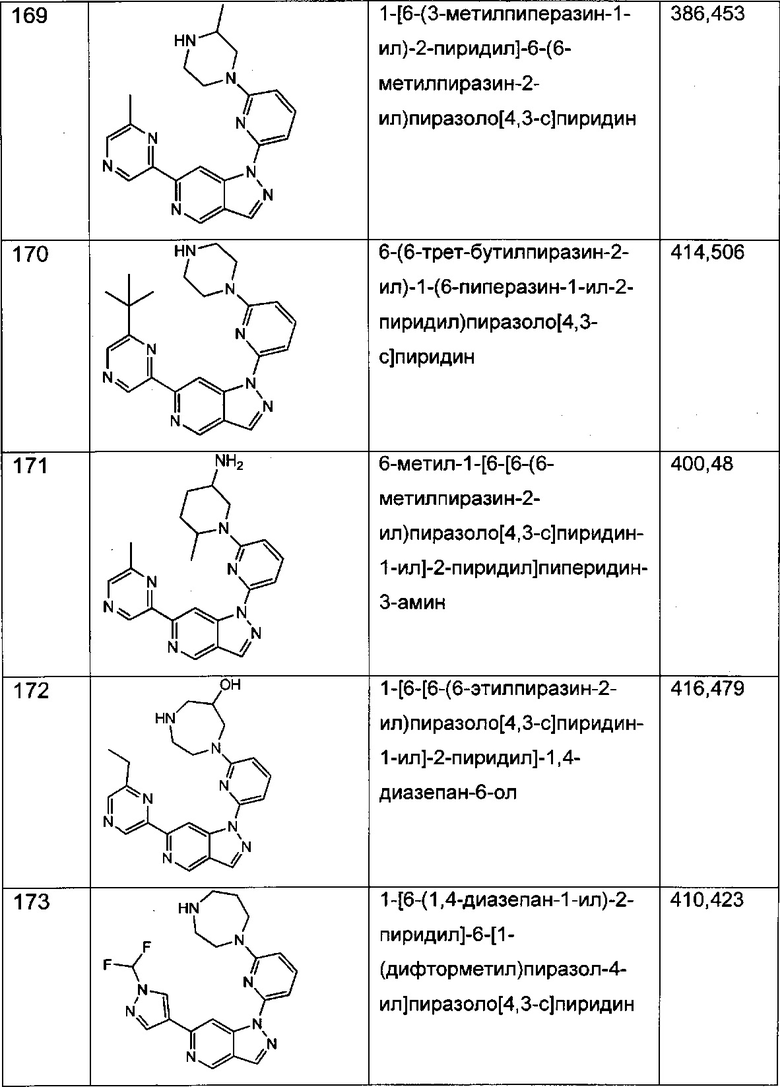
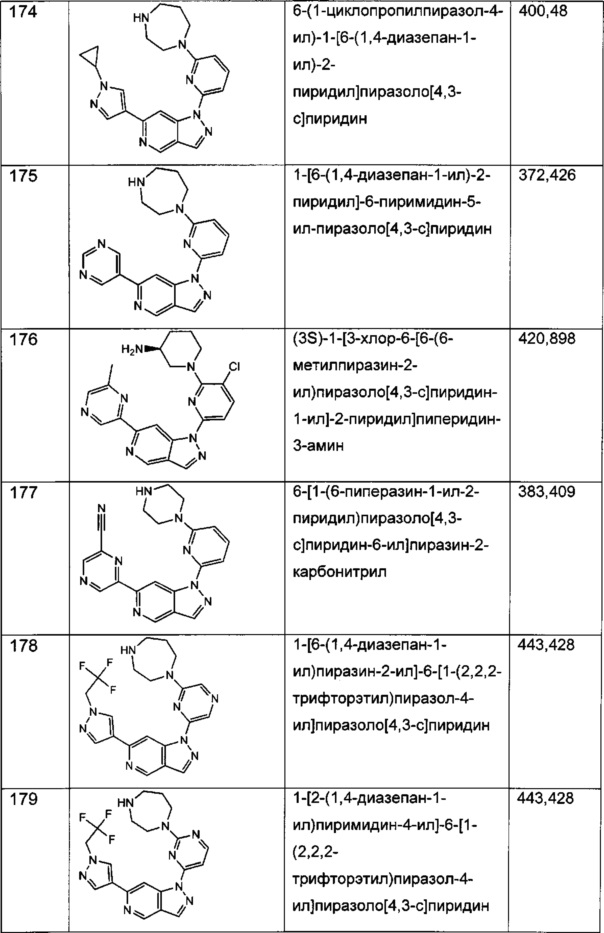
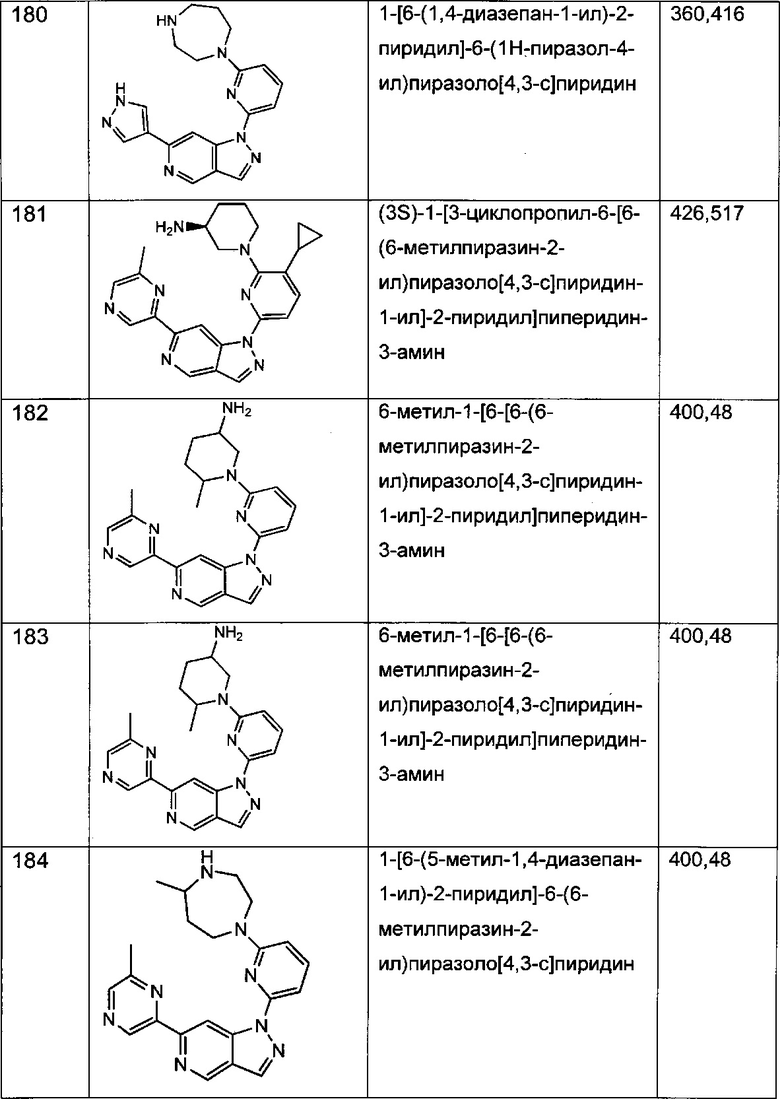
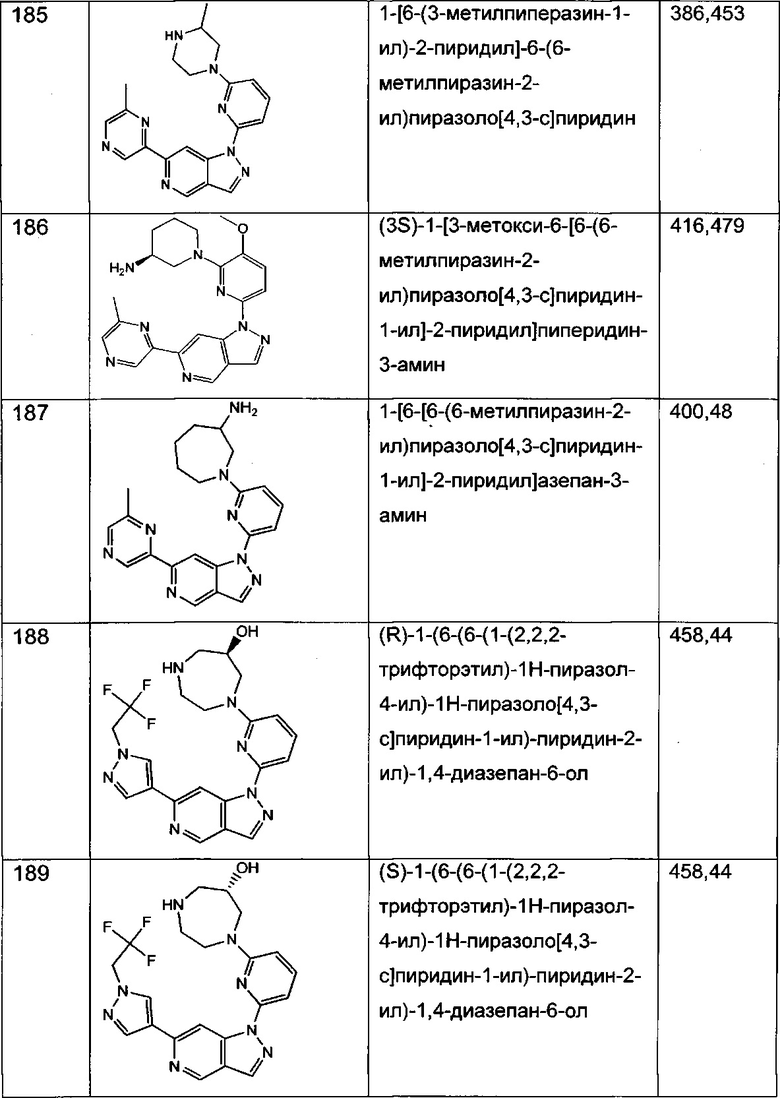
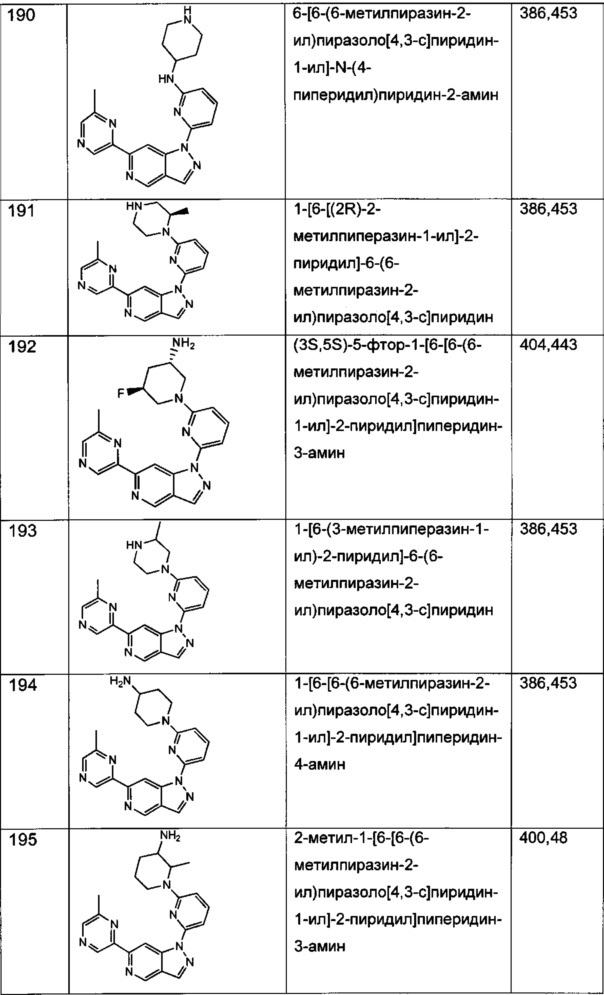
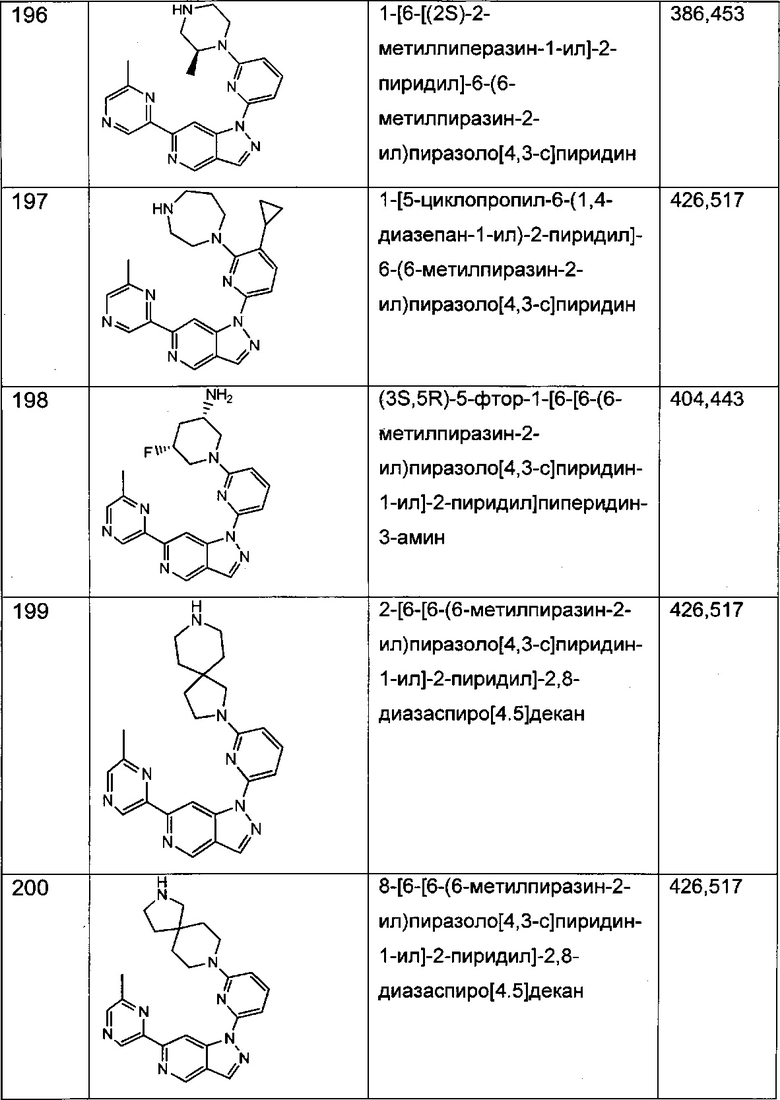
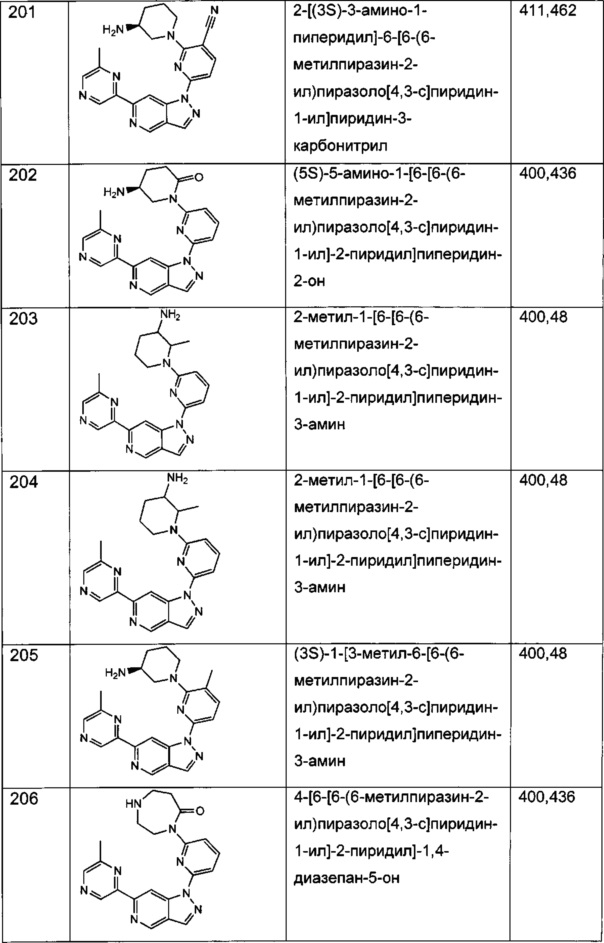
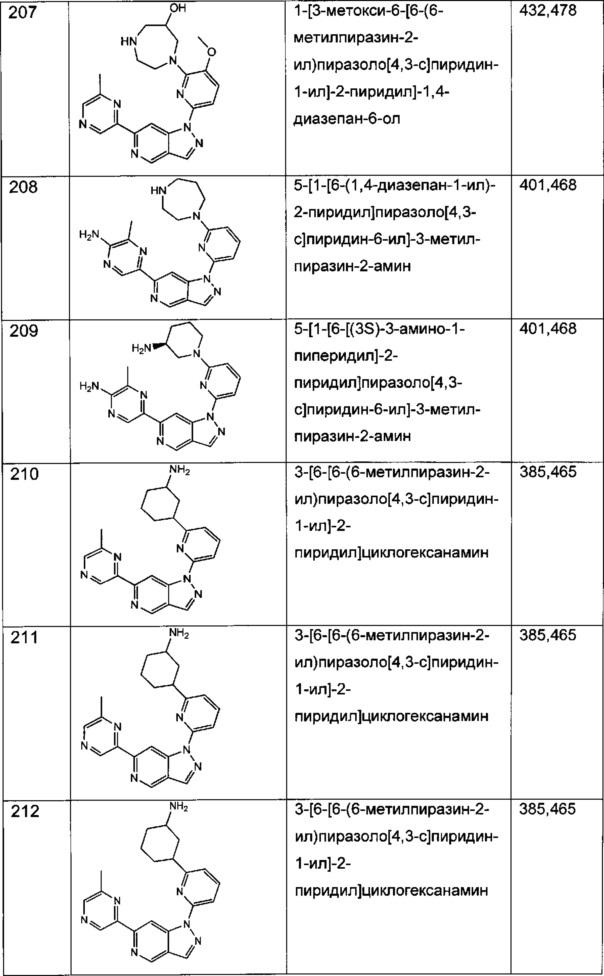
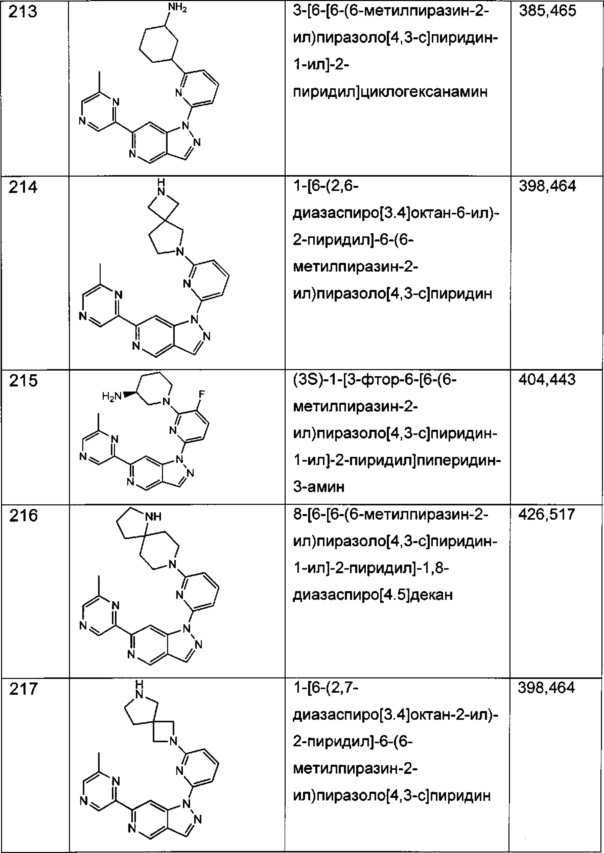
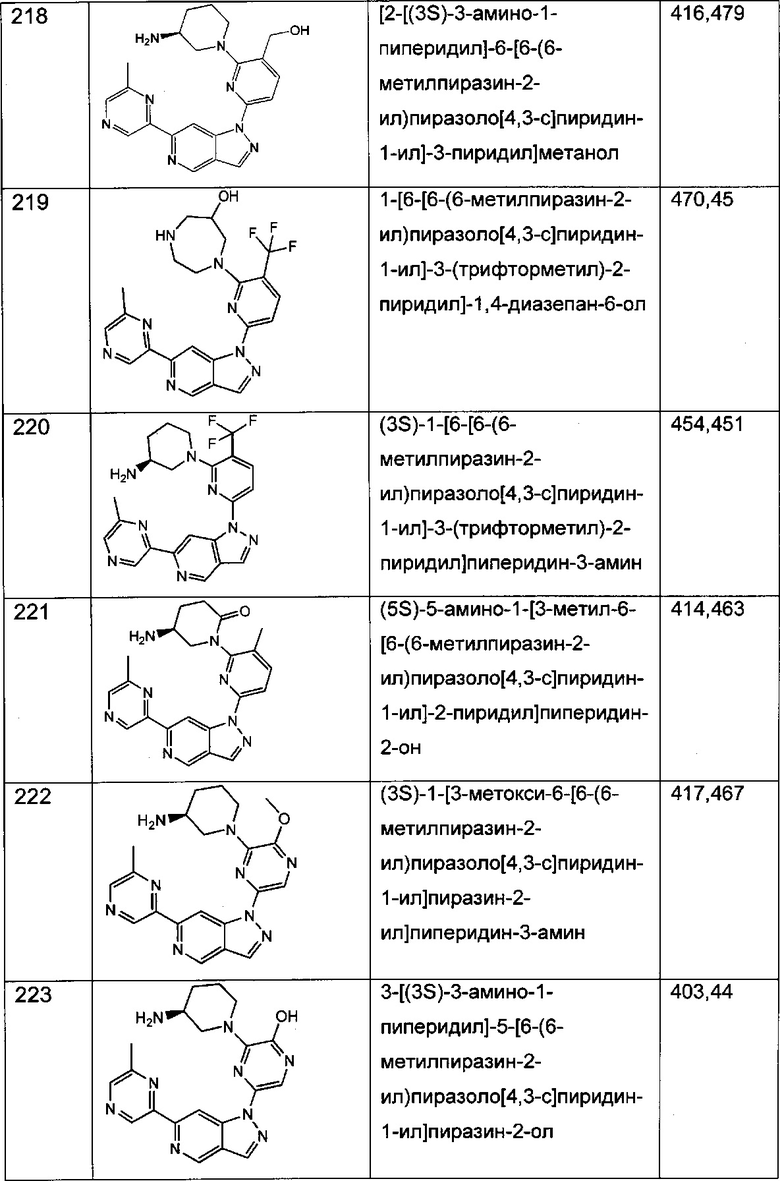
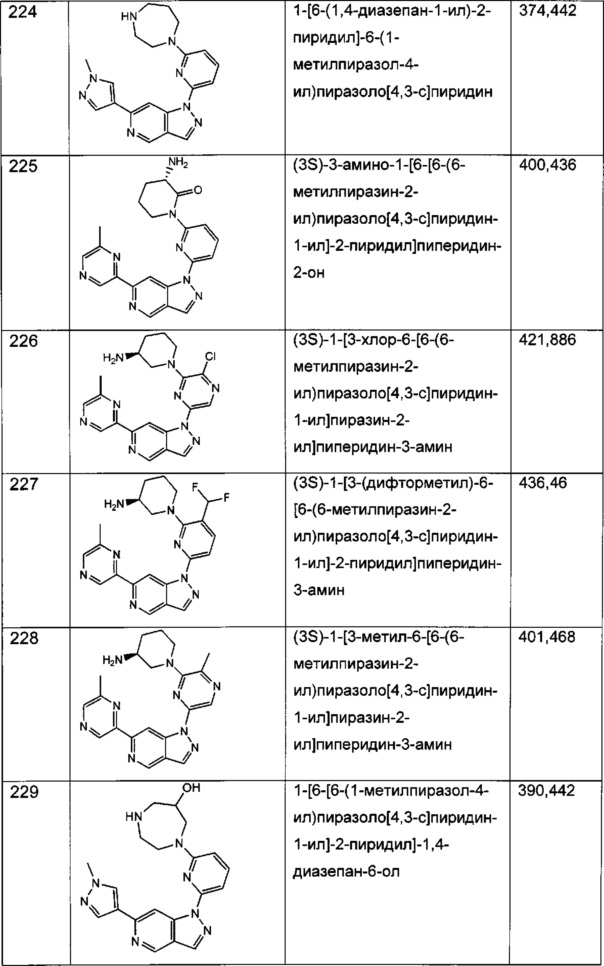
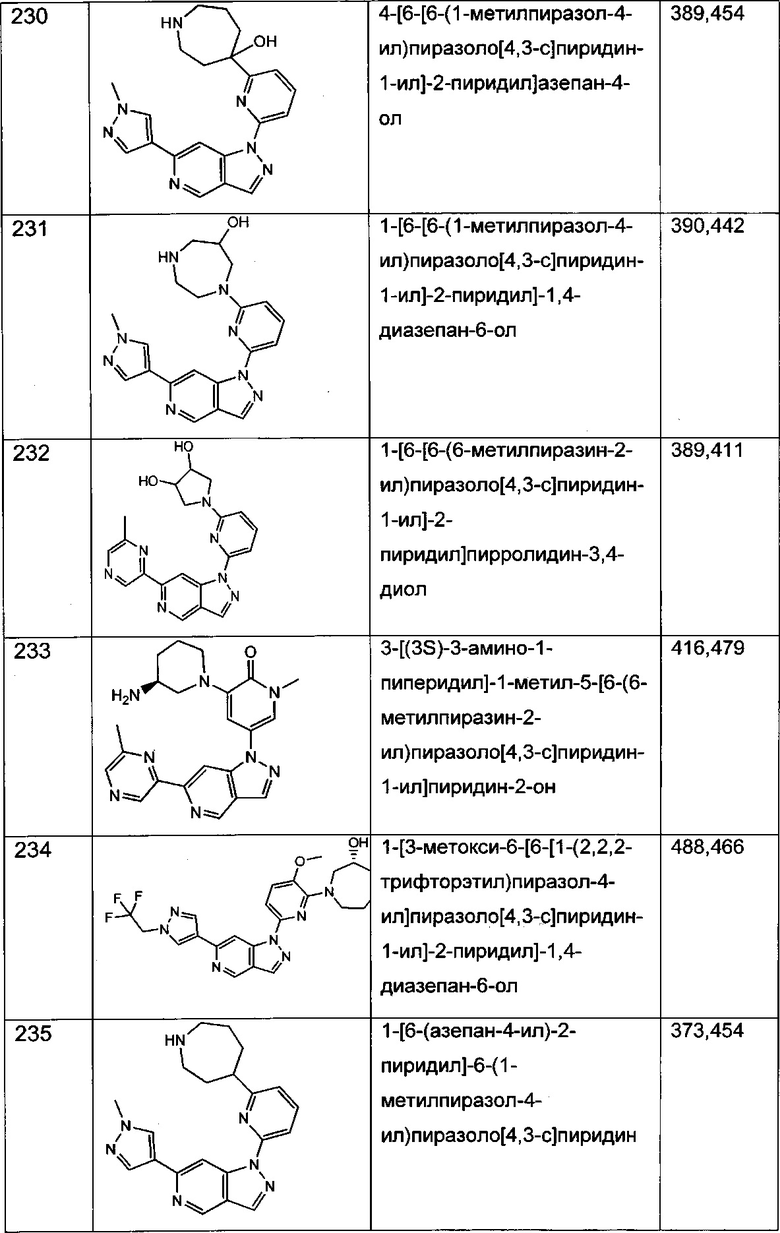
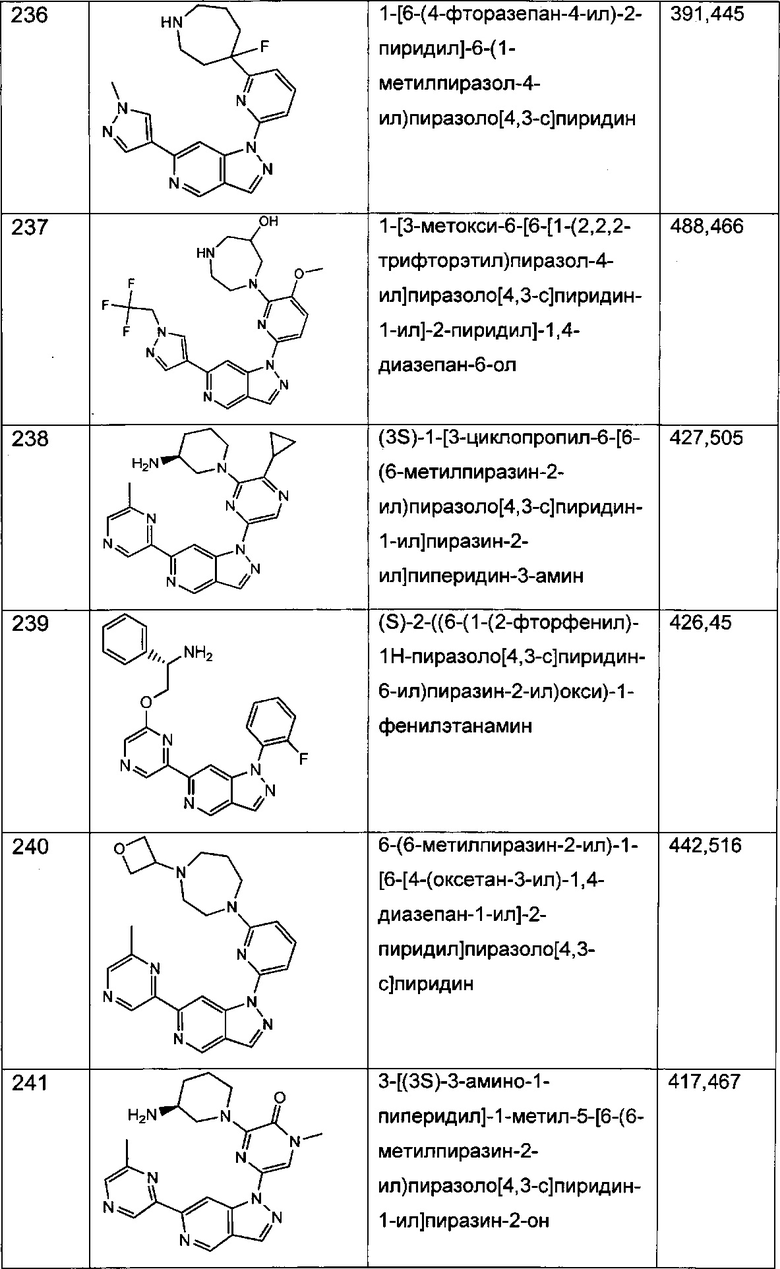
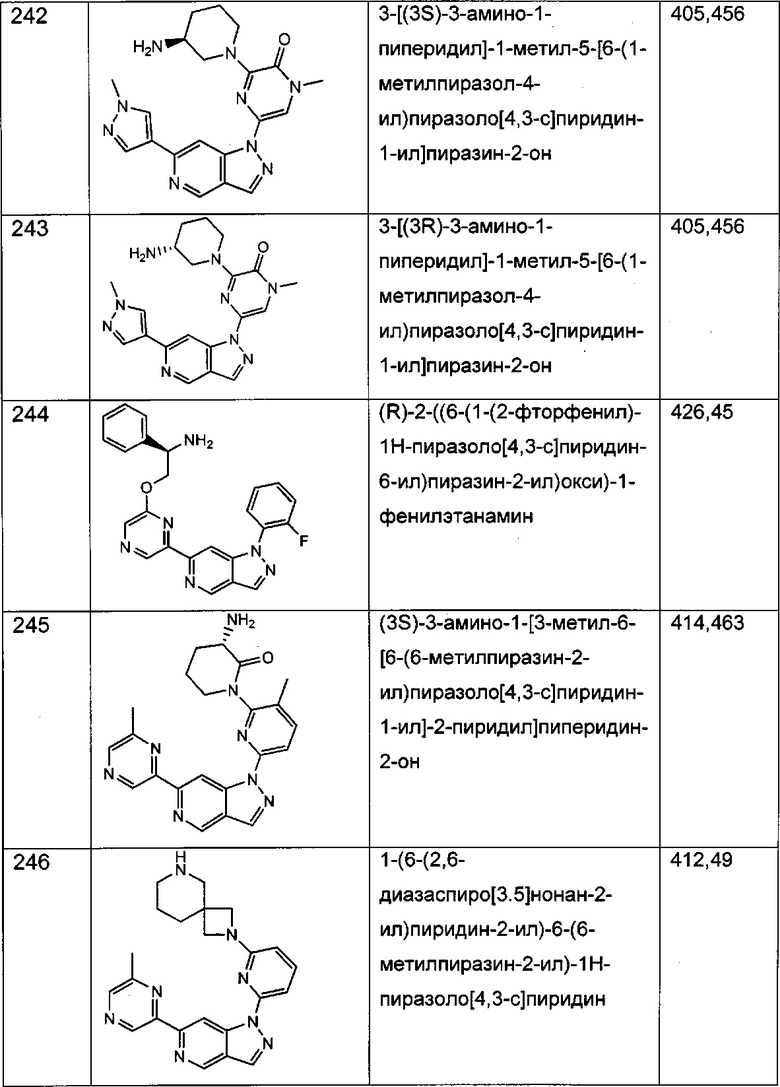
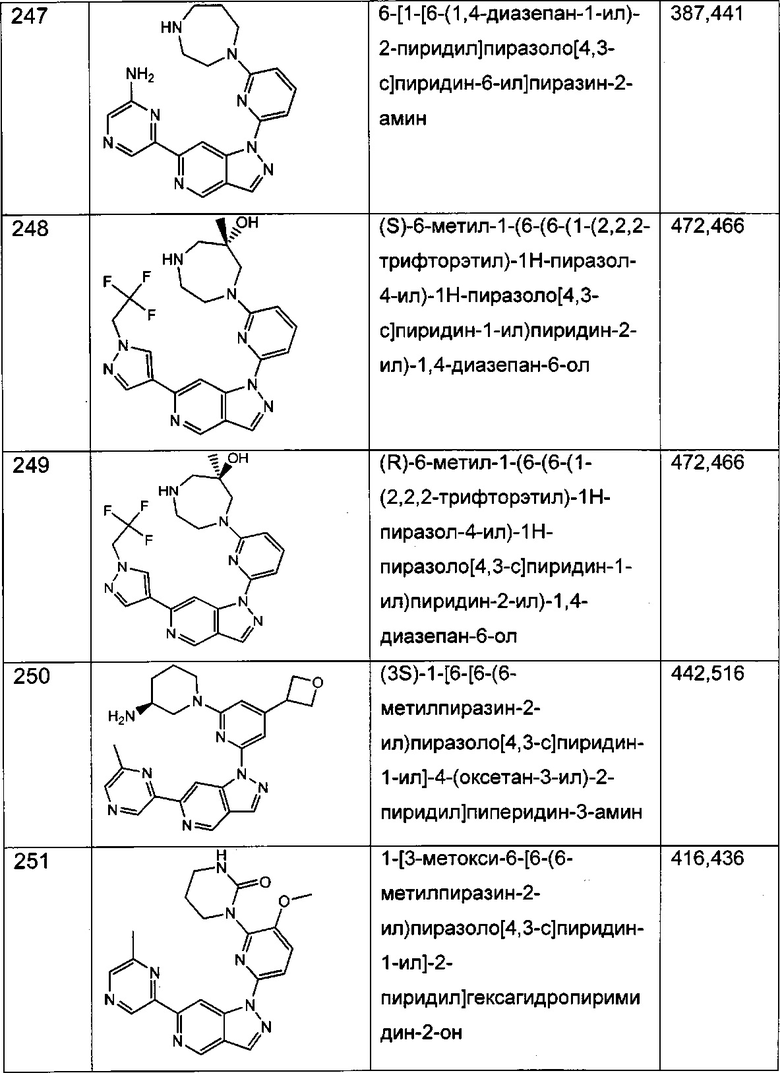
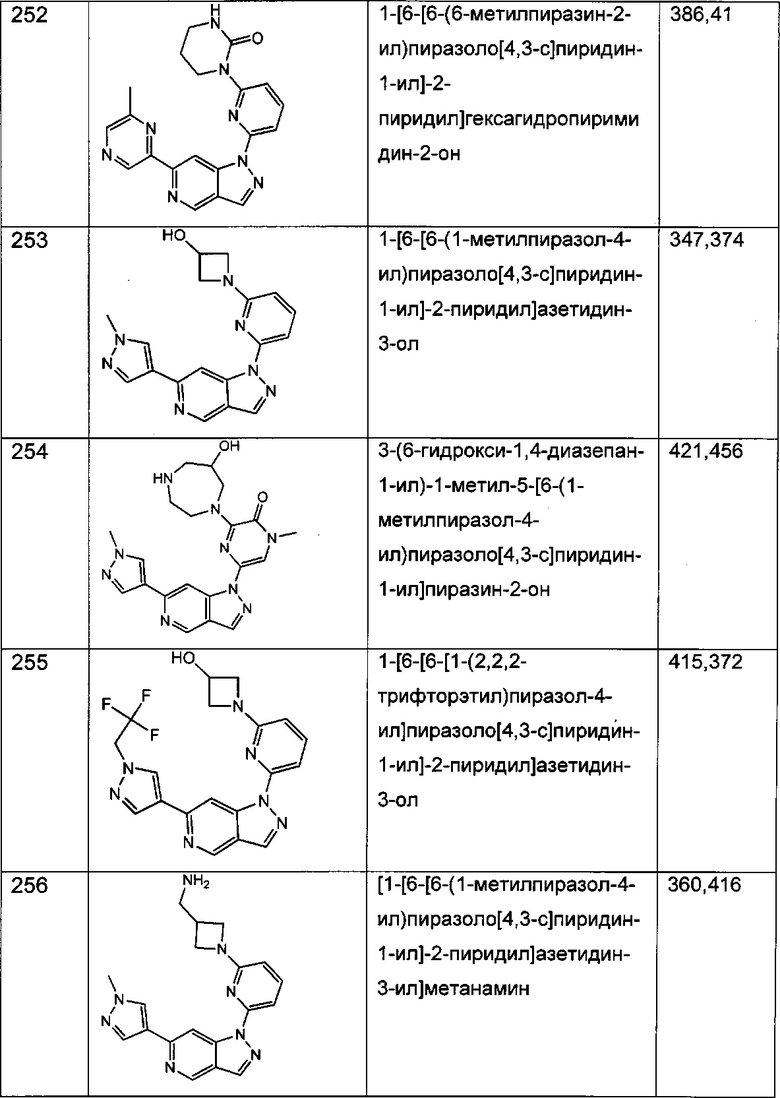
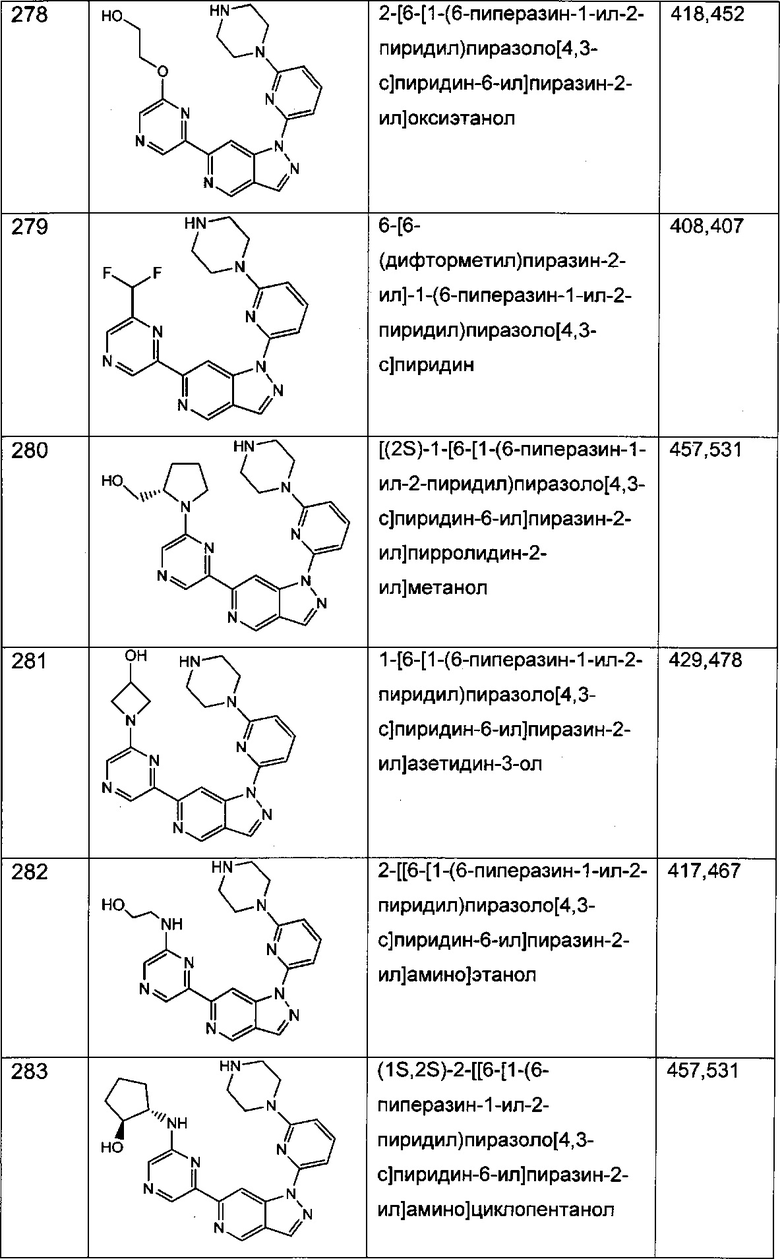
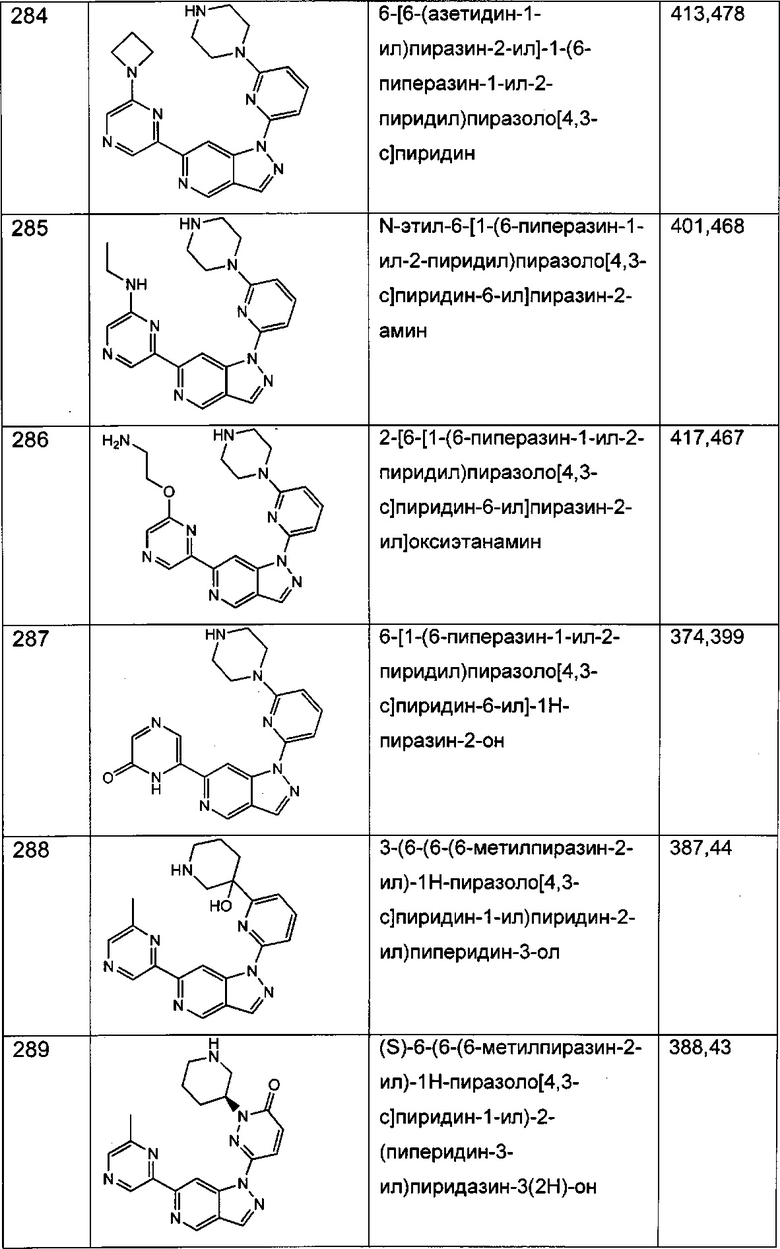
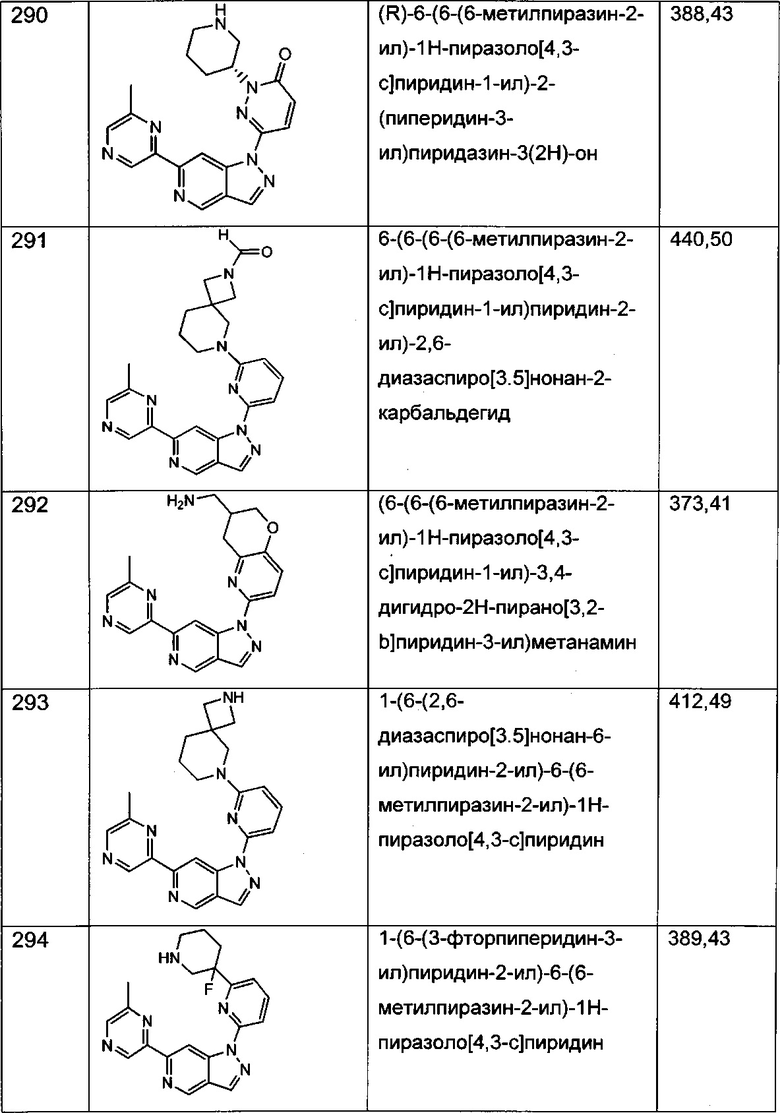
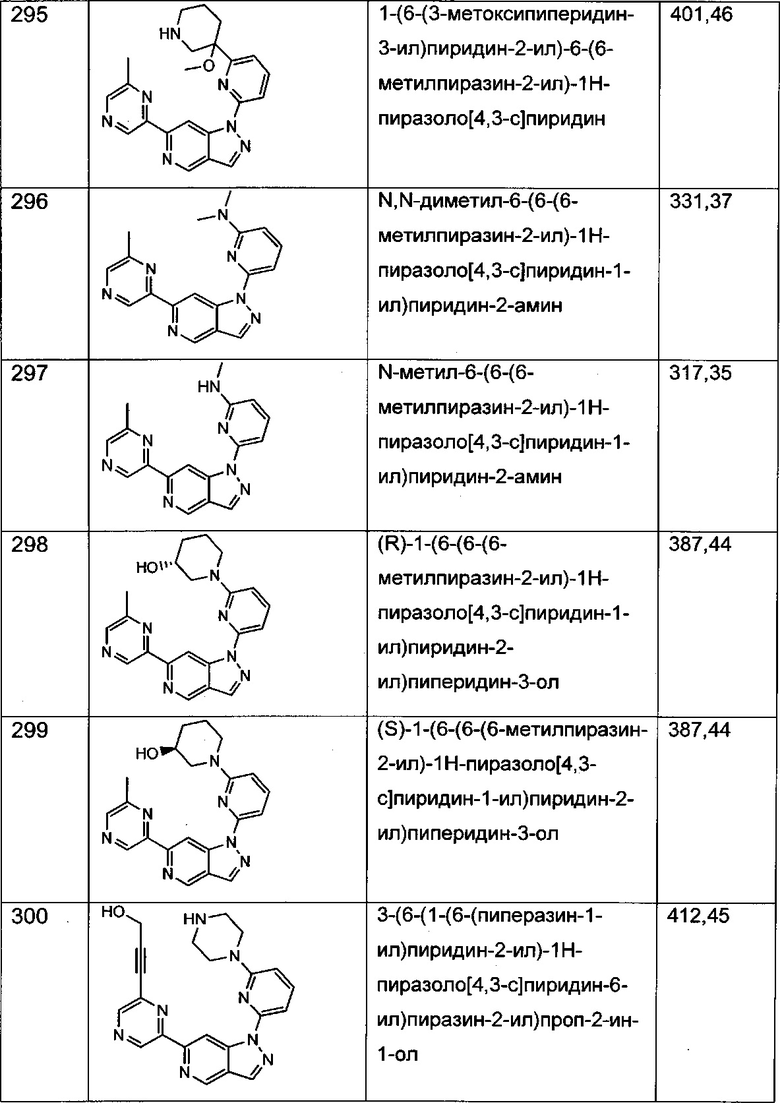
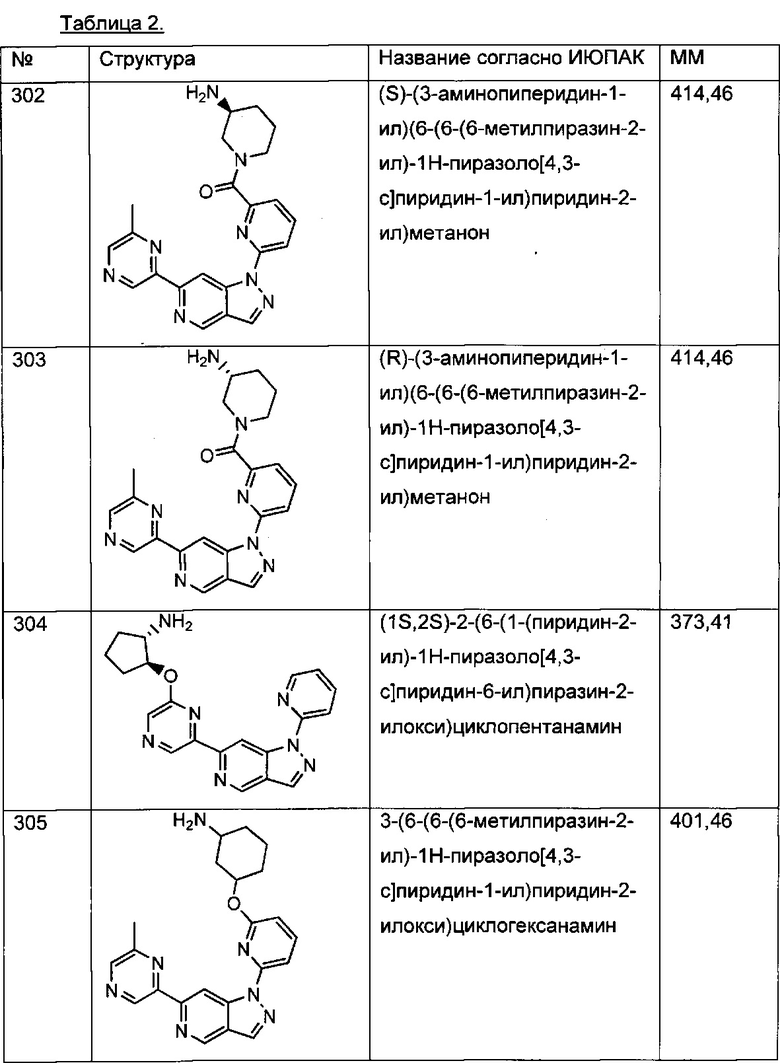
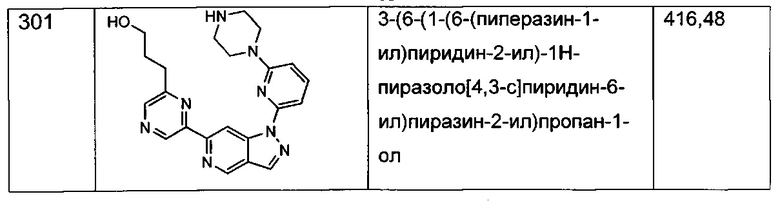
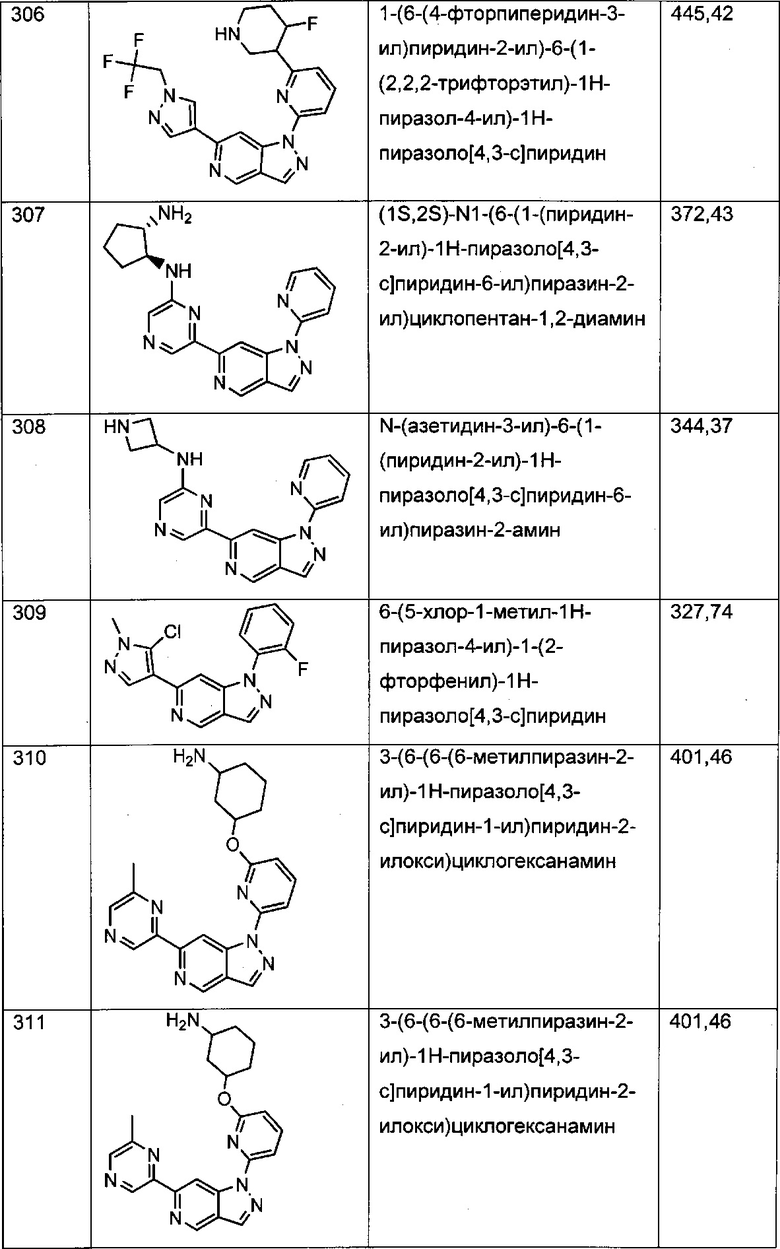
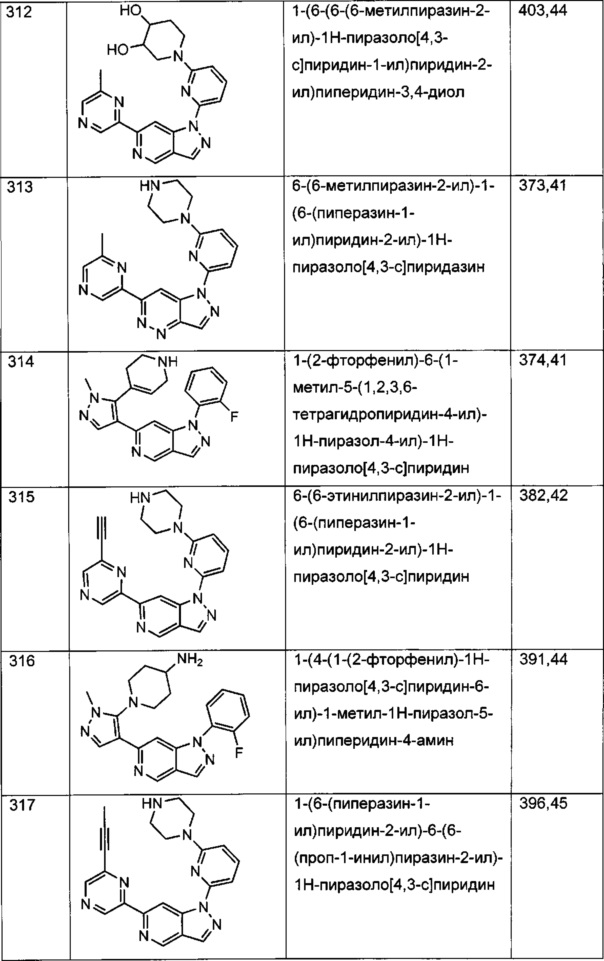
Настоящее изобретение включает композицию (например, фармацевтическую композицию), включающую соединение формулы I и/или его сольваты, гидраты и/или соли, и носитель (фармацевтически приемлемый носитель). Также настоящее изобретение включает композицию (например, фармацевтическую композицию), включающую соединение формулы I и/или его сольваты, гидраты и/или соли, и носитель (фармацевтически приемлемый носитель), дополнительно включающую второе химиотерапевтическое средство, такое как те, что описаны в этом документе. Настоящие композиции применяются для ингибирования аномального клеточного роста или лечения гиперпролиферативного заболевания, такого как рак, у млекопитающего (например, человека). Например, настоящие соединения и композиции применяются для лечения множественной миеломы, лимфомы, острого миелобластного лейкоза, рака предстательной железы, рака молочной железы, гепатоцеллюлярной карциномы, рака поджелудочной железы и/или колоректального рака у млекопитающего (например, человека).
Настоящее изобретение включает способ ингибирования аномального клеточного роста или лечения гиперпролиферативного заболевания, такого как рак, у млекопитающего (например, человека), согласно которому вводят указанному млекопитающему терапевтически эффективное количество соединения формулы I и/или его сольватов, гидратов и/или солей, или их композиции. Например, настоящее изобретение включает способ лечения множественной миеломы, лимфомы, острого миелобластного лейкоза, рака предстательной железы, рака молочной железы, гепатоцеллюлярной карциномы, рака поджелудочной железы и/или колоректального рака у млекопитающего (например, человека), согласно которому вводят указанному млекопитающему терапевтически эффективное количество соединения формулы I и/или его сольватов, гидратов и/или солей, или их композиции.
Настоящее изобретение включает способ ингибирования аномального клеточного роста или лечения гиперпролиферативного заболевания, такого как рак, у млекопитающего (например, человека), согласно которому вводят указанному млекопитающему терапевтически эффективное количество соединения формулы I и/или его сольватов, гидратов и/или солей, или их композиции в сочетании со вторым химиотерапевтическим средством, таким как те, что описаны в этом документе. Например, настоящее изобретение включает способ лечения множественной миеломы, лимфомы, острого миелобластного лейкоза, рака предстательной железы, рака молочной железы, гепатоцеллюлярной карциномы, рака поджелудочной железы и/или колоректального рака у млекопитающего (например, человека), согласно которому вводят указанному млекопитающему терапевтически эффективное количество соединения формулы I и/или его сольватов, гидратов и/или солей, или их композиции в сочетании со вторым химиотерапевтическим средством, таким как те, что описаны в этом документе.
Настоящее изобретение включает способ лечения лимфомы у млекопитающего (например, человека), согласно которому вводят указанному млекопитающему терапевтически эффективное количество соединения формулы I и/или его сольватов, гидратов и/или солей, или их композиции, либо отдельно, либо в сочетании со вторым химиотерапевтическим средством, таким как лекарственное средство на основе антител к анти-В-клеткам (например ритуксан и/или дацетузумаб), гемцитабин, кортикостероиды (например преднизолон и/или дексаметазон), смеси для химиотерапии (например CHOP (циклофосфамид, доксорубицин, винкристин, преднизолон) и/или ICE (ифосфамид, цитоксан, этопозид)), комбинация биопрепаратов и химиотерапии (например ритуксан-IСЕ, дацетузумаб-ритуксан-ICE, R-Gem и/или D-R-Gem), ингибитор Akt, ингибитор PI3K (например GDC-0941 (Genentech) и/или GDC-0980 (Genentech)), рапамицин, аналог рапамицина, ингибитор mTOR, такой как эверолимус или сиролимус, ингибитор МЕК (GDC-0973) и ингибитор Bcl-2 (АВТ-263 или АВТ-199).
Настоящее изобретение включает способ лечения множественной миеломы у млекопитающего (например, человека), согласно которому вводят указанному млекопитающему терапевтически эффективное количество соединения формулы I и/или его сольватов, гидратов и/или солей, или их композиции, либо отдельно, либо в сочетании со вторым химиотерапевтическим средством, таким как мелфалан, "Imids" (иммуномодуляторы, например талидомид, леналидомид и/или помалидомид), кортикостероиды (например дексаметазон и/или преднизолон) и бортезомиб, или другой ингибитор протеасом.
Настоящее изобретение включает способ лечения множественной миеломы, хронического лимфоцитарного лейкоза (ХЛЛ) или острого миелобластного лейкоза (ОМЛ) у млекопитающего (например, человека), согласно которому вводят указанному млекопитающему терапевтически эффективное количество соединения формулы I и/или его сольватов, гидратов и/или солей, или их композиции, либо отдельно, либо в сочетании со вторым химиотерапевтическим средством, таким как цитарабин (агаС), антрациклины (например даунорубицин и/или идарубицин), анти-миелоидные терапевтические средства на основе антител (например SGN-33), анти-миелоидные конъюгаты антитело-лекарственное средство (например MYLOTARG®).
Настоящее изобретение включает способ лечения хронического лимфоцитарного лейкоза (ХЛЛ) у млекопитающего (например, человека), согласно которому вводят указанному млекопитающему терапевтически эффективное количество соединения формулы I и/или его сольватов, гидратов и/или солей, или их композиции, либо отдельно, либо в сочетании со вторым химиотерапевтическим средством, таким как флударабин, циклофосфамид, терапевтические средства на основе антител к анти-В-клеткам (например ритуксан и/или дацетузумаб).
Настоящее изобретение включает способ лечения хронического миелобластного лейкоза (ХМЛ) у млекопитающего (например, человека), согласно которому вводят указанному млекопитающему терапевтически эффективное количество соединения формулы I и/или его сольватов, гидратов и/или солей, или их композиции, либо отдельно, либо в сочетании со вторым химиотерапевтическим средством, таким как ингибитор BCR-abl (например, иматиниб, нилотиниб и/или дазатиниб).
Настоящее изобретение включает способ лечения миелодиспластических заболеваний (МДС) и миелопролиферативных заболеваний, включая истинную полицитемию (ИП), эссенциальную тромбоцитемию (ЭТ) или миелофиброз (МФ), у млекопитающего (например, человека), согласно которому вводят указанному млекопитающему терапевтически эффективное количество соединения формулы I и/или его сольватов, гидратов и/или солей, или их композиции, либо отдельно, либо в сочетании.
Настоящее изобретение включает способ применения настоящих соединений в in vitro, in situ и in vivo диагностике или лечении клеток млекопитающих, организмов или связанных патологических состояний.
Введение соединений по настоящему изобретению (далее "активное соединение(я)") может быть выполнено любым способом, который позволяет доставить соединения к месту действия. Эти способы включают пероральные способы, интрадуоденальные способы, парентеральную инъекцию (включая внутривенную, подкожную, внутримышечную, внутрисосудистую или вливание), местное, путем ингаляции и ректальное введение.
Количество вводимого активного соединения будет зависеть от объекта, подвергаемого лечению, тяжести заболевания или состояния, скорости введения, распределения соединения и выбора лечащего врача. Однако эффективная доза находится в диапазоне от приблизительно 0,001 до приблизительно 100 мг на кг массы тела в день, предпочтительно от приблизительно 1 до приблизительно 35 мг/кг/день, в виде однократных или дробных доз. Для человека весом 70 кг это будет количество от приблизительно 0,05 до 7 г/день, предпочтительно от приблизительно 0,05 до приблизительно 2,5 г/день. В некоторых случаях уровни дозировок ниже нижнего предела вышеуказанного диапазона могут быть более подходящими, при этом в других случаях еще большие дозы можно использовать, не вызывая вредного побочного эффекта, при условии, что подобные большие дозы сначала разделяют на несколько малых доз для введения в течение дня.
Активное соединение можно применять в виде монотерапии или в сочетании с одним или более химиотерапевтическими средствами, например, теми, что описаны в этом документе. Подобное объединенное лечение может быть выполнено посредством одновременного, последовательного или раздельного дозирования отдельных компонентов лечения.
Например, фармацевтическая композиция может находиться в форме, подходящей для перорального введения, такой как таблетка, капсула, пилюля, порошок, составы с замедленным высвобождением, раствор, суспензия для парентеральной инъекции в виде стерильного раствора, суспензия или эмульсия для местного введения в виде мази или крема, или для ректального введения в виде суппозитория. Фармацевтическая композиция может находиться в стандартных лекарственных формах, подходящих для однократного введения точных доз. Фармацевтическая композиция включает традиционный фармацевтический носитель или эксципиент и соединение по изобретению в виде активного ингредиента. Кроме того, она может включать другие лекарственные или фармацевтические агенты, носители, адъюванты и т.п.
Примерные формы для парентерального введения включают растворы или суспензии соединений формулы I в стерильных водных растворах, например, водных пропиленгликолевых или декстрозных растворах. Подобные лекарственные формы при необходимости могут быть соответствующим образом буферизованы.
Подходящие фармацевтические носители включают инертные разбавители или наполнители, воду и разные органические растворители. При необходимости фармацевтические композиции могут содержать дополнительные компоненты, такие как ароматизаторы, связующие вещества, эксципиенты и подобные. Таким образом для перорального введения можно использовать таблетки, содержащие разные эксципиенты, такие как лимонная кислота, вместе с разными разрыхлителями, такими как крахмал, альгиновая кислота и конкретные комплексные силикаты, и со связующими веществами, такими как сахароза, желатин и акация. Дополнительно смазывающие вещества, такие как стеарат магния, лаурилсульфат натрия и тальк, часто используют в процессах таблетирования. Твердые композиции подобного вида также можно использовать в мягких и твердых заполненных желатиновых капсулах. Следовательно, предпочтительные вещества включают лактозу или молочный сахар и высокомолекулярные полиэтиленгликоли. Когда для перорального введения необходимы водные суспензии или эликсиры, тогда активное соединение можно объединить с разными подсластителями или ароматизаторами, окрашивающими или красящими веществами и при необходимости эмульгирующими веществами или суспендирующими веществами вместе с разбавителями, такими как вода, этанол, пропиленгликоль, глицерин, или их сочетания.
Способы получения разных фармацевтических композиций с конкретным количеством активного соединения известны или будут очевидны квалифицированным специалистам в данной области техники. Смотрите, например, Remington's Pharmaceutical Sciences, Mack Publishing Company, Ester, Pa., 15.sup.th Edition (1975).
Введение соединений формулы I
Соединения формулы I по изобретению могут быть введены любым способом, подходящим для состояния, подвергаемого лечению. Подходящие способы включают пероральное, парентеральное (включая подкожное, внутримышечное, внутривенное, внутриартериальное, внутрикожное, интратекальное и эпидуральное), трансдермальное, ректальное, назальное, местное (включая буккальное и подъязычное), вагинальное, интраперитонеальное, внутрилегочное и интраназальное. Для местной иммуносупрессивной терапии соединения могут быть введены в ходе внутриочагового введения, включая перфузируемое или иное взаимодействие трансплантата с ингибитором перед трансплантацией. Следует иметь в виду, что предпочтительный способ может меняться в зависимости от, например, состояния реципиента. Когда соединение вводят перорально, оно может быть разработано в виде пилюли, капсулы, таблетки и т.п.с фармацевтически приемлемым носителем или эксципиентом. Когда соединение вводят парентерально, оно может быть разработано с фармацевтически приемлемым парентеральным наполнителем и в стандартной инъекционной лекарственной форме, как подробно описано ниже.
Доза для лечения больных людей может находиться в диапазоне от приблизительно 10 мг до приблизительно 1000 мг соединения формулы I. Обычная доза может составлять от приблизительно 100 мг до приблизительно 300 мг соединения. Дозу можно вводить один раз в день (QID), два раза в день (BID) или чаще, в зависимости от фармакокинетических и фармакодинамических свойств, включая абсорбцию, распределение, метаболизм и выведение конкретного соединения. Кроме того, факторы токсичности могут влиять на режим дозирования и введения. При пероральном введении пилюлю, капсулу или таблетку можно глотать ежедневно или реже в течение определенного срока. Схему можно повторять в течение ряда циклов терапии.
Способы лечения соединениями формулы I
Соединения по настоящему изобретению используются для лечения гиперпролиферативных заболеваний, состояний и/или расстройств, включая, но не ограничиваясь этим, те, что характеризуются сверхэкспрессией киназ Pim, например, киназ Pim-1, Pim-2 и Pim-3. Таким образом, другой аспект данного изобретения включает способы лечения или предотвращения заболеваний или состояний, которые можно лечить или предотвращать ингибированием киназы Pim. В одном воплощении согласно способу вводят млекопитающему, нуждающемуся в этом, терапевтически эффективное количество соединения формулы I или его стереоизомера, геометрического изомера, таутомера или фармацевтически приемлемой соли. В одном воплощении больного человека лечат соединением формулы I и фармацевтически приемлемым носителем, адъювантом или наполнителем, где указанное соединение формулы I находится в количестве, которое определяемо ингибирует активность киназы Pim.
Виды рака, которые можно лечить согласно способам по данному изобретению, включают, но не ограничиваются этим, рак молочной железы, яичника, шейки матки, предстательной железы, семенника, мочеполового тракта, пищевода, гортани, глиобластому, нейробластому, желудка, кожи, кератоакантому, легкого, плоскоклеточную карциному, крупноклеточную карциному, немелкоклеточную карциному легкого (НМКЛ), мелкоклеточную карциному, аденокарциному легкого, кости, толстой кишки, аденому, поджелудочной железы, аденокарциному, щитовидной железы, фолликулярную карциному, недифференцированную карциному, папиллярную карциному, семиному, меланому, саркому, карциному мочевого пузыря, карциному печени и желчного протока, карциному почки, миелоидные заболевания, лимфоидные заболевания, "волосатых" клеток, ротовой полости и глотки (ротовой), губ, языка, рта, глотки, тонкой кишки, ободочной и прямой кишки, задней кишки, прямой кишки, головного мозга и центральной нервной системы, болезнь Ходжкина и лейкоз.
Согласно другому аспекту данного изобретения предложено соединение по этому изобретению для применения в лечении заболеваний или состояний, описанных в этом документе, у млекопитающего, например, человека, страдающего от подобного заболевания или состояния. Также предложено применение соединения по данному изобретению при получении лекарства для лечения заболеваний и состояний, описанных в этом документе, у теплокровного животного, такого как млекопитающее, например, человек, страдающего от подобного заболевания.
Фармацевтические композиции
Чтобы использовать соединение формулы I для терапевтического лечения (включая профилактическое лечение) млекопитающих, включая людей, его обычно разрабатывают в соответствии со стандартной фармацевтической практикой в виде фармацевтической композиции. Согласно данному аспекту изобретения предложена фармацевтическая композиция, включающая соединение по данному изобретению вместе с фармацевтически приемлемым разбавителем или носителем.
Обычный препарат получают, смешивая соединение формулы I и носитель, разбавитель или эксципиент.Подходящие носители, разбавители и эксципиенты хорошо известны квалифицированным специалистам в данной области техники и включают вещества, такие как углеводы, воски, водорастворимые и/или поддающиеся разбуханию полимеры, гидрофильные или гидрофобные вещества, желатин, масла, растворители, вода и подобные. Конкретный используемый носитель, разбавитель или эксципиент будет зависеть от способов и цели, с которой применяют соединение по настоящему изобретению. Обычно растворители выбирают, основываясь на растворителях, известных квалифицированным специалистам в данной области техники как безопасные (GRAS) для введения млекопитающему. В общем безопасные растворители являются нетоксичными водными растворителями, такими как вода, и другими нетоксичными растворителями, которые растворимы или смешиваются с водой. Подходящие водные растворители включают воду, этанол, пропиленгликоль, полиэтиленгликоли (например, ПЭГ 400, ПЭГ 300) и т.п., и их смеси. Также препараты могут включать один или более буферов, стабилизирующих агентов, поверхностно-активных веществ, смачивающих веществ, смазывающих веществ, эмульгаторов, суспендирующих агентов, консервантов, антиоксидантов, кроющих агентов, скользящих веществ, вспомогательных веществ, красителей, подсластителей, ароматизирующих агентов, вкусовых агентов и других известных добавок для получения превосходного представления лекарства (т.е. соединения по настоящему изобретению или его фармацевтической композиции) или помощи при изготовлении фармацевтического продукта (т.е. лекарства).
Композиции можно получить, используя традиционные методики растворения и смешивания. Например, нерасфасованное лекарственное вещество (т.е. соединение по настоящему изобретению или устойчивую форму соединения формулы I (например, комплекс с производным циклодекстрина или другим известным комплексообразующим агентом) растворяют в подходящем растворителе в присутствии одного или более описанных выше эксципиентов. Соединение по настоящему изобретению обычно изготавливают в фармацевтических лекарственных формах, чтобы получить легко регулируемую дозировку лекарства, и чтобы способствовать соблюдению пациентом предписанной схемы лечения.
Фармацевтическая композиция (или препарат) для применения может быть упакована разными способами в зависимости от способа, используемого для введения лекарства. Как правило изделие для распространения включает контейнер со вложенным в него фармацевтическим препаратом в подходящей форме. Подходящие контейнеры хорошо известны квалифицированным специалистам в данной области техники и включают материалы, такие как флаконы (пластмассовые и стеклянные), пакетики, ампулы, пластиковые пакеты, металлические цилиндры и подобные. Также контейнер может включать систему, защищающую от несанкционированного вскрытия, для предотвращения неосторожного доступа к содержимому упаковки. Кроме того, в контейнер вложена этикетка, которая описывает содержимое контейнера. Также этикетка может включать соответствующие предупреждения.
Фармацевтические композиции соединений по настоящему изобретению можно получить для разных способов и видов введения. Например, соединение формулы I, имеющее требуемую степень чистоты, может быть смешано с фармацевтически приемлемыми разбавителями, носителями, эксципиентами или стабилизаторами (Remington's Pharmaceutical Sciences (1980) 16th edition, Osol, A. Ed.) в форме лиофилизированного препарата, размолотого порошка или водного раствора. Препарат может быть получен путем смешивания при температуре окружающей среды при соответствующем рН и при необходимой степени чистоты с физиологически приемлемыми носителями, т.е. носителями, которые не токсичны к реципиентам при используемых дозировках и концентрациях. рН препарата зависит главным образом от конкретного использования и концентрации соединения, но может находиться в диапазоне от приблизительно 3 до приблизительно 8. Препарат в ацетатном буфере при рН 5 является подходящим воплощением.
Соединение по данному изобретению для применения согласно этому документу предпочтительно является стерильным. В частности, препараты, которые используют при in vivo введении, должны быть стерильными. Подобное обеззараживание легко выполнить в ходе фильтрации через стерилизующие фильтрующие мембраны.
Как правило соединение можно хранить в виде твердой композиции, лиофилизированного препарата или в виде водного раствора.
Фармацевтические композиции по изобретению, включающие соединение формулы I, разрабатывают, дозируют и вводят некоторым образом, т.е. количества, концентрации, схемы, курс лечения, наполнители и способ введения согласуются с надлежащей медицинской практикой. Факторы, рассматриваемые в этой связи, включают конкретное заболевание, подвергаемое лечению, конкретное млекопитающее, подвергаемое лечению, клиническое состояние отдельного пациента, причину заболевания, место доставки вещества, способ введения, планирование введения и другие факторы, известные практикующим врачам. "Терапевтически эффективное количество" соединения, которое вводят, будет зависеть от подобных обстоятельств, и является минимальным количеством, необходимым для предотвращения, улучшения или лечения заболевания, опосредованного фактором свертывания крови. Подобное количество является предпочтительно ниже количества, которое токсично для организма или делает организм 3Начительно более чувствительным к кровотечению.
В качестве общей нормы первоначальное фармацевтически эффективное количество соединения формулы I, вводимого парентерально, на дозу находится в диапазоне приблизительно 0,01-100 мг/кг, а именно приблизительно 0,1 до 20 мг/кг массы тела пациента в день, с обычным первоначальным диапазоном используемого соединения от 0,3 до 15 мг/кг/день.
Приемлемые разбавители, носители, эксципиенты и стабилизаторы не токсичны к реципиентам при используемых дозах и концентрациях и включают буферы, такие как фосфат, цитрат и других органических кислот; антиоксиданты, включая аскорбиновую кислоту и метионин; консерванты (такие как октадецилдиметилбензиламмония хлорид; гексаметония хлорид; бензалкония хлорид, бензетония хлорид; фенол, бутиловый или бензиловый спирт; алкилпарабены, такие как метил или пропилпарабен; катехин; резорцин; циклогексанол; 3-пентанол; и м-крезол); низкомолекулярные (менее чем приблизительно 10 остатков) полипептиды; белки, такие как сывороточный альбумин, желатин или иммуноглобулины; гидрофильные полимеры, такие как поливинилпирролидон; аминокислоты, такие как глицин, глутамин, аспарагин, гистидин, аргинин или лизин; моносахариды, дисахариды и другие углеводы, включая глюкозу, маннозу или декстрины; хелатообразующие агенты, такие как ЭДТА; сахара, такие как сахароза, маннит, трегалоза или сорбит; солеобразующие противоионы, такие как натрий; металлокомплексы (например Zn-протеиновые комплексы); и/или неионные поверхностно-активные вещества, такие как TWEEN™, PLURONICS™ или полиэтиленгликоль (ПЭГ). Активные фармацевтические компоненты также могут быть помещены в микрокапсулы, полученные, например, в ходе методик коацервации или межфазной полимеризацией, например, гидроксиметилцеллюлозные или желатиновые микрокапсулы и поли-(метилметакрилат) микрокапсулы, соответственно, в коллоидные системы доставки лекарства (например, липосомы, альбуминовые микросферы, микроэмульсии, наночастицы и нанокапсулы) или в макроэмульсии. Подобные методики раскрыты в Remington's Pharmaceutical Sciences 16th edition, Osol, A. Ed. (1980).
Можно получить препараты соединений формулы I с замедленным высвобождением. Подходящие примеры препаратов с замедленным высвобождением включают полупроницаемые матрицы из твердых гидрофобных полимеров, содержащие соединение формулы I, матрицы находятся в форме формованных изделий, например, пленок или микрокапсул. Примеры матриц с замедленным высвобождением включают полиэфиры, гидрогели (например, поли(2-гидроксиэтил-метакрилат) или поливиниловый спирт)), полилактиды (US 3773919), сополимеры L-глутаминовой кислоты и гамма-этил-L-глутамата, неразлагающийся этиленвинилацетат, разлагаемые сополимеры молочной кислоты-гликолевой кислоты, такие как LUPRON DEPOT™ (инъецируемые микросферы, состоящие из сополимера молочной кислоты-гликолевой кислоты и лейпролида ацетата), и поли-D-(-)-3-гидроксимасляную кислоту.
Препараты включают те, что подходят для способов введения, подробно описанных в этом документе. Препараты могут быть удобно представлены в стандартной лекарственной форме, и они могут быть получены любым из способов, хорошо известных в области фармацевтики. Главным образом методики и препараты находятся в Remington's Pharmaceutical Sciences (Mack Publishing Co., Easton, PA). Подобные методики включают стадию объединения активного ингредиента с носителем, который составляет один или более вспомогательных ингредиентов. В общем препараты получают, равномерно и тщательно объединяя активный ингредиент с жидкими носителями или тонкоизмельченными твердыми носителями, или обоими, и затем при необходимости придавая форму продукту.
Препараты соединения формулы I, подходящие для перорального введения, можно получить в виде дискретных единиц, таких как пилюли, капсулы, облатки или таблетки, которые содержат предварительно установленное количество соединения формулы I.
Спрессованные таблетки можно получить, сжимая на подходящем аппарате активный ингредиент в сыпучей форме, такой как порошок или гранулы, возможно смешанный со связующим веществом, скользящим веществом, инертным разбавителем, консервантом, поверхностно-активным или диспергирующим веществом. Сформованные таблетки можно получить, формируя на подходящем аппарате смесь порошкообразного активного ингредиента, смоченного инертным жидким разбавителем. Таблетки могут быть покрыты слоем или разделены рисками, и возможно получены таким образом, чтобы обеспечить замедленное или контролируемое высвобождение активного ингредиента из них.
Таблетки, пастилки, леденцы, водные или масляные суспензии, диспергируемые порошки или гранулы, эмульсии, твердые или мягкие капсулы, например, желатиновые капсулы, сиропы или эликсиры можно подготовить для перорального использования. Препараты соединений формулы I, предназначенные для перорального использования, можно получить согласно любому способу, известному в данной области техники для изготовления фармацевтических композиций, и подобные композиции могут содержать один или более агентов, включая подсластители, ароматизаторы, красители и консерванты, для получения приятного на вкус препарата. Приемлемыми являются таблетки, содержащие активный ингредиент в смеси с нетоксичным фармацевтически приемлемым эксципиентом, который подходит для изготовления таблеток. Эти эксципиенты, например, могут представлять собой инертные разбавители, такие как карбонат кальция или натрия, лактоза, фосфат кальция или натрия; гранулирующие агенты и разрыхлители, такие как кукурузный крахмал или альгиновая кислота; связующие агенты, такие как крахмал, желатин или акация; и смазывающие вещества, такие как стеарат магния, стеариновая кислота или тальк. Таблетки могут быть не покрыты оболочкой или могут быть покрыты оболочкой известными методиками, включая микроинкапсулирование, чтобы замедлить разрушение и всасывание в желудочно-кишечном тракте и, следовательно, обеспечить пролонгированное действие в течение длительного периода. Например, можно использовать замедляющее вещество, такое как глицерилмоностеарат или глицерилдистеарат, отдельно или с воском.
Для лечения глаз или других наружных тканей, например, рта и кожи, препараты предпочтительно используют в виде местной мази или крема, содержащего активный ингредиент(ы) в количестве, например, 0,075 до 20% масс/масс. При изготовлении мази активные ингредиенты можно использовать либо с парафиновой, либо водорастворимой мазевой основой. Альтернативно, активные ингредиенты можно приготовить в креме с основой для крема "масло в воде".
При необходимости водная фаза основы для крема может включать многоатомный спирт, т.е. спирт, содержащий две или более гидроксильных групп, такой как пропиленгликоль, бутан-1,3-диол, маннит, сорбит, глицерин и полиэтиленгликоль (включая ПЭГ 400), и их смеси. Препараты для наружного применения желательно могут включать соединение, которое усиливает всасывание или проникновение активного ингредиента через кожу или другие поврежденные области. Примеры подобных усилителей проникновения через кожу включают диметилсульфоксид и родственные аналоги.
Масляная фаза эмульсий по данному изобретению может состоять из известных ингредиентов известным образом. Несмотря на то, что фаза может содержать только эмульгатор, она также может включать смесь по меньшей мере одного эмульгатора и жира или масла, или как жира, так и масла. Гидрофильный эмульгатор, включенный вместе с липофильным эмульгатором, может действовать как стабилизатор. Вместе эмульгатор(ы) с или без стабилизатора(ов) составляют так называемый эмульгирующий воск, и воск вместе с маслом и жиром составляет так называемую эмульгирующую мазевую основу, которая образует масляную дисперсную среду кремовых препаратов. Эмульгаторы и стабилизаторы эмульсии, подходящие для применения при изготовлении препарата по изобретению, включают Tween® 60, Span® 80, цетостеариловый спирт, бензиловый спирт, миристиловый спирт, глицерил моностеарат и лаурилсульфат натрия.
Водные суспензии соединений формулы I содержат активные вещества в смеси с эксципиентами, подходящими для изготовления водных суспензий. Подобные эксципиенты включают суспендирующий агент, такой как карбоксиметилцеллюлоза натрия, кроскармеллоза, повидон, метилцеллюлоза, гидроксипропилметилцеллюлоза, альгинат натрия, поливинилпирролидон, трагакантовая камедь и аравийская камедь, и диспергирующие или увлажняющие агенты, такие как встречающийся в природе фосфатид (например лецитин), продукт конденсации алкиленоксида с жирной кислотой (например полиоксиэтилена стеарат), продукт конденсации этиленоксида с длинноцепочечным алифатическим спиртом (например
гептадекаэтиленоксицетанол), продукт конденсации этиленоксида с неполным эфиром, полученным из жирной кислоты и ангидрида гексита (например полиоксиэтилен сорбитан моноолеат). Также водная суспензия может содержать один или более чем один консервант, такой как этил или н-пропил п-гидроксибензоат, один или более чем один краситель, один или более чем один ароматизатор и один или более чем один подсластитель, такой как сахароза или сахарин.
Фармацевтические композиции соединений формулы I могут находиться в форме стерильного инъекционного препарата, такого как стерильная инъекционная водная или масляная суспензия. Эта суспензия может быть создана в соответствии с известной областью техники, используя те подходящие диспергирующие или увлажняющие агенты и суспендирующие агенты, которые были упомянуты выше. Стерильный инъекционный препарат также может представлять собой стерильный инъекционный раствор или суспензию в нетоксичном парентерально приемлемом разбавителе или растворителе, таком как 1,3-бутандиол. Стерильный инъекционный препарат также может быть получен в виде лиофилизированного порошка. Приемлемыми наполнителями и растворителями, которые можно использовать, являются вода, раствор Рингера и изотонический раствор хлорида натрия. Кроме того, обычно можно использовать стерильные жирные масла в качестве растворителя или суспендирующей среды. С этой целью можно использовать безвкусное жирное масло, включая синтетические моно- или диглицериды. Кроме того, жирные кислоты, такие как олеиновая кислота, можно использовать подобным образом при получении инъекционных препаратов.
Количество активного ингредиента, которое можно объединить с носителем для получения однократной лекарственной формы, будет изменяться в зависимости от подвергаемого лечению организма и конкретного способа введения. Например, препарат с замедленным высвобождением, предназначенный для перорального введения людям, может содержать приблизительно 1 до 1000 мг активного вещества, объединенного с соответствующим и подходящим количеством носителя, которое может изменяться от приблизительно 5 до приблизительно 95% от всего состава (масса:масса). Фармацевтическую композицию можно приготовить для получения легко измеряемых количеств для введения. Например, водный раствор, предназначенный для внутривенного вливания, может содержать от приблизительно 3 до 500 мкг активного ингредиента на миллилитр раствора, с тем чтобы могло происходить вливание подходящего объема при скорости приблизительно 30 мл/ч.
Препараты, подходящие для парентерального введения, включают водные и неводные стерильные инъекционные растворы, которые могут содержать антиоксиданты, буферы, бактериостаты и растворенные вещества, которые делают препарат изотоническим с кровью предполагаемого реципиента; и водные и неводные стерильные суспензии, которые могут включать суспендирующие агенты и загустители.
Препараты, подходящие для местного введения в глаз, также включают глазные капли, где активный ингредиент растворяют или суспендируют в подходящем носителе, особенно водном растворителе для активного ингредиента. Активный ингредиент предпочтительно входит в состав подобных препаратов в концентрации приблизительно 0,5 до 20% масс/масс, например, приблизительно 0,5 до 10% масс/масс, например, приблизительно 1,5% масс/масс.
Препараты, подходящие для местного введения перорально, включают леденцы, включающие активный ингредиент в ароматной основе, обычно сахарозе и акации или трагаканте; пастилки, включающие активный ингредиент в инертной основе, такой как желатин и глицерин, или сахароза и акация; и жидкости для полоскания рта, включающие активный ингредиент в подходящем жидком носителе.
Препараты для ректального введения могут быть представлены в виде суппозитория с подходящей основой, включающей, например, какао-масло или салицилат.
Препараты, подходящие для внутрилегочного или назального введения, имеют размер частиц, например, в диапазоне 0,1 до 500 микрон (включая размеры частиц в диапазоне между 0,1 и 500 микрон с шагом микрон, таким как 0,5, 1, 30 микрон, 35 микрон и т.п.), которые вводят быстрой ингаляцией через носовой канал или ингаляцией через рот, для того чтобы достигнуть альвеолярные мешочки. Подходящие препараты включают водные или масляные растворы активного ингредиента. Препараты, подходящие для введения в форме аэрозоля или сухого порошка, могут быть получены традиционными способами и могут быть доставлены с другими терапевтическими средствами, такими как соединения, до сих пор используемые в лечении или профилактике расстройств, как описано ниже.
Препараты, подходящие для вагинального введения, могут быть представлены в виде пессариев, тампонов, кремов, гелей, мазей, пен или спреев, содержащих в дополнение к активному ингредиенту такие носители, которые, как известно из данной области техники, являются подходящими.
Препараты могут быть упакованы в однодозовые или многодозовые контейнеры, например, запаянные ампулы и пузырьки, и их можно хранить в сублимированном (лиофилизированном) состоянии, требующем только добавление стерильного жидкого носителя, например, воды, для инъекции непосредственно перед применением. Инъекционные растворы и суспензии для немедленного приема получают из стерильных порошков, гранул и таблеток прежде описанного вида. Предпочтительные стандартные лекарственные препараты содержат суточную дозу или единичную суточную часть дозы, как изложено выше в данном документе, или соответствующую часть активного ингредиента.
Кроме того, согласно изобретению предложены композиции для ветеринарии, включающие по меньшей мере один активный ингредиент, как определено выше, вместе с носителем для ветеринарии. Носители для ветеринарии являются веществами, полезными с точки зрения введения композиции, и могут представлять собой твердые, жидкие или газообразные вещества, которые являются иным образом инертными или приемлемыми в области ветеринарии и совместимы с активным ингредиентом. Эти композиции для ветеринарии могут быть введены парентерально, перорально или любым другим требуемым способом.
Комбинированное лечение
Соединения формулы I можно использовать отдельно или в сочетании с другими лекарственными веществами для лечения заболевания или расстройства, описанного в этом документе, такого как гиперпролиферативное заболевание (например, рак). В конкретных воплощениях соединение формулы I объединяют в фармацевтическом комбинированном препарате или режиме дозирования в виде комбинированного лечения со вторым соединением, которое обладает анти-гиперпролиферативными свойствами, или которое используется в лечении гиперпролиферативного заболевания (например, рака). Второе соединение фармацевтического комбинированного препарата или режима дозирования предпочтительно обладает дополнительными к соединению формулы I активностями, при этом они не оказывают отрицательного воздействия друг на друга. Подобные соединения соответственно находятся в комбинации в количествах, которые эффективны для предполагаемого использования. В одном воплощении композиция по этому изобретению включает соединение формулы I в сочетании с химиотерапевтическим средством, таким как описано в этом документе.
Комбинированное лечение можно проводить в виде одновременного или последовательного режима. При последовательном проведении состав может быть введен в ходе двух или более введений. Комбинированное введение включает совместное введение при использовании отдельных препаратов или единственного фармацевтического препарата и последовательное введение в любом порядке, когда предпочтительно существует период времени, когда оба (или все) активные агенты одновременно проявляют свои биологические активности.
Подходящими дозами любого из вышеприведенных совместно вводимых веществ являются те, которые в настоящее время используют, и они могут быть снижены вследствие совместного действия (синергизма) только что установленного вещества и других химиотерапевтических средств или методов лечения.
Комбинированное лечение может давать "синергизм" и оказывать "синергическое" действие, т.е. эффект, достигаемый при совместном использовании активных ингредиентов, больше чем сумма эффектов, которые получают в результате использования соединений по отдельности. Синергетический эффект может быть достигнут, когда активные ингредиенты: (1) совместно готовят и вводят или одновременно доставляют в составе объединенного стандартного лекарственного препарата; (2) доставляют, чередуя, или параллельно в виде отдельных препаратов; или (3) в ходе отдельных режимов. При доставке в ходе чередующегося лечения синергетический эффект может быть достигнут, когда соединения вводят или доставляют последовательно, например, в ходе разных инъекций в отдельных шприцах, отдельных пилюлях или капсулах, или раздельных вливаний. В общем в ходе чередующегося лечения эффективная доза каждого активного ингредиента вводится последовательно, т.е. периодически, при этом при комбинированном лечении эффективные дозы двух или более активных ингредиентов вводят вместе.
В конкретном воплощении противораковой терапии соединение формулы I или его стереоизомер, геометрический изомер, таутомер, сольват, метаболит или фармацевтически приемлемую соль, или пролекарство можно объединить с другими химиотерапевтическими, гормональными средствами или антителами, такими как те, что описаны в этом документе, а также объединить с хирургическим лечением и радиотерапией. Таким образом методы комбинированного лечения согласно настоящему изобретению включают введение по меньшей мере одного соединения формулы I или его стереоизомера, геометрического изомера, таутомера, сольвата, метаболита или фармацевтически приемлемой соли, или пролекарства и применение по меньшей мере одного другого метода противораковой терапии. Количества соединения(й) формулы I и другого фармацевтически активного химиотерапевтического средства(в) и относительные сроки введения выбирают, чтобы достигнуть требуемого комбинированного терапевтического эффекта.
Метаболиты соединений формулы I
Также в объеме данного изобретения находятся in vivo метаболические продукты формулы I, описанные в этом документе. Подобные продукты можно получить, например, в результате окисления, восстановления, гидролиза, амидирования, дезамидирования, этерификации, деэтерификации, ферментативного расщепления и подобных способов из вводимого соединения. Таким образом изобретение включает метаболиты соединений формулы I, включая соединения, полученные в ходе способа, согласно которому приводят в соприкосновение соединение по данному изобретению с млекопитающим в течение периода времени, достаточного для выхода его метаболического продукта.
Обычно продукты обмена веществ определяют, получая меченное радиоактивным изотопом (например, 14С или 3Н) соединение по изобретению, вводя его парентерально в детектируемой дозе (например, больше приблизительно 0,5 мг/кг) животному, такому как крыса, мышь, морская свинка, обезьяна, или человеку, оставляя достаточно времени для осуществления метаболизма (обычно приблизительно 30 секунд до 30 часов) и выделяя его продукты переработки из мочи, крови или других биологических образцов. Эти продукты легко выделяют, поскольку они мечены (другие выделяют, используя антитела, способные связывать эпитопы, оставшиеся в метаболите). Структуры метаболитов определяют обычным образом, например, в ходе анализа МС, ЖХ/МС или ЯМР. В общем анализ метаболитов проводят в том же порядке, что и традиционные исследования метаболизма лекарственных средств, хорошо известные квалифицированным специалистам в данной области техники. Продукты обмена веществ, пока они иным образом не найдены in vivo, можно использовать в анализах диагностики для терапевтической дозировки соединений по изобретению.
В другом воплощении изобретения предложено готовое изделие или "набор", содержащий вещества, полезные для лечения заболеваний и расстройств, описанных выше. Набор содержит контейнер, включающий соединение формулы I. Кроме того, набор может включать этикетку или листок-вкладыш на контейнере или соединенный с контейнером. Термин "листок-вкладыш" используют применительно к инструкциям, обычно включенным в серийные упаковки лекарственных средств, которые содержат информацию о показаниях, способе применения, дозировке, введении, противопоказаниях и/или предупреждения, касающиеся использования подобных лекарственных средств. Подходящие контейнера включают, например, флаконы, пробирки, шприцы, блистерные упаковки и т.п. Контейнер может быть получен из ряда веществ, таких как стекло или пластмасса. Контейнер может содержать соединение формулы I или II или препарат, который эффективен в лечении состояния, и может иметь стерильное отверстие (например, контейнер может представлять собой мешок с раствором для внутривенного введения или флакон, имеющий пробку, поддающуюся прокалыванию иглой для подкожной инъекции). По меньшей мере один активный агент в композиции представляет собой соединение формулы I. Этикетка или листок-вкладыш указывает на то, что композицию используют в лечении состояния, предпочтительно такого, как рак. Кроме того, этикетка или листок-вкладыш может указывать на то, что пациент, которого подвергают лечению, имеет заболевание, такое как гиперпролиферативное заболевание, нейродегенерация, гипертрофия сердца, боль, мигрень или нейротравматическая болезнь или нарушение. В одном воплощении этикетка или листок-вкладыш указывает на то, что композицию, включающую соединение формулы I, можно использовать в лечении заболевания, возникшего в результате аномального клеточного роста. Также этикетка или листок-вкладыш может указывать на то, что композицию можно применять в лечении других заболеваний. Альтернативно или дополнительно, готовое изделие может кроме того включать второй контейнер, включающий фармацевтически приемлемый буфер, такой как бактериостатическая вода для инъекции (BWFI от bacteriostatic water for injection), фосфатно-буферный солевой раствор, раствор Рингера и раствор декстрозы. Он дополнительно может включать другие вещества, необходимые с точки зрения производителя и потребителя, включая другие буферы, разбавители, фильтры, иглы и шприцы.
Кроме того, набор может содержать указания по введению соединения формулы I и, при наличии, второго фармацевтического препарата. Например, если набор содержит первую композиция, включающую соединение формулы I, и второй фармацевтический препарат, тогда набор может дополнительно содержать указания по одновременному, последовательному или раздельному введению первой и второй фармацевтических композиций пациенту, нуждающемуся в этом.
В другом воплощении наборы подходят для доставки твердых пероральных форм соединения формулы I, таких как таблетки или капсулы. Подобный набор предпочтительно включает несколько единиц дозировки. Подобные наборы могут включать бланк, содержащий дозы, предназначенные для их целевого использования. Примером подобного набора является "блистерная упаковка". Блистерные упаковки популярны в упаковочной промышленности и широко используются для упаковки фармацевтических стандартных лекарственных форм. При необходимости можно использовать памятку, например, в виде чисел, букв или других знаков, или с календарной вставкой, указывающей дни в схеме лечения, в которые могут быть введены дозы.
Согласно одному воплощению набор может содержать (а) первый контейнер с соединением формулы I, содержащимся в нем; и возможно (b) второй контейнер со вторым фармацевтическим препаратом, содержащимся в нем, где второй фармацевтический препарат включает второе соединение с антигиперпролиферативной активностью. Альтернативно или дополнительно, набор может кроме того включать третий контейнер, включающий фармацевтически приемлемый буфер, такой как бактериостатическая вода для инъекции (BWFI), фосфатно-буферный солевой раствор, раствор Рингера и раствор декстрозы. Он дополнительно может включать другие вещества, необходимые с точки зрения производителя и потребителя, включая другие буферы, разбавители, фильтры, иглы и шприцы.
В некоторых других воплощениях, где набор содержит композицию соединения формулы I и второе терапевтическое средство, набор может включать контейнер, содержащий отдельные композиции, такие как разделенный флакон или разделенный пакетик из фольги, однако отдельные композиции также могут находиться в одном неразделенном контейнере. Обычно набор содержит указания по введению отдельных компонентов. Форма набора особенно удобна, когда отдельные компоненты предпочтительно вводят в разных лекарственных формах (например, перорально и парентерально), вводят с разными интервалами между приемами, или когда титрование отдельных компонентов состава необходимо лечащему врачу.
Соединения 5-азаиндазола формулы I известны также как пиразоло[4,3-с]пиридин с порядком нумерации в виде:
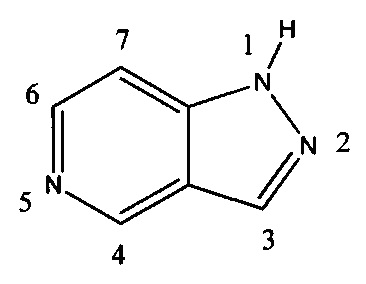
Соединения формулы I можно синтезировать синтетическими способами, которые включают процессы, аналогичные тем, что хорошо известны в химических областях, особенно с учетом описания, содержащегося в данном документе, и процессы для других гетероциклов, описанных в: Comprehensive Heterocyclic Chemistry II, Editors Katritzky and Rees, Elsevier, 1997, например Volume 3; Liebigs Annalen der Chemie, (9): 1910-16, (1985); Helvetica Chimica Acta, 41:1052-60, (1958); Arzneimittel-Forschung, 40(12): 1328-31, (1990), каждый из которых прямо включен в данный документ посредством ссылки. Исходные вещества как правило имеются в продаже, например от Aldrich Chemicals (Milwaukee, WI), или их легко получить, используя способы, хорошо известные квалифицированным специалистам в данной области техники (например получить способами, в общем описанными у Louis F. Fieser and Mary Fieser, Reagents for Organic Synthesis, v. 1-23, Wiley, N.Y. (1967-2006 ed.), или Beilsteins Handbuch der organischen Chemie, 4, Aufl. ed. Springer-Verlag, Berlin, включая дополнения (также доступны в электронной системе базы данных Бельштейна).
Превращения синтетической химии и методология защитных групп (введение и снятие защитных групп), полезные при синтезе соединений формулы I и необходимых реагентов, и промежуточных соединений, известны в данной области техники и включают, например, те, что описаны у R. Larock, Comprehensive Organic Transformations, VCH Publishers (1989); T.W. Greene and P. G.M. Wuts, Protective Groups in Organic Synthesis, 3rd Ed., John Wiley and Sons (1999); и L. Paquette, ed., Encyclopedia of Reagents for Organic Synthesis, John Wiley and Sons (1995) и их последующие редакции.
Соединения формулы I можно получить по отдельности или в виде библиотеки соединений, включающей по меньшей мере 2, например, 5 до 1000 соединений, или 10 до 100 соединений. Библиотеки соединений формулы I можно получить в ходе комбинаторного подхода 'разделения и смешивания' или в ходе множественных параллельных синтезов при использовании либо химии в жидкой фазе, либо твердофазной химии, методами, известными квалифицированным специалистам в данной области техники. Таким образом согласно дополнительному аспекту изобретения предложена библиотека соединений, включающая по меньшей мере 2 соединения или их фармацевтически приемлемые соли.
Согласно общим способам и примерам предложены типовые способы получения соединений формулы I. Квалифицированные специалисты в данной области техники понимают, что другие синтетические способы можно использовать для синтеза соединений формулы I. Несмотря на то, что конкретные исходные вещества и реагенты изображены и обсуждаются на фигурах, общих способах и примерах, их можно легко заменить другими исходными веществами и реагентами, чтобы получить разные производные и/или реакционные условия. Кроме того, многие из примерных соединений, полученных описанными способами, можно дополнительно преобразовать в свете данного описания, используя традиционную химию, хорошо известную квалифицированным специалистам в данной области техники.
При получении соединений формул I может быть необходима защита отдельной функциональной группы (например, первичного или вторичного амина) промежуточных соединений. Необходимость в подобной защите будет изменяться в зависимости от природы отдельной функциональной группы и условий способов получения. Подходящие амино-защитные группы включают ацетил, трифторацетил, трет-бутоксикарбонил (ВОС), бензилоксикарбонил (CBz) и 9-флуоренилметиленоксикарбонил (Fmoc). Необходимость в подобной защите легко определить специалисту в данной области техники. Общее описание защитных групп и их использование смотрите у Т.W. Greene, Protective Groups in Organic Synthesis, John Wiley & Sons, New York, 1991.
Способы разделения
В способах получения соединений формулы I может быть полезно отделить продукты реакции друг от друга и/или от исходных веществ. Требуемые продукты каждой стадии или последовательностей стадий отделяют и/или очищают до необходимой степени однородности методиками, распространенными в данной области техники. Обычно подобные методы разделения включают многофазную экстракцию, кристаллизацию из растворителя или смеси растворителей, перегонку, сублимацию или хроматографию. Хроматография может включать несколько способов, включая, например: обращенно-фазовую и нормально-фазовую; эксклюзионную; ионообменную; способы и аппараты жидкостной хроматографии высокого, среднего и низкого давления; аналитическую в малом масштабе; с псевдодвижущимся слоем (ПДС) и препаративную тонкослойную или толстослойную хроматографию, а также методики тонкослойной и флэш-хроматографии в малом масштабе.
Другой вид способов разделения включает обработку смеси реагентом, выбранным таким образом, чтобы связать или осуществить иным образом отделение требуемого продукта, непрореагировавшего исходного вещества, побочного продукта реакции, или подобного. Такие реагенты включают адсорбенты или абсорбенты, такие как активированный уголь, молекулярные сита, ионообменную среду, или подобные. Альтернативно, реагенты могут представлять собой кислоты в случае основного вещества, основания в случае кислотного вещества, связывающие реагенты, такие как антитела, связывающие белки, селективные хелаторы, такие как краун-эфиры, реагенты жидкость-жидкостной экстракции ионов (LIX), или подобные. Выбор соответствующих способов разделения зависит от природы рассматриваемых веществ, например, температуры кипения и молекулярного веса при перегонке и сублимации, присутствия или отсутствия полярных функциональных групп при хроматографии, стабильности веществ в кислотной и основной среде при многофазной экстракции, и подобного.
Диастереомерные смеси можно разделить на их отдельные диастереомеры, исходя из их физико-химических различий, способами, хорошо известными квалифицированным специалистам в данной области техники, такими как хроматография и/или фракционная кристаллизация. Энантиомеры можно разделить, преобразуя энантиомерную смесь в диастереомерную смесь в ходе реакции с соответствующим оптически активным соединением (например, хиральным вспомогательным веществом, таким как хиральный спирт или хлорангидрид кислоты Мошера), разделяя диастереомеры и преобразуя (например, гидролизуя) отдельные диастереомеры в соответствующие чистые энантиомеры. Также некоторые из соединений по настоящему изобретению могут представлять собой атропоизомеры (например, замещенные биарилы) и рассматриваются как часть данного изобретения. Также энантиомеры можно разделить, используя хиральную колонку ВЭЖХ.
Отдельный стереоизомер, например энантиомер, по существу без своего стереоизомера можно получить разделением рацемической смеси при использовании способа, такого как образование диастереомеров, используя оптически активные расщепляющие агенты (Eliel, Е. and Wilen, S. "Stereochemistry of Organic Compounds", John Wiley & Sons, Inc., New York, 1994; Lochmuller, С.H., (1975) J. Chromatogr., 113(3):283-302). Рацемические смеси хиральных соединений по изобретению можно разделить и выделить любым подходящим способом, включая: (1) образование ионных, диастереомерных солей с хиральными соединениями и разделение в ходе фракционной кристаллизации или другими способами, (2) образование диастереомерных соединений с хиральными дериватизирующими реагентами, разделение диастереомеров и превращение в чистые стереоизомеры, и (3) разделение по существу чистых или обогащенных стереоизомеров непосредственно при хиральных условиях. Смотрите: "Drug Stereochemistry, Analytical Methods and Pharmacology", Irving W. Wainer, Ed., Marcel Dekker, Inc., New York (1993).
Согласно способу (1) диастереомерные соли можно получить в ходе реакции энантиомерно чистых хиральных оснований, таких как бруцин, хинин, эфедрин, стрихнин, α-метил-β-фенилэтиламин (амфетамин) и подобных, с асимметричными соединениями, несущими кислотную функциональную группу, такими как карбоновая кислота и сульфоновая кислота. Диастереомерные соли можно разделить в ходе фракционной кристаллизации или ионной хроматографии. Для разделения оптических изомеров аминных соединений добавление хиральных карбоновой или сульфоновой кислот, таких как камфорсульфоновая кислота, винная кислота, миндальная кислота или молочная кислота, может приводить к образованию диастереомерных солей.
Альтернативно, согласно способу (2) разделяемый субстрат подвергают взаимодействию с одним энантиомером хирального соединения до образования диастереомерной пары (Е. and Wilen, S. "Stereochemistry of Organic Compounds", John Wiley & Sons, Inc., 1994, p. 322). Диастереомерные соединения можно получить в ходе взаимодействия асимметричных соединений с энантиомерно чистыми хиральными дериватизирующими реагентами, такими как ментиловые производные, с последующим разделением диастереомеров и гидролизом, что дает чистый или обогащенный энантиомер. Способ определения оптической чистоты включает получение хиральных эфиров, таких как ментиловый эфир, например, (-) ментилхлорформиата в присутствии основания или эфира Мошера, α-метокси-α-(трифторметил)фенилацетата (Jacob III. J. Org. Chem. (1982) 47:4165) из рацемической смеси и анализ 1Н ЯМР спектра на присутствие двух атропоизомерных энантиомеров или диастереомеров. Устойчивые диастереомеры атропоизомерных соединений могут быть разделены и выделены в ходе нормальной- и обращенно-фазовой хроматографии, следуя способам разделения атропоизомерных нафтил-изохинолинов (WO 96/15111). Согласно способу (3) рацемическую смесь двух энантиомеров можно разделить хроматографически, используя хиральную неподвижную фазу ("Chiral Liquid Chromatography" (1989) W.J. Lough, Ed., Chapman and Hall, New ork; Okamoto, J. Chromatogr., (1990) 513:375-378). Обогащенные или очищенные энантиомеры можно различить способами, используемыми для распознавания других хиральных молекул с асимметричными атомами углерода, такими как оптическое вращение и круговой дихроизм. Общие способы получения
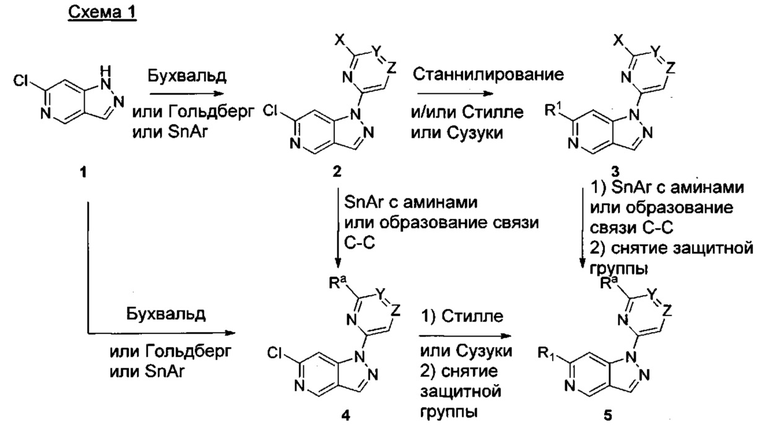
На схеме 1 показан общий синтез соединений 5. Замещенные 6-хлор-N-пиридил-5-азаиндазолы (Y=Z=СН) 2 можно получить в ходе, но не ограничиваясь этим, реакции Бухвальда, Гольдберга или нуклеофильного ароматического замещения (SnAr), начиная с 6-хлор-5-азаиндазола 1. Введение группы R2 в ходе реакции SnAr с разными аминами или реакции образования связи С-С с или без катализа переходными металлами дает соединения 4. Альтернативно, соединения 4 могут быть непосредственно получены из 6-хлор-5-азаиндазола 1 с группой Ra, уже введенной в предшественник пиридина. Последующая реакция Стилле или Сузуки с последующим снятием защитной группы может давать запланированные соединения 5 с разными замещениями R1, Ra. Согласно альтернативной последовательности соединения 5 можно получить в ходе трех или четырехстадийного синтеза, исходя из соединений 2. Во-первых, введение группы R1 посредством станнилирования, последующая реакция Стилле или реакция Сузуки с бороновой кислотой/эфиром дают соединения 3. Во-вторых, добавление группы Ra можно выполнить в ходе либо реакции SnAr с разными аминами, либо реакции образования связи С-С с или без катализа переходными металлами. В конце при кислотных, основных, окислительных или восстановительных условиях снятие защитной группы может давать соединения 5. Подобным образом можно синтезировать замещенные N-пиримидинил-5-азаиндазолы (Y=N, Z=СН) и замещенные N-пиразинил-6-азаиндазолы (Y=СН, Z=N) 5.
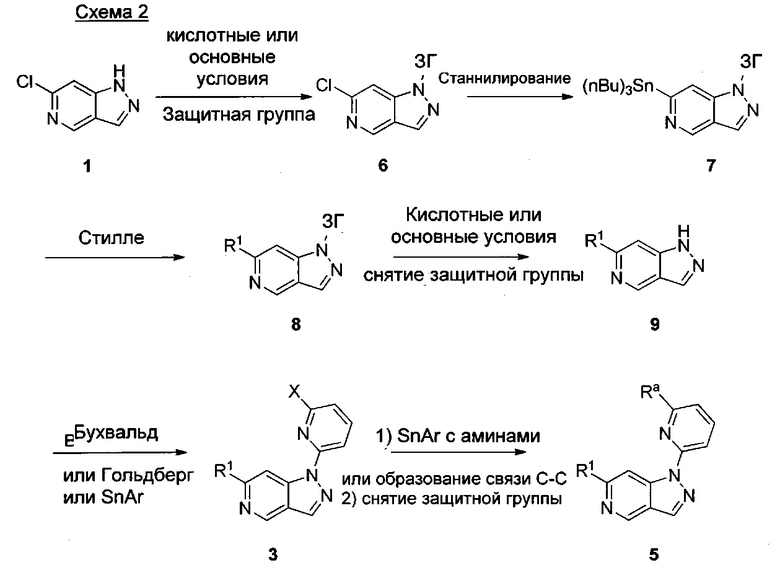
Схема 2 демонстрирует общий синтез соединений 5. Защита 6-хлор-5-азаиндазола 1 либо при кислотных, либо при основных условиях может давать соединения 6. Альтернативно, в 6-положении может находиться либо другой галоген, такой как Вr или I, либо уходящая группа. Защитные группы (3Г) включают, но не ограничиваются этим, группы тетрагидропиранил, 2-(триметилсилил)этокси]метил или ацетил, или другую азот-защитную группу, известную в литературе. Последующая реакция станнилирования, затем реакция Стилле, начиная с соединений 6, могут давать соединения 8. Соединения 9 можно получить, удаляя защитные группы при кислотных или основных условиях. Замещенные N-пиридил-5-азаиндазолы 3 можно синтезировать в ходе, но не ограничиваясь этим, реакции Бухвальда, Гольдберга или нуклеофильного ароматического замещения (SnAr), начиная с 6-хлор-5-азаиндазола 9. Введение группы Ra в ходе реакции SnAr с разными аминами или реакции образования связи С-С с или без катализа переходными металлами с последующим снятием защитной группы дает соединения 5.
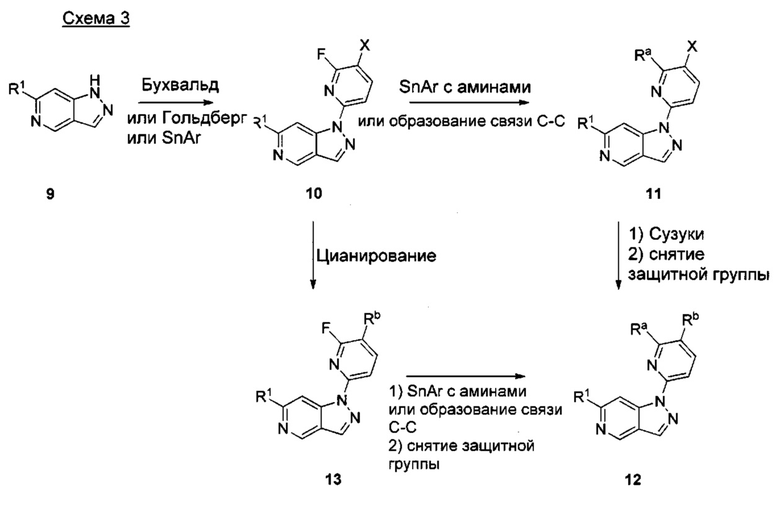
Схема 3 демонстрирует общий синтез соединений 12. Соединения 10 можно синтезировать в ходе, но не ограничиваясь этим, реакции Бухвальда, Гольдберга или нуклеофильного ароматического замещения (SnAr), начиная с 6-хлор-5-азаиндазолов 9. Цианирование соединений 10 при подходящих условиях может давать соединения 13. Введение группы Ra можно выполнить в ходе, но не ограничиваясь этим, реакции SnAr с разными аминами или реакции образования связи С-С с или без катализа переходными металлами. Последующее снятие защитной группы при разных условиях может давать соединения 12. Альтернативно, соединения 12 можно получить в ходе другой последовательности с введением сначала группы Ra, а затем группы Rb.
Схема 4
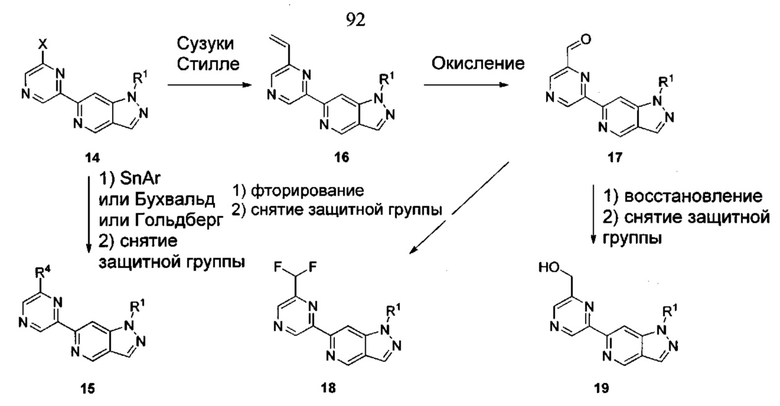
На схеме 4 показан общий синтез соединений 15, 18 и 19. Соединения 15 можно синтезировать в ходе, но не ограничиваясь этим, реакции Бухвальда, Гольдберга или нуклеофильного ароматического замещения (SnAr), начиная с соединений 14, с последующей реакцией снятия защитной группы при необходимости при соответствующих условиях. Введение винильной группы можно выполнить в ходе либо реакции Сузуки, либо реакции Стилле, чтобы получить соединения 16. Либо одностадийное, либо ступенчатое окислительное расщепление соединений 16 может давать альдегиды 17. Затем реакция фторирования или восстановления с последующей реакцией снятия защитной группы при необходимости при соответствующих условиях может приводить к соединениям 18 или 19.
Примеры
Пример 1 6-(1-этилпиразол-4-ил)-1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридин 101
Стадия А: Получение 6-хлор-1-(6-фтор-2-пиридил)пиразоло[4,3-с]пиридина
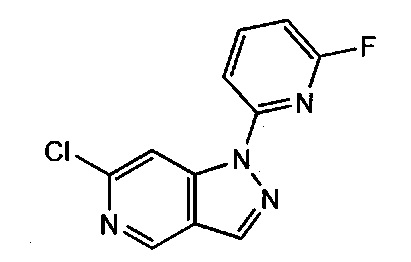
Способ I: Раствор 6-хлор-1Н-пиразоло[4,3-с]пиридина (3,78 г, 24,6 ммоль), карбоната цезия (16,1 г, 49,2 ммоль) и 2,6-дифторпиридина (3,40 г, 29,5 ммоль) в диметилсульфоксиде; 50,0 мл, перемешивали при 70°С в течение 2 часов. Реакцию гасили, вливая в воду, затем экстрагировали ЕtOАс. Органические слои сушили с сульфатом натрия, фильтровали и концентрировали в вакууме. Неочищенный продукт очищали с помощью флэш-хроматографии (элюировали EtOAc/гептаном при 25% ЕtOАс), получая 3,2 г требуемого продукта с выходом 52%. МС (ЭСИ) m/z: 249,2 [М+Н]+.
Способ II: Смесь 6-хлор-1Н-пиразоло[4,3-с]пиридина (13,778 ммоль, 2115,9 мг), 2-бром-6-фтор-пиридина (15,156 ммоль, 2667,3 мг), N,N'-диметилэтилендиамина (13,778 ммоль; 1,215 г; 1,37 мл), иодида меди (13,778 ммоль; 2650,5 мг) и карбоната калия (15,156 ммоль; 2,12 г) в 1,4-диоксане (10 мл) продували аргоном, затем закрывали и перемешивали при 100°С в течение 20 часов. Смесь охлаждали до комнатной температуры и затем фильтровали через Целит. Фильтрат концентрировали; остаток очищали на силикагеле и элюировали 0 до 100% этилацетата в гептане, получая 6-хлор-1-(6-фтор-2-пиридил)пиразоло[4,3-с]пиридин в виде твердого вещества белого оттенка (1,90 г, 55%) МС (ЭСИ) m/z: 249 [М+Н]+.
Стадия В: Получение трет-бутил 4-[6-(6-хлорпиразоло[4,3-с]пиридин-1-ил)-2-пиридил]пиперазин-1-карбоксилата
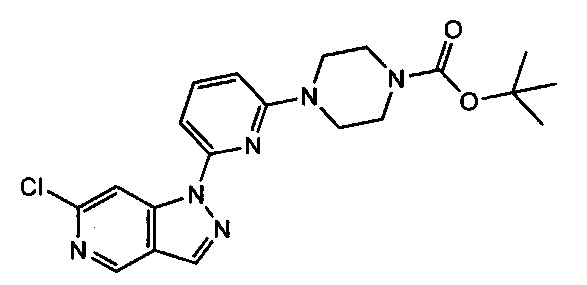
Раствор 6-хлор-1-(6-фтор-2-пиридил)пиразоло[4,3-с]пиридина (100 мг, 0,40 ммоль) и 1-N-Boc-пиперазина (380 мг, 2,0 ммоль) в диметилсульфоксиде (3,0 мл) нагревали при 95°С в течение 4 часов. Реакцию гасили водой и экстрагировали ЕtOАс. Органические слои сушили с сульфатом натрия, фильтровали и концентрировали в вакууме. Неочищенный продукт очищали с помощью флэш-хроматографии (ЕtOАс/гептан 25% ЕtOАс), получая 110 мг требуемого продукта с выходом 66%. МС (ЭСИ) m/z: 415,1 [М+Н]+.
Стадия С: 6-(1-этил-1Н-пиразол-4-ил)-1-(6-(пиперазин-1-ил)пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридин
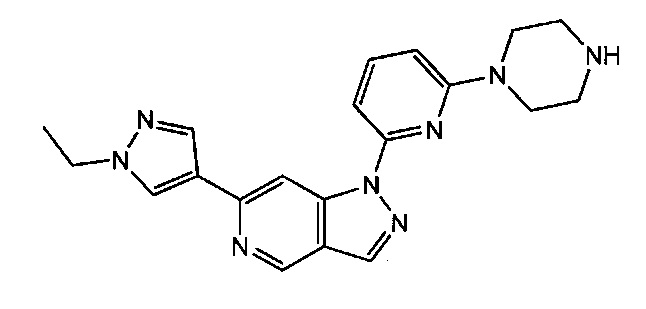
Смесь трет-бутил 4-[6-(6-хлорпиразоло[4,3-с]пиридин-1-ил)-2-пиридил]пиперазин-1-карбоксилата (0,5112 ммоль; 212,1 мг), 1-этил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразола (1,022 ммоль; 227,1 мг), аддукта [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладия (II) дихлорметана (0,05112 ммоль; 42,6 мг), гидрата ацетата калия (0,7668 ммоль; 0,77 мл) и декагидрата карбоната натрия (0,7668 ммоль; 0,77 мл) в ацетонитриле (10 мл) в пробирке высокого давления нагревали в микроволной печи при 150°С в течение 15 минут. Смесь охлаждали до комнатной температуры. Слои разделяли. Водный слой экстрагировали ЕtOАс. Объединенный органический слой концентрировали. Остаток очищали на силикагеле, элюируя 0 до 6% МеОН в ДХМ, получая трет-бутил 4-(6-(6-(1-этил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)пиперазин-1-карбоксилат в виде темно-бежевого твердого вещества.
Смесь трет-бутил 4-(6-(6-(1-этил-1Н-пиразол-4-ил)-1Н-Пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)пиперазин-1-карбоксилата (0,2486 ммоль; 118 мг) в ДХМ (5 мл) и ТФК (5 мл) перемешивали при комнатной температуре в течение ночи. Смесь концентрировали и остаток очищали с помощью обращенно-фазовой ВЭЖХ, получая 6-(1-этил-1Н-пиразол-4-ил)-1-(6-(пиперазин-1-ил)пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридин 101 (47,5 мг, 50%). 1Н ЯМР (400 МГц, ДМСО) δ 9,15-9,11 (s, 1Н), 8,67-8,65 (s, 1Н), 8,54-8,51 (s, 1Н). 8,27-8,24 (s, 1Н), 7,91-7,88 (s, 1Н), 7,78-7,72 (t, J=8,1 Гц, 1Н), 7,24-7,18 (d, J=7,7 Гц, 1Н), 6,80-6,74 (d, J=8,4 Гц, 1Н), 4,26-4,17 (q, J=7,3 Гц, 2Н), 3,65-3,56 (m, 4Н), 2,96-2,86 (m, 4Н), 1,46-1,41 (t, J=7,3 Гц, 3Н); МС (ЭСИ) m/z: 375,1 [М+Н]+.
Пример 2 6-(1-метил-1Н-пиразол-4-ил)-1-(6-(пиперазин-1-ил)пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридин 102
Следуя способам, описанным в примере 1, и начиная с 1-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразола, имеющего структуру:
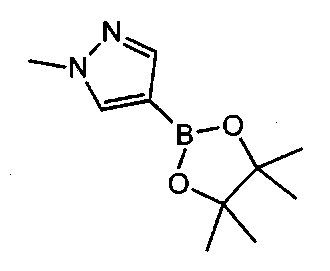
получали 102 в виде твердого вещества белого оттенка (174 мг, 32%) в ходе двух стадий. 1Н ЯМР (400 МГц, ДМСО) δ 9,17-9,07 (s, 1Н), 8,71-8,57 (s, 1Н), 8,56-8,47 (s, 1Н), 8,26-8,15 (s, 1Н), 7,91-7,82 (s, 1Н), 7,80-7,69 (t, J=8,1 Гц, 1Н), 7,26-7,15 (d, J=7,7 Гц, 1Н), 6,81-6,73 (d, J=8,4 Гц, 1Н), 3,99-3,82 (s, 3Н), 3,66-3,52 (m, 4Н), 2,96-2,85 (m, 4Н); МС (ЭСИ) m/z: 361,2 [М+Н]+.
Пример 3 1-(6-(1,4-диазепан-1-ил)пиридин-2-ил)-6-(5-изопропилпиридин-3-ил)-1Н-пиразоло[4,3-с]пиридин 103
Следуя способам, описанным в примере 8, и начиная с 1,4-диазепана, получали 103 в виде твердого вещества белого оттенка (29,4 мг, 24%). 1Н ЯМР (400 МГц, ДМСО) δ 9,36-9,28 (s, 1Н), 9,09-9,04 (d, J=2,0 Гц, 1Н), 9,03-9,01 (s, 1Н), 8,66-8,61 (s, 1Н), 8,59-8,55 (d, J=2,1 Гц, 1Н), 8,30-8,24 (t, J=2,0 Гц, 1Н), 7,76-7,65 (t, J=8,1 Гц, 1Н), 7,23-7,16 (d, J=7,7 Гц, 1Н), 6,65-6,58 (d, J=8,5 Гц, 1Н), 3,93-3,72 (dt, J=10,0, 5,5 Гц, 4Н), 3,12-3,03 (dt, J=14,0, 7,0 Гц, 1Н), 2,99-2,90 (m, 2Н), 2,73-2,66 (m, 2Н), 1,91-1,80 (m, 2Н), 1,33-1,30 (d, J=6,9 Гц, 6H); МС (ЭСИ) m/z: 414,1 [М+Н]+.
Пример 4 6-(5-этилпиридин-3-ил)-1-(6-(пиперазин-1-ил)пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридин 104
Следуя способам, описанным в примере 8, и начиная с 6-(5-этилпиридин-3-ил)-1-(6-фторпиридин-2-ил)-1Н-пиразоло[4,3-с]пиридина и пиперазина, получали 104 в виде твердого вещества белого оттенка (22,3 мг, 18%) за 2 стадии. 1Н ЯМР (400 МГц, ДМСО) δ 9,35-9,27 (s, 1Н), 9,16-9,08 (d, J=2,0 Гц, 1Н), 9,08-9,01 (s, 1Н), 8,67-8,59 (s, 1Н), 8,57-8,50 (d, J=1,9 Гц, 1Н), 8,30-8,21 (s, 1Н), 7,85-7,73 (m, 2Н), 7,66-7,44 (m, 2Н), 7,28-7,23 (d, J=7,7 Гц, 1Н), 6,85-6,78 (d, J=8,4 Гц, 1Н), 3,65-3,57 (m, 4Н), 2,98-2,81 (m, 4Н), 2,79-2,70 (q, J=7,6 Гц, 2Н), 1,75-1,52 (m, 3Н), 1,32-1,24 (t, J=7,6 Гц, 3Н); МС (ЭСИ) m/z: 386,2 [М+Н]+.
Пример 5 6-(5-изопропил пиридин-3-ил)-1 -(6-(пиперазин-1 -ил)пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридин 105
Следуя способам, описанным в примере 8, и начиная с пиперазина, получали 105 в виде твердого вещества белого оттенка (26,6 мг, 22%). 1Н ЯМР (400 МГц, ДМСО) δ 9,37-9,27 (s, 1Н), 9,12 9,06 (d, J=2,0 Гц, 1Н), 9,05-9,02 (s, 1Н), 8,67-8,62 (s, 1Н), 8,60-8,55 (d, J=2,0 Гц, 1Н), 8,34-8,27 (t, J=2,0 Гц, 1Н), 7,80-7,72 (t, J=8,1 Гц, 1Н), 7,29-7,21 (d, J=7,7 Гц, 1Н), 6,86-6,77 (d, J=8,4 Гц, 1Н), 3,66-3,58 (m, 4Н), 3,12-3,03 (dt, J=13,8, 6,9 Гц, 1Н), 2,93-2,82 (m, 4Н), 1,34-1,30 (d, J=6,9 Гц, 6Н); МС (ЭСИ) m/z: 400,2 [М+Н]+.
Пример 6 1-(6-(6-(5-этил пиридин-3-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-6-ол 106
Следуя способам, описанным в примере 8, и начиная с 6-(5-этилпиридин-3-ил)-1-(6-фторпиридин-2-ил)-1Н-пиразоло[4,3-с]пиридина и 1,4-диазепан-6-ола, получали 106 в виде твердого вещества белого оттенка (49,4 мг, 12%). МС (ЭСИ) m/z:.416,1 [М+Н]+.
Пример 7 (R)-1-(6-(6-(5-изопропилпиридин-3-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)пиперидин-3-амин 107
Следуя способам, описанным в примере 8, и начиная с трет-бутил N-[(3R)-3-пиперидил]карбамата, получали 107 в виде твердого вещества белого оттенка (33,5 мг, 27%) в ходе двух стадий. 1Н ЯМР (400 МГц, ДМСО) δ 9,38-9,29 (s, 1Н), 9,14-9,09 (d, J=2,0 Гц, 1Н), 9,06-9,00 (s, 1Н), 8,67-8,61 (s, 1Н), 8,60-8,55 (d, J=2,0 Гц, 1Н), 8,36-8,30 (s, 1Н), 7,79-7,70 (t, J=8,1 Гц, 1Н), 7,23-7,14 (d, J=7,7 Гц, 1Н), 6,84-6,78 (d, J=8,5 Гц, 1Н), 4,31-4,13 (m, 3Н), 3,13-3,04 (dt, J=13,7, 6,6 Гц, 3Н), 2,87-2,79 (m, 1Н), 2,80-2,72 (m, 2Н), 1,96-1,75 (m, 2Н), 1,68-1,52 (dd, J=24,1, 11,8 Гц, 2H), 1,33-1,30 (d, J=7,0 Гц, 7H); МС (ЭСИ) m/z:.414,1 [М+Н]+.
Пример 8 (3S)-1-[6-[6-(5-изопропил-3-пиридил)пиразоло[4,3-с]пиридин-1 -ил]-2-пиридил]пиперидин-3-амин 108
Стадия А: Получение 3-бром-5-изопропенил-пиридина
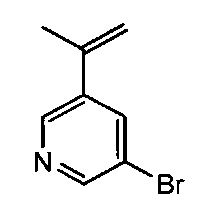
Смесь аддукта [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладия (II) дихлорметана; 98,0 масс. %, гидрата ацетата калия (7,4997 ммоль; 3,7 мл), декагидрата карбоната натрия (7,4997 ммоль; 3,7 мл), ацетонитрила (15 мл) и 3,5-дибромпиридина (4,9998 ммоль; 1184,4 мг) в 2-изопропенил-4,4,5,5-тетраметил-1,3,2-диоксаборолане (4,9998 ммоль; 840,0 мг; 0,940 мл) в пробирке высокого давления нагревали в микроволновой печи при 120°С в течение 3 минут. Смесь охлаждали до комнатной температуры. Слои разделяли. Водный слой экстрагировали ЕtOАс. Объединенный органический слой концентрировали. Остаток очищали на силикагеле, элюируя 0 до 10% МеОН в ДХМ, получая 3-бром-5-изопропенил-пиридин в виде темно-бежевого твердого вещества (512,6 мг, 52%).
Стадия В: Получение 3-(проп-1-ен-2-ил)-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридина
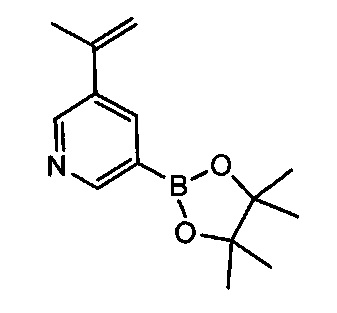
Смесь 3-бром-5-изопропенил-пиридина (5,1767 ммоль; 1025,3 мг), 4,4,5,5-тетраметил-2-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1,3,2-диоксаборолана (7,7651 ммоль; 1972 мг), ацетата калия (7,7651 ммоль; 762,10 мг) и аддукта [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладия (II) дихлорметана (0,25884 ммоль; 216 мг) в 1,4-диоксане (15 мл) в пробирке высокого давления продували азотом в течение 1 минуты, затем закрывали и нагревали при 85°С в течение ночи. Реакционную смесь фильтровали горячей через Целит. Осадок на фильтре промывали ЕtOАс. Отфильтрованное вещество промывали водой и солевым раствором. Органический слой сушили с MgSO4 и затем концентрировали, получая 3-(проп-1-ен-2-ил)-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин, который использовали без очистки.
Стадия С: Получение 1-(6-фторпиридин-2-ил)-6-(5-изопропилпиридин-3-ил)-1Н-пиразоло[4,3-с]пиридина
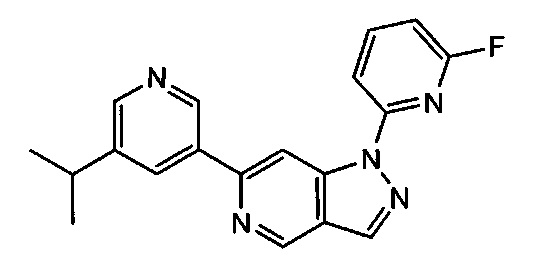
Смесь 6-хлор-1-(6-фтор-2-пиридил)пиразоло[4,3-с]пиридина (1,759 ммоль; 437,3 мг), 3-изопропенил-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридина (2,638 ммоль; 646,6 мг), аддукта [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладия (II) дихлорметана (0,1759 ммоль; 147 мг), гидрата ацетата калия (2,638 ммоль; 1,3 мл) и карбоната натрия (2,638 ммоль; 1,3 мл) в ацетонитриле (10 мл) в пробирке высокого давления нагревали в микроволновой печи при 150°С в течение 5 минут. Смесь охлаждали до комнатной температуры. Слои разделяли. Водный слой экстрагировали ЕtOАс. Объединенный органический слой концентрировали. Остаток очищали на силикагеле, элюируя 0 до 6% МеОН в ДХМ, получая 1-(6-фтор-2-пиридил)-6-(5-изопропенил-3-пиридил)пиразоло[4,3-с]пиридин.
К раствору вышеуказанного 1-(6-фтор-2-пиридил)-6-(5-изопропенил-3-пиридил)пиразоло[4,3-с]пиридина в этаноле (50 мл) в 250 мл круглодонной колбе добавляли катализатор Перлмана (0,3523 ммоль; 247,4 мг). Колбу вакуумировали и соединяли с баллоном водорода. Смесь перемешивали при комнатной температуре в течение 16 часов. Смесь фильтровали через Целит.Фильтрат концентрировали. Остаток очищали на силикагеле, элюируя 0 до 5% МеОН в ДХМ, получая 1-(6-фторпиридин-2-ил)-6-(5-изопропилпиридин-3-ил)-1Н-пиразоло[4,3-с]пиридин (479,2 мг, 82%).
Стадия D: трет-бутил N-[(3S)-1-[6-[6-(5-изопропил-3-пиридил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-3-пиперидил]карбамат
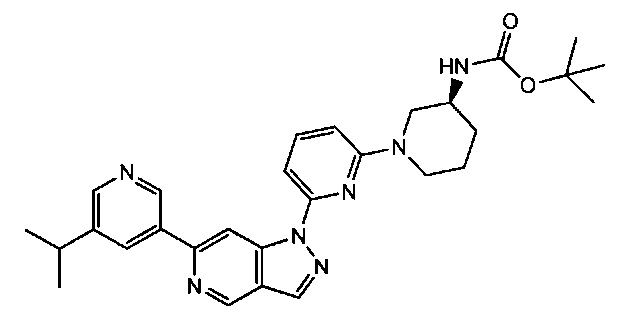
Смесь 1-(6-фтор-2-пиридил)-6-(5-изопропил-3-пиридил)пиразоло[4,3-с]пиридина (0,3032 ммоль; 120,0 мг), трет-бутил N-[(3S)-3-пиперидил]карбамата (0,9095 ммоль; 182,2 мг) и N-метилморфолина (3,032 ммоль; 310 мг; 0,337 мл) в 1-метил-2-пирролидиноне (3 мл) в закрытом сосуде высокого давления нагревали при 120°С в течение ночи. Смесь охлаждали до комнатной температуры и затем разделяли между ЕtOАс и водой. Органический слой концентрировали, получая трет-бутил N-[(3S)-1-[6-[6-(5-изопропил-3-пиридил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-3-пиперидил]карбамат, который использовали без очистки.
Вышеуказанный трет-бутил N-[(3S)-1-[6-[6-(5-изопропил-3-пиридил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-3-пиперидил]карбамат в ДХМ (5 мл) и ТФК (5 мл) перемешивали при комнатной температуре в течение 1 часа. Смесь концентрировали и остаток очищали с помощью обращенно-фазовой ВЭЖХ, получая 108 (33,9 мг, 37%). 1Н ЯМР (400 МГц, ДМСО) δ 9,35-9,30 (s, 1Н), 9,13-9,10 (d, J=2,0 Гц, 1Н), 9,06-9,02 (s, 1Н), 8,66-8,61 (s, 1Н), 8,58-8,55 (d, J=2,0 Гц, 1Н), 8,35-8,31 (d, J=1,9 Гц, 1Н), 7,78-7,70 (t, J=8,1 Гц, 1Н), 7,23-7,17 (d, J=7,7 Гц, 1Н), 6,84-6,78 (d, J=8,5 Гц, 1Н), 4,32-4,14 (dd, J=37,4, 11,8 Гц, 2Н), 3,12-3,01 (td, J=12,8, 5,7 Гц, 2Н), 2,87-2,70 (ddd, J=15,5, 13,1, 7,6 Гц, 2Н), 1,96-1,74 (m, 2Н), 1,64-1,51 (dd, J=24,5, 11,5 Гц, 2Н), 1,33-1,31 (d, J=7,0 Гц, 6Н); МС (ЭСИ) m/z: 414,1 [М+Н]+.
Пример 9 5-[1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридин-6-ил]тиазол 109
Раствор 5-[1-(6-фтор-2-пиридил)пиразоло[4,3-с]пиридин-6-ил]тиазола (50 мг, 0,17 ммоль) и 1-N-boc-пиперазина (175 мг, 0,921 ммоль) в диметилсульфоксиде; 2,0 мл, нагревали при 95°С в течение 8 часов. Реакцию гасили водой и экстрагировали ЕtOАс. Органические слои сушили с сульфатом натрия, фильтровали и концентрировали в вакууме, получая трет-бутил 4-[6-(6-тиазол-5-илпиразоло[4,3-с]пиридин-1-ил)-2-пиридил]пиперазин-1-карбоксилат:
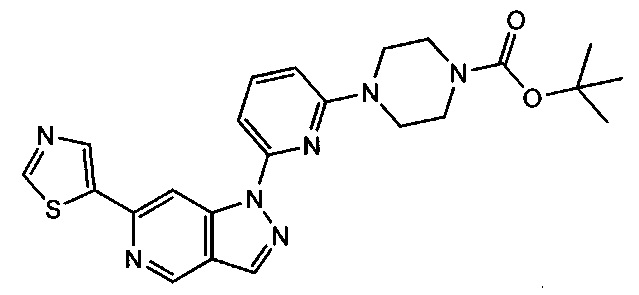
Смесь трет-бутил 4-[6-(6-тиазол-5-илпиразоло[4,3-с]пиридин-1 -ил)-2-пиридил]пиперазин-1-карбоксилата в хлороводороде (4 моль/л) в диоксане (1,5 мл, 6,0 ммоль) и 1,0 мл диоксана перемешивали при к.т.в течение 14 часов. Реакционную смесь концентрировали. Неочищенный продукт подвергали обращенно-фазовой ВЭЖХ, получая 109 (44 мг) с выходом 72%. МС (ЭСИ) m/z:.364,1. 1Н ЯМР (400 МГц, ДМСО) δ 9,20 (d, J=8,2 Гц, 2Н), 8,94 (s, 1Н), 8,64-8,59 (m, 1Н), 8,43 (s, 1Н), 7,77 (t, J=8,1 Гц, 1H), 7,23 (d, J=7,7 Гц, 1H), 6,81 (d, J=8,4 Гц, 1H), 3,65-3,57 (m, 4Н), 2,96-2,88 (m, 4Н).
Пример 10 (3R)-1-[6-(6-тиазол-5-илпиразоло[4,3-с]пиридин-1-ил)-2-пиридил]пиперидин-3-амин 110
Следуя способам получения в примере 9, получали 110. МС (ЭСИ) m/z:.378,1. 1Н ЯМР (400 МГц, ДМСО) δ 9,19 (d, J=13,5 Гц, 2Н), 8,96 (s, 1Н), 8,60 (d, J=9,0 Гц, 2Н), 7,74 (t, J=8,1 Гц, 1Н), 7,18 (d, J=7,7 Гц, 1Н), 6,81 (d, J=8,5 Гц, 1Н), 4,22 (dd, J=10,2, 6,2 Гц, 2Н), 3,15-3,04 (m, 1Н), 2,91-2,74 (m, 2Н), 2,00-1,90 (m, 1Н), 1,90-1,80 (m, 1Н), 1,79-1,50 (m, 3Н), 1,41-1,27 (m, 1Н).
Пример 11 6-(5-циклопропилпиридин-3-ил)-1-(6-(пиперазин-1-ил)пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридин 111
Следуя способам, описанным в примере 8, и начиная с 6-(5-циклопропилпиридин-3-ил)-1-(6-фторпиридин-2-ил)-1Н-пиразоло[4,3-с]пиридина и пиперазина, получали 111 в виде твердого вещества белого оттенка (41,7 мг, 31%). 1Н ЯМР (400 МГц, ДМСО) δ 9,33-9,28 (s, 1Н), 9,06-8,99 (d, J=2,5 Гц, 2Н), 8,66-8,61 (s, 1Н), 8,50-8,45 (d, J=2,1 Гц, 1Н), 8,09-8,03 (t, Л=2,0 Гц, 1Н), 7,81-7,73 (t, J=8,1 Гц, 1Н), 7,29-7,20 (d, J=7,7 Гц, 1Н), 6,85-6,76 (d, J=8,5 Гц, 1Н), 3,65-3,56 (m, 4Н), 2,94-2,84 (m, 4Н), 2,13-2,04 (m, 1Н), 1,12-1,04 (m, 2Н), 0,88-0,81 (m, 2Н); МС (ЭСИ) m/z: 398,2 [М+Н]+.
Пример 12 6-(5-циклопропилпиридин-3-ил)-1-(6-(пиперазин-1-ил)пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридин 112
Следуя способам, описанным в примере 8, и начиная с 6-(5-циклопропилпиридин-3-ил)-1-(6-фторпиридин-2-ил)-1Н-пиразоло[4,3-с]пиридина и 1,4-диазепана, получали 112 в виде твердого вещества белого оттенка (30,9 мг, 22%). 1Н ЯМР (400 МГц, ДМСО) δ 9,37-9,25 (s, 1Н), 9,04-8,98 (s, 2Н), 8,67-8,59 (s, 1H), 8,51-8,45 (d, J=2,1 Гц, 1H), 8,05-7,99 (t, J=2,1 Гц, 1H), 7,74-7,66 (dd, J=14,5, 6,5 Гц, 1H), 7,24-7,15 (t, J=7,4 Гц, 1H), 6,65-6,58 (d, J=8,5 Гц, 1H), 3,90-3,73 (dt, J=10,0, 5,5 Гц, 4H), 3,00-2,91 (m, 2H), 2,75-2,65 (dd, J=13,3, 7,3 Гц, 2H), 2,12-2,04 (m, 1H), 1,91-1,81 (m, 2H), 1,12-1,03 (m, 2H), 0,88-0,81 (m, 2H); МС (ЭСИ) m/z: 412,2 [M+H]+.
Пример 13 (S)-1-(6-(3-метилпиперазин-1-ил)пиридин-2-ил)-6-(5-(оксетан-3-ил)пиридин-3-ил)-1Н-пиразоло[4,3-с]пиридин 113
Следуя способам, описанным в примере 8, и начиная с 1-(6-фторпиридин-2-ил)-6-(5-(оксетан-3-ил)пиридин-3-ил)-1Н-пиразоло[4,3-с]пиридина и (S)-2-метилпиперазина, получали 113 в виде твердого вещества белого оттенка (26,3 мг, 24%). 1Н ЯМР (400 МГц, ДМСО) δ 9,39-9,28 (m, 1Н), 9,20-9,11 (d, J=2,1 Гц, 1Н), 9,11-9,02 (s, 1Н), 8,72-8,61 (m, 2Н), 8,60-8,53 (t, J=2,1 Гц, 1Н), 7,84-7,67 (t, J=8,1 Гц, 1Н), 7,32-7,18 (d, J=7,7 Гц, 1Н), 6,87-6,76 (d, J=8,5 Гц, 1Н), 5,08-4,98 (dd, J=8,2, 6,2 Гц, 2Н), 4,76-4,68 (t, J=6,3 Гц, 2Н), 4,48-4,35 (m, 1Н), 4,28-4,13 (dd, J=20,9, 11,0 Гц, 2Н), 3,06-2,88 (ddd, J=19,7, 14,7, 7,1 Гц, 2Н), 2,87-2,73 (m, 2Н), 2,60-2,53 (m, 1Н), 2,39-2,31 (d, J=7,7 Гц, 1Н), 1,09 -0,99 (dd, J=14,9, 6,2 Гц, 3Н); МС (ЭСИ) m/z: 428,2 [М+Н]+.
Пример 14 6-(5-(оксетан-3-ил)пиридин-3-ил)-1-(6-(пиперазин-1-ил)пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридин 114
Следуя способам, описанным в примере 8, и начиная с 1-(6-фторпиридин-2-ил)-6-(5-(оксетан-3-ил)пиридин-3-ил)-1Н-пиразоло[4,3-с]пиридина и пиперазина, получали 114 в виде твердого вещества белого оттенка (14,3 мг, 13%). 1Н ЯМР (400 МГц, ДМСО) δ 9,36-9,31 (s, 1Н), 9,20-9,14 (d, J=2,1 Гц, 1Н), 9,10-9,05 (s, 1Н), 8,70-8,62 (m, 2Н), 8,57-8,52 (t, J=2,0 Гц, 1Н), 7,81-7,74 (t, J=8,1 Гц, 1Н), 7,28-7,22 (d, J=7,7 Гц, 1Н), 6,85-6,78 (d, J=8,4 Гц, 1Н), 5,08-5,00 (dd, J=8,3, 6,1 Гц, 2Н), 4,77-4,70 (t, J=6,3 Гц, 2Н), 4,47-4,38 (m, 1Н), 3,65-3,56 (m, 4Н), 2,99-2,75 (m, 4Н); МС (ЭСИ) m/z: 414,2 [М+Н]+.
Пример 15 1-(6-(6-(5-циклопропилпиридин-3-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-6-ол 115
Следуя способам, описанным в примере 8, и начиная с 6-(5-циклопропилпиридин-3-ил)-1-(6-фторпиридин-2-ил)-1Н-пиразоло[4,3-с]пиридина и 1,4-диазепан-6-ола, получали 115 в виде твердого вещества белого оттенка (25,1 мг, 17%). 1Н ЯМР (400 МГц, ДМСО) δ 9,31-9,27 (s, 1Н), 9,07-9,00 (dd, J=16,3, 6,5 Гц, 2Н), 8,65-8,59 (d, J=5,6 Гц, 1Н), 8,48-8,44 (t, J=2,8 Гц, 1Н), 8,09-8,03 (t, J=2,0 Гц, 1Н), 7,73-7,67 (t, J=8,1 Гц, 1Н), 7,20-7,14 (d, J=7,7 Гц, 1Н), 6,73-6.68 (d, J=8,5 Гц, 1Н), 4,82-4,73 (s, 1Н), 4,03-3,87 (m, 3Н), 3,74-3,57 (m, 2Н), 3.02-2,93 (t, J=5,4 Гц, 2Н), 2,87-2,75 (dd, J=13,8, 3,8 Гц, 1Н), 2,70-2,60 (dd, J=13,8, 5,9 Гц, 1Н), 2,15-2,03 (m, 1Н), 1,10-1,02 (m, 2Н), 0,92-0,82 (m, 2Н); МС (ЭСИ) m/z:.428,2 [М+Н]+.
Пример 16 1-(6-(6-(5-(оксетан-3-ил)пиридин-3-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-6-ол 116
Следуя способам, описанным в примере 8, и начиная с 1-(6-фторпиридин-2-ил)-6-(5-(оксетан-3-ил)пиридин-3-ил)-1Н-пиразоло[4,3-с]пиридина и 1,4-диазепан-6-ола, получали 116 в виде твердого вещества белого оттенка (7,2 мг, 6%). 1Н ЯМР (400 МГц, ДМСО) δ 9,35-9,29 (s, 1Н), 9,23-9,16 (dd, J=8,9, 2,0 Гц, 1Н), 9,11-9,04 (d, J=8,6 Гц, 1Н), 8,77-8,62 (m, 2Н), 8,55-8,46 (dd, J=15,4, 8,6 Гц, 1Н), 7,74-7,67 (t, J=8,1 Гц, 1Н), 7,21-7,16 (d, J=7,7 Гц, 1Н), 6,77-6,68 (dd, J=8,5, 2,9 Гц, 1Н), 5,69-5,45 (d, J=72,4 Гц, 1Н), 5,06-5,00 (dd, J=8,1, 6,2 Гц, 1Н), 4,81-4,70 (dd, J=13,5, 6,7 Гц, 2Н), 4,48-4,40 (m, 1Н), 4,06-3,85 (dd, J=32,4, 13,9 Гц, 3Н), 3,74-3,53 (m, 2Н), 3,00-2,93 (d, J=2,3 Гц, 2Н), 2,83-2,77 (dd, J=13,8, 3,8 Гц, 1Н), 2,70-2,62 (dd, J=13,2, 6,0 Гц, 1Н); МС (ЭСИ) m/z: 444,2 [М+Н]+.
Пример 17 (S)-1 -(3-хлор-6-(6-(5-этилпиридин-3-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)пиперидин-3-амин 117
Стадия А: 2-[(6-хлорпиразоло[4,3-с]пиридин-1-ил)метокси]этил-триметил-силан
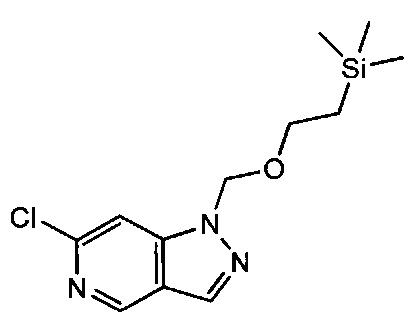
К смеси 6-хлор-1Н-пиразоло[4,3-с]пиридина (12,82 ммоль; 1968 мг) в дихлорметане (50 мл) добавляли 1Ч,М-диизопропилэтиламин (38,45 ммоль, 6,7 мл). Затем добавляли по каплям 2-(триметилсилил)этоксиметилхлорид (19,22 ммоль; 3205 мг; 3,40 мл) при комнатной температуре. Полученную в результате смесь перемешивали в течение ночи. Смесь разделяли между ДХМ и водой. Органический слой концентрировали и остаток очищали на силикагеле, элюируя 0 до 6% МеОН в ДХМ, получая 2-[(6-хлорпиразоло[4,3-с]пиридин-1-ил)метокси]этил-триметил-силан (590 мг, 13%).
Стадия В: триметил-[2-[[6-(5-винил-3-пиридил)пиразоло[4,3-с]пиридин-1-ил]метокси]этил]силан
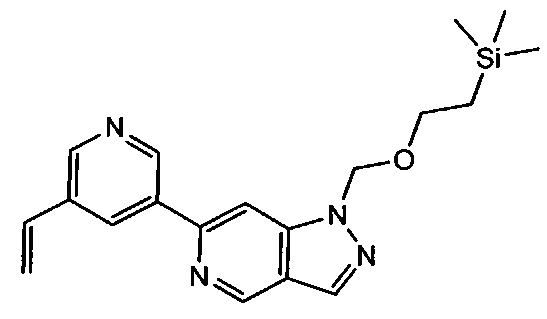
Смесь 2-[(6-хлорпиразоло[4,3-с]пиридин-1-ил)метокси]этил-триметил-силана (1,074 ммоль; 304,8 мг), 3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-5-винил-пиридина (1,611 ммоль; 372,3 мг), аддукта [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладия (II) дихлорметана (0,1074 ммоль; 89,5 мг), ацетата калия (1,611 ммоль; 1,6 мл) и карбоната натрия (1,611 ммоль; 1,6 мл) в ацетонитриле (10 мл) в пробирке высокого давления нагревали в микроволновой печи при 150°С в течение 5 минут. Смесь охлаждали до комнатной температуры. Слои разделяли. Водный слой экстрагировали ЕtOАс. Объединенный органический слой концентрировали. Остаток очищали на силикагеле, элюируя 0 до 6% МеОН в ДХМ, получая триметил-[2-[[6-(5-винил-3-пиридил)пиразоло[4,3-с]пиридин-1-ил]метокси]этил]силан (543,4 мг, 86%).
Стадия С: 6-(5-этил-3-пиридил)-1Н-пиразоло[4,3-с]пиридин
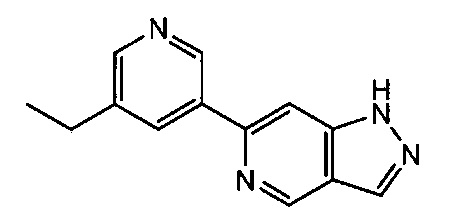
К раствору триметил-[2-[[6-(5-винил-3-пиридил)пиразоло[4,3-с]пиридин-1-ил]метокси]этил]силана (543,4 мг) в этаноле (50 мл) в 250 мл круглодонной колбе добавляли катализатор Перлмана (0,1850 ммоль; 129,9 мг). Колбу вакуумировали и соединяли с баллоном водорода. Смесь перемешивали при комнатной температуре в течение ночи. Смесь фильтровали через Целит. Фильтрат концентрировали. Остаток очищали на силикагеле, элюируя 0 до 5% МеОН в ДХМ, получая 2-[[6-(5-этил-3-пиридил)пиразоло[4,3-с]пиридин-1-ил]метокси]этил-триметил-силан (87 мг, 27%).
Раствор 2-[[6-(5-этил-3-пиридил)пиразоло[4,3-с]пиридин-1-ил]метокси]этил-триметил-силана (0,2456 ммоль; 106,8 мг) и анизола (1,228 ммоль; 133 мг; 0,134 мл) в хлороводороде, 4,0 М в 1,4-диоксане (20 ммоль; 5 мл) перемешивали при комнатной температуре в течение ночи. Смесь концентрировали, получая 6-(5-этил-3-пиридил)-1Н-пиразоло[4,3-с]пиридин (~95,9 мг), который использовали без очистки.
Стадия D: 1-(5-хлор-6-фтор-2-пиридил)-6-(5-этил-3-пиридил)пиразоло[4,3-с]пиридин
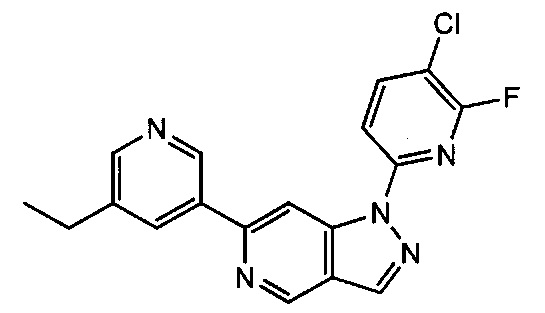
К раствору вышеуказанного 6-(5-этил-3-пиридил)-1Н-пиразоло[4,3-с]пиридина (0,264 ммоль; 95,9 мг) и 6-бром-3-хлор-2-фтор-пиридина (0,396 ммоль; 83,4 мг) в 1,4-диоксане (10 мл) в атмосфере азота добавляли карбонат цезия (0,528 ммоль; 172 мг), ксантфос (0,0449 ммоль; 26,0 мг) и трис(дибензилиденацетон)дипалладий (0) (0,0264 ммоль; 24,2 мг). Полученную в результате смесь закрывали в пробирке высокого давления и нагревали при 100°С в течение 17 часов. Реакционную смесь охлаждали до комнатной температуры и фильтровали через Целит. Осадок на фильтре промывали ДХМ. Фильтрат концентрировали. Остаток очищали на силикагеле, элюируя 0 до 6% МеОН в ДХМ, получая 1-(5-хлор-6-фтор-2-пиридил)-6-(5-этил-3-пиридил)пиразоло[4,3-с]пиридин (54,9 мг, 59%).
Стадия Е: трет-бутил N-[(38)-1-[3-хлор-6-[6-(5-этил-3-пиридил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-3-пиперидил]карбамат
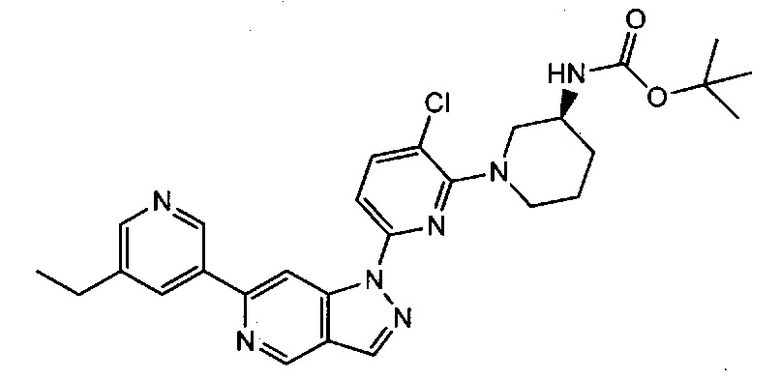
Смесь 1-(5-хлор-6-фтор-2-пиридил)-6-(5-этил-3-пиридил)пиразоло[4,3-с]пиридина (0,155 ммоль; 54,9 мг), трет-бутил N-[(3S)-3-пиперидил]карбамата (0,466 ммоль; 93,2 мг) и N-метилморфолина (1,55 ммоль; 159 мг; 0,172 мл) в 1-метил-2-пирролидиноне (3 мл) в закрытом сосуде высокого давления нагревали при 100°С в течение ночи. Смесь выливали в воду. Осадок собирали фильтрованием и сушили в высоком вакууме, получая трет-бутил N-[(3S)-1-[3-хлор-6-[6-(5-этил-3-пиридил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-3-пиперидил]карбамат (66,6 мг, 80%), который использовали без дополнительной очистки.
К раствору трет-бутил N-[(3S)-1-[3-xлop-6-[6-(5-этил-3-пиридил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-3-пиперидил]карбамата (0,0446 ммоль; 23,8 мг) в метаноле (10 мл) добавляли соляную кислоту, 4,0 М в 1,4-диоксане (5 мл). Полученную в результате смесь перемешивали при комнатной температуре в течение ночи. Смесь концентрировали и остаток очищали с помощью обращенно-фазовой ВЭЖХ, получая 117 (7,0 мг, 33%). 1Н ЯМР (400 МГц, ДМСО) δ 9,36-9,31 (s, 1Н), 9,18-9,11 (m, 2Н), 8,74-8,65 (s, 1Н), 8,58-8,52 (d, J=1,9 Гц, 1Н), 8,34-8,30 (s, 1Н), 8,02-7,97 (d, J=8,4 Гц, 1Н), 7,60-7,55 (d, J=8,4 Гц, 1Н), 3,95-3,81 (dd, J=27,5, 10,2 Гц, 2Н), 3,06-2,97 (t, J=10,2 Гц, 1Н), 2,93-2,84 (t, J=9,5 Гц, 1Н), 2,81-2,72 (m, 3Н), 1,98-1,90 (d, J=12,6 Гц, 1Н), 1,89- 1,80 (d, J=13,3 Гц, 1Н), 1,79-1,68 (d, J=12,9 Гц, 1Н), 1,68-1,48 (s, 2Н), 1,31-1,26 (t, J=7,6 Гц, 3Н), 1,26-1,20 (m, 1Н); МС (ЭСИ) m/z: 434,2 [М+Н]+.
Пример 18 1-(6-(1,4-диазепан-1-ил)пиридин-2-ил)-6-(5-(оксетан-3-ил)пиридин-3-ил)-1Н-пиразоло[4,3-с]пиридин 118
Следуя способам, описанным в примере 8, и начиная с 1-(6-фторпиридин-2-ил)-6-(5-(оксетан-3-ил)пиридин-3-ил)-1Н-пиразоло[4,3-с]пиридина и 1,4-диазепана, получали 118 в виде твердого вещества белого оттенка (22,8 мг, 18%). 1Н ЯМР (400 МГц, ДМСО) δ 9,36-9,33 (s, 1Н), 9,18-9,13 (t, J=4,0 Гц, 1Н), 9,10-9,05 (s, 1Н), 8,68-8,62 (d, J=5,1 Гц, 2Н), 8,55-8,50 (s, 1Н), 7,74-7,69 (dd, J=13,8, 5,6 Гц, 1Н), 7,23-7,18 (d, J=7,7 Гц, 1Н), 6,65-6,61 (d, J=8,5 Гц, 1Н), 5,07-5,00 (dd, J=8,3, 6,1 Гц, 2Н), 4,76-4,69 (t, J=6,3 Гц, 2Н), 4,48-4,36 (гл, 1Н), 3,90-3,83 (t, J=5,8 Гц, 2Н), 3,83-3,77 (d, J=5,3 Гц, 2Н), 3,01-2,93 (m, 2Н), 2,75-2,69 (m, 2Н), 1,89-1,83 (m, 2Н); МС (ЭСИ) m/z: 428,2 [М+Н]+.
Пример 19 3-метил-5-[1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридин-6-ил]изотиазол 119
Раствор трет-бутил 4-[6-(6-хлорпиразоло[4,3-с]пиридин-1-ил)-2-пиридил]пиперазин-1-карбоксилата (120 мг, 0,290 ммоль) и тетракис(трифенилфосфин)палладия (0) (34 мг, 0,0290 ммоль) в 1,0 мл N,N-диметилацетамида добавляли к трибутил-(3-метилизотиазол-5-ил)станнану (224 мг, 0,579 ммоль). Реакционную смесь нагревали при 150°С в течение 45 минут в микроволновой печи (Biotage Inc.). Реакционную смесь фильтровали через целит и концентрировали. Неочищенный продукт разбавляли ЕtOАс, затем промывали водой. Органические слои сушили с сульфатом натрия, фильтровали и концентрировали в вакууме. Неочищенный продукт очищали с помощью флэш-хроматографии (элюировали ЕtOАс/гептаном при 20% ЕtOАс), получая трет-бутил 4-[6-[6-(3-метилизотиазол-5-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперазин-1-карбоксилат (65 мг) с выходом 47%:
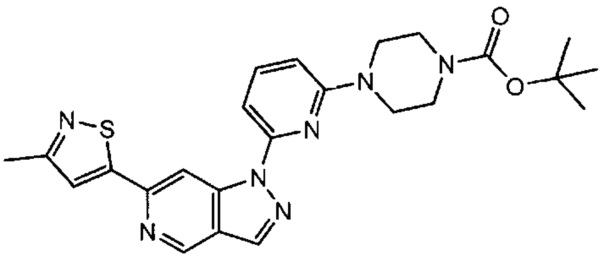
Раствор, содержащий трет-бутил 4-[6-[6-(3-метилизотиазол-5-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперазин-1-карбоксилат (65 мг, 0,136 ммоль) в хлороводороде (4 моль/л) в 1,4-диоксане (2,0 мл, 8,0 ммоль), и 1,4-диоксан; 1,0 мл, перемешивали при к.т.в течение 18 часов. Реакционную смесь концентрировали под вакуумом. Неочищенный продукт подвергали обращенно-фазовой ВЭЖХ, получая 118 (13 мг) с выходом 25%. 1Н ЯМР (400 МГц, ДМСО) δ 9,22 (s, 1Н), 8,96 (s, 1Н), 8,64 (s, 1Н), 7,78 (t, J=8,1 Гц, 1Н), 7,54 (s, 1Н), 7,24 (d, J=7,7 Гц, 1Н), 6,82 (d, J=8,5 Гц, 1Н), 3,65-3,58 (m, 4Н), 2,98-2,90 (m, 4Н). МС (ЭСИ) m/z: 378,1.
Пример 20 5-[1-[6-(1,4-диазепан-1-ил)-2-пиридил]пиразоло[4,3-с]пиридин-6-ил]-3-метил-изотиазол 120
Следуя способам получения в примере 19, получали 120. МС (ЭСИ) т/г.392.1. 1Н ЯМР (400 МГц, ДМСО) δ 9,22 (s, 1Н), 8,92 (d, J=6,9 Гц, 1Н), 8,64 (s, 1Н), 7,74-7,67 (m, 1Н), 7,54 (s, 1Н), 7,17 (d, J=7,7 Гц, 1Н), 6,64 (d, J=8,5 Гц, 1Н), 3,86 (t, J=5,9 Гц, 2Н), 3,83-3,76 (m, 2Н), 3,04-2,97 (m, 2Н), 2,73 (t, J=5,8 Гц, 2Н), 1,90 (dd, J=11,6. 5,8 Гц, 2Н).
Пример 21 (S)-1-(6-(6-(5-этилпиридин-3-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-6-ол 121
Рацемический 1-(6-(6-(5-этилпиридин-3-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-6-ол (30 мг) очищали с помощью хиральной ВЭЖХ, получая энантиомер 121 в виде твердого вещества белого оттенка (7,9 мг, 26%). 1Н ЯМР (400 МГц, ДМСО) δ 9,35-9,28 (s, 1Н), 9,16-9,10 (t, J=4,0 Гц, 1Н), 9,07-9,04 (s, 1Н), 8,67-8,61 (s, 1Н), 8,56-8,50 (d, J=1,8 Гц, 1Н), 8,33-8,28 (s, 1Н), 7,74-7,68 (t, J=8,1 Гц, 1Н), 7,21-7,17 (d, J=7,7 Гц, 1Н), 6,74-6,69 (t, J=7,5 Гц, 1Н), 4,91-4,77 (s, 1Н), 4,06-3,86 (m, 3Н), 3,75-3,57 (m, 2Н), 3,04-2,96 (m, 2Н), 2,86-2,63 (m, 4Н), 1,31-1,25 (t, J=7,6 Гц, 3Н); МС (ЭСИ) m/z: 416,1 [М+Н]+.
Пример 22 (R)-1-(6-(6-(5-этилпиридин-3-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-6-ол 122
Рацемический 1-(6-(6-(5-этилпиридин-3-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-6-ол (30 мг) очищали с помощью хиральной ВЭЖХ, получая энантиомер 122 в виде твердого вещества белого оттенка (7,6 мг, 25%). 1Н ЯМР (400 МГц, ДМСО) δ 9,34-9,28 (s, 1Н), 9,14-9,10 (d, J=1,8 Гц, 1Н), 9,07-9,03 (s, 1Н), 8,67-8,60 (s, 1Н), 8,57-8,49 (d, J=1,8 Гц, 1Н), 8,33 -8,27 (s, 1Н), 7,75-7,68 (t, J=8,1 Гц, 1Н), 7,22-7,16 (d, J=7,7 Гц, 1Н), 6,74-6,68 (d, J=8,5 Гц, 1Н), 4,90-4,74 (s, 1Н), 4,08-3,85 (m, 3Н), 3,76-3,55 (m, 2Н), 3,03-2,95 (t, J=5,4 Гц, 2Н), 2,87-2,64 (m, 4Н), 1,30-1,26 (t, J=7,6 Гц, 3Н); МС (ЭСИ) m/z: 416,1 [М+Н]+.
Пример 23 6-(6-метилпиразин-2-ил)-1-(6-(пиперазин-1-ил)пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридин 123
Стадия А: Получение триметил-(6-метилпиразин-2-ил)станнана
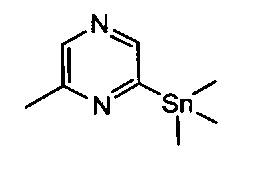
Раствор 2-бром-6-метил-пиразина (300 мг, 1,7 ммоль), гексаметилдиолова (0,45 мл, 2,1 ммоль) и тетракис(трифенилфосфин) (142 мг, 0,123 ммоль) в 8,0 мл 1,4-диоксана продували N2 в течение 5 минут. Реакционную смесь перемешивали при 100°С в течение 18 часов. Реакционную смесь фильтровали через целит. Неочищенный продукт использовали на следующей стадии. МС (ЭСИ) m/z: 259,1.
Стадия В: трет-бутил 4-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперазин-1-карбоксилат
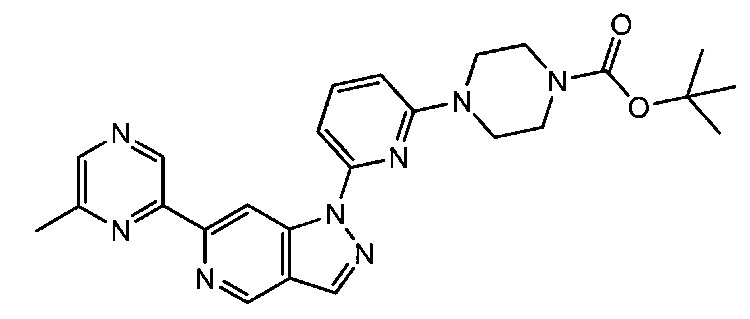
К раствору трет-бутил 4-[6-(6-хлорпиразоло[4,3-с]пиридин-1-ил)-2-пиридил]пиперазин-1-карбоксилата (90 мг; 0,22 ммоль) и тетракис(трифенилфосфин)палладия (0) (25 мг, 0,022 ммоль) в N,N-диметилацетамиде; 2,0 мл, добавляли триметил-(6-метилпиразин-2-ил)станнан (112 мг; 0,436 ммоль). Реакционную смесь нагревали при 150°С в течение 45 минут в микроволновой печи (Biotage). Реакционную смесь фильтровали через целит и концентрировали. Неочищенный продукт разбавляли ЕtOАс, затем промывали водой. Органические слои сушили с сульфатом натрия, фильтровали и концентрировали в вакууме. Неочищенный продукт очищали с помощью флэш-хроматографии (элюировали EtOAc/гептаном при 50% EtOAc), получая 60 мг трет-бутил 4-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперазин-1-карбоксилата с выходом 58%.
Раствор трет-бутил 4-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперазин-1-карбоксилата (60 мг, 0,1270 ммоль) в 1,4-диоксане; 1,0 мл, и хлороводорода (4 моль/л) в 1,4-диоксане (2,0 мл, 8,0 ммоль) перемешивали при к.т.в течение 18 часов. Реакционную смесь концентрировали и подвергали обращенно-фазовой ВЭЖХ, получая 123 (26 мг) с выходом 32%. МС (ЭСИ) m/z:.373,2. 1Н ЯМР (400 МГц, ДМСО) δ 9,59 (s, 1Н), 9,46 (s, 1Н), 9,31 (s, 1Н), 8,66 (s, 1Н), 8,62 (s, 1Н), 7,77 (t, J=8,1 Гц, 1Н), 7,27 (d, J=7,7 Гц, 1Н), 6,80 (d, J=8,4 Гц, 1Н), 3,67-3,60 (m, 4Н), 2,96-2,89 (m, 4Н), 2,63 (s, 3Н).
Пример 24 (3S)-1-[6-[6-(3-метилизотиазол-5-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-3-амин 124
Следуя способам получения в примере 19, получали 124. МС (ЭСИ) m/z:.392,2. 1Н ЯМР (400 МГц, ДМСО) δ 9,22 (s, 1Н), 9,00 (s, 1Н), 8,64 (s, 1Н), 7,92 (s, 1Н), 7,74 (t, J=8,1 Гц, 1Н), 7,21 (d, J=7,7 Гц, 1Н), 6,82 (d, J=8,5 Гц, 1Н), 4,36 (d, J=8,9 Гц, 1Н), 4,13 (d, J=12,8 Гц, 1Н), 3,08-2,98 (m, 1Н), 2,89-2,77 (m, 2Н), 2,48 (s, 3Н), 1,97 (d, J=9,9 Гц, 1Н), 1,88-1,80 (m, 2Н), 1,60 (dd, J=24,6, 11,9 Гц, 1Н), 1,42- 1,29 (m, 1Н).
Пример 25 1-(6-(1,4-диазепан-1-ил)пиридин-2-ил)-6-(1-этил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин 125
Следуя способам, описанным в примере 8, и начиная с 1-этил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразола и 1,4-диазепана, получали 125 в виде твердого вещества белого оттенка (21,5 мг, 17%). 1Н ЯМР (400 МГц, ДМСО) δ 9,15-9,09 (s, 1Н), 8,55-8,48 (s, 1Н), 8,29-8,21 (s, 1Н), 7,92-7,86 (s, 1Н), 7,71 -7,65 (t, J=8,0 Гц, 1H), 7,17-7,12 (d, J=7,7 Гц, 1H), 6,62-6,56 (d, J=8,5 Гц, 1H), 4,24-4,19 (d, J=7,3 Гц, 2H), 3,88-3,84 (t, J=6,0 Гц, 2H), 3,82-3,77 (m, 2H), 3,02-2,95 (m, 2H), 2,76-2,69 (m, 2H), 1,90-1,86 (m, 2H), 1,45-1,42 (t, J=7,3 Гц, 3Н); МС (ЭСИ) m/z: 389,2 [М+Н]+.
Пример 26 (S)-6-(1-этил-1Н-пиразол-4-ил)-1-(6-(3-метилпиперазин-1-ил)пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридин 126
Следуя способам, описанным в примере 8, и начиная с 1-этил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразола и (S)-2-метилпиперазина, получали 126 в виде твердого вещества белого оттенка (19,7 мг, 16%). 1Н ЯМР (400 МГц, ДМСО) δ 9,18-9,09 (s, 1Н), 8,72-8,60 (s, 1Н), 8,56-8,47 (s, 1Н), 8,30 -8,25 (s, 1Н), 7,96-7,89 (s, 1Н), 7,78-7,71 (t, J=8,1 Гц, 1Н), 7,24-7,17 (d, J=7,7 Гц, 1Н), 6,82-6,75 (d, J=8,4 Гц, 1Н), 4,27-4,13 (m, 4Н), 3,09-3,01 (d, J=11,4 Гц, 1Н), 2,99-2,89 (m, 1Н), 2,89-2,76 (m, 2Н), 2,63-2,55 (m, 1Н), 1,47-1,39 (t, J=7,3 Гц, 3Н), 1,13-1,06 (d, J=6,2 Гц, 3Н); МС (ЭСИ) m/z: 389,0 [М+Н]+.
Пример 27 (S)-1-(6-(6-(1-этил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)пирролидин-3-ол 127
Следуя способам, описанным в примере 8, и начиная с 1-этил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразола и (S)-пирролидин-3-ола, получали 127 в виде твердого вещества белого оттенка (18,6 мг, 14%). 1Н ЯМР (400 МГц, ДМСО) 5 9,19-9,05 (s, 1Н), 8,92-8,78 (s, 1Н), 8,55-8,46 (s, 1Н), 8,34 -8,20 (d, J=8,3 Гц, 1Н), 7,99-7,91 (s, 1Н), 7,73-7,64 (t, J=8,0 Гц, 1Н), 7,19-7,09 (d, J=7,7 Гц, 1Н), 6,42-6,35 (d, J=8,3 Гц, 1Н), 5,15-5,01 (d, J=3,7 Гц, 1H), 4,57-4,47 (s, 1Н), 4,26-4,16 (q, J=7,3 Гц, 2H), 3,80-3,71 (d, J=6,4 Гц, 1H), 3,72-3,60 (s, 2Н), 3,58-3,45 (d, J=10,6 Гц, 1H), 2,20-2,09 (ddd, J=13,1, 8,6, 4,6 Гц, 1H), 2,06-1,97 (d, J=3,3 Гц, 1H), 1,48-1,40 (q, J=7,5 Гц, 3Н); МС (ЭСИ) m/z: 376,2 [М+Н]+.
Пример 28 (R)-1-(6-(6-(1-этил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)пирролидин-3-ол 128
Следуя способам, описанным в примере 8, и начиная с 1-этил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразола и (R)-пирролидин-3-ола, получали 128 в виде твердого вещества белого оттенка (18,6 мг, 14%). 1Н ЯМР (400 МГц, ДМСО) δ 9,19-9,05 (s, 1Н), 8,92-8,78 (s, 1Н), 8,55-8,46 (s, 1Н), 8,34 -8,20 (d, J=8,3 Гц, 1Н), 7,99-7,91 (s, 1Н), 7,73-7,64 (t, J=8,0 Гц, 1Н), 7,19- 7,09 (d, J=7,7 Гц, 1Н), 6,42-6,35 (d, J=8,3 Гц, 1Н), 5,15-5,01 (d, J=3,7 Гц, 1Н), 4,57-4,47 (s, 1Н), 4,26-4,16 (q, J=7,3 Гц, 2Н), 3,80-3,71 (d, J=6,4 Гц, 1Н), 3,72 -3,60 (s, 2Н), 3,58-3,45 (d, J=10,6 Гц, 1Н), 2,20-2,09 (ddd, J=13,1, 8,6, 4,6 Гц, 1Н), 2,06-1,97 (d, J=3,3 Гц, 1Н), 1,48-1,40 (q, J=7,5 Гц, 3Н); МС (ЭСИ) m/z: 376,2 [M+H]+.
Пример 29 1-(6-(6-(1-этил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)пиперидин-4-ол 129
Следуя способам, описанным в примере 8, и начиная с 1-этил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразола и пиперидин-4-ола, получали 129 в виде твердого вещества белого оттенка (23,8 мг, 19%). 1Н ЯМР (400 МГц, ДМСО) δ 9,18-9,07 (s, 1Н), 8,70-8,60 (s, 1Н), 8,57-8,49 (s, 1Н), 8,30-8,22 (s, 1Н), 7,94-7,84 (s, 1Н), 7,80-7,66 (t, J=8,1 Гц, 1Н), 7,26-7,10 (d, J=7,7 Гц, 1Н), 6,88-6,73 (d, J=8,4 Гц, 1Н), 4,87-4,71 (d, J=4,2 Гц, 1Н), 4,26-4,18 (q, J=7,3 Гц, 2Н), 4,18-4,08 (dt, J=9,0, 4,3 Гц, 2Н), 3,88-3,77 (dt, J=12,7, 4,3 Гц, 1Н), 3,40-3,31 (m, 2Н), 1,98-1,88 (dd, J=8,7, 4,4 Гц, 2Н), 1,59-1,47 (m, 2Н), 1,47-1,39 (t, J=7,3 Гц, 3Н); МС (ЭСИ) m/z: 390,2 [М+Н]+.
Пример 30 6-(6-метоксипиразин-2-ил)-1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридин 130
Следуя способам получения в примере 23, получали 130. МС (ЭСИ) m/z: 389,2. 1Н ЯМР (400 МГц, ДМСО) δ 9,33 (s, 1Н), 9,28 (s, 1Н), 9,25 (s, 1Н), 8,68 (s, 1Н), 8,40 (s, 1Н), 7,79 (t, J=8,1 Гц, 1Н), 7,26 (d, J=7,7 Гц, 1Н), 6,84 (d, J=8,4 Гц, 1Н), 4,08 (s, 3Н), 3,65-3,58 (m, 5Н), 2,90-2,83 (m, 4Н).
Пример 31 1-(6-(3,3-диметилпиперазин-1-ил)пиридин-2-ил)-6-(1-этил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин 131
Следуя способам, описанным в примере 8, и начиная с 1-этил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразола и 2,2-диметилпиперазина, получали 131 в виде твердого вещества белого оттенка (14,2 мг, 11%). 1Н ЯМР (400 МГц, ДМСО) δ 9,23-9,05 (s, 1Н), 8,69-8,58 (s, 1Н), 8,57-8,48 (d, J=5,7 Гц, 1Н), 8,33-8,20 (s, 1Н), 7,98-7,88 (s, 1Н), 7,75-7,68 (t, J=8,1 Гц, 1Н), 7,21-7,12 (d, J=7,7 Гц, 1Н), 6,82-6,75 (d, J=8,5 Гц, 1Н), 4,25-4,17 (q, J=7,3 Гц, 2Н), 3,64-3,54 (m, 2Н), 3,46-3,41 (s, 2Н), 3,00-2,88 (m, 2Н), 1,47-1,39 (t, J=7,3 Гц, 3Н), 1,19-1,06 (s, 6Н); МС (ЭСИ) m/z: 403,2 [М+Н]+.
Пример 32 1-(6-(6-(1-этил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)пиперидин-4-амин 132
Следуя способам, описанным в примере 8, и начиная с 1-этил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразола и трет-бутил пиперидин-4-илкарбамата, получали 132 в виде твердого вещества белого оттенка (15,2 мг, 12%) за 2 стадии. 1Н ЯМР (400 МГц, ДМСО) δ 9,18-9,06 (s, 1Н), 8,68-8,62 (s, 1Н), 8,56-8,48 (d, J=4,4 Гц, 1Н), 8,31-8,21 (s, 1Н), 7,93-7,85 (s, 1Н), 7,77-7,68 (t, J=8,1 Гц, 1Н), 7,23-7,14 (d, J=7,7 Гц, 1Н), 6,85-6,75 (d, J=8,5 Гц, 1Н), 4,36 -4,26 (d, J=13,1 Гц, 2Н), 4,27-4,16 (q, J=7,3 Гц, 2Н), 3,20-3,10 (dd, J=18,0, 6,6 Гц, 2Н), 2,96-2,87 (td, J=9,9, 4,9 Гц, 1Н), 1,92-1,83 (dd, J=12,7, 2,9 Гц, 2Н), 1,47-1,41 (t, J=7,3 Гц, 3Н), 1,41-1,30 (m, 2Н); МС (ЭСИ) m/z: 389,2 [М+Н]+.
Пример 34 (R)-1-(6-(6-(1-этил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)пиперидин-3-амин 134
Следуя способам, описанным в примере 8, и начиная с 1-этил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразола и (R)-трет-бутил пиперидин-3-илкарбамата, получали 134 в виде твердого вещества белого оттенка (15,3 мг, 12%) за 2 стадии. 1Н ЯМР (400 МГц, ДМСО) δ 9,17-9,08 (s, 1Н), 8,72-8,65 (s, 1Н), 8,54-8,50 (s, 1Н), 8,49-8,43 (s, 1Н), 8,09-7,98 (d, J=15,0 Гц, 1Н), 7,78 -7,65 (t, J=8,1 Гц, 1Н), 7,23-7,12 (d, J=7,7 Гц, 1Н), 6,83-6,70 (d, J=8,5 Гц, 1Н), 4,37-4,29 (d, J=10,4 Гц, 1Н), 4,26-4,11 (m, 3Н), 3,09-2,99 (m, 1Н), 2,89-2,72 (m, 2Н), 2,00-1,91 (d, J=9,4 Гц, 1Н), 1,90-1,73 (m, 2Н), 1,67-1,53 (dd, J=24,3, 12,1 Гц, 1Н), 1,46-1,39 (t, J=7,3 Гц, 3Н), 1,39-1,28 (ddd, J=15,9, 12,4, 3,7 Гц, 1Н); МС (ЭСИ) m/z: 389,2 [М+Н]+.
Пример 35 (3)-1-(6-(6-(1-этил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)пирролидин-3-амин 135
Следуя способам, описанным в примере 8, и начиная с 1-этил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразола и (З)-трет-бутил пирролидин-3-илкарбамата, получали 135 в виде твердого вещества белого оттенка (11,1 мг, 8,5%) за 2 стадии. 1Н ЯМР (400 МГц, ДМСО) δ 9,14-9,09 (s, 1Н), 8,90-8,83 (d, J=16,8 Гц, 1Н), 8,57-8,46 (d, J=16,4 Гц, 1Н), 8,33-8,23 (d, J=12,5 Гц, 1Н), 7,98 -7,91 (d, J=8,6 Гц, 1Н), 7,71 -7,65 (t, J=8,0 Гц, 1Н), 7,17-7,10 (d, J=7,7 Гц, 1Н), 6,41-6,33 (d, J=8,3 Гц, 1Н), 4,26-4,16 (q, J=7,3 Гц, 2Н), 3,82-3,65 (m, 3Н), 3,65-3,54 (s, 1Н), 2,22-2,14 (dt, J=18,7, 6,2 Гц, 1Н), 1,90- 1,78 (m, 1Н), 1,47-1,41 (q, J=7,0 Гц, 3Н); МС (ЭСИ) m/z: 375,2 [М+Н]+.
Пример 36 (R)-1-(6-(6-(1-этил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)пирролидин-3-амин 136
Следуя способам, описанным в примере 8, и начиная с 1-этил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразола и (R)-трет-бутил пирролидин-3-илкарбамата, получали 136 в виде твердого вещества белого оттенка (14,5 мг, 12%) за 2 стадии. 1Н ЯМР (400 МГц, ДМСО) δ 9,16-9,08 (s, 1Н), 8,90-8,85 (s, 1Н), 8,52-8,50 (S, 1Н), 8,29-8,25 (s, 1Н), 7,99-7,92 (m, 1Н), 7,71-7,65 (t, J=8,0 Гц, 1Н), 7,16-7,10 (d, J=7,7 Гц, 1Н), 6,38-6,33 (d, J=8,3 Гц, 1Н), 4,26-4,16 (q, J=7,3 Гц, 2Н), 3,83-3,65 (m, 3Н), 3,64-3,54 (s, 1Н), 2,22-2,12 (dt, J=12,6, 6,3 Гц, 1Н), 1,89-1,79 (td, J=12,9, 6,4 Гц, 1Н), 1,47-1,41 (t, J=7,3 Гц, 3Н); МС (ЭСИ) m/z: 375,2 [М+Н]+.
Пример 37 (3S)-1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-3-амин 137
Следуя способам получения в примере 23, получали 137. 1Н ЯМР (400 МГц, ДМСО) δ 9,59 (s, 1Н), 9,46 (s, 1Н), 9,32 (s, 1Н), 8,66 (s, 1Н), 8,62 (s, 1Н), 7,75 (t, J=8,1 Гц, 1Н), 7,21 (6, J=7,7 Гц, 1Н), 6,81 (d, J=8,5 Гц, 1Н), 4,40 (d, J=13,0 Гц, 1Н), 4,15 (d, J=11,2 Гц, 1Н), 3,17-3,07 (m, 1Н), 2,89-2,75 (m, 2Н), 2,64 (s, 3Н), 1,98-1,81 (m, 2Н), 1,69-1,57 (m, 1Н), 1,40-1,27 (m, 1Н). МС (ЭСИ) m/z: 387,2.
Пример 38 1-[6-(1,4-диазепан-1-ил)-2-пиридил]-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин 138
Следуя способам получения в примере 23, получали 138. МС (ЭСИ) m/z:.387,2. 1Н ЯМР (400 МГц, ДМСО) δ 9,64 (s, 1Н), 9,46 (s, 1Н), 9,32 (s, 1Н), 8,66 (s, 1Н), 8,62 (s, 1Н), 7,71 (t, J=8,1 Гц, 1Н), 7,21 (t, J=6,8 Гц, 1Н), 6,63 (d, J=8,4 Гц, 1H), 3,89 (dd, J=15,6, 9,7 Гц, 4H), 3,08-3,00 (m, 2H), 2,78-2,70 (m, 2H), 2,61 (s, 3Н), 1,93 (dd, J=11,5, 6,0 Гц, 2H).
Пример 39 (S)-1-(3-циклопропил-6-(6-(5-этилпиридин-3-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)пиперидин-3-амин 139
Стадия А: трет-бутил N-[(3S)-1-[3-циклопропил-6-[6-(5-этил-3-пиридил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-3-пиперидил]карбамат
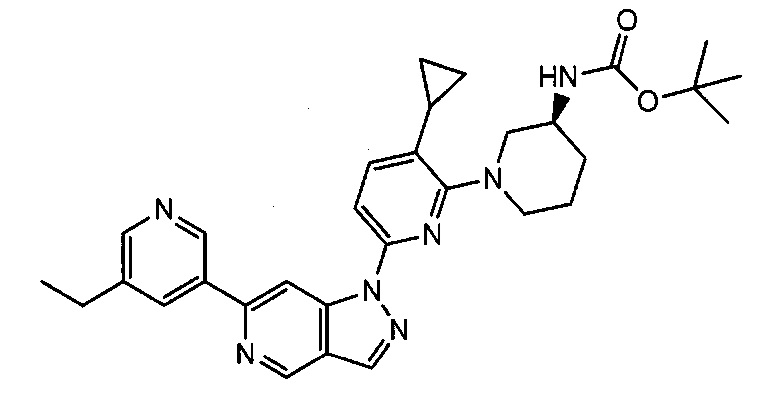
Смесь трет-бутил N-[(3S)-1-[3-хлор-6-[6-(5-этил-3-пиридил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-3-пиперидил]карбамата (0,0801 ммоль; 42,8 мг), циклопропилтрифторбората калия (0,120 ммоль; 18,3 мг), бутилди-1-адамантилфосфина (0,0240 ммоль; 9,07 мг), карбоната цезия (0,240 ммоль; 78,3 мг) и ацетата палладия (II) (0,0160 ммоль; 3,60 мг) в воде (0,5 мл) и толуоле (4,5 мл) продували аргоном в течение 1 минуты. Реакционную смесь в пробирке высокого давления перемешивали при 105°С в течение 3 дней. Слои разделяли. Органический слой концентрировали. Остаток очищали на силикагеле, элюируя 0 до 5% МеОН в ДХМ, получая трет-бутил N-[(3S)-1-[3-циклопропил-6-[6-(5-этил-3-пиридил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-3-пиперидил]карбамат (32,2 мг, 74%).
Стадия В: К раствору трет-бутил N-[(3S)-1-[3-циклопропил-6-[6-(5-этил-3-пиридил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-3-пиперидил]карбамата (0,0597 ммоль; 32,2 мг) в метаноле (10 мл) добавляли соляную кислоту, 4,0 М в 1,4-диоксане (5 мл). Полученную в результате смесь перемешивали при комнатной температуре в течение ночи. Смесь концентрировали и остаток очищали с помощью обращенно-фазовой ВЭЖХ, получая 139 в виде твердого вещества белого оттенка (20 мг, 7,4%). МС (ЭСИ) m/z:.440,3 [М+Н]+.
Пример 40 1-(6-(6-(1-этил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)азепан-4-амин 140
Следуя способам, описанным в примере 8, и начиная с 1-этил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразола и трет-бутил азепан-4-илкарбамата, получали 140 в виде твердого вещества белого оттенка (16,2 мг, 12%) за 2 стадии. 1Н ЯМР (400 МГц, ДМСО) δ 9,15-9,11 (s, 1Н), 8,70-8,65 (d, J=9,8 Гц, 1Н), 8,54-8,47 (d, J=8,1 Гц, 1Н), 8,28-8,25 (d, J=7,4 Гц, 1Н), 7,95-7,87 (s, 1Н), 7,73-7,66 (dd, J=10,5, 5,7 Гц, 1Н), 7,18-7,12 (d, J=7,7 Гц, 1Н), 6,60 -6,54 (t, J=6,6 Гц, 1Н), 4,25-4,18 (q, J=7,3 Гц, 2Н), 3,95-3,86 (s, 1Н), 3,85-3,77 (m, 1Н), 3,75-3,58 (ddd, J=20,2, 14,0, 9,4 Гц, 2Н), 2,94-2,85 (dd, J=12,2, 6,3 Гц, 1Н), 2,07-1,96 (m, 2Н), 1,83-1,74 (m, 1Н), 1,74-1,66 (d, J=14,4 Гц, 1Н), 1,65-1,56 (ddd, J-13,0, 9,1, 4,5 Гц, 1Н), 1,46-1,41 (t, J=7,3 Гц, 3Н), 1,42-1,34 (dd, J=14,2, 4,0 Гц, 1Н); МС (ЭСИ) m/z: 403,2 [М+Н]+.
Пример 41 1-(6-(1,4-диазепан-1-ил)пиридин-2-ил)-6-(5-метилпиридин-3-ил)-1Н-пиразоло[4,3-с]пиридин 141
Следуя способам, описанным в примере 8, и начиная с (5-метилпиридин-3-ил)бороновой кислоты и 1,4-диазепана, получали 141 в виде твердого вещества белого оттенка (23,3 мг, 22%) за 2 стадии. 1Н ЯМР (400 МГц, ДМСО) δ 9,33-9,29 (s, 1Н), 9,08-8,99 (m, 2Н), 8,64-8,61 (s, 1Н), 8,53-8,48 (d, J=1,5 Гц, 1Н), 8,24 -8,21 (s, 1Н), 7,74-7,67 (t, J=8,1 Гц, 1Н), 7,21-7,16 (d, J=7,7 Гц, 1Н), 6,65-6,59 (d, J=8,5 Гц, 1Н), 3,88-3,83 (t, J=6,0 Гц, 2Н), 3,82-3,74 (m, 2Н), 3,02-2,95 (m, 2Н), 2,75-2,69 (m, 2Н), 2,45-2,40 (s, 3Н), 1,92-1,83 (m, 2Н); МС (ЭСИ) m/z: 386,2 [М+Н]+.
Пример 42 (R)-6-(1-этил-1Н-пиразол-4-ил)-1-(6-(3-этилпиперазин-1-ил)пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридин 142
Следуя способам, описанным в примере 8, и начиная с 1-этил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразола и (R)-трет-бутил 2-этилпиперазин-1-карбоксилата, получали 142 в виде твердого вещества белого оттенка (12,7 мг, 10%) за 2 стадии. 1Н ЯМР (400 МГц, ДМСО) δ 9,18-9,06 (s, 1Н), 8,67-8,59 (s, 1Н), 8,56-8,49 (s, 1Н), 8,31-8,25 (s, 1Н), 7,95-7,90 (s, 1Н), 7,78-7,70 (t, J=8,1 Гц, 1Н), 7,23-7,15 (d, J=7,7 Гц, 1Н), 6,84-6,76 (d, J=8,5 Гц, 1Н), 4,27-4,15 (m, 4Н), 3,10-3,03 (d, J=11,7 Гц, 1Н), 3,01 -2,93 (td, J=11,8, 3,0 Гц, 1Н), 2,86-2,77 (td, J=11,6, 3,0 Гц, 1Н), 2,68-2,56 (m, 2Н), 1,48-1,38 (m, 5Н), 0,94-0,87 (t, J=7,5 Гц, 3Н); МС (ЭСИ) m/z: 403,2 [М+Н]+.
Пример 43 N-(6-(6-(1-этил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)азепан-3-амин 143
Следуя способам, описанным в примере 8, и начиная с 1-этил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразола и трет-бутил 3-аминоазепан-1-карбоксилата, получали 143 в виде твердого вещества белого оттенка (3,6 мг, 2,8%) за 2 стадии. МС (ЭСИ) m/z: 403,2 [М+Н]+.
Пример 44 1-(6-пиперазин-1-ил-2-пиридил)-6-пиразин-2-ил-пиразоло[4,3-с]пиридин 144
К раствору трет-бутил 4-[6-(6-хлорпиразоло[4,3-с]пиридин-1-ил)-2-пиридил]пиперазин-1-карбоксилата (40 мг, 0,096 ммоль) и тетракис(трифенилфосфин)палладия (0) (11 мг, 0,0095 ммоль) в 1 мл N,N-диметилацетамида добавляли (2-пиразинил)трибутилолово (0,064 мл, 0,19 ммоль). Реакционную смесь нагревали при 150°С в течение 45 минут в микроволновой печи biotage. Реакционную смесь фильтровали через целит и концентрировали. Неочищенный продукт разбавляли ЕtOАс, затем промывали водой. Органические слои сушили с сульфатом натрия, фильтровали и концентрировали в вакууме. Неочищенный продукт очищали с помощью флэш-хроматографии (элюировали ЕtOАс/гептаном при 20% ЕtOАс), получая 30 мг трет-бутил 4-[6-(6-пиразин-2-илпиразоло[4,3-с]пиридин-1-ил)-2-пиридил]пиперазин-1-карбоксилата с выходом 67%.
Раствор трет-бутил 4-[6-(6-пиразин-2-илпиразоло[4,3-с]пиридин-1-ил)-2-пиридил]пиперазин-1-карбоксилата (30 мг, 0,065 ммоль) в хлороводороде (4 моль/л) в 1,4-диоксане (1,5 мл, 6,0 ммоль) и 1,4-диоксана; 1,5 мл, перемешивали при к.т.в течение 18 часов. Реакционную смесь концентрировали и подвергали обращенно-фазовой ВЭЖХ, получая 144 (12 мг) с выходом 34%. МС (ЭСИ) m/z:.359,1. 1Н ЯМР (400 МГц, ДМСО) δ 9,70 (s, 1Н), 9,65 (d, J=1,1 Гц, 1Н), 9,34 (s, 1Н), 8,78-8,74 (m, 1Н), 8,72 (d, J=2,4 Гц, 1Н), 8,68 (d, J=5,3 Гц, 1Н), 7,77 (t, J=8,1 Гц, 1Н), 7,25 (d, J=7,7 Гц, 1Н), 6,79 (d, J=8,4 Гц, 1Н), 3,67-3,61 (m, 4Н), 2,97-2,90 (m, 4Н).
Пример 45 1-(6-(1,4-Диазепан-1-ил)пиридин-2-ил)-6-(1-трет-бутил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин 145
Стадия А: трет-Бутил 4-(6-бромпиридин-2-ил)-1,4-диазепан-1-карбоксилат
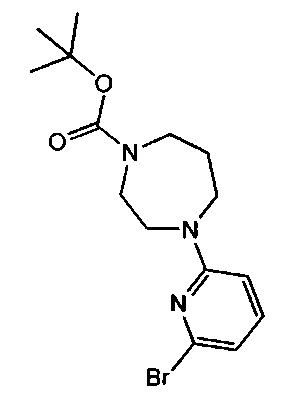
Смесь 2-бром-6-фторпиридина (500 мг, 2,8 ммоль), трет-бутил 1,4-диазепан-1-карбоксилата (568 мг, 2,8 ммоль) в ДИПЭА (1,83 г, 14,2 ммоль) в этаноле (10 мл) нагревали при 100°С в течение 16 часов. Реакционную смесь концентрировали при пониженном давлении и остаток разбавляли ЕtOАс (100 мл). Раствор промывали солевым раствором, сушили над Na2S04 и концентрировали при пониженном давлении, получая трет-бутил 4-(6-бромпиридин-2-ил)-1,4-диазепан-1-карбоксилат в виде бесцветного масла (500 мг, 50%). МС (ЭСИ) m/z: 356 [М+Н]+.
Стадия В: трет-Бутил 4-(6-(6-хлор-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилат
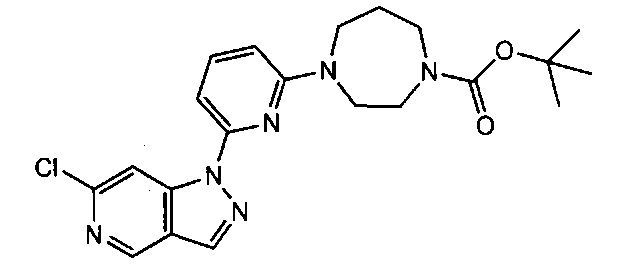
К смеси трет-бутил 4-(6-бромпиридин-2-ил)-1,4-диазепан-1-карбоксилата (2,55 г, 7,16 ммоль) и 6-хлор-1Н-пиразоло[4,3-с]пиридина (1,0 г, 6,51 ммоль) в 1,4-диоксане (20 мл) добавляли Cul (494 мг, 2,6 ммоль), К2СO3 (3,6 г, 26 ммоль) и N1,N2-диметилэтан-1,2-диамин (460 мг, 5,2 ммоль). Смесь нагревали при 100°С в течение 3 часов, контролируя с помощью ЖХМС. После завершения реакции смесь концентрировали при пониженном давлении. Неочищенное вещество очищали с помощью хроматографии на силикагеле, используя петролейный эфир/ЕtOАс (2/1) в качестве элюирующих растворителей, получая трет-бутил 4-(6-(6-хлор-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилат в виде желтого твердого вещества (1,6 г, 57%). МС (ЭСИ) m/z: 429 [М+Н]+.
Стадия С: 1-трет-Бутил-1Н-пиразол.
Смесь 1,1,3,3-тетраметоксипропана (3,7 г, 22,6 ммоль), трет-бутилгидразина гидрохлорида (2,8 г, 22,6 ммоль) и конц. HCl (6 мл, 72 ммоль) в ЕtOН (30 мл) нагревали с обратным холодильником в течение ночи. Реакционную смесь выливали в воду и полученную в результате смесь экстрагировали эфиром (30 мл × 3). Объединенные органические вещества промывали солевым раствором (20 мл), сушили над MgSO4 и концентрировали при пониженном давлении, получая 1-трет-бутил-1Н-пиразол в виде белого твердого вещества (2,5 г, 89%). МС (ЭСИ) m/z: 125 [М+Н]+.
Стадия D: 4-Бром-1-трет-бутил-1Н-пиразол.
К суспензии Na2CO3 (3,6 г, 33,9 ммоль) в CH2Cl2 (30 мл) добавляли 1-трет-бутил-1Н-пиразол (2,1 г, 17 ммоль) и Вr2 (0,9 мл). Смесь перемешивали при комнатной температуре в течение ночи. Образовавшееся твердое вещество удаляли фильтрованием и осадок на фильтре промывали CH2Cl2 (30 мл). Фильтраты промывали водой (20 мл) и солевым раствором (20 мл), сушили (MgSO4) и концентрировали при пониженном давлении, получая неочищенный 4-бром-1-трет-бутил-1Н-пиразол (2,9 г, 85%), который использовали на следующей стадии без дополнительной очистки. МС (ЭСИ) m/z:.203 [М+Н]+.
Стадия Е: 1-трет-Бутил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразол.
Смесь 4-бром-1-трет-бутил-1Н-пиразола (3,3 г, 16,3 ммоль), бис(пинаколато)диборона (8,3 г, 32,6 ммоль), PdCl2(dppf) (1,8 г, 2,4 ммоль) и КОАс (3,2 г, 32,6 ммоль) в 1,4-диоксане (60 мл) нагревали с обратным холодильником в течение 15 часов. После завершения реакции смесь фильтровали и осадок на фильтре промывали ЕtOАс (100 мл). Фильтрат концентрировали при пониженном давлении. Остаток очищали с помощью хроматографии на силикагеле, используя гептан/этилацетат (10% до 50%) в качестве элюирующих растворителей, получая 1-трет-бутил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразол в виде белого твердого вещества (1,0 г, 25%). МС (ЭСИ) m/z:.251 [М+Н]+.
Стадия F: трет-Бутил 4-(6-(6-(1-трет-бутил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилат.
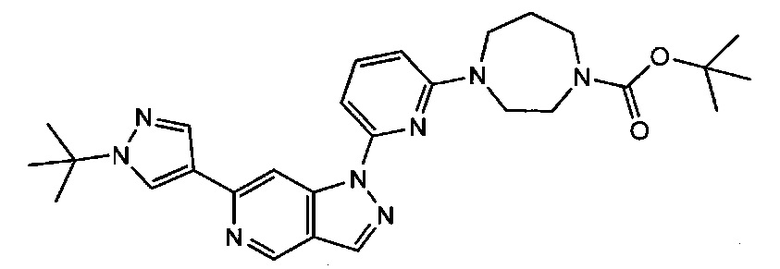
Смесь 1 -трет-бутил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразола (220 мг, 0,88 ммоль), трет-бутил 4-(6-(6-хлор-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилата (377 мг, 0,88 ммоль) и Pd(dppf)Cl2 (64 мг, 0,088 ммоль) в 1,4-диоксане (20 мл) и Na2CO3 (2,0 М, 5 мл) в атмосфере азота нагревали при 100°С в течение 20 часов. Неочищенный продукт очищали с помощью хроматографии на силикагеле, используя петролейный эфир: ЕtOАс (50% ~ 100%) в качестве элюирующих растворителей, получая трет-бутил 4-(6-(6-(1-трет-бутил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилат в виде желтого твердого вещества (240 мг, 53%). МС (ЭСИ) m/z: 517 [М+Н]+.
Стадия G: Раствор трет-бутил 4-(6-(6-(1-трет-бутил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилата (100 мг, 0,19 ммоль) и ТФК (2 мл) в ДХМ (4 мл) перемешивали при комнатной температуре в течение 4 часов. Реакционную смесь концентрировали при пониженном давлении, получая остаток. Остаток разбавляли МеОН (10 мл), нейтрализовали 28% раствором аммиака, концентрировали и очищали с помощью препаративной ВЭЖХ, получая 145 в виде белого твердого вещества (45 мг, 56%). 1Н-ЯМР (500 МГц, CD3OD) δ (ррm) 9,03 (s, 1Н), 8,71 (d, J=6,5 Гц, 1Н), 8,36 (s, 1Н), 8,28 (s, 1Н), 7,98 (s, 1Н), 7,65-7,68 (m, 1Н), 7,25 (d, J=7,5 Гц, 1Н), 6,58 (d, J=8,5 Гц, 1Н), 3,90-3,94 (m, 4Н), 3,14-3,16 (m, 2Н), 2,91-2,94 (m, 2Н), 2,05-2,10 (m, 2Н), 1,68 (s, 9Н); МС (ЭСИ) m/z: 417 [М+Н]+.
Пример 46 1-(6-(1,4-Диазепан-1-ил)пиридин-2-ил)-6-(1-изопропил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин 146
Следуя способам, описанным в примере 61, и начиная с трет-бутил 4-(6-(6-(1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилата и 2-бромпропана, получали 146 в виде желтого твердого вещества (90 мг, 75%) в ходе двух стадий. 1Н-ЯМР (500 МГц, CD3OD) δ (ppm) 8,93 (s, 1Н), 8,54 (s, 1Н), 8,25 (s, 1Н), 8,10 (s, 1Н), 7,86 (s, 1Н), 7,55-7,59 (m, 1Н), 7,15 (d, J=7,5 Гц, 1H), 6,47 (d, J=8,0 Гц, 1H), 4,56-4,63 (m, 1Н), 3,78-3,82 (m, 4Н), 3,06-3,08 (m, 2Н), 2,85-2,87 (m, 2Н), 1,98-2,02 (m, 2Н), 1,57 (d, J=6,5 Гц, 6H); МС (ЭСИ) m/z: 403 [М+Н]+.
Пример 47 1-(6-(1,4-Диазепан-1-ил)пиридин-2-ил)-6-(1-циклобутил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин 147
Следуя способам, описанным в примере 61, и начиная с трет-бутил 4-(6-(6-(1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилата и бромциклобутана, получали 147 в виде желтого твердого вещества (40 мг, 35%) в ходе двух стадий. 1Н-ЯМР (500 МГц, CD3OD) δ (ppm): 9,02 (s, 1Н), 8,66 (s, 1Н), 8,34 (s, 1H), 8,18 (s, 1H), 7,95 (s, 1H), 7,66-7,69 (m, 1H), 7,25 (d, J=7,5 Гц, 1H), 6,59 (d, J=8,5 Гц, 1H), 4,91-4,96 (m, 1H), 3,90-3,95 (m, 4H), 3,20-3,22 (m, 2H), 3,00-3,02 (m, 2H), 2,52-2,63 (m, 4H), 2,08-2,13 (m, 2H), 1,92-1,99 (m, 2H); МС (ЭСИ) m/z: 415 [M+H]+.
Пример 48 5-(1-(6-(1,4-диазепан-1-ил)пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридин-6-ил)-2-метилпиридазин-3(2Н)-он 148
Раствор 4-хлор-1Н-пиридазин-6-она (6,000 ммоль; 783,2 мг), йодметана (7,200 ммоль; 1032 мг; 0,453 мл) и карбоната калия (9,000 ммоль; 1256 мг) в ДМФА (12 мл) перемешивали при комнатной температуре в течение ночи. Смесь фильтровали. Фильтрат разделяли между ЕtOАс и водой. Органический слой концентрировали. Остаток очищали на силикагеле, элюируя 0 до 40% ЕtOАс в ДХМ, получая 5-хлор-2-метил-пиридазин-3-он в виде твердого вещества белого оттенка (514,7, 59%).
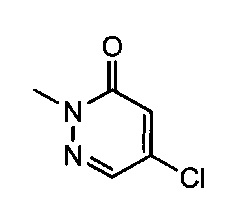
К смеси 5-хлор-2-метил-пиридазин-3-она (3,560 ммоль; 514,7 мг), бис(пинаколато)диборона (5,687 ммоль; 1459 мг) и ацетата калия (7,121 ммоль; 720,5 мг) в 1,4-диоксане (12 мл) в пробирке высокого давления в атмосфере азота добавляли X-PHOS (0,4273 ммоль; 142,3 мг) и трис(дибензилиденацетон)дипалладий (0) (0,1780 ммоль; 163,0 мг). Пробирку закрывали и нагревали при 90°С в течение 2 часов. Реакционную смесь фильтровали горячей через Целит. Осадок на фильтре промывали ЕtOАс. Отфильтрованное вещество промывали водой и солевым раствором. Органический слой сушили с MgSO4 и затем концентрировали, получая 2-метил-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридазин-3-он, который использовали без дополнительной очистки.
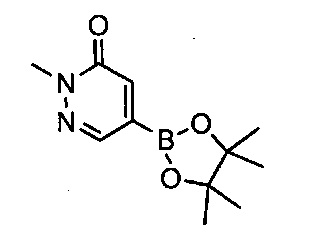
Смесь 6-хлор-1-[6-(1,4-диазепан-1-ил)-2-пиридил]пиразоло[4,3-с]пиридина (0,3190 ммоль; 104,9 мг), 2-метил-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридазин-3-она (0,4786 ммоль; 113,0 мг), аддукта [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладия (II) дихлорметана (0,03190 ммоль; 26,6 мг), ацетата калия (0,4786 ммоль; 0,48 мл) и карбоната натрия (0,4786 ммоль; 0,48 мл) в ацетонитриле (10 мл) в пробирке высокого давления нагревали в микроволновой печи при 150°С в течение 15 минут. Смесь фильтровали через Целит. Отфильтрованное вещество концентрировали. Остаток очищали на силикагеле, элюируя 10% МеОН в ДХМ с 1% NH4OH. Полученный продукт (29 мг, чистота >90%) дополнительно очищали с помощью обращенно-фазовой ВЭЖХ, получая 148 в виде твердого вещества белого оттенка (10,9 мг, 8,5%). 1Н ЯМР (400 МГц, ДМСО) δ 9,39-9,31 (s, 1Н), 9,08-9,01 (s, 1Н), 8,72-8,65 (S, 1Н), 8,56-8,51 (d, J=2,1 Гц, 1Н), 8,31-8,22 (s, 1Н), 7,76 -7,69 (t, J=8,1 Гц, 1Н), 7,42-7,38 (d, J=2,1 Гц, 1Н), 7,22-7,18 (d, J=7,7 Гц, 1Н), 6,69-6,62 (d, J=8,5 Гц, 1Н), 3,87-3,79 (m, 4Н), 3,74-3,72 (s, 3Н), 3,05-3,00 (m, 2Н), 2,83-2,77 (m, 2Н), 1,94-1,87 (m, 2Н); МС (ЭСИ) m/z: 403,2 [М+Н]+.
Пример 49 6-(6-этилпиразин-2-ил)-1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридин 149
Следуя способам получения в примере 23, получали 149. МС (ЭСИ) m/z: 387,2. 1Н ЯМР (400 МГц, ДМСО) δ 9,55 (s, 1Н), 9,50 (s, 1Н), 9,33 (s, 1Н), 8,66 (d, J=3,9 Гц, 2Н), 7,77 (t, J=8,1 Гц, 1H), 7,27 (d, J=7,7 Гц, 1H), 6,81 (d, J=8,5 Гц, 1H), 3,67-3,58 (m, 4Н), 2,91 (dd, J=8,9, 4,5 Гц, 6H), 1,36 (t, J=7,6 Гц, 3Н).
Пример 50 1-[6-(1,4-диазепан-1-ил)-2-пиридил]-6-(6-этилпиразин-2-ил)пиразоло[4,3-с]пиридин 150
Следуя способам получения в примере 23, получали 150. МС (ЭСИ) m/z: 401,2. 1Н ЯМР (400 МГц, ДМСО) δ 9,60 (d, J=6,4 Гц, 1Н), 9,49 (s, 1Н), 9,32 (s, 1Н), 8,66 (d, J=2,8 Гц, 2Н), 7,72 (dd, J=14,7, 6,6 Гц, 1Н), 7,20 (d, J=7,7 Гц, 1Н), 6,62 (d, J=8,5 Гц, 1Н), 3,91 (t, J=6,0 Гц, 2Н), 3,85-3,78 (m, 2Н), 3,01-2,94 (m, 2Н), 2,90 (q, J=7,6 Гц, 3Н), 2,72-2,64 (m, 3Н), 1,94-1,84 (m, 2Н), 1,35 (t, J=7,6 Гц, 3Н).
Пример 51 3-этил-5-[1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридин-6-ил]пиримидин-4-он 151
Следуя способам получения в примере 23, получали 151. МС (ЭСИ) m/z: 403,2. 1Н ЯМР (400 МГц, ДМСО) δ 9,80 (s, 1Н), 9,23 (s, 1Н), 9,02 (s, 1Н), 8,65 (s, 1Н), 8,59 (s, 1Н), 7,74 (t, J=8,1 Гц, 1Н), 7,25 (d, J=7,7 Гц, 1Н), 6,74 (d, J=8,4 Гц, 1Н), 4,08 (q, J=7,1 Гц, 2Н), 3,65-3,57 (m, 4Н), 2,96-2,83 (m, 4Н), 1,36 (t, J=7,1 Гц, 3Н).
Пример 52 2-(4-(1-(6-(1,4-Диазепан-1-ил)пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридин-6-ил)-1Н-пиразол-1-ил)этанол 152
Следуя способам, описанным в примере 61, и начиная с трет-бутил 4-(6-(6-(1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилата и оксирана, получали 152 в виде светло-желтого твердого вещества (102 мг, 71%) в ходе двух стадий. 1Н ЯМР (500 МГц, CDCl3) δ (ppm) 8,941-8,942 (d, J=0,5 Гц, 1H), 8,57 (s, 1Н), 8,17 (s, 1Н), 8,07 (s, 1Н), 7,86 (s, 1Н), 7,57-7,60 (t, J=16 Гц, 1H), 7,22-7,26 (t, J=20,5 Гц, 1H), 6,36-6,37 (d, J=8 Гц, 1H), 4,30-4,32 (t, J=9,5 Гц, 2H), 4,05-4,07 (t, J=9,5 Гц, 2H), 3,77-3,82 (m, 4H), 3,11-3,13 (t, J=10,5 Гц, 2H), 2,88-2,91 (t, J=11,5 Гц, 2H), 2,26 (s, 2H), 1,97-2,01 (m, 2H); МС (ЭСИ) m/z: 405 [М+Н]+.
Пример 53 1-(6-(1,4-Диазепан-1-ил)пиридин-2-ил)-6-(1-(2-фторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин 153
Следуя способам, описанным в примере 61, и начиная с трет-бутил 4-(6-(6-(1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилата и 1-бром-2-фторэтана, получали 153 в виде желтого твердого вещества (60 мг, 87,5%) в ходе двух стадий. 1Н ЯМР (500 МГц, ДМСО-d6) δ (ppm) 9,12 (s, 1Н), 8,63 (s, 1Н), 8,51 (s, 1Н), 8,28 (s, 1Н), 7,95 (s, 1Н), 7,49-7,66 (m, 1H), 7,13-7,15 (d, J=7,5 Гц, 1H), 6,55-6,57 (d, J=8,5 Гц, 1H), 4,88-4,90 (m, 1H), 4,73-4,80 (m, 1H), 4,54-4,58 (m, 1H), 4,49-4,52 (m, 1H), 3,77-3,83 (m, 4H), 2,97-2,99 (m, 2H), 2,70-2,72 (m, 2H), 1,87-1,89 (m, 2H); МС (ЭСИ) m/z: 407 [M+H]+.
Пример 54 1-(6-(1,4-Диазепан-1-ил)пиридин-2-ил)-6-(1 -(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин 154
Следуя способам, описанным в примере 61, и начиная с трет-бутил 4-(6-(6-(1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилата и 2,2,2-трифторэтил трифторметансульфоната, получали 154 в виде белого твердого вещества (45 мг, 31%) в ходе двух стадий. 1Н ЯМР (500 МГц, CDCl3) δ (ppm) 9,060-9,062 (d, J=1 Гц, 1H), 8,76 (s, 1Н), 8,24 (s, 1Н), 8,16 (s, 1Н), 8,05 (s, 1Н), 7,60-7,63 (t, J=16 Гц, 1H), 7,26-7,28 (t, J=7,5 Гц, 1H), 6,42-6,43 (d, J=8,5 Гц, 1H), 4,75-4,78 (t, J=16,5 Гц, 2H), 3,86-3,92 (m, 4H), 3,15-3,17 (t, J=10,5 Гц, 2H), 2,90-2,92 (t, J=11,5 Гц, 2H), 2,01-2,03 (t, J=11,5 Гц, 2H); МС (ЭСИ) m/z: 443 [M+H]+.
Пример 55 2-(4-(1-(6-(1,4-Диазепан-1-ил)пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридин-6-ил)-1Н-пиразол-1-ил)ацетонитрил 155
Следуя способам, описанным в примере 61, и начиная с трет-бутил 4-(6-(6-(1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилата и 2-бромацетонитрила, получали 155 в виде белого твердого вещества (25 мг, 18,5%) в ходе двух стадий. 1Н ЯМР (500 МГц, CDCl3) δ (ppm) 9,064-9,065 (d, J=0,5 Гц, 1H), 8,75 (s, 1Н), 8,25 (s, 1Н), 8,19 (s, 1Н), 8,05 (s, 1Н), 7,61-7,64 (t, J=16,5 Гц, 1H), 7,28 (s, 1Н), 6,43-6,45 (d, J=8,5 Гц, 1H), 5,15 (s, 2Н), 3,88-3,92 (m, 4Н), 3,17-3,19 (t, J=11 Гц, 2H), 2,92-2,94 (t, J=11 Гц, 2H), 2,02-2,05 (t, J=12 Гц, 2H); МС (ЭСИ) m/z: 400 [М+Н]+.
Пример 56 (3S)-1-[6-[6-(6-этилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-3-амин 156
Стадия А: Получение 6-(6-этилпиразин-2-ил)-1-(6-фтор-2-пиридил)пиразоло[4,3-с]пиридина
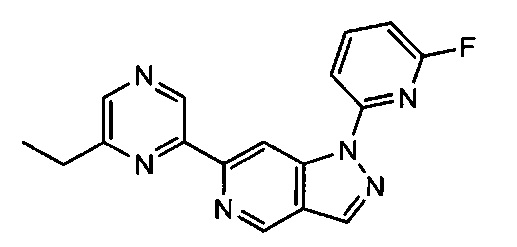
К раствору 6-хлор-1-(6-фтор-2-пиридил)пиразоло[4,3-с]пиридина (85 мг; 0,34 ммоль) и тетракис(трифенилфосфин)палладия (40 мг, 0,034 ммоль) в N,N-диметилацетамиде; 2,0 мл, добавляли (6-этилпиразин-2-ил)-триметил-станнан (185 мг, 0,684 ммоль). Реакционную смесь продували N2 в течение 5 минут, затем нагревали при 150°С в течение 45 минут в микроволновой печи biotage. Реакционную смесь фильтровали через целит и концентрировали. Неочищенный продукт разбавляли ЕtOАс, затем промывали водой. Органические слои сушили с сульфатом натрия, фильтровали и концентрировали в вакууме. Неочищенный продукт очищали с помощью флэш-хроматографии (элюировали ЕtOАс/гептаном при 50% ЕtOАс), получая 6-(6-этилпиразин-2-ил)-1-(6-фтор-2-пиридил)пиразоло[4,3-с]пиридин (45 мг) с выходом 41%. МС (ЭСИ) m/z: 321,2.
Стадия В: (S)-трет-бутил (1-(6-(6-(6-этилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)пиперидин-3-ил)карбамат
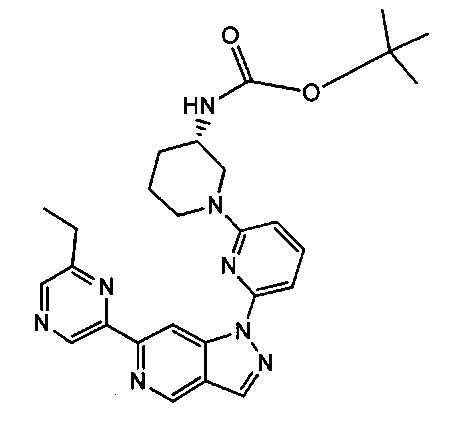
Раствор, содержащий 6-(6-этилпиразин-2-ил)-1-(6-фтор-2-пиридил)пиразоло[4,3-с]пиридин (75 мг, 0,23 ммоль) и трет-бутил N-[(3S)-3-пиперидил]карбамат (234 мг, 1,17 ммоль) в 2,0 мл метилсульфоксида, нагревали при 95°С. Реакцию гасили водой, затем экстрагировали ЕtOАс. Органические слои сушили с сульфатом натрия, фильтровали и концентрировали в вакууме. Неочищенный продукт очищали с помощью флэш-хроматографии (элюировали ЕtOАс/гептаном при 65% ЕtOАс), получая (S)-трет-бутил (1-(6-(6-(6-этилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)пиперидин-3-ил)карбамат (80 мг) с выходом 68%.
Стадия С: Раствор (S)-трет-бутил (1-(6-(6-(6-этилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)пиперидин-3-ил)карбамата (80 мг, 0,16 ммоль) в хлороводороде (4 моль/л) в 1,4-диоксане (2,0 мл, 8,0 ммоль) и 2,0 мл 1,4-диоксана перемешивали при к.т.в течение 18 часов. Реакционную смесь концентрировали и подвергали обращенно-фазовой ВЭЖХ, получая 156 (47 мг) с выходом 50%. 1Н ЯМР (400 МГц, ДМСО) δ 9,55 (s, 1Н), 9,49 (s, 1Н), 9,33 (s, 1Н), 8,66 (d, J=4,9 Гц, 2Н), 7,75 (t, J=8,1 Гц, 1Н), 7,21 (d, J=7,7 Гц, 1Н), 6,82 (d, J=8,5 Гц, 1Н), 4,42 (d, J=13,1 Гц, 1Н), 4,12 (d, J=10,6 Гц, 1Н), 3,17-3,06 (m, 1Н), 2,93 (q, J=7,5 Гц, 2Н), 2,88-2,71 (m, 2Н), 1,84 (ddd, J=17,0, 13,4, 8,1 Гц, 2Н), 1,58 (dd, J=24,7, 11,5 Гц, 1Н), 1,35 (t, J=7,6 Гц, 3Н). МС (ЭСИ) m/z: 401,2.
Пример 57 1-(6-(1,4-Диазепан-1-ил)пиридин-2-ил)-6-(1-(2-(метилсульфонил)этил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин 157
Следуя способам, описанным в примере 61, и начиная с трет-бутил 4-(6-(6-(1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилата и 2-(метилсульфонил)этил 4-метилбензолсульфоната, получали 157 в виде белого твердого вещества (50 мг, 40,6%) в ходе двух стадий. 1Н ЯМР (500 МГц, ДMCO-d6) δ (ppm) 9,16 (s, 1Н), 8,58 (s, 1Н), 8,56 (s, 1Н), 8,39 (s, 1Н), 8,02 (s, 1Н), 7,76-7,79 (t, J=16 Гц, 1H), 7,23-7,24 (d, J=7,5 Гц, 1H), 6,71-6,73 (d, J=8,5 Гц, 1H), 4,64-4,67 (t, J=13,5 Гц, 2H), 4,01-4,03 (t, J=9,5 Гц, 2H), 3,89-3,87 (t, J=11,5 Гц, 2H), 3,76-3,79 (t, J=14 Гц, 2H), 3,32 (s, 2Н), 3,17-3,20 (t, J=10,5 Гц, 2H), 2,94 (s, 3Н), 2,13-2,14 (d, J=4,5 Гц, 2H); МС (ЭСИ) m/z: 467 [М+Н]+.
Пример 58 1-(6-(1,4-Диазепан-1-ил)пиридин-2-ил)-6-(1-(оксетан-3-илметил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин 158
Следуя способам, описанным в примере 61, и начиная с трет-бутил 4-(6-(6-(1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилата и оксетан-3-илметил 4-метилбензолсульфоната, получали 158 в виде желтого твердого вещества (38 мг, 51%) в ходе двух стадий. 1Н-ЯМР (500 МГц, CD3OD) δ (ppm): 9,16-9,19 (m, 1Н), 8,86-8,77 (m, 3Н), 8,43-8,47 (m, 1Н), 7,66-7,73 (m, 1Н), 7,18-7,26 (m, 1Н), 6,63-6,66 (m, 1Н), 4,81-4,83 (m, 2Н), 4,60-4,64 (m, 2Н), 3,75-3,97 (m, 7Н), 3,61-3,64 (m, 1Н), 3,46-3,48 (m, 1Н), 3,10-3,12 (m, 1Н), 2,88-2,90 (m, 1Н), 1,98-2,07 (m, 2Н); МС (ЭСИ) т/г.431 [М+Н]+.
Пример 59 2-(4-(1-(6-(1,4-Диазепан-1-ил)пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридин-6-ил)-1Н-пиразол-1-ил)ацетамид 159
Следуя способам, описанным в примере 61, и начиная с трет-бутил 4-(6-(6-(1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилата и 2-бромацетонитрила, получали 159 в виде белого твердого вещества (12 мг, 36%) в ходе двух стадий. 1Н ЯМР (500 МГц, ДМСО-d6) δ (ppm) 9,11 (s, 1Н), 8,64 (s, 1Н), 8,46 (s, 1Н), 8,20 (s, 1Н), 7,91 (s, 1Н), 7,64-7,70 (m, 1Н), 7,14-7,16 (d, J=12,5 Гц, 3Н), 6,56-6,59 (d, J=14 Гц, 1Н), 4,83 (s, 1Н), 3,78-3,88 (m, 6Н), 2,74-2,78 (m, 3Н), 1,88-1,92 (t, J=20 Гц, 2Н); МС (ЭСИ) m/z: 418 [М+Н]+.
Пример 60 6-(6-метилпиразин-2-ил)-1-[6-(1,2,3,6-тетрагидропиридин-4-ил)-2-пиридил]пиразоло[4,3-с]пиридин 160
Стадия А: трет-бутил 4-[6-(6-хлорпиразоло[4,3-с]пиридин-1-ил)-2-пиридил]-3,6-дигидро-2Н-пиридин-1-карбоксилат
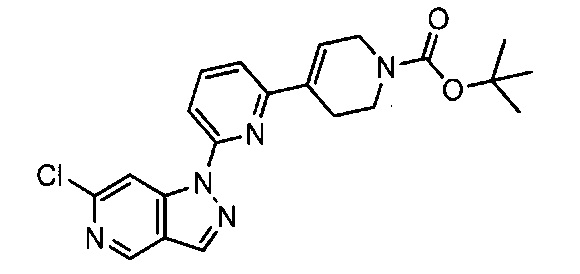
К раствору 1-(6-бром-2-пиридил)-6-хлор-пиразоло[4,3-с]пиридина (150 мг, 0,485 ммоль), трет-бутилового эфира 4-(4,4,5,5-тетраметил-[1,3,2]-диоксаборолан-2-ил)-3,6-дигидро-2Н-пиридин-1-карбоновой кислоты (180 мг, 0,581 ммоль) и 1,1'-бис(дифенилфосфино)ферроценпалладия (II) хлорида (32 мг, 0,039 ммоль) в 5,0 мл ацетонитрила добавляли 1,00 М ацетат калия в воде (0,73 мл, 0,73 ммоль) и 1,00 М карбонат натрия в воде (0,73 мл, 0,73 ммоль). Реакционную смесь перемешивали при 95°С в течение 2 часов. Реакционную смесь фильтровали через целит. Неочищенный продукт очищали с помощью флэш-хроматографии (элюировали ЕtOАс/гептаном при 35% ЕtOАс), получая трет-бутил 4-[6-(6-хлорпиразоло[4,3-с]пиридин-1-ил)-2-пиридил]-3,6-дигидро-2Н-пиридин-1-карбоксилат (185 мг) с выходом 92%. МС (ЭСИ) m/z:.412,2.
Стадия В: трет-бутил 4-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-3,6-дигидро-2Н-пиридин-1-карбоксилат
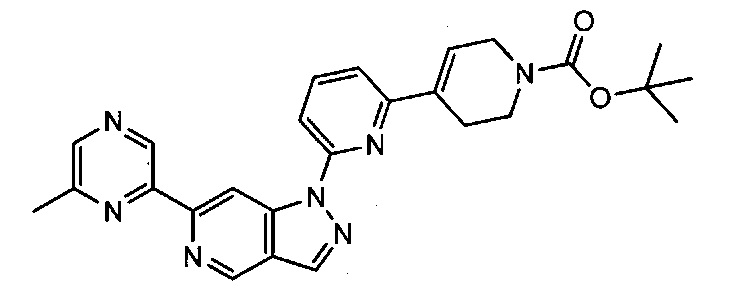
К раствору трет-бутил 4-[6-(6-хлорпиразоло[4,3-с]пиридин-1-ил)-2-пиридил]-3,6-дигидро-2Н-пиридин-1-карбоксилата (200 мг, 0,486 ммоль) и тетракис(трифенилфосфин)палладия (0) (56 мг, 0,049 ммоль) в 5,0 мл N,N-диметилацетамида добавляли триметил-(6-метилпиразин-2-ил)станнан (250 мг, 0,971 ммоль). Реакционную смесь нагревали при 145°С в течение 40 минут в микроволновой печи. Реакционную смесь фильтровали через целит и концентрировали. Неочищенный продукт разбавляли ЕtOАс, затем промывали водой. Органические слои сушили с сульфатом натрия, фильтровали и концентрировали в вакууме. Неочищенный продукт очищали с помощью флэш-хроматографии (элюировали ЕtOАс/гептаном при 65% ЕtOАс), получая 165 мг требуемого продукта с выходом 72%.
Стадия С: Раствор трет-бутил 4-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-3,6-дигидро-2Н-пиридин-1-карбоксилата (40 мг, 0,085 ммоль) в хлороводороде (4 моль/л) в 1,4-диоксане (1,0 мл, 4,0 ммоль) и 1,0 мл 1,4-диоксана перемешивали при к.т.в течение 18 часов. Реакционную смесь концентрировали. Неочищенный продукт разбавляли водой и промывали EtOAc, чтобы удалить трифенилфосфиноксид в качестве побочного продукта. Водный слой концентрировали и подвергали обращенно-фазовой ВЭЖХ, получая 17 мг 160 с выходом 52%. 1Н ЯМР (400 МГц, ДМСО) δ 9,73 (s, 1Н), 9,48 (s, 1Н), 9,34 (s, 1Н), 8,72 (s, 1Н), 8,64 (s, 1Н), 8,03 (t, J=7,9 Гц, 1Н), 7,93 (d, J=8,1 Гц, 1Н), 7,57 (d, J=7,7 Гц, 1Н), 7,02 (s, 1Н), 3,14 (s, 2Н).
Пример 61 1-(6-(1,4-Диазепан-1-ил)пиридин-2-ил)-6-(1-(циклопропилметил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин 161
Стадия А: трет-Бутил 4-(6-бромпиридин-2-ил)-1,4-диазепан-1-карбоксилат
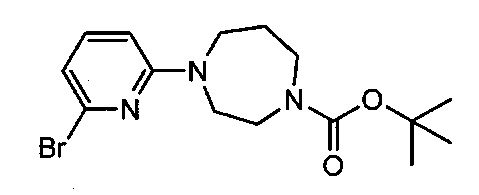
Смесь 2-бром-6-фторпиридина (500 мг, 2,8 ммоль), трет-бутил 1,4-диазепан-1-карбоксилата (568 мг, 2,8 ммоль) в ДИПЭА (1,83 г, 14,2 ммоль) и этанола (10 мл) нагревали при 100°С в течение 16 часов. Затем ее охлаждали, растворитель удаляли при пониженном давлении, и остаток разбавляли EtOAc (100 мл) и промывали солевым раствором. Органический слой сушили над Na2SO4 и концентрировали при пониженном давлении, получая трет-бутил 4-(6-бромпиридин-2-ил)-1,4-диазепан-1-карбоксилат в виде бесцветного масла (500 мг, 50%). МС (ЭСИ) m/z: 356 [М+Н]+.
Стадия В: трет-Бутил 4-(6-(6-хлор-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилат
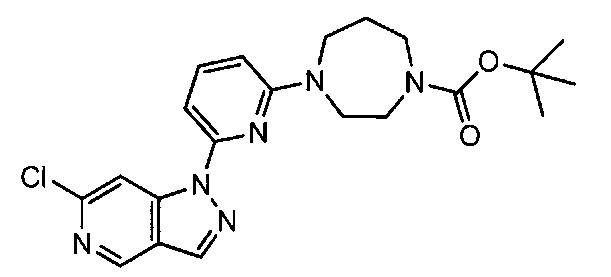
К смеси трет-бутил 4-(6-бромпиридин-2-ил)-1,4-диазепан-1-карбоксилата (2,55 г, 7,16 ммоль) и 6-хлор-1Н-пиразоло[4,3-с]пиридина (1,0 г, 6,51 ммоль) в 1,4-диоксане (20 мл) добавляли Cul (494 мг, 2,6 ммоль), К2СO3 (3,6 г, 26 ммоль) и N1,N2-диметилэтан-1,2-диамин (460 мг, 5,2 ммоль). Смесь нагревали при 100°С в течение 3 часов, контролируя с помощью ЖХ-МС. Реакционную смесь концентрировали при пониженном давлении. Неочищенное вещество очищали с помощью хроматографии на силикагеле, используя петролейный эфир/EtOAc (2/1) в качестве элюирующих растворителей, получая трет-бутил 4-(6-(6-хлор-1Н-пиразоло[4,3-с]-пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1 -карбоксилат в виде желтого твердого вещества (1,6 г, 57%). МС (ЭСИ) m/z: 429 [М+Н]+.
Стадия С: трет-Бутил 4-(6-(6-(1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилат
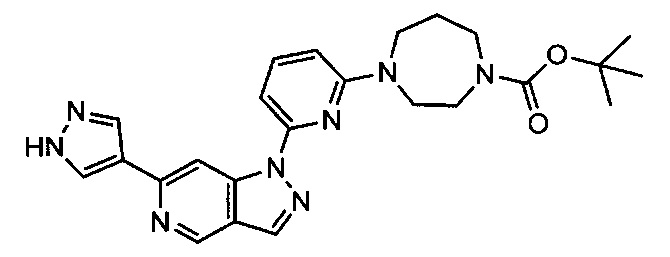
Суспензию трет-бутил 4-(6-(6-хлор-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилата (500 мг, 1,16 ммоль), 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразола (679 мг, 3,5 ммоль), Pd(dppf)Cl2 (47,5 мг, 0,058 ммоль) и водного раствора Na2CO3 (насыщенный, 3 мл) в 1,4-диоксане (10 мл) в атмосфере азота нагревали при 100°С в течение 16 часов. Реакционную смесь фильтровали и фильтрат концентрировали при пониженном давлении. Остаток очищали с помощью хроматографии на силикагеле, используя петролейный эфир/ЕtOАс (1/1) в качестве элюирующих растворителей, получая трет-бутил 4-(6-(6-(1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилат в виде желтого твердого вещества (360 мг, 67%). МС (ЭСИ) m/z: 461 [М+Н]+.
Стадия D: трет-Бутил 4-(6-(6-(1-(циклопропилметил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]-пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилат
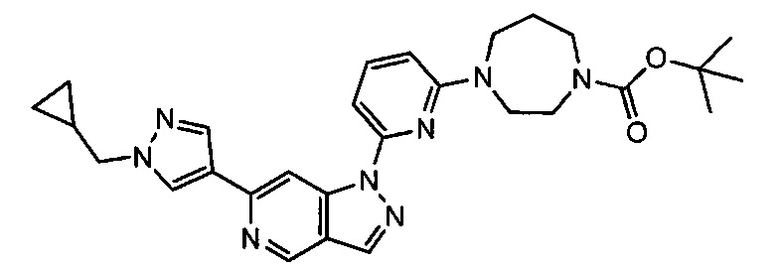
Суспензию 4-(6-(6-(1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилата (200 мг, 0,43 ммоль), (бромметил)циклопропана (100 мг, 0,65 ммоль) и К2СO3 (120 мг, 0,87 ммоль) в ДМФА (10 мл) перемешивали при комнатной температуре в течение 18 часов. Реакционную смесь экстрагировали ЕtOАс (100 мл), промывали солевым раствором (50 мл), сушили над MgSO4 и концентрировали при пониженном давлении. Неочищенное вещество очищали с помощью хроматографии на силикагеле, используя петролейный эфир/ЕtOАс (2/1) в качестве элюирующих растворителей, получая трет-бутил 4-(6-(6-(1-(циклопропилметил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилат в виде белого твердого вещества (200 мг, 89,6%). МС (ЭСИ) m/z: 515 [М+Н]+.
Стадия Е: Раствор трет-бутил 4-(6-(6-(1-(циклопропилметил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]-пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилата (200 мг, 0,39 ммоль) в HCl/MeOH (2 М, 10 мл) перемешивали при комнатной температуре в течение 3 часов. Реакционную смесь концентрировали при пониженном давлении. Неочищенное вещество очищали с помощью обращенно-фазовой препаративной ВЭЖХ, получая 161 в виде желтого твердого вещества (70 мг, 43,5%). 1Н ЯМР (500 МГц, CDCl3) δ (ppm) 9,055-9,057 (d, J=1 Гц, 1Н), 8,74 (s, 1Н), 8,23 (s, 1Н), 8,17 (s, 1Н), 7,97 (s, 1Н), 7,60-7,63 (t, J=16 Гц, 1Н), 7,28 (s, 1Н), 6,41-6,43 (d, J=8 Гц, 1Н), 4,04-4,06 (d, J=7 Гц, 2Н), 3,89-3,94 (m, 4Н), 3,17-3,19 (t, J=11 Гц, 2Н), 2,91-2,93 (t, J=11,5 Гц, 2Н), 2,03-2,06 (t, J=12,5 Гц, 2Н), 1,35-1,36 (m, 1Н), 0,69-0,73 (m, 2Н), 0,43-0,46 (m, 2Н); МС (ЭСИ) m/z: 415 [М+Н]+.
Пример 62 1-(6-(1,4-Диазепан-1-ил)пиридин-2-ил)-6-(1-(2,2-дифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин 162
Следуя способам, описанным в примере 61, и начиная с трет-бутил 4-(6-(6-(1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилата и 1,1-дифтор-2-йодэтана, получали 162 в виде светло-желтого твердого вещества (21 мг, 14,5%) в ходе двух стадий. 1Н ЯМР (500 МГц, CDCl3) δ (ppm) 9,060-9,062 (d, J=1 Гц, 1H), 8,74 (s, 1Н), 8,24 (s, 1Н), 8,11 (s, 1Н), 8,04 (s, 1Н), 7,61-7,64 (t, J=16 Гц, 1H), 7,26-7,28 (t, J=10,5 Гц, 1H), 6,42-6,44 (d, J=8,5 Гц, 1H), 6,04-6,26 (m, 1H), 4,51-4,57 (m, 2H), 3,89-3,93 (m, 4H), 3,17-3,19 (t, J=11 Гц, 2H), 2,92-2,94 (t, J=11 Гц, 2H), 2,02-2,05 (m, 2H); МС (ЭСИ) m/z: 425 [М+Н]+.
Пример 63 1-(6-(1,4-диазепан-1-ил)пиразин-2-ил)-6-(1-этил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин 163
Стадия А: трет-бутил 4-(6-бромпиразин-2-ил)-1,4-диазепан-1-карбоксилат
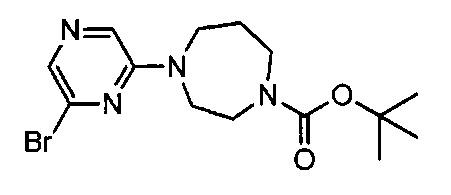
Смесь 2,6-дибромпиразина (5,0198 ммоль; 1194,1 мг), трет-бутил 1,4-диазепан-1-карбоксилата (5,271 ммоль; 1055,6 мг) и триэтиламина (15,06 ммоль; 1539 мг; 2,12 мл) в ИПС (10 мл) в закрытом сосуде высокого давления нагревали при 120°С в течение ночи. Смесь охлаждали до комнатной температуры и затем концентрировали. Остаток очищали на силикагеле, элюируя 0 до 100% EtOAc в гептане, получая трет-бутил 4-(6-бромпиразин-2-ил)-1,4-диазепан-1-карбоксилат (1,6965 г, 95%). МС (ЭСИ) m/z: 357 [М+Н]+.
Стадия В: трет-бутил 4-[6-(6-хлорпиразоло[4,3-с]пиридин-1-ил)пиразин-2-ил]-1,4-диазепан-1-карбоксилат
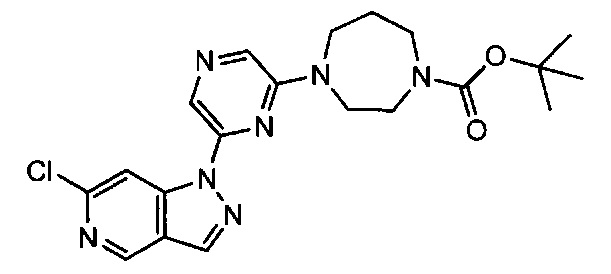
Смесь 6-хлор-1Н-пиразоло[4,3-с]пиридина (2,0 ммоль; 307 мг), трет-бутил 4-(6-бромпиразин-2-ил)-1,4-диазепан-1-карбоксилата (2,199 ммоль; 785,5 мг), N,N'-диметилэтилендиамина (4,0 ммоль; 352,4 мг; 0,398 мл), иодида меди (2,0 ммоль; 380,72 мг) и карбонат калия (2,1990 ммоль; 307 мг) в 1,4-диоксане (15 мл) продували азотом, затем закрывали и перемешивали при 110°С в течение ночи. Смесь охлаждали до комнатной температуры, затем фильтровали через Целит. Фильтрат концентрировали; остаток очищали на силикагеле, элюируя 0 до 100% EtOAc в гептане, получая трет-бутил 4-[6-(6-хлорпиразоло[4,3-с]пиридин-1-ил)пиразин-2-ил]-1,4-диазепан-1-карбоксилат в виде твердого вещества белого оттенка (217,2 мг, 25%). МС (ЭСИ) m/z: 430 [М+Н]+.
Стадия С: трет-бутил 4-[6-[6-(1-этилпиразол-4-ил)пиразоло[4,3-с]пиридин-1-ил]пиразин-2-ил]-1,4-диазепан-1-карбоксилат
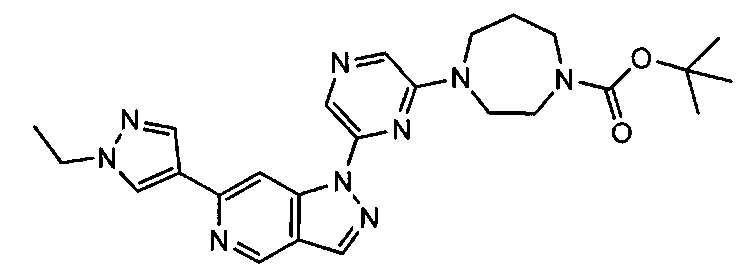
Смесь трет-бутил 4-[6-(6-хлорпиразоло[4,3-с]пиридин-1-ил)пиразин-2-ил]-1,4-диазепан-1-карбоксилата (0,2526 ммоль; 108,6 мг), 1-этил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразола (0,3789 ммоль; 84,16 мг), аддукта [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладия (II) дихлорметана (0,02526 ммоль; 21,1 мг), ацетата калия (0,3789 ммоль; 0,38 мл) и карбоната натрия (0,3789 ммоль; 0,38 мл) в ацетонитриле (10 мл) в пробирке высокого давления нагревали в микроволновой печи при 150°С в течение 15 минут. Смесь охлаждали до комнатной температуры. Слои разделяли. Водный слой экстрагировали ЕtOАс. Объединенные органические слои концентрировали. Остаток очищали на силикагеле, элюируя 0 до 5% МеОН в ДХМ с 1% NH4OH, получая трет-бутил 4-[6-[6-(1-этилпиразол-4-ил)пиразоло[4,3-с]пиридин-1-ил]пиразин-2-ил]-1,4-диазепан-1-карбоксилат (127 мг, ~ 100%).
Стадия D: К раствору трет-бутил 4-[6-[6-(1-этилпиразол-4-ил)пиразоло[4,3-с]пиридин-1-ил]пиразин-2-ил]-1,4-диазепан-1-карбоксилата (0,2596 ммоль; 127,1 мг) в метаноле (5 мл) добавляли соляную кислоту, 4,0 М в 1,4-диоксане (5 мл). Полученную в результате смесь перемешивали при комнатной температуре в течение ночи. Смесь концентрировали и остаток очищали с помощью обращенно-фазовой ВЭЖХ, получая 163 в виде твердого вещества белого оттенка (34,9 мг, 34%). 1Н ЯМР (400 МГц, ДМСО) δ 9,17-9,12 (s, 1Н), 8,60-8,56 (S, 1Н), 8,55-8,52 (s, 1Н), 8,39-8,36 (s, 1Н), 8,27-8,24 (s, 1Н), 8,12-8,08 (s, 1Н), 7,91-7,85 (s, 1Н), 4,25-4,17 (q, J=7,3 Гц, 2Н), 3,92-3,80 (dt, J=10,3, 5,5 Гц, 4Н), 3,05-2,95 (m, 2Н), 2,79-2,71 (m, 2Н), 1,95-1,82 (m, 2Н), 1,46-1,40 (t, J=7,3 Гц, 3Н); МС (ЭСИ) m/z: 390,2 [М+Н]+.
Пример 64 3-(1-(6-(1,4-диазепан-1-ил)пиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-6-ил)-5-метил пиридин-2-ол 164
Стадия А: трет-бутил 4-[6-[6-(2-фтор-5-метил-3-пиридил)пиразоло[4,3-с]пиридин-1 -ил]пиразин-2-ил]-1,4-диазепан-1 -карбоксилат
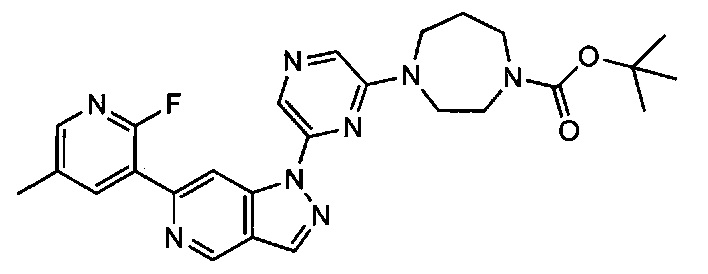
Смесь трет-бутил 4-[6-(6-хлорпиразоло[4,3-с]пиридин-1 -ил)пиразин-2-ил]-1,4-диазепан-1-карбоксилата (0,2526 ммоль; 108,6 мг), 2-фтор-5-метил-3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридина (0,3789 ммоль; 89,84 мг), аддукта [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладия (II) дихлорметана (0,02526 ммоль; 21,1 мг), ацетата калия (0,3789 ммоль; 0,38 мл) и карбоната натрия (0,3789 ммоль; 0,38 мл) в ацетонитриле (10 мл) в пробирке высокого давления нагревали в микроволновой печи при 150°С в течение 15 минут. Смесь охлаждали до комнатной температуры. Слои разделяли. Водный слой экстрагировали ЕtOАс. Объединенные органические слои концентрировали. Остаток очищали на силикагеле, элюируя 0 до 5% МеОН в ДХМ с 1% NH4OH, получая трет-бутил 4-[6-[6-(2-фтор-5-метил-3-пиридил)пиразоло[4,3-с]пиридин-1-ил]пиразин-2-ил]-1,4-диазепан-1-карбоксилат (106,6 мг, 84%).
Стадия В: К раствору трет-бутил 4-[6-[6-(2-фтор-5-метил-3-пиридил)пиразоло[4,3-с]пиридин-1-ил]пиразин-2-ил]-1,4-диазепан-1-карбоксилата (0,2113 ммоль; 106,6 мг) в метаноле (5 мл) добавляли соляную кислоту, 4,0 М в 1,4-диоксане (5 мл). Полученную в результате смесь перемешивали при комнатной температуре в течение ночи. Смесь концентрировали и остаток очищали с помощью обращенно-фазовой ВЭЖХ, получая 164 в виде побочного продукта (18,7 мг, 22%). 1Н ЯМР (400 МГц, ДМСО) δ 9,89-9,85 (s, 1Н), 9,25-9,20 (s, 1Н), 8,64-8,60 (s, 1Н), 8,56-8,52 (d, J=2,6 Гц, 1Н), 8,41-8,38 (s, 1Н), 8,08-8,05 (s, 1Н), 7,33-7,30 (s, 1Н), 3,95-3,84 (m, 4Н), 2,99-2,93 (m, 2Н), 2,71-2,66 (m, 2Н), 2,15-2,13 (s, 3Н), 1,88-1,81 (m, 2Н); МС (ЭСИ) m/z: 403,2 [М+Н]+.
Пример 65 6-(6-циклопропилпиразин-2-ил)-1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридин 165
Следуя способам получения в примере 23, получали 165. МС (ЭСИ) m/z: 399,2. 1Н ЯМР (400 МГц, ДМСО) δ 9,40 (s, 1Н), 9,32 (s, 1Н), 9,28 (s, 1Н), 8,66 (s, 1Н), 8,62 (s, 1Н), 7,77 (t, J=8,1 Гц, 1Н), 7,24 (d, J=7,7 Гц, 1Н), 6,82 (d, J=8,5 Гц, 1Н), 3,66-3,59 (m, 4Н), 2,91-2,85 (m, 4Н), 2,35-2,27 (m, 1Н), 1,21-1,06 (m, =4Н).
Пример 66 6-(6-метилпиразин-2-ил)-1-[6-(4-пиперидил)-2-пиридил]пиразоло[4,3-с]пиридин 166
Стадия А: трет-бутил 4-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-1-карбоксилат
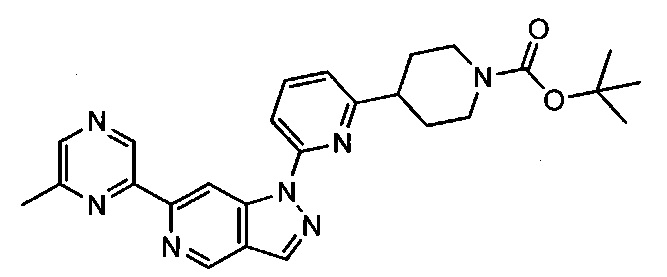
Смесь трет-бутил 4-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-3,6-дигидро-2Н-пиридин-1-карбоксилата (125 мг, 0,266 ммоль) и палладия на активированном угле, восстановленного 10% (28 мг, 0,0266 ммоль) в 10,0 мл этанола, перемешивали в атмосфере Н2 при 40°С в течение 18 часов. Реакционную смесь фильтровали через целит и промывали МеОН. Неочищенный продукт использовали на следующей стадии.
Стадия В: Смесь трет-бутил 4-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-1-карбоксилата; В; 110 мг; 0,2332 ммоль, в хлороводороде (4 моль/л) в 1,4-диоксане (2,0 мл, 8,0 ммоль) и 2,0 мл 1,4-диоксана перемешивали при к.т. в течение 18 часов. Реакционную смесь концентрировали и подвергали обращенно-фазовой ВЭЖХ, получая 166 (13 мг) с выходом 13%. 1Н ЯМР (400 МГц, ДМСО) δ 9,80 (s, 1Н), 9,46 (s, 1Н), 9,34 (s, 1Н), 8,71 (s, 1Н), 8,63 (s, 1Н), 7,99 (t, J=7,9 Гц, 1Н), 7,87 (d, J=8,1 Гц, 1Н), 7,29 (d, J=7,5 Гц, 1Н), 3,15 (d, J=12,0 Гц, 2Н), 2,94 (tt, J=11,8, 3,5 Гц, 1Н), 2,76-2,67 (m, 2Н), 2,66 (s, 3Н), 2,01 (d, J=12,1 Гц, 2Н), 1,85 (qd, J=12,2, 3,8 Гц, 2Н). МС (ЭСИ) m/z: 372,2.
Пример 67 (3S)-1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пирролидин-3-амин 167
Следуя способам получения в примере 23, получали 167. МС (ЭСИ) m/z: 373,2. 1Н ЯМР (400 МГц, ДМСО) δ 9,88 (s, 1Н), 9,45 (s, 1Н), 9,30 (s, 1Н), 8,64 (s, 1Н), 8,62 (s, 1Н), 7,70 (t, J=8,0 Гц, 1Н), 7,18 (d, J=7,7 Гц, 1Н), 6,39 (d, J=8,3 Гц, 1Н), 3,74 (dd, J=28,2, 23,7 Гц, 4Н), 2,64 (s, 3Н), 2,19 (td, J=12,6, 7,1 Гц, 1Н), 1,92-1,78 (m, 2Н).
Пример 68 (3R)-1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пирролидин-3-амин 168
Следуя способам получения в примере 23, получали 168. МС (ЭСИ) m/z: 373,2. 1Н ЯМР (400 МГц, ДМСО) δ 9,88 (s, 1Н), 9,45 (s, 1Н), 9,30 (s, 1Н), 8,63 (S, 1Н), 8,62 (s, 1Н), 7,70 (t, J=8,0 Гц, 1Н), 7,18 (d, J=7,7 Гц, 1Н), 6,39 (d, J=8,3 Гц, 1Н), 3,74 (dd, J=27,9, 23,5 Гц, 4H), 2,64 (s, 3Н), 2,19 (td, J=12,6, 7,1 Гц, 1H), 1,90 -1,80 (m, 2H).
Пример 69 1-[6-(3-метилпиперазин-1-ил)-2-пиридил]-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин 169
Следуя способам получения в примере 23, получали 169. МС (ЭСИ) m/z: 387,2. 1Н ЯМР (400 МГц, ДМСО) δ 9,56 (s, 1Н), 9,46 (s, 1Н), 9,32 (s, 1Н), 8,66 (s, 1Н), 8,63 (s, 1Н), 7,76 (t, J=8,1 Гц, 1Н), 7,24 (d, J=7,7 Гц, 1Н), 6,81 (d, J=8,5 Гц, 1Н), 4,37 (d, J=12,1 Гц, 1Н), 4,17 (d, J=10,7 Гц, 1Н), 3,08 (d, J=11,7 Гц, 1Н), 2,98 (td, J=11,9, 2,9 Гц, 1Н), 2,83 (dd, J=22,0, 9,9 Гц, 1Н), 2,63 (s, 3Н), 2,62-2,54 (m, 1Н), 2,34 (d, J=12,3 Гц, 1Н), 1,04 (d, J=6,3 Гц, 3Н).
Пример 70 6-(6-трет-бутилпиразин-2-ил)-1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридин 170
Следуя способам получения в примере 23, получали 170. МС (ЭСИ) m/z: 415,2. 1Н ЯМР (400 МГц, ДМСО) δ 9,65 (s, 1Н), 9,56 (d, J=1,2 Гц, 1Н), 9,32 (s, 1Н), 8,81 (d, J=1,3 Гц, 1Н), 8,65 (s, 1Н), 7,76 (t, J=8,1 Гц, 1Н), 7,25 (d, J=7,7 Гц, 1Н), 6,79 (d, J=8,4 Гц, 1Н), 3,70-3,58 (m, 4Н), 3,00-2,89 (m, 4Н), 1,43 (s, 9Н).
Пример 71 6-метил-1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-3-амин 171
Стадия А: трет-бутил N-[1-(6-бром-2-пиридил)-6-метил-3-пиперидил]карбамат
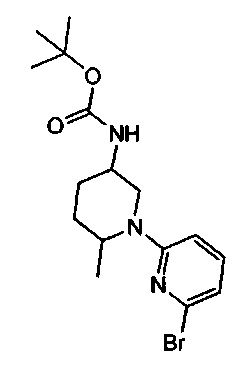
Раствор, содержащий 2-бром-6-фторпиридин (0,95 мл, 6,65 ммоль) и трет-бутил 6-метилпиперидин-3-илкарбамат (750 мг, 3,32 ммоль) в 5,0 мл метилсульфоксида нагревали при 95°С в течение 18 часов. Реакцию гасили водой, затем экстрагировали ЕtOАс. Органические слои сушили с сульфатом натрия, фильтровали и концентрировали в вакууме. Неочищенный продукт очищали с помощью флэш-хроматографии (элюировали ЕtOАс/гептаном при 30% ЕtOАс), получая трет-бутил N-[1-(6-бром-2-пиридил)-6-метил-3-пиперидил]карбамат (480 мг) с выходом 39%. МС (ЭСИ) m/z: 371,2.
Стадия В: трет-бутил N-[1-[6-(6-хлорпиразоло[4,3-с]пиридин-1-ил)-2-пиридил]-6-метил-3-пиперидил]карбамат
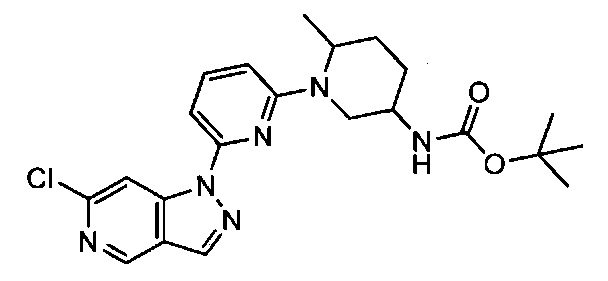
Смесь 6-хлор-1Н-пиразоло[4,3-с]пиридина (100 мг, 0,651 ммоль), трет-бутил N-[1-(6-бром-2-пиридил)-6-метил-3-пиперидил]карбамата (422 мг, 1,14 ммоль), трис(дибензилиденацетон)дипалладия (0) (59 мг, 0,065 ммоль), ксантфоса (78 мг, 0,130 ммоль) и трет-бутилата натрия (129 мг, 1,30 ммоль) в 6,0 мл толуола перемешивали при 100°С в течение 18 часов. Реакционную смесь фильтровали через целит. Неочищенный продукт очищали с помощью флэш-хроматографии (EtOAc/гептан), получая требуемый продукт (185 мг) с выходом 64%. МС (ЭСИ) m/z: 443,2.
Стадия С: Следуя способам получения в примере 23, получали 171. МС (ЭСИ) m/z: 401,2. 1Н ЯМР (400 МГц, ДМСО) δ 9,47 (d, J=6,7 Гц, 2Н), 9,33 (s, 1Н), 8,66 (s, 1Н), 8,62 (s, 1Н), 7,75 (t, J=8,1 Гц, 1Н), 7,21 (d, J=7,7 Гц, 1Н), 6,75 (d, J=8,5 Гц, 1Н), 5,05 -.4,92 (m, 1Н), 4,06 (d, J=7,8 Гц, 1Н), 2,71 (dd, J=6,1, 3,3 Гц, 2Н), 2,65 (s, 3Н), 1,92-1,70 (m, 2Н), 1,70-1,41 (m, 2Н), 1,27 (t, J=6,5 Гц, 3Н).
Пример 72 1-[6-[6-(6-этилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-1,4-диазепан-6-ол 172
Следуя способам получения в примере 56, получали 172. МС (ЭСИ) m/z: 417,2. 1Н ЯМР (400 МГц, ДМСО) δ 9,58 (s, 1Н), 9,47 (d, J=4,1 Гц, 1Н), 9,32 (s, 1Н), 8,65 (d, J=4,1 Гц, 2Н), 7,71 (t, J=8,1 Гц, 1Н), 7,19 (d, J=7,7 Гц, 1Н), 6,74 (d, J=8,5 Гц, 1Н), 4,73 (s, 1Н), 4,11 (dt, J=13,8, 5,1 Гц, 1Н), 4,06-3,97 (m, 1Н), 3,92 (s, 1Н), 3,86-3,70 (m, 1Н), 3,52 (dd, J=14,6, 6,9 Гц, 1Н), 3,00 (t, J=5,4 Гц, 2Н), 2,92 (q, J=7,5 Гц, 2Н), 2,78 (dd, J=13,8, 3,9 Гц, 1Н), 2,69-2,59 (m, 1Н), 1,35 (t, J=7,6 Гц, 3Н).
Пример 73 1-(6-(1,4-Диазепан-1-ил)пиридин-2-ил)-6-(1-(дифторметил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин 173
Стадия А: 1-(дифторметил)-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразол
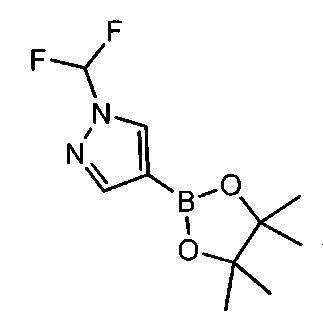
Суспензию 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразола (516 мг, 2,66 ммоль), CF2ClCO2Na (486 мг, 3,19 ммоль) и 18-краун-6 (141 мг, 0,532 ммоль) в CH3CN (150 мл) кипятили с обратным холодильником в течение 20 часов. После охлаждения до комнатной температуры реакционную смесь выливали в воду и экстрагировали ЕtOАс. Экстракты промывали солевым раствором, сушили над MgSO4 и концентрировали при пониженном давлении, получая неочищенный 1-(дифторметил)-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразол (500 мг), который использовали на следующей стадии без дополнительной очистки. МС (ЭСИ) m/z: 245 [М+Н]+.
Стадия В Следуя способам, описанным в примере 45, и начиная с трет-бутил 4-(6-(6-хлор-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилата и 1-(дифторметил)-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразола, получали 173 в виде белого твердого вещества (80 мг, 35%) в ходе трех стадий. 1Н-ЯМР (500 МГц, CD3OD) δ (ppm) 9,06 (s, 1Н), 8,73 (s, 1Н), 8,50 (s, 1Н), 8,34 (s, 1Н), 8,15 (s, 1Н), 7,50-7,67 (m, 2Н), 7,23 (d, J=7,5 Гц, 1Н), 6,58 (d, J=8,0 Гц, 1Н), 3,87-3,90 (m, 4Н), 3,13-3,15 (m, 2Н), 2,91-2,94 (m, 2Н), 2,03-2,08 (m, 2Н); МС (ЭСИ) m/z: 411 [М+Н]+.
Пример 74 1-(6-(1,4-Диазепан-1-ил)пиридин-2-ил)-6-(1-циклопропил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин 174
Следуя способам, описанным в примере 61, и начиная с трет-бутил 4-(6-(6-(1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилата и циклопропилбороновой кислоты, получали 174 в виде желтого твердого вещества (40 мг, 25%) в ходе двух стадий. 1Н ЯМР (500 МГц, ДМСО-d6) δ (ppm) 9,13 (s, 1Н), 8,64 (s, 1Н), 8,52 (s, 1Н), 8,26 (s, 1Н), 7,98 (s, 1H), 7,66-7,70 (t, J=16 Гц, 1H), 7,14-7,17 (t, J=14,5 Гц, 1H), 6,58-6,66 (m, 1H), 6,06-6,12 (m, 1H), 5,21-5,28 (m, 2H), 4,84-4,85 (d, J=10 Гц, 2H), 3,35-3,90 (m, 7H), 2,97-2,99 (t, J=10,5 Гц, 1H), 2,71-2,73 (t, J=12 Гц, 1H), 1,87-1,89 (t, J=10 Гц, 2H); МС (ЭСИ) m/z: 401 [М+Н]+.
Пример 75 1-(6-(1,4-Диазепан-1-ил)пиридин-2-ил)-6-(пиримидин-5-ил)-1Н-пиразоло[4,3-с]пиридин 175
Стадия А трет-Бутил 4-(6-(6-(пиримидин-5-ил)-1Н-пиразоло[4,3-
с]пиридин-1 -ил)пиридин-2-ил)-1,4-диазепан-1 -карбоксилат
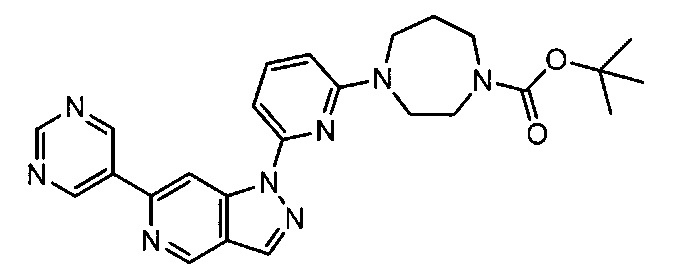
Смесь трет-бутил 4-(6-(6-хлор-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилата (427 мг, 1,0 ммоль), пиримидин-5-илбороновой кислоты (372 мг, 3,0 ммоль), PdCl2(dppf) (73 мг, 0,1 ммоль) и водн. раствора NaHCO3 (318 мг, 3,0 ммоль) в 1,4-диоксане (5,0 мл) в закрытой пробирке продували азотом и перемешивали при 100°С в течение 16 часов. После этого ее охлаждали до комнатной температуры, реакционную смесь фильтровали. Фильтрат концентрировали при пониженном давлении. Неочищенный продукт очищали с помощью хроматографии на силикагеле, используя петролейный эфир:ЕtOАс (5:1~1:1) в качестве элюирующих растворителей, получая трет-бутил 4-(6-(6-(пиримидин-5-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилат в виде желтого твердого вещества (350 мг, выход 74%). ЭСИ (МС) m/z=473 [М+Н]+.
Стадия В: Суспензию трет-бутил 4-(6-(6-(пиримидин-5-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилата (320 мг, 0,68 ммоль) в растворе HCI в МеОН (3,0 н, 20 мл) перемешивали при комнатной температуре в течение 4 часов. Реакционную смесь концентрировали при пониженном давлении. Остаток очищали с помощью препаративной ВЭЖХ, получая 175 в виде светло-желтого твердого вещества (220 мг, выход 87%). 1Н ЯМР (500 МГц, ДМСО-d6) δ (ppm) 9,43 (s, 1Н), 9,39 (s, 1Н), 9,35 (d, J=3,0 Гц, 1H), 9,28 (d, J=3,0 Гц, 1H), 9,06 (d, J=11,5 Гц, 1H), 8,66 (d, J=5,5 Гц, 1H), 7,70 (dd, J=8,0 и 16,5 Гц, 1Н), 7,17 (dd, J=7,5 и 11,0 Гц, 1Н), 6,61 (t, J=8,0 Гц, 1Н), 3,83 (s, 2Н), 3,77 (s, 2Н), 3,56 (m, 1Н), 2,95 (t, J=5,0 Гц, 2Н), 2,70 (t, J=6,0 Гц, 2Н), 1,84 (t, J=5,0 Гц, 2Н). ЭСИ (МС) m/z: 373 [М+1]+.
Пример 76 (S)-1-(3-хлор-6-(6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)пиперидин-3-амин 176
Стадия А: 6-хлор-1-(тетрагидро-2Н-пиран-2-ил)-1Н-пиразоло[4,3-с]пиридин
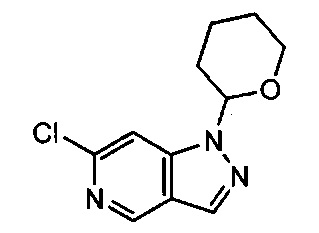
Смесь 6-хлор-1Н-пиразоло[4,3-с]пиридина (11,5 г, 0,075 моль) и 3,4-дигидро-2Н-пирана (19 г, 0,225 моль), и Tos-OH (0,13 г, 0,75 ммоль) в 1,4-диоксане (175 мл) нагревали при 110°С в течение ночи. Смесь охлаждали до комнатной температуры и концентрировали. Неочищенный продукт очищали с помощью колоночной хроматографии на силикагеле (петролейный эфир/этилацетат 20:0-20:1), получая смесь 6-хлор-1-(тетрагидро-2Н-пиран-2-ил)-1Н-пиразоло[4,3-с]пиридина и 6-хлор-2-(тетрагидро-2Н-пиран-2-ил)-2Н-пиразоло[4,3-с]пиридина (13,5 г, выход 76%). МС (ЭСИ) m/z: 238 [М+1]+.
Стадия В: 1-(тетрагидро-2Н-пиран-2-ил)-6-(трибутилстаннил)-1Н-пиразоло[4,3-с]пиридин
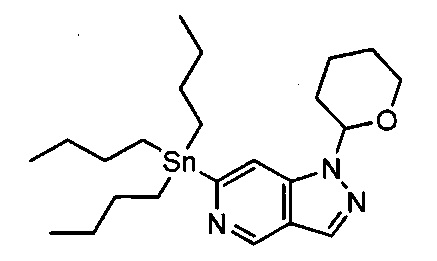
К смеси 6-хлор-1-тетрагидропиран-2-ил-пиразоло[4,3-с]пиридина (19,506 ммоль; 4636,1 мг) в 1,4-диоксане (40 мл) в атмосфере аргона добавляли хлорид лития (117,03 ммоль; 4961,5 мг), бис(трибутилолово) (23,407 ммоль; 14293 мг; 12,45 мл), трис(дибензилиденацетон)дипалладий (0) (0,97528 ммоль; 893,09 мг) и трициклогексилфосфин (2,3407 ммоль; 656,40 мг). Полученную в результате смесь закрывали в пробирке высокого давления и нагревали при 120°С в течение ночи. Смесь фильтровали через целит. Осадок на фильтре промывали ДХМ. Фильтрат концентрировали и остаток очищали на силикагеле, элюируя 0 до 60% ЕtOАс в ДХМ, получая 1-(тетрагидро-2Н-пиран-2-ил)-6-(трибутилстаннил)-1Н-пиразоло[4,3-с]пиридин в виде прозрачного масла (7,1768 г, 74%).
Стадия С: 6-(6-метилпиразин-2-ил)-1-тетрагидропиран-2-ил-пиразоло[4,3-с]пиридин
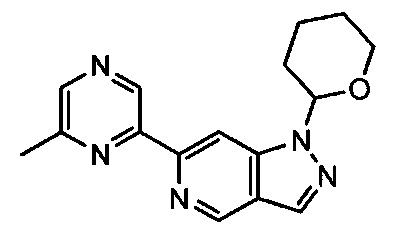
Смесь трибутил-(1-тетрагидропиран-2-илпиразоло[4,3-с]пиридин-6-ил)станнана (7,139 ммоль; 3514,5 мг), 2-хлор-6-метил-пиразина (10,71 ммоль; 1377 мг), трициклогексилфосфина (0,5140 ммоль; 144,1 мг) и трис(дибензилиденацетон)дипалладия (0) (0,2142 ммоль; 196,1 мг) в N,N-диметилацетамиде (15 мл) продували аргоном в течение 1 минуты. Реакционную смесь закрывали в сосуде высокого давления и нагревали при 130°С в течение ночи. Смесь разделяли между ЕtOАс и водой. Органический слой концентрировали и остаток очищали на силикагеле, элюируя 0 до 100% ЕtOАс в ДХМ, получая 6-(6-метилпиразин-2-ил)-1-тетрагидропиран-2-ил-пиразоло[4,3-с]пиридин в виде прозрачного масла (1,3608 г, 60%).
Стадия D: 6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин
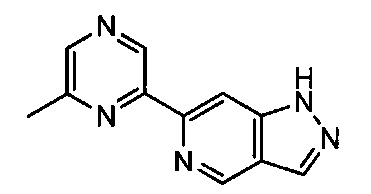
К раствору 6-(6-метилпиразин-2-ил)-1-тетрагидропиран-2-ил-пиразоло[4,3-с]пиридина (4,29 ммоль; 1360,8 мг) в метаноле (10 мл) добавляли соляную кислоту, 4,0 М в 1,4-диоксане (5 мл). Полученную в результате смесь перемешивали при комнатной температуре в течение ночи. Смесь концентрировали и остаток очищали на силикагеле, элюируя 0 до 5% МеОН в ДХМ, получая 6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин в виде твердого вещества белого оттенка (759,5 мг, 88%).
Стадия Е: 1-(5-хлор-6-фтор-2-пиридил)-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин
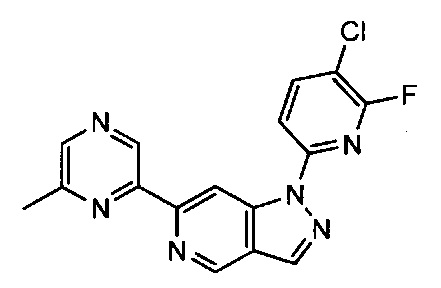
К смеси 6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридина (1,325 ммоль; 279,9 мг) и 6-бром-3-хлор-2-фтор-пиридина (1,988 ммоль; 418,3 мг) в 1,4-диоксане (10 мл) в атмосфере аргона добавляли карбонат цезия (3,975 ммоль; 1295 мг), ксантфос (0,2253 ммоль; 130,4 мг) и трис(дибензилиденацетон)дипалладий (0) (0,1325 ммоль; 121,3 мг). Полученную в результате смесь закрывали в пробирке высокого давления и нагревали при 105°С в течение ночи. Реакционную смесь охлаждали до комнатной температуры и фильтровали через Целит. Осадок на фильтре промывали ДХМ. Фильтрат концентрировали. Остаток очищали на силикагеле, элюируя 0 до 6% МеОН в ДХМ, получая 1-(5-хлор-6-фтор-2-пиридил)-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин (217,1 мг, 48%).
Стадия F: трет-бутил N-[(3S)-1-[3-хлор-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-3-пиперидил]карбамат
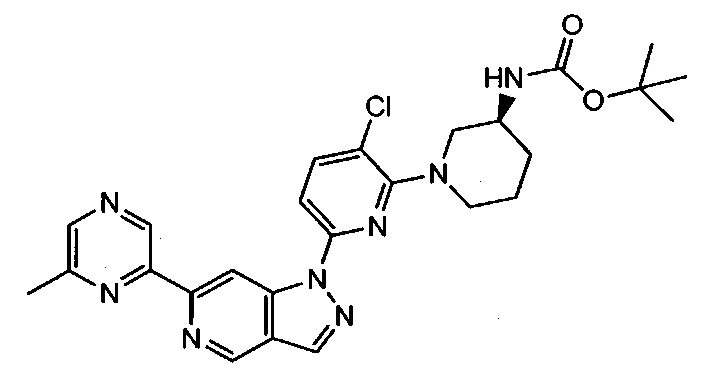
Смесь 1-(5-хлор-6-фтор-2-пиридил)-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридина (0,6372 ммоль; 217,1 мг), трет-бутил N-[(3S)-3-пиперидил]карбамата (1,912 ммоль; 382,9 мг) и N-метилморфолина (3,186 ммоль; 326 мг; 0,354 мл) в 1-метил-2-пирролидиноне (3 мл) в закрытом сосуде высокого давления нагревали при 100°С в течение ночи. Смесь выливали в воду. Осадок собирали фильтрованием, затем очищали на силикагеле, элюируя 0 до 6% МеОН в ДХМ, получая трет-бутил N-[(3S)-1-[3-хлор-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-3-пиперидил]карбамат (229,4 мг, 69%).
Стадия G: К раствору трет-бутил N-[(3S)-1-[3-xлop-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-3-пиперидил]карбамата (0,140 ммоль; 72,7 мг) в метаноле (5 мл) добавляли соляную кислоту, 4,0 М в 1,4-диоксане (5 мл). Полученную в результате смесь перемешивали при комнатной температуре в течение ночи. Смесь концентрировали и остаток очищали с помощью обращенно-фазовой ВЭЖХ, получая 176 в виде твердого вещества белого оттенка (23,3 мг, 40%). 1Н ЯМР (400 МГц, ДМСО) δ 9,67-9,61 (s, 1Н), 9,47-9,42 (s, 1Н), 9,34-9,28 (s, 1Н), 8,71 -8,67 (s, 1Н), 8,64-8,61 (s, 1Н), 8,01-7,94 (d, J=8,4 Гц, 1Н), 7,57-7,51 (d, J=8,4 Гц, 1Н), 3,91-3,83 (d, J=8,8 Гц, 1Н), 3,81-3,72 (d, J=12,3 Гц, 1Н), 3,25-3,19 (m, 1Н), 2,97-2,89 (m, 1Н), 2,77-2,71 (dd, J=11,9, 9,1 Гц, 1Н), 2,67-2,62 (d, J=8,6 Гц, 3Н), 1,98- 1,87 (dd, J=16,2, 6,5 Гц, 2Н), 1,84-1,40 (dd, J=32,9, 22,1 Гц, 3Н), 1,36-1,23 (td, J=13,5, 4,6 Гц, 1Н); МС (ЭСИ) m/z: 421,1 [М+Н]+.
Пример 77 6-[1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридин-6-ил]пиразин-2-карбонитрил 177
Следуя способам получения в примере 23, получали 177. МС (ЭСИ) m/z: 384,1. 1Н ЯМР (400 МГц, ДМСО) δ 9,89 (s, 1Н), 9,61 (s, 1Н), 9,38 (s, 1Н), 9,29 (s, 1Н), 8,71 (s, 1Н), 7,78 (t, J=8,1 Гц, 1Н), 7,30 (d, J=7,7 Гц, 1Н), 6,82 (d, J=8,5 Гц, 1Н), 3,68-3,60 (m, 4Н), 3,02-2,95 (m, 4Н).
Пример 78 1-(6-(1,4-Диазепан-1-ил)пиразин-2-ил)-6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин 178
Стадия А: трет-Бутил 4-(6-бромпиразин-2-ил)-1,4-диазепан-1-карбоксилат
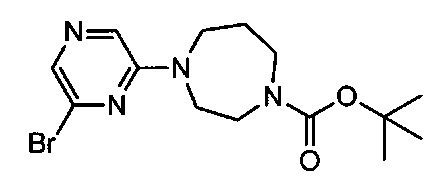
Смесь 2,6-дибромпиразина (0,47 г, 2 ммоль), трет-бутил 1,4-диазепан-1-карбоксилата (0,4 г, 2 ммоль) и ДИПЭА (0,78 г, 6 ммоль) в ЕЮН (10 мл) нагревали при 100°С в течение 15 часов. Реакционную смесь концентрировали при пониженном давлении, получая остаток. Остаток очищали с помощью хроматографии на силикагеле, используя петролейный эфир/этилацетат (5% до 50%) в качестве элюирующих растворителей, получая трет-бутил 4-(6-бромпиразин-2-ил)-1,4-диазепан-1-карбоксилат в виде бесцветного масла (0,5 г, 70%). МС (ЭСИ) m/z: 357 [М+Н]+.
Стадия В: трет-Бутил 4-(6-(6-хлор-1Н-пиразоло[4,3-с]пиридин-1-ил)пиразин-2-ил)-1,4-диазепан-1-карбоксилат
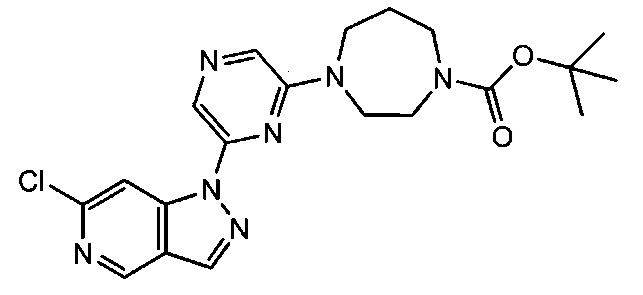
К смеси трет-бутил 4-(6-бромпиразин-2-ил)-1,4-диазепан-1 -карбоксилата (0,45 г, 1,26 ммоль) и 6-хлор-1Н-пиразоло[4,3-с]пиридина (192 мг, 1,26 ммоль) в диоксане (10 мл) добавляли Cul (19 мг, 0,1 ммоль), N1,N2-диметилэтан-1,2-диамин (6,3 ммоль, 0,55 г), К2СO3 (3,78 ммоль, 0,53 г). Реакционную смесь нагревали при 100°С, контролируя с помощью ЖХМС. После завершения реакции смесь концентрировали при пониженном давлении. Неочищенное вещество очищали с помощью хроматографии на силикагеле, используя петролейный эфир/этилацетат (5% до 50%) в качестве элюирующих растворителей, получая трет-бутил 4-(6-(6-хлор-1Н-пиразоло[4,3-с]пиридин-1-ил)пиразин-2-ил)-1,4-диазепан-1-карбоксилат в виде желтого твердого вещества (0,4 г, 74%). МС (ЭСИ) m/z: 430 [М+Н]+.
Стадия С: трет-Бутил 4-(6-(6-(1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиразин-2-ил)-1,4-диазепан-1-карбоксилат
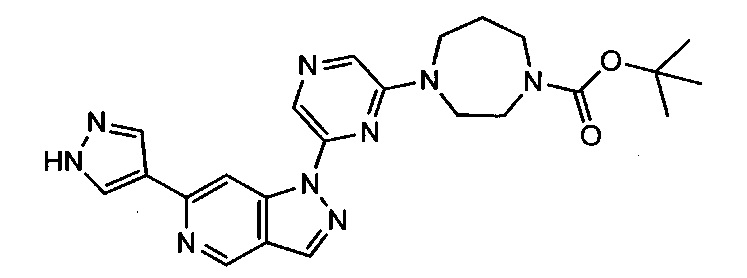
Суспензию трет-бутил 4-(6-(6-хлор-1Н-пиразоло[4,3-с]пиридин-1-ил)пиразин-2-ил)-1,4-диазепан-1-карбоксилата (400 мг, 0,93 ммоль), 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразола (271 мг, 1,4 ммоль), Pd(dppf)Cl2 (81 мг, 0,093 ммоль) и раствора Na2CO3 (2,0 М, 1,5 мл) в 1,4-диоксане (6 мл) в атмосфере аргона в закрытом сосуде нагревали при 120°С в течение 1 часа. Реакционную смесь фильтровали и фильтрат концентрировали при пониженном давлении, получая остаток. Остаток очищали с помощью хроматографии на силикагеле, используя петролейный эфир/этилацетат (10% до 60%) в качестве элюирующих растворителей, получая трет-бутил 4-(6-(6-(1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиразин-2-ил)-1,4-диазепан-1-карбоксилат в виде желтого твердого вещества (180 мг, 42%). МС (ЭСИ) m/z: 462 [М+Н]+.
Стадия D: трет-Бутил 4-(6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]-пиридин-1 -ил)пиразин-2-ил)-1,4-диазепан-1-карбоксилат
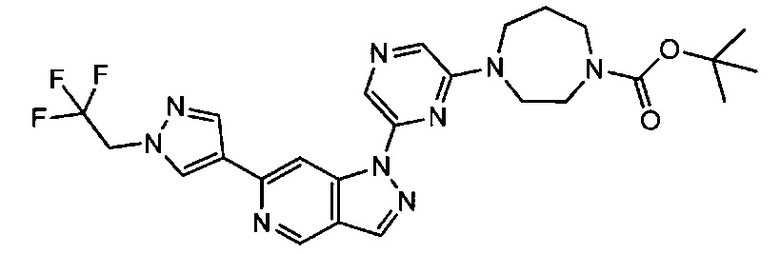
К раствору трет-бутил 4-(6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиразин-2-ил)-1,4-диазепан-1-карбоксилата (100 мг, 0,22 ммоль) в ДМФА (10 мл) добавляли 2,2,2-трифторэтил трифторметансульфонат (100 мг, 0,44 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 2 часов и концентрировали при пониженном давлении. Остаток очищали с помощью хроматографии на силикагеле, используя петролейный эфир/этилацетат (10% до 60%) в качестве элюирующих растворителей, получая трет-бутил 4-(6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиразин-2-ил)-1,4-диазепан-1-карбоксилат в виде белого твердого вещества (80 мг, 80%). МС (ЭСИ) m/z: 544 [М+Н]+.
Стадия Е: К раствору трет-бутил 4-(6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиразин-2-ил)-1,4-диазепан-1-карбоксилата (80 мг, 0,147 ммоль) в 1,4-диоксане (6 мл) добавляли раствор HCl/1,4-диоксана (3,8 М, 6 мл). Реакционную смесь перемешивали при комнатной температуре в течение 2 часов и концентрировали при пониженном давлении, получая неочищенный продукт. Неочищенное вещество очищали с помощью обращенно-фазовой препаративной ВЭЖХ, получая 178 в виде белого твердого вещества (55 мг, 84%). 1Н ЯМР (500 МГц, ДМСО-d6) δ (ррm) 9,17 (s, 1Н), 8,60 (s, 1Н), 8,54 (s, 1Н), 8,37 (d, J=6,0 Гц, 2Н), 8,09 (s, 1Н), 8,02 (s, 1Н), 5,26 (Q, J=9,2 Гц, 2Н), 3,86 (s, 2Н), 3,81 (s, 2Н), 3,01 (t, J=5,5 Гц, 2Н), 2,76 (t, J=5,5 Гц, 2Н), 1,89 (t, J=5,5 Гц, 2Н). МС (ЭСИ) m/z: 444 [М+Н]+.
Пример 79 1-(2-(1,4-Диазепан-1-ил)пиримидин-4-ил)-6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло-[4,3-с]пиридин 179
Следуя способам, описанным в примере 78, и начиная с 2,4-дихлорпиримидина, получали 179 в виде белого твердого вещества (80 мг, 9,5%) в ходе пяти стадий. 1Н ЯМР (500 МГц, ДМСО-d6) δ (ррm) 9,18 (s, 1Н), 8,68 (s, 1Н), 8,64 (s, 1Н), 8,45 (d, J=4,5 Гц, 1Н), 8,39 (s, 1Н), 8,04 (s, 1Н), 7,12 (d, J=5,0 Гц, 1Н), 5,27 (Q, J=9,2 Гц, 2H), 3,98 (s, 2Н), 3,89 (s, 2Н), 3,13 (s, 1Н), 2,95 (s, 1Н), 2,82 (s, 2Н), 2,01 (s, 1Н), 1,81 (s, 1Н). МС (ЭСИ) m/z: 444 [М+Н]+.
Пример 80 1-(6-(1,4-Диазепан-1-ил)пиридин-2-ил)-6-(1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин 180
Следуя способам, описанным в примере 61, и начиная с трет-бутил 4-(6-(6-(1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилата, получали 180 в виде желтого твердого вещества (62 мг, 65,9%) за одну стадию. 1Н ЯМР (500 МГц, MeOD) δ (ppm) 9,084-9,086 (d, J=1 Гц, 1H), 8,68 (s, 1Н), 8,41 (s, 1Н), 8,15 (s, 2Н), 7,77-7,80 (t, J=16,5 Гц, 1H), 7,36-7,38 (d, J=8 Гц, 1H), 6,71-6,73 (d, J=8 Гц, 1H), 4,16-4,19 (t, J=11 Гц, 2H), 3,97-3,99 (t, J=12,5 Гц, 2H), 3,51-3,53 (t, J=11 Гц, 2H), 3,37-3,39 (t, J=11 Гц, 2H), 2,29-2,31 (t, J=11 Гц, 2H), 1,32-1,34 (t, J=14,5 Гц, 2H); МС (ЭСИ) m/z: 361 [М+Н]+.
Пример 81 (S)-1-(3-циклопропил-6-(6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)пиперидин-3-амин 181
Стадия А: трет-бутил N-[(3S)-1-[3-циклопропил-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-3-пиперидил]карбамат
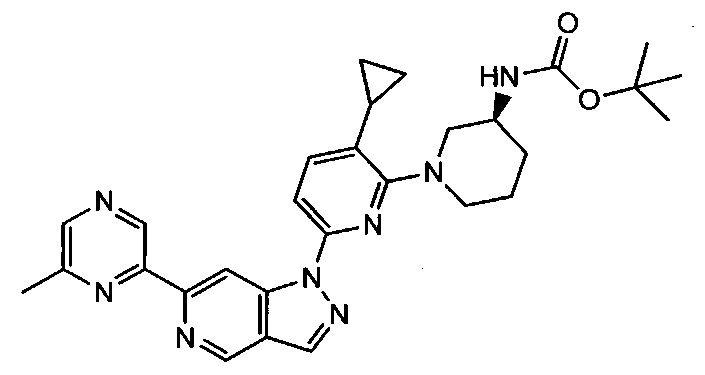
Смесь трет-бутил N-[(3S)-1-[3-хлор-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-3-пиперидил]карбамата (0,2225 ммоль; 115,9 мг), цикпопропилтрифторбората калия (0,3337 ммоль; 50,90 мг), бутилди-1-адамантилфосфина (0,06674 ммоль; 25,19 мг), карбоната цезия (0,6674 ммоль; 217,4 мг) и ацетата палладия (II) (0,04449 ммоль; 9,994 мг) в воде (0,5 мл) и толуоле (4,5 мл) продували аргоном в течение 1 минуты. Реакционную смесь в пробирке высокого давления перемешивали при 105°С в течение 3 дней. Слои разделяли. Органический слой концентрировали. Остаток очищали на силикагеле, элюируя 0 до 5% МеОН в ДХМ, получая трет-бутил N-[(3S)-1-[3-циклопропил-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-3-пиперидил]карбамат (129 мг, ~ 100%).
Стадия В: К раствору трет-бутил N-[(3S)-1-[3-циклопропил-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-3-пиперидил]карбамата (0,2224 ммоль; 117,1 мг) в метаноле (5 мл) добавляли соляную кислоту, 4,0 М в 1,4-диоксане (5 мл). Полученную в результате смесь перемешивали при комнатной температуре в течение ночи. Смесь концентрировали и остаток очищали с помощью обращенно-фазовой ВЭЖХ, получая 181 в виде твердого вещества белого оттенка (46,0 мг, 49%). 1Н ЯМР (400 МГц, ДМСО) δ 9,75-9,71 (s, 1Н), 9,47-9,44 (s, 1Н), 9,33-9,29 (s, 1Н), 8,67 -8,61 (d, J=9,6 Гц, 2Н), 7,55-7,51 (d, J=8,2 Гц, 1Н), 7,49-7,43 (d, J=8,2 Гц, 1Н), 3,86-3,78 (d, J=10,8 Гц, 1Н), 3,65-3,58 (s, 1Н), 3,16-3,09 (s, 1Н), 2,89-2,81 (m, 1Н), 2,68-2,65 (s, 3Н), 2,12-2,04 (m, 1Н), 2,02-1,93 (d, J=8,9 Гц, 2Н), 1,81 -1,69 (m, 1Н), 1,48-1,37 (d, J=8,7 Гц, 1Н), 1,20-1,11 (m, 1Н), 1,09-0,99 (m, 1Н), 0,91-0,84 (m, 1Н), 0,75-0,67 (s, 1Н); МС (ЭСИ) m/z: 427,2 [М+Н]+.
Пример 82 6-метил-1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-3-амин 182
Соединение 182 получали в виде второго пика при хиральном разделении СФХ примера 71. МС (ЭСИ) m/z: 401,2. 1Н ЯМР (400 МГц, ДМСО) δ 9,48 (s, 1Н), 9,45 (s, 1Н), 9,33 (s, 1Н), 8,67 (s, 1Н), 8,62 (s, 1Н), 7,77 (t, J=8,1 Гц, 1Н), 7,23 (d, J=7,7 Гц, 1Н), 6,75 (d, J=8,5 Гц, 1Н), 5,03 (s, 1Н), 4,09 (d, J=8,8 Гц, 1Н), 2,80 (dd, J=19,2, 10,2 Гц, 2Н), 2,64 (s, 3Н), 1,94-1,72 (m, 3Н), 1,66-1,51 (m, 1Н), 1,27 (d, J=6,8 Гц, 3Н).
Пример 83 6-метил-1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-3-амин 183
Соединение 183 получали в виде первого пика при хиральном разделении СФХ примера 71. МС (ЭСИ) m/z: 401,2. 1Н ЯМР (400 МГц, ДМСО) δ 9,48 (s, 1Н), 9,45 (s, 1Н), 9,33 (s, 1Н), 8,67 (s, 1Н), 8,62 (s, 1Н), 7,76 (t, J=8,1 Гц, 1Н), 7,22 (d, J=7,7 Гц, 1Н), 6,75 (d, J=8,5 Гц, 1Н), 5,01 (s, 1Н), 4,13-3,92 (m, 2Н), 2,81-2,73 (m, 2Н), 2,65 (s, 3Н), 1,96-1,69 (m, 2Н), 1,55 (dd, J=14,9, 8,1 Гц, 1Н), 1,26 (d, J=6,8 Гц, 3Н).
Пример 84 1-[6-(5-метил-1,4-диазепан-1-ил)-2-пиридил]-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин 184
Следуя способам получения в примере 23, получали 184. МС (ЭСИ) m/z: 401,2. 1Н ЯМР (400 МГц, ДМСО) δ 9,65 (s, 1Н), 9,45 (s, 1Н), 9,31 (s, 1Н), 8,65 (s, 1Н), 8,62 (s, 1Н), 7,70 (t, J=8,1 Гц, 1Н), 7,20 (d, J=7,7 Гц, 1Н), 6,59 (d, J=8,5 Гц, 1Н), 4,01 (d, J=12,7 Гц, 2Н), 3,86-3,73 (m, 1Н), 3,62 (t, J=10,1 Гц, 1Н), 3,20 (d, J=13,9 Гц, 1Н), 2,98-2,87 (m, 1Н), 2,71-2,62 (m, 1Н), 2,61 (s, 3Н), 2,13-2,02 (m, 1Н), 1,54-1,40 (m, 1Н), 1,00 (d, J=6,4 Гц, 3Н).
Пример 85 1-[6-(3-метилпиперазин-1-ил)-2-пиридил]-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин 185
Соединение 185 получали в виде второго пика при хиральном разделении СФХ примера 69. МС (ЭСИ) m/z: 387,2. 1Н ЯМР (400 МГц, ДМСО) 5 9,56 (s, 1Н), 9,47 (s, 1Н), 9,32 (s, 1Н), 8,66 (s, 1Н), 8,63 (s, 1Н), 7,77 (t, J=8,1 Гц, 1Н), 7,25 (d, J=7,7 Гц, 1Н), 6,82 (d, J=8,5 Гц, 1Н), 4,39 (d, J=12,3 Гц, 1Н), 4,19 (d, J=11,3 Гц, 1Н), 3,12 (d, J=11,8 Гц, 1Н), 3,07-2,98 (m, 1Н), 2,94-2,82 (m, 2Н), 2,63 (s, 3Н), 1,06 (d, J=6,3 Гц, 3Н).
Пример 86 (S)-1-(3-метокси-6-(6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)пиперидин-3-амин 186
Стадия А: трет-бутил N-[(3S)-1-(6-бром-3-метокси-2-пиридил)-3-пиперидил]карбамат
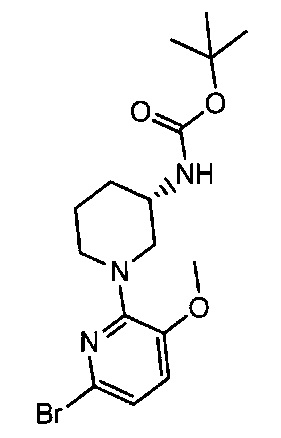
Смесь 6-бром-2-фтор-3-метокси-пиридина (2,030 ммоль; 418,1 мг), трет-бутил N-[(3S)-3-пиперидил]карбамата (3,044 ммоль; 609,7 мг) и N-метилморфолина (6,089 ммоль; 622 мг; 0,676 мл) в 1-метил-2-пирролидиноне (5 мл) в закрытом сосуде высокого давления нагревали при 120°С в течение ночи. Смесь выливали в воду и экстрагировали EtOAc. Органический слой концентрировали. Остаток очищали на силикагеле, элюируя 0 до 40% EtOAc в гептане, получая трет-бутил N-[(3S)-1-(6-бром-3-метокси-2-пиридил)-3-пиперидил]карбамат (743,5 мг, 95%).
Стадия В: трет-бутил N-[(3S)-1-[3-метокси-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-3-пиперидил]карбамат
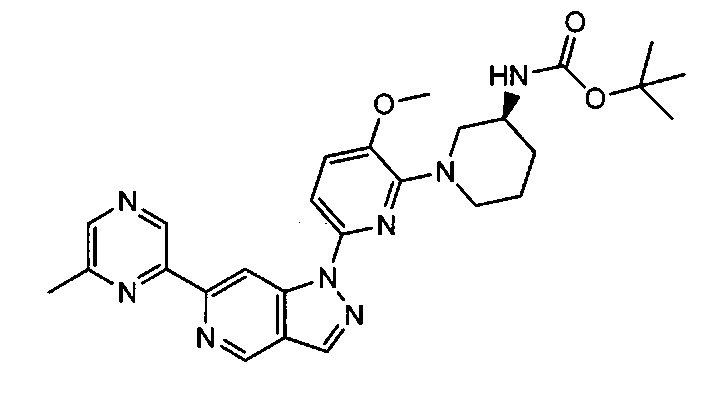
Смесь 6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридина (0,4734 ммоль; 100,0 мг), трет-бутил N-[(3S)-1-(6-бром-3-метокси-2-пиридил)-3-пиперидил]карбамата (0,5681 ммоль, 219,5 мг), N,N'-диметилэтилендиамина (0,4734 ммоль; 41,73 мг; 0,0471 мл), иодида меди (0,4734 ммоль; 91,08 мг) и карбоната калия (0,5208 ммоль; 72,70 мг) в 1,4-диоксане (10 мл) продували аргоном, затем закрывали и перемешивали при 100°С в течение ночи. Смесь охлаждали до комнатной температуры и затем фильтровали через Целит. Фильтрат концентрировали; остаток очищали на силикагеле, элюируя 0 до 100% ЕtOАс в ДХМ, получая трет-бутил N-[(3S)-1-[3-метокси-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-3-пиперидил]карбамат в виде бежевого твердого вещества (142,5 мг, 58%).
Стадия С: К раствору трет-бутил N-[(3S)-1-[3-метокси-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-3-пиперидил]карбамата (0,2758 ммоль; 142,5 мг) в метаноле (10 мл) добавляли соляную кислоту, 4,0 М в 1,4-диоксане (5 мл). Полученную в результате смесь перемешивали при комнатной температуре в течение ночи. Смесь концентрировали и остаток очищали с помощью обращенно-фазовой ВЭЖХ, получая 186 в виде твердого вещества белого оттенка (105,6 мг, 91%). 1Н ЯМР (400 МГц, ДМСО) δ 9,66-9,62 (s, 1Н), 9,48-9,44 (s, 1Н), 9,33-9,28 (s, 1Н), 8,65-8,61 (d, J=3,5 Гц, 2Н), 7,54-7,45 (dd, J=21,6, 8,5 Гц, 2Н), 4,02-3,96 (d, J=10,3 Гц, 1Н), 3,90-3,84 (d, J=11,7 Гц, 4Н), 3,03-2,96 (d, J=9,0 Гц, 1Н), 2,89-2,82 (m, 1Н), 2,65-2,61 (s, 3Н), 1,98-1,86 (t, J=10,6 Гц, 2Н), 1,78-1,67 (d, J=10,2 Гц, 1Н), 1,45-1,35 (dd, J=19,2, 8,9 Гц, 1Н); МС (ЭСИ) m/z: 417,2 [М+Н]+.
Пример 87 1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]азепан-3-амин 187
Следуя способам получения в примере 23, получали 187. МС (ЭСИ) m/z: 401,2. 1Н ЯМР (400 МГц, ДМСО) δ 9,64 (s, 1Н), 9,46 (s, 1Н), 9,32 (s, 1Н), 8,66 (s, 1Н), 8,62 (s, 1Н), 7,73 (t, J=8,0 Гц, 1Н), 7,21 (d, J=7,7 Гц, 1Н), 6,73 (d, J=8,5 Гц, 1Н), 4,39-4,29 (m, 1Н), 4,06 (d, J=12,5 Гц, 1Н), 2,63 (s, 3Н), 2,11 (s, 1Н), 1,76 (s, 3Н), 1,44 (d, J=10,3 Гц, 1Н), 1,27 (d, J=9,6 Гц, 1Н).
Пример 88 и 89 (R)-1-(6-(6-(1-(2,2,2-Трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)-пиридин-2-ил)-1,4-диазепан-6-ол 188 и (S)-1-(6-(6-(1-(2,2,2-Трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)-пиридин-2-ил)-1,4-диазепан-6-ол 189
Стадия А: 1-(6-Бромпиридин-2-ил)-1,4-диазепан-6-ол
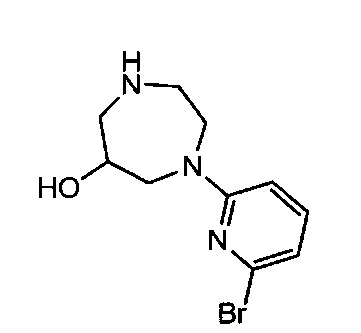
Смесь 2-бром-6-фторпиридина (477 мг, 2,7 ммоль), 1,4-диазепан-6-ола (350 мг, 3 ммоль) и ДИПЭА (1,94 г, 15 ммоль) в этаноле (10 мл) нагревали при 100°С в течение 16 часов. Затем ее охлаждали, реакционную смесь концентрировали при пониженном давлении. Остаток разбавляли ЕtOАс (100 мл) и промывали солевым раствором. Органический слой сушили над Na2SO4 и концентрировали при пониженном давлении, получая 1-(6-бромпиридин-2-ил)-1,4-диазепан-6-ол в виде бесцветного масла (400 мг, 48,9%). МС (ЭСИ) m/z: 272 [М+Н]+.
Стадия В: трет-Бутил 4-(6-бромпиридин-2-ил)-6-гидрокси-1,4-диазепан-1-карбоксилат
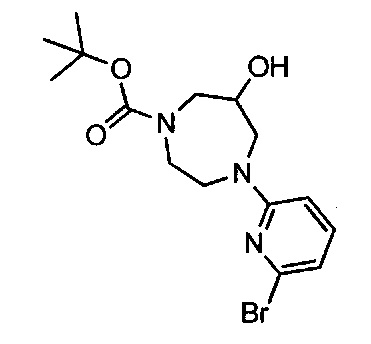
Смесь 1-(6-бромпиридин-2-ил)-1,4-диазепан-6-ола (400 мг, 1,47 ммоль), Вос2O (354 мг, 1,62 ммоль) и Et3N (157 мг, 1,55 ммоль) в ДХМ (10 мл) перемешивали при комнатной температуре в течение 16 часов. Реакционную смесь промывали солевым раствором, сушили над Na2SO4 и концентрировали при пониженном давлении, получая трет-бутил 4-(6-бромпиридин-2-ил)-6-гидрокси-1,4-диазепан-1-карбоксилат в виде бесцветного масла (500 мг, 91%). МС (ЭСИ) m/z: 372 [М+Н]+.
Стадия С: трет-Бутил 4-(6-(6-хлор-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-6-гидрокси-1,4-диазепан-1-карбоксилат
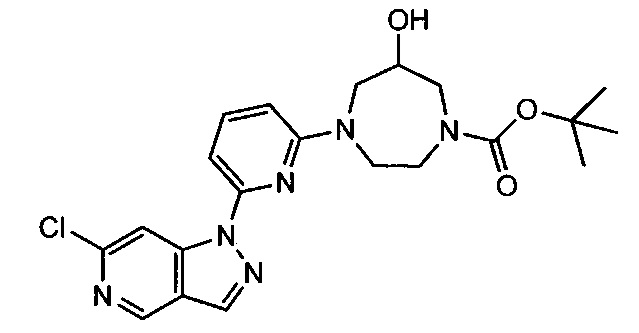
К смеси трет-бутил 4-(6-бромпиридин-2-ил)-6-гидрокси-1,4-диазепан-1-карбоксилата (550 мг, 1,48 ммоль) и 6-хлор-1Н-пиразоло[4,3-с]пиридина (207 мг, 1,34 ммоль) в 1,4-диоксане (20 мл) добавляли Cul (102 мг, 0,54 ммоль), К2СO3 (743 г, 5,4 ммоль) и N1,N2-диметилэтан-1,2-диамин (95 мг, 1,08 ммоль). Реакционную смесь нагревали при 100°С в течение 3 часов, контролируя с помощью ЖХМС. После завершения реакции ее концентрировали при пониженном давлении. Неочищенное вещество очищали с помощью хроматографии на силикагеле, используя петролейный эфир/EtOAc (2/1) в качестве элюирующих растворителей, получая трет-бутил 4-(6-(6-хлор-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-6-гидрокси-1,4-диазепан-1-карбоксилат в виде светло-желтого твердого вещества (160 мг, 24,3%). МС (ЭСИ) m/z: 445 [М+Н]+.
Стадия D: трет-Бутил 4-(6-(6-(1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-6-гидрокси-1,4-диазепан-1-карбоксилат
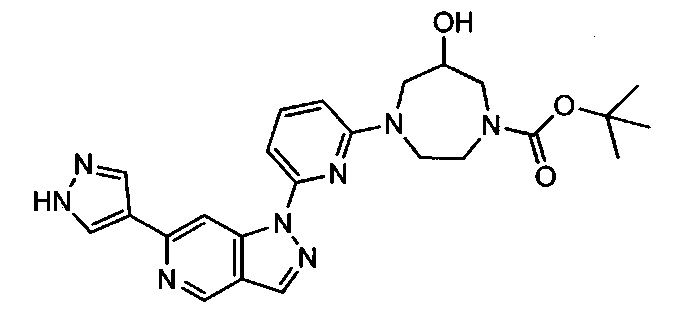
Суспензию трет-бутил 4-(6-(6-хлор-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-6-гидрокси-1,4-диазепан-1-карбоксилата (160 мг, 0,36 ммоль), 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразола (140 мг, 0,72 ммоль), Pd(dppf)Cl2 (147 мг, 0,18 ммоль) и водн. Na2CO3 (2,0 М, 1 мл) в 1,4-диоксане (10 мл) в атмосфере азота нагревали при 100°С в течение 16 часов. Реакционную смесь фильтровали и фильтрат концентрировали при пониженном давлении. Остаток очищали с помощью хроматографии на силикагеле, используя ЕtOАс в качестве элюирующего растворителя, получая трет-бутил 4-(6-(6-(1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-6-гидрокси-1,4-диазепан-1-карбоксилат в виде желтого твердого вещества (60 мг, 35%). МС (ЭСИ) m/z: 477 [М+Н]+.
Стадия Е: трет-Бутил (±)-6-гидрокси-4-(6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилат
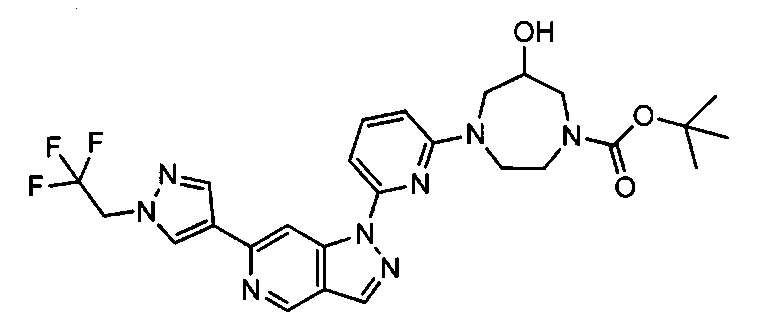
Суспензию трет-бутил 4-(6-(6-(1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-6-гидрокси-1,4-диазепан-1-карбоксилата (150 мг, 0,32 ммоль), 2,2,2-трифторэтил трифторметансульфоната (110 мг, 0,48 ммоль) и К2СO3 (87 мг, 0,64 ммоль) в ДМФА (10 мл) перемешивали при комнатной температуре в течение 18 часов, контролируя с помощью ЖХМС. После завершения реакции реакционную смесь гасили ЕtOАс (100 мл), промывали солевым раствором (50 мл), сушили над MgSO4, концентрировали при пониженном давлении. Остаток очищали с помощью хроматографии на силикагеле, используя петролейный эфир/ЕtOАс (1/1) в качестве элюирующих растворителей, получая трет-бутил (±)-6-гидрокси-4-(6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилат в виде белого твердого вещества (82 мг, 46,5%). МС (ЭСИ) m/z: 559 [М+Н]+.
Стадия F: трет-Бутил (R)-6-гидрокси-4-(6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилат и трет-Бутил (8)-6-гидрокси-4-(6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилат
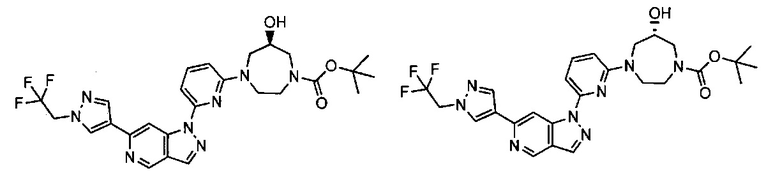
трет-Бутил (±)-6-гидрокси-4-(6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло-[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилат разделяли с помощью хиральной препаративной ВЭЖХ, получая трет-бутил (S)-6-гидрокси-4-(6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилат (70 мг) и трет-бутил (R)-6-гидрокси-4-(6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилат (70 мг).
Стадия G: Смесь трет-бутил (S)-6-гидрокси-4-(6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилата (70 мг, 0,13 ммоль) в HCl/MeOH (4,0 М, 10 мл) перемешивали при комнатной температуре в течение 3 часов, контролируя с помощью ЖХМС. После завершения реакции реакционную смесь концентрировали при пониженном давлении. Неочищенное вещество очищали с помощью обращенно-фазовой преп. ВЭЖХ, получая (R)-1-(6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-6-ол 188 в виде белого твердого вещества (30 мг, 52,6%). 1Н ЯМР (500 МГц, ДМСО-d6) δ (ppm) 9,16 (s, 1Н), 8,74 (s, 1Н), 8,55 (s, 1Н), 8,49 (s, 1Н), 8,21 (s, 1Н), 7,69 (t, J=16 Гц, 1Н), 7,17 (d, J=7,5 Гц, 1Н), 6,66 (d, J=8 Гц, 1Н), 5,18-5,24 (m, 2Н), 4,93 (d, J=5,5 Гц, 1Н), 3,96 (t, J=8,5 Гц, 1Н), 3,88 (m, 2Н), 3,56-3,64 (m, 2Н), 2,98 (t, J=10,5 Гц, 2Н), 2,80-2,84 (m, 1Н), 2,64-2,72 (m, 1Н); МС (ЭСИ) m/z: 459 [М+Н]+.
Стадия Н: Следуя способам, описанным на стадии G, и начиная с трет-бутил (R)-6-гидрокси-4-(6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилата, получали 189 в виде желтого твердого вещества (41 мг, 71,9%). 1Н ЯМР (500 МГц, ДМСО-d6) δ (ppm) 9,16 (s, 1Н), 8,74 (s, 1Н), 8,55 (s, 1Н), 8,49 (s, 1Н), 8,21 (s, 1Н), 7,69 (t, J=16 Гц, 1Н), 7,17 (d, J=7,5 Гц, 1Н), 6,66 (d, J=8 Гц, 1Н), 5,18-5,24 (m, 2Н), 4,93 (d, J=5,5 Гц, 1H), 3,96 (t, J=8,5 Гц, 1H), 3,88 (m, 2H), 3,56-3,64 (m, 2H), 2,98 (t, J=10,5 Гц, 2H), 2,80-2,84 (m, 1H), 2,64-2,72 (m, 1H); МС (ЭСИ) m/z: 459 [M+H]+.
Пример 90 6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-N-(4-пиперидил)пиридин-2-амин 190
Следуя способам получения в примере 23, получали 190. МС (ЭСИ) m/z: 387,2. 1Н ЯМР (400 МГц, ДМСО) δ 9,45 (s, 1Н), 9,42 (s, 1Н), 9,32 (s, 1Н), 8,64 (s, 2Н), 8,35 (s, 1Н), 7,61 (t, J=8,0 Гц, 1Н), 7,10 (d, J=7,7 Гц, 1Н), 6,54 (d, J=8,2 Гц, 1Н), 4,17 (s, 1Н), 3,08-2,97 (m, 2Н), 2,71 (d, J=9,7 Гц, 1Н), 2,67 (s, 3Н), 2,06 (s, 2Н), 1,64 (d, J=9,1 Гц, 2Н).
Пример 91 1-[6-[(2R)-2-метилпиперазин-1-ил]-2-пиридил]-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин 191
Следуя способам получения в примере 71, получали 191. МС (ЭСИ) т/г.387,2. 1Н ЯМР (400 МГц, ДМСО) δ 9,52 (s, 1Н), 9,48 (s, 1Н), 9,32 (s, 1Н), 8,66 (s, 1Н), 8,62 (s, 1Н), 7,76 (t, J=8,1 Гц, 1Н), 7,26 (d, J=7,7 Гц, 1Н), 6,75 (d, J=8,5 Гц, 1Н), 4,60 (s, 1Н), 4,06 (d, J=12,1 Гц, 1Н), 3,19-3,08 (m, 3Н), 2,99 (dt, J=19,3, 7,8 Гц, 2Н), 2,84-2,74 (m, 1Н), 2,64 (s, 3Н), 1,28 (d, J=6,6 Гц, 3Н).
Пример 92 (3S,5S)-5-фтор-1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-3-амин 192
Следуя способам получения в примере 23, получали 192. МС (ЭСИ) m/z: 405,2.
Пример 93 1-[6-(3-метилпиперазин-1-ил)-2-пиридил]-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин 193
Соединение 193 получали в виде первого пика при хиральном разделении СФХ примера 69. МС (ЭСИ) m/z: 387,2. 1Н ЯМР (400 МГц, ДМСО) δ 9,54 (s, 1Н), 9,47 (s, 1Н), 9,33 (s, 1Н), 8,67 (s, 1Н), 8,64 (s, 1Н), 7,80 (t, J=8,1 Гц, 1Н), 7,28 (d, J=7,7 Гц, 1Н), 6,86 (d, J=8,5 Гц, 1Н), 4,43 (d, J=12,4 Гц, 1Н), 4,25 (d, J=12,0 Гц, 1Н), 3,17-3,06 (m, 1Н), 3,03-2,91 (m, 2Н), 2,83-2,71 (m, 1Н), 2,64 (s, 3Н), 1,12 (d, J=6,3 Гц, 3Н).
Пример 94 1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-4-амин 194
Следуя способам получения в примере 23, получали 194. МС (ЭСИ) m/z: 387,2. 1Н ЯМР (400 МГц, ДМСО) δ 9,61 (s, 1Н), 9,47 (s, 1Н), 9,33 (s, 1Н), 8,67 (s, 1Н), 8,64 (s, 1Н), 7,77 (t, J=8,1 Гц, 1Н), 7,27 (d, J=7,7 Гц, 1Н), 6,86 (d, J=8,5 Гц, 1Н), 4,43 (d, J=13,3 Гц, 2Н), 2,65 (s, 3Н), 1,98 (d, J=10,4 Гц, 2Н), 1,48 (dd, J=20,4, 11,1 Гц, 2Н).
Пример 95 2-метил-1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-3-амин 195
Следуя способам получения в примере 71, получали 195. МС (ЭСИ) m/z: 401,2. 1Н ЯМР (400 МГц, ДМСО) 5 9,47 (d, J=5,9 Гц, 2Н), 9,33 (s, 1Н), 8,66 (s, 1Н), 8,62 (s, 1Н), 7,78 (t, J=8,1 Гц, 1Н), 7,21 (d, J=7,7 Гц, 1Н), 6,77 (d, J=8,5 Гц, 1Н), 4,66-4,55 (m, 1Н), 4,42 (d, J=13,7 Гц, 1Н), 3,10- 3,00 (m, 2Н), 2,64 (s, 3Н), 1,92 -1,83 (m, 1Н), 1,65 (dt, J=21,6, 10,4 Гц, 3Н), 1,19 (d, J=6,8 Гц, 3Н).
Пример 96 1 -[6-[(28)-2-метилпиперазин-1 -ил]-2-пиридил]-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин 196
Следуя способам получения в примере 71, получали 196. МС (ЭСИ) m/z: 387,1. 1Н ЯМР (400 МГц, ДМСО) δ 9,53 (s, 1Н), 9,48 (s, 1Н), 9,33 (s, 1Н), 8,67 (s, 1Н), 8,63 (s, 1Н), 7,76 (t, J=8,1 Гц, 1Н), 7,27 (d, J=7,7 Гц, 1Н), 6,75 (d, J=8,5 Гц, 1Н), 4,61 (s, 1Н), 4,07 (d, J=12,0 Гц, 1H), 2,98 (dd, J=20,6, 13,3 Гц, 2H), 2,79 (t, J=10,8 Гц, 1H), 2,64 (s, 3Н), 1,29 (d, J=6,6 Гц, 3Н).
Пример 97 1-(5-циклопропил-6-(1,4-диазепан-1-ил)пиридин-2-ил)-6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин 197
Следуя способам, описанным в примере 81, и начиная с 6-бром-3-хлор-2-фторпиридина и трет-бутил 1,4-диазепан-1-карбоксилата, получали 197 в виде твердого вещества белого оттенка (31,6 мг, 48%) за 4 стадии. 1Н ЯМР (400 МГц, ДМСО) δ 9,66-9,61 (s, 1Н), 9,48-9,42 (s, 1Н), 9,33-9,27 (s, 1Н), 8,66-8,60 (d, J=7,9 Гц, 2Н), 7,53-7,49 (d, J=8,1 Гц, 1Н), 7,39-7,34 (d, J=8,1 Гц, 1Н), 3,94-3,84 (m, 4Н), 3,10-3,06 (m, 2Н), 2,91-2,84 (m, 2Н), 2,65-2,61 (s, 3Н), 2,03-1,91 (tt, J=11,5, 5,6 Гц, 3Н), 1,05-0,92 (m, 3Н), 0,78-0,71 (q, J=5,7 Гц, 2Н); МС (ЭСИ) m/z: 427,2 [М+Н]+.
Пример 98 (3S,5R)-5-фтор-1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-3-амин 198
Следуя способам получения в примере 23, получали 198. МС (ЭСИ) m/z: 405,1. 1Н ЯМР (400 МГц, ДМСО) δ 9,58 (s, 1Н), 9,47 (s, 1Н), 9,33 (s, 1Н), 8,67 (s, 1Н), 8,63 (s, 1Н), 7,78 (t, J=8,1 Гц, 1Н), 7,25 (d, J=7,7 Гц, 1Н), 6,85 (d, J=8,5 Гц, 1Н), 5,10 (d, J=47,2 Гц, 1Н), 4,71 (t, J=13,0 Гц, 1Н), 4,29 (d, J=9,9 Гц, 1Н), 2,96 -2,86 (m, 1Н), 2,65 (s, 3Н), 2,20 (d, J=11,5 Гц, 1Н), 1,69 (dt, J=24,6, 11,4 Гц, 1Н).
Пример 99 2-[6-[6-(6-метил пиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-2,8-диазаспиро[4.5]декан 199
Следуя способам получения в примере 23, получали 199. МС (ЭСИ) m/z: 427,1. 1Н ЯМР (400 МГц, ДМСО) δ 9,82 (s, 1Н), 9,46 (s, 1Н), 9,31 (s, 1Н), 8,64 (d, J=6,3 Гц, 2Н), 7,73 (t, J=8,0 Гц, 1Н), 7,20 (d, J=7,7 Гц, 1Н), 6,46 (d, J=8,3 Гц, 1Н), 3,86 (s, 2Н), 3,00-2,83 (m, 6Н), 2,63 (s, 3Н), 2,02 (t, J=7,0 Гц, 2Н), 1,67 (s, 4Н).
Пример 100 8-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-2,8-диазаспиро[4.5]декан 200
Следуя способам получения в примере 23, получали 200. МС (ЭСИ) m/z: 427,1. 1Н ЯМР (400 МГц, ДМСО) δ 9,62 (s, 1Н), 9,48 (s, 1Н), 9,33 (s, 1Н), 8,67 (s, 1Н), 8,64 (s, 1Н), 7,77 (t, J=8,1 Гц, 1Н), 7,26 (d, J=7,7 Гц, 1Н), 6,87 (d, J=8,5 Гц, 1Н), 3,91-3,80 (m, 2Н), 3,78-3,68 (m, 2Н), 3,13-3,07 (m, 2Н), 2,89 (s, 2Н), 2,65 (S, 3Н), 1,79 (t, J=7,2 Гц, 2Н), 1,71 (t, J=5,3 Гц, 4Н).
Пример 101 (S)-2-(3-аминопиперидин-1-ил)-6-(6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)никотинонитрил 201
Стадия А: 1-(5-бром-6-фтор-2-пиридил)-6-хлор-пиразоло[4,3-с]пиридин и 6-хлор-1-(6-фтор-5-йод-2-пиридил)пиразоло[4,3-с]пиридин
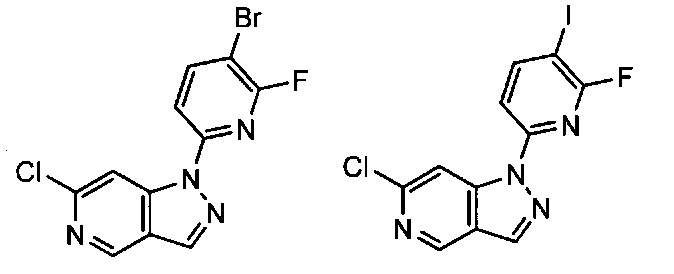
Смесь 6-хлор-1Н-пиразоло[4,3-с]пиридина (2,045 ммоль; 314,0 мг), 3-бром-2-фтор-6-йод-пиридина (2,249 ммоль; 679,0 мг), N,N'-диметилэтилендиамина (0,2045 ммоль; 18,02 мг; 0,0203 мл), иодида меди (2,045 ммоль; 393,3 мг) и карбоната калия (2,249 ммоль; 314,0 мг) в 1,4-диоксане (10 мл) продували аргоном, затем закрывали и перемешивали при 100°С в течение 20 часов. Смесь охлаждали до комнатной температуры и затем фильтровали через Целит. Фильтрат концентрировали; остаток очищали на силикагеле, элюируя 0 до 100% ЕtOАс в гептане, получая смесь 1-(5-бром-6-фтор-2-пиридил)-6-хлор-пиразоло[4,3-с]пиридина (~80 мг, 12%) и 6-хлор-1-(6-фтор-5-йод-2-пиридил)пиразоло[4,3-с]пиридина (~163 мг, 21%).
Стадия В: 6-(6-хлорпиразоло[4,3-с]пиридин-1-ил)-2-фтор-пиридин-3-карбонитрил
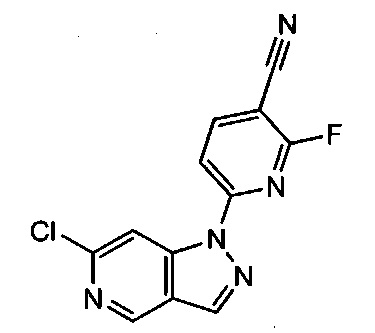
Суспензию 1-(5-бром-6-фтор-2-пиридил)-6-хлор-пиразоло[4,3-с]пиридина (0,7437 ммоль; 243,6 мг), цианида цинка (0,4462 ммоль; 53,47 мг; 0,0289 мл) и тетракис(трифенилфосфин)палладия (0) (0,03719 ммоль; 43,1 мг) в ДМФА (5 мл) дегазировали и затем нагревали при 120°С в течение 3 часов. Смесь охлаждали до комнатной температуры и затем разделяли между ЕtOАс и солевым раствором. Органический слой концентрировали и остаток очищали на силикагеле, элюируя 0 до 60% ЕtOАс в гептане, получая 6-(6-хлорпиразоло[4,3-с]пиридин-1-ил)-2-фтор-пиридин-3-карбонитрил в виде белого твердого вещества (143,2 мг, 70%).
Стадия С: триметил-(6-метилпиразин-2-ил)станнан
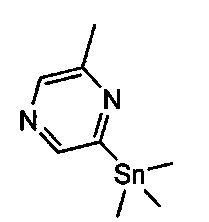
Смесь 2-хлор-6-метил-пиразина (3,357 ммоль; 431,6 мг), гексаметилдиолова (4,03 ммоль; 1361 мг; 0,861 мл) и тетракис(трифенилфосфин)палладия (0) (0,2756 ммоль; 318,5 мг) в 1,4-диоксане (10 мл) продували аргоном. Полученную в результате смесь закрывали в пробирке высокого давления и нагревали при 100°С в течение ночи. Смесь охлаждали до комнатной температуры и фильтровали через Целит. Осадок на фильтре промывали ДХМ. Фильтрат концентрировали, получая триметил-(6-метилпиразин-2-ил)станнан, который использовали без очистки.
Стадия D: трет-бутил N-[(3S)-1-[3-циано-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-3-пиперидил]карбамат
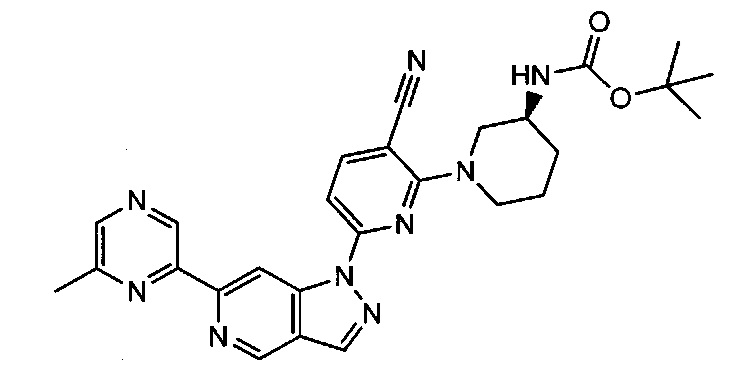
Смесь [(3S)-1-[6-(6-хлорпиразоло[4,3-с]пиридин-1-ил)-3-циано-2-пиридил]-3-пиперидил]карбаминовой кислоты (0,5166 ммоль; 205,5 мг), триметил-(6-метилпиразин-2-ил)станнана (0,7749 ммоль; 199,1 мг) и тетракис(трифенилфосфин)палладия (0) (0,05166 ммоль; 59,8 мг) в N,N-диметилацетамиде (12 мл) продували аргоном. Реакционную смесь закрывали в сосуде высокого давления и нагревали при 150°С в течение 2 часов. Смесь охлаждали до комнатной температуры и затем разделяли между ЕtOАс и водой. Органический слой концентрировали и остаток очищали на силикагеле, элюируя 0 до 5% МеОН в ДХМ, получая трет-бутил N-[(3S)-1-[3-циано-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-3-пиперидил]карбамат в виде желтого твердого вещества (248,6 мг, 94%).
Стадия Е: К раствору трет-бутил N-[(3S)-1-[3-циано-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-3-пиперидил]карбамата (0,4859 ммоль; 248,6 мг) в дихлорметане (8 мл) добавляли ТФК (2 мл). Полученную в результате смесь перемешивали при комнатной температуре в течение 4 часов. Смесь концентрировали и остаток очищали с помощью обращенно-фазовой ВЭЖХ, получая 201 в виде твердого вещества белого оттенка (361,6 мг, 18%). 1Н ЯМР (400 МГц, ДМСО) δ 9,61-9,55 (s, 1Н), 9,48-9,44 (s, 1Н), 9,37-9,33 (s, 1Н), 8,80-8,75 (s, 1Н), 8,66-8,62 (s, 1Н), 8,26-8,19 (m, 2Н), 7,48-7,44 (d, J=8,4 Гц, 1Н), 4,29-4,19 (dd, J=10,7, 6,9 Гц, 2Н), 3,00-2,94 (m, 1Н), 2,66-2,62 (s, 3Н), 2,03-1,89 (dd, J=18,5, 10,2 Гц, 2Н), 1,80-1,66 (m, 1Н), 1,49-1,37 (m, 1Н); МС (ЭСИ) m/z: 412,2 [М+Н]+.
Пример 102 (5S)-5-амино-1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-2-он 202
Стадия А: трет-бутил N-[(3S)-1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-6-оксо-3-пиперидил]карбамат
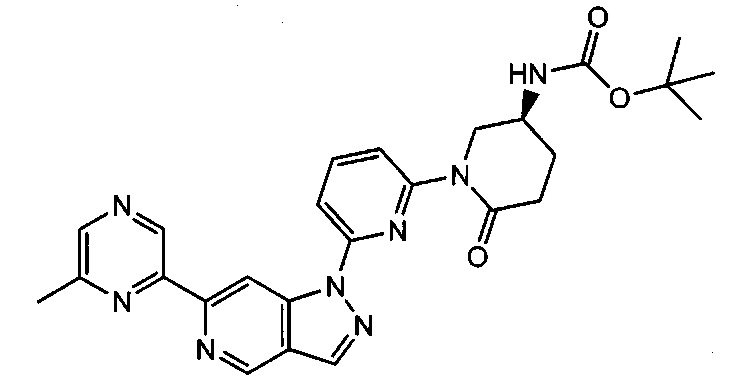
Смесь 6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридина (75 мг, 0,36 ммоль), трет-бутил N-[(3S)-1-(6-бром-2-пиридил)-6-оксо-3-пиперидил]карбамата (158 мг, 0,426 ммоль), трис(дибензилиденацетон)дипалладия (0) (32 мг, 0,036 ммоль), ксантфоса (42 мг, 0,071 ммоль) и трет-бутилата натрия (70 мг, 0,71 ммоль) в 6,0 мл толуола перемешивали при 100°С в течение 18 часов. Реакционную смесь фильтровали через целит. Неочищенный продукт очищали с помощью флэш-хроматографии (элюировали ЕtOАс/гептаном при 100% ЕtOАс), получая трет-бутил N-[(3S)-1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-6-оксо-3-пиперидил]карбамат (50 мг) с выходом 28%.
Стадия В: Раствор трет-бутил N-[(3S)-1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-6-оксо-3-пиперидил]карбамата (45 мг, 0,15 ммоль) в хлороводороде (4 моль/л) в 1,4-диоксане (2,0 мл, 8,0 ммоль) и 2,0 мл 1,4-диоксана перемешивали при к.т.в течение 18 часов. Реакционную смесь разбавляли водой, затем промывали ЕtOАс. Водный слой подщелачивали 1 М NaOH до рН 10 и экстрагировали ЕtOАс. Органические слои сушили с сульфатом натрия, фильтровали и концентрировали в вакууме. Неочищенный продукт подвергали обращенно-фазовой ВЭЖХ, получая 202 (11 мг) с выходом 18%. МС (ЭСИ) m/z: 401,1. 1Н ЯМР (400 МГц, ДМСО) δ 9,61 (s, 1Н), 9,47 (s, 1Н), 9,35 (s, 1H), 8,73 (s, 1H), 8,63 (s, 1H), 8,04 (t, J=8,1 Гц, 1H), 7,83 (d, J=7,9 Гц, 1H), 7,76 (d, J=8,1 Гц, 1H), 4,24 (dd, J=12,2, 3,8 Гц, 1H), 3,94 (dd, J=12,3, 6,3 Гц, 1H), 3,49 (s, 1H), 2,75 (dd, J=12,2, 5,3 Гц, 1H), 2,69 (s, 3Н), 2,63-2,55 (m, 1H), 2,10 (dd, J=13,0, 4,3 Гц, 1H), 1,85-1,72 (m, 1H).
Пример 103 2-метил-1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-3-амин 203
Соединение 203 получали в виде первого пика при хиральном разделении СФХ примера 71. МС (ЭСИ) m/z: 401,1. 1Н ЯМР (400 МГц, ДМСО) δ 9,47 (d, J=7,6 Гц, 2Н), 9,32 (s, 1Н), 8,66 (s, 1Н), 8,62 (s, 1Н), 7,76 (t, J=8,1 Гц, 1Н), 7,21 (d, J=7,7 Гц, 1Н), 6,77 (d, J=8,5 Гц, 1Н), 4,62-4,49 (m, 1Н), 4,41 (d, J=13,7 Гц, 1Н), 3,09 -2,97 (m, 2Н), 2,64 (s, 3Н), 1,86 (d, J=13,0 Гц, 1Н), 1,74-1,49 (m, 3Н), 1,17 (d, J=6,8 Гц, 3Н).
Пример 104 2-метил-1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-3-амин 204
Соединение 204 получали в виде второго пика при хиральном разделении СФХ примера 71. МС (ЭСИ) m/z: 401,1. 1Н ЯМР (400 МГц, ДМСО) δ 9,47 (d, J=5,4 Гц, 2Н), 9,32 (d, J=0,9 Гц, 1Н), 8,65 (d, J=10,3 Гц, 1Н), 8,61 (d, J=5,5 Гц, 1Н), 7,81-7,73 (m, 1Н), 7,21 (d, J=7,7 Гц, 1H), 6,77 (d, J=8,5 Гц, 1H), 4,63-4,52 (m, 1Н), 4,41 (d, J=14,2 Гц, 1H), 3,10-2,99 (m, 2Н), 2,64 (s, 3Н), 1,86 (d, J=12,0 Гц, 1H), 1,76-1,52 (m, 3Н), 1,19 (d, J=6,8 Гц, 3Н).
Пример 105 (S)-1-(3-метил-6-(6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)пиперидин-3-амин 205
Стадия А: 6-бром-2-фтор-3-метил-пиридин
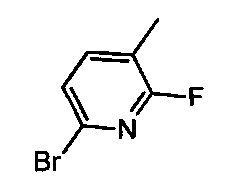
К диизопропиламину (22,001 ммоль; 2240 мг; 3,13 мл) в ТГФ (40 мл) при 0°С добавляли N-бутиллитий (2,5 моль/л) в гексане (24,001 ммоль; 9,6 мл). Реакционную смесь перемешивали при 0°С в течение 0,5 часа и затем охлаждали до -78°С. Добавляли по каплям 2-бром-6-фтор-пиридин (20,001 ммоль; 3520,0 мг) в ТГФ (10 мл). Смесь перемешивали при -78°С в течение 3 часов. Медленно добавляли подметан (22,001 ммоль; 3122,8 мг; 1,37 мл). Смесь нагревали до комнатной температуры, перемешивая в течение 1 часа. Реакцию гасили водой (~50 мл) и перемешивали в течение ночи. Слои разделяли. Органический слой концентрировали и остаток очищали на силикагеле, элюируя 0 до 5% EtOAc в гептане, получая 6-бром-2-фтор-3-метил-пиридин в виде белого твердого вещества (2,08 г, 55%).
Стадия В: Следуя способам, описанным в примере 86, и начиная с трет-бутил N-[(38)-3-пиперидил]карбамата, 6-бром-2-фтор-3-метил-пиридина и 6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридина, получали 205 в виде твердого вещества белого оттенка (4,4 мг, 4,5%) за 3 стадии. 1Н ЯМР (400 МГц, ДМСО) δ 9,75-9,70 (s, 1Н), 9,48-9,44 (s, 1Н), 9,33-9,29 (s, 1Н), 8,68-8,61 (d, J=12,1 Гц, 2Н), 8,38-8,15 (s, 1Н), 7,78-7,74 (d, J=8,1 Гц, 1Н), 7,59-7,55 (d, J=8,0 Гц, 1Н), 2,90-2,84 (m, 1Н), 2,67-2,63 (s, 3Н), 2,37-2,32 (s, 3Н), 2,04-1,95 (d, J=9,2 Гц, 2Н), 1,80-1,68 (d, J=9,4 Гц, 1Н), 1,57-1,47 (d, J=8,6 Гц, 1Н); МС (ЭСИ) m/z: 433,1 [М+Н]+.
Пример 106 4-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1 -ил]-2-пиридил]-1,4-диазепан-5-он 206
Следуя способам получения в примере 102, получали 206. МС (ЭСИ) m/z: 401,1.
Пример 107 1-(3-метокси-6-(6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-6-ол 207
Стадия А: 1 -(6-бром-3-метокси-2-пиридил)-1,4-диазепан-6-ол
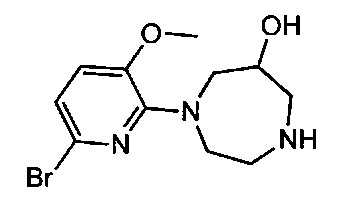
Смесь 6-бром-2-фтор-3-метокси-пиридина (2,660 ммоль; 547,9 мг), 1,4-диазепан-6-ола дигидробромида (3,989 ммоль; 1109 мг) и N,N'-диизопропилэтиламина (10,64 ммоль; 1389 мг; 1,87 мл) в изопропаноле (10 мл) в закрытом сосуде высокого давления нагревали при 100°С в течение ночи. Смесь охлаждали до комнатной температуры и концентрировали. Остаток очищали на силикагеле, элюируя 0 до 10% МеОН в ДХМ, получая 1-(6-бром-3-метокси-2-пиридил)-1,4-диазепан-6-ол (301,2 мг, 37%).
Стадия В: трет-бутил 4-(6-бром-3-метокси-2-пиридил)-6-гидрокси-1,4-диазепан-1-карбоксилат
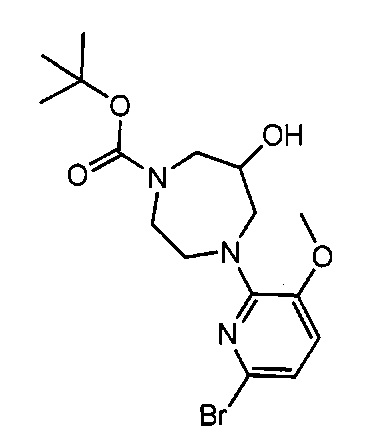
Смесь 1-(6-бром-3-метокси-2-пиридил)-1,4-диазепан-6-ола (0,9968 ммоль; 301.2 мг), трет-бутоксикарбонил трет-бутилкарбоната (1,495 ммоль; 326,3 мг) и гидрокарбоната натрия (9,968 ммоль; 837,4 мг) в дихлорметане (20 мл) перемешивали при комнатной температуре в течение ночи. Смесь концентрировали и остаток очищали на силикагеле, элюируя 0 до 40% ЕtOАс в ДХМ, получая трет-бутил 4-(6-бром-3-метокси-2-пиридил)-6-гидрокси-1,4-диазепан-1-карбоксилат (262,5 мг, 65%).
Стадия С: Следуя способам, описанным в примере 86, и начиная с 6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридина и трет-бутил 4-(6-бром-3-метокси-2-пиридил)-6-гидрокси-1,4-диазепан-1-карбоксилата, получали 207 в виде твердого вещества белого оттенка (4,4 мг, 4,5%) за 2 стадии. МС (ЭСИ) m/z: 433,1 [М+Н]+.
Пример 108 5-(1-(6-(1,4-диазепан-1-ил)пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридин-6-ил)-3-метилпиразин-2-амин 208
Стадия А: трет-бутил N-[(38)-1-[6-(6-хлорпиразоло[4,3-с]пиридин-1-ил)-2-пиридил]-3-пиперидил]карбамат
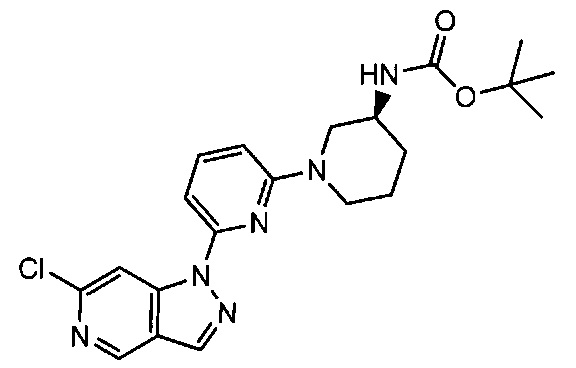
Смесь 6-хлор-1-(6-фтор-2-пиридил)пиразоло[4,3-с]пиридина (2,998 ммоль; 745.3 мг), трет-бутил N-[(3S)-3-пиперидил]карбамата (4,496 ммоль; 900,5 мг) и N-метилморфолина (8,993 ммоль; 919 мг; 0,999 мл) в 1-метил-2-пирролидиноне (10 мл) в закрытом сосуде высокого давления нагревали при 100°С в течение ночи. Смесь выливали в воду. Осадок собирали фильтрованием, затем очищали на силикагеле, элюируя 0 до 40% ЕtOАс в гептане, получая трет-бутил N-[(3S)-1-[6-(6-хлорпиразоло[4,3-с]пиридин-1-ил)-2-пиридил]-3-пиперидил]карбамат (1,0738 г, 84%).
Стадия В: трет-бутил 4-[6-(6-трибутилстаннилпиразоло[4,3-с]пиридин-1-ил)-2-пиридил]-1,4-диазепан-1-карбоксилат
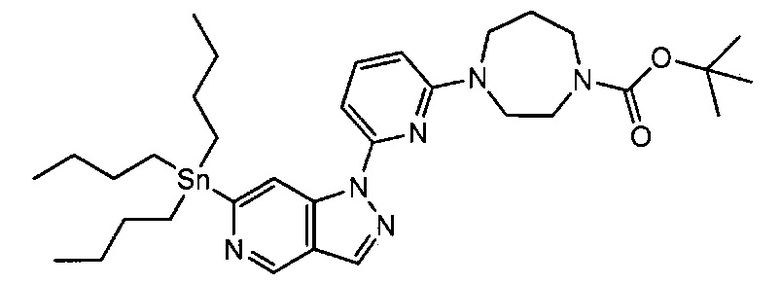
К смеси трет-бутил 4-[6-(6-хлорпиразоло[4,3-с]пиридин-1-ил)-2-пиридил]-1,4-диазепан-1-карбоксилата (1,234 ммоль; 529,4 мг) в 1,4-диоксане (40 мл) в атмосфере аргона добавляли хлорид лития (7,406 ммоль; 314,0 мг), бис(трибутилолово) (1,481 ммоль; 904,5 мг; 0,7879 мл), трис(дибензилиденацетон)дипалладий (0) (0,06172 ммоль; 56,52 мг) и трициклогексилфосфин (0,1481 ммоль; 41,54 мг). Полученную в результате смесь закрывали в пробирке высокого давления и нагревали при 120°С в течение ночи. Смесь охлаждали до комнатной температуры и фильтровали через Целит. Осадок на фильтре промывали ДХМ. Фильтрат концентрировали и остаток очищали на силикагеле, элюируя 0 до 40% ЕtOАс в гептане, получая трет-бутил 4-[6-(6-трибутилстаннилпиразоло[4,3-с]пиридин-1-ил)-2-пиридил]-1,4-диазепан-1-карбоксилат в виде прозрачного масла (400,0 мг, 47%).
Стадия С: трет-бутил 4-[6-[6-(5-амино-6-метил-пиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-1,4-диазепан-1-карбоксилат
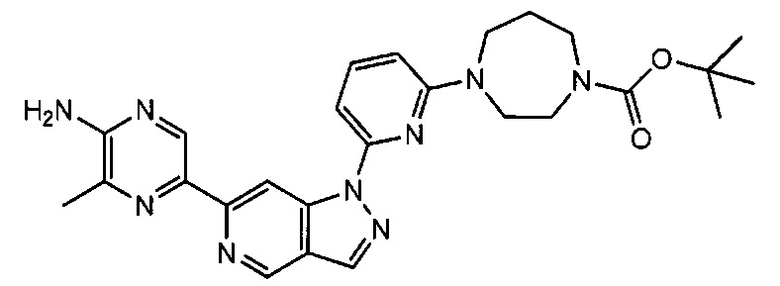
Смесь трет-бутил 4-[6-(6-трибутилстаннилпиразоло[4,3-с]пиридин-1-ил)-2-пиридил]-1,4-диазепан-1-карбоксилата (0,5852 ммоль; 400 мг), 5-бром-3-метил-пиразин-2-амина (1,170 ммоль; 220,1 мг), трициклогексилфосфина (0,1405 ммоль; 39,39 мг) и трис(дибензилиденацетон)дипалладия (0) (0,05852 ммоль; 53,59 мг) в N,N-диметилацетамиде (30 мл) продували аргоном в течение 1 минуты. Реакционную смесь закрывали в микроволновой пробирке Biotage и нагревали в микроволновой печи при 150°С в течение 45 минут. Смесь разделяли между EtOAc и водой. Органический слой концентрировали и остаток очищали на силикагеле, элюируя 10% МеОН в ДХМ, получая трет-бутил 4-[6-[6-(5-амино-6-метил-пиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-1,4-диазепан-1-карбоксилат (115,0 мг, 39%).
Стадия D: К раствору трет-бутил 4-[6-[6-(5-амино-6-метил-пиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-1,4-диазепан-1-карбоксилата (0,2293 ммоль; 115 мг) в метаноле (10 мл) добавляли соляную кислоту, 4,0 М в 1,4-диоксане (5 мл). Полученную в результате смесь перемешивали при комнатной температуре в течение ночи. Смесь концентрировали и остаток очищали с помощью обращенно-фазовой ВЭЖХ, получая 208 в виде твердого вещества белого оттенка (4,0 мг, 4,3%). МС (ЭСИ) m/z: 402,1 [М+Н]+.
Пример 109 (S)-5-(1-(6-(3-аминопиперидин-1-ил)пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридин-6-ил)-3-метилпиразин-2-амин 209
Следуя способам, описанным в примере 108, и начиная с (З)-трет-бутил пиперидин-3-илкарбамата, получали 209 в виде твердого вещества белого оттенка (52,8 мг, 56%) за 4 стадии. 1Н ЯМР (400 МГц, ДМСО) δ 9,34-9,29 (s, 1Н), 9,20-9,13 (s, 1Н), 8,89-8,84 (s, 1Н), 8,58-8,54 (s, 1Н), 7,77-7,69 (t, J=8,1 Гц, 1Н), 7,22-7,15 (d, J=7,7 Гц, 1Н), 6,81-6,73 (d, J=8,5 Гц, 1Н), 6,60-6,51 (s, 2Н), 4,45-4,37 (d, J=13,2 Гц, 1H), 4,18-4,11 (d, J=10,5 Гц, 1H), 3,16-3,08 (dd, J=17,5, 6,7 Гц, 1H), 2,87-2,74 (dt, J=22,9, 9,5 Гц, 2H), 2,47-2,38 (s, 3Н), 1,96-1,90 (d, J=12,7 Гц, 1H), 1,87- 1,79 (m, 1Н), 1,65- 1,53 (d, J=12,8 Гц, 1H), 1,38-1,28 (m, 1H); МС (ЭСИ) m/z: 402,1 [М+Н]+.
Пример 110 3-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]циклогексанамин 210
Соединение 210 получали в виде третьего пика при хиральном разделении СФХ смеси четырех диастереомеров. МС (ЭСИ) m/z: 386,1. 1Н ЯМР (400 МГц, ДМСО) δ 9,68 (s, 1Н), 9,49 (s, 1Н), 9,37 (s, 1Н), 8,74 (s, 1Н), 8,66 (s, 1Н), 8,07-8,02 (гл, 1Н), 7,92 (d, J=8,1 Гц, 1Н), 7,31 (d, J=7,5 Гц, 1Н), 2,65 (s, 3Н), 2,35-2,21 (m, 1Н), 2,19-2,02 (m, 3Н), 1,96-1,72 (m, 4Н).
Пример 111 3-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]циклогексанамин 211
Соединение 211 получали в виде первого пика при хиральном разделении СФХ смеси четырех диастереомеров. МС (ЭСИ) m/z: 386,1. 1Н ЯМР (400 МГц, ДМСО) δ 9,68 (s, 1Н), 9,49 (s, 1Н), 9,37 (d, J=0,8 Гц, 1Н), 8,74 (s, 1Н), 8,66 (s, 1Н), 8,07-8,02 (m, 1Н), 7,92 (d, J=8,1 Гц, 1Н), 7,31 (d, J=7,5 Гц, 1Н), 2,65 (s, 3Н), 2,36-2,22 (m, 2Н), 2,19-2,03 (m, 4Н), 1,93-1,72 (m, 4Н).
Пример 112 3-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1 -ил]-2-пиридил]циклогексанамин 212
Соединение 212 получали в виде второго пика при хиральном разделении СФХ смеси четырех диастереомеров. МС (ЭСИ) m/z: 386,1. 1Н ЯМР (400 МГц, ДМСО) δ 9,72 (s, 1Н), 9,49 (s, 1Н), 9,37 (s, 1Н), 8,75 (s, 1Н), 8,66 (s, 1Н), 8,06-8,01 (m, 1Н), 7,92 (d, J=8,1 Гц, 1Н), 7,29 (d, J=7,4 Гц, 1Н), 3,26 (s, 1Н), 3,04 (t, J=12,1 Гц, 1Н), 2,66 (S, 3Н), 2,25-2,02 (m, 4Н), 1,95 (dd, J=27,3, 12,1 Гц, 1Н), 1,71-1,53 (m, 2Н), 1,46 (dd, J=22,9, 10,7 Гц, 1Н).
Пример 113 3-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]циклогексанамин 213
Соединение 213 получали в виде четвертого пика при хиральном разделении СФХ смеси четырех диастереомеров. МС (ЭСИ) т/г: 386,1. 1Н ЯМР (400 МГц, ДМСО) δ 9,72 (s, 1Н), 9,49 (s, 1Н), 9,37 (s, 1Н), 8,74 (s, 1Н), 8,66 (s, 1Н), 8,06-8,00 (гл, 1Н), 7,92 (d, J=8,2 Гц, 1Н), 7,29 (d, J=7,5 Гц, 1Н), 3,25 (s, 1Н), 3,04 (t, J=12,1 Гц, 1Н), 2,66 (s, 3Н), 2,27-2,02 (m, 4Н), 1,94 (dd, J=25,3, 12,8 Гц, 1Н), 1,73-1,39 (m, 3Н).
Пример 114 1-[6-(2,6-диазаспиро[3.4]октан-6-ил)-2-пиридил]-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин 214
Следуя способам получения в примере 23, получали 214. МС (ЭСИ) m/z: 399,1. 1Н ЯМР (400 МГц, ДМСО) δ 9,80 (s, 1Н), 9,45 (s, 1Н), 9,30 (s, 1Н), 8,64 (d, J=3,3 Гц, 1Н), 8,39 (s, 1Н), 7,73 (t, J=8,0 Гц, 1Н), 7,20 (d, J=7,7 Гц, 1Н), 6,42 (d, J=8,3 Гц, 1Н), 3,73 (dd, J=21,9, 13,3 Гц, 6Н), 3,62 (d, J=8,5 Гц, 2Н), 2,65 (s, 3Н), 2,32 (t, J=6,8 Гц, 2Н).
Пример 115 (S)-1-(3-фтор-6-(6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)пиперидин-3-амин 215
Стадия А: трет-бутил N-[(3S)-1-(6-хлор-3-фтор-2-пиридил)-3-пиперидил]карбамат
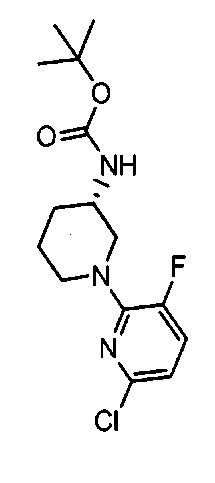
Смесь 2,6-дихлор-3-фтор-пиридина (3,802 ммоль, 631,1 мг), трет-бутил N-[(38)-3-пиперидил]карбамата (3,992 ммоль; 799,6 мг), карбоната калия (7,605 ммоль; 1051 мг), N,N'-диметилэтилендиамина (0,3802 ммоль; 33,52 мг; 0,0409 мл) и иодида меди (I) (3,802 ммоль; 724,1 мг) в 1,4-диоксане (15 мл) продували аргоном, затем закрывали в пробирке высокого давления и нагревали при 105°С в течение ночи. Реакционную смесь охлаждали до комнатной температуры, затем фильтровали через Целит. Фильтрат концентрировали и остаток очищали на силикагеле, элюируя 0 до 20% ЕtOАс в гептане, получая трет-бутил N-[(3S)-1-(6-хлор-3-фтор-2-пиридил)-3-пиперидил]карбамат (279,2 мг, 22%) в виде белого твердого вещества.
Стадия В: трет-бутил N-[(3S)-1-[3-фтор-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-3-пиперидил]карбамат
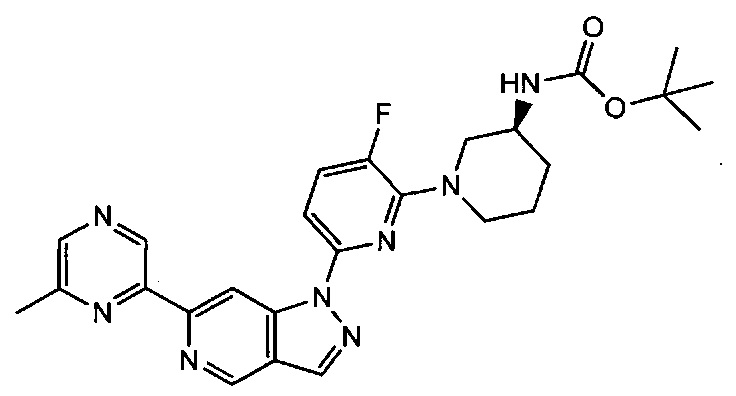
Смесь 6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридина (0,83325 ммоль; 176 мг), трет-бутил N-[(3S)-1-(6-хлор-3-фтор-2-пиридил)-3-пиперидил]карбамата (0,8378 ммоль; 276,3 мг), карбоната цезия (1,6665 ммоль; 543,00 мг), ксантфоса (0,14165 ммоль; 84,500 мг) и трис(дибензилиденацетон)дипалладия (0) (0,083325 ммоль; 77,074 мг) в 1,4-диоксане (10 мл) продували аргоном, затем закрывали и перемешивали при 110°С в течение ночи. Смесь охлаждали до комнатной температуры и фильтровали через Целит. Фильтрат концентрировали и остаток очищали на силикагеле, элюируя 0 до 100% ЕtOАс в гептане, получая трет-бутил N-[(3S)-1-[3-фтор-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-3-пиперидил]карбамат (113,1 мг, 16%).
Стадия С: Смесь трет-бутил N-[(3S)-1-[3-фтор-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-3-пиперидил]карбамата (0,1345 ммоль; 113,1 мг) в ТФК (1 мл) и дихлорметане (4 мл) перемешивали при комнатной температуре в течение ночи. Смесь концентрировали и остаток очищали с помощью обращенно-фазовой ВЭЖХ, получая 215 в виде твердого вещества белого оттенка (42,7 мг, 77%). 1Н ЯМР (400 МГц, ДМСО) δ 9,58-9,55 (s, 1H), 9,47-9,43 (s, 1H), 9,33-9,30 (s, 1H), 8,69-8,65 (s, 1H), 8,64-8,62 (s, 1H), 8,35-8,30 (s, 1H), 7,79-7,72 (dd, J=12,7, 8,5 Гц, 1H), 7,42-7,38 (dd, J=8,4, 2,0 Гц, 1H), 4,05-3,97 (d, J=8,5 Гц, 2H), 3,29-3,26 (d, J=10,8 Гц, 1H), 3,02-2,95 (m, 2H), 2,66-2,60 (s, 3Н), 2,00-1,87 (t, J=14,1 Гц, 2H), 1,80-1,67 (m, 1H), 1,47-1,37 (d, J=10,5 Гц, 1H); МС (ЭСИ) m/z: 405,1 [М+Н]+.
Пример 116 8-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-1,8-диазаспиро[4.5]декан 216
Следуя способам получения в примере 23, получали 216. МС (ЭСИ) m/z: 427,1. 1Н ЯМР (400 МГц, ДМСО) δ 9,61 (s, 1Н), 9,46 (s, 1Н), 9,32 (s, 1Н), 8,66 (s, 1Н), 8,62 (s, 1Н), 7,74 (t, J=8,1 Гц, 1Н), 7,23 (d, J=7,7 Гц, 1Н), 6,83 (d, J=8,5 Гц, 1Н), 3,87-3,70 (m, 4Н), 2,87 (t, J=6,9 Гц, 2Н), 2,63 (s, 3Н), 1,79-1,68 (m, 2Н), 1,68-1,60 (m, 3Н), 1,60-1,52 (m, 3Н).
Пример 117 1-[6-(2,7-диазаспиро[3.4]октан-2-ил)-2-пиридил]-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин 217
Следуя способам получения в примере 23, получали 217. МС (ЭСИ) m/z: 399,1. 1Н ЯМР (400 МГц, ДМСО) δ 9,82 (s, 1Н), 9,46 (s, 1Н), 9,31 (s, 1Н), 8,65 (s, 1Н), 8,63 (s, 1Н), 7,75 (t, J=8,0 Гц, 1Н), 7,26 (d, J=7,7 Гц, 1Н), 6,37 (d, J=8,1 Гц, 1Н), 4,16 (s, 4Н), 3,20 (s, 2Н), 3,02 (t, J=7,1 Гц, 3Н), 2,62 (s, 2Н), 2,14 (t, J=7,1 Гц, 2Н).
Пример 118 (S)-(2-(3-аминопиперидин-1-ил)-6-(6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-3-ил)метанол 218 Стадия А: (6-бром-2-фтор-3-пиридил)метанол
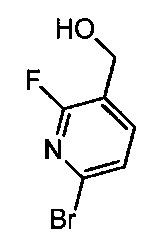
К диизопропиламину (22,001 ммоль; 2240 мг; 3,13 мл) в ТГФ (40 мл) при 0°С добавляли N-бутиллитий (2,5 моль/л) в гексане (24,001 ммоль; 9,6 мл). Реакционную смесь перемешивали при 0°С в течение 0,5 часа и затем охлаждали до -78°С.Добавляли по каплям 2-бром-6-фтор-пиридин (20,001 ммоль; 3520,0 мг) в ТГФ (10 мл). Смесь перемешивали при -78°С в течение 2,5 часов. Быстро добавляли параформальдегид (40,002 ммоль; 3603,3 мг). Смесь нагревали до комнатной температуры и перемешивали в течение ночи. Реакцию гасили водой. Слои разделяли. Водный слой экстрагировали ЕtOАс. Объединенные органические слои концентрировали и остаток очищали на силикагеле, элюируя 0 до 50% ЕtOАс в гептане, получая (6-бром-2-фтор-3-пиридил)метанол (1,4888 г, 36%).
Стадия В: трет-бутил N-[(3S)-1-[6-бром-3-(гидроксиметил)-2-пиридил]-3-пиперидил]карбамат
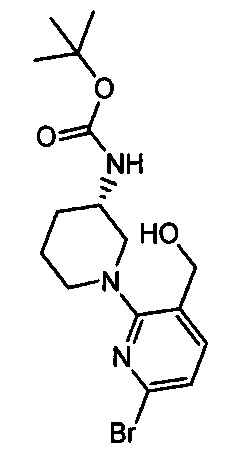
Смесь (6-бром-2-фтор-3-пиридил)метанола (1,766 ммоль; 363,8 мг), трет-бутил N-[(3S)-3-пиперидил]карбамата (2,649 ммоль; 530,5 мг) и N-метилморфолина (5,298 ммоль; 541 мг; 0,588 мл) в 1-метил-2-пирролидиноне (10 мл) в закрытом сосуде высокого давления нагревали при 130°С в течение 4 часов. Смесь выливали в воду и экстрагировали ЕtOАс. Органический слой концентрировали. Остаток очищали на силикагеле, элюируя 0 до 100% ЕtOАс в гептане, получая трет-бутил N-[(3S)-1-[6-бром-3-(гидроксиметил)-2-пиридил]-3-пиперидил]карбамат (546,3 мг, 80%).
Стадия С: Следуя способам, описанным в примере 86, и начиная с 6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридина и трет-бутил N-[(3S)-1-[6-6poM-3-(гидроксиметил)-2-пиридил]-3-пиперидил]карбамата, получали 218 в виде твердого вещества белого оттенка (40,8 мг, 68%) за 2 стадии. 1Н ЯМР (400 МГц, ДМСО) δ 9,77-9,73 (s, 1Н), 9,49-9,45 (s, 1Н), 9,34-9,31 (s, 1Н), 8,69-8,67 (s, 1Н), 8,64-8,61 (s, 1Н), 8,03-7,98 (d, J=8,1 Гц, 1Н), 7,65-7,61 (d, J=8,1 Гц, 1Н), 4,59-4,52 (d, J=2,9 Гц, 2Н), 3,60-3,52 (d, J=12,4 Гц, 1Н), 3,51-3,43 (d, J=9,8 Гц, 1Н), 3,21-3,15 (d, J=10,4 Гц, 1Н), 3,00-2,92 (s, 1Н), 2,74-2,68 (d, J=12,0 Гц, 1Н), 2,67-2,64 (s, 3Н), 1,98-1,89 (d, J=9,4 Гц, 2Н), 1,77-1,66 (m, 1Н), 1,37 -1,26 (d, J=10,0 Гц, 1Н); МС (ЭСИ) m/z: 417,1 [М+Н]+.
Пример 119 1-(6-(6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)-3-(трифторметил)пиридин-2-ил)-1,4-диазепан-6-ол 219
Смесь 1-[6-фтор-5-(трифторметил)-2-пиридил]-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридина (0,213 ммоль; 79,9 мг), 1,4-диазепан-6-ола дигидробромида (1,07 ммоль; 297 мг) и карбоната цезия (2,13 ммоль; 696 мг) в ДМСО (2 мл) и ИПС (4 мл) в закрытом сосуде высокого давления нагревали при 120°С в течение ночи. Смесь охлаждали до комнатной температуры и затем фильтровали через Целит®. Фильтрат концентрировали и остаток очищали с помощью обращенно-фазовой ВЭЖХ, получая 219 в виде твердого вещества белого оттенка (10,8 мг, 11%). 1Н ЯМР (400 МГц, ДМСО) δ 9,59-9,53 (s, 1Н), 9,48 -9,43 (s, 1Н), 9,38-9,33 (s, 1Н), 8,79-8,75 (s, 1Н), 8,66-8,62 (s, 1Н), 8,22-8,17 (d, J=8,5 Гц, 1Н), 7,57-7,52 (d, J=8,5 Гц, 1Н), 4,76-4,67 (s, 1Н), 3,98-3,88 (d, J=10,4 Гц, 3Н), 3,75-3,66 (d, J=14,1 Гц, 1Н), 3,65-3,55 (dd, J=15,3, 8,4 Гц, 1Н), 3,15-3,07 (m, 1Н), 3,06-2,99 (m, 1Н), 2,87-2,79 (dd, J=13,7, 3,4 Гц, 1Н), 2,76 -2,68 (dd, J=13,6, 5,8 Гц, 1Н), 2,69-2,62 (s, 3Н); МС (ЭСИ) m/z: 471,1 [М+Н]+.
Пример 120 (S)-1-(6-(6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)-3-(трифторметил)пиридин-2-ил)пиперидин-3-амин 120
Стадия А: 1-[6-фтор-5-(трифторметил)-2-пиридил]-6-(6-метилпиразин-2-ил)пиразоло[4,3-c]пиридин
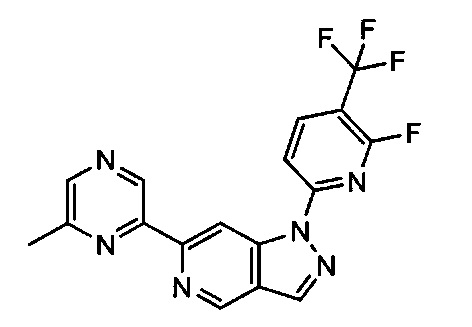
К смеси 6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридина (1,008 ммоль; 213,0 мг) в диметилформамиде (10 мл) при 0°С добавляли гидрид натрия (60% в минеральном масле; 1,210 ммоль; 48,40 мг). Полученную в результате смесь перемешивали в течение 10 минут. Затем добавляли 2,6-дифтор-3-(трифторметил)пиридин (1,008 ммоль; 184,6 мг). Реакционную смесь перемешивали и нагревали до комнатной температуры, и перемешивали в течение 4 часов. Смесь гасили водой и экстрагировали ЕtOАс. Органический слой промывали солевым раствором и затем концентрировали. Остаток очищали на силикагеле, элюируя 0 до 100% EtOAc в гептане. 1-[6-Фтор-5-(трифторметил)-2-пиридил]-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин получали в виде преобладающего изомера (173,6 мг, 46%).
Стадия В: трет-бутил N-[(3S)-1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-3-(трифторметил)-2-пиридил]-3-пиперидил]карбамат
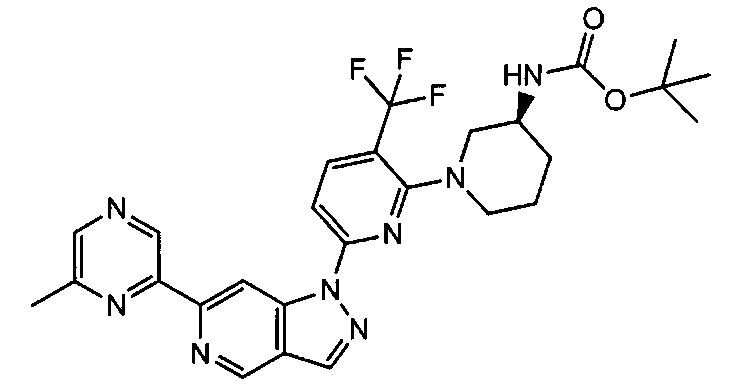
Смесь 1-[6-хлор-5-(трифторметил)-2-пиридил]-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридина (0,0876 ммоль; 59,7 мг), трет-бутил N-[(3S)-3-пиперидил]карбамата (0,263 ммоль; 52,6 мг) и N-метилморфолина (0,263 ммоль; 26,9 мг; 0,0292 мл) в 1-метил-2-пирролидиноне (3 мл) в закрытом сосуде высокого давления нагревали при 120°С в течение ночи. Смесь выливали в воду и экстрагировали ЕtOАс. Органический слой концентрировали. Остаток очищали на силикагеле, элюируя 0 до 100% ЕtOАс в гептане, получая трет-бутил N-[(3S)-1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-3-(трифторметил)-2-пиридил]-3-пиперидил]карбамат в виде белого твердого вещества (37,0 мг, 65%).
Стадия С: Смесь трет-бутил N-[(3S)-1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-3-(трифторметил)-2-пиридил]-3-пиперидил]карбамата (0,0569 ммоль; 37,0 мг) в метаноле (5 мл) и хлороводороде, 4,0 М в 1,4-диоксане (5 мл), перемешивали при комнатной температуре в течение ночи. Смесь концентрировали и остаток очищали с помощью обращенно-фазовой ВЭЖХ, получая 220 в виде твердого вещества белого оттенка (31,0 мг, 81%). 1Н ЯМР (400 МГц, ДМСО) δ 9,67-9,63 (s, 1Н), 9,48-9,45 (S, 1Н), 9,36-9,33 (s, 1Н), 8,78-8,75 (s, 1Н), 8,65-8,62 (s, 1Н), 8,27-8,21 (d, J=8,5 Гц, 1Н), 7,71 -7,65 (d, J=8,5 Гц, 1Н), 3,76-3,62 (dd, J=24,1, 11,7 Гц, 2Н), 3,25-3,19 (d, J=11,2 Гц, 1Н), 2,95-2,80 (dd, J=24,6, 13,2 Гц, 2Н), 2,68 -2,63 (d, J=9,0 Гц, 3Н), 2,00- 1,88 (d, J=14,4 Гц, 2Н), 1,73- 1,63 (d, J=13,2 Гц, 1Н), 1,36-1,22 (dd, J=20,5, 8,6 Гц, 1Н); МС (ЭСИ) m/z: 455,1 [М+Н]+.
Пример 121 (5S)-5-амино-1-[3-метил-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-2-он 221
Стадия А: трет-бутил N-[(3S)-1-(6-хлор-3-метил-2-пиридил)-6-оксо-3-пиперидил]карбамат
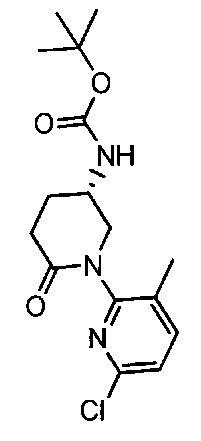
Раствор, содержащий 2-бром-6-хлор-3-метилпиридин (487 мг, 2,24 ммоль), трет-бутил N-[(3S)-6-оксо-3-пиперидил]карбамат (400 мг, 1,87 ммоль), иодид меди (I) (356 мг, 1,87 ммоль), карбонат калия (310 мг, 2,24 ммоль) и N,N'-диметилэтилендиамин (329 мг, 3,73 ммоль) в 12 мл диоксана, перемешивали при 110°С в течение 18 часов. Реакционную смесь фильтровали через целит и концентрировали. Неочищенный продукт очищали с помощью флэш-хроматографии (элюировали ЕtOАс/гептаном при 50% ЕtOАс), получая 350 мг требуемого продукта с выходом 38%. МС (ЭСИ) m/z: 340,1.
Стадия В: трет-бутил N-[(3S)-1-[3-метил-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-6-оксо-3-пиперидил]карбамат
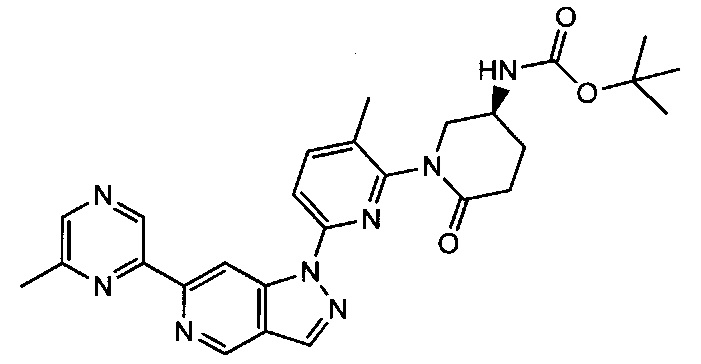
Смесь 6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридина (150 мг, 0,710 ммоль), трет-бутил N-[(3S)-1-(6-хлор-3-метил-2-пиридил)-6-оксо-3-пиперидил]карбамата (497 мг, 1,42 ммоль), трис(дибензилиденацетон)дипалладия (0) (65 мг, 0,071 ммоль), ксантфоса (84 мг, 0,14 ммоль) и трет-бутилата натрия (140 мг, 1,42 ммоль) в 3,0 мл толуола перемешивали при 110°С в течение 18 часов. Реакционную смесь фильтровали через целит. Неочищенный продукт очищали с помощью флэш-хроматографии (элюировали ЕtOАс/гептаном, затем МеОН/ДХМ при 10% МеОН), получая 75 мг требуемого продукта с выходом 20%. МС (ЭСИ) m/z: 515,1.
Стадия С: Раствор трет-бутил N-[(3S)-1-[3-метил-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-6-оксо-3-пиперидил]карбамата (63 мг, 0,12 ммоль) в хлороводороде (4 моль/л) в 1,4-диоксане (2,0 мл, 8,0 ммоль) и 2,0 мл 1,4-диоксана перемешивали при к.т.в течение 18 часов. Реакционную смесь концентрировали в вакууме. Неочищенный продукт подвергали обращенно-фазовой ВЭЖХ, получая 15 мг 221 с выходом 29%. МС (ЭСИ) m/z: 415,1. 1Н ЯМР (400 МГц, ДМСО) δ 9,61 (s, 1Н), 9,48 (s, 1Н), 9,35 (s, 1Н), 8,73 (s, 1Н), 8,64 (s, 1Н), 7,98 (d, J=8,2 Гц, 1Н), 7,93 (d, J=8,3 Гц, 1Н), 4,27 (s, 1Н), 3,86 (s, 1Н), 3,59 (d, J=33,7 Гц, 1Н), 3,40 (s, 1Н), 2,68 (t, J=18,2 Гц, 3Н), 2,20 (d, J=13,0 Гц, 3Н), 2,10 (s, 1Н), 1,85 (s, 2Н).
Пример 122 (3S)-1-[3-метокси-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]пиразин-2-ил]пиперидин-3-амин 222
Стадия А: трет-бутил N-[(3S)-1-[3-метокси-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]пиразин-2-ил]-3-пиперидил]карбамат
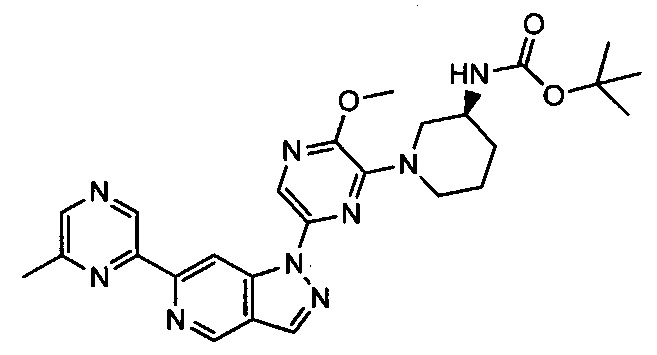
Смесь 6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридина (80 мг; 0,38 ммоль), трет-бутил N-[(3S)-1-(6-бром-3-метокси-пиразин-2-ил)-3-пиперидил]карбамата (181 мг, 0,4550 ммоль), трис(дибензилиденацетон)дипалладия (0) (35 мг, 0,038 ммоль), ксантфоса (45 мг, 0,076 ммоль) и трет-бутилата натрия (75 мг, 0,76 ммоль) в 3,0 мл толуола перемешивали при 110°С в течение 18 часов. Реакционную смесь фильтровали через целит. Неочищенный продукт очищали с помощью флэш-хроматографии (элюировали ЕtOАс/гептаном при 75% ЕtOАс), получая 112 мг требуемого продукта с выходом 57%. МС (ЭСИ) m/z: 518,1.
Стадия В: Раствор трет-бутил N-[(3S)-1-[3-метокси-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]пиразин-2-ил]-3-пиперидил]карбамата (75 мг, 0,15 ммоль) в 4,0 мл дихлорметана и трифторуксусную кислоту (0,80 мл, 10 ммоль) перемешивали при к.т.в течение 4 часов. Реакционную смесь концентрировали и подвергали обращенно-фазовой ВЭЖХ, получая 222 (25 мг) с выходом 41%. МС (ЭСИ) m/z: 418,2. 1Н ЯМР (400 МГц, ДМСО) δ 9,45 (s, 2Н), 9,32 (s, 1Н), 8,67 (s, 1Н), 8,63 (s, 1Н), 8,15 (s, 1Н), 4,24 (d, J=10,2 Гц, 1Н), 4,06 (d, J=13,3 Гц, 1Н), 4,00 (s, 3Н), 3,09 (dd, J=24,2, 12,0 Гц, 3Н), 2,63 (s, 3Н), 1,94 (d, J=15,0 Гц, 2H), 1,76 (d, J=10,0 Гц, 1H), 1,49 (d, J=10,0 Гц, 1H).
Пример 123 3-[(3S)-3-амино-1-пиперидил]-5-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]пиразин-2-ол 223
Раствор трет-бутил N-[(3S)-1-[3-метокси-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]пиразин-2-ил]-3-пиперидил]карбамата (30 мг, 0,058 ммоль) в хлороводороде (4 моль/л) в 1,4-диоксане (1,0 мл, 4,0 ммоль) и 1,0 мл 1,4-диоксана перемешивали при к.т.в течение 2 дней. Реакционную смесь концентрировали и подвергали обращенно-фазовой ВЭЖХ, получая 223 (7 мг, выход 27%). МС (ЭСИ) m/z: 404,1. 1Н ЯМР (400 МГц, ДМСО) 5 9,44 (s, 1Н), 9,28 (s, 1Н), 9,25 (s, 1Н), 8,61 (s, 1Н), 8,57 (s, 1Н), 7,23 (s, 1Н), 4,74 (d, J=11,1 Гц, 1Н), 4,44 (d, J=12,8 Гц, 1Н), 2,92 (s, 2Н), 2,62 (s, 3Н), 1,88 (d, J=16,7 Гц, 2Н), 1,68 (d, J=11,1 Гц, 1Н), 1,39 (d, J=9,5 Гц, 1Н).
Пример 124 1-(6-(1,4-Диазепан-1-ил)пиридин-2-ил)-6-(1-метил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин 224
Стадия А: трет-Бутил 4-(6-(6-хлор-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилат
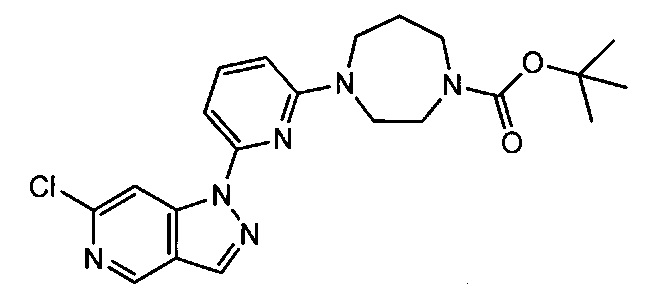
К смеси трет-бутил 4-(6-бромпиридин-2-ил)-1,4-диазепан-1-карбоксилата (2,55 г, 7,16 ммоль) из примера 45 и 6-хлор-1Н-пиразоло[4,3-с]пиридина (1,0 г, 6,51 ммоль) в 1,4-диоксане (20 мл) добавляли Cul (494 мг, 2,6 ммоль), К2СO3 (3,6 г, 26 ммоль) и N1,N2-диметилэтан-1,2-диамин (460 мг, 5,2 ммоль). Смесь нагревали при 100°С в течение 3 часов, контролируя с помощью ЖХМС. После завершения реакции реакционную смесь концентрировали при пониженном давлении. Неочищенное вещество очищали с помощью хроматографии на силикагеле, используя петролейный эфир/ЕtOАс (2/1) в качестве элюирующих растворителей, получая трет-бутил 4-(6-(6-хлор-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилат в виде желтого твердого вещества (1,6 г, 57%). МС (ЭСИ) m/z: 429 [М+Н]+.
Стадия В: трет-Бутил 4-(6-(6-(1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилат
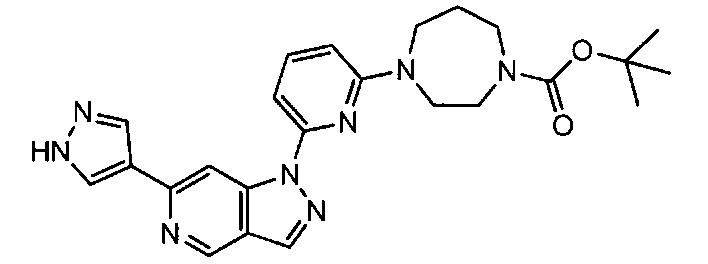
Суспензию трет-бутил 4-(6-(6-хлор-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилата (500 мг, 1,16 ммоль), 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразола (679 мг, 3,5 ммоль), Pd(dppf)Cl2 (47,5 мг, 0,058 ммоль) и водный раствор Na2CO3 (2,0 М, 3 мл) в 1,4-диоксане (10 мл) в атмосфере азота нагревали при 100°С в течение 16 часов. Реакционную смесь фильтровали и фильтрат концентрировали при пониженном давлении. Остаток очищали с помощью хроматографии на силикагеле, используя петролейный эфир/ЕtOАс (1/1) в качестве элюирующих растворителей, получая трет-бутил 4-(6-(6-(1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилат в виде желтого твердого вещества (360 мг, 67%). МС (ЭСИ) m/z: 461 [М+Н]+.
Стадия С: Раствор 4-(6-(6-(1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилата (440 мг, 0,93 ммоль) в растворе HCl/MeOH (2 М, 10 мл) перемешивали при комнатной температуре в течение 3 часов. Реакционную смесь концентрировали при пониженном давлении. Неочищенное вещество очищали с помощью обращенно-фазовой препаративной ВЭЖХ, получая 224 в виде желтого твердого вещества (180 мг, 51,8%). 1Н ЯМР (500 МГц, ДМСО-d6) δ (ppm) 9,095-9,098 (d, J=1,5 Гц, 1Н), 8,61 (s, 1Н), 8,45 (s, 1Н), 8,14 (s, 1Н), 7,87 (s, 1Н), 7,64-7,69 (t, J=13,5 Гц, 1Н), 7,13-7,16 (d, J=12,5 Гц, 1Н), 6,55-6,58 (d, J=14,5 Гц, 1Н), 3,90-3,91 (d, J=8 Гц, 3Н), 3,78-3,87 (m, 6Н), 3,01-3,05 (t, J=13 Гц, 2Н), 1,87-1,91 (m, 2Н); МС (ЭСИ) m/z: 375 [М+Н]+.
Пример 125 (3S)-3-амино-1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-2-он 225
Стадия А: трет-бутил N-[(3S)-1-[6-(6-хлорпиразоло[4,3-с]пиридин-1-ил)-2-пиридил]-2-оксо-3-пиперидил]карбамат
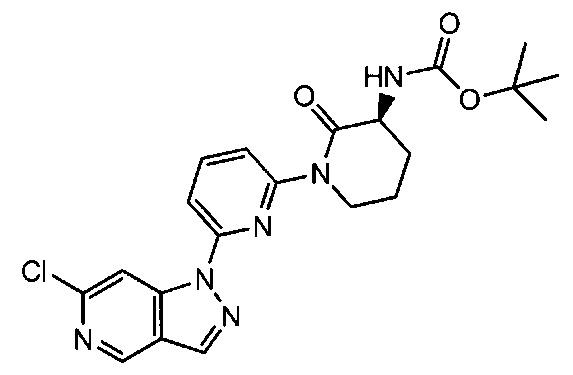
Раствор, содержащий 1-(6-бром-2-пиридил)-6-хлор-пиразоло[4,3-с]пиридин (200 мг, 0,646 ммоль), трет-бутил N-[(3S)-2-оксо-3-пиперидил]карбамат (166 мг, 0,775 ммоль), иодид меди (I) (123 мг, 0,646 ммоль), карбонат калия (107 мг, 0,775 ммоль) и N.N'-диметилэтилендиамин (114 мг, 1,29 ммоль), перемешивали при 110°С в течение 4 часов. Реакционную смесь фильтровали через целит и концентрировали. Неочищенный продукт очищали на колонке isco (элюировали ЕtOАс/геп при 70% ЕtOАс), получая 135 мг требуемого продукта с выходом 47%. МС (ЭСИ) m/z: 443,1.
Стадия В: трет-бутил N-[(3S)-1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-2-оксо-3-пиперидил]карбамат
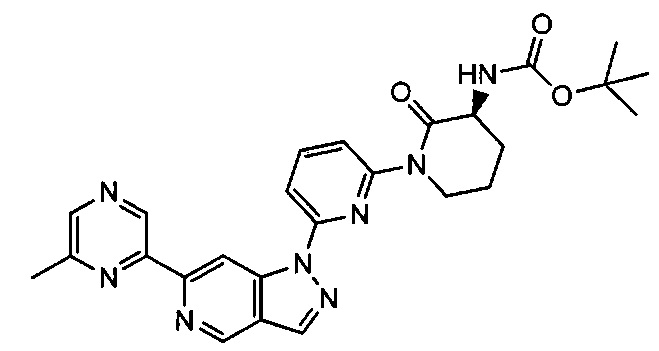
К раствору трет-бутил N-[(3S)-1-[6-(6-хлорпиразоло[4,3-с]пиридин-1-ил)-2-пиридил]-2-оксо-3-пиперидил]карбамата (125 мг, 0,282 ммоль) и тетракис(трифенилфосфин)палладия (0) (32 мг, 0,028 ммоль) в 5,0 мл N,N-диметилацетамида добавляли триметил-(6-метилпиразин-2-ил)станнан (145 мг, 0,565 ммоль). Реакционную смесь нагревали при 145°С в течение 40 минут в микроволновой печи СЕМ. Реакционную смесь фильтровали через целит и концентрировали. Неочищенный продукт разбавляли ЕtOАс, затем промывали водой. Органические слои сушили с сульфатом натрия, фильтровали и концентрировали в вакууме. Неочищенный продукт использовали на следующей стадии. МС (ЭСИ) m/z: 501,1.
Стадия С: Раствор трет-бутил N-[(3S)-1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-2-оксо-3-пиперидиЛ]карбамата (140 мг, 0,280 ммоль) в 4,0 мл дихлорметана и трифторуксусную кислоту (0,80 мл, 10 ммоль) перемешивали при к.т.в течение 3 часов. Реакционную смесь концентрировали и разбавляли водой, затем экстрагировали ЕtOАс. Водный слой подщелачивали 1 М NaOH до рН 10, затем экстрагировали ЕtOАс. Органические слои сушили с сульфатом натрия, фильтровали и концентрировали в вакууме. Неочищенный продукт подвергали обращенно-фазовой ВЭЖХ, получая 225 (44 мг, выход 39%). МС (ЭСИ) m/z: 401,1. 1Н ЯМР (400 МГц, ДМСО) δ 9,60 (s, 1Н), 9,47 (s, 1Н), 9,33 (s, 1Н), 8,72 (s, 1Н), 8,64 (s, 1Н), 8,05 (t, J=8,1 Гц, 1Н), 7,82 (d, J=8,0 Гц, 1Н), 7,74 (d, J=8,1 Гц, 1Н), 4,46-4,33 (m, 1Н), 4,14-4,02 (m, 1Н), 3,58 (dd, J=10,8, 6,4 Гц, 1Н), 2,65 (s, 3Н), 2,24 (dt, J=11,4, 5,3 Гц, 1Н), 2,19-2,00 (m, 2Н), 1,77 (ddd, J=23,0, 10,6, 5,1 Гц, 1Н).
Пример 126 (3S)-1-[3-хлор-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]пиразин-2-ил]пиперидин-3-амин 226
Стадия А: 3,5-дибром-2-хлор-пиразин
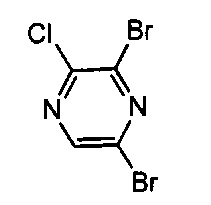
К раствору 3,5-дибромпиразин-2-амина (1,00 г, 3,95 ммоль) в 6,0 мл дихлорметана при 0°С добавляли тетрахлорид титана (1 моль/л) в дихлорметане (3,95 мл, 3,95 ммоль), затем добавляли по каплям трет-бутил нитрит (1,05 мл, 7,91 ммоль). Реакционную смесь нагревали до к.т., затем добавляли более 1 эквивалента TiCl4 и перемешивали в течение 1 часа. Реакцию гасили водой и экстрагировали ДХМ. Органические слои сушили с сульфатом натрия, фильтровали и концентрировали в вакууме. Неочищенный продукт использовали на следующей стадии. МС (ЭСИ) m/z: 272,2.
Стадия В: трет-бутил N-[(3S)-1-(6-бром-3-хлор-пиразин-2-ил)-3-пиперидил]карбамат
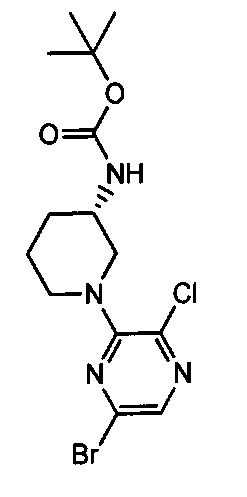
Раствор, содержащий 3,5-дибром-2-хлорпиразин (1,03 г, 3,60 ммоль) и трет-бутил н-[(3S)-3-пиперидил]карбамат (600 мг, 3,00 ммоль) в 5,0 мл метилсульфоксида, нагревали при 85°С.Реакцию гасили водой, затем экстрагировали ЕtOАс. Органические слои сушили с сульфатом натрия, фильтровали и концентрировали в вакууме. Неочищенный продукт очищали с помощью флэш-хроматографии (элюировали ЕtOАс/гептаном при 35% ЕtOАс), получая 350 мг требуемого продукта с выходом 30%. МС (ЭСИ) m/z: 393,2.
Стадия С: трет-бутил N-[(3S)-1-[3-хлор-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]пиразин-2-ил]-3-пиперидил]карбамат
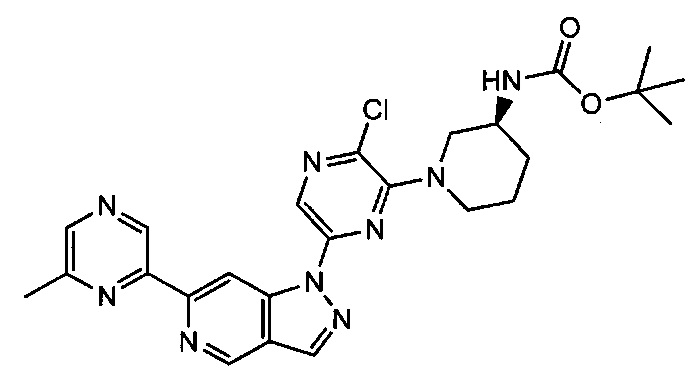
Смесь 6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридина (110 мг, 0,52 ммоль), трет-бутил N-[(3S)-1-(6-бром-3-хлор-пиразин-2-ил)-3-пиперидил]карбамата (252 мг, 0,62 ммоль), трис(дибензилиденацетон)дипалладия (0) (47 мг, 0,052 ммоль), ксантфоса (62 мг; 0,10 ммоль) и трет-бутилата натрия (103 мг, 1,04 ммоль) в 5,0 мл толуола перемешивали при 110°С в течение 18 часов. Реакционную смесь фильтровали через целит. Неочищенный продукт очищали с помощью флэш-хроматографии (элюировали ЕtOАс/гептаном при 75% ЕtOАс), получая 112 мг требуемого продукта с выходом 41%. МС (ЭСИ) m/z: 523,2.
Стадия D: Раствор трет-бутил N-[(3S)-1-[3-хлор-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]пиразин-2-ил]-3-пиперидил]карбамата (30 мг, 0,057 ммоль) в 4,0 мл дихлорметана и трифторуксусную кислоту (0,80 мл, 10 ммоль) перемешивали при к.т.в течение 3 часов. Реакционную смесь концентрировали и разбавляли водой, затем экстрагировали ЕtOАс. Водный слой подщелачивали 1 М NaOH до рН 10, затем экстрагировали ЕtOАс. Органические слои сушили с сульфатом натрия, фильтровали и концентрировали в вакууме. Неочищенный продукт подвергали обращенно-фазовой ВЭЖХ, получая 226 (12 мг, выход 49%). МС (ЭСИ) m/z: 422,1.
Пример 127 (S)-1-(3-(дифторметил)-6-(6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)пиперидин-3-амин 227
Стадия А: [2-фтор-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-3-пиридил]метанол
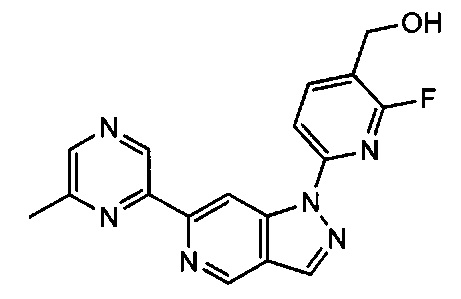
Смесь 6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридина (2,000 ммоль; 422,4 мг), (6-бром-2-фтор-3-пиридил)метанола (2,400 ммоль; 494,4 мг), карбоната калия (4,000 ммоль; 552,8 мг), иодида меди (I) (2,000 ммоль; 380,9 мг) и N,N'-диметилэтилендиамина (0,2000 ммоль; 17,81 мг; 0,0217 мл) в 1,4-диоксане (15 мл) продували аргоном, затем закрывали в пробирке высокого давления и нагревали при 105°С в течение ночи. Смесь охлаждали до комнатной температуры и фильтровали через Целит. Фильтрат концентрировали и остаток очищали на силикагеле, элюируя 0 до 100% ЕtOАс в гептане, получая [2-фтор-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-3-пиридил]метанол (79,5 мг, 12%).
Стадия В: 2-фтор-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]пиридин-3-карбальдегид
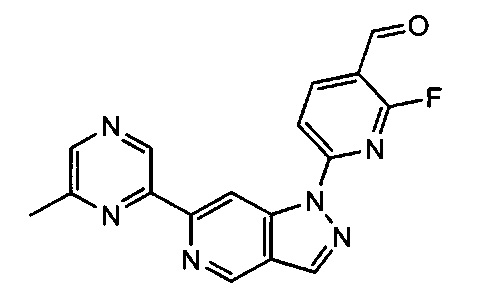
К [2-фтор-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-3-пиридил]метанолу (0,236 ммоль; 79,5 мг) в дихлорметане (10 мл) добавляли периодинан Десса-Мартина (0,355 ммоль; 155 мг). Смесь перемешивали при комнатной температуре в течение 4 часов. Смесь концентрировали и остаток очищали на силикагеле, элюируя 0 до 100% ЕtOАс в ДХМ, получая 2-фтор-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]пиридин-3-карбальдегид в виде светло-желтого твердого вещества (69,7 мг, 88%).
Стадия С: 1-[5-(дифторметил)-6-фтор-2-пиридил]-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин
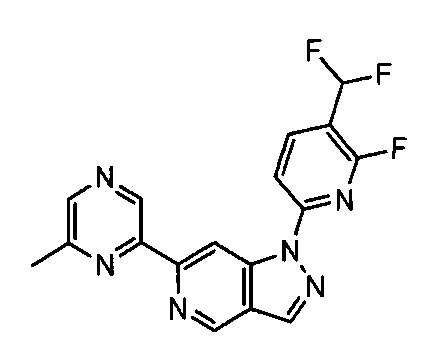
2-фтор-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]пиридин-3-карбальдегид (0,208 ммоль; 69,7 мг) растворяли в дихлорметане (10 мл) и охлаждали до 0°С.Медленно добавляли DEOXO-FLUOR® (1,04 ммоль; 231 мг; 0,19 мл) и смесь перемешивали при комнатной температуре в течение ночи. Смесь концентрировали и остаток очищали на силикагеле, элюируя 0 до 100% EtOAc в ДХМ, получая 1-[5-(дифторметил)-6-фтор-2-пиридил]-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин (34,8 мг, 47%).
Стадия D: трет-бутил N-[(3S)-1-[3-(дифторметил)-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-3-пиперидил]карбамат
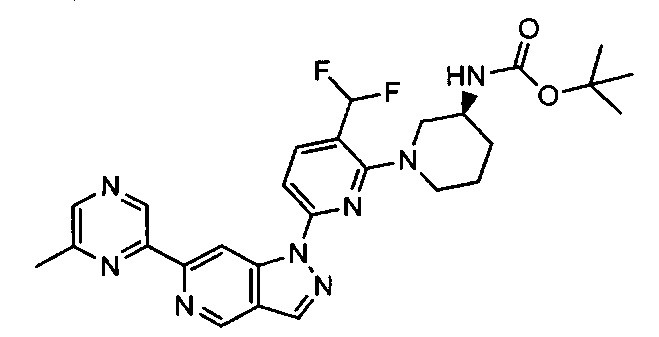
Смесь 1-[5-(дифторметил)-6-фтор-2-пиридил]-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридина (0,0977 ммоль; 34,8 мг), трет-бутил N-[(3S)-3-пиперидил]карбамата (0,147 ммоль; 29,3 мг) и N-метилморфолина (0,244 ммоль; 24,9 мг; 0,0271 мл) в 1-метил-2-пирролидиноне (3 мл) в закрытом сосуде высокого давления нагревали при 100°С в течение ночи. Смесь выливали в воду и экстрагировали EtOAc. Органический слой концентрировали. Остаток очищали на силикагеле, элюируя 0 до 100% ЕtOАс в ДХМ, получая трет-бутил N-[(3S)-1-[3-(дифторметил)-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-3-пиперидил]карбамат (~52,4 мг, 100%).
Стадия Е: Смесь трет-бутил N-[(3S)-1-[3-(дифторметил)-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-3-пиперидил]карбамата (0,0977 ммоль; 52,4 мг) в ТФК (1 мл) и дихлорметане (4 мл) перемешивали при комнатной температуре. Смесь концентрировали и остаток очищали с помощью обращенно-фазовой ВЭЖХ, получая 228 в виде твердого вещества белого оттенка (17,5 мг, 40%). 1Н ЯМР (400 МГц, ДМСО) δ 9,73-9,66 (s, 1H), 9,48-9,42 (s, 1H), 9,36-9,29 (s, 1H), 8,76-8,72 (s, 1H), 8,65-8,61 (d, J=4,9 Гц, 1H), 8,20-8,15 (d, J=8,4 Гц, 1H), 7,74-7,70 (d, J=8,3 Гц, 1H), 7,34-7,05 (t, J=54,2 Гц, 1H), 3,60-3,47 (dd, J=17,4, 12,4 Гц, 2H), 3,06-2,97 (t, J=8,3 Гц, 1H), 2,94-2,86 (dd, J=11,9, 8,2 Гц, 1H), 2,68-2,61 (s, 3Н), 1,98-1,86 (d, J=12,3 Гц, 2H), 1,86-1,67 (dd, J=16,0, 6,7 Гц, 2H), 1,41-1,31 (m, 1H); МС (ЭСИ) m/z: 437,1 [М+Н]+.
Пример 128 (3S)-1-[3-метил-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]пиразин-2-ил]пиперидин-3-амин 228
Стадия А: трет-бутил N-[(3S)-1-[3-метил-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]пиразин-2-ил]-3-пиперидил]карбамат
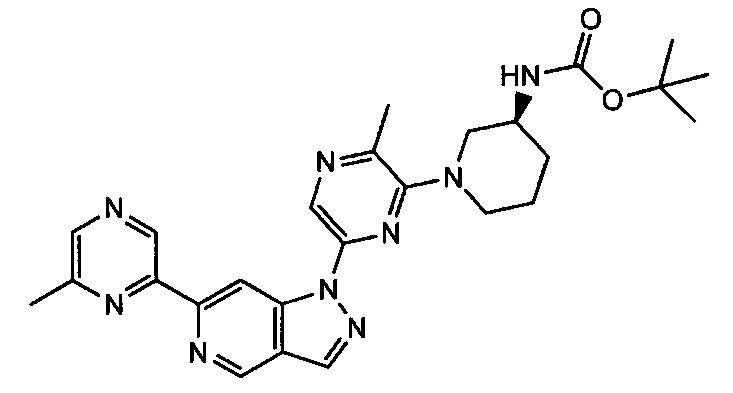
К раствору трет-бутил N-[(3S)-1-[3-хлор-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]пиразин-2-ил]-3-пиперидил]карбамата (50 мг, 0,096 ммоль), триметилбороксина (36 мг, 0,29 ммоль) и аддукта [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладия (II) дихлорметана (8,0 мг, 0,0095 ммоль) в 2,0 мл ацетонитрила добавляли 1,00 М карбонат натрия в воде (0,19 мл, 0,19 ммоль) и 1,00 М ацетат калия в воде (0,19 мл, 0,19 ммоль). Реакционную смесь нагревали в микроволновой печи при 140°С в течение 40 минут. Реакционную смесь фильтровали через целит. Неочищенный продукт очищали с помощью флэш-хроматографии (элюировали ЕtOАс/гептаном при 80% ЕtOАс), получая 34 мг требуемого продукта с выходом 70%. МС (ЭСИ) m/z: 502,2.
Стадия В: Раствор трет-бутил N-[(3S)-1-[3-метил-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]пиразин-2-ил]-3-пиперидил]карбамата (34 мг, 0,068 ммоль) в хлороводороде (4 моль/л) в 1,4-диоксане (2,0 мл, 8,0 ммоль) и 2,0 мл 1,4-диоксана перемешивали при к.т.в течение 18 часов. Неочищенный продукт подвергали обращенно-фазовой ВЭЖХ, получая 228 (15 мг, выход 56%). МС (ЭСИ) m/z: 402,2. 1Н ЯМР (400 МГц, ДМСО) δ 9,58 (s, 1Н), 9,44 (s, 1Н), 9,32 (s, 1Н), 8,71 (s, 1Н), 8,66 (s, 1Н), 8,63 (s, 1Н), 3,67 (d, J=12,3 Гц, 2Н), 3,19 (t, J=11,3 Гц, 1Н), 2,93 (s, 1Н), 2,73 (dd, J=12,1, 9,1 Гц, 1Н), 2,64 (s, 3Н), 2,54 (s, 3Н), 1,94 (d, J=10,2 Гц, 2Н), 1,74 (d, J=11,1 Гц, 1Н), 1,39-1,26 (m, 1Н).
Пример 129 (R)-1-(6-(6-(1-Метил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-6-ол 229
Следуя способам, описанным в примере 124, и начиная с 1,4-диазепан-6-ола, 2-бром-6-фторпиридина, 6-хлор-1Н-пиразоло[4,3-с]пиридина и 1-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразола, получали 229 в виде желтого твердого вещества (40 мг, 24,1%) за шесть стадий. 1Н ЯМР (500 МГц, ДМСО-d6) δ (ррm) 9,09 (s, 1Н), 8,65 (s, 1Н), 8,44 (s, 1Н), 8,25 (s, 1Н), 7,98 (s, 1Н), 7,63-7,68 (m, 1Н), 7,14-7,16 (d, J=12,5 Гц, 1Н), 6,61-6,64 (d, J=14 Гц, 1Н), 4,10-4,14 (m, 1Н), 3,86-3,91 (m, 6Н), 3,55-3,66 (m, 2Н), 2,98-3,04 (m, 3Н), 2,84-2,90 (m, 1Н), 2,69-2,71 (m, 1Н); МС (ЭСИ) m/z: 391 [М+Н]+.
Пример 130 4-(6-(6-(1-Метил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)азепан-4-ол 230
Раствор трет-бутил 4-гидрокси-4-(6-(6-(1-метил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)азепан-1-карбоксилата (200 мг, 0,41 ммоль) в растворе HCl в МеОН (2,0 М, 10 мл) перемешивали при комнатной температуре в течение 1 часа, контролируя с помощью ЖХМС. После завершения реакции реакционную смесь концентрировали при пониженном давлении. Неочищенное вещество очищали с помощью обращенно-фазовой препаративной ВЭЖХ, получая 230 в виде светло-желтого твердого вещества (30 мг, 31%). 1Н ЯМР (500 МГц, CDCl3) δ (ррm) 9,06 (s, 1Н), 8,85 (s, 1Н), 8,26 (s, 1Н), 8,06 (s, 1Н), 8,03 (s, 1Н), 7,88-7,89 (d, J=4,5 Гц, 2Н), 7,56-7,58 (t, J=9 Гц, 1Н), 4,00 (s, 3Н), 3,31-3,38 (m, 2Н), 3,10-3,13 (t, J=13 Гц, 1Н), 2,81-2,83 (t, J=12 Гц, 1Н), 2,37-2,46 (m, 3Н), 2,10-2,17 (m, 4Н), 1,82-1,85 (t, J=14,5 Гц, 1Н); МС (ЭСИ) m/z: 390 [М+Н]+.
Пример 131 (S)-1-(6-(6-(1-Метил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-6-ол 231
Следуя способам, описанным в примере 124, и начиная с 1,4-диазепан-6-ола, 2-бром-6-фторпиридина, 6-хлор-1Н-пиразоло[4,3-с]пиридина и 1-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразола, получали 231 в виде желтого твердого вещества (43 мг, 23,5%) за шесть стадий. 1Н ЯМР (500 МГц, ДМСО-d6) δ (ррm) 9,09 (s, 1Н), 8,65 (s, 1Н), 8,44 (s, 1Н), 8,25 (s, 1Н), 7,98 (s, 1Н), 7,63-7,68 (m, 1Н), 7,14-7,16 (d, J=12,5 Гц, 1Н), 6,61-6,64 (d, J=14 Гц, 1Н), 4,10-4,14 (m, 1Н), 3,86-3,91 (m, 6Н), 3,55-3,66 (m, 2Н), 2,98-3,04 (m, 3Н), 2,84-2,90 (m, 1Н), 2,69-2,71 (m, 1Н); МС (ЭСИ) m/z: 391 [М+Н]+.
Пример 132 1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пирролидин-3,4-диол 232
Следуя способам получения в примере 23, получали 232. МС (ЭСИ) m/z: 390,1. 1Н ЯМР (400 МГц, ДМСО) δ 9,94 (s, 1Н), 9,46 (s, 1Н), 9,31 (s, 1Н), 8,64 (d, J=8,1 Гц, 2Н), 7,71 (t, J=8,0 Гц, 1Н), 7,19 (d, J=7,7 Гц, 1Н), 6,42 (d, J=8,3 Гц, 1Н), 5,23 (d, J=3,1 Гц, 2Н), 4,18 (s, 2Н), 2,66 (s, 3Н).
Пример 133 (S)-3-(3-аминопиперидин-1-ил)-1-метил-5-(6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2(1Н)-он 233
Стадия А: трет-бутил N-[(3S)-1-(5-бром-1-метил-2-оксо-3-пиридил)-3-пиперидил]карбамат
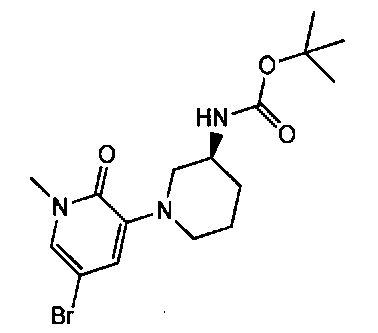
Смесь 3,5-дибром-1-метил-пиридин-2-она (2,000 ммоль; 533,8 мг), трет-бутил N-[(38)-3-пиперидил]карбамата (2,00 ммоль; 401 мг), карбоната цезия (4,0 ммоль; 1303 мг), ксантфоса (0,3400 ммоль; 202,8 мг) и трис(дибензилиденацетон)дипалладия (0) (0,2000 ммоль; 185,0 мг) в 1,4-диоксане (10 мл) продували аргоном, затем закрывали и перемешивали при 110°С в течение ночи. Смесь охлаждали до комнатной температуры и фильтровали через Целит. Фильтрат концентрировали и остаток очищали на силикагеле, элюируя 0 до 100% ЕtOАс в гептане, получая трет-бутил N-[(3S)-1-(5-бром-1-метил-2-оксо-3-пиридил)-3-пиперидил]карбамат в виде желтого твердого вещества (458,6 мг, 59%).
Стадия В: трет-бутил N-[(3S)-1-[1-метил-5-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-оксо-3-пиридил]-3-пиперидил]карбамат
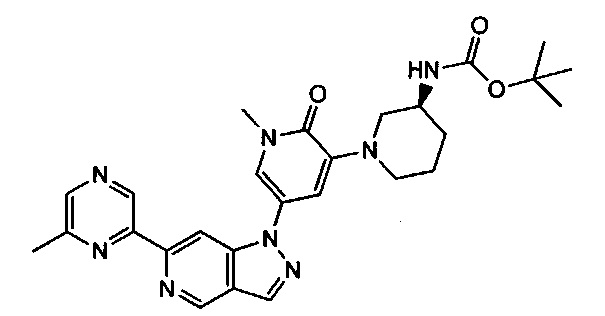
Смесь 6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридина (0,49711 ммоль; 105 мг), трет-бутил N-[(3S)-1-(5-бром-1-метил-2-оксо-3-пиридил)-3-пиперидил]карбамата (0,59653 ммоль; 230,4 мг), N,N'-диметилэтилендиамина (0,049711 ммоль; 4,382 мг; 0,00495 мл), иодида меди (0,49711 ммоль; 95,629 мг) и карбоната калия (0,99422 ммоль; 138,79 мг) в 1,4-диоксане (10 мл) продували аргоном, затем закрывали и перемешивали при 100°С в течение ночи. Смесь охлаждали до комнатной температуры и затем фильтровали через Целит. Фильтрат концентрировали; остаток очищали на силикагеле, элюируя 0 до 6% МеОН в ДХМ, получая трет-бутил N-[(3S)-1-[1-метил-5-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-оксо-3-пиридил]-3-пиперидил]карбамат (116, мг, 45%).
Стадия С: Смесь трет-бутил N-[(3S)-1-[1-метил-5-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-оксо-3-пиридил]-3-пиперидил]карбамата (0,2245 ммоль; 116,0 мг) в ТФК (1 мл) и дихлорметана (4 мл) перемешивали при комнатной температуре в течение ночи. Смесь концентрировали и остаток очищали с помощью обращенно-фазовой ВЭЖХ, получая 233 в виде твердого вещества белого оттенка (51,6 мг, 54%). 1Н ЯМР (400 МГц, ДМСО) δ 9,47-9,40 (S, 1Н), 9,36-9,30 (S, 1Н), 8,66-8,57 (s, 2Н), 8,48-8,40 (s, 1Н), 7,96-7,90 (d, J=2,5 Гц, 1Н), 6,96-6,90 (d, J=2,5 Гц, 1H), 3,69-3,61 (d, J=6,6 Гц, 2H), 3,58-3,52 (s, 3Н), 2,83-2,72 (t, J=9,7 Гц, 1H), 2,63-2,58 (s, 3Н), 2,30-2,23 (m, 1Н), 1,88 -1,81 (d, J=9,0 Гц, 1H), 1,74-1,68 (d, J=13,3 Гц, 1H), 1,63-1,53 (d, J=12,8 Гц, 1H), 1,18-1,06 (m, 1Н); МС (ЭСИ) m/z: 417,2 [М+Н]+.
Пример 134 (R)-1-(3-Метокси-6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло-[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-6-ол 234
Следуя способам, описанным в примере 88, и начиная с 6-бром-2-фтор-3-метоксипиридина и 1,4-диазепан-6-ола, получали 234 в виде желтого твердого вещества (40 мг, 16,5%) в ходе шести стадий. 1Н ЯМР (500 МГц, ДМСО-d6) δ (ppm) 9,14 (s, 1Н), 8,60 (s, 1Н), 8,50 (s, 1Н), 8,46 (s, 1Н), 8,18 (s, 1Н), 7,42 (d, J=8,5 Гц, 1Н), 7,24 (d, J=8,5 Гц, 1Н), 5,19-5,24 (m, 2Н), 4,81 (s, 1Н), 4,16-4,20 (m, 1Н), 3,98-4,02 (m, 2Н), 3,96 (s, 3Н), 3,50-3,54 (m, 2Н), 2,94-3,02 (m, 2Н), 2,85-2,87 (m, 1Н), 2,71-2,75 (m, 1Н); МС (ЭСИ) m/z: 489 [М+Н]+.
Пример 135 1-(6-(азепан-4-ил)пиридин-2-ил)-6-(1-метил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин 235
Стадия А: трет-Бутил 4-(6-бромпиридин-2-ил)-4-гидроксиазепан-1-карбоксилат
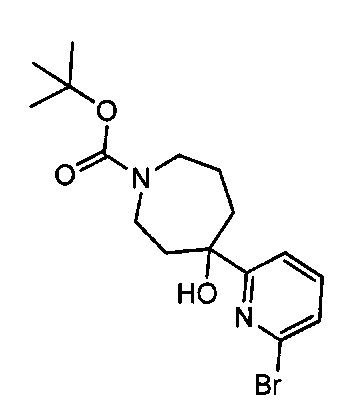
К раствору 2,6-дибромпиридина (0,2 г, 0,84 ммоль) в Et20 (20 мл) при -78°С добавляли 2,5 М раствор н-BuLi в гексане (3,7 мл, 0,928 ммоль) в течение 30 минут.Смесь перемешивали при -78°С в течение 30 минут.К ней добавляли по каплям трет-бутил 4-оксоазепан-1-карбоксилат (180 мг, 084 ммоль) в Et20 (20 мл) в течение 15 минут.Затем смесь перемешивали в течение одного часа, к ней добавляли Н20 (100 мл). Водный слой экстрагировали ЕtOАс (100 мл х 2). Объединенные органические слои промывали 10% раствором NaOH и солевым раствором, сушили над MgS04, концентрировали при пониженном давлении. Неочищенный продукт очищали с помощью хроматографии на силикагеле, используя петролейный эфир/ЕtOАс (9:1) в качестве элюирующих растворителей, получая трет-бутил 4-(6-бромпиридин-2-ил)-4-гидроксиазепан-1-карбоксилат в виде масла (200 мг, 62,5%). МС (ЭСИ) m/z: 371 [М+Н]+.
Стадия В: трет-Бутил 4-(6-(6-хлор-1Н-пиразоло[4,3-с]пиридин-1-
ил)пиридин-2-ил)-4-гидроксиазепан-1-карбоксилат
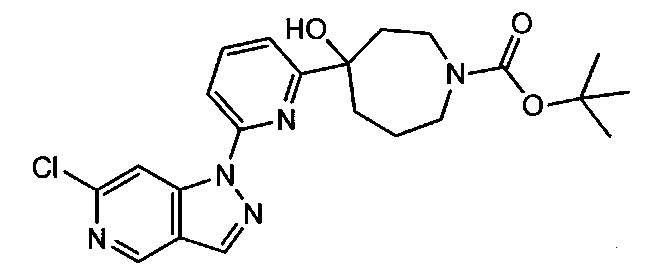
К смеси трет-бутил 4-(6-бромпиридин-2-ил)-4-гидроксиазепан-1-карбоксилата (792 мг, 2,4 ммоль) и 6-хлор-1Н-пиразоло[4,3-с]пиридина (300 мг, 1,94 ммоль) в 1,4-диоксане (20 мл) добавляли Cut (150 мг, 0,78 ммоль), К2С03 (1,08 г, 7,8 ммоль) и М1,№-диметилэтан-1,2-диамин (138 мг, 1,56 ммоль). Смесь нагревали при 100°С в течение 3 часов, контролируя с помощью ЖХМС.После завершения реакции реакционную смесь концентрировали при пониженном давлении. Неочищенное вещество очищали с помощью хроматографии на силикагеле, используя петролейный эфир/ЕtOАс (4/1), получая трет-бутил 4-(6-(6-хлор-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)-4-гидроксиазепан-1 -
5
177
карбоксилат в виде белого твердого вещества (550 мг, 58%). МС (ЭСИ) т/г.444 [М+Н]+.
Стадия С: трет-Бутил 4-гидрокси-4-(6-(6-(1-метил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]-пиридин-1-ил)пиридин-2-ил)азепан-1-карбоксилат
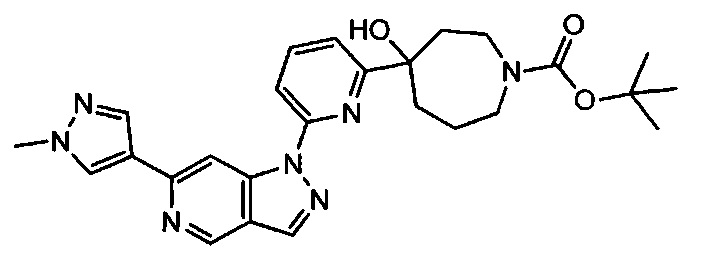
Суспензию трет-бутил 4-(6-(6-хлор-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-4-гидроксиазепан-1-карбоксилата (500 мг, 1,12 ммоль), 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразола (350 мг, 1,69 ммоль), Pd(dppf)CI2 (50 мг, 0,06 ммоль) и водного раствора Na2C03 (2,0 М, 2,0 мл) в 1,4-диоксане (30 мл) в атмосфере азота перемешивали при 100°С в течение 18 часов. Реакционную смесь фильтровали и фильтрат концентрировали при пониженном давлении. Остаток очищали с помощью хроматографии на силикагеле, используя петролейный эфир/ЕtOАс (2/1) в качестве элюирующих растворителей, получая трет-бутил 4-гидрокси-4-(6-(6-(1-метил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)азепан-1-карбоксилат в виде желтого масла (500 мг, 91%). МС (ЭСИ) т/г.490 [М+Н]+.
Стадия D: Смесь трет-бутил 4-гидрокси-4-(6-(6-(1-метил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)азепан-1-карбоксилата (140 мг, 0,29 ммоль) и SOCI2 (10 мл) перемешивали при комнатной температуре в течение 24 часов. Реакционную смесь концентрировали при пониженном давлении. К остатку добавляли МеОН (10 мл) и 10% Pd/C (0,1 г). Смесь перемешивали в атмосфере водорода (40 пси) при комнатной температуре в течение 5 часов, контролируя с помощью ЖХМС.После завершения реакции смесь фильтровали через Целит и фильтрат концентрировали при пониженном давлении. Неочищенное вещество очищали с помощью обращенно-фазовой препаративной ВЭЖХ, получая соль формиата 235 в виде светло-желтого твердого вещества (8 мг, 7,4%). 1Н ЯМР (500 МГц, ДМСО-с/6) 5 (ppm) 9,15 (s, 1Н), 8,75 (s, 1Н), 8,58 (s, 1Н), 8,416-8,421 (d, J=2,5 Гц, 1Н), 8,31 (s, 1Н), 8,01 (s, 1Н), 7,96-7,99 (t, J=15,5 Гц, 1Н), 7,82-7,83 (d, J=8 Гц, 1Н), 7,26-7,28 (d, J=7 Гц, 1Н), 4,08-4,22 (m, 3Н), 3,13-3,31 (m, 6Н), 2,24 (s, 1Н), 2,17-2,19 (d, J=7,5 Гц, 2Н), 1,96-2,03 (m, 3Н); МС (ЭСИ) т/г.374 [М+Н]+.
Пример 136 1-(6-(4-Фторазепан-4-ил)пиридин-2-ил)-6-(1-метил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридина формиат 236
178
Стадия А: 1-(6-(4-Фторазепан-4-ил)пиридин-2-ил)-6-(1-метил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин
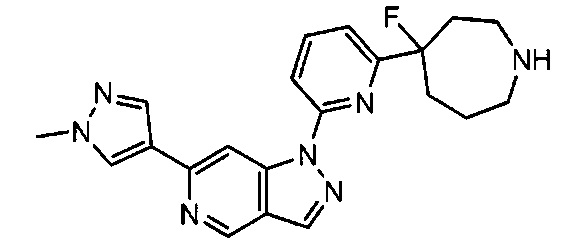
К раствору трет-бутил 4-гидрокси-4-(6-(6-(1-метил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)азепан-1-карбоксилата (150 мг, 0,3 ммоль) в ДХМ (5 мл) добавляли диэтиламиносеры трифторид (ДАСТ, 0,12 мл, 0,9 ммоль). Смесь перемешивали при комнатной температуре в течение 1 часа, контролируя с помощью ЖХМС.После завершения реакции ее концентрировали при пониженном давлении, получая 1-(6-(4-фторазепан-4-ил)пиридин-2-ил)-6-(1-метил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин в виде светло-желтого масла (130 мг, 87%). МС (ЭСИ) m/z: 493 [М+Н]+.
Стадия В: Раствор 1-(6-(4-фторазепан-4-ил)пиридин-2-ил)-6-(1-метил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридина (120 мг, 0,24 ммоль) в растворе HCI в МеОН (2,0 М, 10 мл) перемешивали при комнатной температуре в течение 1 часа. Реакционную смесь концентрировали при пониженном давлении. Неочищенное вещество очищали с помощью обращенно-фазовой препаративной ВЭЖХ, получая соль формиата 236 в виде светло-желтого твердого вещества (18 мг, 18,9%). 1Н ЯМР (500 МГц, ДМСО-сУ6) 6 (ррт) 9,17 (s, 1Н), 8,68 (s, 1Н), 8,62 (s, 1Н), 8,39 (s, 1Н), 8,33 (s, 1Н), 8,10-8,13 (t, J=16 Гц, 1Н), 8,07 (s, 1Н), 7,95-7,97 (d, J=8,5 Гц, 1Н), 7,50-7,51 (d, J=8 Гц, 1Н), 3,93 (s, 3Н), 3,07-3,29 (m, 4Н), 2,64-2,66 (t, J=10,5 Гц, 2Н), 2,22-2,30 (m, 2Н), 2,05-2,06 (t, J=6 Гц, 1Н), 1,92 (s, 1Н); МС (ЭСИ) m/z: 392 [М+Н]+.
Пример 137 (8)-1-(3-Метокси-6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло-[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-6-ол 237
Следуя способам, описанным в примере 88, и начиная с 6-бром-2-фтор-3-метоксипиридина и 1,4-диазепан-6-ола, получали 237 в виде желтого твердого вещества (40 мг, 16,3%) в ходе шести стадий. 1Н ЯМР (500 МГц, ДМСО-Ое) 6 (ррт) 9,14 (s, 1Н), 8,60 (s, 1Н), 8,50 (s, 1Н), 8,46 (s, 1Н), 8,18 (s, 1Н), 7,42 (d, J=8,5 Гц, 1Н), 7,24 (d, J=8,5 Гц, 1Н), 5,18-5,24 (m, 2Н), 4,80 (s, 1Н), 4,16-4,20 (m, 1Н), 3,98-4,02 (m, 2Н), 3,96 (s, 3Н), 3,50-3,54 (m, 2Н), 2,94-3,02 (m, 2Н), 2,84-2,87 (m, 1Н), 2,71-2,75 (m, 1Н); МС (ЭСИ) т/г.489 [М+Н]+.
Пример 138 (3S)-1 -[3-циклопропил-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]пиразин-2-ил]пиперидин-3-амин 238
179
Следуя способам получения в примере 128, получали 238. МС (ЭСИ) m/z: 428,2. 1Н ЯМР (400 МГц, ДМСО) δ 9,61 (s, 1Н), 9,45 (s, 1Н), 9,33 (s, 1Н), 8,71 (s, 1Н), 8,63 (s, 1Н), 8,62 (s, 1Н), 3,86 (d, J=9,5 Гц, 1Н), 3,74 (d, J=11,9 Гц, 1Н), 2,98 (d, J=9,0 Гц, 1Н), 2,86-2,76 (гл, 1Н), 2,65 (s, 3Н), 2,25 (t, J=8,9 Гц, 1Н), 1,96 (d, J=10,1 Гц, 2Н), 1,83-1,64 (m, 2Н), 1,34 (d, J=9,9 Гц, 1Н), 1,09 (ddd, J=24,4, 12,6, 5,7 Гц, 4Н).
Пример 140 6-(6-метилпиразин-2-ил)-1 -(6-(4-(оксетан-3-ил)-1,4-диазепан-1-ил)пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридин 240
Стадия А: 6-хлор-1 -[6-[4-(оксетан-3-ил)-1,4-диазепан-1 -ил]-2-пиридил]пиразоло[4,3-с]пиридин
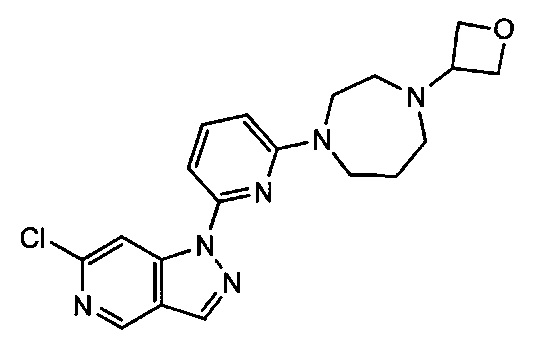
Смесь 6-хлор-1-[6-(1,4-диазепан-1-ил)-2-пиридил]пиразоло[4,3-с]пиридина (0,4094 ммоль; 134,6 мг), оксетан-3-она (0,4912 ммоль; 35,40 мг) и молекулярных сит (4 А) в 1,2-дихлорэтане (12 мл) перемешивали при комнатной температуре в течение 4 часов. Добавляли STAB (0,6141 ммоль; 137,0 мг). Реакционную смесь перемешивали в течение 3 дней. Смесь фильтровали через Целит.Фильтрат концентрировали и остаток очищали на силикагеле, элюируя 0 до 5% МеОН в ДХМ, получая 6-хлор-1-[6-[4-(оксетан-3-ил)-1,4-диазепан-1-ил]-2-
пиридил]пиразоло[4,3-с]пиридин (99,2 мг, 63%).
Стадия В: Смесь триметил-(6-метилпиразин-2-ил)станнана (0,387 ммоль; 99,3 мг), 6-хлор-1-[6-[4-(оксетан-3-ил)-1,4-диазепан-1-ил]-2-пиридил]пиразоло[4,3-с]пиридина (0,258 ммоль; 99,2 мг) и тетракис(трифенилфосфин)палладия (0) (0,0258 ммоль; 29,8 мг) в N,N-диметилацетамиде (3 мл) продували аргоном. Реакционную смесь закрывали в сосуде высокого давления Biotage и нагревали при 150°С в микроволновой печи в течение 45 минут.Смесь фильтровали через Целит.Фильтрат концентрировали и остаток очищали на силикагеле, элюируя 0 до 10% МеОН в ДХМ. Вещество дополнительно очищали с помощью обращенно-фазовой ВЭЖХ, получая 240 в виде твердого вещества белого оттенка (23,3 мг, 20%). 1Н ЯМР (400 МГц, ДМСО) 5 9,66-9,61 (s, 1Н), 9,47-9,44 (s, 1Н), 9,33-9,30 (s, 1Н), 9,06-9,03 (s, ОН), 8,67-8,60 (m, 2Н), 8,52-8,50 (s, 1Н), 7,76-7,68 (td, J=8,1, 3,4 Гц, 2Н), 7,25-7,20 (d,
180
J=7,7 Гц, 1H), 7,17-7,13 (d, J=7,7 Гц, 1H), 6,66-6,59 (dd, J=8,3, 6,0 Гц, 2H), 4,55-4,46 (m, 3Н), 4,41-4,33 (dt, J=15,0, 6,0 Гц, 3Н), 3,98-3,86 (d, J=5,5 Гц, 4H), 3,81-3,73 (m, 2H), 3,67-3,60 (dt, J=11,7, 5,8 Гц, 2H), 2,67-2,63 (s, 2H), 2,62-2,59 (s, 3Н), 2,41-2,36 (dd, J=11,3, 6,0 Гц, 3Н), 2,05-1,93 (dt, J=18,5, 6,1 Гц, 3Н); МС (ЭСИ) m/z: 443,2 [М+Н]+.
Пример 141 (8)-3-(3-аминопиперидин-1 -ил)-1 -метил-5-(6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиразин-2(1Н)-он 241
Стадия А: трет-бутил М-[(38)-1-(6-бром-4-метил-3-оксо-пиразин-2-ил)-3-пиперидил]карбамат
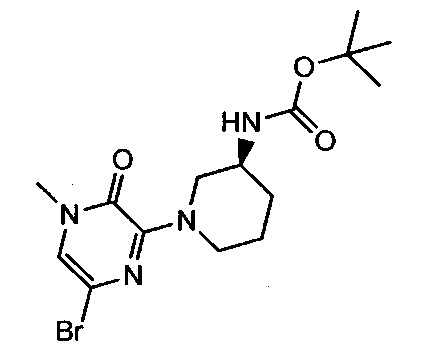
Смесь 3,5-дибром-1-метил-пиразин-2-она (2,025 ммоль; 542,4 мг), трет-бутил М-[(38)-3-пиперидил]карбамата (2,025 ммоль; 405,5 мг), карбоната цезия (4,049 ммоль; 1319 мг), ксантфоса (0,1721 ммоль; 102,7 мг) и трис(дибензилиденацетон)дипалладия (0) (0,1012 ммоль; 93,63 мг) в 1,4-диоксане (10 мл) продували аргоном, затем закрывали и перемешивали при 110°С в течение ночи. Смесь охлаждали до комнатной температуры и фильтровали через Целит.Фильтрат концентрировали и остаток очищали на силикагеле, элюируя 0 до 20% ЕtOАс в ДХМ, получая трет-бутил 1\1-[(38)-1-(6-бром-4-метил-3-оксо-пиразин-2-ил)-3-пиперидил]карбамат в виде желтого твердого вещества (451,0 мг, 58%).
Стадия В: трет-бутил г>1-[(38)-1-[4-метил-6-[6-(6-метилпиразин-2-
ил)пиразоло[4,3-с]пиридин-1-ил]-3-оксо-пиразин-2-ил]-3-пиперидил]карбамат 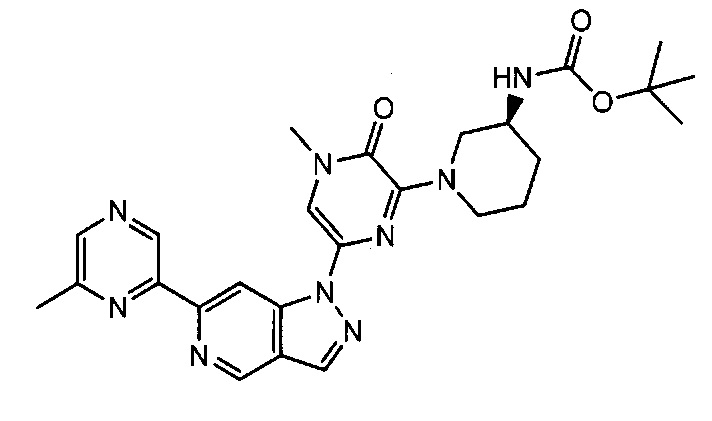
Смесь 6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридина (0,49711 ммоль; 105 мг), трет-бутил г>1-[(38)-1-(6-бром-4-метил-3-оксо-пиразин-2-ил)-3-пиперидил]карбамата (0,6016 ммоль; 233 мг), г>1,М'-диметилэтилендиамина (0,049711 ммоль; 4,382 мг; 0,00495 мл), иодида меди (0,49711 ммоль; 95,629 мг) и карбоната калия (0,99422 ммоль; 138,79 мг) в 1,4-диоксане (10 мл) продували аргоном, затем закрывали и перемешивали при 100°С в течение ночи. Смесь охлаждали до комнатной температуры и затем фильтровали через Целит.Фильтрат концентрировали; остаток очищали на силикагеле, элюируя 0 до % МеОН в ДХМ, получая трет-бутил 1^-[(38)-1-[4-метил-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-3-оксо-пиразин-2-ил]-3-пиперидил]карбамат (181,4 мг, 70%).
Стадия С: Смесь трет-бутил М-[(38)-1-[4-метил-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-3-оксо-пиразин-2-ил]-3-пиперидил]карбамата (0,3505 ммоль; 181,4 мг) в ТФК (1 мл) и дихлорметане (4 мл) перемешивали при комнатной температуре в течение ночи. Смесь концентрировали и остаток очищали с помощью обращенно-фазовой ВЭЖХ, получая 241 в виде твердого вещества белого оттенка (28,1 мг, 18%). 1Н ЯМР (400 МГц, ДМСО) δ 9,47-9,40 (s, 1Н), 9,36-9,30 (s, 1Н), 8,66-8,57 (s, 2Н), 8,48-8,40 (s, 1Н), 7,96-7,90 (d, J=2,5 Гц, 1Н), 6,96-6,90 (d, J=2,5 Гц, 1Н), 3,69-3,61 (d, J=6,6 Гц, 2Н), 3,58-3,52 (s, 3Н), 2,83-2,72 (t, J=9,7 Гц, 1Н), 2,63-2,58 (s, 3Н), 2,30-2,23 (m, 1Н), 1,88 -1,81 (d, J=9,0 Гц, 1Н), 1,74-1,68 (d, J=13,3 Гц, 1Н), 1,63-1,53 (d, J=12,8 Гц, 1Н), 1,18-1,06 (m, 1Н); МС (ЭСИ) m/z: 418,2 [М+Н]+.
Пример 142 (8)-3-(3-Аминопиперидин-1-ил)-1-метил-5-(6-(1-метил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиразин-2(1Н)-он 242
Следуя способам, описанным в примере 124, и начиная с (З)-трет-бутил пиперидин-3-илкарбамата, 3,5-дибром-1 -метилпиразин-2(1Н)-она, 6-хлор-1Н-пиразоло[4,3-с]пиридина и 1-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразола, получали 242 в виде желтого твердого вещества (60 мг, 18,1%) за четыре стадии. 1Н ЯМР (500 МГц, ДМСО-о(6) 6 (ppm) 9,09 (s, 1Н), 8,45 (s, 1Н), 8,37 (s, 1Н), 8,32 (s, 1Н), 8,00 (s, 1Н), 7,64 (s, 1Н), 4,59-4,72 (m, 2Н), 3,91 (s, 3Н), 3,51 (s, 3Н), 2,98-3,04 (m, 1Н), 2,83-2,92 (m, 1Н), 2,80-2,81 (m, 1Н), 1,92-1,94 (m, 1Н), 1,78-1,79 (m, 1Н), 1,61-1,62 (m, 1Н), 1,28-1,34 (m, 1Н); МС (ЭСИ) m/z: 406 (М+Н)+.
Пример 143 (Рч)-3-(3-аминопиперидин-1-ил)-1-метил-5-(6-(1-метил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиразин-2(1Н)-он 243
Следуя способам, описанным в примере 124, и начиная с (Рч)-трет-бутил пиперидин-3-илкарбамата, 3,5-дибром-1-метилпиразин-2(1Н)-она, 6-хлор-1Н
182
пиразоло[4,3-с]пиридина и 1-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразола, получали 243 в виде желтого твердого вещества (58 мг, 17,9%) за четыре стадии. 1Н ЯМР (500 МГц, flMCO-d6) 5 9,09 (s, 1Н), 8,45 (s, 1Н), 8,37 (s, 1Н), 8,32 (s, 1Н), 8,05 (s, 1Н), 7,64 (s, 1Н), 4,59-4,72 (m, 2Н), 3,92 (s, 3Н), 3,51 (s, 3Н), 2,98-3,06 (m, 1Н), 2,80-2,92 (m, 1Н), 2,80-2,81 (m, 1Н), 1,92-1,94 (m, 1Н), 1,78-1,79 (m, 1Н), 1,60-1,62 (m, 1Н), 1,29-1,34 (m, 1Н); МС (ЭСИ) m/z: 406 (М+Н)+.
Пример 145 (38)-3-амино-1 -[3-метил-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-2-он 245
Следуя способам получения в примере 121, получали 245. МС (ЭСИ) m/z: 415,1. 1Н ЯМР (400 МГц, ДМСО) δ 9,63 (s, 1Н), 9,48 (s, 1Н), 9,35 (s, 1Н), 8,72 (s, 1Н), 8,65 (s, 1Н), 7,97 (d, J=8,4 Гц, 1Н), 7,91 (d, J=8,2 Гц, 1Н), 4,41 (s, 1Н), 3,69 (s, 1Н), 3,54 (s, 1Н), 2,66 (s, 3Н), 2,17 (s, 4Н), 1,87 (s, 2Н).
Пример 147 6-(1-(6-(1,4-диазепан-1-ил)пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридин-6-ил)пиразин-2-амин 247
Стадия А: трибутил-[1 -(6-фтор-2-пиридил)пиразоло[4,3-с]пиридин-6-ил]станнан
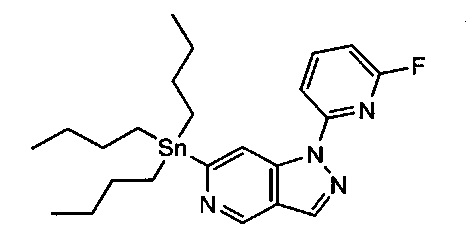
К смеси 6-хлор-1-(6-фтор-2-пиридил)пиразоло[4,3-с]пиридина 6 (3,1411 ммоль; 781 мг) в 1,4-диоксане (40 мл) в атмосфере аргона добавляли хлорид лития (18,847 ммоль; 798,98 мг), бис(трибутилолово) (3,7693 ммоль; 2301,7 мг; 2,005 мл), трис(дибензилиденацетон)дипалладий (0) (0,15705 ммоль; 143,82 мг) и трициклогексилфосфин (0,37693 ммоль; 105,70 мг). Полученную в результате смесь закрывали в пробирке высокого давления и нагревали при 120°С в течение ночи. Смесь фильтровали через Целит.Осадок на фильтре промывали ДХМ. Фильтрат концентрировали и остаток очищали на силикагеле, элюируя 0 до 30% ЕtOАс в гептане, получая трибутил-[1-(6-фтор-2-пиридил)пиразоло[4,3-с]пиридин-6-ил]станнан (1,0933 г, 69%).
Стадия В: 6-бром-1М-[(4-метоксифенил)метил]пиразин-2-амин 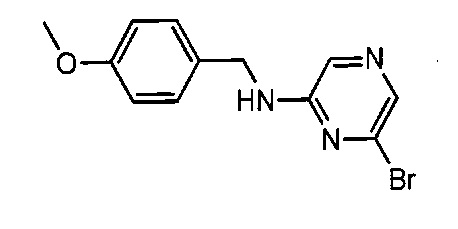
183
Смесь 2,6-дибромпиразина (3,431 ммоль; 816,1 мг), (4-метоксифенил)метанамина (3,431 ммоль; 470,6 мг; 0,4452 мл) и N-метилморфолина (8,577 ммоль; 876 мг; 0,952 мл) в 1-метил-2-пирролидиноне (10 мл) в закрытом сосуде высокого давления нагревали при 100°С в течение ночи. Смесь выливали в воду и экстрагировали ЕtOАс.Органический слой концентрировали. Остаток очищали на силикагеле, элюируя 0 до 100% ЕtOАс в ДХМ, получая 6-бром-1Ч-[(4-метоксифенил)метил]пиразин-2-амин (768,8 мг, 29%).
Стадия С: 6-[1 -(6-фтор-2-пиридил)пиразоло[4,3-с]пиридин-6-ил]-1Ч-[(4-метоксифенил)метил]пиразин-2-амин
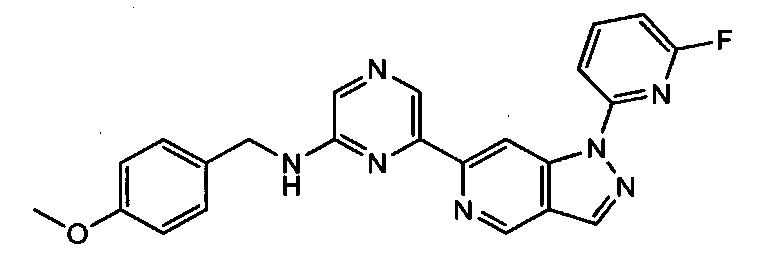
Смесь 6-бром-М-[(4-метоксифенил)метил]пиразин-2-амина (0,9932 ммоль; 768,8 мг), трибутил-[1 -(6-фтор-2-пиридил)пиразоло[4,3-с]пиридин-6-ил]станнана (2,173 ммоль; 1093 мг), трициклогексилфосфина (0,1192 ммоль; 33,42 мг) и трис(дибензилиденацетон)дипалладия (0) (0,04966 ммоль; 45,47 мг) в N,N-диметилацетамиде (15 мл) продували аргоном в течение 1 минуты. Реакционную смесь закрывали и нагревали при 150°С в микроволновой печи в течение 45 минут.Смесь разделяли между ЕtOАс и водой. Органический слой концентрировали и остаток очищали на силикагеле, элюируя 0 до 100% ЕtOАс в гептане, получая 6-[1 -(6-фтор-2-пиридил)пиразоло[4,3-с]пиридин-6-ил]-г>1-[(4-метоксифенил)метил]пиразин-2-амин (316,3 мг, 48%).
Стадия D: трет-бутил 4-[6-[6-[6-[(4-метоксифенил)метиламино]пиразин-2-ил]пиразоло[4,3-с]пиридин-1 -ил]-2-пиридил]-1,4-диазепан-1 -карбоксилат
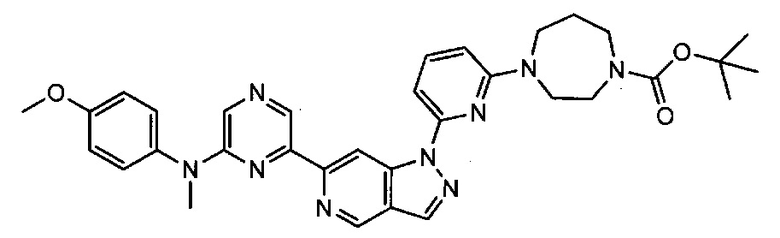
Смесь 6-[1-(6-фтор-2-пиридил)пиразоло[4,3-с]пиридин-6-ил]-1\1-[(4-
метоксифенил)метил]пиразин-2-амина (0,479 ммоль; 316,3 мг), трет-бутил 1,4-диазепан-1-карбоксилата (0,958 ммоль; 192 мг) и N-метилморфолина (1,20 ммоль; 122 мг; 0,133 мл) в 1-метил-2-пирролидиноне (5 мл) в закрытом сосуде высокого давления нагревали при 110°С в течение ночи. Смесь выливали в воду и экстрагировали ЕtOАс.Органический слой концентрировали. Остаток очищали
184
на силикагеле, элюируя 0 до 100% EtOAc в ДХМ, получая трет-бутил 4-[6-[6-[6-[(4-метоксифенил)метиламино]пиразин-2-ил]пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-1,4-диазепан-1-карбоксилат (~ 291 мг, 100%).
Стадия Е: К смеси трет-бутил 4-[6-[6-[6-[(4-
метоксифенил)метиламино]пиразин-2-ил]пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-1,4-диазепан-1-карбоксилата (0,4789 ммоль; 291 мг) в дихлорметане (5 мл) добавляли хлороводород, 4,0 М в 1,4-диоксане (5 мл), и трифлатную кислоту (4,789 ммоль; 733,3 мг; 0,4293 мл). Реакционную смесь перемешивали при комнатной температуре в течение 3 дней. Смесь концентрировали и остаток очищали с помощью обращенно-фазовой ВЭЖХ, получая 247 в виде твердого вещества белого оттенка (50,3 мг, 27%). 1Н ЯМР (400 МГц, ДМСО) 5 9,45-9,41 (s, 1Н), 9,26-9,22 (s, 1Н), 8,76-8,73 (s, 1Н), 8,64-8,58 (s, 1Н), 7,99-7,96 (s, 1Н), 7,73-7,67 (t, J=8,1 Гц, 1Н), 7,16-7,12 (d, J=7,7 Гц, 1Н), 6,63-6,58 (d, J=8,5 Гц, 1Н), 6,33-6,25 (s, 2Н), 3,89-3,82 (dd, J=11,0, 5,2 Гц, 4Н), 3,03-2,98 (m, 2Н), 2,73-2,66 (m, 2Н), 1,91-1,84 (dd, J=11,5, 5,8 Гц, 2Н); МС (ЭСИ) m/z: 388,2 [М+Н]+.
Пример 148 (8)-6-Метил-1-(6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]-пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-6-ол 248 Стадия А: 1 -(6-Бромпиридин-2-ил)-1,4-диазепан-6-ол
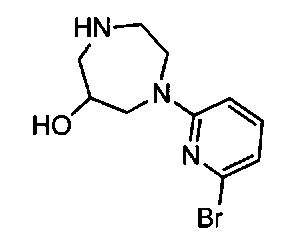
К смеси 2-бром-6-фторпиридина (845 мг, 4,83 ммоль) и 1,4-диазепан-6-ола (560 мг, 4,83 ммоль) в ЕЮН (20 мл) добавляли ДИПЭА (5 мл). Реакционную смесь нагревали при 100°С в течение 15 часов, контролируя с помощью ЖХМС.После завершения реакции ее концентрировали при пониженном давлении. Неочищенное вещество использовали на следующей стадии без дополнительной очистки. МС (ЭСИ) m/z: 272 [М+Н]+.
Стадия В: трет-Бутил 4-(6-бромпиридин-2-ил)-6-гидрокси-1,4-диазепан-1 -карбоксилат
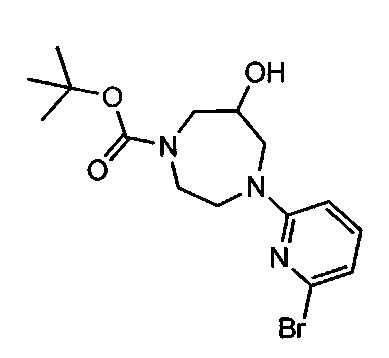 185
185
К смеси 1-(6-бромпиридин-2-ил)-1,4-диазепан-6-ола (900 мг, 3,32 ммоль) в МеОН (20 мл) добавляли ТЭА (5 мл), затем Вос20 (1,81 г, 8,30 ммоль). Смесь перемешивали при комнатной температуре в течение 2 часов. Реакционную смесь очищали с помощью хроматографии на силикагеле, используя ДХМ:МеОН (20:1~10:1) в качестве элюирующих растворителей, получая трет-бутил 4-(6-бромпиридин-2-ил)-6-гидрокси-1,4-диазепан-1-карбоксилат в виде белого твердого вещества (1,11 г, 90%). МС (ЭСИ) m/z: 372 [М+Н]+.
Стадия С: трет-Бутил 4-(6-(6-хлор-1Н-пиразоло[4,3-с]пиридин-1-
ил)пиридин-2-ил)-6-гидрокси-1,4-диазепан-1 -карбоксилат
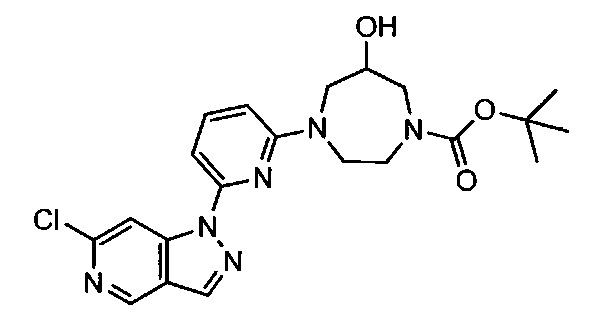
К смеси трет-бутил 4-(6-бромпиридин-2-ил)-6-гидрокси-1,4-диазепан-1-карбоксилата (800 мг, 2,16 ммоль) и 6-хлор-1Н-пиразоло[4,3-с]пиридина (330 мг, 2,16 ммоль) в 1,4-диоксане (25 мл) добавляли Cul (164 мг, 0,86 ммоль), N1,N2-диметилэтан-1,2-диамин (240 мг, 2,7 ммоль) и К2С03(894 мг, 6,48 ммоль). Смесь нагревали при 100°С, контролируя с помощью ЖХМС.После завершения реакции ее концентрировали при пониженном давлении. Неочищенное вещество очищали с помощью хроматографии на силикагеле, используя ДХМ:МеОН (20:1 ~10:1) в качестве элюирующих растворителей, получая трет-бутил 4-(6-(6-хлор-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-6-гидрокси-1,4-диазепан-1-карбоксилат в виде желтого твердого вещества (671 мг, 70%). МС (ЭСИ) m/z: 445 [М+Н]+.
Стадия D: трет-Бутил 4-(6-(6-хлор-1Н-пиразоло[4,3-с]пиридин-1-
ил)пиридин-2-ил)-6-оксо-1,4-диазепан-1 -карбоксилат
186
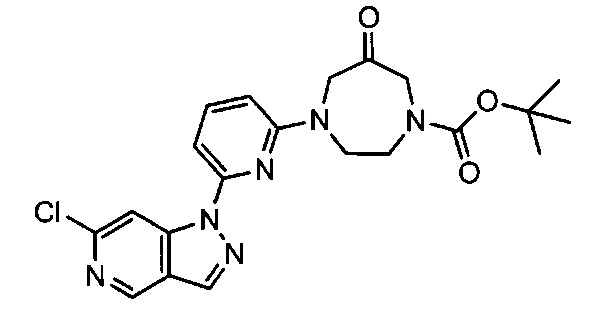
К смеси 4-(6-(6-хлор-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-6-гидрокси-1,4-диазепан-1 -карбоксилата (650 мг, 1,46 ммоль) в ДХМ (20 мл) при 0°С добавляли (1,1,1-триацетокси)-1,1-дигидро-1,2-бензйодоксол-3(1Н)-он (1,24 г, 2,92 ммоль) и перемешивали в течение ночи. Реакционную смесь гасили солевым раствором (40 мл) и экстрагировали ДХМ (100 мл х 3). Объединенные экстракты концентрировали при пониженном давлении. Остаток очищали с помощью хроматографии на силикагеле, используя петролейный эфир/этилацетат (5% до 50%) в качестве элюирующих растворителей, получая 4-(6-(6-хлор-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)-6-оксо-1,4-диазепан-1-карбоксилат в виде желтого масла (516 мг, 80%). МС (ЭСИ) m/z: 443 [М+Н]+.
Стадия Е: трет-Бутил 4-(6-(6-хлор-1Н-пиразоло[4,3-с]пиридин-1-
ил)пиридин-2-ил)-6-гидрокси-6-метил-1,4-диазепан-1-карбоксилат
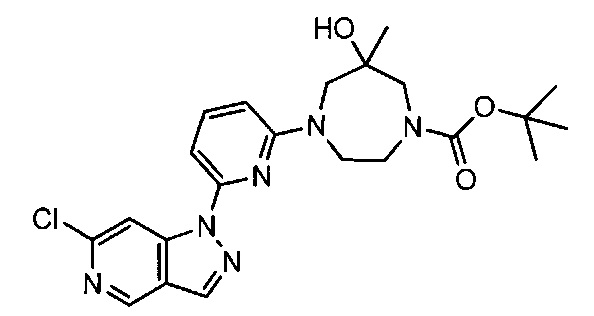
К смеси 4-(6-(6-хлор-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-6-оксо-1,4-диазепан-1 -карбоксилата (460 мг, 1,04 ммоль) в ТГФ (25 мл) при -78°С добавляли реактив Гриньяра CH3MgBr (147 мг, 1,25 ммоль) и перемешивали при -78°С в течение 2 часов. Реакционную смесь гасили 10% раствором NH4CI (25 мл) и экстрагировали ДХМ (80 мл х 3). Объединенные экстракты концентрировали при пониженном давлении. Остаток очищали с помощью хроматографии на силикагеле, используя ДХМ: МеОН (20:1-10:1) в качестве элюирующих растворителей, получая трет-бутил 4-(6-(6-хлор-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-6-гидрокси-6-метил-1,4-диазепан-1-карбоксилат в виде желтого твердого вещества (357 мг, 75%). МС (ЭСИ) m/z: 459 [М+Н]+.
Стадия F: трет-Бутил 4-(6-(6-(1Н-пиразол-4-ил)-1Н-пиразоло[4,3-
с]пиридин-1 -ил)пиридин-2-ил)-6-гидрокси-6-метил-1,4-диазепан-1 -карбоксилат
187
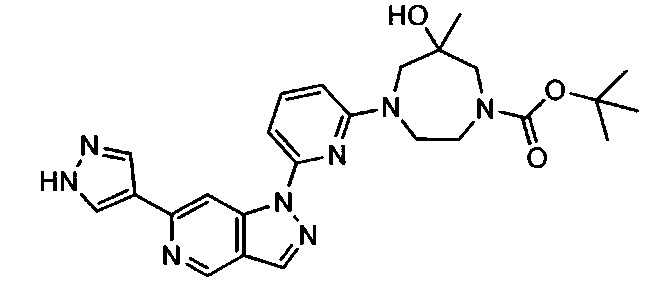
Суспензию трет-бутил 4-(6-(6-хлор-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-6-гидрокси-6-метил-1,4-диазепан-1-карбоксилата (330 мг, 0,72 ммоль), 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразола (140 мг, 0,72 ммоль), Pd(dppf)CI2 (53 мг, 0,072 ммоль) и раствора Na2C03 (2,0 М, 0,72 мл) в 1,4-диоксане (10 мл) в атмосфере аргона в закрытом сосуде нагревали в микроволновой печи при 120°С в течение часа. Реакционную смесь фильтровали и фильтрат концентрировали при пониженном давлении. Остаток очищали с помощью хроматографии на силикагеле, используя ДХМ:МеОН (20:1~10:1) в качестве элюирующих растворителей, получая трет-бутил 4-(6-(6-(1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)-6-гидрокси-6-метил-1,4-диазепан-1 -карбоксилат в виде желтого твердого вещества (212 мг, 60%). МС (ЭСИ) m/z: 491 [М+Н]+.
Стадия G: (Рч)-трет-Бутил 6-гидрокси-6-метил-4-(6-(6-(1-(2,2,2-
трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)-1,4-диазепан-1 -карбоксилат
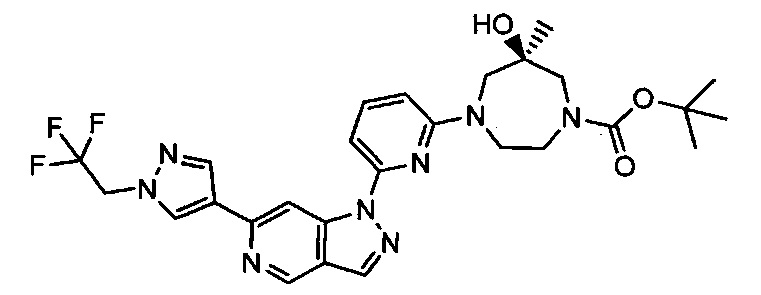
и (З)-трет-Бутил 6-гидрокси-6-метил-4-(6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилат 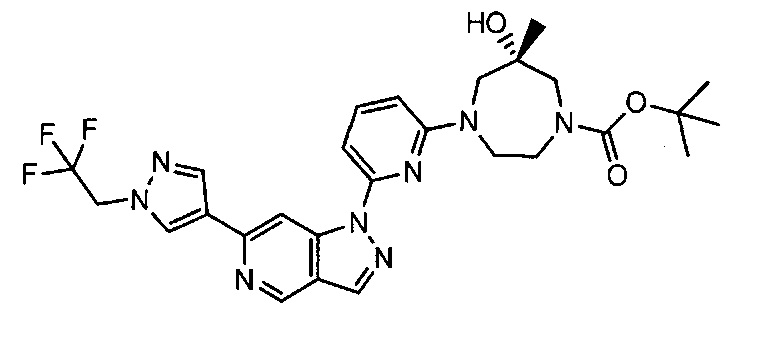
К раствору трет-бутил 4-(6-(6-(1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)-6-гидрокси-6-метил-1,4-диазепан-1 -карбоксилата (200 мг, 0,41 ммоль) в ДМФА (15 мл) добавляли 2,2,2-трифторэтил трифторметансульфонат (473 мг, 2,04 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 18 часов, гасили солевым раствором и экстрагировали ДХМ (100 мл х 3), и концентрировали при пониженном давлении. Остаток очищали с помощью препаративной ВЭЖХ, получая трет-бутил (+)-6-гидрокси-6-метил-4-(6-(6-(1 -(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]-пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилат в виде белого твердого вещества (183 мг, 78%). МС (ЭСИ) m/z=573 [М+Н]+, который разделяли с помощью хиральной препаративной ВЭЖХ, получая (Рч)-трет-бутил 6-гидрокси-6-метил-4-(6-(6-(1 -(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилат (51 мг) и (З)-трет-бутил 6-гидрокси-6-метил-4-(6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)-1,4-диазепан-1 -карбоксилат (48 мг).
Стадия Н: К раствору (Рч)-трет-бутил 6-гидрокси-6-метил-4-(6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилата (46 мг, 0,08 ммоль) в МеОН (3 мл) добавляли раствор HCI (конц. 3,0 мл) и перемешивали при комнатной температуре в течение 4 часов. Смесь концентрировали при пониженном давлении. Неочищенное вещество очищали с помощью обращенно-фазовой препаративной ВЭЖХ, получая 248 в виде белого твердого вещества (36 мг, 94%). 1Н ЯМР (500 МГц, ДМСО-cfe) 6 (ppm) 9,16 (s, 1Н), 8,77 (s, 1Н), 8,54 (s, 1Н), 8,50 (s, 1Н), 8,25 (s, 1Н), 7,67 (t, 1Н), 7,12 (d, 1Н), 6,72 (d, 1Н), 5,25-5,20 (t, 2Н), 4,68 (s, 1Н), 4,03-4,00 (m, 2Н), 3,57-3,48 (m, 2Н), 3,08-3,06 (m, 2Н), 2,72 (d, 1Н), 2,60 (d, 1Н), 1,14 (s, 3Н); МС (ЭСИ) m/z:.473 [М+Н]+.
Пример 149 (Р)-6-Метил-1-(6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]-пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-6-ол 249
Следуя способам, описанным в примере 148, и начиная с (8)-трет-бутил 6-гид рокси-6-метил-4-(6-(6-(1 -(2,2,2-трифторэтил)-1Н-п иразол-4-и л)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)-1,4-диазепан-1 -карбоксилата, получали 249 в виде белого твердого вещества (34 мг, 90%). 1Н ЯМР (500 МГц, flMCO-cfe) 6 (ppm) 9,16 (s, 1Н), 8,77 (s, 1Н), 8,54 (s, 1Н), 8,50 (s, 1Н), 8,25 (s, 1Н), 7,67 (t, 1Н), 7,12 (d, 1Н), 6,72 (d, 1Н), 5,25-5,20 (t, 2Н), 4,68 (s, 1Н), 4,03-4,00 (m, 2Н), 3,57-3,48 (m, 2Н), 3,08-3,06 (m, 2Н), 2,72 (d, 1Н), 2,60 (d, 1Н), 1,14 (s, 3Н); МС (ЭСИ) т/г.473 [М+Н]+.
189
Пример 150 (8)-1-(6-(6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)-4-(оксетан-3-ил)пиридин-2-ил)пиперидин-3-амин 250 Стадия А: 2,6-дифтор-4-(оксетан-3-ил)пиридин
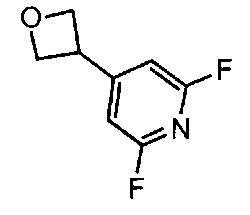
(2,6-Дифтор-4-пиридил)бороновую кислоту (4,0004 ммоль; 635,67 мг), иодид никеля (II) (0,12001 ммоль; 37,503 мг), транс-2-аминоциклогексанола гидрохлорид (0,12001 ммоль; 18,382 мг) и гексаметилдисилазан натрия (4,0004 ммоль; 748,56 мг) взвешивали в микроволновом сосуде СЕМ. Смесь закрывали, затем помещали в атмосферу азота. Добавляли изопропанол (15 мл) и смесь перемешивали в атмосфере азота в течение 5 минут.Затем добавляли 3-йодоксетан (2,0002 ммоль; 368 мг) в изопропаноле (1,5 мл). Сосуд нагревали при 100°С в микроволновой печи в течение 20 минут.Смесь разбавляли ЕЮН (15 мл) и фильтровали через Целит.Осадок на фильтре промывали ЕЮН (2x10 мл). Смесь концентрировали и остаток очищали на силикагеле, элюируя 0 до 50% ЕtOАс в ДХМ, получая 2,6-дифтор-4-(оксетан-3-ил)пиридин (80,1 мг, 23%).
Стадия В: 1 -[6-фтор-4-(оксетан-3-ил)-2-пиридил]-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин
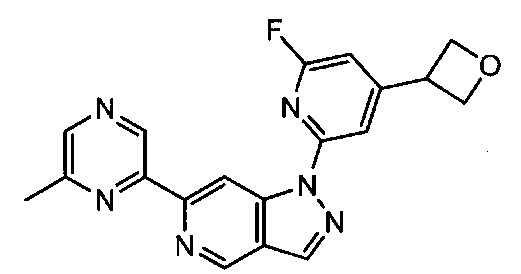
К смеси 6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридина (0,468 ммоль; 98,9 мг) и 2,6-дифтор-4-(оксетан-3-ил)пиридина (0,468 ммоль; 80,1 мг) в ДМФА (5 мл) добавляли карбонат цезия (0,562 ммоль; 183 мг). Полученную в результате смесь перемешивали при комнатной температуре. Смесь фильтровали. Фильтрат разделяли между ЕtOАс и водой. Органический слой концентрировали. Остаток очищали на силикагеле, элюируя 0 до 6% МеОН в ДХМ, получая 1 -[6-фтор-4-(оксетан-3-ил)-2-пиридил]-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин в виде белого твердого вещества (63,2 мг, 31%).
Стадия С: Смесь 1 -[6-фтор-4-(оксетан-3-ил)-2-пиридил]-6-(6-
метилпиразин-2-ил)пиразоло[4,3-с]пиридина (0,1443 ммоль; 63 мг), трет-бутил N-[(38)-3-пиперидил]карбамата (0,4329 ммоль, 80,7 мг) и N-метилморфолина
190
(0,3607 ммоль; 36,9 мг; 0,0401 мл) в 1-метил-2-пирролидиноне (3 мл) в закрытом сосуде высокого давления нагревали при 100°С в течение ночи. Смесь охлаждали до комнатной температуры. Растворители удаляли. Остаток обрабатывали 20% ТФК в ДХМ при комнатной температуре в течение 2 часов. Смесь концентрировали и остаток очищали с помощью обращенно-фазовой ВЭЖХ, получая 250 в виде твердого вещества белого оттенка (17,5 мг, 26%). 1Н ЯМР (400 МГц, ДМСО) δ 9,61-9,57 (s, 1Н), 9,49-9,43 (s, 1Н), 9,36-9,29 (s, 1Н), 8,69-8,66 (s, 1Н), 8,65-8,61 (s, 1Н), 7,33-7,30 (s, 1Н), 6,82-6,76 (s, 1Н), 5,02 -4,95 (m, 2Н), 4,73-4,66 (t, J=6,3 Гц, 2Н), 4,42-4,35 (d, J=13,2 Гц, 1Н), 4,35 -4,27 (dd, J=15,0, 7,2 Гц, 1Н), 4,20-4,13 (d, J=10,7 Гц, 1Н), 3,29-3,21 (m, 2Н), 3,08-3,01 (m, 1Н), 2,98-2,91 (s, 1Н), 2,66-2,61 (s, 3Н), 2,01-1,83 (m, 3Н), 1,71-1,58 (d, J=13,4 Гц, 1Н), 1,51-1,40 (d, J=10,8 Гц, 1Н), 0,99-0,92 (t, J=7,3 Гц, 1Н); МС (ЭСИ) m/z: 443,2 [М+Н]+.
Пример 151 1 -[3-метокси-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1 -ил]-2-пиридил]гексагидропиримидин-2-он 251
Стадия А: 1 -(6-бром-2-пиридил)-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин
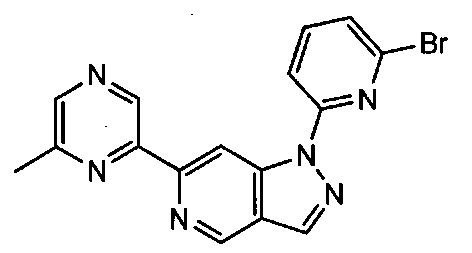
Раствор, содержащий 6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин (250 мг, 1,18 ммоль), 2-бром-6-йод-3-метоксипиридин (570 мг, 1,78 ммоль), иодид меди (I) (225 мг, 1,18 ммоль), карбонат калия (196 мг, 1,42 ммоль) и N,N'-диметилэтилендиамин (0,25 мл, 2,37 ммоль) перемешивали при 85°С в течение 4 часов. Реакционную смесь фильтровали через целит и концентрировали. Неочищенный продукт очищали на колонке isco (элюировали ЕtOАс/геп при 100% ЕtOАс), получая 280 мг требуемого продукта с выходом 59%. МС (ЭСИ) m/z: 397,1.
Стадия В: Раствор, содержащий 1-(6-бром-5-метокси-2-пиридил)-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин (50 мг, 0,126 ммоль), тетрагидро-2-пиримидинон (40 мг, 0,38 ммоль), иодид меди (I) (126 мг, 0,126 ммоль), карбонат калия (21 мг, 0,15 ммоль) и М,М'-диметилэтилендиамин (0,028 мл, 0,252 ммоль), перемешивали при 110°С в течение 18 часов. Реакционную смесь фильтровали через целит и концентрировали. Неочищенный продукт подвергали обращенно-фазовой ВЭЖХ, получая 251 (8 мг, 14%). МС (ЭСИ) m/z: AM Л. 1Н ЯМР (400 МГц,
ДМСО) δ 9,61 (s, 1Н), 9,47 (s, 1Н), 9,33 (s, 1Н), 8,68 (s, 1Н), 8,63 (s, 1Н), 7,89 (d, J=8,7 Гц, 1Н), 7,77 (d, J=8,8 Гц, 1Н), 6,74 (s, 1Н), 3,86 (s, 3Н), 3,35 (d, J=5,4 Гц, 2Н), 2,63 (s, 3Н), 2,16-2,08 (m, 2Н).
Пример 152 1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]гексагидропиримидин-2-он 252
Следуя способам получения в примере 151, получали 252. МС (ЭСИ) m/z: 387,2. 1Н ЯМР (400 МГц, ДМСО) δ 9,65 (s, 1Н), 9,47 (s, 1Н), 9,33 (s, 1Н), 8,70 (s, 1Н), 8,63 (s, 1Н), 7,96-7,86 (m, 2Н), 7,67 (d, J=7,5 Гц, 1Н), 7,12 (s, 1Н), 4,28 -4,21 (m, 2Н), 2,62 (s, 3Н), 2,17-2,08 (m, 2Н).
Пример 153 1 -(6-(6-(1 -Метил-1Н-пиразол-4-ил)-1Н-пиразол о[4,3-с]пиридин-1 -ил)пиридин-2-ил)азетидин-3-ол 253
Следуя способам, описанным в примере 124, и начиная с азетидин-3-ола гидрохлорида и 2-бром-6-фторпиридина, и 6-хлор-1Н-пиразоло[4,3-с]пиридина, получали 253 в виде белого твердого вещества (70 мг, 30,4%) в ходе трех стадий. 1Н ЯМР (500 МГц, flMCO-cf6) 6 (ppm) 9,12 (s, 1Н), 8,77 (s, 1Н), 8,53 (s, 1Н), 8,27 (s, 1Н), 7,93 (s, 1Н), 7,70-7,73 (t, J=15,5 Гц, 1H), 7,21-7,22 (d, J=7,5 Гц, 1H), 6,32-6,33 (d, J=8,5 Гц, 1H), 5,79-5,80 (d, J=6 Гц, 1H), 4,70-4,72 (m, 1Н), 4,39-4,42 (t, J=15 Гц, 2H), 3,93 (s, 3Н), 3,88-3,91 (m, 2Н); МС (ЭСИ) m/z: 348 [М+Н]+.
Пример 154 3-(6-Гидрокси-1,4-диазепан-1-ил)-1-метил-5-(6-(1-метил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиразин-2(1Н)-он 254
Следуя способам, описанным в примере 124, и начиная с 1,4-диазепан-6-ола, 3,5-дибром-1-метилпиразин-2(1Н)-она, 6-хлор-1Н-пиразоло[4,3-с]пиридина и 1 -метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразола, получали 254 в виде желтого твердого вещества (80 мг, 7,2%) в ходе пяти стадий. 1Н ЯМР (500 МГц, ДМСО-сУ6) 5 (ppm) 9,09 (s, 1Н), 8,43 (s, 1Н), 8,30 (s, 1Н), 8,29 (s, 1Н), 8,05 (s, 1Н), 8,00 (s, 1Н), 4,91 (s, 1Н), 4,49 (m, 1Н), 3,92 (m, 1Н), 3,89 (s, 3Н), 3,70-3,71 (m, 2Н), 3,51 (s, 3Н), 2,99-3,02 (m, 1Н), 2,90-2,91 (m, 1Н), 2,74-2,86 (m, 2Н); МС (ЭСИ) m/z: 422 [М+Н]+.
Пример 155 1-(6-(6-(1-(2,2,2-Трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)азетидин-3-ол 255
Следуя способам, описанным в примере 88, и начиная с азетидин-3-ола гидрохлорида, 2-бром-6-фторпиридина и 6-хлор-1Н-пиразоло[4,3-с]пиридина, получали 255 в виде белого твердого вещества (30 мг, 9,6%) в ходе четырех стадий. 1Н ЯМР (500 МГц, flMCO-d6) 6 (ppm) 9,16 (s, 1Н), 8,83 (s, 1Н), 8,555 (s, 1Н), 8,44 (s, 1Н), 8,09 (s, 1Н), 7,70-7,73 (t, J=16 Гц, 1H), 7,21-7,23 (d, J=7,5 Гц, 1H), 6,32-6,34 (d, J=8 Гц, 1H), 5,78-5,80 (d, J=6,5 Гц, 1H), 5,23-5,28 (m, 2Н), 4,71-4,72
(d, J=6 Гц, 1H), 4,39-4,42 (t, J=14,5 Гц, 2H), 3,89-3,91 (m, 2H); МС (ЭСИ) m/z: 416 [М+Н]+.
Пример 156 (1 -(6-(6-(1 -Метил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)азетидин-3-ил)метанамин 256
Следуя способам, описанным в примере 124, и начиная с трет-бутил азетидин-3-илметилкарбамата и 2-бром-6-фторпиридина, и 6-хлор-1Н-пиразоло[4,3-с]пиридина, получали 256 в виде желтого твердого вещества (31 мг, 26,4%) в ходе четырех стадий. 1Н ЯМР (500 МГц, ДМСО-с/6) 6 (ppm) 9,12 (d, 1Н), 8,78 (s, 1Н), 8,52 (s, 1Н), 8,23-8,26 (d, J=16,5 Гц, 1Н), 7,957-7,963 (d, J=3 Гц, 1Н), 7,70-7,73 (t, J=16 Гц, 1Н), 7,19-7,21 (d, J=7,5 Гц, 1Н), 6,28-6,30 (d, J=8 Гц, 1Н), 4,17-4,22 (m, 2Н), 3,87-3,93 (m, 5Н), 2,95-2,96 (d, J=6,5 Гц, 2Н), 2,87-2,89 (m, 1Н); МС (ЭСИ) m/z: 361 [М+Н]+.
Пример 157 1-(6-(6-(1-Метил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)азетидин-3-амин 257
Следуя способам, описанным в примере 124, и начиная с трет-бутил азетидин-3-илкарбамата, 2-бром-6-фторпиридина и 6-хлор-1Н-пиразоло[4,3-с]пиридина, получали 257 в виде желтого твердого вещества (128 мг, 23%) в ходе четырех стадий. 1Н ЯМР (500 МГц, ДМСО-с(6) 6 (ppm) 9,11 (s, 1Н), 8,79 (s, 1Н), 8,51 (s, 1Н), 8,25 (s, 1Н), 7,92 (s, 1Н), 7,69-7,71 (t, J=9 Гц, 1Н), 7,18-7,20 (d, J=9 Гц, 1Н), 6,29-6,30 (d, J=9 Гц, 1Н), 4,33-4,36 (m, 2Н), 3,92-3,93 (m, 1Н), 3,92 (s, 3Н), 3,74-3,77 (m, 2Н), 2,68-2,70 (br, 2Н); МС (ЭСИ) m/z: 347 [М+Н]+.
Пример 158 1-(6-(6-(1-(2,2,2-Трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)азетидин-3-амин 258
Следуя способам, описанным в примере 88, и начиная с трет-бутил азетидин-3-илкарбамата, 2-бром-6-фторпиридина и 6-хлор-1Н-пиразоло[4,3-с]пиридина, получали 258 в виде желтого твердого вещества (80 мг, 15%) в ходе пяти стадий. 1Н ЯМР (500 МГц, ДМСО-с(6) 6 (ppm) 9,16 (s, 1Н), 8,84 (s, 1Н), 8,55 (s, 1Н), 8,45 (s, 1Н), 8,09 (s, 1Н), 7,70-7,74 (t, J=10 Гц, 1Н), 7,21-7,23 (d, J=10 Гц, 1Н), 6,33-6,35 (d, J=10 Гц, 1Н), 5,25-5,27 (m, 2Н), 4,36-4,39 (m, 4Н), 4,00-4,01 (m, 1Н), 3,85-3,87 (m, 2Н); МС (ЭСИ) m/z: 415 [М+Н]+.
Пример 159 1 -[6-(4,4-дифтор-3-пиперидил)-2-пиридил]-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин 259
Стадия А: трет-бутил 3-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-
с]пиридин-1 -ил]-2-пиридил]-4-оксо-пиперидин-1 -карбоксилат
193
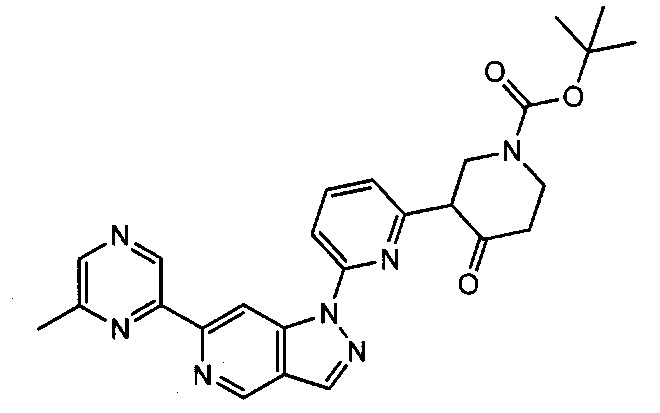
К раствору 1 -(6-бром-2-пиридил)-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридина (125 мг, 0,340 ммоль), трет-бутил 4-оксопиперидин-1 -карбоксилата (100 мг, 0,51 ммоль), ацетата палладия (8,0 мг, 0,034 ммоль) и трет-бутилата натрия (74 мг, 0,75 ммоль) в тетрагидрофуране (8,0 мл, 99 ммоль) добавляли три-трет-бутилфосфин (0,020 мл, 0,068 ммоль). Смесь дегазировали и нагревали при 48°С в течение 2 часов. Реакцию гасили водой, затем экстрагировали ЕtOАс.Органические слои сушили с сульфатом натрия, фильтровали и концентрировали в вакууме. Неочищенный продукт очищали с помощью флэш-хроматографии (элюировали ЕtOАс/гептаном при /5% ЕtOАс), получая 100 мг требуемого продукта с выходом 60%. МС (ЭСИ) m/z: 486,1.
Стадия В: трет-бутил 4,4-дифтор-3-[6-[6-(6-метилпиразин-2-
ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-1-карбоксилат
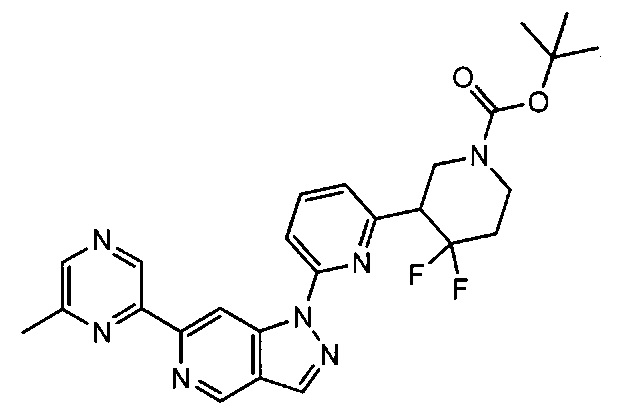
К раствору бис(2-метоксиэтил)аминосеры трифторида (White, A. R. et al (2004) J. Org. Chem., 69:2573-2576, Deoxo-fluor®, Sigma-Aldrich, 0,054 мл, 0,295 ммоль) в дихлорметане (1,0 мл, 16 ммоль) при -78°С добавляли трет-бутил 3-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-4-оксо-пиперидин-1-карбоксилат (65 мг, 0,13 ммоль) в 1,0 мл ДХМ по каплям. Реакционную смесь нагревали до к.т.в течение ночи. Реакционную смесь гасили водой и экстрагировали ДХМ. Органические слои сушили с сульфатом натрия, фильтровали и концентрировали в вакууме. Неочищенный продукт очищали с
194
помощью флэш-хроматографии (элюировали ЕtOАс/гептаном при 60% ЕtOАс), получая 38 мг требуемого продукта с выходом 55%. МС (ЭСИ) m/z: 508,1.
Стадия С: К раствору трет-бутил 4,4-дифтор-3-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1 -ил]-2-пиридил]пиперидин-1 -карбоксилата (50 мг, 0,099 ммоль) в 1,4-диоксане (2,00 мл, 23,4 ммоль) добавляли хлороводород (4 моль/л) в 1,4-диоксане (1,00 мл, 4,00 ммоль). Реакционную смесь перемешивали при к.т.в течение 18 часов. Реакционную смесь концентрировали и подвергали обращенно-фазовой ВЭЖХ, получая 17 мг 259 с выходом 42%. МС (ЭСИ) m/z: 408,1. 1Н ЯМР (400 МГц, ДМСО) δ 9,72 (s, 1Н), 9,46 (s, 1Н), 9,36 (s, 1Н), 8,74 (s, 1Н), 8,63 (s, 1Н), 8,04 (t, J=7,8 Гц, 1Н), 7,98 (d, J=8,2 Гц, 1Н), 7,40 (d, J=7,4 Гц, 1Н), 3,60-3,42 (m, 2Н), 3,18 (d, J=12,8 Гц, 1Н), 2,87 (t, J=12,6 Гц, 1Н), 2,67 (s, 3Н), 2,36 (d, J=18,3 Гц, 1Н), 2,21-2,09 (m, 1Н), 1,99 (d, J=34,4 Гц, 1Н).
Пример 160 и 163 (Рх)-1-(3-метил-6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-6-ол 260 и (S)-1-(3-метил-6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-6-ол 263
Стадия А: 1-(3-Бром-6-йодпиридин-2-ил)-1,4-диазепан-6-ол.
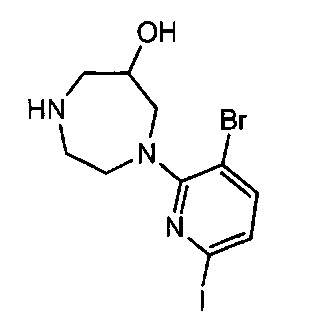
Раствор 3-бром-2-фтор-6-йодпиридина (1,00 г, 3,4 ммоль), 1,4-диазепан-6-ола (510 мг, 4,4 ммоль) и ДИПЭА (2 мл) в ЕЮН (6 мл) в закрытой пробирке перемешивали при 100°С в течение 20 часов. Реакционную смесь концентрировали при пониженном давлении, получая остаток (1,18 г), который использовали на следующей стадии без дополнительной очистки. МС (ЭСИ) m/z: 398 [М+Н]+.
Стадия В: трет-Бутил 4-(3-бром-6-йодпиридин-2-ил)-6-гидрокси-1,4-диазепан-1 -карбоксилат
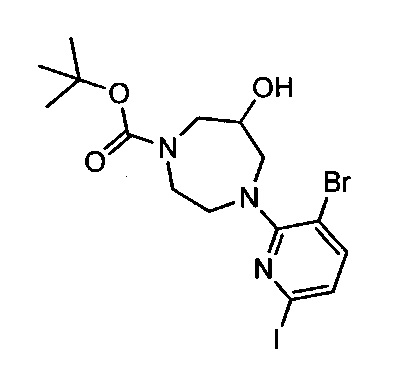 195
195
Раствор 1-(3-бром-6-йодпиридин-2-ил)-1,4-диазепан-6-ола (1,18 г, 3 ммоль), Вос20 (980 мг, 4,5 ммоль) и ТЭА (2 мл) в МеОН (15 мл) перемешивали при комнатной температуре в течение 20 часов. Реакционную смесь концентрировали при пониженном давлении. Остаток очищали с помощью хроматографии на силикагеле, используя EtOAc: петролейный эфир (10% ~ 25%) в качестве элюирующих растворителей, получая трет-бутил 4-(3-бром-6-йодпиридин-2-ил)-6-гидрокси-1,4-диазепан-1-карбоксилат в виде белого твердого вещества (980 мг, 60% за две стадии). МС (ЭСИ) m/z: 498 [М+Н]+.
Стадия С: 6-Хлор-1 -((2-(триметилсилил)этокси)метил)-1Н-пиразоло[4,3-с]пиридин
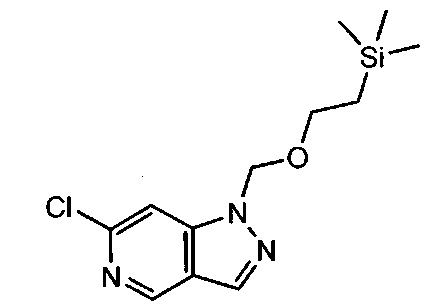
К раствору 6-хлор-1Н-пиразоло[4,3-с]пиридина (2,00 г, 13,1 ммоль) и ДИПЭА (3 мл) в ДХМ (10 мл) добавляли SEMCI (3 мл). Смесь перемешивали при 30°С в течение 20 часов. Реакционную смесь концентрировали при пониженном давлении. Остаток очищали с помощью хроматографии на силикагеле, используя ЕtOАс/петролейный эфир (10%-60%) в качестве элюирующих растворителей, получая 6-хлор-1-((2-(триметилсилил)этокси)метил)-1Н-пиразоло[4,3-с]пиридин в виде бесцветного масла (3,44 г, 93%). МС (ЭСИ) m/z: 284 [М+Н]+.
Стадия D: 6-(1Н-Пиразол-4-ил)-1 -((2-(триметилсилил)этокси)метил)-1Н-пиразоло[4,3-с]-пиридин 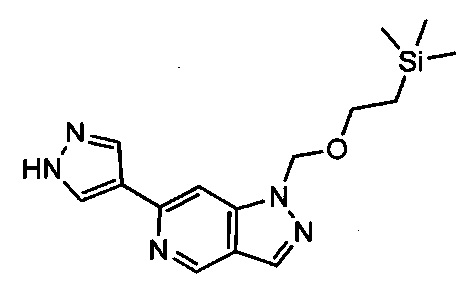
Суспензию 6-хлор-1-((2-(триметилсилил)этокси)метил)-1Н-пиразоло[4,3-с]пиридина (1,30 г, 4,6 ммоль), 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразола (1,16 г, 6 ммоль) и Pd(dppf)CI2 (437 мг, 0,6 ммоль) в водн. Na2C03 (2,0 М, 12 мл) и 1,4-диоксане (20 мл) нагревали при 110°С в течение 20 часов. Реакционную смесь концентрировали при пониженном давлении. Остаток очищали с помощью хроматографии на силикагеле, используя этилацетат/гептаны 50% до 100% в качестве элюирующих растворителей, получая 6-(1Н-пиразол-4-ил)-1 -((2-(триметилсилил)этокси)метил)-1Н-
пиразоло[4,3-с]пиридин в виде желтого масла (670 мг, 46%) и выделенный 1 г исходного вещества. МС (ЭСИ) т/г.316 [М+Н]+.
Стадия Е: 6-(1-(2,2,2-Трифторэтил)-1Н-пиразол-4-ил)-1-((2-(триметилсилил)этокси)метил)-1Н-пиразоло[4,3-с]пиридин
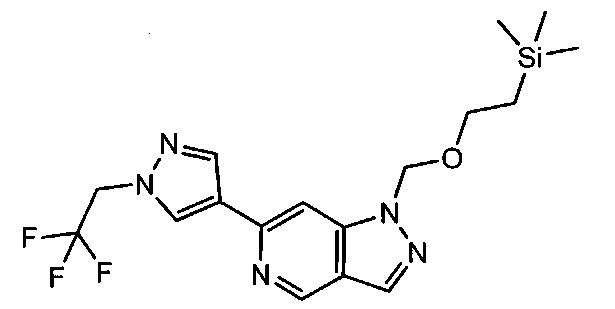
Смесь 6-(1Н-пиразол-4-ил)-1 -((2-(триметилсилил)этокси)метил)-1Н-
пиразоло[4,3-с]пиридина (670 мг, 2,12 ммоль), К2С03 (587 мг, 4,24 ммоль) и 2,2,2-трифторэтил трифторметансульфоната (4 мл) в ДМФА (4 мл) перемешивали при температуре окружающей среды в течение 20 часов. Реакционную смесь гасили ЕtOАс (10 мл) и Н20 (10 мл) и экстрагировали ЕtOАс (10 мл х 3). Экстракты концентрировали при пониженном давлении. Остаток очищали с помощью хроматографии на силикагеле, используя этилацетат/гептан (10% до 70%) в качестве элюирующих растворителей, получая 6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1 -((2-(триметилсилил)этокси)метил)-1Н-пиразоло[4,3-с]пиридин в виде белого твердого вещества (800 мг, 95%). МС (ЭСИ) m/z: 398 [М+Н]+.
Стадия F: 6-(1-(2,2,2-Трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин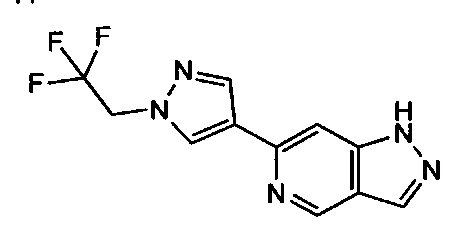
Смесь 6-(1 -(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1 -((2-
(триметилсилил)этокси)-метил)-1Н-пиразоло[4,3-с]пиридина (800 мг, 2,02 ммоль) и ТФК (5 мл) в ДХМ (10 мл) перемешивали при температуре окружающей среды в
197
течение 20 часов. Реакционную смесь концентрировали при пониженном давлении, получая 6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]-пиридин в виде желтого масла (539 мг, 100%). МС (ЭСИ) m/z: 268 [М+Н]+.
Стадия G: трет-Бутил 4-(3-бром-6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло-[4,3-с]пиридин-1 -ил)пиридин-2-ил)-6-гидрокси-1,4-диазепан-1 -карбоксилат
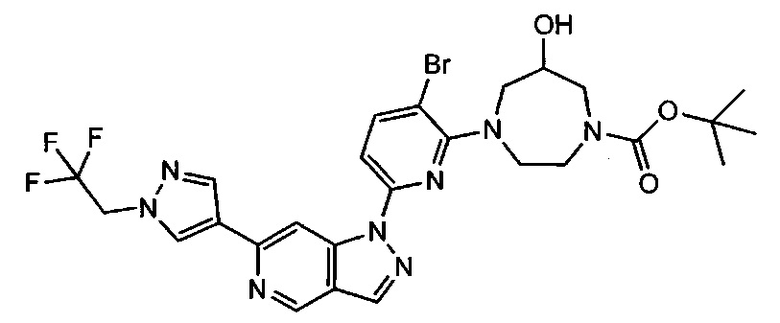
Смесь 6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-
с]пиридина (539 мг, 2,02 ммоль), трет-бутил 4-(3-бром-6-йодпиридин-2-ил)-6-гидрокси-1,4-диазепан-1-карбоксилата (1,00 г, 2,02 ммоль), 1\11,М2-диметилэтан-1,2-диамина (535 мг, 6,06 ммоль), Cul (768 мг, 4,04 ммоль) и К2С03 (1,12 г, 8,08 ммоль) в 1,4-диоксане (10 мл) в атмосфере N2 нагревали при 100°С в течение 20 часов. Реакционную смесь концентрировали при пониженном давлении. Остаток очищали с помощью хроматографии на силикагеле, используя ЕtOАс/петролейный эфир (20% ~ 80%) в качестве элюирующих растворителей, получая трет-бутил 4-(3-бром-6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)-6-гидрокси-1,4-диазепан-1 -карбоксилат в виде белого твердого вещества (244 мг, 19%). МС (ЭСИ) m/z: 637 [М+Н]+.
Стадия Н: трет-Бутил (±)-6-гидрокси-4-(3-метил-6-(6-(1-(2,2,2-
трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)-1,4-диазепан-1 -карбоксилат
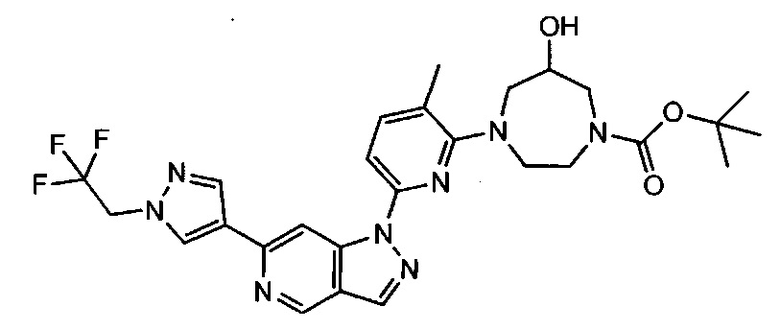
Смесь трет-бутил 4-(3-бром-6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-6-гидрокси-1,4-диазепан-1-карбоксилата (244 мг, 0,38 ммоль), 2,4,6-триметил-1,3,5,2,4,6-
198
триоксатриборинана (194 мг, 1,53 ммоль), Pd2dba3 (174 мг, 0,19 ммоль), Рсу3 (107 мг, 0,38 ммоль) и Cs2C03 (500 мг, 1,53 ммоль) в 1,4-диоксане (10 мл) нагревали в микроволновой печи при 110°С в течение 1,5 часа. Реакционную смесь концентрировали при пониженном давлении. Остаток очищали с помощью хроматографии на силикагеле, используя ЕtOАс/петролейный эфир (20% ~ 80%) в качестве элюирующих растворителей, получая трет-бутил (+)-6-гидрокси-4-(3-метил-6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилат в виде белого твердого вещества (120 мг, 55%). МС (ЭСИ) m/z: 573 [М+Н]+.
Стадия I: (Э)-трет-Бутил 6-гидрокси-4-(3-метил-6-(6-(1-(2,2,2-
трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)-1,4-диазепан-1 -карбоксилат
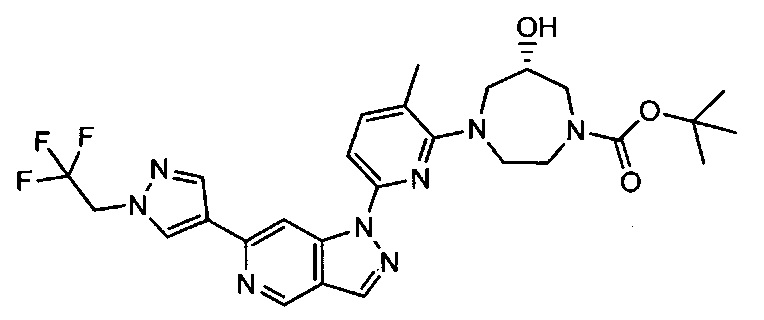
и (Р)-трет-Бутил 6-гидрокси-4-(3-метил-6-(6-(1 -(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)-1,4-диазепан-1 -карбоксилат
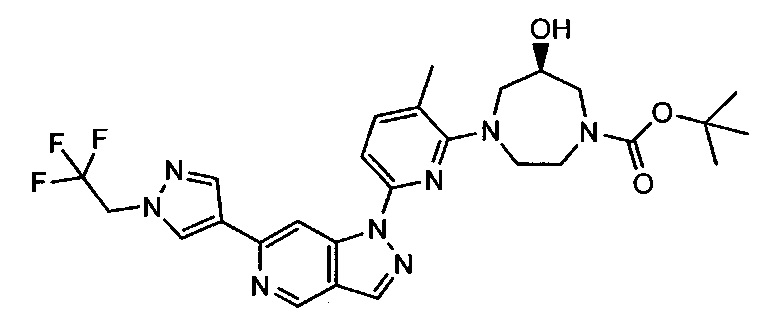
(+)-трет-Бутил 6-гидрокси-4-(3-метил-6-(6-(1 -(2,2,2-трифторэтил)-1Н-
пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилат (160 мг) разделяли с помощью хиральной препаративной ВЭЖХ, получая (З)-трет-бутил 6-гидрокси-4-(3-метил-6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилат (60 мг) и (К)-трет-бутил 6-гидрокси-4-(3-метил-6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилат (60 мг).
Стадия J: Смесь (З)-трет-бутил 6-гидрокси-4-(3-метил-6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)-
199
1,4-диазепан-1 -карбоксилата (60 мг, 0,10 ммоль) в HCI/MeOH (4 М, 10 мл) перемешивали при температуре окружающей среды в течение 20 часов. Реакционную смесь концентрировали при пониженном давлении. Остаток разбавляли МеОН (10 мл), нейтрализовали 28% раствором аммиака, концентрировали при пониженном давлении и очищали с помощью препаративной ВЭЖХ, получая 260 в виде белого твердого вещества (40 мг, 82%). 1Н-ЯМР (500 МГц, CD3OD) 6 (ppm) 9,03 (s, 1Н), 8,76 (s, 1Н), 8,35 (d, J=10,5 Гц, 2Н), 8,16 (s, 1Н), 7,62 (d, J=8 Гц, 1Н), 7,45 (d, J=7,5 Гц, 1Н), 5,03-5,08 (m, 2Н), 4,14-4,21 (m, 1Н), 3,96-3,99 (m, 1Н), 3,51-3,68 (m, 3Н), 3,18-3,33 (m, 3Н), 2,99-3,08 (m, 1Н), 2,38 (s, 3Н); МС (ЭСИ) m/z: 473 [М+Н]+.
Стадия К: Смесь (Рх)-трет-бутил 6-гидрокси-4-(3-метил-6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)-1,4-диазепан-1 -карбоксилата (60 мг, 0,10 ммоль) в HCI/MeOH (4 М, 10 мл) перемешивали при температуре окружающей среды в течение 20 часов. Реакционную смесь концентрировали при пониженном давлении. Остаток разбавляли МеОН (10 мл), нейтрализовали 28% раствором аммиака, концентрировали при пониженном давлении и очищали с помощью препаративной ВЭЖХ, получая 263 в виде белого твердого вещества (40 мг, 82%). 1Н-ЯМР (500 МГц, CD3OD) 6 ppm 8,97 (s, 1Н), 8,66 (s, 1Н), 8,31 (d, J=10,5 Гц, 2Н), 8,11 (s, 1Н), 7,62 (d, J=8 Гц, 1Н), 7,45 (d, J=7,5 Гц, 1Н), 5,07-5,02 (m, 2Н), 4,21-4,14 (m, 1Н), 3,99-3,96 (m, 1Н), 3,68-3,51 (m, 3Н), 3,33-3,18 (m, 3Н), 3,08-2,99 (m, 1Н), 2,38 (s, 3Н); МС (ЭСИ) m/z: 473 [М+Н]+.
Пример 161 (S)-1 -(6-(6-Метокси-6-метил-1,4-диазепан-1 -ил)пиридин-2-ил)-6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин 261
Стадия А: трет-Бутил 4-(6-бромпиридин-2-ил)-6-оксо-1,4-диазепан-1-карбоксилат
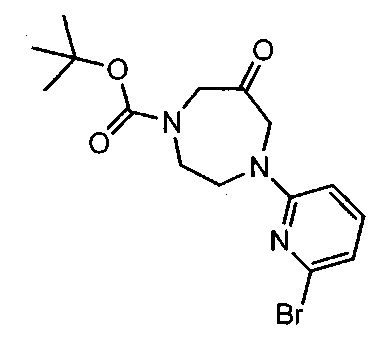
К смеси трет-бутил 4-(6-бромпиридин-2-ил)-6-гидрокси-1,4-диазепан-1-карбоксилата (1,05 г, 2,83 ммоль) из примеров 88, 89, 148 в ДХМ (35 мл) при 0°С добавляли (1,1,1-триацетокси)-1,1-дигидро-1,2-бензйодоксол-3(1Н)-он (2,40 г, 5,66 ммоль). Смесь перемешивали в течение ночи, гасили солевым раствором
200
(40 мл) и ДХМ (30 мл) и экстрагировали ДХМ (100 мл х 3), и концентрировали при пониженном давлении. Остаток очищали с помощью хроматографии на силикагеле, используя петролейный эфир/этилацетат (5% до 50%) в качестве элюирующих растворителей, получая трет-бутил 4-(6-бромпиридин-2-ил)-6-оксо-1,4-диазепан-1 -карбоксилат в виде желтого масла (846 мг, 81%). МС (ЭСИ) m/z: 370 [М+Н]+.
Стадия В: трет-Бутил 4-(6-бромпиридин-2-ил)-6-гидрокси-6-метил-1,4-диазепан-1 -карбоксилат
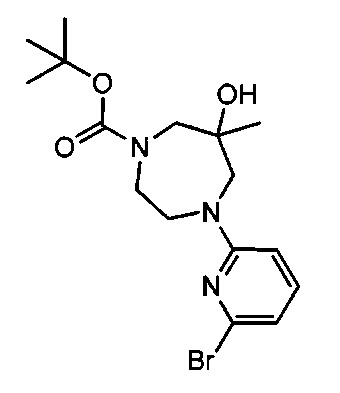
К смеси трет-бутил 4-(6-бромпиридин-2-ил)-6-оксо-1,4-диазепан-1-карбоксилата (800 мг, 2,17 ммоль) в ТГФ (40 мл) при -78°С добавляли CH3MgBr (169 мг, 1,44 ммоль). Смесь перемешивали при -78°С в течение 2 часов, гасили 10% раствором NH4CI (35 мл), экстрагировали ДХМ (100 мл х 3) и концентрировали при пониженном давлении. Остаток очищали с помощью хроматографии на силикагеле, используя ДХМ: МеОН (20:1 ~ 10:1) в качестве элюирующих растворителей, получая трет-бутил 4-(6-бромпиридин-2-ил)-6-гидрокси-6-метил-1,4-диазепан-1-карбоксилат в виде желтого твердого вещества (636 мг, 76%). МС (ЭСИ) m/z: 386 [М+Н]\
Стадия С: трет-Бутил 4-(6-бромпиридин-2-ил)-6-метокси-6-метил-1,4-диазепан-1 -карбоксилат
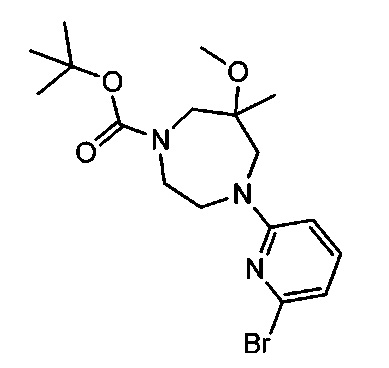
К смеси 4-(6-бромпиридин-2-ил)-6-гидрокси-6-метил-1,4-диазепан-1-карбоксилата (600 мг, 1,56 ммоль) в ДМФА (20 мл) при 0°С добавляли NaH (94 мг, 3,90 ммоль) и перемешивали в течение 30 минут.К смеси добавляли диметилсульфат (295 мг, 2,34 ммоль) и перемешивали при комнатной
201
температуре в течение 15 часов. Ее гасили солевым раствором (20 мл), экстрагировали ЕtOАс (100 мл х 3), концентрировали при пониженном давлении. Остаток очищали с помощью хроматографии на силикагеле, используя петролейный эфир: ЕtOАс (4:1-1:1) в качестве элюирующих растворителей, получая трет-бутил 4-(6-бромпиридин-2-ил)-6-метокси-6-метил-1,4-диазепан-1-карбоксилат в виде желтого масла (554 мг, 89%). МС (ЭСИ) m/z: 400 [М+Н]+.
Стадия D: трет-Бутил 4-(6-(6-хлор-1Н-пиразоло[4,3-с]пиридин-1-
ил)пиридин-2-ил)-6-метокси-6-метил-1,4-диазепан-1 -карбоксилат
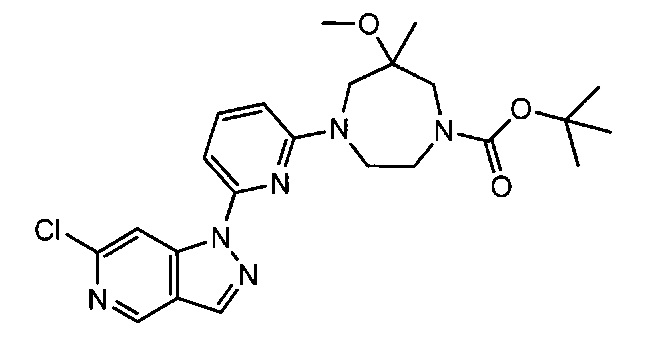
К смеси трет-бутил 4-(6-бромпиридин-2-ил)-6-метокси-6-метил-1,4-диазепан-1-карбоксилата (530 мг, 1,33 ммоль) и 6-хлор-1Н-пиразоло[4,3-с]пиридина (203 мг, 1,33 ммоль) в 1,4-диоксане (30 мл) добавляли Cul (101 мг, 0,53 ммоль), М1,№-диметилэтан-1,2-диамин (94 мг, 1,06 ммоль) и К2С03 (734 мг, 5,32 ммоль). Смесь нагревали при 100°С, контролируя с помощью ЖХМС.После завершения реакции ее концентрировали при пониженном давлении. Неочищенное вещество очищали с помощью хроматографии на силикагеле, используя петролейный эфир: ЕtOАс (3:1~1:1) в качестве элюирующих растворителей, получая трет-бутил 4-(6-(6-хлор-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-6-метокси-6-метил-1,4-диазепан-1-карбоксилат в виде желтого твердого вещества (446 мг, 71%). МС (ЭСИ) m/z: 473 [М+Н]+.
Стадия Е: трет-Бутил 4-(6-(6-(1Н-пиразол-4-ил)-1Н-пиразоло[4,3-
с]пиридин-1 -ил)пиридин-2-ил)-6-метокси-6-метил-1,4-диазепан-1 -карбоксилат
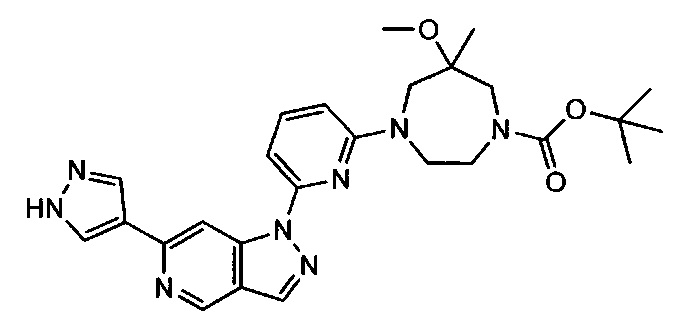
Суспензию трет-бутил 4-(6-(6-хлор-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-6-метокси-6-метил-1,4-диазепан-1-карбоксилата (420 мг, 0,89 ммоль), 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразола (173 мг,
202
0,89 ммоль), Pd(dppf)CI2 (65 мг, 0,089 ммоль) и раствора Na2C03 (2,0 М, 0,9 мл) в 1,4-диоксане (15 мл) в атмосфере аргона в закрытом сосуде нагревали в микроволновой печи при 120°С в течение 1 часа. Реакционную смесь фильтровали и фильтрат концентрировали при пониженном давлении. Остаток очищали с помощью хроматографии на силикагеле, используя петролейный эфир: ЕtOАс (3:1 ~ 1:1) в качестве элюирующих растворителей, получая трет-бутил 4-(6-(6-(1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-6-метокси-6-метил-1,4-диазепан-1-карбоксилат в виде желтого твердого вещества (283 мг, 63%). МС (ЭСИ) m/z: 505 [М+Н]+.
Стадия F: (Рч)-трет-Бутил 6-метокси-6-метил-4-(6-(6-(1-(2,2,2-
трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)-1,4-диазепан-1 -карбоксилат
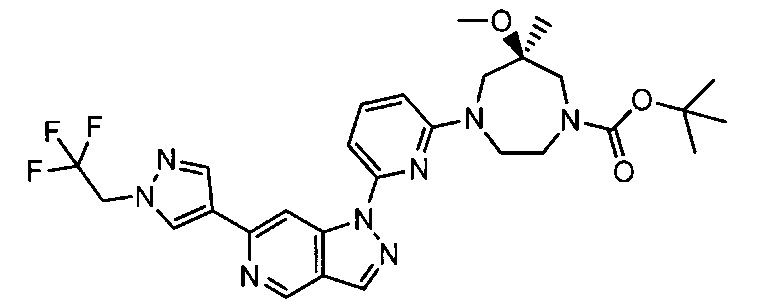
и (З)-трет-Бутил 6-метокси-6-метил-4-(6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилат
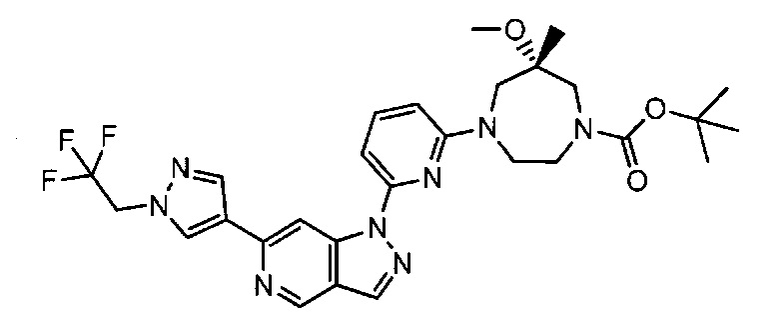
К раствору трет-бутил 4-(6-(6-(1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)-6-метокси-6-метил-1,4-диазепан-1 -карбоксилата (265 мг, 0,53 ммоль) в ДМФА (15 мл) добавляли 2,2,2-трифторэтил трифторметансульфонат (610 мг, 2,63 ммоль). Смесь перемешивали при комнатной температуре в течение 18 часов. Реакционную смесь гасили солевым раствором, экстрагировали ДХМ (100 мл х 3) и концентрировали при
пониженном давлении. Остаток очищали с помощью препаративной ВЭЖХ, получая трет-бутил (+)-6-метокси-6-метил-4-(6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)-1,4-диазепан-1 -
карбоксилат в виде белого твердого вещества (264 мг, 85%). МС (ЭСИ) m/z: 587 [М+Н]+.
трет-Бутил (±)-6-метокси-6-метил-4-(6-(6-(1 -(2,2,2-трифторэтил)-1Н-
пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)-1,4-диазепан-1 -карбоксилат разделяли с помощью хиральной препаративной ВЭЖХ, получая (Рч)-трет-бутил 6-метокси-6-мети л-4-(6-(6-(1 -(2,2,2-трифторэтил)-1Н-п иразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилат (100 мг) и (З)-трет-бутил 6-метокси-6-метил-4-(6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилат (95 мг).
Стадия G: К раствору (Рч)-трет-бутил 6-метокси-6-метил-4-(6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)-1,4-диазепан-1-карбоксилата (100 мг, 0,17 ммоль) в МеОН (5 мл) добавляли HCI (конц., 5 мл). Смесь перемешивали при комнатной температуре в течение 4 часов. Ее концентрировали при пониженном давлении. Неочищенное вещество очищали с помощью обращенно-фазовой препаративной ВЭЖХ, получая 261 в виде белого твердого вещества (75 мг, 91%). 1Н ЯМР (500 МГц, ДМСО-с/6) 6 (ррт) 9,16 (s, 1Н), 8,70 (s, 1Н), 8,55 (s, 1Н), 8,41 (s, 1Н), 8,14 (s, 1Н), 7,68 (t, 1Н), 7,16 (d, 1Н), 6,69 (d, 1Н), 5,27-5,22 (m, 2Н), 4,06-4,03 (m, 2Н), 3,67-3,54 (m, 2Н), 3,12 (s, 3Н), 3,02 (s, 2Н), 2,72 (s, 2Н), 1,14 (s, 3Н); МС (ЭСИ) m/z: 487 [М+Н]+.
Пример 162 (1 -(6-(6-(1 -(2,2,2-Трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)азетидин-3-ил)метанамин 262
Следуя способам, описанным в примере 88, и начиная с трет-бутил азетидин-3-илметилкарбамата, 2-бром-6-фторпиридина и 6-хлор-1Н-пиразоло[4,3-с]пиридина, получали 262 в виде желтого твердого вещества (35 мг, 30,9%) за пять стадий. 1Н ЯМР (500 МГц, ДМСО-с(6) 6 (ррт) 9,15 (s, 1Н), 8,83-8,86 (d, J=12 Гц, 1Н), 8,55 (s, 1Н), 8,43 (s, 1Н), 8,10-8,12 (d, J=7 Гц, 1Н), 7,69-7,72 (t, J=16 Гц, 1Н), 7,19-7,20 (d, J=8 Гц, 1Н), 6,28-6,29 (d, J=8 Гц, 1Н), 5,23-5,25 (d, J=9,5 Гц, 2Н), 4,17-4,20 (m, 2Н), 3,87-3,89 (t, J=12 Гц, 2Н), 2,84-2,86 (d, J=6,5 Гц, 3Н); МС (ЭСИ) m/z: 429 [М+Н]+.
Пример 164 (R)-1 -(6-(6-Метокси-6-метил-1,4-диазепан-1 -ил)пиридин-2-ил)-6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин 264
Следуя способам, описанным в примере 161, и начиная с (З)-трет-бутил 6-метокси-6-метил-4-(6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)-1,4-диазепан-1 -карбоксилата, получали 264 в виде белого твердого вещества (133 мг, 92%). 1Н ЯМР (500 МГц, flMCO-d6) 6 (ррт) 9,16 (s, 1Н), 8,70 (s, 1Н), 8,55 (s, 1Н), 8,41 (s, 1Н), 8,14 (s, 1Н),
204
7,68 (t, 1H), 7,16 (d, 1H), 6,69 (d, 1H), 5,27-5,22 (m, 2H), 4,06-4,03 (m, 2H), 3,67-3,54 (m, 2H), 3,12 (s, 3H), 3,02 (s, 2H), 2,72 (s, 2H), 1,14 (s, 3Н); МС (ЭСИ) m/z: 487 [M+H]+.
Пример 165 3-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1 -ил]-2-пиридил]пиперидин-4-ол 265
Стадия А: трет-бутил 4-гидрокси-3-[6-[6-(6-метилпиразин-2-
ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-1-карбоксилат
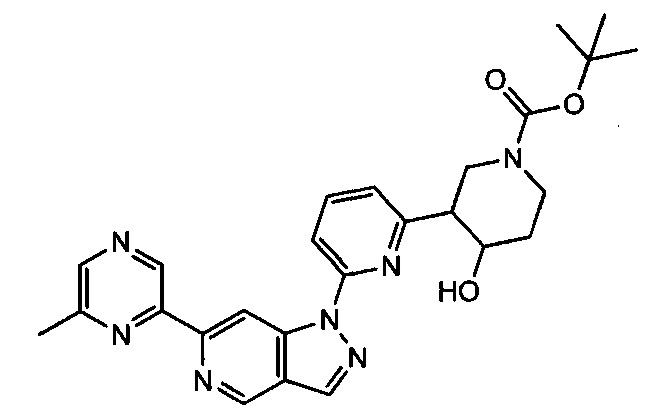
К раствору трет-бутил 3-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-4-оксо-пиперидин-1-карбоксилата (90 мг, 0,18 ммоль) в тетрагидрофуране (8,0 мл) при 0°С добавляли боргидрид натрия (8,0 мг, 0,20 ммоль). Реакционную смесь перемешивали при 0°С в течение 30 минут.Реакционную смесь гасили водой и экстрагировали ЕtOАс.Органические слои сушили с сульфатом натрия, фильтровали и концентрировали в вакууме. Неочищенный продукт очищали с помощью флэш-хроматографии (элюировали ЕtOАс/гептаном при 100% ЕtOАс), получая 40 мг требуемого продукта с выходом 44%. МС (ЭСИ) m/z: 488,1.
Стадия В: К раствору трет-бутил 4-гидрокси-3-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1 -ил]-2-пиридил]пиперидин-1 -карбоксилата (35 мг, 0,072 ммоль) в 1,4-диоксане (2,00 мл, 23,4 ммоль) добавляли хлороводород (4 моль/л) в 1,4-диоксане (1,00 мл, 4,00 ммоль). Реакционную смесь перемешивали при к.т.в течение 18 часов. Реакционную смесь концентрировали и очищали с помощью обращенно-фазовой ВЭЖХ, получая 265. МС (ЭСИ) m/z: 388,1.
Пример 166 1-(6-(2,5-Диазаспиро[3.5]нонан-2-ил)пиридин-2-ил)-6-(1-метил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин 266
Следуя способам, описанным в примере 124, и начиная с трет-бутил 2,5-диазаспиро[3.5]нонан-5-карбоксилата, 2-бром-6-фторпиридина и 6-хлор-1Н-пиразоло[4,3-с]пиридина, получали 266 в виде желтого твердого вещества (10 мг, 5%) в ходе четырех стадий. 1Н ЯМР (500 МГц, ДМСО-cfe) 6 (ppm) 9,12 (s, 1Н), 8,85 (s, 1Н), 8,52 (s, 1Н), 8,26 (s, 1Н), 7,92 (s, 1Н), 7,69-7,72 (t, J=16 Гц, 1Н), 7,18-7,19
(d, J=7,5 Гц, 1H), 6,33-6,34 (d, J=8 Гц, 1H), 4,00-4,01 (d, J=7 Гц, 2H), 3,92 (s, 3Н), 3,87-3,88 (d, J=7 Гц, 2H), 2,715-2,724 (d, J=4,5 Гц, 2H), 1,76-1,78 (t, J=11 Гц, 2H), 1,59-1,60 (d, J=3,5 Гц, 2H), 1,45 (s, 2H); МС (ЭСИ) m/z: 401 [М+Н]+.
Пример 167 1-(6-(2,6-Диазаспиро[3.3]гептан-2-ил)пиридин-2-ил)-6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин 267
Следуя способам, описанным в примере 88, и начиная с трет-бутил 2,6-диазаспиро[3.3]гептан-2-карбоксилата, 2-бром-6-фторпиридина и 6-хлор-1Н-пиразоло[4,3-с]пиридина, получали 267 в виде желтого твердого вещества (58 мг, 11%) в ходе пяти стадий. 1Н ЯМР (500 МГц, ДМСО-с(6) 5 (ppm) 9,15 (s, 1Н), 8,81 (s, 1Н), 8,54 (s, 1Н), 8,47 (s, 1Н), 8,14 (s, 1Н), 7,70-7,73 (t, J=10 Гц, 1Н), 7,21-7,22 (d, J=10 Гц, 1Н), 6,31-6,32 (d, J=9 Гц, 1Н), 5,23-5,27 (m, 2Н), 4,24 (s, 4Н), 4,07-4,08 (m, 1Н), 3,76-3,82 (m, 3Н), 3,42-3,43 (br, 1Н); МС (ЭСИ) m/z: 441 [М+Н]+.
Пример 168 1-(6-(2,6-Диазаспиро[3.3]гептан-2-ил)пиридин-2-ил)-6-(1-метил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин 268
Следуя способам, описанным в примере 124, и начиная с трет-бутил 2,6-диазаспиро[3.3]гептан-2-карбоксилата, 2-бром-6-фторпиридина, 6-хлор-1Н-пиразоло[4,3-с]пиридина и 1-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразола, получали 268 в виде желтого твердого вещества (87 мг, 26%) за четыре стадии. 1Н ЯМР (500 МГц, ДМСО-<У6) 6 (ppm) 9,10 (s, 1Н), 8,74 (s, 1Н), 8,51 (s, 1Н), 8,28 (s, 1Н), 7,98 (s, 1Н), 7,69-7,71 (t, J=9 Гц, 1Н), 7,20-7,21 (d, J=9 Гц, 1Н), 6,30-6,31 (d, J=9 Гц, 1Н), 4,24 (s, 3Н), 4,08 (s, 1Н), 3,86-3,93 (m, 3Н), 3,79-3,83 (m, 2Н), 3,35-3,42 (m, 3Н); МС (ЭСИ) m/z: 373 [М+Н]+.
Пример 169 1-(6-(2,5-Диазаспиро[3.5]нонан-2-ил)пиридин-2-ил)-6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин 269
Следуя способам, описанным в примере 88, и начиная с трет-бутил 2,5-диазаспиро[3.5]нонан-5-карбоксилата, 2-бром-6-фторпиридина и 6-хлор-1Н-пиразоло[4,3-с]пиридина, получали 269 в виде желтого твердого вещества (8 мг, 5%) в ходе пяти стадий. 1Н ЯМР (500 МГц, ДМСО-с/6) 5 (ppm) 9,15-9,16 (d, J=5 Гц, 1Н), 8,84 (s, 1Н), 8,53-8,55 (d, J=9,5 Гц, 1Н), 8,48 (s, 1Н), 8,28-8,29 (d, J=7,5 Гц, 1Н), 7,56-7,59 (t, J=15,5 Гц, 1Н), 7,05-7,09 (m, 2Н), 6,55-6,57 (d, J=8 Гц, 1Н), 5,21-5,26 (m, 2Н), 3,44-3,45 (d, J=4,5 Гц, 2Н), 3,33 (s, 1Н), 2,61-2,64 (t, J=13 Гц, 1Н), 1,90-1,97 (m, 2Н), 1,76 (s, 1Н), 1,57 (s, 1Н), 1,28-1,37 (m, 4Н); МС (ЭСИ) m/z: 469 [М+Н]+.
Пример 170 3-(Аминометил)-1-(6-(6-(1-метил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)азетидин-3-ол 270
Стадия А: 1-(6-(6-(1-Метил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)азетидин-3-он
206
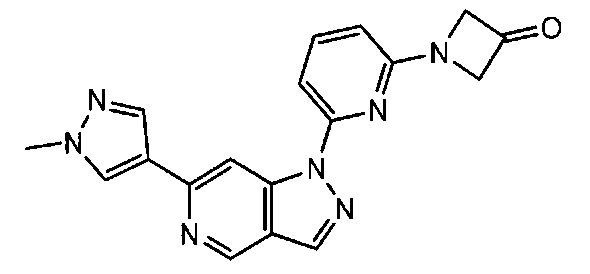
К раствору диметилсульфоксида (225 мг, 2,88 ммоль) в ДХМ (10 мл) при -60°С добавляли оксалилхлорид (366 мг, 2,88 ммоль). Затем смесь перемешивали при -60°С в течение 0,5 часа, к ней по каплям добавляли раствор 1-(6-(6-(1-метил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)азетидин-3-ола (200 мг, 0,58 ммоль) в ДХМ (10 мл) при -60°С.Реакционную смесь перемешивали при -60°С в течение 2 часов, и к ней добавляли триэтиламин (583 мг, 5,76 ммоль) по каплям. Реакционную смесь перемешивали при -60°С еще в течение часа. Ее концентрировали при пониженном давлении, получая белое твердое вещество. Неочищенный продукт (1,1 г), 1-(6-(6-(1-метил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)азетидин-3-он, использовали в следующей реакции без дополнительной очистки. МС (ЭСИ) m/z:.346 [М+Н]+.
Стадия В: 1-(6-(6-(1-Метил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-3-(нитрометил)азетидин-3-ол
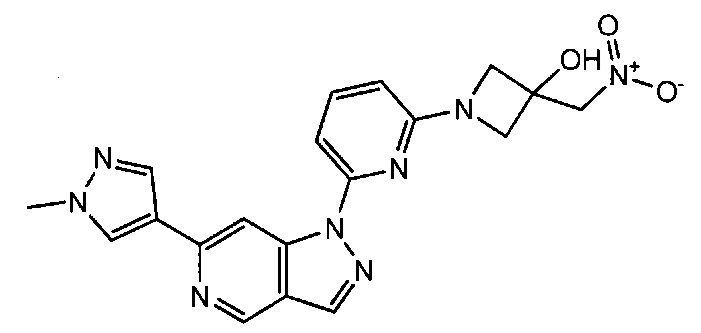
К раствору 1-(6-(6-(1-метил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)азетидин-3-она (1,1 г) в ДХМ (10 мл) при 20°С добавляли нитрометан (1 мл) и триэтиламин (0,5 мл). Смесь перемешивали при температуре окружающей среды в течение 2 часов. Ее концентрировали при пониженном давлении, получая белое твердое вещество. Неочищенный продукт (1,3 г), 1-(6-(6-(1-метил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-3-(нитрометил)азетидин-3-ол, использовали на следующей стадии без дополнительной очистки. МС (ЭСИ) m/z. 407 [М+Н]+.
Стадия С: 3-(Аминометил)-1-(6-(6-(1-метил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)азетидин-3-ол
207
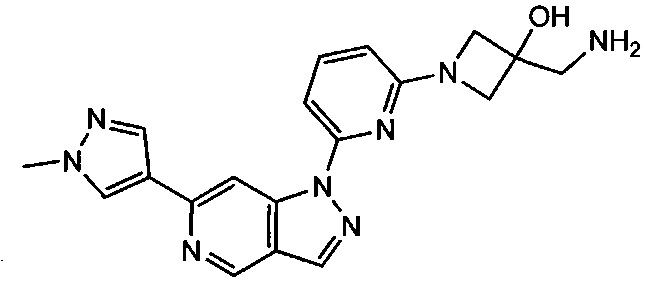
К раствору 1-(6-(6-(1-метил-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-3-(нитрометил)азетидин-3-ола (100 мг, 0,25 ммоль) в МеОН (5 мл) и Н20 (0,5 мл) добавляли порошок Zn (129 мг, 2 ммоль) и NH4CI (132 мг, 2,5 ммоль). Реакционную смесь перемешивали при температуре окружающей среды в течение 2 часов и фильтровали через Целит.Фильтрат концентрировали при пониженном давлении. Остаток очищали с помощью обращенно-фазовой препаративной ВЭЖХ, получая 270 в виде красного твердого вещества (60 мг, 64,8%). 1Н ЯМР (500 МГц, ДМСО-с/б) 6 (ppm) 9,13 (s, 1Н), 8,75 (s, 1Н), 8,53 (s, 1Н), 8,34-8,40 (m, 2Н), 7,98 (s, 1Н), 7,72-7,75 (m, 1Н), 7,24-7,25 (m, 1Н), 6,34-6,36 (d, J=8,5 Гц, 1Н), 4,23-4,25 (d, J=8,5 Гц, 2Н), 3,89-3,97 (m, 5Н), 3,06-3,10 (m, 2Н); МС (ЭСИ) т/г.377 [М+Н]+.
Пример 171 и 172 (R)-1 -[6-(4,4-дифтор-3-пиперидил)-2-пиридил]-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин 271 и (Э)-1-[6-(4,4-дифтор-3-пиперидил)-2-пиридил]-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин 272
Энантиомерные соединения 271 и 272 разделяли с помощью хирального разделения СФХ согласно примеру 159. 1Н ЯМР (400 МГц, ДМСО) δ 9,72 (s, 1Н), 9,46 (s, 1Н), 9,36 (s, 1Н), 8,74 (s, 1Н), 8,63 (s, 1Н), 8,04 (t, J=7,8 Гц, 1Н), 7,98 (d, J=8,2 Гц, 1Н), 7,40 (d, J=7,4 Гц, 1Н), 3,60-3,42 (m, 2Н), 3,18 (d, J=12,8 Гц, 1Н), 2,87 (t, J=12,6 Гц, 1Н), 2,67 (s, 3Н), 2,36 (d, J=18,3 Гц, 1Н), 2,21-2,09 (m, 1Н), 1,99 (d, J=34,4 Гц, 1Н). МС (ЭСИ) m/z: 408,1.
Пример 173 (6-(1-(6-(пиперазин-1-ил)пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридин-6-ил)пиразин-2-ил)метанола дигидрохлорид 273
Стадия А: трет-бутил 4-(6-(6-(6-формилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)пиперазин-1 -карбоксилат 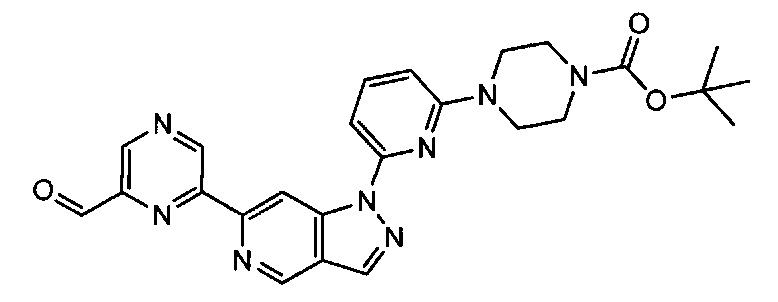
208
Раствор периодата натрия (260 мг, 1,22 ммоль) в 5 мл воды добавляли к раствору трет-бутил 4-[6-[6-[6-(1,2-дигидроксиэтил)пиразин-2-ил]пиразоло[4,3-с]пиридин-1 -ил]-2-пиридил]пиперазин-1 -карбоксилата (315 мг, 0,61 ммоль) в 25 мл тетрагидрофурана и 5 мл воды. Смесь перемешивали в течение 24 часов, концентрировали, остаток разделяли между этилацетатом и водой. Органические экстракты промывали водой, солевым раствором, сушили над сульфатом натрия и концентрировали. Остаток очищали на 12 г силикагелевой колонке, элюируя градиентом этилацетата в гептане, получая 245 мг (83%). МС (ЭСИ) m/z: 505,2 [М+Н20+Н]+.
Стадия В: трет-бутил 4-(6-(6-(6-(гидроксиметил)пиразин-2-ил)-1Н-
пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)пиперазин-1-карбоксилат
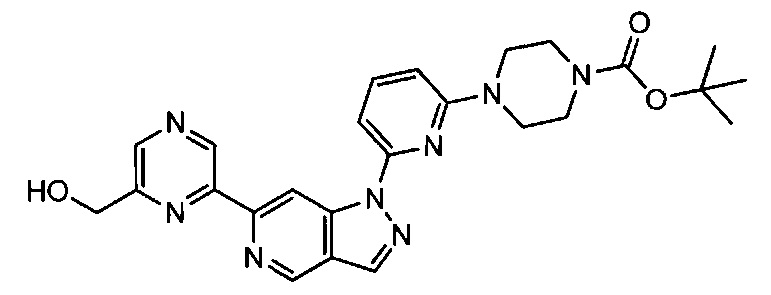
Боргидрид натрия (25 мг, 0,66 ммоль) добавляли частями к раствору трет-бутил 4-[6-[6-(6-формилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперазин-1-карбоксилата (162 мг, 0,33 ммоль) в 6 мл метанола. Смесь перемешивали в течение 1 часа, концентрировали в вакууме, остаток разделяли между этилацетатом и водой. Органические экстракты промывали водой, 1% водн. лимонной кислотой, водой и солевым раствором, сушили над сульфатом натрия и концентрировали. Остаток очищали на 12 г силикагелевой колонке, элюируя 0-7% градиентом метанола в ДХМ, получая 125 мг (77%). МС (ЭСИ) m/z: 489,2 [М+Н]+.
Стадия С: Соединение 273 получали обработкой 4 М HCI в диоксане в метаноле в течение 1-2 часов, собирали фильтрованием из реакционной смеси, растворяли в воде и лиофилизировали. 1Н ЯМР (400 МГц, ДМСО-с!6) 6 9,57 (s, 1Н), 9,52 (s, 1Н), 9,28 (s, 2Н), 8,81 (s, 1Н), 8,71 (s, 1Н), 7,88 (t, J=8,0 Гц, 1Н), 7,39 (d, J=7,8 Гц, 1Н), 6,95 (d, J=8,4 Гц, 1Н), 4,78 (s, 2Н), 3,96 (d, J=5,5 Гц, 4Н), 3,33 (d, J=5,1 Гц, 4Н). МС (ЭСИ) m/z: 389,2 [М+Н]+.
Пример 174 1-(6-(пиперазин-1-ил)пиридин-2-ил)-6-(6-винилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридина дигидрохлорид 274
Стадия А: трет-бутил 4-(6-(6-(6-винилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)пиперазин-1 -карбоксилат
209
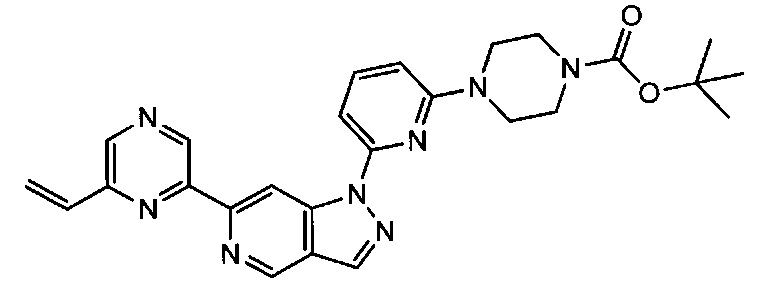
Смесь трет-бутил 4-[6-[6-(6-хлорпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперазин-1 -карбоксилата (493 мг, 1 ммоль), винилтрифторбората калия (335 мг, 2,500 ммоль), комплекса 1,1'-бис(дифенилфосфино)ферроцен-палладия (II) дихлорида, ДХМ (55 мг, 0,07500 ммоль) и триэтиламина (0,63 мл, 4,500 ммоль) в этаноле (9 мл) дегазировали и нагревали в закрытом сосуде в течение 2 часов при 105°С.Смесь оставляли при комнатной температуре на 20 часов. Осадок собирали и промывали этанолом, получая неочищенное вещество, 605 мг (99,8%). МС (ЭСИ) m/z: 485,4 [М+Н]+.
Стадия В: Соединение 274 получали обработкой 4 М HCI в диоксане в метаноле в течение 1-2 часов, собирали фильтрованием из реакционной смеси, растворяли в воде и лиофилизировали. 1Н ЯМР (400 МГц, ДМСО-с!6) 6 9,54 (s, 1Н), 9,46 (s, 1Н), 9,37 (s, 1Н), 9,09 (s, 2Н), 8,95 (s, 1Н), 8,72 (s, 1Н), 7,89 (t, J=8,1 Гц, 1Н), 7,39 (d, J=7,8 Гц, 1Н), 7,03 (dd, J=17,6, 11,0 Гц, 1Н), 6,96 (d, J=8,4 Гц, 1Н), 6,50 (d, J=17,3 Гц, 1Н), 5,80 (d, J=11,2 Гц, 1Н), 3,96 (t, J=5,3 Гц, 4Н), 3,27 (s, 4Н). МС (ЭСИ) m/z: 385,2 [М+Н]\
Пример 175 6-(6-Хлорпиразин-2-ил)-1 -(6-(пиперазин-1 -ил)пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридина дигидрохлорид 275
Стадия А: трет-бутил 4-(6-(6-(трибутилстаннил)-1Н-пиразоло[4,3-
с]пиридин-1 -ил)пиридин-2-ил)пиперазин-1 -карбоксилат
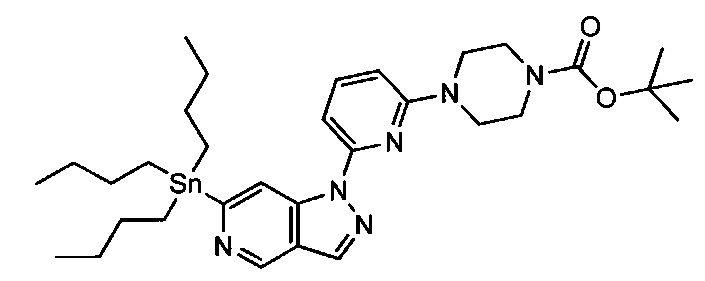
К смеси трет-бутил 4-(6-(6-хлор-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)пиперазин-1-карбоксилата (10 г, 0,024 моль) в ДМФА (100 мл) в атмосфере N2 добавляли LiCI (6,14 г, 0,145 моль), nBu6Sn2 (15,3 г, 0,0264 моль), Pd2(dba)3 (0,44 г, 0,48 ммоль) и Рсу3 (0,27 г, 0,96 ммоль). Полученную в результате смесь нагревали при 130°С в течение ночи. Смесь фильтровали через Целит.Фильтр экстрагировали петролейным эфиром (300 мл х 6). Объединенные органические слои сушили над Na2S04, фильтровали и концентрировали. Неочищенный
210
продукт очищали с помощью колоночной хроматографии на силикагеле (ПЭ:ЭА=50:1), получая 8 (4,5 г, выход 28%) в виде прозрачного масла. 1Н ЯМР (400 МГц, CDCI3) 5 9,26 (d, J=1,2 Гц, 1Н), 8,67-8,60 (m, 1Н), 8,25 (d, J=0,6 Гц, 1Н), 7,68 (t, J=8,1 Гц, 1Н), 7,38 (d, J=7,8 Гц, 1Н), 6,56 (d, J=8,3 Гц, 1Н), 3,66 (s, 9Н), 1,66 -1,57 (m, 6Н), 1,52 (s, 8Н), 1,36 (dd, J=14,6, 7,1 Гц, 6Н), 1,23-1,15 (m, 6Н), 0,88 (t, J=7,3 Гц, 9Н). МС (ЭСИ) m/z: 671 [М+Н]+.
Стадия В: трет-бутил 4-(6-(6-(6-хлорпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)пиперазин-1 -карбоксилат
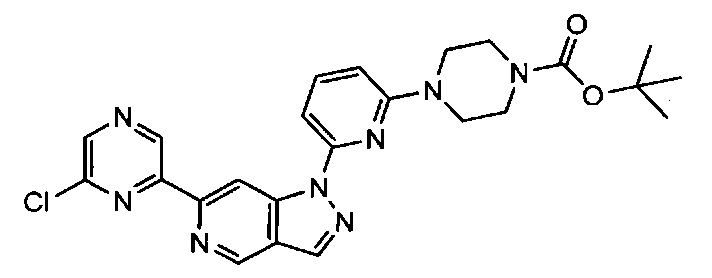
Смесь трет-бутил 4-(6-(6-(трибутилстаннил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)пиперазин-1-карбоксилата (27 г, 0,04 моль), 2,6-дихлорпиразина (8,9 г, 0,06 моль), Pd2(dba)3 (0,37 г, 0,4 ммоль) и Рсу3 (0,23 г, 0,8 ммоль) в ДМА (150 мл) продували N2 в течение 1 минуты. Реакционную смесь нагревали при 130°С в течение ночи. Смесь охлаждали до комнатной температуры, добавляли воду и немного ЭА, перемешивали в течение 10 минут и фильтровали, промывая МТБЭ. Неочищенный продукт очищали с помощью колоночной хроматографии на силикагеле (ПЭ:ЭА=1:1), получая 9 (6,1 г, 30%) в виде желтого твердого вещества. 1Н ЯМР (400 МГц, ДМСО) 5 9,58 (d, J=18,5 Гц, 2Н), 9,33 (s, 1Н), 8,90 (s, 1Н), 8,69 (s, 1Н), 7,80 (t, J=8,1 Гц, 1Н), 7,32 (d, J=7,8 Гц, 1Н), 6,85 (d, J=8,4 Гц, 1Н), 3,64 (s, 8Н), 1,55-1,38 (m, 9Н). МС (ЭСИ) m/z: 493 [М+Н]+.
Стадия С: Соединение 275 получали, удаляя защитную группу Вое с помощью 4 М HCI в диоксане в метаноле. Соответствующий гидрохлорид собирали фильтрованием из реакционной смеси, растворяли в воде и лиофилизировали. 1Н ЯМР (400 МГц, flMCO-d6) 6 9,63 (s, 1Н), 9,51 (s, 1Н), 9,38 (s, 1Н), 9,12 (s, 2Н), 8,91 (s, 1Н), 8,73 (s, 1Н), 7,89 (t, J=8,1 Гц, 1Н), 7,40 (d, J=7,8 Гц, 1Н), 6,95 (d, J=8,4 Гц, 1Н), 3,97 (t, J=5,3 Гц, 4Н), 3,37 (s, 4Н). МС (ЭСИ) m/z: 393,0 [М+Н]+.
Пример 176 6-(6-(бензилокси)пиразин-2-ил)-1 -(6-(пиперазин-1 -ил)пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридин 276
Стадия А: трет-бутил 4-(6-(6-(6-(бензилокси)пиразин-2-ил)-1Н-
пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)пиперазин-1-карбоксилат
211
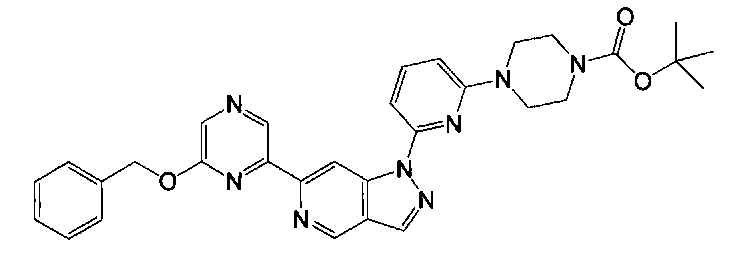
Смесь 3-5 экв. бензилового спирта, 1 экв. трет-бутил 4-(6-(6-(6-хлорпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)пиперазин-1 -карбоксилата, 6-10 экв. трет-бутилата калия в диоксане нагревали при 90°С в течение 2-4 часов. Смесь смешивали с водой и экстрагировали этилацетатом. Органические экстракты промывали водой, солевым раствором, сушили над сульфатом натрия и концентрировали в вакууме. Неочищенные продукты очищали на силикагелевой колонке, элюируя градиентом этилацетата в гептане или метанола в ДХМ, получая трет-бутил 4-(6-(6-(6-(бензилокси)пиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)пиперазин-1-карбоксилат в виде соли дигидрохлорида. МС (ЭСИ) m/z: 603,4 [М+Н]+.
Стадия В: Соединение 276 в виде соли дигидрохлорида получали, удаляя защитную группу Вое с помощью 4 М HCI в диоксане в метаноле в течение 1-2 часов. Соответствующие гидрохлориды собирали фильтрованием из реакционной смеси, растворяли в воде и лиофилизировали. МС (ЭСИ) m/z: 465,3 [М+Н]+.
Пример 177 1-(6-(1-(6-(пиперазин-1-ил)пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридин-6-ил)пиразин-2-ил)этан-1,2-диол 277
Стадия А: трет-бутил 4-(6-(6-(6-(1,2-дигидроксиэтил)пиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)пиперазин-1-карбоксилат
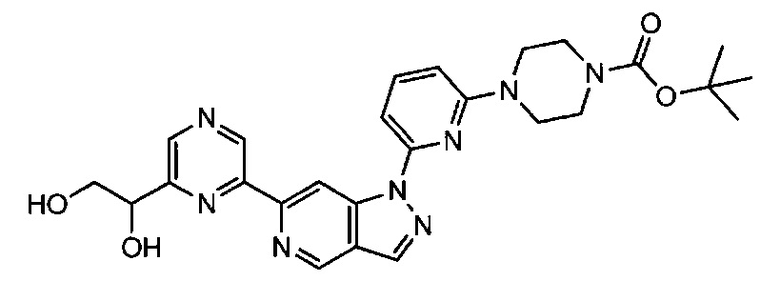
Смесь трет-бутил 4-[6-[6-(6-винилпиразин-2-ил)пиразоло[4,3-с]пиридин-1 -ил]-2-пиридил]пиперазин-1-карбоксилата (513 мг; 1,06 ммоль), N-метилморфолин-1Ч-оксида моногидрата (744 мг, 6,35 ммоль) и 2,5% раствора тетроксида осмия в трет-бутаноле (0,6 мл, 0,04764 ммоль) в 20 мл ацетона и 2,5 мл воды перемешивали при комнатной температуре в течение 24 часов. Смесь фильтровали, смешивали с водой и экстрагировали ЕtOАс.Органические экстракты промывали водой, 5% водн. лимонной кислотой, насыщ. водн.
212
NaHC03, солевым раствором, сушили над Na2S04 и концентрировали. Остаток растирали с этиловым эфиром, осадок собирали фильтрованием и промывали этиловым эфиром, получая трет-бутил 4-(6-(6-(6-(1,2-дигидроксиэтил)пиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)пиперазин-1 -карбоксилат (424 мг, 67%). МС (ЭСИ) m/z: 519,3 [М+Н]+.
Стадия В: Соединение 277 получали в виде соли гидрохлорида обработкой 4 М HCI в диоксане в метаноле в течение 1-2 часов, собирали фильтрованием из реакционной смеси, растворяли в воде и лиофилизировали. 1Н ЯМР (400 МГц, ДМСО-С16) 6 9,57 (s, 1Н), 9,46 (s, 1Н), 9,37 (d, J=1,0 Гц, 1Н), 9,17 (s, 2Н), 8,81 (s, 1Н), 8,72 (s, 1Н), 7,88 (t, J=8,1 Гц, 1Н), 7,40 (d, J=7,8 Гц, 1Н), 6,96 (d, J=8,4 Гц, 1Н), 4,80 (t, J=5,5 Гц, 1Н), 3,98 (t, J=5,3 Гц, 4Н), 3,83 (dd, J=11,1, 5,0 Гц, 1Н), 3,75 (dd, J=11,1, 6,0 Гц, 1Н), 3,33 (s, 4Н). МС (ЭСИ) m/z: 419,2 [М+Н]+.
Пример 178 2-((6-(1-(6-(пиперазин-1-ил)пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридин-6-ил)пиразин-2-ил)окси)этанола дигидрохлорид 278
Следуя способам, описанным в примере 176, и с 3-5 экв. 2-((тетрагидро-2Н-пиран-2-ил)окси)этанола получали 278. 1Н ЯМР (400 МГц, flMCO-d6) 6 9,35 (s, 1Н), 9,24 (m, 3Н), 8,71 (s, 1Н), 8,42 (s, 1Н), 7,88 (t, J=8,1 Гц, 1Н), 7,36 (d, J=7,8 Гц, 1Н), 6,96 (d, J=8,4 Гц, 1Н), 4,49 (t, J=5,0 Гц, 2Н), 3,97 (t, J=5,3 Гц,4Н), 3,89 (t, J=5,0 Гц, 2Н), 3,27 (s, 4Н). МС (ЭСИ) m/z: 419,2 [М+Н]+.
Пример 179 6-(6-(дифторметил)пиразин-2-ил)-1-(6-(пиперазин-1-ил)пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридина трифторацетат 279
Стадия А: трет-бутил 4-(6-(6-(6-(дифторметил)пиразин-2-ил)-1Н-
пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)пиперазин-1-карбоксилат
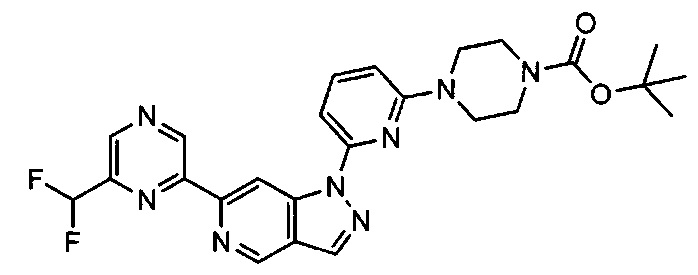
Смесь трет-бутил 4-[6-[6-(6-формилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперазин-1-карбоксилата (49 мг, 0,10 ммоль) и Deoxo-fluor® (50 масс. %) в толуоле (0,175 мл, 0,40 ммоль) в 4 мл ДХМ перемешивали в течение 24 часов. Смесь концентрировали в вакууме, остаток разделяли между этилацетатом и насыщенным водным гидрокарбонатом натрия. Органические экстракты промывали вода, 5% водной лимонной кислотой, водой, солевым раствором, сушили над сульфатом натрия и концентрировали. Неочищенный остаток очищали на 4 г силикагелевой колонке, элюируя 0-70% градиента
этилацетата в гептане, получая 38 мг трет-бутил 4-(6-(6-(6-(дифторметил)пиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)пиперазин-1-карбоксилата (74%). МС (ЭСИ) m/z: 509,3 [М+Н]+.
Стадия В: Раствор трет-бутил 4-[6-[6-[6-(дифторметил)пиразин-2-ил]пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперазин-1-карбоксилата (16) (38 мг, 0,075 ммоль) в 3 мл трифторуксусной кислоты перемешивали в течение 2 часов. Смесь концентрировали в вакууме, остаток растирали с этиловым эфиром, собирая осадок фильтрованием. Твердое вещество промывали этиловым эфиром, сушили на воздухе, повторно растворяли в воде и лиофилизировали, получая 279 в виде соли трифторацетата (16 мг, 42%). 1Н ЯМР (400 МГц, ДМСО-d6) 6 9,86 (s, 1Н), 9,51 (s, 1Н), 9,41 (s, 1Н), 9,07 (s, 1Н), 8,89 (d, J=30,2 Гц, 2Н), 8,74 (s, 1Н), 7,89 (t, J=8,1 Гц, 1Н), 7,41 (d, J=7,8 Гц, 1Н), 7,25 (t, J=54,2 Гц, 1Н), 6,96 (d, J=8,4 Гц, 1Н), 3,94 (t, J=5,3 Гц, 4Н), 3,36-3,31 (m, 4Н). МС (ЭСИ) m/z: 409,2 [М+Н]+.
Пример 180 (8)-(1-(6-(1-(6-(пиперазин-1-ил)пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридин-6-ил)пиразин-2-ил)пирролидин-2-ил)метанола дигидрохлорид 280
Смесь 3-5 экв. (8)-пирролидин-2-илметанола, 1 экв. трет-бутил 4-(6-(6-(6-хлорпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1 -ил)пиридин-2-ил)пиперазин-1 -карбоксилата, 6-10 экв. фторида цезия в ДМСО нагревали при 105°С в течение 12-24 часов. Смесь смешивали с водой и экстрагировали этилацетатом. Органические экстракты промывали водой, солевым раствором, сушили над сульфатом натрия и концентрировали в вакууме. Неочищенные продукты очищали на силикагелевой колонке, элюируя градиентом этилацетата в гептане или ДХМ. Группу Вое удаляли с помощью 4 М HCI в диоксане в метаноле. Неочищенный продукт собирали фильтрованием, растворяли в воде и лиофилизировали, получая 280.1Н ЯМР (400 МГц, flMCO-d6) 6 9,37 (s, 1Н), 9,31 -9,19 (m, 2Н), 9,10 (s, 1Н), 8,80 (s, 1Н), 8,73 (s,1H), 8,19 (s, 1Н), 7,89 (t, J=8,1 Гц, 1Н), 7,35 (d, J=7,8 Гц, 1Н), 6,97 (d, J=8,5 Гц, 1Н), 4,21 (d, J=6,0 Гц, 1Н), 3,93 (t, J=5,3 Гц, 4Н), 3,58 (m, 1Н), 3,49 (m, 2Н), 3,22 (d, J=5,4 Гц, 4Н), 2,06 (m, 4Н). МС (ЭСИ) m/z: 458,3.
Пример 181 1-(6-(1-(6-(пиперазин-1-ил)пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридин-6-ил)пиразин-2-ил)азетидин-3-ол 281
Следуя способам, описанным в примере 180, получали 281. 1Н ЯМР (400 МГц, flMCO-d6) 5 9,28 (s, 1Н), 9,22 (s, 1Н), 8,91 (s, 1Н), 8,64 (s, 1Н), 8,27 (s, 1Н),7,96 (s, 1Н), 7,77 (t, J=8,1 Гц, 1Н), 7,24 (d, J=7,7 Гц, 1Н), 6,83 (d, J=8,4 Гц,
1Н), 4,72-4,62 (m,1H), 4,37 (dd, J=8,7, 6,7 Гц, 2H), 3,89 (dd, J=8,9, 4,6 Гц, 2H), 3,63 (t, J=5,1 Гц, 4H), 2,86 (dd, J=6,3, 3,9 Гц, 4H). МС (ЭСИ) m/z: 430,3.
Пример 182 2-[[6-[1 -(6-пиперазин-1 -ил-2-пиридил)пиразоло[4,3-с]пиридин-6-ил]пиразин-2-ил]амино]этанол 282
Следуя способам, описанным в примере 180, получали 282. 1Н ЯМР (400 МГц, flMCO-d6) 5 9,41 (d, J=7,8 Гц, 3Н), 9,21 (s, 1Н), 8,78 (s, 1Н), 8,70 (s, 1Н), 8,13 (s, 1Н), 7,89 (t, J=8,1 Гц, 1Н), 7,35 (d, J=7,8 Гц, 1Н), 6,98 (d, J=8,5 Гц, 1Н), 3,97 (t, J=5,2 Гц,4Н), 3,68 (t, J=5,9 Гц, 2Н), 3,60-3,51 (m, 2Н), 3,25 (s, 4Н). МС (ЭСИ) m/z: 418,2.
Пример 183 (18,28)-2-((6-(1-(6-(пиперазин-1-ил)пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридин-6-ил)пиразин-2-ил)амино)циклопентанол 283
Следуя способам, описанным в примере 180, получали 283. 1Н ЯМР (400 МГц, flMCO-d6) 6 9,38 (s, 1Н), 9,22 (s, 2Н), 9,19 (s, 1Н), 8,74 (s, 1Н), 8,69 (s, 1Н), 8,09 (s, 1Н), 7,89 (t, J=8,1 Гц, 1Н), 7,35 (d, J=7,8 Гц, 1Н), 7,18 (s, 1Н), 6,98 (d, J=8,4 Гц, 1Н), 4,01 (t, J=5,1 Гц, 2Н), 3,94 (t, J=5,2 Гц, 4Н), 3,25 (s,4H), 2,19 (dq, J=13,7, 6,8 Гц, 1Н), 1,90 (ddt, J=14,6, 8,9, 4,2 Гц, 1Н), 1,73 (tp, J=10,3, 5,3 Гц, 2Н), 1,56 (ddq, J=26,2, 13,5, 6,9, 6,0 Гц, 2Н). МС (ЭСИ) m/z: 458,3.
Пример 184 6-(6-(азетидин-1 -ил)пиразин-2-ил)-1 -(6-(пиперазин-1 -ил)пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридин 284
Следуя способам, описанным в примере 180, получали 284. 1Н ЯМР (400 МГц, flMCO-d6) 6 9,25 (d, J=18,9 Гц, 2Н), 8,89 (s, 1Н), 8,64 (s, 1Н), 7,93 (s, 1Н), 7,77 (t, J=8,1 Гц, 1Н), 7,22 (d, J=7,7 Гц, 1Н), 6,82 (d, J=8,5 Гц, 1Н), 4,16 (t, J=7,5 Гц, 4Н), 3,60 (dd, J=6,3, 3,8 Гц, 4Н), 2,84 (dd, J=6,1, 4,0 Гц, 4Н), 2,44 (q, J=7,5 Гц, 2Н). МС (ЭСИ) m/z: 414,2.
Пример 185 М-этил-6-(1-(6-(пиперазин-1-ил)пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридин-6-ил)пиразин-2-амин 285
Следуя способам, описанным в примере 180, получали 285 в виде соли дигидрохлорида. 1Н ЯМР (400 МГц, flMCO-d6) 6 9,32 (s, 1Н), 9,24 (s, 2Н), 9,17 (s, 1Н), 8,73 (s, 1Н), 8,70 (s, 1Н), 8,03 (s, 1Н), 7,88 (t, J=8,1 Гц, 1Н), 7,35 (d, J=7,7 Гц, 1Н), 7,20 (s, 1Н), 6,97 (d, J=8,4 Гц, 1Н), 3,95 (t, J=4,2 Гц, 4Н), 3,44 (q, J=7,2 Гц, 2Н), 3,23 (t, J=4,2 Гц, 4Н), 1,27 (t, J=7,2 Гц, 3Н). МС (ЭСИ) m/z: 402,2.
Пример 186 2-((6-(1-(6-(пиперазин-1-ил)пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридин-6-ил)пиразин-2-ил)окси)этанамин 286
Следуя способам, описанным в примере 176, получали 286 в виде соли тригидрохлорида. МС (ЭСИ) m/z: 418,3 [М+Н]+.
Пример 901 Активность связывания киназы Pim
Ферменты PIM-1, -2 и -3 получали как гибридные белки, экспрессированные в бактерии, и очищали с помощью колоночной хроматографии IMAC (Sun, X., Chiu, J.F., and Не, Q.Y. (2005) Expert Rev. Proteomics, 2:649-657). Флуоресцентно-меченный Pim-специфический пептидный субстрат по заказу синтезировала American Peptide Company (Sunnyvale, CA). Рабочий буфер содержал 10 мМ HEPES, рН 7,2, 10 мМ MgCI2, 0,01% Твин 20, 2 мМ ДТТ. Конечный буфер содержал 190 мМ HEPES, рН 7,2, 0,015% Brij-35, 0,2% покрывающего реагента 3 (Caliper Life Sciences, Hopkinton, MA), 20 мМ ЭДТА. Разделительный буфер содержал 100 мМ HEPES, рН 7,2, 0,015% Brij-35, 0,1% покрывающего реагента 3, 1:200 покрывающего реагента 8 (Caliper Life Sciences, Hopkinton, MA), 10 мМ ЭДТА и 5% ДМСО.
Реакции с PIM проводили в конечном объеме 10 мкл на лунку в 384-луночном планшете. Стандартную ферментативную реакцию инициировали, добавляя 5 мкл 2Х АТФ и исследуемого соединения к 5 мкл 2Х фермента и FAM-пептида, содержащим 20 пМ PIM1, 50 пМ PIM2 или 55 пМ PIM3, 1 мкМ FAM-пептид и 10 мкМ АТФ, в рабочий буфер. Через 90 минут инкубации при комнатной температуре реакцию фосфорилирования останавливали, добавляя 10 мкл конечного буфера. Продукт и субстрат в каждой независимой реакции разделяли на 12-канальном микрожидкостном чипе (Caliper Life Sciences, Hopkinton, MA), работающем на Caliper LC3000® (Caliper Life Sciences, Hopkinton, MA). Разделение продукта и субстрата оптимизировали, выбирая электрическое напряжение и давление, используя программное обеспечение устройства оптимизации для Caliper (Hopkinton, MA). Для разделения использовали условия нисходящего напряжения -500 В, восходящего напряжения -2150 В и давления скрининга -1,2 пси. Продукт и флуорофор субстрата возбуждали при 488 нм и детектировали при 530 нм. Превращение субстрата рассчитывали по электрофореграмме, используя программное обеспечение HTS Well Analyzer (Caliper Life Sciences, Hopkinton, MA). Вычисляли 3Начения Ki для исследуемого соединения. Смотрите в таблицах 3 и 4 репрезентативные Ki для PIM1, PIM2, PIM3 LC3K в микромолярных 3Начениях примерных соединений.
Пример 902 Анализы эффективности пролиферации клеток in vitro
Родительскую линию BaF3 получали из архива DSMZ. Получали линии BaF3, трансфицированные с PIM1 или PIM2. ИЛ-3 мышей покупали у R&D Systems. G418 покупали у Clontech. Среда для родительской линии BaF3 содержала RPMI, 10% ЭБС, 2 мМ L-глутамин, 2 нг/мл мИЛ-3. Среда для линий BaF3 PIM1 & 2 содержала RPMI, 10% ЭБС, 2 мМ L-глутамин, 250 мкг/мл. Среда
216
для линии MM1.S (клетки множественной миеломы) содержала RPMI, 10% ЭБС, 2 мМ L-глутамин.
BaF3, мышиная интерлейкин-3 зависимая pro-В клеточная линия, родительские клетки, клетки BaF3 PIM1, клетки BaF3 PIM2 и клетки MM1.S (множественная миелома) высевали при 2к/лунка, бкУлунка, 5к/лунка и 10k/лунка соответственно в 384-луночный планшет при 45 мкл/лунка. Исследуемое соединение добавляли при 5 мкл/лунка. Клетки BaF3 (родительские и трансфицированные) инкубировали в течение ночи, при этом клетки MM1.S инкубировали в течение 72 часов при 37°С, 5% С02. Реактив CELL TITER GLO® (Promega) добавляли при 50 мкл/лунка, планшеты инкубировали в течение 30 минут, и их люминесценцию считывали на НТ Analyst. Вычисляли 3Начения ИК50/ЕС50 исследуемого соединения.
Репрезентативные соединения настоящего изобретения исследовали, как описано выше, и было найдено, что они проявляют Ki/HK5o/EC5o, как показано ниже, в таблицах 3 и 4. 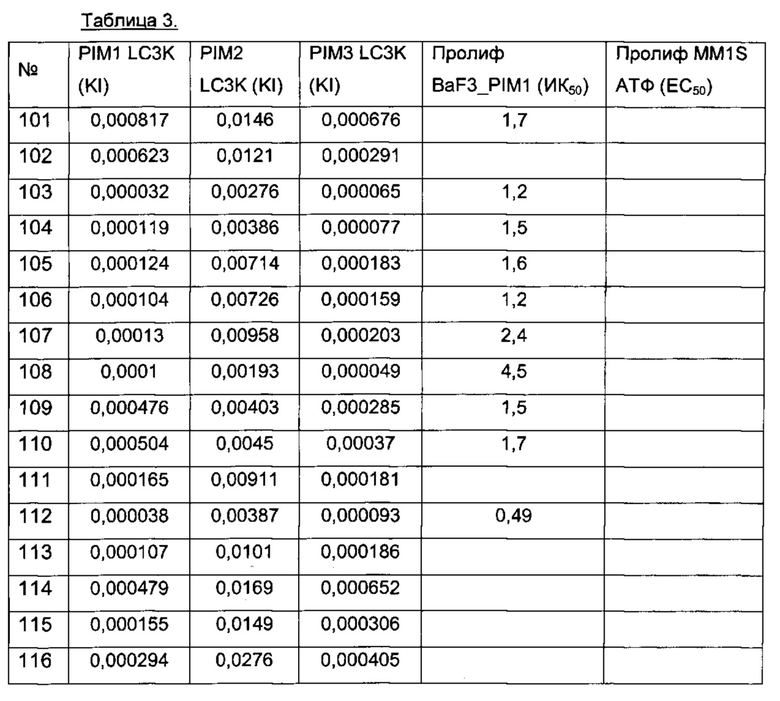
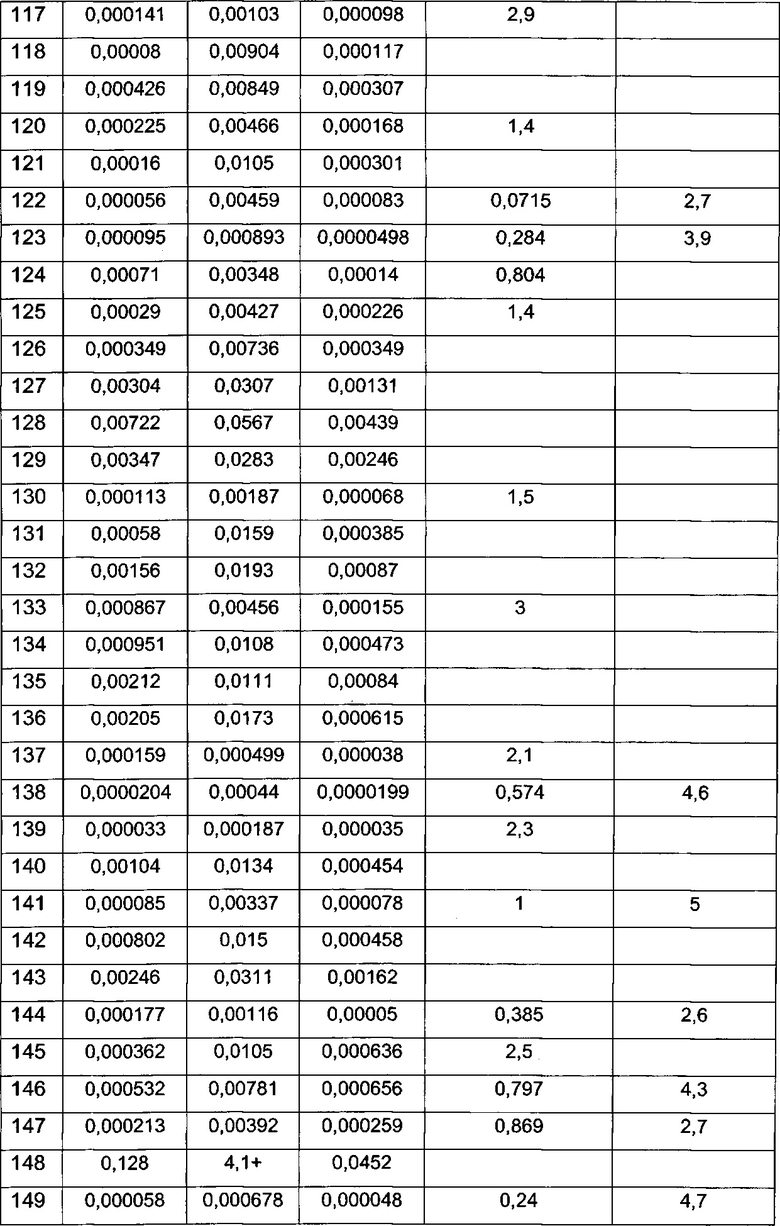
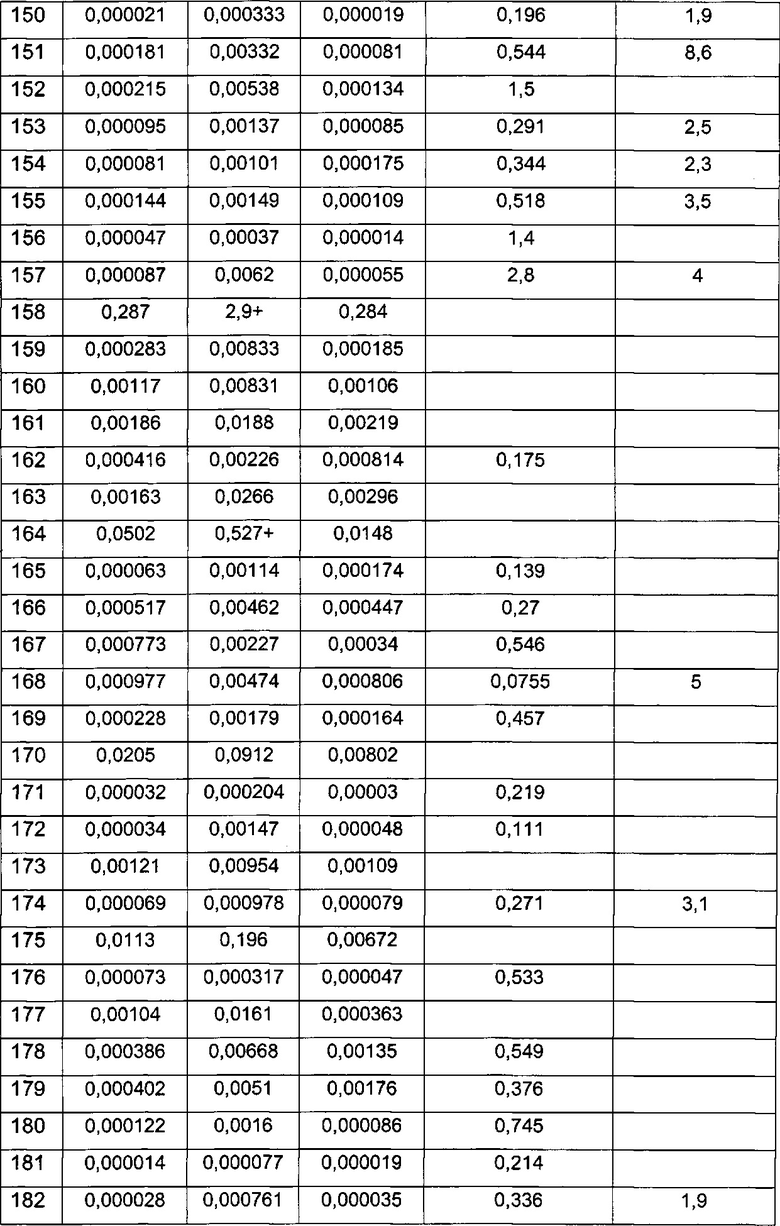
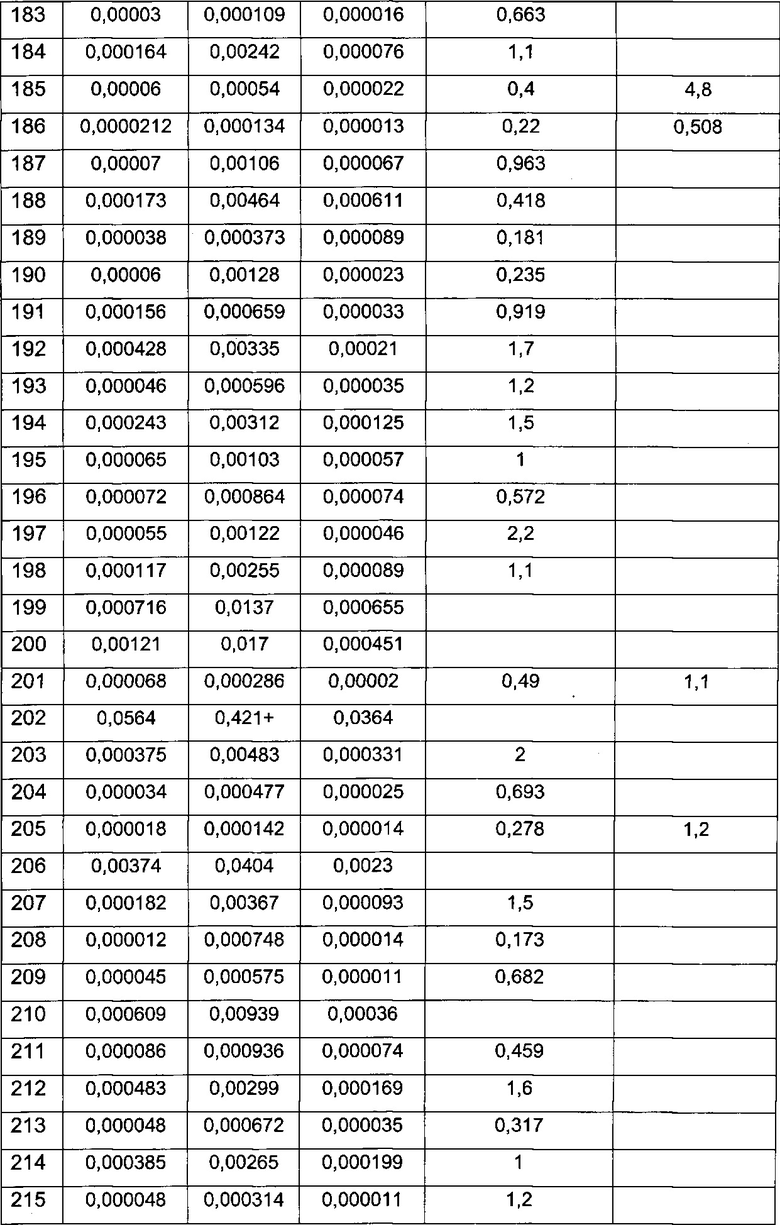
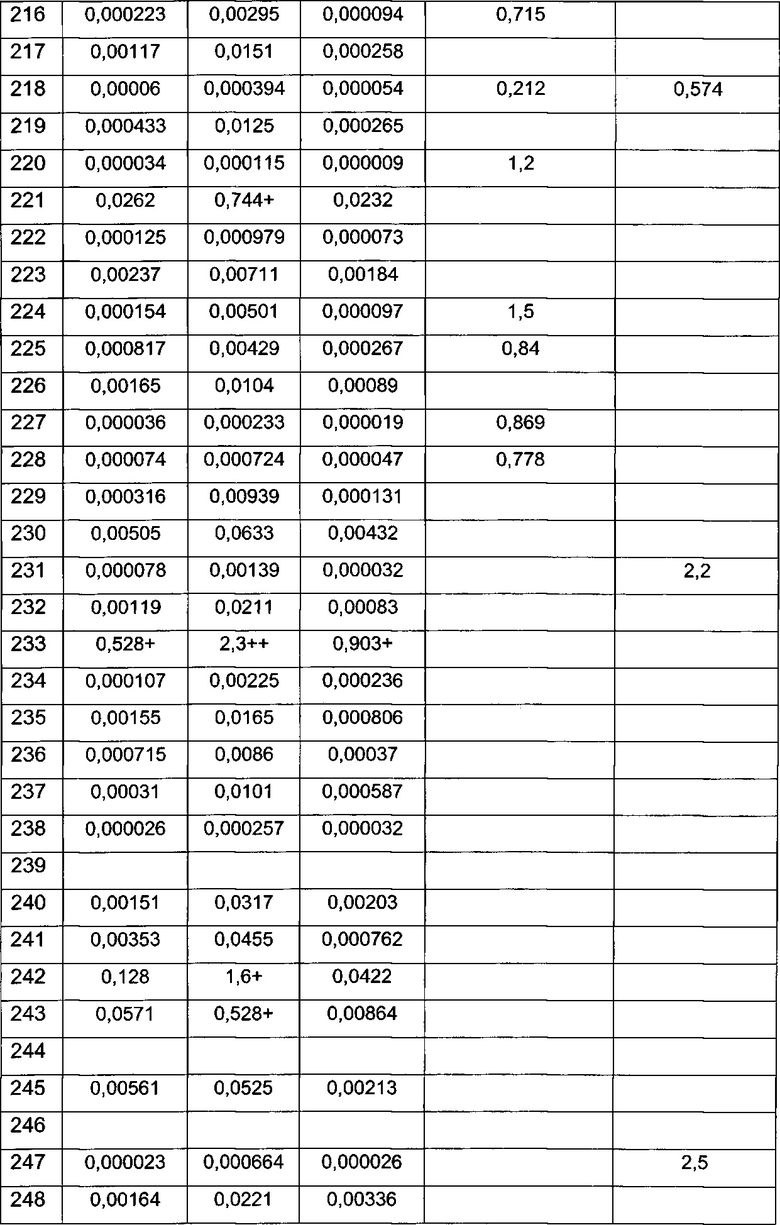
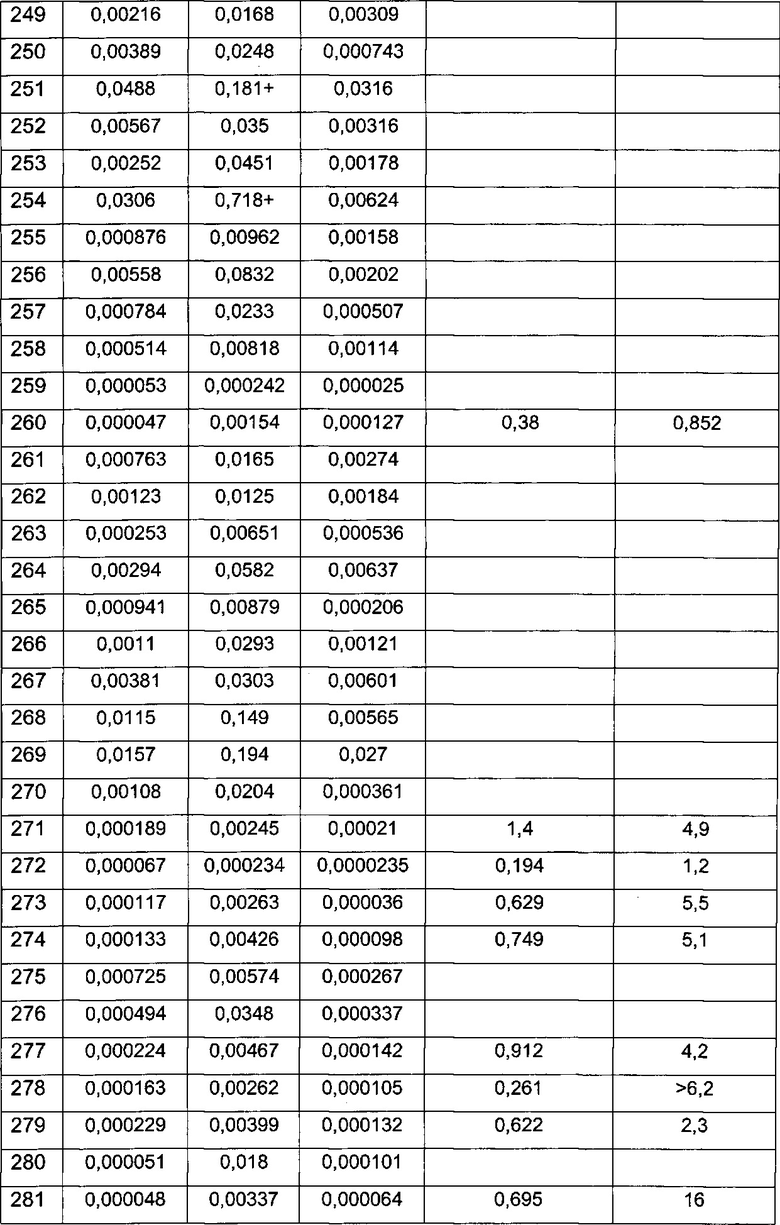
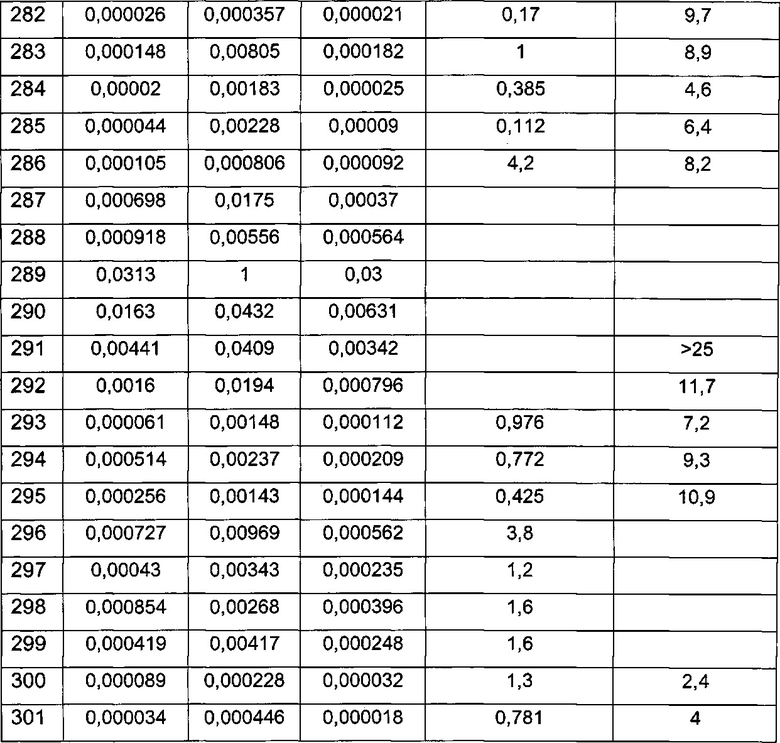
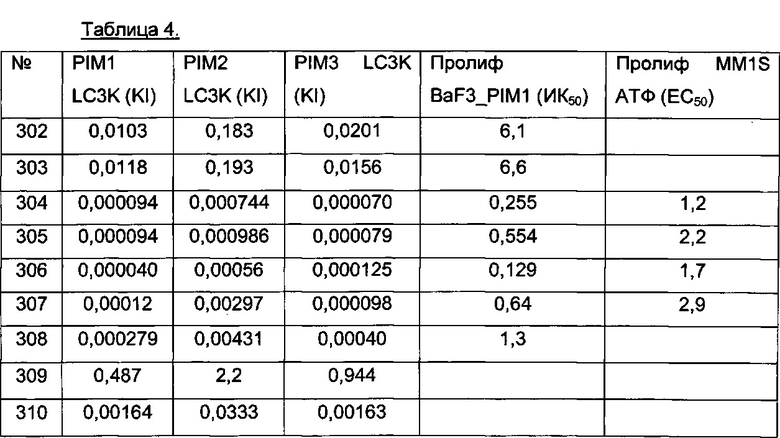
223
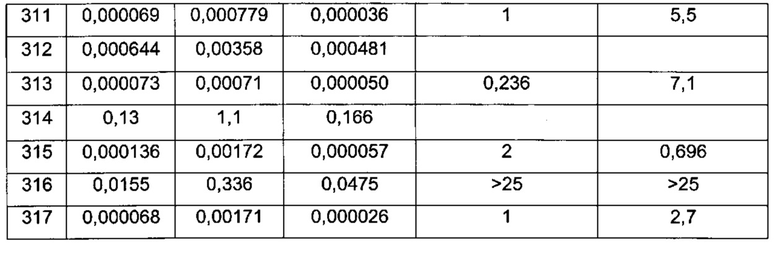
Несмотря на то, что вышеизложенное изобретение описано довольно подробно с помощью иллюстраций и примеров в целях разъяснения, описание и примеры не должны рассматриваться как ограничение объема изобретения. Все патенты и научная литература, приведенные в этом документе, включены в этот документ полностью путем ссылки на них.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЗАМЕЩЕННОЕ ПРОИЗВОДНОЕ 2Н-ПИРАЗОЛА | 2016 |
|
RU2722363C2 |
| ТРИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ, ОБЕСПЕЧИВАЮЩИЕ РАЗРУШЕНИЕ БЕЛКА IKAROS И БЕЛКА AIOLOS | 2020 |
|
RU2833608C2 |
| Применение 1H-пиразоло[4,3-b]пиридинов в качестве ингибиторов PDE1 | 2017 |
|
RU2759380C2 |
| ИНГИБИТОРЫ ФУРИНА | 2019 |
|
RU2799824C2 |
| БИЦИКЛИЧЕСКИЕ ЛАКТАМЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2827714C1 |
| ХИМИЧЕСКИЕ СОЕДИНЕНИЯ 637: ПИРИДОПИРИМИДИНДИОНЫ В КАЧЕСТВЕ ИНГИБИТОРОВ PDE4 | 2008 |
|
RU2479584C2 |
| ПРОИЗВОДНЫЕ МОРФОЛИН-ПИРИДИНА | 2015 |
|
RU2690154C2 |
| НОВЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ КАК ИНГИБИТОРЫ МОНОАЦИЛГЛИЦЕРИНЛИПАЗЫ | 2019 |
|
RU2769507C1 |
| КОМПОЗИЦИИ, СОДЕРЖАЩИЕ БЕНЗОПИПЕРАЗИН, В КАЧЕСТВЕ ИНГИБИТОРОВ БРОМОДОМЕНОВ ВЕТ | 2014 |
|
RU2720237C2 |
| СОЕДИНЕНИЯ ПИРИДАЗИНАМИДА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ТИРОЗИНКИНАЗЫ СЕЛЕЗЕНКИ (SYK) | 2013 |
|
RU2627661C2 |
Изобретение относится к конкретным соединениям, являющимся производными 5-азаиндазола, которые указаны в формуле изобретения. Эти соединения полезны для ингибирования киназы Pim и для лечения заболеваний, таких как рак, опосредованных киназой Pim. Раскрыты способы применения соединений формулы (I) в in vitro, in situ и in vivo диагностике, предотвращении или лечении подобных заболеваний в клетках млекопитающих или связанных патологических состояний. 4 н. и 2 з.п. ф-лы, 4 табл., 188 пр.
1. Соединение, выбранное из следующих соединений:
6-(1-этилпиразол-4-ил)-1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридина;
6-(1-метилпиразол-4-ил)-1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридина;
1-[6-(1,4-диазепан-1-ил)-2-пиридил]-6-(5-изопропил-3-пиридил)пиразоло[4,3-с]пиридина;
6-(5-этил-3-пиридил)-1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридина;
6-(5-изопропил-3-пиридил)-1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридина;
1-[6-[6-(5-этил-3-пиридил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-1,4-диазепан-6-ол;
(3R)-1-[6-[6-(5-изопропил-3-пиридил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-3-амина;
(3S)-1-[6-[6-(5-изопропил-3-пиридил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-3-амина;
5-[1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридин-6-ил]тиазола;
(3R)-1-[6-(6-тиазола-5-илпиразоло[4,3-с]пиридин-1-ил)-2-пиридил]пиперидин-3-амина;
6-(5-циклопропил-3-пиридил)-1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридина;
6-(5-циклопропил-3-пиридил)-1-[6-(1,4-диазепан-1-ил)-2-пиридил]пиразоло[4,3-с]пиридина;
1-[6-[(3S)-3-метилпиперазин-1-ил]-2-пиридил]-6-[5-(оксетан-3-ил)-3-пиридил]пиразоло[4,3-с]пиридина;
6-[5-(оксетан-3-ил)-3-пиридил]-1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридина;
1-[6-[6-(5-циклопропил-3-пиридил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-1,4-диазепан-6-ола;
1-[6-[6-[5-(оксетан-3-ил)-3-пиридил]пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-1,4-диазепан-6-ола;
(3S)-1-[3-хлор-6-[6-(5-этил-3-пиридил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-3-амина;
1-[6-(1,4-диазепан-1-ил)-2-пиридил]-6-[5-(оксетан-3-ил)-3-пиридил]пиразоло[4,3-с]пиридина;
3-метил-5-[1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридин-6-ил]изотиазола;
5-[1-[6-(1,4-диазепан-1-ил)-2-пиридил]пиразоло[4,3-с]пиридин-6-ил]-3-метил-изотиазола;
(S)-1-[6-[6-(5-этил-3-пиридил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-1,4-диазепан-6-ола;
(R)-1-[6-[6-(5-этил-3-пиридил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-1,4-диазепан-6-ола;
6-(6-метилпиразин-2-ил)-1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридина;
(3S)-1-[6-[6-(3-метилизотиазола-5-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-3-амина;
1-[6-(1,4-диазепан-1-ил)-2-пиридил]-6-(1-этилпиразол-4-ил)пиразоло[4,3-с]пиридина;
6-(1-этилпиразол-4-ил)-1-[6-[(3S)-3-метилпиперазин-1-ил]-2-пиридил]пиразоло[4,3-с]пиридина;
(3S)-1-[6-[6-(1-этилпиразол-4-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пирролаидин-3-ола;
(3R)-1-[6-[6-(1-этилпиразол-4-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пирролаидин-3-ола;
1-[6-[6-(1-этилпиразол-4-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-4-ола;
6-(6-метоксипиразин-2-ил)-1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридина;
1-[6-(3,3-диметилпиперазин-1-ил)-2-пиридил]-6-(1-этилпиразол-4-ил)пиразоло[4,3-с]пиридина;
1-[6-[6-(1-этилпиразол-4-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-4-амина;
(3S)-1-[6-[6-(1-этилпиразол-4-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-3-амина;
(3R)-1-[6-[6-(1-этилпиразол-4-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-3-амина;
(3S)-1-[6-[6-(1-этилпиразол-4-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пирролаидин-3-амина;
(3R)-1-[6-[6-(1-этилпиразол-4-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пирролаидин-3-амина;
(3S)-1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-3-амина;
1-[6-(1,4-диазепан-1-ил)-2-пиридил]-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридина;
(3S)-1-[3-циклопропил-6-[6-(5-этил-3-пиридил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-3-амина;
1-[6-[6-(1-этилпиразол-4-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]азепан-4-амина;
1-[6-(1,4-диазепан-1-ил)-2-пиридил]-6-(5-метил-3-пиридил)пиразоло[4,3-с]пиридина;
1-[6-[(3R)-3-этилпиперазин-1-ил]-2-пиридил]-6-(1-этилпиразол-4-ил)пиразоло[4,3-с]пиридина;
N-[6-[6-(1-этилпиразол-4-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]азепан-3-амина;
1-(6-пиперазин-1-ил-2-пиридил)-6-пиразин-2-ил-пиразоло[4,3-с]пиридина;
6-(1-трет-бутилпиразол-4-ил)-1-[6-(1,4-диазепан-1-ил)-2-пиридил]пиразоло[4,3-с]пиридина;
1-[6-(1,4-диазепан-1-ил)-2-пиридил]-6-(1-изопропилпиразол-4-ил)пиразоло[4,3-с]пиридина;
6-(1-циклобутилпиразол-4-ил)-1-[6-(1,4-диазепан-1-ил)-2-пиридил]пиразоло[4,3-с]пиридина;
5-[1-[6-(1,4-диазепан-1-ил)-2-пиридил]пиразоло[4,3-с]пиридин-6-ил]-2-метил-пиридазин-3-она;
6-(6-этилпиразин-2-ил)-1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридина;
1-[6-(1,4-диазепан-1-ил)-2-пиридил]-6-(6-этилпиразин-2-ил)пиразоло[4,3-с]пиридина;
3-этил-5-[1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридин-6-ил]пиримидин-4-она;
2-[4-[1-[6-(1,4-диазепан-1-ил)-2-пиридил]пиразоло[4,3-с]пиридин-6-ил]пиразол-1-ил]этанола;
1-[6-(1,4-диазепан-1-ил)-2-пиридил]-6-[1-(2-фторэтил)пиразол-4-ил]пиразоло[4,3-с]пиридина;
1-[6-(1,4-диазепан-1-ил)-2-пиридил]-6-[1-(2,2,2-трифторэтил)пиразол-4-ил]пиразоло[4,3-с]пиридина;
2-[4-[1-[6-(1,4-диазепан-1-ил)-2-пиридил]пиразоло[4,3-с]пиридин-6-ил]пиразол-1-ил]ацетонитрила;
(3S)-1-[6-[6-(6-этилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-3-амина;
1-[6-(1,4-диазепан-1-ил)-2-пиридил]-6-[1-(2-метилсульфонилэтил)пиразол-4-ил]пиразоло[4,3-с]пиридина;
1-[6-(1,4-диазепан-1-ил)-2-пиридил]-6-[1-(оксетан-3-илметил)пиразол-4-ил]пиразоло[4,3-с]пиридина;
2-[4-[1-[6-(1,4-диазепан-1-ил)-2-пиридил]пиразоло[4,3-с]пиридин-6-ил]пиразол-1-ил]ацетамида;
6-(6-метилпиразин-2-ил)-1-[6-(1,2,3,6-тетрагидропиридин-4-ил)-2-пиридил]пиразоло[4,3-с]пиридина;
6-[1-(циклопропилметил)пиразол-4-ил]-1-[6-(1,4-диазепан-1-ил)-2-пиридил]пиразоло[4,3-с]пиридина;
1-[6-(1,4-диазепан-1-ил)-2-пиридил]-6-[1-(2,2-дифторэтил)пиразол-4-ил]пиразоло[4,3-с]пиридина;
1-[6-(1,4-диазепан-1-ил)пиразин-2-ил]-6-(1-этилпиразол-4-ил)пиразоло[4,3-с]пиридина;
3-[1-[6-(1,4-диазепан-1-ил)пиразин-2-ил]пиразоло[4,3-с]пиридин-6-ил]-5-метил-пиридин-2-ола;
6-(6-циклопропилпиразин-2-ил)-1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридина;
6-(6-метилпиразин-2-ил)-1-[6-(4-пиперидил)-2-пиридил]пиразоло[4,3-с]пиридина;
(3S)-1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пирролаидин-3-амина;
(3R)-1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пирролаидин-3-амина;
1-[6-(3-метилпиперазин-1-ил)-2-пиридил]-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридина;
6-(6-трет-бутилпиразин-2-ил)-1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридина;
6-метил-1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-3-амина;
1-[6-[6-(6-этилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-1,4-диазепан-6-ола;
1-[6-(1,4-диазепан-1-ил)-2-пиридил]-6-[1-(дифторметил)пиразол-4-ил]пиразоло[4,3-с]пиридина;
6-(1-циклопропилпиразол-4-ил)-1-[6-(1,4-диазепан-1-ил)-2-пиридил]пиразоло[4,3-с]пиридина;
1-[6-(1,4-диазепан-1-ил)-2-пиридил]-6-пиримидин-5-ил-пиразоло[4,3-с]пиридина;
(3S)-1-[3-хлор-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-3-амина;
6-[1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридин-6-ил]пиразин-2-карбонитрил;а
1-[6-(1,4-диазепан-1-ил)пиразин-2-ил]-6-[1-(2,2,2-трифторэтил)пиразол-4-ил]пиразоло[4,3-с]пиридина;
1-[2-(1,4-диазепан-1-ил)пиримидин-4-ил]-6-[1-(2,2,2-трифторэтил)пиразол-4-ил]пиразоло[4,3-с]пиридина;
1-[6-(1,4-диазепан-1-ил)-2-пиридил]-6-(1Н-пиразол-4-ил)пиразоло[4,3-с]пиридина;
(3S)-1-[3-циклопропил-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-3-амина;
6-метил-1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-3-амина;
6-метил-1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-3-амина;
1-[6-(5-метил-1,4-диазепан-1-ил)-2-пиридил]-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридина;
1-[6-(3-метилпиперазин-1-ил)-2-пиридил]-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридина;
(3S)-1-[3-метокси-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-3-амина;
1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]азепан-3-амина;
(R)-1-(6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)-пиридин-2-ил)-1,4-диазепан-6-ола;
(S)-1-(6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)-пиридин-2-ил)-1,4-диазепан-6-ола;
6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]- N-(4-пиперидил)пиридин-2-амина;
1-[6-[(2R)-2-метилпиперазин-1-ил]-2-пиридил]-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридина;
(3S,5S)-5-фтор-1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-3-амина;
1-[6-(3-метилпиперазин-1-ил)-2-пиридил]-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридина;
1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-4-амина;
2-метил-1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-3-амина;
1-[6-[(2S)-2-метилпиперазин-1-ил]-2-пиридил]-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридина;
1-[5-циклопропил-6-(1,4-диазепан-1-ил)-2-пиридил]-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридина;
(3S,5R)-5-фтор-1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-3-амина;
2-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-2,8-диазаспиро[4.5]декана;
8-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-2,8-диазаспиро[4.5]декана;
2-[(3S)-3-амино-1-пиперидил]-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]пиридин-3-карбонитрила;
(5S)-5-амино-1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-2-она;
2-метил-1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-3-амина;
2-метил-1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-3-амина;
(3S)-1-[3-метил-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-3-амина;
4-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-1,4-диазепан-5-она;
1-[3-метокси-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-1,4-диазепан-6-ола;
5-[1-[6-(1,4-диазепан-1-ил)-2-пиридил]пиразоло[4,3-с]пиридин-6-ил]-3-метилпиразин-2-амина;
5-[1-[6-[(3S)-3-амино-1-пиперидил]-2-пиридил]пиразоло[4,3-с]пиридин-6-ил]-3-метилпиразин-2-амина;
3-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]циклогексанамина;
1-[6-(2,6-диазаспиро[3.4]октан-6-ил)-2-пиридил]-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридина;
(3S)-1-[3-фтор-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-3-амина;
8-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-1,8-диазаспиро[4.5]декана;
1-[6-(2,7-диазаспиро[3.4]октан-2-ил)-2-пиридил]-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридина;
[2-[(3S)-3-амино-1-пиперидил]-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-3-пиридил]метанола;
1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-3-(трифторметил)-2-пиридил]-1,4-диазепан-6-ола;
(3S)-1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-3-(трифторметил)-2-пиридил]пиперидин-3-амина;
(5S)-5-амино-1-[3-метил-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-2-он;
(3S)-1-[3-метокси-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]пиразин-2-ил]пиперидин-3-амина;
3-[(3S)-3-амино-1-пиперидил]-5-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]пиразин-2-ола;
1-[6-(1,4-диазепан-1-ил)-2-пиридил]-6-(1-метилпиразол-4-ил)пиразоло[4,3-с]пиридина;
(3S)-3-амино-1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-2-она;
(3S)-1-[3-хлор-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]пиразин-2-ил]пиперидин-3-амина;
(3S)-1-[3-(дифторметил)-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-3-амина;
(3S)-1-[3-метил-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]пиразин-2-ил]пиперидин-3-амина;
1-[6-[6-(1-метилпиразол-4-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-1,4-диазепан-6-ола;
4-[6-[6-(1-метилпиразол-4-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]азепан-4-ола;
1-[6-[6-(1-метилпиразол-4-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-1,4-диазепан-6-ола;
1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пирролаидин-3,4-диола;
3-[(3S)-3-амино-1-пиперидил]-1-метил-5-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]пиридин-2-она;
1-[3-метокси-6-[6-[1-(2,2,2-трифторэтил)пиразол-4-ил]пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]-1,4-диазепан-6-ола;
1-[6-(азепан-4-ил)-2-пиридил]-6-(1-метилпиразол-4-ил)пиразоло[4,3-с]пиридина;
1-[6-(4-фторазепан-4-ил)-2-пиридил]-6-(1-метилпиразол-4-ил)пиразоло[4,3-с]пиридина;
1-[3-метокси-6-[6-[1-(2,2,2-трифторэтил)пиразол-4-ил]пиразоло[4,3-с]пиридина-1-ил]-2-пиридил]-1,4-диазепан-6-ола;
(3S)-1-[3-циклопропил-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]пиразин-2-ил]пиперидин-3-амина;
(S)-2-((6-(1-(2-фторфенил)-1Н-пиразоло[4,3-с]пиридин-6-ил)пиразин-2-ил)окси)-1-фенилэтанамина;
6-(6-метилпиразин-2-ил)-1-[6-[4-(оксетан-3-ил)-1,4-диазепан-1-ил]-2-пиридил]пиразоло[4,3-с]пиридина;
3-[(3S)-3-амино-1-пиперидил]-1-метил-5-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]пиразин-2-она;
3-[(3S)-3-амино-1-пиперидил]-1-метил-5-[6-(1-метилпиразол-4-ил)пиразоло[4,3-с]пиридин-1-ил]пиразин-2-он;
3-[(3R)-3-амино-1-пиперидил]-1-метил-5-[6-(1-метилпиразол-4-ил)пиразоло[4,3-с]пиридин-1-ил]пиразин-2-она;
(R)-2-((6-(1-(2-фторфенил)-1Н-пиразоло[4,3-с]пиридин-6-ил)пиразин-2-ил)окси)-1-фенилэтанамина;
(3S)-3-амино-1-[3-метил-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-2-он;
1-(6-(2,6-диазаспиро[3.5]нонан-2-ил)пиридин-2-ил)-6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридина;
6-[1-[6-(1,4-диазепан-1-ил)-2-пиридил]пиразоло[4,3-с]пиридин-6-ил]пиразин-2-амина;
(S)-6-метил-1-(6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-6-ола;
(R)-6-метил-1-(6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-6-ола;
(3S)-1-[6-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-4-(оксетан-3-ил)-2-пиридил]пиперидин-3-амина;
1-[3-метокси-6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]гексагидропиримидин-2-она;
1-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]гексагидропиримидин-2-она;
1-[6-[6-(1-метилпиразол-4-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]азетидин-3-ола;
3-(6-гидрокси-1,4-диазепан-1-ил)-1-метил-5-[6-(1-метилпиразол-4-ил)пиразоло[4,3-с]пиридин-1-ил]пиразин-2-она;
1-[6-[6-[1-(2,2,2-трифторэтил)пиразол-4-ил]пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]азетидин-3-ола;
[1-[6-[6-(1-метилпиразол-4-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]азетидин-3-ил]метанамина;
1-[6-[6-(1-метилпиразол-4-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]азетидин-3-амина;
1-[6-[6-[1-(2,2,2-трифторэтил)пиразол-4-ил]пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]азетидин-3-амина;
1-[6-(4,4-дифтор-3-пиперидил)-2-пиридил]-6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридина;
(R)-1-(3-метил-6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-6-ола;
(S)-1-(6-(6-метокси-6-метил-1,4-диазепан-1-ил)пиридин-2-ил)-6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридина;
[1-[6-[6-[1-(2,2,2-трифторэтил)пиразол-4-ил]пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]азетидин-3-ил]метанамина;
(S)-1-(3-метил-6-(6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-1,4-диазепан-6-ола;
(R)-1-(6-(6-метокси-6-метил-1,4-диазепан-1-ил)пиридин-2-ил)-6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридина;
3-[6-[6-(6-метилпиразин-2-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]пиперидин-4-ола;
1-[6-(2,5-диазаспиро[3.5]нонан-2-ил)-2-пиридил]-6-(1-метилпиразол-4-ил)пиразоло[4,3-с]пиридина;
1-[6-(2,6-диазаспиро[3.3]гептан-2-ил)-2-пиридил]-6-[1-(2,2,2-трифторэтил)пиразол-4-ил]пиразоло[4,3-с]пиридина;
1-[6-(2,6-диазаспиро[3.3]гептан-2-ил)-2-пиридил]-6-(1-метилпиразол-4-ил)пиразоло[4,3-с]пиридина;
1-[6-(2,5-диазаспиро[3.5]нонан-2-ил)-2-пиридил]-6-[1-(2,2,2-трифторэтил)пиразол-4-ил]пиразоло[4,3-с]пиридина;
3-(аминометил)-1-[6-[6-(1-метилпиразол-4-ил)пиразоло[4,3-с]пиридин-1-ил]-2-пиридил]азетидин-3-ола;
(S)-1-(6-(4,4-дифторпиперидин-3-ил)пиридин-2-ил)-6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридина;
(R)-1-(6-(4,4-дифторпиперидин-3-ил)пиридин-2-ил)-6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридина;
[6-[1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридин-6-ил]пиразин-2-ил]метанола;
1-(6-пиперазин-1-ил-2-пиридил)-6-(6-винилпиразин-2-ил)пиразоло[4,3-с]пиридина;
6-(6-хлорпиразин-2-ил)-1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридина;
6-(6-бензилоксипиразин-2-ил)-1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридина;
1-[6-[1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридин-6-ил]пиразин-2-ил]этан-1,2-диола;
2-[6-[1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридин-6-ил]пиразин-2-ил]оксиэтанола;
6-[6-(дифторметил)пиразин-2-ил]-1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридина;
[(2S)-1-[6-[1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридин-6-ил]пиразин-2-ил]пирролаидин-2-ил]метанола;
1-[6-[1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридин-6-ил]пиразин-2-ил]азетидин-3-ола;
2-[[6-[1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридин-6-ил]пиразин-2-ил]амино]этанола;
(1S,2S)-2-[[6-[1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридин-6-ил]пиразин-2-ил]амино]циклопентанола;
6-[6-(азетидин-1-ил)пиразин-2-ил]-1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридина;
N-этил-6-[1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридин-6-ил]пиразин-2-амина;
2-[6-[1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридин-6-ил]пиразин-2-ил]оксиэтанамина;
6-[1-(6-пиперазин-1-ил-2-пиридил)пиразоло[4,3-с]пиридин-6-ил]-1Н-пиразин-2-он;
3-(6-(6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)пиперидин-3-ола;
(S)-6-(6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)-2-(пиперидин-3-ил)пиридазин-3(2Н)-она;
(R)-6-(6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)-2-(пиперидин-3-ил)пиридазин-3(2Н)-она;
6-(6-(6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)-2,6-диазаспиро[3.5]нонан-2-карбальдегида;
(6-(6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)-3,4-дигидро-2Н-пирано[3,2-b]пиридин-3-ил)метанамина;
1-(6-(2,6-диазаспиро[3.5]нонан-6-ил)пиридин-2-ил)-6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридина;
1-(6-(3-фторпиперидин-3-ил)пиридин-2-ил)-6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридина;
1-(6-(3-метоксипиперидин-3-ил)пиридин-2-ил)-6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридина;
N,N-диметил-6-(6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-амина;
N-метил-6-(6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-амина;
(R)-1-(6-(6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)пиперидин-3-ола;
(S)-1-(6-(6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)пиперидин-3-ола;
3-(6-(1-(6-(пиперазин-1-ил)пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридин-6-ил)пиразин-2-ил)проп-2-ин-1-ола; и
3-(6-(1-(6-(пиперазин-1-ил)пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридин-6-ил)пиразин-2-ил)пропан-1-ола.
2. Соединение, выбранное из следующих соединений:
(S)-(3-аминопиперидин-1-ил)(6-(6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)метанона;
(R)-(3-аминопиперидин-1-ил)(6-(6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)метанона;
(1S,2S)-2-(6-(1-(пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридин-6-ил)пиразин-2-илокси)циклопентанамина;
3-(6-(6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-илокси)циклогексанамина;
1-(6-(4-фторпиперидин-3-ил)пиридин-2-ил)-6-(1-(2,2,2-трифторэтил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридина;
(1S,2S)-N1-(6-(1-(пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридин-6-ил)пиразин-2-ил)циклопентан-1,2-диамина;
N-(азетидин-3-ил)-6-(1-(пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридин-6-ил)пиразин-2-амина;
6-(5-хлор-1-метил-1Н-пиразол-4-ил)-1-(2-фторфенил)-1Н-пиразоло[4,3-с]пиридина;
3-(6-(6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-илокси)циклогексанамина;
3-(6-(6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-илокси)циклогексанамина;
1-(6-(6-(6-метилпиразин-2-ил)-1Н-пиразоло[4,3-с]пиридин-1-ил)пиридин-2-ил)пиперидин-3,4-диола;
6-(6-метилпиразин-2-ил)-1-(6-(пиперазин-1-ил)пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридазина;
1-(2-фторфенил)-6-(1-метил-5-(1,2,3,6-тетрагидропиридин-4-ил)-1Н-пиразол-4-ил)-1Н-пиразоло[4,3-с]пиридина;
6-(6-этинилпиразин-2-ил)-1-(6-(пиперазин-1-ил)пиридин-2-ил)-1Н-пиразоло[4,3-с]пиридина;
1-(4-(1-(2-фторфенил)-1Н-пиразоло[4,3-с]пиридин-6-ил)-1-метил-1Н-пиразол-5-ил)пиперидин-4-амина и
1-(6-(пиперазин-1-ил)пиридин-2-ил)-6-(6-(проп-1-инил)пиразин-2-ил)-1Н-пиразоло[4,3-с]пиридина.
3. Фармацевтическая композиция для лечения заболеваний и расстройств, опосредованных ингибиторами киназы Pim, включающая соединение по любому из пп. 1-2 и фармацевтически приемлемый носитель, скользящее вещество, разбавитель или эксципиент.
4. Фармацевтическая композиция по п. 3 для применения при лечении заболевания или расстройства, выбранного из рака, иммунологических нарушений, сердечно-сосудистого заболевания, вирусной инфекции, воспаления, расстройств обмена веществ / эндокринной функции и неврологических нарушений, где заболевание или расстройство опосредовано киназой Pim.
5. Применение соединения по любому из пп. 1-2 при изготовлении лекарственного средства для лечения рака, иммунологических нарушений, сердечно-сосудистого заболевания, вирусной инфекции, воспаления, расстройств обмена веществ / эндокринной функции и неврологических нарушений; где лекарственное средство опосредует киназу Pim.
6. Соединение по любому из пп. 1-2 для применения при лечении рака, иммунологических нарушений, сердечно-сосудистого заболевания, вирусной инфекции, воспаления, расстройств обмена веществ / эндокринной функции и неврологических нарушений, где лекарственное средство опосредует киназу Pim.
| GYTE VILKAUSKAITE ET AL, Sonogashira-Type Reactions with 5-Chloro-1-phenyl-1H-pyrazole-4-carbaldehydes: A Straightforward Approach to Pyrazolo[4,3-c]pyridines, EUROPEAN JOURNAL OF ORGANIC CHEMISTRY, 2011, N 26, pages 5123 - 5133 | |||
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| GISELE A NISHIGUCHI ET AL, Discovery of novel 3,5-disubstituted indole derivatives as potent inhibitors of Pim-1, Pim-2, and Pim-3 protein kinases, BIOORGANIC & MEDICINAL CHEMISTRY LETTERS, 2011, vol | |||
| Выбрасывающий ячеистый аппарат для рядовых сеялок | 1922 |
|
SU21A1 |
| СОЕДИНЕНИЯ И КОМПОЗИЦИИ В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОТЕИНКИНАЗ | 2006 |
|
RU2387653C2 |
Авторы
Даты
2018-08-30—Публикация
2013-06-26—Подача