Область техники, к которой относится изобретение
Настоящее изобретение относится к раствору на основе морской воды для аппликаций на глаза, кожу иди слизистые оболочки.
Уровень техники
Солевые растворы широко применяются в офтальмологии в качестве индифферентного вещества для наружных глазных средств, растворов для промывки контактных линз или кондиционеров для внутриглазных имплантатов. Солевые растворы широко применяются также в оториноларингологии для промывания полостей носа.
Другие композиции стремятся приблизиться более точно к составу морской воды. Так, в заявке на патент FR 2803205 раскрыт водный раствор на основе морской воды, содержание некоторых ингредиентов которого изменено посредством избирательного электродиализа. Снижение показателя pH, низкая осмотическая концентрация раствора, соответственно высокая концентрация калия и низкая концентрация натрия, магния, кальция и хлора по отношению к аналогичным концентрациям в морской воде делают возможным применение в гигиене глаз.
В заявке на патент FR 2843029 описан раствор на основе морской воды для промывки контактных линз. Некоторые свойства его компонентов могут быть изменены; так, его показатель pH и его осмотическая концентрация могут быть ниже аналогичных показателей природной морской воды. Эти изменения могут быть еще дополнены высокой концентрацией калия и низкой концентрацией натрия, магния, кальция и хлора.
Однако такие, известные из уровня техники растворы на основе морской воды не позволяют избирательно удовлетворять некоторые потребности, в частности, касающиеся терапии глаз и слизистых оболочек, в частности, их эффективность часто остается весьма ограниченной при лечении патологий, предполагающих взаимодействие с рецепторами Р2Х, такими, как Р2Х7.
Для полного или частичного устранения присущих уровню техники недостатков настоящее изобретение имеет своей целью композицию, приготовленную на основе очищенной воды с pH от 5,5 до 7,5, осмотической концентрацией от 200 до 400 м осм./кг, удельной проводимостью от 17 до 22,5 мСм/см при 25°C, с использованием от 1 до 20% фильтрованной морской воды, в которой содержание соли калия составляет от 90 до 180 ммоль/л. Концентрации приведены по отношению к конечному содержанию после добавки соли, это относится также к совокупности концентраций, описанных ниже в настоящей заявке (если только специально упоминается другая ссылка). Морская вода рассматривается как источник всех микроэлементов в той мере, в какой они, почти все, присутствуют в большей или меньшей концентрации.
Предпочтительно композиция согласно изобретению содержит соль калия в количестве менее 150 ммоль/л, предпочтительно от 95 до 145 ммоль/л, более предпочтительно от 98 до 141 ммоль/л.
Осмотическая концентрация раствора измеряется методом, описанным в Европейской фармакопеи 6.0 (шестое издание), пункт 2.2.35. Удельная проводимость измеряется метолом, описанным в Европейской фармакопеи 6.0, пункт 2.2.38. Осмотическая концентрация раствора составляет предпочтительно 250-350 миллиосмолей/кг, даже 270-330 миллиосмолей/кг.
В таблице 1 приведены содержащиеся в морской воде элементы, их теоретическое содержание в частях на миллион.
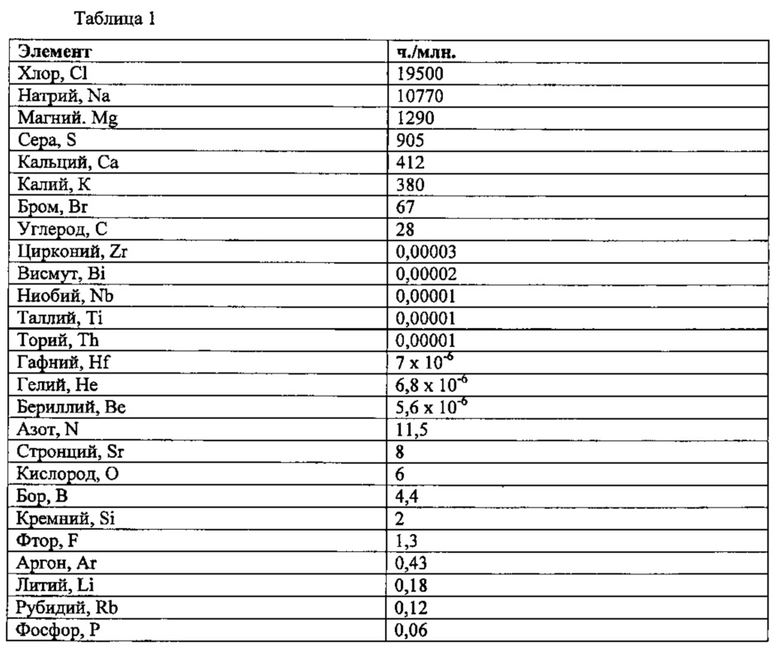
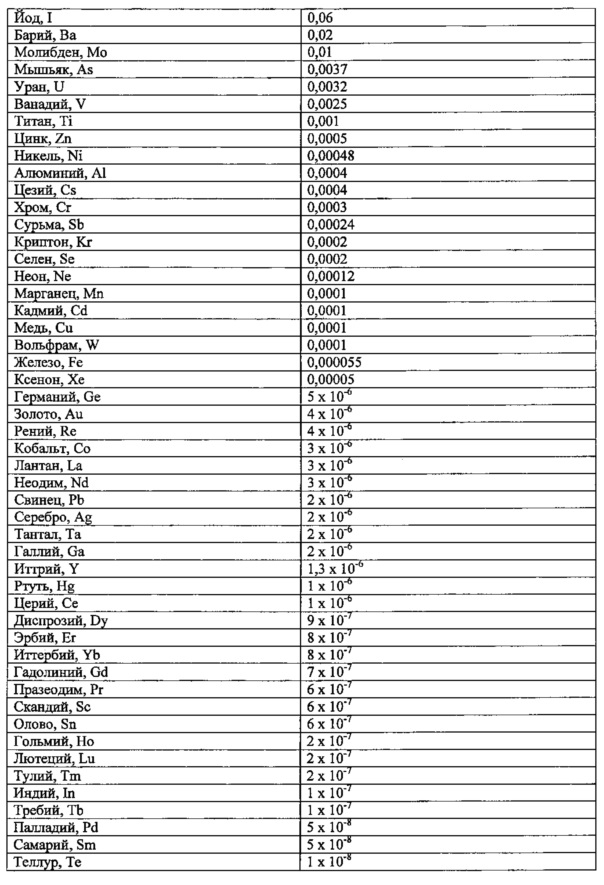

Из таблицы 1 следует, что в морской воде присутствуют многие химические элементы в более или менее значительном количестве. Эти концентрации выражены в средних показателях, способных изменяться в зависимости от географического места расположения моря и даже от места забора морской воды.
Морская вода для приготовления композиции согласно изобретению закачивается непосредственно в море с обеспечением ее начального состояния и, следовательно, свойственных ей свойств. Концентрация входящих в состав воды элементов может меняться в зависимости от географического расположения места закачивания и при необходимости требуется изменять содержание некоторых элементов. Следовательно, место закачивания выбирается с таким расчетом, чтобы вода могла использоваться непосредственно, без изменения концентрации образующих ее элементов.
Следовательно, морская вода выбирается, например, таким образом, чтобы в ней натрий не присутствовал в слишком большом количестве, учитывая, что этот элемент вовлекается в воспалительные процессы при его содержании в слишком большом количестве.
Используемая в рамках изобретения морская вода имеет показатель pH от 7,5 до 8,5 и содержит соли или ионы в количестве, близком к теоретическому составу морской воды (таблица 1). Используемая морская вода отбирается с учетом ее особо подходящих местоположений:
- отсутствие вблизи промышленных предприятий и наличие экологически чистой окружающей среды;
- не вклинившееся место отбора: постоянное обновление воды;
- течения в зоне, способствующие обновлению воды;
- удовлетворительное качество, признанное специальными организациями, такими, как Исследовательский институт Франции по эксплуатации моря (IFREMER) и Департаментская дирекция по санитарным и общественным делам (DDASS).
Раскрытие изобретения
Совершенно неожиданно авторами изобретения было установлено, что раствор на основе морской воды, разбавленный в диапазоне показателя в соответствии с композицией согласно изобретению, в сочетании с добавкой соли цинка в рекомендованных количествах, позволяет после аппликации на глазе получить в результате синергетического эффекта ответ, создающий специальный электрический сигнал, способный воздействовать на ионные каналы клеток глаза. При этом выяснилось, что композиция по изобретению, в частности, ее ионы, обеспечивают пассивный и активный транспорт в направлении к клеткам, обусловленный их ионными каналами.
Неожиданно в отношении композиции согласно изобретению выяснилось, что она обладает большой толерантностью по отношению к наиболее непрочным тканям (снижение окислительного или воспалительного стресса…), таким, как поверхность глаза и слизистые оболочки, и противоапоптическим действием (в результате воздействия на рецептор Р2Х7). Она может применяться для непосредственных аппликаций (промывки) или в качестве индифферентного вещества (в косметике, медицинских устройствах...). Исследование цитотоксичности раствора согласно изобретению позволило определить его высокую толерантность при использовании в офтальмологии. Проведены разные испытания для оценки цитотоксичности и для лучшего определения толерантности композиции согласно изобретению по отношению к разным типам клеток (роговичным и конъюнктивальным) поверхности глаза.
Морская вода, как основа композиции согласно изобретению, представляет собой источник разных химических элементов, присутствующих в более или менее значительной концентрации. Физико-химические свойства морской воды обусловлены равновесным состоянием между анионами и катионами. Эти элементы ведут себя как комплекс взаимодействующих между собой биомолекул. В рамках изобретения синергия воздействия проявляется не только между разными ионами, но также и при наличии в композиции солей цинка.
Морскую воду разбавляют, обогащают цинком и доводят до состояния, необходимого для получения раствора с необходимыми диапазоном pH и осмотической концентрацией путем добавки соли. Предпочтительно используемой солью является хлорид калия. Взаимодействие между ионами цинка и разными элементами морской воды усиливает ее воздействие на стрессовое состояние клеток.
Предпочтительно pH композиции составляет от 6 до 7,2.
Заявителем было проведено исследование на рецепторах Р2Х гибели клеток. Этими рецепторами являются ионотропические рецепторы, вызывающие катионный импульс после их активации. Точнее говоря, из приведенных выше рецепторов Р2Х рецептор Р2Х7 вызывает воспалительные ответы, перепроизводство реакционноспособных видов кислорода, апоптоз и даже цитолиз. Разные сравнительные испытания показали, как это описано в экспериментальной части, что активизация рецепторов Р2Х7 сильно замедляется в присутствии композиции на основе морской воды согласно изобретению. Подавление активности рецепторов Р2Х7 может быть уподоблено состоянию «не смерти» клеток, при этом ослабляются воспалительные явления и апоптоз. Также это доказывает хорошую толерантность клеток.
Предпочтительно композицию на основе морской воды обогащают цинком, в частности, солью типа Zn(X)2 при концентрации 125-500 мкмоль/л, при этом X означает любой тип противоаниона в комплексе с катионом Zn2+.
В качестве источника цинка предпочтительно вводить в композицию согласно изобретению хлорид цинка (ZnCl2), который способствует взаимодействиям с другими входящими в состав морской воды элементами. В этих рамках настоящее изобретение относится предпочтительно к описанной выше композиции, в которой солью цинка выступает хлорид цинка (ZnCl2).
Предпочтительно Zn(X)2 вводится в количестве от 200 до 300 мкмоль/л.
Композиция согласно изобретению содержит соль калия, которой является предпочтительно хлорид калия (KCl).
Обогащение морской воды другими ионами, такими, как Mg2+ или Ca2+, не дает таких убедительных результатов, как это достигается при использовании Zn2+.
Предпочтительно морская вода присутствует в композиции в количестве от 3 до 17%.
Композиция может применяться в качестве индифферентного или контактного вещества, в зависимости от назначения.
Композиция согласно изобретению предназначена преимущественно для применения в качестве лекарства при лечении глазных болезней путем инактивации рецепторов гибели клеток типа Р2Х7.
Также композиция согласно изобретению может применяться в качестве наружного глазного средства, искусственных слез, раствора для промывки глазных линз, раствора для промывки глаз и/или в качестве материала контейнера для глазного имплантата. Вследствие своей полярности она обладает хорошими моющими и растворяющими свойствами. Поэтому она позволяет промывать глаз в случае попадания в него вредных продуктов, не вызывая при этом раздражения и способствуя регенерации клеток.
Композиция согласно изобретению описана с учетом применения именно в офтальмологии, однако она может применяться в любой другой области, связанной с клеточной физиологией, для других органов, таких, как органы в области оториноларингологии, в частности, слизистые оболочки носа, для профилактики таких недомоганий, как риниты, носовые гиперемии, сухости в носу, синуситы или бронхиты.
Композиция согласно изобретению может также наносится на кожу и слизистые оболочки влагалища, в частности, при проведении интимной гигиены. Композиция согласно изобретению предпочтительно предназначена для применения в качестве лекарства для лечения слизистых оболочек носа, рта, влагалища и/или кожи.
Поэтому при промывании пораженных тканей, слизистых оболочек или кожи композиция согласно изобретению может способствовать благодаря своим свойствам заживлению. Композиция согласно изобретению предназначена преимущественно для применения в качестве лекарства при лечении рубцов слизистых оболочек и/или кожи.
Композиция согласно изобретению может также применяться в виде аэрозоли, капель или индифферентного вещества при солюбилизации молекул, представляющих терапевтический интерес, таких, как гиалуроновая кислота, полифенолы или кислоты жирного ряда.
Также настоящее изобретение относится к способу приготовления описанной выше композиции в рамках изобретения, включающему в себя следующие этапы:
а) закачка морской воды;
б) при необходимости предварительная обработка морской воды посредством первого естественного или искусственного фильтра;
в) фильтрация морской воды, прошедшей при необходимости предварительную обработку, через второй фильтр, средний диаметр пор которого составляет менее или равен 5 мкм;
г) последующая фильтрация через третий фильтр, средний диаметр пор которого меньше среднего диаметра пор второго фильтра и составляет менее или равен 0,45 мкм;
д) разбавление отфильтрованного раствора очищенной водой.
На этапе а) отобранную перекачиванием морскую воду фильтруют при необходимости (этап б)) посредством либо естественного фильтра, например, песка, либо искусственного фильтра, например, сита, для удержания частиц крупного размера. После этого вода предпочтительно хранится в емкости для предварительной обработки. Затем эта морская вода снова подается в трубопроводы насосом для ее фильтрации.
Предварительно обработанная морская вода фильтруется на этапах в) и г) через два фильтра, средний диаметр пор которых составляет соответственно от 5 до 1 мкм (для этапа в)), и менее 0,45 мкм (для этапа г)). На этом этапе фильтрации вода подается предпочтительно в фильтрационный комплекс в составе трубопроводов, содержащих предпочтительно фильтры в виде цилиндрических патронов. Пример на фильтрационный комплекс описан ниже в экспериментальной части.
Настоящее изобретение станет более понятным из описания приводимой ниже экспериментальной части, примеры и фигуры в которой приведены единственно в иллюстративных целях и не являются ограничивающими. Для иллюстрации результатов экспериментальной части схема 1 имеет схематический вид с поперечным сечением по фильтрационному комплексу, обеспечивающему фильтрацию морской воды перед разбавлением при получении композиции согласно изобретению.
Осуществление изобретения
Осмотическая концентрация раствора измеряется методом, описанным в Европейской фармакопеи 6.0 (шестое издание), пункт 2.2.35. Удельная проводимость измеряется методом, описанным в Европейской фармакопеи 6.0, пункт 2.2.38.
1) Приготовление композиции согласно изобретению с содержанием 5% морской воды (схема 1)
5 литров морской воды, отобранной в южной части Финистера путем закачки, профильтровали через пирамидальное сито. Отобранная таким образом морская вода была помещена в емкость для предварительной обработки. Затем провели перекачивание этой морской воды с использованием насоса.
Предварительно обработанную морскую воду подали в трубопроводы фильтрационного комплекса 1, представленного на схеме. 1. Фильтрационный комплекс 1 содержит впускное отверстие 2 для морской воды. Это впускное отверстие 2 для воды сообщено с расходомером 3, подключенным к нижней части корпуса 4 предфильтра 5 (1 мкм). Выходное отверстие предфильтра 5 (всегда в нижней части корпуса 4) сообщено с нижней частью корпуса 6 фильтра 7 (0,22 мкм), выходное отверстие которого сообщено с трубопроводом для сбора воды после фильтрации для ее хранения в резервуаре 8.
После этого в отфильтрованный раствор добавили дистиллированную воду, хлорид цинка и хлорид калия для получения композиции 1) с содержанием 250 мкмоль/л ZnCl2 и 140,9 мкмоль/л KCl. Удельная проводимость раствора составила 20 мСм/см при 25°C, осмотическая концентрация - 300 мОсмолей/кг.
2) Исследование жизнеспособности клеток
Эпителиальные соединительные клетки человека (WKD) инкубировали в разных культурных средах и оценивали жизнеспособность путем испытания нейтральным красным. Нейтральное красное инкубировали в течение 3 часов при 37°C вместе с клетками, после этого клетки промыли фосфатно-солевым буферным раствором и применили раствор из уксусной кислоты и этанола для отделения нейтрального красного от клеток и получения однородной окраски. Прибором для количественного определения флюоресценции служил цитометр, приспособленный для микропластин (Sifire, TECAN). Испытание нейтральным красным рекомендовано для оценки цитотоксичности медицинских устройств стандартом ISO 10993-5 в редакции от июля 2010 года. Результаты этого испытания выражены в процентах по отношению к контрольным клеткам.

Можно видеть, что композиция с содержанием 5% морской воды и KCl в количестве 140,9 ммоль/л имеет улучшенную клеточную толерантность по сравнению с эквивалентной композицией, содержащей только морскую воду, и что кроме того эта толерантность не снизилась из-за присутствия ZnCl2 в количестве 250 мкмоль/л.
3) Измерение окислительно-восстановительного состояния клеток
Композицию, приготовленную в первой части (обозначенную ниже как композиция 1)), тестировали для определения ее цитотоксической способности. Цитотоксическое вещество обладает способностью понижать окислительно-восстановительный потенциал клетки. Это ведет к снижению активности окислительно-восстановительных ферментов и, следовательно, к гибели клеток.
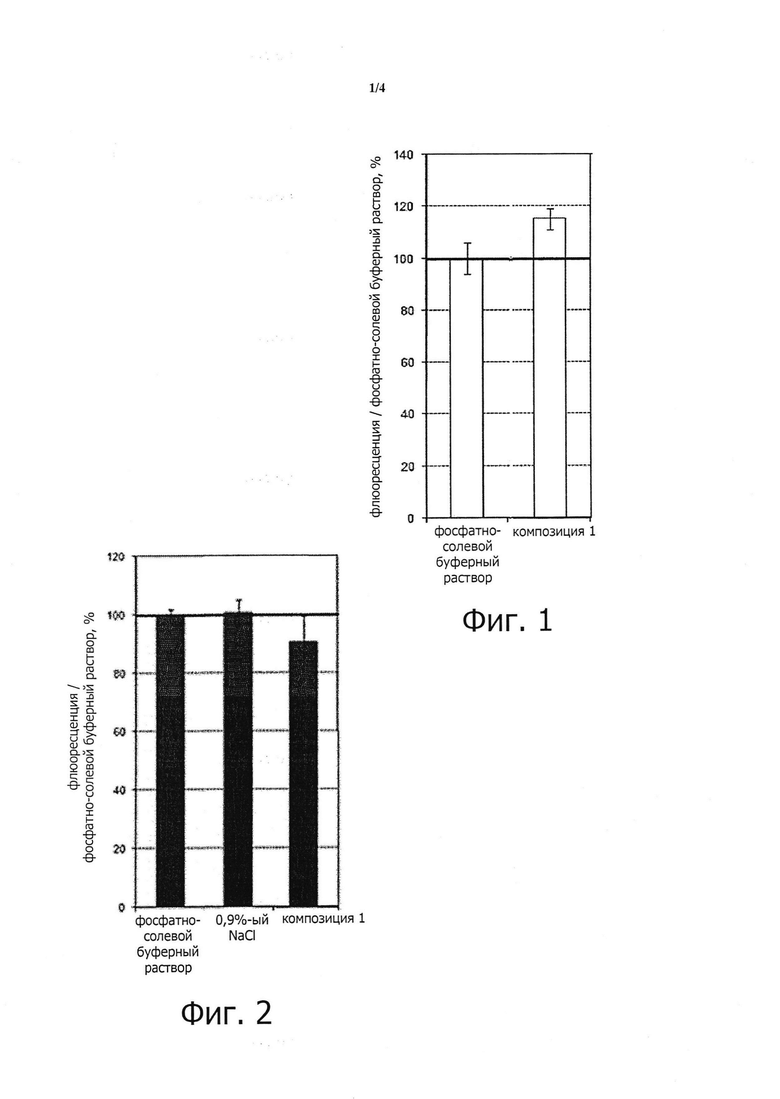
При проведении испытания наблюдался флюоресцирующий зонд, метаболический краситель, определяющий дыхательную активность клетки, который инкубировали в течение 6 часов при 37°C вместе с клетками. Прибором для количественного определения флюоресценции служил цитометр, приспособленный для микропластин (Safire, TECAN). Это испытание является составной частью испытаний, предложенных для оценки цитотоксического глазного потенциала многофункциональных растворов для ухода за контактными линзами в стандарте NF S11-820 в редакции от февраля 2012 года. Интенсивность флюоресценции пропорциональна окислительно-восстановительной способности и, в широком смысле, количеству живых клеток. Испытания проводились в сравнении с 0,9%-ым раствором NaCl и фосфатно-солевым буферным раствором (этот раствор широко применяется для клеточной культуры), результаты представлены на фиг.1 и 2. Результаты, нанесенные по оси ординат, показывают процент флюоресценции, который определили по отношению к фосфатно-солевому буферному раствору (или % флюоресценции/фосфатно-солевой буферный раствор). Этот показатель рассчитали путем деления интенсивности флюоресценции обработанных клеток на интенсивность флюоресценции не обработанных клеток (инкубированных фосфатно-солевым буферным раствором), затем умножили на 100 для получения процентного выражения. На фиг. 1 представлены результаты инкубации соединительных эпителиальных клеток человека в течение 1 часа, на фиг. 2 - результаты, касающиеся инкубации роговичных эпителиальных клеток человека в течение 1 часа.
Результаты свидетельствуют о том, что композиция не вызывает снижения окислительно-восстановительного потенциала клеток конъюнктивы по отношению к контрольной пробе.
Отмечено легкое снижение флюоресценции для клеток роговой оболочки, однако оно не является статистически значительным.
В заключение следует отметить, что инкубация в композиции (1) не ведет к потере окислительно-восстановительного потенциала, т.е. не происходит уменьшения количества живых клеток. Следовательно, композиция 1 хорошо переносится.
4) Изменение активности Р2Х7
Соединительные эпителиальные клетки человека подвергли инкубации в разных солевых растворах, при этом определяли активность рецепторов Р2Х7 посредством теста YO-PRO-1. Зонд YO-PRO-1 входил в клетки через отверстие мембранной поры, образовавшееся при активации рецептора Р2Х7. Увеличение флюоресценции соответствует активации рецептора 2РХ7. Активация рецептора 2РХ7 является признаком апоптоза. Прибором для количественного определения флюоресценции служил цитометр, приспособленный для микропластин (Safire, TECAN).
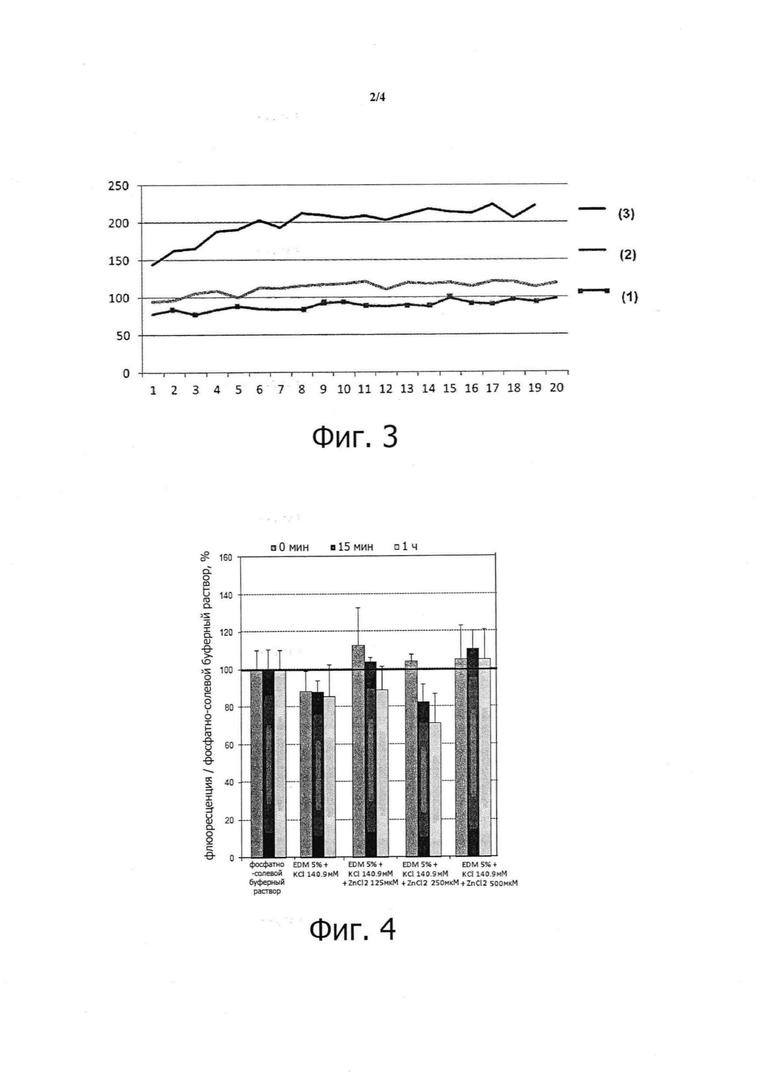
При рассмотрении фиг.3 (по оси абсцисс отложено время в минутах, по оси ординат отложены относительные единицы флюоресценции) можно заключить, что композиция (2) с содержанием 5% морской воды и 140,9 ммоль/л KCl замедляет активность рецептора Р2Х7, это замедление заметно по отношению к контрольной композиции (3) с содержанием 0,9% NaCl, и что кроме того это замедление усиливается в результате присутствия ZnCl2 в количестве 250 мкмоль/л в композиции (1) (для сведения: композиция (1) содержит 5% морской воды, 140,9 ммоль/л KCl и 250 мкмоль/л ZnCl2).
5) Ингибирование продукции реакционноспособных видов кислорода
Продуцирование реакционноспособных видов кислорода измеряли на соединительных эпителиальных клетках человека посредством теста H2DCF-DA. Этот зонд входит в клетки и гидролизуется межклеточными ферментами. После гидролиза зонд захватывается клетками и может быть окислен присутствующими реакционноспособными видами кислорода. Такая окисленная форма является флюоресцентной. Прибором для количественного определения флюоресценции служил цитометр, приспособленный для микропластин (Safire, TECAN).
Испытания проводились со ссылкой на фосфатно-солевой буферный раствор (последний широко применяется в клеточной культуре), результаты представлены на фиг. 4. На оси ординат они показывают полученный процент флюоресценции по отношению к фосфатно-солевому буферному раствору. Этот показатель рассчитывался путем деления интенсивности флюоресценции обработанных клеток на интенсивность флюоресценции не обработанных клеток (инкубированных посредством фосфатно-солевого буферного раствора), затем умножили на 100 для получения процента.
При рассмотрении фиг. 4 можно отметить, что следующие растворы могут быть охарактеризованы следующим образом:
- раствор из 5% морской воды и 140,9 ммоль KCl: отмечается замедление окислительного стресса;
- раствор из 5% морской воды, 140,9 ммоль KCl и 250 мкмоль ZnCl2: замедление окислительного стресса является оптимальным.
При более высоких содержаниях ZnCl2 или при его более низких содержаниях эффект замедления выражен слабее или даже отсутствует.
6) Оценка эффективности композиции (1) при промывке глаза после воздействия токсичного вещества
При работе in vitro исследовалось влияние промывки химически обожженного глаза разными растворами (Said и др. 2009).
Оценивалась жизнеспособность клеток путем испытаний нейтральным красным в течение 24 часов после ожога метанолом или едким натром при последующей аппликации промывочных растворов. Нейтральный красный инкубировали в течение 3 часов при 37°C вместе с клетками, затем клетки промыли фосфатно-солевым буфером, применили раствор из уксусной кислоты и этанола для высвобождения нейтрального красного из клеток и гомогенизировали окраску. Прибором для количественного определения флюоресценции служил цитометр, приспособленный для микропластин (Safire, TECAN). Испытание нейтральным красным рекомендовано для оценки цитотоксичности медицинских устройств стандартом ISO 10993-5 в редакции от июля 2010 года. Результаты этого испытания, выраженные в процентах по отношению к контрольным клеткам, представлены на фиг. 5 (p<0,001 показано по отношению к другим композициям, распределенным по круговой диаграмме).
Было установлено, что промывка композицией (1) улучшает выживание клеток и их регенерацию после их химического ожога. Это улучшение является статистически значительным по сравнению с другими примененными растворами (в т.ч. 0,9%-ым NaCl).
Исследование проводилось на кроликах. В приводимой ниже таблице 3 представлены результаты испытаний по Дрезу (Draize), проведенных после ожога глаза химическим щелочным продуктом с последующей промывкой разными растворами. При этом испытании применялся также заживляющий препарат (Euronac®) после промывки 0,9%-ым раствором NaCl или композицией (1) согласно изобретению.
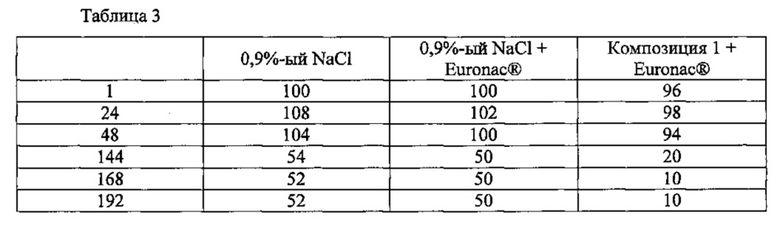
Первая строчка в этой таблице указывает на разные виды обработки, первый столбец содержит указание на продолжительность в часах.
Чем ниже показатель, тем меньше степень раздражения. Можно видеть, что промывка с помощью 0,9%-го NaCl до аппликации препарата Euronac®, выпущенного в продажу лабораториями Doliage (заживляющее наружное глазное средство), не снизила показатель ниже 50%, тогда как раствор по изобретению снизил этот показатель до 20, затем до 10 за одну неделю (примечание: показатель менее 15 указывает на отсутствие раздражения).
Результаты этого исследования позволяют построить наилучший прогноз в том случае, когда глаз промывается композицией (1) вместо раствора типа 0,9%-ый NaCl перед аппликацией заживляющего наружного глазного средства.
7) Исследование промывочной способности препаратов для ухода за контактными линзами
На жестких линзах, загрязненных раствором из перуксусной кислоты и перекиси водорода, провели предварительное исследование. Во время этого предварительного исследования было установлено, что композиция (1) позволяет произвести эффективную промывку данным раствором.
Исследования были распространены на промывку многофункциональными растворами, применяемыми при уходе за гидрофильными гибкими контактными линзами.
Первая серия испытаний проводилась следующим образом:
- 3 типа линз были подвержены действию разных многофункциональных растворов,
- жизнеспособность клеток после расположения линз на слой из роговичных клеток наблюдали через микроскоп и определяли путем измерения нейтральным красным,
- эксперимент возобновили после промывки линз раствором согласно изобретению. Промывки 0,9%-ым NaCl и композицией по изобретению сравнили.
В следующей таблице 4 приведены полученные результаты жизнеспособности клеток.
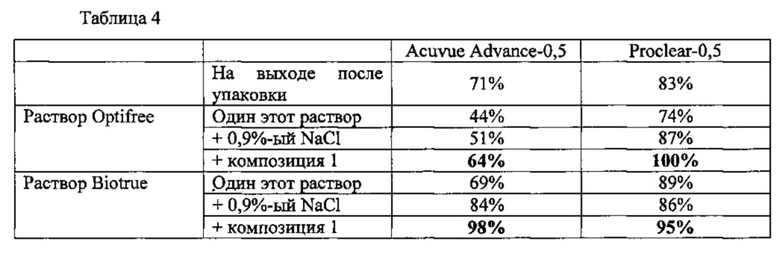
Были исследованы разные типы линз и многофункциональных растворов для ухода за контактными линзами (Biotrue и Optifree). Раствор Biotrue выпущен в продажу фирмой Bausch & Lomb и содержит гиалуроновую кислоту, сульфобетаин, полоксамин, борную кислоту, борат натрия, эдетат натрия, полиаминопропилбиганид, поликатерн и хлорид натрия; раствор Optifree выпущен в продажу фирмой Alcon и содержит в числе прочего Tetronic 1304, Polyquad®, Aldox®, буферный раствор из соли лимонной кислоты, хлорид натрия, эдетат натрия. Эти оба раствора выпущены в продажу и предназначены для ухода за гибкими контактными линзами.
Сравнили промывки посредством 0,9%-го NaCl и композиции 1. Линзы погрузили на 96 часов в 100 мл многофункционального раствора (= 20 циклам ухода, протокол Food and Drag Administration 1994 FDA Premarket Notification 510(k) Guidance Document for Daily Wear Contact Lens), затем промыли замачиванием в течение 24 часа в 100 мл раствора 1 или 0,9%-го NaCl.
Во всех случаях промывка уменьшала потерю жизнеспособности клеток.
Существенное улучшение было зафиксировано после промывки контактных линз.
Композиция (1) согласно изобретению обеспечивает превосходную жизнеспособность клеток.
8) Исследование защиты от воспаления на макрофагах
Измерялось высаливание провоспалительных цитокинов (TNF-α) на микрофагах методом ELISA (Enzyme-Linked Immunosorbent Assay). Этот метод позволяет дозировать протеины в пробе; в данном случае метод ELISA позволил определить количество цитокина TNF-α, высвободившегося в надосадочную жидкость у клетки под действием макрофагов в результате воспалительного стресса. Специфичный антиген цитокина TNF-α иммобилизируют на подложку в виде микропланшета с 96 отверстиями. На нее помещали надосадочную жидкость от клеток и TNF-α мог соединиться со своим антигеном. Первичное антитело позволило распознать TNF-α, вторичное антитело, связанное с энзимом, соединилось с первичным антителом. Колориметрическая ферментная реакция позволила обнаружить комплекс антител. Прибором для количественного определения поглощения служил цитометр, приведенный в соответствие с микропластинами (Safire, TECAN). Одновременно проводилась эталонная серия на основе раствора TNF-α для преобразования абсорбционной способности в количество протеина (пг/мл).
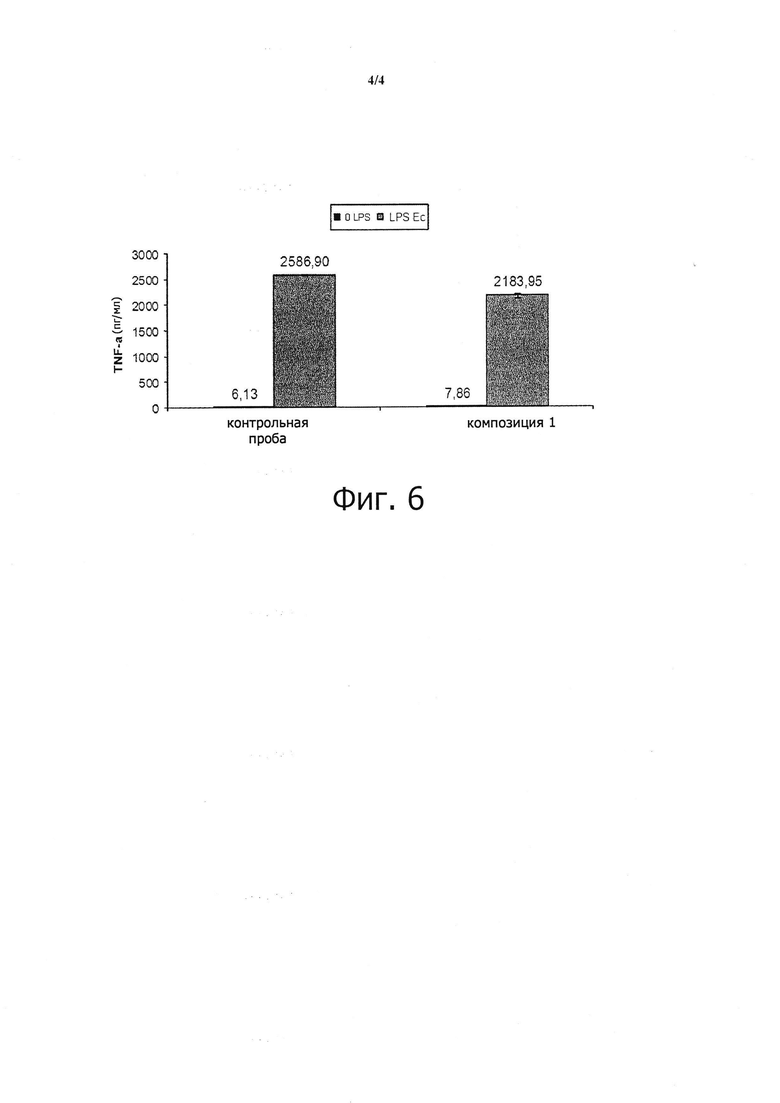
Испытания проводились с учетом культуральной среды, результаты представлены на фиг. 6.
Отложенные по оси ординат, эти результаты указывают на количество TNF-α, которое определили в надосадочном слое макрофагов в пг/мл. Макрофаги инкубировали в композиции 1, разбавленной культуральной средой в соотношении 1: 2, и стимулировали липополисахаридом Escherichia Coli в течение 24 часов при 37°C.
На фиг. 6 представлены результаты, полученные для контрольной пробы без применения липополисахарида (О LPS) и с применением липополисахарида Escherichia Coli. Также на фиг. 6 приведены результаты, полученные для композиции (1) без применения липополисахарида Escherichia Coli и с его применением. Согласно фиг. 6 композиция (1) благоприятна для снижения воспалительных явлений.
В таблице 5 указаны результаты, представленные на фиг. 6 и выраженные в виде соотношения: количество TNF-α, секретированное в контрольной пробе без липополисахарида, отнесено к 1, а количества TNF-α, секретированные в других условиях, соотнесены с количеством TNF-α, секретированным в контрольной пробе (при этом количество TNF-α разделено на количество TNF-α в контрольной пробе).

В том случае, когда клетки стимулировали посредством липополисахарида для возбуждения воспаления предварительная инкубация с применением разведенной в соотношении 1:2 композиции 1 снижала производство TNF-α (x422 → x356).
| название | год | авторы | номер документа |
|---|---|---|---|
| ГЛАЗНЫЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ МУКОАДГЕЗИВНЫЕ ПОЛИСАХАРИДЫ, СПОСОБНЫЕ СТИМУЛИРОВАТЬ ВОССТАНОВЛЕНИЕ ЭПИТЕЛИЯ РОГОВИЦЫ | 2013 |
|
RU2663449C2 |
| ГЛАЗНЫЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ МУКОАДГЕЗИВНЫЕ ПОЛИСАХАРИДЫ, СПОСОБНЫЕ СТИМУЛИРОВАТЬ ВОССТАНОВЛЕНИЕ ЭПИТЕЛИЯ РОГОВИЦЫ | 2006 |
|
RU2493854C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ИНГИБИРОВАНИЯ ПУТИ JAK | 2010 |
|
RU2557982C2 |
| 1-ЭТАНОЛАМИД PGF ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2001 |
|
RU2252212C2 |
| АМИДНЫЕ СОЕДИНЕНИЯ | 2015 |
|
RU2684906C2 |
| Замещенные производные N-[2-(4-феноксипиперидин-1-ил)-2-(1,3-тиазол-5-ил)этил]бензамида и N-[2-(4-бензилоксипиперидин-1-ил)-2-(1,3-тиазол-5-ил)этил]бензамида в качестве антагонистов P2X7 рецептора | 2017 |
|
RU2755705C2 |
| КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ БОЛЕЗНИ ГЛАЗ, СВЯЗАННОЙ С НУКЛЕИНОВЫМИ КИСЛОТАМИ | 2012 |
|
RU2642609C2 |
| iPHK-ОПОСРЕДОВАННОЕ ИНГИБИРОВАНИЕ СВЯЗАННЫХ С ФАКТОРОМ НЕКРОЗА ОПУХОЛИ АЛЬФА СОСТОЯНИЙ | 2007 |
|
RU2469090C2 |
| СПОСОБЫ ЛЕЧЕНИЯ С ИСПОЛЬЗОВАНИЕМ СОЕДИНЕНИЯ-ИНГИБИТОРА JAK | 2018 |
|
RU2764979C2 |
| КОМПОЗИЦИЯ ДЛЯ ОБРАБОТКИ КОНТАКТНЫХ ЛИНЗ | 1998 |
|
RU2139094C1 |

Изобретение относится к раствору на основе морской воды для аппликаций на глаза, кожу и слизистые оболочки. Водная композиция получена на основе очищенной воды, имеет показатель pH 5,5-7,5, осмотическую концентрацию 200-400 миллиосмолей/кг, удельную проводимость 17-22,5 мСм/см при 25°C и приготовлена с использованием фильтрованной морской воды в количестве 1-20%, соли калия в концентрации 90-180 ммоль/л и Zn(X)2 в концентрации 200-300 мкмоль/л. 2 н. и 9 з.п. ф-лы, 5 табл., 6 ил.
1. Водная композиция, предназначенная для аппликаций на глаза, кожу или слизистые оболочки, полученная на основе очищенной воды, имеющая показатель рН 5,5–7,5, осмотическую концентрацию 200–400 миллиосмолей/кг, удельную проводимость 17–22,5 мСм/см при 25ºС и приготовленная с использованием фильтрованной морской воды в количестве 1–20%, соли калия в концентрации 90–180 ммоль/л и Zn(X)2 в концентрации 200-300 мкмоль/л, где Х означает любой тип противоиона в комплексе с катионом Zn2+.
2. Композиция по п. 1, имеющая рН 6–7,2.
3. Композиция по п. 1 или 2, в которой ионами Х- являются ионы хлоридов.
4. Композиция по любому из пп. 1, 2, в которой солью калия является хлорид калия.
5. Композиция по любому из пп. 1, 2 для применения в качестве лекарства при лечении глазных болезней путём инактивации рецепторов гибели клеток типа Р2Х7.
6. Композиция по любому из пп. 1, 2 для применения по меньшей мере в качестве одного из элементов, выбранного из наружного глазного средства, искусственных слёз, раствора для промывки контактных линз, раствора для промывки глаз и вещества контейнера для глазного имплантата.
7. Композиция по любому из пп. 1, 2 для применения в качестве лекарства при лечении по меньшей мере одного из элементов, выбранного из слизистых оболочек носа, слизистых оболочек рта, слизистых оболочек влагалища и кожи.
8. Композиция по любому из пп. 1, 2 для применения в качестве лекарства при лечении для заживления по меньшей мере одного из элементов, выбранных из слизистых оболочек и кожи.
9. Композиция по любому из пп. 1, 2 для применения в качестве индифферентного вещества при солюбилизации молекул, имеющих терапевтическое значение.
10. Способ приготовления композиции по любому из пп. 1–9, включающий в себя следующие этапы:
а) закачивание морской воды;
б) добавление к отфильтрованному раствору соли цинка и соли калия;
в) разбавление отфильтрованного раствора очищенной водой.
11. Способ приготовления композиции по п. 10, дополнительно включающий в себя после этапа а) следующие этапы:
- предварительная обработка морской воды посредством первого естественного или искусственного фильтра после этапа а);
- фильтрация морской воды, прошедшей при необходимости предварительную обработку, через второй фильтр, средний диаметр пор которого составляет менее или равен 5 мкм;
- последующая фильтрация через третий фильтр, средний диаметр пор которого меньше среднего диаметра пор второго фильтра и составляет менее или равен 0,45 мкм.
| Грузоподъёмное устройство | 2022 |
|
RU2803205C1 |
| DE 10027474 A1, 15.03.2001 | |||
| Tomokazu Watano et al | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| J | |||
| Pharmacol., 2002, 89, pages 296 - 301 | |||
| ГЛАЗНЫЕ КАПЛИ ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНИ СУХОГО ГЛАЗА | 2011 |
|
RU2459615C1 |
Авторы
Даты
2018-10-12—Публикация
2014-04-29—Подача