ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к 4-[(1S)-1-({[4-бром-1-(изохинолин-3-илметил)-3-метил-1H-пиразол-5-ил]карбонил}амино)этил]бензойной кислоте (далее по тексту иногда именуемой «соединением A») или ее солям, которые применимы в качестве действующего ингредиента фармацевтической композиции, например, фармацевтической композиции для лечения хронической почечной недостаточности и/или диабетической нефропатии.
УРОВЕНЬ ТЕХНИКИ
Простагландин E2 (далее по тексту именуемый «PGE2») известен в качестве одного из метаболитов в каскаде арахидоновой кислоты. PGE2 проявляет различные виды физиологической активности и вовлечен в появление и усиление боли, провоспалительное действие и антивоспалительное действие, маточные сокращения, содействие перистальтике пищеварительного тракта, пробуждение, ингибирование секреции желудочной кислоты, гипотензивное действие, ингибирование агрегации тромбоцитов, содействие резорбции костной ткани, ангиогенное действие и т.п.
Существует четыре подтипа рецепторов PGE2, а именно EP1, EP2, EP3 и EP4, которые широко распространены в различных тканях. Активация рецептора EP1 вызывает повышение внутриклеточного уровня Ca2+. Активация рецептора EP3 приводит к повышению внутриклеточного уровня Ca2+ и вызывает ингибирование аденилат циклазы, за счет чего понижается внутриклеточный уровень cAMP. Активация рецепторов EP2 и EP4 вызывает активацию аденилат циклазы, за счет чего повышаются внутриклеточные уровни cAMP. В частности, считается, что рецептор EP4 связан с расслаблением гладкой мускулатуры, активацией или подавлением воспалительной реакции, дифференцировкой лимфоцитов, гипертрофией или пролиферацией мезангиальных клеток, секрецией слизи в желудочно-кишечном тракте и т.п. (Pharmacology & Therapeutics 2013, 138:485-502; Pharmacological Reviews 2013, 65:1010-1052; and American Journal of Physiology Renal Physiology 2004, 287, F673-F681).
Ингибитор рецептора PGE2 т.е. антагонист рецептора EP, обладает способностью связываться с рецептором EP и ингибировать действие PGE2 на рецептор EP. Соответственно, ожидается, что антагонист рецепторов EP будет являться средством лечения заболеваний, вызванных PGE2. В том числе ожидается, что антагонист рецептора EP4 будет являться лекарственным средством для лечения заболеваний, связанных с EP4, например, почечных заболеваний, воспалительных заболеваний и различных видов боли у людей и животных (Journal of American Society Nephrology 2010, 21:1678-1690; Proceedings of the National Academy of Sciences, 2010, 107:12233-12238; и The Journal of Pharmacology and Experimental Therapeutics 2008, 325:425-434). Кроме того, антагонист, проявляющий селективность в отношении рецептора EP4, предпочтителен, поскольку он позволяет избежать побочных эффектов, связанных с антагонизмом к другим рецепторам EP1, EP2, и EP3 (Physiological Reviews 1999, 79:1193-1226; и Annual Reviews Physiology 2001, 63:579-605).
В патентном документе 1 сообщается о соединении, представленном приведенной ниже формулой (B), в качестве антагониста рецептора EP4.
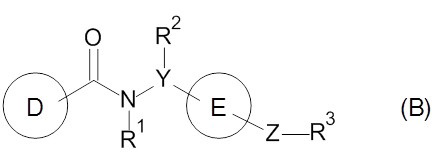
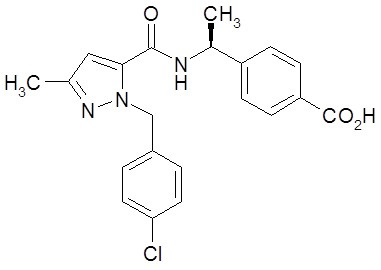
(В этой формуле, циклический фрагмент D представляет собой группу приведенной ниже формулы (III) или аналогичную, и в этой формуле циклический фрагмент D1 представляет собой моноциклический или бициклический азотсодержащий гетероцикл, который может быть замещен фенилом, R41 означает -X2-B4, X2 означает C1-6 алкилен или подобный фрагмент, и B4 представляет собой арил, гетероцикл или подобный фрагмент, каждый из которых может быть замещен 1-5 одинаковыми или различными группами, выбранными из числа групп R4. Со значением остальных символов можно ознакомиться в указанном патентом документе.)
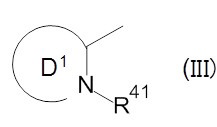
В примере 205 указанного патентного документа, раскрыто следующее типовое соединение, и это соединение приведено, как конкретное соединение, в котором циклический фрагмент D1 представляет собой пиразол.
В патентном документе 2 сообщается о соединении, представленном приведенной ниже формулой (C), в качестве антагониста рецептора EP4.
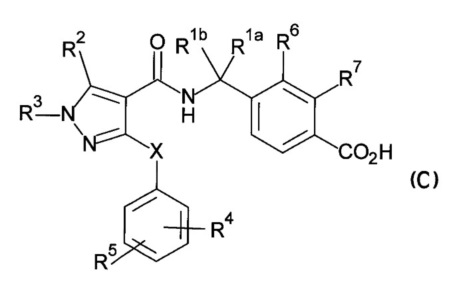
(В приведенной формуле, R2 означает метил, фторметил, и т.п., и R4 представляет собой фторметил, метокси и т.п. Со значением остальных символов в формуле можно ознакомиться в указанном патентом документе.)
В патентном документе 3 сообщается о соединении приведенной ниже формулы (D), в качестве антагониста рецептора EP4
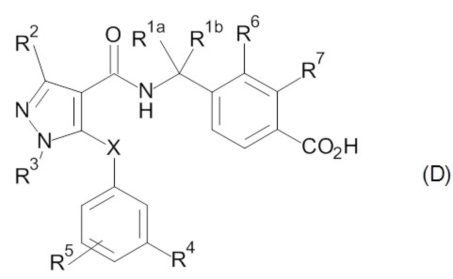
(В этой формуле, R2 означает метил, фторметил (например, монофторметил, дифторметил и трифторметил) и т.п., и R4 представляет собой фторметил, метокси и т.п. Со значением остальных символов можно ознакомиться в указанном патентом документе.)
В патентном документе 4 сообщается о соединении, представленном приведенной ниже формулой (E), как о лиганде рецептора EP4
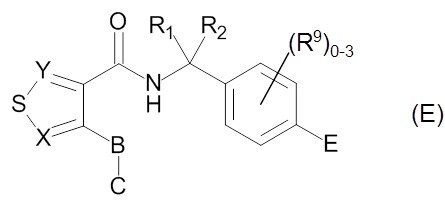
(Для ознакомления со значениями символов в этой формуле следует обратиться к указанному патентному документу.)
В патентном документе 5 сообщается о соединении приведенной ниже формулы (F), в качестве антагониста рецептора EP4.
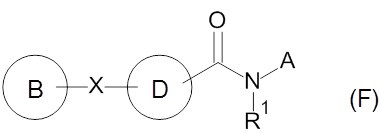
(В этой формуле, циклический фрагмент B и циклический фрагмент D являются одинаковыми или отличаются друг от друга и представляют собой арилы, которые могут являться замещенными, или гетероциклы, которые могут быть замещенными, X означает простую связь, -R00- и т.п., R00 означает низший алкилен, и R1 означает H и т.п. A означает группу приведенной ниже формулы (II) и т.п. и в этой приведенной ниже формуле, Y означает CH и т.п., R2 означает R0 и т.п., R0 означает низший алкил, Z означает простую связь и т.п., R3 означает -COOH и т.п. Со значением остальных символов можно ознакомиться в указанном патентом документе.)
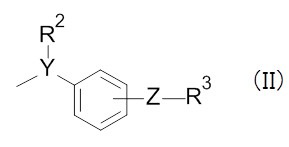
В этом патентном документе не раскрыто конкретное соединение, в котором цикл D представляет собой пиразол.
В патентных документах 1-5, структуры соединений, конкретно раскрытых в примерах, отличаются от соединения A.
Документы известного уровня техники
Патентные документы
Патентный документ 1: WO 2009/139373
Патентный документ 2: WO 2012/103071
Патентный документ 3: WO 2012/039972
Патентный документ 4: WO 2008/017164
Патентный документ 5: WO 2009/005076
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Проблемы, которые предполагалось решить настоящим изобретением
В изобретении предложено соединение, которое пригодно в качестве действующего ингредиента фармацевтической композиции, например, фармацевтической композиции для лечения хронической почечной недостаточности и/или диабетической нефропатии.
Средства для решения указанной проблемы
Авторы настоящего изобретения провели обширные исследования по поиску соединения, оказывающее антагонистическое действие на рецептор EP4, и обнаружили, что 4-[(1S)-1-({[4-бром-1-(изохинолин-3-илметил)-3-метил-1H-пиразол-5-ил]карбонил}амино)этил]бензойная кислота (соединение A), представленная формулой (I), или ее соли обладают отличным антагонистическим действием на рецептор EP4, что позволило завершить работу над настоящим изобретением.
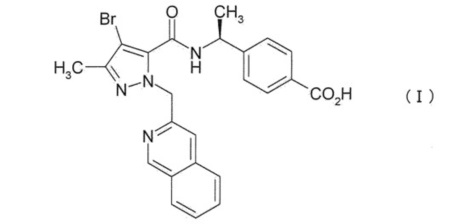
Таким образом, настоящее изобретение относится к соединению A или его соли, а также к фармацевтической композиции, содержащей соединение A или его соль и фармацевтически приемлемый эксципиент.
Кроме того, настоящее изобретение относится к фармацевтической композиции для предотвращения или лечения хронической почечной недостаточности и/или диабетической нефропатии, содержащей соединение A или его соль, а также фармацевтически приемлемый эксципиент.
Далее, настоящее изобретение относится к применению соединения A или его соли для получения фармацевтической композиции, предназначенной для предотвращения или лечения хронической почечной недостаточности и/или диабетической нефропатии; применению соединения A или его соли для предотвращения или лечения хронической почечной недостаточности и/или диабетической нефропатии; соединению A или его соли для предотвращения или лечения хронической почечной недостаточности и/или диабетической нефропатии; а также к способу предотвращения или лечения хронической почечной недостаточности и/или диабетической нефропатии, включающему введение субъекту эффективного количества соединения A или его соли. В контексте настоящего изобретения, «субъект» представляет собой человека или животного, не являющегося человеком, которому необходима профилактика или лечение, и в одном из вариантов осуществления, человека, которому необходима профилактика или лечение.
Эффекты настоящего изобретения
Соединение A или его соль оказывают антагонистическое действие на рецептор EP4 и их можно применять в качестве действующих ингредиентов фармацевтической композиции для предотвращения и/или лечения хронической почечной недостаточности и/или диабетической нефропатии.
Варианты осуществления изобретения
Ниже показаны варианты осуществления соединения A или его соли по настоящему изобретению. Кроме того, в настоящем описании простое упоминание соединения A означает соединение A в свободной форме, а не в форме соли.
(1) Соединение A или его соль.
(1-1) Соединение A.
(1-2) Метансульфонат соединения A.
(2) Кристаллическая форма соединения A или его соли, описанных в (1).
(3) Кристаллическая форма соединения A, описанного в (1-1).
(3-1) Кристаллическая форма соединения A, описанная в (3), для которой температура появления эндотермического пика при дифференциальной сканирующей калориметрии (DSC анализ) составляет приблизительно 253°C.
(3-2) Кристаллическая форма соединения A, описанная в (3), которая демонстрирует пики при углах 2θ (°) равных примерно 5,7, примерно 7,9, примерно 11,5, примерно 13,1 и примерно 17,9 на картине дифракции рентгеновских лучей на порошке при использовании источника с медным анодом.
(3-3) Кристаллическая форма соединения A, описанная в (3), которая демонстрирует пики при углах 2θ (°) равных примерно 5,7, примерно 7,9, примерно 8,3, примерно 8,9, примерно 9,2, примерно 11,5, примерно 12,5, примерно 13,1, примерно 15,8, примерно 16,3, примерно 16,7, примерно 17,2, примерно 17,9, примерно 18,5 и примерно 19,5 на картине дифракции рентгеновских лучей на порошке при использовании источника с медным анодом.
(3-4) Кристаллическая форма соединения A, описанная в (3), для которой температура появления эндотермического пика в DSC анализе составляет приблизительно 253°C, и на картине дифракции рентгеновских лучей на порошке присутствуют пики при углах 2θ (°) равных примерно 5,7, примерно 7,9, примерно 11,5, примерно 13,1 и примерно 17,9 при использовании источника с медным анодом.
(3-5) Кристаллическая форма соединения A, описанная в (3), для которой температура появления эндотермического пика в DSC анализе составляет приблизительно 253°C, и на картине дифракции рентгеновских лучей на порошке присутствуют пики при углах 2θ (°) равных примерно 5,7, примерно 7,9, примерно 8,3, примерно 8,9, примерно 9,2, примерно 11,5, примерно 12,5, примерно 13,1, примерно 15,8, примерно 16,3, примерно 16,7, примерно 17,2, примерно 17,9, примерно 18,5 и примерно 19,5 при использовании источника с медным анодом.
(4) Кристаллическая форма метансульфоната соединения A, описанного в (1-2).
(4-1) Кристаллическая форма метансульфоната соединения A, описанная в (4), для которой температура появления эндотермического пика в DSC анализе составляет приблизительно 192°C.
(4-2) Кристаллическая форма метансульфоната соединения A, описанная в (4), которая демонстрирует пики при углах 2θ (°) равных примерно 4,7, примерно 9,5, примерно 12,0, примерно 13,2, примерно 13,7, примерно 15,3, примерно 18,8, примерно 20,3, примерно 20,9 и примерно 22,8 на картине дифракции рентгеновских лучей на порошке при использовании источника с медным анодом.
(4-3) Кристаллическая форма метансульфоната соединения A, описанная в (4), для которой температура появления эндотермического пика в DSC анализе составляет приблизительно 192°C, и на картине дифракции рентгеновских лучей на порошке присутствуют пики при углах 2θ (°) равных примерно 4,7, примерно 9,5, примерно 12,0, примерно 13,2, примерно 13,7, примерно 15,3, примерно 18,8, примерно 20,3, примерно 20,9 и примерно 22,8 при использовании источника с медным анодом.
(5-1) Фармацевтическая композиция, содержащая соединение, описанное в любом из (1)-(1-2), а также фармацевтически приемлемый эксципиент.
(5-2) Фармацевтическая композиция, содержащая кристаллическую форму, описанную в любом из (2)-(4-3), а также фармацевтически приемлемый эксципиент.
(5-3) Фармацевтическая композиция для профилактики или лечения хронической почечной недостаточности и/или диабетической нефропатии, содержащая соединение, описанное в любом из (1)-(1-2), а также фармацевтически приемлемый эксципиент.
(5-4) Фармацевтическая композиция для профилактики или лечения хронической почечной недостаточности и/или диабетической нефропатии, содержащая кристаллическую форму, описанную в любом из (2)-(4-3), а также фармацевтически приемлемый эксципиент.
(6-1) Применение соединения, описанного в любом из (1)-(1-2), для производства фармацевтической композиции, предназначенной для профилактики или лечения хронической почечной недостаточности и/или диабетической нефропатии.
(6-2) Применение кристаллической формы, описанной в любом из (2)-(4-3), для производства фармацевтической композиции, предназначенной для профилактики или лечения хронической почечной недостаточности и/или диабетической нефропатии.
(7-1) Соединение, описанное в любом из (1)-(1-2), для профилактики или лечения хронической почечной недостаточности и/или диабетической нефропатии.
(7-2) Кристаллическая форма, описанная в любом из (2)-(4-3), для профилактики или лечения хронической почечной недостаточности и/или диабетической нефропатии.
(8-1) Применение соединения, описанного в любом из (1)-(1-2), для профилактики или лечения хронической почечной недостаточности и/или диабетической нефропатии.
(8-2) Применение кристаллической формы, описанной в любом из (2)-(4-3), для профилактики или лечения хронической почечной недостаточности и/или диабетической нефропатии.
(9-1) Способ профилактики или лечения хронической почечной недостаточности и/или диабетической нефропатии, включающий введение субъекту эффективного количества соединения, описанного в любом из (1)-(1-2).
(9-2) Способ профилактики или лечения хронической почечной недостаточности и/или диабетической нефропатии, включающий введение субъекту эффективного количества кристаллической формы, описанной в любом из (2)-(4-3).
Кроме того, настоящее изобретение дополнительно включает фармацевтически приемлемое пролекарство соединения A или его соль. Термин «фармацевтически приемлемое пролекарство» относится к соединению, имеющему группу, которая может быть превращена в карбоксильную группу в результате сольволиза или в физиологических условиях. Примеры групп, которые подходят для получения пролекарств, включают группы, описанные в Prog. Med., 5, 2157-2161 (1985) или ʺPharmaceutical Research and Developmentʺ (Hirokawa Publishing Company, 1990), vol. 7, Drug Design, 163-198.
В настоящем изобретении, соль соединения A является фармацевтически приемлемой солью, и соединение A может в некоторых случаях образовывать кислотно-аддитивную соль или соль с основанием. Конкретные примеры солей включают кислотно-аддитивные соли с неорганическими кислотами, такими как хлористоводородная кислота, бромистоводородная кислота, йодистоводородная кислота, серная кислота, азотная кислота и фосфорная кислота, или с органическими кислотами, такими как муравьиная кислота, уксусная кислота, пропионовая кислота, щавелевая кислота, малоновая кислота, янтарная кислота, фумаровая кислота, малеиновая кислота, молочная кислота, яблочная кислота, миндальная кислота, винная кислота, дибензоилвинная кислота, дитолилвинная кислота, лимонная кислота, метансульфоновая кислота, этансульфоновая кислота, бензолсульфоновая кислота, п-толуолсульфоновая кислота, аспарагиновая кислота и глутаминовая кислота, а также соли с неорганическими основаниями, такими как гидроксиды натрия, калия, магния, кальция и алюминия, или с органическими основаниями, такими как метиламин, этиламин, этаноламин, лизин и орнитин, соли с различными аминокислотами, такими как ацетиллейцин или с производными аминокислот, а также соли аммония.
Кроме того, настоящее изобретение дополнительно включает различные гидраты или сольваты, а также полиморфы соединения A или его солей. Далее, настоящее изобретение включает также соединение A или его соли, меченые различными радиоактивными или не радиоактивными изотопами.
В настоящем описании термины «примерно», «около», использованные при описании дифракционного угла (2θ(°)) на картине дифракции рентгеновских лучей на порошке и температуры появления (°C) эндотермического пика в анализе DSC, включают обычно допустимый диапазон погрешности способа измерения данных, и как правило означает величину, при которой начинается дифракционный пик и эндотермический пик. Диапазон погрешности измерения дифракционного угла (2θ(°)) в способе дифракции рентгеновских лучей на порошке составляет, в одном из вариантов осуществления, ±0,2°, и в другом варианте осуществления±0,1°. Диапазон погрешности определения температуры появления эндотермического пика на термограмме DSC (°C) составляет в одном из вариантов осуществления ±2°C и в другом варианте осуществления ±1°C.
Кроме того, что касается картины дифракции рентгеновских лучей на порошке, расстояния между плоскостями в кристаллической решетке и общий вид дифракционной картины важны для идентификации кристаллов, с точки зрения характера данных, причем дифракционные углы и интенсивность пиков могут слегка меняться в зависимости от направления роста кристалла, размера частиц и условий регистрации рентгенограммы.
Методика получения
Соединение A или его соль можно получать с помощью различных методик синтеза, с учетом характерных особенностей их основной структуры и типов заместителей. В настоящее время, в зависимости от типов функциональных групп, с точки зрения методики получения в некоторых случаях эффективно замещать функциональные группы подходящими защитными группами (группы, которые способны легко превращаться в функциональные группы) на стадиях, в которых принимают участие исходные вещества и интермедиаты. Примеры защитных групп включают защитные группы, описанные в ʺGreene's Protective Groups in Organic Synthesis (4th edition, 2006)ʺ, P. G. M. Wuts и T. W. Greene и подобные, которые следует выбирать и применять в зависимости от условий проведения реакции. В таких методиках, желаемое соединение можно получать путем введения защитных групп для проведения реакции и затем, если это желательно, удаления защитных групп.
Кроме того, можно получать пролекарство соединения A, путем введения определенной группы на стадиях, начиная от исходных веществ и до интермедиатов, способами, аналогичными упомянутым выше для защитных групп, или путем проведения дополнительных реакций с участием уже полученного соединения A. Реакцию можно проводить способом, известным специалисту в данной области техники, например, с использованием общих методик этерификации, амидирования, дегидратации и т.п.
Ниже по тексту будут описаны типовые способы получения соединения A. Каждый из способов получения можно осуществлять по методикам, приведенным в документах, упомянутых в настоящем описании. В связи с этим, способы получения по настоящему изобретению не ограничены приведенными ниже примерами. Кроме того, если конкретно не указано иное, в случае, если символы в структурных формулах в способе получения по настоящему изобретению, используются также в других структурных формулах, одни и те же символы имеют одинаковые значения.
Способ получения 1
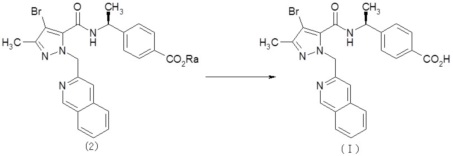
На приведенной выше схеме, Ra представляет собой линейный или разветвленный алкил, включающий от 1 до 6 атомов углерода, например, метил, этил и т.п.
Соединение A, представленное формулой (I), можно получить гидролизом соединения, представленного общей формулой (2). В данном случае, реакцию гидролиза можно проводить по методике, описанной в упомянутой выше книге: Greene's Protective Groups in Organic Synthesis (4th edition, 2006).
Синтез исходных веществ
Способ получения исходных веществ 1
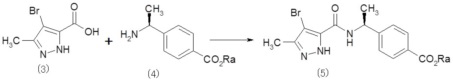
Исходное соединение (5) можно получить реакцией амидирования соединения (3) и соединения (4).
Взаимодействие проводят, используя эквивалентные количества соединения (3) и соединения (4) или избыточное количество любого из них, при перемешивании смеси в диапазоне температур от охлаждения до нагревания, предпочтительно, при температурах от -20°C до 60°C, как правило в течение 0,1 часа-5 дней, в растворителе, который не принимает участия в реакции, в присутствии конденсирующего агента. На растворитель, применяемый в данной реакции, не накладывается конкретных ограничений, и примеры таких растворителей включают ароматические углеводороды, такие как бензол, толуол, ксилол и т.п., галогенированные углеводороды, такие как дихлорметан (DCM), 1,2-дихлорэтан (DCE), хлороформ и т.п., простые эфиры, такие как диэтиловый эфир, тетрагидрофуран (ТГФ), диоксан, диметоксиэтан (DME) и т.п., N,N-диметилформамид (ДМФА), диметилсульфоксид (ДМСО), этилацетат, ацетонитрил, вода или их смеси. В качестве конденсирующего агента в некоторых случаях предпочтительно могут применяться гексафторфосфат 1-[бис(диметиламино)метилен]-1H-1,2,3-триазоло[4,5-b]пиридин-1-ий-3-оксида (HATU), гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида, 1-(3-диметиламинопропил)-3-этилкарбодиимид, дициклогексилкарбодимиид (DCC), 1,1ʹ-карбонилдиимидазол (CDI), азид дифенилфосфорной кислоты, оксихлорид фосфора, полистирольная смола, несущая конденсирующий агент, например, PS-карбодиимид (Argonaut Technologies, Inc., USA) и т.п., но конденсирующие агенты не ограничиваются перечисленными. Далее, при проведении реакции в некоторых случаях может оказаться предпочтительным применение добавок, таких как, например, 1-гидроксибензотриазол (HOBt) или подобных, и в некоторых случаях для гладкого протекания реакции может быть предпочтительно проводить ее в присутствии, например, органического основания, такого как триэтиламин (TEA), N,N-диизопропилэтиламин (DIPEA), N-метилморфолин (NMM) и т.п., или неорганического основания, такого как карбонат калия, карбонат натрия, гидроксид калия и т.п. Кроме того, предпочтительно применять полистирольную смолу, несущую изоцианат, например, PS-Isocyanate (Argonaut Technologies, Inc., USA) и т.п. для удаления избытка амина после завершения реакции. Помимо этого, для удаления избытка карбоновой кислоты и упомянутых выше добавок и т.п. после завершения реакции может применяться полистирольная смола, несущая четвертичную аммониевую соль, например, MP-Carbonate (Argonaut Technologies, Inc., USA).
Кроме того, может применяться способ, в котором соединение (3) превращают в его реакционноспособное производное, и затем это реакционноспособное производное вводят во взаимодействие с соединением (4). В этом случае, примеры реакционноспособного соединения (3) включают галогенангидриды кислоты, которые получают взаимодействием с галогенирующими агентами, такими как оксихлорид фосфора, тионилхлорид и т.п., смешанные ангидриды кислот, которые получают взаимодействием с изобутилхлорформиатом и т.п., активные эфиры, которые получают конденсацией с HOBt и т.п. и прочие реакционноспособные производные. Взаимодействие этих реакционноспособных производных с соединением (4) можно проводить при температурах в диапазоне от охлаждения до нагревания, предпочтительно от -20°C до 60°C, в растворителе, который инертен к компонентам и продуктам реакции, например, галогенированных углеводородах, ароматических углеводородах и простых эфирах.
Способ получения исходных веществ 2
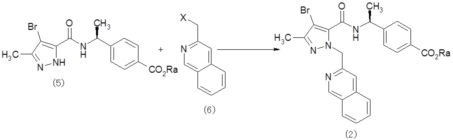
На схеме X означает уходящую группу.
Исходное соединение (2) можно получать реакцией алкилирования между соединением (5) и соединением (6).
Конкретные примеры уходящей группы X включают галоген, метансульфонилокси, п-толуолсульфонилокси, трифторметансульфонилокси и подобные группы.
Реакцию проводят, используя эквивалентные количества соединения (5) и соединения (6) или избыточные количества любого из соединений, осуществляя перемешивание смеси в диапазоне температур от охлаждения до нагревания до кипения с обратным холодильником, предпочтительно от 0°C до 80°C, в растворителе, который не взаимодействует с компонентами и продуктами реакции, или без растворителя, как правило, в течение периода времени от 0,1 часа до 10 дней. Примеры растворителей, применяемых для проведения реакции, не ограничены конкретными рамками, но включают ароматические углеводороды, такие как бензол, толуол, ксилол и т.п, простые эфиры, такие как диэтиловый эфир, ТГФ, диоксан, DME и т.п., галогенированные углеводороды, такие как DCM, DCE, хлороформ и т.п., ДМФА, ДМСО, 1-метил-2-пирролидон, диметилацетамид, ацетон, этилацетат, ацетонитрил и их смеси. В некоторых случаях для гладкого протекания реакции может быть предпочтительно проводить реакцию в присутствии органического основания, такого как TEA, DIPEA, NMM и т.п. или неорганического основания, такого как трет-бутоксид калия, карбонат цезия, карбонат калия, карбонат натрия, гидроксид калия и т.п.
Соединение A выделяют и очищают в форме свободного соединения, его соли, гидрата, сольвата или полиморфа. Соль соединения A можно получать стандартной реакцией получения солей.
Выделение и очистку можно проводить с применением стандартных химических операций, таких как экстракция, дробная кристаллизация, различные типы фракционной хроматографии и т.п.
Например, оптические изомеры можно получать стандартными способами оптического разделения рацемических соединений (например, дробной кристаллизацией с превращением соединения в диастереомерные соли с оптически активными основаниями или кислотами, хроматографией с использованием хиральной колонки и т.п., а также другими способами), или их можно получать из подходящих оптически активных исходных соединений.
Фармакологическую активность соединения A подтверждали следующими тестами.
Тестовый пример 1: Тест для оценки сродства к крысиному рецептору EP4
Конструирование вектора экспрессии крысиного рецептора EP4:
Ген крысиного рецептора EP4 (учетный No GenBank: NM_032076.1) трансфецировали в вектор экспрессии pcDNA3.1-V5-His-TOPO (Invitrogen Inc.).
Временная экспрессия крысиного рецептора EP4:
Вектор экспрессии крысиного рецептора EP4 трансфецировали в клетки HEK-293 (ATCC No: CRL-1573). Трансфекцию осуществляли согласно приложенной инструкции, используя реагент Lipofectamine (зарегистрированная торговая марка) 2000 (Invitrogen Inc.). После трансфекции клетки культивировали в культуральной среде α-MEM в течение 20-24 часов.
Получение фракции мембран:
Культуральную среду удаляли отсасыванием, в 15 см чашку добавляли 10 мл охлажденного фосфатного буферного солевого раствора(PBS) и соскребали клетки, используя скребок для клеток (Sumitomo Bakelite). Клетки собирали, центрифугировали (250×g, 4°C, 5 мин) и затем суспендировали в 6 мл охлажденного 20 ммоль/л Tris-HCl (pH 7,4; Nakalai Tesque Inc., содержащим 5 ммоль/л этилендиаминтетрауксусной кислоты (EDTA, Nakalai Tesque Inc.)) на чашку. Полученную смесь гомогенизировали с использованием прибора Polytron (зарегистрированная торговая марка) и гомогенат центрифугировали (69 000×g, 20 мин, 4°C). Полученный осадок ресуспендировали в охлажденном 20 ммоль/л Tris-HCl, повторно гомогенизировали используя Polytron и гомогенат центрифугировали (69 000×g, 20 мин, 4°C). Полученный осадок суспендировали в 50 ммоль/л HEPES-NaOH (Dojindo Laboratories) (pH 7,5) в количестве 1 мл на чашку, затем гомогенизировали и хранили при охлаждении до -80°C в качестве фракции мембран. Одновременно, часть полученного продукта использовали для измерения концентрации белка. Измерение концентрации белка проводили в двух независимых параллельных экспериментах, используя набор для определения белка Bio-Rad Protein assay kit (Bio-Rad Laboratories) согласно приложенному стандартному протоколу.
Исследование связывания
[3H]PGE2 и фракцию клеточных мембран разбавляли аналитическим (50 ммоль/л HEPES-NaOH, 10 ммоль/л, MgCl2, pH 7,5) и тестируемое соединение и немеченый PGE2 (Cayman) разбавляли ДМСО и аналитическим буфером. Использовали реакционную жидкость (200 мкл) следующего состава: 50 мкл 50 ммоль/л HEPES-NaOH (pH 7,5), 10 ммоль/л MgCl2, 0,3 нмоль/л [3H]PGE2 (Perkin Elmer), 100 мкл фракции клеточных мембран, содержащей крысиный EP4 (200 мкг белка/мл) и 50 мкл тестируемого соединения (конечные концентрации 0,1, 0,3, 1, 3, 10, 30 и 100 нмоль/л). Для измерения неспецифического связывания, немеченый PGE2 (Cayman) добавляли до конечной концентрации 1 мкмоль/л. Конечную концентрацию ДМСО устанавливали на уровне 1%. Реакционную жидкость инкубировали в 96-луночном микропланшете (Sumitomo Bakelite) при комнатной температуре в течение 1 часа. Реакционную жидкость фильтровали через фильтровальную бумагу UniFilter-96GF/B (Perkin Elmer), используя харвестер FilterMate (Perkin Elmer). Фильтровальную бумагу после фильтрования три раза промывали 300 мкл/лунку охлажденного аналитического буфера и затем высушивали в сушильном устройстве в течение ночи. К фильтрату добавляли 50 мкл/лунку жидкого сцинтиллятора MicroScint20 (Perkin Elmer). Измеряли радиоактивность, используя прибор TopCount (Perkin Elmer). Измерения в каждом случае проводили один раз в двух параллельных опытах. Специфическое связывание определяли путем вычитания неспецифического связывания из общего связывания. Значения Ki вычисляли стандартным способом.
В результате проведенных измерений, было обнаружено, что значение Ki соединения A для крысиного рецептора EP4 составляет 0,874 нмоль/л. Следует отметить, что значение Ki соединения примера 205 патентного документа 1 для крысиного рецептора EP4 составляло 140 нмоль/л.
Тестовый пример 2: Тест для определения сродства к человеческому рецептору EP4
Исследование связывания:
[3H]PGE2 и фракцию клеточных мембран, содержащую человеческий EP4 (Chemicon), разбавляли аналитическим буфером (50 ммоль/л HEPES-NaOH, 5 ммоль/л MgCl2, 1 ммоль/л CaCl2 (pH 7,4), 0,5% альбумин бычьей сыворотки (BSA)), кроме того тестируемое соединение и немеченый PGE2 (Sigma) разбавляли ДМСО и аналитическим буфером. Реакционная смесь (250 мкл) имела следующий состав: 175 мкл аналитического буфера, содержащего [3H]PGE2 (конечная концентрация 2,9 нмоль/л), 50 мкл фракции клеточных мембран (Chemicon, 40 мкг белка/мл) и 25 мкл тестируемого соединения (конечная концентрация 0,1, 1, 10, 100 и 1000 нмоль/л). Для измерения неспецифического связывания, добавляли немеченый PGE2 до конечной концентрации 10 мкмоль/л. Конечная концентрация ДМСО составляла 1%. Реакционную смесь инкубировали при 25°C в течение 60 минут. Реакционную смесь фильтровали с использованием фильтровальной бумаги GF/C (Whatman), используя клеточный харвестер (Brandel). После фильтрования, фильтровальную бумагу трижды промывали 1 мл раствора, содержащего 50 ммоль/л HEPES-NaOH (pH 7,4), 500 ммоль/л NaCl и 0,1% BSA. Фильтровальную бумагу GF/C помещали в аналитический флакон и добавляли к нему 5 мл жидкого сцинтиллятора Atomlight. Радиоактивность измеряли с помощью счетчика сцинтилляции жидкостей (Perkin Elmer). Каждое измерение проводили один раз в двух параллельных опытах. Специфическое связывание определяли вычитанием неспецифического связывания из общего связывания. Значения Ki вычисляли по стандартной методике.
В результате проведенных измерений было обнаружено, что значение Ki соединения A для человеческого рецептора EP4 составляло 1,46 нмоль/л.
Тестовый пример 3: Тест для определения антагонистического действия на человеческий рецептор EP4 путем измерения количества cAMP в человеческих клетках Jurkat
Клеточная культура:
Клетки Jurkat (выделены из лейкемической T-лимфомы человека) культивировали при 37°C в атмосфере 5% CO2, используя культуральную среду RPMI1640 (номер продукта 11879020, Invitrogen Inc.) c добавкой 10% сыворотки телят (FBS). После пролиферации клеток до половинной конфлюентности, к культуре добавляли индометацин с конечной концентрацией 5 мкмоль/л, и клетки культивировали в течение еще 18 часов. Клетки собирали в 15 мл пробирки Spitz, добиваясь концентрации 1×106 клеток/мл, с использованием Cell Banker (Mitsubishi Kagaku Iatron), и хранили при -80°C.
Обработка соединением:
Препараты тестируемого соединения получали разбавлением аналитическим буфером, содержащим 0,5% BSA (1×HBSS (буферированный солевой раствор Хэнка, Nissui Pharmaceutical Co., Ltd.), 20 ммоль/л HEPES-NaOH (Nakalai Tesque Inc.) (pH 7,4), 0,5 ммоль/л IBMX (3-изобутил-1-метилксантин, WAKO), 0,02% CHAPS (Sigma), 0,5% BSA (Sigma) и 2 мкмоль/л индометацин (Sigma)), доводя до 3-кратной концентрации относительно конечной концентрации. Готовили PGE2 в концентрации 300 нмоль/л с использованием аналитического буфера, содержащего 0,5% BSA. Клетки Jurkat, хранившиеся при низкой температуре, готовили в концентрации 1×106 клеток/мл путем оттаивания при 37°C с использованием аналитического буфера, содержащего 0,5% BSA. В лунки 384-луночного черного микропланшета с U-образным дном (Corning) добавляли тестируемые соединения (до конечной концентрации 0,01, 0,03, 0,1, 0,3, 1, 3 и 10 нмоль/л), клетки и PGE2 в указанном порядке в объеме 5 мкл, после чего встряхивали на шейкере для планшетов и затем инкубировали при комнатной температуре в течение 30 минут. Для определения количества cAMP без стимулирования PGE2, создавали группу образцов, в которые не добавляли PGE2.
Измерение и анализ количества cAMP:
Для измерения содержания cAMP использовали набор cAMP HiRange kit (Cisbio international). После инкубирования в каждую лунку добавляли 5 мкл реагента d2, который был разбавлен до 0,6-кратной концентрации буфером для лизиса (50 ммоль/л фосфатоного буфера (pH 7,0), 0,8 моль/л KF, 1% TritonX-100, 0,2% BSA), после чего осуществляли встряхивание на шейкере для планшетов. Затем в каждую лунку добавляли 5 мкл криптата европия из состава набора, который разбавляли до 0,6-кратной концентрации буфером для лизиса, после чего встряхивали на шейкере для планшетов и инкубировали при комнатной температуре в течение 60 минут, защищая от действия света. После инкубирования измеряли интенсивность флуоресценции криптата при 620 нм и интенсивность флуоресценции d2 при 665 нм, используя прибор ARVO1420 (Perkin Elmer). В каждую лунку добавляли cAMPs в концентрации 280, 70, 17,5, 4,38, 1,09, 0,27 и 0,068 нмоль/л и измеряли интенсивность флуоресценции, как описано выше, получая стандартную кривую. Все измерения проводили в трех параллельных экспериментах. Значения IC50 для соединения вычисляли способом логистической регрессии, исходя из количества cAMP при обработке соединением, принимая количество cAMP при добавлении PGE2 за 100% и принимая количество cAMP без добавления PGE2 за 0%. Вычисляли среднее значение из трех экспериментальных результатов.
По итогам проведенных измерений было обнаружено, что значение IC50 для выработки cAMP под действием PGE2 (100 нмоль/л) для соединения A в человеческих клетках Jurkat составляло 0,16 нмоль/л.
Тестовый пример 4: Тест для определения антагонистического действия на крысиный рецептор EP4 путем измерения количества cAMP
Конструирование вектора, экспрессирующего крысиный рецептор EP4: Конструирование данного вектора осуществляли способом, аналогичным описанному в тестовом примере 1.
Получение клеток, устойчиво экспрессирующих крысиный рецептор EP4:
Вектор экспрессии крысиного рецептора EP4 трансфецировали в клетки CHO-K1 (ATCC No.:CCL-61). Трансфекцию осуществляли согласно приложенной инструкции, используя реагент Lipofectamine (зарегистрированная торговая марка) 2000 (Invitrogen Inc.). После трансфекции клетки культивировали в культуральной среде α-MEM (No продукта 12571063, Invitrogen Inc.), содержащей G418 (Nakalai Tesque Inc.), для получения клона, устойчивого к лекарственному веществу.
Клеточная культура и обработка соединением:
Клетки CHO-K1, устойчиво экспрессирующие крысиный рецептор EP4, высевали в 96-луночные планшеты в количестве 0,5×104 клеток/100 мкл и культивировали в течение ночи. Культуральную среду заменяли смесью 2 мкмоль/л индометацин/0,5% BSA/культуральная среда α-MEM, которую через 60 минут заменяли смесью 1 ммоль/л IBMX/2 мкмоль/л индометацин/0,5% BSA/ культуральная среда α-MEM. Через 10 минут добавляли тестируемые соединения (до конечной концентрации 0,1, 0,3, 1, 3 и 10 нмоль/л) и затем через 10 минут добавляли PGE2 до конечной концентрации 100 нмоль/л (конечная концентрация ДМСО 0,1%). Для определения количества cAMP, образующегося в результате добавления PGE2, создавали группу образцов без добавления PGE2. Клетки культивировали и проводили реакцию в инкубаторе в атмосфере CO2 (37°C, 5%CO2). Через 30 минут удаляли культуральную среду и добавляли 100 мкл/лунку 0,2% Triton X-PBS для лизиса клеток. Тесты проводили дважды в двух параллельных экспериментах.
Измерение и анализ количества cAMP:
Содержание cAMP в клеточном лизате измеряли с использованием набора cAMP HiRange kit. Клеточный лизат из каждой лунки распределяли по лункам 384-луночных черных микропланшетов с U-образным дном в количестве 10 мкл, к лизату добавляли по 5 мкл реагента d2 и криптата европия в указанном порядке, после чего инкубировали при комнатной температуре в течение 60 минут, защищая от действия света. После инкубирования измеряли интенсивность флуоресценции криптата при 620 нм и интенсивность флуоресценции d2 при 665 нм, используя прибор ARVO1420. В каждую лунку добавляли cAMPs в концентрации 280, 70, 17,5, 4,38, 1,09, 0,27 и 0,068 нмоль/л, получая стандартную кривую, и измеряли интенсивность флуоресценции, как описано выше. Значения IC50 для тестируемых соединений вычисляли способом логистической регрессии, исходя из количества cAMP при обработке тестируемым соединением, принимая количество cAMP при добавлении PGE2 в конечной концентрации 100 нмоль/л за 100% и принимая количество cAMP без добавления PGE2 за 0%. Вычисляли среднее значение из двух экспериментальных результатов.
По итогам проведенных измерений было обнаружено, что значение IC50 для выработки cAMP под действием PGE2 (100 нмоль/л), для соединения A в крысиных клетках CHO-K1, экспрессирующих рецептор EP4, составляло 1,04 нмоль/л.
Тестовый пример 5: Тест in vivo для оценки антагонистического действия на крысиный рецептор EP4
Для теста использовали крыс SD (самцов в возрасте 6 недель), которым обеспечивали достаточный доступ к пище. Крысам осуществляли пероральное (po) введение тестируемого соединения, растворенного в смеси ПЭГ400:20% Tween80: 1 моль/л водный раствор NaHCO3=1:4:5, в дозировке 0,03 мг/кг (5 мл/кг). Через 1 час осуществляли подкожное (sc) введение в спину крыс активного метаболита (ONO-AE1-437 (CAS No.256382-23-7)) агониста EP4 ONO-4819, растворенного в физиологическом солевом растворе, в дозировке 0,01 мг/кг (5 мл/кг). Через 30 минут в хвостовую вену вводили липополисахарид (LPS, 0,01 мг/кг) (2 мл/кг), и через 60 минут под анестезией отбирали примерно 0,5 мл крови в гепарин-содержащие пробирки. Эти образцы крови центрифугировали (1000×g, 10 минут, 4°C) для отделения плазмы. Концентрацию TNF-α в плазме крыс измеряли с помощью набора ELISA kit (DuoSet ELISA, R&D Systems). Вычисляли степень ингибирования в группе, получавшей тестируемое соединение (n=5), относительно выработки TNF-α при ингибирующем действием агониста EP4, принимая концентрацию TNF-α в группе (n=5), не получавшей ONO-AE1-437, за 100%, и концентрацию TNF-α в группе (n=5), получавшей ONO-AE1-437, за 0%.
В результате проведенных измерений, было обнаружено, что соединение A ослабляло ингибирующее действие агониста EP4 ONO-AE1-437 (0,01 мг/кг, sc) на выработку TNF-α на 38%.
Тестовый пример 6: Тест для оценки влияния на активность ренина в плазме крыс
В этом тесте использовали крыс SD (самцов в возрасте 7 недель) в условиях достаточного доступа к пище. Тестируемое соединение, растворенное в смеси ПЭГ 400:20% Tween 80:1 моль/л водный раствор NaHCO3=1:4:5, перорально (po) вводили крысам в дозировке 0,3 мг/кг (5 мл/кг). Через 1 час подкожно вводили в спину крысам активный метаболит (ONO-AE1-437) агониста EP4 ONO-4819, растворенный в физиологическом солевом растворе в дозировке 0,01 мг/кг (5 мл/кг). Через 10 минут крыс обезглавливали без анестезии и собирали примерно 2 мл крови в пробирку, содержащую 3 мг EDTA⋅2Na. Образцы крови центрифугировали (1000×g, 10 минут, 4°C) для отделения плазмы. К 100 мкл плазмы добавляли 100 мкл аналитического буфера (20,4 мл 2 моль/л NaH2PO4, 9,3 мл 1 моль/л Na2HPO4, 15 мл 0,5 моль/л EDTA⋅2Na и 0,1 г CHAPS смешивали, затем смешивали с дистиллированной водой и разбавляли до 50 мл, pH 5,55) и 1 мкл 100 ммоль/л гидрохлорида 4-(2-аминоэтил)бензолсульфонил фторида. Половину полученной смеси собирали и затем инкубировали при 37°C в течение 90 минут. Другую половину хранили при 4°C и использовали для холостого опыта. Концентрацию ангиотензина I в обоих образцах измеряли способом ELISA и концентрацию, полученную при вычитании величины для холостой реакции из величины для образца, инкубированного при 37°C, принимали за показатель активности ренина в плазме (активность ренина в плазме (PRA)). Принимая PRA, соответствующее степени ингибирования в группе (n=5), не получавшей ONO-AE1-437, за 100% и PRA в группе (n=4), получавшей ONO-AE1-437, за 0%, вычисляли степень ингибирования для группы (n=5), получавшей тестируемое соединение.
В результате проведенных исследований было установлено, что соединение A (0,3 мг/кг po) ингибировало увеличение PRA, возникавшее из-за действия агониста EP4 ONO-AE1-437 (0,1 мг/кг, sc), на 102%.
Тестовый пример 7: Тест для исследования влияния на содержание альбумина в моче мышей db/db с диабетом 2 типа
Для проведения теста использовали мышей db/db (самцов в возрасте 8 недель) с диабетом 2 типа. Концентрации альбумина в образцах мочи, полученных при сборе мочи в течение 24 часов, измеряли способом ELISA с использованием антитела против мышиного альбумина (RAM/Alb/7S, Nordic Immunology), и концентрации креатинина в моче измеряли с использованием CRE-EN Kainos (Kainos Co., Ltd.). Вычисляли соотношение альбумин-креатинин (ACR) в моче, и распределяли животных в группу, не получающую тестируемого соединения (n=12), и группу, получающую тестируемое соединение (n=12), так, чтобы между группами не было существенных различий по параметру ACR. Тестируемое соединение, суспендированное в 0,5% растворе метилцеллюлозы (MC), перорально вводили животным из соответствующей группы в дозировке 0,3 мг/кг один раз в день в течение одной недели (10 мл/кг). Другой группе осуществляли пероральное введение 0,5% раствора MC в объеме 10 мл/кг один раз в день в течение одной недели. Мочу собирали в течение 24 часов после завершения последнего введения и, используя полученные значения ACR в качестве индикатора, исследовали благоприятное влияние тестируемого соединения на нефропатию в ранней стадии у мышей с диабетом 2 типа. Определяли уменьшение ACR в группе, получавшей тестируемое соединение, принимая значение ACR в группе, не получавшей тестируемого соединения, за 100%.
В результате проведенной оценки, было обнаружено, что соединение A (0,3 мг/кг, po) уменьшает значение ACR у мышей db/db с диабетом 2 типа на 44% при пероральном введении в течение одной недели.
Тестовый пример 8: Тест для исследования влияния на деятельность почек при 5/6 нефрэктомии (5/6 Nx) у крыс с хронической почечной недостаточностью
Для этого теста использовали крыс Wistar (самцы в возрасте 8 недель). При анестезии пентобарбиталом удаляли две трети левой почки, и через 1 неделю целиком удаляли правую почку (5/6 Nx). Через 2 недели после завершения 5/6 Nx, измеряли концентрации белка в образцах мочи, полученных при сборе мочи в течение 24 часов, используя набор для анализа белка Bio-Rad Protein assay kit, и концентрацию креатинина в моче измеряли с использованием Determiner L CRE (Kyowa Medex Co., Ltd.)). Вычисляли соотношение белок-креатинин в моче (UPCR), и распределяли животных в группу, получающую тестируемое соединение (n=12), и группу, не получающую тестируемого соединения (n=12), так, чтобы между группами не было существенных различий по параметру UPCR. Тестируемое соединение, суспендированное в 0,5% растворе MC, перорально вводили животным соответствующей группы в дозировке 0,2 мг/кг один раз в день в течение 6 недель (5 мл/кг). Животным другой группы перорально вводили 0,5% раствор MC в объеме 5 мл/кг один раз в день в течение 6 недель. Мочу собирали в течение 24 часов после окончания последнего введения и, используя полученные значения UPCR в качестве индикатора, исследовали благоприятное влияние тестируемого соединения на нефропатию у крыс с хронической почечной недостаточностью. Определяли уменьшение UPCR в группе, получавшей тестируемое соединение, принимая значение UPCR в группе, не получавшей тестируемого соединения, за 100%.
В результате проведенной оценки, было обнаружено, что соединение A (0,2 мг/кг, po) уменьшало значение UPCR у крыс с хронической почечной недостаточностью из-за нефрэктомии 5/6 на 47% при пероральном введении в течение 6 недель.
Тестовый пример 9: Тест для оценки антагонистического действия на крысиный рецептор EP1/EP2/EP3 (определение селективности)
Оценивали антагонистическое действие соединения A на другие подтипы (EP1, EP2 и EP3) крысиных рецепторов PGE2. При исследовании действия тестируемого соединения, для рецепторов EP1 и EP3, в качестве индикатора использовали внутриклеточное содержание Ca2+, и для рецептора EP2 в качестве индикатора использовали внутриклеточное содержание cAMP.
Конструирование вектора экспрессии крысиных рецепторов EP1, EP2 или EP3:
Ген крысиного рецептора EP1 (идентификационный номер GenBank: D88751.1), ген крысиного рецептора EP2 (идентификационный номер GenBank: NM_031088.1) или ген крысиного рецептора EP3 (идентификационный номер GenBank: NM_012704.1) включали, соответственно, в вектор экспрессии pcDNA3.1-V5-His-TOPO (Invitrogen Inc.).
Получение клеток, устойчиво экспрессирующих крысиные рецепторы EP1, EP2 или EP3:
Вектор, экспрессирующий крысиные рецепторы EP1, EP2 или EP3, трансфецировали в клетки HEK-293 (для устойчивой экспрессии крысиных рецепторов EP1 или EP3, ATCC No:CRL-1573) или клетки CHO-K1 (для устойчивой экспрессии крысиного рецептора EP2, ATCC No:CCL-61). Трансфекцию проводили согласно приложенной инструкции, используя реагент Lipofectamine (зарегистрированная торговая марка) 2000 (Invitrogen Inc.). После трансфекции клетки культивировали в культуральной среде D-MEM (для устойчивой экспрессии крысиных рецепторов EP1 или EP3) (No продукта 11885084, Invitrogen Inc.), содержащей G418 (Nakalai Tesque Inc.) и культуральной среде α-MEM (для устойчивой экспрессии крысиного рецептора EP2), содержащей G418, для получения клона, устойчивого к лекарственным веществам.
Культивирование клеток, устойчиво экспрессирующих рецептор EP2, и обработка соединением:
Клетки CHO-K1, устойчиво экспрессирующие крысиный EP2, высевали в 96-луночные планшеты в количестве 1×104 клеток/100 мкл и культивировали в течение ночи при 37°C и 5% CO2, используя культуральную среду α-MEM с добавкой 10% FBS. Культуральную среду заменяли смесью 2 мкмоль/л индометацин/0,1% BSA/культуральная среда α-MEM и после этого через 60 минут, заменяли смесью 1 ммоль/л IBMX/ 2 мкмоль/л индометацин/ 0,1% BSA/культуральная среда α-MEM (продукт No. 12571063, Invitrogen Inc.). Через 10 минут добавляли тестируемые соединения (в конечной концентрации 0,01, 0,1, 1 и 10 мкмоль/л) и затем через 10 минут добавляли PGE2 в конечной концентрации 100 нмоль/л (конечная концентрация ДМСО 0,1%). Для вычисления количества cAMP, вырабатываемого при добавлении PGE2, создавали группу образцов, к которым не добавляли PGE2. Клетки культивировали и проводили реакцию в инкубаторе с CO2 (37°C, 5%CO2). Через 30 минут удаляли культуральную среду и добавляли 100 мкл/лунку 0,2% Triton X-PBS для лизиса клеток. Описанный тест проводили один раз в двух параллельных экспериментах.
Измерение и анализ количества cAMP в клетках, устойчиво экспрессирующих рецептор EP2:
Количество cAMP, присутствующего в клеточном лизате, измеряли с использованием набора cAMP HiRange kit по методике, аналогичной описанной в тестовом примере 4. Вычисляли отношение количества cAMP при обработке тестируемым соединением, принимая количество cAMP при добавлении PGE2 с конечной концентрацией 100 нмоль/л за 100%, и количество cAMP без добавления PGE2 за 0%.
В результате проведенных оценок, соединение A не продемонстрировало ингибирующего действия величиной 50% или более вплоть до концентрации 10 000 нмоль/л на увеличение содержания cAMP в клетках под действием PGE2 за счет влияния на крысиный рецептор EP2.
Культивирование клеток, устойчиво экспрессирующих рецепторы EP1 и EP3, и обработка соединением:
Клетки HEK-293, устойчиво экспрессирующие крысиные рецепторы EP1 или EP3, высевали в 96-луночные планшеты в количестве 1×104 клеток/100 мкл и культивировали в течение ночи при 37°C и 5% CO2, используя культуральную среду D-MEM с добавкой 10% FBS. К аналитическому буферу (1×HBSS, 20 ммоль/л HEPES-NaOH (pH 7,4), 0,6 мг/мл пробенецид, 0,1% BSA) добавляли флуоресцентный реагент Dye из аналитического набора Ca3 Assay kit (Molecular Devices, LLC) в соотношении 70:1. Культуральную среду заменяли разбавленным раствором Dye, после чего инкубировали в течение 3 часов. К полученным образцам добавляли соединение (в конечной концентрации 1 или 10 мкмоль/л), растворенное в ДМСО и аналитический буфер. Через 5 минут добавляли PGE2 до конечной концентрации 100 нмоль/л (конечная концентрация ДМСО 1%). Тесты, в которых использовались клетки, устойчиво экспрессирующие крысиный рецептор EP1 или крысиный рецептор EP3, проводили по одному разу в двух параллельных экспериментах.
Измерение и анализ концентрации Ca2+ в клетках, устойчиво экспрессирующих рецепторы EP1 или EP3:
Внутриклеточную концентрацию Ca2+ измеряли с помощью FLIPR tetra (Molecular Devices, LLC.), используя интенсивность флуоресценции красителя Dye в качестве индикатора. Для измерения повышения внутриклеточной концентрации Ca2+ при добавлении PGE2, создавали группу образцов без добавления PGE2. Принимая концентрацию Ca2+ при добавлении PGE2 до конечной концентрации 100 нмоль/л за 100%, и концентрацию Ca2+ при отсутствии PGE2 за 0%, вычисляли концентрацию Ca2+ в процентах при обработке тестируемым соединением.
В результате проведенных измерений было установлено, что соединение A не оказывало ингибирующего действия величиной 50% или более вплоть до концентрации 10 000 ммоль/л на увеличение внутриклеточной концентрации Ca2+ под действием PGE2 за счет влияния на крысиные рецепторы EP1 или EP3.
Тестовый пример 10: Оценка влияния на желудочно-кишечные расстройства у крыс
В исследовании использовали крыс SD (самцов в возрасте 7 недель). Тестируемое соединение, растворенное в смеси PEG 400:20% Tween 80:1 моль/л водный раствор NaHCO3=1:4:5, перорально вводили в дозировке 3 мг/кг (n=5,5 мл/кг) в течение 7 дней. Указанную выше жидкую смесь перорально вводили группе, которая не получала тестируемого соединения (n=5), в объеме 5 мл/кг в течение 7 дней. После голодания в течение ночи, отбирали кровь для гематологического исследования и биохимического анализа на следующий день после последнего введения. После отбора крови, животных, которых подвергали эвтаназии посредством кровопускания, немедленно вскрывали и извлекали из организма желудок, двенадцатиперстную кишку, тощую кишку, подвздошную кишку, слепую кишку, ободочную кишку, прямую кишку и печень. Извлеченные органы фиксировали в 10% растворе формалина в нейтральном буфере и использовали для гистопатологического исследования.
В ходе исследования не удалось обнаружить данных, свидетельствующих о том, что соединение A вызывает аномалии в желудочно-кишечном тракте.
Проведенные тесты подтвердили, что соединение A обладает сродством к рецептору EP4 и демонстрирует отличное антагонистическое действие на рецептор EP4 (Тестовые примеры 1-5). Было подтверждено, что соединение A ингибирует увеличение PRA, вызванное агонистом EP4 (Тестовый пример 6). Было подтверждено, что соединение A проявляет благоприятное действие в тесте по исследованию влияния на альбумин в моче у мышей db/db с диабетом 2 типа и в тесте по исследованию влияния на деятельность почек при нефрэктомии 5/6 (5/6 Nx) у крыс с хронической почечной недостаточностью (тестовые примеры 7 и 8).
Соответственно, соединение A или его соль можно применять для профилактики или лечения хронической почечной недостаточности и/или диабетической нефропатии.
По результатам приведенного выше тестового примера 1 было обнаружено, что соединение A обладает высоким сродством к рецептору EP4 по сравнению с соединением примера 205 патентного документа 1. Далее, на основании результатов приведенного выше тестового примера 10 было установлено, что существуют лишь незначительные опасения, что соединение A вызовет расстройства желудочно-кишечного тракта.
Результаты приведенных выше тестовых примеров подтвердили, что соединение A или его соль оказывают антагонистическое действие на рецептор EP4 и могут применяться в качестве действующих ингредиентов фармацевтической композиции, предназначенной для профилактики или лечения различных заболеваний, связанных с EP4, и т.п. Примеры заболеваний, связанных с EP4, включают почечные заболевания (например, склероз почек, подагрическую почку, поликистозную болезнь почек, нефротический синдром, острый нефрит, рецидивирующую гематурию, стойкую гематурию, хронический нефрит, быстропрогрессирующий нефрит, острую почечную недостаточность, хроническую почечную недостаточность, диабетическую нефропатию и синдром Барттера), воспалительные заболевания кожи (например, солнечный ожог, ожоги, экзему и дерматит), ишемические заболевания сердца, вызванные артериосклерозом (например, инфаркт миокарда и стенокардию), расстройства мозгового кровообращения, вызванные артериосклерозом (например, инсульт, инсульт, включающий лакунарный инфаркт, тромбоз сосудов мозга, мозговое кровоизлияние, субарахноидальное кровоизлияние и инфаркт мозга), язвенные болезни (например, язву желудка и язву двенадцатиперстной кишки), злокачественные раковые заболевания и их метастазы (например, рак ободочной кишки и рак груди), боль (например, острую послеоперационную боль, травматическую боль, боль после удаления швов, боль в шее, плечах и запястьях, плечевой периартрит, остеоартрит (OA), запястный туннельный синдром, ревматоидный артрит (RA), хроническую послеоперационную боль, интерстициальный цистит, болевой синдром мочевого пузыря, небактериальный хронический простатит (CP/CPPS), боль после повреждения позвоночника, боль после инфаркта мозга, рассеянный склероз (боль), боль от болезни Паркинсона, невропатическую боль при диабете, постгерпетическую боль, невропатическую боль при ВИЧ, невралгию тройничного нерва, фибромиалгию, боль в нижней части спины (ноцицептивную нелокализованную боль в нижней части спины, в т.ч. невропатическую боль в нижней части спины), стеноз спинномозгового канала в поясничной области, боль при спинальных расстройствах (за исключением стеноза поясничного отдела позвоночника и травмы спинного мозга), таламическую боль, мигрень, головную боль, синдром усталых ног (зуд в ступнях), раковую боль и синдром раздраженного кишечника), в частности, почечные заболевания, такие как хроническая почечная недостаточность и/или диабетическая нефропатия.
Кроме того, соединение A или его соль могут применяться в качестве агента для лечения и/или профилактики различных типов отеков (например, сердечного отека и отека мозга), гипертензии, например, злокачественной гипертензии, предменструального синдрома, почечных камней, мочеизнурения, вызванного острыми или хроническими заболеваниями, гиперфосфатемии и т.п.
Помимо этого, соединение A или его соль могут применяться в качестве агента для лечения и/или профилактики различных типов полиурии (например, центрального несахарного диабета, нефрогенного несахарного диабета, физиогенного несахарного диабета, сахарного диабета, расстройств абсорбции хлорида натрия и полидипсии (патологической жажды)).
Фармацевтические композиции, содержащую соединение A или его соль в качестве действующего ингредиента, можно получать широко известными способами, применяя эксципиенты, традиционно используемые в технике, т.е. фармацевтические эксципиенты, фармацевтические носители и т.п.
Введение может осуществляться в составе любой из форм, предназначенных для перорального введения, например, таблеток, пилюль, капсул, гранул, порошков, жидких препаратов и т.п.; или парентерального введения путем инъекции, например, внутриартериальной, внутривенной или внутримышечной инъекции, в форме суппозиториев, глазных капель, глазных мазей, чрескожных жидких препаратов, мазей, чрескожных пластырей, чресслизистых жидких препаратов, чресслизистых пластырей и ингаляторов.
В качестве твердой композиции для перорального введения применяются таблетки, порошки, гранулы или подобные лекарственные формы. В таких твердых композициях один или несколько действующих ингредиентов смешаны по крайней мере с одним инертным эксципиентом. Согласно традиционному способу, композиция может содержать инертные добавки, такие как смазывающее средство, дезинтегрирующее средство, стабилизирующий агент и солюбилизирующий агент. При необходимости, таблетки или пилюли можно покрыть сахарным покрытием или пленкой из желудочного или кишечного материала.
Жидкие композиции для перорального применения включают фармацевтически приемлемые эмульсии, растворы, суспензии, сиропы, эликсиры или подобные составы, и они содержат широко применяемые инертные разбавители, например, очищенную воду или этанол. Помимо инертного разбавителя, такая жидкая композиция может содержать вспомогательный агент, например, солюбилизирующий агент, увлажняющий агент, суспендирующий агент, подсластитель, вкусовую добавку, ароматизатор и антисептик.
Составы для инъекций, предназначенные для парентерального введения, включают стерильные водные или неводные жидкие препараты, суспензии и эмульсии. Водные растворители включают, например, дистиллированную воду для инъекций и физиологический солевой раствор. Примеры неводных растворителей включают спирты, например, этанол. Такая композиция дополнительно может содержать средство для регулирования тоничности, антисептик, смачивающий агент, эмульгирующий агент, диспергирующий агент, стабилизирующий агент или солюбилизирующий агент. Такие составы стерилизуют, например, фильтрованием через фильтры, удерживающие бактерии, включением в состав бактерицидного компонента или облучением. Кроме того, составы для инъекций можно готовить путем получения стерильной твердой композиции, и ее растворением или суспендированием перед применением в стерильной воде или стерильном растворителе для инъекций.
Примеры составов для наружного применения включают мази, пластыри, кремы, желе, компрессы, спреи, лосьоны, глазные капли, глазные мази и т.п. Такие составы включают широко применяемые основы мазей, основы лосьонов, водные или неводные жидкие препараты, суспензии, эмульсии и т.п.
В качестве трансмукозальных средств, например, ингаляторов, трансназальных агентов и т.п., применяются составы в твердой, полутвердой или жидкой форме, и их можно получать широко известными способами. Например, в такие составы можно с успехом включать известные эксципиенты, а также агенты, регулирующие pH, антисептики, ПАВ, смазывающие компоненты, стабилизирующие агенты, загустители и т.п. Для введения таких составов могут применяться подходящие устройства для ингаляции или вдувания. Например, соединение можно вводить индивидуально или в форме порошка, являющегося смесью нескольких компонентов, или в форме раствора или суспензии в комбинации с фармацевтически приемлемым носителем с использованием хорошо известного устройства или распылителя, например, устройства для дозированной ингаляции и т.п. Ингалятор для сухого порошка или подобный может быть предназначен для однократного или многократного применения, и в нем может использоваться сухой порошок или порошок-содержащая капсула. В качестве альтернативы, состав может иметь такую форму, как аэрозольный спрей под давлением в котором применяется подходящий пропеллент, например, подходящий газ, такой как хлорфторалкан и диоксид углерода, или другие формы.
При пероральном введении, дневная дозировка предпочтительно составляет от примерно 0,001 до 100 мг/кг, в одном из вариантов осуществления, от 0,1 до 30 мг/кг, и в другом варианте осуществления, от 0,1 до 10 мг/кг массы тела, при введении одной дозой или в виде 2-4 отдельных доз. При внутривенном введении, подходящая дневная дозировка составляет от примерно 0,0001 до 10 мг/кг массы тела, один, два или более раз в день. Кроме того, трансмукозальное средство вводят в диапазоне дозировок от 0,001 до 100 мг/кг массы тела один, два или более раз в день. Решение о подходящей дозировке принимают в соответствии с индивидуальной ситуацией, с учетом симптомов, возраста и пола пациента, а также других показателей.
Соединение A может применяться в комбинации с различными средствами для лечения или средствами для профилактики перечисленных выше заболеваний, при которых, как считается, соединение A является эффективным. Препараты, которые предполагается применять совместно, могут вводиться одновременно или отдельно и непрерывно, или через желаемые промежутки времени. Препараты, которые предполагается вводить совместно с соединением A, можно включать в состав смеси или можно готовить индивидуально.
ПРИМЕРЫ
Способы получения соединения A, представленного формулой (I), или его соли будут более подробно описаны ниже по тексту с привлечением примеров. Способы получения соединения A или его соли не ограничиваются только способами (методиками) приведенных ниже конкретных примеров, и соединение A или его соль можно получать любыми способами, которые известны специалисту в данной области техники.
Кроме того, осуществляли DSC анализ и эксперименты по дифракции рентгеновских лучей на порошке, согласно описанным ниже методикам.
(1) DSC анализ
DSC анализ проводили с использованием приборов Q1000 и Q2000 производства TA Instruments. Приблизительно 2 мг образца помещали в алюминиевую кювету для образца, предназначенную для такого применения, и непрерывно измеряли и регистрировали разность теплового потока в калориях между образцом и эталоном (пустой алюминиевой кюветой для образца) при установке диапазона измерений от комнатной температуры до 300°C и скорости нагревания 10°C/мин при незакрытой кювете с образцом в атмосфере азота (50 мл/мин). Помимо этого, работу с прибором, включая обработку данных, проводили в соответствии с методиками и процедурами, описанными в инструкции для каждого прибора.
(2) Дифракция рентгеновских лучей на порошке
Дифракцию рентгеновских лучей на порошке исследовали с использованием прибора RINT-TTRII в следующих условиях: трубка: Cu, ток трубки: 300 мА, напряжение на трубке 50 кВ, интервал выборки: 0,020°, скорость сканирования: 4°/мин, длина волны: 1,54056 Ангстрема и диапазон регистрации углов дифракции (2θ): от 2,5 до 40°. Помимо этого, работу с прибором, включая обработку данных, проводили в соответствии с методиками и процедурами, указанными для каждого прибора.
Кроме того, в примерах используются следующие сокращения. ESI+: значения m/z в ESI масс-спектрах, ЯМР-ДМСО-d6: пик δ (м.д.) в спектрах 1H ЯМР в ДМСО-d6.
Наконец, для удобства концентрацию в моль/л обозначают как М. Например, 1М водный раствор гидроксида натрия означает водный раствор гидроксида натрия 1 моль/л.
Пример 1: Синтез 4-[(1S)-1-({[4-бром-1-(изохинолин-3-илметил)-3-метил-1H-пиразол-5-ил]карбонил}амино)этил]бензойной кислоты (I)
Стадия 1: Синтез метил 4-[(1S)-1-{[(4-бром-3-метил-1H-пиразол-5-ил)карбонил]амино}этил]бензоата (5a)
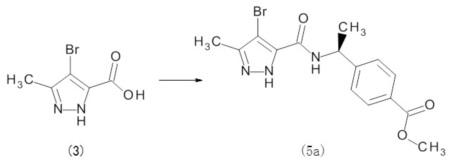
К смеси 4-бром-3-метил-1H-пиразол-5-карбоновой кислоты (3) (1,00 г), ДМФА (20 мл), гидрохлорида метил 4-[(1S)-1-аминоэтил]бензоата (1,26 г) и HOBt (0,99 г) добавляли 1-(3-диметиламинопропил)-3-этилкарбодиимид (1,2 мл) и затем перемешивали при комнатной температуре в течение ночи. К смеси добавляли этилацетат, после чего перемешивали при охлаждении льдом. К смеси добавляли 10% водный раствор лимонной кислоты, затем осуществляли разделение на органический и водный слои, и водный слой экстрагировали этилацетатом. Полученные органические слои объединяли, последовательно промывали насыщенным водным раствором гидрокарбоната натрия, водой и насыщенным раствором соли, высушивали над безводным сульфатом магния и затем фильтровали. Фильтрат концентрировали при пониженном давлении и получали метил 4-[(1S)-1-{[(4-бром-3-метил-1H-пиразол-5-ил) карбонил]амино}этил]бензоат (5a) (1,75 г).
ESI+: 366, 368.
Стадия 2: Синтез метил 4-[(1S)-1-({[4-бром-1-(изохинолин-3-илметил)-3-метил-1H-пиразол-5-ил]карбонил}амино)этил]бензоата (2a)
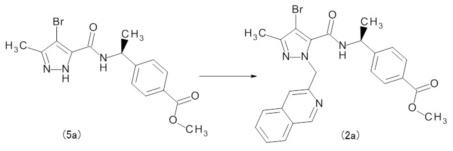
Смесь метил 4-[(1S)-1-{[(4-бром-3-метил-1H-пиразол-5-ил) карбонил]амино}этил]бензоата (5a) (1,72 г) и ДМФА (20,0 мл) перемешивали при охлаждении льдом. К смеси добавляли трет-бутоксид калия (580 мг) и перемешивали в течение 0,5 часа. К полученной смеси добавляли смесь 3-(бромметил)изохинолина (1,10 г) и ДМФА (14 мл), после чего поднимали температуру реакционной смеси до комнатной и перемешивали в течение 10 дней. Полученную смесь охлаждали льдом и при перемешивании добавляли к ней 10% водный раствор лимонной кислоты, после чего перемешивали некоторое время и экстрагировали этилацетатом. Полученный органический слой последовательно промывали насыщенным водным раствором гидрокарбоната натрия, водой и насыщенным раствором соли, высушивали над безводным сульфатом магния и затем фильтровали. Фильтрат концентрировали при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат=6:4), получая метил 4-[(1S)-1-({[4-бром-1-(изохинолин-3-илметил)-3-метил-1H-пиразол-5-ил]карбонил}амино)этил]бензоат (2a) (518 мг).
ЯМР-ДМСО-d6: 9,28 (1H, д, J=7,8 Гц), 9,23 (1H, с), 8,13 (1H, д, J=7,8 Гц), 7,89 (1H, д, J=7,8 Гц), 7,81-7,76 (1H, м), 7,72-7,64 (3H, м), 7,50 (1H, с), 7,38 (2H, д, J=8,3 Гц), 5,65-5,54 (2H, м), 5,12-5,04 (1H, м), 3,83 (3H, с), 2,17 (3H, с), 1,37 (3H, д, J=7,0 Гц).
Стадия 3: Синтез 4-[(1S)-1-({[4-бром-1-(изохинолин-3-илметил)-3-метил-1H-пиразол-5-ил]карбонил}амино)этил]бензойной кислоты (I)
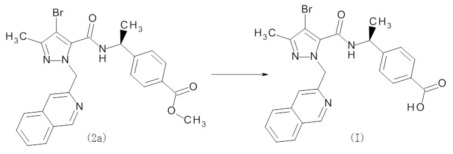
К смеси метил 4-[(1S)-1-({[4-бром-1-(изохинолин-3-илметил)-3-метил-1H-пиразол-5-ил]карбонил}амино)этил]бензоата (2a) (486 мг), ТГФ (10,0 мл) и метанола (10,0 мл) при охлаждении льдом добавляли 2М водный раствор гидроксида натрия (5,0 мл) и затем перемешивали при комнатной температуре в течение 17 часов. К смеси при охлаждении льдом добавляли 1М хлористоводородную кислоту (10,0 мл), затем повышали температуру реакционной смеси до комнатной и перемешивали в течение 2 часов. Выпавшее в осадок твердое вещество собирали фильтрованием и промывали водой, получая 4-[(1S)-1-({[4-бром-1-(изохинолин-3-илметил)-3-метил-1H-пиразол-5-ил]карбонил}амино)этил]бензойную кислоту (I) (411 мг) в виде кристаллов.
ESI+: 493, 495;
ЯМР-ДМСО-d6: 12,9-12,7 (1H, м), 9,30 (1H, д, J=7,8 Гц), 9,24 (1H, с), 8,13 (1H, д, J=8,1 Гц), 7,91 (1H, д, J=8,1 Гц), 7,81-7,76 (1H, м), 7,74-7,66 (3H, м), 7,53 (1H, с), 7,40 (2H, д, J=8,2 Гц), 5,60 (2H, с), 5,14-5,03 (1H, м), 2,16 (3H, с), 1,37 (3H, д, J=7,0 Гц)
Элементный анализ: вычислено для C24H21BrN4O3: C, 58,43; H, 4,29; N, 11,36; Br, 16,20.
Найдено: C, 58,33; H, 4,38; N, 11,24; Br, 16,07.
В результате исследования кристаллического порошка, полученного на стадии 3 примера 1, способом дифракции рентгеновских лучей при использовании трубки с медным анодом, была получена рентгенограмма, включающая пики при углах 2θ (°)=5,7, 7,9, 8,3, 8,9, 9,2, 11,5, 12,5, 13,1, 15,8, 16,3, 16,7, 17,2, 17,9, 18,5 и 19,5.
При проведении DSC анализа кристаллов, полученных на стадии 3 примера 1, температура появления эндотермического пика составила 253°C.
Пример 2: Синтез метансульфоната 4-[(1S)-1-({[4-бром-1-(изохинолин-3-илметил)-3-метил-1H-пиразол-5-ил]карбонил}амино)этил]бензойной кислоты (Ia)
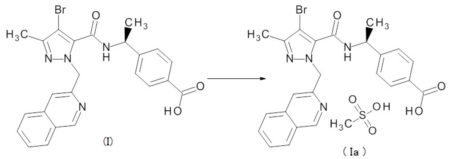
К смеси 4-[(1S)-1-({[4-бром-1-(изохинолин-3-илметил)-3-метил-1H-пиразол-5-ил]карбонил}амино)этил]бензойной кислоты (I) (1000,0 мг) и диоксана (30 мл) при охлаждении льдом добавляли метансульфоновую кислоту (140 мкл). Полученную смесь нагревали до 90°C и перемешивали в течение 1 часа. После охлаждения до комнатной температуры, выпавшее в осадок твердое вещество собирали фильтрованием, получая метансульфонат 4-[(1S)-1-({[4-бром-1-(изохинолин-3-илметил)-3-метил-1H-пиразол-5-ил]карбонил}амино)этил]бензойной кислоты (Ia) в виде кристаллов (1030 мг).
ESI+: 493, 495;
ЯМР-ДМСО-d6: 9,32 (1H, с), 9,27 (1H, д, J=7.7 Гц), 8,17 (1H, д, J=7,9 Гц), 7,95 (1H, д, J=7,9 Гц), 7,90-7,79 (1H, м), 7,77-7,66 (3H, м), 7,59 (1H, с), 7,40 (2H, д, J=7,8 Гц), 5,71-5,54 (2H, м), 5,16-5,00 (1H, м), 2,33 (3H, с), 2,17 (3H, с), 1,37 (3H, д, J=7,1 Гц);
Элементный анализ: Вычислено для C24H21BrN4O3⋅CH4O3S: C, 50,94; H, 4,27; N, 9,50; S, 5,44; Br, 13,56;
Найдено: C, 50,65; H, 4,25; N, 9,36; S, 5,41; Br, 13,42;
В результате исследования кристаллического порошка, полученного в примере 2, способом дифракции рентгеновских лучей при использовании трубки с медным анодом, была получена рентгенограмма, включающая пики при углах 2θ (°)=4,7, 9,5, 12,0, 13,2, 13,7, 15,3, 18,8, 20,3, 20,9 и 22,8.
При проведении DSC анализа кристаллов, полученных в примере 2, температура появления эндотермического пика составила 192°C.
ПРОМЫШЛЕННАЯ ПРИМЕНИМОСТЬ
Соединение A или его соли проявляют антагонистическое действие в отношении рецептора EP4 и могут применяться в качестве действующего ингредиента фармацевтической композиции, предназначенной для профилактики и/или лечения хронической почечной недостаточности и/или диабетической нефропатии.
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЙ АГОНИСТ ЕР4 | 2011 |
|
RU2564414C2 |
| ПРИМЕНЕНИЕ АНТАГОНИСТОВ РЕЦЕПТОРА EP4 ДЛЯ ЛЕЧЕНИЯ NASH-АССОЦИИРОВАННОГО РАКА ПЕЧЕНИ | 2017 |
|
RU2762193C2 |
| БЕЛКИ, СВЯЗЫВАЮЩИЕ ПРОСТАГЛАНДИН Е2, И ИХ ПРИМЕНЕНИЕ | 2009 |
|
RU2559525C2 |
| ПРИМЕНЕНИЕ АНТАГОНИСТОВ РЕЦЕПТОРА EP4 ДЛЯ ЛЕЧЕНИЯ NASH-АССОЦИИРОВАННОГО РАКА ПЕЧЕНИ | 2017 |
|
RU2717331C2 |
| 4-АЛКИНИЛИМИДАЗОЛЬНОЕ ПРОИЗВОДНОЕ И ЛЕКАРСТВЕННОЕ СРЕДСТВО, ВКЛЮЧАЮЩЕЕ ТАКОЕ ПРОИЗВОДНОЕ В КАЧЕСТВЕ АКТИВНОГО ИНГРЕДИЕНТА | 2014 |
|
RU2662806C2 |
| СОДЕРЖАЩИЕ АЗОТ 6-ЧЛЕННЫЕ ЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ | 2018 |
|
RU2772958C2 |
| ЛИШЕННЫЕ ПОБОЧНЫХ ЭФФЕКТОВ ПРОИЗВОДНЫЕ ПРОСТАГЛАНДИНОВ ДЛЯ ЛЕЧЕНИЯ ГЛАУКОМЫ | 1998 |
|
RU2207858C2 |
| ПРОСТАМИДЫ И ИХ АНАЛОГИ, ОБЛАДАЮЩИЕ НЕЙРОЗАЩИТНЫМ ДЕЙСТВИЕМ | 2011 |
|
RU2474426C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2011 |
|
RU2606510C2 |
| АМИДНОЕ СОЕДИНЕНИЕ | 2009 |
|
RU2479576C9 |
Изобретение относится к 4-[(1S)-1-({[4-бром-1-(изохинолин-3-илметил)-3-метил-1H-пиразол-5-ил]карбонил}амино)этил]бензойной кислоте или ее фармацевтически приемлемой соли, предпочтительно к метансульфонатной соли и наиболее предпочтительно к кристаллической метансульфонатной соли указанного выше соединения. В изобретении разработано соединение, оказывающее антагонистическое действие на рецептор EP4. Данное соединение и его фармацевтически приемлемые соли можно применять в качестве действующего ингредиента фармацевтической композиции для профилактики и/или лечения различных заболеваний, связанных с EP-4, например хронической почечной недостаточности и/или диабетической нефропатии. 6 н. и 5 з.п. ф-лы, 12 пр.
1. 4-[(1S)-1-({[4-бром-1-(изохинолин-3-илметил)-3-метил-1H-пиразол-5-ил]карбонил}амино)этил]бензойная кислота или ее фармацевтически приемлемая соль.
2. Соединение по п.1, которое представляет собой метансульфонат 4-[(1S)-1-({[4-бром-1-(изохинолин-3-илметил)-3-метил-1H-пиразол-5-ил]карбонил}амино)этил]бензойной кислоты.
3. Соединение по п.2, которое представляет собой кристаллическую форму метансульфоната 4-[(1S)-1-({[4-бром-1-(изохинолин-3-илметил)-3-метил-1H-пиразол-5-ил]карбонил}амино)этил]бензойной кислоты.
4. Соединение по п.3, которое представляет собой кристаллическую форму с температурой появления эндотермического пика на термограмме DSC 192°C и имеет пики на картине дифракции рентгеновских лучей на порошке при использовании трубки с медным анодом при углах 2θ (°), равных 4,7, 9,5, 12,0, 13,2, 13,7, 15,3, 18,8, 20,3, 20,9 и 22,8.
5. Фармацевтическая композиция, обладающая антагонистическим действием на рецептор EP4, содержащая соединение или его фармацевтически приемлемую соль по п.1, а также фармацевтически приемлемый эксципиент.
6. Фармацевтическая композиция, содержащая соединение или его фармацевтически приемлемую соль, а также фармацевтически приемлемый эксципиент по п.5, для профилактики или лечения хронической почечной недостаточности и/или диабетической нефропатии.
7. Применение соединения или его фармацевтически приемлемой соли по п.1 для производства фармацевтической композиции для профилактики или лечения хронической почечной недостаточности и/или диабетической нефропатии.
8. Соединение или его фармацевтически приемлемая соль по п.1 для профилактики или лечения хронической почечной недостаточности и/или диабетической нефропатии.
9. Применение соединения или его фармацевтически приемлемой соли по п.1 для профилактики или лечения хронической почечной недостаточности и/или диабетической нефропатии.
10. Способ профилактики или лечения хронической почечной недостаточности и/или диабетической нефропатии, включающий введение субъекту эффективного количества соединения или его фармацевтически приемлемой соли по п.1.
11. Фармацевтическая композиция, обладающая антагонистическим действием на рецептор EP4, содержащая кристаллическую форму по п.3, а также фармацевтически приемлемый эксципиент.
| АМИДНОЕ СОЕДИНЕНИЕ | 2009 |
|
RU2479576C9 |
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
Авторы
Даты
2019-04-16—Публикация
2015-03-25—Подача