ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к способу контроля гликозилирования рекомбинантного гликопротеина.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Как слитый белок TNFR-Fc, в котором лиганд-связывающая часть человеческого рецептора TNF-α р75 (TNFR, рецептор TNF-α) связана с Fc-фрагментом человеческого IgG1, этанерцепт был представлен компанией Amgen под торговым названием Энбрел (Enbrel) в 2002 г. Этанерцепт конкурентно ингибирует связывание с рецепторами TNF-α на поверхности клетки in vivo, ингибируя посредством этого связанный с TNF-α иммунный ответ. Соответственно, этанерцепт используют как ингибитор TNF-α при ревматоидном артрите, псориазе, анкилозирующем спондилите и так далее, и в настоящее время проводятся клинические исследования по его применению при васкулите, болезни Альцгеймера и болезни Крона.
В то же время, генный рекомбинантный фармацевтический продукт представляет собой фармацевтический продукт, содержащей в качестве активного ингредиента пептид, белок и так далее, полученный с использованием методики генетических манипуляций. Применение биотехнолоии обеспечивает преимущества, состоящие в возможности получения большого числа высоко чистых рекомбинантных белков, которые трудно получить в естественном состоянии, но сама экспрессионная структура может быть нестабильной, поскольку ген целевого белка вводят в клетку-хозяина извне. Кроме того, белки получают экспрессией гена в микроорганизме или клетке животного или растения, но не в организме человека, рекомбинантные белки могут отличаться от нативных белков по структурным, физико-химическим, иммунохимическим и биологическим свойствам и особенностям (Kwon, et al., FDC Legislation Research V, vol. 1, 2, 13-21, 2010).
В частности, в случае гликопротеина, гликозилирование и структура или форма гликоформы (сахарной цепи) могут различаться в зависимости от условий культивирования. Иными словами, в процессе получения гликопротеинов различия в структурах гликоформ или количествах сахаридов, составляющих структуру гликоформы, ведут к различным типам гликоформ, приводя посредством этого к неоднородности в зависимости от различий в условиях получения. В случае гликопротеинов с отличающимися структурами гликоформ, они отличаются от нативных форм по перемещениям или распределению в тканях in vivo или являются антагонистами нативных форм, приводя к нежелательной реакции. При продолжительном введении в течение длительного периода времени они действуют как антигены и могут приводить к иммунологическим проблемам.
Как описано выше, поскольку гликоформы могут быть важным фактором, который может влиять на фармацевтический эффект и перемещения in vivo, контроль структур гликопротеинов очень важен в области разработки рекомбинантных гликопротеиновых продуктов для лекарственных средств и разработки технологий массового производства.
В этом отношении, в публикации патента Кореи №2011-0139292, в качестве предшествующего уровня техники, раскрыт контроль гликозилирования белка и связанные с этим композиции и способы, и в публикации патента Кореи №2012-0134116 раскрыт способ увеличения числа занятых сайтов N-гликозилирования на терапевтических гликопротеинах.
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Техническая задача
С учетом описанного выше предшествующего уровня техники, авторы настоящего изобретения приложили значительные усилия, чтобы найти способ контроля гликозилирования рекомбинантного гликопротеина, и в результате подтвердили, что гликозилирование рекомбинантного гликопротеина можно контролировать путем использования культуральной среды, содержащей инсулин, завершив посредством этого настоящее изобретение.
Техническое решение
Основной задачей настоящего изобретения является обеспечение способа контроля паттерна гликозилирования рекомбинантного гликопротеина, включающего культивирование микроорганизма, содержащего полинуклеотид, кодирующий рекомбинантный гликопротеин, в культуральной среде, содержащей инсулин.
Другой задачей настоящего изобретения является обеспечение способа контроля паттерна гликозилирования рекомбинантного гликопротеина, включающего: (а) культивирование микроорганизма, содержащего полинуклеотид, кодирующий рекомбинантный гликопротеин, в культуральной среде для выращивания микроорганизма; и (б) добавление инсулина в культуральную среду и культивирование указанного микроорганизма с получением гликопротеина.
Полезный эффект
Способ контроля гликозилирования рекомбинантного гликопротеина по настоящему изобретению позволяет контролировать активность, фолдинг, секрецию, стабильность, период полувыведения рекомбинантого гликопротеина из плазмы и иммунный ответ на него.
ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
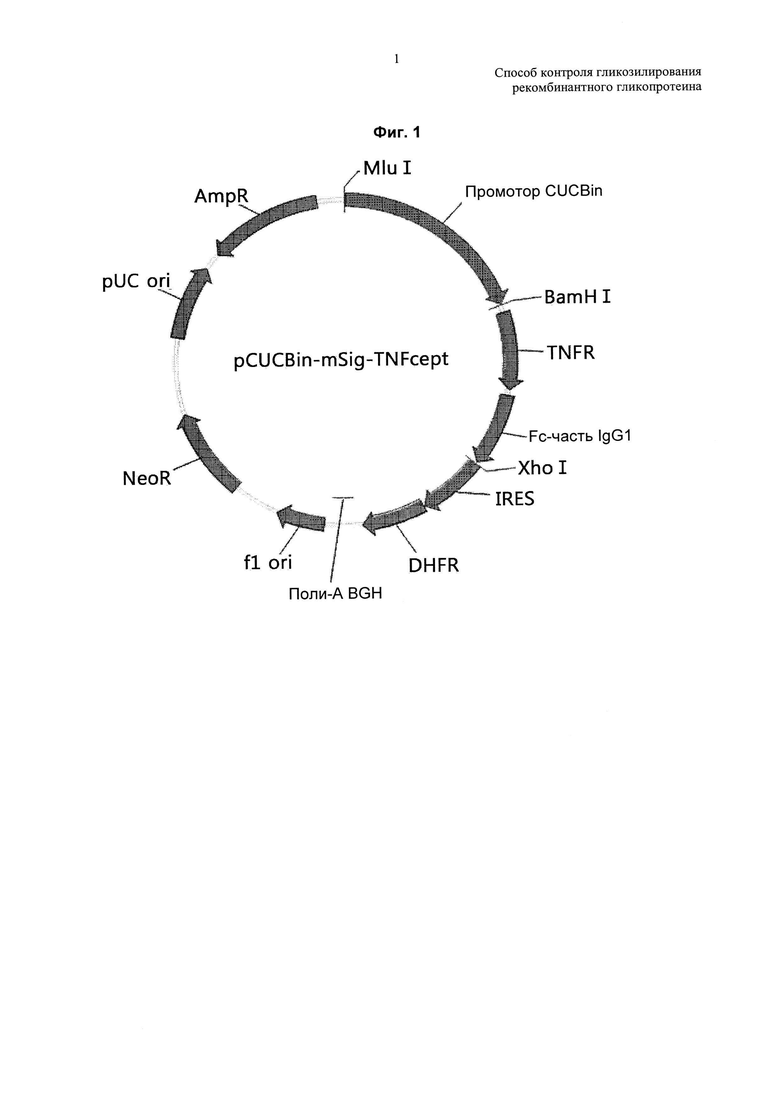
На ФИГ. 1 показана карта расщепления pCUCBin-mSig-TNFcept.
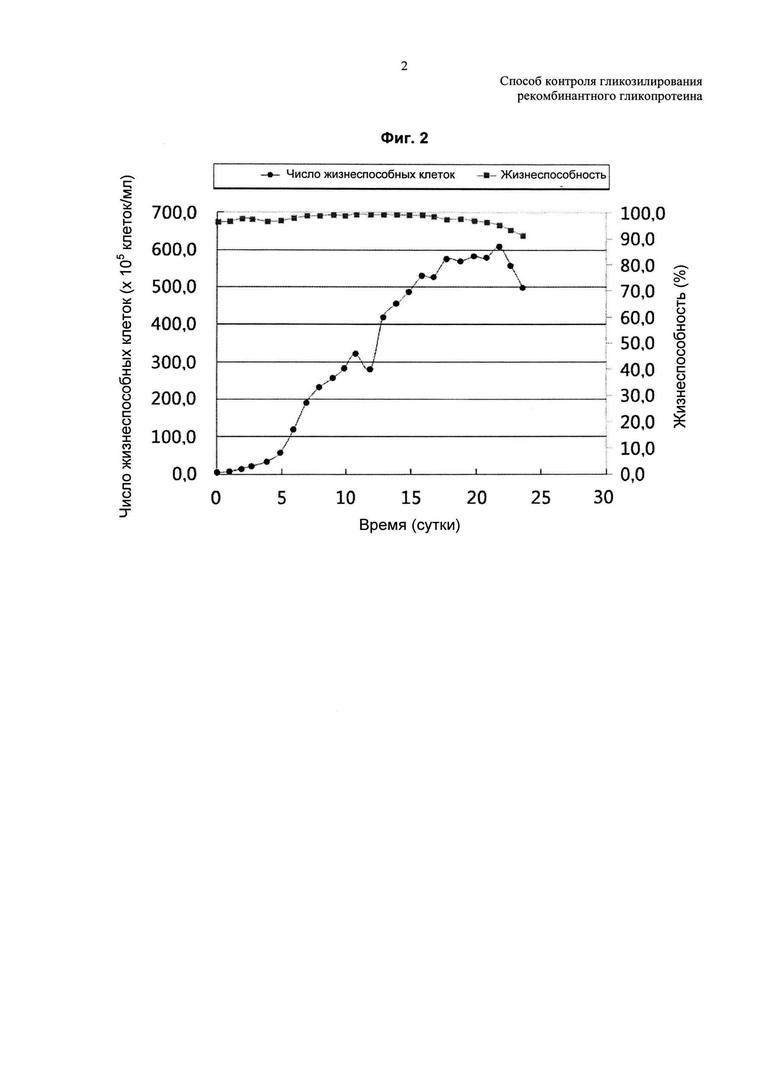
На ФИГ. 2 показаны число жизнеспособных клеток (единица измерения: 105 клеток/мл) и жизнеспособность (%) в зависимости от продолжительности культивирования клеток (единица измерения: сутки) в типичном воплощении настоящего изобретения.
НАИЛУЧШИЙ ВАРИАНТ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
В качестве аспекта, направленного на выполнение указанных выше задач, согласно настоящему изобретению предложен способ контроля паттерна гликозилирования рекомбинантного гликопротеина, включающий культивирование микроорганизма, содержащего полинуклеотид, кодирующий рекомбинантный гликопротеин, в культуральной среде, содержащей инсулин.
Гликопротеин относится к белку, в котором сахарид связан с определенной аминокислотой полипептида, и сахарид может относиться к гликоформе, например, гликоформе, в которой связаны по меньшей мере один или два моносахарида. В качестве примера, гликоформа, как олигосахарид, где с гликопротеином связаны различные моносахариды, может содержать такие моносахариды, как фукоза, N-ацетилглюкозамин, N-ацетилгалактозамин, галактоза, манноза, сиаловая кислота, глюкоза, ксилозы, маннозо-6-фосфат и так далее, их разветвленные формы и так далее.
В качестве примера, рекомбинантный гликопротеин может представлять собой слитый белок иммуноглобулина. Слитый белок иммуноглобулина может содержать Fc-область, представляющую собой часть иммуноглобулина, содержащую константный домен 2 тяжелой цепи (CH2), константный домен 3 тяжелой цепи (CH3) и шарнирную область, без вариабельных доменов тяжелой и легкой цепей, константного домена 1 тяжелой цепи (CH1) и константного домена легкой цепи (CL1) иммуноглобулина (Ig).
В качестве еще одного примера, рекомбинантный гликопротеин может представлять собой слитый белок TNFR-Fc.
Рецептор фактора некроза опухоли (TNFR) относится к рецепторному белку, связывающемуся с TNF-α. Белок TNFR может представлять собой, без ограничения, белок TNFRI(p55) или белок TNFRII(p75), предпочтительно белок TNFRII. Кроме того, TNFRII может быть использован альтернативно с представителем 1 В суперсемейства рецептора фактора некроза опухоли (TNFRSF1B). Белок TNFRII разделяют на 4 домена и трансмембранную область, например, без ограничения, белок TNFRII, состоящий из 235 аминокислот, включая 4 домена и трансмембранную область. Информация о белках TNFRI и TNFRII может быть получена из известных баз данных, таких как GenBank Национальных институтов здравоохранения США. Например, белки TNFRI и TNFRII могут представлять собой, без ограничения, белки с регистрационным номером NP_001056 или Р20333.
Обладая биологической активностью по связыванию с TNF-α, сверхэкспрессия которого in vivo, как известно, приводит к различным заболеваниям, белок TNFR может быть использован для лечения заболеваний, опосредованных TNF-α. Для применения в указанных целях белок TNFR может быть получен и использован в форме слитого белка, период полувыведения которого увеличен слиянием Fc-области иммуноглобулина и белка TNFR.
Слитый белок «рецептор фактора некроза опухоли (TNFR) - Fc» относится к слитому белку, где весь белок TNFR или его часть связаны с Fc-областью иммуноглобулина посредством ферментативной реакции, или к продукту, где эти два полипептида экспрессированы с получением одного полипептида посредством генетических манипуляций. Слитый белок TNFR-Fc может иметь белок TNFR и Fc-область иммуноглобулина, связанные друг с другом, без ограничения, непосредственно или через пептидный линкер. Неограничивающим примером слитого белка TNFR-Fc может быть этанерцепт (патент США 7915225; 5605690; Re. 36755).
Слитый белок TNFR-Fc может быть получен слиянием всего белка TNFR или его части с Fc-областью иммуноглобулина, например, без ограничения, 232 аминокислот Fc-области иммуноглобулина, включая шарнирную область, и аминокислотных сайтов 1-235 TNFRII. Кроме того, кодоны слитого белка TNFR-Fc могут быть оптимизированы в соответствии с клетками-хозяевами для экспрессии, и слитый белок TNFR-Fc может, например, без ограничения, представлять собой слитый белок TNFR-Fc, кодоны которого оптимизированы специально для клеток СНО. Слитый белок TNFR-Fc представляет собой не только какую-либо одну аминокислотную последовательность, но также аминокислотные последовательности, на 70% или более, предпочтительно на 80% или более, более предпочтительно на 90% или более, еще более предпочтительно на 95% или более, наиболее предпочтительно на 98% аналогичны этой аминокислотной последовательностью, и включает все белки, обладающие активностью по существенному связыванию с TNF-α. Очевидно, при условии, что последовательность, обладающая таким сходством, представляет собой аминокислотную последовательность, идентичную слитому белку TNFR-Fc, или аминокислотную последовательность, обладающую соответствующей биологической активностью, объем настоящего изобретения включает белковые мутанты с аминокислотными последовательностями, часть которых удалена, модифицирована, заменена или добавлена.
Fc относится к части иммуноглобулина, содержащей константный домен 2 тяжелой цепи CH2), константный домен 3 тяжелой цепи (CH3) и шарнирную область, без вариабельных доменов тяжелой и легкой цепей, константного домена 1 тяжелой цепи CH1) и константного домена легкой цепи (CL1) иммуноглобулина (Ig). Кроме того, Fc-область по настоящему изобретению включает не только нативную форму аминокислотной последовательности, но также ее производные аминокислотные последовательности. Производная аминокислотная последовательность означает, что один или более чем один аминокислотный остаток нативной формы аминокислотной последовательности отличается в силу делеции, вставки, консервативной или неконсервативной замены или их комбинации. Кроме того, Fc-область иммуноглобулина может представлять собой Fc-область, имеющую происхождение от IgG, IgM, IgE, IgA или IgD, или их комбинаций или гибридов. Кроме того, Fc-область иммуноглобулина предпочтительно имеет происхождение от IgG, который, как известно, увеличивает период полувыведения связывающего белка, и более предпочтительно имеет происхождение от IgG1, но не ограничена этим подклассом и может быть получена из IgG любого подкласса (IgG1, IgG2, IgG3 и IgG4).
Fc-область может быть получена генетически или получением гена, кодирующего Fc-область, с использованием рекомбинантного вектора или расщеплением очищенных поликлональных антител или моноклональных антител подходящим ферментом, таким как папаин, пепсин и так далее, соответственно.
Слитый белок TNFR-Fc может быть получен ведением вектора экспрессии, содержащего полинуклеотид, кодирующий слитый белок, в клетку-хозяина и его экспрессией. В типичном воплощении настоящего изобретения в качестве вектора экспрессии, содержащего полинуклеотид, кодирующий слитый белок TNFR-Fc, использовали вектор pCUCBin-mSig-TNFcept, и трансформировали им клетки СНО для экспрессии слитого белка TNFR-Fc.
В настоящем изобретении микроорганизм может быть использован в том же значении, что клетка-хозяин или трансформант.Неограничивающим примером может быть линия животных клеток, растительная или дрожжевая клетка-хозяин. В типичном воплощении настоящего изобретения в качестве микроорганизма использовали клетки яичника китайского хомячка (клетки СНО), но без ограничения ими, при условии, что микроорганизм может быть трансформирован полинуклеотидом, кодирующим рекомбинантный гликопротеин.
Полинуклеотид, при условии, что его можно экспрессировать в микроорганизме, может быть введен в хромосому и расположен в ней или расположен вне хромосомы. Полинуклеотид включает РНК и ДНК, кодирующие целевой белок. Способ введения полинуклеотида не ограничен, при условии, что его применяют в данной области. В качестве примера, полинуклеотид может быть введен в микроорганизм в форме экспрессионной кассеты, генной конструкции, содержащей все обязательные элементы, необходимые для самостоятельной экспрессии. В качестве еще одного примера, может быть использован способ модификации вектором экспрессии, содержащим последовательность полинуклеотида, кодирующую целевой белок, функционально связанный с подходящей регуляторной последовательностью таким образом, что целевой белок может быть экспрессирован в подходящей клетке-хозяине. Регуляторная последовательность содержит промотор, инициирующий транскрипцию, случайную операторную последовательность для регуляции транскрипции, последовательность, кодирующую подходящий домен связывания с рибосомами на мРНК, и последовательность для регуляции транскрипции и трансляции. После трансформации подходящей клетки-хозяина вектор может быть реплицирован или функционировать независимо от генома хозяина, или может быть интегрирован в сам геном хозяина. Относительно вектора, используемого в настоящем изобретении, может не быть конкретных ограничений, при условии, что вектор может быть реплицирован в клетке-хозяине, и может быть использован любой вектор, известный в данной области.
Паттерн гликозилирования рекомбинантного гликопротеина означает паттерн экспрессии гликоформы, проявляющийся при гликозилировании гликопротеина. Примеры паттерна гликозилирования включают наличие гликозилирования, связывающего сахарид с белком, тип сахарида, тип гликозилирования, содержание сахарида, состав моносахарида (сахаридов), включая молярное соотношение, расположение гликоформы, структуру гликоформы, включая последовательность, место гликозилирования, количество занятых сайтов гликозилирования, число гликоформ и относительное содержание в соответствии со структурой. В зависимости от паттерна гликозилирования рекомбинантного гликопротеина возможны различия по биологической активности или стабильности in vivo.
В настоящем изобретении инсулин может контролировать N-связанное гликозилирование рекомбинантного гликопротеина. В настоящем изобретении N-связанное гликозилирование может быть использовано в том же значении, что N-гликозилирование. В качестве примера, инсулин может снижать содержание N-гликанов в рекомбинантном гликопротеине. В настоящем изобретении N-гликан может быть использован в том же значении, что N-гликоформа, и может относиться к случаю, когда сахарид связан с аспарагином белка.
В настоящем изобретении инсулин может контролировать О-связанное гликозилирование рекомбинантного гликопротеина. В настоящем изобретении N-связанное гликозилирование может быть использовано в том же значении, что О-гликозилирование. В качестве еще одного примера, инсулин может снижать содержание О-гликанов в рекомбинантном гликопротеине. В настоящем изобретении О-гликан может быть использован в том же значении, что О-гликоформа, и может относиться к случаю, когда сахарид связан с серином или треонином белка.
В настоящем изобретении инсулин может контролировать N-связанное гликозилирование и О-связанное гликозилирование рекомбинантного гликопротеина.
В типичном воплощении настоящего изобретения было обнаружено, что добавление инсулина влияет на паттерн гликозилирования гликопротеина (Таблица 2). Конкретно, было подтверждено, что добавление инсулина контролирует и снижает содержание N-гликанов и/или О-гликанов. В частности, было подтверждено, что в процессе культивирования клеток, способных продуцировать гликопротеин, добавление инсулина в фазе продуцирования играет важную роль в контроле паттерна гликозилирования.
Концентрация инсулина может составлять от 0,0001 мг/л до 1 г/л относительно общего объема культуральной среды. В типичном воплощении настоящего изобретения было подтверждено, что содержание N-гликанов и/или О-гликанов можно контролировать и снижать по мере повышения концентрации инсулина (Таблица 2).
Ограничений относительно культуральной среды нет, при условии, что ее используют в данной области для культивирования микроорганизма или клетки-хозяина, содержащих полинуклеотид, кодирующий гликопротеин. Например, культуральная среда может содержать аминокислоту, такую как L-глутамин, тимидин, аланин, моногидрохлорид аргинина, моногидрат аспарагина, аспарагиновую кислоту, цистеин, глицин, гистидин, изолейцин, лейцин, моногидрохлорид лизина, метионин, фенилаланин, пролин, серии, треонин, триптофан, тирозин (динатриевую соль, дигидрат) и валин. В качестве еще одного примера, культуральная среда может содержать глюкозу, бикарбонат натрия, хлорид натрия, безводный хлорид кальция, пентагидрат сульфата меди, нонагидрат нитрата железа, гептагидрат сульфата железа, хлорид калия, безводный сульфат магния, безводный хлорид магния, фосфат натрия (одноосновный или двухосновный, моногидрат), гептагидрат сульфата цинка, гипоксантин, дигидрохлорид путресцина, пируват натрия, биотин, D-пантотенат кальция, хлорид холина, цианкобаламин, фолиевую кислоту, i-инозит, никотинамид, моногидрохлорид пиридоксаля, моногидрохлорид пиридоксина, рибофлавин, моногидрохлорид тиамина, безводную глюкозу, хлорид калия, фосфат натрия (NaH2PO4⋅H2O), гидрокарбонат натрия (NaHCO3), HEPES (свободная кислота), сульфат декстрана, хлорид натрия, аскорбиновую кислоту, D-биотин, Нурер 1510 или комбинацию из двух или более. Исходная культура для посева может также содержать МТХ для повышения уровня экспрессии.
Культивирование может представлять собой метод перфузионного культивирования. Культивирование может представлять собой метод культивирования перфузией культуральной жидкости вокруг микроорганизма. Метод перфузионного культивирования позволяет легко контролировать концентрацию инсулина в соответствии с целевым паттерном гликозилирования.
В качестве еще одного аспекта, согласно настоящему изобретению предложен способ контроля паттерна гликозилирования рекомбинантного гликопротеина, включающий: (а) культивирование микроорганизма, содержащего полинуклеотид, кодирующий рекомбинантный гликопротеин, в культуральной среде для выращивания микроорганизма; и (б) добавление инсулина в культуральную среду и культивирование указанного микроорганизма с получением гликопротеина.
В качестве примера, рекомбинантный гликопротеин может представлять собой слитый белок иммуноглобулина. В качестве еще одного примера, рекомбинантный гликопротеин может представлять собой слитый белок TNFR-Fc, описанный выше.
Стадия (а), представляющая собой стадию роста, может дополнительно включать культивирование для посева.
Культуральная среда по стадии (а) не может содержать инсулин.
Стадия (б) может представлять собой стадию добавления инсулина в различных концентрациях в соответствии с целевым паттерном гликозилирования. В типичном воплощении настоящего изобретения было обнаружено, что в фазе роста содержание N-гликанов и/или О-гликанов варьировало в зависимости от добавления инсулина. В частности, было подтверждено, что добавление инсулина позволяет контролировать и снижать содержание N-гликанов и/или О-гликанов. В частности, было подтверждено, что в процессе культивирования клеток, способных продуцировать гликопротеин, добавление инсулина в фазе продуцирования играет важную роль в контроле паттерна гликозилирования.
Концентрация инсулина может составлять от 0,0001 мг/л до 1 г/л относительно общего объема культуральной среды. Было подтверждено, что содержание N-гликанов и/или О-гликанов можно контролировать и снижать по мере повышения концентрации инсулина (Таблица 2).
Инсулин может контролировать N-связанное гликозилирование и О-связанное гликозилирование рекомбинантного гликопротеина. В качестве примера, инсулин может снижать содержание N-гликанов в рекомбинантном гликопротеине. В качестве еще одного примера, инсулин может снижать содержание О-гликанов в рекомбинантном гликопротеине.
В качестве еще одного аспекта, согласно настоящему изобретению предложен состав культуральной среды для контроля паттерна гликозилирования рекомбинантного гликопротеина. Инсулин можно включать в концентрации от 0,0001 мг/л до 1 г/л относительно общего объема культуральной среды.
Например, в процессе культивирования микроорганизма эту культуральную среду можно использовать только в фазе продуцирования.
ВАРИАНТ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Далее настоящее изобретение будет подробно описано следующими типичными воплощениями. Тем не менее, типичные воплощения раскрыты здесь исключительно в иллюстративных целях, и их не следует толковать как ограничение объема настоящего изобретения.
Пример 1: Получение клеточной линии для получения гликопротеина
1-1. Получение вектора
Применяли методы, чаще всего используемые в молекулярной биологии, такие как обработка рестрикционными ферментами, очистка плазмидной ДНК, конъюгация участков ДНК и трансформация Е. coli, с минимальными модификациями способов, описанных в Molecular Cloning (2nd edition), Sambrook etal.
Ген человеческого рецептора TNF р75 (TNFR) клонировали с использованием библиотеки кДНК, где в качестве матрицы была использована мРНК, выделенная из клеточной линии HUVEC, и проводили слияние клонированного гена с Fc-областью человеческого IgGi, получая TNFR-IgGi. С использованием вектора pTOP-BA-RL-pA (публикация патента Кореи №10-2012-0059222; содержит «CMVe», «СВ» и «интрон бета-актина») в качестве матрицы и TNFR-IgG1 получали вектор pCUCBin-mSig-TNFcept.
1-2. Культивирование материнских клеток
В качестве материнских клеток использовали CHO/dhfr- (CHODXB11). CHO/dhfr- представляют собой клетки с дефицитом дигидрофолатредуктазы (DHFR), выделенные из клеток СНО.
1-3. Трансформация и выбор клеточной линии-продуцента
Трансформированные клетки получали с использованием CHO/dhfr- (CHODXB11) и вектора pCUCBin-mSig-TNFcept, содержащего ген рецептора TNF р75 (TNFR), и ген амплифицировали, используя концентрацию МТХ. Клетки идентифицировали как трансформированные клетки и отбирали отдельные клоны в качестве клеточной линии-продуцента. Затем клеточные линии помещали в стеклянную емкость и хранили в жидком азоте.
Пример 2: Культивирование клеточной линии для получения гликопротеина и сбор белка
Использовали разные культуральные среды в зависимости от фазы культивирования. Для получения основной культуральной среды инсулин, 5,8 г/л, добавляли в среду X011SB (Merck Millipore, номер по каталогу 102443). В фазе культивирования для посева использовали среду (Media EC-SI), где в основную культуральную среду были добавлены Юг/л безводной глюкозы (Sigma) и 0,584 г/л глутамина, глицина и серина (Sigma). В фазе роста использовали среду (EC-GM), где в основную культуральную среду были добавлены 5 г/л безводной глюкозы и 0,584 г/л L-глутамина, глицина и серина. В фазе продукции использовали среду (ЕС-РМ), где в основную культуральную среду были добавлены 15 г/л безводной глюкозы и 0,584 г/л L-глутамина, глицина и серина.
Стеклянную емкость с клеточной линией, полученной в Примере 1, быстро размораживали на водяной бане и содержащиеся в ней клетки перемещали в пробирку Falcon, содержащую 10 мл культуральной среды. Полученные клетки центрифугировали и удаляли супернатант. Затем клетки ресуспендировали в 10 мл среды ЕС-SI и высевали их в колбу Эрленмейера до конечного объема 50 мл. Клетки культивировали с использованием биореактора для клеточных культур CelliGen310 объемом 5 л, получая 2 л по рабочему объему. По достижении числа жизнеспособных клеток 2×106 клеток/мл после пятикратного культивирования инокулята, культуральную среду начинали заменять на EC-GM посредством перфузионного культивирования. По мере роста числа жизнеспособных клеток повышали скорость смены культуральной среды для эффективного разделения клеток. Когда число жизнеспособных клеток достигало 1,5×107 клеток/мл (Фиг. 2), культуральную среду меняли на ЕС-РМ, переходя от фазы роста к фазе продуцирования. Сбор повторяли в общей сложности четыре раза и собранный белок очищали. Полученное значение представляло собой среднее значение четырех сборов.
Пример 3: Анализ содержания гликанов 3-1. Анализ содержания О-гликанов Образец, очищенный в Примере 2, разбавляли буфером с 25 мМ фосфатом натрия и рН 6,3 до 100 мкл и концентрации 1,0 мг/мл. К каждому образцу добавляли по 4 мкл N-гликозидазы F (1 ЕД/мкл Roche), 2 мкл нейраминидазы (1 ЕД/100 мкл) и 2 мкл трипсина (1 мг/мл, Promega) и проводили взаимодействие при 37°С в течение 18 часов. Затем проводили LC-MS-анализ.
Вносили 80 мкл образца и триптические пептиды затем анализировали с использованием C18RP (4,6 мм × 250 мм, 5 мкм, 300 A; Vydac, номер по каталогу 218ТР54). В качестве подвижной фазы А использовали 0,1% TFA в воде и в качестве подвижной фазы В использовали 0,1% TFA в 80%-м холодном CAN. Анализ проводили в условиях градиента на протяжении 150 минут.Используя UV-детектор, пептид выявляли на 215 нм, и исследуемый материал, разделенный посредством LC, соединяли с масс-спектрометром (LTQXL, Thermo) для MS-анализа и расчета относительной площади (%) О-гликопептидов.
3-2. Анализ содержания N-гликанов
Образец, очищенный в Примере 2, и стандартный образец (этанерцепт, Pfizer) разбавляли разбавителем для образцов (25 мМ фосфат натрия (буфер с рН 6,3)) до 3,0 мг/мл. Смешивали по 100 мкл каждого образца и 6 мкл раствора N-гликозидазы F и проводили взаимодействие при 37°С в течение 20 часов.
После взаимодействия в раствор добавляли 400 мкл этанола и перемешивали на вихревой мешалке. Полученный раствор центрифугировали, после чего супернатант переносили в пробирку типа Эппендорф и полностью высушивали с использованием концентратора SpeedVac. После добавления 10 мкл агента для мечения 2-АА к высушенному образцу и их перемешивания смесь подвергали взаимодействию при 45°С и охлаждали до комнатной температуры.
На одноразовую пробирку для культивирования помещали картридж GlycoClean S, после чего последовательно пропускали дистиллированную воду, 30%-й ацетат и ацетонитрил. Охлажденный образец вносили в центр мембраны картриджа и пропускали с ацетонитрилом. Для элюирования N-гликанов в картридж вносили дистиллированную воду, собирая элюат в пробирку типа Эппендорф. Полученный раствор гликанов лиофилизировали и хранили до анализа.
Анализ проводили, используя колонку для HPLC (AsahiPak NH2P-50 4Е, 4,6×250 мм) в условиях градиента в течение 130 минут с использованием 0,5 мМ ацетата аммония (рН 6,7) и 250 мМ ацетата аммония (рН 5,6) в качестве подвижных фаз А и В, соответственно. Для выявления использовали флуорометрический детектор и рассчитывали суммарную площадь пиков по числу сиаловых кислот, присутствующих на конце N-гликана. В случае отсутствия сиаловой кислоты его отмечали как нейтральный. В случае одной (моносиалил) и двух (дисиалил) их отмечали как -1 и -2, соответственно.
Экспериментальный пример 1. Культивирование клеточной линии с использованием культуральной среды без инсулина, добавляемого в фазе продуцирования
Для культивирования клеточной линии использовали такую же культуральную среду, как в фазе продукции в Примере 2, но без инсулина. Анализировали содержание N-гликанов (%) и долю относительной площади (%) О-гликопептидов при разной температуре, и они показаны в Таблице 1 ниже.
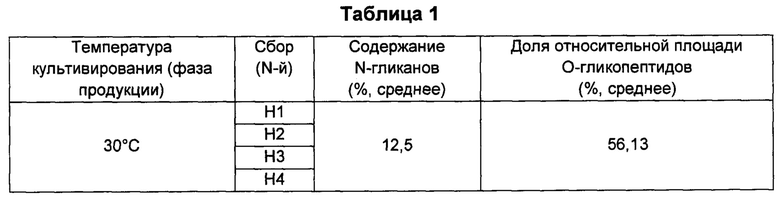
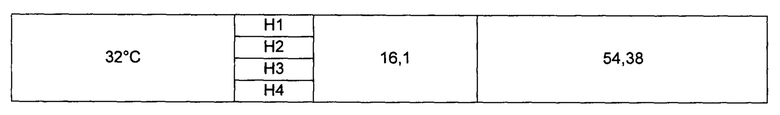
Экспериментальный пример 2. Сравнение изменений в паттернах гликозилирования в зависимости от добавления инсулина в фазе продукции
Сравнивали паттерны гликозилирования в зависимости от добавления инсулина, и они показаны в Таблице 2 ниже.
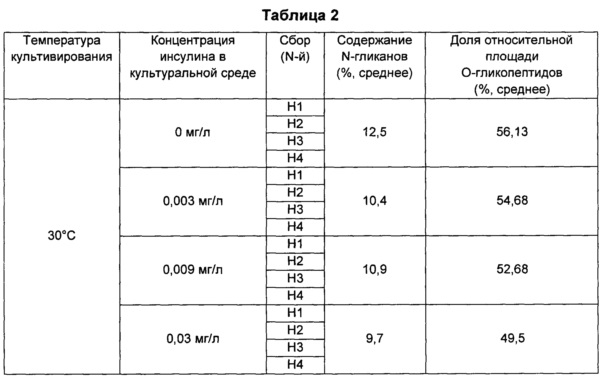
В результате было показано, что в процессе культивирования клеток, способных продуцировать гликопротеин, добавление инсулина в фазе продукции влияло на паттерн гликозилирования. В частности, было показано, что содержание N-гликанов и/или О-гликанов изменялось в зависимости от добавления инсулина. Конкретно, было подтверждено, что добавление инсулина позволяет контролировать и снижать содержание N-гликанов и/или О-гликанов.
Несмотря на то, что настоящее изобретение было описано со ссылкой на конкретные иллюстративные воплощения, специалистам в области, к которой относится настоящее изобретение, будет ясно, что настоящее изобретение может быть воплощено в других конкретных формах без выхода за рамки технической сущности или существенных характеристик настоящего изобретения. Таким образом, описанные выше воплощения во всех отношениях являются иллюстративными и не являются ограничивающими. Кроме того, объем настоящего изобретения определен приложенной формулой изобретения, но не подробным описанием, и следует понимать, что все модификации или варианты, имеющие происхождение от значений и объема настоящего изобретения и его эквивалентов, включены в объем приложенной формулы изобретения.
ПРОМЫШЛЕННАЯ ПРИМЕНИМОСТЬ
Поскольку он позволяет изменять содержание N-гликанов и/или О-гликанов в зависимости от добавления инсулина, особенно в фазе роста, способ контроля паттерна гликозилирования рекомбинантного гликопротеина по настоящему изобретению может быть очень полезен при получении фармацевтического рекомбинантного гликопротеина, где единообразие связывания сахаридных молекул играет важную роль.
Группа изобретений относится к области биотехнологии. Предложен способ контроля паттерна гликозилирования рекомбинантного гликопротеина, включающий культивирование микроорганизма, содержащего полинуклеотид, кодирующий рекомбинантный гликопротеин, в культуральной среде, содержащей инсулин. Предложен способ контроля паттерна гликозилирования рекомбинантного гликопротеина, включающий (а) культивирование микроорганизма, содержащего полинуклеотид, кодирующий рекомбинантный гликопротеин, в культуральной среде для выращивания микроорганизма и (б) добавление инсулина в культуральную среду и культивирование указанного микроорганизма с получением гликопротеина. Группа изобретений позволяет контролировать и снижать содержание N-гликанов или О-гликанов в рекомбинантном гликопротеине по мере повышения концентрации инсулина в культуральной среде, что может быть полезно при получении фармацевтического рекомбинантного гликопротеина. 2 н. и 10 з.п. ф-лы, 2 ил., 2 табл., 5 пр.
1. Способ контроля паттерна гликозилирования рекомбинантного гликопротеина, включающий культивирование микроорганизма, содержащего полинуклеотид, кодирующий рекомбинантный гликопротеин, в культуральной среде, содержащей инсулин, где инсулин снижает содержание N-гликана или О-гликана в рекомбинантном гликопротеине.
2. Способ по п.1, где рекомбинантный гликопротеин представляет собой слитый белок иммуноглобулина.
3. Способ по п.1, где рекомбинантный гликопротеин представляет собой слитый белок TNFR (рецептор фактора некроза опухоли)-Fc.
4. Способ по п.1, где концентрация инсулина составляет от 0,0001 до 0,03 мг/л относительно общего объема культуральной среды.
5. Способ по п.1, где инсулин контролирует N-связанное гликозилирование и О-связанное гликозилирование.
6. Способ по п.1, где культивирование представляет собой метод перфузионного культивирования.
7. Способ контроля паттерна гликозилирования рекомбинантного гликопротеина, включающий:
(а) культивирование микроорганизма, содержащего полинуклеотид, кодирующий рекомбинантный гликопротеин, в культуральной среде для выращивания микроорганизма; и
(б) добавление инсулина в культуральную среду и культивирование указанного микроорганизма с получением гликопротеина, где инсулин снижает содержание N-гликана или О-гликана в рекомбинантном гликопротеине.
8. Способ по п.7, где стадия (б) представляет собой стадию добавления инсулина в различных концентрациях в соответствии с заданным паттерном гликозилирования.
9. Способ по п.7, где рекомбинантный гликопротеин представляет собой слитый белок иммуноглобулина.
10. Способ по п.7, где рекомбинантный гликопротеин представляет собой слитый белок TNFR-Fc.
11. Способ по п.7, где концентрация инсулина составляет от 0,0001 до 0,03 мг/л относительно общего объема культуральной среды.
12. Способ по п.7, где культивирование представляет собой метод перфузионного культивирования.
| KR 20090029841 A, 23.03.2009 | |||
| MARIE-CLAIRE BIOL-N’GARAGBA et al., Regulation of the intestinal glycoprotein glycosylation during postnatal development: role of hormonal and nutritional factors, Biochimie Vol | |||
| Устройство для выпрямления опрокинувшихся на бок и затонувших у берега судов | 1922 |
|
SU85A1 |
| Накладной висячий замок | 1922 |
|
SU331A1 |
| ПОЛУЧЕНИЕ ГЛИКОПРОТЕИНОВ | 2007 |
|
RU2463345C2 |
| US 20120276631 A1, 01.11.2012 | |||
| WO 9961650 A1, 02.12.1999 | |||
| KR 20110139292 A, 28.12.2011. | |||
Авторы
Даты
2018-10-25—Публикация
2015-12-30—Подача