{Область техники, к которой относится изобретение}
{0001}
Настоящее изобретение относится к новым кристаллическим формам 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида.
Более конкретно, настоящее изобретение относится к полиморфным формам L-тартратной соли соединения и к способам его получения, к композициям, содержащим их, и к применениям таких полиморфов.
{Уровень техники}
{0002}
Соединение 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида описывается в WO97/024369 как секретагог гормона роста, а также его активность агониста по отношению к рецептору грелина. Соединение назвали капроморелин, и оно разрабатывается на стадии клинических исследований. Способ синтеза соединения также описан в EP-1031575.
{0003}
Однако публично не известны ни кристаллы, ни смесь других кристаллических форм 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида.
{Список цитирования}
{Патентная литература}
{0004}
{PL 1} WO97/024369.
{PL 2} EP-1031575.
{Сущность изобретения}
{Техническая проблема}
{0005}
Как хорошо известно специалистам в данной области, всегда было желательно найти или получить кристаллы или кристаллические формы для создания лекарственных средств, улучшенных с различных точек зрения, включая составление рецептуры и изготовление лекарственных средств (см. Byrn S. R. et al., Solid-State Chemistry of Drugs 2nd ed., pp 3-43 и 461-503, 1999, SSCI, Inc.).
{0006}
Соответственно, были предприняты серьезные попытки обнаружить или получить кристаллы или кристаллическую форму 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида после того, как указанное соединение было раскрыто в 1997 (WO97/024369) Pfizer Inc.
{0007}
Несмотря на столь большое количество попыток, до сих пор не были идентифицированы фармацевтически приемлемые кристаллические формы указанного соединения.
После обширных и тщательных исследований авторам настоящего изобретения удалось найти весьма условия получения кристаллической формы, что привело к получению долгожданной кристаллической формы (полиморфной формы I) указанного соединения а L-тартрата.
{0008}
Как раскрыто в рабочем примере настоящего изобретения, полиморфной формы I была определена.
{0009}
Целью настоящего изобретения является создание фармацевтически приемлемых кристаллических форм 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида, которые можно было бы легко, экономично и воспроизводимо получать для применения в фармацевтических композициях, обладающих постоянными эксплуатационными характеристиками, такими как, например, превосходная стабильность и негигроскопичность. Кроме того, целью настоящего изобретения является создание способов получения композиций, в которых содержатся и используются такие полиморфные формы.
{Решение проблемы}
{0010}
Таким образом, настоящее изобретение предлагает:
[1] Полиморфную форму I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида L-тартрата, которая отличается картиной дифракции рентгеновского излучения на порошках (PXRD), полученной с помощью облучения излучением Cu-Kalpha (Cu-Ka), которая содержит главные пики при 2-Thetao 4,4, 10,2, 12,5, 13,2, 13,7, 16,4, 16,6, 18,5, 19,3 и 21,7 +/- 0,2;
{0011}
[2]
Полиморфную форму I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида L-тартрата, как описано в [1], которая дополнительно отличается данными дифференциальной сканирующей калориметрии (DSC), в которых оно демонстрирует эндотермическое событие примерно при 177oC;
{0012}
[3]
Полиморфную форму I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида L-тартрата, как описано в [1] или [2], которая дополнительно отличается инфракрасным (ИК) спектром (KBr), который показывает полосы поглощения при 3349, 3107, 3036, 2983, 2870, 2770, 2526, 1705, 1662, 1625, 1531, 1454, 1442, 1220, 1132, 1109, 1089 и 704 +/- 2 см-1.
{0013}
[4]
Фармацевтическую композицию, содержащую Полиморфную Форму I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида L-тартрата, как описано в любом из [1] - [2], вместе с одним или несколькими фармацевтически приемлемыми наполнителями;
{0014}
[5]
Полиморфную форму I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида L-тартрата, как описано в любом из пп. [1] - [3], для использования в качестве лекарственного препарата;
{0015}
[6]
Применение Полиморфной формы I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида L-тартрата, как описано в любом из пп.[1] - [3], или фармацевтической композиции, как описано в [4], при приготовлении лекарственного препарата для куративного, паллиативного или профилактического лечения болезненных состояний, опосредованных активностью агониста рецепторов грелина;
{0016}
[7]
Способ лечения болезненных состояний, опосредованных активностью рецепторов грелина, который включает введение эффективного количества Полиморфной формы I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида L-тартрата, как описано в любом из пп. [1] - [3], или фармацевтической композиции, как описано в [4], животному, включая человека, нуждающемуся в таком лечении.
{0017}
[8]
Способ получения Полиморфной формы I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида L-тартрата, как описано в [1] - [3], включающий стадию экспонирования 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида для органического растворителя, предпочтительно, этилацетата, в условиях L-винной кислоты в спирте, предпочтительно, в метиловом спирте, этиловом спирте и изопропиловом спирте, более предпочтительно, в метиловом спирте и изопропиловом спирте;
{0018}
[9]
Способ получения Полиморфной формы I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида L-тартрата, как описано в любом из пп. [1] - [3], включающий стадию экспонирования 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида для этилацетата при условиях L-винной кислоты в метаноле или изопропиловом спирте.
{0019}
[10]
Способ получения Полиморфной формы I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида L-тартрата, как описано в любом из пп. [1] - [3], включающий стадию экспонирования 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида для спирта, выбранного из метилового спирта, этилового спирта и изопропилового спирта.
{0020}
[11]
Способ получения Полиморфной формы I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида L-тартрата, как описано в [10], включающий стадию экспонирования 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида для метанола или изопропанола.
{Преимущества осуществления настоящего изобретения}
{0021}
Как указано выше, это объект настоящего изобретения, чтобы найти или подготовить кристаллические или кристаллическую форму обладающего неожиданно отличные физико-химические характеристики в разработке лекарственных средств из различных точек зрения, включая составление рецептуры и изготовление лекарственного средства. Неожиданно было обнаружено, что указанной задачи можно достичь с помощью настоящего изобретения, в котором предложены кристаллические полиморфные формы 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида, известные как полиморфная форма I.
До сих пор не было найдено фармацевтически приемлемых кристаллических форм указанного соединения, несмотря на многочисленные попытки специалистов в данной области.
{0022}
Все полиморфы по настоящему изобретению обладают превосходными и неожиданными преимуществами по сравнению с белым твердым веществом, раскрытым ранее в WO97/024369.
Обнаружено, что полиморфная форма I более стабильны, чем белое твердое вещество, раскрытое ранее в WO97/024369.
{0023}
Кроме того, было обнаружено, что полиморфные формы по настоящему изобретению применимы для крупномасштабного синтеза. Они обладают приемлемыми характеристиками в твердом состоянии для создания твердой лекарственной формы.
{Краткое описание рисунков}
{0024}
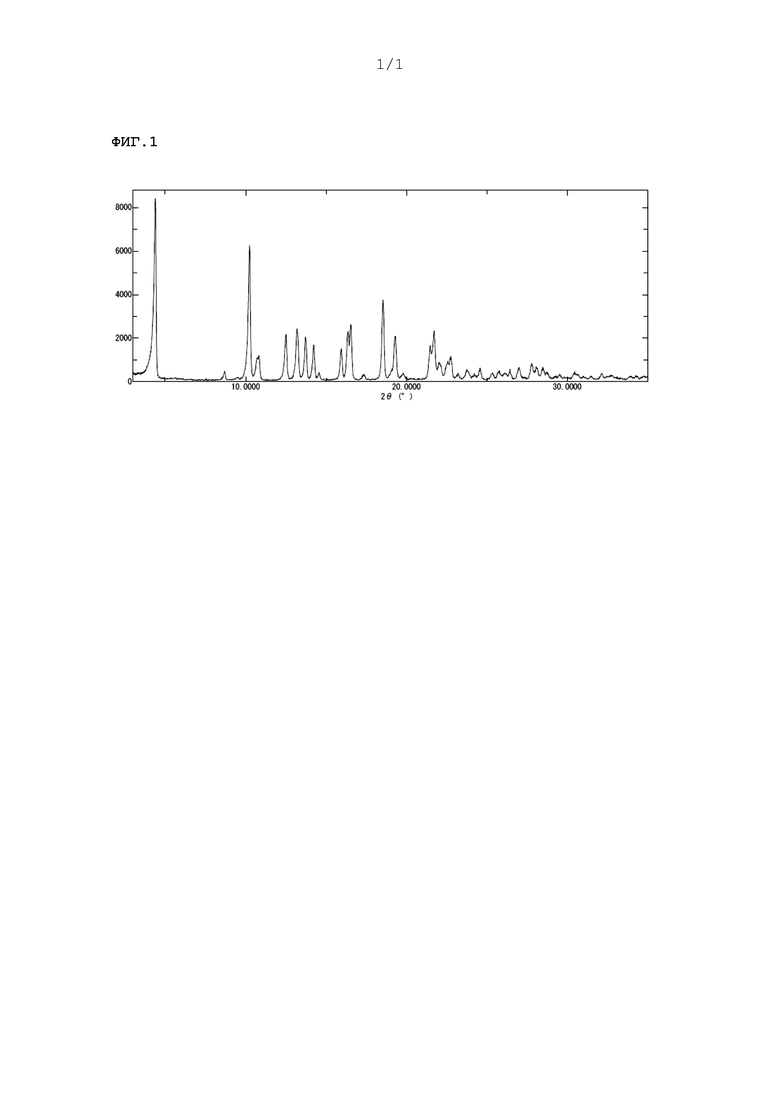
{ФИГ.1}
демонстрирует картину PXRD полиморфной формы I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида.
{Описание вариантов осуществления}
{0025}
Соответственно, в настоящем изобретении предложена кристаллическая полиморфная форма I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида L-тартрата, которая характеризуется картиной порошковой дифракции рентгеновских лучей (PXRD), полученной в результате облучения источником Cu-K-альфа, которая включает основные пики при 2-Thetao 4,4, 10,2, 12,5, 13,2, 13,7, 16,4, 16,6, 18,5, 19,3 и 21,7 (°) +/- 0,2;
{0026}
Полиморфная форма I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида L-тартрата, как описано выше, которая дополнительно характеризуется данными дифференциальной сканирующей калориметрии (DSC), в которых она демонстрирует эндотермическое событие примерно при 177oC;
{0027}
Полиморфная форма I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида L-тартрата, как описано выше, которая дополнительно отличается инфракрасным (ИК) спектром (KBr), который показывает полосы поглощения при 3349, 3107, 3036, 2983, 2870, 2770, 2526, 1705, 1662, 1625, 1531, 1454, 1442, 1220, 1132, 1109, 1089 и 704 +/- 2 см-1;
{0028}
В качестве следующего аспекта настоящего изобретения предложена полиморфная форма I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида L-тартрата по настоящему изобретению, предназначенная для применения в качестве лекарственного средства.
{0029}
Качестве еще одного аспекта настоящего изобретения, предлагается использование Полиморфной формы I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида L-тартрата по настоящему изобретению при приготовлении лекарственного препарата для лечения любого заболевания, для которого показан агонист рецепторов грелина, в частности, для куративного, профилактического или паллиативного лечения 1) желудочно-кишечного расстройства, 2) расстройства, отличающегося отсутствием аппетита, подавлением аппетита, или расстройства, дающего в результате уменьшение приема пищи, и 3) заболевания, в которое вовлечен высокий уровень секреции желудочного сока.
{0030}
Желудочно-кишечное расстройство может выбираться из группы, состоящей из послеоперационной кишечной непроходимости, гастропареза, дисфункции пищеварительного тракта, вызываемой опиоидами, хронической псевдонепроходимости желудочно-кишечного тракта, острой псевдонепроходимости ободочной и толстой кишки (синдрома Огильви), отсутствия энтеральной моторики, синдрома короткой кишки, тошноты, синдрома воспаленного кишечника с преобладающими констипациями (IBS), хронической констипации, функциональной диспепсии, синдрома диспепсии, связанного с раком, заболевания трансплантат против хозяина, задержки опорожнения кишечника, желудочно-кишечной дисфункции или задержки опорожнения кишечника, проявляющегося в сочетании с другими болезненными состояниями, отсутствия моторики желудочно-кишечного тракта или задержки опорожнения кишечника, возникающего при лечении критических состояний, желудочно-кишечной дисфункции или задержки опорожнения кишечника в результате лечения фармацевтическими агентами, рефлюксного гастроэзофагита (GERD), язв желудка и кишечника, гастроэнтерита и болезни Крона.
{0031}
Расстройство отличается отсутствием аппетита, подавлением аппетита, или результат уменьшения приема пищи может представлять собой кахексию, где кахексия вызывается раком, хронической сердечной недостаточностью, синдромом приобретённого иммунодефицита (AIDS), заболеванием почек, мышечными дистрофиями или старением.
{0032}
Заболевание, в которое вовлечен высокий уровень секреции желудочного сока, может представлять собой ахлоргидрию.
{0033}
В качестве альтернативного аспекта, предлагается способ лечения любого заболевания, при котором показан агонист рецептора грелина, в частности для куративного, профилактического или паллиативного лечения 1) желудочно-кишечного расстройства, 2) расстройства, отличающегося отсутствием аппетита, подавлением аппетита, или расстройства, которое дает в результате уменьшение приема пищи, и 3) заболевания, в которое вовлечен высокий уровень секреции желудочного сока, включающий введение терапевтически эффективного количества Полиморфной формы I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида L-тартрата по настоящему изобретению животному, включая человека, нуждающемуся в таком лечении.
{0034}
Полиморфная форма I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида L-тартрата по настоящему изобретению является полезной для общего лечения болезненных состояний, опосредованных активностью агониста рецептора грелина.
{0035}
Полиморфная форма I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида L-тартрата по настоящему изобретению может также быть полезной для лечения расстройства или состояния, выбранного из группы, состоящей из 1) желудочно-кишечного расстройства, 2) расстройства, отличающегося отсутствием аппетита, подавлением аппетита, или расстройства, которое дает в результате уменьшение приема пищи, и 3) заболевания, в которое вовлечен высокий уровень секреции желудочного сока.
{0036}
Схемы синтеза для получения 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида описаны в WO97/024369 и в разделе Примеры, ниже.
{0037}
Полиморфная форма I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида L-тартрата может быть получена посредством кристаллизации из раствора 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида в органическом растворителе, таком как этилацетат, посредством добавления спирта, например, раствора L-тартрата в метиловом спирте.
{0038}
Органические растворители, включая сложный эфир карбоновой кислоты, такой как этилацетат, и спирт, такой как метиловый спирт, этиловый спирт и изопропиловый спирт, могут использоваться для кристаллизации Полиморфной формы I.
{0039}
Полиморфная форма I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида L-тартрата по настоящему изобретению можно вводить отдельно или в комбинации с одним или более из других лекарственных средств (или в виде любой их комбинации). Обычно их вводят в виде композиции вместе с одним или более из фармацевтически приемлемых эксципиентов. Термин ‘эксципиент’ здесь используют для описания любого ингредиента, отличного от соединения по настоящему изобретению. Выбор эксципиента в значительной степени зависит от таких факторов, как конкретный способ введения, влияние эксципиента на растворимость и стабильность и характер лекарственной формы.
{0040}
Таким образом, в следующем аспекте настоящего изобретения предложена фармацевтическая композиция, включающая полиморфной формы I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида L-тартрата и один или более из подходящих эксципиентов. Указанные композиции являются подходящими для лечения болезненных состояний, опосредованных активностью рецепторов грелина.
{0041}
Массовая степень чистоты полиморфной формы I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида L-тартрата по настоящему изобретению не ограничена, но предпочтительно использовать практически чистые полиморфные формы для конкретных вариантов осуществления настоящего изобретения.
{0042}
Во избежание недоразумений, если в описании используют выражение ‘практически чистые’, оно означает по меньшей мере 90 масс.% степени чистоты. Более предпочтительно, ‘практически чистые’ означает по меньшей мере 95 масс.% степени чистоты и наиболее предпочтительно означает по меньшей мере 98 масс.% степени чистоты.
Ссылки в описании на термин «лечение» включают ссылки на лечение, паллиативное лечение и профилактику.
{0043}
В отношении введения животным, отличным от человека, термин ‘фармацевтический’, используемый в описании, можно заменить термином ‘ветеринарный’.
{0044}
Фармацевтические композиции, подходящие для доставки полиморфной формы по настоящему изобретению, и способы их получения будут хорошо понятны специалистам в данной области. Такие композиции и способы их получения можно найти, например, в Remington’s Pharmaceutical Sciences, 19th Edition (Mack Publishing Company, 1995); полиморфизм: In the Pharmaceutical Industry by Rolf Hilfiker (John Wiley & Sons, 2006).
{0045}
ОРАЛЬНОЕ ВВЕДЕНИЕ
Полиморфную форму I по настоящему изобретению можно вводить орально. Оральное введение может включать проглатывание, с тем, чтобы указанное соединение попадало в желудочно-кишечный тракт, и/или введение за щеку, на язык или под язык, в результате чего соединение попадает в кровоток непосредственно изо рта.
{0046}
Лекарственные формы, подходящие для орального введения, включают твердое вещество, полутвердое вещество и жидкие системы, такие как таблетки; мягкие или твердые капсулы, содержащие мульти- или нано-частицы, жидкости или порошки; пастилки (включая наполненные жидкостью); жвачки; гели; быстрорастворимые формы; пленки; суппозитории; спреи; и защечные или мукоадгезивные пластыри.
{0047}
Жидкие лекарственные формы включают суспензии, растворы, сиропы и эликсиры. Такие лекарственные формы можно использовать в качестве наполнителей для мягких или твердых капсул (изготовленных, например, из желатина или гидроксипропилметилцеллюлозы), и обычно они включают носитель, например, воду, этанол, полиэтиленгликоль, пропиленгликоль, метилцеллюлозу или подходящее масло, и один или более из эмульгирующих агентов и/или суспендирующих агентов. Жидкие лекарственные формы можно также получить путем восстановления твердого вещества, взятого из пакета, например, саше.
{0048}
Полиморфную форму по настоящему изобретению можно также использовать в быстрорастворимых, быстрораспадающихся лекарственных формах, таких как описано в Expert Opinion in Therapeutic Patents, 11 (6), 981-986, by Liang and Chen (2001).
{0049}
Для лекарственных форм в виде таблеток, в зависимости от дозы, лекарственное средство может составлять от 1 масс.% до 80 масс.% лекарственной формы, более типично от 5 масс.% до 60 масс.% лекарственной формы. Кроме лекарственного средства, таблетки обычно содержат разрыхлитель. Примеры разрыхлителей включают натриевый гликолят крахмала, карбоксиметилцеллюлозу натрия, карбоксиметилцеллюлозу кальция, кроскармеллозу натрия, кросповидон, поливинилпирролидон, метилцеллюлозу, микрокристаллическую целлюлозу, замещенную низшим алкилом гидроксипропилцеллюлозу, крахмал, прежелатинизированный крахмал и альгинат натрия. Как правило, разрыхлитель составляет от 1 масс.% до 25 масс.%, предпочтительно от 5 масс.% до 20 масс.% лекарственной формы.
{0050}
Связующие вещества обычно используют для придания когезивных свойств композициям в виде таблеток. Подходящие связующие вещества включают микрокристаллическую целлюлозу, желатин, сахара, полиэтиленгликоль, природные и синтетические смолы, поливинилпирролидон, прежелатинизированный крахмал, гидроксипропилцеллюлозу и гидроксипропилметилцеллюлозу. Таблетки могут также содержать разбавители, такие как лактоза (моногидрат, высушенный распылением моногидрат, безводный моногидрат и т.п.), маннит, ксилит, декстрозу, сахарозу, сорбит, микрокристаллическую целлюлозу, крахмал и дигидрат двухосновного фосфата кальция.
Таблетки могут также необязательно включать поверхностно-активные вещества, такие как лаурилсульфат натрия и полисорбат 80, и скользящие вещества, такие как диоксид кремния и тальк. Если они присутствуют, поверхностно-активные вещества могут составлять от 0,2 масс.% до 5 масс.% таблетки, и скользящие вещества могут составлять от 0,2 масс.% до 1 масс.% таблетки.
{0051}
Таблетки также обычно содержат лубриканты (смазывающие вещества), такие как стеарат магния, стеарат кальция, стеарат цинка, стеарилфумарат натрия и смеси стеарата магния с лаурилсульфатом натрия. Лубриканты обычно составляют от 0,25 масс.% до 10 масс.%, предпочтительно от 0,5 масс.% до 3 масс.% таблетки.
Другие возможные ингредиенты включают антиоксиданты, красители, отдушки, консерванты и придающие вкус агенты.
Примеры таблеток содержат примерно до 80% лекарственного средства, примерно от 10 масс.% до примерно 90 масс.% связующего вещества, примерно от 0 масс.% до примерно 85 масс.% разбавителя, примерно от 2 масс.% до примерно 10 масс.% разрыхлителя и примерно от 0,25 масс.% до примерно 10 масс.% лубриканта.
{0052}
Смеси для таблеток можно прессовать непосредственно или вальцеванием для получения формы таблетки. Смеси для таблеток или порционные смеси альтернативно могут быть гранулированы влажными, сухими или в расплаве, в застывшем расплаве, или могут быть экструдированы перед таблетированием. Конечная лекарственная форма может содержать один или более из слоев и может быть с нанесенным покрытием или без него; она может быть даже инкапсулирована.
{0053}
Рецептурный состав таблеток обсуждается в Pharmceutical Dosage Forms: Tablets, Vol. 1, by H. Lieberman and L. Lachman (Marcel Dekker, New York, 1980). Pharmaceutical Dosage Forms: Tablets, Third Edition, Volume 2:Rational Design and Formulation, by Larry L. Augsburger and Hoag W. Stephen (Informa Healthcare, Published June 2008).
{0054}
Предназначенные для орального приема пленки для людей или для использования в ветеринарии обычно бывают водорастворимыми или набухающими в воде тонкими пленками лекарственных форм, которые могут быстро растворяться, или могут быть мукоадгезивными и обычно включают полиморфную форму в соответствии с настоящим изобретением, могут быть пленкообразующими полимерами, связующим, растворителем, увлажнителем, пластификатором, стабилизатором или эмульгатором, модифицирующим вязкость агентом и растворителем. Некоторые из компонентов таких лекарственных форм могут выполнять более одной функции.
{0055}
Полиморфная форма по настоящему изобретению может быть растворимой или нерастворимой. Водорастворимые соединения обычно могут составлять от 1 масс.% до 80 масс.%, более типично от 20 масс.% до 50 масс.% растворенного вещества. Менее растворимые соединения могут составлять более высокую долю композиции, обычно вплоть до 88 масс.% растворенного вещества. Альтернативно, полиморфная форма по настоящему изобретению может быть в форме шариков, состоящих из множества частиц.
{0056}
Пленкообразующий полимер можно выбрать из природных полисахаридов, белков или синтетических гидроколлоидов, и обычно они присутствуют в диапазоне от 0,01 до 99 масс.%, более типично в диапазоне от 30 до 80 масс.%.
{0057}
Другие возможные ингредиенты включают антиоксиданты, красители, придающие вкус вещества и усилители вкуса, консерванты, стимулирующие слюноотделение агенты, охлаждающие агенты, co-растворители (включая масла), мягчительные средства, увеличивающие объем вещества, противовспенивающие агенты, поверхностно-активные вещества и маскирующие вкус агенты.
{0058}
Пленки в соответствии с настоящим изобретением обычно получают путем сушки выпариванием тонких водных пленок, нанесенных на удаляемую поддерживающую подложку или бумагу.
{0059}
Такой способ можно осуществить в сушильном шкафу или в тоннеле, обычно в комбинированной сушилке для нанесения покрытий, или сушкой вымораживанием или вакуумированием.
{0060}
Твердые композиции для орального введения можно составить для немедленного и/или модифицированного высвобождения. Лекарственные формы с модифицированным высвобождением включают отсроченное-, пролонгированное-, импульсное-, контролируемое-, направленное и программируемое высвобождение.
{0061}
Подходящие лекарственные формы с модифицированным высвобождением для целей настоящего изобретения описаны в патенте США № 6106864. Подробности других подходящих технологий высвобождения, такие как высокоэнергетические дисперсии и осмотические частицы и частицы с нанесенным покрытием можно найти в Pharmaceutical Technology On-line, 25(2), 1-14, by Verma et al. (2001). Использование жевательной резинки для достижения контролируемого высвобождения описано в WO 00/35298.
{0062}
ПАРЕНТЕРАЛЬНОЕ ВВЕДЕНИЕ
Полиморфную форму по настоящему изобретению можно также вводить непосредственно в кровоток, в мышцы или во внутренние органы. Подходящие способы парентерального введения включают внутривенное, внутриартериальное, внутрибрюшинное, интратекальное, интравентрикулярное, интрауретральное, интрастернальное, внутричерепное, внутримышечное, интрасиновиальное и подкожное. Подходящие устройства для парентерального введения включают иглы (включая микроиглы), инжекторы, инжекторы без иголок и инфузионные методы.
{0063}
Парентеральные лекарственные формы обычно представляют собой водные растворы, которые могут содержать эксципиенты, такие как соли, углеводы и буферирующие вещества (предпочтительно с pH от 3 до 9), но для некоторых областей применения они могут быть составлены более подходящими, например, в виде стерильных неводных растворов или в виде сухих форм, предназначенных для использования вместе с подходящими носителями, такими как стерильная, не содержащая пирогенов вода.
{0064}
Получение парентеральных лекарственных форм в стерильных условиях, например, путем лиофилизации, можно легко осуществить, используя стандартные фармацевтические методы, хорошо известные специалистам в данной области.
{0065}
Лекарственные формы для парентерального введения можно составить для немедленного и/или модифицированного высвобождения. Лекарственные формы с модифицированным высвобождением включают отложенное-, пролонгированное-, импульсное-, контролируемое-, направленное и программируемое высвобождение. Таким образом, полиморфную форму по настоящему изобретению можно получить в виде суспензии или в виде твердого вещества, полутвердого вещества или тиксотропной жидкости для введения в виде имплантируемых депо, обеспечивающих модифицированное высвобождение активного соединения. Примеры таких лекарственных форм включают стенты с нанесенным лекарственным средством и полутвердые вещества и суспензии, содержащие микросферы на основе сополимера молочной и гликолевой кислоты (PLGA), заполненные лекарственным средством.
{0066}
МЕСТНОЕ ВВЕДЕНИЕ
Полиморфную форму по настоящему изобретению можно также вводить местно, (интра)дермально или трансдермально в кожу или в слизистую. Типичные лекарственные формы для таких целей включают гели, гидрогели, лосьоны, растворы, кремы, мази, тонкие порошки, повязки, пенки, пленки, кожные пластыри, прокладки, импланты, губки, волокна, бинты и микроэмульсии. Можно также использовать липосомы. Типичные носители включают спирт, воду, минеральное масло, жидкий вазелин, белый вазелин, глицерин, полиэтиленгликоль и пропиленгликоль. Могут быть включены усиливающие проницаемость вещества - см., например, J Pharm Sci, 88 (10), 955-958, by Finnin and Morgan (October 1999).
{0067}
Другие средства для местного введения включают доставку путем электропорации, ионофореза, фонофореза, сонофореза и инъекции с помощью микроиглы или без иглы (например, Powderject (торговая марка), Bioject (торговая марка) и т.д.). Местное введение можно также осуществить, используя пластыри, такие как трансдермальные ионофоретические пластыри.
{0068}
Препараты для местного введения могут быть приготовлены для немедленного и/или модифицированного высвобождения. Препараты для модифицированного высвобождения включают отложенное-, пролонгированное-, импульсное-, контролируемое-, направленное и программируемое высвобождение.
{0069}
Полиморфную форму по настоящему изобретению можно также вводить интраназально или путем ингаляции, обычно в форме сухого порошка (или отдельно, в виде смеси, например, в сухой смеси с лактозой, или в виде смешанных частиц компонентов, например, смешанных с фосфолипидами, такими как фосфатидилхолин) из сухих порошковых ингаляторов, в виде аэрозоля, распыляемого из контейнера под давлением, с помощью помпы, спрея, распылителя (предпочтительно распылителя с использованием электрогидродинамики для получения тумана из тонких частиц), или ингаляторов с использованием или без использования подходящего пропеллента, такого как 1,1,1,2-тетрафторэтан или 1,1,1,2,3,3,3-гептафторпропан, или в виде капель для носа. Для интраназального применения порошок может включать биоадгезивное вещество, например, хитозан или циклодекстрин.
{0070}
Контейнер под давлением, помпа, спрей, распылитель или аэрозольный аппарат содержат раствор или суспензию полиморфной формы в соответствии с настоящим изобретением, которые включают, например, этанол, водный этанол или подходящие альтернативные вещества для диспергирования, солюбилизации или усиления высвобождения активного вещества, пропеллент(ы) в качестве растворителя и необязательно поверхностно-активное вещество, такое как триолеат сорбитана, олеиновая кислота или олигомолочная кислота.
{0071}
Перед использованием в сухих порошковых или суспензионных композициях полученное лекарственное средство измельчают до размера, подходящего для доставки с помощью ингаляции (обычно менее 5 микрон). Это можно осуществить, используя подходящий способ измельчения, такой как размол на спиральной струйной мельнице, размол на струйной мельнице с кипящим слоем, обработку сверхкритической жидкости для получения наночастиц, гомогенизацию при высоком давлении или сушку вымораживанием.
{0072}
Можно приготовить капсулы (полученные, например, из желатина или гидроксипропилметилцеллюлозы), блистеры и картриджи для использования в ингаляторах или инсуффляторах, которые содержат порошковую смесь соединения по настоящему изобретению, подходящего порошкового основания, такого как лактоза или крахмал, и рабочего модификтора, такого как l-лейцин, маннит или стеарат магния. Лактоза может быть безводной или может быть в форме моногидрата, предпочтительно последнее. Другие подходящие эксципиенты включают декстран, глюкозу, мальтозу, сорбит, ксилит, фруктозу, сахарозу и трегалозу.
{0073}
Подходящая композиция раствора для применения в распылителе с использованием электрогидродинамики для создания тумана из тонких частиц, может содержать от 1 мкг до 20 мг соединения по настоящему изобретению на впрыскивание, и объем впрыскивания может меняться от 1 мкл до 100 мкл. Типичная композиция может включать полиморфную форму в соответствии с настоящим изобретением, пропиленгликоль, стерильную воду, этанол и хлорид натрия. Альтернативные растворители, которые можно использовать вместо пропиленгликоля, включают глицерин и полиэтиленгликоль.
{0074}
Подходящие отдушки, такие как ментол и левоментол, или подсластители, такие как сахарин или сахарин натрия, можно добавить к указанным препаратам по настоящему изобретению, предназначенным для ингаляционного/интраназального введения.
{0075}
Препараты для ингаляционного/интраназального введения можно приготовить для немедленного и/или модифицированного высвобождения, используя, например, PLGA. Препараты для модифицированного введения включают отложенное-, пролонгированное-, импульсное-, контролируемое-, направленное и программируемое высвобождение.
{0076}
В случае сухих порошковых ингаляторов и распылителей, дозированная единица определяется посредством клапана, который обеспечивает доставку отмеренного количества. Устройства в соответствии с настоящим изобретением обычно приспособлены для введения отмеренной дозы или «впрыска», содержащих от 1 мкг до 20 мг Полиморфной формы I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида L-тартрата. Общая суточная доза будет обычно находиться в диапазоне от 1 мкг до 100 мг, которые могут быть введены в виде разовой дозы или чаще в виде разделенных доз в течение дня.
{0077}
РЕКТАЛЬНОЕ/ВНУТРИВАГИНАЛЬНОЕ ВВЕДЕНИЕ
Полиморфную форму по настоящему изобретению можно вводить ректально или вагинально, например, в форме суппозитория, пессария или с помощью клизмы. Масло какао представляет собой традиционную основу суппозитория, но могут быть использованы соответствующим образом различные альтернативы.
{0078}
Препараты для ректального/вагинального введения можно приготовить для немедленного и/или для модифицированного высвобождения. Препараты для модифицированного высвобождения включают отложенное-, пролонгированное-, импульсное-, контролируемое-, направленное и программируемое высвобождение.
{0079}
ОКУЛЯРНОЕ/АУРАЛЬНОЕ ВВЕДЕНИЕ
Полиморфную форму по настоящему изобретению можно также вводить непосредственно в глаз или ухо, обычно в форме капель в микронизированной суспензии или раствора в изотоническом, pH-установленном, стерильном физиологическом растворе. Другие лекарственные формы, подходящие для введения в глаза и уши, включают мази, гели, биоразлагаемые (например, абсорбирующие гель губки, коллаген) и небиоразлагаемые (например, силиконовые) импланты, прокладки, линзы и частицы или везикулярные системы, такие как ниосомы или липосомы. Вместе с консервантом, таким как бензалконийхлорид, может быть включен полимер, такой как сшитая полиакриловая кислота, поливиниловый спирт, гиалуроновая кислота, целлюлозный полимер, например, гидроксипропилметилцеллюлоза, гидроксиэтилцеллюлоза или метилцеллюлоза, или гетерополисахаридный полимер, например, геллановая камедь. Такие лекарственные формы можно также доставлять, используя ионтофорез.
{0080}
Препараты для окулярного/аурального введения можно приготовить для немедленного и/или модифицированного высвобождения. Препараты для модифицированного высвобождения включают отложенное-, пролонгированное-, импульсное-, контролируемое-, направленное или программируемое высвобождение.
{0081}
ДРУГИЕ ТЕХНОЛОГИИ
Полиморфную форму по настоящему изобретению можно комбинировать с растворимыми макромолекулярными соединениями, такими как циклодекстрин и его подходящие производные или полимеры, содержащие полиэтиленгликоль, для улучшения их растворимости, скорости растворения, маскировки вкуса, биодоступности и/или стабильности для использования в любом из перечисленных выше способов введения.
Как обнаружено, комплексы лекарственное средство-циклодекстрин, например, обычно пригодны для большинства лекарственных форм и способов введения. Можно использовать комплексы как включения, так и невключения. В качестве альтернативы непосредственному комплексообразованию с лекарственным средством, циклодекстрин можно использовать в качестве вспомогательной добавки, т.е. в качестве носителя, разбавителя или солюбилизатора. Наиболее часто для таких целей используют альфа-, бета- и гамма-циклодекстрины, примеры которых можно найти в международных патентных публикациях WO 91/11172, WO 94/02518, WO 98/55148 и у Evrard, B., et al., Journal of Controlled Release 96 (3), pp. 403-410, 2004.
{0082}
ДОЗИРОВКИ
Для лечения или предупреждения болезненных состояний, опосредованных активностью рецепторов грелина, подходящие уровни доз полиморфной формы I по настоящему изобретению составляют примерно от 0,0001 до 1000 мг в день, предпочтительно примерно от 0,001 до 100 мг в день, более предпочтительно примерно от 0,005 до 50 мг в день и наиболее предпочтительно примерно от 1 до 50 мг в день активного соединения. Данные соединения можно вводить по схеме от 1 до 4 раз в день. В некоторых случаях, однако, можно использовать дозы вне указанных пределов.
{0083}
Такие дозы основаны на среднем человеке-пациенте с массой примерно от 60 кг до 70 кг. Врач легко сможет определить величину дозы для субъектов, масса которых выходит за указанные рамки, для таких, как дети и пожилые люди. Во избежание недоразумений, ссылки в описании на «лечение» включают ссылки на лечение, паллиативное лечение и профилактику.
{0084}
Полиморфную форму по настоящему изобретению можно также необязательно комбинировать с другим фармакологически активным соединением, или с двумя или более другими фармакологически активными соединениями, особенно для лечения болезненных состояний, опосредованных активностью рецепторов грелина. Например, полиморфную форму I по настоящему изобретению, как определено выше, можно вводить одновременно, последовательно или отдельно в комбинации с одним или более из агентов, выбранных из:
{0085}
- опиоидных анальгетиков, например, морфина, героина, гидроморфона, оксиморфона, леворфанола, леваллорфана, метадона, меперидина, фентанила, кокаина, кодеина, дигидрокодеина, оксикодона, гидрокодона, пропоксифена, налмефена, налорфина, налоксона, налтрексона, бупренорфина, буторфалона, налбуфина или пентазоцина;
{0086}
- нестероидных противовоспалительных лекарственных средств (NSAID), например, аспирина, диклофенака, дифлусинала, этодолака, фенбуфена, фенопрофена, флуфенисала, флурбипрофена, ибупрофена, индометацина, кетопрофена, кеторолака, меклофенамовой кислоты, мефенаминовой кислоты, мелоксикама, набуметона, напроксена, нимесулида, нитрофлурбипрофена, олсалазина, оксапрозина, фенилбутазона, пироксикама, сульфасалазина, сулиндака, толметина или зомепирака;
{0087}
- барбитуратных седативных соединений, например, амобарбитала, апробарбитала, бутабарбитала, бутабитала, мефобарбитала, метарбитала, метогекситала, пентобарбитала, фенобарбитала, секобарбитала, талбутала, теамилала или тиопентала;
{0088}
- бензодиазепинов, обладающих седативным действием, например, хлордиазепоксида, клоразепата, диазепама, флуразепама, лоразепама, оксазепама, темазепама или триазолама;
{0089}
- антагонистов H1, обладающих седативным действием, например, дифенгидрамина, пириламина, прометазина, хлорфенирамина или хлорциклизина;
- седативных соединений, таких как глутетимид, мепробамат, метаквалон или дихлоралфеназон;
{0090}
- релаксантов скелетных мышц, например, баклофена, карисопродола, хлорзоксазона, циклобензаприна, метокарбамола или орфенадрина;
{0091}
- антагонистов рецепторов NMDA, например, декстрометорфана ((+)-3-гидрокси-N-метилморфинан) или его метаболит декстрорфан ((+)-3-гидрокси-N-метилморфинан), кетамина, мемантина, пирролохинолина, хинина, цис-4-(фосфонометил)-2-пиперидинкарбоновой кислоты, будипина, EN-3231 (МорфиДекс (зарегистрированная торговая марка), комбинированного препарата морфина и декстрометорфана), топирамата, нерамексана или перзинфотела, включая антагонист NR2B, например, ифенпродила, траксопродила или (-)-(R)-6-{2-[4-(3-фторфенил)-4-гидрокси-1-пиперидинил]-1-гидроксиэтил-3,4-дигидро-2(1H)-хинолинона;
{0092}
- альфа-адренергетиков, например, доксазосина, тамсулосина, клонидина, гуанфацина, дексмедетомидина, модафинила или 4-амино-6,7-диметокси-2-(5-метан-сульфонамидо-1,2,3,4-тетрагидроизохинол-2-ил)-5-(2-пиридил)хиназолина;
{0093}
- трициклических антидепрессантов, например, дезипрамина, имипрамина, амитриптилина или нортриптилина;
{0094}
- противосудорожных соединений, например, карбамазепина, ламотригина, топиратмата или валпроата;
{0095}
- антагонистов тахикинина (NK), особенно антагонистов NK-3, NK-2 или NK-1, например, альфаR,9R)-7-[3,5-бис(трифторметил)бензил]-8,9,10,11-тетрагидро-9-метил-5-(4-метилфенил)-7H-[1,4]диазоцино[2,1-g][1,7]-нафтиридин-6,13-диона (TAK-637), символ "α" пишется "альфа" в данном спецификация 5-[[(2R,3S)-2-[(1R)-1-[3,5-бис(трифторметил)фенил]этокси-3-(4-фторфенил)-4-морфолинил]метил]-1,2-дигидро-3H-1,2,4-триазол-3-она (MK-869), апрепитанта, ланепитанта, дапитанта или 3-[[2-метокси-5-(трифторметокси)фенил]метиламино]-2-фенилпиперидина (2S,3S);
{0096}
- мускариновых антагонистов, например, оксибутинина, толтеродина, пропиверина, троспия хлорида, дарифенацина, солифенацина, темиверина и ипратропия;
{0097}
- селективных ингибиторов COX-2, например, целекоксиба, рофекоксиба, парекоксиба, валдекоксиба, деракоксиба, эторикоксиба или лумиракоксиба;
{0098}
- анальгетиков, являющихся производными анилина, в частности парацетамола;
{0099}
- нейролептиков, таких как дроперидол, хлорпромазин, галоперидол, перфеназин, тиоридазин, мезоридазин, трифлуоперазин, флуфеназин, клозапин, оланзапин, рисперидон, зипразидон, кветиапин, сертиндол, арипипразол, сонепипразол, блонансерин, илоперидон, пероспирон, раклоприд, зотепин, бифепрунокс, азенапин, луразидон, амисульприд, балаперидон, палиндор, эпливансерин, озанетант, римонабант, меклинертант, Мираксион (зарегистрированная торговая марка) или саризотан;
{0100}
- агонистов ванилоидных рецепторов (например, резинифератоксина) или антагонистов (например, капсазепина);
{0101}
- агонистов или антагонистов рецепторов транзиторного потенциала катионных каналов подтипа (V1, V2, V3, V4, M8, A1);
{0102}
- бета-адренергетиков, таких как пропранолол;
{0103}
- локальных анестезирующих соединений, таких как мексилетин;
{0104}
- кортикостероидов, таких как дексаметазон;
{0105}
- агонистов или антагонистов рецепторов 5-HT, особенно агонистов 5-HT1B/1D, таких как элетриптан, суматриптан, наратриптан, золмитриптан или ризатриптан;
{0106}
- антагонистов рецепторов 5-HT2A, таких как R(+)-альфа-(2,3-диметоксифенил)-1-[2-(4-фторфенилэтил)]-4-пиперидинметанол (MDL-100907);
{0107}
- холинергических (никотиновых) анальгетиков, таких как изпрониклин (TC-1734), (E)-N-метил-4-(3-пиридинил)-3-бутен-1-амин (RJR-2403), (R)-5-(2-азетидинилметокси)-2-хлорпиридин (ABT-594) или никотин;
{0108}
- трамадола (зарегистрированная торговая марка);
{0109}
- ингибиторов PDEV, таких как 5-[2-этокси-5-(4-метил-1-пиперазинил-сульфонил)фенил]-1-метил-3-н-пропил-1,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-он (силденафил), (6R,12aR)-2,3,6,7,12,12a-гексагидро-2-метил-6-(3,4-метилендиоксифенил)пиразино[2’,1’:6,1]пиридо[3,4-b]индол-1,4-дион (IC-351 или тадалафил), 2-[2-этокси-5-(4-этилпиперазин-1-ил-1-сульфонил)фенил]-5-метил-7-пропил-3H-имидазо[5,1-f][1,2,4]триазин-4-он (варденафил), 5-(5-ацетил-2-бутокси-3-пиридинил)-3-этил-2-(1-этил-3-азетидинил)-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-он, 5-(5-ацетил-2-пропокси-3-пиридинил)-3-этил-2-(1-изопропил-3-азетидинил)-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-он, 5-[2-этокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-2-[2-метоксиэтил]-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-он, 4-[(3-хлор-4-метоксибензил)амино]-2-[(2S)-2-(гидроксиметил)пирролидин-1-ил]-N-(пиримидин-2-илметил)пиримидин-5-карбоксамид, 3-(1-метил-7-оксо-3-пропил-6,7-дигидро-1H-пиразоло[4,3-d]пиримидин-5-ил)-N-[2-(1-метилпирролидин-2-ил)этил]-4-пропоксибензолсульфониламид;
{0110}
- альфа-2-дельта лигандов, таких как габапентин, прегабалин, 3-метилгабапентин, (1альфа,3альфа,5альфа)(3-аминометил-бицикло[3.2.0]гепт-3-ил)уксусная кислота, (3S,5R)-3-аминометил-5-метилгептановая кислота, (3S,5R)-3-амино-5-метилгептановая кислота, (3S,5R)-3-амино-5-метилоктановая кислота, (2S,4S)-4-(3-хлорфенокси)пролин, (2S,4S)-4-(3-фторбензил)пролин, [(1R,5R,6S)-6-(аминометил)бицикло[3.2.0]гепт-6-ил]уксусная кислота, 3-(1-аминометилциклогексилметил)-4H-[1,2,4]оксадиазол-5-он, C-[1-(1H-тетразол-5-илметил)циклогептил]метиламин, (3S,4S)-(1-аминометил-3,4-диметилциклопентил)уксусная кислота, (3S,5R)-3-аминометил-5-метилоктановая кислота, (3S,5R)-3-амино-5-метилнонановая кислота, (3S,5R)-3-амино-5-метилоктановая кислота, (3R,4R,5R)-3-амино-4,5-диметилгептановая кислота и (3R,4R,5R)-3-амино-4,5-диметилоктановая кислота;
{0111}
- каннабиноидов;
{0112}
- антагонистов метаботропных глутаматных рецепторов подтипа 1 (mGluR1);
{0113}
- ингибиторов обратного захвата серотонина, таких как сертралин, метаболит сертралина деметилсертралин, флуоксетин, норфлуоксетин (метаболит десметил флуоксетина), флувоксамин, пароксетин, циталопрам, метаболит циталопрама десметилциталопрам, эсциталопрам, d,l-фенфлурамин, фемоксетин, ифоксетин, цианодотиепин, литоксетин, дапоксетин, нефазодон, церикламин и тразодон;
{0114}
- ингибиторов обратного захвата норадреналина (норэпинефрина), таких как мапротилин, лофепрамин, миртазапин, оксапротилин, фезоламин, томоксетин, миансерин, бупроприон, метаболит бупроприона гидроксибупроприон, номифензин и вилоксазин (Вивалан (зарегистрированная торговая марка)), особенно селективных ингибиторов обратного захвата норадреналина, таких как ребоксетин, в частности (S,S)-ребоксетин;
{0115}
- двойных ингибиторов обратного захвата серотонин-норадреналина, таких как венлафаксин, метаболит венлафаксина O-десметилвенлафаксин, кломипрамин, метаболит кломипрамина десметилкломипрамин, дулоксетин, милнаципран и имипрамин;
{0116}
- ингибиторов индуцируемой синтазы оксида азота (iNOS), таких как S-[2-[(1-иминоэтил)амино]этил]-L-гомоцистеин, S-[2-[(1-иминоэтил)амино]этил]-4,4-диоксо-L-цистеин, S-[2-[(1-иминоэтил)амино]этил]-2-метил-L-цистеин, (2S,5Z)-2-амино-2-метил-7-[(1-иминоэтил)амино]-5-гептеновая кислота, 2-[[(1R,3S)-3-амино-4-гидрокси-1-(5-тиазолил)бутил]тио]-5-хлор-3-пиридинкарбонитрил; 2-[[(1R,3S)-3-амино-4-гидрокси-1-(5-тиазолил)бутил]тио]-4-хлорбензонитрил, (2S,4R)-2-амино-4-[[2-хлор-5-(трифторметил)фенил]тио]-5-тиазолбутанол, 2-[[(1R,3S)-3-амино-4-гидрокси-1-(5-тиазолил)бутил]тио]-6-(трифторметил)-3-пиридинкарбонитрил, 2-[[(1R,3S)-3-амино-4-гидрокси-1-(5-тиазолил)бутил]тио]-5-хлорбензонитрил, N-[4-[2-(3-хлорбензиламино)этил]фенил]тиофен-2-карбоксамидин или гуанидиноэтилдисульфид;
{0117}
- ингибиторов ацетилхолинэстеразы, таких как донепезил;
{0118}
- антагонистов простагландина E2 подтипа 4 (EP4), таких как N-[({2-[4-(2-этил-4,6-диметил-1H-имидазо[4,5-c]пиридин-1-ил)фенил]этил}амино)карбонил]-4-метилбензолсульфонамид или 4-[(1S)-1-({[5-хлор-2-(3-фторфенокси)пиридин-3-ил]карбонил}амино)этил]бензойная кислота;
{0119}
- антагонистов лейкотриена B4; таких как 1-(3-бифенил-4-илметил-4-гидроксихроман-7-ил)циклопентанкарбоновая кислота (CP-105696), 5-[2-(2-карбоксиэтил)-3-[6-(4-метоксифенил)-5E-гексенил]оксифенокси]валериановая кислота (ONO-4057) или DPC-11870,
{0120}
- ингибиторов 5-липоксигеназы, таких как зилеутон, 6-[(3-фтор-5-[4-метокси-3,4,5,6-тетрагидро-2H-пиран-4-ил])феноксиметил]-1-метил-2-хинолон (ZD-2138), или 2,3,5-триметил-6-(3-пиридилметил), 1,4-бензохинон (CV-6504);
{0121}
- блокаторов натриевых каналов, таких как лидокаин;
{0122}
- блокаторов кальциевых каналов, таких как зиконотид, зонисамид, мибефрадил;
{0123}
- антагонистов 5-HT3, таких как ондансетрон;
- химиотерапевтических лекарственных средств, таких как оксалиплатин, 5-фторурацил, лейковорин, паклитаксел;
- антагонистов пептида, связанного с геном кальцитонина (CGRP);
- антагонистов брадикинина (BK1 и BK2);
- блокаторов потенциалозависимых натриевых каналов (Nav1.3, Nav1.7, Nav1.8);
- блокаторов потенциалозависимых кальциевых каналов (N-тип, T-тип);
- антагонистов P2X (рецепторов ионных каналов типа ATP);
- восприимчивых к кислоте антагонистов ионных каналов (ASIC1a, ASIC3);
- антагониста ангиотензина AT2;
- антагонистов хемокинового рецептора CCR2B;
- ингибиторов катепсина (B, S, K);
- агонистов или антагонистов рецепторов сигма 1;
{0124}
и их фармацевтически приемлемых солей и сольватов.
{0125}
Такие комбинации предоставляют значительные преимущества, включая синергическую активность при лечении.
{0126}
КОМБИНАЦИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ И НАБОР
Одним из вариантов настоящего изобретения является комбинация полиморфной формы по настоящему изобретению и лекарственного средства для лечения желудочно-кишечных заболеваний, которое отличается от полиморфной формы по настоящему изобретению. «Комбинация» в соответствии с настоящим изобретением может присутствовать в виде «фиксированной комбинации» или в виде «набора частей комбинации». «Фиксированную комбинацию» определяют как комбинацию, в которой (i) по меньшей мере одно лекарственное средство для лечения желудочно-кишечных заболеваний, которое отличается от полиморфной формы по настоящему изобретению, и (ii) полиморфная форма присутствуют в виде единого целого. «Набор частей комбинации» определяют как комбинацию, в которой (i) по меньшей мере одно лекарственное средство для лечения желудочно-кишечных заболеваний, которое отличается от полиморфной формы по настоящему изобретению, и (ii) полиморфная форма присутствуют в более чем одной единичной форме. Компоненты «набора частей комбинации» можно вводить одновременно, последовательно или отдельно. Молярное отношение лекарственного средства для лечения желудочно-кишечных заболеваний, которое отличается от полиморфной формы по настоящему изобретению, к полиморфной форме, используемой в соответствии с настоящим изобретением, находится в интервале от 1:100 до 100:1, таком как от 1:50 до 50:1 или от 1:20 до 20:1, или от 1:10 до 10:1. Два лекарственных средства можно вводить отдельно в том же отношении.
{0127}
Настоящее изобретение распространяется на комбинации, включающие полиморфную форму I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида L-тартрата и один или более из терапевтических агентов, таких как перечислены выше, для одновременного, раздельного или последовательного применения для лечения, профилактики или паллиативного лечения болезненных состояний, опосредованных активностью рецепторов грелина.
{0128}
ПРИМЕРЫ
Следующий пример приводится только для сравнения.
{0129}
АНАЛИЗ
{0130}
Порошковая дифракция рентгеновских лучей (PXRD)
PXRD анализ осуществляют, используя порошковый дифрактометр рентгеновских лучей Rigaku RINT-TTR с использованием излучения источника Cu-K-альфа. Образцы можно также измерять в условиях высоких/низких температур, используя присоединение держателя образца, обеспечивающего переменную температуру. Прибор снабжен рентгеновской трубкой с точной фокусировкой. Напряжение на трубке и ток устанавливают на 50 кВ и 300 мА, соответственно. Щели расходимости и рассеивания устанавливают на 0,5° и ширину приемной щели устанавливают на 0,15 мм. Дифрагированное излучение регистрируется сцинтилляционным детектором на основе NaI. Тета-два тета непрерывно сканируют со скоростью 4°/мин (размер шага 0,02°) с 3 до 40(°) 2-тета. Для юстировки прибора используют кремниевый стандарт. Результаты собирают и анализируют, используя систему Rigaku X-ray system. Образцы для анализа готовят, помещая их в алюминиевый держатель образца, который вращается в горизонтальном направлении со скоростью 60 об/мин во время накопления результатов.
{0131}
Термогравиметрия/дифференциальный термический анализ (TG/DTA)
TG/DTA осуществляют, используя Seiko 6200R систему. Образец помещают в алюминиевый TG/DTA держатель. Каждый образец нагревают в токе азота при скорости 5°C/мин, вплоть до конечной температуры 300°C. В качестве калибровочного стандарта используют металлический индий. Приводимые значения округлены и поэтому их следует считать приблизительными.
{0132}
Дифференциальная сканирующая калориметрия (DSC)
DSC анализ осуществляют, используя прибор Mettler Toledo DSC822. Образец помещают в алюминиевый DSC тигель и тщательно регистрируют массу. Тигель закрывают крышкой с маленькими отверстиями и затем обжимают. Каждый образец нагревают в токе азота при скорости 5°C/мин, вплоть до конечной температуры 220°C. Металлический индий используют в качестве калибровочного стандарта. Приводимые значения округлены и поэтому их следует считать приблизительными.
{0133}
ИК Спектроскопия с Фурье преобразованием
Инфракрасные спектры получают на спектрофотометре Shimadzu IRPrestage-21 (FT-IR), снабженном источником луча в виде нагреваемой проволоки с черным покрытием, расщепителем луча из германия, нанесенного в виде покрытия на бромид калия (KBr), и пироэлектрическим детектором высокой чувствительности (DLATGS). Каждый спектр представляет собой 40 складываемых вместе сканирований, собранных при спектральном разрешении 4 см-1. Приготовление образца состоит в размещении диска на основе KBr, приготовленного из образца и KBr. Набор фоновых данных получают с помощью контрольного диска из KBr без образцов. Спектр Log MR (R = коэффициент отражения) получают, когда берут отношения двух этих наборов данных, сравнивая их друг с другом. Калибровку длины волны осуществляют с использованием полистирола. Полученные величины округляются, и по этой причине они должны рассматриваться как приблизительные.
{0134}
Исследования гигроскопичности с использованием анализа динамической сорбции пара (DVS)
Исследования гигроскопичности проводят, используя систему измерения поверхности Surface Measurement Systems DVS-1. Образец помещают на микровесы в прибор и контролируют изменения массы в процессе цикла сорбции/десорбции при 25°C. Одна из программ сорбции/десорбции состоит из записи сорбции от 0 до 95% относительной влажности (RH) и записи десорбции от 95 до 10% RH. Другая программа состоит из записи сорбции от 40 до 95% RH и записи десорбции от 95 до 0% RH, с последующей записью второй сорбции от 0 до 40% RH. Обе программы осуществляют при 5% инкрементах RH и образец оставляют для уравновешивания на 360 минут или до тех пор, пока не достигается равновесие на каждой стадии. В конце DVS эксперимента образец измеряют с помощью PXRD.
{0135}
Ядерный магнитный резонанс (ЯМР)
Результаты ЯМР получают на спектрометре 270 МГц (JEOL JNM-LA270) или 300 МГц (JEOL JNM-LA300), используя дейтерированный хлороформ (99,8% D) или диметилсульфоксид (99,9% D) в качестве растворителя, если не указано иное, относительно тетраметилсилана (ТМС) в качестве внутреннего стандарта, выраженные в частях на миллион (м.д.); обычно используемые сокращения представляют собой: с=синглет, д=дублет, т=триплет, кв=квартет, м=мультиплет, шир.=широкий и т.д.
{0136}
Измерения методом высокоэффективной жидкостной хроматографии (ВЭЖХ)
Данные ВЭЖХ получают с помощью ВЭЖХ системы Waters Alliance 2695 с детектором 2996 PDA, используя следующие условия:
Колонка: Inertsil ODS-3 (3 микрометра, 4,6×150 мм),
Элюент: ацетонитрил/10мМ ацетат аммония=32:68,
Детектирование: УФ на 215 нм,
Скорость потока: 1 мл/мин, и
Температура колонки: 40°C.
Обработку данных осуществляют, используя программное обеспечение Empower 2 от Waters Corporation.
{0137}
Химические символы имеют свои обычные значения; M (моль(и) на литр), л (литр(ы)), мл (миллилитр(ы)), г (грамм(ы)), мг (миллиграмм(ы)), моль (моли), ммоль (миллимоли).
{0138}
Пример 1
Получение
2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида
Это соединение синтезируют в соответствии с обычным способом, описанным в WO97/024369.
{0139}
Пример 2
Получение
2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида
Это соединение синтезируют в соответствии с обычным способом, описанным в EP-1031575.
{0140}
Пример 3
Получение
Полиморфной формы I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида L-тартрата
Смесь 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида, полученного в соответствии со способом Примера 1 (1,0 молярный эквивалент), растворяют в этилацетате. Органический слой экстрагируют очищенной водой и/или фильтруют. Добавляют раствор L-винной кислоты (1,0 молярный эквивалент) в метаноле и перемешивают. Раствор нагревают, и метанол/этилацетат удаляют посредством дистилляции. Добавляют изопропанол, и раствор нагревают с обратным холодильником с получением желаемого полиморфного преобразования. Твердые продукты выделяют, промывают и сушат в вакууме с получением соли указанного в заглавии соединения.
Использование раствора L-винной кислоты в изопропаноле вместо метанола дает такие же кристаллы, характеризуемые ниже.
т.пл. (начало плавления согласно DSC): 177oC.
Кристалличность согласно PXRD: кристаллы (Фиг.1). Главные пики при 2-Thetao: 4,4, 10,2, 12,5, 13,2, 13,7, 16,4, 16,6, 18,5, 19,3 и 21,7. Каждый пик имеет пределы ошибки +/- 0,2.
MS (FAB) m/z: 506 (M+H) + с дополнительными пиками наблюдают при m/z 421, 263 и 244.
ИК (KBr): 3349, 3107, 3036, 2983, 2870, 2770, 2526, 1705, 1662, 1625, 1531, 1454, 1442, 1220, 1132, 1109, 1089, и 704 см-1.
Анал. вычисл. для C28H35N5O4 C4H6O6: C, 58,6; H, 6,3; N, 10,7. Найдено: C, 58,6; H, 6,4; N, 10,8.
{0141}
Пример 4
[Исследование гигроскопичности]
В исследованиях гигроскопичности с помощью анализа динамической сорбции паров (DVS), Полиморфная форма I показывает хорошие результаты (<2%) относительно поглощения влажности, при относительной влажности (RH) 40%, 80% и 90% при 25oC, по сравнению с соединением, полученным в Примере 2.
{0142}
Пример 5
[Исследование стабильности]
Исследования стабильности твердого продукта осуществляют с использованием камеры с контролем температуры/влажности Nagano Science Constant LH-20-11M, LH-21-11M, LTL-200D3CJ-14 или LTX-01. Образец помещают в камеру и экспонируют при 25oC/60% RH, 40oC/75% RH и/или облучают с помощью ксеноновой лампы. Кристаллическую форму, тепловое поведение, чистоту и/или изменение массы полученного в результате образца после экспонирования или облучения оценивают с помощью XRPD, TG/DTA или DSC, HPLC, микровесов, соответственно.
Полиморфная форма I, как обнаружено, является стабильной по сравнению с соединением, полученным в Примере 2.
{0143}
Пример 6
[Исследование растворимости]
Полиморфная форма I показывает хорошую растворимость (>300 мг/мл) в водных буферных растворах при pH ниже 5.
{0144}
Пример 7
[Исследование фотостабильности]
Образцы для исследования фотостабильности хранятся в открытых чашках с крышками из кварцевого стекла, и второй набор образцов при 25oC/60% RH и 40oC/75% RH хранится в открытых круглых бутылках из стекла янтарного цвета, покрытых марлей.
В итоге, при хранении Полиморфной формы I более 3 месяцев, не обнаружено значительных изменений во внешнем виде, в картинах дифракции рентгеновского излучения и в ИК спектрах. Не наблюдается значительных потерь сильнодействия для любого из образцов для исследования стабильности в течение 3 месяцев.
| название | год | авторы | номер документа |
|---|---|---|---|
| СТИМУЛЯТОРЫ СЕКРЕЦИИ ГОРМОНА РОСТА | 1996 |
|
RU2172742C2 |
| ПРОИЗВОДНЫЕ СЕРИНА В КАЧЕСТВЕ АГОНИСТОВ ГРЕЛИНОВЫХ РЕЦЕПТОРОВ | 2015 |
|
RU2695649C2 |
| ПРОИЗВОДНЫЕ ПИРАЗОЛОПИРИДИНА В КАЧЕСТВЕ БЛОКАТОРОВ TTX-S | 2013 |
|
RU2652117C2 |
| КОНДЕНСИРОВАННОЕ ХИНОЛИНОВОЕ ПРОИЗВОДНОЕ И ЕГО ПРИМЕНЕНИЕ | 2005 |
|
RU2384571C2 |
| ПРИМЕНЕНИЕ СИГМА-ЛИГАНДОВ ОТ БОЛИ ПРИ РАКЕ КОСТЕЙ | 2011 |
|
RU2585095C2 |
| АМИДЫ КОНДЕНСИРОВАННОГО ПИПЕРИДИНА В КАЧЕСТВЕ МОДУЛЯТОРОВ ИОННЫХ КАНАЛОВ | 2014 |
|
RU2741810C2 |
| β-ЛАКТАМЫ | 1995 |
|
RU2143435C1 |
| ПРИМЕНЕНИЕ СИГМА-ЛИГАНДОВ ПРИ ИНДУЦИРОВАННОЙ ОПИОИДАМИ ГИПЕРАЛГЕЗИИ | 2011 |
|
RU2589899C2 |
| ПРОИЗВОДНЫЕ ПИРАЗОЛОПИРИДИНА | 2011 |
|
RU2561276C2 |
| ПОЛИЦИКЛИЧЕСКИЕ СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ РЕСПИРАТОРНО-СИНЦИТИАЛЬНЫХ ВИРУСНЫХ ИНФЕКЦИЙ | 2004 |
|
RU2422444C2 |
Изобретение относится к полиморфной форме I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида L-тартрата. Полиморфная форма I отличается картиной дифракции рентгеновского излучения на порошках (PXRD), полученной с помощью облучения излучением Cu-Kalpha (Cu-Ka), которая содержит главные пики при 2-Thetao 4,4, 10,2, 12,5, 13,2, 13,7, 16,4, 16,6, 18,5, 19,3 и 21,7 +/- 0,2. Также предложена фармацевтическая композиция, применение полиморфной формы I, способ лечения болезненных состояний, опосредованных активностью рецепторов грелина, и способ получения полиморфной формы I. Полиморфная форма I обладает низкой гигроскопичностью и прекрасной стабильностью. 5 н. и 4 з.п. ф-лы, 1 ил., 7 пр.
1. Полиморфная форма I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида L-тартрата, которая отличается картиной дифракции рентгеновского излучения на порошках (PXRD), полученной с помощью облучения излучением Cu-Kalpha (Cu-Ka), которая содержит главные пики при 2-Thetao 4,4, 10,2, 12,5, 13,2, 13,7, 16,4, 16,6, 18,5, 19,3 и 21,7 +/- 0,2.
2. Полиморфная форма I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида L-тартрата по п.1, которая дополнительно отличается данными дифференциальной сканирующей калориметрии (DSC), в которых она демонстрирует температуру плавления (температура начала процесса) примерно 177oC.
3. Полиморфная форма I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида L-тартрата по п.1 или 2, которая дополнительно отличается инфракрасным (ИК) спектром (KBr), который показывает полосы поглощения при 3349, 3107, 3036, 2983, 2870, 2770, 2526, 1705, 1662, 1625, 1531, 1454, 1442, 1220, 1132, 1109, 1089 и 704 +/- 2 см-1.
4. Фармацевтическая композиция для лечения болезненных состояний, опосредованных активностью рецепторов грелина, включающая полиморфную форму I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида L-тартрата по любому из пп.1-3, вместе с одним или несколькими фармацевтически приемлемыми наполнителями.
5. Полиморфная форма I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида L-тартрата по любому из пп.1-3 для применения в качестве лекарственного препарата для лечения болезненных состояний, опосредованных активностью рецепторов грелина.
6. Применение полиморфной формы I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида L-тартрата по любому из пп.1-3 или фармацевтической композиции по п.4 при приготовлении лекарственного препарата для куративного, паллиативного или профилактического лечения болезненных состояний, опосредованных активностью агониста рецепторов грелина.
7. Способ лечения болезненных состояний, опосредованных активностью рецепторов грелина, который включает введение эффективного количества полиморфной формы I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида L-тартрата по любому из пп.1-3 или фармацевтической композиции для лечения болезненных состояний, опосредованных активностью рецепторов грелина по п.4, животному, включая человека, нуждающемуся в таком лечении.
8. Способ получения полиморфной формы I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида L-тартрата по любому из пп.1-3, включающий стадию растворения 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида в органическом растворителе и смешение с L-винной кислоты в спирте.
9. Способ получения полиморфной формы I 2-амино-N-[2-(3a-(R)-бензил-2-метил-3-оксо-2,3,3a,4,6,7-гексагидро-пиразоло[4,3-c]пиридин-5-ил)-1-(R)-бензилоксиметил-2-оксо-этил]изобутирамида L-тартрата по п.8, в котором органический растворитель представляет собой этилацетат и спирт выбран из группы, состоящей из метилового спирта, этилового спирта или изопропилового спирта.
| Зажимная головка правильно-растяжной машины | 1981 |
|
SU1031575A1 |
| WO 1997024369 A1, 10.07.1997 | |||
| US 20120322821 A1, 20.12.2012 | |||
| BYRN S | |||
| et al, Pharmaceutical Solids: A Strategic Approach to Regulatory Considerations, Pharmaceutical Research, 1995, v | |||
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| СПОСОБ МНОГОКРАТНОГО РАДИОПРИЕМА | 1924 |
|
SU945A1 |
| BAVIN M., Polymorphism in process development | |||
| (crystal structure transformations), Chemistry and Industry, 1989, v | |||
| Устройство для электрической сигнализации | 1918 |
|
SU16A1 |
| Приспособление для получения световых декораций на прозрачном экране | 1920 |
|
SU527A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПИРАЗОЛПИРИДИНОВОГО ПРОИЗВОДНОГО ИЛИ ЕГО СОЛИ | 1990 |
|
RU2007403C1 |
| TOKUNAGA T | |||
| et al, Oxindole Derivatives as Orally Active Potent Growth Hormone Secretagogues, J | |||
| Med | |||
| Chem., 2001, v | |||
| Приспособление для плетения проволочного каркаса для железобетонных пустотелых камней | 1920 |
|
SU44A1 |
| Прибор для получения стереоскопических впечатлений от двух изображений различного масштаба | 1917 |
|
SU26A1 |
| РЕГИСТРАТОР ДЛЯ БУМАГ | 1926 |
|
SU4641A1 |
Авторы
Даты
2018-10-26—Публикация
2014-05-28—Подача