ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
{0001} Настоящее изобретение относится к новым производным серина, способам их получения, промежуточным соединениям, применимым в данных способах и фармацевтическим композициям, содержащим данные соединения. Кроме того, изобретение относится к применению производных серина в терапии, например, в качестве модуляторов рецепторов секретагогов гормона роста (называемых также грелиновым рецептором или рецептором GHSRIa) и/или для лечения и/или профилактики раковой анорексии/кахексии, кахексии и анорексии, вызванных приемом противораковых препаратов, гипералгезии, вызванной приемом противораковых препаратов, ХОБЛ (хронической обструктивной болезни легких)/кахексии при ХОБЛ, саркопении, нарушений пищевого поведения и неврологических нарушений пищевого поведения, подавления потери веса, восстановления в раннем послеоперационном периоде у раковых пациентов, хронической инфекции дыхательных путей, воспаления, воспалительных заболеваний кишечника (ВЗК), ФД (функциональной диспепсии), констипации, диабетического гастопареза и гастопареза, сердечной недостаточности, инфаркта миокарда, диабетической невропатии, болезни Паркинсона, рассеянного склероза, диагностики и лечения дефицита гормона роста, улучшения качества жизни (КЖ) в пожилом возрасте, нарушения перистальтики кишечника у пациентов с травмой спинного мозга, послеоперационной кишечной непроходимости и кишечной непроходимости, вызванной приемом морфина.
ПРЕДШЕСТВУЮЩАЯ ОБЛАСТЬ ТЕХНИКИ
{0002} Грелин представляет собой эндогенный лиганд рецептора секретагогов гормона роста (ГР). Изначально его выделяли из желудка, и он представляет собой пептидный гормон, состоящий из 28 аминокислот, в котором серин н-октаноилирован в 3-положении. Он обладает высокой активностью в отношении высвобождения ГР и поэтому предполагается, что он играет важную роль в поддержании высвобождения ГР и энергетического гомеостаза (NPL 1). В частности, он, по-видимому, проявляет сильное аппетит-стимулирующее действие. Далее известно, что грелиновый агонист применим для лечения и/или профилактики раковой анорексии/кахексии(NPL 2, 3 and 4), кахексии и анорексии, вызванных приемом противораковых препаратов (NPL 4 and 5), гипералгезии, вызванной приемом противораковых препаратов (NPL 5), ХОБЛ (хронической обструктивной болезни легких)/кахексии при ХОБЛ (NPL 6 and 7), саркопении (NPL 8), нарушений пищевого поведения и неврологических нарушений пищевого поведения (NPL 9), подавления потери веса (NPL 10), восстановления в раннем послеоперационном периоде у раковых пациентов (NPL 11), хронической инфекции дыхательных путей (NPL 7), воспаления (NPL 12), ВЗК (NPL 12), ФД (NPL 4), констипации (NPL 9), диабетического гастопареза и гастопареза (NPL 4 и 13), сердечной недостаточности (NPL 14, 15 т 16), инфаркта миокарда (NPL 14, 15 и 16), диабетической невропатии (NPL 17), болезни Паркинсона (NPL 18), рассеянного склероза (NPL 19), диагностики и лечения дефицита гормона роста (NPL 20), улучшения КЖ в пожилом возрасте (NPL 20), нарушения перистальтики кишечника у пациентов с травмой спинного мозга (NPL 21), послеоперационной кишечной непроходимости (NPL 4 и 22) и кишечной непроходимости, вызванной приемом морфина (NPL 22).
{Список цитирования}
{Непатентная литература}
{0003} {NPL 1} Scientifica 2013, Article ID 518909 (http://dx.doi.org/10.1155/2013/518909), 25 страниц, 2013
{NPL 2} The Oncologist 12, 594-600, 2007.
{NPL 3} Support Care Cancer 21, 2409-2415, 2013
{NPL 4} Neurogastroenterol Motil 20, 177-184, 2008
{NPL 5} Endocrinology 149, 455-460, 2008
{NPL 6} BMC Pulmonary Medicine 13, 37-46, 2013
{NPL 7} Methods in Enzymology 514, 399-407, 2012
{NPL 8} Arch Med Sci 9, 166-171, 2013
{NPL 9} Frontiers in Endocrinology 4, 1-27, 2013
{NPL 10} Ann intern Med 149, 601-611, 2008
{NPL 11} Gastric Cancer 17, 200-205, 2014
{NPL 12} Mol Nutr Food Res 52, 855-866, 2008
{NPL 13} Neurogastroenterol Motil 25, e140-e150, 2013
{NPL 14} Journal of Cardiology 59, 8-13, 2012
{NPL 15} Curr Opin Clin Nutr Metab Care 16, 619-624, 2013
{NPL 16} Endocrinology 153, 2436-2443, 2012
{NPL 17} Biochemical and Biophysical Research Communications 389, 405-408, 2009
{NPL 18} Stereotact Funct Neurosurg 90, 104-112, 2012
{NPL 19} Ir J neurol 12, 60-65, 2013
{NPL 20} Drug Discovery Today 4, 497-506, 1999
{NPL 21} Neurogastroenterol Motil 21, 71-77, 2009
{NPL 22} Peptides 26, 1598-1601, 2005
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Техническая задача
{0004} Таким образом, желательно найти новые соединения, которые модулируют активность грелинового рецептора.
Решение задачи
{0005} [1] В данном изобретении предоставлено соединение следующей формулы (I):
{0006} {Формула 1}
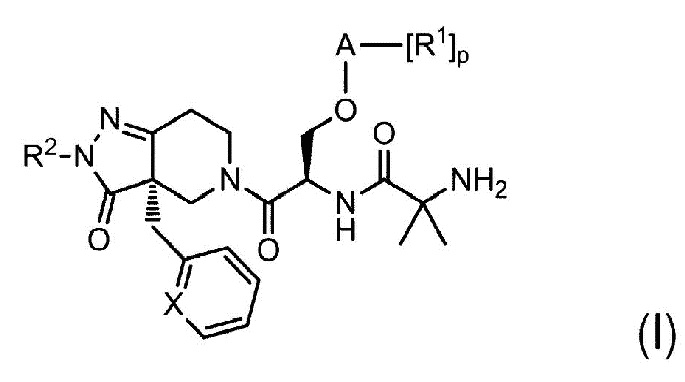 ,
,
в которой:
A представляет собой арил, предпочтительно, арил представляет собой фенил, нафтил или пиридил, более предпочтительно, арил представляет собой фенил или пиридил, наиболее предпочтительно, арил представляет собой фенил, 2-пиридил или 3-пиридил,
X представляет собой CH или N;
R1 независимо выбирают из группы, включающей в себя (1) водород, (2) галоген, (3) C1-6 алкил, где алкил является незамещенным или замещен одним или более заместителями, независимо выбранными из галогена, гидрокси, -O-C1-6 алкила, амино, C1-6 алкиламино и (C1-6 алкил)(C1-6 алкил)N-, (4) -O-C1-6 алкила, где алкил является незамещенным или замещен одним или более заместителями, независимо выбранными из галогена, гидрокси, -O-C1-6 алкила, амино, C1-6 алкиламино и (C1-6 алкил)(C1-6 алкил)N-, (5) -CN и (6) -SO2C1-6 алкила; предпочтительно, R1 независимо выбирают из группы, включающей в себя (1) водород, (2) галоген, (3) трифторметил, (4) трифторметокси и (5) -CN, более предпочтительно, R1 независимо выбирают из группы, включающей в себя (1) водород, (2) -F, (3) -Cl, (4) трифторметил, (5) трифторметокси и (6) -CN;
R2 представляет собой водород или C1-6 алкил, где алкил является незамещенным или замещен одним или более заместителями, независимо выбранными из галогена, гидрокси, -O-C1-6 алкил, амино, C1-6 алкиламино и (C1-6 алкил)(C1-6 алкил)N-, предпочтительно, R2 представляет собой C1-6 алкил, где алкил является незамещенным или содержит от одного до трех заместителей, независимо выбранных из галогена, более предпочтительно, R2 представляет собой метил или дифторэтил, наиболее предпочтительно, R2 представляет собой метил или 2,2-дифторэтил,
p равен 1, 2, 3, или 4; если p равен двум или больше двух, R1 могут быть одинаковыми или различными, предпочтительно, p равен 1 или 2;
или его фармацевтически приемлемая соль.
{0007} [2] В настоящем изобретении предоставлено соединение, представленное приведенной выше формулой (I), по пункту [1],
в котором:
A представляет собой фенил, нафтил или пиридил,
или его фармацевтически приемлемая соль.
{0008} [3] В настоящем изобретении предоставлено соединение, представленное приведенной выше формулой (I), по пункту [1] или [2],
в котором:
A представляет собой фенил, нафтил или пиридил,
R2 представляет собой водород или C1-C6 алкил, где алкил является незамещенным или содержит от одного до трех заместителей, независимо выбранных из галогена,
или его фармацевтически приемлемая соль.
{0009} [4] В настоящем изобретении предоставлено соединение, представленное приведенной выше формулой (I), по любому из пунктов с [1] по [3],
в котором:
A представляет собой фенил, нафтил или пиридил,
R1 независимо выбирают из группы, включающей в себя: (1) водород, (2) галоген, (3) трифторметил, (4) трифторметокси, (5) -CN и (6) -SO2C1-6 алкил;
R2 представляет собой C1-6 алкил, где алкил является незамещенным или содержит от одного до трех заместителей, независимо выбранных из галогена,
или его фармацевтически приемлемая соль.
{0010} [5] В настоящем изобретении предоставлено соединение, представленное приведенной выше формулой (I), по любому из пунктов с [1] по [4],
в котором:
A представляет собой фенил, нафтил или пиридил,
R1 независимо выбирают из группы, включающей в себя: (1) водород, (2) -F, (3) -Cl, (4) трифторметил, (5) трифторметокси, (6) -CN и (7) -SO2CН3,
R2 представляет собой метил или дифторэтил,
или его фармацевтически приемлемая соль.
{0011} [6] В настоящем изобретении предоставлено соединение, представленное приведенной выше формулой (I), по любому из пунктов с [1] по [5],
в котором:
A представляет собой фенил, 2-пиридил или 3-пиридил,
R1 независимо выбирают из группы, включающей в себя: (1) водород, (2) -F, (3) -Cl, (4) трифторметил, (5) трифторметокси и (6) -CN,
R2 представляет собой метил или 2,2-дифторэтил,
или его фармацевтически приемлемая соль.
{0013} [7] Подходящие индивидуальные соединения по настоящему изобретению представляют собой:
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(2,4-дифторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-феноксипропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(4-хлорфенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-хлорфенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3,5-дихлорфенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-(2-(трифторметил)фенокси)пропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3,4-дифторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(2-хлорфенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3,5-бис(трифторметил)фенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-фторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-метоксифенил)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(2-фторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(нафталин-2-илокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(нафталин-1-илокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-((5-хлорпиридин-3-ил)окси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-цианофенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-(пиридин-2-илокси)оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-((5-фторпиридин-3-ил)окси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-((6-(трифторметил)пиридин-2-ил)окси)оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(4-цианофенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-(2,2-дифторэтил)-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-феноксипропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-феноксипропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-3-(2-хлорфенокси)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(2-фторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-3-(3-хлорфенокси)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-метоксифенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-фторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид, и
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(4-фторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
или его фармацевтически приемлемая соль.
{0013} [8] Более подходящие индивидуальные соединения по настоящему изобретению представляют собой:
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(2,4-дифторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-феноксипропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3,4-дифторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-фторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-метоксифенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(2-фторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-цианофенокси)-1-оксопропан-2-ил)-2 метилпропанамид;
2-амино-N-((R)-1-((R)-2-(2,2-дифторэтил)-3-окси-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-фенкосипропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-3-(2-хлорфенокси)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(2-фторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-метоксифенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-фторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид, и
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(4-фторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
или его фармацевтически приемлемую соль.
{0014} [9] В настоящем изобретении предоставлена фармацевтическая композиция, содержащая соединение или его фармацевтически приемлемую соль, описанное в любом из пунктов с [1] по [8], и фармацевтически приемлемый носитель.
{0015} [10] В настоящем изобретении предоставлена фармацевтическая композиция по пункту [9], содержащая также другой фармакологически активный агент.
{0016} [11] В настоящем изобретении предоставлен способ лечения животного, включая человека, страдающего состоянием или нарушением, опосредованным грелиновым рецептором, который включает в себя введение указанному субъекту эффективного количества соединения формулы (I) или фармацевтически приемлемой соли по любому из пунктов с [1] по [8].
{0017} [12] В настоящем изобретении предоставлен способ по пункту [11], где указанное состояние или нарушение выбирают из группы, включающей в себя: раковую анорексию/кахексию, кахексию и анорексию, вызванные приемом противораковых препаратов, гипералгезию, вызванную приемом противораковых препаратов, ХОБЛ/кахексию при ХОБЛ, саркопению, нарушения пищевого поведения и неврологические нарушения пищевого поведения, подавление потери веса, восстановление в раннем послеоперационном периоде у раковых пациентов, хроническую инфекцию дыхательных путей, воспаление, ВЗК, ФД, констипацию, диабетический гастопарез и гастопарез, сердечную недостаточность, инфаркт миокарда, диабетическую невропатию, болезнь Паркинсона, рассеянный склероз, диагностику и лечение дефицита гормона роста, улучшение КЖ)в пожилом возрасте, нарушение перистальтики кишечника у пациентов с травмой спинного мозга, послеоперационную кишечную непроходимость и кишечную непроходимость, вызванную приемом морфина, и их сочетания.
{0018} [13] В настоящем изобретении предоставлено применение соединения, описанного в любом из пунктов с [1] по [8], или его фармацевтически приемлемая соль, или его композиция для получения лекарственного средства для лечения состояния или нарушения, опосредованного грелиновым рецептором.
{0019} [14] В настоящем изобретении предоставлено применение по пункту [13], в котором указанное состояние или нарушение выбирают из группы, включающей в себя: раковую анорексию/кахексию, кахексию и анорексию, вызванные приемом противораковых препаратов, гипералгезию, вызванную приемом противораковых препаратов, ХОБЛ/кахексию при ХОБЛ, саркопению, нарушения пищевого поведения и неврологические нарушения пищевого поведения, подавление потери веса, восстановление в раннем послеоперационном периоде у раковых пациентов, хроническую инфекцию дыхательных путей, воспаление, ВЗК, ФД, констипацию, диабетический гастопарез и гастопарез, сердечную недостаточность, инфаркт миокарда, диабетическую невропатию, болезнь Паркинсона, рассеянный склероз, диагностику и лечение дефицита гормона роста, улучшение КЖ в пожилом возрасте, нарушение перистальтики кишечника у пациентов с травмой спинного мозга, послеоперационную кишечную непроходимость и кишечную непроходимость, вызванную приемом морфина, и их сочетания.
{0020} [15] В настоящем изобретении предоставлено соединение по любому из пунктов с [1] по [8], или его фармацевтически приемлемая соль для применения при лечении состояния или нарушения, опосредованного грелиновым рецептором.
{0021} [16] В настоящем изобретении предоставлен способ получения фармацевтической композиции, включающий в себя смешивание соединения по одному из пунктов от [1] до [8] или его фармацевтически приемлемой соли с фармацевтически приемлемым носителем, разбавителем или эксципиентом.
{0022} [17] В настоящем изобретении предоставлен способ определения отклика гормона роста (ГР) натощак у находящихся в сознании мышей, включающий в себя пероральное введение тестируемых соединений мышам линии BALB/c.
{0023} [18] В настоящем изобретении предоставлен способ определения вызванной приемом цисплатина кахексии/анорексии у крыс, включающий в себя введение тестируемых соединений и цисплатина по вечерам крысам, содержащимся в хороших условиях.
{0024} [19] В настоящем изобретении предоставлен способ определения кахексии (потери массы тела и мышечной атрофии) у крыс, имеющих клетки AH-130, включающий в себя пероральное введение тестируемых соединений неполовозрелым самцам крыс, которым вводили внутрибрюшинную инъекцию более 1×108 клеток асцитной гепатомы AH-130.
ПРЕИМУЩЕСТВЕННЫЕ ЭФФЕКТЫ ИЗОБРЕТЕНИЯ
{0025} Сериновые производные по настоящему изобретению являются агонистами грелинового рецептора и имеют ряд терапевтических применений, в частности, при лечении раковой анорексии/кахексии, кахексии и анорексии, вызванных приемом противораковых препаратов, гипералгезии, вызванной приемом противораковых препаратов, ХОБЛ/кахексии при ХОБЛ, саркопении, нарушений пищевого поведения и неврологических нарушений пищевого поведения, подавления потери веса, восстановления в раннем послеоперационном периоде у раковых пациентов, хронической инфекции дыхательных путей, воспаления, ВЗК, ФД, констипации, диабетического гастопареза и гастопареза, сердечной недостаточности, инфаркта миокарда, диабетической невропатии, болезни Паркинсона, рассеянного склероза, диагностики и лечения дефицита гормона роста, улучшения КЖ в пожилом возрасте, нарушения перистальтики кишечника у пациентов с травмой спинного мозга, послеоперационной кишечной непроходимости и кишечной непроходимости, вызванной приемом морфина.
{0026} Как показано на следующей схеме I, настоящее изобретение характеризуется сериновым фрагментом в центральной части производных серина. Pfizer Inc. раскрывает агонист грелинового рецептора в WO97/24369, который считается структурно близкой областью техники. Наиболее близким соединением считается соединение примера 183 в WO97/24369, представляющее собой производное гомосерина, показанное на схеме II. Производные серина по настоящему изобретению проявляют значительно более высокую активность в отношении грелинового рецептора по сравнению с примерами с использованием гомосерина. Как показано в таблице 7 в опыте настоящего описания, исключение одного атома углерода из производного гомосерина неожиданно приводит к значительному повышению активности.
{0027} {Формула 2}
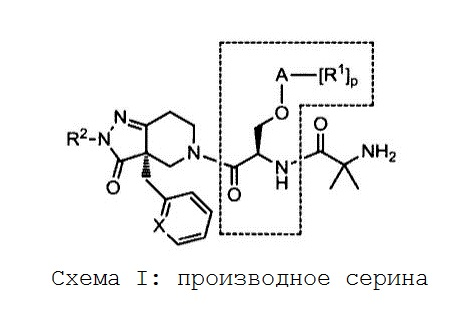
{Формула 3}
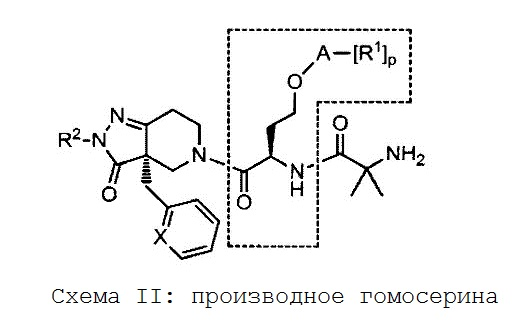
{0028} Что касается других соединений, раскрытых в данной области техники, соединения по настоящему изобретению могут проявлять меньшую токсичность, хорошую абсоробцию и распределение, хорошую растворимость, меньшее связывание с белками плазмы, меньшее межлекарственное взимодействие, высокую устойчивость к инактивации в процессе метаболизма, сниженную ингибирующую активность в отношении каналов HERG и/или удлинение укороченного интервала QT.
Описание вариантов осуществления
{0029} Специалистам в данной области техники понятно, что используемые в настоящем описании термины «галоген» или «галоид» подразумевают использование атомов фтора, хлора, брома и йода. Аналогичным образом, 1-6, как в C1-6, обозначает число, включающее в себя 1, 2, 3, 4, 5 или 6. В соответствии с данным определением, например, C1-6, как в C1-6 алкиле, обозначает алкильную группу, содержащую 1, 2, 3, 4, 5 или 6 атомов углерода. Группа, обозначенная как независимо содержащая заместители, может быть независимо замещена несколькими подобными заместителями.
{0030} Использованный в настоящем описании термин «алкил» означает линейный насыщенный одновалентный углеводородный радикал или разветвленный насыщенный одновалентный углеводородный радикал, например, метил, этил, пропил, 2-пропил, бутил (включая все изомерные формы), пентил (включая все изомерные формы) и так далее.
{0031} Использованный в настоящем описании термин «арил» означает моно- или бикарбоциклический цикл, который может содержать от 0 до 4 гетероатомов, выбранных из O, N и S, но не ограниченный фенилом, нафтилом, бензофуранилом, бензофуразанилом, бензимидазолонилом, бензоимидазолилом, бензоизотиазолилом, бензоизоксазолилом, бензотиадиазолилом, бензотиазолилом, бензоксадиазолилом, бензоксазолонилом, бензоксазолилом, бензотиофенилом, бензотриазолилом, карбазолилом, карболинилом, хроманилом, циннолинилом, 2,3-диоксоиндолилом, фуранилом, фуразанилом, фуропиридилом, фуропирролилом, имидазолилом, имидазопиразинилом, имидазопиридинилом, имидазопиримидинилом, имидазотиазолилом, индазолилом, индолазинилом, индолинилом, индолилом, изобензофуранилом, изохроманилом, изоиндолилом, изохинолилом, изоксазолопиридилом, изоксазолинилом, изоксазолилом, изотиазолилом, нафтиридинилом, оксазолинилом, оксадиазолилом, оксазолилом, оксетанилом, 2-оксоиндолилом, фталазилом, пиразолопиридилом, пиразолопиримидилом, пиразолилом, пиразинилом, пиридилом, пиримидилом, пиридазинилом, пиридопиримидинилом, пирролопиридилом, пирролилом, хиназолинилом, хинолилом, хиноксалинилом, тетразолопиридилом, тетразолилом, тиадиазолилом, тиазолилом, тиофенилом, тиенопиразинилом, тиенопиразолилом, тиенопирролилом, триазолопиримидинилом, триазолилом, 4-оксо-1,4-дигидрохинолилом, 2-оксо-1,2-дигидропиридилом, 4-оксо-1,4-дигидропиримидилом, 2-оксо-1,2-дигидрохинолилом, 4-оксо-4H-пиридо[1,2-a]пиримидилом, 4-оксо-1,4-дигидро-1,8-нафтиридилом и их N-оксидами.
{0032} Использованный в настоящем описании термин «лечение» относится к облегчению указанного состояния, исключение или ослабление симптомов данного состояния, замедление или остановку развития состояния и предупреждение или задержку рецидива состояния у ранее пораженного заболеванием пациента или субъекта.
{0033} Использованный в настоящем описании термин «вечер» относится к промежутку времени примерно от 16:00 до 24:00, предпочтительно примерно от 17:00 до 20:00.
{0034} Использованный в настоящем описании артикль единственного числа "a" или "an" относится к формам как единственного, так и множественного числа объекта, к которому он относится, если не указано иначе.
{0035} Использованный в настоящем описании термин «животное» включает в себя млекопитающего субъекта или немлекопитающего субъекта. Примеры подходящего млекопитающего субъекта могут включать в себя, без ограничения, человека, грызунов, домашних животных, домашний скот и приматов. Подходящие грызуны могут включать в себя, но не ограничены перечисленным, мышей, крыс, хомячков, песчанок и морских свинок. Подходящие домашние животные могут включать в себя, но не ограничены перечисленным, кошек, собак, кроликов и хорьков. Подходящий домашний скот может включать в себя, но не ограничен перечисленным, лошадей, козлов, овец, свиней, крупный рогатый скот, лам и альпаков. Подходящие приматы могут включать в себя, но не ограничены перечисленным, шимпанзе, лемуров, макак, мартышек, паукообразных обезьян и зеленых мартышек. Примеры подходящего немлекопитающего субъекта могут включать в себя, без ограничения, птиц, пресмыкающихся, земноводных и рыб. Неограничивающие примеры птиц включают в себя кур, индюков, уток, и гусей. Предпочтительным млекопитающим субъектом является человек.
{0036} Соли соединений по настоящему изобретению также входят в рамки изобретения. Соли соединений формулы (I) предпочтительно являются фармацевтически приемлемыми, в связи с их потенциальным применением в медицине. Подходящие фармацевтически приемлемые соли могут включать в себя кислотно-аддитивные соли. Фармацевтически приемлемую кислотно-аддитивную соль можно получить взаимодействием соединения формулы (I) с подходящей неорганической или органической кислотой (такой как бромистоводородная, хлористоводородная, йодистоводородная, серная, азотная, фосфорная, п-толуолсульфоновая, метансульфоновая или нафталинсульфоновая кислота), необязательно в подходящем растворителе, таком как органический растворитель, получая соль, которую обычно выделяют, например, кристаллизацией и фильтрованием. Примеры фармацевтически приемлемых кислотно-аддитивных солей соединения формулы (I) включают в себя соли HCI, HBr, HI, сульфатные или гидросульфатные, нитратные, фосфатные или гидрофосфатные, ацетатные, бензоатные, сукцинатные, сахаратные, фумаратные, малеатные, лактатные, цитратные, тартратные, глюконатные, камзилатные, метансульфонатные, этансульфонатные, бензолсульфонатные, п-толуолсульфонатные и памоатные соли. По поводу обзоров по подходящим фармацевтическим солям смотри Berge et al, J. Pharm, Sci, 66, 1-19, 1977; P L Gould, International Journal of Pharmaceutics, 33 (1986), 201-217; и Bighley et al, Encyclopedia of Pharmaceutical Technology, Marcel Dekker Inc, New York 1996, Volume 13, page 453-497. Другие соли, не являющиеся фармацевтически приемлемыми, например, трифторацетатная соль, могут применяться для получения соединений по настоящему изобретению, и данные соли образуют следующий аспект изобретения. В рамки изобретения входят все возможные стехиометрические и нестехиометрические формы солей соединений формулы (I).
{0037} Специалистам в области органической химии будет понятно, что многие органические соединения могут образовывать комплексы с растворителями, в которых они реагируют или из которых их осаждают или кристаллизуют. Подобные комплексы известны как «сольваты». Например, комплекс с водой известен как «гидрат». Сольваты соединения по настоящему изобретению входят в рамки данного изобретения.
{0038} Соли и сольваты, содержащие фармацевтически неприемлемые противоионы или ассоциированные растворители, входят в рамки настоящего изобретения, например, для использования в качестве промежуточных соединений для получения других соединений формулы (I) и фармацевтически приемлемых солей на их основе.
{0039} Соединения формулы (I) в кристаллической форме могут образовывать полиморфы, которые входят в рамки настоящего изобретения.
{0040} В рамки настоящего изобретения входят также так называемые «пролекарства» на основе соединений формулы (I). Таким образом, некоторые производные соединений формулы (I), сами по себе обладающие небольшой или отсутствием фармакологической активности, можно, при введении их внутрь или снаружи организма, превратить в соединения формулы (I), обладающие требуемой активностью, например, путем гидролитического расщепления или путем гидролиза. Такие производные называются «пролекарствами». Дополнительную информацию относительно применения пролекарств можно найти в Pro-drugs as Novel Delivery Systems, Vol. 14, ACS Symposium Series (T Higuchi and W Stella) и Bioreversible Carriers in Drug Design, Pergamon Press, 1987 (ed. E B Roche, American Pharmaceutical Association).
{0041} Пролекарства в соответствии с данным изобретением, например, можно получить заменой соответствующих функциональных групп, имеющихся в соединении формулы (I), на некоторые группы, которые известны специалистам в данной области как «прогруппы», как описано, например, в Design of Prodrugs H. Bundgaard (Elsevier, 1985). Некоторые примеры пролекарств в соответствии с данным изобретением включают в себя:
(i) соединения, в которых гидрокси-группу заменяют на группу, превращающуюся in vivo в гидроксильную группу, если соединение формулы (I) содержит спиртовую группу (-OH). Указанная группа, превращающаяся in vivo в гидроксильную группу, означает группу, которая способна превращаться in vivo в гидроксильную группу, например, в результате гидролиза и/или под действием фермента, например, эстеразы. Примеры указанной группы включают в себя, но не ограничены, группы сложного и простого эфиров, легко гидролизуемые in vivo. Предпочительными являются группы, замещающие атом водорода гидроксигруппы ацилоксиалкилом, 1-(алкоксикарбонилокси)алкилом, фталидилом и ацилоксиалкилоксикарбонилом, таким как пивалоилоксиметилоксикарбонил, и
(ii) в случае, когда соединение формулы (I) содержит аминогруппу, примером пролекарства является производное пирролпиридинона, полученное реакцией с подходящим галогенангидрилом кислоты или подходящим ангидридом кислоты. Особенно предпочтительным в качестве пролекарства производным пирролпиридинона является -NHCO (CH2)2OCH3, -NHCOCH(NH2)CH3 или тому подобное.
{0042} Другие примеры замещающих групп в соответствии с упомянутыми выше примерами и примерами пролекарств других типов можно найти в приведенных выше ссылках.
{0043} Кроме того, соединения формулы (I) можно вводить в виде пролекарств. В контексте настоящего описания, «пролекарство» на основе соединения формулы (I) представляет собой функционализированное производное данного соединения, которое, при введении пациенту, со временем высвобождает соединения формулы (I) in vivo. Введение соединения формулы (I) в качестве пролекарства может позволить специалисту в данной области сделать одну или более операцию из числа:
(a) модификации начала действия соединения in vivo, (b) модификации продолжительности действия соединения in vivo, (c) модификации переноса или распределения соединения in vivo, (d) модификации растворимости соединения in vivo и (e) преодоления побочного эффекта или другой сложности, с которой сталкиваются в случае данного соединения. Обычные функционализированные производные, используемые для получения пролекарств, включают в себя модификации соединения, химически или ферментативно расщепляемые in vivo. Подобные модификации, включающие в себя получение фосфатов, амидов, сложных эфиров, тиоэфиров, карбонатов и карбаматов, хорошо известные специалистам в данной области.
{0044} В некоторых соединениях формулы (I) может присутствовать один или более хиральных атомов углерода. В таких случаях соединения формулы (I) существуют в виде стереоизомеров. Настоящее изобретение включает в себя все оптические изомеры, такие как стереоизомерные формы соединений формулы (I), включая энантиомеры, диастереомеры и их смеси, такие как рацематы. Различные стереоизомерные формы можно отделить или разделить одну от другой стандартными способами, или любой данный изомер можно получить стандартным стереоселективным или асимметрическим синтезом.
{0045} Некоторые из описанных здесь соединений могут существовать в виде различных таутомерных форм, и следует понимать, что изобретение включает в себя все подобные таутомерные формы.
{0046} Настоящее изобретение включает в себя также все подходящие изотопные варианты соединения по настоящему изобретению. Изотопный вариант соединения по настоящему изобретению определяют как соединение, в котором, по меньешй мере, один атом замещен атомом с тем же атомным номером, но с атомной массой, которая отличается от атомной массы, обычно имеющейся в природе. Примеры изотопов, которые могут быть введены в соединения изобретения, включают в себя изотопы водорода, углерода, азота, кислорода, фосфора, серы, фтора и хлора, такие как 2H, 3H, 13C, 14C, 15N, 17O, 18O, 31P, 32P, 35S, 18F и 36CI, соответственно. Некоторые изотопно-замещенные варианты данного изобретения, например, содержащие такой радиоактивный изотоп, как 3H или 14C, применимы в лекарственных препаратах и/или исследованиях по распределению субстрата в тканях. Изотопы трития, т. е. 3H, и углерода-14, т. е. 14C, особенно предпочтительны вследствие простоты их получения и обнаружения. Кроме того, замещение такими изотопами, как дейтерий, т. е. 2H, может дать определенные терапевтические преимущества благодаря большей метаболической стабильности, например, увеличение периода полувыведения in vivo или пониженные требования к дозировке и, следовательно, в некоторых обстоятельствах может оказаться предпочтительным. Как правило, изотопно-замещенные варианты соединений по настоящему изобретению можно получить стандартными методами, такими как иллюстративные методы или методы, описанные в разделе «Соединения» далее, при использовании соответствующих изотопно-замещенных производных подходящих реагентов.
{0047} Таким образом, в следующем варианте осуществления настоящего изобретения предоставлены соединения формулы (I) и их фармацевтически приемлемые соли или сольваты для применения для лекарственной терапии и, в частности, для лечения нарушений, опосредованных грелиновым рецептором.
{0048} В следующем варианте осуществления настоящее изобретение направлено на способы модулирования активности грелинового рецептора для предупреждения и/или лечения нарушений, опосредованных грелиновым рецептором.
{0049} В следующем варианте осуществления в настоящем изобретении предоставлен способ лечения животного, включая человека, страдающего нарушением, опосредованным грелиновым рецептором, включающий в себя введение указанному субъекту эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли или сольвата. Подобное лечение включает в себя стадию введения терапевтически эффективного количества соединения формулы (I), включая его фармацевтически приемлемую соль или сольват. Подобное лечение может также включать в себя стадию введения терапевтически эффективного количества фармацевтической композиции, содержащей соединение формулы (I), включая его фармацевтически приемлемую соль или сольват.
{0050} В следующем варианте осуществления в настоящем изобретении предоставлено применение соединения формулы (I) или его фармацевтически приемлемой соли или сольвата для получения лекарственного препарата для лечения нарушения, опосредованного грелиновым рецептором.
{0051} Было показано, что действие эндогенного лиганда грелина на грелиновый рецептор приводит к высокой активности высвобождения гормона роста, стимуляции аппетита, стимуляции перистальтики кишечника и секреции кислоты, положительному воздействию на сердечно-сосудистую систему и непосредственному влиянию на остеогенез. Таким образом, при помощи модулятора грелинового рецептора можно добиться положительного эффекта при лечении дефицита гормона роста, пищевых расстройств, заболевания желудочно-кишечного тракта, сердечно-сосудистых заболеваний, остеопороза, старения и катаболических состояний или хронического вастинг-синдрома (Kojima and Kangawa, Nature Clinical Practice, Feb 2006, VoI. 2, No.2, 80-88). Модулятор грелинового рецептора может также дать положительный эффект при лечении нарушений сна (Brain Research, 1088 (2006) 131-140).
{0052} Конкретные нарушения, которые связаны с грелиновым рецептором и, таким образом, могут быть опосредованы грелиновым рецептором, так что модулятор грелинового рецептора может привести к положительному эффекту, включают в себя ожирение и факторы риска, связанные с ожирением, включающие в себя диабет, осложнения, связанные с диабетом, метаболический синдром, нарушения в работе сердечно-сосудистой системы (включая атеросклероз и дислипидемию).
{0053} Прочие заболевания и/или состояния, опосредованные грелиновым рецептором, включают в себя лечение состояния с дефицитом гормона роста, увеличение мышечной массы, увеличение плотности костной ткани, лечение половой дисфункции у мужчин и женщин, способствование набору массы тела, способствование поддержанию массы тела, способствование увеличению аппетита (например, способствование набору массы тела, поддержанию массы тела, или увеличению аппетита полезно для пациентов, страдающих нарушением, или получающих лечение, связанное с потерей массы тела). Примеры заболеваний или нарушений, связанных с потерей массы тела, включают в себя анорексию, булимию, раковую кахексию, СПИД, вастинг-синдром, кахексию и вастинг-синдром у ослабленных пожилых людей. Примеры методов лечения, сопровождающихся потерей массы тела, включают в себя химиотерапию, лучевую терапию, временную или постоянную иммобилизацию и диализ.
{0054} Следующие заболевания или состояния включают в себя нарушения сна, застойную сердечную недостаточность, нарушение обмена веществ, улучшение функции памяти, рак груди, рак щитовидной железы, устранение поражения ишемического нерва или повреждения мышц.
{0055} Соединения по настоящему изобретению действуют путем модулирования активности грелинового рецептора. Они способны активировать/дезактивировать данный рецептор за счет действия в качестве агониста, частичного агониста, обратного агониста, антагониста или частичного антагониста.
{0056} Пищевые расстройства включают в себя нервную анорексию (307.1), включая подтипы ограничительного типа и тип компульсивного переедания/очищения кишечника, нейрогенную булимию (307.51), включая подтипы очистительного типа и неочистительного типа, ожирение, компульсивное расстройство пищевого поведения, и неуточненное расстройство пищевого поведения (307.50) [цифры в скобках, приведенные выше после перечисленных заболеваний относятся к коду классификации в Diagnostic and Statistical Manual of Mental Disorders, 4th Edition, опубликованном Американской ассоциацией психиатров (DSM-IV) и/или International Classification of Diseases, 10th Edition (ICD-10)].
{0057} В следующем варианте осуществления изобретения в настоящем изобретении предоставлено применение соединения формулы (I) или его фармацевтически приемлемой соли или сольвата для получения лекарственного препарата для лечения расстройства пищевого поведения.
{0058} В следующем варианте осуществления изобретения в настоящем изобретении предоставлен способ лечения животного, включая человека, страдающего расстройством пищевого поведения, включающий в себя введение указанному субъекту эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли или сольвата.
{0059} Заболевания желудочно-кишечного такта включают в себя непроходимость кишечника, язвенную болезнь желудка и воспалительные заболевания кишечника, такие как болезнь Крона и неспецифический язвенный колит. Соединения по настоящему изобретению могут также применяться для лечения с целью облегчения симптомов, связанных с гастроэзофагеальным рефлюксом и/или расстройством пищеварения, с кахексией, связанной с нарушением аппетита/обмена веществ, и для лечения паралитической непроходимости кишечника или псевдонепроходимости, и состояний, связанных с констипацией, таких как синдром раздраженного кишечника с преобладанием запоров.
{0060} Сердечно-сосудистые заболевания включают в себя сердечную недостаточность и дилатационную кардиомиопатию.
{0061} Катаболические состояния или хронический вастинг-синдром можно наблюдать у пациентов в послеоперационный период, и они также включают в себя вастинг-синдром, связанный со СПИДом и раком, такой как раковая анорексия.
{0062} Хотя для терапевтического применения можно вводить терапевтически эффективное количество соединения формулы (I) или его фармацевтически приемлемой соли или сольвата в виде сырого химического вещества, можно предоставить активный ингредиент в виде фармацевтической композиции. Таким образом, в следующем варианте осуществления в изобретении предоставлена фармацевтическая композиция, содержащая соединение формулы (I) или его фармацевтически приемлемую соль или сольват, в смеси с одним или более фармацевтически приемлемыми носителями, разбавителями или эксципиентами. Носитель(носители), разбавитель(разбавители) или эксципиент(эксципиенты) должны быть приемлемыми в смысле совместимости с другими ингредиентами препарата и не причинять вреда его реципиенту. В следующем варианте осуществления в изобретении также предоставлен способ получения фармацевтической композиции, включающий в себя смешивание соединения формулы (I), или его фармацевтически приемлемой соли или сольвата, с одним или более фармацевтически приемлемыми носителями, разбавителями или эксципиентами.
{0063} Фармацевтические композиции по настоящему изобретению могут быть составлены для введения любым подходящим способом, например, пероральным (включая буккальный или сублингвальный), ректальным, назальным, местным (включая буккальный, сублингвальный или трансдермальный), вагинальным или парентеральным (включая подкожный, внутримышечный, внутривенный или внутрикожный) способом. Таким образом, фармацевтические композиции по настоящему изобретению можно составить, например, в виде таблеток, капсул, порошков, гранул, пастилок, кремов или жидких препаратов, таких как растворы или суспензии для перорального применения или стерильные растворы или суспензии для парентерального применения. Подобные фармацевтические препараты можно приготовить любым способом, известный в области фармацевтики, например, смешивая активный ингредиент с носителем(носителями) или эксципиентом(эксципиентами).
{0064} Таблетки и капсулы для перорального введения могут иметь вид однократной дозы и могут содержать стандартные эксципиенты, такие как связующие средства, например, сироп, аравийскую камедь, желатин, сорбит, трагакант или поливинилпирролидон, наполнители, например, лактозу, сахар, кукурузный крахмал, фосфат кальция, сорбит или глицин, смазывающие вещества для таблетирования, например, стеарат магния, тальк, полиэтиленгликоль или оксид кремния, разрыхлители, например, картофельный крахмал, или приемлемые увлажняющие вещества, такие как лаурилсульфат натрия. На таблетки можно нанести покрытие с использованием методов, которые хорошо известны в обычной фармацевтической практике. Жидкие препараты для перорального введения могут иметь форму, например, водных или масляных суспензий, растворов, эмульсий, сиропов или эликсиров, или могут быть представлены в виде сухого продукта для разведения водой или другим подходящим носителем перед применением. Такие жидкие препараты могут содержать стандартные добавки, такие как суспендирующие вещества, например, сорбит, метилцеллюлозу, сироп глюкозы, желатин, гидроксиэтилцеллюлозу, карбоксиэтилцеллюлозу, гель стеарата алюминия или гидрированные пищевые жиры, эмульгаторы, например, лецитин, моноолеат сорбита или аравийскую камедь, неводные носители (которые могут включать в себя пищевые масла), например, миндальное масло, жирные сложные эфиры, такие как эфиры глицерина, пропиленгликоля или этилового спирта, консерванты, например, метил- или пропил п-гидроксибензоат или сорбиновую кислоту и, при желании, стандартные вкусовые или окрашивающие агенты.
{0065} Препараты для местного применения по настоящему изобретению могут быть предоставлены, например, в виде мазей, кремов или лосьонов, глазных мазей и глазных или ушных капель, повязок с пропиткой и аэрозолей, и могут содержать соответствующие стандартные добавки, такие как консерванты, растворители, способствующие проникновению лекарственного средства, и смягчающие средства в мазях и кремах. Данные препараты могут также содержать совместимые стандартные носители, такие как основы для крема или мази, и этанол или олеиловый спирт для лосьонов. Такие носители могут составлять примерно от 1% примерно до 98% препарата. Как правило, они составляют примерно до 80% препарата.
{0066} Фармацевтические препараты, подходящие для парентерального введения, включают в себя водные и неводные стерильные растворы для инъекций, которые могут содержать антиоксиданты, буферные вещества, бактериостатические средства и растворенные вещества, придающие препарату изотоничность с кровью предполагаемого реципиента, и водные и неводные стерильные суспензии, которые могут содержать суспендирующие агенты и загустители. Препараты могут быть представлены в виде однодозовых или многодозовых контейнеров, например, запаянные ампулах или сосудах, и могут храниться в лиофилизированном состоянии, с необходимостью лишь добавить стерильный жидкий носитель, например, воду для инъекций, непосредственно перед применением. Приготовленные для немедленного приема растворы и суспензии можно приготовить из стерильных порошков, гранул и таблеток.
{0067} Фармацевтические препараты, подходящие для ректального введения, могут быть представлены в виде свечей или клизм.
{0068} Фармацевтические препараты, подходящие для назального введения, в которых носитель представляет собой твердое вещество, могут включать в себя крупнодисперсный порошок с размером частиц, например, от 20 до 500 микрон, который вводят путем вдыхания через нос, т. е. быстрой ингаляцией через носовой ход из контейнера с порошком, прижимаемого к носу. Подходящие препараты с жидким носителем для введения в виде назального спрея или назальных капель, включают в себя водные или масляные растворы активного ингредиента.
{0069} Фармацевтические препараты, подходящие для введения путем ингаляции, включают в себя мелкодисперсные порошки или аэрозоли, генерируемые при помощи различных аэрозолей, небулайзеров или инсуффляторов, распыляющих отмеренные дозы.
{0070} Фармацевтические препараты, подходящие для вагинального введения, могут быть представлены в виде суппозиториев, тампонов, гелей, паст, пен или спреевых препаратов.
{0071} Нужно понимать, что помимо упомянутых выше ингредиентов, препараты могут содержать другие вещества, обычно применяемые в данной области, с учетом типа рассматриваемого препарата.
{0072} Терапевтически эффективное количество соединения формулы (I), или его фармацевтически приемлемой соли или сольвата, будет зависеть от ряда факторов, включая, например, возраст и массу тела человека или другого животного, точного состояния, требующего лечения, и его тяжести, природы препарата и способа введения и, в конечном итоге, будет оставлено на усмотрение лечащего врача или ветеринара. Однако эффективное количество соединения формулы (I) для лечения нарушений, опосредованных грелиновым рецептором, как правило, будет составлять от 0,1 до 100 мг/кг массы тела реципиента (животного) в сутки, а обычно, от 1 до 10 мг/кг массы тела в сутки. Так, для взрослого животного массой 70 кг фактическое количество в сутки обычно составляло бы от 70 до 700 мг, и данное количество можно давать в виде разовой дозы в сутки, или, чаще всего, в виде нескольких (например, двух, трех, четырех, пяти или шести) субдоз в сутки, так что общее количество суточной дозы будет таким же. Эффективное количество его фармацевтически приемлемой соли или сольвата можно определить как долю эффективного количества самого соединения формулы (I).
{0073} Соединение формулы (I), или его фармацевтически приемлемую соль или сольват для применения в настоящем изобретении можно использовать в виде комбинации с одним или более другими терапевтическими средствами. Таким образом, в следующем варианте осуществления в изобретении предоставлена комбинация, включающая в себя соединение формулы (I), или его фармацевтически приемлемую соль или сольват, вместе с другим терапевтическим средством, которое может представлять собой, например, дополнительное средство против ожирения. Еще в одном варианте осуществления в изобретении также предоставлено применение комбинации, включающей в себя соединение формулы (I), или его фармацевтически приемлемой соли или сольвата, с дополнительным терапевтическим средством, при лечении нарушений, опосредованных грелиновым рецептором.
{0074} В случае использования соединения формулы (I), или его фармацевтически приемлемой соли или сольвата, в комбинации с одним или более прочими терапевтическими средствами, данные соединения можно вводить либо последовательно, либо одновременно любым общепринятым способом.
{0075} Комбинации, относящиеся к упомянутым выше, можно представить в виде фармацевтического препарата и, таким образом, фармацевтические препараты, содержащие определенную выше комбинацию, оптимальным образом, вместе с фармацевтически приемлемым носителем или эксципиентом, составляют еще один вариант осуществления данного изобретения. Отдельные компоненты подобных комбинаций можно вводить либо последовательно, либо одновременно в виде индивидуальных или объединенных фармацевтических препаратов.
{0076} В случае нахождения в одном и том же фармацевтическом препарате следует учитывать, что два данных соединения должны быть стабильны и совместимыми друг с другом и с другими компонентами препарата, и что они могут быть составлены в виде препарата для введения. При составлении отдельных препаратов их можно предоставить в виде любого подходящего препарата, обычно способом, который известен для подобных соединений в данной области.
{0077} При использовании соединения в комбинации со вторым терапевтическим средством, проявляющим активность против того же заболевания, доза каждого из соединений может отличаться от дозы в случае, когда данное соединение используется индивидуально. Специалисты в данной области легко определят подходящие дозы.
{0078} Соединения по настоящему изобретению можно эффективно соединить с другим фармакологически активным соединением, или с двумя или более другими фармакологически активными соединениями, в частности, для лечения воспаления, боли и урологических заболеваний или нарушений. Например, агонист грелинового рецептора, в частности, соединение формулы (I), или его пролекарство или его фармацевтически приемлемую соль или сольват, можно вводить одновременно, последовательно, или раздельно в комбинации с одним или более средствами, выбранными из:
{0079} - опиоидного анальгетика, например, морфина, героина, гидроморфона, оксиморфона, леворфанола, леваллорфана, метадона, меперидина, фентанила, кокаина, кодеина, дигидрокодеина, оксикодона, гидрокодона, пропоксифена, налмефена, налорфина, налоксона, налтрексона, бупренорфина, буторфанола, налбуфина или пентазоцина,
{0080} - нестероидного противовоспалительного лекарственного средства (NSAID), например, аспирина, диклофенака, дифлузинала, фенопрофена, флуфенизала, флурбипрофена, ибупрофена, индометацина, кетопрофена, кеторолака, меклофенамовой кислоты, мефенамовой кислоты, мелоксикама, набуметона, напроксена, нимесулида, нитрофлурбипрофена, олсалазина, оксапрозина, фенилбутазона, пироксикама, сульфасалазина, сулиндака, толметина, толметина или зомепирака,
{0081} - седативного препарата на основе барбитуратов, например, амобарбитала, апробарбитала, бутабарбитала, мефобарбитала, метарбитала, метогекситала, пентобарбитала, фенобарбитала, секобарбитала, талбутала, тиамилала или тиопентала,
{0082} - бензодиазепина, обладающего седативным действием, например, хлордиазепоксида, клоразепата, диазепама, флуразепама, лоразепама, оксазепама, оксазепама, темазепама или триазолама,
{0083} - антагониста H1, обладающего седативным действием, например, дифенгидрамина, пириламина, прометазина, хлорфенирамина или хлорциклизина,
- седативного средства, такого как глутетимид, мепробамат, метаквалон или дихлорарфеназон,
{0084} - мышечного релаксанта, например, баклофена, карисопродола, хлорзоксазона, циалобензаприна, метокарбамола или орфенадрина,
{0085} - антагониста NMDA рецептора, например, декстрометорфана ((+)-3-гидрокси-N-метилморфинан) или его метаболита декстрорфана ((+)-3-гидрокси-N-метилморфинан), кетамина, мемантина, пирролхинолинхинина, цис-4-(фосфонометил)-2-пиперидинкарбоновой кислоты, будипина, EN-3231 (MorphiDex (торговая марка), комбинированного препарата морфина и декстроморфана), топирамата, нерамаксана или перзинфотела, включая антагонист NR2B, например, ифенпродила, траксопродила или (-)-(R)-6-{2-[4-(3-фторфенил)-4-гидрокси-1-пиперидинил]-1-гидрокисэтил-3,4-дигидро-2(1H)-хинолина;
{0086} - альфа-адренергического средства, например, дозаксозина, тамсулозина, клонидина, гуанфацина, дексмедетомидина, модафинила, или 4-амино-6,7-диметокси-2-(5-метансульфонамидо-1,2,3,4-тетрагидроизохинол-2-ил)-5-(2-пиридил)хиназолина,
{0087} - трициклического антидепрессанта, например, дезипрамина, имипрамина, амитриптилина или нортриптилина,
{0088} - противосудорожного средства, например, карбамазепина, ламотригина, топиратмата или вальпроата,
{0089} - антагониста тахикининов (NK), в частности, антагониста NK-3, NK-2 или NK-1, например, альфаR,9R)-7-[3,5-бис(трифторметил)бензил]-8,9,10,11-тетрагидро-9-метил-5-(4-метилфенил)-7H-[1,4]диазоцино[2,1-g][1,7]-нафтиридин-6-13-диона (TAK-637), 5-[[(2R,3S)-2-[(1R)-1-[3,5-бис(трифторметил)фенил]этокси-3-(4-фторфенил)-4-морфолинил]-метил]-1,2-дигидро-3H-1,2,4-триазол-3-она (MK-869), апрапитанта, ланепитанта, дапитанта или 3-[[2-метокси-5-(трифторметокси)фенокси]-метиламино]-2-фенилпиперидина (2S,3S);
{0090} - мускаринового антагониста, например, оксибутинина, толтеродина, пропиверина, хлорида троспия, дарифенацина, солифенацина, темиверина и ипратропия,
{0091} - селективного ингибитора COX-2, например, целекоксиба, рофекоксиба, парекоксиба, валдекоксиба, деракоксиба, эторикоксиба или лумиракоксиба,
{0092} - анальгетика, являющегося производным анилина, в частности, парацетамолa,
{0093} - нейролептического средства, такого как дроперидол, хлорпромазин, галоперидол, перфеназин, тиоридазин, мезоридазин, трифлуоперазин, флуфеназин, клозапин, оланзапин, рисперидон, зипрасидон, кветиапин, сертиндол, арипипразол, сонепипразол, блонансерин, илоперидон, пероспирон, раклоприд, зотепин, бифепрунокс, азенапин, луразидон, амисульприд, балаперидон, палиндор, эпливансерин, озанетант, римонабант, меклинертант, мираксион (торговое название) или саризотан,
{0094} - агониста ванилоидного рецептора (например, резинифератоксин) или антагониста ванилоидного рецептора (например, капсазепин),
{0095} - агониста или антагониста катионного канала транзиторного рецепторного потенциала подтипа (V1, V2, V3, V4, M8, M2, A1);
{0096} - бета-адренергического средства, такого как пропранолол,
{0097} - анестетика местного действия, такого как мексилетин,
{0098} - кортикостероида, такого как дексаметазон,
{0099} - агониста или антагониста 5-HT-рецепторов, в частности, агониста 5-HT1B/1D, такого как элетриптан, суматриптан, наратриптан, золмитриптан или ризатриптан,
{0100} - антагониста 5-HT2A-рецепторов, такого как R(+)-альфа-(2,3-диметоксифенил)-1-[2-(4-фторфенилэтил)]-4-пиперидинметанол (MDL-100907);
{0101} - холинергического (никотического) анальгетика, такого как испрониклин (TC-1734), (E)-N-метил-4-(3-пиридинил)-3-бутен-1-амин (RJR-2403), (R)-5-(2-азетидинилметокси)-2-хлорпиридин (ABT-594) или никотин;
{0102} - трамадола (торговое название);
{0103} - ингибитора PDEV, такого как 5-[2-этокси-5-(4-метил-1-пиперазинилсульфонил)фенил]-1-метил-3-н-пропил-1,6-дигидро-7H-пиразол[4,3-d]пиримидин-7-он (силденафил), (6R,12aR)-2,3,6,7,12,12a-гексагидро-2-метил-6-(3,4-метилендиоксифенил)пиразин[2',1':6,1]пиридо[3,4-b]индол-1,4-дион (IC-351 или тадалафил), 2-[2-этокси-5-(4-этилпиперазин-1-илсульфонил)фенил]-5-метил-7-пропил-3H-имидазо[5,1-f][1,2,4]триазин-4-он (варденафил), 5-(5-ацетил-2-бутокси-3-пиридинил)-3-этил-2-(1-этил-3-азетидинил)-2,6-дигидро-7H-пиразол [4,3-d]пиримидин-7-он, 5-(5-ацетил-2-пропокси-3-пиридинил)-3-этил-2-(1-изо-3-азетидинил)-2,6-дигидро-7H-пиразол[4,3-d]пиримидин-7-он, 5-[2-этокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-2-[2-метоксиэтил]-2,6-дигидро-7H-пиразол[4,3-d]пиримидин-7-он, 4-[(3-хлор-4-метоксибензил)амино]-2-[(2S)-2-(гидроксиметил)пирролидин-1-ил]-N-(пиримидин-2-илметил)пиримидин-5-карбоксамид, 3-(1-метил-7-оксо-3-пропил-6,7-дигидро-1H-пиразол [4,3-d]пиримидин-5-ил)-N-[2-(1-метилпирролидин-2-ил)этил]-4-пропоксибензолсульфонамид,
{0104} - альфа-2-дельта лиганда, такого как габапентин, прегабалин, 3-метилгабапентин, (3-(аминометил)бицикло[3.2.0]гепт-3-ил)уксусная кислота, (3S,5R)-3-(аминометил)-5-метилгептановая кислота, (3S,5R)-3-амино-5-метилгептановая кислота, (3S,5R)-3-амино-5-метилоктановая кислота, (2S,4S)-4-(3-хлорфенокси)пролин, (2S,4S)-4-(3-фторбензил)пролин, [(1R,5R,6S)-6-(аминометил)бицикло[3.2.0]гепт-6-ил]уксусная кислота, 3-((1-(аминометил)циклогексил)метил)-4H-[1,2,4]оксадиазол-5-он, C-[1-((1H-тетразол-5-ил)метил)циклогептил]метиламин, (3S,4S)-(1-(аминометил)-3,4-диметилциклопентил)уксусная кислота, (3S,5R)-3-(аминометил)-5-метилоктановая кислота, (3S,5R)-3-амино-5-метилнонановая кислота, (3S,5R)-3-амино-5-метилоктановая кислота, (3R,4R,5R)-3-амино-4,5-диметилгептановая кислота и (3R,4R,5R)-3-амино-4,5-диметилоктановая кислота,
{0105} - каннабиноида;
{0106} - антагониста метаботропного глутаматного рецептора подтипа 1 (mGluR1);
{0107} - ингибитора обратного захвата серотонина, такого как сертралин, сертралиновый метаболит десметилсертралин, флуоксетин, норфлуоксетин (десметиловый метаболит флуоксетина), флувоксамин, пароксетин, циталопрам, метаболит циталопрама десметилциталопрам, эсциталопрам, d,l-фенфлурамин, фемоксетин, ифоксетин, фенфлурамин, фемоксетин, ифоксетин, цианодотиепин, литоксетин, дапоксетин, нефазодон, церикламин и тразодон,
{0108} - ингибитора обратного захвата норадреналина (норэпинефрина), такого как мапротилин, лофепрамин, миртазапин, оксапротилин, фезоламин, томоксетин, миансерин, бупропион, метаболит бупропиона гидроксибупропион, номифензин и вилоксазин (вивалан (торговое название)), в особенности селективного ингибитора обратного захвата норадреналина, такого как ребоксетин, в частности, (S,S)-ребоксетин;
{0109} - двойного ингибитора обратного захвата серотонина-норадреналина, такого как венлафаксин, метаболит венлафаксина O-десметилвенлафаксин, кломипрамин, метаболит кломипрамин десметилкломипрамин, дулоксетин, милнаципран и имипрамин,
{0110} - ингибитора индуцибельной синтазы оксида азота (iNOS), такого как S-[2-[(1-иминоэтил)амино]этил]-L-гомоцистеин, S-[2-[(1-иминоэтил)-амино]этил]-4,4-диоксо-L-цистеин, S-[2-[(1-иминоэтил)амино]этил]-2-метил-L-цистеин, (2S,5Z)-2-амино-2-метил-7-[(1-иминоэтил)амино]-5-гептеновая кислота, 2-[[(1R,3S)-3-амино-4- гидрокси-1-(5-тиазолил)-бутил]тио]-5-хлор-3-пиридинкарбонитрил, 2-[[(1R,3S)-3-амино-4-гидрокси-1-(5-тиазолил)бутил]тио]-4-хлорбензонитрил, (2S,4R)-2-амино-4-[[2-хлор-5-( трифторметил)фенил]тио]-5-тиазолбутанол, 2-[[(1R,3S)-3-амино-4-гидрокси-1-(5-тиазолил)бутил]тио]-6-(трифторметил)-3-пиридинкарбонитрил, 2-[[(1R,3S)-3-амино-4-гидрокси-1-(5-тиазолил)бутил]тио]-5-хлорбензонитрил, N-[4-[2-(3-хлорбензил амино)этил]фенил]тиофен-2-карбоксамидин, или гуанидинэтилдисульфид,
{0111} - ингибитора ацетилхолинэстеразы, такого как донепезил,
{0112} - антагониста простагландина E2 подтипа 4 (EP4), такого как N-[({2-[4-(2-этил-4,6-диметил-1H-имидазо[4,5-c]пиридин-1-ил)фенил]этил}амино)карбонил]-4-метилбензолсульфонамид или 4-[(1S)-1-({[5-хлор-2-(3-фторфенокси)пиридин-3-ил]карбонил} амино)этил]бензойная кислота;
{0113} - антагониста лейкотриена B4, такого как 1-(3-дифенил-4-илметил-4-гидрокси-хроман-7-ил)-циклопентанкарбоновая кислота (CP-105696), 5-[2-(2-карбоксиэтил)-3-[6-(4-метоксифенил)-5E-гексенил]оксифенокси]валериановая кислота (ONO-4057) или DPC-11870,
{0114} - ингибитора 5-липоксигеназы, такого как зилейтон, 6-[(3-фтор-5-[4-метокси-3,4,5,6-тетрагидро-2H-пиран-4-ил])фенокси-метил]-1-метил-2-хинолон (ZD-2138) или 2,3,5-триметил-6-(3-пиридилметил)-1,4-бензохинон (CV-6504);
{0115} - блокатора натриевого канала, такого как лидокаин,
{0116} - блокатора кальциевого канала, такого как зиконотид, зонизамид, мибефрадил,
{0117} - антагониста 5-HT3-рецепторов, такого как ондансетрон,
- антагониста белка, генетически связанного с кальцитонином (CGRP);
- антагониста брадикинина (BK1 и BK2);
- блокатора потенциал-зависимых натриевых каналов (Nav1.3, Nav1.7, Nav1.8);
- блокатора потенциал-зависимых кальциевых каналов (N-type, T-type);
- aнтагониста P2X (АТФ-активируемый ионный канал);
- aнтагониста кислоточувствительного ионного канала (ASIC1a, ASIC3);
- aнтагониста ангиотензина AT2;
- aнтагониста хемокинового рецептора CCR2B;
- ингибитора катепсина (B, S, K);
- агониста или aнтагониста сигма-1 рецептора;
{0118} и их фармацевтически приемлемых солей и сольватов.
{0119} В частности, терапевтическое или профилактическое средство в соответствии с настоящим изобретением можно предпочтительно использовать в комбинации с химиотерапевтическими средствами, иммунотерапевтическими средствами, диуретиками и так далее.
{0120} Примеры химиотерапевтических средств включают в себя алкилирующие агента, такие как циклофосфамид, ифосфамид, мелфалан, бусульфан, нимустин, ранимустин, темозоломид и т.д, антиметаболиты метаблоизма нуклеиновых кислот, такие как метотрексат, фторурацил, тегафур, кармофур, доксифлуридин, капецитабин, окфосфат цитарабина, гемцитабин, меркаптопурин, флударабин и т. д, протиоопухолевые антибиотики, такие как доксорубицин, пирарубицин, эпирубицин, идарубицин, митоксантрон, митомицин С, блеомицин, пепломицин и т.д, ингибиторы микротрубочек, такие как винкристин, винбластин, виндезин, винорельбин, паклитаксел, доцетаксел и т.д., лекарственные средства на основе платины, такие как цисплатин, карбоплатин, недаплатин и т.д., ингибиторы топоизомеразы, такие как иринотекан, ногитекан, этопозид и т.д. молекулярно-таргетные терапевтические средства, такие как трастузумаб, ритуксимаб, иманитиб и т.д., или тому подобное.
{0121} Примеры иммунотерапевтических средств включают в себя производные мурималдипептида, лентинан, сизофиран, убенимекс, пицибанил, крестин, интерферон, интерлейкин, колониестимулирующий фактор гранулоцитов, эритропоэтин и т.д.
{0122} Примеры диуретиков включают в себя лекарственные средства на основе производных ксантинов, такие как теобромин-натрий с салицилатом натрия, тиазидные лекарственные средства, такие как этиазид, циклопентиазид, трихлорметиазид, гидрохлортиазид, гидрофлуметиазид, бензил гидрохлортиазид, пенфлутизид, политиазид, метиклотиазид, анти-альдостероновые препараты, такие как спиронолактон, триамтерен и т.д., ингибиторы карбоангидразы, такие как ацетазоламид и т.д., хлорбензолсульфонамидные препараты, такие как хлорталидон, мефрузид, индапамид, фуросемид, азосемид и т.д., изосорбид, этакриновая кислота, пиператин, буметанид и т.д.
{0123} Такие комбинации предоставляют значительные преимущества при терапевтическом использовании, включая синергетическую активность.
{0124} Все публикации, включая, но не ограничиваясь патентами и патентными публикациями, цитированные в данном описании, включены в данное описание посредством ссылки, как если бы каждая отдельная публикация была специально и индивидуально включена в настоящее описание ссылкой во всей ее полноте.
{0125} Общие методы синтеза
{0126} В настоящей заявке используются сокращения, имеющие следующие значения:
DCM Хлористый метилен
DMA N,N-диметилацетамид
DME 1,2-диметоксиэтан
DMF N,N-диметилфорамид
DMSO Диметилсульфоксид
EDC 1-Этил-3-(3-диметиламинопропил)карбодиимида гидрохлорид
EtOAc Этилацетат
EtOH Этанол
ESI Ионизация электроспреем
HOBT 1-Гидроксибензотриазол
HBTU Гексафторфосфат O-(бензотриазол-1-ил)-N,N,N',N'-тетраметилурония
HPLC Высовоэффективная жидкостная хроматография
LC Жидкостная хроматография
LG Уходящая группа
MeCN Ацетонитрил
MeOH метанол
MГц Мегагерц
MS Масс-спектрометрия
NMR Ядерный магнитный резонанс
PG Защитная группа
T3P 2,4,6-Триоксид 2,4,6-трипропил-1,3,5,2,4,6-триокситрифосфинана
TBME Метил-трет-бутиловый эфир
TFA Трифторуксусная кислота
THF Тетрагидрофуран
TLC Тонкослойная хроматография
tR Время удерживания
UV УФ-излучение
{0127} Термин «основание» также не имеет особенного ограничения в отношении природы используемых оснований, и равным образом может использоваться любое основание, которое обычно используется в реакциях данного типа. Примеры подобных оснований включают в себя: гидроксиды щелочных металлов, такие как гидроксид лития, гидроксид натрия, гидроксид калия и гидроксид бария, фосфат калия, гидриды щелочных металлов, такие как гидрид лития, гидрид натрия и гидрид калия, алкоголяты щелочных металлов, такие как метилат натрия, этилат натрия и трет-бутилат калия, карбонаты щелочных металлов, такие как карбонат лития, карбонат натрия, карбонат калия и карбонат цезия, гидрокарбонаты щелочных металлов, такие как гидрокарбонат лития, гидрокарбонат натрия и гидрокарбонат калия, амины, такие как N-метилморфолин, триэтиламин, трипропиламин, трибутиламин, диизопропилэтиламин, N-метилпиперидин, пиридин, 4-пирролидинпиперидин, пиколин, 2,6-ди(трет-бутил)-4-метилпиридин, хинолин, N,N-диметиланилин, N,N-диэтиланилин, 1,5-диазабицикло[4.3.0]нон-5-ен (DBN), 1,4-диазабицикло[2.2.2]октан (DABCO), 1,8-диазабицикло[5.4.0]ундец-7-ен (DBU), лутидин и коллидин, амиды щелочных металлов, такие как амид лития, амид натрия, амид калия, диизопропиламид лития, диизопропиламид калия, диизопропиламид натрия, бис(триметилсилил)амид лития и бис(триметилсилил)амид калия. Из числа указанных оснований предпочтительными являются диизопропилэтиламин, DBU, DBN, DABCO, пиридин, лутидин, коллидин, карбонат натрия, гидрокарбонат натрия, гидроксид натрия, карбонат калия, гидрокарбонат калия, гидроксид калия, гидроксид бария, фосфат калия и карбонат цезия.
{0128} Реакции хорошо и предпочтительно протекают в присутствии инертного растворителя. В отношении природы используемого растворителя нет особого ограничения, при условии, что он не оказывает неблагоприятного воздействия на реакцию или на участвующие реагенты, и что он способен растворять реагенты, по меньшей мере, в некоторой степени. Примеры подходящих растворителей включают в себя, но не ограничиваются перечисленным: галогенсодержащие углеводороды, такие как хлористый метилен, хлороформ, четыреххлористый углерод и дихлорэтан, простые эфиры, такие как диэтиловый эфир, диизопропиловый эфир, ТГФ и диоксан, ароматические углероводороды, такие как бензол, толуол и нитробензол, амиды, такие как ДМФА, N,N-диметилацетамид (DMA) и гексаметилфосфортриамид, амины, такие как N-метилморфолин, триэтиламин, трипропиламин, трибутиламин, диизопропилэтиламин, N-метилпиперидин, пиридин, 4-пирролидинпиперидин, N,N-диметиланилин и N,N-диэтиланилин, спирты, такие как метанол, этанол, пропанол, изопропанол и бутанол, нитрилы, такие как ацетонитрил и бензонитрил, сульфоксиды, такие как диметилсульфоксид (ДМСО) и сульфолан, кетоны, такие как ацетон и диэтилкетон. Из указанных растворителей предпочтительными являются ДМФА, DMA, ДМСО, ТГФ, диэтиловый эфир, диизопропиловый эфир, диметоксиэтан, ацетонитрил, хлористый метилен, дихлорэтан и хлороформ, но не ограничиваясь перечисленным.
Примеры
{0129} Настоящее изобретение иллюстрировано следующими неограничивающими примерами, в которых, если не указано иначе: все реагенты являются коммерчески доступными, все манипуляции проводили при комнатной температуре или температуре окружающей среды, то есть примерно в интервале 18-25°C, выпаривание растворителя проводили на роторном испарителе при пониженном давлении, при температуре бани примерно до 60°C, мониторинг протекания реакций осуществляли методом тонкослойной хроматографии (ТСХ) или ЖХ-МС (масс-спектр низкого разрешения) и продолжительность реакции приведена только в целях иллюстрации, структуру и чистоту всех выделенных соединения подтверждали, по меньшей мере, одним из следующих методов: ТСХ (пластины для ТСХ с предварительно нанесенным силикагелем Merck 60 F254 или пластины для ВЭТСХ с предварительно нанесенным силикагелем Merck NH2 F254), масс-спектрометрия или ЯМР. Выходы приведены лишь с целью иллюстрации. Колоночную флэш-хроматографию проводили с использованием Wakogel (зарестрированная торговая марка) C-300HGT или Fuji Silysia Chromatorex (зарестрированная торговая марка) DM2035 (амино-тип, 30-50 микрометров) или силикагеля Biotage (32-63 мм, KP-Sil) или силикагеля, модифицированный аминогруппами, Biotage (35-75 мм, KP-NH). Данные масс-спектров низкого разрешения (ESI) получали при использовании следующего прибора:
{0130} Прибор; Waters Alliance 2695 с системой ВЭЖХ с детектором UV2487 и масс-спектрометр ZQ2000
{0131} Очистку соединений методом ВЭЖХ (препаративной ЖХ-МС) осуществляли с использованием следующего прибора и условий.
{0132} Прибор: Waters MS-trigger с системой автоочистки
Колонка: Waters XBridge C18, 19×50 мм, размер частиц 5 микрометров.
Условие A: Метанол или ацетонитрил/0,05% (об./об.) водного раствора аммиака
Условие B: Метанол или ацетонитрил Acetonitrile/0,05% (об./об.) водного раствора муравьиной кислоты
Условия для определения времени удерживания для ВЭЖХ:
{0133} Метод: QC1
Прибор: Waters ACQUITY Ultra Performance LC с детектором TUV и масс-спектрометром ZQ2000
Колонка: Waters ACQUITY C18, 2,1×100 мм, размер частиц 1,7 микрометров
Температура колонки: 60°C
Скорость ввода: 0,7 мл/мин
Время анализа: 3 мин
UV детектирование: 210 нм
MS детектирование: ESI положительный/отрицательный режим
Подвижные фазы:
A1: 10 мМ ацетата аммония
B1: Ацетонитрил
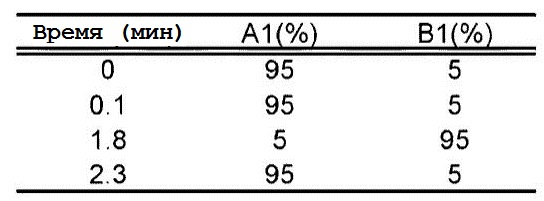
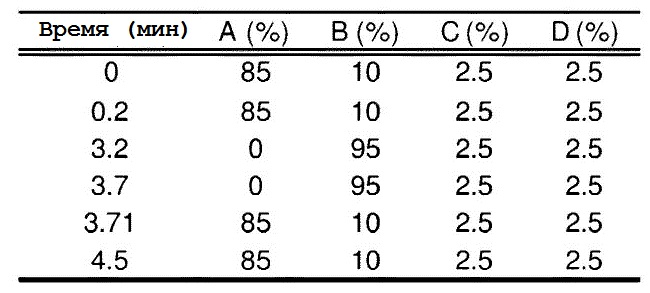
Таблица 1. Программа градиента:
{Таблица 1}
{0134} Прибор: QC2
Прибор: Система ВЭЖХ Waters Alliance2795 с детектором 2996PDA и масс-спектрометром ZQ2000
Колонка: XBridge C18, 4,6×50 мм, размер частиц 3,5 микрометров.
Температура колонки: 45°C
Скорость ввода: 1,2 мл/мин
Время анализа: 4,5 мин
УФ-детектирование: 210-400 нм (интервал сканирования)
МС-детектирование: ESI положительный/отрицательный режим
Подвижные фазы:
A: Вода
B: Ацетонитрил
C: 1% водный раствор муравьиной кислоты
D: 1% водный раствор аммиака
Таблица 2. Программа градиента:
{Таблица 2}
{0135} Оценку оптической чистоты проводили на следующем приборе и в условиях:
Прибор: Система ВЭЖХ Waters Alliance2695 с детектором 2996PDA
Колонка: DAICEL CHIRALCEL OD-H, 4,6×250 мм, размер частиц 5 микрометров
Температура колонки: 25°C (комнатная температура)
Подвижная фаза: н-Гексан/2-пропанол/диэтиламин=90/10/0,1 (об./об./об.)
Скорость ввода: 1 мл/мин
Время анализа: 30 мин
Температура автоматического дозатора: 5°C
УФ-детектирование: 259 нм
{0136} Спектры ЯМР регистрировали при частоте 270 МГц (спектрометр JEOL JNM-LA 270) или 300 МГц (JEOL JNM-LA300) с использованием в качестве растворителя дейтерированного хлороформа (99,8% D) или диметилсульфоксида (99,9% D), если не указано иначе, относительно тетраметилсилана (ТМС) в качестве внутреннего стандарта, в миллионных долях (м.д.), при этом используются стандартные сокращения: с=синглет, д=дублет, т=триплет, кв=квартет, м=мультиплет, уш=уширенный, и т.д. Химические символы имеют свое обычное значение: M (моль на литр), л (литр(ы)), мл (миллилитр(ы)), г (грамм), мг (миллиграмм), моль, ммоль (миллимоль).
Название каждому из полученных соединений обычно дают при помощи программы ChemBioDraw (Ultra, version 12.0, CambridgeSoft).
{0137} Все производные серина формулы (I) можно получить по методикам, описанным в представленных далее общих методах, или конкретными способами, описанными в разделе примеров и в разделе получение, или при помощи их обычной модификации. Настоящее изобретение также включает в себя любой или любые данные способы получения производных серина формулы (I), а также любых новых промежуточных соединений, использованных в настоящем изобретении.
{0138} В следующих общих методах используются такие же дескрипторы, как и определенные ранее для производных серина формулы (I), если не указано иначе.
{0139} {Формула 4}
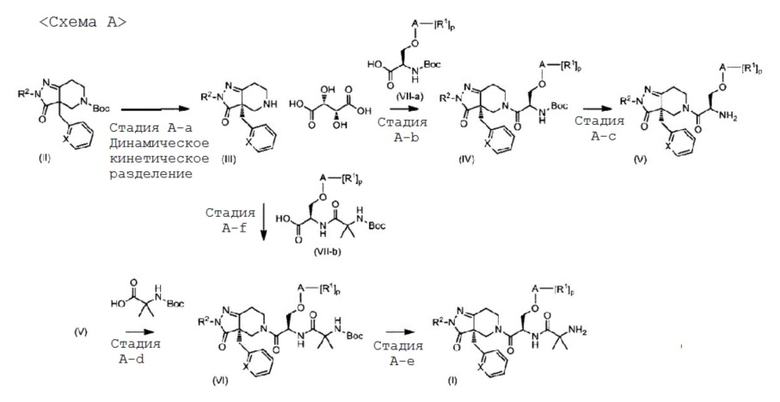
{0140} На стадии A-a соединение формулы (III) можно получить из соединения формулы (II) путем удаления защиты с последующим динамическим кинетическим разделением соответствующей соли. Удаление защиты можно осуществить обычными методами, которые известны спеицалистам в данной области (типичные амино-защитные группы описаны в "Protective Groups in Organic Synthesis Forth Edition" под редакцией T. W. Greene et al. (John Wiley & Sons, 2007)). Кроме того, соединение с удаленной защитой можно перевести в энантиомерно чистую соль путем динамического кинетического разделения с энантиомерно чистой кислотой, без ограничения, такой как D-винная кислота, с использованием подходящего растворителя. Примеры подходящего растворителя включают в себя такие растворители, как DCM (хлористый метилен), ацетон, EtOAc, ТГФ и вода. Динамическое кинетическое разделение можно провести при температуре примерно от 0 до 150°C, более предпочтительно, примерно от 20 до 100°C. Динамическое кинетическое разделение можно провести, как правило, в течение примерно от 1 ч до 48 ч.
{0141} На стадии A-b соединение формулы (IV) можно получить из соединения формулы (III) амидированием с использованием соединения формулы (VII-a) при помощи подходящего конденсируюшего реагента, без ограничения, такого как T3P, HBTU и EDC-HOBT. Конденсацию можно предпочтительно осуществлять в присутствии основания, такого как триэтиламин и N,N-диизопропилэтиламин в подходящем растворителе, таком как EtOAc, ТГФ, ДМФА, DMA и DCM при температуре примерно от -70 до 60°C в течение примерно 1-24 часов.
{0142} На стадии A-c соединение формулы (V) можно получить из соединения формулы (IV) путем удаления защиты. Удаление защиты можно осуществить обычными методами, которые известны в данной области (типичные амино-защитные группы описаны в "Protective Groups in Organic Synthesis Forth Edition" под редакцией T. W. Greene et al. (John Wiley & Sons, 2007)).
{0143} На стадии A-d соединение формулы (VI) можно получить из соединения формулы (V) амидированием с использованием 2-((трет-бутоксикарбонил)амино)-2-метилпропановой кислоты при помощи подходящего конденсируюшего реагента, без ограничения, такого как T3P, HBTU и EDC-HOBT. Конденсацию можно предпочтительно осуществлять в присутствии основания, такого как триэтиламин и N,N-диизопропилэтиламин в подходящем растворителе, таком как EtOAc, ТГФ, ДМФА, DMA и DCM при температуре примерно от 0 до 60°C в течение примерно 1-24 часов.
{0144} На стадии A-e соединение формулы (I) можно получить из соединения формулы (VI) путем удаления защиты. Удаление защиты можно осуществить обычными методами, которые известны в данной области (типичные амино-защитные группы описаны в "Protective Groups in Organic Synthesis Forth Edition" под редакцией T. W. Greene et al. (John Wiley & Sons, 2007)).
{0145} На стадии A-f соединение формулы (VI) можно получить из соединения формулы (III) амидированием с использованием соединения формулы (VII-b) при помощи подходящего конденсируюшего реагента, без ограничения, такого как T3P, HBTU и EDC-HOBT. Конденсацию можно предпочтительно осуществлять в присутствии основания, такого как триэтиламин и N,N-диизопропилэтиламин в подходящем растворителе, таком как EtOAc, ТГФ, ДМФА, DMA и DCM при температуре примерно от -40 до 60°C в течение примерно 1-24 часов.
{0146} {Формула 5}
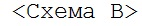
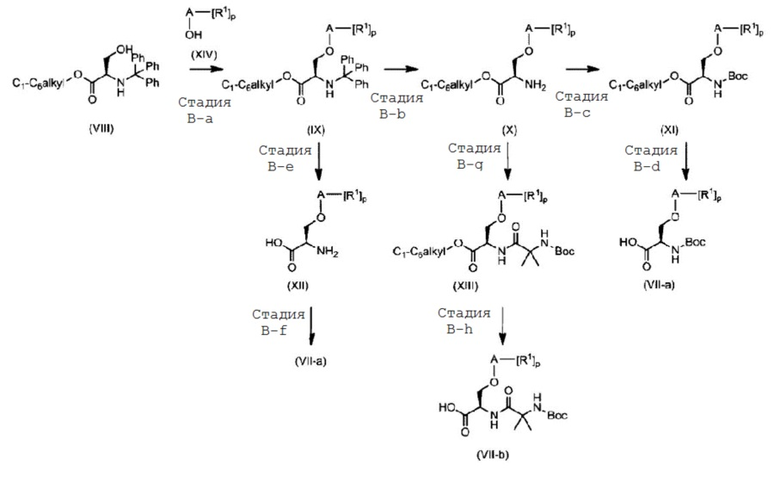
{0147} На стадии B-a соединение формулы (IX) можно получить из соединения формулы (VIII) реакцией Мицунобу с соединением формулы (XIV). Реакцию Мицунобу можно провести в органическом растоврителе в присутствии азодикарбоксилата, включающего в себя, но не ограничиваясь перечисленым, диэтилазодикарбоксилат, диизопропилазодикарбоксилат, ди-трет-бутилазодикарбоксилат и бис(2-метоксиэтил)азодикарбоксилат, в качестве реагента сочетания, а также в присутствии подходящего восстановителя, включающего в себя, но без ограничения, трифенилфосфин в инертном органическом растворителе. Примеры подходящего инертного органического растворителя включают в себя такие растворители, как ТГФ, 1,4-диоксан, MeCN, TBME и толуол. Реакцию можно проводить при температуре примерно от -20 до 150°C, более предпочтительно, примерно от 0 до 60°C. Продолжительность реакции составляет примерно от 30 минут до 48 часов, более предпочтительно, примерно от 30 минут до 24 часов.
{0148} На стадии B-b соединение формулы (X) можно получить из соединения формулы (IX) путем удаления защиты. Удаление защиты можно осуществить обычными методами, которые известны в данной области (типичные амино-защитные группы описаны в "Protective Groups in Organic Synthesis Forth Edition" под редакцией T. W. Greene et al. (John Wiley & Sons, 2007)).
{0149} На стадии B-с соединение формулы (XI) можно получить из соединения формулы (X) путем защиты аминогруппы. Защиту можно ввести обычными методами, которые известны в данной области (типичные амино-защитные группы описаны в "Protective Groups in Organic Synthesis Forth Edition" под редакцией T. W. Greene et al. (John Wiley & Sons, 2007)).
{0150} На стадии B-d соединение формулы (VII-a) можно получить гидролизом соединения сложного эфира формулы (XI). Гидролиз можно осуществить при помощи стандартных методик. По обычной методике, гидролиз проводят в основных условиях, например, в присутствии гидроксида натрия, гидроксида калия или гидроксида лития. Подходящие растворители включают в себя, но не ограничиваются перечисленным, воду, метанол, этанол, пропанол, бутанол, 2-метоксиэтанол, этиленгликоль, ТГФ, DME, 1,4-диоксан, ДМФА и DMA. Реакцию можно проводить при температуре примерно от 20 до 100°C в течение примерно от 10 мин до 24 ч.
{0151} На стадии B-e соединение формулы (XII) можно получить обработкой в кислых условиях. По обычной методике реакцию можно провести в кислых условиях, например, в присутствии хлористоводородной кислоты, бромистоводородной кислоты. Подходящие растворители включают в себя, но не ограничиваются перечисленным, воду, 1,4-диоксан, ТГФ, MeCN. Реакцию можно проводить при температуре примерно от 50 до 120°C в течение примерно от 1 ч до 24 ч.
{0152} На стадии B-f соединение формулы (VII-a) можно получить из соединения формулы (XII) путем защиты аминогруппы. Защиту можно ввести обычными методами, которые известны в данной области (типичные амино-защитные группы описаны в "Protective Groups in Organic Synthesis Forth Edition" под редакцией T. W. Greene et al. (John Wiley & Sons, 2007)).
{0153} На стадии B-g соединение формулы (XIII) можно получить из соединения формулы (X) путем защиты аминогруппы. Защиту можно ввести обычными методами, которые известны в данной области (типичные амино-защитные группы описаны в "Protective Groups in Organic Synthesis Forth Edition" под редакцией T. W. Greene et al.
{0154} На стадии B-h соединение формулы (VII-b) можно получить гидролизом соединения сложного эфира формулы (XIII). Гидролиз можно осуществить по стандартным методикам. По обычной методике, гидролиз проводят в основных условиях, например, в присутствии гидроксида натрия, гидроксида калия или гидроксида лития. Подходящие растворители включают в себя, но не ограничиваются перечисленным, воду, метанол, этанол, пропанол, бутанол, 2-метоксиэтанол, этиленгликоль, ТГФ, DME, 1,4-диоксан, ДМФА и DMA. Реакцию можно проводить при температуре примерно от 20 до 100°C в течение примерно от 10 мин до 24 ч.
{0155} {Формула 6}
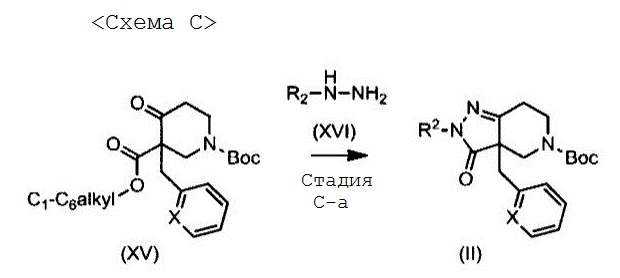
{0156} На стадии C-a соединение формулы (II) можно получить из соединения формулы (XV) путем образования in situ гидразона с соединением формулы (XVI) с последующим замыканием цикла. Реакцию можно проводить в присутствии ацетата металла, включающего в себя, без ограничения, ацетат натрия, ацетат калия и ацетат лития. Подходящие растворители включают в себя, но не ограничиваются перечисленным, метанол, этанол, пропанол, бутанол, 2-метоксиэтанол, этиленгликоль, ТГФ, DME и 1,4-диоксан. Реакцию можно проводить при температуре примерно от 50 до 150°C в течение примерно от 1 ч до 48 ч.
{0157} Все исходные вещества в следующих общих синтезах могут быть коммерчески доступными или получаться стандартными способами, известными специалистам в данной области, которые описаны далее в части синтеза промежуточных соединений.
{0158} Синтез ядра
Соединения ядра получают следующим образом. Названия и структуры соединения ядра представлены в таблице 3.
{0159} Ядро 1: 3a-Бензил-2-(2,2-дифторэтил)-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она 2,2,2-трифторацетат
{0160} Стадия 1: Трет-бутил 3a-бензил-2-(2,2-дифторэтил)-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-карбоксилат
Смесь 1-трет-бутил 3-метил 3-бензил-4-оксопиперидин-1,3-дикарбоксилата (2,4 г, 7,0 ммоль), гидрохлорида (2,2-дифторэтил)гидразина (930 мг, 7,0 ммоль) и ацетата натрия (2,3 г, 28 ммоль) в EtOH (40 мл) перемешивали в течение 24 ч при температуре кипения. После охлаждения до комнатной температуры смесь концентрировали в вакууме. Остаток разбавляли EtOAc (80 мл). Разбавленную смесь промывали водой и сушили над Na2SO4. После фильтрования фильтрат концентрировали в вакууме. Остаток очищали колоночной хроматографией (силикагель, элюирование 25% EtOAc в гексане), получая указанное в заголовке соединение в виде твердого вещества белого цвета (1,8 г, выход 65%).
MS (ESI) m/z: 394 (M+H) +
{0161} Стадия 2: 3a-Бензил-2-(2,2-дифторэтил)-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она 2,2,2-трифторацетат
К раствору трет-бутил 3a-бензил-2-(2,2-дифторэтил)-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-карбоксилата (100 мг, 0,25 ммоль) в DCM (3 мл) прибавляли трифторуксусную кислоту (2 мл) при 0°C, и перемешивали смесь в течение 1 ч при той же температуре. Смесь концентрировали в вакууме, получая указанное в заголовке соединение в виде смолы светло-желтого цвета (104 мг, выход >99%).
MS (ESI) m/z: 294 (M+H) +, 292 (M-H) -
{0162} Ядро 2: (2S,3S)-2,3-Дигидроксисукцинат (R)-2-(2,2-дифторэтил)-3a-(пиридин-2-илметил)-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она
{0163} Стадия 1: Трет-бутил 2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-карбоксилат
Указанное в заголовке соединение получали с выходом 87% (3600 мг, смола светло-фиолетового цвета) из 1-трет-бутил 3-метил 4-оксо-3-(пиридин-2-илметил)пиперидин-1,3-дикарбоксилата (3700 мг, 11 ммоль) по аналогии со стадией 1 ядра 1.
ЯМР 1H (270 МГц, CDCl3) дельта 8,38 (1H, д, J=3.9 Гц), 7,58-7,50 (1H, м), 7,13-7,05 (2H, м), 5,94-5,30 (1H, м), 4,75-4,40 (2H, уш.), 4,10-3,76 (2H, м), 3,42-3,26 (2H, м), 2,93-2,50 (4H, м), 1,53 (9H, с).
MS (ESI) m/z: 395 (M+H) +.
{0164} Стадия 2: (R)-2-(2,2-Дифторэтил)-3a-(пиридин-2-илметил)-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-он
Раствор требутил 2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-карбоксилата (4,9 г, 13 ммоль, рацемический) в DCM (50 мл) охлаждали до 0°C и медленно прибавляли трифторуксусную кислоту (4,1 мл). Смесь перемешивали при комнатной температуре в течение 1,5 ч, а затем охлаждали до 0°C. К полученной суспензии прибавляли триэтиламин (9,6 мл, 69 ммоль) при той же температуре. Полученный желтый прозрачный раствор разбавляли DCM (50 мл), промывали насыщенным раствором соли (30 мл x 3), сушили над Na2SO4, фильтровали и концентрировали в вакууме, получая указанное в заголовке соединение в виде масла коричневого цвета (3,8 г, выход >100%).
MS (ESI) m/z: 295 (M+H) +.
ЯМР 1H (270 МГц, CDCl3) дельта 8.41 (1H, д, J=5,9 Гц), 7,58-7,51 (1H, м), 7,14-7,06 (2H, м), 5,76 (1H, тт, J=55,7 Гц, 4,6 Гц), 4,16-3,72 (2H, м), 3,53-3,32 (4H, м), 2,74-2,52 (4H, м). Сигнал NH не наблюдался.
MS (ESI) m/z: 295 (M+H) +.
{0165} Стадия 3: (2S,3S)-2,3-Дигидросукцинат (R)-2-(2,2-дифторэтил)-3a-(пиридин-2-илметил)-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она
(R)-2-(2,2-Дифторэтил)-3a-(пиридин-2-илметил)-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-он (прибл. 12,5 ммоль) растворяли в DCM (6 мл) и ацетоне (20 мл). К смеси прибавляли раствор D-винной кислоты (2,07 г, 13,8 ммоль) в смеси ацетон-вода (7:3, 10 мл) при комнатной температуре. Смесь мгновенно превращалась в белую суспензию. Снова добавляли ацетон (10 мл), чтобы облегчить перемешивание смеси. После перемешивания при комнатной температуре в течение ночи, смесь фильтровали и промывали осадок холодным ацетоном (10 мл) и сушили при пониженном давлении при 40°C в течение 3 часов, получая указанное в заголовке соединение в виде твердого вещества белого цвета (4,68 г, 84%).
ЯМР 1H (ДМСО-d6, 270 МГц) дельта 8,33 (1H, д, J=5,9 Гц), 7,66-7,60 (1H, м), 7,19-7,08 (2H, м), 5,96 (1H, тт, J=55,3 Гц, 4,0 Гц), 4,28 (2H, с), 4,03-3,74 (2H, м), 3,62 (1H, д, J=14,1 Гц), 3,41-3,18 (4H, м), 3,14 (1H, д, J=14,1 Гц), 2,50-2,33 (2H, м).
MS (ESI) m/z: 295 (M+H) +.
{0166} {Таблица 3}
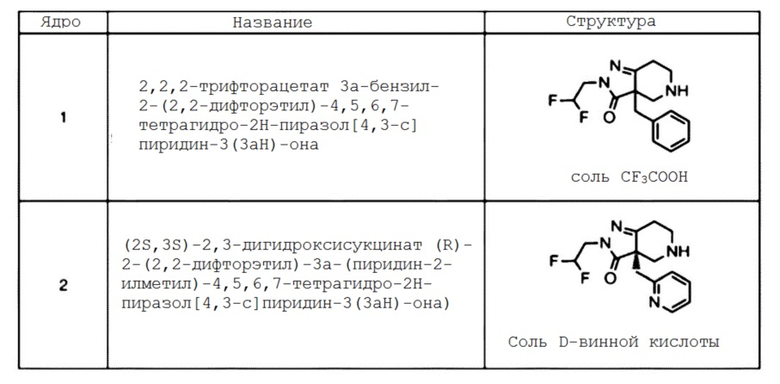
{0167} Синтез промежуточных соединений
Промежуточные соединения получали следующим образом. Названия и структуры промежуточных соединений приведены в таблице 4.
{0168} Промежуточное соединение 1: (R)-2-((трет-бутоксикарбониламино)амино)-3-(2,4-дифторфенокси)пропановая кислота
{0169} Стадия 1: (R)-метил 3-(2,4-дифторфенокси)-2-(тритиламино)пропаноат
К перемешиваемому раствору (R)-метил 3-гидрокси-2-(тритиламино)пропаноата (800 мг, 2,2 ммоль), 2,4-дифторфенола (370 мг, 2,9 ммоль) и трифенилфосфина (760 мг, 2,9 ммоль) в ТГФ (15 мл) прибавляли по каплям раствор бис(2-метоксиэтил)азодикарбоксилата (670 мг, 2,9 ммоль) в ТГФ (2 мл) при 0°C. Смесь перемешивали при комнатной температуре в течение 2 ч. Смесь концентрировали и разбавляли остаток EtOAc (50 мл). Разбавленную смесь промывали насыщенным водным раствором NaHCO3, а затем насыщенным раствором соли, и сушили над Na2SO4. После фильтрования фильтра концентрировали. Остаток очищали колоночной хроматографией (силикагель, элюирование от 3% до 13% EtOAc в гексане), получая указанное в заголовке соединение в виде бесцветной смолы (771 мг, выход 74%).
ЯМР 1H (300 МГц, CDCl3) дельта 7,52 (6H, д, J=7,3 Гц), 7,30-7,16 (9H, м), 6,99-6,72 (3H, м), 4,29 (1H, д, J=9,5, 5,2 Гц), 4,02 (1H, дд, J=9,5, 6,9 Гц), 3,78-3,71 (1H, м), 3,24 (3H, с), 2,88 (1H, д, J=10,3 Гц).
MS (ESI) m/z: наблюдался сигнал фрагмента с массой 243 (положительный ион).
{0170} Стадия 2: (R)-метил 2-((трет-бутоксикарбонил)амино)-3-(2,4-дифторфенокси)пропаноат
К перемешиваемому раствору (R)-метил 3-(2,4-дифторфенокси)-2-(тритиламино)пропаноата (760 мг, 1,6 ммоль) в DCM (10 мл) прибавляли трифторуксусную кислоту (3,7 мл) при комнатной температуре и перемешивали смесь в течение 2 ч при той же температуре. К смеси прибавляли MeOH (25 мл) и перемешивали полученную смесь в течение 5 мин, а затем концентрировали в вакууме. Остаток растворяли в DCM (20 мл), а затем последовательно прибавляли к смеси триэтиламин (0,67 мл, 4,8 ммоль) и ди-трет-бутилдикарбонат (530 мг, 2,4 ммоль) при комнатной температуре. После перемешивания в течение 2 ч комнатной температуре смесь концентрировали в вакууме. Остаток очищали колоночной хроматографией (силикагель, элюирование от 5% до 14% EtOAc в гексане), получая указанное в заголовке соединение в виде бесцветной смолы (470 мг, выход 88%).
ЯМР 1H (300 МГц, CDCl3) дельта 6,96-6,75 (3H, м), 5,53 (1H, d, J=8,8 Гц), 4,66-4,63 (1H, м), 4,42 (1H, дд, J=8,8, 2,9 Гц), 4,25 (1H, дд, J=9,2, 3,3 Гц), 3,79 (3H, с), 1,46 (9H, с).
MS (ESI) m/z: 232 (M-Boc+H) +.
{0171} Стадия 3: (R)-2-((трет-бутоксикарбонил)амино)-3-(2,4-дифторфенокси)пропановая кислота
К перемешиваемому раствору (R)-метил 2-((трет-бутоксикарборнил)амино)-3-(2,4-дифторфенокси)пропаноата (470 мг, 1,4 ммоль) в ТГФ (10 мл) прибавляли к смеси моногидрат LiOH (65 мг, 1,6 ммоль), а затем воду (2 мл). Смесь перемешивали в течение 30 мин при комнатной температуре. К смеси прибавляли 0,5н хлористоводородную кислоту (2 мл), а затем экстрагировали смесь EtOAc (50 мл x 2). Экстракт сушили над Na2SO4. После фильтрования фильтрат концентрировали в вакууме. Остаток очищали колоночной хроматографией (силикагель, элюирование 9% MeOH в DCM), получая указанное в заголовке соединение в виде бесцветной смолы (200 мг, выход 45%).
MS (ESI) m/z: 318 (M+H)+, 316 (M-H)-.
{0172} Промежуточное соединение 2: (R)-2-((трет-бутоксикарбонил)амино)-3-феноксипропановая кислота
{0173} Стадия 1: (R)-Метил 3-фенокси-2-(тритиламино)пропаноат
Указанное в заголовке соединение получали с выходом 23% (390 мг, бесцветная смола) из (R)-метил 3-гидрокси-2-(тритиламино)пропаноата (1,4 г, 3,9 ммоль) и фенола (0,73 г, 7,8 ммоль) аналогично стадии 1 промежуточного соединения 1.
ЯМР 1H (300 МГц, CDCl3) дельта 7,54-7,49 (6H, m), 7,30-7,16 (11H, м), 6,96 (1H, т, J=7,3 Гц), 6,88 (2H, д, J=8,0 Гц), 4,26 (1H, дд, J=9,2, 4,8 Гц), 4,03-4,00 (1H, м), 3,76-3,72 (1H, м), 3,22 (3H, с), 2,88 (1H, уш.с).
MS (ESI) m/z: наблюдался сигнал фрагмента с массой 243 (положительный ион).
{0174} Стадия 2: (R)-метил 2-((трет-бутоксикарбонил)амино)-3-феноксипропаноат
Указанное в заголовке соединение получали с выходом 87% (230 мг, бесцветная смола) из (R)-метил 3-фенокси-2-(тритиламино)пропаноата (390 мг, 0,89 ммоль) аналогично стадии 2 промежуточногго соединения 1.
ЯМР 1H (300 МГц, CDCl3) дельта 7,28 (2H, т, J=7,7 Гц), 6.98 (1H, т, J=7,3 Гц), 6,88 (2H, д, J=8,1 Гц), 5.52 (1H, д, J=8,0 Гц), 4,67 (1H, дт, J=8,8, 2,6 Гц), 4,40 (1H, дд, J=9,2, 2,7 Гц), 4,20 (1H, дд, J=9,5, 2,9 Гц), 3,77 (3H, с), 1,49 (9H, с).
MS (ESI) m/z: 232 (M-Boc+H) +.
{0175} Стадия 3: (R)-2-((трет-бутоксикарбонил)амино)-3-феноксипропановая кислота
Указанное в заголовке соединение получали с выходом 73% (150 мг, бесцветная смола) из (R)-метил 2-((трет-бутоксикарбонил)амино)-3-феноксипропаноата (220 мг, 0,75 ммоль) аналогично стадии 3 промежуточного соединения 1.
MS (ESI) m/z: 282 (M+H)+, 280 (M-H)-.
{0176} Промежуточное соединение 3: (R)-2-((трет-бутоксикарбонил)амино)-3-(4-хлорфенокси)пропановая кислота
{0177} Стадия 1: (R)-метил 3-(4-хлорфенокси)-2-(тритиламино)пропаноат
Указанное в заголовке соединение получали с выходом 56% (730 мг, бесцветная смола) из (R)-метил 3-гидрокси-2-(тритиламино)пропаноата (1,0 г, 2,8 ммоль) и 4-хлорфенола (0,46 г, 3,6 ммоль) аналогично стадии 1 промежуточного соединения 1.
ЯМР 1H (300 МГц, CDCl3) дельта 7,53-7,49 (6H, м), 7,28-7,16 (11H, м), 6,82-6,77 (2H, м), 4,20 (1H, дд, J=9,2, 4,8 Гц), 4,00-3,95 (1H, м), 3,80-3,67 (1H, м), 3,23 (3H, с), 2,87 (1H, д, J=10,3 Гц).
MS (ESI) m/z: наблюдался сигнал фрагмента с массой 243 (положительный ион).
{0178} Стадия 2: (R)-Метил 2-((трет-бутоксикарбонил)амино)-3-(4-хлорфенокси)пропаноат
Указанное в заголовке соединение получали с выходом 95% (480 мг, бесцветная смола) из (R)-метил 3-(4-хлорфенокси)-2-(тритиламино)пропаноата (720 мг, 1,5 ммоль) аналогично стадии 2 промежуточного соединения 1.
ЯМР 1H (300 MГц, CDCl3) дельта 7,23 (2H, д, J=8,8 Гц), 6,81 (2H, д, J=9,5 Гц), 5,49 (1H, д, J=8,1 Гц), 4,74-4,61 (1H, м), 4,37 (1H, дд, J=9,2, 2,7 Гц), 4,18 (1H, дд, J=9,5, 2,9 Гц), 3,72 (3H, с), 1,46 (9H, с).
MS (ESI) m/z: 230 (M-Boc+H)+.
{0179} Стадия 3: (R)-2-((Трет-бутоксикарбонил)амино)-3-(4-хлорфенокси)пропановая кислота
Указанное в заголовке соединение получали с выходом 58% (260 мг, бесцветная смола) из (R)-метил 2-((трет-бутоксикарбонил)амино)-3-(4-хлорфенокси)пропаноата (480 мг, 1,4 ммоль) аналогично стадии 3 промежуточного соединения 1.
MS (ESI) m/z: 316 (M+H)+, 314 (M-H -.
{0180} Промежуточное соединение 4: (R)-2-((трет-бутоксикарбонил)амино)-3-(3-хлорфенокси)пропановая кислота
{0181} Стадия 1: (R)-метил 3-(3-хлорфенокси)-2-(тритиламино)пропаноат
Указанное в заголовке соединение получали с выходом 76% (890 мг, бесцветная смола) из (R)-метил 3-гидрокси-2-(тритиламино)пропаноата (900 мг, 2,5 ммоль) и 3-хлорфенола (420 мг, 3,2 ммоль) аналогично стадии 1 промежуточного соединения 1.
ЯМР 1H (300 MГц, CDCl3) дельта 7,53-7,13 (16H, м), 6,95-6,70 (3H, м), 4,23 (1H, дд, J=9,2, 4,7 Гц), 3,99 (1H, дд, J=9,5, 6,6 Гц), 3,77-3,68 (1H, м), 3,23 (3H, с), 2,88 (1H, д, J=10,3 Гц).
MS (ESI) m/z: наблюдался сигнал фрагмента с массой 243 (положительный ион).
{0182} Стадия 2: (R)-метил 2-((трет-бутоксикарбонил)амино)-3-(3-хлорфенокси)пропаноат
Указанное в заголовке соединение получали с выходом 73% (450 мг, бесцветная смола) из (R)-метил 3-(3-хлорфенокси)-2-(тритиламино)пропаноата (880 мг, 1,8 ммоль) аналогично стадии 2 промежуточного соединения 1.
ЯМР 1H (300 MГц, CDCl3) дельта 7,20 (1H, т, J=8,1 Гц), 6,96 (1H, д, J=8,0 Гц), 6,89 (1H, т, J=2,2 Гц), 6,77 (1H, дд, J=8,4, 2,6 Гц), 5,49 (1H, д, J=4,4 Гц), 4,69-4,65 (1H, м), 4,38 (1H, дд, J=9,2, 2,6 Гц), 4,20 (1H, дд, J=8,8, 2,9 Гц), 3,78 (3H, с), 1,46 (9H, с).
MS (ESI) m/z: 230 (M-Boc+H) +.
{0183} Стадия 3: (R)-2-((трет-бутоксикарбонил)амино)-3-(3-хлорфенокси)пропановая кислота
Указанное в заголовке соединение получали с выходом 57% (240 мг, бесцветная смола) из (R)-метил 2-((трет-бутоксикарбонил)амино)-3-(3-хлорфенокси)пропаноата (440 мг, 1,3 ммоль) аналогично стадии 3 промежуточного соединения 1.
MS (ESI) m/z: 316 (M+H)+, 314 (M-H)-.
{0184} Промежуточное соединение 5: (R)-2-((трет-бутоксикарбонил)амино)-3-(3,5-дихлорфенокси)пропановая кислота
{0185} Стадия 1: (R)-Метил 3-(3,5-дихлорфенокси)-2-(тритиламино)пропаноат
Указанное в заголовке соединение получали с выходом 42% (530 мг, бесцветная смола) из (R)-метил 3-гидрокси-2-(тритиламино)пропаноата (900 мг, 2,5 ммоль) и 3,5-дихлорфенола (530 мг, 3,2 ммоль) аналогично стадии 1 промежуточного соединения 1.
ЯМР 1H (300 MГц, CDCl3) дельта 7,51 (6H, д, J=7,3 Гц), 7,35-7,17 (9H, м), 6,98-6,95 (1H, уш.с.), 6,78 (2H, д, J=1,5 Гц), 4,21 (1H, дд, J=9,2, 4,8 Гц), 3,97 (1H, дд, J=8,8, 6,6 Гц), 3,74-3,67 (1H, м), 3,25 (3H, с), 2,88 (1H, д, J=10,3 Гц).
MS (ESI) m/z: наблюдался сигнал фрагмента с массой 243 (положительный ион).
{0186} Стадия 2: (R)-Метил 2-((трет-бутоксикарбонил)амино)-3-(3,5-дихлорфенокси)пропаноат
Указанное в заголовке соединение получали с выходом 85% (320 мг, бесцветная смола) из (R)-метил 3-(3,5-дихлорфенокси)-2-(тритиламино)пропаноата (520 мг, 1,0 ммоль) аналогично стадии 2 промежуточного соединения 1.
ЯМР 1H (300 MГц, CDCl3) дельта 6,98 (1H, д, J=1,5 Гц), 6,79 (2H, д, J=1,5 Гц), 5,45 (1H, д, J=8,8 Гц), 4,68-4,65 (1H, м), 4,37 (1H, дд, J=8,8, 1,5 Гц), 4,20 (1H, дд, J=9,2, 2,6 HГц), 3,79 (3H, с), 1,46 (9H, с).
MS (ESI) m/z: 264 (M-Boc+H) +.
{0187} Стадия 3: (R)-2-((трет-бутоксикарбонил)амино)-3-(3,5-дихлорфенокси)пропановая кислота
Указанное в заголовке соединение получали с выходом 48% (140 мг, бесцветная смола) из (R)-метил 2-((трет-бутоксикарбонил)амино)-3-(3,5-дихлорфенокси)пропаноата (310 мг, 0,85 ммоль) аналогично стадии 3 промежуточного соединения 1.
MS (ESI) m/z: 250 (M-Boc+H)+, 348 (M-H)-.
{0188} Промежуточное соединение 6: (R)-2-((трет-бутоксикарбонил)амино)-3-(2-(трифторметил)фенокси)пропановая кислота
{0189} Стадия 1: (R)-метил 3-(2-(трифторметил)фенокси)-2-(тритиламино)пропаноат
Указанное в заголовке соединение получали с выходом 55% (690 мг, бесцветная смола) из (R)-метил 3-гидрокси-2-(тритиламино)пропаноата (900 мг, 2,5 ммоль) и 2-(трифторметил)фенола (530 мг, 3,2 ммоль) аналогично стадии 1 промежуточного соединения 1.
ЯМР 1H (300 MГц, CDCl3) дельта 7,56-7,46 (7H, м), 7,30-7,17 (10H, м), 7,04-6,96 (2H, м), 4,36 (1H, дд, J=8,8, 3,6 Гц), 4,07-4,02 (1H, м), 3,82-3,74 (1H, м), 3,22 (3H, с), 2,92 (1H, д, J=10,3 Гц).
MS (ESI) m/z: наблюдался сигнал фрагмента с массой 243 (положительный ион).
{0190} Стадия 2: (R)-метил 2-((трет-бутоксикарбонил)амино)-3-(2-(трифторметил)фенокси)пропаноат
Указанное в заголовке соединение получали с выходом 86% (420 мг, бесцветная смола) из (R)-метил 3-(2-(трифторметил)фенокси)-2-(тритиламино)пропаноата (680 мг, 1,3 ммоль) аналогично стадии 2 промежуточного соединения 1.
ЯМР 1H (300 MГц, CDCl3) дельта 7,56 (1H, д, J=8,1 Гц), 7,49 (1H, т, J=8,1 Гц), 7,05 (1H, т, J=7,3 Гц), 6,96 (1H, д, J=8,1 Гц), 5,51 (1H, д, J=8,8 Гц), 4,72 (1H, дт, J=8,8, 2,6 Гц), 4,48 (1H, дд, J=8,8, 2,2 Гц), 4,30 (1H, дд, J=9,2, 2,6 Гц), 3,78 (3H, с), 1,46 (9H, с).
MS (ESI) m/z: 364 (M+H) +.
{0191} Стадия 3: (R)-2-((трет-бутоксикарбонил)амино)-3-(2-(трифторметил)фенокси)пропановая кислота
Указанное в заголовке соединение получали с выходом 55% (220 мг, бесцветная смола) из (R)-метил 2-((трет-бутоксикарбонил)амино)-3-(2-(трифторметил)фенокси)пропаноата (410 мг, 1,1 ммоль) аналогично стадии 3 промежуточного соединения 1.
MS (ESI) m/z: 250 (M-Boc+H)+, 348 (M-H)-.
{0192} Промежуточное соединение 7: (R)-2-((трет-бутоксикарбонил)амино)-3-(3,4-дифторфенокси)пропановая кислота
{0193} Стадия 1: (R)-метил 3-(3,4-дифторфенокси)-2-(тритиламино)пропаноата
Указанное в заголовке соединение получали с выходом 56% (660 мг, бесцветная смола) из (R)-метил 3-гидрокси-2-(тритиламино)пропаноата (900 мг, 2,5 ммоль) и 3,4-дифторфенола (420 мг, 3,2 ммоль) аналогично стадии 1 промежуточного соединения 1.
ЯМР 1H (300 MГц, CDCl3) дельта 7,52-7,49 (6H, м), 7,30-7,17 (9H, м), 7,05 (1H, кв, J=9,3 Гц), 6,73-6,65 (1H, м), 6,59-6,53 (1H, м), 4,17 (1H, дд, J=9,5, 5,1 Гц), 3,94 (1H, дд, J=9,5, 6,6 Гц), 3,73-3,66 (1H, м), 3,24 (3H, с), 2,87 (1H, д, J=10,3 Гц).
MS (ESI) m/z: наблюдался сигнал фрагмента с массой 243 (положительный ион).
{0194} Стадия 2: (R)-метил 2-((трет-бутоксикарбонил)амино)-3-(3,4-дифторфенокси)пропаноат
Указанное в заголовке соединение получали с выходом 81% (370 мг, бесцветная смола) из (R)-метил 3-(3,4-дифторфенокси)-2-(тритиламино)пропаноата (650 мг, 1,4 ммоль) аналогично стадии 2 промежуточного соединения 1.
ЯМР 1H (300 MГц, CDCl3) дельта 7,06 (1H, кв, J=9,3 Гц), 6,75-6,67 (1H, м), 6,61-6,55 (1H, м), 5,46 (1H, д, J=8,0 Гц), 4,70-4,61 (1H, м), 4,34 (1H, дд, J=8,8, 2,9 Гц), 4,16 (1H, дд, J=9,5, 2,9 Гц), 3,78 (3H, с), 1,46 (9H, с).
MS (ESI) m/z: 332 (M+H) +.
{0195} Стадия 3: (R)-2-((трет-бутоксикарбонил)амино)-3-(3,4-дифторфенокси)пропановая кислота
Указанное в заголовке соединение получали с выходом 57% (200 мг, светло-коричневая смола) из (R)-метил 2-((трет-бутоксикарбонил)амино)-3-(3,4-дифторфенокси)пропаноата (360 мг, 1,1 ммоль) аналогично стадии 3 промежуточного соединения 1.
MS (ESI) m/z: 318 (M-Boc+H)+, 316 (M-H)-.
{0196} Промежуточное соединение 8: (R)-2-((трет-бутоксикарбонил)амино)-3-(2-хлорфенокси)пропановая кислота
{0197} Стадия 1: (R)-метил 3-(2-хлорфенокси)-2-(тритиламино)пропаноат
Указанное в заголовке соединение получали с выходом 68% (880 мг, бесцветное твердое вещество) из (R)-метил 3-гидрокси-2-(тритиламино)пропаноата (1000 мг, 2,8 ммоль) и 2-хлорфенола (460 мг, 3,2 ммоль) аналогично стадии 1 промежуточного соединения 1.
ЯМР 1H (300 MГц, CDCl3) дельта 7,53 (6H, д, J=7,3 Гц), 7,36-6,92 (11H, м), 6,93-6,88 (2H, м), 4,35 (1H, дд, J=8,8, 5,1 Гц), 4,05-3,99 (1H, м), 3,85-3,78 (1H, м), 3,24 (3H, с), 2,91 (1H, д, J=10,3 Гц).
MS (ESI) m/z: 494 (M+Na+H)+.
{0198} Стадия 2: (R)-Метил 2-((трет-бутоксикарбонил)амино)-3-(2-хлорфенокси)пропаноат
Указанное в заголовке соединение получали с выходом 90% (550 мг, бесцветное масло) из (R)-метил 3-(2-хлорфенокси)-2-(тритиламино)пропаноата (870 мг, 1,8 ммоль) аналогично стадии 2 промежуточного соединения 1.
ЯМР 1H (300 MГц, CDCl3) дельта 7,35 (1H, дд, J=8,1, 1,5 Гц), 7,21 (1H, тд, J=7,7, 1,5 Гц), 6,96-6,90 (2H, м), 5,60 (1H, д, J=8,8 Гц), 4,76-4,66 (1H, м), 4,45 (1H, дд, J=9,2, 2,6 Гц), 4,27 (1H, дд, J=9,5, 2,9 Гц), 3,80 (3H, с), 1,46 (9H, с).
MS (ESI) m/z: 330 (M+H)+.
{0199} Стадия 3: (R)-2-((трет-бутоксикарбонил)амино)-3-(2-хлорфенокси)пропановая кислота
Указанное в заголовке соединение получали с выходом 51% (260 мг, бесцветная смола) из (R)-метил 2-((трет-бутоксикарбонил)амино)-3-(2-хлорфенокси)пропаноата (540 мг, 1,6 ммоль) аналогично стадии 3 промежуточного соединения 1.
MS (ESI) m/z: 216 (M-Boc+H) +, 314 (M-H) -.
{0200} Промежуточное соединение 9: (R)-3-(3,5-бис(трифторметил)фенокси)-2-((трет-бутоксикарбонил)амино)пропановая кислота
{0201} Стадия 1: (R)-метил 3-(3,5-бис(трифторметил)фенокси)-2-(тритиламино)пропаноат
Указанное в заголовке соединение получали с выходом 35% (550 мг, бесцветная смола) из (R)-метил 3-гидрокси-2-(тритиламино)пропаноата (1000 мг, 2,8 ммоль) и 3,5-бис(трифторметил)фенола (830 мг, 3,6 ммоль) аналогично стадии 1 промежуточного соединения 1.
ЯМР 1H (300 MГц, CDCl3) дельта 7,52 (6H, д, J=7,3 Гц), 7,34-7,18 (12H, м), 4,28 (1H, дд, J=9,5, 4,4 Гц), 4,03 (1H, дд, J=9,5, 6,6 Гц), 3,81-3,70 (1H, м), 3,28 (3H, с), 2,93 (1H, д, J=9,5 Гц).
MS (ESI) m/z: наблюдался сигнал фрагмента с массой 243 (положительный ион).
{0202} Стадия 2: (R)-метил 3-(3,5-бис(трифторметил)фенокси)-2-((трет-бутоксикарбонил)амино)пропаноат
Указанное в заголовке соединение получали с выходом 96% (390 мг, бесцветное масло) из (R)-метил 3-(3,5-бис(трифторметил)фенокси)-2-(тритиламино)пропаноата (540 мг, 0,94 ммоль) аналогично стадии 2 промежуточного соединения 1.
ЯМР 1H (300 MГц, CDCl3) дельта 7,50 (1H, с), 7,31 (2H, с), 5,50 (1H, д, J=8,0 Гц), 4,79-4,69 (1H, м), 4,49 (1H, дд, J=9,1, 2,6 Гц), 4,33 (1H, 8,8, 2,9 Гц), 3,81 (3H, с), 1,46 (9H, с).
MS (ESI) m/z: 432 (M+H)+.
{0203} Стадия 3: (R)-3-(3,5-бис(трифторметил)фенокси)-2-((трет-бутоксикарбонил)амино)пропановая кислота
Указанное в заголовке соединение получали с выходом 30% (110 мг, бесцветная смола) из (R)-метил 3-(3,5-бис(трифторметил)фенокси)-2-((трет-бутоксикарбонил)амино)пропаноата (380 мг, 0,88 ммоль) аналогично стадии 3 промежуточного соединения 1.
MS (ESI) m/z: 418 (M+H)+, 416 (M-H)-.
{0204} Промежуточное соединение 10: (R)-2-((трет-бутоксикарбонил)амино)-3-(3-фторфенокси)пропановая кислота
{0205} Стадия 1: (R)-метил 3-(3-фторфенокси)-2-(тритиламино)пропаноат
Указанное в заголовке соединение получали с выходом 74% (1400 мг, бесцветная смола) из (R)-метил 3-гидрокси-2-(тритиламино)пропаноата (1500 мг, 4,2 ммоль) и 3-фторфенола (610 мг, 5,4 ммоль) аналогично стадии 1 промежуточного соединения 1.
ЯМР 1H (300 MГц, CDCl3) дельта 7,60-7,48 (6H, м), 7,31-7,15 (10H, м), 6,70-6,55 (3H, м), 4,22 (1H, дд, J=9,9, 5,3 Гц), 3,99 (1H, дд, J=9,2, 6,6 Гц), 3,76-3,68 (1H, м), 3,23 (3H, с), 2,88 (1H, д, J=10,5 Гц).
MS (ESI) m/z: 478 (M+Na) +.
{0206} Стадия 2: (R)-Метил 2-((трет-бутоксикарбонил)амино)-3-(3-фторфенокси)пропаноат
Указанное в заголовке соединение получали с выходом 77% (290 мг, бесцветное масло) из (R)-метил 3-(3-фторфенокси)-2-(тритиламино)пропаноата (550 мг, 1,2 ммоль) аналогично стадии 2 промежуточного соединения 1.
ЯМР 1H (300 MГц, CDCl3) дельта 7,26-7,18 (1H, м), 6,72-6,57 (3H, м), 5,48 (1H, д, J=7,9 Гц), 4,72-4,62 (1H, м), 4,38 (1H, дд, J=9,2, 2,6 Гц), 4,20 (1H, дд, J=9,2, 3,3 Гц), 3,78 (3H, с), 1,46 (9H, с).
MS (ESI) m/z: 314 (M+H)+.
{0207} Стадия 3: (R)-2-((трет-бутоксикарбонил)амино)-3-(3-фторфенокси)пропановая кислота
Указанное в заголовке соединение получали с выходом 29% (80 мг, бесцветная смола) из (R)-метил 2-((трет-бутоксикарбонил)амино)-3-(3-фторфенокси)пропаноата (290 мг, 0,93 ммоль) аналогично стадии 3 промежуточного соединения 1.
MS (ESI) m/z: 300 (M+H) +, 298 (M-H) -.
{0208} Промежуточное соединение 11: (R)-2-((трет-бутоксикарбонил)амино)-3-(3-метоксифенокси)пропановая кислота
{0209} Стадия 1: (R)-метил 3-(3-метоксифенокси)-2-(тритиламино)пропаноат
Указанное в заголовке соединение получали с выходом 43% (830 мг, бесцветная смола) из (R)-метил 3-гидрокси-2-(тритиламино)пропаноата (1500 мг, 4,2 ммоль) и 3-метоксифенола (670 мг, 5,4 ммоль) аналогично стадии 1 промежуточного соединения 1.
ЯМР 1H (300 MГц, CDCl3) дельта 7,60-7,50 (6H, м), 7,30-7,13 (10H, м), 6,54-6,40 (3H, м), 4,24 (1H, дд, J=9,2, 5,3 Гц), 4,01 (1H, дд, J=9,2, 6,6Гц), 3,82 (3H, с), 3,80-3,70 (1H, м), 3,23 (3H, с), 2,88 (1H, д, J=10,5 Гц).
MS (ESI) m/z: наблюдали сигнал фрагмента 243 (положительный ион).
{0210} Стадия 2: (R)-метил 2-((трет-бутоксикарбонил)амино)-3-(3-метоксифенокси)пропаноата
Указанное в заголовке соединение получали с выходом 93% (530 мг, светло-коричневое масло) из (R)-метил 3-(3-метоксифенокси)-2-(тритиламино)пропаноата (820 мг, 1,8 ммоль) аналогично стадии 2 промежуточного соединения 1.
ЯМР 1H (300 MГц, CDCl3) дельта 7,17 (1H, т, J=8,2 Гц), 6,55-6,44 (3H, м), 5,49 (1H, д, J=7,9 Гц), 4,68-4,62 (1H, м), 4,38 (1H, дд, J=9,6, 2,3 Гц), 4,18 (1H, дд, J=9,2, 2,6 Гц), 3,78 (3H, с), 3,77 (3H, с), 1,46 (9H, с).
MS (ESI) m/z: 326 (M+H)+.
{0211} Стадия 3: (R)-2-((трет-бутоксикарбонил)амино)-3-(3-меткосифенокси)пропановая кислота
Указанное в заголовке соединение получали с выходом 43% (220 мг, бесцветная смола) из (R)-метил 2-((трет-бутоксикарбонил)амино)-3-(3-метоксифенокси)пропаноата (530 мг, 1,6 ммоль) аналогично стадии 3 промежуточного соединения 1.
MS (ESI) m/z: 312 (M+H) +, 310 (M-H) -.
{0212} Промежуточное соединение 12: (R)-2-((трет-бутоксикарбонил)амино)-3-(2-фторфенокси)пропановая кислота
{0213} Стадия 1: (R)-метил 3-(2-фторфенокси)-2-(тритиламино)пропаноат
Указанное в заголовке соединение получали с выходом 71% (890 мг, бесцветная смола) из (R)-метил 3-гидрокси-2-(тритиламино)пропаноата (1000 мг, 2,8 ммоль) и 2-фторфенола (400 мг, 3,6 ммоль) аналогично стадии 1 промежуточного соединения 1.
ЯМР 1H (300 MГц, CDCl3) дельта 7,52 (6H, д, J=7,2 Гц), 7,28-7,15 (9H, м), 6,97-6,87 (4H, м), 4,32 (1H, дд, J=9,2, 5,3 Гц), 4,06 (1H, дд, J=9,9, 6,6 Гц), 3,78 (1H, уш.с.), 3,23 (3H, с), 2,89 (1H, уш.с.).
MS (ESI) m/z: наблюдался сигнал фрагмента с массой 243 (положительный ион).
{0214} Стадия 2: (R)-метил 2-((трет-бутоксикарбонил)амино)-3-(2-фторфенокси)пропаноат
Указанное в заголовке соединение получали с выходом 89% (550 мг, бесцветное масло) из (R)-метил 3-(2-фторфенокси)-2-(тритиламино)пропаноата (890 мг, 2,0 ммоль) аналогично стадии 2 промежуточного соединения 1.
ЯМР 1H (300 MГц, CDCl3) дельта 7,10-7,02 (2H, м), 6,98-6,90 (2H, м), 5,54 (1H, д, J=7,9 Гц), 4,71-4,61 (1H, м), 4,46 (1H, дд, J=9,2, 2,6 Гц), 4,27 (1H, дд, J=9,6, 3,0 Гц), 3,78 (3H, с), 1,46 (9H, с).
MS (ESI) m/z: 314 (M+H)+.
{0215} Стадия 3: (R)-2-((трет-бутоксикарбонил)амино)-3-(2-фторфенокси)пропановая кислота
Указанное в заголовке соединение получали с выходом 50% (260 мг, бесцветный густой раствор) из (R)-метил 2-((трет-бутоксикарбонил)амино)-3-(2-фторфенокси)пропаноата (550 мг, 1,7 ммоль) аналогично стадии 3 промежуточного соединения 1.
MS (ESI) m/z: 300 (M+H)+, 298 (M-H)-.
{0216} Промежуточное соединение 13: (R)-2-(2-((трет-бутоксикарбонил)амино)-2-метилпропанамидо)-3-(4-цианофенокси)пропановая кислота
{0217} Стадия 1: (R)-метил 3-(4-цианофенокси)-2-(тритиламино)пропаноат
Указанное в заголовке соединение получали с выходом 49% (630 мг, твердое вещество белого цвета) из (R)-метил 3-гидрокси-2-(тритиламино)пропаноата (1000 мг, 2,8 ммоль) и 4-гидроксибензонитрила (660 мг, 5,5 ммоль) аналогично стадии 1 промежуточного соединения 1.
ЯМР 1H (300 MГц, CDCl3) дельта 7,58 (2H, д, J=8,6 Гц), 7,56-7,48 (6H, м), 7,30-7,15 (9H, м), 6,91 (2H, д, J=8,6 Гц), 4,25 (1H, дд, J=9,2, 4,6 Гц), 4,03 (1H, дд, J=9,2, 5,9 Гц), 3,74 (1H, м), 3,25 (3H, с), 2,90 (1H, д, J=9,9 Гц).
MS (ESI) m/z: наблюдался сигнал фрагмента с массой 243 (положительный ион).
{0218} Стадия 2: (R)-метил 2-(2-((трет-бутоксикарбонил)амино)-2-метилпропанамидо)-3-(4-цианофенокси)пропаноат
К перемешиваемому раствору (R)-метил 3-(4-цианофенокси)-2-(тритиламино)пропаноата (630 мг, 1,4 ммоль) в DCM (8 мл) медленное прибавляли трифторуксусную кислоту (3 мл) при комнатной температуре и перемешивали смесь в течение 2 ч при той же температуре. К смеси добавляли MeOH (1 мл). Полученную смесь перемешивали в течение 5 мин, а затем концентрировали в вакууме. Остаток растворяли в DCM (5 мл), а затем к данному раствору последовательно прибавляли 2-((трет-бутоксикарбонил)амино)-2-метилпропановую кислоту (280 мг, 1,4 ммоль), 1-этил-3-(3-диметиламинопропил)карбодиимида гидрохлорида (WSC, 390 мг, 2,0 ммоль), 1H-бензо[d][1,2,3]триазол-1-ол (HOBt, 210 мг, 1,4 ммоль) и триэтиламин (0,94 мл, 6,8 ммоль) при комнатной темпепатуре. После перемешивания в течение ночи к смеси приьавляли насыщенный водный раствор NaHCO3 и экстрагировали смесь DCM (30 мл x 2). Экстракт сушили над Na2SO4. После фильтрования фильтрат концентрировали в вакууме. Остаток очищали колоночной хроматографией (силикагель, элюирование от 25% до 50% EtOAc в гексане), получая указанное в заголовке соединение в виде твердого вещества белого цвета (220 мг, выход 40%).
ЯМР 1H (300 MГц, CDCl3) дельта 7,57 (2H, д, J=8,6 Гц), 7,33 (1H, м), 6,93 (2H, д, J=8,6 Гц), 4,97 (1H, м), 4,84 (1H, м), 4,43 (1H, дд, J=9,2, 3,3 Гц), 4,29 (1H, дд, J=9,2, 2,6 Гц), 3,78 (3H, с), 1,49 (3H, с), 1,47 (3H, с), 1,33 (9H, с).
MS (ESI) m/z: 406 (M+H)+, 404 (M-H)-.
{0219} Стадия 3: (R)-2-(2-((трет-бутоксикарбонил)амино)-2-метилпропанамидо)-3-(4-цианофенокси)пропановая кислота
Указанное в заголовке соединение получали с выходом 24% (51 мг, бесцветное масло) из (R)-метил 2-(2-((трет-бутоксикарбонил)амино)-2-метилпропанамидо)-3-(4-цианофенокси)пропаноата (220 мг, 0,54 ммоль) аналогично стадии 3 промежуточного соединения 1.
MS (ESI) m/z: 392 (M+H)+.
{0220} Промежуточное соединение 14: (R)-2-((трет-бутоксикарбонил)амино)-3-(нафтелен-2-илокси)пропановая кислота
{0221} Стадия 1: (R)-метил 3-(нафталин-2-илокси)-2-(тритиламино)пропаноат
Указанное в заголовке соединение получали с выходом 32% (430 мг, твердое вещество белого цвета) из (R)-метил 3-гидрокси-2-(тритиламино)пропаноата (1000 мг, 2,8 ммоль) и нафталин-2-ола (520 мг, 3,6 ммоль) аналогично стадии 1 промежуточного соединения 1.
ЯМР 1H (300 MГц, CDCl3) дельта 7,77-7,70 (3H, м), 7,56-7,40 (7H, м), 7,40-7,10 (12H, м), 4,39 (1H, дд, J=9,2, 4,6Гц), 4,17-4,08 (1H, м), 3,82-3,77 (1H, м), 3,24 (3H, с), 2,94 (1H, д, J=10,6Гц)
MS (ESI) m/z: наблюдался сигнал фрагмента с массой 243 (положительный ион).
{0222} Стадия 2: (R)-метил 2-((трет-бутоксикарбонил)амино)-3-(нафталин-2-илокси)пропаноат
Указанное в заголовке соединение получали с выходом 95% (290 мг, бесцветное масло) из (R)-метил 3-(нафталин-2-илокси)-2-(тритиламино)пропаноата (430 мг, 0,88 ммоль) аналогично стадии 2 промежуточного соединения 1.
ЯМР 1H (300 MГц, CDCl3) дельта 7,78-7,64 (3H, м), 7,47-7,32 (2H, м), 7,15-7,09 (2H, м), 5,55 (1H, д, J=8,6 Гц), 4,75-4,68 (1H, м), 4,52 (1H, дд, J=9,2, 2,6 Гц), 4,33 (1H, дд, J=9,2, 3,3 Гц), 3,78 (3H, с), 1,47 (9H, с).
MS (ESI) m/z: 246 (M-Boc+H) +.
{0223} Стадия 3: (R)-2-((трет-бутоксикарбонил)амино)-3-(нафталин-2-илокси)пропановая кислота
Указанное в заголовке соединение получали с выходом 46% (130 мг, бесцветный густой раствор) из (R)-метил 2-((трет-бутоксикарбонил)амино)-3-(нафталин-2-илокси)пропаноата (290 мг, 0,84 ммоль) аналогично стадии 3 промежуточного соединения 1.
MS (ESI) m/z: 332 (M+H)+, 330 (M-H)-.
{0224} Промежуточное соединение 15: (R)-2-((трет-бутоксикарбонил)амино)-3-(нафталин-1-илокси)пропановая кислота
{0225} Стадия 1: (R)-метил 3-(нафталин-1-илокси)-2-(тритиламино)пропаноат
Указанное в заголовке соединение получали с выходом 46% (920 мг, твердое вещество белого цвета) из (R)-метил 3-гидрокси-2-(тритиламино)пропаноата (1500 мг, 4,2 ммоль) и нафталин-1-ола (780 мг, 5,4 ммоль) аналогично стадии 1 промежуточного соединения 1.
ЯМР 1H (300 MГц, CDCl3) дельта 8,16 (1H, д, J=8,6 Гц), 7,78 (1H, д, J=7,9 Гц), 7,56 (6H, д, J=7,9 Гц), 7,50-7,33 (4H, м), 7,30-7,17 (9H, м), 6,81 (1H, д, J=7,9 Гц), 4,46 (1H, дд, J=8,9, 4,9 Гц), 4,26-4,20 (1H, м), 3,93-3,85 (1H, м), 3,25 (3H, с), 3,01 (1H, д, J=10,5 Гц).
MS (ESI) m/z: наблюдался сигнал фрагмента с массой 243 (положительный ион).
{0226} Стадия 2: (R)-метил 2-((трет-бутоксикарбонил)амино)-3-(нафталин-1-илокси)пропаноат
Указанное в заголовке соединение получали с выходом >99% (650 мг, бесцветное масло) из (R)-метил 3-(нафталин-1-илокси)-2-(тритиламино)пропаноата (910 мг, 1,9 ммоль) аналогично стадии 2 промежуточного соединения 1.
ЯМР 1H (300 MГц, CDCl3) дельта 8,15-8,12 (1H, м), 7,81-7,78 (1H, м), 7,52-7,44 (3H, м), 7,36 (1H, т, J=7,9 Гц), 6,78 (1H, д, J=7,9 Гц), 5,63 (1H, д, J=8,6 Гц), 4,87-4,77 (1H, м), 4,52 (1H, дд, J=9,2, 2,7 Гц), 4,42 (1H, дд, J=8,9, 2,3 Гц), 3,79 (3H, с), 1,46 (9H, с).
MS (ESI) m/z: 246 (M-Boc+H)+.
{0227} Стадия 3: (R)-2-((трет-бутоксикарбонил)амино)-3-(нафталин-1-илокси)пропановая кислота
Указанное в заголовке соединение получали с выходом 69% (420 мг, бесцветный густой раствор) из (R)-метил 2-((трет-бутоксикарбонил)амино)-3-(нафталин-1-илокси)пропаноата (640 мг, 1,9 ммоль) аналогично стадии 3 промежуточного соединения 1.
MS (ESI) m/z: 332 (M+H)+, 330 (M-H)-.
{0228} Промежуточное соединение 16: (R)-2-((трет-бутоксикарбонил)амино)-3-((5-хлорпиридин-3-ил)окси)пропановая кислота
{0229} Стадия 1: (R)-метил 3-((5-хлорпиридин-3-ил)окси)-2-(тритиламино)пропаноат
Указанное в заголовке соединение получали с выходом 37% (720 мг, твердое вещество белого цвета) из (R)-метил 3-гидрокси-2-(тритиламино)пропаноата (1500 мг, 4,2 ммоль) и 5-хлорпиридин-3-ола (700 мг, 5,4 ммоль) аналогично стадии 1 промежуточного соединения 1.
ЯМР 1H (300 MГц, CDCl3) дельта 8,20 (1H, д, J=1,3 Гц), 8,16 (1H, д, J=2,0 Гц), 7,53-7,45 (6H, м), 7,34-7,15 (10H, м), 4,25 (1H, дд, J=9,2, 4,6 Гц), 4,02 (1H, дд, J=9,2, 6,6 Гц), 3,77-3,69 (1H, м), 3,27 (3H, с), 2,95 (1H, д, J=9,9 Гц).
MS (ESI) m/z: наблюдался сигнал фрагмента с массой 243 (положительный ион).
{0230} Стадия 2: (R)-2-((трет-бутоксикарбонил)амино)-3-((5-хлорпиридин-3-ил)окси)пропановая кислота
К раствору (R)-метил 3-((5-хлорпиридин-3-ил)окси)-2-(тритиламино)пропаноата (600 мг, 1,3 ммоль) в диоксане (10 мл) прибавляли 6н хлористоводородную кислоту (3 мл) при комнатной температуре. Смесь перемешивали при температуре кипения в течение 4 ч. После охлаждения до комнатной температуры смесь концентрировали в вакууме, получая твердое вещество белого цвета. Данное твердое вещество белого цвета суспендировали в диоксане (5 мл) и последовательно прибавляли к смеси насыщенный водный раствор NaHCO3 (1 мл) и ди-трет-бутилдикарбонат (550 мг, 2,5 ммоль). Смесь перемешивали в течение 5 ч при комнатной температуре и разбавляли водой (40 мл). Смесь промывали DCM (10 мл x 2) и подкисляли водный слой добавлением 2н хлористоводородной кислоты (~pH5). Водный слой экстрагировали EtOAc (40 мл x 2) и сушили экстракт над Na2SO4. После фильтрования фильтрат концентрировали в вакууме, получая указанное в заголовке соединение в виде бесцветной смолы (390 мг, выход 97%).
ЯМР 1H (300 MГц, CDCl3) дельта 8,24 (1H, с), 8,18 (1H, с), 7,32-7,27 (1H, м), 5,59 (1H, д, J=7,2Гц), 4,75-4,66 (1H, м), 4,53-4,45 (1H, м), 4,40-4,33 (1H, м), 1,47 (9H, с). Сигнал COOH не наблюдался.
MS (ESI) m/z: 317 (M+H)+, 315 (M-H)-.
{0231} Промежуточное соединение 17: (R)-2-((трет-бутоксикарбонил)амино)-3-(3-цианофенокси)пропановая кислота
{0232} Стадия 1: (R)-метил 3-(3-цианофенокси)-2-(тритиламино)пропаноат
Указанное в заголовке соединение получали с выходом 23% (580 мг, бесцветное твердое вещество) из (R)-метил 3-гидрокси-2-(тритиламино)пропаноата (2000 мг, 5,5 ммоль) и 3-гидроксибензонитрила (1000 мг, 8,3 ммоль) аналогично стадии 1 промежуточного соединения 1.
ЯМР 1H (300 MГц, CDCl3) дельта 7,52 (6H, д, J=7,3 Гц), 7,50-7,16 (11H, м), 7,11-7,08 (2H, м), 4,26-4,21 (1H, м), 4,03-3,97 (1H, м), 3,77-3,69 (1H, м), 3,25 (3H, с), 2,90 (1H, д, J=9,9 Гц).
MS (ESI) m/z: наблюдался сигнал фрагмента с массой 243 (положительный ион).
{0233} Стадия 2: (R)-метил 2-((трет-бутоксикарбонил)амино)-3-(3-цианофенокси)пропаноат
Указанное в заголовке соединение получали с выходом 93% (370 мг, бледно-желтое масло) из (R)-метил 3-(3-цианофенокси)-2-(тритиламино)пропаноата (570 мг, 1,2 ммоль) аналогично стадии 2 промежуточного соединения 1.
ЯМР 1H (300 MГц, CDCl3) дельта 7,41-7,36 (1H, м), 7,28 (1H, д, J=6,6 Гц), 7,14-7,10 (2H, м), 5,48 (1H, д, J=7,9 Гц), 4,69 (1H, д, J=7,9 Гц), 4,41 (1H, дд, J=9,2, 2,6 Гц), 4,25 (1H, дд, J=9,2, 3,3 Гц), 3,79 (3H, с), 1,46, 1,49 (9H, с).
MS (ESI) m/z: 221 (M-Boc+H)+.
{0234} Стадия 3: (R)-2-((трет-бутоксикарбонил)амино)-3-(3-цианофенокси)пропановая кислота
Указанное в заголовке соединение получали с выходом 45% (150 мг, бесцветная смола) из (R)-метил 2-((трет-бутоксикарбонил)амино)-3-(3-цианофенокси)пропаноата (360 мг, 1,1 ммоль) аналогично стадии 3 промежуточного соединения 1.
MS (ESI) m/z: 307 (M+H)+.
{0235} Промежуточное соединение 18: (R)-2-((трет-бутоксикарбонил)амино)-3-(пиридин-2-илокси)пропановая кислота
{0236} Стадия 1: (R)-метил 3-(пиридин-2-илокси)-2-(тритиламино)пропаноат
Указанное в заголовке соединение получали с выходом 15% (887 мг, бесцветная смола) из (R)-метил 3-гидрокси-2-(тритиламино)пропаноата (5000 мг, 14 ммоль) и пиридин-2-ола (2000 мг, 21 ммоль) аналогично стадии 1 промежуточного соединения 1 при использовании (E)-диазен-1,2-диилбис(пиперидин-1-илметанона) (ADDP, 7000 мг, 28 ммоль) и трибутилфосфина (5600 мг, 28 ммоль) вместо бис(2-метоксиэтил)азодикарбоксилата и трифенилфосфина, соответственно.
MS (ESI) m/z: наблюдался сигнал фрагмента с массой 243 (положительный ион).
{0237} Стадия 2: (R)-2-((трет-бутоксикарбонил)амино)-3-(пиридин-2-илокси)пропановая кислота
Указанное в заголовке соединение получали с выходом 38% (210 мг, бесцветная смола) из (R)-метил 3-(пиридин-2-илокси)-2-(тритиламино)пропаноата (860 мг, 2,0 ммоль) аналогично стадии 2 промежуточного соединения 16.
MS (ESI) m/z: 283 (M+H)+, 281 (M-H)-.
{0238} Промежуточное соединение 19: (R)-2-((трет-бутоксикарбонил)амино)-3-((5-фторпиридин-3-ил)окси)пропановая кислота
{0239} Стадия 1: (R)-метил 3-((5-фторпиридин-3-ил)окси)-2-(тритиламино)пропаноат
Указанное в заголовке соединение получали с выходом 40% (760 мг, твердое вещество белого цвета) из (R)-метил 3-гидрокси-2-(тритиламино)пропаноата (1500 мг, 4,2 ммоль) и 5-фторпиридин-3-ола (560 мг, 5,0 ммоль) аналогично стадии 1 промежуточного соединения 1.
MS (ESI) m/z: наблюдался сигнал фрагмента с массой 243 (положительный ион).
{0240} Стадия 2: (R)-2-((трет-бутоксикарбонил)амино)-3-((5-фторпиридин-3-ил)окси)пропановая кислота
Указанное в заголовке соединение получали с выходом 46% (230 мг, бесцветная смола) из (R)-метил 3-((5-фторпиридин-3-ил)окси)-2-(тритиламино)пропаноата (760 мг, 1,7 ммоль) аналогично стадии 2 промежуточного соединения 16.
MS (ESI) m/z: 301 (M+H)+, 299 (M-H)-.
{0241} Промежуточное соединение 20: (R)-2-((трет-бутоксикарбонил)амино)-3-((6-(трифторметил)пиридин-2-ил)окси)пропановая кислота
{0242} Стадия 1: (R)-метил 3-((6-(трифторметил)пиридин-2-ил)окси)-2-(тритиламино)пропаноат
Указанное в заголовке соединение получали с выходом 81% (2300 мг, бесцветная смола) из (R)-метил 3-гидрокси-2-(тритиламино)пропаноата (2000 мг, 5,5 ммоль) и 6-(трифторметил)пиридин-2-ола (900 мг, 5,5 ммоль) аналогично стадии 1 промежуточного соединения 1.
ЯМР 1H (300 MГц, CDCl3) дельта 7,68 (1H, т, J=7,9 Гц), 7,51 (6H, д, J=7,9 Гц), 7,28-7,14 (10H, м), 6,88 (1H, д, J=8,6 Гц), 4,78 (1H, дд, J=10,9, 4,9 Гц), 4,47 (1H, дд, J=10,9, 6,9 Гц), 3,77 (1H, квинт, J=5,6 Гц), 3,16 (3H, с), 2,86 (1H, д, J=10,5 Гц).
MS (ESI) m/z: наблюдался сигнал фрагмента с массой 243 (положительный ион).
{0243} Стадия 2: (R)-2-((трет-бутоксикарбонил)амино)-3-((6-(трифторметил)пиридин-2-ил)окси)пропановая кислота
Указанное в заголовке соединение получали с выходом 70% (580 мг, бесцветное твердое вещество) из (R)-метил 3-((6-(трифторметил)пиридин-2-ил)окси)-2-(тритиламино)пропаноата (1200 мг, 2,4 ммоль) аналогично стадии 2 промежуточного соединения 16.
MS (ESI) m/z: 251 (M-Boc+H)+, 349 (M-H)-.
{0244} Промежуточное соединение 21: (R)-2-((трет-бутоксикарбонил)амино)-3-(4-фторфенокси)пропановая кислота
{0245} Стадия 1: (R)-метил 3-(4-фторфенокси)-2-(тритиламино)пропаноат
Указанное в заголовке соединение получали с выходом 15% (96 мг, бесцветная смола) из (R)-метил 3-гидрокси-2-(тритиламино)пропаноата (0,50 г, 1,4 ммоль) и 4-фторфенола (0,20 г, 1,8 ммоль) аналогично стадии 1 промежуточного соединения 1.
MS (ESI) m/z: 478 (M+Na)+ и наблюдался сигнал фрагмента с массой 243 (положительный ион).
{0246} Стадия 2: (R)-2-((трет-бутоксикарбонил)амино)-3-(4-фторфенокси)пропановая кислота
Указанное в заголовке соединение получали с выходом 72% (45 мг, бесцветное масло) из (R)-метил 3-(4-фторфенокси)-2-(тритиламино)пропаноата (95 мг, 0,21 ммоль) аналогично стадии 2 промежуточного соединения 16.
ЯМР 1H (270 MГц, CDCl3): дельта 7,00-6,93 (2H, м), 6,86-6,80 (2H, м), 5,49 (1H, д, J=7,9 Гц), 4,68 (1H, д, J=8,6 Гц), 4,40 (1H, дд, J=9,2, 2,6 Гц), 4,19 (1H, дд, J=9,2, 3,3 Гц).
MS (ESI) m/z: 300 (M+H)+, 298 (M-H)-.
{0247} {Таблица 4-1}
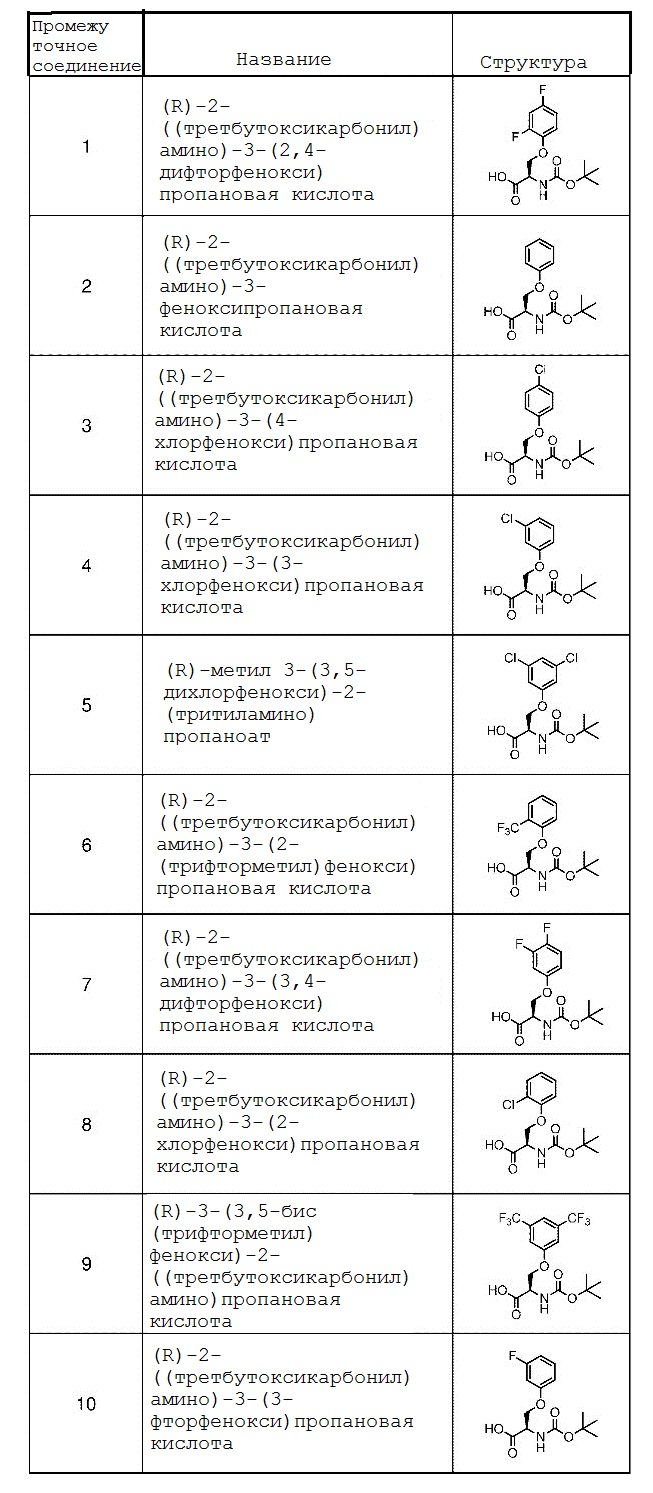
{0248} {Таблица 4-2}
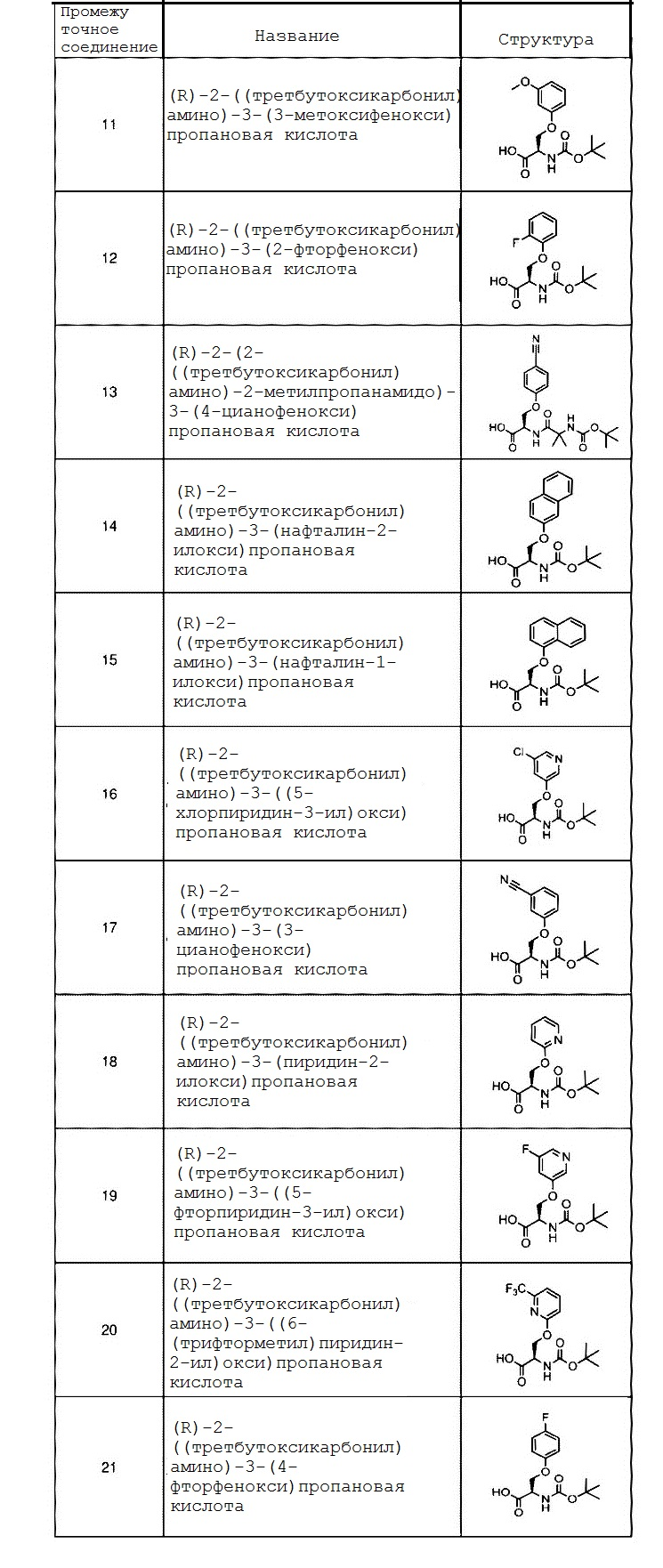
{0249} Пример 1: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(2,4-дифторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид
{0250} Стадия 1: Трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(2,4-дифторфенокси)-1-оксопропан-2-ил)карбамат
Суспензию (R)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (2R,3R)-2,3-дигидросукцинат (100 мг, 0,25 ммоль) в EtOAc (3 мл) охлаждали до -5°C в атмосфере азота и прибавляли к суспензии триэтиламин (0,18 мл, 1,3 моль) при той же температуре. После перемешивания в течение 20 мин к смеси последовательно прибавляли при той же температуре раствор (R)-2-((трет-бутоксикарбонил)амино)-3-(2,4-дифторфенокси)пропановой кислоты (113 мг, 0,36 ммоль, стадия 3 промежуточного соединения 1) в EtOAc (2 мл) и 2,4,6-трипропил-1,3,5,2,4,6-триокситрифосфинан 2,4,6-триоксид (0,30 мл, 0,51 ммоль; 1,7 M раствор в EtOAc). После перемешивания в течение 1 ч при -5°C, смесь гасили добавлением насыщенного водного раствора NaHCO3 (5 мл). Смесь разбавляли водой и экстрагировали EtOAc (20 мл x 3). Объединенные органические слои промывали насыщенным раствором соли и сушили над Na2SO4. После фильтрования фильтрат концентрировали в вакууме. Остаток очищали колоночной хроматографией (силикагель, элюирование 50% EtOAc в гексане), получая указанное в заголовке соединение в виде бесцветного твердого вещества (72 мг, выход 52%).
MS (ESI) m/z: 543 (M+H)+
{0251} Стадия 2: (R)-5-((R)-2-амино-3-(2,4-дифторфенокси)пропаноил)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-он
К перемешиваемому раствору трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(2,4-дифторфенокси)-1-оксопропан-2-ил)карбамата (70 мг, 0,13 ммоль) в DCM (1 мл) прибавляли трифторуксусную кислоту (1 мл) в виде одной порции при 0°C, и продолжали перемешивание в течение 1 ч при той же температуре. Смесь концентрировали в вакууме и разбавляли остаток DCM (5 мл). Экстракт промывали насыщенным водным раствором NaHCO3, а затем насыщенным раствором соли, и сушили над Na2SO4. После фильтрования фильтрат концентрировали в вакууме, получая указанное в заголовке соединение в виде бесцветной смолы (66 мг, выход >99%).
MS (ESI) m/z: 443 (M+H)+
{0252} Стадия 3: Трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(2,4-дифторфенокси)-1-оксопропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамат
К раствору (R)-5-((R)-2-амино-3-(2,4-дифторфенокси)пропаноил)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (66 мг, 0,15 ммоль), 2-((трет-бутоксикарбонил)амино)-2-метилпропановой кислоты (38 мг, 0,19 ммоль) и триэтиламина (0,083 мл, 0,60 ммоль) в DCM (1 мл) прибавляли гексафторфосфат O-(бензотриазол-1-ил)-N,N,N',N'-тетраметилурония (HBTU, 68 мг, 0,18 ммоль) при комнатной температуре. После перемешивания в течение 1 ч смесь концентрировали в вакууме. Остаток пропускали через колоткую хроматографическую колонку (амино-гель, элюирование EtOAc), получая указанное в заголовке соединение в виде бесцветной смолы (60 мг, выход 87%).
MS (ESI) m/z: 628 (M+H)+, 626 (M-H)-
{0253} Стадия 4: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(2,4-дифторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид
К перемешиваемому раствору трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(2,4-дифторфенокси)-1-оксопропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамата (81 мг, 0,13 ммоль) в DCM (1 мл) прибавляли трифторуксусную кислоту (1 мл) в виде одной порции при 0°C, и продолжали перемешивалие в течение 2 ч при той же температуре. Смесь концентрировали в вакууме и разбавляли остаток DCM (5 мл). Раствор промывали насыщенным водным раствором NaHCO3, а затем насыщенным раствором соли, и сушили над Na2SO4. После фильтрования растворитель и летучие вещества удаляли. Остаток очищали препаративной ЖХ-МС, получая 11 мг (выход 16%) указанного в заголовке соединения.
Условия препаративной ЖХ-МС и способа контроля качества (КК) приведены в таблице 5.
{0254} Пример 2: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-феноксипропан-2-ил)-2-метилпропанамид
{0255} Стадия 1: Трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-феноксипропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 50% (510 мг, твердое вещество белого цвета) из (2R,3R)-2,3-дигидроксисукцината (R)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (800 мг, 2,0 ммоль) и (R)-2-((трет-бутоксикарбонил)амино)-3-феноксипропановой кислоты (630 мг, 2,2 ммоль, стадия 3 промежуточного соединения 2) аналогично стадии 1 примера 1.
ЯМР 1H (300 MГц, CDCl3) дельта 7,31-7,15 (5H, м), 7,10-6,90 (3H, м), 6,87 (2H, д, J=7,9 Гц), 5,52-5,42 (1H, м), 5,23-5,05 (2H, м), 4,61-4,50 (1H, m), 4,26-4,08 (2H, м), 3,23 (1H, д, J=13,2 Гц), 3,09 (3H, с), 3,08-2,90 (2H, м), 2,66-2,50 (2H, м), 1,45 (9H, с). Сигнал NHBoc не наблюдался.
MS (ESI) m/z: 507 (M+H)+, 505 (M-H)-.
{0256} Стадия 2: (R)-5-((R)-2-амино-3-феноксипропаноил)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-он
Указанное в заголовке соединение получали с выходом 95% (390 мг, твердое вещество белого цвета) из трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-феноксипропан-2-ил)карбамата (800 мг, 2,0 ммоль) аналогично стадии 2 примера 1.
MS (ESI) m/z: 407 (M+H)+.
{0257} Стадия 3: Трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-феноксипропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 99% (560 мг, твердое вещество белого цвета) из (R)-5-((R)-2-амино-3-феноксипропаноил)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (390 мг, 0,96 ммоль) и 2-((трет-бутоксикарбонил)амино)-2-метилпропановой кислоты (230 мг, 1,2 ммоль) аналогично стадии 3 примера 1.
ЯМР 1H (300 MГц, CDCl3) дельта 7,35-7,12 (5H, м), 7,10-7,04 (2H, м), 7,00-6,84 (3H, м), 5,52-5,42 (1H, м), 5,07 (1H, д, J=12,5 Гц), 4,85 (1H, уш.с.), 4,64-4,52 (1H, м), 4,30-4,22 (1H, м), 4,16-4,10 (1H, м), 3,19 (1H, д, J=13,8 Гц), 3,07 (3H, с), 3,05-2,85 (2H, м), 2,64-2,50 (2H, м), 1,51 (3H, с), 1,49 (3H, с), 1,38 (9H, с). Сигналы CONH и NHBoc не наблюдались.
MS (ESI) m/z: 592 (M+H)+, 590 (M-H)-.
{0258} Стадия 4: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-феноксипропан-2-ил)-2-метилпропанамид
Указанное в заголовке соединение получали с выходом 86% (395 мг, твердое вещество белого цвета) из трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-феноксипропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамата (550 мг, 0,93 ммоль) аналогично стадии 4 примера 1. В данном случае указанное в заголовке соединение очищали колоночной хроматогарфией (NH-гель, элюирование от 0% до 80% EtOAc в гексане).
ЯМР 1H (300 MГц, CDCl3) дельта 8,45 (1H, д, J=7,3 Гц), 7,30-7,15 (5H, м), 7,12-6,85 (5H, м), 5,45-5,35 (1H, м), 5,09 (1H, д, J=12,5 Гц), 4,61 (1H, д, J=10,6 Гц), 4,24 (2H, д, J=6,6 Гц), 3,22 (1H, д,J=13,1 Гц), 3,08 (3H, с), 3,10-2,85 (3H, м), 2,65-2,48 (2H, м), 1,40 (3H, с), 1,35 (3H, с). Сигнал NH2 не наблюдался.
MS (ESI) m/z: 492 (M+H)+, 490 (M-H)-.
Часть продукта дополнительно очищали препаративной ЖХ-МС хроматографией, получая указанное в заголовке соединение.
{0259} Пример 3: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(4-хлорфенокси)-1-оксопропан-2-ил)-2-метилпропанамид
{0260} Стадия 1: Трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(4-хлорфенокси)-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 53% (73 мг, твердое вещество белого цвета) из (R)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-он (2R,3R)-2,3-дигидроксисукцината (100 мг, 0,25 ммоль) и (R)-2-((трет-бутоксикарбонил)амино)-3-(4-хлорфенокси)пропановой кислоты (110 мг, 0,36 ммоль, стадия 3 промежуточного соединения 3) аналогично стадии 1 примера 1.
MS (ESI) m/z: 541 (M+H)+.
{0261} Стадия 2: (R)-5-((R)-2-амино-3-(4-хлорфенокси)пропаноил)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-он
Указанное в заголовке соединение получали с выходом >99% (61 мг, бесцветная смола) из трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(4-хлорфенокси)-1-оксопропан-2-ил)карбамата (70 мг, 0,13 ммоль) аналогично стадии 2 примера 1.
MS (ESI) m/z: 441 (M+H)+.
{0262} Стадия 3: Трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразоло[4,3-c]пиридин-5(3H)-ил)-3-(4-хлорфенокси)-1-оксопропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамата
Указанное в заголовке соединение получали с выходом 94% (81 мг, бесцветная смола) из (R)-5-((R)-2-амино-3-(4-хлорфенокси)пропаноил)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (61 мг, 0,14 ммоль) и 2-((трет-бутоксикарбонил)амино)-2-метилпропановой кислоты (35 мг, 0,17 ммоль) аналогично стадии 3 примера 1.
ЯМР 1H (300 MГц, CDCl3) дельта 7,31-7,18 (5H, м), 7,09-7,08 (2H, м), 6,82 (2H, д, J=8,8 Гц), 5,46 (1H, кв, J=7,1 Гц), 5,08 (1H, д, J=12,5 Гц), 4,86 (1H, s), 4,62-4,51 (1H, m), 4,31-4,20 (1H, м), 4,16-4,03 (1H, м), 3,19 (1H, д, J=13,9 Гц), 3,08-2,86 (7H, м), 2,65-2,53 (2H, м), 1,50 (3H, с), 1,49 (3H, с), 1,37 (9H, с).
MS (ESI) m/z: 626 (M+H)+, 624 (M-H)-.
{0263} Стадия 4: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(4-хлорфенокси)-1-оксопропан-2-ил)-2-метилпропанамид
Указанное в заголовке соединение получали с выходом 16% (11 мг) из трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(4-хлорфенокси)-1-оксопропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамата (81 мг, 0,13 ммоль) аналогично стадии 4 примера 1.
{0264} Пример 4: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-хлорфенокси)-1-оксопропан-2-ил)-2-метилпропанамид
{0265} Стадия 1: Трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-хлорфенокси)-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 61% (105 мг, бесцветная смола) из (R)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-он (2R,3R)-2,3-дигидроксисукцината (100 мг, 0,25 ммоль) и (R)-2-((трет-бутоксикарбонил)амино)-3-(3-хлорфенокси)пропановой кислоты (120 мг, 0,38 ммоль, стадия 3 синтеза промежуточного соединения 4) аналогично стадии 1 примера 1.
MS (ESI) m/z: 541 (M+H)+.
{0266} Стадия 2: (R)-5-((R)-2-амино-3-(3-хлорфенокси)пропаноил)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-он
Указанное в заголовке соединение получали с выходом >99% (79 мг, бесцветная смола) из трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-хлорфенокси)-1-оксопропан-2-ил)карбамата (95 мг, 0,18 ммоль) аналогично стадии 2 примера 1.
MS (ESI) m/z: 441 (M+H)+.
{0267} Стадия 3: Трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-хлорфенокси)-1-оксопропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом >99% (100 мг, бесцветная смола) из (R)-5-((R)-2-амино-3-(3-хлорфенокси)пропаноил)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (68 мг, 0,15 ммоль) и 2-((трет-бутоксикарбонил)амино)-2-метилпропановой кислоты (39 мг, 0,19 ммоль) аналогично стадии 3 примера 1.
MS (ESI) m/z: 626 (M+H)+, 624 (M-H)-.
{0268} Стадии 4: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-хлорфенокси)-1-оксопропан-2-ил)-2-метилпропанамид
Указанное в заголовке соединение получали с выходом 14% (11 мг) из трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-хлорфенокси)-1-оксопропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамата (92 мг, 0,15 ммоль) аналогично стадии 4 примера 1.
{0269} Пример 5: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3,5-дихлорфенокси)-1-оксопропан-2-ил)-2-метилпропанамид
{0270} Стадия 1: Трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3,5-дихлорфенокси)-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 47% (86 мг, бесцветная смола) из (2R,3R)-2,3-дигидроксисукцината (R)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (130 мг, 0,32 ммоль) и (R)-2-((трет-бутоксикарбонил)амино)-3-(3,5-дихлорфенокси)пропановой кислоты (130 мг, 0,38 ммоль, стадия 3 синтеза промежуточного соединения 5) аналогично стадии 1 примера 1.
MS (ESI) m/z: 575 (M+H)+.
{0271} Стадия 2: (R)-5-((R)-2-амино-3-(3,5-дихлорфенокси)пропаноил)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-он
Указанное в заголовке соединение получали с выходом >99% (70 мг, бесцветная смола) из трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3,5-дихлорфенокси)-1-оксопропан-2-ил)карбамата (76 мг, 0,13 ммоль) аналогично стадии 2 примера 1.
MS (ESI) m/z: 475 (M+H)+.
{0272} Стадия 3: Трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3,5-дихлорфенокси)-1-оксопропан-2-ил)амино)-2-метил-1-оксопропан-2-)карбамат
Указанное в заголовке соединение получали с выходом >99% (89 мг, бесцветная смола) из (R)-5-((R)-2-амино-3-(3,5-дихлорфенокси)пропаноил)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (61 мг, 0,13 ммоль) и 2-((трет-бутоксикарбонил)амино)-2-метилпропановой кислоты (33 мг, 0,16 ммоль) аналогично стадии 3 примера 1.
MS (ESI) m/z: 660 (M+H)+, 658 (M-H)-.
{0273} Стадия 4: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3,5-дихлорфенокси)-1-оксопропан-2-ил)-2-метилпропанамид
Указанное в заголовке соединение получали с выходом 18% (12 мг) из трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3,5-дихлорфенокси)-1-оксопропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамата (81 мг, 0,12 ммоль) аналогично стадии 4 примера 1.
{0274} Пример 6: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-(2-(трифторметил)фенокси)пропан-2-ил)-2-метилпропанамид
{0275} Стадия 1: Трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-(2-(трифторметил)фенокси)пропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 66% (77 мг, бесцветная смола) из (2R,3R)-2,3-дигидроксисукцината (R)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (130 мг, 0,32 ммоль) и (R)-2-((трет-бутоксикарбонил)амино)-3-(2-(трифторметил)фенокси)пропановой кислоты (85 мг, 0,24 ммоль, стадия 3 синтеза промежуточного соединения 6) аналогично стадии 1 примера 1.
MS (ESI) m/z: 575 (M+H)+, 573 (M-H)-.
{0276} Стадия 2: (R)-5-((R)-2-амино-3-(2-(трифторметил)фенокси)пропаноил)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-он
Указанное в заголовке соединение получали с выходом 86% (45 мг) из трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-(2-(трифторметил)фенокси)пропан-2-ил)карбамата (64 мг, 0,11 ммоль) аналогично стадии 2 примера 1.
{0277} Стадия 3: Трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-(2-(трифторметил)фенокси)пропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом >99% (79 мг, бесцветная смола) из (R)-5-((R)-2-амино-3-(2-(трифторметил)фенокси)пропаноил)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (45 мг, 0,095 ммоль) и 2-((трет-бутоксикарбонил)амино)-2-метилпропановой кислотой (23 мг, 0,11 ммоль) аналогично стадии 3 примера 1.
MS (ESI) m/z: 660 (M+H)+, 658 (M-H)-.
{0278} Стадия 4: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-(2-(трифторметил)фенокси)пропан-2-ил)-2-метилпропанамид
Указанное в заголовке соединение получали с выходом 22% (14 мг) из трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-(2-(трифторметил)фенокси)пропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамата (75 мг, 0,11 ммоль) аналогично стадии 4 примера 1.
{0279} Пример 7: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3,4-дифторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид
{0280} Стадия 1: Трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3,4-дифторфенокси)-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 66% (73 мг, бесцветная смола) из (2R,3R)-2,3-дигидроксисукцината (R)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (130 мг, 0,32 ммоль) и (R)-2-((трет-бутоксикарбонил)амино)-3-(3,4-дифторфенокси)пропановой кислоты (77 мг, 0,24 ммоль, стадия 3 синтеза промежуточного соединения 7) аналогично стадии 1 примера 1.
MS (ESI) m/z: 543 (M+H)+, 541 (M-H)-.
{0281} Стадия 2: (R)-5-((R)-2-амино-3-(3,4-дифторфенокси)пропаноил)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-он
Указанное в заголовке соединение получали с выходом 92% (54 мг) из трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3,4-дифторфенокси)-1-оксопропан-2-ил)карбамата (72 мг, 0,13 ммоль) аналогично стадии 2 примера 1.
MS (ESI) m/z: 443 (M+H)+.
{0282} Стадия 3: Трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3,4-дифторфенокси)-1-оксопропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом >99% (91 мг, бесцветная смола) из (R)-5-((R)-2-амино-3-(3,4-дифторфенокси)пропаноил)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (54 мг, 0,12 ммоль) и 2-((трет-бутоксикарбонил)амино)-2-метилпропановой кислоты (23 мг, 0,11 ммоль) аналогично стадии 3 примера 1.
MS (ESI) m/z: 628 (M+H)+, 626 (M-H)-.
{0283} Стадия 4: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3,4-дифторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид
Указанное в заголовке соединение получали с выходом 15% (12 мг) из трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3,4-дифторфенокси)-1-оксопропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамата (91 мг, 0,15 ммоль) аналогично стадии 4 примера 1.
{0284} Пример 8: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(2-хлорфенокси)-1-оксопропан-2-ил)-2-метилпропанамид
{0285} Стадия 1: Трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(2-хлорфенокси)-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 60% (66 мг, бесцветное твердое вещество) из (2R,3R)-2,3-дигидроксисукцината (R)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-он (80 мг, 0,20 ммоль) и (R)-2-((трет-бутоксикарбонил)амино)-3-(2-хлорфенокси)пропановой кислоты (77 мг, 0,24 ммоль, стадия 3 синтеза промежуточного соединения 8) аналогично стадии 1 примера 1.
MS (ESI) m/z: 541 (M+H)+, 539 (M-H)-.
{0286} Стадия 2: (R)-5-((R)-2-амино-3-(2-хлорфенокси)пропаноил)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-он
Указанное в заголовке соединение получали с выходом >99% (58 мг) из трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(2-хлорфенокси)-1-оксопропан-2-ил)карбамата (61 мг, 0,11 ммоль) аналогично стадии 2 примера 1.
MS (ESI) m/z: 441 (M+H)+.
{0287} Стадия 3: Трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(2-хлорфенокси)-1-оксопропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 96% (79 мг, бесцветная смола) из (R)-5-((R)-2-амино-3-(2-хлорфенокси)пропаноил)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (58 мг, 0,13 ммоль) и 2-((трет-бутоксикарбонил)амино)-2-метилпропановой кислоты (32 мг, 0,16 ммоль) аналогично стадии 3 примера 1.
MS (ESI) m/z: 626 (M+H)+, 624 (M-H)-.
{0288} Стадия 4: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(2-хлорфенокси)-1-оксопропан-2-ил)-2-метилпропанамид
Указанное в заголовке соединение получали с выходом 22% (13 мг) из трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(2-хлорфенокси)-1-оксопропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамата (69 мг, 0,11 ммоль) аналогично стадии 4 примера 1.
{0289} Пример 9: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3,5-бис(трифторметил)фенокси)-1-оксопропан-2-ил)-2-метилпропанамид
{0290} Стадия 1: Трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3,5-бис(трифторметил)фенокси)-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 43% (54 мг, бесцветная смола) из (2R,3R)-2,3-дигидроксисукцината (R)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридил-3(3aH)-она (80 мг, 0,20 ммоль) и (R)-3-(3,5-бис(трифторметил)фенокси)-2-((трет-бутоксикарбонил)амино)пропановой кислоты (100 мг, 0,24 ммоль, стадия 3 синтеза промежуточного соединения 9) аналогично стадии 1 примера 1.
MS (ESI) m/z: 643 (M+H)+, 641 (M-H)-.
{0291} Стадия 2: (R)-5-((R)-2-амино-3-(3,5-бис(трифторметил)фенокси)пропаноил)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-он
Указанное в заголовке соединение получали с выходом 91% (40 мг) из трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3,5-бис(трифторметил)фенокси)-1-оксопропан-2-ил)карбамата (52 мг, 0,081 ммоль) аналогично стадии 2 примера 1.
MS (ESI) m/z: 543 (M+H)+.
{0292} Стадия 3: Трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3,5-бис(трифторметил)фенокси)-1-оксопропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом >99% (55 мг, бесцветная смола) из (R)-5-((R)-2-амино-3-(3,5-бис(трифторметил)фенокси)пропаноил)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (40 мг, 0,074 ммоль) и 2-((трет-бутоксикарбонил)амино)-2-метилпропановой кислоты (32 мг, 0,16 ммоль) аналогично стадии 3 примера 1.
MS (ESI) m/z: 728 (M+H)+, 726 (M-H)-.
{0293} Стадия 4: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3,5-бис(трифторметил)фенокси)-1-оксопропан-2-ил)-2-метилпропанамид
Указанное в заголовке соединение получали с выходом 32% (14 мг) из трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3,5-бис(трифторметил)фенокси)-1-оксопропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамата (50 мг, 0,069 ммоль) аналогично стадии 4 примера 1.
{0294} Пример 10: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-фторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид
{0295} Стадия 1: Трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-фторфенокси)-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 45% (48 мг, бесцветная смола) из (2R,3R)-2,3-дигидроксисукцината (R)-3a-бензин-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (80 мг, 0,20 ммоль) и (R)-2-((трет-бутоксикарбонил)амино)-3-(3-фторфенокси)пропановой кислоты (79 мг, 0,26 ммоль, стадия 3 синтез промежуточного соединения 10) аналогично стадии 1 примера 1.
MS (ESI) m/z: 525 (M+H)+, 523 (M-H)-.
{0296} Стадия 2: Трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-фторфенокси)-1-оксопропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамат
К перемешиваемому раствору трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-фторфенокси)-1-оксопропан-2-ил)карбамата (30 мг, 0,057 ммоль) в DCM (2 мл) прибавляли трифторуксусную кислоту (2 мл) в виде одной порции при 0°C, и продолжали перемешивание в течение 2 ч при той же температуре. Смесь концентрировали в вакууме, получая густой раствор желтого цвета. Остаток растворяли в DCM (4 мл). К смеси добавляли триэтиламин (0,017 мл, 0,23 ммоль) и гексафторфосфат O-(бензотриазол-1-ил)-N,N,N',N'-тетраметилурония (HBTU, 27 мг, 0,072 ммоль) при комнатной температуре. После перемешивания в течение 1 ч смесь концентрировали в вакууме. Остаток пропускали через короткую хроматографическую колонку (амино-гель, элюирование EtOAc), получая указанное в заголовке соединение в виде твердого вещества белого цвета (51 мг, выход >99%).
MS (ESI) m/z: 610 (M+H)+, 608 (M-H)-.
{0297} Стадия 3: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-фторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид
Указанное в заголовке соединение получали с выходом 32% (13 мг, бесцветная смола) из трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-фторфенокси)-1-оксопропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамата (48 мг, 0,079 ммоль) аналогично стадии 4 примера 1.
{0298} Пример 11: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-метоксифенокси)-1-оксопропан-2-ил)-2-метилпропанамид
{0299} Стадия 1: Трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-метоксифенокси)-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 62% (85 мг, бесцветная смола) из (2R,3R)-2,3-дигидроксисукцината (R)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (80 мг, 0,20 ммоль) и (R)-2-((трет-бутоксикарбонил)амино)-3-(3-метоксифенокси)пропановой кислоты (103 мг, 0,33 ммоль, стадия 3 синтеза промежуточного соединения 11) аналогично стадии 1 примера 1.
MS (ESI) m/z: 537 (M+H)+, 535 (M-H)-.
{0300} Стадия 2: Трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-метоксифенокси)-1-оксопропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 96% (78 мг, твердое вещество белого цвета) из трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-метоксифенокси)-1-оксопропан-2-ил)карбамата (70 мг, 0,13 ммоль) аналогично стадии 2 примера 10.
MS (ESI) m/z: 622 (M+H)+, 620 (M-H)-.
{0301} Стадия 3: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-метоксифенокси)-1-оксопропан-2-ил)-2-метилпропанамид
Указанное в заголовке соединение получали с выходом 18% (9 мг) из трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-метоксифенокси)-1-оксопропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамата (60 мг, 0,097 ммоль) аналогично стадии 4 примера 1.
{0302} Пример 12: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(2-фторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид
{0303} Стадия 1: Трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(2-фторфенокси)-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 57% (76 мг, бесцветная смола) из (2R,3R)-2,3-дигидроксисукцината (R)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (100 мг, 0,25 ммоль) и (R)-2-((трет-бутоксикарбонил)амино)-3-(2-фторфенокси)пропановой кислоты (114 мг, 0,38 ммоль, стадия 3 синтеза промежуточного соединения 12) аналогично стадии 1 примера 1.
MS (ESI) m/z: 525 (M+H)+, 523 (M-H)-.
{0304} Стадия 2: Трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(2-фторфенокси)-1-оксопропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом >99 % (74 мг, бесцветная смола) из трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(2-фторфенокси)-1-оксопропан-2-ил)карбамата (60 мг, 0,11 ммоль) аналогично стадии 2 примера 10.
MS (ESI) m/z: 610 (M+H)+, 608 (M-H)-.
{0305} Стадия 3: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(2-фторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид
Указанное в заголовке соединение получали с выходом 22% (11 мг) из трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(2-фторфенокси)-1-оксопропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамата (60 мг, 0,098 ммоль) аналогично стадии 4 примера 1.
{0306} Пример 13: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(нафталин-2-илокси)-1-оксопропан-2-ил)-2-метилпропанамид
{0307} Стадия 1: Трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(нафталин-2-илокси)-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 45% (90 мг, твердое вещество белого цвета) из (2R,3R)-2,3-дигидроксисукцината (R)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (140 мг, 0,36 ммоль) и (R)-2-((трет-бутоксикарбонил)амино)-3-(нафталин-2-илокси)пропановой кислоты (130 мг, 0,39 ммоль, стадия 3 синтеза промежуточного соединения 14) аналогично стадии 1 примера 1.
MS (ESI) m/z: 557 (M+H)+, 555 (M-H)-.
{0308} Стадия 2: Трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(нафталин-2-илокси)-1-оксопропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом >99% (100 мг, бесцветная смола) из трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(нафталин-2-илокси)-1-оксопропан-2-ил)карбамата (87 мг, 0,15 ммоль) аналогично стадии 2 примера 10.
MS (ESI) m/z: 642 (M+H)+, 640 (M-H)-.
{0309} Стадия 3: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(нафталин-2-илокси)-1-оксопропан-2-ил)-2-метилпропанамид
Указанное в заголовке соединение получали с выходом 14% (13 мг) из трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(нафталин-2-илокси)-1-оксопропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамата (100 мг, 0,16 ммоль) аналогично стадии 4 примера 1.
{0310} Пример 14: 2-Амино-N-((R)-1-((R)-3a-бензин-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(нафталин-1-илокси)-1-оксопропан-2-ил)-2-метилпропанамид
{0311} Стадия 1: Трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(нафталин-1-илокси)-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 67% (140 мг, бесцветная смола) из (2R,3R)-2,3-дигидроксисукцината (R)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (150 мг, 0,38 ммоль) и (R)-2-((трет-бутоксикарбонил)амино)-3-(нафталин-1-илокси)пропановой кислоты (150 мг, 0,46 ммоль, стадия 3 синтеза промежуточного соединения 145) аналогично стадии 1 примера 1.
MS (ESI) m/z: 557 (M+H)+, 555 (M-H)-.
{0312} Стадия 2: Трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(нафталин-1-илокси)-1-оксопропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 82% (120 мг, бесцветная смола) из трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(нафталин-1-илокси)-1-оксопропан-2-ил)карбамата (130 мг, 0,23 ммоль) аналогично стадии 2 примера 10.
MS (ESI) m/z: 642 (M+H)+, 640 (M-H)-.
{0313} Стадия 3: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(нафталин-1-илокси)-1-оксопропан-2-ил)-2-метилпропанамид
Указанное в заголовке соединение получали с выходом 14% (13 мг) из трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(нафталин-1-илокси)-1-оксопропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамата (110 мг, 0,17 ммоль) аналогично стадии 4 примера 1.
{0314} Пример 15: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-((5-хлорпиридин-3-ил)окси)-1-оксопропан-2-ил)-2-метилпропанамид
{0315} Стадия 1: Трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-((5-хлорпиридин-3-ил)окси)-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 53% (170 мг, бесцветная смола) из (2R,3R)-2,3-дигидроксисукцината (R)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (250 мг, 0,64 ммоль) и (R)-2-((трет-бутоксикарбонил)амино)-3-((5-хлорпиридин-3-ил)окси)пропановой кислоты (180 мг, 0,58 ммоль, стадия 2 синтеза промежуточного соединения 16) аналогично стадии 1 примера 1.
MS (ESI) m/z: 542 (M+H)+, 540 (M-H)-.
{0316} Стадия 2: Трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-((5-хлорпиридин-3-ил)окси)-1-оксопропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 86% (170 мг, твердое вещество белого цвета) из требутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-((5-хлорпиридин-3-ил)окси)-1-оксопропан-2-ил)карбамат (160 мг, 0,30 ммоль) аналогично стадии 1 примера 10.
MS (ESI) m/z: 627 (M+H)+, 625 (M-H)-.
{0317} Стадия 3: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-((5-хлорпиридин-3-ил)окси)-1-оксопропан-2-ил)-2-метилпропанамид
Указанное в заголовке соединение получали с выходом 11% (16 мг) из трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-((5-хлорпиридин-3-ил)окси)-1-оксопропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамата (170 мг, 0,27 ммоль) аналогично стадии 4 примера 1.
{0318} Пример 16: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-цианофенокси)-1-оксопропан-2-ил)-2-метилпропанамид
{0319} Стадия 1: Трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-цианофенокси)-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 42% (110 мг, бесцветная смола) из (2R,3R)-2,3-дигидроксисукцината (R)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (190 мг, 0,48 ммоль) и (R)-2-((трет-бутоксикарбонил)амино)-3-(3-цианофенокси)пропановой кислоты (150 мг, 0,48 ммоль, стадия 3 синтеза промежуточного соединения 17) аналогично стадии 1 примера 1.
MS (ESI) m/z: 532 (M+H)+, 530 (M-H)-.
{0320} Стадия 2: Трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-цианофенокси)-1-оксопропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом >99% (113 мг, бесцветная смола) из трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-цианофенокси)-1-оксопропан-2-ил)карбамата (86 мг, 0,16 ммоль) аналогично стадии 2 примера 10.
MS (ESI) m/z: 617 (M+H)+, 615 (M-H)-.
{0321} Стадия 3: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-цианофенокси)-1-оксопропан-2-ил)-2-метилпропанамид
Указанное в заголовке соединение получали с выходом 14% (12 мг) из трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-цианофенокси)-1-оксопропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамата (100 мг, 0,17 ммоль, Стадия X примера X) аналогично стадии 4 примера 1.
{0322} Пример 17: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-(пиридин-2-илокси)пропан-2-ил)-2-метилпропанамид
{0323} Стадия 1: Трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-(пиридин-2-илокси)пропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 68% (140 мг, бесцветная смола) из (2R,3R)-2,3-дигидроксисукцината (R)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (160 мг, 0,41 ммоль) и (R)-2-((трет-бутоксикарбонил)амино)-3-(пиридин-2-илокси)пропановой кислоты (140 мг, 0,49 ммоль, стадия 2 синтеза промежуточного соединения 18) аналогично стадии 1 примера 1.
MS (ESI) m/z: 508 (M+H)+, 506 (M-H)-.
{0324} Стадия 2: Трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-(пиридин-2-илокси)пропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 86% (130 мг, бесцветная смола) из трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-(пиридин-2-илокси)пропан-2-ил)карбамата (130 мг, 0,25 ммоль) аналогично стадии 2 примера 10.
MS (ESI) m/z: 593 (M+H)+, 591 (M-H)-.
{0325} Стадия 3: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-(пиридин-2-илокси)пропан-2-ил)-2-метилпропанамид
Указанное в заголовке соединение получали с выходом 12% (12 мг) из трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-(пиридин-2-илокси)пропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамата (120 мг, 0,20 ммоль) аналогично стадии 4 примера 1.
{0326} Пример 18: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-((5-фторпиридин-3-ил)окси)-1-оксопропан-2-ил)-2-метилпропанамид
{0327} Стадия 1: Трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-((5-фторпиридин-3-ил)окси)-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 58% (120 мг, бесцветное твердое вещество) из (2R,3R)-2,3-дигидроксисукцината ( (R)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она 150 мг, 0,38 ммоль) и (R)-2-((трет-бутоксикарбонил)амино)-3-((5-фторпиридин-3-ил)окси)пропановой кислоты (130 мг, 0,42 ммоль, стадия 2 синтеза промежуточного соединения 19) аналогично стадии 1 примера 1.
MS (ESI) m/z: 526 (M+H)+, 524 (M-H)-
{0328} Стадия 2: Трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-((5-фторпиридин-3-ил)окси)-1-оксопропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 95% (120 мг, бесцветная смола) из трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-((5-фторпиридин-3-ил)окси)-1-оксопропан-2-ил)карбамата (110 мг, 0,20 ммоль) аналогично стадии 2 примера 10.
MS (ESI) m/z: 611 (M+H)+, 609 (M-H)-.
{0329} Стадия 3: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-((5-фторпиридин-3-ил)окси)-1-оксопропан-2-ил)-2-метилпропанамид
Указанное в заголовке соединение получали с выходом 15% (13 мг) из трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-((5-фторпиридин-3-ил)окси)-1-оксопропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамата (110 мг, 0,17 ммоль) аналогично стадии 4 примера 1.
{0330} Пример 19: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-((6-(трифторметил)пиридин-2-ил)окси)пропан-2-ил)-2-метилпропанамид
{0331} Стадия 1: Трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-((6-(трифторметил)пиридин-2-ил)окси)пропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 78% (170 мг, бесцветное твердое вещество) из (2R,3R)-2,3-дигидроксисукцината (R)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (150 мг, 0,38 ммоль) и (R)-2-((трет-бутоксикарбонил)амино)-3-((6-(трифторметил)пиридин-2-ил)окси)пропановой кислоты (150 мг, 0,42 ммоль, стадия 2 синтеза промежуточного соединения 20) аналогично стадии 1 примера 1.
MS (ESI) m/z: 576 (M+H)+, 574 (M-H)-
{0332} Стадия 2: Трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-((6-(трифторметил)пиридин-2-ил)окси)пропан-2-ил) амино)-2-метил-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 98% (180 мг, бесцветная смола) из трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-((6-(трифторметил)пиридин-2-ил)окси)пропан-2-ил)карбамата (160 мг, 0,28 ммоль) аналогично стадии 2 примера 10.
MS (ESI) m/z: 661 (M+H)+, 659 (M-H)-.
{0333} Стадия 3: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-((6-(трифторметил)пиридин-2-ил)окси)пропан-2-ил)-2-метилпропанамид
Указанное в заголовке соединение получали с выходом 8% (12 мг) трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-((6-(трифторметил)пиридин-2-ил)окси)пропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамата (170 мг, 0,26 ммоль) аналогично стадии 4 примера 1.
{0334} Пример 20: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(4-цианофенокси)-1-оксопропан-2-ил)-2-метилпропанамид
{0335} Стадия 1: Трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(4-цианофенокси)-1-оксопропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 36% (29 мг, твердое вещество белого цвета) из (2R,3R)-2,3-дигидроксисукцината (R)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (51 мг, 0,13 ммоль) и (R)-2-(2-((трет-бутоксикарбонил)амино)-2-метилпропанамидо)-3-(4-цианофенокси)пропановой кислоты (51 мг, 0,13 ммоль, стадия 3 синтеза промежуточного соединения 13) аналогично стадии 1 примера 1.
MS (ESI) m/z: 617 (M+H)+, 617 (M-H)-
{0336} Стадия 2: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(4-цианофенокси)-1-оксопропан-2-ил)-2-метилпропанамид
Указанное в заголовке соединение получали с выходом 54% (13 мг) из трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(4-цианофенокси)-1-оксопропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамата (29 мг, 0,047 ммоль) аналогично стадии 4 примера 1.
{0337} Пример 21: 2-Амино-N-((R)-1-((R)-3a-бензил-2-(2,2-дифторэтил)-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-фенкосипропан-2-ил)-2-метилпропанамид
{0338} Стадия 1: Трет-бутил ((2R)-1-(3a-бензил-2-(2,2-дифторэтил)-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-феноксипропан-2-ил)карбамат (диастереомерная смесь)
Указанное в заголовке соединение получали с выходом 84% (120 мг, бесцветная смола) из 2,2,2-трифторацетата 3a-бензил-2-(2,2-дифторэтил)-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (100 мг, 0,26 ммоль, стадия 2 синтеза ядра 1) и (R)-2-((трет-бутоксикарбонил)амино)-3-феноксипропановой кислоты (86 мг, 0,31 ммоль, стадия 3 синтеза промежуточного соединения 2) аналогично стадии 1 примера 1.
MS (ESI) m/z: 557 (M+H)+, 555 (M-H)-
{0339} Стадия 2: Трет-бутил (1-(((2R)-1-(3a-бензил-2-(2,2-дифторэтил)-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-феносипропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамат (диастереомерная смесь)
Указанное в заголовке соединение получали с выходом >99% (200 мг, твердое вещество белого цвета) из трет-бутил ((2R)-1-(3a-бензил-2-(2,2-дифторэтил)-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-феноксипропан-2-ил) карбамата (120 мг, 0,22 ммоль) аналогично стадии 2 примера 10.
MS (ESI) m/z: 642 (M+H)+, 640 (M-H)-.
{0340} Стадия 3: 2-Амино-N-((R)-1-((R)-3a-бензил-2-(2,2-дифторэтил)-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-феноксипропан-2-ил)-2-метилпропанамид
Указанное в заголовке соединение получали с выходом 6% (10 мг) из трет-бутил (1-(((2R)-1-(3a-бензил-2-(2,2-дифторэтил)-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-феноксипропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамата (200 мг, 0,31 ммоль) аналогично стадии 4 примера 1.
В этом случае требуемый диастереомер выделяли в виде более полярного диастереомера в условиях препаративной ЖХ-МС.
{0341} Пример 22: 2-Амино-N-((R)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-феноксипропан-2-ил)-2-метилпропанамид
{0342} Стадия 1: Трет-бутил ((R)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-феноксипропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 40% (50 мг, бесцветная смола) из (2S,3S)-2,3-дигидроксисукцината (R)-2-(2,2-дифторэтил)-3a-(пиридин-2-илметил)-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (100 мг, 0,23 ммоль, стадия 3 синтеза ядра 2) и (R)-2-((трет-бутоксикарбонил)амино)-3-феноксипропановой кислоты (76 мг, 0,27 ммоль, стадия 3 синтеза промежуточного соединения 2) аналогично стадии 1 примера 1.
MS (ESI) m/z: 558 (M+H)+, 556 (M-H)-.
{0343} Стадия 2: (R)-5-((R)-2-амин -3-феноксипропаноил)-2-(2,2-дифторэтил)-3a-(пиридин-2-илметил)-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-он
К перемешиваемому раствору трет-бутил ((R)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-феноксипропан-2-ил)карбамата (50 мг, 0,090 ммоль) в DCM (1 мл) прибавляли трифторуксусную кислоту (5 мл) при комнатной темпепратуре и перемешивали смесь в течение 30 мин при той же температуре. Смесь концентрировали в вакууме. Остаток очищали на картридже с сильной катионообменной смолой (Isolute (зарегистрированная торговая марка) SCX, 1 г/6 мл, Biotage), получая указанное в заголовке соединение в виде прозрачной бесцветной смолы (35 мг, выход 84%).
MS (ESI) m/z: 458 (M+H)+.
{0344} Стадия 3: 2-Амино-N-((R)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-феноксипропан-2-ил)-2-метилпропанамид
Раствор (R)-5-((R)-2-амино-3-феноксипропаноил)-2-(2,2-дифторэтил)-3a-(пиридин-2-илметил)-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (34 мг, 0,074 ммоль) и 2-((трет-бутоксикарбонил)амино)-2-метилпропановой кислоты (18 мг, 0,089 ммоль) в EtOAc (2 мл) охлаждали до 0°C. К данной смеси последовательно прибавляли триэтиламин (0,031 мл, 0,22 ммоль) и 2,4,6-триоксид 2,4,6-трипропил-1,3,5,2,4,6-триоксатрифосфинана (0,087 мл, 0,15 ммоль; 1,7 M раствор в EtOAc) и перемешивали полученную смесь в течение 1 ч при той же температуре. Смесь концентрировали в вакууме. Затем к остатку прибавляли трифторуксусную кислоту (2 мл) и перемешивали смесь в течение 30 мин при комнатной температуре. Смесь концентрировали в вакууме. Остаток очищали на картридже с сильной катионообменной смолой (BondElute (зарегистрированная торговая марка) SCX, 1 г/6 мл, Varian Inc.), а затем дополнительно очищали препаративной ЖХ-МС, получая 10 мг (выход 25%) указанного в заголовке соединения.
{0345} Пример 23: 2-Амино-N-((R)-3-(2-хлорфенокси)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксопропан-2-ил)-2-метилпропанамид
{0346} Стадия 1: Трет-бутил ((R)-3-(2-хлорфенокси)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 30% (40 мг, бесцветная смола) из (2S,3S)-2,3-дигидроксисукцината (R)-2-(2,2-дифторэтил)-3a-(пиридин-2-илметил)-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (100 мг, 0,23 ммоль, стадия 3 синтеза ядра 2) и (R)-2-((трет-бутоксикарбонил)амино)-3-(2-хлорфенокси)пропановой кислоты (85 мг, 0,27 ммоль, стадия 3 синтеза промежуточного соединения 8) аналогично стадии 1 примера 1.
MS (ESI) m/z: 592 (M+H)+, 590 (M-H)-.
{0347} Стадия 2: (R)-5-((R)-2-амино-3-(2-хлорфенокси)пропаноил)-2-(2,2-дифторэтил)-3a-(пиридин-2-илметил)-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-он
Указанное в заголовке соединение получали с выходом 89% (33 мг, бесцветное масло) из трет-бутил ((R)-3-(2-хлорфенокси)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксопропан-2-ил) карбамата (40 мг, 0,068 ммоль) аналогично стадии 2 примера 22.
MS (ESI) m/z: 492 (M+H)+.
{0348} Стадия 3: 2-Амино-N-((R)-3-(2-хлорфенокси)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксопропан-2-ил)-2-метилпропанамид
Указанное в заголовке соединение получали с выходом 28% (10 мг) из (R)-5-((R)-2-амино-3-(2-хлорфенокси)пропаноил)-2-(2,2-дифторэтил)-3a-(пиридин-2-илметил)-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (30 мг, 0,060 ммоль) аналогично стадии 3 примера 22.
{0349} Пример 24: 2-Амино-N-((R)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(2-фторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид
{0350} Стадия 1: Трет-бутил ((R)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(2-фторфенокси)-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 31% (41 мг, бесцветная смола) из (2S,3S)-2,3-дигидроксисукцината (R)-2-(2,2-дифторэтил)-3a-(пиридин-2-илметил)-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (100 мг, 0,23 ммоль, стадия 3 синтеза ядра 2) и (R)-2-((трет-бутоксикарбонил)амино)-3-(2-фторфенокси)пропановой кислоты (81 мг, 0,27 ммоль, стадия 3 синтеза промежуточного соединения 12) аналогично стадии 1 примера 1.
MS (ESI) m/z: 576 (M+H)+, 574 (M-H)-.
{0351} Стадия 2: (R)-5-((R)-2-амино-3-(2-фторфенокси)пропаноил)-2-(2,2-дифторэтил)-3a-(пиридин-2-илметил)-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-он
Указанное в заголовке соединение получали с выходом 92% (31 мг, бесцветное масло) из трет-бутил ((R)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(2-фторфенокси)-1-оксопропан-2-ил)карбамата (41 мг, 0,071 ммоль) аналогично стадии 2 примера 22.
MS (ESI) m/z: 476 (M+H)+.
{0352} Стадия 3: 2-Амино-N-((R)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил 3-(2-фторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид
Указанное в заголовке соединение получали с выходом 30% (11 мг) из (R)-5-((R)-2-амино-3-(2-фторфенокси)пропаноил)-2-(2,2-дифторэтил)-3a-(пиридин-2-илметил)-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (31 мг, 0,065 ммоль) аналогично стадии 3 примера 22.
{0353} Пример 25: 2-Амино-N-((R)-3-(3-хлорфенокси)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксопропан-2-ил)-2-метилпропанамид
{0354} Стадия 1: Трет-бутил ((R)-3-(3-хлорфенокси)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 37% (49 мг, бесцветная смола) из (2S,3S)-2,3-дигидроксисукцината (R)-2-(2,2-дифторэтил)-3a-(пиридин-2-илметил)-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (100 мг, 0,23 ммоль, стадия 3 синтеза ядра 2) и (R)-2-((трет-бутоксикарбонил)амино)-3-(3-хлорфенокси)пропановой кислоты (85 мг, 0,27 ммоль, стадия 3 синтеза промежуточного соединения 4) аналогично стадии 1 примера 1.
MS (ESI) m/z: 592 (M+H)+, 590 (M-H)-.
{0355} Стадия 2: (R)-5-((R)-2-амино-3-(3-хлорфенокси) пропаноил)-2-(2,2-дифторэтил)-3a-(пиридин-2-илметил)-4,5,6,7-тетрагидро-2H-пиразо[4,3-c]пиридин-3(3aH)-он
Указанное в заголовке соединение получали с выходом 87% (36 мг, бесцветное масло) из трет-бутил ((R)-3-(3-хлорфенокси)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксопропан-2-ил) карбамата (49 мг, 0,083 ммоль) аналогично стадии 2 примера 22.
MS (ESI) m/z: 492 (M+H)+.
{0356} Стадия 3: 2-Амино-N-((R)-3-(3-хлорфенокси)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксопропан-2-ил)-2-метилпропанамид
Указанное в заголовке соединение получали с выходом 22% (9 мг) из (R)-5-((R)-2-амино-3-(3-хлорфенокси)пропаноил)-2-(2,2-дифторэтил)-3a-(пиридин-2-илметил)-4,5,6,7-тетрагидро-2H-пиразол [4,3-c]пиридин-3(3aH)-она (36 мг, 0,072 ммоль, стадия 3 примера 22) аналогично стадии 3 примера 22.
{0357} Пример 26: 2-Амино-N-((R)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-метоксифенокси)-1-оксопропан-2-ил)-2-метилпропанамид
{0358} Стадия 1: Трет-бутил ((R)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-метоксифенокси)-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 48% (64 мг, бесцветная смола) из (2S,3S)-2,3-дигидроксисукцината (R)-2-(2,2-дифторэтил)-3a-(пиридин-2-илметил)-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (100 мг, 0,23 ммоль, стадия 3 синтеза ядра 2) и (R)-2-((трет-бутоксикарбонил)амино)-3-(3-methoxyphenoxy) пропановой кислоты (84 мг, 0,27 ммоль, стадия 3 синтеза промежуточного соединения 11) аналогично стадии 1 примера 1.
MS (ESI) m/z: 588 (M+H)+, 586 (M-H)-.
{0359} Стадия 2: (R)-5-((R)-2-амино-3-(3-метоксифенокси) пропаноил)-2-(2,2-дифторэтил)-3a-(пиридин-2-илметил)-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-он
Указанное в заголовке соединение получали с выходом 82% (43 мг, бесцветное масло) трет-бутил ((R)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-метоксифенокси)-1-оксопропан-2-ил) карбамата (64 мг, 0.11 ммоль) аналогично стадии 2 примера 22.
MS (ESI) m/z: 488 (M+H)+.
{0360} Стадия 3: 2-Амино-N-((R)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-метоксифенокси)-1-оксопропан-2-ил)-2-метилпропанамид
Указанное в заголовке соединение получали с выходом 24% (12 мг) из (R)-5-((R)-2-амино-3-(3-метоксифенокси)пропаноил)-2-(2,2-дифторэтил)-3a-(пиридин-2-илметил)-4,5,6,7-тетрагидро-2H-пиразол [4,3-c]пиридин-3(3aH)-она (43 мг, 0,089 ммоль) аналогично стадии 3 примера 22.
{0361} Пример 27: 2-Амино-N-((R)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-фторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид
{0362} Стадия 1: Трет-бутил ((R)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-фторфенокси)-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 36% (47 мг, бесцветная смола) из (2S,3S)-2,3-дигидроксисукцината (R)-2-(2,2-дифторэтил)-3a-(пиридин-2-илметил)-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (100 мг, 0,23 ммоль, стадия 3 синтеза ядра 2) и (R)-2-((трет-бутоксикарбонил)амино)-3-(3-фторфенокси)пропановой кислоты (100 мг, 0,34 ммоль, стадия 3 синтеза промежуточного соединения 10) аналогично стадии 1 примера 1.
MS (ESI) m/z: 576 (M+H)+, 574 (M-H)-.
{0363} Стадия 2: (R)-5-((R)-2-амино-3-(3-фторфенокси) пропаноил)-2-(2,2-дифторэтил)-3a-(пиридин-2-илметил)-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-он
Указанное в заголовке соединение получали с выходом 91% (35 мг, бесцветное масло) из трет-бутил ((R)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-фторфенокси)-1-оксопропан-2-ил)карбамата (47 мг, 0,082 ммоль) аналогично стадии 2 примера 22.
MS (ESI) m/z: 476 (M+H)+.
{0364} Стадия 3: 2-Амино-N-((R)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-фторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид
Указанное в заголовке соединение получали с выходом 36% (15 мг) из (R)-5-((R)-2-амино-3-(3-фторфенокси)пропаноил)-2-(2,2-дифторэтил)-3a-(пиридин-2-илметил)-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (35 мг, 0,074 ммоль) аналогично стадии 2 примера 22.
{0365} Пример 28: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(4-фторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид
{0366} Стадия 1: Трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(4-фторфенокси)-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 56% (45 мг, твердое вещество белого цвета) из (2R,3R)-2,3-дигидроксисукцината (R)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (60 мг, 0,15 ммоль) и (R)-2-((трет-бутоксикарбонил)амино)-3-(4-фторфенокси)пропановой кислоты (45 мг, 0,15 ммоль, стадия 2 синтеза промежуточного соединения 16) аналогично стадии 1 примера 1.
MS (ESI) m/z: 525 (M+H)+, 523 (M-H)-.
{0367} Стадия 2: (R)-5-((R)-2-амино-3-(4-фторфенокси) пропаноил)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-он
Указанное в заголовке соединение получали с количественным выходом (37 мг, бесцветное масло) из трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(4-фторфенокси)-1-оксопропан-2-ил)карбамата (45 мг, 0,086 ммоль) аналогично стадии 2 примера 1.
{0368} Стадия 3: Трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(4-фторфенокси)-1-оксопропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 96% (50 мг, бесцветное масло) из (R)-5-((R)-2-амино-3-(4-фторфенокси) пропаноил)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол [4,3-c] пиридин-3(3aH)-она (37 мг, 0,86 ммоль) и 2-((трет-бутоксикарбонил) амино)-2-метилпропановой кислоты (26 мг, 1,3 ммоль) аналогично стадии 3 примера 1.
MS (ESI) m/z: 610 (M+H)+.
{0369} Стадия 4: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(4-фторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид
Указанное в заголовке соединение получали с выходом 22% (11 мг) из трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(4-фторфенокси)-1-оксопропан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамата (45 мг, 0,074 ммоль) аналогично стадии 4 примера 1.
Условия препаративной ЖХ-МС и способа контроля качества (КК) представлены в таблице 5.
{0370} {Таблица 5-1}
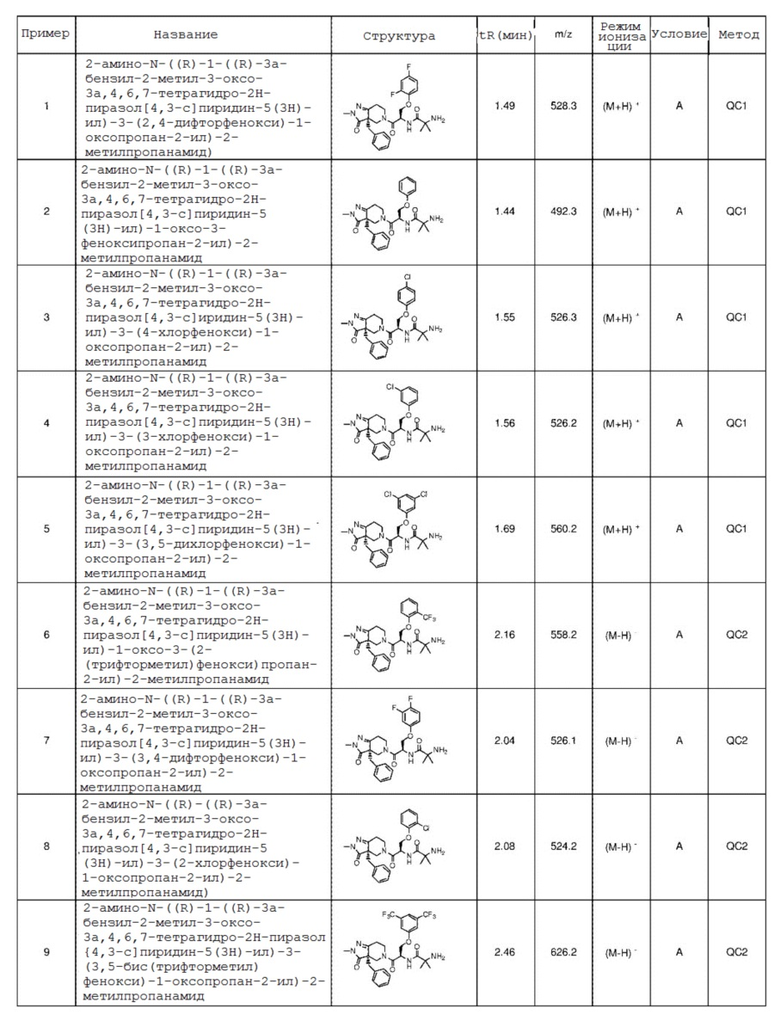
{371} {Таблица 5-2}
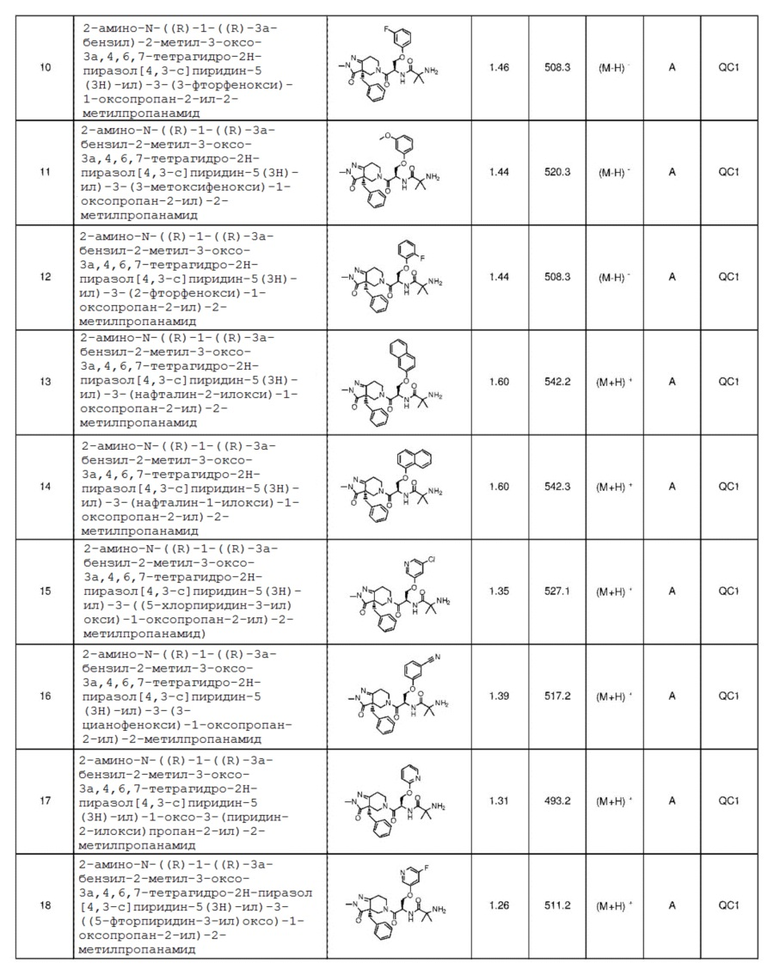
{0372}
{Таблица 5-3}
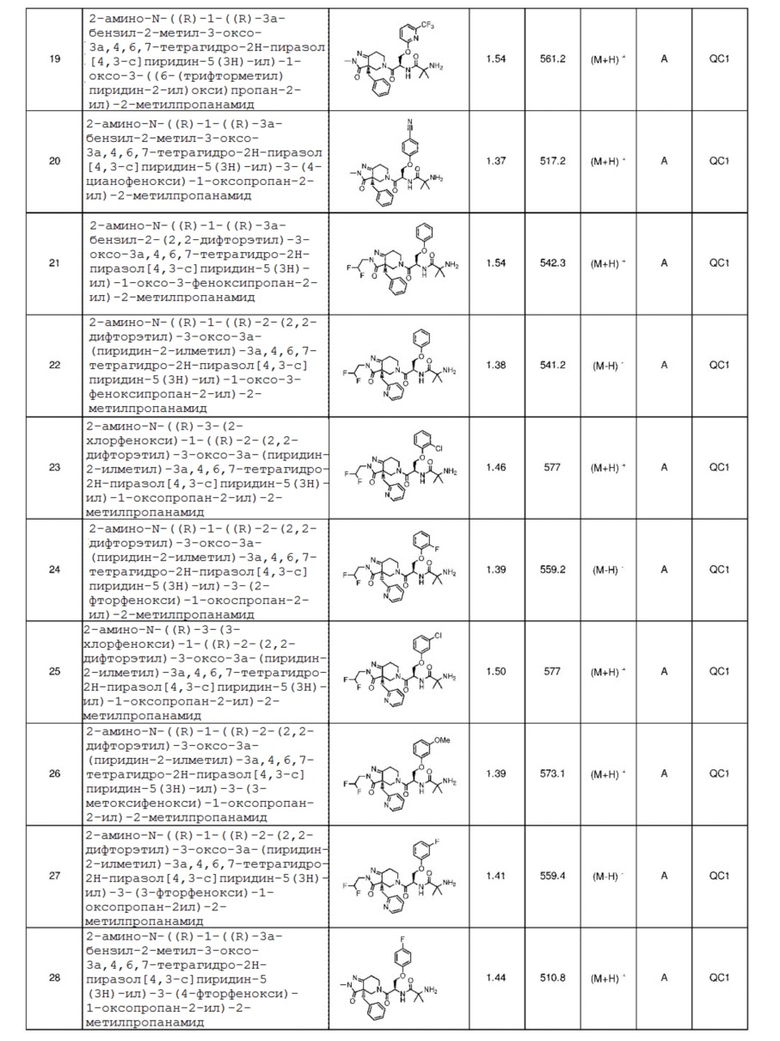
{0373} Пример сравнения 1: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-4-феноксибутан-2-ил)-2-метилпропанамид
{0374} Стадия 1: Трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-гидрокси-1-оксобутан-2-ил)карбамат
Суспензию (2R,3R)-2,3-дигидроксисукцината (R)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (1500 мг, 3,81 ммоль) в EtOAc (30 мл) охлаждали до -50°C в атмосфере азота и прибавляли по каплям триэтиламин (1,06 мл, 7,62 ммоль) при той же температуре, давая возможность образоваться свободному основанию из (2R,3R)-2,3-дигидроксисукцината (R)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она и получая соль с тартратом триэтиламмония. После перемешивания смеси в течение 15 мин прибавляли к смеси по каплям дополнительное количество триэтиламина (1,59 мл, 11,4 ммоль) и перемешивали смесь при -50°C в течение 10 мин. К смеси добавляли растворенный в EtOAc (20 мл) (R)-2-((трет-бутоксикарбонил)амино)-4-гидроксибутаноат триэтиламмония в течение 15 мин, и 2,4,6-триоксид 2,4,6-трипропил-1,3,5,2,4,6-триоксотрифосфинана (4,49 мл, 7,63 ммоль, 1,7 M раствор в EtOAc) в течение 10 мин. После перемешивания смеси еще в течение 2 ч при -50°C, реакционную смесь гасили добавлением насыщенного водного раствора NaHCO3 (50 мл) при той же температуре. Смесь нагревали до комнатной температуры, разбавляли водой (50 мл) и экстрагировали EtOAc (50 мл x3). Объединенные органические слои промывали насыщенным раствором соли и сушили над Na2SO4. После фильтрования фильтрат концентрировали в вакууме. Остаток очищали колоночной хроматографией (силикагель, элирование 5% MeOH в EtOAc), получая указанное в заголовке соединение в виде бесцветного твердого вещества (1170 мг, выход 69%).
MS (ESI) m/z: 445 (M+H)+.
{0375} Стадия 2: Трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-4-феноксибутан-2-ил)карбамат
К раствору трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-гидрокси-1-оксобутан-2-ил)карбамата (200 мг, 0,45 ммоль), фенола (64 мг, 0,68 ммоль) и трифенилфосфина (236 мг, 0,90 ммоль) в ТГФ (8 мл) прибавляли по каплям раствор бис(2-метоксиэтил)азодикарбоксилата (211 мг, 0,90 ммоль) в ТГФ (1 мл) при 0°C. После перемешивания при комнатной температуре в течение ночи смесь разбавляли водой и экстрагировали EtOAc. Экстракт промывали насыщенным водным раствором NaHCO3 и насыщенным водным раствором соли и сушили над Na2SO4. После фильтрования фильтрат концентрировали в вакууме. Остаток очищали колоночной хроматографией (силикагель, от 15% до 50% EtOAc в гексане), получая указанное в заголовке соединение (194 мг, выход 83%) в виде твердого вещества белого цвета.
MS (ESI) m/z: 521 (M+H)+.
{0376} Стадия 3: (R)-5-((R)-2-амино-4-феноксибутаноил)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-он
К раствору трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-4-феноксибутан-2-ил)карбамата (194 мг, 0,37 ммоль) в DCM (5 мл) прибавляли трифторуксусную кислоту (2 мл) при 0°C и перемешивали смесь при той же температуре в течение 30 мин. Затем смесь концентрировали в вакууме, а остаток разбавляли DCM и промывали смесь насыщенным водным раствором NaHCO3, а затем насыщенным водным раствором соли и сушили над Na2SO4. После фильтрования фильтрат концентрировали в вакууме. Остаток очищали колоночной хроматографией (силикагель, от 10% до 50% EtOAc в гексане), получая указанное в заголовке соединение в виде бесцветной смолы (104 мг, выход 67%).
MS (ESI) m/z: 421 (M+H)+.
{0377} Стадия 4: Трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-4-феноксибутан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамат
К суспензии (R)-5-((R)-2-амино-4-феноксибутаноил)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (100 мг, 0,24 ммоль), 2-((трет-бутоксикарбонил)амино)-2-метилпропановой кислоты (73 мг, 0,36 ммоль) и триэтиламина (0,13 мл, 0,95 ммоль) в DCM (6 мл) прибавляли гексафторфосфат O-(бензотриазол-1-ил)-N,N,N',N'-тетраметилурония (HBTU, 48 мг, 0,36 ммоль) при комнатной температуре. После перемешивания при той же температуре в течение ночи, смесь концентрировали в вакууме. Остаток пропускали через короткую хроматографическую колонку (силикагель, элюирование от 2% до 20% EtOAc в гексане), получая указанное в заголовке соединение в виде бесцветного твердого вещества (131 мг, выход 91%).
MS (ESI) m/z: 506 (M-Boc+H)+.
{0378} Стадия 5: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-4-феноксибутан-2-ил)-2-метилпропанамид
К раствору трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-4-феноксибутан-2-ил)амино)-2-метил-1-оксопропан-2-ил) карбамата (130 мг, 0,22 ммоль) в DCM (4 мл) прибавляли трифторуксусную кислоту (2 мл) при 0°C. После перемешивания при той же температуре в течение 2 ч, смесь концентрировали в вакууме. Остаток разбавляли DCM и промывали смесь насыщенным водным раствором NaHCO3 и насыщенным водным раствором соли и сушили над Na2SO4. После фильтрования профильтрованный растворитель и летучие вещества удаляли. Остаток очищали препаративной ЖХ-МС, получая 9,4 мг (выход 9%) указанного в заголовке соединения в виде твердого вещества светло-коричневого цвета.
Условия препаративной ЖХ-МС и способ контроля качества (КК) представлены в таблице 6.
{0379} Пример сравнения 2: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-(3,4-дифторфенокси)-1-оксобутан-2-ил)-2-метилпропанамид
{0380} Стадия 1: Трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-(3,4-дифторфенокси)-1-оксобутан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом >99% (187 мг, масло) из трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо -3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-гидрокси-1-оксобутан-2-ил)карбамата (150 мг, 0,34 ммоль) и 3,4-дифторфенола (132 мг, 1,0 ммоль) аналогично стадии 2 примера 1.
MS (ESI) m/z: 557 (M+H)+, 555 (M-H)-.
{0381} Стадия 2: (R)-5-((R)-2-амино-4-(3,4-дифторфенокси)бутаноил)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-он
Указанное в заголовке соединение получали с выходом 41% (62 мг, твердое вещество желтого цвета) из трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-(3,4-дифторфенокси)-1-оксобутан-2-ил)карбамата (187 мг, 0,34 ммоль) аналогично стадии 3 примера 1.
MS (ESI) m/z: 457 (M+H)+.
{0382} Стадия 3: Трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-(3,4-дифторфенокси)-1-оксобутан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом >99% (84 мг, бесцветное твердое вещество) из (R)-5-((R)-2-амино-4-(3,4-дифторфенокси)бутаноил)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (60 мг, 0,13 ммоль) аналогично стадии 4 примера 1.
MS (ESI) m/z: 542 (M-Boc+H)+.
{0383} Стадия 4: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-(3,4-дифторфенокси)-1-оксобутан-2-ил)-2-метилпропанамид
Указанное в заголовке соединение получали с выходом 12% (9,3 мг) из трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-(3,4-дифторфенокси)-1-оксобутан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамата (84 мг, 0,13 ммоль) аналогично стадии 5 примера 1.
{0384} Пример сравнения 3: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-(3,5-бис(трифторметил)фенокси)-1-оксобутан-2-ил)-2-метилпропанамид
{0385} Стадия 1: Трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-(3,5-бис(трифторметил)фенокси)-1-оксобутан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 45% (213 мг, твердое вещество белого цвета) из трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-гидрокси-1-оксобутан-2-ил)карбамата (130 мг, 0,29 ммоль) и 3,5-бис(трифторметил)фенола (202 мг, 0,88 ммоль) аналогично стадии 2 примера 1.
MS (ESI) m/z: 601 (M-tBu+H)+.
{0386} Стадия 2: (R)-5-((R)-2-амино-4-(3,5-бис(трифторметил)фенокси)бутаноил)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-он
Указанное в заголовке соединение получали с выходом 62% (50 мг, твердое вещество коричневого цвета) из трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-(3,5-бис(трифторметил)фенокси)-1-оксобутан-2-ил)карбамата (213 мг, 0,15 ммоль) аналогично стадии 3 примера 1.
MS (ESI) m/z: 557 (M+H)+.
{0387} Стадия 3: Трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-(3,5-бис(трифторметил)фенокси)-1-оксобутан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом >99% (67 мг, твердое вещество белого цвета) из (R)-5-((R)-2-амино-4-(3,5-бис(трифторметил)фенокси)бутаноил)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (50 мг, 0,090 ммоль) аналогично стадии 4 примера 1.
MS (ESI) m/z: 742 (M+H)+.
{0388} Стадия 4: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-(3,5-бис(трифторметил)фенокси)-1-оксобутан-2-ил)-2-метилпропанамид
Указанное в заголовке соединение получали с выходом 23% (12 мг) из трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-(3,5-бис(трифторметил)фенокси)-1-оксобутан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамата (59 мг, 0,080 ммоль) аналогично стадии 5 примера 1.
{0389} Пример сравнения 4: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-(4-фторфенокси)-1-оксобутан-2-ил)-2 метилпропанамид
{0390} Стадия 1: Трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-(4-фторфенокси)-1-оксобутан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 45% (213 мг, твердое вещество белого цвета) из трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3c]пиридин-5(3H)-ил)-4-гидрокси-1-оксобутан-2-ил)карбамата (60 мг, 0,14 ммоль) и 4-фторфенола (30 мг, 0,27 ммоль) аналогично стадии 2 примера 1.
MS (ESI) m/z: 601 (M-tBu+H)+.
{0391} Стадия 2: (R)-5-((R)-2-амино-4-(4-фторфенокси)бутаноил)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-он
Указанное в заголовке соединение получали с выходом 13% (24 мг, смола коричневого цвета) из трет-бутил ((R)-1-((R)-3a-бензи-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-(4-фторфенокси)-1-оксобутан-2-ил)карбамата (191 мг, 0,43 ммоль) аналогично стадии 3 примера 1.
MS (ESI) m/z: 439 (M+H)+.
{0392} Стадия 3: Трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-(4-фторфенокси)-1-оксобутан-2-ил)амино)-2-метил-1-оксопропан-2-ил) карбамат
Указанное в заголовке соединение получали с выходом 82% (28 мг, бесцветная смола) из (R)-5-((R)-2-амино-4-(4-фторфенокси)бутаноил)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (24 мг, 0,055 ммоль) аналогично стадии 4 примера 1.
MS (ESI) m/z: 624 (M+H)+, 622 (M-H)-.
{0393} Стадия 4: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-(4-фторфенокси)-1-оксобутан-2-ил)-2-метилпропанамид
Указанное в заголовке соединение получали с выходом 42% (9,8 мг) из трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-(4-фторфенокси)-1-оксобутан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамата (28 мг, 0,045 ммоль) аналогично стадии 5 примера 1.
{0394} Пример сравнения 5: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-((5-фторпиридин-3-ил)окси)-1-оксобутан-2-ил)-2-метилпропанамид
{0395} Стадия 1: Трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-((5-фторпиридин-3-ил)окси)-1-оксобутан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом >99% (182 мг, смола бледно-коричневого цвета) из трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-гидрокси-1-оксобутан-2-ил)карбамата (150 мг, 0,34 ммоль) и 5-фторпиридин-3-ола (57 мг, 0,51 ммоль) аналогично стадии 2 примера 1.
MS (ESI) m/z: 540 (M+H)+.
{0396} Стадия 2: (R)-5-((R)-2-амино-4-((5-фторпиридин-3-ил)окси)бутаноил)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол [4,3-c]пиридин-3(3aH)-он
Указанное в заголовке соединение получали с выходом 21% (32 мг, твердое вещество светло-коричневого цвета) из трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-((5-фторпиридин-3-ил)окси)-1-оксобутан-2-ил)карбамата (182 мг, 0,34 ммоль) аналогично стадии 3 примера 1.
MS (ESI) m/z: 440 (M+H)+.
{0397} Стадия 3: Трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-((5-фторпиридин-3-ил)окси)-1-оксобутан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом 89% (38 мг, твердое вещество светло-коричневого цвета) из (R)-5-((R)-2-амино-4-((5-фторпиридин-3-ил)окси)бутаноил)-3a-бензил-2-метил-4,5,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-3(3aH)-она (30 мг, 0,068 ммоль) аналогично стадии 4 примера 1.
MS (ESI) m/z: 625 (M+H)+, 623 (M-H)-.
{0398} Стадия 4: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-((5-фторпиридин-3-ил)окси)-1-оксобутан-2-ил)-2-метилпропанамид
Указанное в заголовке соединение получали с выходом 32% (9,7 мг) из трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-((5-фторпиридин-3-ил)окси)-1-оксобутан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамата (38 мг, 0,061 ммоль) аналогично стадии 5 примера 1.
{0399} Пример сравнения 6: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-(3-цианофенокси)-1-оксобутан-2-ил)-2-метилпропанамид
{0400} Стадия 1: Трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-(3-цианофенокси)-1-оксобутан-2-ил)карбамат
К раствору трет-бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-гидрокси-1-оксобутан-2-ил)карбамата (150 мг, 0,34 ммоль), 3-гидроксибензонитрила (60 мг, 0,51 ммоль), и трибутилфосфина (0,17 мл, 0,38 ммоль) в ТГФ (2 мл) прибавляли по каплям раствор 1,1'-(азокарбонил)дипиперидина (170 мг, 0,65 ммоль) в ТГФ (4 мл) при 0°C. После перемешивания при комнатной температуре в течение 3 дней, смесь разбавляли насыщенным водным раствором NaHCO3 и EtOAc для разделения. Органический слой сушили над Na2SO4. После фильтрования фильтрат концентрировали в вакууме. Остаток очищали колоночной хроматографией (силикагель, от 50% до 75% EtOAc в гексане), получая указанное в заголовке соединение в виде бесцветной смолы (105 мг, выход 57%).
MS (ESI) m/z: 546 (M+H)+, 544 (M-H)-.
{0401} Стадия 2: 3-((R)-3-амино-4-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-оксобутокси)бензонитрил
Указанное в заголовке соединение получали с выходом >99% (74 мг, масло светло-коричневого цвета) из бутил ((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-(3-цианофенокси)-1-оксобутан-2-ил)карбамата (91 мг, 0,17 ммоль) аналогично стадии 3 примера 1.
MS (ESI) m/z: 446 (M+H)+.
{0402} Стадия 3: Трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-(3-цианофенокси)-1-оксобутан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамат
Указанное в заголовке соединение получали с выходом >99% (105 мг, смола желтого цвета) из 3-((R)-3-амино-4-((R)-3a-бензил -2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-оксобутокси)бензонитрила (74 мг, 0,17 ммоль) аналогично стадии 4 примера 1.
MS (ESI) m/z: 631 (M+H)+, 629 (M-H)-.
{0403} Стадия 4: 2-Амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-(3-цианофенокси)-1-оксобутан-2-ил)-2-метилпропанамид
Указанное в заголовке соединение получали с выходом 19% (17 мг) из трет-бутил (1-(((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-4-(3-цианофенокси)-1-оксобутан-2-ил)амино)-2-метил-1-оксопропан-2-ил)карбамата (105 мг, 0,17 ммоль) аналогично стадии 5 примера 1.
{0404} {Таблица 6}
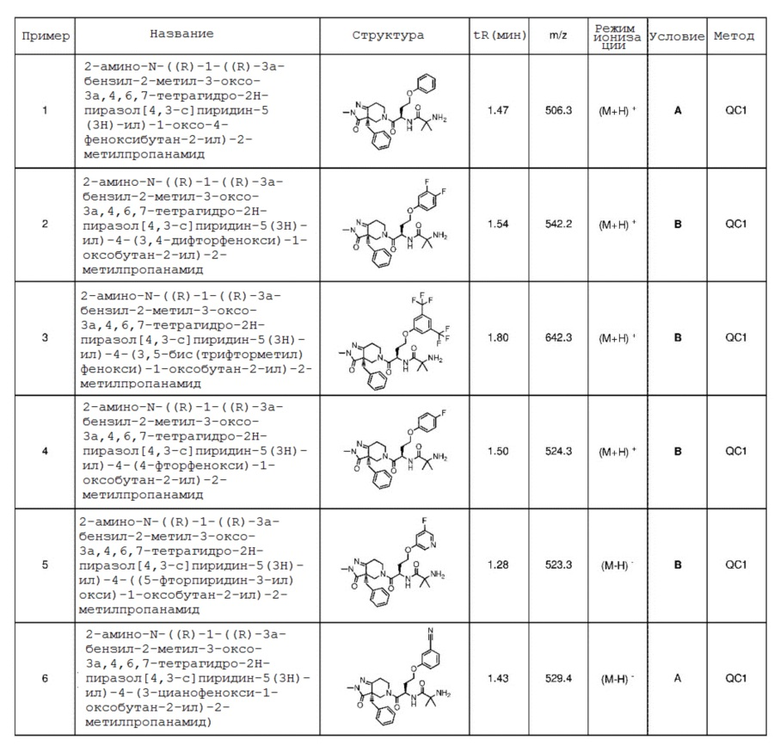
{0405} Фармакологические исследования in vitro
{0406} Измерение инфлюкса Ca2+ в клетки HEK293, стабильно экспрессирующие человеческий грелиновый рецептор, вызванного агонистической активностью грелинового рецептора
Клетки HEK293, стабильно экспрессирующие человеческий грелиновый рецептор, содержали в модифицированной по способу Дульбекко среде Игла (с высоким содержание глюкозы) с добавкой 10% фетальной бычьей сыворотки, 100 единиц/мл пенициллина, 100 микрог/мл стрептомицина и 500 микрог/мл G418 при 37°C во влажной камере, содержащей 5% CO2, и выращивали до конфлюэнтности 60-80%. За день до проведения анализа клетки высевали в 384-луночные планшеты с поли-D-лизиновым покрытием (BD FALCON) при плотности 10000 клеток на лунку, и выдерживали в течение ночи в инкубаторе.
{0407} В день анализа клетки трижды промывали буфером анализа (сбалансированный солевой раствор Хенкса, содержащий 20 мМ HEPES, pH7,4) и инкубировали в течение 1 часа при комнатной температуре для введения 0,5 микроМ реагента Fluo-4 AM (Invitrogen).
{0408} После удаления Fluo-4 и промывания буфером анализа в клетки добавляли соединения в различной концентрации. Мониторинг изменений во внутриклеточной концентрации кальция проводили при помощи спектрофотометра для чтения планшетов для визуализации флуоресценции FDSS6000 (Hamamatsu Photonics).
{0409} Значения EC50 для соединений по настоящему изобретению определяли из исследований 11-точечной зависимости доза-эффект. Кривые получали с использованием среднего дупликатных лунок для каждой экспериментальной точки. В итоге, значения EC50 вычисляли с использованием кривой дозы наилучшего приближения, определенной при помощи XLfit (ID Business Solutions Ltd).
{0410} В описанных выше анализах все тестированные соединения проявили EC50 примерно менее 500 наноМ. Предпочтительные соединения проявляют EC50 примерно менее 50 наноМ в описанных выше анализах.
Более предпочтительные соединения проявляют EC50 примерно менее 10 наноМ в описанных выше анализах.
{0411} Предпочтительные соединения представляют собой:
Соединения примеров 1-8, 10-14, 16 и 21-27.
{0412} Более предпочтительные соединения представляют собой:
Соединения примеров 9, 17, 18 и 20.
{0413} Таблица 7. Соотношение EC50 h-грелина для производного серина и производного гомосерина
{Таблица 7}
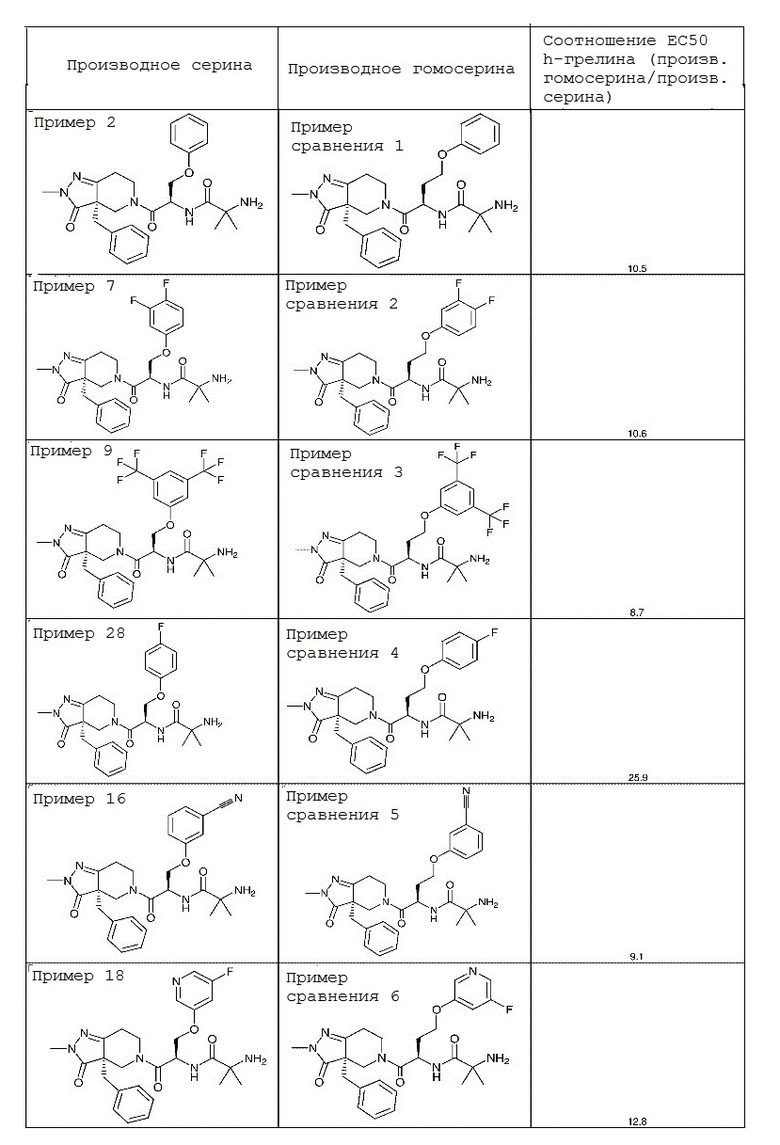
{0414} Фармакологические иследования in vivo
{0415} Отклик гормона роста (ГР) у мышей, находящихся в сознании
Самок мышей линии BALB/c (возраст 7 недель) приобретали у Charles River Japan и расселяли по четыре или пять животных в одну клетку. После голодания в течение ночи перорально вводили тестируемые соединия. Пробы крови отбирали через 5, 10, 30 минут после введения лекарственного препарата. Для каждого контрольного момента времени использовали двух или трех животных. Концентрацию ГР в плазме мыши измеряли при помощи набора EIA (EIA KIT для гормона роста крысы, SPI-Bio, Франция).
{0416} В описанном выше анализе соединения по настоящему изобретению проявляют концентрацию ГР в плазме крови мышей, большую или равную 15 нг/мл.
{0417} Как правило, для исследования грелиновых соединений использовали анестезированных крыс (ссылка на стандартный способ: Endocrinol Japan 31 (1984) 539-547, Journal of Endocrinology 171 (2001) 481-489, Gastroenterology 123 (2002) 1120-1128, Peptides 32 (2011)1001-1007). Поскольку в стандартных способах анализа требуется внутривенное введение тестируемых соединений, они не подходят для поискового исследования перорально вводимых лекарственных средств. Однако описанный выше анализ можно применять для перорального введения натощак, который применим для оценки высвобождения гормона роста тестируемых соединений при поиске новых лекарственных средств. Это первый пример способа анализа отклика гормона роста (ГР) на мышах натощак, находящихся в сознании, в котором производят оценку высвобождения гормона роста.
{0418} Эффект вызванной цисплатином кахексии/анорексии у крыс
Самцов крыс Male Wistar (возраст 7-8 недель) приобретали у Japan SLC, Inc. и расселяли индивидуально в помещении с контролируемой температурой и влажностью с 12-часовым циклом света и тьмы (свет включали в 8 часов утра). Крыс адаптировали к обстановке эксперимента, по меньшей мере, в течение 5 дней и дважды брали на руки. Пищу и воду давали по желанию. Крыс делили на две группы, а именно плацебо-контролируемую и получающую цисплатин группы. Начиная с 0 дня по 2 день внутрибрюшинно вводили цисплатин (0,6 мг/кг/сутки, Wako Pure Chemical) в конце светового цикла. Крысам плацебо-группы давали только физиологический раствор. Тестируемые соединения вводили перорально в течение 3 дней (от 0 дня по 2 день) непосредственно перед введением цисплатина. Для предупреждения вызванной цисплатином нефротоксичности, сразу после введения физиологического раствора или цисплатина подкожно вводили 2-3 мл физиологического раствора. Оценку массы тела и потребления пищи проводили ежедневно от 0 дня по 4 день.
{0419} Наблюдается статистически значимое снижение массы тела и потребления пищи у крыс, получающих цисплатин. Пероральное введение соединений существенно повышало массу тела и потребление пищи у крыс, получавших цисплатин.
{0420} В некоторых сообщениях имеются данные о том, что грелин влияет на снижение потребления пищи в течение короткого периода времени (ссылка на стандартный способ: Endocrinology 149 (2008) 455-460, Endocrinology 151 (2010) 3773-3782, Neurogastroenterol Motil 25 (2013) 373-e292, Peptides 46 (2013) 13-19, Vitamins and Hormones 92 (2013) 301-317). Отсутствуют сообщения о том, что агонисты грелина проявляют супрессию стойкой потери массы и супрессию снижения потребления пищи в течение 5-дневного исследования. При применении стандартных способов исследования в течение целых 5 дней, они приводили к неудаче вследствии вызванной цисплатином нефротоксичности у крыс. При решении данного вопроса были предприняты большие усилия. Окончательное изменение условий: 1) введение вечером, 2) использование крысы, с которой хорошо обращались, привыкавшей к обстановке эксперимента в течение, по меньшей мере, 5 дней, и которую брали на руки, по меньшей мере, дважды, и 3) введение физиологического раствора, неожиданно, приводит к успешным результатам, которые применимы для оценки кахексии/анорексии при поиске новых лекарственных средств. Это первый пример способа анализа вызванной цисплатином кахексии/анорексии у крыс.
{0421} Влияние на кахексию у крыс, имеющих клетки AH-130
Самцов крыс Male Wistar (возраст 4 недели) приобретали у Japan SLC, Inc. и расселяли индивидуально в помещении с контролируемой температурой и влажностью с 12-часовым циклом света и тьмы (свет включали в 8 часов утра). Крыс адаптировали к обстановке эксперимента, по меньшей мере, в течение 5 дней и дважды брали на руки. Пищу и воду давали по желанию. Крыс делили на две группы, а именно плацебо-контролируемую и группу носителей опухолей. Последним вводили внутрибрюшинно свыше 1×108 клеток асцитной гепатомы AH-130 (Tohoku University, Сендай, Япония) в 0 день. Крысам плацебо-группы давали только PBS. Группу носителей опухоли разделяли на получавших лечение и не получавших его, при этом первой группе вводили тестируемые соединения перорально в течение 9 дней (от 0 дня по 8 день) в конце световой фазы. Массу тела измеряли дважды в неделю. В конце эксперимента крыс умерщвляли действием CO2 и иссекали и взвешивали ткань большой грудной мышцы.
{0422} Через пять дней после заражения клетками асцитной гепатомы AH-130 масса тела заметно снижена по сравнению с плацебо-группой. У крыс, которым вводили соединения по настоящему изобретению, масса тела и масса большой грудной мышцы на 9 день значительно больше по сравнению с контрольной группой.
{0423} Сообщения о том, что агонисты грелина подавляют стойкую потерю массы, отсутствуют. При решении данного вопроса были предприняты большие усилия. Окончательное изменение условий: 1) использование неполовозрелых крыс вместо половозрелых крыс, 2) увеличение количества клеток (свыше 1×108 клеток асцитной гепатомы AH-130) и 3) введение вечером, неожиданно привело к успешным результатам. Данный способ анализа применим для оценки кахексии при поиске новых лекарственных средств. Это первый успешный пример способа анализа в отношении кахексии (потеря массы и мышечная атрофия) у крыс, имеющих клетки AH-130.
| название | год | авторы | номер документа |
|---|---|---|---|
| АМИДЫ КОНДЕНСИРОВАННОГО ПИПЕРИДИНА В КАЧЕСТВЕ МОДУЛЯТОРОВ ИОННЫХ КАНАЛОВ | 2014 |
|
RU2741810C2 |
| СТИМУЛЯТОРЫ СЕКРЕЦИИ ГОРМОНА РОСТА | 1996 |
|
RU2172742C2 |
| ГЕМИНАЛЬНО-ЗАМЕЩЕННЫЕ ЦИАНОЭТИЛПИРАЗОЛОПИРИДОНЫ В КАЧЕСТВЕ ИНГИБИТОРОВ JANUS КИНАЗ | 2014 |
|
RU2664533C2 |
| ПРОИЗВОДНЫЕ ПИРАЗОЛОПИРИДИНА В КАЧЕСТВЕ БЛОКАТОРОВ TTX-S | 2013 |
|
RU2652117C2 |
| БИЦИКЛИЧЕСКИЕ ЛАКТАМЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2716136C2 |
| ПРОЛЕКАРСТВА СОПРЯЖЕННО-БИЦИКЛИЧЕСКИХ АНТАГОНИСТОВ C5aR | 2019 |
|
RU2794327C2 |
| N-(2-ЦИАНОГЕТЕРОЦИКЛИЛ)ПИРАЗОЛОПИРИДОНЫ В КАЧЕСТВЕ ИНГИБИТОРОВ ЯНУС-КИНАЗЫ | 2014 |
|
RU2669922C2 |
| ПОЛИМОРФНЫЕ ФОРМЫ | 2014 |
|
RU2670978C9 |
| ЦИКЛОАЛКИЛНИТРИЛПИРАЗОЛОПИРИДОНЫ В КАЧЕСТВЕ ИНГИБИТОРОВ ЯНУС-КИНАЗЫ | 2014 |
|
RU2655380C2 |
| БИЦИКЛИЧЕСКИЕ ЛАКТАМЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2827714C1 |
Изобретение относится к соединению формулы (I)
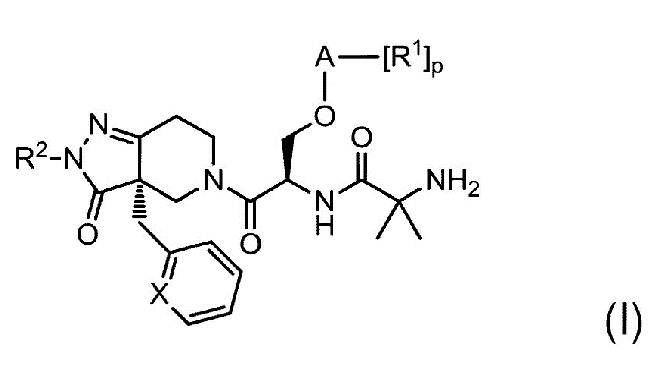 ,
,
в которой: A представляет собой фенил, нафтил или пиридил; X представляет собой CH или N; R1 независимо выбирают из группы, включающей (1) водород, (2) галоген, (3) C1-6 алкил, где алкил является незамещенным или замещен одним или более заместителями, независимо выбранными из галогена, (4) -O-C1-6 алкила, где алкил является незамещенным, и (5) -CN; R2 представляет собой водород или C1-6 алкил, где алкил является незамещенным или замещен одним или более заместителями, независимо выбранными из галогена; p равен 1 или 2; или его фармацевтически приемлемой соли, и их применению в терапии в качестве модулятора рецептора секретного гормона роста (называемого также грелиновым рецептором или рецептором GHSRla). 8 н. и 17 з.п. ф-лы, 7 табл., 28 пр.
1. Соединение следующей формулы (I)
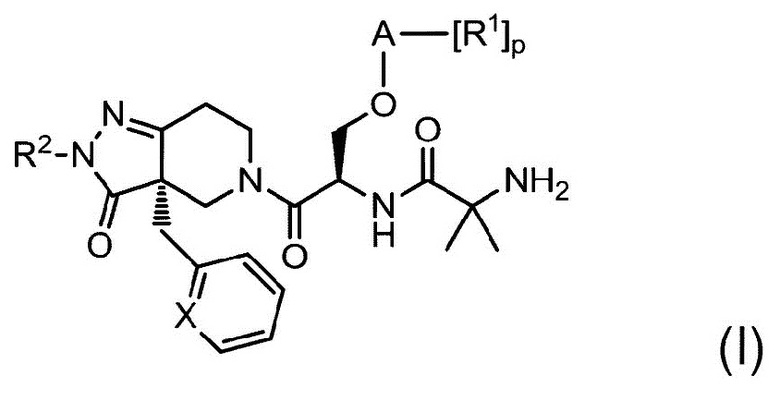
в которой:
A представляет собой фенил, нафтил или пиридил;
X представляет собой CH или N;
R1 независимо выбирают из группы, включающей (1) водород, (2) галоген, (3) C1-6 алкил, где алкил является незамещенным или замещен одним или более заместителями, независимо выбранными из галогена, (4) -O-C1-6 алкила, где алкил является незамещенным, и (5) -CN;
R2 представляет собой водород или C1-6 алкил, где алкил является незамещенным или замещен одним или более заместителями, независимо выбранными из галогена;
p равен 1 или 2;
или его фармацевтически приемлемая соль.
2. Соединение, представленное приведенной выше формулой (I), по п. 1,
в которой:
A представляет собой фенил, нафтил или пиридил,
R2 представляет собой водород или C1-6 алкил, где алкил является незамещенным или содержит от одного до трех заместителей, независимо выбранных из галогена,
или его фармацевтически приемлемая соль.
3. Соединение, представленное приведенной выше формулой (I), по п. 1,
в которой:
A представляет собой фенил, нафтил или пиридил,
R1 независимо выбирают из группы, включающей (1) водород, (2) галоген, (3) трифторметил, (4) трифторметокси, и (5) -CN;
R2 представляет собой C1-6 алкил, где алкил является незамещенным или содержит от одного до трех заместителей, независимо выбранных из галогена,
или его фармацевтически приемлемая соль.
4. Соединение, представленное приведенной выше формулой (I), по п.1,
в которой:
A представляет собой фенил, нафтил или пиридил,
R1 независимо выбирают из группы, включающей (1) водород, (2) -F, (3) -Cl, (4) трифторметил, (5) трифторметокси и (6) -CN;
R2 представляет собой метил или дифторэтил,
или его фармацевтически приемлемая соль.
5. Соединение, представленное приведенной выше формулой (I), по п. 1,
в которой:
A представляет собой фенил, 2-пиридил или 3-пиридил,
R1 независимо выбирают из группы, включающей (1) водород, (2) -F, (3) -Cl, (4) трифторметил, (5) трифторметокси и (5) -CN,
R2 представляет собой метил или 2,2-дифторэтил,
или его фармацевтически приемлемая соль.
6. Соединение по п. 1, где соединения выбирают из группы, включающей:
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(2,4-дифторфенокси)-1-оксопропан-2-ил)-2 метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-феноксипропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(4-хлорфенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-хлорфенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3,5-дихлорфенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-(2-(трифторметил)фенокси)пропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3,4-дифторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(2-хлорфенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3,5-бис(трифторметил)фенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-фторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-метоксифенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(2-фторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(нафталин-2-илокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(нафталин-1-илокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-((5-хлорпиридин-3-ил)окси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-цианофенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-(пиридин-2-илокси)пропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-((5-фторпиридин-3-ил)окси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-((6-(трифторметил)пиридин-2-ил)окси)пропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(4-цианофенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-(2,2-дифторэтил)-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-феноксипропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-феноксипропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-3-(2-хлорфенокси)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(2-фторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-3-(3-хлорфенокси)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-метоксифенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-фторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид; и
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(4-фторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
или его фармацевтически приемлемая соль.
7. Соединение по п. 1, где соединения выбирают из группы, включающей:
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(2,4-дифторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-феноксипропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3,4-дифторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-фторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-метоксифенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(2-фторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-цианофенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-1-оксо-3-феноксипропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(2-фторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-метоксифенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
2-амино-N-((R)-1-((R)-2-(2,2-дифторэтил)-3-оксо-3a-(пиридин-2-илметил)-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(3-фторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид и
2-амино-N-((R)-1-((R)-3a-бензил-2-метил-3-оксо-3a,4,6,7-тетрагидро-2H-пиразол[4,3-c]пиридин-5(3H)-ил)-3-(4-фторфенокси)-1-оксопропан-2-ил)-2-метилпропанамид;
или его фармацевтически приемлемой соли.
8. Фармацевтическая композиция, обладающая агонистической активностью грелинового рецептора, содержащая эффективное количество соединения или его фармацевтически приемлемой соли, как описано в п. 1, и фармацевтически приемлемый носитель.
9. Способ лечения животного, включая человека, страдающего состоянием или нарушением, опосредованным грелиновым рецептором, включающий введение упомянутому субъекту эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли по п. 1.
10. Способ по п. 9, в котором указанное состояние или нарушение выбирают из группы, включающей: раковую анорексию/кахексию, кахексию и анорексию, вызванные приемом противораковых препаратов, гипералгезию, вызванную приемом противораковых препаратов, ХОБЛ/кахексию при ХОБЛ, саркопению, нарушения пищевого поведения и неврологические нарушения пищевого поведения, подавление потери веса, восстановление в раннем послеоперационном периоде у раковых пациентов, хроническую инфекцию дыхательных путей, воспаление, ВЗК, ФД, констипацию, диабетический гастопарез и гастопарез, сердечную недостаточность, инфаркт миокарда, диабетическую невропатию, болезнь Паркинсона, рассеянный склероз, диагностику и лечение дефицита гормона роста, улучшение КЖ в пожилом возрасте, нарушение перистальтики кишечника у пациентов с травмой спинного мозга, послеоперационную кишечную непроходимость и кишечную непроходимость, вызванную приемом морфина, и их сочетания.
11. Применение соединения по п. 1, или его фармацевтически приемлемой соли, или его композиции, для получения лекарственного средства для лечения состояния или нарушения, опосредованного грелиновым рецептором.
12. Применение по п. 11, в котором указанное состояние или нарушение выбирают из группы, включающей: раковую анорексию/кахексию, кахексию и анорексию, вызванные приемом противораковых препаратов, гипералгезию, вызванную приемом противораковых препаратов, ХОБЛ/кахексию при ХОБЛ, саркопению, нарушения пищевого поведения и неврологические нарушения пищевого поведения, подавление потери веса, восстановление в раннем послеоперационном периоде у раковых пациентов, хроническую инфекцию дыхательных путей, воспаление, ВЗК, ФД, констипацию, диабетический гастопарез и гастопарез, сердечную недостаточность, инфаркт миокарда, диабетическую невропатию, болезнь Паркинсона, рассеянный склероз, диагностику и лечение дефицита гормона роста, улучшение КЖ в пожилом возрасте, нарушение перистальтики кишечника у пациентов с травмой спинного мозга, послеоперационную кишечную непроходимость и кишечную непроходимость, вызванную приемом морфина, и их сочетания.
13. Соединение по п. 1, или его фармацевтически приемлемая соль, для применения в лечении состояния или нарушения, опосредованного грелиновым рецептором.
14. Способ получения фармацевтической композиции, включающий смешивание соединения по п. 1, или его фармацевтически приемлемой соли, с фармацевтически приемлемым носителем, разбавителем или эксципиентом.
15. Способ анализа отклика гормона роста (ГР) у мышей натощак, находящихся в сознании, включающий пероральное введение соединения по п. 1 мышам линии BALB/c и измерение концентрации ГР в плазме мыши.
16. Способ исследования вызванной цисплатином кахексии/анорексии у крыс, включающий введение соединения по п. 1 перед введением цисплатина и введение физиологического раствора вечером крысам, имеющим хороший уход.
17. Способ исследования кахексии (потери массы и мышечной атрофии) у крыс, имеющих клетки AH-130, включающий пероральное введение соединения по п. 1 вечером половозрелым самцам крыс, получившим инъекцию свыше 1×108 клеток асцитной гепатомы AH-130.
| WO 1997024369 A1 10.07.1997 | |||
| Carpino, P | |||
| A., Lefker, B | |||
| A., Toler, S | |||
| M., Pan, L | |||
| C., Hadcock, J | |||
| R., Cook, E | |||
| R | |||
| Thompson, D | |||
| D | |||
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
| Pyrazolinone-piperidine dipeptide growth hormone secretagogues (GHSs) | |||
| Bioorganic & Medicinal Chemistry, 11(4), 581-590 | |||
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| WO 1995013069 A1 18.05.1995 | |||
| US 5652235 A 29.07.1997 | |||
| СПОСОБ ПОЛУЧЕНИЯ ПИРАЗОЛПИРИДИНОВОГО ПРОИЗВОДНОГО ИЛИ ЕГО СОЛИ | 1990 |
|
RU2007403C1 |
Авторы
Даты
2019-07-25—Публикация
2015-08-05—Подача