Изобретение относится к медицине, точнее к трансплантации органов, и может найти применение при подготовке реципиента к трансплантации.
Отсутствие эффективных лекарственных препаратов, повышающих синтетическую функцию печени у пациентов с различной степенью выраженности печеночной недостаточности, стимулирует разработку новых технологий терапии для пациентов с терминальной стадией заболевания печени.
В настоящее время единственным способом решения этой проблемы является трансплантация печени. Поскольку в Российской Федерации большой дефицит донорских органов, данная проблема является очень актуальной. Так, показатель донорства печени в Российской Федерации составляет 2,1 на 1 млн. населения, что в 7-8 раз ниже данных европейских стран. Так, по данным VII сообщения регистра Российского трансплантологического общества по итогам 2014 г. в листе ожидания на трансплантацию печени находилось 635 пациентов, нуждавшихся в трансплантации. Смертность в листе ожидания за 2014 г. составила 88 человек.
Полагаем, что методом снижения смертности от печеночной недостаточности вследствие прогрессирования заболевания в листе ожидания трансплантации печени может явиться применение клеточных технологий на основе мезенхимных (МСК) и гемопоэтических стволовых клеток (ГСК). Одним из наиболее подходящих источников стволовых клеток является собственный костный мозг человека.
На основании экспериментальных и клинических данных показано, что гемопоэтические стволовые клетки (CD34+) костного мозга в условиях in vitro в присутствии фактора роста гепатоцитов (HGF) начинают экспрессировать цитокератин 19 (CK19), обнаруживается РНК альбумина и при сохранении пролиферативной активности (Ki67) после 28 дней культивирования улучшается функция печени оцениваемая по критериям Child-Turcotte-Pugh, Model for End-Stage Liver Disease (MELD). S. Terai, T. Ishikawa с соавторами [«Improved Liver Function in Patients with Liver Cirrhosis After Autologous Bone Marrow Cell Infusion Therapy», STEMCELLS 2006; 24:2292-2298] выявили эффективность аутотрансплантации мононуклеарной фракции костного мозга человека при системном внутривенном введении клеток. У 9 пациентов с циррозом печени различной этиологии, на 4 и 24 неделе после введения клеток отмечено статистически значимое улучшение значений Child-Turcotte-Pugh (р<0.05), повышение уровня альбумина и общего белка в крови (р<0.05), увеличение пролиферативной активности (альфа фетопротеин, ядерный клеточный пролиферативный антиген) гепатоцитов в биоптате (р<0.05), снижение уровня асцита, по данным компьютерной томографии в постинфузионном периоде.
В свою очередь N. Levicar, М. Pai с соавторами [«Long-term clinical results of autologous infusion of adult bone marrow derived CD34+ cells in patients with chronic liver disease», Cell Proliferation 2008, 41 (Suppl. 1), 115-125] использовали внутрипортальную и артериальную методики инфузии изолированной популяции CD34+ клеток аутологичного костного мозга, из периферической крови полученных при помощи мобилизации костного мозга пациентов с использованием гранулоцитарно-макрофагального колониестимулирующего фактора.
И все же количество известных клинических исследований недостаточно, в связи с чем остается актуальным вопрос способов получения ГСК и их доставки. Широкого распространения не получил ни один из ранее описанных методов.
Наиболее близким по технической сущности и достигаемому результату является способ, описанный авторами N. Levicar, М. Pai [«Long term clinical results of autologous infusion of adult bone marrow derived CD34+ cells in patients with chronic liver disease», Cell Proliferation 2008, 41 (Suppl. 1), 115-125]. Этот способ взят нами в качестве прототипа.
Авторы в качестве регенеративного материала использовали изолированную популяцию CD34+ клеток аутологичного костного мозга, полученных из периферической крови при помощи мобилизации костного мозга пациентов с использованием гранулоцитарно-макрофагального колониестимулирующего фактора. В последующем полученные клетки вводились медленно в портальную вену. Авторами отмечено снижение уровня билирубина и повышение альбумина в крови исследуемых пациентов, а у 2 из них разрешение асцита в течение 12 мес. наблюдения. Серьезных осложнений в процессе исследования и корреляции терапевтического эффекта с концентрацией введенных пациентам клеток (1×106-2×108 клеток) авторами не выявлено. Вместе с тем прототип, на наш взгляд, недостаточно полно оценивает функциональное состояние печени, качество жизни пациентов после введения ГСК. И таким образом не позволяет судить о прогрессировании цирроза печени.
Технический результат настоящего изобретения заключается в замедлении прогрессирования цирроза печени за счет внутрипортального введения реципиенту мононуклеарных клеток аутологичного костного мозга со скоростью, равной скорости портального кровотока реципиента, и последующего мониторинга интегральных показателей MELD, Child-Turcotte-Pugh, качества жизни, общего состояния реципиента, ультразвуковой эластометрии печени, а также морфологического и иммунногистохимического исследования биоптатов печени до и после введения клеток.
Этот результат достигается тем, что в известном способе, включающем получение из аутологичного биологического материала мононуклеарных клеток и оценку у реципиента в динамике содержания билирубина, альбумина, согласно изобретению, в качестве аутологичного биологического материала используют костный мозг реципиента, получаемый у него методом трепан-аспирации в количестве 200-300 мл билатерально из заднего бугра подвздошной кости, мононуклеарные клетки выделяют из полученного материала, оценивают их жизнеспособность и количество в них ГСК, после чего определяют скорость портального кровотока реципиента и с такой же скоростью осуществляют автоматизированное внутрипортальное введение мононукеалрных клеток инжектором, затем не реже одного раза в два месяца проводят мониторинг интегральных показателей MELD, Child-Turcotte-Pugh, качества жизни реципиента, не реже одного раза в 3 месяца выполняют ультразвуковую эластометрию печени, а также морфологическое и иммунногистохимическое исследование биоптатов печени до и через 2 месяца после введения клеток, и при сохранении полученных данных в динамике на исходном уровне или их улучшении судят о замедлении прогрессирования цирроза печени.
Использование в качестве биологического материала аутологичного костного мозга реципиента в объеме от 200 до 300 мл обеспечивает получение необходимого и достаточного количества мононуклеарных клеток, способствующих усилению регенерации гепатоцитов, что приводит к замедлению прогрессирования цирроза печени у реципиентов в листе ожидания.
Определение у выделенных мононуклеарных клеток их жизнеспособности и количества в них ГСК позволяет оценить качество полученного материала.
Определение скорости портального кровотока является необходимым условием для выбора скорости последующего введения мононуклеарных клеток, обеспечивая равномерное распределение их по всем сегментам печени. Автоматизированное введение этих клеток позволяет вводить их со скоростью, соответствующей установленной скорости портального кровотока и предотвращает потерю клеток по коллатералям портальной системы.
Мониторирование интегральных показателей MELD, Child-Turcotte-Pugh и качества жизни до и не реже одного раза в два месяца после введения мононуклеарных клеток позволяет оценить степень тяжести и динамику состояния реципиента.
Использование ультразвуковой эластометрии печени не реже одного раза в три месяца позволяет неинвазивно оценить плотность печеночной ткани, что отражает степень выраженности фиброза печени.
Морфологическое и иммунногистохимическое исследования биоптатов печени до и через два месяца после введения мононуклеарных клеток позволяют судить об изменении пролиферативной активности гепатоцитов, что является маркером регенерации.
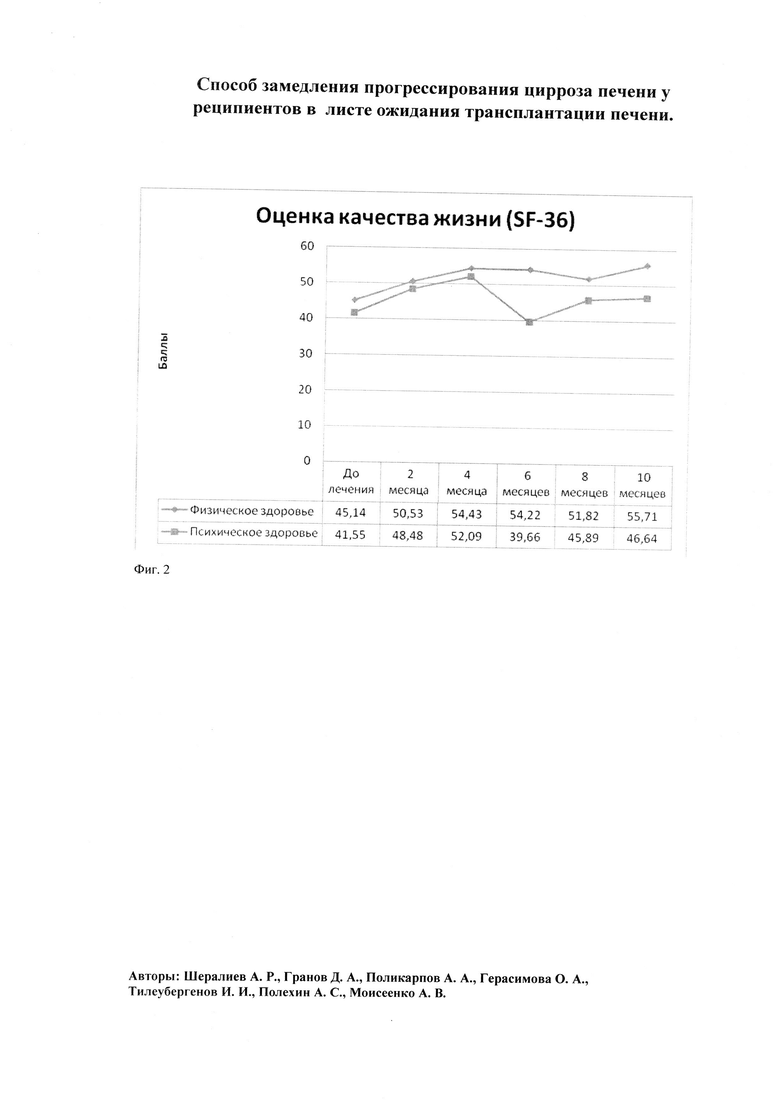
Оценка качества жизни реципиента до введения мононуклеарных клеток и после, проводимая по опроснику SF-36, характеризует физическое и психологическое состояние его здоровья.
Кратность указанных выше исследований определена нами опытным путем в процессе наблюдения в динамике.
Сущность способа поясняется примером.
Пример
Пациентка Б. 54 лет (1961 г. р.), поступила 17.05.2016 г. в ФГБУ «Российский научный центр радиологии и хирургических технологий (РНЦРХТ)» в плановом порядке с диагнозом: неверифицированный цирроз печени (МКБ-К74.6).
Из анамнеза заболевания:
Считает себя больной с мая 2015 г., когда впервые начала отмечать желтушность склер и кожных покровов. Обследовалась по месту жительства, клинически установлен цирроз печени. В июле 2015 г. была направлена на консультацию в ФГБУ «РНЦРХТ» с целью определения показаний к трансплантации печени.
В результате обследования в клинике по протоколу отбора на трансплантацию противопоказаний не выявлено. Пациентка согласилась на оперативное лечение и была включена в лист ожидания. На фоне консервативной терапии в период ожидания трансплантации печени с июля 2015 г. по май 2016 г. у пациентки отмечено снижение содержания билирубина в сыворотке крови с 280 до 50 мкмоль/л. Улучшилось общее состояние пациентки. Вместе с этим дальнейшего снижения этих показателей при амбулаторной консервативной терапии получить не удалось.
Поскольку в листе ожидания ФГБУ «РНЦРХТ» находятся около 130 человек, а период ожидания в среднем составляет более 8 месяцев. В апреле 2016 в ходе планового визита пациентке предложена внутрипортальная инфузия мононуклеарных клеток аутологичного костного мозга. Реципиенту выдан буклет с подробным описанием процедуры. После получения информированного согласия она обследовалась по разработанному нами протоколу. На госпитальном этапе выполнено лабораторное исследование крови: клинический, биохимический анализ крови, коагулограмма (Табл. 1), в которой жирным шрифтом выделены наиболее значимые показатели.
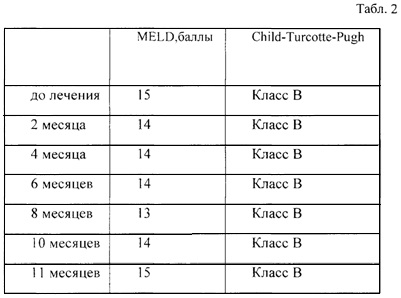
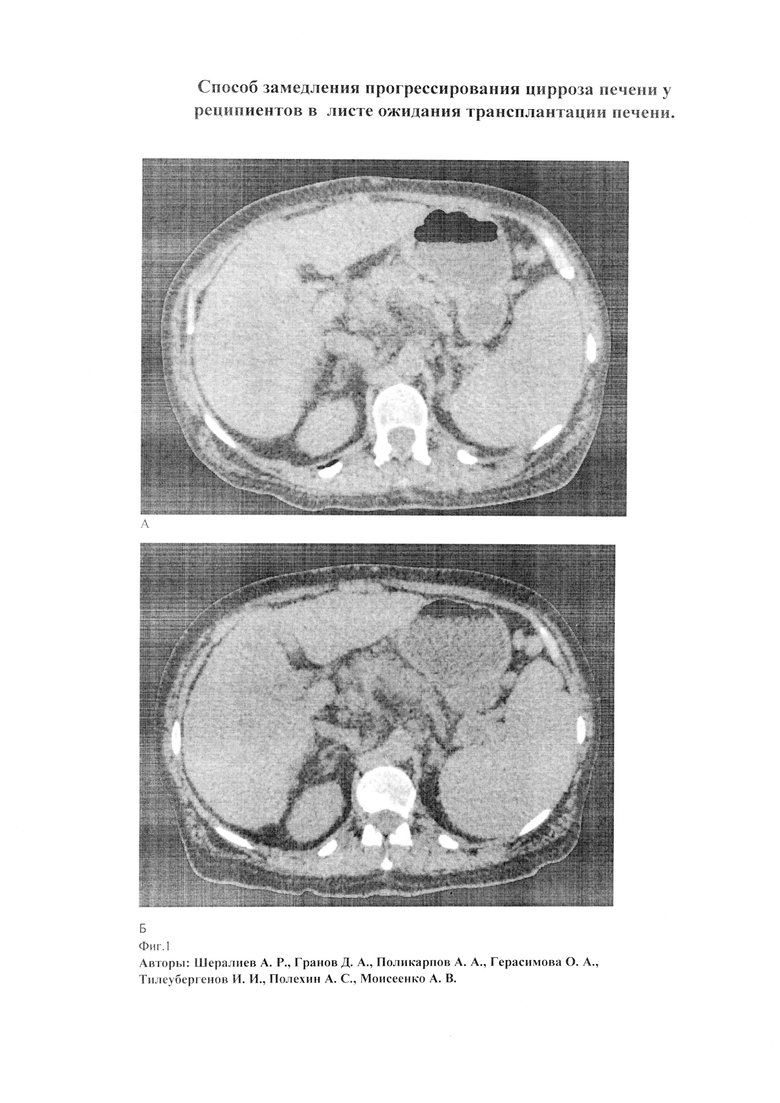
Оценен исходный статус реципиента, а в последующем после введения клеток каждые 2 месяца исследовалась функция печени по критериям Child-Turcotte-Pugh, MELD для (Табл. 2). Выполнена спиральная компьютерная томография (СКТ) грудной клетки, живота, таза с контрастным усилением: оценены сосуды печени и плотность печеночной ткани (Фиг. 1А). На томограмме асцит не визуализировался. Произведена ультразвуковая эластометрия печени (Табл. 3). При оценке плотности в 3 сегментах печени: SIII, SV, SVI получены значения 46 кРа, 35 кРа, 40 кРа соответственно.
Оценено исходное качество жизни реципиента по опроснику SF-36 (Фиг. 2). Полученные результаты физического и психологического здоровья 45.14 и 41.44 баллов соответственно. На основании вышеперечисленных исследований установлено, что пациентке показано лечение с использованием клеточной терапии.
18.05.2016 г. под местной анестезией в условиях перевязочной и стерильного операционного поля выполнена трепан-биопсия печени под ультразвуковой навигацией для морфологического и иммунногистохимического исследования биоптатов печени. Процедуру перенесла удовлетворительно, осложнений не наблюдалось. В полученном биоптате печени оценивалось количество митотических и двуядерных клеток, иммунногистохимические маркеры пролиферации: Ki67, альфа-фетопротеин (AFP) (Фиг. 3 А, Б). При световой микроскопии при увеличении 400Х на Фиг. 3А визуализируется выраженная инфильтрация, воспаление, количество двуядерных клеток составило 19 клеток/мм2, митозов не обнаружено. На Фиг. 3Б представлены результаты иммунногистохимического исследования маркерами:
Ki67 - 2%, альфа-фетопротеин - не экспрессировался.
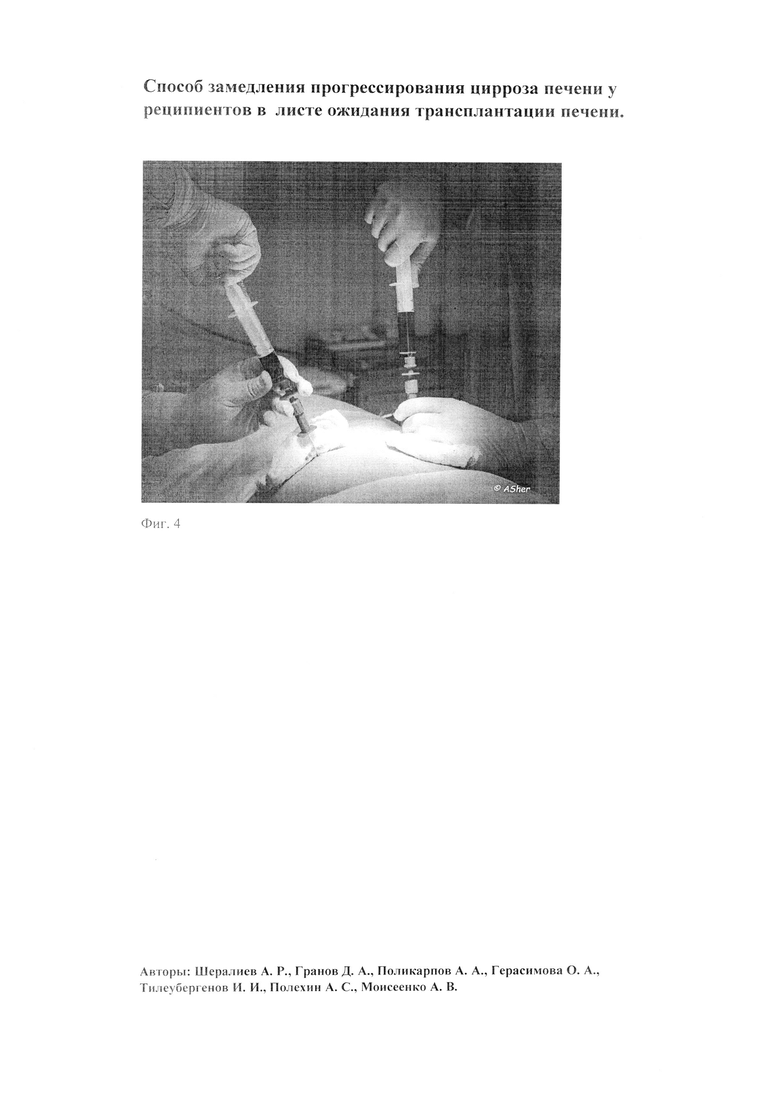
24.05.2016 г. в 10:35 в условиях операционной под местной анестезией методом билатеральной трепан-аспирации из заднего гребня подвздошной кости (Фиг. 4) выполнен забор аутологичного костного мозга в объеме 256 мл. Для забора костного мозга использовался набор для биопсии костного мозга 14 G х 70 mm и (TSUNAMI MEDICAL, Italy). Для аспирации костного мозга использовался стандартный шприц объемом 20 мл, содержащий 4 мл предварительно разведенного в физиологическом растворе антикоагулянта (200 мл NaCl 0,9% + 5 мл - 25000 БД гепарина). Для сбора материала использовался трансфузионный пакет-контейнер объемом 350 мл. После процедуры забора костного мозга полученный материал был отправлен в термоконтейнере в лабораторию Покровского банка стволовых клеток (Спб), где в течение 2 часов осуществлялся процесс изоляции мононуклерных клеток при помощи автоматизированного сепаратора костного мозга (SEPАХ, Sepax Technologies, USA).
После получения мнонуклеарных клеток осуществлялся качественный анализ популяции мезенхимных и гемопоэтических клеток, а также оценка их жизнеспособности при помощи проточной цитометрии (BeckmanCoulter, USA). Жизнеспособность полученных клеток составила 90%. В качестве среды для мононуклеарных клеток использовался буферный раствор состоящий из NaCl 0,9%, раствора 20% человеческого альбумина, 2500 ЕД р-ра гепарина. Полученная и ресуспензированная фракция мононуклеарных клеток в буферной среде составила 93.8 мл.
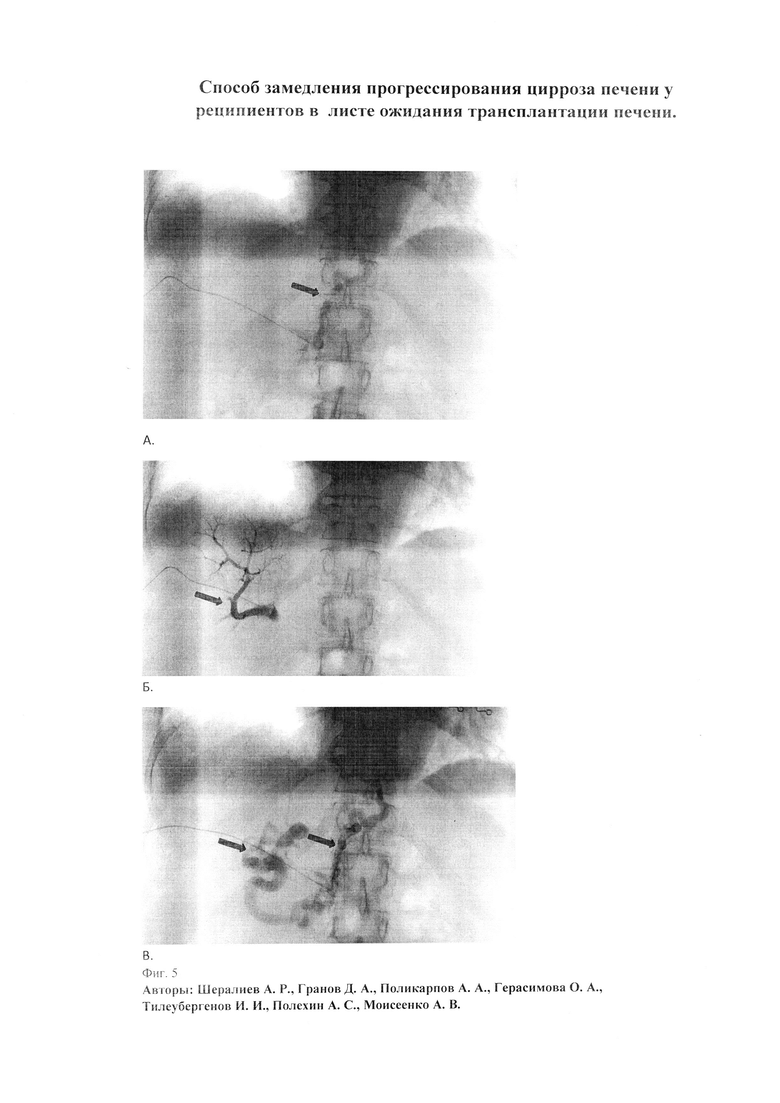
24.05.2016 г. в 16:45 в интервенционной операционной под местной анестезией раствора 1% лидокаина под ультразвуковым контролем по передней подмышечной линии в VIII межреберье произведена пункция портальной вены. Дилатационный катетер размером 4 F (1.3 мм) установлен в ствол портальной вены, выполнена серия снимков при введении 25 мл 60% ультрависта со скоростью 3 мл/с. Анатомия воротной вены типичная. Диаметр ствола воротной вены 11 мм. При помощи введения 25 мл 60% ультрависта с разными скоростями (0,5 мл/с, 0.8 мл/с, 1.0 мл/с и 1.5 мл/с) определена скорость адекватной перфузии сегментарных ветвей портальной вены, выполнено введение мононуклеарных клеток в портальную вену. Как видно на фигуре при скорости введения 0.5 мл/сек (Фиг. 5А) сегментарные ветви портальной вены не визуализировались, контрастное вещество протекало по коллатералям портальной вены. При скорости введения 0.8 мл/сек (2880 мл/час) (Фиг. 5Б) достигнуто равномерное контрастирование всех сегментарных ветвей портальной вены и отсутствие кровотока по коллатералям.
Эта скорость (0.8 мл/сек) выбрана в качестве оптимальной. При дальнейшем увеличении скорости введения контрастного вещества (Фиг. 5В) 1 мл/сек и 1.5 мл/сек визуализировались коллатерали портальной вены, в связи с чем 93.8 мл суспензии мононуклеарных клеток введены с уровня бифуркации портальной вены со скоростью 0.8 мл/сек (2880 мл/ч) во избежание потери клеток по коллатералям. Пункционный канал пломбирован гемостатической губкой, катетер удален, асептическая повязка. По завершении операции выполнено ультразвуковое исследование, по данным которого исключено кровотечение в месте манипуляции. В раннем послеоперационном периоде в ходе наблюдения за пациенткой осложнений и нежелательных явлений отмечено не было.
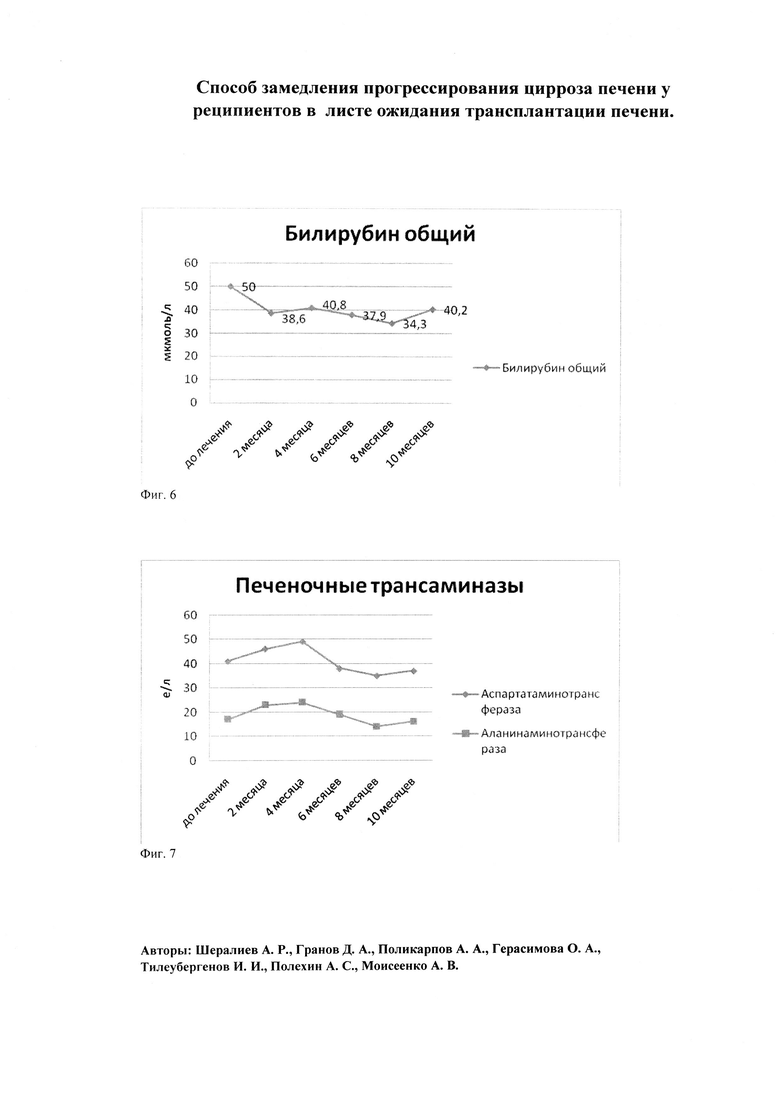
Далее каждые 2 месяца оценивались показатели функции печени (Табл. 1; Фиг. 6; 7; 8), прогностические шкалы MELD, Child-Turcotte-Pugh (Табл. 2), качество жизни (Фиг. 2), каждые 3 месяца ультразвуковая эластометрия печени (Табл. 3). Через 2 мес. после введения клеток выполнено СКТ брюшной полости и печени (Фиг. 1Б). Наличия асцита и и опухолевых новообразований не отмечено.
Результаты гистологического и иммунногистохимического исследования печени представлены на Фиг. 3В, Г. После введения мононуклеарных клеток через 2 месяца отмечено снижение воспалительной инфильтрации, существенное увеличение количества двуядерных клеток с 19 до 40 клеток/мм2 (Фиг. 3В) Митозов не обнаружено. При иммунногистохимическом исследовании выявлено повышение маркера Ki67 - 5%, экспрессии альфа-фетопротеина не обнаружено.
За 10 месяцев наблюдения у пациентки улучшились функциональные показатели печени: уменьшилось содержание билирубина получено снижение значения билирубина и печеночных трансаминаз, увеличилась концентрация альбумина в сыворотке крови. Улучшились показатели качества жизни пациентки. Отмечено снижение плотности печеночной ткани, улучшение морфологических параметров печени, что характеризует стабилизацию цирроза печени, а по ряду показателей улучшение ее функционального состояния.
К настоящему времени проведено введение мононуклеарных клеток аутологичного костного мозга 6 реципиентам из листа ожидания центра РНЦРХТ. Все они находятся в удовлетворительном состоянии, ни у одного из них не отмечено осложнений.
Достигнутые результаты лечения позволяют надеяться на увеличение срока дожития до трансплантации печени.
Предлагаемый способ по сравнению с известными имеет ряд преимуществ, основным из которых является комплексная динамическая оценка состояния печени и здоровья реципиента. При этом способ внутрипортальной доставки мононуклеарных клеток аутологичного костного мозга является малоинвазивным, персонализированным, поскольку в нем скорость введения мононуклеарных клеток равной скорости сегментарной перфузии печени реципиента.
Способ разработан авторами ФГБУ РНЦРХТ и прошел клиническую апробацию у 6 реципиентов из листа ожидания на трансплантацию центра с положительными результатами.


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ комплексного лечения осложнений цирроза печени через один хирургический доступ | 2024 |
|
RU2838304C1 |
| СПОСОБ ТРЕХЭТАПНОГО МИНИ-ИНВАЗИВНОГО ЛЕЧЕНИЯ ОСЛОЖНЕНИЙ ЦИРРОЗА ПЕЧЕНИ | 2023 |
|
RU2816786C1 |
| СПОСОБ РЕГЕНЕРАТИВНОЙ КЛЕТОЧНОЙ ТЕРАПИИ ДЛЯ ЛЕЧЕНИЯ ГЕПАТОЦЕЛЛЮЛЯРНОЙ НЕДОСТАТОЧНОСТИ ПРИ ЦИРРОЗЕ ПЕЧЕНИ | 2023 |
|
RU2822653C1 |
| СПОСОБ ПОДДЕРЖАНИЯ ФУНКЦИОНАЛЬНОГО СОСТОЯНИЯ ЦИРРОТИЧЕСКИ ИЗМЕНЕННОЙ ПЕЧЕНИ У ПАЦИЕНТОВ В ЛИСТЕ ОЖИДАНИЯ ТРАНСПЛАНТАЦИИ ОРГАНА | 2018 |
|
RU2682874C1 |
| Способ прогнозирования прогрессирующего течения цирроза печени вирусной этиологии | 2021 |
|
RU2784344C1 |
| Способ оценки риска смерти при циррозе печени | 2021 |
|
RU2761729C1 |
| РАДИОНУКЛИДНЫЙ СПОСОБ ОПРЕДЕЛЕНИЯ ДИСФУНКЦИИ ПЕЧЕНИ ПОСЛЕ ОРТОТОПИЧЕСКОЙ ТРАНСПЛАНТАЦИИ | 2019 |
|
RU2718294C1 |
| СПОСОБ ЛЕЧЕНИЯ ХРОНИЧЕСКИХ ДИФФУЗНЫХ ЗАБОЛЕВАНИЙ ПЕЧЕНИ | 2004 |
|
RU2283113C2 |
| Способ оценки риска неблагоприятного исхода для больного циррозом, находящегося в листе ожидания трансплантации печени | 2020 |
|
RU2737582C1 |
| Способ прогнозирования риска возникновения ранней дисфункции трансплантата трупной печени | 2021 |
|
RU2765462C1 |


Изобретение относится к медицине, а именно точнее к трансплантологии, и может быть использован при подготовке реципиента к трансплантации печени. Способ замедления прогрессирования цирроза печени у реципиентов в листе ожидания трансплантации печени включает получение из аутологичного биологического материала мононуклеарных клеток (МНК). В качестве аутологичного биологического материала используют костный мозг реципиента, который получают методом трепан-аспирации в количестве 200-300 мл билатерально из заднего бугра подвздошной кости. МНК выделяют из полученного материала, оценивают их жизнеспособность и количество в них гемопоэтических стволовых клеток. Определяют скорость портального кровотока реципиента, обеспечивают равномерное контрастирование всех сегментарных ветвей портальной вены и отсутствие кровотока по коллатералям. Далее осуществляют автоматизированное внутрипортальное введение МНК инжектором. Затем не реже одного раза в два месяца проводят мониторинг интегральных показателей MELD, Child-Turcotte-Pugh, качества жизни реципиента, каждые 3 месяца оценивают результаты ультразвуковой эластометрии печени, а также морфологическое и иммунногистохимическое исследование биоптатов печени до и после введения клеток. При сохранении полученных данных в динамике на исходном уровне или их улучшении судят о замедлении прогрессирования цирроза печени. Использование данного способа позволяет замедлить прогрессирование цирроза печени у реципиентов путем введения МНК со скоростью, равной скорости портального кровотока реципиента, обеспечивая уменьшение потери МНК по коллатералям. 1 пр., 3 табл., 8 ил.
Способ замедления прогрессирования цирроза печени у реципиентов в листе ожидания трансплантации печени, включающий получение из аутологичного биологического материала мононуклеарных клеток (МНК) и оценку у реципиента в динамике содержания билирубина, альбумина и отличающийся тем, что в качестве аутологичного биологического материала используют костный мозг реципиента, который получают методом трепан-аспирации в количестве 200-300 мл билатерально из заднего бугра подвздошной кости, МНК выделяют из полученного материала, оценивают их жизнеспособность и количество в них гемопоэтических стволовых клеток, определяют скорость портального кровотока реципиента, обеспечивают равномерное контрастирование всех сегментарных ветвей портальной вены и отсутствие кровотока по коллатералям, осуществляют автоматизированное внутрипортальное введение МНК инжектором, затем не реже одного раза в два месяца проводят мониторинг интегральных показателей MELD, Child-Turcotte-Pugh, качества жизни реципиента, каждые 3 месяца оценивают результаты ультразвуковой эластометрии печени, а также морфологическое и иммунногистохимическое исследование биоптатов печени до и после введения клеток и при сохранении полученных данных в динамике на исходном уровне или их улучшении судят о замедлении прогрессирования цирроза печени.
| Andre Castro Lyra et al | |||
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| JanSahulte am Esch II et al | |||
| Топочная решетка для многозольного топлива | 1923 |
|
SU133A1 |
| Приспособление для автоматического перевода стрелок машинистом | 1922 |
|
SU463A1 |
| ЛЫЗИКОВ А.Н | |||
| И др | |||
| Значение методов визуализационной диагностики цирроза печени и портальной гепертензии // Проблемы здоровья и экологии, 2016, [он-лайн], [найдено 18.01.2018] | |||
| Найдено из Интернет: https://cyberleninka.ru/article/n/znachenie-metodov-vizualizatsionnoy-diagnostiki-tsirroza-pecheni-i-portalnoy-gipertenzii | |||
| Федеральный информационный фонд отечественных и иностранных каталогов на промышленную продукцию, 2011 // [он-лайн], [найдено 18.01.2018] | |||
| Найдено из Интернет: http://промкаталог.рф/PublicDocuments/1104852.pdf | |||
| N | |||
| Leviсar et al | |||
| Нивелир для отсчетов без перемещения наблюдателя при нивелировании из средины | 1921 |
|
SU34A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2018-11-02—Публикация
2017-05-24—Подача