Изобретение относится к медицине, в том числе к гастроэнтерологии и трансплантологии, и может быть использовано для лечения больных терминальной стадией диффузных заболеваний печени.
Распространенность цирроза печени за последние 30 лет возросла на 5,2 миллиона, смертность от данного заболевания в 2019 г. составила 1,48 млн человек, что на 8,1% выше в сравнении с 2017 г. (Moon AM, Singal AG, Tapper ЕВ, 2020). Хроническая печеночная недостаточность является причиной нарушения синтетической функции печени, развития холестаза, коагулопатии, гипопротеинемии и определяется во всех случаях терминальной стадии цирроза печени. До настоящего времени проблема коррекции печеночной недостаточности остается не решенной (Global Burden of Diseases, Injuries, and Risk Factors Study, 2019). Единственным радикальным методом лечения больных терминальной стадией диффузного поражения печени является трансплантация печени, однако дефицит донорских органов приводит к длительному нахождению больных в "листе ожидания", что ассоциируется с высокой летальностью в период ожидания операции (Готье С.В., 2017). Основными причинами летальных исходов являются прогрессирование гепатоцеллюлярной недостаточности и осложнения портальной гипертензии, причем в большинстве случаев данные осложнения у больных циррозом печени встречаются совместно (Шабунин А.В., 2022).
Самыми назначаемыми при лечении цирроза печени в России являются гепатопротекторы, эффективность которых спорна. Некоторые авторы считают назначение этой группы препаратов оправданным как на стационарном, так и на амбулаторном этапах лечения (Минушкин О.Н., 2013 г.; Лазебник Л.Б., 2009; Атькова О.Ю., Полубенцева Е.И., 2011 г.; Ивашкин В.Т., 2006 г.), тогда как по некоторым данным назначение гепатопротекторов на стадии цирроза печени является нецелесообразны или недоказанным (Баранова Л.А., Беленкова Ю.Н., 2011 г.; Герок В., Блюм X.Е., 2009 г.; Ш. Шерлок 1999 г; Е. Купц, 2008 г). В настоящее время в клиническую практику внедрены молекулярные абсорбирующие рециркулирующие системы (MARS) и модули для сепарации и адсорбции фракционированной плазмы (FPSA) - системы Prometheus, однако применение этих методов ограничивается высокой стоимостью и кратковременных клиническим эффектом (V. Stadlbauer, 2006). Таким образом, целесообразность поиска альтернативных методов лечения для коррекции синтетической функции печени актуальны, своевременны и перспективны. Эффективным методом коррекции гепатоцеллюлярной недостаточности является внутрипортальное введение мононуклеарных CD34+ стволовых клеток (МНК). Кондиционированные МНК способны к миграции в область повреждения печеночной ткани в ответ на выделяемый ею фактор стромальных клеток (Шералиев, 2021), могут индуцировать дедифференцировку зрелых гепатоцитов в овальные клетки, экспрессирующие маркеры стволовых и родоначальных клеток печени (Шералиев, 2021). Секреция факторов трофики подавляет активизацию звездчатых клеток, приводит к увеличению пролиферации гепатоцитов и их предшественников.
Протокол стимуляции, выделения и интрапортального введения мононуклеарных стволовых клеток (CD34+):
1 этап: Введение колоний стимулируюшего фактора в дозе 10 мкг/кг в течение 4-6 суток. На 4е сутки проводится клинический анализ крови с оценкой уровня лейкоцитов, при возрастании уровня более 10*109, выполняется подсчет уровня CD34+ клеток методом проточной цитометрии.
При повышении концентрации более 10 млн клеток на мл целесообразен аферез клеток из периферическрй крови, при уровне менее 10 млн клеток на мл показано продолжить стимуляцию лейкопоэза до 6 суток с повторной гемоцитометрией и проточной цитофлоуметрией для оценки концентрации CD34+. При достижении уровня CD34+ клеток 10-15 млн на мл, проводится аферез мононуклеарных клеток аутологического костного мозга из периферической крови с использованием гравитационого сепаратора SPECTRA OPTIA с последующей шоковой заморозкой культуры клеток.
2 этап: В условиях рентгеноперационной под местной анестезией под контролем ультразвукового исследования производится пункция и катетеризация ветви воротной вены (Фиг. 1)
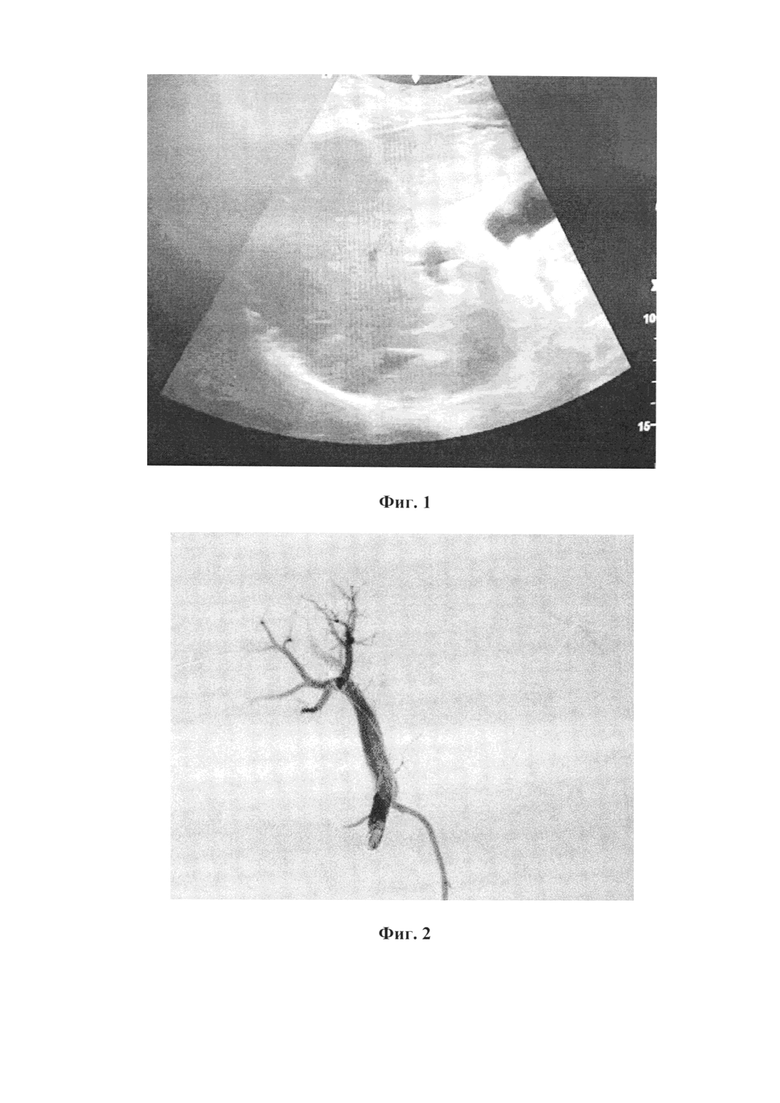
Далее катетер устанавливается в стволе воротной вены и выполняется контрольная портография (Фиг. 2).
После установки катетера выполняется введение культуры мононуклеарных стволовых клеток в систему воротной вены (Фиг. 3)
Пункционный канал пломбируется гемостатической губкой.
Послеоперационный период:
Пациенту рекомендуется постельный режим на 3-6 часов. На следующие сутки выполняется контрольное ультразвуковое исследование для исключения гематом в паренхиме печени и околопеченочном пространстве, тромбоза в системе воротной вены. Определяется содержание гемоглобина и эритроцитов в периферической крови. При неосложненном послеоперационном периоде выписка возможна на первые сутки после инвазивного вмешательства.
Осуществление предложенного способа представлено примером: Пациент Г., 45 лет, госпитализирован с жалобами на иктеричность кожи и склер, увеличение размеров живота, слабость, сонливость. Цирроз печени алкогольного генеза диагностирован 2 года назад, дважды перенес эпизоды декомпенсации в виде отечно-асцитического синдрома. Абстиненция от алкоголя более 6 мес.При ЭГДС выявлено варикозное расширение вен пищевода (ВРВП) 2 ст., проведено лигирование ВРВП. По данным ультразвукового исследования и компьютерной томографии с внутривенным контрастированием органов брюшной полости диагностирована гепатомегалия, расширение ствола воротной вены до 14 мм, селезеночной вены до 10 мм, гиперспленизм. Установлен диагноз: цирроз печени алкогольного генеза класс В по СТР MELD 16 баллов. Портальная гипертензия. ВРВП 1 ст. Спленомегалия, гиперспленизм.
Учитывая явления печеночной недостаточности консилиумом принято решение о применении методики клеточной терапии.
На первом этапе выполнена стимуляция косного мозга путем введение гранулоцитарно-макрофагального колонийстимулирующего фактора в дозе 900 мкг в сутки в течении 6 дней. Отмечался умеренной выраженный артралгический синдром, не потребовавший коррекции. При контрольном обследовании в периферической крови отмечалось увеличение количества лейкоцитов до 30,64×109/л, при проточной цитофлуометрии выявлена концентрация CD34+ 15×109/л, после чего выполнена мобилизация мононуклеарных клеток. Далее выполнен качественный анализ МНК и популяции CD 34+ с оценкой их жизнеспособности и последующей шоковой заморозкой.
Через 3 дня в рентгеноперационной после пункционной биопсии печени выполнено интрапортальное введение культуры мононуклеарных стволовых клеток. Неосложненное течение послеоперационного периода.
Пациент выписан из стационара на 2 послеоперационные сутки. После выписки из стационара рекомендован прием спиронолактона 100 мг/сутки. При гистологическом исследовании выявлены признаки лимфоцитарной инфильтрации с формированием ложной дольки.
Через 12 недель при плановом обследовании: MELD - 10 баллов, Child-Pugh-Turcotte, класс А (8 баллов), при УЗИ органов брюшной полости свободной жидкости не определяется, при ЭГДС - варикозное расширение вен пищевода 1 степени, варикозно-расширенных вен в желудке нет. При гистологическом исследовании ткани печени определяется значительное уменьшение количества лимфоцитов, признаков воспалительной активности нет.
Описание изображений:
Фиг. 1. Пункция ветви воротной вены под ультразвуковым контролем.
Фиг. 2. Контрольная портография после установки катетера в стволе воротной вены.
Фиг. 3 Интраоперационное фото. Подготовка культуры мононуклеарных стволовых клеток к интрапортальному введению.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ТРЕХЭТАПНОГО МИНИ-ИНВАЗИВНОГО ЛЕЧЕНИЯ ОСЛОЖНЕНИЙ ЦИРРОЗА ПЕЧЕНИ | 2023 |
|
RU2816786C1 |
| Способ комплексного лечения осложнений цирроза печени через один хирургический доступ | 2024 |
|
RU2838304C1 |
| Способ лечения больных циррозом печени, осложненным портальной гипертензией и гиперспленизмом | 2021 |
|
RU2783657C1 |
| СПОСОБ ЛЕЧЕНИЯ ЦИРРОЗОВ ПЕЧЕНИ РАЗЛИЧНОЙ ЭТИОЛОГИИ | 2015 |
|
RU2593007C1 |
| Способ гипотермической оксигенированной перфузии в трансплантации печени и почки | 2021 |
|
RU2773291C1 |
| СПОСОБ ЗАМЕДЛЕНИЯ ПРОГРЕССИРОВАНИЯ ЦИРРОЗА ПЕЧЕНИ У РЕЦИПИЕНТОВ В ЛИСТЕ ОЖИДАНИЯ ТРАНСПЛАНТАЦИИ ПЕЧЕНИ | 2017 |
|
RU2671560C1 |
| СПОСОБ УСТАНОВКИ ДРЕНАЖЕЙ ПРИ ПАНКРЕАТОДУОДЕНАЛЬНОЙ РЕЗЕКЦИИ | 2022 |
|
RU2789210C1 |
| СПОСОБ ЛЕЧЕНИЯ ПОСЛЕОПЕРАЦИОННОГО ГИПОПАРАТИРЕОЗА ПОСЛЕ ОПЕРАТИВНОГО ВМЕШАТЕЛЬСТВА У БОЛЬНЫХ С ВТОРИЧНЫМ ГИПЕРПАРАТИРЕОЗОМ | 2023 |
|
RU2817205C1 |
| Способ гипотермической оксигенированной двойной машинной перфузии трансплантата печени от посмертного донора | 2023 |
|
RU2830104C1 |
| Способ диагностики лекарственно индуцированного поражения печени у больных с неалкогольной жировой болезнью печени | 2018 |
|
RU2695021C1 |

Изобретение относится к медицине, в том числе к гастроэнтерологии и трансплантологии, и может быть использовано для регенеративной клеточной терапии при лечении гепатоцеллюлярной недостаточности при циррозе печени. Выполняют стимуляцию косного мозга путем введения гранулоцитарно-макрофагального колонийстимулирующего фактора в дозе 10 мкг/кг в течение 4-6 суток. Затем проводят оценку уровня лейкоцитов. При возрастании уровня более 10*109 выполняется подсчет концентрации CD34+ клеток методом проточной цитометрии. При концентрации CD34+ клеток 10-15 млн на мл проводят аферез мононуклеарных клеток аутологического костного мозга из периферической крови с использованием гравитационого сепаратора SPECTRA OPTIA с последующей шоковой заморозкой культуры клеток. Через 3 дня после пункционной биопсии печени выполняют катетеризацию ствола воротной вены с интрапортальным введением культуры мононуклеарных стволовых CD34+ клеток. Изобретение обеспечивает регенеративную клеточную терапию для лечения гепатоцеллюлярной недостаточности при циррозе печени». 1 пр., 3 ил.
Способ регенеративной клеточной терапии для лечения гепатоцеллюлярной недостаточности при циррозе печени, заключающийся в том, что выполняют стимуляцию косного мозга путем введения гранулоцитарно-макрофагального колонийстимулирующего фактора в дозе 10 мкг/кг в течение 4-6 суток, затем проводят оценку уровня лейкоцитов, при возрастании уровня более 10*109 выполняется подсчет концентрации CD34+ клеток методом проточной цитометрии, при концентрации CD34+ клеток 10-15 млн на мл проводят аферез мононуклеарных клеток аутологического костного мозга из периферической крови с использованием гравитационого сепаратора SPECTRA OPTIA с последующей шоковой заморозкой культуры клеток, через 3 дня после пункционной биопсии печени выполняют катетеризацию ствола воротной вены с интрапортальным введением культуры мононуклеарных стволовых CD34+ клеток.
| СПОСОБ ЛЕЧЕНИЯ ХРОНИЧЕСКИХ ДИФФУЗНЫХ ЗАБОЛЕВАНИЙ ПЕЧЕНИ | 2004 |
|
RU2283113C2 |
| БИОТРАНСПЛАНТАТ, СПОСОБ ЛЕЧЕНИЯ ХРОНИЧЕСКИХ ЗАБОЛЕВАНИЙ ПЕЧЕНИ И СПОСОБ ЛЕЧЕНИЯ ЦИРРОЗА ПЕЧЕНИ И ПОРТАЛЬНОЙ ГИПЕРТЕНЗИИ | 2007 |
|
RU2368384C2 |
| БИОТРАНСПЛАНТАТ, СПОСОБ ЛЕЧЕНИЯ ХРОНИЧЕСКИХ ЗАБОЛЕВАНИЙ ПЕЧЕНИ И СПОСОБ ЛЕЧЕНИЯ ЦИРРОЗА ПЕЧЕНИ И ПОРТАЛЬНОЙ ГИПЕРТЕНЗИИ | 2007 |
|
RU2368384C2 |
| Способ лечения острой печеночной недостаточности | 2018 |
|
RU2701792C1 |
| WO 2007075812 A2, 05.07.2007 | |||
| Подземное сооружение | 1990 |
|
SU1718727A3 |
| Коткас И | |||
| Е., Земляной В | |||
| П Эффективность использования стволовых клеток в лечении цирроза печени (экспериментальное исследование) | |||
| ТАВРИЧЕСКИЙ МЕДИКО-БИОЛОГИЧЕСКИЙ ВЕСТНИК | |||
| Способ восстановления спиралей из вольфрамовой проволоки для электрических ламп накаливания, наполненных газом | 1924 |
|
SU2020A1 |
Авторы
Даты
2024-07-11—Публикация
2023-08-18—Подача