Изобретение относится к области аналитической химии, а именно к фотометрическому методу анализа, и может быть использовано для определения содержания железа Fe(III) в растворах чистых солей, содержащих Fe(III) в очень малой концентрации.
Важнейшей задачей, стоящей перед аналитическими лабораториями является мониторинг состояния и загрязнения объектов окружающей среды. Одним из наиболее важных показателей качества воды, как питьевой, так и природной (поверхностной и подземной), является содержание ионов Fe(III), концентрация которых зависит от многих факторов. Для определения железа(III) фотометрическим методом предложены органические реагенты различных классов, среди которых широко применяются хелатообразующие реагенты, содержащие ОН-группы и донорные атомы азота.
Выбор в качестве органического реагента ксиленолового оранжевого (КО) обусловлен тем, что данный реагент является доступным и широко применяемым металлохромным индикатором для прямого комплексонометрического определения ионов различных металлов, в том числе и Fe(III), но в то же время для спектрофотометрического определения используется редко.
Fe(III) в слабокислой среде образует с КО комплексное соединение [1] биколор, обладающее невысокой чувствительностью. Введение в систему третьего компонента поверхностно-активного вещества (ПАВ), вероятно, может повысить чувствительность определения Fe(III) как известно из литературы [2, 3].
Наиболее близким по технической сущности к заявляемому изобретению является способ фотометрического определения Fe(III) в растворах чистых солей, который включает переведение Fe (III) в комплексное соединение с органическим реагентом и ПАВ в слабокислой среде, нагревание на водяной бане и последующее фотометрирование полученного раствора, при этом к раствору Fe (III) с рН 3,9-5,2 добавляют 50-кратное количество органического реагента, в качестве которого используют ксиленоловый оранжевый, 1,8-2,2 мл раствора ПАВ в виде 2%-ного раствора ETHAL LA-7, и воды до 10 мл объема с последующим нагреванием на водяной бане при температуре 60-80°С в течение 15 мин и добавлением в полученный раствор 1 мл ацетона [4].
Недостатками известного способа являются низкая устойчивость окраски раствора (2 час), длительное время нагревания (15 мин), необходимость наличия дополнительно органического растворителя -ацетона, отрицательно влияющего на организм человека, а также дорогостоящего французского ПАВ - ETHAL LA-7.
Технический результат заключается в сокращении времени проведения анализа, улучшении его воспроизводимости, повышении устойчивости окраски полученного комплексного соединения, за счет использования ПАВ в виде этоксилата перфтороктилового спирта и использования кюветы с толщиной равной 0,5 см.
Сущность изобретения заключается в том, что в способе фотометрического определения Fe (III) производят переведение Fe (III) в комплексное соединение с органическим реагентом - КО и ПАВ в слабокислой среде. Для построения градуировочного графика к 0,5 мл (0,8-2,0)⋅10-3 М раствору Fe (III) с рН равным 4,0-5,0, создаваемым введением 3,0 мл ацетатного буферного раствора, добавляют 1,0 мл 1⋅10-2 М раствора КО и 0,2 мл 4⋅10-3 М раствора ПАВ в виде этоксилата перфтороктилового спирта. Добавляют дистиллированную воду до 10 мл объема, нагревают на водяной бане при температуре 60-80°С в течение 10 мин и фотометрируют полученный раствор при длине волны равной 540 нм и толщине кюветы равной 0,5 см.
Сущность изобретения заключается в том, что в способе фотометрического определения Fe(III) производят переведение Fe(III) в комплексное соединение с органическим реагентом - КО и ПАВ в слабокислой среде. Для построения градуировочного графика к (0,8-2,0)⋅10-3 М раствору Fe(III) с рН равным 4,0-5,0, создаваемым введением 3,0 мл ацетатного буферного раствора, добавляют 1,0 мл 1⋅10-2 М раствора КО и 0,2 мл 4⋅10-3 М раствора ПАВ в виде этоксилата перфтороктилового спирта. Добавляют дистиллированную воду до 10 мл объема, нагревают на водяной бане при температуре 60-80°С в течение 10 мин и фотометрируют полученный раствор при длине волны равной 540 нм и толщине кюветы равной 0,5 см.
В изобретении используют следующие реагенты:
1. ПАВ-1 - этоксилат перфтороктилового спирта:
F-(-CH2-CH2-)8-(-CH2-CH2O-)7-H.
2. ПАВ-2 - 3, 6, 9, 12, 15, 18, 21 - гептаоксолентриаконтанол-1:
С10Н(2n+1)О-(-CH2-CH2-О-)7-Н, где n=10.
4⋅10-3 М растворы ПАВ готовят растворением рассчитанной навески в дистиллированной воде.
3. Стандартный 1⋅10-2 М раствор Fe(III) готовят растворением рассчитанной навески сульфата Fe(III) (х.ч.) в воде при подкислении раствором серной кислоты (H2SO4) для предотвращения гидролиза. Точную концентрацию полученного раствора определяют гравиметрическим методом. Для изучения оптимальных условий комплексообразования Fe(III) с КО рабочий раствор Fe(III) 1⋅10-3 М получают разбавлением исходного раствора дистиллированной водой.
4. 1⋅10-2 М раствор КО, который готовят растворением соответствующей навески в дистиллированной воде. КО - органический реагент, применяемый при комплексонометрическом титровании. Температура плавления 222°С; растворим в воде, не растворим в этаноле, диэтиловом эфире. Получают аминометилированием крезолового красного действием CH2O и иминодиуксусной кислотой в СН3СООН.
5. Для создания необходимой кислотности среды применяют ацетатные буферные растворы, которые готовят из 1 М раствора СН3СООН и 1 М раствора CH3COONa согласно данным табл. 1.
Пример. Определение оптимальных условий комплексообразования Fe(III) с КО в присутствии ПАВ-1.
В градуированные пробирки помещают по 0,5 мл 1⋅10-3 М раствора Fe(III) с рН равным 4,7, по 3 мл ацетатных буферных растворов с переменным значением рН, по 1 мл 1⋅10-2 М раствора КО, по 0,2 мл 4⋅10-3 М раствора ПАВ-1. Ионную силу растворов для хорошей воспроизводимости анализа равную 0,6 поддерживают постоянной добавлением рассчитанного количества раствора нитрата калия (KNO3). Общий объем раствора доводят до 10 мл дистиллированной водой. Реакционную смесь нагревают 10 мин на водяной бане при температуре равной 60-80°С, по охлаждении фотометрируют относительно растворов сравнения. На фиг. 1 показаны спектры светопоглощения комплекса Fe(III) + КО + ПАВ-1 (1) и КО + ПАВ-1 (2); фиг. 2 - зависимость А - рН комплекса Fe(III) + КО + ПАВ-1; фиг. 3 - зависимость А - VПАВ, мл, для комплекса Fe(III) + КО + ПАВ-1; фиг. 4 - зависимость А - VКО, мл, для комплекса Fe(III) + КО + ПАВ-1.
Линейность градуировочного графика для системы Fe(III) + КО + ПАВ-1 (λmax=540 нм; рНопт=4,1; VПАВ=0,2 мл 4⋅10-3 М; VКO=1 мл 10-2 М) соблюдается в интервале концентраций (0,8-2)⋅10-3 М Fe(III).
Расчет величины молярного коэффициента светопоглощения комплексного соединения Fe(III) + КО + ПАВ-1:

Температуру и продолжительность нагревания устанавливали опытным путем. Интенсивность окраски полученных комплексных соединений сохраняется в течение 5 час.
При сравнении величин молярных коэффициентов светопоглощения комплексного соединения Fe(III) с КО в присутствии ПАВ-1 и отсутствии ПАВ-1 (εFe(II[)+КО=26000) [3, с. 339] оказалось, что:
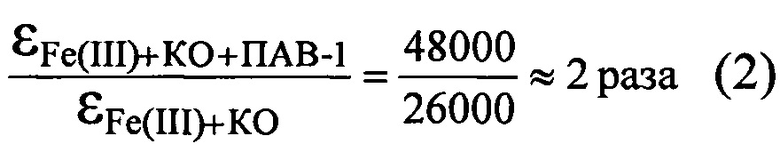
величина молярного коэффициента светопоглощения трехкомпонентного комплексного соединения оказалась больше, чем бинарного.
Методом изомолярных серий установлено соотношение Me : R между Fe(III) и КО при постоянной концентрации ПАВ-1 равное 1:2. Вероятная структура комплексного соединения Fe(III) + КО + ПАВ-1 при соотношении компонентов Me : R=1:2 представлена на фиг. 5.
Вытесняя водород из аминогрупп в КО Fe(III) образует с азотом донорно-акцепторную связь и такую же связь с хиноидным кислородом фенильного кольца основы. Подобные же связи Fe(III) образует еще с одной молекулой КО, так как соотношение Me : R=1:2. Возникает шесть донорно-акцепторных связей с азотом, что допускается для трехвалентного элемента, у которого координационное число равно 4 или 6. Образуются шесть 5-ти- и 6-ти-членных циклов (при соотношении Me : R=1:2). Этому способствуют особенности ПАВ-1, который группирует, сближает КО и Fe(III), за счет чего величина молярного коэффициента светопоглащения резко возрастает.
Разработаны оптимальные условия комплексообразования Fe(III) с КО в трехкомпонентной фотометрической системе в присутствии ПАВ-1 - этоксилата перфтороктилового спирта (λmax, рНопт, VКО, VПАВ, температура и время нагревания, пределы линейности градуровочного графика). Сравнение величин молярных коэффициентов светопоглощения по сравнению с бинарной показало, что чувствительность увеличилась ~ в 2 раза в трехкомпонентной системе по сравнению с соответствующей бинарной, что позволяет определять Fe(III) в анализируемом растворе до 10-5 М концентрации.
Изучение оптимальных условий комплексообразования Fe(III) с КО в присутствии ПАВ-2:
В градуированные пробирки помещают по 1 мл 1⋅10-3 М раствора Fe(III), по 3 мл ацетатных буферных растворов с переменным значением рН 3,0-5,0, по 0,1 мл 4⋅10-3 М раствора ПАВ-2, по 0,5 мл 1⋅10-2 М раствора КО. Ионную силу растворов для хорошей воспроизводимости анализа равную 0,6 поддерживают постоянной добавлением рассчитанного количества раствора нитрата калия (KNO3). Общий объем раствора доводят до 10 мл дистиллированной водой. Реакционную смесь нагревают 10 мин на водяной бане при температуре равной 60-80°С, по охлаждении фотометрируют относительно растворов сравнения. На фиг. 6 показаны спектры светопоглощения комплекса Fe(III) + КО + ПАВ-2 (1) и КО + ПАВ-2 (2); фиг. 7 - зависимость А - рН комплекса Fe(III) + КО + ПАВ-2; фиг. 8 - зависимость А - VПАВ, мл, для комплекса Fe(III) + КО + ПАВ-2; фиг. 9 - зависимость А - VКО, мл, для комплекса Fe(III) + КО + ПАВ-2.
Линейность градуировочного графика для системы Fe(III) + КО + ПАВ-2 (λmax=440 нм; pHmax=4,1; VПАВ-2=0,1 мл 4⋅10-3 М; VКО=0,5 мл 10-2 М) соблюдается в интервале концентраций (1-6)⋅10-4 М Fe(III).
Расчет величины молярного коэффициента светопоглощения комплексного соединения Fe(III) + КО + ПАВ-2:

Температуру и продолжительность нагревания устанавливают опытным путем. Интенсивность окраски полученных комплексных соединений сохраняется в течение 5 час. Чувствительность определения Fe(III) с КО в присутствии ПАВ-2 по сравнению с бинарным комплексом не изменяется.
Методом изомолярных серий установлено соотношение Me : R=1:1 при постоянной концентрации ПАВ-2.
По сравнению с известным бинарным комплексным соединением Fe(III) с КО предлагаемое позволяет повысить чувствительность способа фотометрического определения Fe(III) за счет использования органического реагента КО в присутствии ПАВ-1 - этоксилата перфтороктилового спирта. Молярный коэффициент светопоглощения предлагаемого способа в 2 раза превышает эту величину в соответствующем бинарном комплексном соединении Fe(III) с КО, что позволяет определять Fe(III) в растворах чистых солей в очень малой концентрации.
Кроме того по сравнению с прототипом толщина кюветы равная 0,5 см быстро заполняется, время нагревания на водяной бане комплексного соединения для получения максимальной интенсивности окраски сокращено на 5 мин, соответственно для анализа требуется меньше времени. У предлагаемого способа хорошая воспроизводимость анализа, образующийся комплекс более устойчив (окраска сохраняется в течение 5 час), комплексное соединение не выпадает в осадок, а реакция его образования идет в водной среде, поэтому отсутствует необходимость в органических растворителях, отрицательно влияющих на организм человека.
Источники информации
1. Булатов М.И., Калинкин И.П., Практическое руководство по фотоколориметрическим и спектрофотометрическим методам анализа. - «Химия», 1976. - С. 244, 406.
2. Hiroto Watanabe. Spektrophotometric determination of cobalt with 1-(2-pyridilazo-2 naftanol and surfact-ants. - Talanta, Vol. 21 pp. 295 - 302, 1974/ Хирото Ватанабе. Спектрофотометрическое определение кобальта с 1-(2-пиридилазо)-2-нафтанолом и поверхностно-активными веществами. - Таланта, 1974. Вып. 21, - С. 295-302.
3. RU 2312338, МПК G01N 31/22, G01N 21/78, опубл. 10.12.2007.
4. RU 2531053, МПК G01N 31/22, G01N 21/78, опубл. 20.10.2014.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ фотометрического определения железа (III) | 2017 |
|
RU2664504C1 |
| СПОСОБ ФОТОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ ЖЕЛЕЗА (III) В РАСТВОРАХ ЧИСТЫХ СОЛЕЙ | 2007 |
|
RU2331875C1 |
| СПОСОБ ФОТОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ ЖЕЛЕЗА (II) В РАСТВОРАХ ЧИСТЫХ СОЛЕЙ И ИСКУССТВЕННЫХ СМЕСЕЙ | 2006 |
|
RU2298171C1 |
| СПОСОБ ФОТОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ ЭРБИЯ (III) В РАСТВОРАХ ЧИСТЫХ СОЛЕЙ | 2010 |
|
RU2439540C1 |
| СПОСОБ ФОТОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ ХРОМА (III) В РАСТВОРАХ ЧИСТЫХ СОЛЕЙ | 2014 |
|
RU2553910C1 |
| СПОСОБ ФОТОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ ЖЕЛЕЗА (III) В РАСТВОРАХ ЧИСТЫХ СОЛЕЙ | 2013 |
|
RU2531053C1 |
| СПОСОБ ФОТОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ ЖЕЛЕЗА (III) В РАСТВОРАХ ЧИСТЫХ СОЛЕЙ | 2007 |
|
RU2340892C1 |
| СПОСОБ ФОТОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ ЖЕЛЕЗА (III) В РАСТВОРАХ ЧИСТЫХ СОЛЕЙ | 2009 |
|
RU2395079C1 |
| СПОСОБ ФОТОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ ЖЕЛЕЗА (III) В РАСТВОРАХ ЧИСТЫХ СОЛЕЙ | 2008 |
|
RU2363946C1 |
| СПОСОБ ФОТОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ ЖЕЛЕЗА (III) В РАСТВОРАХ ЧИСТЫХ СОЛЕЙ | 2010 |
|
RU2420733C1 |


Изобретение относится к области аналитической химии, а именно к фотометрическому методу анализа, и может быть использовано для определения содержания железа (III) в растворах чистых солей, содержащих железо (III) в очень малой концентрации. Способ включает переведение железа (III) в комплексное соединение с органическим реагентом - ксиленоловым оранжевым и поверхностно-активным веществом в слабокислой среде, добавление дистиллированной воды до 10 мл объема с нагреванием на водяной бане при температуре 60-80°С и последующим фотометрированием полученного раствора после его охлаждения, при этом для построения градуировочного графика к 0,5 мл (0,8-2,0)⋅10-3 М раствора железа (III) с рН, равным 4,0-5,0, создаваемым введением 3,0 мл ацетатного буферного раствора, добавляют 1,0 мл 1⋅10-2 М раствора ксиленолового оранжевого и 0,2 мл 4⋅10-3 М раствора поверхностно-активного вещества в виде этоксилата перфтороктилового спирта и дистиллированную воду до 10 мл, при этом нагревание на водяной бане осуществляют в течение 10 мин, а при фотометрировании используют кювету толщиной, равной 0,5 см. Достигается повышение точности и надежности, а также – ускорение анализа. 1 пр., 1 табл., 9 ил.
Способ фотометрического определения железа (III) в растворах чистых солей в присутствии поверхностно-активного вещества, включающий переведение железа (III) в комплексное соединение с органическим реагентом - ксиленоловым оранжевым и поверхностно-активным веществом в слабокислой среде, добавление дистиллированной воды до 10 мл объема с нагреванием на водяной бане при температуре 60-80°С и последующим фотометрированием полученного раствора после его охлаждения, отличающийся тем, что для построения градуировочного графика к 0,5 мл (0,8-2,0)⋅10-3 М раствора железа (III) с рН, равным 4,0-5,0, создаваемым введением 3,0 мл ацетатного буферного раствора, добавляют 1,0 мл 1⋅10-2 М раствора ксиленолового оранжевого и 0,2 мл 4⋅10-3 М раствора поверхностно-активного вещества в виде этоксилата перфтороктилового спирта и дистиллированную воду до 10 мл, при этом нагревание на водяной бане осуществляют в течение 10 мин, а при фотометрировании используют кювету толщиной, равной 0,5 см.
| СПОСОБ ФОТОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ ЖЕЛЕЗА (III) В РАСТВОРАХ ЧИСТЫХ СОЛЕЙ | 2013 |
|
RU2531053C1 |
| СПОСОБ ФОТОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ ЖЕЛЕЗА (III) В РАСТВОРАХ ЧИСТЫХ СОЛЕЙ | 2007 |
|
RU2331875C1 |
| СПОСОБ ФОТОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ ЖЕЛЕЗА (II) В РАСТВОРАХ ЧИСТЫХ СОЛЕЙ И ИСКУССТВЕННЫХ СМЕСЕЙ | 2006 |
|
RU2298171C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ЖЕЛЕЗА (III) И АЛЮМИНИЯ (III) В КИСЛЫХ РАСТВОРАХ | 1993 |
|
RU2043629C1 |
| CN 106841194 A, 13.06.2017 | |||
| CN 104568942 A, 29.04.2015. | |||
Авторы
Даты
2018-12-13—Публикация
2017-07-04—Подача