Изобретение относится к области экспериментальной медицины, клеточной биологии и клеточной терапии и может использоваться в клинической практике после клинической апробации для стимуляции веса плода и сохранения беременности в 1-ом триместре беременности.
Вес эмбриона и плода является одним из критериев оценки успешности внутриутробного развития и обычно должен соответствовать нормальному весу на данном сроке беременности. Вес устанавливают непосредственно после рождения, его величина влияет на дальнейшее развитие ребенка. Отставание веса и роста плода является одними из проявлений угрозы сохранения беременности или риска рождения ребенка с низким весом, что, в свою очередь, является риском последующего отставания развития ребенка. В большинстве случаев нарушения роста выявляются постнатально, но они напрямую связаны с процессами, протекающими на протяжении всего эмбрионального периода. В настоящее время остается актуальным изучение механизмов регуляции развития и роста плода, начиная с ранних сроков беременности.
В регуляцию течения беременности и роста плодов вовлечены все основные метаболические системы матери и плода. Кроме того, плацента частично принимает на себя синтез стероидных, белковых и пептидных гормонов, которые влияют как на развитие плода, так и на материнский организм.
Одним из важнейших регуляторов роста и веса растущего организма у млекопитающих являются стероидные гормоны. Сюда относятся прогестерон, эстрогены и глюко- и минералкортикоиды. Синтез прогестерона усиливается в сохранившемся желтом теле после имплантации бластоцисты и нарастает до конца беременности. У человека с 8-й недели беременности синтез прогестерона почти полностью переходит к плаценте.
Известно, что введение прогестерона (прогестинов) в повышенных дозах не нарушает и не изменяет рост, вес и развитие плодов, как у экспериментальных животных, так и у человека. С целью стимуляции роста и веса плода и нормального течения беременности на ранних сроках в клинической практике помимо прогестерона, используют также аспирин и гепарин. [Duckitt K., Quareshi А., 2011. Reccurent miscarriage. BMJ Clin. Evid. 2011. 1409]. В конце беременности плацента секретирует ежедневно 250 мг прогестерона в сутки. Таким образом, прогестерон функционирует как важнейший участник регуляции беременности, роста и веса плода, подавляя сократительную активность матки и выступая как иммуносупрессор.
Основным представителем эстрогенов, секретируемых плацентой, является эстриол. Эстрогены стимулируют образование рецепторов для прогестерона в матке и рост матки. 90% эстриола имеет плацентарное происхождение и 10% образуется из эстрона и эстрадиола, секретируемых яичниками матери. У человека при нормально протекающей беременности уровень эстриола растет параллельно росту уровня прогестерона. Имеется прямая связь между размерами плода, массой плаценты, состоянием надпочечников плода и уровнем эстриола в крови беременной. По данным Кащеевой (2007) снижение уровня эстриола в крови беременной связано с гипотрофией плода, гипоплазией надпочечников плода, синдромом Дауна, внутриутробной инфекцией, угрозой гибели плода, лечением большими дозами кортикостероидов и др. Значительное снижение уровня эстриола в крови матери указывает на возникновение угрозы прерывания беременности. Повышение уровня эстриола в крови беременных наблюдается при многоплодной беременности или крупном плоде.
Концентрация глюкокортикоидов и минералкортикоидов при беременности возрастает. Кортизол продуцируется и в надпочечниках плода и в плаценте так, что концентрация кортизола в крови матери отражает как состояние плода, так и состояние плаценты. При состоянии напряжения концентрация кортизола возрастает более чем на 50%, при истощении фетально-плацентарного комплекса концентрация снижается более чем на 50% от нормы.
По мере развития беременности увеличивается продукция пролактина, подготавливающего молочные железы к лактации. Плацентарный лактоген обладает низкой стимулирующей активностью гормона роста (ГР).
Одним из основных регуляторов роста и развития плодов является ГР, вырабатываемый клетками передней доли гипофиза. При беременности у человека в плаценте также синтезируется плацентарный гормон роста (ПГР), отличающийся от гипофизарного ГР по 13 аминокислотным остаткам. Предполагается, что ПГР участвует в контроле уровня инсулиноподобного фактора роста 1 типа (ИПФ-1).
ГР контролирует рост плодов на ранних сроках постнатальной жизни, включая подростковый возраст. Избыток ГР на начальных сроках беременности вызывает у трансгенных по гену ГР мышей и ягнят отставание веса тела. Также вес новорожденных телят уменьшается после введения беременным коровам ГР, начиная с ранних сроков беременности. У свиней после химической стимуляции синтеза ГР вес поросят увеличивается. При этом наблюдается значительное последействие в виде усиления роста, нарушений метаболических путей матери и функции плаценты, усиление накопления жира, тучность [Oberbauer А.М. 2015. Developmental programming: the role of growth hormone. J. of Animal Science and Biotechnology, v. 6:8, DOI 10.1186/s40104-015-0001 -8].
Таким образом, можно заключить, что взаимоотношения между ГР и ростом плодов изучены не полностью и что продолжительное воздействие экзогенного гипофизарного ГР разрушает нормальные взаимоотношения метаболических путей и поэтому не используется на ранних сроках беременности для регуляции веса плода.
В плаценте также обнаружен соматостатин, ингибитор ГР. Важнейшими участниками регуляции роста плода и беременности являются инсулино-подобный фактор роста 1 (ИФР-1), грелин и лептин. Грелин синтезируется в моруле, в эмбриональных тканях более поздних сроков развития, в плаценте, участвует в регуляции дифференцировки клеток эндометрия и в имплантации. Грелин обладает ГР-рилизинг активностью, т.е. стимулирует активность ГР. Представления о максимальных концентрациях грелина в крови матери в течение беременности противоречивы. На ранних сроках беременности у мышей показано, что как повышенный уровень грелина в крови при помощи ежедневных инъекций, так и подавление его активности при помощи антагонистов, оказывают негативный эффект на оплодотворение, имплантацию и эмбриональное развитие, зарегистрированное на 18-й день беременности, что указывает на то, что грелин в адекватной концентрации выполняет физиологическую функцию в регуляции беременности на ранних сроках [Luque Е.М., Torres P.J., De Loredo N., Vincent iL. M., Stutz G., Santillan M.E., Ruiz R.D., De Cuneo M.F., Martini A.C., Role of ghrelin in fertilization, early embryo development, and implantation period. Society for reproduction and fertility. DOI: 10.1530/REP. 14-0129], что указывает на трудности использования грелина с целью стимуляции развития плода на ранних сроках беременности. Лептин рассматривается как один из важных регуляторов роста плода. Лептин синтезируется в синцитиотрофобласте и в клетках материнской части плаценты. Предполагается, что лептин участвует в регуляции инвазии клеток трофобласта в спиральные артерии плаценты. В крови матери его начинают определять с 18 недели беременности. Можно допустить, что возможность его определения в крови связана с ростом плаценты. У женщин пониженный уровень лептина в крови в первом триместре беременности предшествует самопроизвольному прерыванию беременности [А.А. Александрова Л.В. Гутникова Е.Г. Деревянчук. Геномные и постгеномные маркеры развития плаценты и плода (учебно-методическое пособие), «ЮЖНЫЙ ФЕДЕРАЛЬНЫЙ УНИВЕРСИТЕТ», Ростов-на-Дону, 2011].
Из представленных данных следует, что механизмы регуляции роста и развития плода и течения беременности на каждом из периодов беременности отличаются от предшествующего. Развитие системы регуляции развития плода осложняется тем обстоятельством, что плацента также принимает на себя функцию регулятора течения беременности и роста плода. Регуляция беременности осуществляется сбалансированной системой гормонов и ростовых факторов, концентрации которых изменяются в процессе беременности как в сторону повышения, так и в сторону понижения при участии органов и тканей матери, плода и плаценты. Изменения концентрации какого-либо участника регуляционной системы из-за экзогенного введения или гормона, или фактора роста нарушает динамическое равновесие между всеми членами регуляторной системы и тормозит рост плода. Подтверждением этого является торможение роста плодов после повышения концентрации ГР при беременности [Oberbauer А.М. 2015. Developmental programming: the role of growth hormone. J. of Animal Science and Biotechnology, v. 6:8, DOI 10.1186/S40104-015-0001-8].
Началом изучения использования клеточной терапии для регуляции развития плодов и протекания беременности на ранних сроках у млекопитающих и человека являются исследования, доказывающие положительное влияние внутриматочной трансплантации так называемых мезенхимальных эндометриальных стволовых клеток человека на рост децидуа крыс в период до 11-го дня беременности [Михайлов В.М., Домнина А.П., Никольский Н.Н. 2014. Способ стимуляции образования децидуальной оболочки эндометрия в эксперименте. Патент RU 2515475, 2014]
[Mikhailov V.M., Domnina А.P., Sokolova А.V., Rosanov J.M., Kaminskaya, Nikolski N.N. Bone marrow cells influences for function of rat decidua. J. Cell Sci. Ther, 2015. 6:4, DOI: 4172/2217-7013. 1000224;
Mikhailov V.M., Sokolova A.V., Skripkina N.S., Kaminskaya E.V., Domnina A.P., Nikolsky N.N. Further Characteristics of Pregnant Bone Marrow Cells Action on Rat Development during Early Pregnancy J. of Genetic Synd.& Gene Ther., 2017.8:1, DOI: 10.4172/2157-7412.1000316].
В качестве прототипа нами выбран способ стимуляции веса плода в эксперименте, заключающийся в однократном внутривенном введении в организм беременной крысы клеток костного мозга (ККМ) в пост-имплантационном периоде развития в момент гаструляции и плацентации эмбрионов, то есть на 9 или 10, или 11, или 13 день беременности. [Mikhailov V.M., Domnina А.P., Sokolova А.V., Rosanov J.M., Kaminskaya, Nikolski N.N. Bone marrow cells influences for function of rat decidua. J. Cell Sci. Ther, 2015. 6:4, DOI: 4172/2217-7013. 1000224;
Mikhailov V.M., Sokolova A.V., Skripkina N.S., Kaminskaya E.V., Domnina A.P., Nikolsky N.N. Further Characteristics of Pregnant Bone Marrow Cells Action on Rat Development during Early Pregnancy J. of Genetic Synd. & Gene Ther., 2017.8:1, DOI: 10.4172/2157-7412.1000316]
К недостаткам способа, выбранного в качестве прототипа, можно отнести то, что забор такого биологического материала как костный мозг у беременных женщин при использовании его в клинической практике после получения соответствующего разрешения представляет опасность из-за использования наркоза, что является риском для благополучного вынашивания беременности.
Техническим результатом, достигаемым с помощью изобретения, является расширение арсенала действующих средств для стимуляции веса плодов в эксперименте и в клинической практике после получения разрешения на клиническое применение данного способа, а также исключение использования наркоза у беременной женщины на ранних сроках ее беременности.
Технический результат изобретения достигается тем, что в качестве стимулятора веса плода в организм беременной крысы на 9 или 10 или 11 день беременности однократно вводят подкожно в область каждого из сосков молочной железы 100 мкл суспензии клеток-мононуклеаров пуповинной крови человека, содержащей 6.9 миллион клеток так, чтобы общее количество инъецированных клеток составило 69 миллион клеток пуповинной крови человека в объеме 1000 мкл.
Способ осуществляется следующим образом:
Беременных самок получают после утреннего отбора среди самок-крыс, содержавшихся одну ночь вместе с самцами и имеющих во влагалищном мазке сперматозоиды, выявляемые с помощью микроскопирования на микроскопе (об. 10x, ок. 7х) утреннего влагалищного мазка, приготовленного при помощи ватного тампона, смоченного стерильным физиологическим раствором [Михайлов В. М. 1967. Патогенное действие нефроцитоксической сыворотки на эмбриональное развитие белых крыс. Бюлл. Экспер. Биол. и Мед., №6, стр. 97-100]. Крыс, содержащих сперматозоиды в утреннем мазке, обозначали как крысы 1-го дня беременности.
Мононуклеарную фракцию КПК (ООО Покровский банк стволовых клеток, Санкт-Петербург) получают при помощи центрифугирования клеточной суспензии в градиенте плотности 63% раствора перколла, приготовленного на стерильном сбалансированном солевом растворе без Са2+ и Mg2. Нами был использован полисахарид перколл производства фирмы SIGMA (США), но возможно использование перколла и других фирм производителей. Использовалась центрифуга К-23 (Janetzki, DDR). Свежеполученные КПК при комнатной температуре в объеме 5 мл наслаивают на 7 мл 63%-го раствора перколла и центрифугируют 20 мин при 1500 g. По окончанию верхний слой клеток в перколле удаляют при помощи 5 мл шприца и помещают в свежую пробирку для отмывания от избытка перколла в сбалансированном солевом растворе без Са2+ и Mg2+ и центрифугируют 10 мин при 700 g. Концентрацию клеток-мононуклеаров определяют при помощи подсчета в камере Горяева.
На 9 или 10 день или 11 день беременности животному однократно инъецируют мононуклеарную фракцию пуповинной крови человека. Для этого животное вводят в эфирный наркоз. Местом инъекций является поверхность живота. Животное под эфирным наркозом привязывают к станку.
Затем подкожно в область каждого соска молочной железы беременной крысы инъецируют 100 мкл клеточной суспензии, содержащей 6.9 миллионов мононуклеаров пуповинной крови человека. На каждой крысе для трансплантации используют пространство около 10-ти или 12-ти сосков молочной железы (в зависимости от наличия у крысы 10 или 12 сосков) так, чтобы общее количество инъецированных клеток соответствовала 69 миллиону клеток пуповинной крови человека в объеме 1000 мкл.
Существенные отличительные признаки и причинно-следственная связь между ними и достигаемым техническим результатом:
В качестве стимулятора веса беременной крысе вводят подкожно в область каждого из сосков молочной железы 100 мкл суспензии клеток-мононуклеаров пуповинной крови человека, содержащей 6.9 миллионов клеток так, чтобы общее количество инъецированных клеток составило 69 миллионов клеток пуповинной крови человека в объеме 1000 мкл.
Эффективность действия клеток пуповинной крови может быть обосновано тем, что ростовые факторы находятся в КПК в сбалансированном состоянии друг с другом и с клетками-мишенями. Активация секреции регулируется сигналами со стороны клеток-мишеней. Поэтому поступление ростовых факторов из трансплантированных КПК в ткани плода и матки не нарушает функционирование системы регуляции беременности и веса плода. Подтверждением тому является отсутствие нарушений течения беременности после трансплантации беременным крысам в период гаструляции КПК человека.
КПК обогащена стволовыми клетками с плюрипотентными свойствами [Harris D.T., Rogers I. 2007. Umbilical cord blood: a unique source of pluripotent stem cells for regenerative medicine. Curr. Stem Cell Res. Ther. 2: 301-309]. По аналогии с мнением авторов, использующих КПК для клеточной терапии в клинической практике, мы считаем, что в основе стимулирующего действия трансплантации КПК человека на рост плодов, плацент и ход беременности беременных крыс является секреция ими ростовых факторов, цитокинов, и др. [Harris D.Т. 2009. Non-hematological uses of cord blood stem cells. Britich J of Hematology, 147: 177-184; Смирнов B.H., Пальцев M.A. 2012. Почему пуповинная кровь? Стимуляция нейрогенеза в гиппокампе как наиболее вероятный механизм паракринных эффектов клеток пуповиной крови. В кн: Терапевтический потенциал клеток пуповинной крови при негематологических заболеваниях. Ред.: М.А. Пальцева и В.Н. Смирнова. М.: Из-во «ШИКО», 2012. стр. 15-31;
Ballen К. 2017. Umbilical Cord Blood Transplanta, 6(5): 1312-1315. 10.1002/sctm. 17-0069].
В Институте цитологии РАН описано стимулирующее действие ККМ крыс на рост децидуа у крыс [Михайлов и др., 2014]. У млекопитающих децидуальная оболочка обеспечивает возможность гаструляции и последующего развития зародыша после имплантации. Нормальное развитие млекопитающих с гемохориальным типом плаценты вне децидуализированной матки невозможно [Mikhailov V.М. Life cycle of decidual cells. Academic Press, 2003, vol. 227, pp 1-63]. Можно допустить, что трансплантация КПК также стимулирует функцию децидуа, обеспечивая, тем самым, успех гаструляции и дальнейшего постимплантационного развития зародыша. Таким образом, стимулирующее действие КПК на клетки эмбриона может быть результатом как прямого действия секреции КПК на клетки эмбриона, так и быть опосредованным через влияние на рост плодов децидуальной оболочки и функционирование желтого тела.
По аналогии с мнением авторов, использующих для клеточной терапии развития децидульной оболочки крыс мезенхимальные стволовые эндометриальные клетки человека [Михайлов В.М., Домнина А.П., Никольский Н.Н. 2014. Способ стимуляции образования децидуальной оболочки эндометрия в эксперименте. Патент RU 2515475, 2014] мы считаем, что в основе стимулирующего действия трансплантации КПК на вес плодов, плацент и течение беременности, является секреция ими ростовых факторов, цитокинов, и др.
Известно использование в клинической практике аллогенной трансплантации КПК, включающей в себя такие болезни нервной системы как церебральный паралич, ишемическая энцефалопатия, травматическое повреждение мозга, аутизм [Смирнов В.Н., Пальцев М.А. 2012. Стимуляция нейрогенеза в гиппокампе как наиболее вероятный механизм паракринных эффектов клеток пуповиной крови. В кн: Терапевтический потенциал клеток пуповинной крови при негематологических заболеваниях. Ред.: М.А. Пальцев и В.Н. Смирнов. М.: Из-во «ШИКО», 2012. стр. 15-31]. Основными механизмами действия в неврологии являются: а) индукция эндогенного нейрогенеза, реализуемая через синтез стволовыми клетками различных факторов роста (ФР) (нейрональный ФР, ФР эндотелия, ФР фибробластов 2, неротропина-3 и других; б) иммуномодуляция и противовоспалительное действие за счет синтеза противовоспалительных интерлейкинов (ИЛ-4, ИЛ-10); в) предотвращение патологической агрегации белка путем стимуляции секреции протеолитических ферментов в микроглии (например Аβ разлагающий фермент) и аутофагии.
При сердечно-сосудистых заболеваниях КПК секретируют цитокины, которые стимулируют ангиогенез [Wu К.Н., Zhou В., Mo Х.М. et al., 2007. Therapeutic potential of human umbilical cord-derived stem cells in ischemic diseases. Transplant Proa, 39: 1620-1622, Ballen K. 2017. Umbilical Cord Blood Transplant, 6(5): 1312-1315. 10.1002/sctm.17-0069], наиболее значимыми из которых являются фактор роста эндотелия сосудов (ФРЭС), фактор роста фибробластов-b (ФРФ b), фактор роста гепатоцитов (ФРГ) и простагландин Е2.
Недавно выяснилось, что внеклеточные везикулы, в том числе экзосомы и микровезикулы, являются важными медиаторами межклеточных коммуникаций в росте и развитии сосудов [Todorova D, Simoncini S, Lacroix R et al. Extracellular vesicles in angiogenesis. Circ Res 2017; 120:1658-1673]. Экзосомы содержат ряд биологически активных молекул, в том числе пептидов, белков, липидов и нуклеиновых кислоты (микро-РНК и мРНК), действующих как регуляторы функций эндотелиальных клеток и стимулирующих или ингибирующих ангиогенез паракринным или эндокринным путем. Например, было показано что экзосомы CD34+ клеток улучшают перфузию за счет поглощения эндотелиальными клетками мРНК-126-3р подавляющую экспрессию гена SPRED1, и одновременно активирующую экспрессию ФРЭС, ANGF1, ангиопоэтина-2, и ММП-9 [Mathiyalagan Р, Liang Y, Kim D et al. Angiogenic mechanisms of human CD341 stem cell exosomes in the repair of ischemic hindlimb. Circ Res 2017; 120:1466-1476]. Также за счет подобных механизмов действия КПК человека используются для лечения воспалительных заболеваний желудочно-кишечного тракта, роговицы, артрита, гепатита.
Трансплантированные крысам КПК человека улучшают моторную функцию мозга. На крысиной модели инфаркта миокарда показано, что КПК уменьшают размер инфаркта. Трансплантация КПК человека улучшает функционирование правого желудочка у мышей [Oommen, О.S. Yamada, S. Cantero Peral, К.A. Campbell, Е.S. Bruinsma, A. Terzic, and Т.J. Nelson. 2015. Human umbilical cord blood-derived mononuclear cells improve murine ventricular function upon intramyocardial delivery in right ventricular chronic pressure overload. Stem Cell Res Ther. 2015; 6(1): 50].
Таким образом, КПК обладают широким спектром терапевтического действия, как при воспалительных, так и при дегенеративных заболеваниях.
В доступной литературе информации об использовании трансплантации КПК для стимуляции веса плодов, как в клинической практике, так и в эксперименте, нами не обнаружено. Выявленное впервые рост-стимулирующего действия трансплантации КПК человека в период гаструляции на рост плодов и течение беременности у крыс открывает возможность как для понимания клеточно-молекулярных механизмов регуляции роста плодов, так и для использования трансплантации КПК для клеточной терапии ранней беременности.
Апробация способа была проведена на 54 половозрелых белых беспородных крысах-самках массой 200-250 г, 26 из которых были беременными на 9, 10, 11 и 13 дни беременности. 28 беременных самок были использованы как чистый контроль без введения клеток пуповинной крови (КПК). Источником крыс был питомник Рапполово. (Ленинградская область). Для регистрации стимулирующего действия КПК на вес плодов клетки пуповинной крови вводили в объеме 1 мл и в концентрациях (71, 68, и 26) × 106 клеток. Местом инъекций была поверхность живота животного, которое под эфирным наркозом было привязано к станку. Клеточную суспензию вводили в область около каждого из 10 или 12-ти сосков молочной железы. Беременных самок получали после утреннего отбора среди самок-крыс, содержащихся ночь вместе с самцами и имеющих во влагалищном мазке сперматозоиды. Крыс, содержащих сперматозоиды в утреннем мазке, обозначали как крысы 1-го дня беременности. Животных вскрывали в обеденное время на 18-й день беременности после их гибели при передозировке диэтилового эфира. Выбор для вскрытия 18 дня беременности обусловлен тем, что на этом сроке беременности у крыс питомника «Рапполово» заканчивается органогенез, переходящий в стадию роста [Михайлов В.М. 1970. Анализ механизмов патогенного действия иммунной антипочечной сыворотки на эмбриогенез. Рукопись диссертации на соискание уч. степени канд. мед. наук. Ленинград, Институт Экспериментальной Медицины АМН СССР]. При вскрытии подсчитывали количество желтых тел, мест имплантации, живых и резорбированных плодов с плацентами. Плоды и плаценты фиксировали в жидкости Буэна одни сутки и взвешивали. Для регистрации возможных поверхностной уродств развития плоды изучали под бинокулярной лупой [Михайлов В.М. Патогенное действие нефроцитотоксической сыворотки на эмбриональное развитие белых крыс. Бюллетень экспериментальной биологии, медицины, 1967, Т63, с. 97-100].
Анализ полученных гистологических срезов матки 10-го дня беременности через 24 часа после введения КПК показал, что трансплантация клеток пуповинной крови человека в область сосков молочной железы беременных самок крыс не нарушает дифференцировку клеток децидуа и организацию ткани матки, сохраняя в децидуа взаимное расположение эмбриона и плаценты.
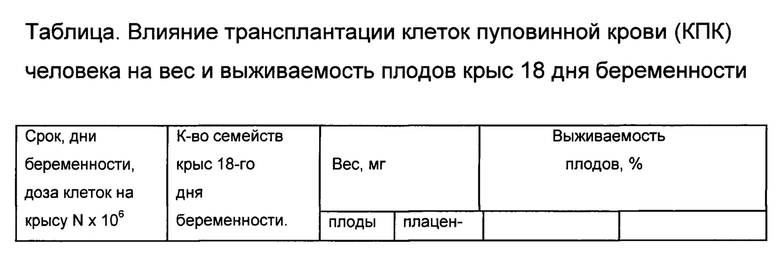
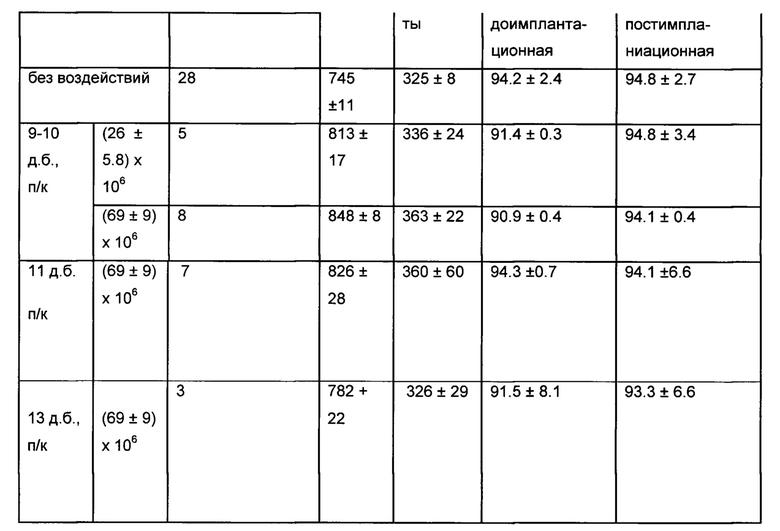
Результаты, представленные в таблице, показывают, что подкожная трансплантация крысам на 9 или на 10 или на 11 дни беременности КПК в дозе (69±9)×106 достоверно (Р<0.01) увеличивает вес 18 дневных плодов от контрольного уровня 745±11 мг до 848±8 мг в случаи введения на 9 или на 10 дни беременности а в случае введения КПК на 11 день беременности - до 826±28 мг. Достоверных различий веса между группами плодов после трансплантации КПК на 9 и 10 дни беременности не обнаружено. Трансплантация КПК на 13 день беременности в дозе (69±9)×106 клеток увеличивает вес плодов только до 782 мг. Различие с весом контрольных плодов недостоверно, Р>0.05. Вес плодов достоверно ниже при сравнении с весом плодов после трансплантации КПК на 9, 10 и на 11 дни беременности, Р<0.05. Таким образом, КПК стимулирует вес плодов крыс при трансплантации в период гаструляции и плацентации. Эффект КПК снижается при трансплантации в конце плацентации на 13 день беременности. Сравнение пред- и постимплантационой выживаемости плодов (см. таблицу) показывает, что предимплантационная выживаемость колеблется в различных группах крыс от 90% до 94% (средняя для 4 опытных групп 92.0%), тогда как постимплантационная выживаемость вырастает от 92% до уровня контрольной группы 94.0%. Повышение выживаемости имеется в каждой группе из 4-х. Возможно, что введение КПК увеличивает постимплантационную выживаемость плодов до некого максимума, характерного для этих групп животных в данное время сезона при имеющемся качестве кормов и содержания в общем помещении вивария.
Таким образом, после трансплантации КПК выживаемость плодов не снижается, что свидетельствует о том, что КПК, стимулируя вес плодов, не нарушают течение беременности.
Максимальный средний вес плодов после подкожной трансплантации КПК в дозе (69±9)×106 на 9-10 дни беременности достигает 848±8 мг. КПК в дозе (26±5.8)×106 трансплантируемых клеток увеличивают вес плодов до 813±17 мг, что выше контрольного (Р<0.01). Разница веса плодов после действиями доз КПК (26±5.8)×106 и (69±9)×106 клеток на 9-10 дни беременности достоверна при Р<0.05.
При этом после дозы 26 миллионов вес плацент остается на контрольном уровне. При дозе 69 миллионов вес плацент растет параллельно с ростом веса плодов на 9-10 и 11 дни беременности. При трансплантации на 13 день беременности доза КПК 69 миллионов не оказывает влияния на вес плацент. Таким образом, вес плодов более чувствителен к изменению дозы КПК, чем вес плацент. Рост веса плодов 18 дня беременности после трансплантации КПК на 9-10, и 11 дни беременности коррелирует с ростом веса плацент.
Из полученных данных следует, что стимуляция роста плодов крыс 18 дня беременности при действии КПК достигает максимальных величин при подкожной трансплантации КПК на 9, 10 и 11-ый дни беременности. Обращает на себя внимание, что трансплантированные клеточные популяции КПК человека, также как и ККМ крыс, стимулировали постимплантационную выживаемость плодов, то есть не нарушали течения беременности.
Сопоставление событий и сроков развития человека и крыс показывает, что, несмотря на значительное расхождение по продолжительности беременности, сроки начальных стадий развития незначительно отличаются друг от друга по продолжительности. Этапы морфологического развития эмбрионов на 9, 10 и 11 дни беременности крыс соответствуют примерно 20-22 и 24-30 дням беременности у человека, рассчитанных по классификации сроков беременности Института Карнеги (США) от момента оплодотворения [Witschi, Е. (1962) Development: Rat. In: Growth Including Reproduction and Morphological Development. Altman, P.L. and D.S. Dittmer, ed. Fed. Am. Soc. Exp.Biol., Washington DC,. pp 304-314]. В соответствии с принятой классификацией, эти стадии развития обозначаются как преэмбриональный и эмбриональный (начальный период органогенеза) периоды. В течение 20-22 дней и 24-30 дней беременности у человека и 9-11 дней беременности у крыс формируются зародышевые листки, сосуды, хорда, нервная пластинка, сердце. Аллантоис достигает базальной пластинки плаценты [Зыбина Е.Д.. Цитология трофобласта. Ленинград. Наука, 1986, 191 с]. Органогенез у человека заканчивается на 60 день беременности [Баранов B.C., Кузнецова Т.В. 2007. Цитогенетика эмбрионального развития человека. СПб. Изд-во Н-Л. - 640 с]. У крыс органогенез заканчивается к 18 дню беременности, после которого происходит преимущественно рост массы тела. Авторы обоих сопоставлений подчеркивают статистический уровень определения сроков развития. Выделение клеток трофобласта у человека и крыс происходит в бластоцисте до имплантации, у человека на стадии 32 бластомеров. У крыс имплантация происходит на 6 день после осеменения, у человека на 5-7 дни после оплодотворения с активным участием клеток трофобласта [Зыбина Е.Д.. Цитология трофобласта. Ленинград. Наука, 1986, 191 с; Mikhailov V. М. Life cycle of decidual cells. Academic Press, 2003, pp 1-63; Баранов B.C., Кузнецова Т.В. 2007. Цитогенетика эмбрионального развития человека. СПб. Изд-во Н-Л. - 640 с]. Третичные ворсины плаценты васкуляризуются и начинают функционировать у человека как плацента на 5-7 неделях беременности [Баранов B.C., Кузнецова Т.В. 2007. Цитогенетииа эмбрионального развития человека. СПб. Изд-во Н-Л. - 640 с; (А.А. Александрова Л.В. Гутникова Е.Г. Деревянчук. Геномные и постгеномные маркеры развития плаценты и плода (учебно-методическое пособие), «ЮЖНЫЙ ФЕДЕРАЛЬНЫЙ УНИВЕРСИТЕТ», Ростов-на-Дону, 2011].
У крыс будущие третичные клетки трофобласта появляются, начиная с 10 дня беременности из эктоплацентарного конуса. Они заселяют стенки сосудов матки, участвуя в формировании кровеносной системы плаценты к 14-16 дня беременности [Зыбина Е.Д.. Цитология трофобласта. Ленинград. Наука, 1986, 191 с.; Mikhailov V.М. Life cycle of decidual cells. Academic Press, 2003, pp 1-63]. Таким образом, введение КПК человека крысам на 9 или 10, или 11 дни беременности стимулирует гаструляцию и плацентацию у крыс. Позитивное действие трансплантации КПК человека на рост плодов, плацент и течение беременности у крыс начинается в преэмбриональном периоде беременности, когда происходит закладка тканей и отдельных органов. Реализация действия КПК осуществляется в эмбриональном периоде беременности.
Таким образом, заявляемый способ расширяет арсенал действующих средств для стимуляции веса плодов на ранних сроках беременности в эксперименте, а также в клинической практике после получения разрешения на клиническое применение данного способа и исключит использование наркоза у беременной женщины на ранних сроках ее беременности.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ СТИМУЛЯЦИИ ОБРАЗОВАНИЯ ДЕЦИДУАЛЬНОЙ ОБОЛОЧКИ ЭНДОМЕТРИЯ В ЭКСПЕРИМЕНТЕ | 2012 |
|
RU2515475C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЭНДОМЕТРИАЛЬНЫХ СТВОЛОВЫХ КЛЕТОК ЧЕЛОВЕКА, ПРЕДНАЗНАЧЕННЫХ ДЛЯ РЕГЕНЕРАЦИИ ТКАНИ | 2014 |
|
RU2595375C2 |
| СПОСОБ СТИМУЛИРОВАНИЯ РЕГЕНЕРАЦИИ СПИННОГО МОЗГА С ПОМОЩЬЮ ГЕНЕТИЧЕСКИ МОДИФИЦИРОВАННЫХ КЛЕТОК КРОВИ ПУПОВИНЫ ЧЕЛОВЕКА | 2013 |
|
RU2521225C2 |
| Способ прогнозирования внутрижелудочковых кровоизлияний у недоношенных новорожденных, родившихся у матерей с преэклампсией | 2022 |
|
RU2792565C1 |
| СПОСОБ ВЫБОРА ТАКТИКИ ВЕДЕНИЯ БЕРЕМЕННЫХ С ПЛАЦЕНТАРНОЙ НЕДОСТАТОЧНОСТЬЮ И СИНДРОМОМ ЗАДЕРЖКИ РОСТА ПЛОДА /СЗРП/ | 2015 |
|
RU2595884C1 |
| Способ профилактики хронической гипоксии и задержки развития плода | 2018 |
|
RU2699559C2 |
| СПОСОБ СТИМУЛЯЦИИ НАРУШЕННОГО СПЕРМАТОГЕНЕЗА И СИНТЕЗА ТЕСТОСТЕРОНА С ПОМОЩЬЮ ТРАНСПЛАНТАЦИИ НЕОНАТАЛЬНОЙ ТЕСТИКУЛЯРНОЙ ТКАНИ | 2017 |
|
RU2669027C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ СДВИГА КИСЛОТНО-ЩЕЛОЧНОГО РАВНОВЕСИЯ КРОВИ ПЛОДА ВО ВРЕМЯ БЕРЕМЕННОСТИ | 2023 |
|
RU2810176C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ПРЕЖДЕВРЕМЕННОЙ ОТСЛОЙКИ НОРМАЛЬНО РАСПОЛОЖЕННОЙ ПЛАЦЕНТЫ | 2024 |
|
RU2825067C1 |
| СПОСОБ ДИАГНОСТИКИ ЗАДЕРЖКИ РАЗВИТИЯ ЛЕГКИХ ПЛОДОВ И НОВОРОЖДЕННЫХ | 2013 |
|
RU2516889C1 |
Изобретение относится к медицине, а именно к экспериментальной медицине, клеточной биологии. В качестве стимулятора веса плода в организм беременной крысы на 9 или 10 или 11 день беременности однократно вводят подкожно в область каждого из сосков молочной железы 100 мкл суспензии клеток-мононуклеаров пуповинной крови человека, содержащей 6.9 миллиона клеток. При этом общее количество инъецированных клеток должно составить 69 миллионов клеток пуповинной крови человека в объеме 1000 мкл. Способ позволяет расширить арсенал действующих средств для стимуляции веса плодов в эксперименте и в клинической практике после получения разрешения на клиническое применение данного способа, а также исключить использование наркоза у беременной женщины на ранних сроках ее беременности. 1 табл.
Способ стимуляции веса плода на ранних сроках беременности в эксперименте, заключающийся во введении в организм беременной крысы стимулятора веса на 9 или 10 или 11 день беременности, отличающийся тем, что в качестве стимулятора веса плода беременной крысе однократно вводят подкожно в область каждого соска молочной железы 100 мкл суспензии клеток мононуклеаров пуповинной крови человека, содержащей 6.9 миллиона клеток, так, чтобы общее количество инъецированных клеток составило 69 миллионов клеток пуповинной крови человека в объеме 1000 мкл.
| МИХАЙЛОВ В.М., ДОМНИНА А.П., СОКОЛОВА А.В., РОЗАНОВ Ю.М., КАМИНСКАЯ К.В., и др | |||
| Влияние клеток костного мозга на функцию крысиного децидуа | |||
| J Cell Sci Ther, 2015, N6: 224 | |||
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| СПОСОБ СТИМУЛЯЦИИ ОБРАЗОВАНИЯ ДЕЦИДУАЛЬНОЙ ОБОЛОЧКИ ЭНДОМЕТРИЯ В ЭКСПЕРИМЕНТЕ | 2012 |
|
RU2515475C1 |
| СПОСОБ ВЫДЕЛЕНИЯ МЕЗЕНХИМАЛЬНЫХ СТВОЛОВЫХ КЛЕТОК | 2004 |
|
RU2252252C1 |
| ЙЫЛМАЗ Т.С | |||
| и др | |||
| Участие мононуклеаров пуповинной крови человека в физиологической регенерации почки крысы | |||
| Клеточная трансплантология и тканевая инженерия | |||
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| КУДРЯШОВА Н.В | |||
| и др | |||
| Мононуклеарные клетки пуповинной крови человека, трансфицированные двухкассетными плазмидами (vegf + нейротрофический фактор) для терапии бокового амиотрофического склероза | |||
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| BARKER J.N | |||
| et al | |||
| Searching for unrelated donor hematopoietic stem cells: availability and speed of umbilical cord blood versus bone marrow | |||
| Biol | |||
| Blood Marrow Transplant | |||
| Топчак-трактор для канатной вспашки | 1923 |
|
SU2002A1 |
| Vol | |||
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| Аппарат для нагревания окружающей его воды | 1920 |
|
SU257A1 |
Авторы
Даты
2018-12-18—Публикация
2018-04-02—Подача