Предполагаемое изобретение относится к медицине, биотехнологии, регенеративной медицине, в частности к способам количественной оценки клеток в составе клеточно-инженерной конструкции (скаффолда).
Одним из основных направлений современной регенеративной медицины и биотехнологий является разработка тканезамещающих материалов для восстановления поврежденных тканей и органов. Развитие скаффолд-технологий связано, прежде всего, с культивированием клеток на трехмерных матрицах естественного или искусственного происхождения с целью пространственного формирования будущего органа или его фрагмента для трансплантата. Одной из актуальных проблем, возникающих при исследовании в области скаффолд-технологий, является объективный прямой количественный анализ клеток культивируемых в скаффолде позволяющий охарактеризовать цитотоксические свойства клеточной матрицы, жизнеспособность и пролиферативную активность клеток в клеточно-инженерной конструкции. Данная проблема связана с особенностями культивирования клеток на трехмерных матрицах, в том числе с ограничением возможности прямого подсчета клеток при использовании световой микроскопии, что обусловлено трехмерностью структуры матриц и распределением клеток по всей толще скаффолда. Так же большинство скаффолдов не прозрачны, что вообще исключает методы количественного анализа с использованием световой микроскопии.
Существуют методы количественного анализа клеточной составляющей скаффолдов основанные на оценке метаболической активности клеток, например МТТ-тест. Однако эти методы являются косвенными и имеют большую погрешность, что связано с различной метаболической активностью клеток, например, находящихся в различных фазах митоза. Так же высокой степенью погрешности характеризуются методы, основанные на прямом подсчете количества клеток выделенных из скаффолда, что связано с потерей клеток при разрушении матрицы.
В качестве прототипа выбран способ определения количества клеток (см. Rowe S.L., Lee S., Stegemann J.P. Influence of thrombin concentration on the mechanical and morphological properties of cell-seeded fibrin hydrogels // Acta Biomater. 2007. Vol. 3., N.1., P. 59-67), применяемый для фибриновых и коллагеновых скаффолдов, включающий дегидратацию и ферментирование скаффолда, разбавление и окрашивание полученных образцов флуорохромом Hoechst 33258, обладающим высокой специфичностью к двухцепочечной молекуле ДНК, проведение флуоресцентной микроскопии с количественным определением ДНК и последующим вычислением абсолютного количества клеток в скаффолде.
Способ, представленный в прототипе, является косвенным и основан не на прямом подсчете клеток, а на количественном анализе ДНК в разрушенном скаффолде с последующим преобразованием количества ДНК в число клеток путем математического пересчета. Существенным недостатком представленного прототипа является необходимость дегидратации, разрушения скаффолда путем ферментации в протеиназе К и последующее разбавление полученных образцов, что может приводить к потере части клеточной составляющей скаффолда и вносить существенную погрешность в количественный анализ. Еще одним недостатком является длительность и трудоемкость способа, так только подготовительная часть анализа (ферментация) занимает от 16 до 20 часов, таким образом, для реализации всего способа необходимо более суток непрерывной работы. Так же крайне неудобен способ выражения результатов в виде абсолютного числа клеток в скаффолде. В связи с тем, что скаффолд может иметь значительные размеры и при этом достаточно малое количество клеток или наоборот небольшие размеры, но большое количество клеток способ не дает представления о плотности клеток в объеме скаффолда, а для получения последнего необходимы данные о размере скаффолда требующие проведения дополнительных измерений. Для корректного сравнения количества клеток в нескольких скаффолдах при использовании способа-прототипа по их абсолютному числу необходимы абсолютно идентичные образцы по размерам, что не всегда возможно реализовать в реальных условиях (например, клетки, растущие в скаффолде, могут изменять его структуру, что приводит к ретракции образцов и изменению их размеров). Таким образом, данный способ ограничивает возможность проведения последующего сравнительного анализа при работе с различными по размерам скаффолдами или их фрагментами.
Задача предполагаемого изобретения - усовершенствование способа.
Технический результат - объективизация, сокращение временных затрат и трудоемкости, повышение точности исследования количества клеток в составе скаффолда с относительно равномерным распределением клеток.
Технический результат осуществляется за счет того, что в способе, включающем окрашивание образцов флуорохромом Hoechst, обладающим высокой специфичностью к двухцепочечной молекуле ДНК и проведение флуоресцентной микроскопии, исследуемые образцы скаффолдов не подвергают предварительной подготовке, цифровую флуоресцентную микроскопию проводят в 10 полях зрения с послойной съемкой по оси Z на заданную глубину с последующей сшивкой изображений, полученные снимки обрабатывают с применением фильтров по интенсивности флуоресцентного свечения и по площади объекта, проводят промежуточный статистический анализ с расчетом общего количества клеток в каждом снимке и среднего количества клеток в 10 снимках, с последующим перерасчетом количества клеток в 1 мм3 скаффолда.
Способ количественного анализа клеточной составляющей скаффолда с относительно равномерным распределением клеток осуществляют следующим образом.
1. Фрагмент скаффолда помещают в 24-х луночный планшет для флуоресцентной микроскопии с непрозрачными боковыми стенками. Затем проводят прижизненное окрашивание ядер клеток в скаффолде с применением флуорохрома Hoechst 3334 обладающим высокой специфичностью к двухцепочечной молекуле ДНК. В лунку, содержащую фрагмент скаффолда и 2 мл культуральной среды (в зависимости от клеток, культивируемых в скаффолде DMEM или α-МЕМ содержащей 10% эмбриональной телячьей сыворотки), добавляют 1 мкл раствора Hoechst 33342 в концентрации 10 мкг/мл. Планшет помещают в термостат и инкубируют в течение 30 мин. при 37°C. После инкубации фрагмент скаффолда дважды отмывают фосфатным буфером. Затем к фрагменту скаффолда добавляют 1 мл фосфатного буфера для предотвращения пересыхания образца.
2. Планшет с фрагментом скаффолда переносят на оборудование позволяющее проводить цифровую флуоресцентную микроскопию (например: фотометр-имиджер Cytation™ 5). В 10 полях зрения с использованием объектива с 4-х кратным увеличением проводят послойную съемку по оси Z на заданную глубину не более 500 μm с последующей сшивкой изображений (стекинг, Z-stack). При использовании функции Z-stack объектив перемещается вдоль оси Z, снимает несколько изображений, извлекает только те участки, которые находятся в фокусе, и синтезирует их в полностью сфокусированное изображение.
3. Снимки в количестве 10 штук полученные по п. 2 обрабатывают с применением фильтров порога интенсивности флуоресцентного свечения (при анализе учитываются объекты с интенсивностью свечения более 7000 условных единиц) и площади объекта (при анализе учитываются объекты с площадью менее 30 μm). Применение данных фильтров позволяет снизить погрешность при количественном анализе. Так объекты с интенсивностью свечения ниже выбранного яркостного порога относят к объектам более светлым и исключаются из анализа (например: окрашенные клеточные ядра, залегающие в более глубоких слоях скаффолда, чем анализируемый слой). Применение фильтра порога интенсивности флуоресцентного свечения так же позволяет разделить ряд близкорасположенных клеточных ядер - в центре ядра имеют более интенсивное свечение, чем по периферии, таким образом, происходит разделение объектов по интенсивности свечения и при анализе учитываются объекты с яркостью выше пороговой - центральные части ядер. Применение фильтра по площади объекта позволяет не учитывать при анализе объекты с площадью более заданной, что дает возможность исключить объекты, не относящиеся к клеточным ядрам (например: остатки красителя) или скопления близкорасположенных клеток которые не удалось разделить при применении предыдущего фильтра.
4. Затем проводят промежуточный статистический анализ:
а) расчет общего количества клеток в каждом из 10 снимков (по п. 2-3);
б) расчет среднего количества клеток в 10 снимках (по п. 2-3).
5. Вычисляют количество клеток в 1 мм3 скаффолда по формуле:
K=N/B*C*500*10-9,
где K - количество клеток в 1 мм3;
N - среднее количество клеток на 10 снимках по п. 4б;
В - размер анализируемого поля зрения в μm по оси x при использовании объектива с 4-х кратным увеличением;
С - размер анализируемого поля зрения в μm по оси y при использовании объектива с 4-х кратным увеличением;
500 - размер анализируемого поля зрения в μm по оси z при использовании объектива с 4-х кратным увеличением;
10-9 - коэффициент, определяющий перевод μm3 в мм3.
Пример 1
Для исследования количества клеток взяты два фрагмента фибрин-коллагенового скаффолда с относительно равномерным распределением клеток (МСК крысы) и известной начальной концентрацией клеток (120 клеток/мм3). Скаффолд инкубировался в культуральной среде α-МЕМ содержащей 10% эмбриональной телячьей сыворотки в клеточном инкубаторе с содержанием CO2 5% и температурой 37°C. Фрагмент скаффолда №1 был взят на исследование после 1 суток инкубации, фрагмент №2 был взят после 9 суток инкубации. Согласно представленного способа фрагменты скаффолдов были окрашены Hoechst 33342 и проведен последующий количественный анализ клеточной составляющей скаффолда. Цифровая флуоресцентная микроскопия проводилась на фотометр-имиджере Cytation™ 5 (BioTek), при длине волны возбуждения 377 нм и длине волны эмиссии 447 нм. В 10 полях зрения с использованием объектива с 4-х кратным увеличением проведена послойная съемка по оси Z на заданную глубину 500 μm с последующей сшивкой изображений с и использованием функции Z-stack. В=1968 μm, С=1455 μm.
Результат:
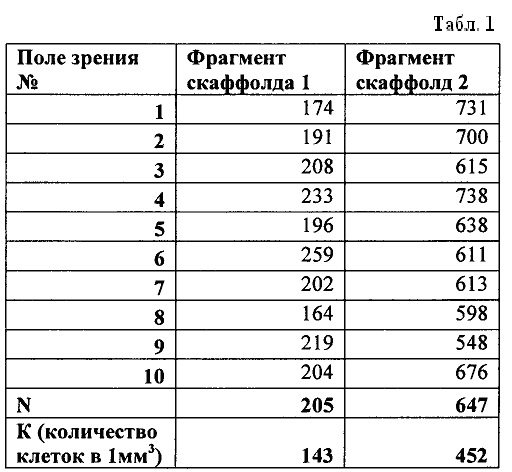
После первых суток инкубации скаффолда в культуральной среде количество клеток увеличилось в 1,2 раза (Табл. 1). После девяти суток инкубации скаффолда в культуральной среде количество клеток увеличилось в 3,8 раза. Можно заключить, что скаффолд не цитотоксичен, обладает свойствами обеспечивающими высокую жизнеспособность и пролиферативную активность клеток.
Пример 2.
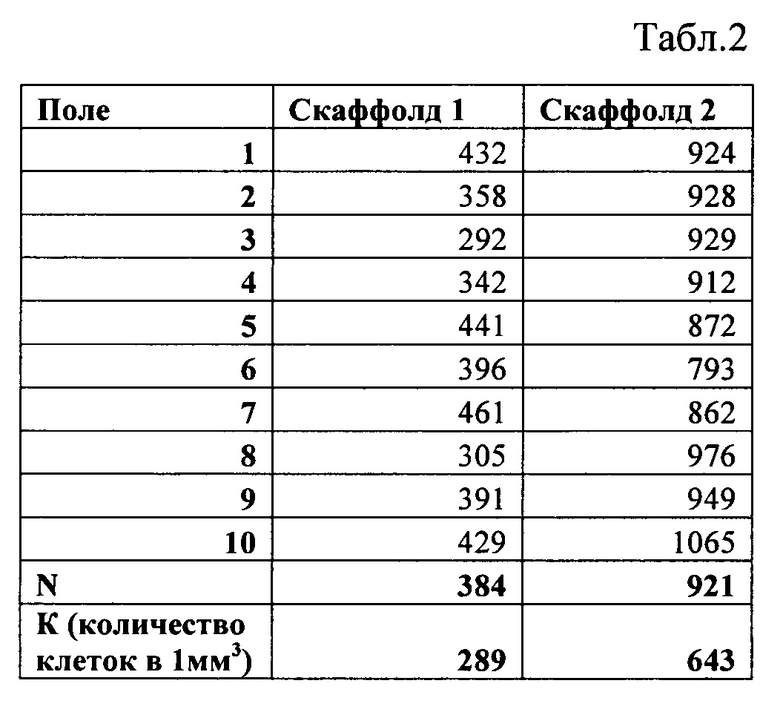
Для исследования количества клеток взяты два фибрин-коллагеновых скаффолда содержащих дермальные фибробласты человека с разницей в концентрации клеток в 2 раза (скаффолд №1 - начальная концентрация клеток 90 клеток/мм3; скаффолд №2 - 180 клеток/мм3) и относительно равномерным распределением клеток по всему объему скаффолда. Скаффоды инкубировались в течении 3 суток в культуральной среде DMEM содержащей 10% эмбриональной телячьей сыворотки в клеточном инкубаторе с содержанием СO2 5% и температурой 37°C. Затем согласно представленного способа фрагменты скаффолдов были окрашены Hoechst 33342 и проведен последующий количественный анализ клеточной составляющей скаффолда. Цифровая флуоресцентная микроскопия проводилась на фотометр-имиджере Cytation™ 5 (BioTek), при длине волны возбуждения 377 нм и длине волны эмиссии 447 нм. В 10 полях зрения с использованием объектива с 4-х кратным увеличением проведена послойная съемка по оси Z на заданную глубину 500 μm с последующей сшивкой изображений с и использованием функции Z-stack. В=1968 μm, С=1455 μm.
Результат:
После трех суток инкубации скаффолдов в культуральной среде в скаффолде №1 количество клеток увеличилось в 3,2 раза, в скаффолде №2 количество клеток увеличилось в 3,4 раза (Табл. 2). При этом концентрация клеток в скаффолде №2 была больше, чем в скаффолде №1 в 2,2 раза. Можно заключить, что в обоих скаффолдах дермальные фибробласты человека имели высокую пролиферативную активность, при этом в скаффолде №2 она была выше, чем в сокаффолде №1.
Преимуществами представленного способа количественного анализа клеточной составляющей скаффолда являются:
- прямой, а не косвенный анализ количества клеток в скаффолде по подсчету количества ядер;
- возможность проведения исследования без разрушения структуры скаффолда, что позволяет повысить точность исследований;
- возможность проведения исследования без дополнительной предварительной подготовки образцов до окрашивания, что снижает трудоемкость и существенно сокращает временные затраты на проведение количественного анализа клеточной составляющей скаффолда;
- возможность проведения исследований на скаффолдах или их фрагментах различных размеров, что существенно расширяет сферу применения способа и возможности при проведении научно-исследовательских работ с клеточно-инженерными конструкциями;
- выражение конечного результата в количестве клеток на единицу объема скаффолда, что дает представление о плотности клеток в скаффолде и возможность последующего корректного сопоставления количества клеток в независимости от размера анализируемых скаффолдов или их фрагментов.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОЦЕНКИ МИГРАЦИИ КЛЕТОК В СТРУКТУРУ МАТЕРИАЛА ИЛИ СКАФФОЛДА | 2020 |
|
RU2740566C1 |
| Способ оценки дифференцировки мезенхимальных стволовых клеток в трёхмерных скаффолдах | 2023 |
|
RU2818354C1 |
| СПОСОБ ДОСТАВКИ БИОЛОГИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ В СКАФФОЛД | 2018 |
|
RU2665155C1 |
| СПОСОБ ПРОЛОНГИРОВАНИЯ ВЫСВОБОЖДЕНИЯ БИОЛОГИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ ИЗ ТЕНЕЙ ЭРИТРОЦИТОВ | 2018 |
|
RU2683322C1 |
| Способ определения жизнеспособности клеток в биомедицинских клеточных продуктах в процессе регенерации | 2021 |
|
RU2777257C1 |
| Способ характеристики пористости скаффолдов и/или клеточно-инженерных конструкций | 2019 |
|
RU2695061C1 |
| Способ in vitro определения биосовместимости скаффолдов для нейротрансплантации | 2020 |
|
RU2776455C2 |
| Способ количественной оценки доли клеток в эпителиально-мезенхимальном переходе в асцитической жидкости и солидных опухолях рака яичников | 2018 |
|
RU2704814C1 |
| Способ молекулярной количественной детекции локальной распространенности немелкоклеточного рака легкого методом двойного иммунофлуоресцентного окрашивания нормальной и опухолевой ткани органа | 2020 |
|
RU2732973C1 |
| СПОСОБ ОЦЕНКИ МОРФОЛОГИИ ПЫЛЬЦЕВЫХ ЗЕРЕН РАСТЕНИЙ | 2013 |
|
RU2563356C2 |
Изобретение относится к медицине, биотехнологии, регенеративной медицине, в частности к способам количественной оценки клеток в составе клеточно-инженерной конструкции (скаффолда). Раскрыт способ количественного анализа клеточной составляющей скаффолда, который включает окрашивание образцов флуорохромом, обладающим высокой специфичностью к двухцепочечной молекуле ДНК, и проведение флуоресцентной микроскопии. При этом исследуемые образцы скаффолдов не подвергают дополнительной предварительной пробоподготовке до окрашивания, цифровую флуоресцентную микроскопию проводят в 10 полях зрения с послойной съемкой по оси Z на заданную глубину с последующей сшивкой изображений, полученные снимки обрабатывают с применением фильтров по интенсивности флуоресцентного свечения и по площади объекта, проводят промежуточный статистический анализ с расчетом общего количества клеток в каждом снимке и среднего количества клеток в 10 снимках с последующим перерасчетом количества клеток в 1 мм3 скаффолда. Изобретение обеспечивает сокращение временных затрат, трудоемкости и повышение точности исследования количества клеток в составе скаффолда. 2 табл., 2 пр.
Способ количественного анализа клеточной составляющей скаффолда, включающий окрашивание образцов флуорохромом, обладающим высокой специфичностью к двухцепочечной молекуле ДНК, и проведение флуоресцентной микроскопии, отличающийся тем, что исследуемые образцы скаффолдов не подвергают дополнительной предварительной пробоподготовке до окрашивания, цифровую флуоресцентную микроскопию проводят в 10 полях зрения с послойной съемкой по оси Z на заданную глубину с последующей сшивкой изображений, полученные снимки обрабатывают с применением фильтров по интенсивности флуоресцентного свечения и по площади объекта, проводят промежуточный статистический анализ с расчетом общего количества клеток в каждом снимке и среднего количества клеток в 10 снимках с последующим перерасчетом количества клеток в 1 мм3 скаффолда.
| АНТОНОВА Л.В | |||
| и др | |||
| Сравнительное тестирование in vitro биодеградируемых сосудистых имплантатов для оценки перспективы использования в тканевой инженерии // Комплексные проблемы сердечно-сосудистых заболеваний, 2015, N 4, стр.34-41 | |||
| BAJCSY P | |||
| et al | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Microsc., 2015, V.260, pp.363-376 | |||
| DANA H | |||
| et al | |||
| Hybrid Multiphoton Volumetric Functional Imaging of Large Scale Bioengineered Neuronal Networks // Nat | |||
| Commun., 2014, V.5, pp.1-15 | |||
| US 20110125029 A1, 26.05.2011. | |||
Авторы
Даты
2018-12-19—Публикация
2017-07-17—Подача