Настоящее изобретение относится к комбинации поликарбофила, поливинилпирролидона, глицерина и пропиленгликоля, которая, благодаря конкретным массовым процентам и соотношениям, представляет собой гелеобразующее средство, так же как пленкообразующее средство. Настоящее изобретение, кроме того, относится к фармацевтическим и ветеринарным композициям, так же как к медицинским устройствам, содержащим комбинацию по изобретению.
УРОВЕНЬ ТЕХНИКИ
Местное введение активных ингредиентов преимущественно обеспечивает максимальную концентрацию ингредиента непосредственно около биологической фазы и одновременно позволяет избегать того, что его распространение в тканях может вызывать ненужные риски токсичности или непереносимости.
На время удержания композиции в участке нанесения критически влияет консистенция композиции. Таким образом, в конкретном случае фармацевтической композиции, неоптимизированный носитель может отрицательно влиять на терапевтическую эффективность такой композиции.
В случае кожного введения, высокая вязкость композиции требует более интенсивного распределения, вызывающего жжение или боль, если ткани раздражены или повреждены; в то время как невязкую композицию можно быстро удалять из участка введения.
В конкретном случае местной фармацевтической композиции, часто рассматривают замедленное высвобождение активного ингредиента. В этом отношении, в замедленное высвобождение активного ингредиента вовлечены полимеры, которые, как правило, высвобождают лекарственное средство с контролируемой скоростью благодаря диффузии из полимера или посредством растворения полимера с течением времени. Местное введение лекарственных средств изменяет скорость, с которой лекарственные средства входят в ткань, и фармакокинетику лекарственного средства, таким образом, правильно разработанные материалы могут оптимизировать терапевтический эффект посредством контроля скорости высвобождения лекарственного средства.
Таким образом, остается давно испытываемая и неудовлетворенная потребность в материале, позволяющем соответствующую доставку активного ингредиента.
В дополнение к вышеуказанному, специалист в данной области дополнительно сталкивается с другими техническими проблемами при составлении местной фармацевтической композиции, из-за природы включенного в нее активного ингредиента. Некоторые из активных ингредиентов, известные в данной области, обладают низкой растворимостью в воде или являются почти полностью нерастворимыми в системах гидрофобного растворителя.
Соответственно, является сложным получить местный состав, содержащий достаточную растворенную концентрацию активного ингредиента для проявления его полного эффекта, а также для оптимизации проникновения соединения в кожу.
В дополнение к простоте высвобождения, является важным также, что любой состав фармацевтически активного соединения должен являться стабильным в течение длительных периодов времени, не должен терять своей активности, не должен обесцвечиваться или формировать нерастворимые вещества или комплексы, а также не должен является неприемлемо раздражающим кожу или слизистую оболочку.
Несмотря на приложенные усилия, все еще существует необходимость предоставления композиций с приемлемой биоадгезией, стабильностью и улучшенной биодоступностью включенных в них активных ингредиентов.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Авторы настоящего изобретения, в попытке разработать гелевую композицию с приемлемыми биоадгезивными свойствами, обнаружили комбинацию, решающую вышеупомянутые проблемы посредством выбора конкретных эксципиентов, в конкретных количествах и массовых соотношениях.
Неожиданно обнаружили, что комбинация, содержащая поликарбофил, поливинилпирролидон, глицерин, пропиленгликоль и трометамол или их соли, в конкретных массовых процентах и соотношениях, является способной формировать биоадгезивный гель, без необходимости включения какого-либо гелеобразующего средства.
Таким образом, в первом аспекте настоящее изобретение относится к комбинации, содержащей следующие ингредиенты:
- поликарбофил в количестве, составляющем от 1 до 5% по массе,
- поливинилпирролидон в количестве, составляющем от 4 до 8% по массе,
- глицерин в количестве, составляющем от 1 до 10% по массе, и
- пропиленгликоль в количестве, составляющем от 20 до 40% по массе, где:
массовое соотношение поливинилпирролидон:поликарбофил составляет между 1:1 и 4:1,
массовое соотношение глицерин:поликарбофил составляет от 1:1 до 2:1, и
массовое соотношение пропиленгликоль:поликарбофил составляет от 8:1 до 20:1.
Обнаружено, что комбинация по настоящему изобретению является способной формировать пленку, когда она расположена на ткани организма.
Следует отметить, что ни один из эксципиентов, формирующих комбинацию из первого аспекта по изобретению, не известен в данной области как гелеобразующее средство. Фактически, поликарбофил известен как биоадгезивное средство; поливинилпирролидон известен как дезинтегрирующее средство, суспендирующее средство, увеличивающее вязкость средство и связующее для таблеток; глицерин известен как увлажняющее средство; и пропиленгликоль известен как эмульгатор, суспендирующее средство и увеличивающее вязкость средство.
До настоящего времени, точно установлено, что для любой гелевой композиции необходимо включение по меньшей мере одного из гелеобразующих средств, известных в данной области, для получения такой текстуры. Одним из наиболее широко известных гелеобразующих средств является карбопол. Хорошо известно, что включение гелеобразующего средства, такого как карбопол, помимо обеспечения такой гелевой текстуры, увеличивает вязкость полученной композиции. Как хорошо известно специалисту в данной области, увеличение вязкости композиции может отрицательно влиять на диффузию средства (которое должно оказывать намеченный эффект) через матрикс и/или на введение композиции в конкретной зоне, оба из которых отрицательно влияют на биодоступность активного ингредиента и таким образом, на эффективность композиции.
Неожиданно, комбинация, такая как упомянутая в первом аспекте изобретения, обеспечивает формирование геля без необходимости включения гелеобразующих средств, таких как карбопол. Комбинацию по изобретению можно легко наносить и, кроме того, она обладает подходящей вязкостью, чтобы не оказывать неблагоприятного воздействия на биодоступность включенного в нее средства. В последнем, как проиллюстрировано ниже, одним из наиболее заметных преимущественных признаков комбинации по изобретению является то, что присутствует высокая биодоступность включенного в нее активного ингредиента, с вытекающими преимуществами высокой эффективности, уменьшенной дозы и/или уменьшенного количества нанесений продукта. Такая высокая биодоступность, характеризующая композиции, содержащие комбинацию по изобретению, по меньшей мере обусловлена подходящей вязкостью комбинации гелевой матрицы по первому аспекту изобретения.
В дополнение к вышесказанному, для геля, сформированного посредством комбинации по первому аспекту изобретения, показаны биоадгезивные свойства. Как показано ниже, когда композицию, содержащую комбинацию по первому аспекту изобретения и активный ингредиент, наносят на конкретную зону, наблюдают, что высокая концентрация активного ингредиента присутствует на коже, и что такой ингредиент диффундирует из гелевой матрицы к коже, для проникновения в нее и обеспечения его терапевтического применения, без достижения системного кровотока. Для достижения такого поведения, комбинация по изобретению проявляет адгезию к ткани организма, где ее наносят, формируя тонкую пленку (которая является ответственной за высокую биоадгезивность, наблюдаемую с комбинацией по изобретению). Благодаря сильной биоадгезии и физико-химическим свойствами гелевой матрицы (определяемым посредством эксципиентов, процентов и соотношений, составляющих комбинацию по изобретению), активный ингредиент диффундирует из гелевой матрицы и проникает в кожу.
Дополнительным преимуществом комбинации по изобретению является то, что когда ее наносят на эпителиальные клетки, а именно, кожу и слизистые мембраны (слизистые оболочки), не наблюдают раздражения или разъедания (как подтверждено с помощью тестов раздражения/разъедания кожи, включенных ниже).
Принимая во внимание вышеупомянутые преимущества биоадгезивности, биодоступности и отсутствия токсичности, комбинация по первому аспекту изобретения становится хорошим носителем для составления фармацевтических или ветеринарных композиций.
Таким образом, во втором аспекте, настоящее изобретение относится к фармацевтической или ветеринарной композиции, содержащей комбинацию, как определено выше, вместе с: (a) терапевтически эффективным количеством активного ингредиента или его фармацевтически или ветеринарно приемлемой соли; и (b) другими подходящими фармацевтически или ветеринарно приемлемыми эксципиентами и/или носителями.
Многие из коммерческих гелевых фармацевтических или ветеринарных композиций характеризуются тем фактом, что активный ингредиент (который оказывает намеченный эффект) является преципитированным в матрице. Эта преципитация, которая может быть обусловлена отсутствием стабильности в гелевой матрице, неблагоприятно влияет на биодоступность активного ингредиента.
Неожиданно, фармацевтическая или ветеринарная композиция по второму аспекту, содержащая комбинацию по изобретению, является прозрачной, без детекции какого-либо преципитата в гелевой матрице. Без связи с теорией, считают, что комбинация по изобретению предоставляет гелевую матрицу с подходящим физико-химическим окружением, обеспечивая стабилизацию добавленного активного ингредиента, таким образом, не происходит преципитации. Таким образом, комбинация с такими эксципиентами в конкретных соотношениях и процентах по первому аспекту изобретения улучшает биодоступность включенного в нее гидрофильного активного ингредиента. В этой связи, обнаружено также, что трометамол в конкретном массовом проценте и соотношении, помогает в растворении активного ингредиента в матрице.
Фармацевтическая или ветеринарная композиция по изобретению, благодаря лучшей биодоступности гидрофильного активного ингредиента, обладает улучшенной эффективностью. Таким образом, доза композиции, необходимая для получения желательного терапевтического эффекта, является более низкой, и/или количество нанесений, необходимых для желательного эффекта, можно уменьшать.
В данной области существует множество способов получения гелевых фармацевтических или ветеринарных композиций. Как известно специалисту в данной области, при получении таких составов, одной из наиболее критических проблем является получение композиции без сгустков. Многие из известных в настоящее время способов предоставляют гелевые композиции со сгустками (которые можно наблюдать визуально). Такие композиции со сгустками являются неприемлемыми с фармацевтической точки зрения и, таким образом, изготовители вынуждены тратить время и деньги на дополнительные стадии/способы в попытке растворить их.
Авторы настоящего изобретения разработали способ пригодного получения фармацевтических или ветеринарных композиций, как определено во втором аспекте изобретения.
Таким образом, в третьем аспекте настоящее изобретение относится к способу получения фармацевтической или ветеринарной композиции, как определено выше, где способ включает в себя следующие стадии: (a) смешивание активного ингредиента или его фармацевтической или ветеринарной соли с пропиленгликолем при встряхивании; (b) добавление поливинилпирролидона; (c) добавление глицерина; (d) добавление поликарбофила; и (e) добавление других подходящих фармацевтически или ветеринарно приемлемых эксципиентов и/или носителей.
С помощью такого способа преодолены проблемы сгустков, временных затрат и повторных затрат больших количеств денег при получении таких композиций без сгустков.
Авторы изобретения обнаружили, что два аспекта способа являются критическими для получения такой композиции без сгустков: (1) активный ингредиент добавляют до гелеобразования комбинации (которое имеет место при присутствии всех четырех эксципиентов, то есть после проведения стадии (d)); и (2) включение активного ингредиента в пропиленгликоль необходимо проводить при встряхивании.
Благодаря отсутствию преципитатов и сгустков, фармацевтические или ветеринарные композиции по настоящему изобретению являются прозрачными.
Более того, композиции по изобретению также являются стабильными.
Фармацевтическую или ветеринарную композицию можно вводить в нескольких формах, как подробно объяснено ниже. Среди них, композицию по второму аспекту изобретения можно изготавливать в форме набора.
Таким образом, в четвертом аспекте настоящее изобретение относится к набору, содержащему комбинацию, как определено в первом аспекте изобретения или композицию, как определено во втором аспекте изобретения, и подложку.
Как подробно обсуждают выше, комбинация по настоящему изобретению действует как гелеобразующее средство благодаря конкретному выбору эксципиентов, массовых процентов и соотношений.
Таким образом, в пятом аспекте, настоящее изобретение относится к использованию комбинации по первому аспекту изобретения в качестве гелеобразующего средства.
Кроме того, как объяснено выше, когда комбинацию по изобретению наносят на ткань организма (такую как кожа, слизистая оболочка, среди прочих), она формирует, немедленно после контакта, пленку. Без связи с теорией, считают, что когда комбинацию по изобретению наносят на ткань организма.
Таким образом, в шестом аспекте, настоящее изобретение относится к использованию комбинации, как определено выше, в качестве пленкообразующего средства посредством расположения комбинации на ткани организма, таким образом, абсорбции влаги из ткани и формирования пленки на поверхности ткани организма.
Наконец, в седьмом аспекте, настоящее изобретение относится к фармацевтической или ветеринарной композиции, как определено выше, для использования в качестве лекарственного средства.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
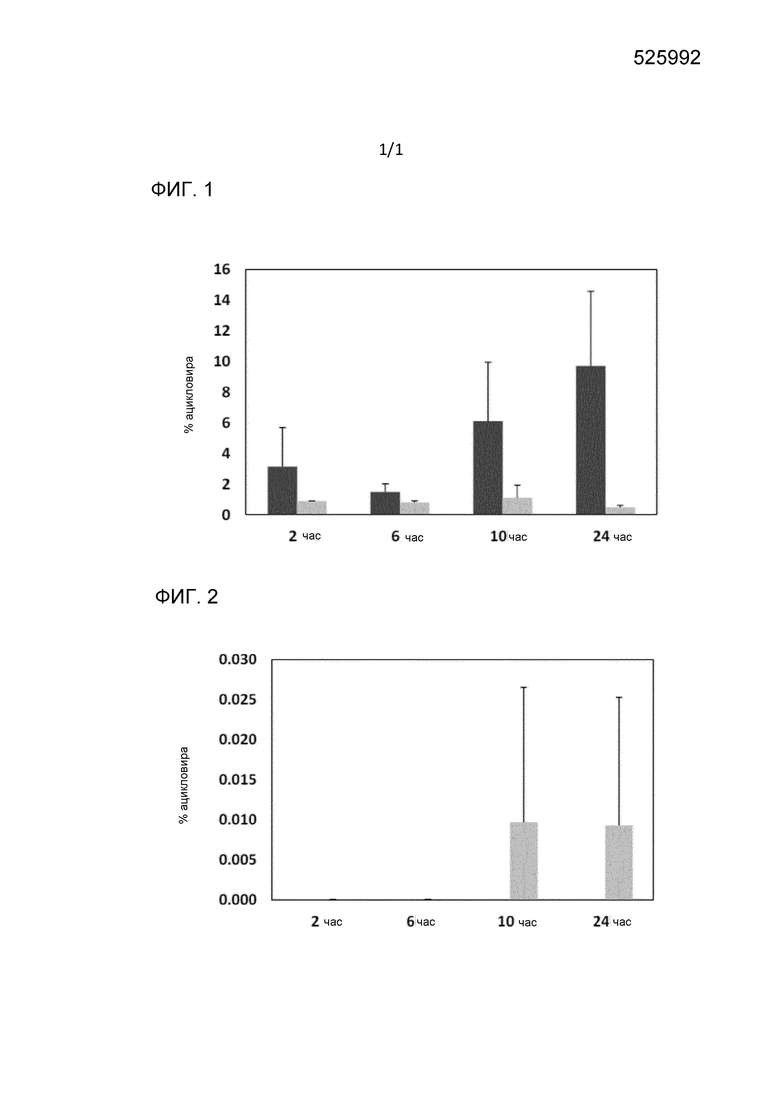
На Фиг. 1 показано общее количество ацикловира (%) в образцах кожи человека после 5 нанесений состава 1 (черный столбец) или эталонной композиции (серый столбец) на время 2, 6, 10 час и 24 час. Наблюдают «эффект накопления» при нанесении композиции по изобретению, где концентрация ацикловира в 5 или 21 раз выше по сравнению с концентрацией ацикловира, доступной при нанесении эталонной композиции. Y-ось: мг ацикловира; X-ось: время (выраженное в часах), в которое отбирали образцы.
На Фиг. 2 показано общее количество ацикловира (%) в рецепторной жидкости после 5 нанесений состава 1 (черный столбец) или эталонной композиции (серый столбец) на время 2, 6, 10 час и 24 час. Y-ось: мг ацикловира; X-ось: время (выраженное в часах), в которое отбирали образцы.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Как указано выше, настоящее изобретение относится к комбинации поликарбофила, поливинилпирролидона, глицерина и пропиленгликоля в конкретных массовых количествах и соотношениях.
Термин «процент (%) по массе» относится к проценту каждого ингредиента комбинации по отношению к общей массе.
Термин «массовое соотношение» относится к соотношению масс поликарбофила:поливинилпирролидона и глицерина:пропиленгликоля.
По настоящему изобретению, термин «поликарбофил» следует понимать как высокомолекулярный полимер акриловой кислоты, перекрестно сшитый с дивинилгликолем формулы (I).
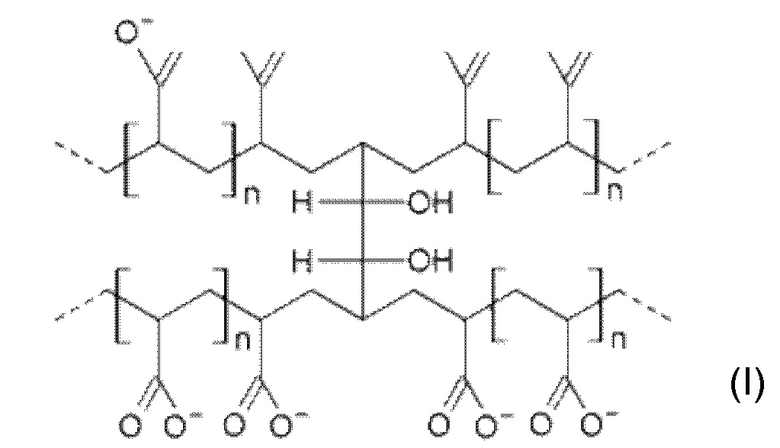
Его широко использовали для улучшения доставки активных ингредиентов к различным слизистым мембранам.
По настоящему изобретению, термин «поливинилпирролидон» и молекулярную формулу (C6H9NO)n следует понимать как водорастворимый полимер, полученный из мономера N-винилпирролидона:
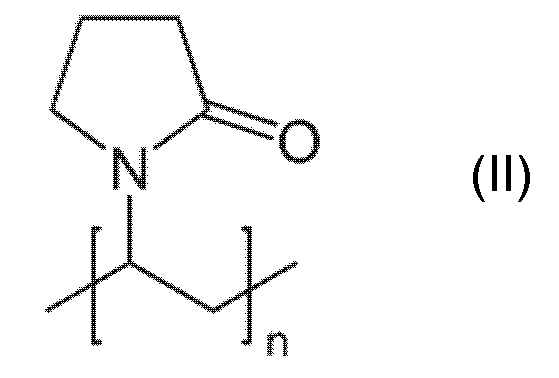 ,
,
и он имеет номер CAS 9003-39-8. Механизм остановки реакции полимеризации делает возможным получение растворимого поливинилпирролидона почти любой молекулярной массы. Различная длина цепей приводит к различной вязкости. Традиционно, степень полимеризации характеризуют значением K, которое в основном является функцией вязкости в водном растворе (иллюстративные неограничивающие примеры: K-15, K-25, K-30, K-60 и PVP K-90).
В одном варианте осуществления поликарбофил присутствует в количестве 3% по массе.
В другом варианте осуществления поливинилпирролидон присутствует в количестве 6% по массе.
В другом варианте осуществления глицерин присутствует в количестве 2% по массе.
В другом варианте осуществления пропиленгликоль присутствует в количестве 30% по массе.
По настоящему изобретению термин «гель» следует понимать как полутвердую форму, состоящую из жидкости (такой как вода или спирт), сгущенной с помощью комбинации по изобретению. В этих полутвердых системах жидкая фаза заключена внутри трехмерной матрицы с конкретной степенью ретикуляции.
По настоящему изобретению, термин «гидрогель» следует понимать как трехмерные, гидрофильные, полимерные сети, способные впитывать большие количества воды или биологических жидкостей. Сети состоят из гомополимеров или сополимеров, и являются нерастворимыми из-за присутствия химических перекрестных сшивок (узлы, мостики), или физических перекрестных сшивок, таких как переплетения или кристаллиты. Последние обеспечивают сетчатую структуру и физическую целостность. Эти гидрогели обладают термодинамической совместимостью с водой, которая позволяет им набухать в водной среде.
В одном варианте осуществления первого аспекта изобретения соотношение поликарбофил:поливинилпирролидон составляет 0,5:1.
В другом варианте осуществления первого аспекта изобретения массовое соотношение поливинилпирролидон:поликарбофил составляет 2:1.
В другом варианте осуществления первого аспекта изобретения массовое соотношение между глицерином:поликарбофилом составляет от 0,5:1 до 1:1.
В другом варианте осуществления первого аспекта изобретения массовое соотношение пропиленгликоль:поликарбофил составляет 10:1.
В одном варианте осуществления первого аспекта изобретения, комбинация включает регулирующее pH средство.
Иллюстративные неограничивающие примеры регулирующих pH средств включают в себя, среди прочих, уксусную кислоту, молочную кислоту, лимонную кислоту, этаноламин, муравьиную кислоту, щавелевую кислоту, гидроксид калия, гидроксид натрия, триэтаноламин, лимонную кислоту, цитрат мононатрия или монокалия, цитрат динатрия или дикалия, цитрат тринатрия или трикалия, фосфорную кислоту, фосфат мононатрия или монокалия, фосфат динатрия или дикалия, фосфат тринатрия или трикалия, глицин, трометамол или их смеси. Предпочтительно, регулирующее pH средство представляет собой трометамол. Обнаружено, что включение трометамола в комбинацию по изобретению улучшает стабильность полученного геля и помогает в растворении активного ингредиента в матриксе.
В одном варианте осуществления первого аспекта изобретения комбинация содержит трометамол в % по массе, составляющих от 1 до 5%, и в массовом соотношении трометамол:поликарбофил 1:1.
Предпочтительно, комбинация по первому аспекту изобретения представляет собой комбинацию, содержащую:
- поликарбофил: 3% по массе
- поливинилпирролидон: 6% по массе,
- глицерин: 2% по массе,
- пропиленгликоль: 30% по массе, и
- трометамол: 3% по массе.
Как упомянуто выше, в следующем аспекте настоящее изобретение относится к фармацевтической или ветеринарной композиции, содержащей комбинацию по первому аспекту изобретения, вместе с: (a) терапевтически эффективным количеством активного ингредиента или его фармацевтически приемлемой соли; и (b) подходящие фармацевтически или ветеринарно пригодные наполнители и/или носители.
Выражение «терапевтически эффективное количество», как применяют в настоящем документе, относится к количеству соединения, которое при введении является достаточным для предотвращения развития, или облегчения до некоторой степени, одного или нескольких симптомов заболевания, на которое оно нацелено. Конкретную дозу соединения, вводимого по этому изобретению, естественно, определяют конкретные условия, сопровождающие случай, включая вводимое соединение, способ введения, конкретное состояние, подвергающееся лечению, и подобные соображения.
Активный ингредиент можно выбирать из гидрофильных или гидрофобных активных ингредиентов, которые, необязательно, могут являться инкапсулированными. Иллюстративные неограничивающие примеры активных ингредиентов, которые можно включать в композицию по изобретению, представляют собой: химиотерапевтические средства, включая противовирусные средства (такие как ацикловир, пенцикловир, валацикловир, идоксуридин, тромантадин, имиквимод и метронидазол; антибиотики (такие как фусидовая кислота, мупироцин, гентамицин, неомицин, ретапамулин, клиндамицин, эритромицин и хлортетрациклин); противогрибковые средства, такие как производные имидазола и триазола (включая бифоназол, клотримазол, эберконазол, эконазол, фентиконазол, флутримазол, кетоконазол, миконазол, оксиконазол, сертаконазол, тиоконазол); нистатин, нафтифин, тербинафин, толнафтат и циклопирокс; способствующие заживлению средства, такие как Arnica montana, Centella asiatica и бекаплермин; местные антигистаминные средства, такие как дифенгидрамин, диметиндин и прометазин; местные анестетики, такие как лидокаин, бензокаин и татракаин; противопсориазные средства, такие как этанерцепт, адалимумаб, устекинумаб, дитранол, кальципотриол, кальцитриол, такальцитол и тазаротен; противовоспалительные средства, такие как средства стероидной природы (включая дексаметазон, преднизолон, триамцинолон, фторметолон, бетаметазон, будезонид, гидрокортизон, клобетазон, беклометазон, дезоксиметазон, метилпреднизолон) и нестероидные средства (AINE) (включая диклофенак, ацеклофенак, бензидамин, декскетопрофен, этофенамат, фепрадинол, ибупрофен, индометацин, кетопрофен, пироксикам); ретиноиды (такие как третиноин, изотретиноин и адапален); антисептические и дезинфицирующие средства (такие как хлоргексидин, борная кислота, триклозан); такролимус; гидрохинон; миноксидил; финастерид.
В одном варианте осуществления по второму аспекту изобретения композиция находится в форме гидрогеля, и активный ингредиент представляет собой: i) гидрофильный активный ингредиент или его соль, который, необязательно, является инкапсулированным, или, альтернативно, (ii) инкапсулированный гидрофобный активный ингредиент.
По настоящему изобретению термин «гидрофильный активный ингредиент» следует понимать как лекарственное средство, которое обладает поляризационным зарядом и способно связывать водород, что позволяет ему более легко растворяться в воде, чем в масле или других гидрофобных растворителях. Также известно как «полярное лекарственное средство», и оба термина можно использовать взаимозаменяемо.
По настоящему изобретению, термин «гидрофобный активный ингредиент» следует понимать как лекарственное средство, которое проявляет тенденцию являться неполярным и, таким образом, предпочитать другие нейтральные молекулы и неполярные растворители, а не воду. Гидрофобные молекулы в воде часто кластеризуются вместе, формируя мицеллы.
Как хорошо известно специалисту в данной области, параметром, пригодным для определения того, является ли активный ингредиент гидрофильным или гидрофобным, является определение его коэффициента распределения (P). Коэффициент распределения (P) представляет собой соотношение концентрации конкретного соединения в смеси из двух несмешивающихся фаз в равновесии. Обычно один из выбранных растворителей представляет собой воду, в то время как второй является гидрофобным, таким как октанол. Гидрофобные активные ингредиенты обладают высокими коэффициентами распределения октанол/вода, и гидрофильные активные ингредиенты обладают низкими коэффициентами распределения октанол/вода. Значение log P также известно в качестве показателя липофильности/гидрофильности. Логарифм соотношения концентраций неионизованного растворенного вещества в растворителях при конкретном pH называют log P: Значение log P также известно в качестве показателя липофильности:
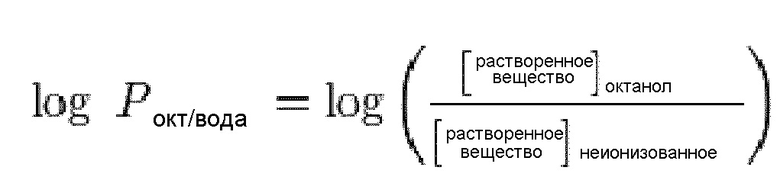 ,
,
где «растворенное вещество» представляет собой активный ингредиент.
По настоящему изобретению, выражение «инкапсулированный» следует понимать, как заключенный в микро- или наносистемах доставки, таких как микрочастица или наночастица.
Термин «микрочастица» следует понимать как относительно твердые сферические частицы с диаметром между 1 и 1000 микрометров, формирующие непрерывную систему сети или матрицы, составленную из одного или нескольких полимерных веществ, в которых диспергирован активный ингредиент. В соответствии с их структурой, микрочастицы можно классифицировать на микрокапсулы и микросферы. Таким образом, микрокапсулы представляют собой везикулярные системы, в которых активный ингредиент ограничен полостью и окружен полимерной мембраной; и микросферы представляют собой матричные системы, в которых активный ингредиент диспергирован.
Термин «наночастица», как применяют в настоящем документе, относится к частице, обладающей по меньшей мере двумя измерениями в наношкале, в частности, со всеми тремя измерениями в наношкале, где наношкала лежит в диапазоне от приблизительно 1 нм до приблизительно 1000 нм.
По настоящему изобретению, термин «фармацевтически или ветеринарно приемлемая соль» следует понимать как охватывающий любую соль, сформированную из любых фармацевтически или ветеринарно приемлемых нетоксичных кислот, включая неорганические или органические кислоты. Не существует ограничений относительно солей, за исключением того, что если их используют для терапевтических целей, они должны являться фармацевтически приемлемыми. Такие кислоты включает в себя, например, уксусную, бензолсульфоновую, бензойную, камфорсульфоновую, лимонную, этансульфоновую, фумаровую, глюконовую, глутаминовую, бромистоводородную, соляную, молочную, малеиновую, яблочную, миндальную, метансульфоновую, фосфорную, сорбиновую, янтарную, серную, виннокаменную, п-толуолсульфоновую кислоту и т.п.
Получение фармацевтически или ветеринарно приемлемых солей гидрофильных активных ингредиентов можно осуществлять способами, известными в данной области. Например, их можно получать из исходного соединения, содержащего основную или кислую группу, общепринятыми химическими способами. Как правило, такие соли, например, получают посредством реакции форм свободной кислоты или основания этих соединений со стехиометрическим количеством подходящих фармацевтически приемлемых основания или кислоты в воде или в органическом растворителе или в их смеси.
По настоящему изобретению, термин «фармацевтически приемлемые наполнители или носители» относится к фармацевтически приемлемым материалам, композициям или носителям. Каждый компонент должен являться фармацевтически приемлемым в смысле совместимости с другими ингредиентами фармацевтической композиции. Он должен также являться пригодным для использования в контакте с тканью или органом человека и животных без избыточной токсичности, раздражения, аллергического ответа, иммуногенности или других проблем или осложнений, в соответствии с целесообразным соотношением польза/риск. Подобным образом, термин «ветеринарно приемлемый» означает пригодный для использования в контакте с не относящимся к человеку животным.
Как показано ниже, в разделе Примеры, когда наносят фармацевтическую композицию по изобретению и анализируют образцы кожи в различное время, наблюдают большое увеличение концентрации активного ингредиента в коже по сравнению с контролем.
В одном варианте осуществления для фармацевтической или ветеринарной композиции по второму аспекту изобретения показан профиль замедленного высвобождения.
По настоящему изобретению, выражение «профиль замедленного высвобождения» следует понимать как высвобождение активного ингредиента с предопределенной скоростью, чтобы поддерживать постоянную концентрацию лекарственного средства в течение конкретного периода времени с минимальными побочными эффектами.
Фармацевтическую или ветеринарную композицию по настоящему изобретению можно вводить в любой пригодной форме, например, местно, внутрикожно или чрескожно. Предпочтительно, композицию вводят местно.
В одном варианте осуществления для фармацевтической или ветеринарной композиции показано замедленное высвобождение, и ее вводят местно.
В другом варианте осуществления фармацевтическая или ветеринарная композиция находится в форме биоадгезивной пленки.
Несколько способов хорошо известно в данной области для получения биоадгезивной пленки.
Для местного введения, пригодные фармацевтические наполнители или носители включают в себя, но без ограничения, гидратирующие средства, смягчающие средства, эмульгаторы, увлажняющие средства, регулирующие pH средства, антиоксиданты, консерванты, носители или их смеси. Используемые наполнители или носители обладают аффинностью к коже, являются хорошо переносимыми, стабильными, и их используют в количестве, адекватном для обеспечения желаемой консистенции и простоты нанесения.
Когда фармацевтическая композиция по настоящему изобретению является местной, ее можно составлять в нескольких формах, которые включают в себя, но без ограничения, растворы, суспензии, гидрогели, эмульгели, липогели, лосьоны, гели, мази, пасты и кремы, среди прочих. Эти местные фармацевтические композиции можно получать способами, хорошо известными в данной области. Подходящие фармацевтические наполнители и/или носители, и их количества, легко могут определить специалисты в данной области в соответствии с типом получаемого состава.
Примеры пригодных гидратирующих средств включают в себя, среди прочих, коллаген, аминокислоты коллагена, диметиконол, глицин, гиалуроновую кислоту, гиалуронат диметилсиланола, стеарат магния, мальтит, мальтозу, пирролидонкарбоновую кислоту (PCA), марганец-PCA, натрий-PCA, маннит, трегалозу, трилактин, глюкозу, глутаминовую кислоту, эритрит, стеароилглутамат алюмния, медь ацетилметионат или дитридецил димер дилинолеат.
Примеры пригодного эмульгатора включают в себя, среди прочих, глицерилтриолеат, глицерилолеат, ацетилированный дистеарат сахарозы, триолеат сорбитана, моностеарат полиоксиэтилена, моноолеат глицерина, дистеарат сахарозы, моностеарат полиэтиленгликоля, октилфеноксиполи(этиленокси)этанол, пентаизостеарат диацилглицерина, сесквиолеат сорбитана, гидроксилированный ланолин, лецитин, ланолин, триглицерилдиизостеарат, олеиловый эфир полиоксиэтилена, стеароил-2-лактилат кальция, лауроиллактилат натрия, стеароиллактилат натрия, цетеарилглюкозид, сесквистеарат метилглюкозида, монопальмитат сорбитана, сополимер метоксиполиэтиленгликоля-22/додецилгликоля, сополимер полиэтиленгликоля-45/додецилгликоля, дистеарат полиэтиленгликоля 400 и глицерилстеарата, сложные эфиры полиглицерила-3 из канделильского воска/жожоба/рисовых отрубей, цетиловый фосфат, цетиловый фосфат калия или их смеси.
Примеры пригодных coрастворителей для помощи в диспергировании лекарственного средства включают в себя, среди прочих, олеиловую кислоту, фосфолипиды, бензиловый спирт, бензилбензоат, бензоаты C12-C15 жирных кислот и транскутол.
Примеры пригодных хелатирующих средств для помощи в диспергировании или солюбилизации лекарственного средства представляют собой циклодекстрин и полифосфаты.
Примеры пригодных поверхностно-активных средств включают в себя, среди прочих, неионное, ионное (либо анионное, либо катионное) или цвиттерионное (или амфотерное, где головка поверхностно-активного вещества содержит две группы с противоположными зарядами) поверхностно-активные вещества. Примеры анионных поверхностно-активных веществ представляют собой, например, поверхностно-активные вещества на основе анионов сульфата, сульфоната или карбоксилата, такие как перфтороктаноат (PFOA или PFO), алкилбензолсульфонат, мыла, соли жирных кислот, или соли алкилсульфата, такие как перфтороктансульфонат (PFOS), додецилсульфат натрия (SDS), лаурилсульфат аммония или лауриловый эфир сульфата натрия (SLES). Примеры катионных поверхностно-активных веществ представляют собой, например, поверхностно-активные вещества на основе катионов четверичного аммония, таких как алкилтриметиламмоний, включая бромид цетилтриметиламмония (известный также как CTAB) или бромид гексадецилтриметиламмония, хлорид цетилпиридиния (CPC), амин полиэтоксилированного жира (POEA), хлорид бензалкония (BAC) или хлорид бензэтония (BZT). Примеры цвитерионных поверхностно-активных веществ включают в себя, но без ограничения, додецилбетаин, кокамидопропилбетаин или кокоамфоглицинат. Примеры неионных поверхностно-активных веществ включают в себя, но без ограничения, алкилполи(этиленоксид), алкилфенолполи(этиленоксид), сополимеры поли(этиленоксида), поли(пропиленоксида) (с коммерческим наименованием полоксамеры или полоксамины), алкилполиглюкозиды, включая октилглюкозид и децилмальтозид, жирные спирты, включая цетиловый спирт и олеиловый спирт, кокамид MEA, кокамид DEA или полисорбаты, включая твин 20, твин 80 или додецилдиметиламиноксид.
Примеры пригодных местных увлажняющих веществ включают в себя, среди прочих, глицерин, диглицерин, этилгексилглицерин, глюкозу, мед, молочную кислоту, полиэтиленгликоль, пропиленгликоль, сорбит, сахарозу, полидекстрозу, натрий гиалуронат, лактат натрия, тагатозу или трегалозу.
Примеры пригодных местных регулирующих pH средств включают в себя, среди прочих, уксусную кислоту, молочную кислоту, лимонную кислоту, этаноламин, муравьиную кислоту, щавелевую кислоту, гидроксид калия, гидроксид натрия, триэтаноламин, лимонную кислоту, цитрат мононатрия или монокалия, цитрат динатрия или дикалия, цитрат тринатрия или трикалия, фосфорную кислоту, фосфат мононатрия или монокалия, фосфат динатрия или дикалия, фосфат тринатрия или трикалия, глицин или их смеси.
Примеры пригодных антиоксидантов включают в себя, среди прочих, средства для поглощения свободных радикалов или восстанавливающие средства, такие как ацетилцистеин, аскорбиновая кислота, аскорбилпальмитат, бутилированный гидрокситолуол, экстракт зеленого чая, кофейная кислота, цистеин, токоферол, убихинон, пропилгаллат, бутилгидроксианизол, бутилированный гидрокситолуол (BHT) и их смеси.
Примеры пригодных консервантов включают в себя, среди прочих, бензойную кислоту, бутилпарабен, этилпарабен, диазолидинилмочевину, имидомочевину, пропилпарабен, метилпарабен, сорбиновую кислоту, сорбат калия, бензоат натрия, феноксиэтанол, триклозан или их смеси.
Композиции, упомянутые выше, включают также носитель. Примеры носителей включают в себя, но без ограничения, воду, бутиленгликоль, этанол, изопропанол или силиконы. Предпочтительно, носитель представляет собой воду.
Кроме того, композиции по настоящему изобретению могут содержать другие ингредиенты, такие как ароматизаторы, красители и другие компоненты, известные в данной области для использования в местных составах.
Фармацевтическую или ветеринарную композицию можно наносить на интактную или поврежденную кожу.
Повреждения кожи можно классифицировать на первичные и вторичные повреждения. Первичные повреждения кожи варьируют по цвету или текстуре, которые могут присутствовать при рождении (такие как родимые пятна), или которые могут быть приобретены на протяжении жизни лица, такие как повреждения, ассоциированные с инфекционными заболеваниями (например, псориазом), аллергическими реакциями (например, сыпью или контактным дерматитом) или агентами внешней среды (например, солнечным ожогом, экстремальными давлением или температурой). Вторичные повреждения кожи представляют собой те изменения кожи, которые возникают в результате первичных повреждений кожи, либо как естественное прогрессирование, либо в результате манипуляции лица (например, расчесывания или ковыряния) с первичным повреждением. Основными типами вторичных повреждений кожи являются, среди прочих, язвы, чешуйки, струпья, эрозия, царапины, шрамы, лихенификация и атрофии.
Настоящее изобретение относится, в третьем аспекте изобретения, к способу получения фармацевтической или ветеринарной композиции, содержащей комбинацию по первому аспекту изобретения. Как указано выше, такая композиция не имеет сгустков.
В одном варианте осуществления способа по третьему аспекту, поликарбофил предварительно просеивают.
В другом варианте осуществления способа по третьему аспекту изобретению активный ингредиент, или его фармацевтически или ветеринарно приемлемую соль предварительно растворяют в спиртовом растворителе.
Термин «спиртовой растворитель» следует понимать как C1-C10 спиртовой растворитель. Иллюстративными неограничивающими примерами спиртовых растворителей являются, среди прочих, метанол, этанол, пропанол, изопропанол, бутанол, изобутанол.
Настоящее изобретение также относится к набору, содержащему комбинацию или композицию, как определено выше, и подложку.
Подложка может являться покрытой комбинацией по настоящему изобретению, при условии, что сохраняются биоадгезивные свойства, подробно описанные выше. Предпочтительно, материал-носитель является покрытым, и более предпочтительно, является покрытым с одной стороны. В случае покрытия, не проводят стадии сушки (в таком случае комбинация или композиция по изобретению может утратить свои преимущественные свойства).
По настоящему изобретению термин «подложка» следует понимать как любой общепринятый материал-носитель, известный для использования в перевязке. Является предпочтительным, чтобы материал-носитель был изготовлен из неэластичных волокон. Материал-носитель, как правило, является либо вязаным, штампованным, тканым, либо нетканым. Он, необязательно, находится в форме пены или пленки. Волокна изготовлены из хлопка, вискозы, полиэфира, полиамида, полипропилена, полиамида или шерсти, или их смеси.
Способы получения таких медицинских устройств хорошо известны специалистам в данной области.
Кроме того, набор может включать в себя инструкции для его использования в любом из применений, упомянутых выше.
В шестом аспекте, настоящее изобретение относится к комбинации по изобретению в форме формирующего пленку средства посредством накопления комбинации на ткани организма, таким образом, абсорбции влаги из ткани, и формирования пленки над поверхностью ткани организма.
На протяжении описании и формулы изобретения слово «содержать» и варианты слова, не предназначены для исключения других технических признаков, добавок, компонентов или стадий. Более того, слово «содержать» включает случай «состоять из». Дополнительные объекты, преимущества и признаки изобретения станут очевидными специалистам в данной области после изучения описания или их можно изучить посредством практического осуществления изобретения. Следующие примеры представлены с целью иллюстрации и не предназначены для ограничения настоящего изобретения. Более того, настоящее изобретение охватывает все возможные комбинации конкретных и предпочтительных вариантов осуществления, описанных в настоящем документе.
ПРИМЕРЫ
Пример 1: Состав с комбинацией по изобретению и ацикловиром (Состав 1)
Поликарбофил (Noveon AA-1)
PVP 30
Ментол кристаллический
Трометамол
Глицерин
Пропиленгликоль
Деионизированная вода
Все компоненты взвешивали на коммерческих высокоточных весах. Затем кристаллический ментол измельчали в ступке и затем его растворяли, при встряхивании, в пропиленгликоле. Раствор помещали в сосуд для преципитации и, при встряхивании, вводили ацикловир.
С другой стороны, трометамол растворяли в деионизированной воде. Затем, вводили повидон и растворяли, при встряхивании, в растворе трометамола. Полученный раствор вводили в полученный ранее раствор ацикловира и, с использованием эмульгатора Bi-agi®, вводили глицерин. При введении, Noveon AA-1 просеивали (размер ячеек: 0,5 мм) и медленно вводили в эмульсию с использованием коммерческого эмульгатора Bi-agi®, таким образом, получая состав 1.
Пример 2: Состав с комбинацией по изобретению и фусидовой кислотой (Состав 2)
Поликарбофил (Noveon
Повидон (PVK 29/32)
Тимол
Трометамол
Глицерин
Пропиленгликоль
Деионизированная вода
Следовали такому же способу, как способ в примере 1, для получения состава 1, при условии, что использовали тимол вместо кристаллического ментола.
Пример 3: Дермальная доставка и анализ абсорбции через кожу состава 1
A) Материалы и методы
A.1. Использовали кожные мембраны человеческого абдоминального происхождения от женщин после пластической операции. Расщепленную кожу (приблизительно 500 p.m) получали с помощью дерматома, и она содержала роговой слой, эпидермис и часть дермы. Фрагменты кожи получали для использования в диффузионной ячейке (диаметр участка воздействия 10 мм) с помощью штампа. Фрагменты кожи замораживали между предметными стеклами при -15°C. Толщину полученной расщепленной кожи измеряли между двумя предметными стеклами.
Поскольку получение мембраны может приводить к повреждению кожи, целостность кожной мембраны проверяли перед ее установкой в диффузионную ячейку.
A.2. Фосфатно-солевой буфер (PBS) использовали в качестве рецепторной жидкости. Для достижения свободного от пузырьков воздуха равновесия диффузионной тест-системы и диффузионных ячеек, рецепторную жидкость дегазировали перед использованием.
A.3. Диффузионную ячейку разрабатывали с политетрафторэтеновой (PTFE)-донорной и -акцепторной частью для потока через диффузионную ячейку для горизонтального воздействия на поверхность кожи. Площадь области воздействия кожи составляла приблизительно 80 мм2. Диффузионные ячейки устанавливали в термостатируемый блок под контролем микропроцессора. Многоканальный перистальтический насос соединяли с рецепторной частью диффузионной ячейки, и сбор образцов осуществляли с помощью программируемого коллектора фракций.
Замороженную кожу промывали акцепторной жидкостью (PBS) и помещали в акцепторный отсек. Диффузионную ячейку закрывали с помощью рецепторного отсека и уравновешивали с помощью дегазированной рецепторной жидкости (PBS) в горизонтальном положении в термоблоке. Диффузионные ячейки доводили до температуры приблизительно 32°C.
Наконец, кожу, встроенную в диффузионную ячейку, проверяли на целостность барьера с использованием меченной тритием воды. Кратко, после уравновешивания кожных мембран в течение приблизительно 15 мин, 40 мкл меченной тритием воды (1 кБк) наносили на поверхность кожи в течение 20 мин. Поток рецепторной жидкости регулировали для доставки приблизительно 0,2 мл/час. Затем неабсорбированную жидкость промокали ватной палочкой и 40 пл PBS наносили на поверхность кожи. Эффлюент из проточной ячейки собирали в течение дополнительных 60 мин. Кожу рассматривали как неповрежденную, если не более 2% нанесенной радиоактивности выделяли из рецепторной жидкости.
B. Способ
Тестировали два различных состава: Состав 1 (Пример 1) и, в качестве контроля, выбрали зовиракс.
Для каждого состава, 3 повтора получали для каждого времени отбора образцов, из-за высокой межиндивидуальной вариабельности. Во все периоды времени отбора образцов, кожу, рецепторную жидкость и оставшийся тестируемый и контрольный продукт выделяли для аналитического анализа.
Количество нанесений контрольного и тестируемого состава, 7 мг/диск кожи (соответствующее 9 мг/см2), составляло 5 раз за 24 час (время нанесения 0 час, 4 час, 8 час, 12 час, 16 час), следуя рекомендованной дозе из справочных инструкций производителя. Тестируемое/контрольное вещество не удаляли ни в какое время, но добавляли к ранее нанесенному составу.
Сбор рецепторной жидкости начинали во временной точке t 0 час. Поток рецепторной жидкости регулировали для доставки приблизительно 0,2 мл/час.
Во временных точках 2 час, 6 час, 10 час и 24 час соответствующие образцы кожи, рецепторной жидкости и смывов с кожи собирали для их последующего анализа LC-MS.
В конце периода воздействия, остатки тестируемого и контрольного продукта вытирали с донорной стороны диффузионной ячейки, так же как с поверхности кожи, с помощью ватной палочки. Кроме того, проводили различные стадии промывки с помощью PBS рецепторной жидкости для удаления для удаления оставшегося тестируемого/контрольного вещества. Ватные палочки и промывочную жидкость сохраняли при -15°C для дальнейшего анализа оставшегося и контрольного продукта.
Диски кожи и собранную рецепторную жидкость сохраняли при 5,15°C для дальнейшего анализа.
C. Анализ данных
Все образцы сохраняли замороженными до проведения анализа.
На момент анализа, образцы кожи и образцы оставшегося тестируемого и контрольного продукта обрабатывали для экстракции всего ацикловира. Это проводили с помощью гомогенизации кожи с использованием системы FastPrep24 (MP Biomedicals) с последующей тепловой экстракцией (60°C, 30 мин) и преципитацией белка с использованием ацетонитрила.
После преципитации ацикловира во всех подлежащих анализу образцов, следовали способу детекции LC-MS/MS. Кратко, использовали систему жидкостной хроматографии (Agilent серии 1200) с детектором масс (AB Sciex, API 4000M), содержащую систему сбора данных Analyst версии 1.4.2.
Для хроматографического разделения соединений использовали колонку HPLC (Luna Hilie (3 tim, 100x2,0 мм, Phenomenex) в условиях изократического градиента с ацетонитрилом и 50 мМ форматом аммония в качестве подвижной фазы.
Конкретные условия представляли собой:
GCV: приблизительно 3,6 мин
Из полученных данных получали профиль абсорбции через кожу.
D. Результаты
На Фиг. 1, где количество ацикловира определяют в коже, можно наблюдать, что существует значительный эффект накопления, когда вводят композицию по изобретению. Фактически, показано, что через 10 и 24 час количество ацикловира, доступное на коже, значительно выше по сравнению с количеством, полученным при нанесении контрольного состава.
Эти данные поддерживают тот факт, что комбинация по изобретению обеспечивает матрицу, внутри которой активный ингредиент является высоко биодоступным.
Кроме того, такой эффект «накопления», наблюдаемый с составом по изобретению, является показателем его сильного биоадгезивного профиля. Чтобы получить такое поведение, комбинация по изобретению проявляет адгезию к ткани организма, где она нанесена, формируя тонкую пленку (которая является ответственной за высокую биоадгезивность, наблюдаемую с комбинацией по изобретению). Благодаря сильной биоадгезии и физико-химическим свойствам гелевой матрицы (определяемым эксципиентами, процентами, и соотношениями, составляющими комбинацию по изобретению), активный ингредиент диффундирует из гелевой матрицы и проникает в кожу.
Вышеуказанное дополнительно поддерживают данные из таблицы 3, где указано количество ацикловира на коже после нескольких промывок рецепторной жидкостью:
Как можно видеть, количество ацикловира, детектированное в коже, является по меньшей мере 2-кратным, когда состав 1 наносят на кожу, по сравнению с количеством лекарственного средства при нанесении контрольной композиции.
Кроме того, на Фиг. 2 показано, что ацикловир не детектируют в рецепторных жидкостях, собранных, когда нанесенный состав представляет собой состав из примера 1, в отличие от результатов, полученных с контрольным составом. Это является показателем того, что матрица, обеспеченная комбинацией информации, обеспечивает подходящее окружение для заключенного в ней лекарственного средства таким образом, что его доставляют непрерывным образом, оно проникает в кожу, но не достигает системного кровотока.
E. Заключения
Это означает, что комбинация по изобретению обеспечивает матрицу, которая: (a) не оказывает отрицательного влияния на биодоступность лекарственного средства, но напротив, гарантирует значительную биодоступность лекарственного средства, (b) указанное лекарственное средство остается в коже на протяжении более длительного периода времени (что объясняет такой эффект накопления), (c) обладает лучшим биоадгезивным профилем, чем контрольная композиция, гарантируя, даже в неблагоприятных условиях (таких как промывки кожи), количество активного ингредиента, по меньшей мере удваивающее количество, доступное с контрольной композицией, и (d) лекарственное средство не достигает системного кровотока.
Из полученных результатов, таким образом, можно заключить, что комбинацию по настоящему изобретению можно использовать для составления фармацевтической или ветеринарной композиции с использованием более низких количеств активного ингредиента или со снижением дозы/количества нанесений для получения желательного терапевтического эффекта.
В общем, композиция по изобретению обеспечивает важные дополнительные коммерческие преимущества, как получение гидрофильной биоадгезивной пленки, которая действует как высвобождающий резервуар или матрица, обеспечивая сохранение активного вещества в течение более длительного периода по сравнению с общепринятыми видами лечения. Ее биоадгезивные свойства вместе с ее эстетическими свойствами (прозрачностью) облегчают соблюдение режима лечения пациентом (снижают среднюю продолжительность обработки).
Хотя эти анализы проводили с помощью состава 1, специалисту в данной области понятно, что преимущества, на которые указано в этом примере, так же как на протяжении всего описания, обусловлены комбинацией эксципиентов, в указанных соотношениях и массовых процентах.
Пример 4: Токсикологические анализы для состава 1
Ацикловир является хорошо известным веществом, профиль безопасности которого твердо установлен. Однако для проверки профиля безопасности комбинации по изобретению, осуществили набор исследований безопасности и требуемой переносимости с составом 1 (в этом разделе, обозначенном также как «тестируемый продукт»), из которых исследование кожной переносимости на кроликах в однократной дозе, исследование кожной переносимости на кроликах в повторяющихся дозах и исследование глазной переносимости на кроликах в однократной дозе включены ниже.
В качестве контроля использовали носитель состава 1, то есть: поликарбофил (Noveon AA-1): 3 г; PVP 30: 6 г; кристаллический ментол: 0,10 г; трометамол: 3 г; глицерин: 2 г; пропиленгликоль: 30 г; и деионизированная вода: 55,90 г. Все компоненты смешивали, как описано в примере 1.
Как заключили, состав 1 обладает отличной кожной переносимостью в условиях клинического применения по меньшей мере с такими же границами безопасности и эффективности, как его контрольный продукт.
Пример 4.1: Исследование глазной переносимости на кроликах в однократной дозе: острое глазное раздражение/разъедание
A) Цель
Целью этого исследования являлась оценка глазной переносимости (тест раздражения/разъедания) состава 1, после нанесения однократной дозы в конъюктивальный мешок кроликов.
В этом исследовании являлось необходимым продолжать до полной оценки симптомов (интенсивность, время начала, обратимость), вызванных продуктом, чтобы получить степень раздражения или разъедания. В исследовании необработанный глаз использовали в качестве контроля.
B) Условия тестирования
Исходный тест (раздражение/разъедание): Новозеландским кроликам проводили однократное нанесение 0,1 мл тестируемого продукта в конъюктивальный мешок правого глаза. Левый глаз являлся необработанным и служил в качестве контроля.
Через 72 часа после введения и в отсутствие разъедания, авторы настоящего изобретения переходили к реализации следующего подтверждающего теста.
Подтверждающий тест (раздражение): В отсутствие сильного раздражения, двум новозеландским кроликам одновременно проводили однократное нанесение 0,1 мл тестируемого продукта в конъюктивальный мешок правого глаза. Левый глаз обоих кроликов являлся необработанным и служил в качестве контроля.
Поскольку эффектов разъедания или раздражения не детектировали в течение 72 часов, не являлось необходимым оценивать обратимость, и исследование прекратили. Таким образом, для каждого из 3 животных, период наблюдения составлял 3 суток (72 часа).
C) Способ
Животных обозначали и распределяли по индивидуальным клеткам. После периода акклиматизации начинали исходный тест и для этого, за 24 часа до введения, авторы настоящего изобретения переходили к обследованию глаз первого животного, с использованием лупы и фонарика. Животному, обозначенному как 1, проводили нанесение однократной дозы 0,1 мл тестируемого продукта в конъюктивальный мешок правого глаза. Продукт наносили посредством осторожного оттягивания нижнего века наружу от глазного яблока. После нанесения, веки удерживали вместе в течение приблизительно одной секунды, чтобы предотвратить потерю материала. Левый глаз являлся необработанным и служил в качестве контроля. В отсутствие признаков разъедания или сильного раздражения, авторы настоящего изобретения проводили подтверждающий тест, и для этого авторы настоящего изобретения переходили одновременно к двум другим животным из исследования (обозначенным 2 и 3) таким же способом, как описано выше.
Ни для одного животного не показали раздражения глаз, дефектов глаз или изменений роговицы перед введением, так что всех животных могли использовать. Животных направляли на исследование, которое включало в себя: клиническое обследование и оценку глазного раздражения/разъедания, как подробно описано ниже.
D) Клиническое обследование
Выживаемость/смертность: ежесуточно, в течение 3 суток после введения.
Масса животного: при прибытии животных, в начале и перед умерщвлением, как в PNT-BT-502.
Общие симптомы: до и после введения, и ежесуточно в течение 3 суток после.
E) Оценка разъедания глаза
Глазное разъедание оценивали в качестве части исходного теста, немедленно после нанесения продукта и через 1, 24, 48 и 72 часов. Его оценивали в отношении присутствия-отсутствия, повреждения считали необратимыми в форме: перфорации или значительного изъязвления роговицы, изъязвления или некроза конъюнктивы, некроза третьего века, внутриглазной геморрагии, помутнения роговицы 4 степени, которое сохраняется в течение 48 часов, и отсутствия реакции радужной оболочки глаза на свет 2 степени, которое сохраняется в течение 72 часов.
На время оценки через один час после нанесения, не присутствовало остатков тестируемого продукта, так что не было необходимости промывки солевым раствором.
F) Оценка раздражения глаза
Глазное раздражение оценивали для 3 животных из исследования (исходное и подтверждающее исследования); через 1, 24, 48 и 72 часа после нанесения продукта. В отсутствие раздражения, не являлось необходимым исследовать обратимость, и исследование прекратили через 72 часа обработки.
Наблюдали степень и природу раздражения, так же как любое гистопатологическое повреждение. Оценку глазных повреждений проводили при иммобилизации животного в специальных захватах. Оценивали глазную реакцию (числовые значения между 0 и 4) в соответствии с таблицей 4:
По окончании пилотной фазы, животных умерщвляли посредством летальной инъекции, с предварительным усыплением. Оба глаза у всех животных вырезали для патологоанатомического анализа. Образцы фиксировали в 10% формальдегиде и перерабатывали, разрезали и посылали в Отделение морфологии CIMA для их погружения, нарезки и окрашивания (гематоксилином-эозином), и для получения гистологических препаратов. Патологоанатомическое обследование этих препаратов проводили в Отделении патологоанатомической диагностики для лабораторных животных (DAPAL) Университета Сарагосы.
H) Результаты и обсуждение
H.1. Выживаемость/смертность и общие симптомы: не зарегистрировано летальности ни для одного из животных, которым вводили тестируемый продукт. Для экспериментальных животных не показано изменений в общем состоянии.
H.2. Макроскопическая оценка глазного разъедания: исследование глазного разъедания в исходном тесте не показало присутствия необратимого повреждения, такого как перфорация или значительное изъязвление роговицы, изъязвление или некроз конъюнктивы, некроз третьего века, внутриглазная геморрагия, помутнение роговицы 4 степени, которое сохраняется в течение 48 часов, и отсутствие реакции радужной оболочки глаза на свет 2 степени, которое сохраняется в течение 72 часов.
H.3. Макроскопическая оценка глазного раздражения: как отражено в таблице 5, после нанесения тестируемого продукта, не наблюдали отека или изменений в конъюнктиве, радужной оболочке или роговице.
Оценка глазного раздражения. Индивидуализированные данные
Средние изменения в роговице, радужной оболочке, конъюнктиве и отеке. Индивидуализированные данные
Определили, что не присутствовало раздражения.
H.4. Микроскопические обнаружения: не наблюдали морфологических различий между обработанными и контрольными образцами.
I) ЗАКЛЮЧЕНИЕ
Состав 1 классифицировали как не раздражающий.
Гистологическое обследование глазных яблок не выявило морфологических различий между обработанными и контрольными образцами.
Пример 4.2: Исследование кожной переносимости повторяющейся дозы у кроликов
A) Цель: оценка местной переносимости тестируемого продукта у кроликов, после дермального нанесения повторяющейся дозы 1 мл/120 см2 (8,3 мкл/см2), 4 раза ежесуточно, вплоть до максимум 10 суток, с оценкой переносимости на сутки 1, 5 и 10. Более того, чтобы оценить влияние носителя состава на полученные данные переносимости, в исследование включали группу животных, параллельно с группой обработки, которым вводили носитель тестируемого продукта.
Наконец, чтобы оценить обратимость повреждений кожи, которые могут возникать после введения тестируемого продукта или его носителя в течение 10 суток, авторы настоящего изобретения включали две группы животных (группу обратимости после обработки и группу обратимости после носителя), в которых, если считали необходимым, период наблюдения могли продлевать до 7 суток после последнего введения.
B) Условия тестирования
Распределение
24 самца новозеландских кроликов, в 2 группах (n=12) и - лечение и носитель-. Каждую группу делили на 4 подгруппы (n=3) -a, b, c и обратимости-.
Позология
4 ежесуточных дермальных нанесения (в диапазоне 2,5 часов ± 15 минут) тестируемого продукта 1 мл/120 см2 (8,3 мкл/см2). Нанесения проводили в выбритой области 120 см2 (приблизительно 10% ткани организма). Количество нанесений зависело от подгрупп, и для каждой подгруппы сутки начала обработки считали сутками 0:
Подгруппа a: введение только одни сутки (Сутки 0).
Подгруппа b: ежесуточное введение в течение 5 суток (Сутки 0-4, включительно).
Подгруппа c: ежесуточное введение в течение 10 суток (Сутки 0-9, включительно).
Подгруппа обратимости: ежесуточное введение в течение 10 суток (Сутки 0-9, включительно).
Период наблюдения:
• группы обработки и носителя (подгруппы a, b и c): Вплоть до 16 часов после последнего введения.
• группы обработки и носителя (подгруппы обратимости): Вплоть до 72 часов после последнего введения.
C) Способ
Животных обозначали и распределяли на две группы: группа обработки и группа носителя, состоящие из 12 животных. В свою очередь, каждую группу делили на 4 подгруппы -a, b, c и обратимости-, сформированные из 3 животных каждая. Содержание животных являлось индивидуализированным.
Распределение животных, расписание введения и наблюдения отражены в таблице 7:
(8,3 мкл/см2)
1-3
(8,3 мкл/см2)
4-6
(8,3 мкл/см2)
7-9
(8,3 мкл/см2)
10-12
(8,3 мкл/см2)
1-3
(8,3 мкл/см2)
4-6
(8,3 мкл/см2)
7-9
(8,3 мкл/см2)
10-12
Животных брили, и область 12 см x 10 см (120 см2) отмечали несмываемой краской на спине животного (приблизительно 10% ткани организма), и следили, чтобы сохранить область ясно идентифицируемой на протяжении исследования, выбривая и отмечая область при необходимости. В этой области, животным вводили ежесуточно 4 введения 1 мл тестируемого продукта или его носителя (8,3 мкл/см2 площади поверхности), с интервалом 2,5 часа ± 15 минут, в течение 1, 5 или 10 суток в соответствии с подгруппой.
Выполняли дермальное нанесение, и для этого в шприц заряжали 1 мл тестируемого продукта (или носителя тестируемого продукта), наносили в центр отмеченной области на спине животного (область нанесения) и рукой подлежащий нанесению продукт распределяли по ограниченной области. Животное не возвращали в клетку, пока не наблюдали формирование нелипкой адгезивной пленки. Область введения ни в одном из случаев не промывали, так что даже когда в ходе последующего введения наблюдали остатки адгезивной пленки, новое нанесение выполняли поверх них.
Животных из всех групп/подгрупп включали в исследование, которое включало в себя: клиническое обследование и оценку местной переносимости, как подробно описано ниже.
D) Клиническое обследование
Выживаемость/смертность: ежесуточно
Общие симптомы: поведение животных мониторировали ежесуточно в ходе периода введения. Исследование включало в себя оценку общего состояния, активности, положения тела, цвета кожи, глаз, слизистых мембран и присутствия/отсутствия судорог, тремора, диареи и пилоэрекции. Масса животного: при прибытии животных, в начале и перед умерщвлением.
E) Оценка местной переносимости (Макроскопическая оценка): природу и диапазон наблюдаемой реакции оценивали макроскопически. Оценивали присутствие покраснения, отека, шелушения. Сутки наблюдения представляли собой сутки 1 для подгрупп a, b, c и обратимости; сутки 5 для подгрупп b, c и обратимости; и сутки 10 для группы c и обратимости. Для исследования обратимости изменений, наблюдаемых после 10 суток обработки, проводили оценку подгруппы на время 24, 48 и 72 часа после последнего введения (сутки 10, 11 и 12).
Животных умерщвляли посредством летальной инъекции, с предварительным усыплением.
Затем образцы кожи получали, разрезали и посылали в Отделение морфологии CIMA для их погружения, нарезки и окрашивания (гематоксилином-эозином). Патологоанатомическое обследование проводили в Отделении патологоанатомической диагностики для лабораторных животных (DAPAL) Университета Сарагосы.
F) Результаты и обсуждение
F.1. Выживаемость/смертность и общие симптомы: не зарегистрировано смертности ни для одного из животных, которым вводили тестируемый продукт или его носитель. Для животных не показано изменений в общем состоянии на протяжении суток обработки.
Выживаемость/смертность.
Индивидуализированные данные для групп обработки
F.2. Макроскопическая оценка: введение тестируемого продукта в 4 нанесениях/сутки на протяжении 1, 5 и 10 суток оцененное в подгруппах после обработки a, после обработки b, после обработки c и после обработки, группа обратимости, не вызывало признаков кожных нарушений ни у одного из подвергнутых лечению животных (см. таблицу 9).
Что касается группы животных, которым вводили носитель, на сутки 5 (после 20 нанесений) наблюдали присутствие очень слабого покраснения (степени 1) у двух животных (обозначенных как 7 и 12). В случае животного 12, покраснение сопровождалось шелушением умеренной интенсивности. Тяжесть покраснения и шелушения уменьшалась до макроскопической оценки, проведенной на сутки 10 (после 40 нанесений). Оценки животного 12 из подгруппы обратимости с носителем, через 24, 48 и 72 часа после обработки, подтвердили регрессию покраснения, в то время как шелушение оставалось с очень низкой интенсивностью, едва заметное.
Оценка кожной переносимости для групп обработки. Индивидуализированные данные на сутки 1, 5 и 10
Количественная оценка покраснения, отека и шелушения, выраженная как:
Замечание 1: При любой оценке присутствовал какой-либо другой признак, такой как язвы, кровотечение, корка или другой.
G) ЗАКЛЮЧЕНИЕ
Дермальное нанесение тестируемого продукта в количестве 1 мл/120 см2 при 4 нанесениях ежесуточно в течение 10 суток, являлось не раздражающим и полностью безопасным.
Пример 4.3: Исследование кожной переносимости на кроликах в однократной дозе: острое кожное раздражение/разъедание
A) Цель: целью этого исследования являлась оценка дермальной кожной переносимости (раздражения/разъедания) тестируемого продукта после нанесения однократной дозы на интактную кожу у кроликов.
Для оценки влияния носителя состава на наблюдаемые эффекты, в исследовании предусматривали его нанесение на независимую отдельную область (рассматриваемую как контрольную область носителя). Наконец, у каждого животного, необработанная область служила областью отрицательного контроля.
B) Условия тестирования
Исходный тест (раздражение/разъедание): Новозеландским кроликам вводили однократную 0,5 мл дозу как тестируемого продукта (область обработки), так и его носителя (контрольная область носителя), нанесенную дермально в область спины животного, на ткань организма приблизительно 6 см2 для каждой области введения. Период воздействия составлял 4 часа. В отсутствие признаков разъедания в течение 72 часов, авторы настоящего изобретения переходили к реализации следующего теста (подтверждающего теста).
Подтверждающий тест (тест раздражения): Двум новозеландским кроликам вводили однократную дозу 0,5 мл тестируемого продукта (область обработки) и его носителя (контрольная область носителя), нанесенную дермально в область спины животного, на ткань организма приблизительно 6 см2 для каждого нанесения. Период воздействия составлял 4 часа. Период наблюдения (за сутки 0 принимали сутки нанесения продукта): Поскольку не детектировали разъедающих или раздражающих эффектов в течение 72 часов, не являлось необходимым оценивать обратимость, и исследование прекратили. Таким образом, для каждого из 3 животных, период наблюдения составлял 3 суток (72 часа).
C) Способ
Животных обозначали и распределяли по индивидуальным клеткам. После периода акклиматизации начинали исходный тест, и для этого приблизительно за 24 часа до введения, спину первого животного аккуратно выбривали.
Для дермального введения в шприц заряжали 0,5 мл тестируемого продукта, которые наносили в центр обрабатываемой отмеченной области на спине животного, и рукой продукт распределяли по определенной области. Затем авторы настоящего изобретения эквивалентным образом переходили к носителю. Через 90 минут после введения, марлю помещали на каждую область введения. Наконец, эластичный бинт помещали вокруг марли, которую фиксировали пластырем. Перевязочную подушку удаляли через 4 часа после нанесения. Обе области оценивали, немедленно после удаления бинта и через 1, 24, 48 и 72 часов.
Поскольку не детектировано эффектов разъедания через 72 часа, авторы настоящего изобретения переходили к подтверждающему тесту. Для этого авторы настоящего изобретения переходили сходным образом к другим двум животным из этого исследования. Трех животных направляли на исследование, которое включало в себя: клиническое обследование и оценку кожного раздражения, как подробно описано ниже.
D) Клиническое обследование
Выживаемость/смертность: ежесуточно, в течение 3 суток после введения. Масса животного: при прибытии животных, в начале и перед умерщвлением.
Общие симптомы: до и после введения, и ежесуточно в течение 3 суток после.
E) Оценка кожного разъедания
Кожное разъедание оценивали в качестве части исходного теста, после удаления бинта и через 1, 24, 48 и 72 часа. Реакцию оценивали в отношении присутствия-отсутствия для язв, кровотечения и корки с геморрагическим компонентом.
F) Оценка раздражения кожи
Раздражение кожи оценивали для 3 животных из исследования (исходный и подтверждающий тест) через 1, 24, 48 и 72 часов после удаления бинта. Не наблюдали изменений, так что не являлось необходимым продлевать период исследования.
Наблюдали степень и природу раздражения, так же как возможное гистопатологическое повреждение. Реакции кожи оценивали (числовые значения между 0 и 4) в соответствии со следующей таблицей (шкала дермальной оценки принята из руководства OECD 404). В ней анализировали присутствие других местных реакций кожи, а также любой системный эффект.
G) Патология
После завершения экспериментальной фазы животных умерщвляли посредством летальной инъекции, с предварительным усыплением.
Образцы кожи отбирали из обработанных областей (тестируемым продуктом и его носителем) и из области отрицательного контроля (необработанной области) всех животных, для патологоанатомического исследования. Образцы фиксировали в 4% формальдегиде и перерабатывали, разрезали и посылали в Отделение морфологии CIMA для их погружения, нарезки и окрашивания (гематоксилином-эозином), и для получения гистологических препаратов. Патологоанатомическое обследование этих препаратов проводили в Отделении патологоанатомической диагностики для лабораторных животных (DAPAL) Университета Сарагосы.
H) Результаты и обсуждение
H.1. Выживаемость/смертность и общие симптомы: не зарегистрировано смертности ни для одного из животных, которым вводили тестируемый продукт. Для экспериментальных животных не показано изменений в общем состоянии.
H.2. Макроскопическое исследование разъедания кожи: как отражено в таблицах 10 и 11, исследование разъедания кожи, проведенное в исходном тесте, не показало присутствия язв, кровотечения или корок в областях, где наносили тестируемый продукт или его носитель.
Оценка разъедания кожи с тестируемым продуктом. Индивидуализированные данные
(после удаления повязки)
Оценка разъедания кожи с носителем.
Индивидуализированные данные
(после удаления повязки)
H.3. Макроскопическое исследование раздражения кожи: как отражено в таблицах 12 и 13, исследование раздражения кожи не показало присутствия покраснения, отека или любых других реакций в областях, где наносили тестируемый продукт или его носитель.
Оценка раздражения кожи с тестируемым продуктом. Индивидуализированные данные
Оценка раздражения кожи с носителем.
Индивидуализированные данные
I) ЗАКЛЮЧЕНИЕ
Индекс раздражения кожи (IIC), рассчитанный для тестируемого продукта, обладает значением ноль. Наблюдали отсутствие покраснения, отека или других реакций в областях нанесения. В соответствии с вышеуказанным заключили, что тестируемый продукт классифицирован как не раздражающий.
Гистологическое обследование областей после введения тестируемого продукта или носителя не показало значительных изменений. Обнаружения описали, для обеих областей, и для одного из животных, изменения с очень низкой интенсивностью без клинической значимости, рассматриваемые как обратимый механизм адаптации кожи.
Группа изобретений относится к области фармацевтики и ветеринарии, а именно к комбинации для местного нанесения на кожу, которая представляет собой биоадгезивный гель и содержит: i) 1-5 % мас. поликарбофила, ii) 4-8 % мас. поливинилпирролидона, iii) 1-10 % мас. глицерина, iv) 20-40 % мас. пропиленгликоля, при этом массовое соотношение (ii):(i) составляет от 1:1 до 4:1, массовое соотношение (iii):(i) составляет от 0,5:1 до 2:1 и массовое соотношение (iv):(i) составляет от 8:1 до 20:1; и к применению данной комбинации в качестве гелеобразующего или пленкообразующего средства. Изобретение также относится к фармацевтической или ветеринарной гелевой композиции, содержащей указанную комбинацию совместно с активным ингредиентом и эксципиентами и/или носителями; и к способу получения таких композиций. Группа изобретений обеспечивает предоставление гелевых композиций для местного применения на коже, обладающих высокой биоадгезивностью, стабильностью и биодоступностью активного ингредиента. 7 н. и 10 з.п. ф-лы, 6 пр., 13 табл., 2 ил.
1. Комбинация для местного нанесения на кожу, которая представляет собой биоадгезивный гель и содержит:
- поликарбофил в количестве, составляющем от 1 до 5% по массе,
- поливинилпирролидон в количестве, составляющем от 4 до 8% по массе,
- глицерин в количестве, составляющем от 1 до 10% по массе, и
- пропиленгликоль в количестве, составляющем от 20 до 40% по массе,
при этом массовое соотношение поливинилпирролидон:поликарбофил составляет от 1:1 до 4:1,
массовое соотношение глицерин:поликарбофил составляет от 0,5:1 до 2:1, и
массовое соотношение пропиленгликоль:поликарбофил составляет от 8:1 до 20:1.
2. Комбинация для местного нанесения на кожу по п.1, где массовое соотношение поливинилпирролидон:поликарбофил составляет 2:1.
3. Комбинация для местного нанесения на кожу по п. 1 или п.2, где массовое соотношение глицерин:поликарбофил составляет от 0,5:1 до 1:1.
4. Комбинация для местного нанесения на кожу по п. 1 или 2, где массовое соотношение пропиленгликоль:поликарбофил составляет 10:1.
5. Комбинация для местного нанесения на кожу по п. 1, где
массовое соотношение поливинилпирролидон:поликарбофил составляет 2:1 и массовое соотношение пропиленгликоль:поликарбофил составляет 10:1, или
массовое соотношение глицерин:поликарбофил составляет от 0,5:1 до 1:1 и массовое соотношение пропиленгликоль:поликарбофил составляет 10:1, или
массовое соотношение поливинилпирролидон:поликарбофил составляет 2:1, массовое соотношение глицерин:поликарбофил составляет от 0,5:1 до 1:1 и массовое соотношение пропиленгликоль:поликарбофил составляет 10:1.
6. Комбинация для местного нанесения на кожу по п. 1, дополнительно содержащая средство регулирующее pH.
7. Комбинация для местного нанесения на кожу по п. 6, где
массовое соотношение поливинилпирролидон:поликарбофил составляет 2:1, или
массовое соотношение глицерин:поликарбофил составляет от 0,5:1 до 1:1, или
массовое соотношение пропиленгликоль:поликарбофил составляет 10:1, или
массовое соотношение поливинилпирролидон:поликарбофил составляет 2:1 и массовое соотношение пропиленгликоль:поликарбофил составляет 10:1, или
массовое соотношение глицерин:поликарбофил составляет от 0,5:1 до 1:1 и массовое соотношение пропиленгликоль:поликарбофил составляет 10:1, или
массовое соотношение поливинилпирролидон:поликарбофил составляет 2:1, массовое соотношение глицерин:поликарбофил составляет от 0,5:1 до 1:1 и массовое соотношение пропиленгликоль:поликарбофил составляет 10:1.
8. Комбинация для местного нанесения на кожу по п.6 или п.7, где средство регулирующее pH представляет собой трометамол.
9. Комбинация для местного нанесения на кожу по п. 1, содержащая:
- поликарбофил в количестве 3% по массе,
- поливинилпирролидон в количестве 6% по массе,
- глицерин в количестве 2% по массе,
- пропиленгликоль в количестве 30% по массе и
- трометамол в количестве 3% по массе.
10. Фармацевтическая гелевая композиция для местного нанесения на кожу, содержащая комбинацию для местного нанесения на кожу по любому из пп. 1-9, вместе с: (a) терапевтически эффективным количеством активного ингредиента или его фармацевтически приемлемой соли и (b) другими подходящими фармацевтически приемлемыми эксципиентами и/или носителями.
11. Фармацевтическая гелевая композиция для местного нанесения на кожу по п.10, которая принадлежит к типу замедленного высвобождения.
12. Ветеринарная гелевая композиция для местного нанесения на кожу, содержащая комбинацию для местного нанесения на кожу по любому из пп. 1-9, вместе с: (a) терапевтически эффективным количеством активного ингредиента или его ветеринарно приемлемой соли и (b) другими подходящими ветеринарно приемлемыми эксципиентами и/или носителями.
13. Ветеринарная гелевая композиция для местного нанесения на кожу по п.12, которая принадлежит к типу замедленного высвобождения.
14. Способ получения композиции для местного нанесения на кожу по любому из пп. 10-13, где способ включает в себя следующие стадии:
(a) смешивание активного ингредиента или его фармацевтически или ветеринарно приемлемой соли с пропиленгликолем при встряхивании;
(b) добавление поливинилпирролидона;
(c) добавление глицерина;
(d) добавление поликарбофила и
(e) добавление других подходящих фармацевтически или ветеринарно приемлемых эксципиентов и/или носителей.
15. Набор для формирования пленки на коже, содержащий фармацевтическую гелевую композицию для местного нанесения на кожу по любому из пп.10-11 или ветеринарную гелевую композицию для местного нанесения на кожу по любому из пп. 12-13 и подложку, которая представляет собой материал-носитель, используемый в перевязочных материалах.
16. Применение комбинации для местного нанесения на кожу по любому из пп. 1-9 в качестве гелеобразующего средства.
17. Способ применения комбинации для местного нанесения на кожу по любому из пп. 1-9 в качестве пленкообразующего средства посредством расположения комбинации на коже, тем самым абсорбируя влагу из кожи и формируя пленку на поверхности кожи.
| Корпус свободновихревого насоса | 1987 |
|
SU1413292A1 |
| CN 102038672 A, 04.05.2011 | |||
| WO 2012102750 A1, 02.08.2012 | |||
| US 20100234336 A1, 16.09.2010 | |||
| ДИКЛОФЕНАКОВЫЙ ГЕЛЬ | 2007 |
|
RU2463038C2 |
Авторы
Даты
2019-01-22—Публикация
2013-12-16—Подача