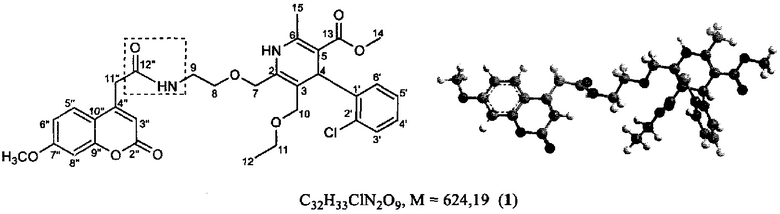
Изобретение относится к медицине и химико-фармацевтической промышленности, и касается нового антиаритмического средства на основе гибридной молекулы производных 1,4-дигидропиридина-кумарина, а именно (4-(2-хлор-фенил)-3-(этоксикарбонил)-5-(метоксикарбонил)-6-метил-2-[[2-[N-((7-метокси-2-оксо-2Н-хромен-4-ил)ацетил)-амино]этокси]метил]-1,4-дигидропиридина, формулы 1,
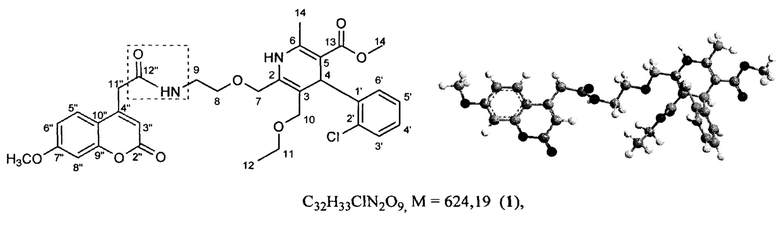
которое обладает выраженной антиаритмической активностью по сравнению с препаратом верапамилом и может найти применение в медицинской практике при лечении сердечно-сосудистых заболеваний.
Известно, что в медицинской практике применяется ряд препаратов-блокаторов кальциевых каналов из разных классов химических соединений, а именно, фенилалкаламины (феноптин, прениламин и др.), 1,4-дигидропири-дины (нифедипин, амлодипин, нимодипин и др.), бензотиазепины (дилтиазем, клентиазем и др.), дифенилпиперазины (циннаризин, флунарицин) и диарил-аминопропиламины (бепридил), обладающих коротким и прологированным действием. [Энциклопедия лекарств РЛС, 2017; Kowey, P.R., Marinchak, R.А., Rials, S.J., Bharucha, D.В. Classification and pharmacology of antiarrhythmic drugs // American heart journal. 2000. Vol. 140. №.1. P. 12-20; Sweetman S.C. Martindale: The Complete Drug Reference. London, Chicago, 36th ed., 2009; Абышев А.З. Лекарственные препараты антиангинального действия - антагонисты ионов кальция (фенилалкилы, 1,4-дигидропиридины и бензотиазепины): убечно-методические пособие / А.З. Абышев, С.Н. Трусов, А.В. Ложкин. СПб.: Изд-во СПХФА, 2010. 148 с.].
Однако, перечисленные выше, блокаторы кальциевых каналов обладают большой частотой развития побочных эффектов (верапамил до 10%, дилтиазем до 4% а нифедипин от 20 до 41% пациентов), проявляющихся в виде отечности голеней, гипотонии, изменения частоты сердечных сокращений, гипергликемии, головной боли, головокружения, повышенной утомляемости, гиперемии кожных покровов и др. [Dougall Н.Т., McLay J. А comparative review of the adverse effects of calcium antagonists // Drug Safety. 1996. Vol. 15. №. 2. P. 91-106].
Кроме того, отмечено, что использование коротко действующих дигидропиридинов, особенно нифедипина, может увеличивать риск развития злокачественных опухолей, инфаркта миокарда и смерти у больных артериальной гипертензией [Кулешова Э.В. Антагонисты кальция и их роль при лечении заболеваний сердечно-сосудистой системы (часть 1) // Вестник аритмологии. 1999. №11. С. 28-34; Goldbourt U., Behar S., Reicher-Reiss H. Early administration of nifedipine in suspected acute myocardial infarction. The secondary prevention reinfarction Israeli nifedipine trial 2 study // Arch. Intern. Med. 1993. Vol. 153. P. 345-353; Muller J. E., Morrison J., Stone P.H. et al. Nifedipine therapy for patients with threatened and acute myocardial infarction: a randomized, double-blind, placebo-controlled comparison // Circulation. 1984. Vol. 69. P. 740-747].
С другой стороны, за последние несколько лет с развитием фармацевтической химии, гибридный подход при создании новых высокоактивных гибридных лекарственных средств, получил значительное внимание, поскольку он позволил синтезировать целый ряд гибридных субстанций с улучшенной биологической активностью по отношению к исходным соединениям. [Calderone V. An update on hybrid drugs in cardiovascular drug research // Expert. Opin. Drug Discov. 2008. Vol. 3. №. 12. P. 1397-1408; Mishra S., Singh P. Hybrid molecules: The privileged scaffolds for various pharmaceuticals. European journal of medicinal chemistry. 2016. Vol. 124. P. 500-536].
Одной из важных групп биологически активных веществ в практической медицине являются производные 2Н-хромен-2-она (2Н-1-бензопиран-2-она, кумарина). На основе природных и синтетических кумаринов создан ряд современных лекарственных средств, в частности, диуманкал-форте, анкардин-форте, анкардин-ретард [Абышев А.З., Дьячук Г.И. Средство для лечения ишемическои болезни сердца // Патент РФ №2155036, 27.08.2000; Абышев А.З., Агаев Э.М., Марищенко О.В. Способ получения таблеток диуманкала-forte по 0,01 г // Патент РФ №2187303, 20.08.2002; Абышев А.З., Агаев Э. М. Анкардин-retard - средство пролонгированного антикальциевого действия // Патент РФ №2219927, 27.12.2003] и других лекарственных субстанций для лечения сердечно-сосудистого заболевания. [Абышев А.З., Крауз В.А., Ивкин Д.Ю. Антиаритмическое средство на основе 4-метил-7,7'-этилендиокси-2Н-1-дибензопиран-2,2'-диона // Патент РФ №2427368, Бюл. №23, 28.08.2011; Абышев А.З., Агаев Э.М. Производные 2Н-1-бензопиран-2-она, проявляющие антикальциевую активность // Патент РФ №2242471, Бюл. №, 20.12.2004].
В связи с изложенным, разработка новых блокаторов кальциевых каналов из других групп гетероциклических или гибридных соединений, лишенных вышеперечисленных побочных действий, обладающих выраженной антиаритмической активностью, является актуальной для практической медицины, особенно для клинической кардиологии.
Задача изобретения - расширение арсенала антиаритмических средств, поиск нового средства на основе соединений гибридных молекул 1,4-дигидро-пиридина-кумарина с фрагментом блокаторов кальциевых каналов, имеющего низкую токсичность и обладающего более высокой антиаритмической активностью, чем соединения, применяющиеся в медицинской практике, а именно фенилалкиламины и бензотиазепины.
Важным аспектом является тот факт, что нативные молекулы блокаторов кальциевых каналов 1,4-дигидропиридинового ряда не обладает собственной антиаритмической активностью. В то же время, в данном исследовании показано наличие выраженного антиаритмического эффекта у вещества гибридной структуры, включающего 1,4-дигидропиридиновый фрагмент.
Изобретение иллюстрируется примерами синтеза, исследований острой токсичности и антиаритмической активности.
Пример 1. Методика синтеза 4-(2-хлорфенил)-3-(этоксикарбонил)-5-(метоксикарбонил)-6-метил-2-[[2-N-((7-метокси-2-оксо-2Н-хромен-4-ил)ацетил)-амино]этокси]метил]-1,4-дигидропиридина.
Синтез заявляемого соединения представлен на следующей схеме:
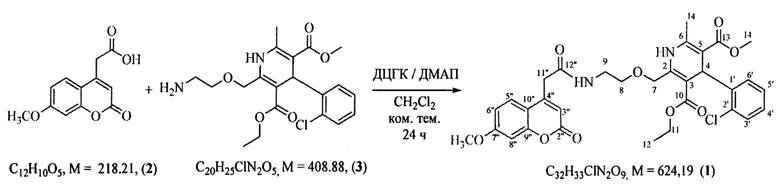
В отличие от предыдущих методик ацилирования, по которым использованы ангидриды или хлорангидриды кислот в качестве сильных ацилирующих агентов, синтез заявляемого соединения был осуществлен из амлодипина и широко доступной (7-метоксикумарин-4-ил)уксусной кислоты с помощью водоотнимающего реагента дициклогексилкарбодиимида (ДЦГК) и катализатора N,N-диметиламинопиридина (ДМАП).
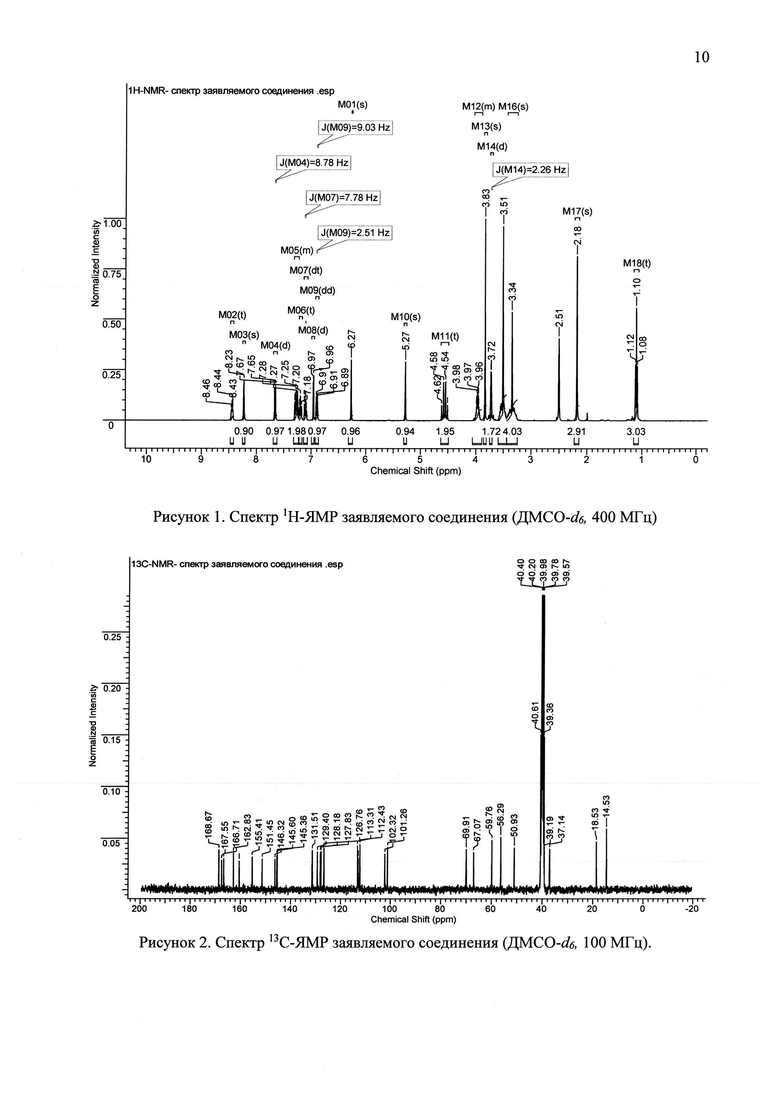
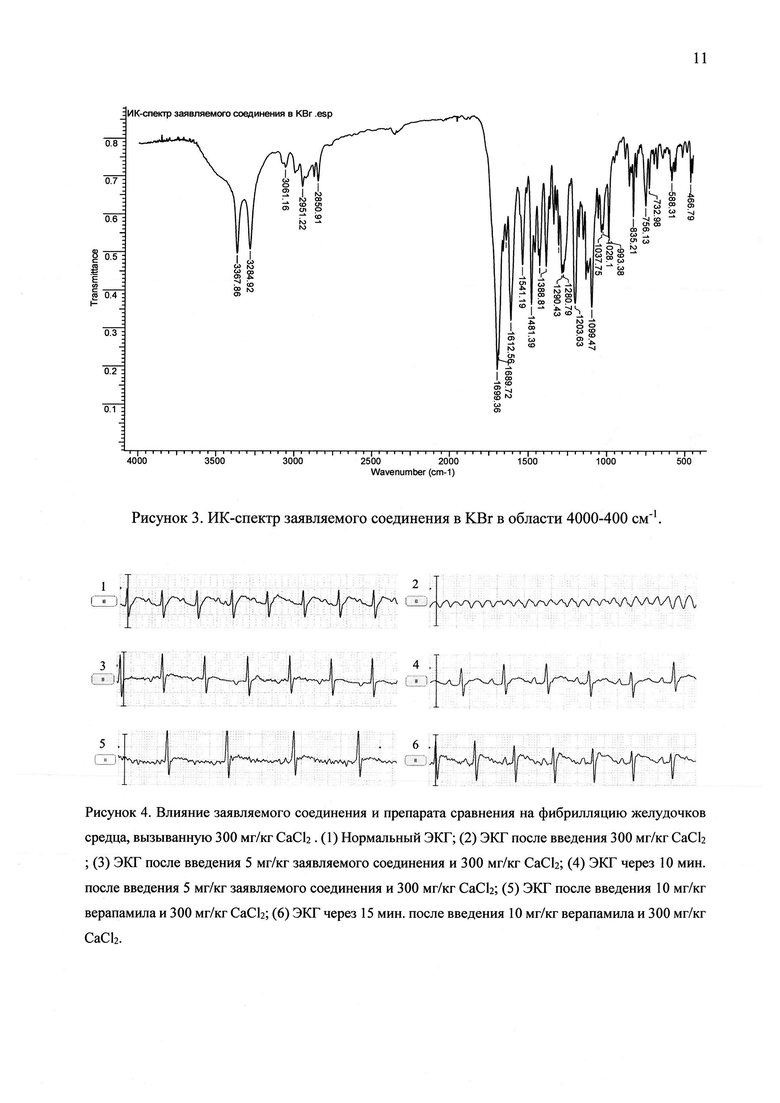
Структура заявляемого соединения подтверждена современными методами: ТСХ, ИК-, ЯМР-спектроскопии и масс-спектрометрии. ИК-спектры регистрированы на спектрометре «ФС-М-1201» в дисках с КBr. Спектры ЯМР 1Н и 13С зарегистрированы на спектрометре «Bruker» Avance III 400 MHz (при рабочей частоте 400 МГц и 100 МГц, соответственно). В качестве растворителя использован: ДМСО-d6; внутренний стандарт-тетраметилсилан (SiMe4), δ-шкала порядка 0-15 м.д. и 0-250 м.д. Масс-спектры высокого разрешения записаны на масс-спектрометре ESI-TOF MX 5311, ионизация электрораспылением с прямым вводом образца (скорость потока 4 μл/мин).
Методика синтеза заявляемого соединения (1): В колбу емкостью 100 мл, снабженную мешалкой, помещают 0,51 г (7-метоксикумарин-4-ил)уксусной кислоты (2) (2,32 ммоль), 0,90 г амлодипина (3) (2,20 ммоль) и 30 мл сухого метилена хлорида, 28,06 мг ДМАП (0,23 ммоль). К реакционной смеси постепенно добавляют 0,48 г ДЦК (2,33 ммоль) при 0°C. Затем реакционную смесь перемешивают при комнатной температуре (20-25°C) в течение 24 ч (контроль ТСХ до окончания кислоты). Полученную суспензию охлаждают, отфильтровывают для удаления образованного осадка дициклогексил-мочевины. Фильтрат отгоняют. Чистый продукт получают с помощью хроматографии на колонке, заполненной силикагелем Л 100/160 μм с использованием смеси этилацетат : гексан (90:10, об/об) в качестве элюента. При этом получают 0,97 г (69,2%) белого порошкообразного вещества, с т.пл. 172-174°C. Полученное соединение - плохо растворим в спирте, мало растворим в этилацетате, легко растворим в хлороформе, практически не растворим в воде и петролейном эфире.
ТСХ-система: метилен хлористый-этанол (20:1). ТСХ-пластинка: Сорбфил ПТСХ-П-А-УФ (силикагель СТХ-1А, УФ-254 нм). Детекция пятен осуществлялась с помощью УФ лампы при длине волны 254 нм или 365 нм. Заявляемое соединение имеет Rf 0,67.
ИК спектр (KBr, ν, см-1): 3284-3367 (N-H), 2951 (С-Н), 1689-1699 (С=O), 1612 (С=С), 1203-1280 (С-О), 1099 (С-Cl), 1028-1037 (С-О-С).
ИК спектр (вазелиновое масло, ν, см-1): 3284-3365 (N-H), 2955 (С-Н), 1689-1699 (С=O), 1614 (С=С), 1203-1290 (С-О), 1099 (С-Cl), 1028-1037 (С-О-С).
Спектр ЯМР 1Н (ДМСО-d6), δ, м.д. (J, Гц): 1.10 (3H, т, J=7.03, Н-12), 2.18 (Н, с, Н-15), 3.51 (5H, уш. с, Н-8, Н-14), 3.72 (2Н, д, J=2.26, Н-11''), 3.83 (3Н, с, -ОСН3), 3.90-4.04 (2Н, м, Н-11), 4.56 (2Н, кв., J=14.31, Н-7), 5.27 (1H, с, Н-4), 6.27 (1H, с, Н-3''), 6.90 (1H, д. д, J=9.03, 2.51, Н-8''), 6.96 (1Н, д, J=2.26, Н-6''), 7.11 (1Н, д. т, J=7.78, J=1.25, Н-4'), 7.20 (1H, т, J=7.28, Н-5'), 7.23-7.32 (2Н, м, Н-3', 6'), 7.66 (1Н, д, J=8.78, Н-5''), 8.23 (1Н, с, 9-NH-),), 8.44 (1Н, т, J=5.52, -NH-).
Спектр ЯМР 13С (ДМСО-d6), δ, м. д.: 14,53 (С-12); 18,53 (С-15); 37,14 (С-4); 39,19 (С-9); 39,43 (С-11''); 50,93 (С-14); 56,29 (7-ОСН3); 59,76 (С-11); 67,07 (С-7); 69,91 (С-8); 101,26 (С-8''); 102,29 (С-3); 102,32 (С-5); 112,43 (С-3''); 112,99 (С-6''); 113,31 (С-10''); 126,76 (С-5''); 127,83 (С-5'); 128,18 (С-4'); 129,4 (С-3'); 131,51 (С-6'); 131,58 (С-2'); 145,36 (С-6); 145,6 (С-1'); 146,32 (С-2); 151,45 (С-9''); 155,41 (С-4''); 160,54 (С-7''); 162,83 (С-2", С-7); 166,71 (С-10); 167,55 (С-13); 168,67 (С-12'').
ЭСИ-масс-спектр: Найдено, m/z: 625,211 [М+Н]+. C31H34ClN2O9. Вычислено, m/z: 625,195.
Таким образом, приведенные хроматографические и спектральные данные полностью согласуются со структурой заявляемого соединения (см. рис. 1-3).
Пример 2. Определение острой токсичности заявляемого соединения.
Определение острой токсичности было проведено на белых беспородных мышах массой 18-20 г, разделенных на 4 группы по 3 животных в каждой, по экспресс-методу Прозоровского [Прозоровский В.Б. Экспресс-метод определения средней эффективной дозы и ее ошибки // Фармакол. и токсикол. 1978. №4. С. 497].
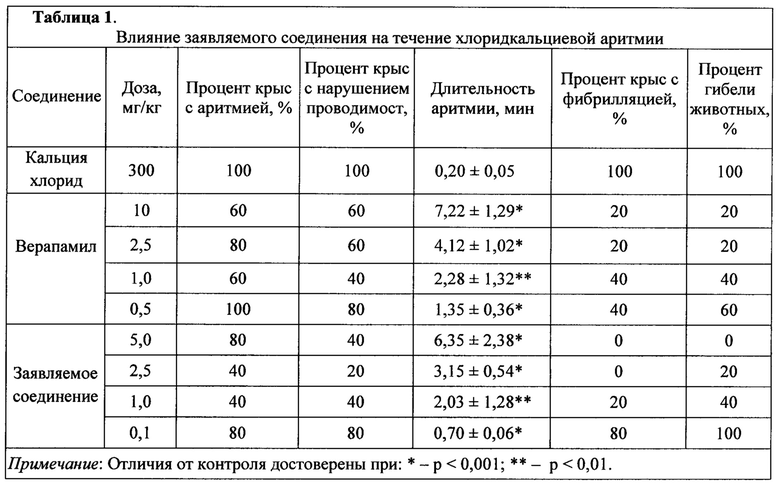
Исследуемые вещества вводят внутрибрюшинно в различных дозах от 300 мг/кг до 2000 мг/кг и по таблице определяют острую токсичность. Результаты эксперимента, приведенные в таблице 1, свидетельствуют о том, что заявляемое средство по классификации Hodge и Sterner [Hodge, Н.С. Sterner J.Н. Tabulation of toxicity classes // American Industrial Hygiene Association Journal. 1949. Vol. 10. P. 93-96.] относится к 5-му классу токсичности и является практически нетоксичным соединениям.
Пример 3. Испытание антиаритмической активности заявляемого соединения на модели аритмии, вызванной внутривенным введением хлорида кальция крысам.
В качестве скринингового исследования антиаритмической активности субстанций, являющихся по факту блокаторами кальциевых каналов, используют модель хлоридкальциевой аритмии. Опыты проводят на белых беспородных крысах-самцах массой 180-250 г. Животные получены из питомника «Рапполово» (Ленинградская область), все манипуляции проводят в соответствии с правилами, принятыми Европейской конвенцией по защите позвоночных животных, используемых для экспериментальных и других научных целей (принятой в Страсбурге 18.03.1986 г. и подтвержденной в Страсбурге 15.06.2006 г. ). Животных разделяют на группы по 5 особей в каждой. Желудочковую аритмию вызывают внутривенным введением 10% раствора хлорида кальция в дозе 300 мг/кг. Антиаритмическую активность заявляемого соединения изучают при внутривенном введении в дозах от 0,1 мг/кг до 5,0 мг/кг за 2 мин до аритмогенного агента. Препаратом сравнения является верапамил в дозе 10 мг/кг. Электрокардиограмму (ЭКГ) регистрируют во втором стандартном отведении на приборе «Поли-Спектр-8/В» (Нейрософт, Россия). Оценивают процент крыс с аритмией, с нарушением проводимости, длительность аритмии и процент гибели животных. ЭКГ обработывают с помощью программы Poly-Spectrum (Нейрософт, Россия). Эффективную дозы (ЭД50) и их ошибки определяют по методу Миллера и Тейтнера [Miller L.C., Tainter M.L. Estimation of LD50 and its error by means of log-probit graph paper // Proc. Soc. Exp. Bio. Med. 1944. Vol. 57. P. 261]. Статистическую обработку проводят с использованием t-критерия Стьюдента.
Данные, представленные в таблице 1 показывают, что при введении заявляемого соединения в дозе от 0,10 до 5,0 мг/кг после введения аритмогена в 40-80% случаев развивалась слабая брадикардия и восстанавливался синусовый ритм в 60-100% случаев через 10 мин, а в случае препарата сравнения верапамила в дозе от 0,50 до 10,0 мг/кг после введения аритмогена в 60-100% случаев развивалась мерцательная аритмия и восстанавливался синусовый ритм в 40-80% случаев через 15 мин. Влияние заявляемого соединения и препарата сравнения на фибрилляцию желудочков сердца, вызванную 300 мг/кг хлоридом кальция, приведено на рисунке 4.
На основании полученных данных видно, что заявляемое соединения (1) более эффективно на модели хлоридкальциевой аритмии, чем препарат сравнения.
С учетом данных, полученных в примерах 2 и 3, по токсичности заявляемого соединения и его антиаритмической активности на модели хлоридкальциевой аритмии, можно определить антиаритмический индекс (АИ)=ЛД50/ЭД50.
Результаты эксперимента, приведенные в таблице 2, свидетельствуют о том, что заявляемое соединение (1) проявляет высокую антиаритмическую активность, превосходит известный препарат сравнения верапамил и обладает выраженной терапевтической широтой.
Таким образом, заявляемая гибридная молекула (4-(2-хлорфенил)-3-(этокси-карбонил)-5-(метоксикарбонил)-6-метил-2-[[2-[N-((7-метокси-2-оксо-2Н-хро-мен-4-ил)ацетил)амино]этокси]метил]-1,4-дигидропиридина (1) является практически нетоксичным соединением и более эффективным на модели хлоридкальциевой аритмии, чем препарат сравнения. Выявленные свойства свойства позволяют рекомендовать его для проведения клинических испытаний как новый относительно безопасный блокатор кальциевых каналов с выраженным антиаритмическим действием с целью дальнейшего внедрения в медицинскую практику.

| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИКОАГУЛЯНТНОЕ СРЕДСТВО НЕПРЯМОГО ДЕЙСТВИЯ НА ОСНОВЕ ДИУМАНКАЛА | 2018 |
|
RU2671983C9 |
| СРЕДСТВО ПРОЛОНГИРОВАННОГО АНТИКАЛЬЦИЕВОГО ДЕЙСТВИЯ В ВИДЕ 0,1% РАСТВОРА ДЛЯ ВНУТРИВЕННОГО ВВЕДЕНИЯ | 2004 |
|
RU2255728C1 |
| ПРОИЗВОДНЫЕ 2-Н-1-БЕНЗОПИРАН-2-ОНА, ПРОЯВЛЯЮЩИЕ АНТИКАЛЬЦИЕВУЮ АКТИВНОСТЬ | 2003 |
|
RU2242471C1 |
| АНТИАРИТМИЧЕСКОЕ СРЕДСТВО НА ОСНОВЕ 4-МЕТИЛ-7,7'-ЭТИЛЕНДИОКСИ-2Н-1-ДИБЕНЗОПИРАН-2,2'-ДИОНА | 2010 |
|
RU2427368C1 |
| ИММУНОМОДУЛИРУЮЩЕЕ И ПРОТИВОВИРУСНОЕ СРЕДСТВО НА ОСНОВЕ (2-((КУМАРИН-7-ИЛ)ОКСИ)ЭТИЛ) 3-ГИДРОКСИ-20(29)-ЛУПЕН-28-ОАТА | 2018 |
|
RU2686743C1 |
| ГИБРИДНЫЕ КУМАРИНЫ, ОБЛАДАЮЩИЕ НЕПРЯМЫМ АНТИКОАГУЛЯНТНЫМ ДЕЙСТВИЕМ | 2018 |
|
RU2672062C1 |
| АНТИКОАГУЛЯНТНОЕ СРЕДСТВО НЕПРЯМОГО ДЕЙСТВИЯ НА ОСНОВЕ НОВОЙ ГИБРИДНОЙ МОЛЕКУЛЫ ВАРФАРИНА С ОСТОЛЕВОЙ КИСЛОТОЙ | 2018 |
|
RU2677647C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ИШЕМИЧЕСКОЙ БОЛЕЗНИ СЕРДЦА | 1998 |
|
RU2155036C2 |
| ФТОРИРОВАННЫЕ 4-ФУРФУРИЛ-3,4-ДИГИДРО-2Н-БЕНЗО[1,4]ТИАЗИН-1,1-ДИОКСИДЫ, ОБЛАДАЮЩИЕ ВЫСОКОЙ АРИТМИЧЕСКОЙ АКТИВНОСТЬЮ | 2016 |
|
RU2626239C1 |
| 5-АМИНО-ЭКЗО-3-АЗАТРИЦИКЛО[5.2.1.0]ДЕКАН-4-ОН, ПРОЯВЛЯЮЩИЙ АНТИАРИТМИЧЕСКУЮ, ПРОТИВОВОСПАЛИТЕЛЬНУЮ, АНАЛЬГЕТИЧЕСКУЮ И НООТРОПНУЮ АКТИВНОСТЬ | 2005 |
|
RU2281938C1 |
Изобретение относится к химико-фармацевтической промышленности и представляет собой антиаритмическое средство, включающее (4-(2-хлорфенил)-3-(этоксикарбонил)-5-(метоксикарбонил)-6-метил-2-[[2-[N-(7-метокси-2-оксо-2Н-хромен-4-ил)ацетил)амино]этокси]метил]-1,4-дигидропиридин в качестве активного вещества. Изобретение позволяет получить новое соединение, обладающее высокой антиаритмической активностью и низкой токсичностью. 4 ил., 2 табл., 3 пр.
Антиаритмическое средство, включающее (4-(2-хлорфенил)-3-(этоксикарбонил)-5-(метоксикарбонил)-6-метил-2-[[2-[N-(7-метокси-2-оксо-2Н-хромен-4-ил)ацетил)амино]этокси]метил]-1,4-дигидропиридин в качестве активного вещества
Авторы
Даты
2019-02-05—Публикация
2018-03-28—Подача