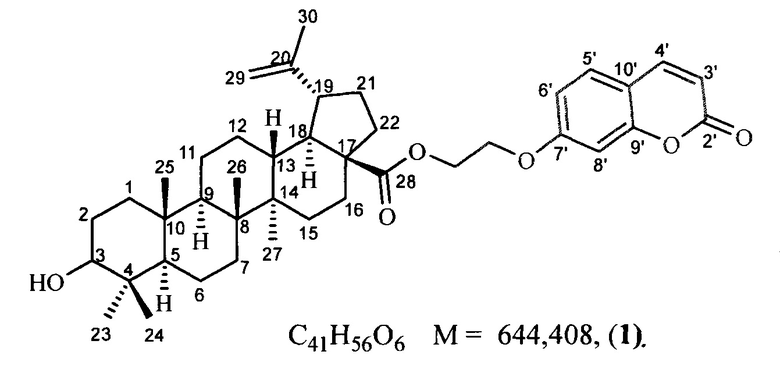
Изобретение относится к медицине и химико-фармацевтической промышленности и касается нового иммуномодулирующего и противовирусного средства на основе гибридной молекулы производных тритерпеноида-кумарина, а именно (2-((кумарин-7-ил)окси)этил) 3-гидрокси 20(29)-лупен-28-оата, формулы 1,

которое обладает выраженной иммуномодулирующей и противовирусной активностью и может найти применение в медицинской практике при лечения и профилактике вирусных инфекций.
Одной из актуальных задач современной медицины является разработка новых эффективных лекарственных средств для лечения и профилактики вирусных инфекций, поскольку глобализация, мобильность населения и характер передачи вирусных инфекций способствуют их активному распространению по всему миру. Эпидемия «птичьего» гриппа H5N1 (1997-2006) и затем пандемия гриппа 2009 г., вызванная вирусом свиного происхождения A(H1N1)pdm09, сделали настоятельно необходимой ревизию состояния проблемы с разработкой противовирусных препаратов [Киселев О.И. Химиопрепараты и химиотерапия гриппа. Санкт-Петербург, Росток, 2012].
В настоящее время для лечения гриппа А в медицине используются два вида противовирусных препаратов адамантановой структуры - ингибиторы М2 ионных каналов - амантадин и римантадин [Scholtissek С, Quack G., Klenk H.D., Webster R.G., Antiviral Res. 1998, 37, 83-95], ингибиторы нейраминидазы (NA) - занамивир или реленза (GlaxoWellcome/Biota) и оселтамивир или тамифлю (Hofrman-La-Roche/Gilead) [Colman P.M., J. Antimicrob. Chemother. 1999 Nov;44 Suppl B:17-22]. Однако, обе группы соединений имеют свои недостатки. В отношении группы производных адамантана можно отметить сравнительно высокую токсичность, узкий спектр действия (препараты активны против гриппа А, но не против гриппа В) и быстрое формирование устойчивости вируса к препаратам. Для ингибиторов нейраминидазы характерны формирование резистентности вирусов и высокая стоимость синтеза, что делает эти препараты менее доступными для широкого использования. Кроме того, для ингибиторов NA характерна низкая биодоступность. Так, занамивир применяется только в виде ингаляций, что затрудняет его использование у маленьких детей и пожилых пациентов [Зарубаев В.В, Киселев О. И, Карпинская Л.А, Морковник А.С, Диваева Л.Н. Средство, представляющее собой амид глицирризиновой кислоты с 5-аминоурацилом, проявляющее противовирусную активность в отношении вируса гриппа A/H1N1 // Патент РФ No 2568849С1, 20.11.2015; Hurt А.С, Selleck P., Komadina N., Shaw R., Brown L., Barr I.G. Susceptibility of highly pathogenic (H5N1) avian influenza viruses to the neuraminidase inhibitors and adamantanes //Antiviral Res, 2007, 7, 228-231; Zhang J., Xu W. Recent advances in anti-influenza agents with neuraminidase as target//Mini-Rev. Med. Chem., 2006,6, 429-448].
Как показала практика, для разработки новых лекарственных средств наиболее перспективна химическая модификация доступных природных соединений с высоким уровнем биологической активности на основе подхода «структура-активность». Среди биологически активных веществ весьма важными в практическом отношении также являются производные тритерпеноида, в частности бетуленоловой кислоты. Она представляет большой интерес для медицины и фармации как анти-ВИЧ (например, препарат «Бевиримат») и противоопухолевое средство, ее производные также обладают иммуномодулирующим, противовирусным, гепатопротекторным, противоязвенным и многими другими действиями [Абышев, А.З., Абышев, Р. А., Нгуен, В. X., Морозова, В. А. Производные бетуленола как перспективные анти-ВИЧ агенты // Медицинский академический журнал. 2013.Т.13. №2. С.15-32; Абышев, А.З. Природные и синтетические тритерпеноиды / А.З. Абышев, В.X. Нгуен. Санкт-Петербург: Арт-Экспресс, 2015. 284 с].
Необходимо заметить, что за последние несколько лет с развитием фармацевтической химии, гибридный подход при создании новых высокоактивных гибридных лекарственных средств, получил значительное внимание, поскольку он позволил синтезировать целый ряд гибридных субстанций с улучшенной биологической активностью по отношению к исходным соединениям. [Calderone V. An update on hybrid drugs in cardiovascular drug research // Expert. Opin. Drug Discov. 2008. Vol. 3. №. 12. P. 1397-1408; Mishra S., Singh P. Hybrid molecules: The privileged scaffolds for various pharmaceuticals. European journal of medicinal chemistry. 2016. Vol.124. P. 500-536].
Кроме того, в настоящее время также внимание зарубежных и российских ученных привлякают, в основном, производные 2Н-1-бензопиран-2-она (кумарина) природного и синтетического происхождения из-за их выраженных фармакологических активностей, таких как противовирусной, анти-ВИЧ, иммуномодулирующей, противоопухолевой и других активностей [Hassan, М. Z. Therapeutic potential of coumarins as antiviral agents / M. Z. Hassan, H. Osman, M. A. Ali, M. J. Ahsan. // European journal of medicinal chemistry. - 2016. - Vol.123. - P. 236-255; Абышев, A.3. Природные и синтетические кумарины и флавоноиды / А.3. Абышев, Э.М. Агаев, Р.А. Абышев - Баку: Наука и образование, 2014. 482 с], что представляет определенный теоретический и практический интерес при создании гибридных молекул на основе новых производных кумарина для профилактики и лечения многих заболеваний.
В связи с изложенным, задачей настоящего изобретения является расширение арсенала иммуномодулирующих и противовирусных средств и поиск нового средства на основе высокоактивных гибридных молекул тритерпеноида-кумарина.
Изобретение иллюстрируется примерами синтеза, исследований иммуномодулирующей и противовирусной активности оригинальной гибридной молекулы (1).
Пример 1. Методика синтеза (2-((кумарин-7-ил)окси)этил) 3-гидрокси 20(29)-лупен-28-оата (1).
Синтез заявляемого соединения представлен на следующей схеме:
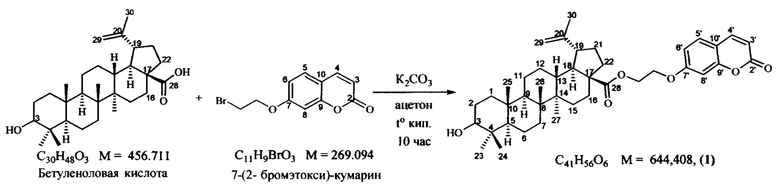
Синтез заявляемого соединения было осуществлено по реакцию этерификации Вильямсона в присутствии карбоната калия в ацетоне при температуре 50-60°С. В качестве исходных соединений использовали 7-(2-бромэтокси)-кумарин (7-БЭК) и бетуленоловую кислоту, которые были получены ранее [Абышев, А.З. Природные и синтетические тритерпеноиды / А.З. Абышев, В. X. Нгуен. Санкт-Петербург: Арт-Экспресс, 2015. 284 с].
Структура полученного соединения подтверждена современными физико-химичекими методами: ИК-, ЯМР-спектроскопии и масс-спектрометрии (фиг. 1-4).
ИК-спектры регистрированы на спектрометре «ФС-М-1201» в дисках с КВr. Спектры ЯМР 1Н и 13С зарегистрированы на спектрометре «Bruker» Avance III 400 MHz (при рабочей частоте 400 МГц и 100 МГц, соответственно). В качестве растворителя использован: ДМСО-d6; внутренний стандарт-тетраметилсилан (SiMe4), δ-шкала порядка 0-15 м.д. и 0-250 м.д. ЭСИ-масс-спектры были сняты на времяпролетном масс-спектрометре высокого разрешения с ортогональным вводом и электрораспылительным источником ионов (ESI-TOF) МХ5310.
Методика синтеза заявляемого соединения (1): В круглодонную колбу на 100 мл помещают навески 1,0 г (2,2 ммоль) бетуленоловой кислоты, 0,58 г (2,2 ммоль) 7-(2- бромэтокси)-кумарина (7-БЭК), 1,0 г (7,25 ммоль) карбоната калия и добавляют 30 мл ацетона, снабженной магнитной мешалкой. Реакционную смесь нагревают и постоянно перемешивают при температуре 50-60°С до полного исчезновения исходного 7-БЭК по ТСХ-контролю (около 10 часов). Затем реакционную смесь охлаждают и осадок отфильтровывают. Фильтрат отгоняют. Чистые продукты получают с помощью хроматографии на колонке, заполненной силикагелем Л 40/100 μм с использованием смеси метилен хлористый : этилацетат (40:1) в качестве элюента. При этом получено 0,76 г (53,5%) соединения (1) белого порошкообразного вещества с т.пл. 177-180°С. Полученное соединение легко растворим в хлороформе и метилене хлористом, растворим в ацетоне и спирте, практически не растворим в воде.
ТСХ-система: бензол : этилацетат - (3:1). ТСХ-пластинка : Сорбфил ПТСХ-П-А-УФ (силикагель СТХ-1А, УФ-254 нм). Детекция пятен осуществлялась с помощью УФ лампы при длине волны 254 нм или 365 нм. Заявляемое соединение имеет Rf=0,52.
ИК спектр (KBr, ν, см-1): 3527,96 (ср.), 3057,31 (сл.), 2945,43 (с), 2870,2 (ср.), 2848,98 (ср.), 1724,44 (оч.с), 1703,22 (оч.с), 1612,56 (оч.с), 1508,4 (ср.), 1471,75 (ср.), 1450,53 (ср.), 1350,23 (ср.), 1282,72 (с), 1236,42 (с), 1155,41 (с), 1134,19 (с), 1043,53 (ср.), 993,38 (ср.), 881,51 (ср.), 848,72 (ср.), 617,25 (сл.) (фиг. 1).
ИК спектр (вазелиновое масло, ν, см-1): 3524,1 (ср.), 3055,38 (ср.), 2953,15 (с), 2924,21 (оч.с), 2852,84 (оч.с), 1724,44 (ср.), 1701,29 (ср.), 1612,56 (ср.), 1508,4 (сл.), 1462,11 (с), 1458,25 (с), 1377,23 (ср.), 1282,72 (ср.), 1236,42 (ср.), 1132,26 (ср.), 993,38 (сл.), 850,64 (сл.), 721,41 (сл.) (фиг. 2).
Спектр ЯМР 1Н (ДМСО-d6), δ, м. д. (J, Гц): 0,62 - 1,05 (м-комплекс, 15 Н) 1,07 - 1,78 (м-комплекс, 19 Н) 1,85 - 1,99 (м-комплекс, 2 Н) 2,16 (т, J=10,79, 10,29 Hz, 1 Н) 2,27 (д, J=7,03 Hz, 1 Н) 3,01 (д, J=10,04 Hz, 1 Н, Нβ-19) 3,18 (д, J=7,03 Hz, 1 Н, Нα-3) 4,26 (уш, с„ 2 Н, -ОСН2-) 4,50 (д, J=3,01 Hz, 2 Н, -ОСН2-) 4,61 (уш, с„ 1 Н, На-29) 4,73 (уш, с„ 1 Н, Нб-29) 6,29 (д, J=9,29 Hz, 1 Н, Н-3') 6,81 - 6,91 (м-комплекс, 2 Н, Н-6', Н-8') 7,41 (д, J=8,53 Hz, 1 Н, Н-5') 7,67 (д, J=9,29 Hz, 1 Н, Н-4') (фиг. 3).
Спектр ЯМР 13С (ДМСО-d6), δ, м. д.: 14,69, 15,37, 15,95, 16,05, 18,24, 19,35, 20,8, 25,46, 27,37, 27,98, 29,59, 30,59, 32,1, 34,23, 36,99, 37,13, 38,34, 38,67, 38,84, 40,62, 42,38, 47,04, 49,4, 50,43, 55,28, 56,65, 61,6, 66,58, 78,95, 101,63, 109,73, 112,82, 112,88, 113,42, 128,91, 143,33, 150,43, 155,8, 161,12, 161,67, 176,04 (фиг. 4).
ЭСИ-масс-спектр: Найдено, m/z: 645,423 [М+Н]+. С41Н56О6. Вычислено, m/z: 645,425.
Таким образом, приведенные хроматографические и спектральные данные полностью согласуются со структурой заявляемого соединения (см. фиг. 1-4).
Пример 2. Испытание иммуномодулирующей активности заявляемого соединения в тесте антителообразования мышей к Т-зависимому антигену эритроцитам барана.
Работа была выполнена на мышах линии CB57BL/6 массой 18-20,0 грамм, полученных из питомника «Рапполово» (ФГУП ПЛЖ «Рапполово» РАМН, Ленинградская область), прошли необходимый карантин и содержались в стандартных условиях сертифицированного вивария на обычном пищевом рационе, со свободным доступом к воде.
Иммуномодулирующая активность заявляемого соединения была определена в тесте антителообразования у лабораторных мышей к Т-зависимому антигену эритроцитам барана. Оценка антителообразования проводилась в тесте гемагглютинации (РГА).
Иммунизация. Перед иммунизацией эритроциты барана трижды отмывают в стерильном изотоническом растворе натрия хлорида. Животных иммунизируют 0,5 мл 1% суспензии эритроцитов барана (2×108 клеток/мышь) внутрибрюшинно однократно.
Введение тестируемого объекта. В день иммунизации вводят испытуемые вещества внутрижелудочно, предварительно эмульгируя в воде добавлением твина 80 в дозе 10 мг/кг.
Получение образцов сыворотки крови. На высоте иммунного ответа (7 дней после иммунизации забирают кровь из ретроорбитального синуса в пробирки с активатором свертывания по 1 мл. После того, как кровь свернется, ее центрифугируют 10 мин при 2000 об/мин. Отбирают 100 μл сыворотки в отдельные пробирки. Для инактивации комплемента пробы инкубировали при 56°С в течении 60 минут.
Постановка реакции гемагглютинации (РГА).
Этапы проведения РГА:
1. В первую лунку (№1) планшета для проведения реакции РГА вносят 0,9 мл изотонического раствора NaCl, во все остальные - по 0,1 мл.
2. В первую лунку (№1) вносят 0,1 мл сыворотки (разведение 1/10).
3. Сыворотку раститровывают: в лунке №1 раствор перемешивают при помощи пипетки; удаляют 0,8 мл; отбирают 0,1 мл и переносят в лунку №2 (разведение сыворотки 1/20); снова перемешивают и 0,1 мл переносят в лунку №3 (разведение сыворотки 1/40) и так далее до лунки №11; из лунки №11 0,1 мл удаляют. Лунка №12 - отрицательный контроль.
4. Во все лунки добавляют 0,1 мл 2% суспензии эритроцитов.
5. Через 2 часа наблюдают реакцию агглютинации.
Затем проводят учет результатов по образованию агрегатов эритроцитов в виде дискообразных осадков, распадающихся на хлопья при встряхивании. При резко положительной РГА (++++) происходит просветление жидкости и образуется агглютинат в виде перевернутого «зонтика». При положительной реакции (+++) происходит неполное просветление жидкости и образуется хорошо выраженный «зонтик». При слабоположительной реакции (++) эритроциты образуют характерное широкое кольцо с небольшим просветом в центре. При слабоположительной реакции (+) эритроциты образуют плотное кольцо небольшого размера с незначительным просветом в центре. Когда на дне лунки образуется плотный осадок эритроцитов в виде диска с ровными краями «пуговки», реакцию оценивают как отрицательную (-). Для каждого животного отмечают наибольшее из разведений, в котором реакция агглютинации наблюдалась отчетливо (++). Далее подсчитывали индекс реакции по Сергиеву: результат реакции, выраженный плюсами (4+; 3+; 2+ и 1+), умножают на частное от деления в данной пробе на степень разведения в первой. Оценочный индекс выводится из суммы оценок реакции в каждой лунке. Статистическую обработку проводили с использованием U-критерия Манна Уитни.
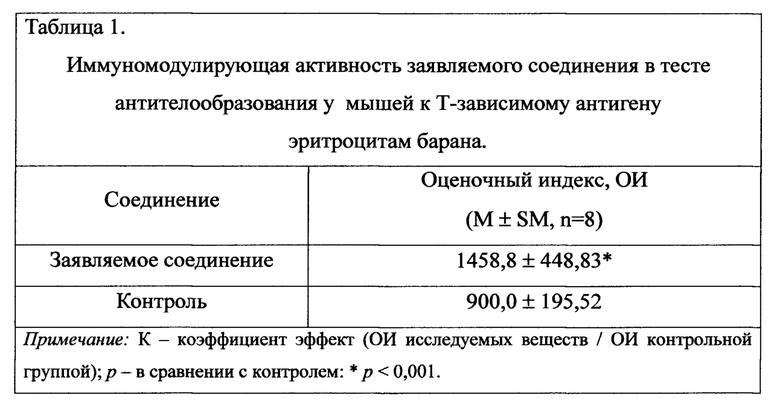
Анализ полученных результатов исследования, представленных в таблице 1, показали, что заявляемое соединение приводит к повышению оценочного индекса (1458,8±448,83) на 62% в сравнение с контролем. Обнаруженные отличия были статистически значимыми в сравнении с контрольной группой (р<0,001).
Таким образом, проведенное исследование позволяет предложить наличие у заявляемого соединения иммуномодулирующего действия, в частности направленного на активацию гуморального ответа.
Пример 3. Испытание противовирусной активности заявляемого соединения на модели летальной гриппозной пневмонии у мышей, вызванной вирусом гриппа A/California/07/09 (H1N1)pdm09
Животные. Работа была выполнена на белых мышах линии Balb/c массой 18-20 г (возраст 6-8 недель), самках, полученных из питомника Филиал «Столбовая» ФГБУН НЦБМТ ФМБА России, Московская область).
Вирусы. В исследовании использован штамм вируса гриппа A/California/07/09 (H1N1)pdm09, адаптированный к мышам. Пассажная история - Е4/Е3М8Е1.
Исследуемые образцы:
- Исследуемые субстанции: заявляемое соединение (1) - (2-((кумарин-7-ил)окси)этил) 3-гидрокси 20(29)-лупен-28-оат.
- Препарат сравнения: Осельтамивир фосфат (Тамифлю), производство «Ф.Хоффманн-Ля Рош Лтд.», капсулы 75 мг, серия N1030, дата выпуска 01.04.2016.
- Контрольное вещество: фосфатно-солевой буфер.
Введение исследуемых образцов животным
При изучении противовирусной активности in vivo субстанции вводили животным перорально по лечебно-профилактической схемам (за 1 день, за 1 час и через 1, 2, и 3 сутки после заражения). Дозировка препарата сравнения тамифлю составляла 20 мг/кг, исследуемых субстанций - 10 мг/кг.
Заражение животных и забор органов. Мышей заражали интраназально под легким эфирным наркозом вирусом в дозе 1 МЛД50 на мышь в объеме 50 мкл. Наблюдение за животными осуществляли в течение 14 дней. Ежедневно проводили взвешивание мышей и фиксировали гибель животных в контрольных и опытных группах.
Индекс защиты рассчитывали по формуле: ИЗ=(Мс - Me) / Мс×100%, где Мс и Me - проценты гибели животных в отрицательной контрольной группе и экспериментальной группе, получавшей изучаемое или контрольное соединение, соответственно.
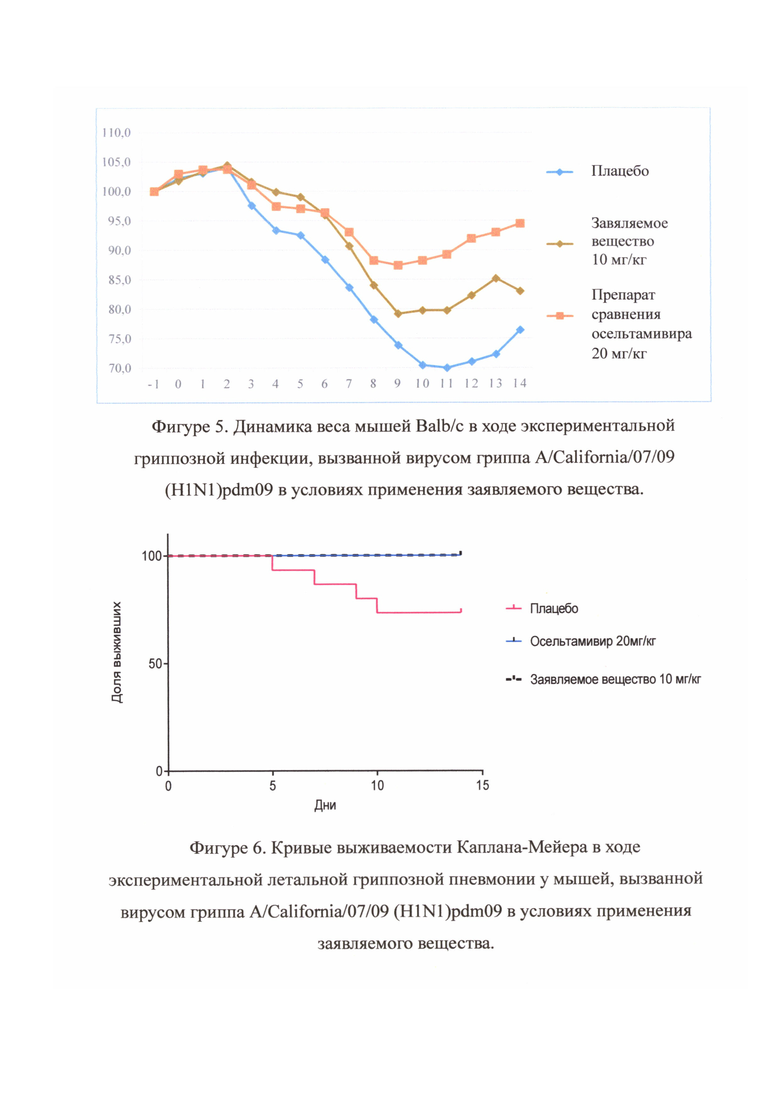
В ходе исследования показано, что инфицирование вирусом гриппа приводило к развитию у лабораторных мышей патологического процесса. Внешние признаки заболевания проявлялись в ограничении подвижности животных, учащению и поверхностности дыхания, а также снижении потребления корма и воды, приводящему к потере веса и гибели животных. Перечисленные признаки являются типичными для гриппозной пневмонии. Динамика весовых показателей животных в ходе гриппозной пневмонии показана на фигуре 5.
Из представленных данных видно, что инфицирование использованным вирусом приводит к значительной потере веса животными относительно исходных показателей, достигающей к 11 суткам - 30%. При сравнении веса животных на 4 сутки после инфицирования не выявлено статистически значимых отличий между группами, однако, при сравнении веса на 7 и 10 сутки отмечено статистически достоверное улучшение весовых показателей как у животных, получавших препарат сравнения (Тамифлю), так и у животных, получавших заявляемой субстанции (1) (фиг. 5). Полученные данные по динамике веса согласовались с результатами анализа динамики гибели животных. Данные о динамике гибели животных в ходе гриппозной пневмонии приведены на фигуре 6.
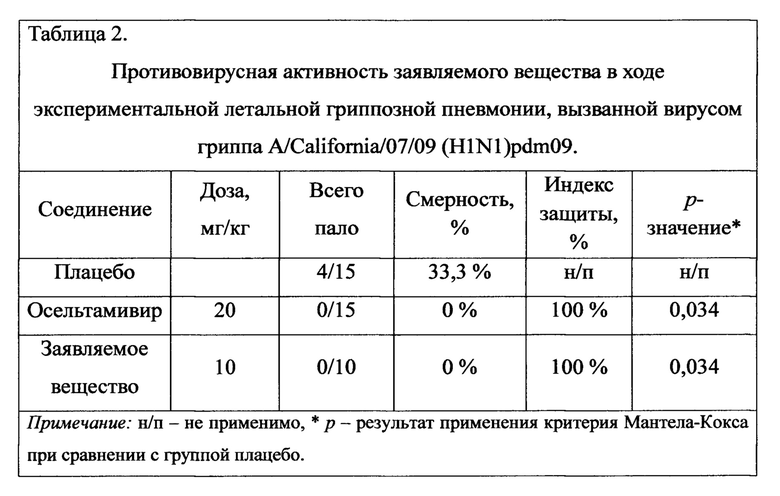
Как следует из полученных результатов из таблицы 2, инфицирование использованным вирусом приводило к гибели животных, начиная с 5 суток, достигающей к концу эксперимента 33,3%. Использование препарата сравнения осельтамивира фосфата (Тамифлю) снижало этот показатель до 0% (р=0,034), что соответствует индексу защиты (ИЗ) 100%, соответственно и согласуется с имеющейся информацией о чувствительности использованного вируса к осельтамивиру. Применение заявляемого вещества также снижало специфическую смертность животных до 0%, что соответствует индексу защиты (ИЗ) 100%.
Таким образом, заявляемое вещество - (2-((кумарин-7-ил)окси)этил) 3-гидрокси-20(29)-лупен-28-оат (1) обладает иммуномодулирующими свойствами, оказывая влияние на активацию гуморального ответа и выраженной противовирусной активностью в отношении вируса гриппа A/California/07/09 (H1N1)pdm09 у мышей Balb/c при лечебно-профилактическом режиме применения в дозах 10 мг/кг. Выявленные свойства позволяют рекомендовать его для проведения клинических испытаний как новое имунномодулирующее и противовирусное средство с целью дальнейшего внедрения в медицинскую практику.
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИКОАГУЛЯНТНОЕ СРЕДСТВО НЕПРЯМОГО ДЕЙСТВИЯ НА ОСНОВЕ ДИУМАНКАЛА | 2018 |
|
RU2671983C9 |
| ГИБРИДНЫЕ КУМАРИНЫ, ОБЛАДАЮЩИЕ НЕПРЯМЫМ АНТИКОАГУЛЯНТНЫМ ДЕЙСТВИЕМ | 2018 |
|
RU2672062C1 |
| АНТИАРИТМИЧЕСКОЕ СРЕДСТВО НА ОСНОВЕ ГИБРИДНОЙ МОЛЕКУЛЫ АМЛОДИПИНА С (7-МЕТОКСИКУМАРИН-4-ИЛ)УКСУСНОЙ КИСЛОТОЙ | 2018 |
|
RU2678969C1 |
| АНТИКОАГУЛЯНТНОЕ СРЕДСТВО НЕПРЯМОГО ДЕЙСТВИЯ НА ОСНОВЕ НОВОЙ ГИБРИДНОЙ МОЛЕКУЛЫ ВАРФАРИНА С ОСТОЛЕВОЙ КИСЛОТОЙ | 2018 |
|
RU2677647C1 |
| ПРОИЗВОДНЫЕ 2-Н-1-БЕНЗОПИРАН-2-ОНА, ПРОЯВЛЯЮЩИЕ АНТИКАЛЬЦИЕВУЮ АКТИВНОСТЬ | 2003 |
|
RU2242471C1 |
| ИММУНОМОДУЛИРУЮЩЕЕ СРЕДСТВО НА ОСНОВЕ 3-О-ПРОПИОНАТА АЛЛОБЕТУЛЕНОЛА (19β,28-ЭПОКСИ-18α-ОЛЕАНАН-3β-ИЛ И ПРОПИОНАТ) | 2013 |
|
RU2554475C2 |
| СРЕДСТВО ПРОЛОНГИРОВАННОГО АНТИКАЛЬЦИЕВОГО ДЕЙСТВИЯ В ВИДЕ 0,1% РАСТВОРА ДЛЯ ВНУТРИВЕННОГО ВВЕДЕНИЯ | 2004 |
|
RU2255728C1 |
| ШТАММ А/Salekhard/01/2009(H1N1)v ВИРУСА ГРИППА А СУБТИПА H1N1 ДЛЯ ИССЛЕДОВАНИЯ ЛЕЧЕБНОЙ И ПРОФИЛАКТИЧЕСКОЙ ЭФФЕКТИВНОСТИ ПРЕПАРАТОВ ПРОТИВ ВИРУСА ГРИППА | 2011 |
|
RU2457242C1 |
| Пентавалентная субъединичная вакцина против респираторных инфекций и способ ее получения | 2022 |
|
RU2804948C2 |
| ИНГИБИТОР РЕПРОДУКЦИИ ВИРУСА ГРИППА А НА ОСНОВЕ ЭКСТРАКТА БАЗИДИАЛЬНОГО ГРИБА Laetiporus sulphureus | 2011 |
|
RU2475530C2 |


Изобретение относится к медицине и химико-фармацевтической промышленности и касается нового иммуномодулирующего и противовирусного средства на основе гибридной молекулы производных тритерпеноида-кумарина, а именно (2-((кумарин-7-ил)окси)этил) 3-гидрокси 20(29)-лупен-28-оата. Заявляемое соединение обладает иммуномодулирующими свойствами, оказывая влияние на активацию гуморального ответа, и выраженной противовирусной активностью в отношении вируса гриппа A/California/07/09 (H1N1)pdm09 у мышей Balb/c при лечебно-профилактическом режиме применения в дозах 10 мг/кг, может найти применение в медицинской практике при лечении и профилактике вирусных инфекций. 6 ил., 2 табл., 3 пр.
Иммуномодулирующее и противовирусное средство, включающее (2-((кумарин-7-ил)окси)этил) 3-гидрокси 20(29)-лупен-28-оата в качестве активного вещества,
| Colman PM | |||
| "A novel approach to antiviral therapy for influenza", J Antimicrob Chemother, 1999, vol | |||
| Приспособление для плетения проволочного каркаса для железобетонных пустотелых камней | 1920 |
|
SU44A1 |
| Печь для сжигания твердых и жидких нечистот | 1920 |
|
SU17A1 |
| Абышев А.З | |||
| и др | |||
| "Производные бетуленола как перспективные анти-ВИЧ агенты", Медицинский академический журнал, 2013, т | |||
| Насос | 1917 |
|
SU13A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Прибор для нагревания перетягиваемых бандажей подвижного состава | 1917 |
|
SU15A1 |
| Hassan M | |||
| Z | |||
| et al | |||
| "Therapeutic potential of coumarins as antiviral agents", European Journal of Medicinal Chemistry, 2016, vol | |||
| Устройство для разметки подлежащих сортированию и резанию лесных материалов | 1922 |
|
SU123A1 |
| Стеклографический печатный станок с ножной педалью | 1922 |
|
SU236A1 |
| СРЕДСТВО, ПРЕДСТАВЛЯЮЩЕЕ СОБОЙ АМИД ГЛИЦИРРИЗИНОВОЙ КИСЛОТЫ С 5-АМИНОУРАЦИЛОМ, ПРОЯВЛЯЮЩЕЕ ПРОТИВОВИРУСНУЮ АКТИВНОСТЬ В ОТНОШЕНИИ ВИРУСА ГРИППА A/H1N1 | 2014 |
|
RU2568849C9 |
Авторы
Даты
2019-04-30—Публикация
2018-11-01—Подача