Введение
Изобретение относится к биотехнологии, а именно: к способу получения бифункциональной молекулы для терапии рассеянного склероза (PC). Объектом исследования является химерный белок, состоящий из модуля доставки - пептида основного белка миелина МВР84-106, слитного с цитотоксическим модулем - константным доменом иммуноглобулина человека. Аутоантиген - пептид основного белка миелина МВР84-106 является одним из основных биомаркеров патологических лимфоцитов, при этом имеет высокую стабильность к протеолитической деградации. Константный домен иммуноглобулина человека является естественным сигналом иммунной системы для деградации клетки-мишени по механизму комплимент-зависимой цитотоксичности. Объединение перечисленных модулей в единую молекулу позволяет получать бифункцональный цитотоксический белок, направленно элиминирующий специфические патологические лимфоциты при PC.
Известны способы получения прототипов бифункциональных цитотоксических молекул в составе слитного белка на основе специфического пептида и токсических агентов на основе барназы, псевдомонадного токсина и константного Fc-домена антитела человека (Stepanov, А.V., Belogurov, A.A., Ponomarenko, N.A., Stremovskiy, О.A., Kozlov, L.V., Bichucher, А.М., et al. (2011). Design of Targeted В Cell Killing Agents. PloS One, 6(6), e20991. http://doi.org/10.1371/journal.pone.0020991.t001). Прототипы препаратов иммунотоксинов высокоспецифично (с избирательностью до 5000 раз в сравнении с иммунотоксином не содержащим таргетного участка) взаимодействовали с клетками мишенями и вызывали значительный цитотоксический эффект. Вариантов использования слитного белка МВР84-106 и константного домена иммуноглобулина человека на сегодняшний день не известно.
Область техники
Изобретение относится к области биотехнологии, в частности, предложена рекомбинантная плазмидная ДНК, кодирующая слитный белок МВР84-106 и константный домен иммуноглобулина человека. И способ получения белка MBP84-106-Fc для терапии рассеянного склероза.
Уровень техники
Изобретение относится к биотехнологии, а именно: к способу получения бифункционального агента для терапии социально-значимого заболевания - рассеянного склероза (PC).
Объектом разработки является пептид основного белка миелина МВР84-106, слитный с константным доменом иммуноглобулина человека. Аутоантиген - пептид основного белка миелина МВР84-106 является одним из основных биомаркеров патологических лимфоцитов при этом имеет высокую стабильность к протеолитической деградации. Константный домен иммуноглобулина человека является естественным сигналом иммунной системы для деградации клетки-мишени по механизму комплимент-зависимой цитотоксичности. Объединение перечисленных модулей в единую молекулу позволяет получать бифункцональный цитотоксический препарат, направленно элиминирующий специфические патологические лимфоциты при PC.
Известны способы получения прототипов бифункциональных цитотоксических молекул в составе слитного белка на основе специфического пептида и токсических агентов на основе барназы, псевдомонадного токсина и константного Fc-домена антитела человека (Stepanov, А.V., Belogurov, A.A., Ponomarenko, N.A., Stremovskiy, О.A., Kozlov, L.V., Bichucher, А.М., et al. (2011). Design of Targeted В Cell Killing Agents. PloS One, 6(6), e20991. Прототипы препаратов иммунотоксинов высокоспецифично (с избирательностью до 5000 раз в сравнении с иммунотоксином не содержащим таргетный участок) взаимодействовали с клетками мишенями и вызывали значительный цитотоксический эффект. Все представленные методики заключаются в генно-инженерном способе получения бифункциональных молекул, однако, способы получения слитного белка пептида основного белка миелина МВР84-106 с константным доменом иммуноглобулина человека, на настоящий момент не описаны.
Известна плазмида pYR-GCEVH, содержащая тяжелую цепь антитела HCAb к раку кишечника человека, и плазмида pYR-GCEVL, содержащая легкую цепь антитела к раку кишечника человека [Xiong Н., Ran Y., Xing J., Yang X., Li Y. and Chen Z. Expression vectors for human-mouse chimeric antibodies // Journal of Biochemistry and Molecular Biology. - 2005. - V. 38 (4). - P. 414-419]. Плазмида pYR-GCEVL включает в себя ген устойчивости к неомицину/генетицину под управлением раннего промотора вируса SV40 с удаленным энхансером. Транскрипция гена легкой цепи находится под контролем CMV на 5' конце и терминатора бычьего гормона роста (BGHT), на 3' конце находится сайт полиаденилирования. Плазмида pYR-GCEVH включает в себя ген dhfr под управлением раннего промотора вируса SV40. Транскрипция гена легкой цепи находится под контролем CMV на 5' конце и терминатора бычьего гормона роста (BGHT), на 3' конце находится сайт полиаденилирования.
Культура клеток dhfr (-) СНО (АТСС, США), дефицитных по дигидрофолатредуктазе (ДГФР), была ко-трансфецирована с использованием равных количеств плазмид pYR-GCEVH, pYR-GCEVL. После проведения нескольких раундов селекции была получена культура, клоны которой продуцировали химерные антитела с выходом от 30 до 100 мкг/мл кондиционированной среды [Xiong и др., 2005].
Известны плазмиды phCMV-VHRhD-g1C-neo и phCMV-VLRhD-KR-neo, кодирующие антитела против RhD антигена. Плазмида phCMV-VHRhD-g1C-neo содержит вариабельную и константную области тяжелой цепи под контролем главного раннего энхансера цитомегаловируса и промотор начала инициации транскрипции рекомбинантных тяжелых химерных цепей антитела, а также бактериальный ген устойчивости к неомицину под контролем раннего промотора SV40. Плазмида phCMV-VLRhDKR-neo содержит вариабельную и константную области легкой цепи под контролем раннего энхансера цитомегаловируса и промотор начала инициации транскрипции рекомбинантных легких химерных цепей антитела. В данной плазмиде ген устойчивости к неомицину под контролем раннего промотора SV40 был заменен геном dhfr из плазмиды pSV2-dhfr (Subramani S., Mulligan R., Berg P. Expression of the mouse dihydrofolatereductase complementary deoxyribonucleic acid in simian virus 40 vectors // Mol Cell Biol - 1981. - V. 1 (9). - P. 854-864). В обе плазмиды были внесены секреторные последовательности перед вариабельными доменами цепей антител, отделяющими их от интронных последовательностей. После проведения трансфекции клеточной линии СНО, дефицитной по гену ДГФР, и нескольких раундов селекции клонов, полученных из трансформированной культуры CHO-mAb с использованием МТХ (до 1000 нМ) и селективного антибиотика G418 (600 мкг/мл) были получены относительно устойчивые клоны с продукцией до 110 мкг/мл химерных антител [Chusainow J., Yang Y.S, Yeo J.H.M., Toh P.C., Asvadi P., Wong N.S.C., Miranda G.S. Yap. A Study of Monoclonal Antibody-Producing CHO Cell Lines: What Makes a Stable High Producer // Biotechnology and Bioengineering. - 2009. - V. 102 (4). - P. 1182-1196].
Раскрытие изобретения
Изобретение решает задачу создания технологии для ускорения и повышения экономичности процесса получения препарата основного белка миелина МВР84-106, слитого с константной областью человеческого антитела F10 (MBP84-106-Fc).
Технический результат достигается за счет увеличения уровня биологического синтеза MBP84-106-Fc клетками-продуцентами при использовании селективного цитостатического препарата (метотрексата).
Поставленная задача решается путем конструирования рекомбинантной плазмидной ДНК, обозначенной pOptiVEC-MBP84-106-Fc, и содержащей
- фрагмент плазмиды pOptiVEC™-TOPO®, включающий промотор/энхансер ранних генов цитомегаловируса человека (CMV), внутренний сайт связывания (IRIS), ген ДГФР, сигнал полиаденилирования тимидинкиназы вируса герпеса, сайт начала репликации в Е. coli из плазмиды pUC, ген β-лактамазы, а также следующие модификации - единичный сайт узнавания рестриктазы MluI вместо сайта узнавания рестриктазы SalI в положении 23, единичные сайты узнавания рестриктаз NheI и XhoI после промотора CMV для клонирования ДНК МВР84-106-Fc;
- фрагмент ДНК, включающий фланкированную сайтами рестрикции NheI и XhoI кДНК MBP84-106-Fc под контролем промотора/энхансера ранних генов цитомегаловируса человека (CMV);
Также настоящее изобретение представляет способ получения культуры клеток яичника китайского хомячка СНО - продуцента MBP84-106-Fc путем трансфекции клеток упомянутой выше рекомбинантной плазмидной ДНК.
Также настоящее изобретение представляет линию клеток яичника китайского хомячка СНО - продуцента MBP84-106-Fc, называемую далее CHO-S18 и полученную путем трансфекции линии клеток СНО DG44 упомянутой выше рекомбинантной плазмидной
ДНК.
Также настоящее изобретение представляет способ получения MBP84-106-Fc, включающий:
- культивирование в питательной среде упомянутой линии клеток культуры СНО-S18,
- выделение полученного целевого белка из культуральной жидкости.
В частном варианте воплощения настоящего изобретения указанная плазмида может представлять собой плазмиду, состоящую из:
фрагмента плазмиды pOptiVEC™-TOPO®, включающего промотор/энхансер ранних генов цитомегаловируса человека (CMV), обеспечивающий высокий уровень экспрессии целевых белков в клетках млекопитающих, внутренний сайт связывания рибосом (IRES), ген ДГФР для ауксотрофной селекции трансфецированных клеток СНО DG44 и геномной амплификации стабильных клеточных линий с использованием метатрексата, сигнал полиаденилирования тимидинкиназы вируса герпеса для правильной терминации и процессинга рекомбинантных транскриптов, сайт начала репликации в Е. coli из плазмиды pUC, ген β-лактамазы, а также следующие модификации - единичный сайт узнавания рестриктазы MluI вместо сайта узнавания рестриктазы SalI в положении 23, единичные сайты узнавания рестриктаз NheI и XhoI после промотора CMV для клонирования кДНК МВР84-106;
NheI/XhoI - фрагмента ДНК, включающего фланкированную сайтами рестрикции NheI и XhoI кДНК лидерного пептида тяжелой цепи моноклонального антитела F10, необходимого для секреции рекомбинантного константного фрагмента иммуноглобулина человека, слитного с фрагментом основного белка миелина 84-106 из клеток-продуцентов СНО в культуральную среду, кДНК фрагмента основного белка миелина МВР84-106, кодирующую фрагмент основного белка миелина, включающий в себя аминокислотные остатки данного белка с 84 по 106 включительно, и кДНК константного фрагмента иммуноглобулина человека, а именно константных доменов СН2, СН3 тяжелой цепи иммуноглобулина изотипа IgG1 человека.
Наличие в плазмиде pOptiVEC-MBP84-106-Fc активного гена ДГФР, находящегося под контролем IRES, позволяет проводить селекцию и амплификацию чужеродных последовательностей, интегрированных в геном клетки СНО DG44 (dhfr-/- вариант линии клеток СНО-K1), в среде, содержащей метотрексат.
Технический эффект изобретения заключается в том, что культура, трансфецированная плазмидой pOptiVEC-MBP884-106-Fc продуцирует бифункциональную молекулу MBP84-106-Fc для терапии рассеянного склероза в среду культивирования.
Экспрессия бифункциональной молекулы MBP84-106-Fc может быть осуществлена в эукариотических клетках. Примером эукариотической клетки, пригодной для продукции слитного белка МВР84-106 с константным доменом иммуноглобулина человека, согласно настоящему изобретению являются, но не ограничиваются ими, клетки яичников Cricetulus griseus (СНО). Примерами клеток яичников Cricetulus griseus (СНО), применимых в рамках настоящего изобретения, являются, но не ограничиваются ими, клетки яичников Cricetulus griseus (СНО) клетки СНО DG44 (Invitrogen).
Способом согласно настоящему изобретению является способ получения МВР84-106-Fc, включающий выращивание трансформированных клеток эукариот в питательной среде и выделение полученных антител из культуральной жидкости.
Выращивание клеток эукариот осуществляют в атмосфере 5% СО2 в режиме культивирования с перемешиванием в синтетических средах, таких как среда OptiCHO, в течение 3-6 суток.
После выращивания твердые компоненты, такие как клетки, могут быть удалены из культуральной жидкости методом центрифугирования или фильтрации с использованием мембраны, а затем белок может быть выделен и очищен методом осаждения с солями, с использованием сульфата натрия или сульфата аммония, аффинной хроматографии, ионообменной хроматографии и т.п.
Предложенные рекомбинантная плазмида pOptiVEC-MBP84-106-Fc и способ получения линии культивируемых клеток СНО, основанный на использовании рекомбинантной плазмиды pOptiVEC-MBP84-106-Fc, впервые получены авторами данного изобретения, в научной и патентной литературе не описаны.
Осуществление изобретения
Пример 1. Конструирование рекомбинантной плазмидной ДНК pOptiVEC-MBP84-106-Fc.
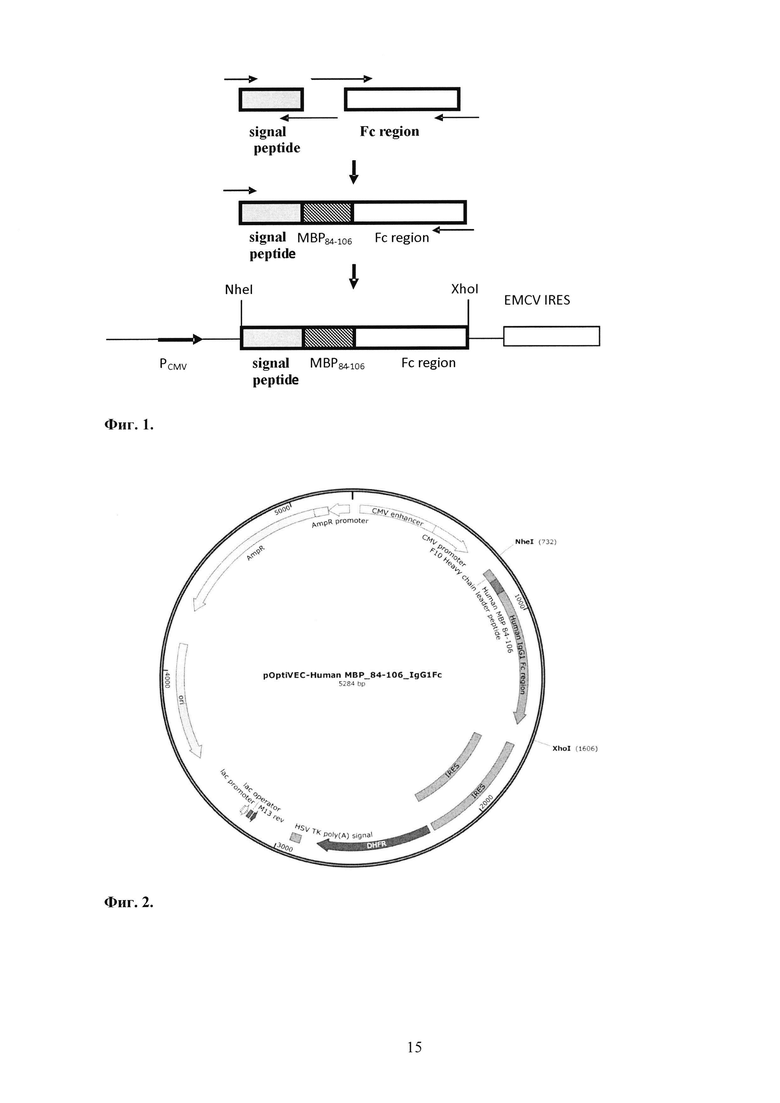
Конструирование плазмиды pOptiVEC-MBP84-106-Fc проводят по схеме, изложенной на фигуре 1, с использованием праймеров, приведенных в таблице 1.
Последовательности:
SEQ ID NO: 1
аминокислотная последовательность лидерного пептида тяжелой цепи моноклонального антитела F10
SEQ ID NO: 2
нуклеотидная последовательность, кодирующая лидерный пептид тяжелой цепи моноклонального антитела F10
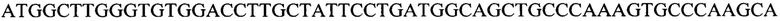
SEQ ID NO: 3
нуклеотидная последовательность, кодирующая фрагмент основного белка миелина 84-106 (МВР84-106)
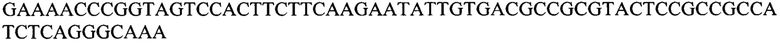
SEQ ID NO: 4
аминокислотная последовательность фрагмента основного белка миелина 84-106 (МВР84-106)
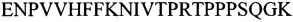
SEQ ID NO: 5
нуклеотидная последовательность, кодирующая Fc-фрагмент антитела IgG1 (домены СН2-СН3) человека

SEQ ID NO: 6
аминокислотная последовательность Fc-фрагмента антитела IgG1 (доменов СН2-СН3) человека

Итоговая последовательность:
NheI

XhoI

Жирным шрифтом отмечен сигнальный пептид, подчеркиванием выделена область Fc, между сигнальным пептидом и областью Fc находится последовательность МВР84-106, после области Fc находится нетранслируемая область. На 5'- и 3'-концах курсивом выделены сайты узнавания рестриктаз NheI и XhoI, соответственно. Результирующая генетическая конструкция изображена на фигуре 2.
Пример 2. Получение линии CHO-S18, продуцента MBP84-106-Fc с применением плазмиды pOptiVEC-MBP84-106-Fc.
Для получения линии СНО-18, стабильного продуцента рекомбинантного слитного белка МВР84-106 с константным доменом иммуноглобулина человека проводят трансфекцию клеток яичника китайского хомячка СНО DG44 dhfr - плазмидой pOptiVEC-MBP84-106-Fc. Клетки культивируют в среде CD DG44 (Invitrogen) с добавлением 200 мМ раствора L-Глутамина до конечной концентрации 8 мМ и содержащей 0,18% (v/v) Pluronic F-68 (Invitrogen). Во флаконы Эрленмейера объемом 125 мл засевают 30 мл клеточной суспензии (4,5 млн клеток) при постоянном пемешивании на орбитальном шейкере с частотой 130 об/мин и через 20-24 ч проводят трансфекцию с использованием реагента Freestyle МАХ (Invitrogen) [Freestyle MAX Reagent Protocol, http://tools.invitrogen.com/content/sfs/manuals/freestyle_max_reagent_man.pdf]. Плазмидную ДНК добавляют к клеткам в виде ДНК-липосомного преципитата. Преципитат готовят следующим образом: при комнатной температуре во флакон А вносят 18 мкг ДНК плазмиды в 1200 мкл среды OptiPRO SFM (Invitrogen), перемешивают, добавляют 15 мкл реагента Freestyle MAX (Invitrogen), инкубируют от 10 до 20 минут при комнатной температуре. После инкубации перемешивают пипетированием и по каплям вносят в культуральный флакон. Культуральный флакон инкубируют при температуре 37°С, 98% влажности, в атмосфере 8% СО2 и непрерывном перемешивании 130 об/мин.
Через 48 ч после трансфекции клетки отмывают и помещают в ростовую среду CD OptiCHO (Invitrogen) (без тимидина и гипоксантина) с добавлением 200 мМ раствора L-Глутамина до конечной концентрации 8 мМ и содержащей 0,18% (v/v) Pluronic F-68 на 48 ч. Клетки инкубируют в селективной среде в течение двух недель, смену среды и поддержание концентрации клеток в среде проводят каждые трое суток.
Через 14 дней после помещения в селективные условия в культуре остаются клетки, способные существовать без добавления в среду тимидина и гипоксантина. При достижении культурой времени удвоения популяции 24 часа производят полную замену среды на среду CD DG44, содержащей 8 мМ L-Глутамина, 0,18% Pluronic F-68, 50 нМ метотрексата.
Через 14 дней после помещения в среду, содержащую метотрексат, остаются только клетки, способные существовать в присутствии 50 нМ метотрексата. При достижении культурой времени удвоения популяции 24 часа производят полную замену среды на среду CD DG44, содержащую 8 мМ L-Глутамина, 0,18% (v/v) Pluronic F-68, 100 нМ метотрексата.
Данную процедуру увеличения концентрации метотрексата проводят до тех пор, пока не будет достигнута устойчивость клеток к концентрации метотрексата равной 500 нМ.
Таким образом, получают культуру CHO-S18, клетки которой стабильно продуцируют MBP84-106-Fc в культуральную жидкость с выходом до 20 мкг/мл среды при культивировании в условиях перемешивания со скоростью 130 об/мин.
Пример 3. Получение, выделение и очистка белкового продукта с помощью линии клеток CHO-S18, продуцирующей MBP84-106-Fc.
Получение белкового продукта с применением линии CHO-S18 производят в колбах Эрленмейера различного объема без рассекателей в ростовой среде CD OptiCHO (без тимидина и гипоксантина) с добавлением 200 мМ раствора L-Глутамина до конечной концентрации 8 мМ и 0,18% (v/v) Pluronic F-68 без добавления дополнительных количеств питательных веществ при постоянном перемешивании с частотой 135 об/мин при температуре 37°С, 98% влажности в атмосфере 8% СО2. Культивирование для получения белкового продукта производят не менее 14 дней.
После окончания культивирования для получения продукта MBP84-106-Fc от культуры CHO-S18 полученную кондиционированную среду от культуры CHO-S18 центрифугируют при 4000 об/мин в течение 30 мин. Супернатант смешивают в соотношении 4:1 с Буфером для нанесения (50 мМ Трис-HCl, рН=7.0) и наносят на подготовленную Белок А-агарозную колонку (Gibco BRL, США). При элюции используют Буфер для элюции (100 мМ глицина, рН 3,0) и Нейтрализующий буфер (1 М Трис-HCl, рН 8,0). Колонку с 2 мл Белок А-агарозы промывают 3 раза по 4 мл Буфером для нанесения. Далее наносят смесь супернатанта кондиционированной среды и Буфера для нанесения. Образец наносят при комнатной температуре с помощью перистальтического насоса. После нанесения образца колонку промывают 3 раза по 20 мл Буфером для нанесения. Смывание белка MBP84-106-Fc с колонки производят с помощью 6 фракций по 2 мл Буфера для элюции. К образцу добавляют Нейтрализующий буфер в соотношении 1 часть буфера на 9 частей прошедшего через колонку Буфера для элюции.
Полученные образцы выделенного белка MBP84-106-Fc диализуют против ФСБ (фосфатно-солевой буфер, 137 мМ NaCl, 2,7 мМ KCl, 10 мМ Na2HPO4, 1,76 мМ KH2PO4, рН 7,4) и хранят при температуре +4°С.
Оценку гомогенности и степени очистки препарата проводят как с использованием электрофоретического метода, так и аналитической гель-проникающей ВЭЖХ.
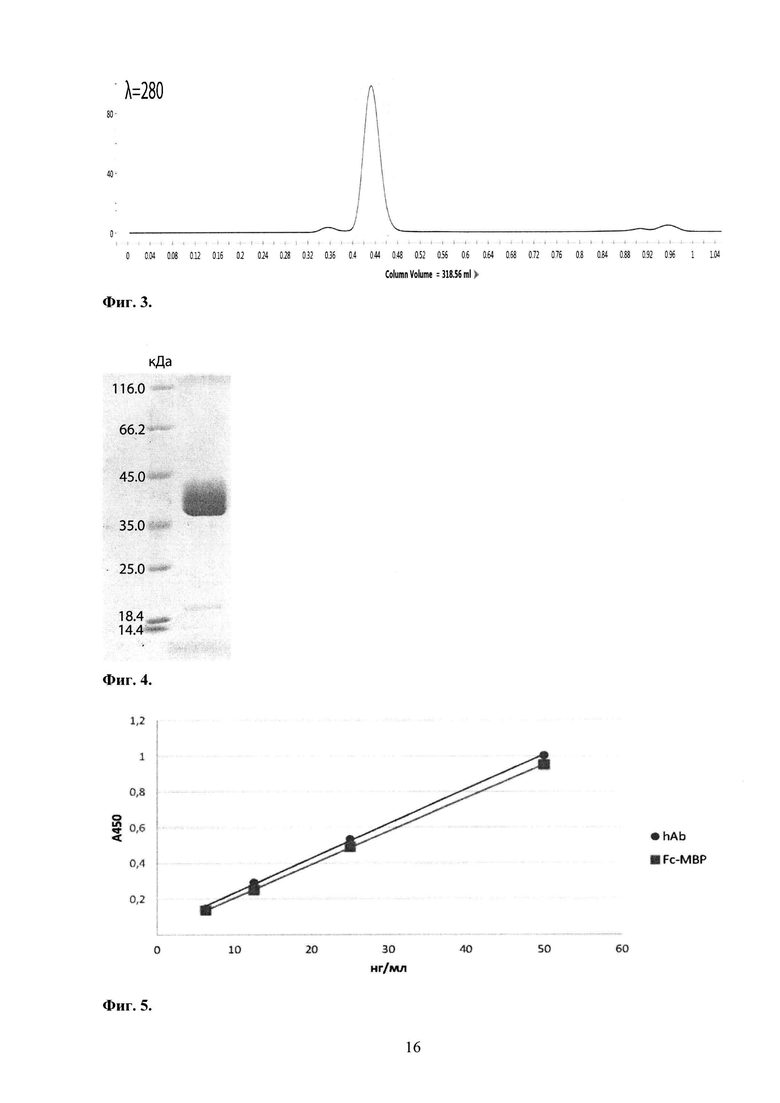
Препараты рекомбинантных белка MBP84-106-Fc, полученные в ходе выделения с помощью аффинной хроматографии на Белок А-агарозе, анализируют на хроматографической ВЭЖХ системе Knauer (Германия), оснащенной колонкой Супердекс-200-10/300GL. Исследование проводят в протекающем буфере А (100 мМ Трис-HCl, 150 мМ NaCl, рН 7,5). Детекцию осуществляют при длине волны 230 нм УФ-детектором 2600 (UV detector 2600).
Элюция MBP84-106-Fc с колонки происходит в интервале 31-34 мин от момента старта проведения хроматографического анализа. Данные хроматографического анализа свидетельствуют о более чем 98%-ной чистоте полученного препарата рекомбинантных антител.
Электрофорез проводят в 10%-ном полиакриламидном геле. В качестве контроля используют неокрашенный белковый маркер молекулярных весов (Fermentas, Великобритания). Перед внесением к 15 мкл образца антител добавляют 5 мкл Буфера для нанесения с 2-меркаптоэтанолом (2-МЭ) (200 мМ Трис-HCl, рН 6,8, 400 мМ 2-МЭ, 4% натрия додецилсульфат, 0,01% бромофеноловый синий, 40%-ный глицерин). Образцы для внесения на гель инкубируют при температуре 95°С в течение 5 мин.
Полученные образцы продукта MBP84-106-Fc (Фиг. 3) характеризуются следующими показателями:
- гомогенность препарата не менее 98% (по данным гель-электрофореза в 10%-ном полиакриламидном геле с денситометрией);
- молекулярная масса - 28119 Да (по данным гель-электрофореза с белковыми маркерами молекулярных весов);
Пример 4. Получение, выделение и очистка MBP84-106-Fc с применением гель-проникающей хроматографии
После окончания культивирования для получения препарата рекомбинантного MBP84-106-Fc полученную кондиционированную среду от культуры CHO-S18 центрифугируют при 4000 об/мин в течение 30 мин. Супернатант смешивают в соотношении 4:1 с Буфером для нанесения (50 мМ Трис-HCl, рН 7,0) и наносят на подготовленную Белок А-агарозную колонку (Gibco BRL, США). При элюции используют Буфер для элюции (100 мМ глицина, рН 3,0) и Нейтрализующий буфер (1 М Трис-HCl, рН 8,0). Колонку с 2 мл Белок А-агарозы промывают 3 раза по 4 мл Буфером для нанесения. Далее наносят смесь супернатанта кондиционированной среды и Буфера для нанесения. Образец наносят при комнатной температуре с помощью перистальтического насоса. После нанесения образца колонку промывают 3 раза по 20 мл Буфером для нанесения. Смывание препарата рекомбинантного Fc-MBP с колонки производят с помощью 6 фракций по 2 мл Буфера для элюции. К образцу добавляют Нейтрализующий буфер в соотношении 1 часть буфера Полученные образцы выделенных антител диализуют против ФСБ (фосфатно-солевой буфер, 137 мМ NaCl, 2,7 мМ KCl, 10 мМ Na2HPO4, 1,76 мМ KH2PO4, рН 7,4), концентрируют с помощью Amicon Ultracel (10000NMWL) до 4 мл (15 мин 4°С, 5000g) и хранят при температуре +4°С. Проводят гель-фильтрационную хроматографию с использованием хроматографической колонки Superdex 75 16/600 GL (GE Healthcare Life Sciences). Буфер нанесения: ФСБ (фосфатно-солевой буфер, 137 мМ NaCl, 2,7 мМ KCl, 10 мМ Na2HPO4, 1,76 мМ KH2PO4, рН 7,4). Скорость потока: 2,5 мл/мин. Очищенная фракция препарата рекомбинантного Fc-MBP выходит с 0,4 по 0,47 объем колонки. Типичная хроматограмма процесса очистки представлена на фигуре 4.
Оценку гомогенности и степени очистки препарата проводят как с использованием электрофоретического метода, так и иммуноферментного анализа. Элюция препарата рекомбинантного MBP84-106-Fc с колонки происходит в интервале 0,4-0,47 объема колонки от момента старта проведения хроматографической очистки.
Электрофорез проводят в 12%-ном полиакриламидном геле. В качестве контроля используют неокрашенный белковый маркер молекулярных весов (Fermentas, Великобритания). Перед внесением к 15 мкл образца антител добавляют 5 мкл Буфера для нанесения с 2-меркаптоэтанолом (2-МЭ) (200 мМ Трис-HCl, рН 6,8, 400 мМ 2-МЭ, 4% натрия додецилсульфат, 0,01% бромофеноловый синий, 40%-ный глицерин). Образцы для внесения на гель инкубируют при температуре 95°С в течение 5 мин.
Иммуноферментный анализ препарата рекомбинатного MBP84-106-Fc, приведенный на фигуре 5, проводили с использованием антивидовых антител анти-Fc (anti-human anti-Fc hrp Sigma Aldrich). Препарат рекомбинатного MBP84-106-Fc анализировали в двукратных разведениях от 6 до 50 нг/мл (в соответсвии с оптической плотностью белка). В качестве калибровки и положительного контроля использовалась титровка препарата поликлональных очищенных антител человека из сыворотки крови (hAb) при концентрации от 6 до 50 нг/мл.
Полученные образцы препарата рекомбинантного MBP84-106-Fc характеризуются следующими показателями:
- гомогенность препарата не менее 98% (по данным гель-электрофореза в 12%-ном полиакриламидном геле с денситометрией);
- молекулярная масса - 28000 Да (по данным гель-электрофореза с белковыми маркерами молекулярных весов);
Изобретение иллюстрируют следующие графические материалы:
Фиг. 1. Схема конструирования экспрессионной плазмиды pOptiVEC-MBP84-106-Fc. PCMV - CMV промотор; EMCV IRES - независимый сайт инициирования рибосомы; NheI, XhoI - эндонуклеазы рестрикции
Фиг. 2. Физическая карта рекомбинантной плазмиды pOptiVEC-MBP84-106-Fc со следующими обозначениями: bla promoter - промотор гена β-лактамазы, CMV promoter -промотор/энхансер ранних генов цитомегаловируса человека, CMV Forward priming site -сайт отжига праймера CMV Forward, МВР84-106 - пептид основного белка миелина, Fc -константный домен тяжелой цепи антитела F10 человека, EMCV IRES reverse primer binding site - сайт отжига праймера EMCV IRES reverse primer, EMCV IRES - внутренний сайт связывания рибосом (IRES) вируса энцефаломиокардита, DHFR - ген дигидрофолатредуктазы, TK polyA - сигнал полиаденилирования тимидинкиназы вируса герпеса, pUC origin - последовательность, отвечающая за репликацию плазмиды pUC, Ampicillin (bla) resistance gene - ген устойчивости к антибиотику ампициллину. MluI, SphI, XhoI, SacII, NheI, NdeI, XbaI, SalI, BglII, PvuI - сайты эндонуклеаз рестрикции.
Фиг. 3. Электрофореграмма с денситометрией рекомбинантного препарата MBP84-106-Fc со следующими обозначениями: кДа - белковые стандарты молекулярного веса; Е1 - объединенная фракция препарата MBP84-106-Fc; kDa - единица молекулярного веса, килодальтон.
Фиг. 4. Профиль гель-фильтрационной хроматографии с использованием колонки Superdex75 для финальной очистки препарата рекомбинатного MBP84-106-Fc
Фиг. 5. Иммуноферментный анализ по специфическому узнаванию антител анти-Fc (anti-human) с препаратом рекомбинатного Fc-MBP. В качестве калибровки и положительного контроля использовалась титровка препарата поликлональных очищенных антител человека из сыворотки крови (hAb) при концентрации от 6 до 50 нг/мл.
Таблица 1. Структура использованных олигонуклеотидов.

Заявка № 2016152258/10(083704) (дата подачи 29.12.2016, заявитель Федеральное государственное бюджетное учреждение науки Институт биоорганической зимии им. академиков М.М. Шемякина и Ю.А. Овчинникова Российской академии наук(ИБХ РАН), RU)
РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК pOptiVEC-MBP84-106-Fc, КОДИРУЮЩАЯ КОНСТАНТНЫЙ ФРАГМЕНТ ИММУНОГЛОБУЛИНА ЧЕЛОВЕКА, СЛИТНОГО С ФРАГМЕНТОМ ОСНОВНОГО БЕЛКА МИЕЛИНА, ЛИНИИ ЭУКАРИОТИЧЕСКИХ КЛЕТОК – ПРОДУЦЕНТОВ УКАЗАННОГО БЕЛКА И СПОСОБ ПОЛУЧЕНИЯ БЕЛКА MBP84-106-Fc ДЛЯ ТЕРАПИИ РАССЕЯННОГО СКЛЕРОЗА
Последовательности:
SEQ ID NO:1
аминокислотная последовательность лидерного пептида тяжелой цепи моноклонального антитела F10
MAWVWTLLFLMAAAQSAQA
SEQ ID NO:2
нуклеотидная последовательность, кодирующая лидерный пептид тяжелой цепи моноклонального антитела F10
ATGGCTTGGGTGTGGACCTTGCTATTCCTGATGGCAGCTGCCCAAAGTGCCCAAGCA
SEQ ID NO:3
нуклеотидная последовательность, кодирующая фрагмент основного белка миелина 84-106 (MBP84-106)
GAAAACCCGGTAGTCCACTTCTTCAAGAATATTGTGACGCCGCGTACTCCGCCGCCATCTCAGGGCAAA
SEQ ID NO:4
аминокислотная последовательность фрагмента основного белка миелина 84-106 (MBP84-106)
ENPVVHFFKNIVTPRTPPPSQGK
SEQ ID NO:5
нуклеотидная последовательность, кодирующая Fc-фрагмент антитела IgG1 (домены CH2-CH3) человека
GACAAAACTCACACATGCCCACCGTGCCCAGCACCTGAACTCCTGGGGGGACCGTCAGTCTTCCTCTTCCCCCCAAAACCCAAGGACACCCTCATGATCTCCCGGACCCCTGAGGTCACATGCGTGGTGGTGGACGTGAGCCACGAAGACCCTGAGGTCAAGTTCAACTGGTACGTGGACGGCGTGGAGGTGCATAATGCCAAGACAAAGCCGCGGGAGGAGCAGTACAACAGCACGTACCGGGTGGTCAGCGTCCTCACCGTCCTGCACCAGGACTGGCTGAATGGCAAGGAGTACAAGTGCAAGGTCTCCAACAAAGCCCTCCCAGCCCCCATCGAGAAAACCATCTCCAAAGCCAAAGGGCAGCCCCGAGAACCACAGGTGTACACCCTGCCCCCATCCCGGGATGAGCTGACCAAGAACCAGGTCAGCCTGACCTGCCTGGTCAAAGGCTTCTATCCCAGCGACATCGCCGTGGAGTGGGAGAGCAATGGGCAGCCGGAGAACAACTACAAGACCACGCCTCCCGTGCTGGACTCCGACGGCTCCTTCTTCCTCTACAGCAAGCTCACCGTGGACAAGAGCAGGTGGCAGCAGGGGAACGTCTTCTCATGCTCCGTGATGCATGAGGCTCTGCACAACCACTACACGCAGAAGAGCCTCTCCCTGTCTCCGGGTAAA
SEQ ID NO:6
аминокислотная последовательность Fc-фрагмента антитела IgG1 (доменов CH2-CH3) человека
DKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
| название | год | авторы | номер документа |
|---|---|---|---|
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК, КОДИРУЮЩАЯ ХИМЕРНОЕ АНТИТЕЛО ПРОТИВ ФАКТОРА НЕКРОЗА ОПУХОЛИ-АЛЬФА ЧЕЛОВЕКА, ЛИНИЯ ЭУКАРИОТИЧЕСКИХ КЛЕТОК-ПРОДУЦЕНТ ХИМЕРНОГО АНТИТЕЛА И СПОСОБ ПОЛУЧЕНИЯ ХИМЕРНОГО АНТИТЕЛА | 2013 |
|
RU2555533C9 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК pBiPr-ABIgA2m1F16-ht ДЛЯ ПОЛУЧЕНИЯ РЕКОМБИНАНТНОГО ИММУНОГЛОБУЛИНА А ИЗОТИПА IGA2m1 | 2016 |
|
RU2671477C2 |
| Способ получения димерной формы иммуноглобулина IgA1-изотипа в клетках млекопитающих | 2023 |
|
RU2822890C1 |
| Способ получения димерной формы мутантного иммуноглобулина IgA2m1-изотипа в клетках млекопитающих | 2023 |
|
RU2822889C1 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК pBiPr-ABIgA1FI6-Intht ДЛЯ ПОЛУЧЕНИЯ РЕКОМБИНАНТНОГО ИММУНОГЛОБУЛИНА А ИЗОТИПА IgA1 | 2016 |
|
RU2664184C2 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК pBiPr-ABIgA1FI6-ht ДЛЯ ПОЛУЧЕНИЯ РЕКОМБИНАНТНОГО ИММУНОГЛОБУЛИНА А ИЗОТИПА IGA1 | 2016 |
|
RU2656142C1 |
| СПОСОБ ПОЛУЧЕНИЯ РЕКОМБИНАНТНОГО ИММУНОГЛОБУЛИНА IGA2m1-ИЗОТИПА В КЛЕТКАХ МЛЕКОПИТАЮЩИХ | 2022 |
|
RU2801178C1 |
| КЛЕТОЧНАЯ ЛИНИЯ huFSHIK, СЕКРЕТИРУЮЩАЯ РЕКОМБИНАНТНЫЙ ЧЕЛОВЕЧЕСКИЙ ФСГ | 2012 |
|
RU2502798C2 |
| СПОСОБ ПОЛУЧЕНИЯ БЕЛКА | 2010 |
|
RU2563514C2 |
| ГУМАНИЗИРОВАННОЕ АНТИТЕЛО И АНТИГЕНСВЯЗЫВАЮЩИЙ ФРАГМЕНТ (Fab), СВЯЗЫВАЮЩИЕСЯ С ИНТЕРФЕРОНОМ- γ ЧЕЛОВЕКА, ФРАГМЕНТЫ ДНК, КОДИРУЮЩИЕ УКАЗАННОЕ АНТИТЕЛО И АНТИГЕНСВЯЗЫВАЮЩИЙ ФРАГМЕНТ, КЛЕТКА, ТРАНСФОРМИРОВАННАЯ ФРАГМЕНТОМ ДНК, И СПОСОБ ПОЛУЧЕНИЯ УКАЗАННОГО АНТИТЕЛА И АНТИГЕНСВЯЗЫВАЮЩЕГО ФРАГМЕНТА | 2013 |
|
RU2539752C2 |
Изобретение относится к области биотехнологии, конкретно к рекомбинантному получению терапевтических белков, и может быть использовано для получения слитого белка MBP84-106-Fc, состоящего из лидерного пептида тяжелой цепи моноклонального антитела FI0, слитого с фрагментом основного белка миелина 84-106 (МВР84-106) и затем с Fc-фрагментом антитела IgG 1 (домены СН2-СН3) человека, в клетках яичника китайского хомячка (СНО). Конструируют рекомбинантный бипромоторный вектор экспрессии pOptiVEC-MBP84-106-Fc, обеспечивающий биосинтез бифункциональной молекулы MBP84-106-Fc в культивируемых клетках СНО. Линию клеток CHO-S18 - продуцента MBP84-106-Fc - получают путем трансфекции клеток линии СНО DG44 вектором pOptiVEC-MBP84-106-Fc. Предложенное изобретение позволяет получить линию клеток СНО, стабильно продуцирующую в культуральную жидкость белок MBP84-106-Fc с выходом 20 мкг в мл кондиционированной среды. 4 н. и 3 з.п. ф-лы, 5 ил., 1 табл., 4 пр.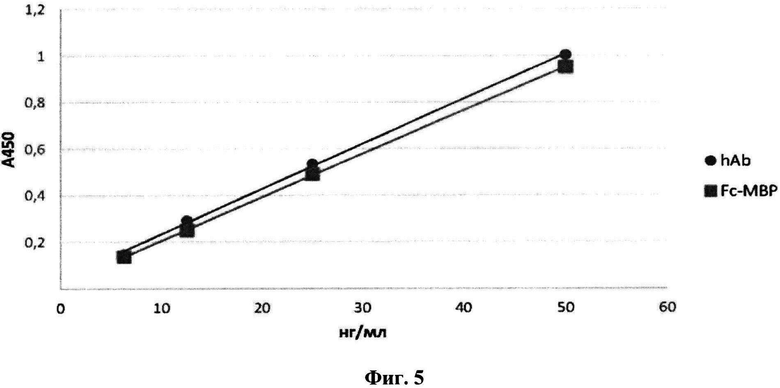
1. Рекомбинантная плазмидная ДНК pOptiVEC-MBP84-106-Fc, способная к экспрессии в клетках СНО слитого белка MBP84-106-Fc, состоящего из лидерного пептида тяжелой цепи моноклонального антитела FI0, слитого с фрагментом основного белка миелина 84-106 (МВР84-106) и затем с Fc-фрагментом антитела IgG 1 (домены СН2-СН3) человека, соотносимая с физической картой, приведенной на фиг. 2, содержащая:
- фрагмент плазмиды pOptiVEC™-TOPO®, включающий промотор/энхансер ранних генов цитомегаловируса человека (CMV), ген ДГФР, сигнал полиаденилирования тимидинкиназы вируса герпеса, сайт начала репликации в Е. coli из плазмиды pUC, ген β-лактамазы, а также следующие модификации - единичный сайт узнавания рестриктазы MluI вместо сайта узнавания рестриктазы SalI в положении 23, единичные сайты узнавания рестриктаз NheI и XhoI после промотора CMV для клонирования ДНК MBP84-106-Fc;
- фрагмент ДНК, включающий фланкированную сайтами рестрикции NheI и XhoI ДНК - MBP84-106-Fc с нуклеотидными последовательностями SEQ ID NO: 2, SEQ ID NO: 3 и SEQ ID NO: 5, под контролем промотора/энхансера ранних генов цитомегаловируса человека (CMV).
2. Рекомбинантная плазмидная ДНК по п. 1, характеризующаяся тем, что в ней содержится фрагмент ДНК, кодирующий аминокислотную последовательность лидерного пептида тяжелой цепи моноклонального антитела F10 с аминокислотной последовательностью SEQ ID NO: 1.
3. Рекомбинантная плазмидная ДНК по п. 1, характеризующаяся тем, что в ней содержится фрагмент ДНК, кодирующий аминокислотную последовательность фрагмента основного белка миелина 84-106 (МВР84-106) SEQ ID NO: 4.
4. Рекомбинантная плазмидная ДНК по п. 1, характеризующаяся тем, что в ней содержится фрагмент ДНК, кодирующий аминокислотную последовательность Fc-фрагмента антитела IgG1 (доменов СН2-СН3) человека SEQ ID NO: 6.
5. Способ получения эукариотической линии клеток CHO-S18 - продуцента MBP84-106-Fc, которая получена путем трансфекции клеток линии СНО DG44 (не являющейся эмбриональными клетками человека) рекомбинантной плазмидной ДНК по п. 1.
6. Линия эукариотических клеток CHO-S18 - продуцент MBP84-106-Fc, полученная путем трансфекции клеток линии СНО DG44 рекомбинантной плазмидной ДНК по п. 1.
7. Способ получения слитного белка МВР84-106 с константным доменом иммуноглобулина человека (MBP84-106-Fc), включающий:
- культивирование в питательной среде клеток линии CHO-S18 - продуцент МВР84-106-Fc по п. 5,
- выделение полученного целевого белка MBP84-106-Fc из культуральной жидкости.
Авторы
Даты
2019-02-05—Публикация
2016-12-29—Подача