Изобретение относится к области медицины и химико-фармацевтической промышленности, а именно к трансдермальным препаратам для профилактики и лечения болезней суставов и мягких тканей, содержащим в качестве активных компонентов хондропротекторы и нестероидные противовоспалительные средства.
Остеоартрит (далее - OA) - хроническое прогрессирующее заболевание синовиальных суставов, этиология которого неизвестна. OA относят к тяжелым недугам человечества, а проблема лечения этого заболевания является одной из ключевых в терапии, ортопедии, ревматологии и клинической фармации. OA широко распространен среди людей пожилого и зрелого возраста, характеризуется дегенерацией суставного хряща, структурными изменениями субхондральной кости, умеренно или выражено протекающими синовитами, хроническим течением и тенденцией к прогрессированию. Все это обуславливает снижение трудоспособности (в среднем в 60% случаев) и приводит в 11,5% случаев к инвалидности больных наиболее трудоспособного возраста [1].
Особую значимость приобретает данная проблема в связи с ростом продолжительности жизни человека. Согласно проведенным эпидемиологическим исследованиям, дистрофические изменения в суставах обнаруживаются в 50% случаев у людей старше 40 лет, а в возрасте 70 лет это заболевание отмечено у 90% населения. В целом, удельный вес OA в общей структуре заболеваемости населения составляет 12% и занимает первое место среди патологий суставов [1].
При OA нарушения определяются во всех структурных компонентах сустава, но наиболее выраженные изменения прослеживаются в суставном хряще, в соответствии с которыми выделяют 4 стадии OA. Имеются разные точки зрения на гистохимические и метаболические нарушения в суставном хряще при OA, в частности, снижение содержания глюкозаминогликанов (ГАГ), связанное с угасанием биохимических процессов в хондроцитах. Кроме того, отмечается понижение способности хряща удерживать вновь синтезированные хондроцитами макромолекулы ГАГ в матриксе за счет превращения их в форму, не способную вступать в связь с гиалуроновой кислотой. С развитием дистрофических и деструктивных нарушений в суставном хряще снижается плотность хондроцитов за счет их гибели [1, 2].
Разрушение суставного хряща возможно из-за воздействия ферментов, которые образуются при воспалении. Существенным звеном в патогенезе заболевания может быть повышение биосинтеза простагландинов и накопление их в синовиальной жидкости, что способствует повреждению хрящевой ткани и индукции синовита (воспаления синовиальной оболочки). Воспалительный процесс в условиях OA приводит к деструкции суставного хряща [1, 2].
OA сопровождается болью, которая усиливается при прогрессировании заболевания [3]. Нестероидные противовоспалительные средства (далее НПВС) используют для системного и местного лечения OA при острой и хронической боли [1-4]. Основной механизм действия НПВС - способность к угнетению активности циклооксигеназы (ЦОГ), благодаря чему снижается биосинтез простагландинов и других медиаторов воспаления. ЦОГ-1 отвечает за синтез тромбоксана и простагландинов, которые регулируют физиологические функции; в частности, защиту слизистых оболочек, а ЦОГ-2 - преимущественно за синтез простагландинов, которые принимают участие в развитии воспалительного процесса и боли [4]. Ингибирование ЦОГ-1 ведет к развитию эрозивно-язвенных процессов в гастродуоденальной зоне [4]. Такой специфический синдром называется НПВС-гастродуоденопатия. Механизм поражения слизистой при применении НПВС осуществляется следующим образом: торможение синтеза простагландинов в слизистой уменьшает опосредованную простагландинами выработку защитной слизи и бикарбонатов, что приводит к появлению эрозий и язв, которые могут осложняться кровотечением или перфорацией. Среди НПВС наиболее выраженным ульцерогенным действием обладают неселективные ингибиторы ЦОГ, к которым, в частности, относятся индометацин, кеторолак, диклофенак, пироксикам и кетопрофен, оказывающие в то же время сильное противовоспалительное и обезболивающее действие [4]. Поэтому при OA перспективным является накожное применение лекарственных средств с неселективными НПВС, что обеспечивает их трансдермальное проникновение к воспаленному суставу и эффективное терапевтическое действие при низкой биодоступности, благодаря чему может снижаться частота и выраженность побочных эффектов [5-8]. При этом перпективным неселективным НПВС для симптоматического лечения OA является кетопрофен, который не оказывает хондротоксического действия [1].
Известен препарат Фастум® гель 2,5%, содержащий кетопрофен в концентрации 2,5% (сведения взяты из ИМП, опубликованной 21.12.2010). Этот препарат наиболее широко применяется для накожного применения при лечении OA [1, 2, 7, 8]. Однако данному препарату свойственен недостаток; он предназначен только для симптоматической терапии, связанной с уменьшением воспаления и боли, и не способствует восстановлению хрящевой ткани.
Известны препараты в форме гелей и кремов, содержащие хондропротекторы, например, Хондроксид® гель 5%, содержащий 5% хондроитин сульфата. Однако этому препарату свойственны недостатки, связанные с тем, что хондроитин сульфат имеет большую молекулярную массу 20000-30000 а.е.м., вследствие чего не может проникать через кожу и оказывать хондропротекторное действие при OA, так как оптимальная проницаемость связана с небольшой молекулярной массой менее 500 а.е.м. [9-11]. Известен препарат Хондроксид® Максимум крем 8%, содержащий 8% глюкозамина сульфата калия хлорида, имеющего низкую молекулярную массу, и применяемый для лечения OA. Однако этому препарату также свойственны недостатки; он предназначен для оказания только хондропротекторного действия и из-за отсутствия в его составе НПВС не обладает противовоспалительной и анальгетической активностью. В составе трансдермального препарата отсутствуют усилители проникновения, что разработчики попытались компенсировать большим содержанием хондропротектора.
В данный момент на территории РФ действует патент RU 2582278 (ЗАО «ФармФирма «Сотекс», 25.04.2013), защищающий трансдермальное средство для лечения и профилактики болезней суставов и мягких тканей, содержащее глюкозамин или его фармацевтически приемлемую соль, кетопрофен, N-метилпирролидон (усилитель проникновения), пропиленгликоль, антиоксидант для хондропротектора (лидокаин и лимонную кислоту), полимер для образования геля в кислой среде и эмульгаторы. Указанный патент выбран в качестве прототипа, поскольку описанное в нем средство содержит комбинацию хондропротектора глюкозамина и НПВС кетопрофена, которые находятся в фармацевтически приемлемой основе в растворенном состоянии, а основа обеспечивает их трансдермальный транспорт, благодаря N-метилпирролидону, с проявлением хондропротекторного, противовоспалительного и анальгетического действия в опытах in vivo.
Однако описанное в прототипе средство не удовлетворяет существующим требованиям к стабильности. Срок его хранения составляет всего около 1 года. Как показали исследования авторов настоящей заявки, в условиях более длительного хранения количество образовавшихся продуктов разложения кетопрофена и глюкозамина превышает допустимые пределы, а содержание кетопрофена и глюкозамина соответственно уменьшается ниже допустимых пределов, что не позволяет выпускать указанный препарат серийно как готовое лекарственное средство и резко ограничивает возможность его применения у больных OA только как экстемпорального лекарственного средства.
Задача настоящего изобретения - повышение стабильности и увеличение сроков хранения препарата, содержащего кетопрофен и глюкозамин в форме геля.
При создании такой композиции необходимо сбалансированно подобрать вспомогательные вещества и тип основы с учетом того, что кетопрофен и глюкозамина гидрохлорид обладают различными химическими и физико-химическими свойствами. Кетопрофен является органической кислотой, а глюкозамина гидрохлорид - солью органического основания. Глюкозамина гидрохлорид легко растворим в воде, а кетопрофен легко растворим в этаноле и практически не растворим в воде. Понижение температуры при хранении препарата должно предотвращать разложение глюкозамина, но при этом может происходить кристаллизация растворенного кетопрофена.
Поставленная задача решается посредством создания нового состава трансдермального средства для лечения и профилактики болезней суставов и мягких тканей, содержащего фармацевтически необходимое количество хондропротектора, нестероидного противовоспалительного средства, антиоксиданта для хондропротектора, гелеоюразователя, способного образовывать гелив кислой среде, смеси эмульгаторов 1 и 2 рода и смеси растворителей, где в качестве хондропротектора оно содержит глюкозамин или его фармацевтически приемлемую соль, в качестве нестероидного противовоспалительного средства - кетопрофен, отличающийся тем, что смесь растворителей содержит N-метилпирролидон (далее NMП), полиэтиленгликоль 400 (далее ПЭГ 400) и воду, а антиоксидант для хондропротектора представляет собой натрия метабисульфит, при этом рН среды находится в пределах от 3 до 2.
Техническим результатом заявленного изобретения является увеличение стабильности препарата, заключающееся в существенном снижении образования продуктов разложения глюкозамина и модификации кетопрофена, а также увеличении срока хранения, как минимум, до 2-х лет.
Краткое описание чертежей.
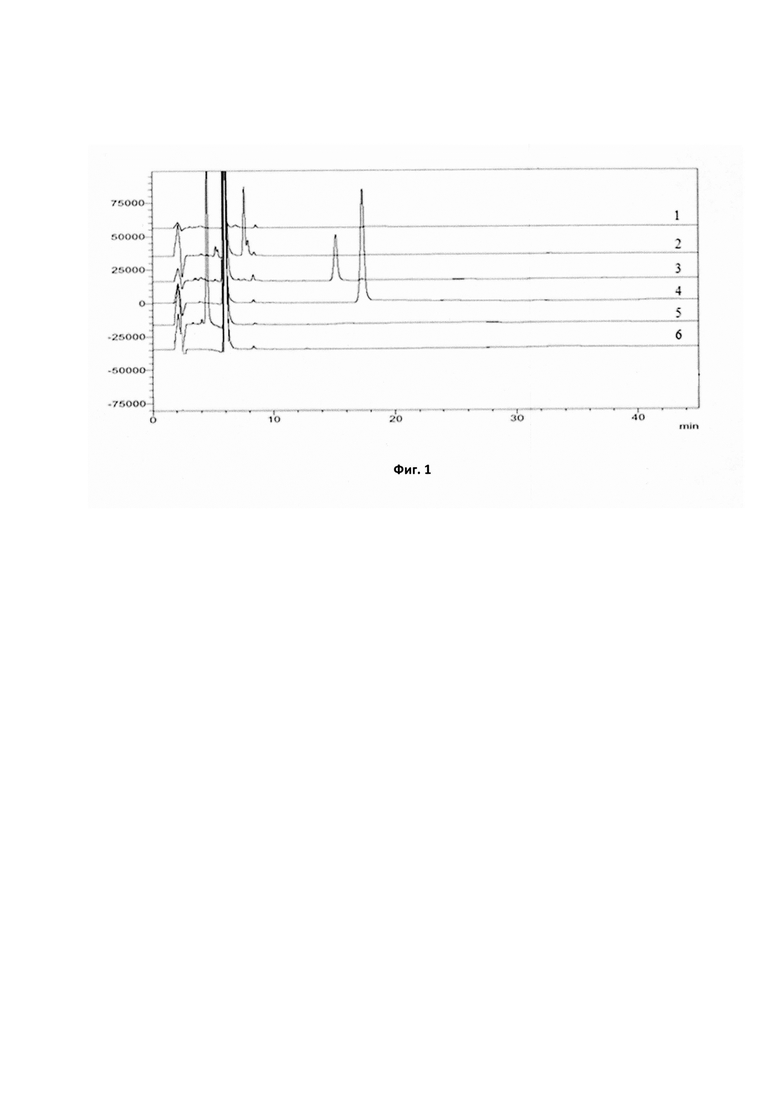
Фиг. 1 - Хроматограммы растворов кетопрофена 2,5% с рН 3,0, демонстрирующие образование примесей кетопрофена в стрессовых условиях при температуре 60°С после 12 недель хранения, со следующим составом растворителей (сверху вниз): 1) 50% N-метилпирролидона (NМП), 15% воды, 35% ПЭГ 400; 2) 50% NМП, 15% воды, 35% пропиленгликоля (ПГ); 3) 50% NMП, 15% воды, 35% диэтиленгликоля моноэтилового эфира (ДМЭ) (Transcutol® Р); 4) 50% NMП, 15% воды, 35% этанола (96%); 5) 65% NМП, 5% воды, 30% глицерина; 6) 85% NMП, 15% воды.
Фиг. 2 - УФ-спектры поглощения кетопрофена и примесей кетопрофена, образовавшихся в растворах с ПГ, этанолом и глицерином, снятые при хроматографировании растворов кетопрофена.
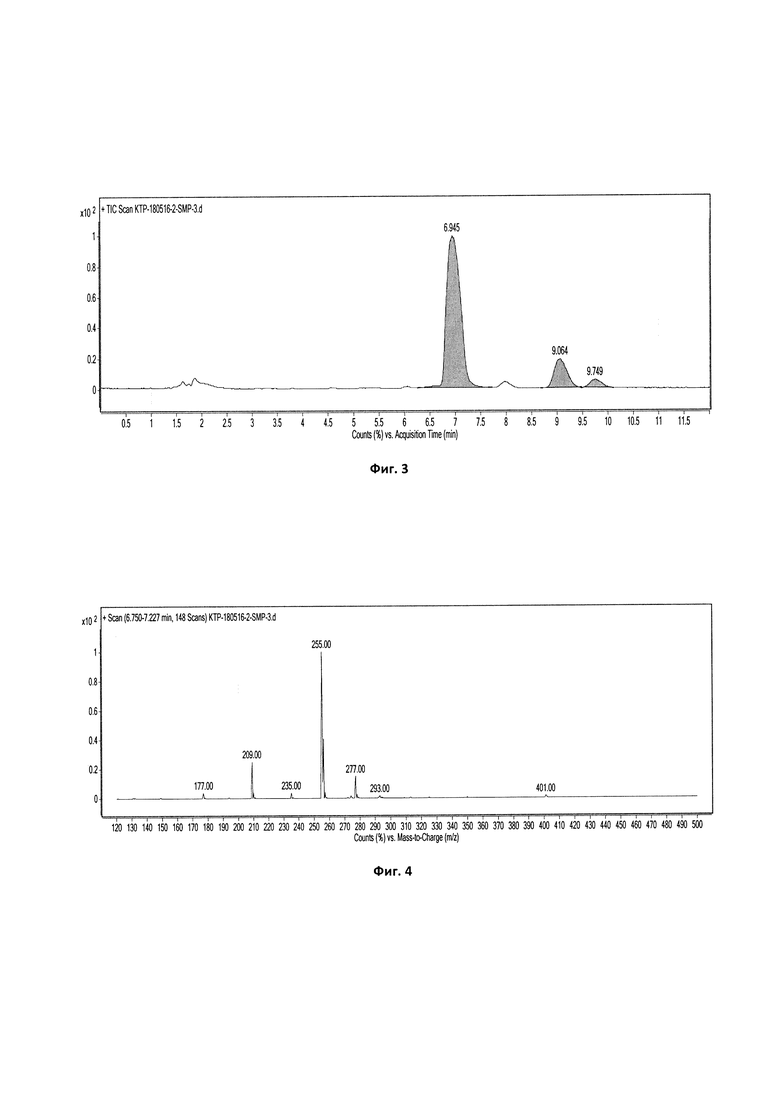
Фиг. 3 - Хроматограмма модельного раствора кетопрофена, содержащего ПГ, полученная в режиме сканирования масс в диапазоне 120-500 m/z, где пик со временем удерживания (Rt) 6,945 мин соответствует кетопрофену; пик с Rt=9,064 мин - кетопрофена ПГ эфиру, пик с Rt=9,749 мин - кетопрофена ПГ эфиру.
Фиг. 4 - Масс-спектр пика с Rt=6,945 мин (см. фиг. 3) с М.м.=254 а.е.м.
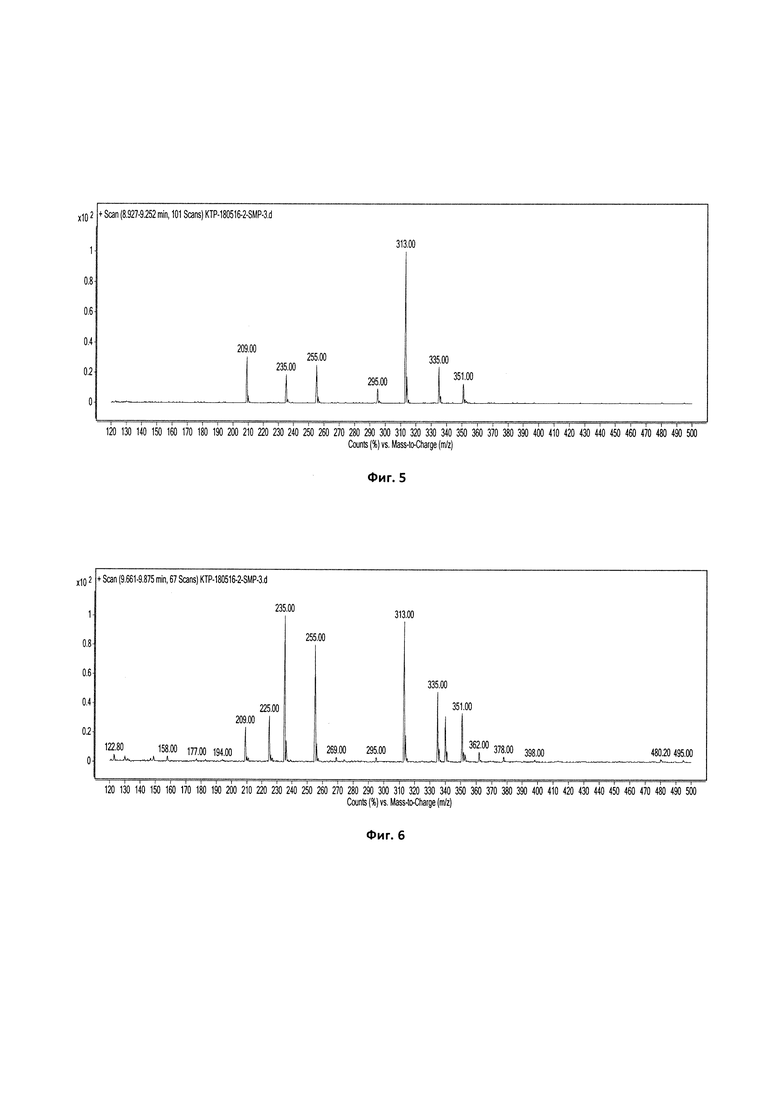
Фиг. 5 - Масс-спектр пика с Rt=9,064 мин (см. фиг. 3) с М.м.=313 а.е.м.
Фиг. 6 - Масс-спектр пика с Rt=9,749 мин (см. фиг. 3) с М.м.=313 а.е.м.
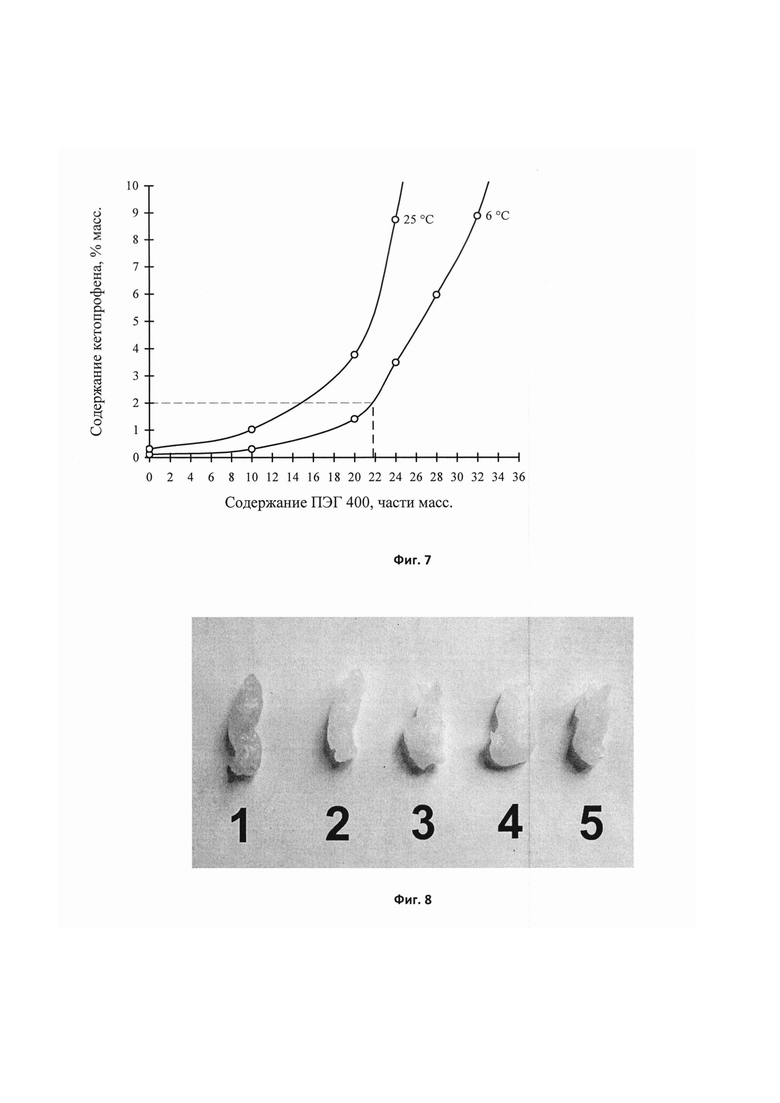
Фиг. 7 - Графики зависимостей растворимости кетопрофена в смешанных растворителях NMП - ПЭГ 400 - вода при температурах 6°С и 25°С от содержания ПЭГ 400 (при постоянном содержании NMП 18 масс. %).
Фиг. 8 - Фотографии лабораторных образцов препарата после хранения в течение 1 года при температуре 25°С и разном содержании натрия метабисульфита: 0% (препарат-прототип), 0,25%, 0,50%, 0,75%, 1,00%.
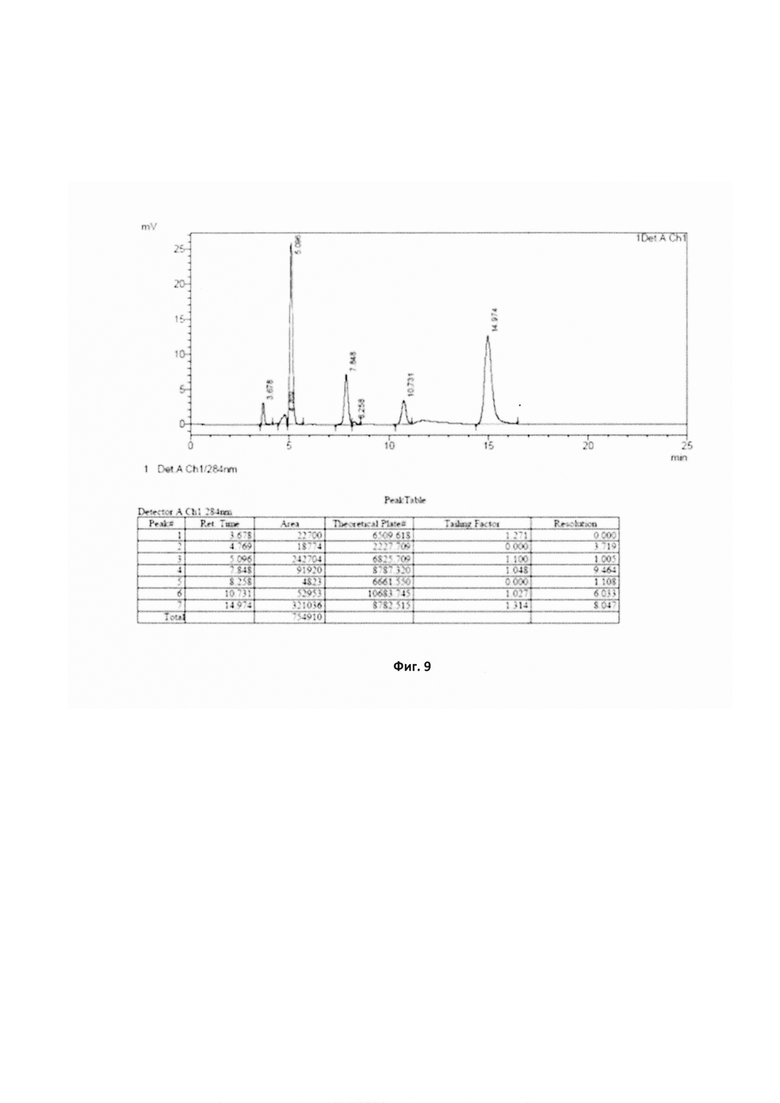
Фиг. 9 - Хроматограмма испытуемого раствора препарата-прототипа, полученная в условиях количественного определения примесей глюкозамина после хранения препарата-прототипа при температуре 25°С в течение 1 года, где пик с Rt=14,974 мин соответствует гидроксиметилфурфуролу (ГМФ), а пики со временами удерживания 3,678 мин, 4,769 мин, 5,096 мин, 7,848 мин, 8,258 мин и 10,731 мин - неидентифицированным продуктам разложения глюкозамина.
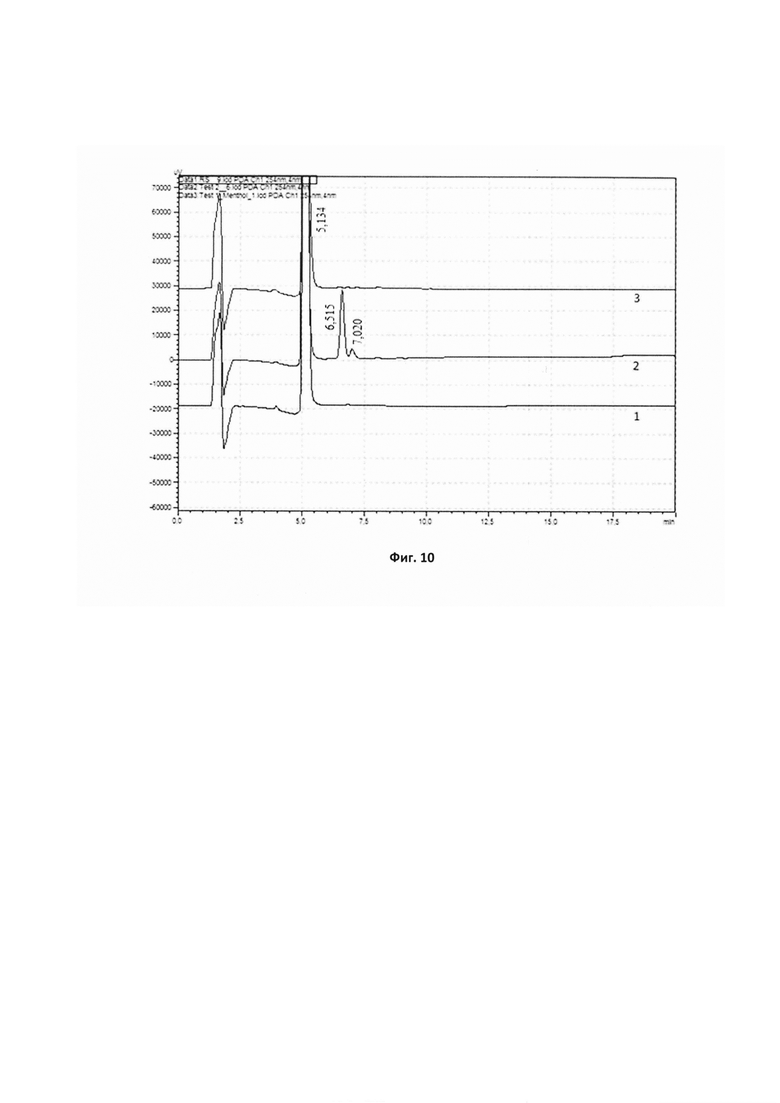
Фиг. 10 - Хроматограммы, полученные в условиях количественного определения примесей кетопрофена, где: 1) хроматограмма раствора сравнения, 2) хроматограмма испытуемого раствора препарата, содержащего ПГ и натрия метабисульфит, 3) хроматограмма испытуемого раствора препарата, содержащего ПЭГ 400 и натрия метабисульфит, после 6 месяцев хранения при температуре 25°С.
Примечание. Пики с Rt≈5,134 мин на хроматограммах 1, 2 и 3 соответствуют кетопрофену; пики с Rt=6,515 мин и Rt=7,020 мин на хроматограмме 2 соответствуют кетопрофена ПГ эфирам. На хроматорамме испытуемого раствора (1) пики посторонних примесей отсутствуют.
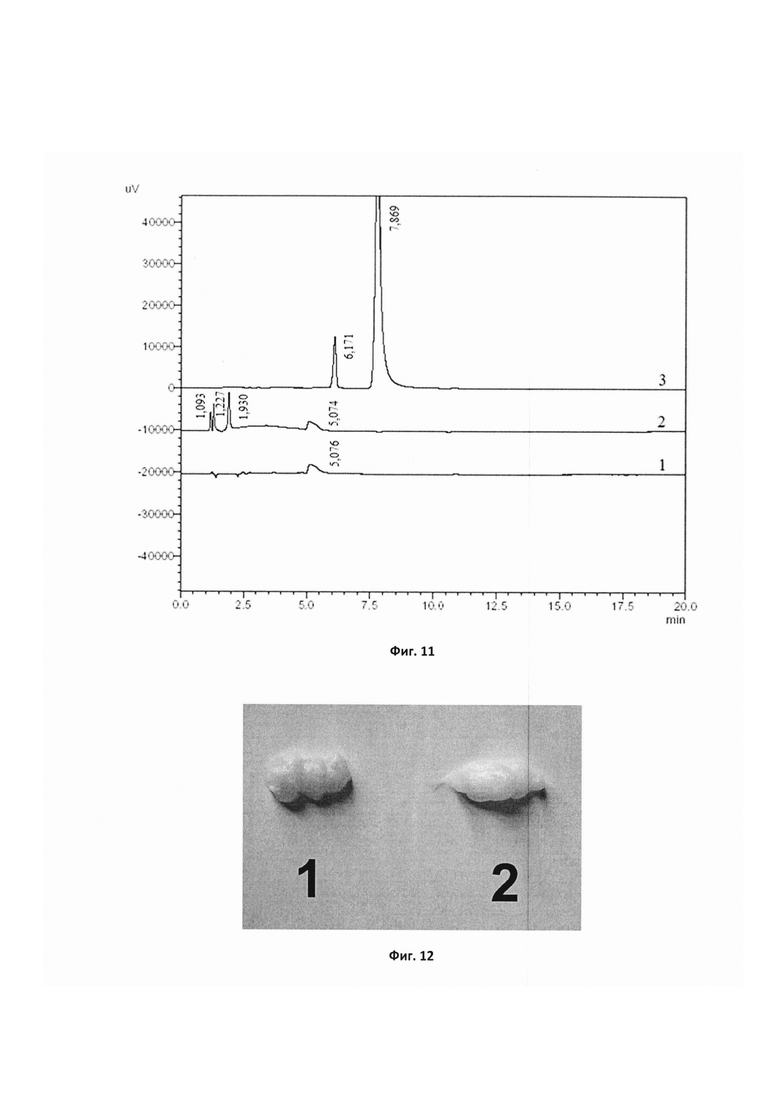
Фиг. 11 - Хроматограммы, полученные в условиях количественного определения примесей глюкозамина, где: 1) хроматограмма раствора плацебо; 2) хроматограмма испытуемого раствора препарата после 6 мес хранения при 25°С; 3) хроматограмма стандартного раствора, содержащего ГМФ и метилпиразин.
Примечание. Пики с Rt=5,076 мин и Rt=5,074 мин на хроматограммах 1 и 2 соответствуют основе препарата; пики с Rt=1,093 мин, Rt=1,227 мин и 1,930 мин на хроматограмме 2 соответствуют неидентифицированным примесям; пик с Rt=6,171 мин на хроматограмме стандартного раствора 3 соответствует ГМФ, а пик с Rt=7,869 мин - метилпиразину. На хроматорамме раствора (2) пик ГМФ отсутствует.
Фиг. 12 - Фотографии образцов препарата-прототипа (1) и препарата, содержащего ПЭГ 400 и натрия метабисульфит (2), после 1 года хранения при температуре 25°С.
Изучение взаимодействия кетопрофена с гидрофильными растворителями
Препарат кетопрофена в форме геля стандартизован в монографии «Ketoprofen Gel» Британской Фармакопеи. Так, в геле кетопрофена, в состав которого входит этиловый спирт, с установленными границами рН от 5,0 до 7,5 предлагается нормировать в качестве посторонних примесей кетопрофена этиловый эфир на уровне не более 4%. То есть, кетопрофен, являясь органической кислотой, образует в процессе хранения сложный эфир с этанолом. В композиции согласно прототипу содержится пропиленгликоль, который также содержит гидроксильные группы, а рН геля нормируется в пределах от 2,0 до 3,0. Поэтому было исследовано образование продуктов модификации кетопрофена в зависимости от состава смешанных растворителей и рН растворов при стрессовых условиях - температуре (60±2)°С. Предварительно была разработана методика количественного определения кетопрофена и проведена ее валидация. Разработанная методика соответствовала требованиям по следующим валидационным показателям: специфичность, правильность, линейность, прецизионность [12]. Также была разработана и валидирована методика количественного определения неидентифицированных примесей кетопрофена (по кетопрофену), которая также соответствовала определенным валидационным характеристикам [12].
Предварительно было установлено, что кетопрофен не образует продуктов модификации с N-метилпирролидоном (NMP), который использовали в составе всех экспериментальных образцов смешанных растворителей в концентрации 50 масс. % для растворения кетопрофена. Были приготовлены различные растворы, которые содержали 2,5% кетопрофена, растворенного в смешанных растворителях, содержащих 50% NMP, 15% воды и около 35% либо пропиленгликоля (ПГ), либо глицерина, либо этанола 96%, либо диэтиленгликоля моноэтилового эфира (ДМЭ, Transcutol® Р), либо ПЭГ 400. В качестве контрольного образца был приготовлен раствор, содержащий 2,5% кетопрофена, 85% NMP и 15% воды. Далее, в каждой тройной системе доводили рН раствора до 3,0; 5,0 или 7,0 при помощи либо фосфорной кислоты, либо калия гидроксида, после чего данные растворы выдерживали в течение 12 недель при температуре 60°С.
После проведения исходного анализа данных растворов на количественное содержание кетопрофена и количественное содержание посторонних примесей было обнаружено, что в процессе изготовления экспериментальных образцов растворов примеси кетопрофена не образуются. Примеси образовывались в процессе хранения растворов и при воздействии на них высокой температуры 60°С. Некоторые результаты анализов растворов кетопрофена после их хранения при температуре 60°С представлены в табл. 1.
Как видно из хроматограмм на фиг. 1, во всех растворах образовалась примесь кетопрофена A (Rt≈8,2 мин) в концентрациях от 0,78% до 0,92% (в среднем 0,87%) (табл. 1). Полученные результаты свидетельствуют, что образование кетопрофена примеси А не зависит от состава растворителей и рН растворов, а обусловлено воздействием на растворы кетопрофена стрессового фактора - высокой температуры 60°С. При хранении растворов при температуре 25°С кетопрофена примесь А не образовывалась.
В растворах, содержащих ПЭГ 400, ПГ, ДМЭ, этанол или глицерин, то есть растворители с гидроксильными группами, в процессе хранения при температуре 60°С образуются неидентифицированные примеси. Так, на хроматограммах растворов, содержащих ПГ или глицерин, обнаруживаются по два дополнительных пика, а в растворах с этанолом и ДМЭ - по одному пику (фиг. 1). В растворе с ПЭГ 400 примеси также образовались, однако в гораздо меньшем количестве (табл. 1). В контрольном растворе, содержащем NMП и воду, неидентифицированные примеси не обнаруживаются (фиг. 1, табл. 1).
В качестве примеров на фиг. 2 представлены полученные на хроматографе с диодно-матричным детектором УФ-спектры кетопрофена и примесей кетопрофена, образовавшихся при наличии в растворах ПГ, этанола или глицерина. Эти УФ-спектры идентичны и имеют максимум оптического поглощения при 255 нм, что свидетельствует о наличии одинаковой хромофорной группы. Очевидно, что образовавшиеся примеси являются производными кетопрофена.
Для идентификации указанных примесей были получены хроматограммы модельных растворов на хроматографе с масс-детектором, а также масс-спектры кетопрофена и примесей с определением их молекулярных масс (табл. 1). Пример хроматограммы представлен на фиг. 3, а примеры масс-спектров - на фиг. 4, 5 и 6.
Как следует из фиг. 3-6, масс-спектр пика с Rt=6,945 мин соответствует масс-спектру кетопрофена, а пики с Rt=9,064 мин и Rt=9,749 мин на хроматограмме, представленной на фиг. 3, принадлежат двум сложным эфирам кетопрофена и ПГ, которые имеют одинаковые молекулярные массы 312 а.е.м. В растворах кетопрофена, содержащих глицерин, также образуются два глицериновых эфира кетопрофена с одинаковыми молекулярными массами 329 а.е.м. Наличие двух пиков примесей в растворах кетопрофена с ПГ и глицерином могло быть связано либо с образованием сложных эфиров с разными энантиомерами кетопрофена, поскольку кетопрофен является рацематом, либо со взаимодействием молекул кетопрофена с разными гидроксигруппами растворителей. При использовании в растворах вместо рацемата (кетопрофена) одного энантиомера (декскетопрофена) на хроматограммах были также получены по два пика примесей, что свидетельствует об образовании сложных эфиров кетопрофена с разными гидроксигруппами ПГ или глицерина.
При наличии в растворе кетопрофена этанола образуется примесь с М.м.=282 а.е.м., что соответствует кетопрофена этиловому эфиру; при наличии ДМЭ (Transcutol® Р) - эфир ДМЭ и кетопрофена с М.м.=370 а.е.м. (табл. 1).
ПЭГ 400 является смесью полиэтиленгликолей, которые имеют разные молекулярные массы и содержат концевые гидроксильные группы. При хранении растворов кетопрофена при температуре 60°С образуются соответственно ПЭГ эфиры кетопрофена с разными молекулярными массами, которые на хроматограмме выходят в виде одного пика (фиг. 1).
Табл. 1 - Результаты анализов растворов кетопрофена после хранения при температуре 60°С
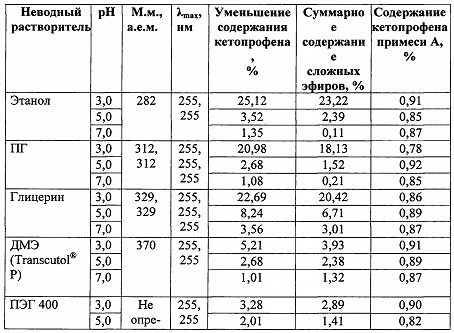

Падение концентрации кетопрофена в растворах в процессе хранения сопровождается увеличением содержания эфиров кетопрофена (табл. 1). По уменьшению содержания продуктов взаимодействия кетопрофена и гидрофильных растворителей последние можно расположить в ряду: этанол > глицерин > ПГ > ДМЭ > ПЭГ 400 > NMП. При этом NMП эфиров с кетопрофеном не образует.
Как следует из данных табл. 1, с уменьшением рН растворов увеличивается содержание эфиров кетопрофена с этанолом, ПГ, глицерином, ДМЭ и ПЭГ 400. При рН=7,0 уменьшение содержания кетопрофена несущественно, а образование эфиров отсутствует или минимально. При рН=5,0 падение содержания кетопрофена оказывается больше в среднем в 2,4 раза, и соответственно больше образуется эфиров кетопрофена. В растворах, имеющих рН=3,0 и содержащих этанол, ПГ и глицерин, содержание кетопрофена уменьшается на 21-25%, а содержание сложных эфиров возрастает до 18-23%. При рН=3,0 падение содержания кетопрофена и образование сложных эфиров оказываются наименьшими в случае ПЭГ 400. При этом падение содержания кетопрофена меньше зависит от рН, а содержание образовавшихся эфиров оказывается примерно в 6-10 раз меньше по сравнению с растворами, содержащими этанол, глицерин и ПГ. Можно прогнозировать, что образование эфиров кетопрофена с ПЭГ 400 при температуре 25°С окажется несущественным для стабильности препарата.
По результатам исследований для разработки геля кетопрофена, имеющего кислую среду, рационально в качестве растворителей использовать NMП, ПЭГ 400 и воду в соотношениях, оптимальных для растворения кетопрофена и глюкозамина гидрохлорида. То есть, вместо пропиленгликоля, использованного в составе препарата-прототипа, следует использовать ПЭГ 400.
Исследование растворимости кетопрофена и глюкозамина гидрохлорида в системе растворителей N-метилпирролидон - ПЭГ 400 - вода
В табл. 2 и на фиг. 7 показано влияние массового соотношения между ПЭГ 400 и водой (при постоянном содержании NMP 18 масс. %) на растворимость кетопрофена при температурах 6°С (условия холодильника) и 25°С (верхний предел температуры хранения).
Таблица 2 - Растворимость кетопрофена в смесях NMP (18 частей масс.) - ПЭГ 400 - вода, при температурах 6°С и 25°С при разных массовых соотношениях между ПЭГ 400 и водой
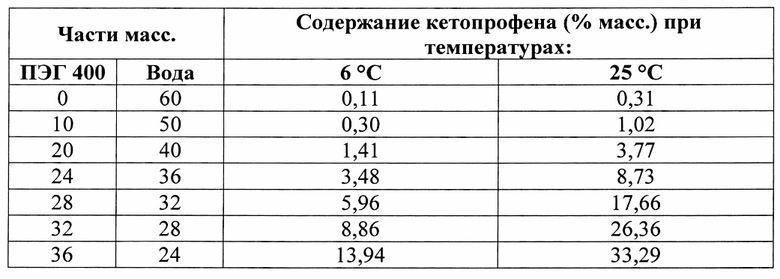
Как следует из данных, представленных в табл. 2 и на фиг. 7, 2 г кетопрофена растворяются в смешанном растворителе NMП - ПЭГ 400 -вода при температурах 6°С и 25°С, если содержание ПЭГ 400 составляет соответственно 22 г и 15 г. При постоянном содержании в смеси NMP 18 г растворимость гидрофобного вещества кетопрофена тем выше, чем больше содержание ПЭГ 400. Однако с увеличением содержания ПЭГ 400 уменьшается растворимость гидрофильного вещества глюкозамина гидрохлорида и возрастает риск его кристаллизации тем больше, чем ниже температура (табл. 3).
Таблица 3 - Кристаллизация кетопрофена и глюкозамина гидрохлорида при разных массовых соотношениях между ПЭГ 400 и водой и при разных температурах
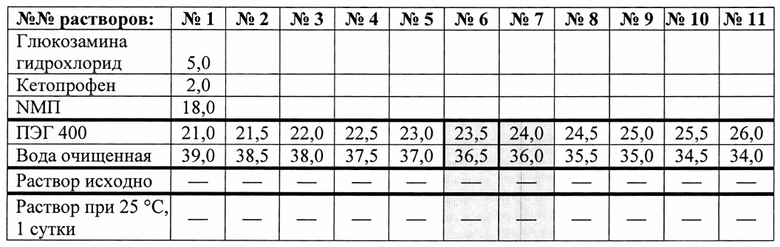
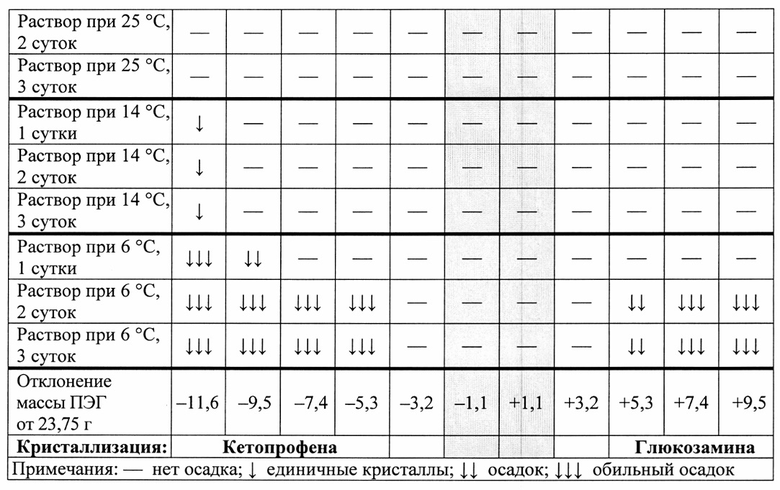
Как следует из табл. 3, оптимальным для растворимости обоих действующих веществ в дисперсионной среде геля является содержание ПЭГ 400 от 23,5 г до 24,0 г. При температурах 25°С и 14°С кетопрофен и глюкозамина гидрохлорид растворимы при содержании ПЭГ 400 приблизительно 23,75 г±10%. С понижением температуры растворимость уменьшается; при температуре 14°С единичные кристаллы кетопрофена появляются при содержании ПЭГ 400 21,0 г, а при температуре 6°С на вторые сутки хранения раствора обильный осадок кетопрофена образуется при содержании ПЭГ 400 22,5 г. При температуре 6°С осадок глюкозамина гидрохлорида образуется при содержании ПЭГ 400 25,0 г. С понижением температуры область массовых соотношений между ПЭГ 400 и водой, при которой имеют место стабильные растворы гидрофильного и гидрофобного действующих веществ сужается. При температуре 6°С кетопрофен и глюкозамина гидрохлорид растворимы при содержании ПЭГ 400 23,75 г±3,2%. То есть, существует риск, что при сдвиге массового соотношения между ПЭГ 400 и водой в ту или иную сторону и при низкой температуре в условиях холодильника произойдет кристаллизация одного из действующих веществ. Кристаллизация носит обратимый характер при повышении температуры, то есть при температуре 15-25°С выпавшие кристаллы растворяются. Однако, несмотря на это, оптимальным для хранения препарата следует считать температурный интервал от 15°С до 25°С, при котором обеспечивается физическая стабильность растворов действующих веществ.
Исследования стабильности препарата при новом составе растворителя и выбор нового состава антиоксидантов
В реакторе-гомогенизаторе была наработана опытная серия препарата с составом согласно прототипу. Серия препарата была расфасована в тубы по 30 г и заложена на хранение при температуре (25±2)°С.
Однако уже через 6-12 месяцев хранения стало очевидно, что при таком составе глюкозамина гидрохлорид нестабилен: препарат приобретал в процессе хранения желтый цвет (образец 1, фиг. 8), что было вызвано значительным накоплением продуктов разложения глюкозамина гидрохлорида, в частности, гидроксиметилфурфурола (ГМФ). Хроматограмма испытуемого раствора препарата-прототипа, демонстрирующая профиль образующихся продуктов разложения глюкозамина гидрохлорида, представлена на фиг. 9. Как видно из хроматограммы, представленной на фиг. 9, после 1 года хранения при температуре 25°С в препарате образуется ГМФ и еще 6 неидентифицированных примесей. Содержание ГМФ составило около 0,1%, что обусловило желтый цвет геля.
Для дальнейших исследований была изготовлена серия препарата согласно прототипу, в которой ПГ был заменен на ПЭГ 400. Однако кардинальных изменений относительно стабильности глюкозамина гидрохлорида и соответственно изменения цвета препарата при его хранении такая замена не принесла. В связи с этим потребовалось изменить систему антиоксидантов, состоящую из лидокаина гидрохлорида, лимонной кислоты моногидрата и бутилгидроксианизола (как в прототипе), на более эффективный антиоксидант.
В качестве нового антиоксиданта был выбран натрия метабисульфит, который, с одной стороны, обеспечивает антиоксидантное действие, а, с другой стороны, создает кислую среду, необходимую для стабилизации глюкозамина гидрохлорида (табл. 4). Оптимальное содержание натрия метабисульфита, при котором препарат имел белый цвет (образец 2, фиг. 8) и сохранял его в процессе хранения, а гели имели рН от 2,35 до 3,02, находится в пределах от 0,2% до 0,3% (табл. 4). При более высоком содержании натрия метабисульфита рН гелей был выше 3,0, а гели приобретали лимонно-желтый цвет, свидетельствующий об образовании примеси ГМФ (образцы 3, 4 и 5, фиг. 8).
Таблица 4 - Составы (в процентах) некоторых экспериментальных образцов препарата с ПЭГ 400 и натрия метабисульфитом
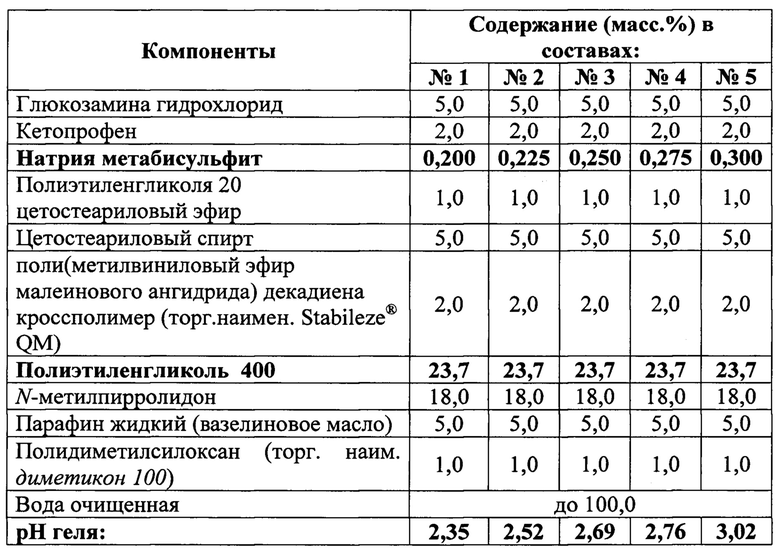
В реакторе-гомогенизаторе была наработана опытная серия препарата массой 3 кг, в которой ПГ был заменен на ПЭГ 400, а лидокаина гидрохлорид, лимонная кислота моногидрат и бутилгидроксианизол - на натрия метабисульфит (табл. 5). Препарат был расфасован в тубы по 30 г и заложен на хранение при (25±2)°С.
Таблица 5 - Состав наработанного препарата
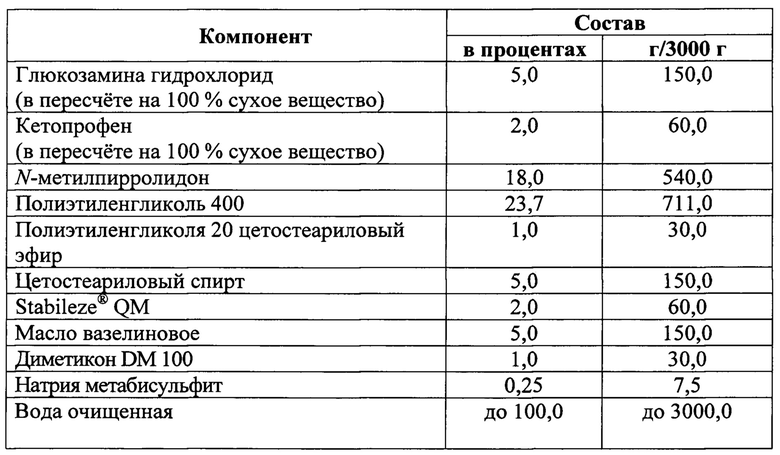
Параллельно была наработана опытная серия препарата, которая вместо ПЭГ 400 содержала ПГ. Образцы двух серий препарата после их хранения в течение 6 месяцев при температуре 25°С были проанализированы на содержание продуктов модификации кетопрофена. Хроматограммы представлены на фиг. 10. Как следует из хроматограмм, представленных на фиг. 10, в препарате, содержащем ПГ, уже после 6 месяцев хранения при температуре 25°С образовались два эфира кетопрофена и ПГ, которые соответствуют пикам с Rt=6,515 мин и Rt=7,020 мин (фиг. 10); суммарное содержание этих ПГ эфиров кетопрофена составило 2,363%. На хроматорамме испытуемого раствора препарата (1) (фиг. 10), содержащего ПЭГ 400 и натрия метабисульфит, пики посторонних примесей отсутствовали.
Как следует из данных, представленных на фиг. 9 и фиг. 11, замена антиоксидантов, использованных в препарате-прототипе, на 0,25% натрия метабисульфита приводит к изменению профиля примесей, образующихся при хранении препарата при температуре 25°С. На хроматограмме испытуемого раствора препарата с натрия метабисульфитом, хранившегося 6 месяцев, отсутствует пик ГМФ, а количество неидентифицируемых примесей с шести сокращается до трех (фиг. 11). Одна из примесей является производным метилпиразина, характеризуется относительным временем удерживания (относительно метилпиразина) около 0,25, а ее накопление характеризует процесс разложения глюкозамина гидрохлорида. Если препарат-прототип из-за образования ГМФ при хранении быстро приобретает желтый цвет (образец 1, фиг. 12), то препарат, содержащий 0,25% натрия метабисульфита, сохраняет белый цвет (образец 2, фиг. 12) или при длительном хранении приобретает лишь едва заметный желтоватый оттенок вследствие образования незначительных количеств ГМФ. В препарате-прототипе количество образующегося ГМФ оказывается приблизительно в 10 раз больше.
Результаты анализов образцов серии препарата, содержащего натрия метабисульфит и ПЭГ 400, представлены в табл. 6.
Таблица 6 - Результаты анализов препарата в процессе хранения при (25±2)°С
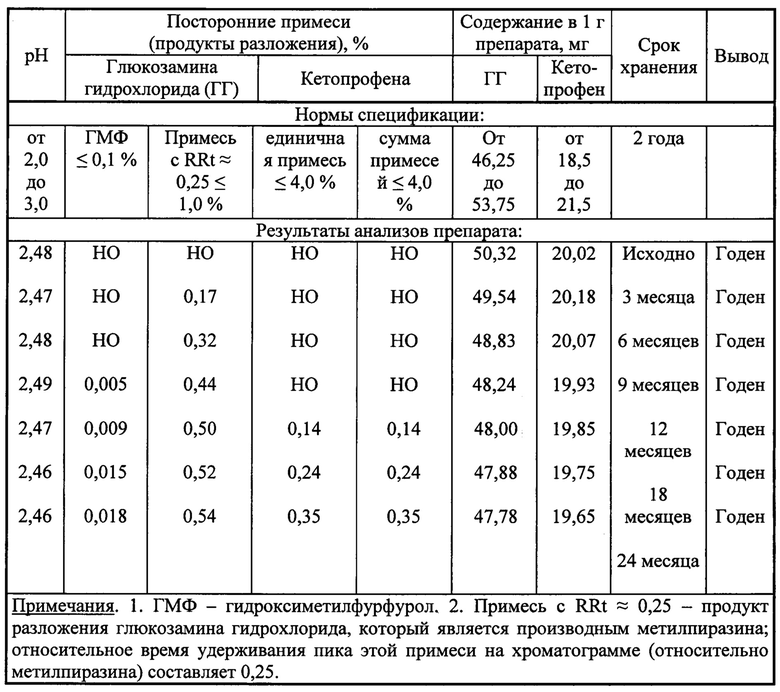
Как следует из данных анализов, представленных в табл. 6, препарат в течение двух лет сохраняет стабильность по критическим показателям качества. Тенденции к увеличению содержания посторонних примесей и уменьшению содержания действующих веществ находятся в пределах, установленных в спецификации. Препарат-прототип не соответствовал требованиям спецификации по содержанию примесей и действующих веществ (глюкозамина гидрохлорида и кетопрофена) уже после 1 года хранения.
Таким образом, трансдермальное средство согласно настоящему изобретению обладает повышенной стабильностью, а также более продолжительным сроком годности (не менее двух лет).
Способ получения трансдермального состава согласно заявленному изобретению
Стадия 1. Приготовление основы геля
В вакуумный реактор-гомогенизатор №1 последовательно загружают предварительно отвешенные ПЭГ 400 и Stabilese® QM. Загрузка Stabilese® QM проводится порциями (4-5 порций), между загрузками смесь перемешивают при помощи лопастной мешалки со скребками с частотой вращения около 30-60 об/мин и турбинной мешалки с частотой вращения 1500-3000 об/мин в течение 5-10 мин. По окончании загрузки последней порции Stabilese® QM смесь перемешивают при помощи лопастной мешалки с частотой вращения около 30-60 об/мин и турбинной мешалки с частотой вращения 1500-3000 об/мин в течение 10-20 мин до получения однородной дисперсии.
В вакуумный реактор-гомогенизатор №1 с дисперсией Stabilese® QM загружают предварительно отвешенные на весах спирт цетостеариловый и полиэтиленгликоля 20 цетостеариловый эфир, включают нагрев и при перемешивании при помощи лопастной мешалки при частоте вращения 30-60 об/мин смесь нагревают до температуры (65±5)°С. По достижении этой температуры включают мешалки и смесь перемешивают при помощи лопастной мешалки со скребками с частотой вращения 30-60 об/мин и турбинной мешалки с частотой вращения 1500-3000 об/мин в течение 10-15 мин до получения однородной дисперсии. Затем включают охлаждение, и смесь перемешивают при помощи лопастной мешалки со скребками с частотой вращения около 30-60 об/мин до температуры (50±2)°С.
Стадия 2. Приготовление раствора кетопрофена
В емкость №2 загружают предварительно отвешенные на весах кетопрофен и N-метилпиролидон. При необходимости смесь нагревают до температуры 25-35°С и перемешивают с помощью мешалки до полного растворения кетопрофена.
Стадия 3. Приготовление водного раствора
В реактор №3 последовательно загружают предварительно отвешенные на весах воду очищенную, глюкозамина гидрохлорид и натрия метабисульфит. При необходимости смесь нагревают до температуры 25-35°С и перемешивают с помощью мешалки до полного растворения всех компонентов. В настоящем способе глюкозамин и/или кетопрофен и/или N-метилпиролидон и/или полиэтиленгликоль 400 и/или натрия метабисульфит находятся в виде истинных растворов.
Стадия 4. Приготовление геля
В реактор-гомогенизатор №1 при включенной лопастной мешалке со скребками загружают раствор кетопрофена со стадии 2. Затем в реактор-гомогенизатор №1 загружают предварительно взвешенные на весах масло вазелиновое и диметикон 100. В реакторе-гомогенизаторе №1 создают вакуум глубиной от -0,05 МПа до -0,07 МПа и перемешивают массу с помощью лопастной мешалки со скребками с частотой вращения 30-60 об/мин в течение 10-20 минут с одновременным охлаждением до температуры 35-37°С.
В реактор-гомогенизатор №1 порциями в 4-5 приемов загружают водный раствор со стадии 3 при включенной лопастной мешалке со скребками с частотой вращения 30-60 об/мин. По окончании загрузки водного раствора создают вакуум глубиной от -0,05 МПа до -0,07 МПа и перемешивают массу с помощью лопастной мешалки со скребками с частотой вращения 30-60 об/мин и турбинной мешалки с частотой вращения 1500-3000 об/мин в течение 10-15 мин до получения однородной дисперсии в течение 10-25 минут. При необходимости массу в реакторе-гомогенизаторе №1 охлаждают, чтобы температура не превышала 37-38°С.
Затем включают охлаждение, и гель охлаждают до температуры 20-25°С при перемешивании лопастной мешалкой со скребками с частотой вращения 30-60 об/мин. По окончании перемешивания при необходимости в реакторе-гомогенизаторе №1 создают вакуум глубиной от -0,05 МПа до -0,06 МПа и гель выдерживают без перемешивания в течение 1 часа для дегазации.
После получения положительных результатов анализа нерасфасованный гель выгружают из реактора-гомогенизатора №1 в промежуточную емкость для транспортирования, которую герметично закрывают.
Стадия 5. Дозирование геля в тубы
В промежуточной емкости гель транспортируют в помещение для фасования и выгружают частями в бункер тубонаполнительного автомата. Гель дозируют по 30 г или 50 г в тубы. Температура воздуха в производственном помещении при фасовании геля в тубы должна находиться в пределах от 18°С до 25°С. Заполненные тубы зафальцовывают; при этом на тубу наносится оттиск с указанием серии и срока годности.
Стадия 6. Упаковка туб в пачки
Каждую тубу вместе с инструкцией по медицинскому применению упаковывают в пачку.
Стадия 7. Упаковка пачек в коробки
Пачки с тубами упаковывают в групповую упаковку (коробки). Коробки закрывают и наклеивают на каждую из них групповую этикетку.
Исследования фармакологической активности
Далее проводили сравнительные исследования специфического фармакологического действия лекарственного средства нового состава. Сравнение проводили между препаратом, содержащим 2% кетопрофена, ПЭГ 400 и натрия метабисульфит (образец №1, см. табл. 5) и представленным на рынке препаратом Фастум® гель, содержащим 2,5% кетопрофена (образец №2).
Исследования проведены на 32 крысах массой 150-190 г (в среднем 175 г). Во время эксперимента животные находились в виварии при 18-25°С, влажности 50-60%, естественном световом режиме «день-ночь», в стандартных пластиковых клетках, на стандартном пищевом рационе [13].
Образцы №1 и №2 наносили на кожу стопы крыс до голеностопного сустава в количестве 100 мг, дважды: за 30 мин до и непосредственно после инъекции флогогенного агента. Суммарное количество препарата, наносимое на крысу, составило 200 мг, что с учетом средней массы крыс (175 г) соответствовало 1,1 г/кг (в расчете по лекарственной форме). Выбор дозы проводили экспериментально путем определения количества образцов сравниваемых препаратов, необходимого для их нанесения тонким слоем на всю поверхность голеностопа.
Экссудативный воспалительный отек вызывали через 30 мин после первого нанесения сравниваемых препаратов субплантарной инъекцией в правую заднюю стопу крыс 0,08 мл 0,5% водного раствора каррагенина [14].
Противовоспалительный эффект (ПЭ) оценивали по степени ингибирования прироста отека стопы на фоне применения препаратов по сравнению с контролем - группой нелеченых животных. Объем стопы измеряли до (исходно) и затем через 1, 3 и 5 ч после инъекции флогистика на электронном плетизмометре (мод. 7150, «Уго Базиле», Италия). ПЭ рассчитывали по формуле:
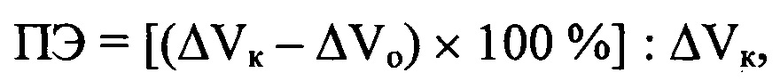
где ΔVк и ΔVо - средний прирост объема отечной стопы в контрольной и опытной группах соответственно.
Порог болевой чувствительности (ПБЧ) регистрировали через 3 ч после инъекции флогистика методом Рендалл-Селитто при механическом болевом раздражении на анальгезиметре («Уго Базиле», Италия; мод. 7200). Анальгетический эффект (АЭ) рассчитывали по увеличению ПБЧ у крыс, которым наносили сравниваемые препараты, сравнительно с контрольными нелечеными животными, рассчитывая его по формуле:
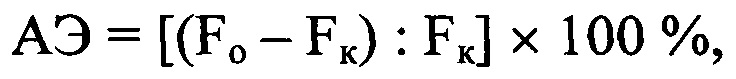
где Fо и Fк - пороговая сила давления на стопу (г) в опытных и контрольной группах, соответственно.
Статистическую обработку результатов проводили общепринятыми в фармакологии методами, рассчитывая средние значения показателей 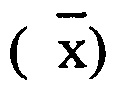 и стандартную ошибку
и стандартную ошибку 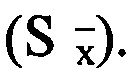 Достоверность различий между средними определяли по t критерию Стьюдента. Вероятность полученных результатов оценивали на уровне значимости не менее 95% (р<0,05) [15, 16]. Результаты исследования
Достоверность различий между средними определяли по t критерию Стьюдента. Вероятность полученных результатов оценивали на уровне значимости не менее 95% (р<0,05) [15, 16]. Результаты исследования
Результаты исследования противовоспалительной и анальгетической активности представлены в табл. 7.
Таблица 7 - Противовоспалительный и анальгетический эффекты образцов №1 и №2 у крыс с каррагениновым воспалением стопы
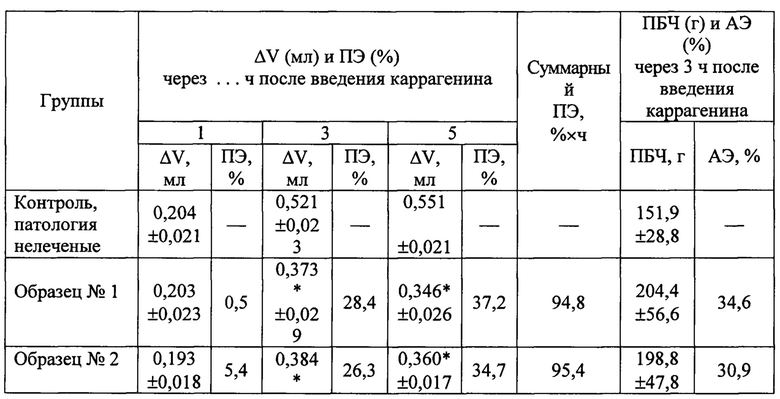

Примечания. 1. Препараты наносили накожно двукратно (за 30 мин до и непосредственно после инъекции флогистика) в суммарной дозе 200 мг/животное;
2. ΔV, мл - прирост объема воспаленной стопы крыс;
3. ПЭ, % - противовоспалительный эффект;
4. ПБЧ, г - порог болевой чувствительности воспаленной стопы крыс;
5. АЭ, % - анальгетический эффект;
6. * - р<0,05 сравнительно с контролем;
7. Число животных в группе = 8.
Субплантарная инъекция раствора каррагенина приводит к развитию острого воспалительного экссудативного отека, который у нелеченых крыс достигает максимума к 3 ч. При этом в первые 10-20 мин происходит дегрануляция тучных клеток и высвобождение гистамина и серотонина, в течение 1-2 ч развитие отека поддерживается накапливающимися в очаге воспаления брадикинином и другими кининами, к 3 ч - простагландинами [17]. Таким образом, в первые 3 часа в патогенез каррагенинового воспаления включаются все основные медиаторы боли и воспаления, на которые направлено действие изучаемых препаратов.
Противовоспалительная активность
Двукратное накожное нанесение образца №1 (препарат с содержанием кетопрофена 2,0% согласно настоящему изобретению) и образца №2 (препарат Фастум® гель с содержание кетопрофена 2,5%) оказывает противовоспалительный эффект, состоящий в уменьшении прироста объема воспаленной стопы крыс сравнительно с нелеченым контролем (табл. 7). К 3 ч прирост объема воспаленной стопы в группах леченых крыс достигал достоверных различий с нелеченым контролем. ПЭ сравниваемых препаратов достоверно проявлялся к 3 ч после введения каррагенина, составив для образца №1 - 28,4%, а для образца №2 - 26,3%. К 5 ч выраженность противовоспалительного эффекта препаратов возрастала, составив соответственно: 37,2% и 34,7% (табл. 7). Суммарные противовоспалительные эффекты обоих препаратов были практически идентичны.
Анальгетическая активность
Двукратная аппликация образцов №1 и №2 оказывает также анальгетическое действие, состоящее в возрастании порога болевой чувствительности (ПБЧ) воспаленной стопы крыс при ее механическом сдавливании (табл. 7). Анальгетические эффекты препаратов были сопоставимы, однако анальгетический эффект образца №1 (34,6%) несколько превышал анальгетический эффект образца №2 (30,9%).
Исследования показали, что состав по настоящему изобретению обеспечивает противовоспалительный эффект и анальгетический эффект, сопоставимые с аналогичными эффектами препарата Фастум® гель при уменьшенном на 20% содержании кетопрофена. В свою очередь, сниженная концентрация кетопрофена позволит также снизить риск возникновения ульцерогенного эффекта.
Список литературы
1. Остеоартроз: консервативная терапия: монография / Н.А. Корж и др.; под ред. Н.А. Коржа, Н.В. Дедух, И.А. Зупанца. Харьков: Золотые страницы, 2007. 424 с.
2. Коваленко В.Н., Борткевич О.П. Остеоартроз. Практическое руководство. Киев: Морион, 2005. 448 с.
3. Analgesics for Osteoarthritis: An Update of the 2006. Comparative Effectiveness Reviews / R. Chou, M.S. McDonagh, E. Nakamoto et al. Rockville (MD): Agency for Healthcare Research and Quality (US). 2011. Vol. 38. P. 1-148.
4. Боль и проблема безопасности НПВС: монография / А.В. Курята, Т.К. Лысунец, А.В. Зайченко, А.В. Черкасова. Днепропетровск: Герда, 2014. 84 с.
5. Herndon С.М. Topical delivery of nonsteroidal anti-inflammatory drugs for osteoarthritis J. Pain Palliat. Care Pharmacother. 2012. 26 (1). P. 18-23.
6. Barkin R.L. The pharmacology of topical analgesics. Postgrad Med. 2013. Jul; 125(4 Suppl. 1). P. 7-18.
7. Barthel H.R., Axford-Gatley R.A. Topical nonsteroidal antiinflammatory drugs for osteoarthritis. Postgrad Med. 2010. Nov; 122(6). P. 98-106.
8. Artman R.D., Barthel H.R. Topical therapies for osteoarthritis. Drugs. 2011. Jul 9; 71(10). P. 1259-1279.
9. Drug Delivery Across Physiological Barriers / Ed. Silvia Muro. Pan Stanford Reference, 2016. 426 p.
10. Alkilani A.Z., McCrudden M.T.C., Donelly R.F. Transdermal Drug Delivery: Innovative Pharmaceutical Developments Based on Disruption of the Barrier Properties of the Stratum Corneum. Pharmaceutics. 2015. №7. p. 438-470.
11. Topical and Transdermal Drug Delivery: Principles and Practice / Ed. Benson H.A., Watkinson A.C. Wiley: Hoboken, NJ, USA, 2012. 464 p.
12. Руководство по валидации методик анализа лекарственных средств / Под ред. Н.В. Юргеля, А.Л. Младенцева, А.В. Бурдейна и др.; Разработчики В.Л. Багирова, А.И. Гризодуб, Т.Х. Чибиляев и др. - М.: Фармацевтическая промышленность, 2007. - 58 с.
13.  з утримання лабораторних тварин та роботи з ними /
з утримання лабораторних тварин та роботи з ними /  О.С. Хромов,
О.С. Хромов, 
 2002. - 156 с.
2002. - 156 с.
14. Ferreira S.H. Prostaglandin hyperalgesia and the control of inflammatory pain // In: The pharmacology of inflammation / Ed. I.L. Bonta, M.A. Bray, M.J. Parnham. - Amsterdam, New York, Oxford, 1985. - P. 107-116.
15. Урбах В.Ю. Статистический анализ в биологических и медицинских исследованиях. - М.: Медицина, 1975. - 295 с.
16. Лапач С.Н., Чубенко А.В., Бабич П.Н. Статистические методы в биологических исследованиях с использованием Excel. - К.: Морион, 2000. - 320 с.
17. Тринус Ф.П., Мохорт Н.А., Клебанов Б.М. Нестероидные противовоспалительные средства. - Киев, 1975. - С. 208-209.
| название | год | авторы | номер документа |
|---|---|---|---|
| ТРАНСДЕРМАЛЬНОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ БОЛЕЗНЕЙ СУСТАВОВ И МЯГКИХ ТКАНЕЙ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И КОМБИНИРОВАННЫЙ ТРАНСДЕРМАЛЬНЫЙ ПРЕПАРАТ ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ БОЛЕЗНЕЙ СУСТАВОВ И МЯГКИХ ТКАНЕЙ | 2013 |
|
RU2582278C2 |
| КОМБИНИРОВАННАЯ АКТИВНАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ ОПОРНО-ДВИГАТЕЛЬНОГО АППАРАТА | 2015 |
|
RU2582974C1 |
| НАРУЖНОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ СУСТАВОВ И МЯГКИХ ТКАНЕЙ | 2007 |
|
RU2377974C2 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНЕЙ СУСТАВОВ | 2004 |
|
RU2259204C1 |
| ЛЕКАРСТВЕННАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНЕЙ СУСТАВОВ (ВАРИАНТЫ) | 2009 |
|
RU2408380C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНЕЙ СУСТАВОВ | 2004 |
|
RU2260432C1 |
| Препарат для симптоматической терапии заболеваний опорно-двигательного аппарата и способ его получения | 2016 |
|
RU2614958C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ДЕГЕНЕРАТИВНЫХ ПРОЦЕССОВ ОПОРНО-ДВИГАТЕЛЬНОГО АППАРАТА | 2024 |
|
RU2827071C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ АРТРОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ В ЛИОФИЛИЗИРОВАННОЙ ФОРМЕ ДЛЯ ИНЪЕКЦИЙ | 2024 |
|
RU2827073C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ХОНДРОИТИН СУЛЬФАТ И/ИЛИ ГИАЛУРОНИДАЗУ И ЛИПОСОМЫ ДЛЯ МЕСТНОГО ПРИМЕНЕНИЯ | 2010 |
|
RU2473350C2 |

Изобретение относится к области медицины и химико-фармацевтической промышленности, а именно к трансдермальному средству для лечения и профилактики болезней суставов и мягких тканей, содержащему фармацевтически необходимое количество хондропротектора, нестероидного противовоспалительного средства, антиоксиданта для хондропротектора, гелеобразователя, способного образовывать гели в кислой среде, смеси неионогенных эмульгаторов 1 и 2 рода и смеси растворителей, где в качестве хондропротектора оно содержит глюкозамин или его фармацевтически приемлемую соль, в качестве нестероидного противовоспалительного средства - кетопрофен, отличающемуся тем, что смесь растворителей содержит N-метилпирролидон, полиэтиленгликоль 400 и воду, а антиоксидант для хондропротектора представляет собой натрия метабисульфит, при этом рН среды находится в пределах от 3 до 2. Изобретение обеспечивает увеличение стабильности препарата, заключающееся в существенном снижении образования продуктов разложения глюкозамина и модификации кетопрофена, а также увеличение срока хранения как минимум до 2-х лет. 5 з.п. ф-лы, 7 табл., 12 ил.
1. Трансдермальное средство для лечения и профилактики болезней суставов и мягких тканей, содержащее фармацевтически необходимое количество хондропротектора, нестероидного противовоспалительного средства, антиоксиданта для хондропротектора, гелеобразователя, способного образовывать гели в кислой среде, смеси неионогенных эмульгаторов 1 и 2 рода и смеси растворителей, где в качестве хондропротектора оно содержит глюкозамин или его фармацевтически приемлемую соль, в качестве нестероидного противовоспалительного средства - кетопрофен, отличающееся тем, что смесь растворителей содержит N-метилпирролидон, полиэтиленгликоль 400 и воду, а антиоксидант для хондропротектора представляет собой натрия метабисульфит, при этом рН среды находится в пределах от 3 до 2.
2. Трансдермальное средство по п. 1, отличающееся тем, что в качестве смеси неионогенных эмульгаторов оно содержит смесь цетостеарилового спирта и полиэтиленгликоля 20 цетостеарилового эфира.
3. Трансдермальное средство по п. 2, отличающееся тем, что в качестве гелеобразователя, способного образовывать гели в кислой среде, оно содержит поли(метилвиниловый эфир малеинового ангидрида) декадиена кроссполимер.
4. Трансдермальное средство по пп. 1-3, отличающееся тем, что дополнительно оно содержит эмольент в виде парафина жидкого и полидиметилсилоксана или в виде жирного масла или другого липофильного эмольента.
5. Трансдермальное средство по п. 4, характеризующееся следующим составом, мас.%:
6. Трансдермальное средство по п. 5, характеризующееся следующим составом, мас.%:
| ТРАНСДЕРМАЛЬНОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ БОЛЕЗНЕЙ СУСТАВОВ И МЯГКИХ ТКАНЕЙ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И КОМБИНИРОВАННЫЙ ТРАНСДЕРМАЛЬНЫЙ ПРЕПАРАТ ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ БОЛЕЗНЕЙ СУСТАВОВ И МЯГКИХ ТКАНЕЙ | 2013 |
|
RU2582278C2 |
| WO 2005116086 A1, 08.12.2005. | |||
Авторы
Даты
2019-04-18—Публикация
2018-06-22—Подача