Изобретение относится к химико-фармацевтической промышленности, а именно к средствам наружного применения для лечения дегенеративно-дистрофических заболеваний суставов и мягких тканей.
Проблема лечения болезней суставов (артрозы, артриты, артрозо-артриты, остеоартрозы (ОА) и остеохондрозы) в настоящее время чрезвычайно актуальна. Важность ее подтверждает проведение под эгидой ВОЗ Международной декады, посвященной костно-суставным заболеваниям в 2000-2010 гг.
У лиц пожилого возраста ОА - наиболее частая причина болевого синдрома и инвалидизации. В странах Запада в структуре заболеваемости они занимают 4 место у женщин и 8 у мужчин [1]. В России болезни опорно-двигательного аппарата занимают второе место по количеству дней и третье место по случаям временной нетрудоспособности среди всех классов болезней.
В основе патогенеза ОА лежит деполимеризация белково-полисахаридных комплексов внеклеточного матрикса, которая приводит к появлению трещин, эрозий и деструкции хряща. Соли кальция, откладывающиеся в окружающих тканях в виде оссификатов, в свою очередь, дополнительно травмируют сустав, усиливая воспаление и боль.
Лечение проводят нестероидными противовоспалительными средствами (НПВС): неселективными ингибиторами циклооксигеназ-1 и 2 (ЦОГ-1 и ЦОГ-2) (ибупрофен, диклофенак, бутадион и т.д.) или селективными ингибиторами ЦОГ-2 коксибами (целебрекс).
Однако в основном механизме терапевтического действия НПВС заложен и механизм их главного побочного эффекта. Препараты этого класса ингибируют синтез специфических простагландинов в слизистой оболочке желудочно-кишечного тракта, обладающих протекторным действием, что ведет к образованию пептических эрозивно-язвенных повреждений желудка и двенадцатиперстной кишки, которые, по данным эндоскопических исследований, отмечаются у 10-20% пациентов, регулярно принимающих НПВС [2].
Коксибы же обладают меньшим повреждающим воздействием на органы желудочно-кишечного тракта, но имеют специфические побочные эффекты со стороны сердечно-сосудистой системы: кардиотоксическое действие, увеличение риска тромбозов [3]. К тому же они весьма дорогостоящие.
Таким образом, лечение ОА с использованием НПВС и коксибов сопряжено с серьезными рисками для здоровья пациентов, тем более, что последние чаще всего принадлежат к старшей возрастной группе, а возраст старше 65 лет является относительным противопоказанием для применения этих препаратов.
В комплексном лечении ОА, особенно при выраженных болях и воспалительных изменениях в суставах, используются внутрисуставные или параартикулярные инъекции глюкокортикоидов (гидрокортизон, дипроспан). Однако следует учитывать, что повторные инъекции глюкокортикоидов способны оказывать повреждающее действие на суставной хрящ и костную ткань [4]. К тому же лечение НПВС и гормонами - только симптоматическое.
В настоящее время полноценное лечение ОА невозможно без применения хондропротекторов (глюкозамин, хондроитинсульфат), поскольку они относятся к естественным метаболитам хрящевой ткани. Глюкозамин (ГА) используется хондроцитами как исходный материал для синтеза протеогликанов, глюкозаминогликанов и гиалуроновой кислоты. Хондроитин образуется из глюкозамина и является важной частью структуры хряща, определяющей его физико-химические свойства.
Эти препараты тормозят процессы деструкции хряща, препятствуют повреждающему действию НПВС на хондроциты и матрикс хряща и наряду с усилением анаболических и ослаблением катаболических процессов проявляют отчетливое противовоспалительное действие. Однако при оральном приеме биодоступность их сравнительно невелика: хондроитин - 10-15%, глюкозамин - 20-25% [5].
В настоящее время широкое распространение в медицинской практике для лечения болезней суставов получили препараты на основе сахаридов (соли глюкозамина, хондроитинсульфат) в форме таблеток, инъекций и наружных средств.
Лечение этими препаратами не только уменьшает воспаление и боли в суставах, но и продуцирует восстановление разрушенной хрящевой ткани [6].
В патенте РФ №2259204 предложено средство для лечения суставов, содержащее соль глюкозамина, выбранную из группы:
- гидрохлорид глюкозамина, натрий, калий, кальция сульфат глюкозамина;
- противовоспалительное средство, выбранное из группы: ибупрофен, нимесулид, пироксикам, мелоксикам, соль диклофенака, индометацин, кетопрофен;
- диметилсульфоксид (ДМСО) в качестве агента, увеличивающего проницаемость вышеописанных препаратов в ткани и суставы;
- мазевую основу.
В описании к патенту указано, что препараты наружного применения на основе диклофенака обладают высокой гастроцептивной активностью и другими побочными эффектами.
Применение противовоспалительных средств, в том числе и диклофенака, в сочетании с солью глюкозамина позволяет получить синергетический эффект и снизить дозу противовоспалительного средства.
ДМСО используется в композиции в качестве противовоспалительного и обезболивающего средства, а также в качестве компонента, обеспечивающего проникновение лекарственных субстанций через биологические мембраны.
Наряду с этим он может оказывать ряд побочных эффектов: возможны гиперемия кожи, зуд и ощущение жжения в месте нанесения препарата; временное появление чесночного запаха изо рта, что обусловлено наличием метаболита ДМСО. Описаны единичные случаи развития аллергических реакций немедленного типа (крапивница и отек Квинке).
В патенте РФ №2260432 предложено средство для лечения болезней суставов, содержащее в качестве НПВС вещества, выбранные из группы: ибупрофен, нимесулид, пироксикам, мелоксикам, диклофенака соль, индометацин, кетопрофен, а в качестве хондропротекторов комбинацию соли хондроитинсульфата и глюкозамина.
Средство содержит также ДМСО и мазевую основу. Как уже упоминалось, при использовании ДМСО следует учитывать токсичность данного реагента.
В патенте РФ №2271811 предложено средство для лечения болезней суставов, содержащее соль глюкозамина, ДМСО как транспортирующую систему и мазевую основу.
Патент РФ №2021811 защищает средство для лечения болезней суставов, содержащее хондроитинсульфат, ДМСО в качестве трансдермального агента и мазевую основу.
Необходимость использования ДМСО для улучшения проникновения хондропротекторов обусловлена тем, что хондроитинсульфат обладает различной молекулярной массой (8000-50000 дальтон), что ограничивает диффузию субстанции в зону суставов и существенно снижает эффективность ингибирования процесса разрушения хрящевой ткани.
В патенте РФ №2271812 предложено средство для лечения болезней суставов, содержащее комбинацию хондропротективных компонентов - соль глюкозамина и хондроитинсульфат, ДМСО и мазевую основу.
Все указанные выше средства содержат ДМСО в качестве трансдермальной транспортной системы, которая, к сожалению, обладает рядом побочных эффектов.
Известны средства для лечения заболеваний опорно-двигательного аппарата, содержащие соли глюкозамина без применения ДМСО.
В патенте РФ №2238099 предложена композиция, содержащая гидролизованный коллаген, хлорид глюкозамина, микроводоросль спирулину, элементарную серу, витамин С и цеолин. В этом составе отсутствует система трансдермального переноса гидрофильных компонентов, в результате чего не решена проблема биодоступности.
В патенте РФ №2275199 средство для лечения болезней суставов содержит соль глюкозамина, консервант, неионогенное поверхностно-активное вещество, в частности, моноэфир олеиновой кислоты и полиоксиэтилированного сорбитола. При этом в качестве консерванта применяют бензиловый спирт, метабисульфит натрия, нипагин, нипазол. В данном составе в качестве трансдермальной системы используют известный ПАВ, который сам по себе не улучшает состояние суставов или тканей.
Аналогичное техническое решение описано в патенте РФ №2275190, в котором хондропротекторный компонент состоит из комбинации хондроитинсульфата и соли глюкозамина.
Другим перспективным направлением лечения болезней ОА является использование для этих целей комплексонов фосфоновых кислот, в частности ксидифона (соли 1-гидроксиэтилидендифосфоновой кислоты), которые благодаря своей способности образовывать прочные растворимые комплексы с ионами кальция влияют на рассасывание оссификатов. Таким образом, комплексоны имеют другой механизм действия и иную мишень по сравнению с хондропротекторами и НПВС.
Пероральное применение 2% раствора ксидифона угнетает патологическую резорбцию костной ткани, снижает количество и активность остеокластов, обладает мембраностабилизирующей, противовоспалительной и кальцийрегулирующей активностью. Однако при исследовании фармакокинетики ксидифона выяснено, что препарат всасывается через неповрежденную кожу значительно лучше, чем через стенку желудочно-кишечного тракта (3-5% по сравнению с 0,5-1,0% соответственно) [7].
Удерживая ионы кальция в растворенном состоянии, ксидифон предупреждает рецидивное камнеобразование, устраняя возможность образования нерастворимых солей кальция (оксалатов, фосфатов и т.д.), обладает умеренным противовоспалительным действием при интерстициальном нефрите.
Ксидифон подобно другим комплексонам способен ускорять выведение тяжелых металлов: свинца, олова, сурьмы, стронция, магния, кремния, не нарушая баланса микроэлементов.
Ксидифон регулирует кальциевый обмен - предупреждает чрезмерный выход кальция из костей, препятствуя развитию остеопороза, предупреждает патологическую кальцификацию мягких тканей, предотвращает кристаллообразование, а также рост и агрегацию кристаллов кальциевых солей в моче.
В настоящее время созданы и запатентованы различные композиции для наружного применения, в состав которых входит ксидифон или другие производные фосфоновых кислот.
В качестве средства для регуляции обмена кальция ксидифон описан в авторском свидетельстве СССР №1741801. Для повышения стабильности препарата и предотвращения образования малорастворимых трехзамещенных солей предлагается определенное соотношение монокалиевой соли и гидроксида натрия (17-25% и 3,5-4,0% соответственно). Кроме того, предлагается способ получения, преследующий те же цели и предусматривающий определенный порядок слива компонентов и поддержания рН раствора в интервале 5,8-6,5.
В патенте РФ №2155588 предложен способ увеличения массы костной ткани при переломах.
В патентах РФ №2101015 и №2149824 предлагается наружное средство и способ лечения неврологических заболеваний и заболеваний опорно-двигательного аппарата с болевым синдромом и отечностью, которое содержит 0,5-3,0% ксидифона и 97,0-99,5% основы. В качестве основы предлагаются мази, кремы, эмульсии, содержащие растительные масла (оливковое, вазелиновое, пшеничное и т.д.).
Предложен также способ лечения, заключающийся в том, что состав наносят на поверхность кожи 1 раз в сутки с экспозицией 1-1,5 часа. В описании к патенту отмечается, что при лечении известными методами аппликации с применением препарата, содержащего ксидифон, наблюдается низкий терапевтический эффект, что объясняется недостаточным проникновением препарата через кожный покров. Известно, что абсорбция ксидифона не превышает 5%. Применение же электрофоретических методов лечения связано с рядом противопоказаний (непереносимость, сердечно-сосудистые заболевания, онкология и т.д.).
Предложенный авторами патента РФ №2101015 состав позволяет повысить проникновение ксидифона через кожу. Действительно, как следует из [8], введение ксидифона в состав эмульсии или геля несколько увеличивает эффективность его обезболивающего действия при нанесении в область ожога. Существенного же увеличения эффективности в этом случае нельзя ожидать, т.к. ксидифон - хорошо растворимое соединение с низким коэффициентом распределения, и лишь небольшая его часть будет адсорбирована на поверхности жировых частиц эмульсии, а основная часть вещества по-прежнему останется в растворе.
В патенте РФ №2124881 предложено наружное лечебно-косметическое средство, включающее липидный носитель, эмульгатор, консервант и фосфоновый комплексон.
В качестве фосфоновых комплексонов предлагается использовать следующие известные фосфоновые кислоты:
- оксиметилендифосфоновая;
- оксиэтилидендифосфоновая;
- фосфонмуравьиная;
- аминодиметилендифосфоновая;
- этилендиаминотетраметиленфосфоновая;
- гексаметилендиаминотетраметиленфосфоновая;
- 4-амино-1-гидроксибутан-1-дифосфоновая;
- 6-амино-1-гидроксигексан-1-дифосфоновая;
- 1-гидрокси-2-имидазол-1-ил-этандифосфоновая, щелочные и аммонийные соли этих кислот, смеси этих кислот и их солей.
По мнению авторов, эти соединения в составе средств для наружного применения оказывают двойную функцию. Во-первых, они являются активными лекарственными субстанциями, регулирующими минеральный обмен в организме, а также способны оказывать противоинфекционное действие. Во-вторых, данные соединения обладают невыявленным ранее свойством - являются структурирующими веществами, способными укрепить эмульсионную структуру, что сопровождается повышением гомогенности и термостабильности, и, как следствие, повышением проникновения активных компонентов через кожу. В патенте не приводится документальных доказательств невыявленного ранее свойства.
По мнению авторов, благодаря хорошей проницаемости через кожу запатентованного состава активные компоненты проникают в организм уже при низких концентрациях, что делает средство применимым даже при использовании малых доз препаратов, например, в случае лечения детей младшего возраста.
В этом патенте гидрофобная фаза мазевой основы рассматривается как трансдермальная транспортная система, способствующая лучшему проникновению ксидифона (K, Na- соли ОЭДФК) через роговой слой кожи. Однако процент связывания ксидифона с масляной фазой невелик, т.к. это хорошо растворимое в воде, полностью ионизированное соединение, молекула которого имеет несколько отрицательных зарядов. В представленной рецептуре в патенте отсутствуют какие-либо компоненты, которые либо усиливали бы адсорбцию ксидифона на поверхности частиц масла (например, положительно заряженные компоненты), либо увеличивали бы его растворимость в масляной фазе за счет прямого связывания с ксидифоном.
Применение солей оксиэтилидендифосфоновой кислоты представляет собой весьма перспективное направление, так как данный препарат в отличие от НПВС и хондропротекторов влияет на рассасывание оссификатов благодаря своей способности образовывать прочные растворимые комплексы с ионами кальция. Известно, что проницаемость клеточных структур кожи для этого препарата достаточно низка (3-5%) в силу его гидрофильности: это соединение хорошо растворимо в воде и в его молекуле присутствуют несколько отрицательных зарядов. Следовательно, необходимо применять достаточно высокие концентрации солей оксиэтилидендифосфоновой кислоты, что может повлечь за собой нежелательные побочные эффекты, например местнораздражающее действие.
Однако комплексоны на основе дифосфоновых кислот, в том числе широко используемый ксидифон, обладают рядом недостатков, которые снижают их эффективность при использовании для лечения болезней опорно-двигательного аппарата.
Во-первых, это недостаточная проницаемость через ткани, обусловленная гидрофильностью солей оксиэтилидендифосфоновой кислоты, которая была отмечена в материалах вышеуказанных патентов.
Во-вторых, низкая активность или даже ее отсутствие, как в случае комплексона в физиологическом растворе, что показано в наших экспериментальных исследованиях.
Фиг.1 - спектр поглощения комплекса ксидифона (2% вес. или 8*10-2 М) с ионами кальция (10-4 М СаСl2): 1 - в воде; 2 - в присутствии 0,9% хлорида натрия.
Поэтому была изучена возможность образования комплекса ксидифона с солями ионов кальция в присутствии 0,9% хлорида натрия и установлено, что в этих условиях не наблюдается появление максимума на 275 нм, т.е. комплекс не образуется (фиг.1, кривая 2).
В третьих, соли оксиэтилидендифосфоновой кислоты не обладают хондропротекторным действием.
Задачей настоящего изобретения является одновременное достижение нескольких технических эффектов при лечении болезней опорно-двигательного аппарата, а именно:
- повышение проницаемости лекарственного средства через ткани;
- возможность регулирования обмена ионов кальция в физиологических условиях;
- восстановление и обновление соединительной и хрящевой ткани (хондропротекторное действие);
- противовоспалительный и обезболивающий эффекты.
Поставленная задача достигается предлагаемым техническим решением, состоящим в том, что средство для лечения болезней опорно-двигательного аппарата содержит в качестве основного активного компонента новый комплексонат производных дифосфоновых кислот и аминов углеводов (Алантофосфон), экстракт красного перца, мазевую основу. Состав может дополнительно содержать хондроитинсульфат в качестве хондропротектора.
Средство для лечения заболеваний суставов и мягких тканей на основе производных дифосфоновых кислот содержит в качестве активного ингредиента комплексонат Na, K- соли 1- гидроксиэтилендифосфоновой кислоты и глюкозамина, вспомогательные вещества и воду при следующем соотношении ингредиентов, в мас.%:
Средство может дополнительно содержать экстракт красного перца в количестве 0,1-5 мас.%.
Кроме того, средство дополнительно может содержать хондроитинсульфат в количестве 0,3-5 мас.%, при этом средство может быть выполнено в форме геля, крема.
Наиболее близким техническим решением из известного уровня техники к предложенному техническому решению является средство для лечения болезней суставов, описанное в патенте РФ №2271812.
Средство по патенту РФ №2271812 содержит в составе в качестве активного ингредиента (субстанции) соли хондроитинсульфата (натриевые, калиевые, кальциевые) и соли глюкозамина (гидрохлорид глюкозамина или натриевые, калиевые и кальциевые соли сульфата глюкозамина), а также ДМСО в качестве противовоспалительного, обезболивающего и трансдермального транспортного агента и любые известные мазевые основы.
В описании к патенту отмечено, что одномоментное включение в состав средства смеси полисахарида - соли хондроитинсульфата и моносахарида - соли глюкозамина обеспечивает достижение известного синергетического эффекта в лечении артрологических заболеваний, поскольку экзогенный глюкозамин дополнительно продуцирует синтез хондроцитами эндогенных хондроитинсульфатов и протеогликанов, являясь их универсальным предшественником.
Использование ДМСО обусловлено тем, что он обладает противовоспалительным и обезболивающим действием, кроме того, способен проникать через биологические мембраны, являясь трансдермальным транспортным агентом.
Компоненты в известном составе взяты в следующих соотношениях (массовые %):
Соль глюкозамина - 0,6-10,0;
Хондроитинсульфат - 0,5-10,0;
ДМСО - 1,0-2,0;
Мазевая основа - остальное.
В качестве мазевой основы известное средство содержит компоненты, применяемые для получения собственно мазей, гелей, линиментов, кремов, паст. В частности, ланолин, вазелин, глицерин, соли полиакриловой кислоты.
Для компенсации кислотности используемых солей сульфатов глюкозамина до физиологически приемлемых значений рН мазей (значение рН 4,0-8,0) в основы в процессе приготовления могут быть дополнительно внесены неорганические основания, например гидроксид натрия, или иные известные фармацевтически приемлемые органические основания, например этаноламины: диэтаноламин (2,2'-иминодиэтанол), триэтаноламин, троламин.
Как уже было сказано ранее, недостатком прототипа является необходимость использования в качестве трансдермального транспортного средства достаточно токсичного ДМСО. Кроме того, для компенсации кислотности используемых солей сульфата глюкозамина необходима щелочная обработка.
Предложенное техническое решение отличается от прототипа следующими признаками: в качестве активного компонента предлагается использовать новое химическое соединение, представляющее собой комплексонат производных дифосфоновых кислот с аминами углеводов, в том числе глюкозамином, общей структурной формулы:
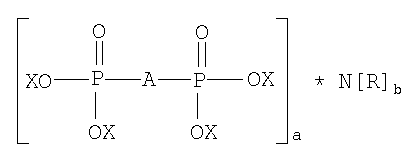
где X=H, Na, K
n=1-6
a, b=1
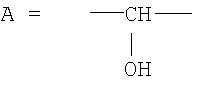 или
или 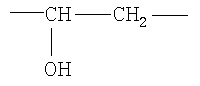 , или
, или
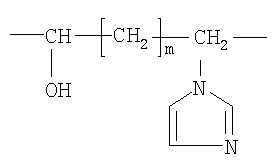
m=2, 4
R - аминоуглеводный радикал, выбранный из группы:
- глюкозамин, ацетилглюкозамин, сульфат глюкозамина,
- галактозамин, ацетилгалактозамин, сульфат галактозамина;
- маннозамин, ацетилманнозамин, сульфат маннозамина;
- фруктозамин, ацетилфруктозамин, сульфат фруктозамина.
В качестве обезболивающего средства предлагается использовать экстракт перца.
Указанное отличие позволяет:
- увеличить проницаемость лекарственного средства без необходимости использования ДМСО, обладающего рядом побочных эффектов;
- обеспечить регуляцию обмена кальция, что невозможно достигнуть с помощью одних аминоуглеводов, не являющихся комплексонами по отношению к ионам металлов;
- обеспечить противовоспалительные свойства;
- увеличить содержание хондроитинсульфата без потери проницаемости.
Указанные технические эффекты достигаются за счет применения в лечебном средстве нового комплексоната производных дифосфоновых кислот с аминоуглеводами, который обладает следующими свойствами:
- пониженной гидрофильностью, которая позволяет увеличить трансдермальное поступление действующих веществ и уменьшить побочные эффекты, например раздражающее действие; при образовании комплексоната происходит нейтрализация отрицательных зарядов в молекуле производного дифосфоновой кислоты и положительных в молекуле аминов углеводов, что повышает гидрофобность комплексоната в целом;
- способностью связывать ионы кальция не только в водной среде, но и в физиологическом растворе, что позволяет увеличить эффективность в качестве регулятора кальциевого обмена, предупреждая резорбцию костной ткани, кальцинацию костей и мягких тканей. Связывая избыточные ионы кальция, дифосфоновая составляющая комплексоната способствует улучшению микроциркуляции в органах и тканях, предупреждает гиперкоагуляцию и секрецию гистамина в очаге поражения [7];
- способностью к восстановлению и обновлению соединительных и хрящевых тканей, которая обусловлена наличием в молекуле комплексоната аминоуглевода, стимулятора синтеза протеогликанов и гиалуроновой кислоты.
Другой отличительный признак - экстракт красного перца, содержащий капсаицин, который снижает передачу периферических болевых импульсов в ЦНС, т.е. служит дополнительным обезболивающим средством [9].
Хондроитинсульфат - компонент, являющийся необязательным в составе лечебного средства, но который улучшает фосфорно-кальциевый обмен в хрящевой и соединительной ткани, подавляет активность ферментов, вызывающих поражение хрящевой ткани, стимулирует синтез гликозаминогликанов, способствует регенерации суставной сумки и хрящевых поверхностей суставов, увеличивает продукцию внутрисуставной жидкости, снижает болезненность и увеличивает подвижность пораженных суставов [10].
Обладая структурной схожестью с гепарином, препятствует образованию фибриновых тромбов в синовиальном и субхондральном микроциркулярном русле, поддерживает вязкость синовиальной жидкости [10].
Примеры получения комплексоната
Комплексонаты получают по следующей методике: инкубируют производное дифосфоновой кислоты в концентрации 2% и амин углеводорода в концентрации от 0,1 до 15% в течение 60 мин при 40 °С. Далее определяют оптическую плотность реакционной среды при длине волны 275 нм. Доказательством получения новых комплексонатов и их свойств как комплексонов служат нижеприведенные УФ-спектры смеси производных дифосфоновых кислот и глюкозамина. Следует отметить, что ни производные дифосфоновых кислот, ни глюкозамин в данной области (250-300 нм) не имеют максимума поглощения.
Пример 1
Инкубируют раствор Na,K-соль 1-гидроксиэтилидендифосфоновой кислоты (2% вес. или 8*10-2 М) с глюкозамином (2% вес. или 4,4·10-2 М) в воде, в отсутствие хлорида кальция и снимают УФ-спектр (кривая 1 на фиг.2). Те же компоненты инкубируются в присутствии 10-3 М хлорида кальция (кривая 2 на фиг.2).
Фиг.2 - спектры поглощения комплексоната Na,K- соли 1-гидроксиэтилидендифосфоновой кислоты (2% или 8*10-2 М) с глюкозамином (2% вес. или 4,4·10-2 М) в отсутствие (1) и присутствии хлорида кальция (10-3 М) (2). Условия инкубации: 60 мин при 40°С.
Пример 2
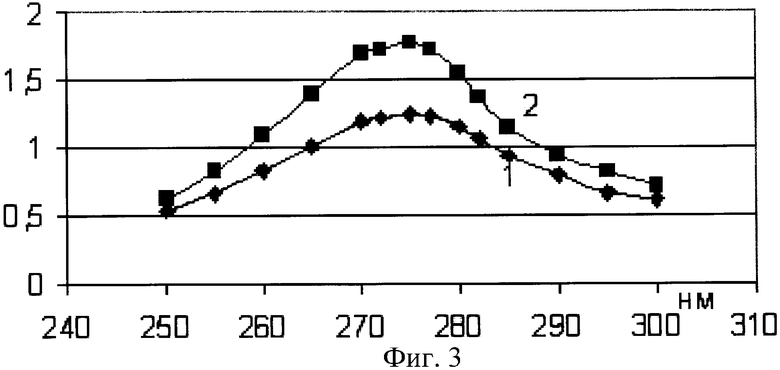
Инкубируют раствор Na,K-соль 1-гидроксиэтилидендифосфоновой кислоты (2% или 8*10-2 М) с глюкозамином (12% вес. или 26,4·10-2 М) в воде, в отсутствие хлорида кальция и снимают УФ-спектр (кривая 1 на фиг.3). Те же компоненты инкубируют в присутствии хлорида кальция (10-3 М) (кривая 2 на фиг.3).
Как следует из фиг.2 и фиг.3 величина оптической плотности в максимуме увеличивается при увеличении содержания глюкозамина.
Фиг.3 - спектр поглощения комплексоната Na,K- соли 1-гидроксиэтилидендифосфоновой кислоты (2% или 8*10-2 М) с глюкозамином (12% вес. или 26,4·10-2 М) в отсутствие ионов кальция (1) и в присутствии 2*10-3 М СаС12 (2).
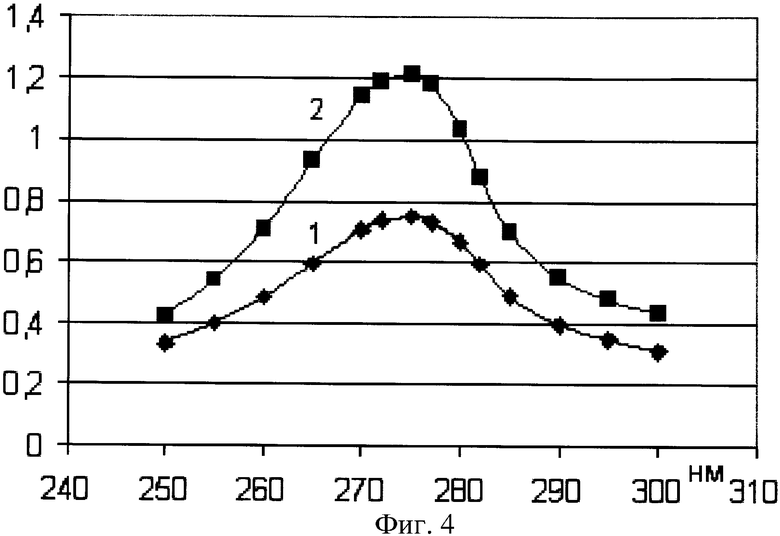
При продолжении инкубации до 24 часов на спектре происходит сдвиг максимума поглощения в длинноволновую область спектра (фиг.4) и появляется дополнительная окраска.
Фиг.4 - спектр поглощения комплексоната Na,K-соли 1-гидроксиэтилидендифосфоновой кислоты с глюкозамином при инкубировании в течение 60 мин при 40°С(1) и в течение 24 ч при комнатной температуре (2).
При варьировании условий образования установлено, что в отличие от ксидифона, который не образует комплекса с ионами кальция в физиологическом растворе, новый комплексонат производных дифосфоновых кислот с аминами углеводов является комплексоном ионов кальция не только в водной фазе, но и в физиологическом растворе (0,9% хлорид натрия), что доказано экспериментально.
Далее установили, что образовавшийся комплексонат способен взаимодействовать с ионами кальция. Этот вывод был сделан на основании того, что при добавлении соли кальция в среду, содержащую комплексонат, происходило повышение оптической плотности при длине волны, равной 275 нм (фиг.2, 3 кривые 2). Иными словами, наблюдали тот же эффект, что и при добавлении ионов кальция к ксидифону в отсутствие аминов углеводов.
Образование электронейтрального комплексоната дает основание говорить о повышении его проницаемости через кожу, достижении кровеносного русла и о взаимодействии с ионами кальция, регулирующем его обмен.
Примеры состава наружного средства для лечения болезней суставов
Пример 1
Состав №1: эмульгатор - 4,5 мас.% (смесь моноглицеридов - 2 г, цетилстеариловый спирт - 1,5 г), эмолент - 4 мас.% (масло соевое - 4 г), загуститель - 1 мас.% (цетилгидроксиэтилцеллюлоза - 1 г), увлажняющая добавка - 5 мас.% (пропиленгликоль - 5 г), биологически активный компонент (хондроитинсульфат - 3 мас.%, комплексонат соли 1-гидроксиэтилидендифосфоновой кислоты и глюкозамина - 2 мас.%,), консерванты (фенохем - 0,4 мас.% и эуксил К100 - 0,1 мас.%) - 0,5 мас.%, отдушка - 0,15 мас.%, вода до 100 мас.%.
Пример 2
Состав №2: эмульгатор - 4,5 мас.% (смесь моноглицеридов - 2 г, цетилстеариловый спирт - 1,5 г), эмолент - 4 мас.% (масло соевое - 4 г), загуститель - 1 мас.% (цетилгидроксиэтилцеллюлоза - 1 г), увлажняющая добавка - 5 мас.% (пропиленгликоль - 5 г), биологически активный компонент (комплексонат соли 1-гидроксиэтилидендифосфоновой кислоты и глюкозамина - 2 мас.%,), СО2 экстракт перца - 0,1 мас.%, консерванты (фенохем - 0,4 мас.% и эуксил К100 - 0,1 мас.%) - 0,5 мас.%, вода до 100 мас.%.
Пример 3
Состав №3: эмульгатор - 4,5 мас.% (смесь моноглицеридов - 2 г, цетилстеариловый спирт - 1,5 г), эмолент - 4 мас.% (масло соевое - 4 г), загуститель - 1 мас.% (цетил гидроксиэтилцеллюлоза - 1 г), увлажняющая добавка - 5 мас.% (пропиленгликоль - 5 г), биологически активный компонент (хондроитинсульфат - 3 мас.%, комплексонат глюкозамина и соли 1-гидроксиэтилидендифосфоновой кислоты - 2 мас.%, СО2 экстракт перца - 0,1 мас.%, консерванты (фенохем - 0,4 мас.% и эуксил К100 - 0,1 мас.%) - 0,5 мас.%, вода - до 100 мас.%.
Пример 4
Состав №4: липидный носитель - 2 мас.% (соевые фосфолипиды - 2 г), загуститель - 2 мас.% (гидроксиэтилцеллюлоза - 2 г), увлажняющая добавка - 5 мас.% (пропиленгликоль - 5 г), биологически активный компонент (комплексонат глюкозамина и соли 1-гидроксиэтилидендифосфоновой кислоты - 2 мас.%), консервант (эуксил К100- 0,1 г) - 0,1 мас.%, вода - до 100 мас.%).
Описание получения наружного средства для лечения болезней суставов
Получение наружного средства для лечения болезней суставов состоит из нескольких стадий, описанных в примере 5.
Пример 5
- приготовление жировой фазы. Взвесить согласно составу, указанному в примере 1, компоненты жировой фазы (эмульгатор и эмолент). Нагреть массу до t 72-75°С. Жировая фаза готова, если в массе отсутствуют частицы нерасплавленного сырья. Температура фазы 72-75°С.
- Приготовление водной фазы. Продиспергировать в отмеренном количестве воды загуститель, увлажняющую добавку, хондроитинсульфат (учесть воду, необходимую для приготовления комплексоната). Нагреть водную фазу до температуры 75-78°С.
- Приготовление эмульсии. Соединить при работающей мешалке водную фазу с жировой. Перемешивать до образования однородной эмульсии.
- Приготовление раствора комплексоната. В учтенном количестве горячей воды растворить глюкозамин, добавить соль 1-гидроксиэтилидендифосфоновой кислоты. При температуре массы эмульсии 45-50°С добавить в эмульсию приготовленный раствор комплексоната. При постоянном перемешивании ввести консерванты, отдушку. Перемешивать до образования однородной эмульсии.
Пример 6
В рассчитанном количестве воды продиспергировать липиды, добавить увлажняющую добавку, биологически активный компонент. Затем при перемешивании ввести загуститель и перемешивать до образования гелеобразной однородной массы. Ввести консерванты.
Клинические испытания были проведены на добровольцах.
Клинические испытания предлагаемого крема в виде наружных аппликаций 2 раза в день применяли в течение 2-4 недель на группе пациентов из 17 человек, страдающих хроническими заболеваниями суставов и параартикулярных тканей, и пациентов с травмами мягких тканей конечностей. Пациенты до проведения клинических испытаний длительное время использовали мазь «Хондроксид», крем «Кси-крем», гели с НПВС, которые не дали выраженного положительного эффекта.
ПРИМЕРЫ
Пример 7
Ш.А.В, 18 лет. Во время тренировки получил травму левого локтевого сустава. Для уменьшения болей применял гели с НПВС (фастум-гель, финал-гель) в течение 1 месяца. Боли продолжали беспокоить. Пациент жаловался на ограничение движения в локтевом суставе. При ультразвуковом исследовании (УЗИ) определялись оссификация и перерастяжение в области медиальной коллатеральной связки левого локтевого сустава. После применения крема в течение 2-х недель боли практически исчезли. Как показало контрольное УЗИ, значительно уменьшился оссификат в поврежденной связке. Функция левого локтевого сустава восстановилась.
Пример 8
К.С.С, 60 лет. Жалобы на боли в обоих коленных суставах в течение нескольких лет. При УЗИ отмечается неровность контура правого и левого надколенников, более выраженная слева. Диагноз: хондромаляция надколенников. Применял крем в течение 3-х недель. Отмечал выраженное уменьшение болей, улучшение функции обоих коленных суставов (увеличение подвижности). При контрольном УЗИ отмечено уменьшение хондромаляции левого надколенника.
Пример 9
Г.Н.А, 61 год. Жалобы на боли и отек, ограничение движения в правом коленном суставе. Диагноз: невыраженный синовит, деформирующий артроз 2-й степени. Применяла крем в течение 3-х недель. После окончания курса УЗИ показало положительную динамику: исчезновение свободной жидкости в правом коленном суставе, уплотнение кортикального слоя, исчезновение оссификатов.
Пример 10
Т.Т.А, 53 года. Жалобы на боли в левом голеностопном суставе. Диагноз: посттравматические дегенеративные изменения в левом голеностопном суставе. Начальные проявления дегенеративного остеоартроза. Применяла крем в течение 3-х недель, после чего отмечала заметное улучшение. При контрольном УЗИ отмечается положительная динамика: выпот уменьшился в размерах, оссификаты стали менее плотными.
Пример 11
А.Л.C. При УЗИ лучезапястного сустава по латеральной поверхности определяется гипоэхогенный участок, являющийся жидкостным компонентом. В межсуставном пространстве визуализируются локальные краевые оссификаты, возникшие вследствие дегенеративных изменений костной ткани. После 3-недельного применения крема при контрольном УЗИ ранее описываемая свободная жидкость по латеральному краю не определяется. Оссификаты по-прежнему видны. Исчез болевой синдром. Восстановилась активность движений.
Пример 12
Н.С.Н, 55 лет. Дагноз: асептический некроз головки правого бедра. После применения крема значительно уменьшилась интенсивность болей в суставе.
Пример 13
С.А.Ю, 37 лет. Ушиб левой голени месячной давности. При осмотре определяется застарелая, очень плотная организовавшаяся гематома размером (3,0×3,5×2,5). После недели применения крема гемотома “зацвела”, значительно уменьшились ее размеры. Стала менее плотной, спала опухоль. При повторном осмотре спустя две недели следов гематомы не обнаружено.
Пример 14
А.Л.А, 47 лет. Диагноз: деформирующий артроз правого коленного сустава. Применение крема в течение 3 недель способствовало уменьшению отечности сустава, синовита, боли.
После курса применения крема, содержащего комплексонат, в течение 2-3 недель все пациенты не отмечали какого-либо побочного действия.
В качестве контроля использовали крем, аналогичный вышеописанной рецептуре, но содержащий ксидифон (2%) в свободном состоянии и не содержащий комплексонат.
Пример 15
Контроль. Г.Т.А, 54 г. Жалобы на боли и ограничение движения в правом лучезапястном суставе. При УЗИ поставлен диагноз: карпальный синдром. Использовала крем, не содержащий комплексонат, в течение 3-х недель. Контрольное УЗИ показало наличие свободной жидкости в синовиальном влагалище сухожилий в незначительном количестве. Сохраняется неровность кортикального слоя костей кисти с невыраженными включениями - краевыми оссификатами. Сделано заключение об отсутствии положительной динамики.
Пример 16
Контроль. Ю.Я.Б, 57 лет. Заключение после УЗИ: в межфаланговых сочленениях первого и второго пальцев стопы определяются гиперэхогенные краевые оссификаты и незначительное количество свободной жидкости. По подошвенной поверхности со стороны первого пальца находятся массивные оссификаты размерами до 1,7 мм. Применяла крем, не содержащий комплексонат, в течение 3-х недель. Пациентка отмечала усиление болевого синдрома и общее ухудшение. Контрольное УЗИ не обнаружило положительную динамику.
ЗАКЛЮЧЕНИЕ: при местном применении композиции, содержащей комплексонат оксиэтилидендифосфоновой кислоты и аминоуглеводов, отмечена положительная динамика следующих показателей:
- уменьшается или исчезает синовит и отечность сустава,
- по данным УЗИ оссификаты в мягких тканях становятся менее плотными, уменьшаются в размерах,
- значительно снижается или купируется болевой симптом,
- уменьшается плотность и размер гематом.
Совокупность перечисленных эффектов не отмечалась при использовании аналогов.
Предлагаемое наружное средство оказывает не только симптоматическое, но и патогенетическое воздействие благодаря нормализации обмена кальция и улучшения трофики компонентов сустава.
Оно практически не имеет противопоказаний, может использоваться длительное время.
Предложенные лечебные средства могут быть применены при хронических заболеваниях суставов, сопровождающихся разрушением хрящевой и разрежением костной ткани (деформирующие остеоартрозы, остеохондрозы позвоночника, ревматоидные артриты); для ускорения реабилитации после переломов костей, повреждений капсулы суставов, связок; при повреждении и воспалении сухожилий, слизистых сумок (бурситы); при дегенеративных заболеваниях мягких тканей в области сустава, в том числе с наличием воспалительного эксудата и оссификатов, при острых травмах и ушибах мягких тканей; для профилактики образования оссификатов в имеющихся гематомах.
ЛИТЕРАТУРА
1. Murray Cjl, Lopez AD. The global burben of disease. Geneva: World Health Organization, 1997.
2. Wolfe MM, Lichtenstein DR, Singh G. Gastrointestinal toxicity of nonsteroidal anti-inflammatory drugs. N Engl. J Hed, 1999; 340: 1888-99.
3. Mukherjee D, Nissen SE, Topol EJ. Risk of cardiovascular events associated with selective COX-2 inhibitors. JAMA 2001; 286: 954-959.
4. Walker-Bone K. Javaid K, Arden N, Cooper C. Medical managment of osteoarthritis. BMJ 2000; 321: 936-40.
5. Руденко В.Г. «Хондропротекторы - основа конструктивной терапии заболеваний суставов. 2005.
6. Насонов Е.Л. Клинические рекомендации и алгоритм для практикующих врачей. Ревматология, М., 2004, k.Pavelka, Archives Internal Medicine N10, 2002, N7, 2003).
7. Матковская Т.А., Попов К.И., Э.А.Юрьева. Бифосфонаты. Свойства, строение и применение в медицине. Стр.156.
8. Барышникова Г.И. Разработка и исследование лекарственных форм ксидифона. Автореферат диссертации на соискание ученой степени к. фарм. наук. Москва. 1985.
9. Zhang W.Y., Li-Wan-Po A. The effectiveness of topically applied capsaicin. A meta-analysis. Eur J Clin Pharmacol 1994, 46, 517-522.
10. Государственный реестр лекарственных средств. М., «Научный центр экспертизы средств медицинского применения», 2004, т.2, стр.1615.
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЙ КОМПЛЕКСОНАТ ПРОИЗВОДНЫХ ДИФОСФОНОВЫХ КИСЛОТ С АМИНАМИ УГЛЕВОДОВ И ЛЕЧЕБНО-КОСМЕТИЧЕСКОЕ СРЕДСТВО НА ЕГО ОСНОВЕ | 2007 |
|
RU2412194C2 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНЕЙ СУСТАВОВ | 2004 |
|
RU2260432C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНЕЙ СУСТАВОВ | 2004 |
|
RU2259204C1 |
| КОМБИНИРОВАННАЯ АКТИВНАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ ОПОРНО-ДВИГАТЕЛЬНОГО АППАРАТА | 2015 |
|
RU2582974C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНЕЙ СУСТАВОВ | 2004 |
|
RU2271812C1 |
| ТРАНСДЕРМАЛЬНОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ БОЛЕЗНЕЙ СУСТАВОВ И МЯГКИХ ТКАНЕЙ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И КОМБИНИРОВАННЫЙ ТРАНСДЕРМАЛЬНЫЙ ПРЕПАРАТ ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ БОЛЕЗНЕЙ СУСТАВОВ И МЯГКИХ ТКАНЕЙ | 2013 |
|
RU2582278C2 |
| ЛЕКАРСТВЕННАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНЕЙ СУСТАВОВ (ВАРИАНТЫ) | 2009 |
|
RU2408380C1 |
| Трансдермальный препарат для лечения и профилактики болезней суставов и мягких тканей | 2018 |
|
RU2685436C1 |
| НАРУЖНОЕ СРЕДСТВО И СПОСОБ ЛЕЧЕНИЯ НЕВРОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ И ЗАБОЛЕВАНИЙ ОПОРНО-ДВИГАТЕЛЬНОГО АППАРАТА С БОЛЕВЫМ СИНДРОМОМ И ОТЕЧНОСТЬЮ | 1995 |
|
RU2101015C1 |
| КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ И ПРЕДУПРЕЖДЕНИЯ ОСТЕОАРТРИТА И ОСТЕОАРТРОЗА СУСТАВОВ | 2011 |
|
RU2509569C2 |


Изобретение относится к химико-фармацевтической промышленности и касается наружного средства для лечения заболеваний суставов и мягких тканей (остеоартрозов, остеохондрозов, тендовагинитов, бурситов, лигаментитов и других) на основе комплексона производных дифосфоновых кислот с аминами углеводов, который обладает хондропротекторной, кальцийрегулирующей и противовоспалительной активностью. Средство для лечения заболеваний суставов и мягких тканей на основе производных дифосфоновых кислот содержит в качестве активного ингредиента комплексонат Na, К- соли 1-гидроксиэтилендифосфоновой кислоты и глюкозамина, вспомогательные вещества и воду и выполнено в форме геля или крема. Средство позволяет уменьшить или убрать синовит и отечность сустава, уменьшить в размерах или размягчить оссификаты в мягких тканях, значительно понизить или купировать болевой симптом, а также уменьшить плотность и размер гематом. 3 з.п. ф-лы, 4 ил.
1. Средство для лечения заболеваний суставов и мягких тканей на основе производных дифосфоновых кислот, содержащее дополнительно вспомогательные вещества и воду, отличающееся тем, что в качестве активного ингредиента оно содержит комплексонат Na, К-соли 1-гидроксиэтилендифосфоновой кислоты и глюкозамина при следующем соотношении ингредиентов, мас.%:
2. Средство по п.1, отличающееся тем, что оно дополнительно содержит экстракт красного перца в количестве 0,1-5%.
3. Средство по п.1, отличающееся тем, что оно дополнительно содержит хондроитин сульфат в количестве 0,3-5%.
4. Средство по п.1, или 2, или 3, отличающееся тем, что оно может быть выполнено в форме геля, крема.
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНЕЙ СУСТАВОВ | 2004 |
|
RU2271812C1 |
| НАРУЖНОЕ ЛЕЧЕБНО-КОСМЕТИЧЕСКОЕ СРЕДСТВО | 1997 |
|
RU2124881C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНЕЙ СУСТАВОВ | 2004 |
|
RU2271811C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНЕЙ СУСТАВОВ | 2005 |
|
RU2275190C1 |
| US 5500417 A, 19.03.1996. | |||
Авторы
Даты
2010-01-10—Публикация
2007-12-24—Подача