Область техники, к которой относится изобретение
Изобретение относится к биотехнологии и медицине, в частности к получению антиоксидантного и нейропротекторного средства на основе эмбриональных тканей птиц. Эмбриональные ткани птиц, схожие по своим свойствам с плацентой, но являющиеся более дешевым и доступным сырьем получают все большее распространение в качестве сырья для получения биопрепаратов и пищевых добавок.
Полученное средство расширяет арсенал недорогих по себестоимости пептидсодержащих препаратов из природного доступного сырья, обладающих антиоксидантным и нейропротекторным свойствами.
Уровень техники
Различные стрессовые ситуации, экологические проблемы, неправильное питание перегружают антиоксидантную защиту организма и могут вызвать дисбаланс взаимоотношений систем свободнорадикального окисления и общей антиоксидантной активности ( et al., 2009; Патент RU 2292214).
et al., 2009; Патент RU 2292214).
Многие патологии центральной нервной системы, при которых наблюдаются деструктивные процессы нейронов головного мозга, связаны с активацией перекисного окисления липидов, в результате которого образуются свободные радикалы. Избыток свободных радикалов, отрицательно воздействующих на ДНК нейронов мозга, может вызвать изменение в генетическом коде и гибель клетки. Среди основных механизмов нейронального повреждения различают гиперпродукцию активных форм кислорода (Попова М.С. и др., 2008;.Зозуля Ю.А. и др., 2000; Смирнова И.Н. и др., 2006; Федорова Т.Н., 2004; Calabrese V. et al., 2000).
Антиоксидантная защита организма при оксидативном стрессе неспособна полностью нейтрализовать образующийся избыток активных форм кислорода. В этих условиях очевидна целесообразность использования антиоксидантных препаратов, способных защитить мозговую ткань от повреждения (Патент RU 2514632; Nonaka Sh. et al., 1998.). В последние годы повышен интерес к выявлению объектов природного происхождения, содержащих биологически активные вещества, обладающие антиоксидантными свойствами.
Известно антиоксидантное нейропротекторное средство - пикамилон (натриевая соль N-никотинол-γ-аминомасляной кислоты. Наличие в химической структуре пикамилона гаммааминомасляной кислоты и никотиновой кислоты обусловливает его ноотропное и вазоактивное действие. Он улучшает мозговое кровообращение и позитивно влияет на метаболизм ткани головного мозга. Препарат оказывает также антигипоксическое, антиоксидантное и антиагрегантное действие, обладает транквилизирующим эффектом. Механизм действия пикамилона обусловлен его взаимодействием с ГАМК-рецепторами (Горчакова Н.А. и др., 2010). Однако данное средство имеет ряд побочных эффектов: аллергические реакции, головную боль, головокружение, чувство тревоги.
Известна фармацевтическая нейропротекторная и антиоксидантная композиция, содержащая 100-250 мг 3-оксипиридина или его фармацевтически приемлемого производного, или фармацевтически приемлемой соли этого производного и 100-400 мг холина альфосцерата, отличающаяся тем, что дополнительно содержит 400-500 мг фармацевтически приемлемого производного магния, 10-50 мг пиридоксина или его фармацевтически приемлемого производного, 10-50 мг никотинамида, 15-30 мг идебенона, 15-30 мг убихинона (коэнзима Q10) и 5-40 мг фармацевтически приемлемого производного цинка и фармацевтически приемлемые вспомогательные вещества (Патент RU 2385722). К недостаткам данной композиции относится дороговизна конечного продукта.
К настоящему времени доказано, что многочисленные продукты, полученные из гидролизованных пищевых белков, обладают заслуживающей внимания антиоксидантной активностью против перекисного окисления липидов (Kitts D.D., Weiler K., 2003).
Исследователями была выявлена антиоксидантная активность в гидро-лизатах на основе креветок (Suetsuna K., 2000), сока после приготовления тунца (Jao C.L., Kо W.C., 2002), сайды Аляски {Theragra chalcogramma) (Je J.Y., et al., 2005; Kim S.K. et al., 2001), Area subcrenata Lischke (Song Li., 2008).
Однако наибольший интерес вызывают гидролизаты различных эмбриональных тканей и белков куриного яйца (Lee S.K. et al., 2002; Li Y.F. et al., 2012; Lu C.L., Baker R.C., 1987; Park P.J. et al., 2001; Sakanaka S. et. al., 2004; Sakanaka S., Tachibana Y., 2006; Sun H. et al., 2014), схожие по своим свойствам с плацентой, но являющиеся более дешевым и доступным сырьем для получения средств с антиоксидантным и нейропротекторным свойствами.
Известен способ приготовления ферментативного гидролизата из утиных яиц (Chen Y. et al., 2009). Для этого утиные яйца очищали, разбивали и разделяли. Белок яйца в количестве 600 мл гомогенизировали (IKA-T25BS1, Германия) на низкой скорости в течение 60 с. После гомогенизации белок в 10 раз разбавляли 0,1 М фосфатным буфером (рН 7,0) и затем использовали для эксперимента. Папаин, трипсин, химотрипсин, алкалазу и флавозерм (от Sigma-Aldrich Co., США) добавляли при соотношениях фермента к субстрату (отношения ф/с) 1%, 2%, 3%, 4% и 5%. Оптимальные параметры температуры и рН: папаин (40°С, рН 7,0); трипсин и химотрипсин (40°C, рН 8,0); алкалазу и флавозерм (50°C, рН 8,0). Полученные гидролизаты нагревали в кипящей воде в течение 5 мин для инактивации ферментов, а затем центрифугировали при 4°C и 5000 об/мин в течение 10 мин. Супернатант фильтровали через ватман №1 и фильтрат хранили при 5°C. К недостаткам данной композиции относится дороговизна конечного продукта.
Sun Н. с соавторами (2014) готовили однородную суспензию яиц куриного эмбриона с использованием высокоскоростного гомогенизатора (1000 об/мин, 5 мин). Гомогенат (1 г) смешивали с 10 мл раствора пепсина (1 г пепсина в 200 мл 0,1 моль/л HCl) и смесь инкубировали на встряхивающей водяной бане при 37°C в течение 2 часов. рН повышали до 7,5 с помощью 0,1 моль/л NaHCO3. Далее добавляли 10 мл раствора трипсина (1 г трипсина в 200 мл 0,1 моль/л NaHCO3) и инкубировали на встряхивающей водяной бане при 37°C в течение 2 часов. Затем образцы гидролизата инкубировали в кипящей воде в течение 3-10 мин для дезактивации ферментативной активности. Центрифугировали при 10000 g в течение 10 мин и разделяли на две фракции: супернатант, в виде биодоступной фракции и остаточной фракции. Супернатант лиофилизировали (сублимационная сушилка Dura-Dry MP, FTS Systems, Inc., Ridge, NY), измельчали и хранили при минус 70°C. К недостаткам данной композиции относится дороговизна конечного продукта.
Li Xi с соавторами (2012) для приготовления гидролизата все содержимое инкубационных куриных яиц гомогенизировали, лиофилизировали и хранили при 20°C до использования. Яичный порошок куриного эмбриона сначала растворяли в воде (5%, масса/объем), а затем рН образца доводили до 2,0 с помощью 1 н HCl и смесь инкубировали с пепсином при 800 Ед/мл на встряхивающей ванне в течение 2 ч при 37°C со скоростью встряхивания 100 об/мин. Затем образец нейтрализовали 1 М NaOH до рН 7,0 и добавляли панкреатин (2 мг/мл) и смесь желчных экстрактов (0,3 мг/мл) для дальнейшей инкубации на протяжении 2 часов. Для дезактивации ферментативной активности проводили кипячение в течение 10 мин. После гидролиза в смесь (1:1, об/об) добавляли петролейный эфир для экстракции биоактивных веществ в течение 4 ч с использованием магнитной мешалки. Затем смесь переносили в колбу, соединенную с обратным холодильником, где дополнительную экстракцию проводили на водяной бане при 80°C в течение 4 часов. Процесс разделения двух экстрактов проводили с помощью высокоскоростной центрифуги. Затем водорастворимую часть лиофилизировали. К недостаткам данной композиции относится дороговизна конечного продукта.
Наиболее близким к способу получения средства по настоящему изобретению является способ изготовления биологически активных препаратов на основе эмбриональных тканей. Этот способ предусматривает: измельчение мягких эмбриональных тканей, их гомогенизацию в дисперсионной среде на основе воды до разрушения клеточных оболочек, отделение (например, фильтрованием или центрифугированием) неразрушенных клеточных элементов, гидролиз гомогената в присутствии консерванта при температуре 4-45°C в течение времени от двух суток до шести недель, причем тем дольше, чем ниже температура, термообработку гидролизата при температуре 60-120°C до денатурации балластных веществ, отделение денатурированных термолабильных веществ и выделение из гидролизата термостабильного целевого продукта со средней молекулярной массой менее 10 кДа путем фракционирования, выполняемого, например: ультрафильтрацией, или центрифугированием при ускорении свыше 1500 g в течение 20-40 мин, или диализом через полупроницаемую пленку и/или гельфильтрацией, стерилизацию, разлив и укупорку препарата. Целевым продуктом при этом служит супернатант, содержащий в качестве действующего начала смесь относительно низкомолекулярных термостабильных веществ неопределенного состава со средней молекулярной массой в пределах 0,7-10,0 кДа (Патент RU 2132688).
Однако описанный способ связан с существенными энергозатратами и обладает низкой производительностью.
Технический результат изобретения заключается в получении недорогих по себестоимости средства, обладающего антиоксидантными и нейропротекторными свойствами, из доступного природного сырья.
Раскрытие изобретения
Средство, обладающее антиоксидантным и нейропротекторным свойствами, представляющее собой содержащий в качестве действующего начала не менее 0,4% аминокислот и 0,9% низкомолекулярных пептидов продукт кислотного гидролиза обезжиренного сублимата эмбриональных и внеэмбриональных тканей куриных эмбрионов.
Ниже описан один из способов получения средства согласно изобретению. Такие параметры являются оптимальными, но не единственно возможными, поскольку гидролиз можно осуществить различными концентрациями соляной кислоты и при других параметрах автоклавирования, а также при других соотношениях разбавителя и сублимата эмбриональных и внеэмбриональных тканей куриных эмбрионов, получая тот же качественный набор биологически активных веществ, который и определяет антиоксидантные и нейропротекторные свойства средства. Сами же антиоксидантные и нейропротекторные свойства средства, являются суммарным действием, как низкомолекулярных пептидов, так и других компонент, образующихся при гидролизе эмбриональных и внеэмбриональных тканей куриных эмбрионов. Данные параметры определяют только количество образующихся в процессе гидролиза биологически активных веществ.
Средство, обладающее антиоксидантным и нейропротекторным свойствами, получают следующим способом. Из сублимата эмбриональных и внеэмбриональных тканей 10-ти суточных куриных эмбрионов удаляют липиды 5-ти кратной экстракцией петролейным эфиром с последующим высушиванием обезжиренного остатка, полученный белоксодержащий порошок тщательно измельчают, затем растворяют в дистиллированной воде в количестве (1:25-30), перемешивают и затем к раствору добавляют НС1 до ее концентрации 0,5-0,6% и выдерживают при 50-55°C в течение 60 мин при перемешивании, затем полученную массу автоклавируют при 125-130°C в течение 60-65 мин, а после нейтрализуют 1 М NaOH до рН 6,8-7,2, центрифугируют при 4600-4800 g в течение 100-120 мин при температуре 2-4°C, полученную после центрифугирования жидкость последовательно фильтруют с применением мембран для стерилизации и удаления не гидролизованных белков.
Основные физико-химические показатели средства представлены в таблицах 1-2. Плотность (ρ20) определялась по Европейской Фармакопее и была рассчитана как отношение массы вещества к его объему при 20°C. Для определения использовался стеклянный пикнометр. Количество сухого вещества определяли весовым методом с помощью влагомера Ohaus MB 25 (Ohaus Corporation, США) при 105°C. Ионометрию проводили с использованием рН-метра S400-B (Mettler Toledo, Испания). Степень гидролиза (%) определялась как отношение аминного азота к общему азоту. Аминный азот, определяли методом формальдегидного титрования, а общий азот титримет-рическим методом по Кьельдалю. Концентрацию пептидов определяли би-уретовым методом с 1% пептоном в качестве стандарта и с использованием УФ-спектрофотометра СФ-102 (ООО «НПО ИНТЕРФОТОФИЗИКА», Россия). Количество моносахариддов определяли реакцией с пикриновой кислотой (по Креселиусу-Зейферту) с использованием УФ-спектрофотометра СФ-102 (ООО «НПО ИНТЕРФОТОФИЗИКА», Россия). Анализ состава свободной аминокислоты проводили в автоматическом анализаторе аминокислот ARACUS (ABACUS, Германия).

Результаты свидетельствуют о том, что полученное средство, содержит в качестве действующего начала не менее 0,4% аминокислот (аминный азот 68,6±2,8 мг %) и 0,9% низкомолекулярных пептидов (940±88 мг %) (таб. 1).

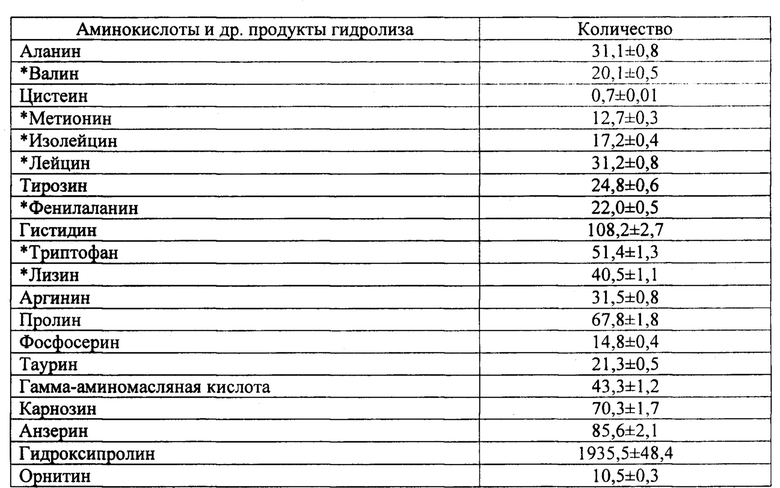
Примечание: 1Значения, указанные для Asp, включают Asp+Asn; Значения, указанные для Glu, включают Glu+Gln; *Незаменимые аминокислоты.
Метионин, гистидин, лизин, лейцин, фенилаланин, аргинин, тирозин и пролин считаются общепринятыми антиоксидантами. Антиоксидантным действием также обладают гистидинсодержащие дипептиды - анзерин и кар-нозин. Гамма-аминомасляная кислота, лизин, глицин, изолейцин, лейцин, фенилаланин, аргинин, триптофан, глутаминовая кислота, аспарагиновая кислота, валин, тирозин и аланин, присутствующие в полученном средстве, обладают выраженным нейропротекторным действием (таб. 2).
Антиоксидантная активность полученного средства была определена in vitro тремя методами: методом нейтрализации АБТС радикальной активности, анализом ингибирования перекисного окисления липидов и электрохимическим методом.
Метод нейтрализации АБТС радикальной активности воспроизводился в соответствии с методикой, описанной Metelitza D.I. et al. (2001). Исходные растворы включали хромоген, содержащий АБТС-радикал (АБТС+), Трис-HCl буфер (20 ммоль/л, рН 7,4) и 0,95 ммоль/л раствор тролокса. Рабочий раствор готовили растворением хромогена, содержащего АБТС+ в 20 мл Трис-HCl буфере. К 1,98 мл рабочего раствора добавили 0,02 мл заявленного средства, выдержали 3 мин и замеряли оптическую плотность при длине волны 734 нм на УФ-спектрофотометре СФ 102 (ООО НПО ИНТЕРОФОТОФИКА, Россия). В качестве эталона использовали раствор тролокса (6-гидрокси-2,5,7,8-тетраметилхроман-2-карбоновой кислоты). В отрицательном контроле вместо заявленного средства использовали дистиллированную воду.
По результатам проведенного исследования было выявлено, что полученное средство обладает высокой антиоксидантной активностью при ингибировании АБТС-радикала, тролоксовый эквивалентный антиоксидантного потенциала составил 1,84 мкМ/мл тролокса.
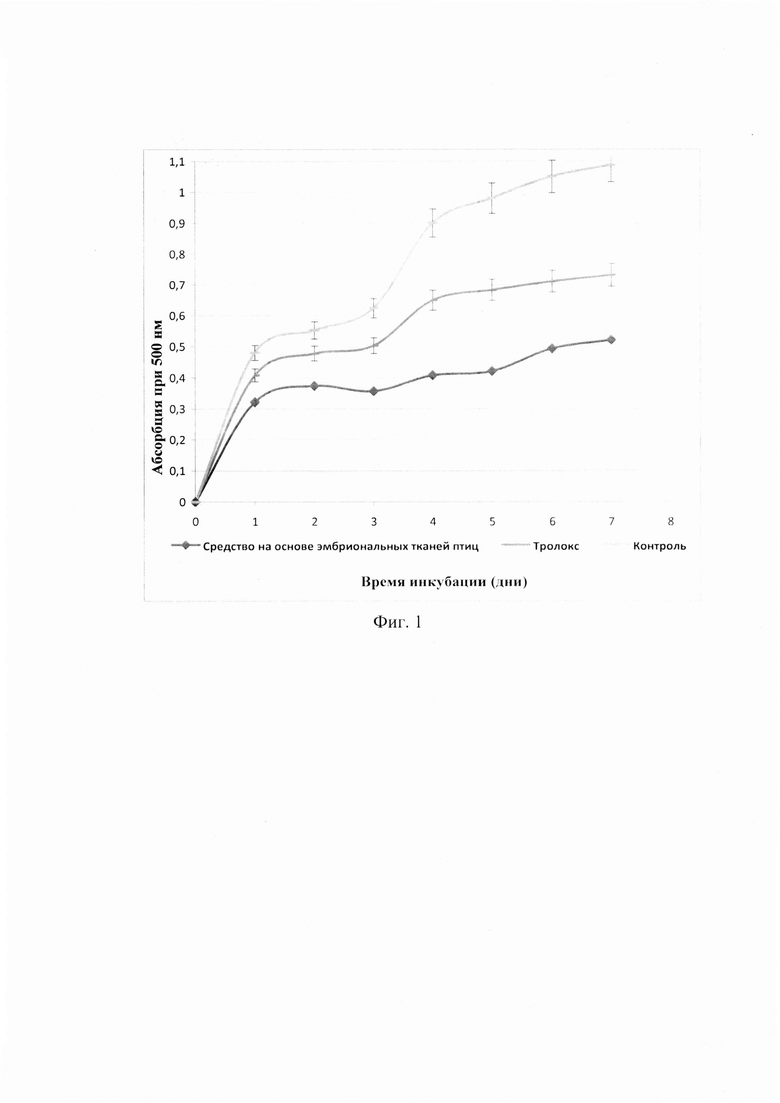
Ингибирующую активность перекисного окисления липидов полученного средства измеряли в эмульсионной системе в соответствии со способом, описанным Qian Z.J. et al. (2008). К 4 мл фосфатного буфера (50 мМ, рН 7,0) внесли изучаемое средство (0,04 мл) и добавили 0,1 г олеиновой кислоты в 4-х мл этанола (99,5 мас. %, водный раствор). Общий объем довели до 10 мл дистиллированной водой, смешали в герметичной конической пробирке с закручивающейся крышкой и инкубировали при 40°C, в темноте в течение 7 суток. Степень окисления оценивали ежедневно с использованием тиоцианата железа. Для этого реакционный раствор содержащий липиды (100 мкл) смешивали с 4,7 мл этанола (75 мас %, водный раствор), 0,1 мл водного раствора тиоцианата аммония (30% мас/об) и 0,1 мл раствора хлорида железа (II) (20 мМ в 3,5% (об/об) HCl). Через 3 мин поглощающую способность измеряли при 500 нм с использованием УФ-спектрофотометра СФ 102 (ООО НПО ИНТЕРОФОТОФИКА, Россия). Тролокс использовался в качестве антиоксидантного эталона. В отрицательном контроле вместо заявленного средства использовали деионизированную воду.
Анализ ингибирования перекисного окисления липидов в моделирующей эмульсии олеиновой кислоты, свидетельствует о том, что полученное средство показало значительно более высокую степень ингибирования перекисного окисления липидов, чем тролокс в концентрации 0,95 ммоль/л. На Фиг. 1 представлено ингибирование перекисного окисления липидов под влиянием средства на основе эмбриональных тканей птиц.
Общая антиоксидантная способность электрохимическим методом определялась в соответствии с  et al. (2010) и Hoyos-Arbelaez J. et al. (2017) на жидкокристаллическом приборе «Цвет-Яуза-01-AA» с амперометрическим детектированием (Россия). В качестве эталонного вещества использовали раствор галловой кислоты. В процессе анализа калибровочный график строится для 5 последовательных измерений каждого из 5 калибровочных растворов галловой кислоты. Результатом является среднее арифметическое 5 измерений. На основе полученных данных построен калибровочный график, который описывается уравнением Y=аХ+b,
et al. (2010) и Hoyos-Arbelaez J. et al. (2017) на жидкокристаллическом приборе «Цвет-Яуза-01-AA» с амперометрическим детектированием (Россия). В качестве эталонного вещества использовали раствор галловой кислоты. В процессе анализа калибровочный график строится для 5 последовательных измерений каждого из 5 калибровочных растворов галловой кислоты. Результатом является среднее арифметическое 5 измерений. На основе полученных данных построен калибровочный график, который описывается уравнением Y=аХ+b,
где: X - массовая концентрация галловой кислоты, мг/л
Y - сигнал галловой кислоты (площадь пика), хА/с
С использованием метода электрохимического анализа в заявленном средстве обнаружен высокий уровень общей антиоксидантной способности в пересчете на галловую кислоту - 3,3 мг/л.
Следующим этапом исследований стало изучение нейропротекторного действия полученного средства in vivo на лабораторных животных при моделировании экспериментальной интоксикации хлоридом алюминия (AlCl3) в дозе 100 мг/кг на протяжении 90 дней. В результате интоксикации хлоридом алюминия (AlCl3) в дозе 100 мг/кг в гиппокампе крыс развивается комплекс изменений соответствующих картине болезни Альцгеймера.
Эксперимент проводили на 60 самках крыс линии Вистар, разделенных на 3 группы:
I группа: интактные животные (n=20);
II группа (контроль) - животные с моделью экспериментальной алюминиевой интоксикации (n=20);
III группа (опытная) - животные с моделью экспериментальной алюминиевой интоксикации, получали подкожные инъекции заявленного средства с 80 по 85 сутки исследования в дозе 4,5 мг (пептидов) на кг живой массы.
На 91 день исследования животных умерщвляли в камере с углекислым газом и отбирали мозг.
Данные, полученные в результате исследования, обрабатывали используя программное обеспечение GraphPad Prism версия 5 (GraphPad Software, Inc., La Jolla, CA, USA). Межгрупповое различие было измерено односторонним анализом дисперсии (ANOVA), за которым следовал поспеет Даннета. Значение Р<0,05 считалось статистически значимым.
Результаты, подтверждающие нейропротекторное действие заявленного средства представлены в таблицах 3 и 4.
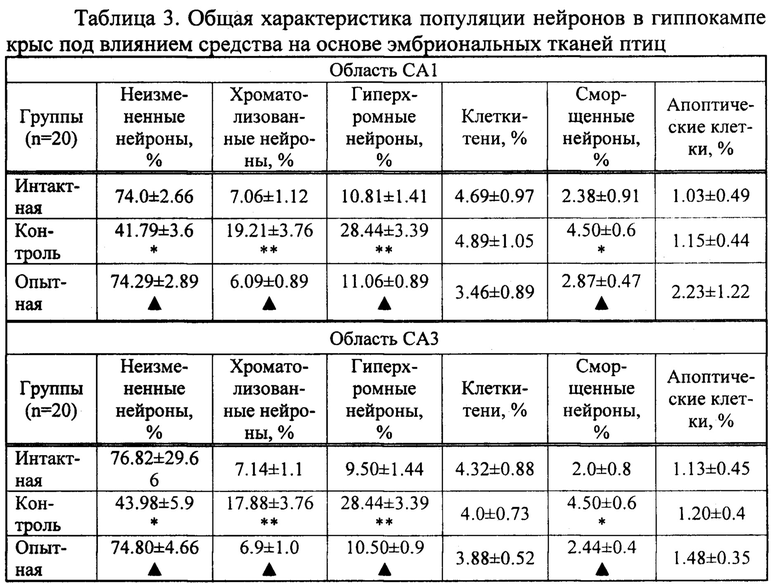
Достоверность различий от параметров интактной группы: *≤0,005; **≤0,0005. Достоверность различий параметров экспериментальной группы от контроля:  ≤0,005.
≤0,005.

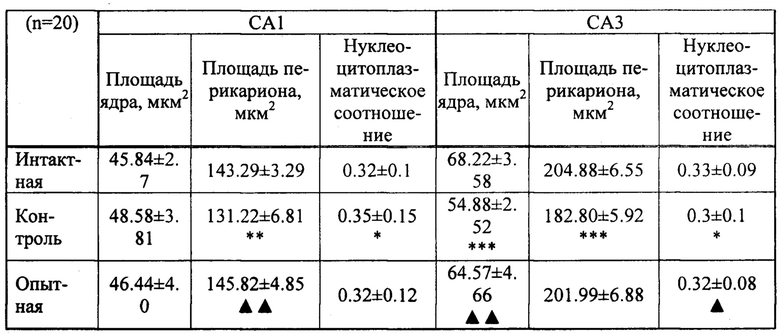
Достоверность различий от параметров интактной группы *≤0,05, **≤0,005, ***≤0.0005. Достоверность различий параметров экспериментальной группы от контроля:  ≤0,05;
≤0,05; 
 ≤0,005.
≤0,005.
Результаты морфологических изменений в гиппокампе крыс контрольной группы в целом соответствует картине болезни Альцгеймера.
Применение крысам опытной группы полученного средства приводит к нормализации показателей характеризующих популяцию нейронов в гипокампе, что свидетельствует о его нейропротекторном действии.
Литература
Горчакова, Н.А. Фармакология спорта / Н.А. Горчакова, Я.С. Гудивок, Л.М. Гунина и др. - К.: Изд-во Олимп. Литература, 2010. - 640 с.
Зозуля, Ю.А. Свободнорадикальное окисление и антиоксидантная защита при патологии головного мозга / Ю.А. Зозуля, В.А. Барабой, Д.А. Сутковой. - М.: Знание, 2000. - С. 226-231.
Патент RU 2292214. Средство, обладающее антиоксидантной активностью // Шилова И.В., Краснов Е.А, Кувачева Н.В., Новожеева Т.П. - Опубл. 10.05.2009.
Патент RU 2385722. Фармацевтическая нейропротекторная, антиоксидантная, антигипоксантная, антиапоптотическая и мембранопротекторная композиция и способ лечения // Кожока Т.Г., Филимонов В.А., Ясинский С.Я. - Опубл. 10.04.2010.
Патент RU 2514632. Антиоксидантное, стресс- и нейропротекторное фармакологическое средство - коменат калия // Шурыгина Л.В., Злищева Э.И., Кравцов А.А., Андросова Т.В., Злищева Л.И., Полещук Л.А., Скороход Н.С. - Опубл. 27.04.2014.
Патент RU 2132688. Способ изготовления биологически активных препаратов из эмбриональных тканей // Шорох Д.Б., Писоцкий А.А., Шевченко А.А., Волощенко Ю.В., Диденко Н.Ю. - Опубл. 10.07.1999.
Попова, М.С. Индукция клеточного цикла, амилоид-бета и свободные радикалы в механизме развития нейродегенеративных процессов в мозге / М.С. Попова, М.Ю. Степаничев // Нейрохимия. - 2008. - Т. 25. - №3. - С. 170-178.
Смирнов, И.Н. Клиническая эффективность и антиоксидантная активность мексидола при хронических цереброваскулярных заболеваниях / И.Н. Смирнова, Т.Н. Федорова, М.М. Танашян, З.А. Суслина // Нервные болезни. - 2006 .- №1. - С. 33-36.
Федорова, Т.Н. Окислительный стресс и защита головного мозга от ишемического повреждения: Дисс. д-ра биол. наук: 03.00.04: Москва. - 2004. - 298 с.
Calabrese, V. NO synthase and NO-dependet signal pathways in brain aging and neuredegenerative disorders: the role of oxidant/antioxidant balance / V. Calabrese, Т.Е. Bates, A.M. Stella // Neurochem. - 2000. - V.25. - P. 1315-1341.
Chen, Y.C. Antioxidative activities of hydrolysates from duck egg white using enzymatic hydrolysis / Y.C Chen, H.S. Chang, C.T. Wang, F.Y. Cheng // Asian-Aust. J. Anim. Sci. - 2009. - 22, (11). - P. 1587-1593.
 B. Antioxidant and anti-inflammatory properties of cancer preventive peptide lunasin in RAW 264.7 macrophages / B.
B. Antioxidant and anti-inflammatory properties of cancer preventive peptide lunasin in RAW 264.7 macrophages / B.  , C.-C. Hsieh, B.O. Lumen // Biochemical and Biophysical Research Communications. - 2009. - 390. - P. 803-808.
, C.-C. Hsieh, B.O. Lumen // Biochemical and Biophysical Research Communications. - 2009. - 390. - P. 803-808.
Hoyos-Arbelaez, J. Electrochemical methods as a tool for determining the antioxidant capacity of food and beverages. A review / J. Hoyos-Arbelaez, M. Vazquez, J. Contreras-Calderon // Food Chem. - 2017. - 221. - P. 1371-1381. doi:10.1016/j.foodchem.2016.11.017.
Jao, C.L. 1,1-Diphenyl-2-picrylhydrazyl (DPPH) radical scavenging by protein hydrolysates from tuna cooking juice / C.L. Jao, W.C. Ко // Fisheries Sci. - 2002. - 68. - P. 430-435.
Je, J.Y. Antioxidant activity of peptide isolated from Alaska pollack (Theragra chalcogramma) frame protein hydrolysate / J.Y. Je, P.J. Park, S.K. Kim // Food Res. Int. - 2005. - 38. - P. 45-50.
Kim, S.K. Isolation and characterization of antioxidative peptides from gelatin hydrolysate of Alaska pollack skin / S.K. Kim, Y.T. Kim, H.G. Byun, K.S. Nam, D.S. Joo, F. Shahidi // J. Agr. Food Chem. - 2001. - 49. - P. 1984-1989.
Kitts, D.D. Bioactive proteins and peptides from food sources. Applications of bioprocesses used in isolation and recovery / D.D. Kitts, K. Weiler // Curr. Pharm. Design. - 2003. - 9. - P. 1309-1323.
Lee, S.K. Antioxidant activity of phosvitin in phosphatidylcholine liposomes and meat model systems / S.K. Lee, J.H. Han, E.A. Decker // J. Food Sci. - 2002. - 67. - P. 37-41.
Li, Y.F. Bioactivities of chicken essence / Y.F. Li, R.R. He, B. Tsoi, H. Kurihara // Journal of Food Science. - 2012. - 77 (4). - P. 105-110. doi:10.1111/j.1750-3841.2012.02625.x.
Li, Xi Chicken embryo extracts enhance spleen lymphocyte and peritoneal macrophages function / Xi Li, Y. Su, J. Sun, Y. Yang // J. of Ethnopharmacol. -2012. - 144. - P. 255-260. doi:10.1016/j.jep.2012.09.001.
Lu, C.L. Characteristics of egg yolk phosvitin as an antioxidant for inhibiting metal-catalyzed phospholipid oxidations / C.L. Lu, R.C. Baker // Poult. Sci. - 1987. - 65. - P. 2065-2070.
Metelitza, D.I. Initiation and inhibition of free radical processes in H2O2-metmyoglobin (methemoglobin)-2,2'-azino-bis-(3-ethylbenzthiazoline-6-sulfonic acid) systems / D.I. Metelitza, A.N. Eryomin, D.O. Sviridov, V.S. Kamyshnikov // Biokhimiya. - 2001. - Vol. 66 (5). - P. 628-639.
Nonaka, Sh. Lithium protects rat cerebellar granule cells against apoptosis induced by anticonvulsants, phenytoin and carbamazepine / Sh. Nonaka, N. Katsube and D.-M. Chuang // JPET. - 1998. - Vol. 286. - P. 539-547.
Park, PJ. Purification and characterization of antioxidative peptides from protein hydrolysate of lecithin-free egg yolk / P.J. Park, W.K. Jung, K.S. Nam, F. Shahidi, S.K. Kim // J. AOCS. - 2001. - 78. - P. 651-656.
 J. Electrochemical determination of antioxidant capacity of fruit tea infusions / J.
J. Electrochemical determination of antioxidant capacity of fruit tea infusions / J.  L. Valek, T. Stipcevic, S. Martinez // Food Chem. - 2010. - 121 (3). - P. 820-825. doi:10.1016/j.foodchem.2009.12.090.
L. Valek, T. Stipcevic, S. Martinez // Food Chem. - 2010. - 121 (3). - P. 820-825. doi:10.1016/j.foodchem.2009.12.090.
Qian, Z.J. Free radical scavenging activity of a novel antioxidative peptide purified from hydrolysate of bullfrog skin / Z.J. Qian, W.K. Jung, S.K. Kim // Rana catesbeiana Shaw. Bioresource Technology. - 2008. - 99(6). - P. 1690-1698.
Sakanaka, S. Antioxidant activity of egg-yolk protein hydrolysates in a linoleic acid oxidation system / S. Sakanaka, Y. Tachibana, N. Ishihara, L.R. Juneja // Food Chem. - 2004. - 86. - P. 99-103.
Sakanaka, S. Active oxygen scavenging activity of egg-yolk protein hydrolysates and their effects on lipid oxidation in beef and tuna homogenates / S. Sakanaka, Y. Tachibana // Food Chem. - 2006. - 95. - P. 243-249.
Song, Li. Antioxidant activities of hydrolysates of Area subcrenata prepared with three proteases / Li. Song, T. Li, R. Yu, Ch. Yan, Sh. Ren and Yu Zhao // Mar. Drugs. - 2008. - 6. - P. 607-619. doi:10.3390/md6040607.
Suetsuna, K. Antioxidant peptides from the protease digest of prawn (Penaeus japonicus) muscle / K. Suetsuna // Mar. Biotechnol. - 2000. - 2. - P. 5-10.
Sun, H. Antioxidant activities of chick embryo egg hydrolysates / H. Sun, T. Ye, Y. Wang, L. Wang, Y. Chen, B. Li // Food Sci. & Nutr. - 2014. - 2 (1). - P. 58-64. doi: 10.1002/fsn3.77/
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения полиэлектролитных микрокапсул | 2017 |
|
RU2641034C1 |
| ИММУНОМОДУЛЯТОР | 2020 |
|
RU2747986C1 |
| СПОСОБ ОЦЕНКИ КАЧЕСТВА СУТОЧНЫХ ЦЫПЛЯТ | 2019 |
|
RU2734943C1 |
| СПОСОБ ОЦЕНКИ СУТОЧНОГО МОЛОДНЯКА ПТИЦЫ | 2018 |
|
RU2699719C1 |
| ПРИМЕНЕНИЕ 6-ГИДРОКСИ-2,2,4-ТРИМЕТИЛ-1,2-ДИГИДРОХИНОЛИНА В КАЧЕСТВЕ ГЕПАТОПРОТЕКТОРА | 2017 |
|
RU2677883C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПОЗИЦИИ НА ОСНОВЕ ФЛАВОНОИДОВ ДЛЯ ПРИМЕНЕНИЯ В КОСМЕТИЧЕСКИХ СРЕДСТВАХ | 2022 |
|
RU2788579C1 |
| Средство растительного происхождения, обладающее антиоксидантным действием | 2022 |
|
RU2794091C1 |
| ПИТАТЕЛЬНАЯ СРЕДА ПЛОТНАЯ ДЛЯ КУЛЬТИВИРОВАНИЯ БРУЦЕЛЛ | 2019 |
|
RU2728379C1 |
| БИЦИКЛИЧЕСКИЕ ПИРИМИДИНЫ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ-АКТИВАТОРЫ АНТИОКСИДАНТНОЙ ПРОГРАММЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЦИТОПРОТЕКТОРОВ | 2014 |
|
RU2545758C1 |
| ШТАММ ОДНОКЛЕТОЧНОЙ МИКРОВОДОРОСЛИ MALLOMONAS KALINAE - ПРОДУЦЕНТ КАРОТИНОИДА ФУКОКСАНТИНА | 2017 |
|
RU2644260C1 |
Изобретение относится к фармацевтической промышленности, а именно к средству с антиоксидантными и нейропротекторными свойствами. Средство, обладающее антиоксидантным, нейропротекторным свойствами, полученное путем удаления липидов из сублимата эмбриональных и внеэмбриональных тканей куриных эмбрионов, экстракцией петролейным эфиром с последующим высушиванием обезжиренного остатка, затем полученный белоксодержащий порошок тщательно измельчают, растворяют в дистиллированной воде, перемешивают, добавляют HCl, выдерживают при перемешивании, затем полученную массу автоклавируют, а после нейтрализуют 1 М NaOH и центрифугируют, полученную после центрифугирования жидкость последовательно фильтруют с применением мембран для стерилизации и удаления не гидролизованных белков, при определенных условиях. Вышеописанное средство расширяет арсенал пептидсодержащих средств из природного сырья, обладающих антиоксидантными и нейропротекторными свойствами. 4 табл., 1 ил.
Средство, обладающее антиоксидантным и нейропротекторным свойствами, полученное путем удаления липидов из сублимата эмбриональных и внеэмбриональных тканей 10-ти суточных куриных эмбрионов 5-ти кратной экстракцией петролейным эфиром с последующим высушиванием обезжиренного остатка, затем полученный белоксодержащий порошок тщательно измельчают, растворяют в дистиллированной воде в количестве 1:25-30, перемешивают и затем к раствору добавляют HCl до ее концентрации 0,5-0,6% и выдерживают при 50-55°С в течение 60 мин при перемешивании, затем полученную массу автоклавируют при 125-130°С в течение 60-65 мин, а после нейтрализуют 1 М NaOH до рН 6,8-7,2, центрифугируют при 4600-4800 g в течение 100-120 мин при температуре 2-4°С, полученную после центрифугирования жидкость последовательно фильтруют с применением мембран для стерилизации и удаления не гидролизованных белков.
| СПОСОБ ИЗГОТОВЛЕНИЯ БИОЛОГИЧЕСКИ АКТИВНЫХ ПРЕПАРАТОВ ИЗ ЭМБРИОНАЛЬНЫХ ТКАНЕЙ | 1996 |
|
RU2132688C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ФЕРМЕНТАТИВНОГО ГИДРОЛИЗАТА ТКАНЕЙ КУРИНОГО ЭМБРИОНА ДЛЯ ПРИГОТОВЛЕНИЯ ЗАЩИТНЫХ СРЕД ПРИ ПРОИЗВОДСТВЕ СУХИХ ВИРУСНЫХ ВАКЦИН | 1984 |
|
SU1277457A1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ БИОСТИМУЛЯТОРА ЭМБРИОНАЛЬНОГО | 2001 |
|
RU2197251C2 |
| СПОСОБ ПРИГОТОВЛЕНИЯ НИЗКОМОЛЕКУЛЯРНОГО КОМПЛЕКСА АКТИВИРОВАННОГО ЭМБРИОНАЛЬНОГО (НИКА-ЭМ) | 2014 |
|
RU2560845C1 |
| Xi Li et al | |||
| Chicken embryo extracts enhance spleen lymphocyte and peritoneal macrophages function // Journal of Ethnopharmacology | |||
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| Аппарат для электрической передачи изображений без проводов | 1920 |
|
SU144A1 |
| - P | |||
| Гудок | 1921 |
|
SU255A1 |
Авторы
Даты
2019-04-24—Публикация
2018-01-10—Подача