Изобретение относится к области биотехнологии, в частности к выращиванию бактерий на питательной среде с целью увеличения количества белковых компонентов в клеточных культурах.
Известен способ промышленного культивирования штаммов E.coli, полученных на основе штамма bl21(de3), несущего ген t7 rna полимеразы под контролем lacuv5 промотора, с повышенным синтезом биомассы и выходом целевого белка в тельцах включения (см. патент на изобретение RU 2473683, МПК C12N 1/21). Способ предусматривает выращивание инокулята на основе штамма BL21(DE3) E.coli, несущего ген Т7 RNA полимеразы под контролем lacUV5 промотора, до середины логарифмической фазы роста на питательной среде с использованием в качестве источника углерода глюкозы в концентрации 10 г/л при температуре 38°С, перемешивании 200 об/мин в течение 3 ч, засев ферментера инокулятом с посевной дозой 10%, культивирование микроорганизмов при 38°С, концентрации растворенного кислорода 80% при максимальной скорости перемешивания 1200 об/мин, максимальном уровне аэрации 1 объем воздуха/мин: 1,2 объема культуральной жидкости, рН 7,00; окончание ферментации на 12-13 ч культивирования; осаждение клеток штамма-продуцента E.coli. Вначале культивирования добавляют 50%-ный (мас. %) раствор глюкозы, в середине логарифмической фазы роста производят порционную добавку 80%-го (мас. %) раствора глицерина и с конца логарифмической фазы роста культуры осуществляют дробные добавки 25%-ного (мас. %) раствора лактозы. После культивирования содержащую рекомбинантные целевые белки в виде нерастворимых тел включения биомассу осаждают. Изобретение позволяет повысить выход биомассы и целевого белка с единицы объема культуральной среды.
Наиболее близким к заявляемому является способ увеличения производства белка (см. заявку на изобретение WO 8606410, МПК С12Р 21/02). Способ обеспечивает увеличение количества получаемого белка путем культивирования кишечной палочки, имеющей выраженный вектор, который содержит структурный ген белка. Способ включает в себя выращивание кишечной палочки на среде, содержащей источник ионов железа, марганца или их смеси, и источник азота природного происхождения для увеличения количества белка свободного от метионина, соответствующего поступательному стартовому ко дону ATG. Где этот белок, свободный от метионинового остатка, может быть получен в увеличенном количестве и соответствует инициирующему кодону ATG.
Однако существенным недостатком данных способов является использование геномодифицированных организмов для увеличения количества синтезируемого белка на селективных питательных средах.
Техническая проблема настоящего изобретения заключается в разработке способа синтеза белка без внедрения генетических векторов, обеспечивая расширение арсенала способов синтеза белка в биотехнологии.
Технический результат заявляемого изобретения заключается в увеличении количества синтезируемого белка в различных видах культур бактериальных клеток за счет покрытия поверхности бактериальных клеток полимерными слоями и последующим выращиванием клеток на питательной среде.
Технический результат достигается тем, что в способе синтеза белка в культуре бактериальных клеток, включающем выращивание клеток на питательной среде, согласно решению, на поверхность выращенных клеток наносят положительно заряженный слой полимера путем инкубирования в растворе положительно заряженного полимера, центрифугируют или фильтруют, промывают, затем на поверхность клеток наносят отрицательно заряженный слой полимера путем инкубирования в растворе отрицательно заряженного полимера, центрифугируют или фильтруют, промывают; нанесение слоев повторяют до получения необходимого их количества и заданного размера клеточных агрегатов; после чего клетки, покрытые полимерными слоями, помещают на питательную среду, выращивают и отделяют полученный продукт, при этом культуру используют в количествах 106-1020 кое/мл, клетки промывают перед нанесением полимеров и после их нанесения растворами с ионной силой в диапазоне 0-0.155 моль/л, концентрации полимеров выбирают в диапазоне 0.1 мг/мл-10 мг/мл, клетки инкубируют в растворе полимеров в течение 4-15 минут.
В качестве положительно заряженного полиэлеткролита используют полилизин, или протамин сульфат или полиаллиламин гидрохлорид или полиэтиленимин или полидиаллилдиметиламмоний хлорид или хитозан.
В качестве отрицательно заряженного полимера используют альгинат или гиалуроновую кислоту или полиакриловую кислоту или полистиролсульфонат натрия или полимолочную кислоту, или полиглутаминовую кислоту или сульфат целлюлозы.
Оптимальную температуру для покрытия выбирают в диапазоне от 2 до 46°С.
В случае использования центрифугирования реакционный объем смеси выбирают в диапазоне 0.5 мл - 1 л и центрифугируют в диапазоне 700-10000g в течение 30 сек - 5 минут, в случае использования метода фильтрования, выбирают в диапазоне 1 л - 50 л и используют фильтрующие материалы с размером пор не менее 0.45 микрон.
Размер клеточных агрегатов варьируют от 5 до 200 микрон. Изобретение поясняется чертежами
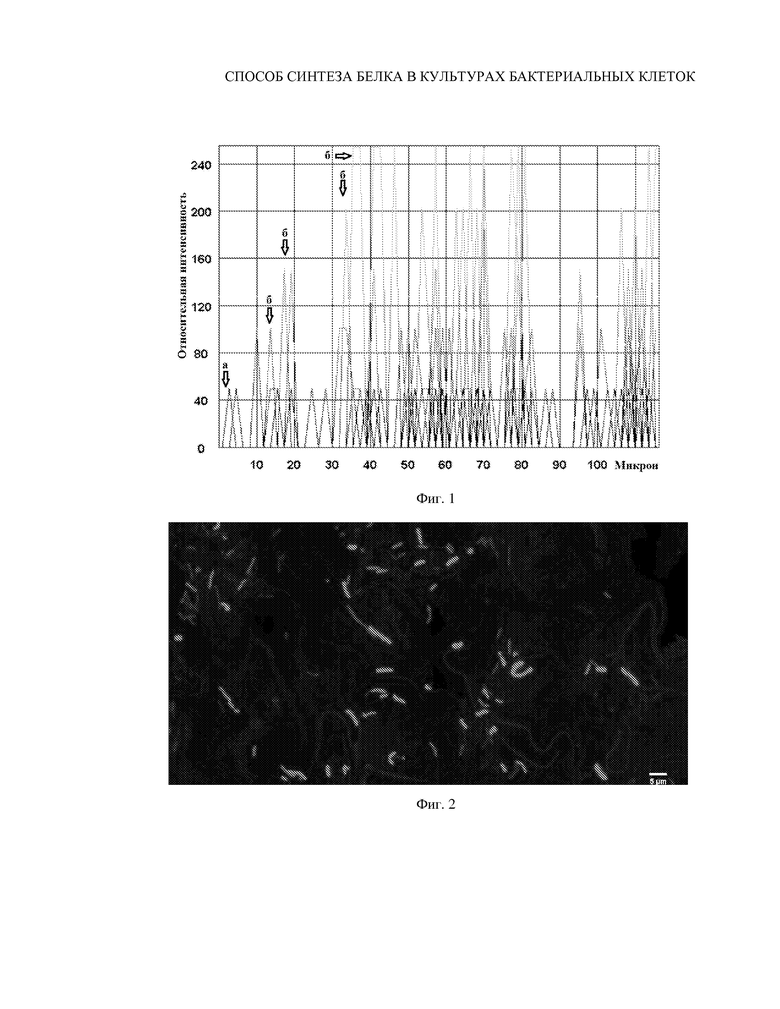
На фиг. 1 - представлена относительная интенсивность зеленого флуоресцирующего белка в клетках, покрытых полимерными оболочками и контрольных клетках (E.coli Тор 10) при наблюдении на конфокальном микроскопе: а) флуоресценция контрольных клеток, которая находятся на уровне 40-50 относительных единиц, б) флуоресценция клеток с увеличенным содержанием, которая достигает значения в 255 относительных единиц.
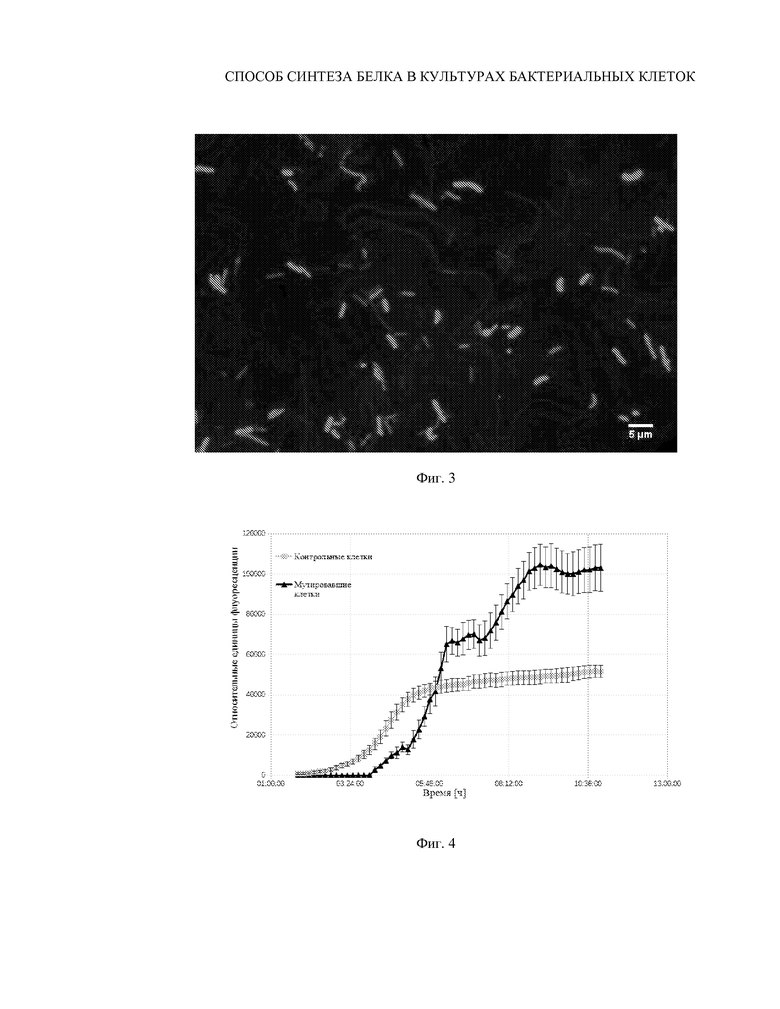
На фиг. 2 и фиг. 3 - представлены образцы клеток с увеличенным содержанием белка (наиболее яркие при увеличенном размере) и контрольных клеток.
На фиг. 4 - представлено спектрофотометрическое измерение флуоресценции популяции покрытых полимерными оболочками и контрольных клеток в питательной среде. Значения флуоресценции белка покрытых клеток составляли 103027±11659 в стационарной фазе роста, значения флуоресценции белка контрольных клеток 51492±2980, т.е. увеличение содержания белка составляло порядка 2 раз. Измерения проводились с целью дополнительного подтверждения увеличения количества синтезируемого белка в клетках с модифицированным покрытием, по сравнению с контрольными клетками.
Способ представляет собой процедуру нанесения полимерных слоев на поверхность клеток с целью увеличения количества синтезируемых белковых компонентов клеток. Способ включает в себя модификацию поверхности клеток методом послойной адсорбции противоположно заряженных полимеров и последующим термостатированием культуры до температуры оптимальной для роста. Нанесение слоев продолжается до достижения заданных технологических параметров, в частности, количества синтезируемого белка, количества и заданного размера клеточных агрегатов. Необходимо отметить, что нанесение большего числа слоев приводит к увеличению содержания белка в клетках, но в тоже время увеличивает продолжительность и трудоемкость проведения операций.
Способ увеличения синтеза белка в культурах бактериальных клеток заключается в следующем.
Выращенную культуру в количестве 10-10 кое/мл промывают растворами с ионной силой в диапазоне 0-0.155 моль/л. Для инкапсуляции бактерий, основанной на электростатическом взаимодействии поверхности клетки с полимером, используют пары противоположно заряженных полимеров. В качестве положительно заряженных полиэлеткролитов используют полилизин, или протамин сульфат, или полиаллиламин гидрохлорид, или полиэтиленимин, или полидиаллилдиметиламмоний хлорид или хитозан.
А в качестве отрицательно заряженных полимеров используют альгинат или гиалуроновую кислоту или полиакриловую кислоту или полистиролсульфонат натрия или полимолочную кислоту, или полиглутаминовую кислоту или сульфат целлюлозы. Полимеры растворяют в деионизованной воде в диапазоне концентраций 0.1 мг/мл-10 мг/мл и при необходимости доводят до оптимального значения рН для бактериальной культуры. Раствор положительно заряженного полимера добавляют к приготовленной культуре в объемном соотношении 1:1, где реакционный объем находится в интервале 0.5 мл - 1 л (в случае центрифугирования) и инкубируют в течение 4-15 минут в диапазоне температур 2-46°С. Инкубированный образец центрифугируют в диапазоне 900-10000g в течение 30 сек - 5 минут. Данный способ может быть также осуществлен методом фильтрования, реакционный объем которого находится в диапазоне 1 л - 50 л, и где используют фильтрующие материалы с размером пор не менее 0.45 микрон.
Затем к полученному раствору добавляют отрицательно заряженный полимер в объемном соотношении 1:1 и инкубируют в течение 4-15 минут и промывают. Отличие промывки в случае отрицательного полимера заключается лишь в разнице для скорости и времени центрифугирования, которые используются в заданных диапазонах (900-10000 g в течение 30 сек - 5 минут), данный шаг также возможно заменить методом фильтрации. Эту процедуру повторяют до достижения желаемого числа слоев. Полученную биомассу помещают на питательную среду при оптимальной температуре для роста. Размер клеточных агрегатов, полученных в ходе данного способа, с увеличенным содержанием белков может варьироваться от 5 до 200 микрон. Выживаемость культуры подтверждают с использованием методов конфокальной микроскопии и спектрофотометрических измерений.
Примеры практической реализации способа. Пример 1.
Приготовление полимеров.
Для данного примера инкапсуляции использовали пары противоположно заряженных полимеров полиэтиленимин и полистиролсульфонат натрия, которые разбавляют в деионизованной воде в конечной концентрации 2.5 мг/мл. Полученные растворы помещают в ультразвуковую ванну на 15 мин. В дальнейшем полимеры титруют до значения рН=7.
Инкапсуляция.
Изначально, раствор полиэтиленимина добавляют к промытым клеткам, в количестве 1012 кое/мл в объемном соотношении 1:1 (реакционной объем смеси 2 мл) и инкубируют в течение 5 минут при комнатной температуре (25°С). После чего клетки центрифугируют при 700 g в течение 2 мин. Осажденную на поверхности культуру промывают 2 раза в растворе хлорида натрия (0.155 моль/л) и ресуспензируют клетки в объеме раствора путем промывки. После покрытия первым полимером, клетки инкубируют в растворе полистиролсульфоната натрия в объемном соотношении 1:1, используя те же условия. Промывку производят аналогичным образом кроме времени и силы центрифугирования, которые были 3 мин и 1500 g соответственно для формирования достаточно плотного слоя клеток. Эту процедуру повторяют до достижения 6 слоев. Пример 2.
Приготовление полимеров.
В данном примере использовали пары противоположно заряженных полимеров полиаллиламин гидрохлорид и полиакриловая кислота, которые разбавляют в деионизованной воде в конечной концентрации 10 мг/мл. Полученные растворы помещают в ультразвуковую ванну на 15 мин. В дальнейшем полимеры титруют до значения рН=7.
Инкапсуляция.
Изначально, раствор полиаллиламин гидрохлорида добавляют к промытым клеткам, в количестве 1020 кое/мл в объемном соотношении 1:1 (реакционной объем смеси 500 мл) и инкубируют в течение 15 минут при температуре 46°С. После чего клетки центрифугируют при 6000 g в течение 5 мин. Осажденную на поверхности культуру промывают 2 раза в растворе хлорида натрия (0.0775 моль/л) и ресуспензируют клетки в объеме раствора путем промывки. После покрытия первым полимером, клетки инкубируют в растворе полиакриловой кислоты в объемном соотношении 1:1, используя те же условия. Промывку производят аналогичным образом кроме времени и силы центрифугирования, которые были 5 мин и 10000 g соответственно для формирования достаточно плотного слоя клеток. Эту процедуру повторяют до достижения 4 слоев. Пример 3.
Приготовление полимеров.
Для данного примера использовали пары противоположно заряженных полимеров хитозан и полиглутаминовая кислота, которые разбавляют в деионизованной воде в конечной концентрации 0,1 мг/мл. Полученные растворы помещают в ультразвуковую ванну на 15 мин. В дальнейшем полимеры титруют до значения рН=7.
Инкапсуляция.
Изначально, раствор хитозана добавляют к промытым клеткам, в количестве 106 кое/мл в объемном соотношении 1:1 (реакционной объем смеси 1 мл) и инкубируют в течение 10 минут при температуре (2°С). После чего клетки центрифугируют при 2000 g в течение 4 мин. Осажденную на поверхности культуру промывают 2 раза в деионизованной воде и ресуспензируют клетки в объеме раствора путем промывки. После покрытия первым полимером, клетки инкубируют в растворе полиглутаминовой кислоты в объемном соотношении 1:1, используя те же условия. Промывку производят аналогичным образом кроме времени и силы центрифугирования, которые были 6 мин и 4000 g соответственно для формирования достаточно плотного слоя клеток. Эту процедуру повторяют до достижения 8 слоев.
Пример 4.
Приготовление полимеров.
В данном примере использовали пары противоположно заряженных полимеров полилизин и полимолочной кислоты, которые разбавляют в деионизованной воде в конечной концентрации 3 мг/мл. Полученные растворы помещают в ультразвуковую ванну на 15 мин. В дальнейшем полимеры титруют до значения рН=7.
Инкапсуляция.
Изначально, раствор полилизина добавляют к промытым клеткам, в количестве 1010 кое/мл в объемном соотношении 1:1 (реакционной объем смеси 1 л) и инкубируют в течение 10 минут при температуре (15°С). Культуру промывают методом фильтрования в растворе хлорида натрия (0.03975 моль/л) и ресуспензируют клетки в объеме раствора путем промывки. После покрытия первым полимером, клетки инкубируют в растворе полимолочной кислоты в объемном соотношении 1:1, используя те же условия. Промывку производят аналогичным образом с использованием фильтрующего материала с размером пор 0.45 микрон. Эту процедуру повторяют до достижения 10 слоев.
Увеличение количества синтезируемого белка.
Приготовление культуры.
В качестве примера увеличения количества синтезируемого белка была выбрана культура Escherichia coli top 10 как модельный организм поведения бактериальных клеток. Из этого следует, что данный способ может быть применен к другим штаммам бактериальных клеток (Neidhardt F.С, Ingraham J.L., Schaechter M. Physiology of the bacterial cell: a molecular approach. - Sunderland: Sinauer, 1990. - T. 20, Ankeny R.A., Leonelli S. What's so special about model organisms? //Studies in History and Philosophy of Science Part A. - 2011. - T. 42. - №. 2. - C. 313-323.;
http://study.com/academy/lesson/escherichia-coli-e-coli-as-a-model-organism-or-host-cell.html; https://www.emlab.com/s/sampling/env-report-03-2010.html; Lee P.S., Lee K.H. Escherichia coli-a model system that benefits from and contributes to the evolution of proteomics //Biotechnology and bioengineering. - 2003. - T. 84. - №. 7. - C. 801-814.), Культура была преобразована с pRSET-emGFP плазмидом путем электропорации с использованием стандартных протоколов. Необходимо отметить, что введение плазмида pRSET-emGFP использовалось лишь для проверки данной гипотезы. Данную культуру культивировали на питательном бульоне (объем 100 мл, Nutrient Broth №2) с добавлением ампициллина с концентрацией 100 мг/мл. Эта смесь была помещена на роторный шейкер для выращивания около 3 часов при температуре 37°С до достижения оптической плотности равной 0.2. В дальнейшем, 50 мл полученной культуры концентрировали методом центрифугирования при 5000 g в течение 6 мин. Затем бактериальную культуру промывали от остатков питательной среды в 0.09% раствора хлорида натрия 3 раза и центрифугировали при 3000 g в течение 3 мин.
Подготовленные клетки после процедуры нанесения (см. Пример 1) были помещены в объеме 4 мкл на предметное стекло, содержащее питательную агарную среду, и накрыты покровным стеклом. Для наблюдения был использован конфокальный микроскоп Leica TCS SP8X, оснащенный боксом с возможностью нагрева до 37°С. Образец был помещен в камеру, где термостатировался до заданной температуры в течение всего времени эксперимента с использованием 100х увеличивающего объектива (НСХ PL АРО 100х/1.44 OIL) (фиг. 1-4). Предварительные эксперименты с использованием других культур P.stutzeri, S. aureus, В. subtilis и различных штаммов E.coli также показали положительный эффект использования данного способа с целью увеличения количества синтезируемого белка.
Заявляемое изобретение может быть осуществлено не только в вариантах, которые представлены в настоящем описании для иллюстрации, а в различных комбинациях параметров, которые ограничиваются только формулой в настоящем изобретении.
Кроме того, следует понимать, что различные признаки, аспекты и функциональные возможности, описанные в одном или нескольких отдельных примерах, не ограничены в отношении их применимости к различным вариантам осуществления данного биотехнологического процесса, и вместо этого могут применяться, отдельно или в различных комбинациях, к одному или нескольким способам реализации изобретения.
Необходимо отметить, что возможность нанесения полимеров на поверхность бактериальных клеток была показана в следующих работах: см. WO 200845806, МПК A61K-009/48; A61K-035/00; A61K-035/12; B01J-013/22 и др., см. Franz В. et al. Layer by Layer Nano Encapsulation of Microbes: Controlled Cell Surface Modification and Investigation of Substrate Uptake in Bacteria //Macromolecular bioscience. - 2010. - T. 10. - №. 2. - C. 164-172., см. см. Balkundi S.S. et al. Encapsulation of bacterial spores in nanoorganized polyelectrolyte shells //Langmuir. - 2009. - T. 25. - №. 24. - C. 14011-14016, однако, данные методы не использовались для увеличения количества синтезируемого белка и эффектов, аналогичных предложенному в патенте, не наблюдалось.
Данный способ позволяет расширить арсенал средств для синтезирования белка и может быть также применен в сочетании с методами генной инженерии.
Изобретение относится к области биотехнологии, в частности к способу синтеза белка в культурах бактериальных клеток. Способ включает модификацию поверхности клеток методом послойной адсорбции противоположно заряжённых полимеров и последующее термостатирование культуры клеток. Культуру клеток используют в количествах 106 – 1020 КОЕ/мл. Перед нанесением и после нанесения полимеров клетки промывают растворами с ионной силой в диапазоне 0–0,155 моль/л. В качестве положительно заряженного полимера используют полилизин, протамин сульфат, полиаллиламин гидрохлорид, полиэтиленимин, полидиаллилдиметиламмоний хлорид или хитозан. В качестве отрицательно заряженного полимера используют альгинат, гиалуроновую кислоту, полиакриловую кислоту, полистиролсульфонат натрия, полимолочную кислоту, полиглутаминовую кислоту или сульфат целлюлозы. Концентрации полимеров выбирают в диапазоне 0,1 мг/мл – 10 мг/мл. Клетки инкубируют в растворе полимеров в течение 4–15 мин. В случае использования центрифугирования реакционный объем смеси выбирают в диапазоне 0,5 мл – 1 л и центрифугируют в диапазоне 700–10000 g в течение 30 с – 5 мин. В случае фильтрования реакционный объем смеси выбирают в диапазоне 1 л – 50 л и используют фильтрующие материалы с размером пор не менее 0,45 мкм. Изобретение позволяет увеличить количество синтезируемого белка в различных видах культур бактериальных клеток без снижения выживаемости клеток. 1 з.п. ф-лы, 4 ил., 4 пр.
1. Способ синтеза белка в культуре бактериальных клеток, включающий выращивание клеток на питательной среде, отличающийся тем, что на поверхность выращенных клеток наносят положительно заряженный слой полимера путем инкубирования в растворе положительно заряженного полимера, центрифугируют или фильтруют, промывают, затем на поверхность клеток наносят отрицательно заряженный слой полимера путем инкубирования в растворе отрицательно заряженного полимера, центрифугируют или фильтруют, промывают; нанесение слоев повторяют до получения необходимого их количества и заданного размера клеточных агрегатов; после чего клетки, покрытые полимерными слоями, помещают на питательную среду, выращивают и отделяют полученный продукт, при этом культуру используют в количествах 106 - 1020 КОЕ/мл, клетки промывают перед нанесением полимеров и после их нанесения растворами с ионной силой в диапазоне 0–0,155 моль/л, в качестве положительно заряженного полимера используют полилизин или протамин сульфат, или полиаллиламин гидрохлорид, или полиэтиленимин, или полидиаллилдиметиламмоний хлорид, или хитозан, в качестве отрицательно заряженного полимера используют альгинат или гиалуроновую кислоту, или полиакриловую кислоту, или полистиролсульфонат натрия, или полимолочную кислоту, или полиглутаминовую кислоту, или сульфат целлюлозы, концентрации полимеров выбирают в диапазоне 0,1 мг/мл – 10 мг/мл, клетки инкубируют в растворе полимеров в течение 4–15 мин, в случае использования центрифугирования реакционный объем смеси выбирают в диапазоне 0,5 мл – 1 л и центрифугируют в диапазоне 700–10000 g в течение 30 с – 5 мин, в случае использования метода фильтрования – выбирают в диапазоне 1 л – 50 л и используют фильтрующие материалы с размером пор не менее 0,45 мкм.
2. Способ по п. 1, отличающийся тем, что оптимальную температуру для покрытия и инкубирования выбирают в диапазоне от 2 до 46°C.
| FRANZ B | |||
| et al | |||
| "Layer by Layer Nano Encapsulation of Microbes: Controlled Cell Surface Modification and Investigation of Substrate Uptake in Bacteria" | |||
| Macromolecular bioscience | |||
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Способ получения суррогата олифы | 1922 |
|
SU164A1 |
| PRIYA A | |||
| J | |||
| et al | |||
| "Enhanced Survival of Probiotic Lactobacillus acidophilus by Encapsulation with Nanostructured Polyelectrolyte Layers through Layer-by-Layer Approach" | |||
| J Agric Food Chem, 2011, v.59, p.11838-11845 | |||
| WO 2012101167 A1, 02.08.2012 | |||
| BORKOWSKA M | |||
| et al | |||
| "The Cytotoxic Effect of Polyelectrolyte Shells Coated Bacterial Cells on Human Leukemia Cells", J Nanomed Nanotechol | |||
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| BALKUNDI S | |||
| S | |||
| et al | |||
| "Encapsulation of bacterial spores in nanoorganized polyelectrolyte shells", Langmuir | |||
| Колосоуборка | 1923 |
|
SU2009A1 |
| Видоизменение пишущей машины для тюркско-арабского шрифта | 1923 |
|
SU25A1 |
| no | |||
| Пишущая машина для тюркско-арабского шрифта | 1922 |
|
SU24A1 |
| p | |||
| Воздухонагревательный аппарат | 1927 |
|
SU14011A1 |
| WO 2008045806 A2, 17.04.2008 | |||
| КАПСУЛА ДЛЯ КЛЕТОК, ПРОДУЦИРУЮЩИХ ВИРУСНЫЕ ЧАСТИЦЫ, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И ИСПОЛЬЗОВАНИЯ | 1996 |
|
RU2187301C2 |
Авторы
Даты
2019-05-21—Публикация
2017-07-10—Подача